Азотсодержащие гетероциклические соединения и фунгицид для сельского хозяйства или садоводства
Номер патента: 23328
Опубликовано: 31.05.2016
Авторы: Нисимура Сатоси, Сибаяма Котаро, Синоки Ясуюки, Кувахара Раито, Сато Мотоаки, Ёкояма Масахиро, Китамура Дзури
Формула / Реферат
1. Азотсодержащее гетероциклическое соединение, представленное формулой (I)
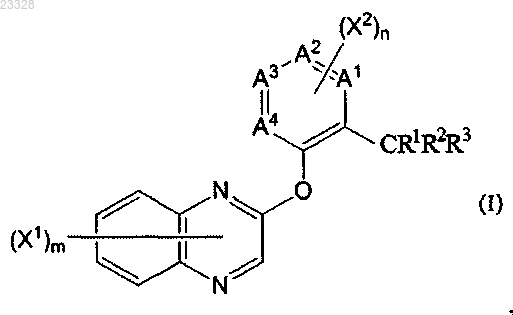
или его соль, где в указанной формуле
R1-R3 соответственно и независимо представляют собой атом водорода, С1-8-алкильную группу, гидрокси C1-6-алкильную группу, С2-8-алкенильную группу, C1-8-ацильную группу, C1-6-алкоксикарбонильную группу, ди-C1-6-алкилкарбамоильную группу, гидроксильную группу, C1-6-алкоксигруппу, C2-6-алкенилоксигруппу, галогеногруппу или цианогруппу,
при условии, что R1-R3 не все являются атомами галогена, R1-R3 не все являются С1-8-алкильными группами, когда любой из R1-R3 представляет собой атом водорода, остальные два не являются C1-8-алкильными группами, а когда любой из R1-R3 представляет собой С1-8-алкильную группу, остальные два не являются атомами водорода;
X1 соответственно и независимо представляет собой C1-6-алкильную группу или галогеногруппу;
m представляет число X1 и равен целому числу от 0 до 3;
X2 представляет собой галогеногруппу;
n представляет число X2 и равен 0 или 1; и
А1, А2, А3 и А4 соответственно и независимо представляют собой атом углерода или атом азота.
2. Азотсодержащее гетероциклическое соединение или его соль по п.1, в котором А2, А3 и А4 представляют собой атомы углерода.
3. Азотсодержащее гетероциклическое соединение или его соль по п.2, в котором А1 в формуле (I) представляет собой атом азота.
4. Фунгицид для сельского хозяйства или садоводства, включающий в качестве активного ингредиента по меньшей мере одно соединение, выбранное из группы, состоящей из азотсодержащих гетероциклических соединений и их солей по любому из пп.1-3.
Текст
АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ФУНГИЦИД ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА ИЛИ САДОВОДСТВА Фунгицид для сельского хозяйства или садоводства, содержащий в качестве активного ингредиента по меньшей мере одно соединение, выбранное из группы, состоящей из азотсодержащих гетероциклических соединений, представленных формулой (I) (R1-R3 представляют собой атомы водорода, алкильные группы или тому подобное, X1 представляет собой галогеногруппу или подобную группу, m равен целому числу от 0 до 3, X2 представляет собой галогеногруппу, n равен 0 или 1 и А 1-А 4 представляют собой атомы углерода или атомы азота), и их солей. Изобретение относится к фунгициду для сельского хозяйства или садоводства, который обладает надежным действием и может использоваться безопасно, а также к азотсодержащему гетероциклическому соединению, которое может быть использовано в качестве активного ингредиента фунгицида для сельского хозяйства или садоводства. Для настоящего изобретения испрашивается приоритет по заявке на патент Японии 2011-113174,поданной 20 мая 2011, заявке на патент Японии 2011-143478, поданной 28 июня 2011, заявке на патент Японии 2011-254368, поданной 21 ноября 2011, и заявке на патент Японии 2011-274141, поданной 15 декабря 2011, все из которых включены в данное описание посредством ссылок. Уровень техники Для борьбы с болезнями сельскохозяйственных или садовых культур используются самые разнообразные и многочисленные средства. Однако, так как эффективность многих средств такой борьбы неудовлетворительна, их применение оказывается ограниченным появлением патогенов, резистентных по отношению к лекарственным средствам, а также химическими повреждениями или загрязнениями растений и токсичностью для людей, домашнего скота и рыбы, или существенным воздействием на окружающую среду. Ни одно из известных средств борьбы не является полностью удовлетворительным. Таким образом, существует насущная потребность в разработке лекарственного средства, который был бы мало подвержен указанным недостаткам. В патентном документе 1, если рассматривать его с точки зрения настоящего изобретения, описываются производные 3-(дигидро(тетрагидро)изохинолин-1-ил)хинолина, представленные следующими формулами: где R1 и R2 представляют собой алкильные группы или подобные группы, R3 и R4 представляют собой атомы водорода, атомы галогена или подобные группы, R5 представляет собой атом водорода, алкильную группу или подобную группу, X1 представляет собой атом галогена, алкильную группу или подобную группу, Y1 представляет собой атом галогена, алкильную группу или подобную группу, n равен целому числу от 0 до 4, и m равен целому числу от 0 до 6, а также гербицид, содержащий такие соединения в качестве активного ингредиента. Кроме того, в патентном документе 2 раскрывается производное 3-(изохинолин-1-ил)хинолина,представленное формулой где цикл A1 и цикл B1 представляют собой бензольные циклы или тому подобное, R6-R9 представляют собой атомы галогена, алкильные группы, гидроксильные группы, алкоксигруппы или подобные группы, Q представляет собой N или N-R10 (где R10 представляет собой атом водорода, гидроксильную группу, алкильную группу или подобную группу), Х 2 представляет собой атом галогена, алкильную группу или подобную группу, Y2 представляет собой атом галогена, алкильную группу или подобную группу, n2 равен целому числу от 0 до 4, и m2 равен целому числу от 0 до 6, и связи, содержащие штриховые линии, представляют собой простые связи или двойные связи, а также инсектицид, содержащий такое соединение в качестве активного ингредиента. Кроме того, в патентном документе 3 раскрывается эфирное производное феноксипропионовой кислоты, представленное формулой где Y3 представляет собой атом галогена, R11, R12 и R13 соответственно и независимо представляют собой низшую алкильную группу или низшую алкоксигруппу, и R14 представляет собой низшую алкиль-1 023328 ную группу), а также гербицид, содержащий такое соединение в качестве активного ингредиента. Кроме того, в патентном документе 4 раскрывается производное хиноксалина, представленное формулой где Х 4 представляет собой атом водорода, атом галогена или подобную группу, Y4 представляет собой атом галогена или алкильную группу, Z4 представляет собой атом кислорода или атом серы, и R15 иR16 представляют собой алкильные группы, а также инсектицид, содержащий такое соединение в качестве активного ингредиента. Кроме того, в патентном документе 5 раскрывается фармацевтическая композиция, содержащая соединение, представленное формулой где R17 представляет собой атом водорода, алкильную группу или подобную группу, R18 представляет собой пиридильную группу, арильную группу или подобную группу, и n3 равен целому числу от 2 до 5. Документы известного уровня техники Патентные документы. Патентный документ 1: международная патентная публикацияWO 2005/070917. Патентный документ 2: международная патентная публикацияWO 2007/011022. Патентный документ 3: первая публикация не прошедшей экспертизу заявки на патент ЯпонииНО 5-148235. Патентный документ 4: первая публикация не прошедшей экспертизу заявки на патент ЯпонииS58-92960. Патентный документ 5: патент США 5578596. Непатентные документы. Непатентный документ 1: Journal of Medicinal Chemistry, 1981, Vol. 24, (1), pp. 93-101. Раскрытие изобретения Задачи, решаемые изобретением. Целью настоящего изобретения является фунгицид для сельского хозяйства или садоводства, который обладает надежным действием и может быть использован безопасно, а также азотсодержащее гетероциклическое соединение или его соль, которые могут быть использованы в качестве активного ингредиента фунгицида для сельского хозяйства или садоводства. Методы решения поставленных задач. Авторы настоящего изобретения провели широкомасштабные исследования для решения вышеуказанных задач. Результаты таких исследований привели к получению азотсодержащего гетероциклического соединения, представленного формулой (I), и его солей. Авторы настоящего изобретения обнаружили, что такое азотсодержащее гетероциклическое соединение обладает надежным действием и может быть безопасно использовано в качестве активного ингредиента фунгицида для сельского хозяйства или садоводства. Кроме того, на базе обнаруженных сведений были проведены дополнительные исследования, что и привело к осуществлению настоящего изобретения. А именно, настоящее изобретение включает описанные ниже аспекты.R1-R3 соответственно и независимо представляют собой атом водорода, C1-8-алкильную группу,гидрокси C1-6-алкильную группу, С 2-8-алкенильную группу, C1-8-ацильную группу, C1-6 алкоксикарбонильную группу, ди-C1-6-алкилкарбамоильную группу, гидроксильную группу, C1-6 алкоксигруппу, C2-6-алкенилоксигруппу, галогеногруппу или цианогруппу,при условии, что R1-R3 не все являются атомами галогена, R1-R3 не все являются C1-8-алкильными группами, когда любой из R1-R3 представляет собой атом водорода, остальные два не являются C1-8 алкильными группами, а когда любой из R1-R3 представляет собой С 1-8-алкильную группу, остальные два не являются атомами водорода;X1 соответственно и независимо представляет собой C1-6-алкильную группу или галогеногруппу;m представляет число X1 и равен целому числу от 0 до 3;n представляет число X2 и равен 0 или 1; и А 1, А 2, А 3 и А 4 соответственно и независимо представляют собой атом углерода или атом азота.[2] Азотсодержащее гетероциклическое соединение или его соль по [1], в котором А 2, А 3 и А 4 представляют собой атомы углерода.[3] Азотсодержащее гетероциклическое соединение или его соль по [2], в котором А 1 в формуле (I) представляет собой атом азота.[4] Фунгицид для сельского хозяйства или садоводства, включающий в качестве активного ингредиента по меньшей мере одно соединение, выбранное из группы, состоящей из азотсодержащих гетероциклических соединений и их солей по любому из [1]-[3]. Эффект, достигаемый с помощью настоящего изобретения. Азотсодержащее гетероциклическое соединение по настоящему изобретению представляет собой новое соединение, которое может быть использовано в качестве активного ингредиента фунгицида для сельского хозяйства или садоводства. Фунгицид для сельского хозяйства или садоводства по настоящему изобретению является безопасным химическим средством, которое обладает надежной и высокой контролирующей эффективностью,не вызывает химического повреждения растений и обладает низкой токсичностью для людей, домашнего скота или рыбы, и оказывает слабое действие на окружающую среду. Варианты осуществления изобретения Далее приводится подробное описание настоящего изобретения с разделением на разделы, касающиеся 1) азотсодержащего гетероциклического соединения и 2) фунгицида для сельского хозяйства или садоводства. 1) Азотсодержащее гетероциклическое соединение. Азотсодержащее гетероциклическое соединение по настоящему изобретению является соединением, представленным формулой (I) (также может называться "соединением (I)"). Азотсодержащее гетероциклическое соединение по настоящему изобретению включает гидраты,различные типы сольватов, кристаллические полиморфы или тому подобное. Кроме того, азотсодержащее гетероциклическое соединение по настоящему изобретению включает стереоизомеры на основе асимметричных атомов углерода или двойных связей и т.п., а также их смеси. Сначала приводится пояснение терминов "незамещенный" и "замещенный", используемых в контексте формулы (I). Термин "незамещенная" относится к группе, представляющей собой только группу, выступающую в качестве исходного центра. Когда в описании группы ничего не сказано о "замещении", и в описании только лишь приведено название группы, служащей в качестве исходного центра, такое определение относится к "незамещенной" группе, если только явным образом не указано иное. С другой стороны, термин "замещенный" относится к случаю, когда произвольный атом водорода группы, служащей в качестве исходного центра, замещен группой, имеющей структуру, которая совпадает со структурой исходного центра или отличается от нее. Таким образом, "заместитель" представляет собой другую группу, связанную с группой, служащей в качестве исходного центра. Может присутствовать как один заместитель, так и два или больше заместителей. Два или больше заместителей могут быть одинаковьми или различными. Термин "C1-6", например, показывает, что число атомов углерода в группе, служащей в качестве исходного центра, составляет 1-6. Это число атомов углерода не включает число атомов углерода, присутствующих в заместителях. Например, бутильная группа, имеющая этоксигруппу в качестве своего заместителя, классифицируется как С 2-алкокси-С 4-алкильная группа. В отношении "заместителей" не накладывается никаких особенных ограничений, при условии что они химически допустимы и позволяют получить эффект по настоящему изобретению. Примеры групп, способных представлять собой "заместители", включают атомы галогена, такие как атом фтора, атом хлора, атом брома или атом иода; C1-6-алкильные группы, такие как метильная группа,этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, втор-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа или н-гексильная группа; С 3-6 циклоалкильные группы, такие как циклопропильная группа, циклобутильная группа, циклопентильная группа или циклогексильная группа; C2-6-алкенильные группы, такие как винильная группа, 1 пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3 бутенильная группа, 1-метил-2-пропенильная группа, 2-метил-2-пропенильная группа, 1-пентенильная группа, 2-пентенильная группа, 3-пентенильная группа, 4-пентенильная группа, 1-метил-2-бутенильная группа, 2-метил-2-бутенильная группа, 1-гексенильная группа, 2-гексенильная группа, 3-гексенильная группа, 4-гексенильная группа или 5-гексенильная группа; С 3-6-циклоалкенильные группы, такие как 2 циклопропенильная группа, 2-циклопентенильная группа или 3-циклогексенильная группа; C2-6 алкинильные группы, такие как этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1 бутинильная группа, 2-бутинильная группа, 3-бутинильная группа, 1-метил-2-пропинильная группа, 2 метил-3-бутинильная группа, 1-пентинильная группа, 2-пентинильная группа, 3-пентинильная группа, 4 пентинильная группа, 1-метил-2-бутинильная группа, 2-метил-3-пентинильная группа, 1-гексинильная группа или 1,1-диметил-2-бутинильная группа; C1-6-алкоксигруппы, такие как метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, втор-бутоксигруппа, изобутоксигруппа или трет-бутоксигруппа; C2-6-алкенилоксигруппы, такие как винилоксигруппа, аллилоксигруппа, пропенилоксигруппа или бутенилоксигруппа; C2-6-алкинилоксигруппы, такие как этинилоксигруппа или пропаргилоксигруппа; С 6-10-арильные группы, такие как фенильная группа или нафтильная группа; С 6-10 арилоксгруппы, такие как феноксигруппа или 1-нафтоксигруппа; С 7-11-аралкильные группы, такие как бензильная группа или фенетильная группа; С 7-11-аралкилоксигруппы, такие как бензилоксигруппа или фенетилоксигруппа; C1-7-ацильные группы, такие как формильная группа, ацетильная группа, пропионильная группа, бензоильная группа или циклогексилкарбонильная группа; С 1-7-ацилоксигруппы, такие как формилоксигруппа, ацетилоксигруппа, пропионилоксигруппа, бензоилоксигруппа или циклогексилкарбонилоксигруппа; C1-6-алкоксикарбонильные группы, такие как метоксикарбонильная группа, этоксикарбонильная группа, н-пропоксикарбонильная группа, изопропоксикарбонильная группа, нбутоксикарбонильная группа или трет-бутоксикарбонильная группа; карбоксильную группу; гидроксильную группу; оксогруппу; C1-6-галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа, 1-фтор-н-бутильная группа или перфтор-н-пентильная группа; C2-6-галогеналкенильные группы, такие как 2-хлор-1-пропенильная группа или 2-фтор-1-бутенильная группа; C2-6-галогеналкинильные группы, такие как 4,4-дихлор-1 бутинильная группа, 4-фтор-1-пентинильная группа или 5-бром-2-пентинильная группа; C1-6 галогеналкоксигруппы, такие как 2-хлор-н-пропоксигруппа или 2,3-дихлорбутоксигруппа; C2-6 галогеналкенилоксигруппы, такие как 2-хлорпропенилоксигруппа или 3-бромбутенилоксигруппа; С 6-10 галогенарильные группы, такие как 4-хлорфенильная группа, 4-фторфенильная группа или 2,4 дихлорфенильная группа; С 6-10-галогенарилоксигруппы, такие как 4-фтолрфеноксигруппа или 4-хлор-1 нафтоксигруппа; C1-7-галогенацильные группы, такие как хлорацетильная группа, трифторацетильная группа, трихлорацетильная группа или 4-хлорбензоильная группа; цианогруппу; изоцианогруппу; нитрогруппу; изоцианатогруппу; цианатогруппу; азидную группу; аминогруппу; C1-6-алкиламиногруппы, такие как метиламиногруппа, диметиламиногруппа или диэтиламиногруппа; С 6-10-ариламиногруппы, такие как анилиногруппа или нафтиламиногруппа; С 7-11-аралкиламиногруппы, такие как бензиламиногруппа или фенилэтиламиногруппа; C1-7-ациламиногруппы, такие как формиламиногруппа, ацетиламиногруппа,пропаноиламиногруппа, бутириламиногруппа, изопропилкарбониламиногруппа или бензоиламиногруппа; C1-6-алкоксикарбониламиногруппы, такие как метоксикарбониламиногруппа, этоксикарбониламиногруппа, н-пропоксикарбониламиногруппа или изопропоксикарбониламиногруппа; карбамоильную группу; замещенные карбамоильные группы, такие как диметилкарбамоильная группа, фенилкарбамоильная группа или N-фенил-N-метилкарбамоильная группа; иминоС 1-6-алкильные группы, такие как иминометильная группа, (1-имино)этильная группа или (1-имино)н-пропильная группа; гидроксииминоС 1-6 алкильные группы, такие как гидроксииминометильная группа, (1-гидроксиимино)этильная группа или(1-гидроксиимино)пропильная группа; C1-6-алкоксииминоС 1-6-алкильные группы, такие как метоксииминометильная группа или (1-метоксиимино)этильная группа; меркаптогруппу; изотиоцианатогруппу; тиоцианатогруппу; C1-6-алкилтиогруппы, такие как метилтиогруппа, этилтиогруппа, н-пропилтиогруппа,изопропилтиогруппа, н-бутилтиогруппа, изобутилтиогруппа, втор-бутилтиогруппа или третбутилтиогруппа; C2-6-алкенилтиогруппы, такие как винилтиогруппа или аллилтиогруппа; C2-6 алкинилтиогруппы, такие как этинилтиогруппа или пропаргилтиогруппа; С 6-10-арилтиогруппы, такие как фенилтиогруппа или нафтилтиогруппа; гетероарилтиогруппы, такие как тиазолтиогруппа или пиридилтиогруппа; С 7-11-аралкилтиогруппы, такие как бензилтиогруппа или фенилэтилтиогруппа; (С 1-6 алкилтио)карбонильные группы, такие как (метилтио)карбонильная группа, (этилтио)карбонильная группа,(н-пропилтио)карбонильная группа,(изопропилтио)карбонильная группа,(нбутилтио)карбонильная группа, (изобутилтио)карбонильная группа, (втор-бутилтио)карбонильная группа или (трет-бутилтио)карбонильная группа; C1-6-алкилсульфинильные группы, такие как метилсульфинильная группа, этилсульфинильная группа или трет-бутилсульфинильная группа; C2-6 алкенилсульфинильные группы, такие как аллилсульфинильная группа; С 2-6-алкинилсульфинильные группы, такие как пропаргилсульфинильная группа; С 6-10-арилсульфинильные группы, такие как фенилсульфинильная группа; гетероарилсульфинильные группы, такие как тиазолилсульфинильная группа или пиридилсульфинильная группа; С 7-11-аралкилсульфинильные группы, такие как бензилсульфинильная группа или фенетилсульфинильная группа; C1-6-алкилсульфонильные группы, такие как метилсульфонильная группа, этилсульфонильная группа или трет-бутилсульфонильная группа; C2-6 алкенилсульфонильные группы, такие как аллилсульфонильная группа; C2-6-алкинилсульфонильные группы, такие как пропаргилсульфонильная группа; С 6-10-арилсульфонильные группы, такие как фенилсульфонильная группа; гетероарилсульфонильные группы, такие как тиазолилсульфонильная группа или пиридилсульфонильная группа; С 7-11-аралкилсульфонильные группы, такие как бензилсульфонильная группа или фенетилсульфонильная группа; 5-членные гетероарильные группы, такие как пирролильная группа, фурильная группа, тиенильная группа, имидазолильная группа, пиразолильная группа, оксазолильная группа, изоксазолильная группа, тиазолильная группа, изотиазолильная группа, триазолильная группа, оксадиазолильная группа, тиодиазолильная группа или тетразолильная группа; 6-членные гетероарильные группы, такие как пиридильная группа, пиразинильная группа, пиримидинильная группа,пиридазинильная группа или триазинильная группа; насыщенные гетероциклические группы, такие как азиридинильная группа, эпоксигруппа, пирролидинильная группа, тетрагидрофуранильная группа, пиперидильная группа, пиперазинильная группа или морфолинильная группа; три-С 1-6-алкилсилильные группы, такие как триметилсилильная группа, триэтилсилильная группа или трет-бутилдиметилсилильная группа; и трифенилсилильную группу. Кроме того, такие "заместители" в свою очередь могут иметь свои "заместители". Например, заместитель в форме бутильной группы может иметь в качестве заместителя этоксигруппу или другой заместитель. Иными словами, заместитель может быть этоксибутильной группой.R представляет собой группу CR1R2R3 или цианогруппу.R1-R3 соответственно и независимо представляют собой атом водорода, незамещенную или замещенную C1-8-алкильную группу, незамещенную или замещенную С 2-8-алкенильную группу, незамещенную или замещенную С 2-8-алкинильную группу, незамещенную или замещенную С 3-8-циклоалкильную группу, незамещенную или замещенную С 4-8-циклоалкенильную группу, незамещенную или замещенную С 6-10-арильную группу, незамещенную или замещенную гетероциклическую группу, незамещенную или замещенную С 1-8-ацильную группу, незамещенную или замещенную (1-имино)С 1-8-алкильную группу, незамещенную или замещенную карбоксильную группу, незамещенную или замещенную карбамоильную группу, незамещенную или замещенную гидроксильную группу, незамещенную или замещенную аминогруппу, незамещенную или замещенную меркаптогруппу, замещенную сульфонильную группу, галогеногруппу, цианогруппу или нитрогруппу,при том условии, что R1-R3 не все являются атомами галогена, R1-R3 не все являются незамещенными C1-8-алкильными группами, когда любой из R1-R3 представляет собой атом водорода, остальные два не являются незамещенными C1-8-алкильными группами, и когда любой из R1-R3 представляет собой незамещенную C1-8-алкильную группу, остальные два не являются атомами водорода."С 1-8-Алкильная группа" представляет собой насыщенную углеводородную группу, состоящую из 1-8 атомов углерода. С 1-8-Алкильная группа может быть линейной или разветвленной. Примеры C1-8 алкильных групп включают метальную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, н-гексильную группу, н-гептильную группу, н-октильную группу, изопропильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, изопентильную группу, неопентильную группу, 2-метилбутильную группу, 2,2-диметилпропильную группу и изогексильную группу. Из них предпочтительными являются C1-6-алкильные группы. Примеры "замещенных С 1-8-алкильных групп" включают циклоалкилалкильные группы, такие как циклопропилметильная группа, 2-циклопропилэтильная группа, циклопентилметильная группа или 2-циклогексилэтильная группа, и предпочтительно С 3-6 циклоалкилС 1-8-алкильные группы; циклоалкенилалкильные группы,такие как циклопентенилметильная группа,3 циклопентенилметильная группа, 3-циклогексенилметильная группа или 2-(3-циклогексенил)этильная группа, и предпочтительно С 4-6-пиклоалкенилС 1-6-алкильные группы; галогеналкильные группы, такие как фторметильная группа, хлорметильная группа, бромметильная группа, дифторметильная группа, дихлорметильная группа, дибромметильная группа, трифторметильная группа, трихлорметильная группа, трибромметильная группа, 2,2,2-трифторэтильная группа, 2,2,2 трихлорэтильная группа, пентафторэтильная группа, 4-фторбутильная группа, 4-хлорбутильная группа,3,3,3-трифторпропильная группа, 2,2,2-трифтор-1-трифторметилэтильная группа, перфторгексильная группа, перхлоргексильная группа, перфтороктильная группа, перхлороктильная группа, 2,4,6 трихлоргексильная группа, перфтордецильная группа или 2,2,4,4,6,6-гексафтороктильная группа, и предпочтительно C1-6-галогеналкильные группы; арилалкильные (аралкильные) группы, такие как бензильная группа, фенетильная группа, 3 фенилпропильная группа, 1-нафтилметильная группа или 2-нафтилметильная группа, и предпочтительны С 6-10-арилС 1-6-алкильные группы; гетероарилалкильные группы, такие как 2-пиридилметильная группа, 3-пиридилметильная группа,-5 023328 4-пиридилметильная группа, 2-(2-пиридил)этильная группа, 2-(3-пиридил)этильная группа, 2-(4 пиридил)этильная группа, 3-(2-пиридил)пропильная группа, 3-(3-пиридил)пропильная группа, 3-(4 пиридил)пропильная группа, 2-пиридинилметильная группа, 3-пиразинилметильная группа, 2-(2 пиразинил)этильная группа, 2-(3-пиразинил)этильная группа, 3-(2-пиразинил)пропильная группа, 3-(3 пиразинил)пропильная группа, 2-пиримидилметильная группа, 4-пиримидилметильная группа, 2-(2 пиримидил)этильная группа, 2-(4-пиримидил)этильная группа, 3-(2-пиримидил)пропильная группа, 3-(4 пиримидил)пропильная группа, 2-фурилметильная группа, 3-фурилметильная группа, 2-(2 фурил)этильная группа, 2-(3-фурил)этильная группа, 3-(2-фурил)пропильная группа или 3-(3 фурил)пропильная группа, и предпочтительно 5-6-членные гетероарилС 1-6-алкильные группы; гидроксиалкильные группы, такие как гидроксиметильная группа, 1-гидроксиэтильная группа, 2 гидроксиэтильная группа, 1-гидроксипропильная группа, 3-гидроксипропильная группа, 1-гидрокси-1 метилэтильная группа, 2-гидрокси-1,1-диметилэтильная группа, 2-гидрокси-1,1-диметилпропильная группа или 2-гидрокси-2-метилпропильная группа, и предпочтительно гидроксиС 1-6-алкильные группы; алкоксиалкильные группы, такие как метоксиметильная группа, этоксиметильная группа, 2 метоксиэтильная группа, 2-этоксиэтильная группа, метокси-н-пропильная группа, 1-пропоксиэтильная группа, втор-бутоксиметильная группа, трет-бутоксиэтильная группа, 2,2-диметоксиэтильная группа или 2,2-диметокси-1,1-диметилэтильная группа, и предпочтительно C1-6-алкоксиС 1-6-алкильные группы; ацилоксиалкильные группы, такие как формилоксиметильная группа, ацетоксиметильная группа, 2 ацетоксиэтильная группа, пропионилоксиметильная группа или пропионилоксиэтильная группа, и предпочтительно С 1-7-ацилоксиС 1-6-алкильные группы; триалкилсилилоксиалкильные группы, такие как триметилсилилоксиметильная группа или третбутилдиметилсилилоксиметильная группа, и предпочтительно три-C1-6-алкилсилилокси C1-6-алкильные группы; арилсульфонилоксиалкильные группы, такие как тозилоксиметильная группа или 2-тозилокси-1,1 диметилэтильная группа, и предпочтительно C1-6-алкилзамещенные С 6-10-арилсульфонилоксиС 1-6 алкильные группы; цианоалкильные группы, такие как цианометильная группа, 2-цианоэтильная группа или 1-циано-1 метилэтильная группа, и предпочтительно цианоС 1-6-алкильные группы; ацилалкильные группы, такие как формилметильная группа, 2-формилэтильная группа, 3 формилпропильная группа, 1-формил-1-метилэтильная группа, 2-формил-1,1-диметилэтильная группа,ацетилметильная группа, 2-ацетилэтильная группа, 3-ацетилпропильная группа, 1-ацетил-1-метилэтильная группа или 2-ацетил-1,1-диметилэтильная группа, и предпочтительно С 1-7-ацилС 1-6-алкильные группы; 2-гидроксииминоалкильные группы, такие как 2-гидроксииминометильная группа, 2 гидроксиимино-1-метилэтильная группа, 2-гидроксиимино-1,1-диметилэтильная группа или 2 гидроксииминопропильная группа, и предпочтительно 2-гидроксииминоС 2-6-алкильные группы; ацилалкильные группы, такие как ацетилметильная группа, 2-ацетилэтильная группа, 3 ацетилпропильная группа, 1-ацетил-1-метилэтильная группа или 2-ацетил-1,1-диметилэтильная группа, и предпочтительно С 1-7-ацилС 1-6-алкильные группы; карбоксиалкильные группы, такие как карбоксиметильная группа, 2-карбоксиэтильная группа, 3 карбоксипроильная группа, 1-карбокси-1-метилэтильная группа или 2-карбокси-1,1-диметилэтильная группа, и предпочтительно карбоксиС 1-6-алкильные группы; алкоксикарбонилалкильные группы, такие как метоксикарбонилметильная группа, 2-метоксикарбонилэтильная группа, 3-метоксикарбонилпропильная группа, 1-метоксикарбонил-1-метилэтильная группа или 2-метоксикарбонил-1,1-диметилэтильная группа, и предпочтительно C1-6-алкоксикарбонил С 1-6-алкильные группы; и азидоалкильные группы, такие как азидометильная группа, 2-азидоэтильная группа или 1-азидо-1 метилэтильная группа, и предпочтительно азидоС 1-6-алкильные группы."С 2-8-Алкенильная группа" представляет собой ненасыщенную углеводородную группу, состоящую из 2-8 атомов углерода, имеющую по меньшей мере одну углерод-углеродную двойную связь. С 2-8 Алкенильная группа может быть линейной или разветвленной. Примеры С 2-8-алкенильных групп включают винильную группу, 1-пропенильную группу, изопропенильную группу, аллильную группу, 1 бутенильную группу, 2-бутенильную группу, 3-бутенильную группу, 1-пентенильную группу, 2 пентенильную группу, 3-пентенильную группу, 4-пентенильную группу, 1-гексенильную группу, 2 гексенильную группу, 3-гексенильную группу, 4-гексенильную группу, 5-гексенильную группу, 1 гептенильную группу, 6-гептенильную группу, 1-октенильную группу, 7-октенильную группу, 1 метилаллильную группу, 2-метилаллильную группу, 1-метил-2-бутенильную группу и 2-метил-2 бутенильную группу. Из них предпочтительными являются C2-6-алкенильные группы. Примеры "замещенных С 2-8-алкенильных групп" включают галогеналкенильные группы, такие как 3-хлор-2-пропенильная группа, 4-хлор-2-бутенильная группа, 4,4-дихлор-3-бутенильная группа, 4,4 дифтор-3-бутенильная группа, 3,3-дихлор-2-пропенильная группа, 2,3-дихлор-2-пропенильная группа,3,3-дифтор-2-пропенильная группа или 2,4,6-трихлор-2-гексенильная группа, и предпочтительны C2-6-6 023328"С 2-8-Алкинильная группа" представляет собой ненасыщенную углеводородную группу, состоящую из 2-8 атомов углерода, имеющую по меньшей мере одну углерод-углеродную тройную связь. С 2-8 Алкинильная группа может быть линейной или разветвленной. Примеры С 2-8-алкинильных групп включают этинильную группу, 1-пропинильную группу, пропаргильную группу, 1-бутинильную группу, 2 бутинильную группу, 3-бутинильную группу, 1-пентинильную группу, 2-пентинильную группу, 3 пентинильную группу, 4-пентинильную группу, 1-гексинильную группу, 1-метил-2-пропинильную группу, 2-метил-3-бутинильную группу, 1-метил-2-бутинильную группу, 2-метил-3-пентинильную группу и 1,1-диметил-2-бутинильную группу. Из них предпочтительными являются С 2-6-алкинильные группы. Примеры "замещенных С 2-8-алкинильных групп" включают галогеналкинильные группы, такие как 3-хлор-1-пропинильная группа, 3-хлор-1-бутинильная группа, 3-бром-1-бутинильная группа, 3-бром-2 пропинильная группа, 3-иод-2-пропинильная группа, 3-бром-1-гексинильная группа, 4,4,6,6-тетрафтор-1 додецинильная группа, 5,5-дихлор-2-метил-3-пентинильная группа или 4-хлор-1,1-диметил-2 бутинильная группа, и предпочтительны C2-6-галогеналкинильные группы."С 3-8-Циклоалкильная группа" представляет собой алкильную группу с 3-8 атомами углерода, имеющую циклическую структуру. Примеры С 3-8-циклоалкильной группы включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу и циклооктильную группу. Из них предпочтительными являются С 3-6-циклоалкильные группы. Примеры "С 3-8-циклоалкильных групп" включают алкилзамещенные циклоалкильные группы, такие как 2,3,3-триметилциклобутильная группа, 4,4,6,6-тетраметилциклогексильная группа или 1,3 дибутилциклогексильная группа, и предпочтительны С 3-6-циклоалкильные группы, замещенные 1-3 C1-6 алкильными группами."С 4-8-Циклоалкенильная группа" представляет собой алкенильную группу с 4-8 атомами углерода,имеющую циклическую структуру. Примеры С 4-8-циклоалкенильной группы включают 1 циклобутенильную группу, 1-циклопентенильную группу, 1-циклогексенильную группу, 3 циклогексенильную группу, 3-циклогептенильную группу и 4-циклооктенильную группу. Примеры "замещенных С 4-8-циклоалкенильных групп" включают алкилзамещенные циклоалкенильные группы, такие как 2-метил-3-циклогексенильная группа или 3,4-диметил-3-циклогексенильная группа, и предпочтительны С 4-6-циклоалкенильные группы, замещенные 1-3 C1-6-алкильными группами."С 6-10-Арильная группа" представляет собой моноциклическую или полициклическую арильную группу с 6-10 атомами углерода. Кроме того, до тех пор, пока по меньшей мере один из циклов полициклической арильной группы является ароматическим циклом, остальные циклы могут представлять собой насыщенные алициклические циклы, ненасыщенные алициклические циклы или ароматические циклы. Примеры С 6-10-арильных групп включают фенильную группу, нафтильную группу, азуленильную группу, инденильную группу, инданильную группу и тетралинильную группу. Из них предпочтительной является фенильная группа. Примеры "замещенных С 6-10-арильных групп" включают алкилзамещенные арильные группы, галогензамещенные арильные группы и алкоксизамещенные арильные группы, такие как 2-хлорфенильная группа, 3,5-дихлорфенильная группа, 4-фторфенильная группа, 3,5-дифторфенильная группа, 4 трифторметилфенильная группа или 2-метокси-1-нафтильная группа, и предпочтительны С 1-6 алкилзамещенные С 6-10-арильные группы, галогензамещенные С 6-10-арильные группы и C1-6 алкоксизамещенные арильные группы."Гетероциклическая группа" представляет собой группу, которая содержит в качестве составляющих элементов цикла 1-4 гетероатома, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. Гетероциклическая группа может быть моноциклической или полициклической. Примеры гетероциклических групп включают 5-членные гетероарильные группы, 6-членные гетероарильные группы, конденсированные гетероарильные группы, насыщенные гетероциклические группы и частично ненасыщенные гетероциклические группы. Примеры 5-членных гетероарильных групп включают пирролильные группы, такие как пиррол-1 ильная группа, пиррол-2-ильная группа или пиррол-3-ильная группа; фурильные группы, такие как фуран-2-ильная группа или фуран-3-ильная группа; тиенильные группы, такие как тиофен-2-ильная группа или тиофен-3-ильная группа; имидазолильные группы, такие как имидазол-1-ильная группа, имидазол-2 ильная группа, имидазол-4-ильная группа или имидазол-5-ильная группа; пиразолильные группы, такие как пиразол-1-ильная группа, пиразол-3-ильная группа, пиразол-4-ильная группа или пиразол-5-ильная группа; оксазолильные группы, такие как оксазол-2-ильная группа, оксазол-4-ильная группа или оксазол 5-ильная группа; изоксазолильные группы, такие как изоксазол-3-ильная группа, изоксазол-4-ильная группа или изоксазол-5-ильная группа; тиазолильные группы, такие как тиазол-2-ильная группа, тиазол 4-ильная группа или тиазол-5-ильная группа; изотиазолильные группы, такие как изотиазол-3-ильная группа, изотиазол-4-ильная группа или изотиазол-5-ильная группа; триазолильные группы, такие как 1,2,3-триазол-1-ильная группа, 1,2,3-триазол-4-ильная группа, 1,2,3-триазол-5-ильная группа, 1,2,4 триазол-1-ильная группа, 1,2,4-триазол-3-ильная группа или 1,2,4-триазол-5-ильная группа; оксадиазолильные группы, такие как 1,2,4-оксадиазол-3-ильная группа, 1,2,4-оксадиазол-5-ильная группа или 1,3,4-оксадиазол-2-ильная группа; тиадиазолильные группы, такие как 1,2,4-тиадиазол-3-ильная группа,1,2,4-тиадиазол-5-ильная группа или 1,3,4-тиадиазол-2-ильная группа; и тетразолильные группы, такие как тетразол-1-ильная группа или тетразол-2-ильная группа. Примеры 6-членных гетероарильных групп включают пиридильные группы, такие как пиридин-2 ильная группа, пиридин-3-ильная группа или пиридин-4-ильная группа; пиразинильные группы, такие как пиразин-2-ильная группа или пиразин-3-ильная группа; пиримидинильные группы, такие как пиримидин-2-ильная группа, пиримидин-4-ильная группа или пиримидин-5-ильная группа; и пиридазинильные группы, такие как пиридазинин-3-ильная группа или пиридазинин-4-ильная группа. Примеры конденсированных гетероарильных групп включают индол-1-ильную группу, индол-2 ильную группу, индол-3-ильную группу, индол-4-ильную группу, индол-5-ильную группу, индол-6 ильную группу, индол-7-ильную группу, бензофуран-2-ильную группу, бензофуран-3-ильную группу,бензофуран-4-ильную группу, бензофуран-5-ильную группу, бензофуран-6-ильную группу, бензофуран 7-ильную группу, бензотиофен-2-ильную группу, бензотиофен-3-ильную группу, бензотиофен-4-ильную группу, бензотиофен-5-ильную группу, бензотиофен-6-ильную группу, бензотиофен-7-ильную группу,бензимидазол-1-ильную группу, бензимидазол-2-ильную группу, бензимидазол-4-ильную группу, бензимидазол-5-ильную группу, бензоксазол-2-ильную группу, бензоксазол-4-ильную группу, бензоксазол 5-ильную группу, бензотиазол-2-ильную группу, бензотиазол-4-ильную группу, бензотиазол-5-ильную группу, хинолин-2-ильную группу, хинолин-3-ильную группу, хинолин-4-ильную группу, хинолин-5 ильную группу, хинолин-6-ильную группу, хинолин-7-ильную группу, хинолин-8-ильную группу и подобные группы. Примеры других гетероциклических групп включают 3-членные насыщенные гетероциклические группы, такие как азиридин-1-ильная группа, азиридин-2-ильная группа или оксиранильная группа; 5 членные насыщенные гетероциклические группы, такие как пирролидин-1-ильная группа, пирролидин-2 ильная группа, пирролидин-3-ильная группа, тетрагидрофуран-2-ильная группа, тетрагидрофуран-3 ильная группа или [1,3]диоксиран-2-ильная группа; 6-членные насыщенные гетероциклические группы,такие как пиперидин-1-ильная группа, пиперидин-2-ильная группа, пиперидин-3-ильная группа, пиперидин-4-ильная группа, пиперазин-1-ильная группа, пиперазин-2-ильная группа, морфолин-2-ильная группа, морфолин-3-ильная группа или морфолин-4-ильная группа; и такие группы, как 1,3-бензодиоксол-4 ильная группа, 1,3-бензодиоксол-5-ильная группа, 1,4-бензодиоксол-5-ильная группа, 1,4-бензодиоксан 6-ильная группа,3,4-дигидро-2 Н-1,5-бензодиоксепин-6-ильная группа,3,4-дигидро-2 Н-1,5 бензодиоксепин-7-ильная группа, 2,3-дигидробензофуран-4-ильная группа, 2,3-дигидробензофуран-5 ильная группа, 2,3-дигидробензофуран-6-ильная группа и 2,3-дигидробензофуран-7-ильная группа. Примеры "замещенных гетероциклических групп" включают 4-хлор-2-пиридинильную группу, 3 хлор-2-пиразинильную группу, 4-метил-2-пиридинильную группу, 5-трифторметил-2-пиримидинильную группу и 3-метил-2-хинолинильную группу."C1-8-Ацильная группа" представляет собой группу, в которой атом водорода, C1-6-алкильная группа, C2-6-алкенильная группа, C2-6-алкинильная группа, С 6-7-арильная группа или 5-7-членная гетероциклическая группа связана с карбонильной группой. Примеры C1-8-ацильных групп включают формильную группу, алкилкарбонильную группу, такую как ацетильная группа, пропионильлная группа, н-пропилкарбонильная группа, н-бутилкарбонильная группа, пентаноильная группа, валерильная группа, октаноильная группа, изопропилкарбонильная группа, изобутилкарбонильная группа, пивалоильная группа или изовалерильная группа, и предпочтительныC1-6-алкилкарбонильные группы; алкенилкарбонильные группы, такие как акрилоильная группа или метакрилоильная группа, и предпочтительны C2-6-алкенилкарбонильные группы; алкинилкарбонильные группы, такие как пропионильная группа, и предпочтительны C2-6-алкинилкарбонильные группы; С 6-7 арилкарбонильные группы, такие как бензоильная группа; и гетероциклические карбонильные группы,такие как 2-пиридилкарбонильная группа или тиенилкарбонильная группа. Примеры "замещенных C1-8-ацильных групп" включают галогенацильные группы, такие как монофторацетильная группа, монохлорацетильная группа, монобромацетильная группа, дифторацетильная группа, дихлорацетильная группа, дибромацетильная группа, трифторацетильная группа, трихлорацетильная группа, трибромацетильная группа, 3,3,3-трифторпропионильная группа, 3,3,3-трихлорпропионильная группа или 2,2,3,3,3-пентафторпропионильная группа, и предпочтительны C1-8-галогенацильные группы."(1-Имино)С 1-8-алкильная группа" представляет собой иминометильную группу или группу, в которой C1-7-алкильная группа связана с иминометильной группой. Примеры (1-имино)С 1-8-алкильной группы включают иминометильную группу, (1-имино)этильную группу, (1-имино)пропильную группу, (1 имино)бутильную группу, (1-имино)пентильную группу, (1-имино)гексильную группу и (1 имино)гептильную группу. Из них предпочтительными являются (1-имино)С 1-6-алкильные группы. Примеры "замещенных (1-имино)С 1-8-алкильных групп" включают (1-гидроксиимино)алкильные группы, такие как гидроксииминометильная группа, (1-гидроксиимино)этильная группа, (1-гидроксиимино)пропильная группа или (1-гидроксиимино)бутильная группа, и предпочтительны (1 гидроксиимино)С 1-6-алкильные группы; и (1-алкоксиимино)алкильные группы, такие как метоксииминометильная группа, (1-этоксиимино)метильная группа, (1-метоксиимино)этильная группа, (1-третбутоксиимино)этильная группа или (1-этоксиимино)этильная группа, и предпочтительны (1 -(С 1-6 алкокси)имино)С 1-6-алкильные группы."Замещенная карбоксильная группа" представляет собой группу, в которой C1-6-алкильная группа,C2-6-алкенильная группа, C2-6-алкинильная группа, С 6-10-арильная группа, С 6-10-арилС 1-6-алкильная группа или 5-6-членная гетероциклическая группа связана с карбонильной группой. Примеры "замещенных карбоксильных групп" включают алкоксикарбонильные группы, такие как метоксикарбонильная группа, этоксикарбонильная группа, н-пропоксикарбонильная группа, изопропоксикарбонильная группа, н-бутоксикарбонильная группа, изобутоксикарбонильная группа, Третбутоксикарбонильная группа, н-пентилоксикарбонильная группа или н-гексилоксикарбонильная группа,и предпочтительны C1-6-алкоксикарбонильные группы; алкенилоксикарбонильные группы, такие как винилоксикарбонильная группа или аллилоксикарбонильная группа, и предпочтительны C2-6-алкенилоксикарбонильные группы; алкинилоксикарбонильные группы, такие как этинилоксикарбонильная группа или пропаргилоксикарбонильная группа, и предпочтительны C2-6-алкинилоксикарбонильные группы; арилоксикарбонильные группы, такие как феноксикарбонильная группа или нафтоксикарбонильная группа, и предпочтительны С 6-10-арилоксикарбонильные группы; и аралкилоксикарбонильные группы, такие как бензилоксикарбонильная группа, и предпочтительны С 6-10-арилС 1-6-алкоксикарбонильные группы."Замещенная карбамоильная группа" представляет собой группу, в которой C1-6-алкильная группа,C2-6-алкенильная группа, С 2-6-алкинильная группа, С 6-10-арильная группа, С 6-10-арилС 1-6-алкильная группа или 5-0-членная гетероциклическая группа связана с карбамоильной группой. Примеры "замещенных карбамоильных групп" включают моноалкилкарбамоильные группы или диалкилкарбамоильные группы, такие как метилкарбамоильная группа, этилкарбамоильная группа, диметилкарбамоильная группа или диэтилкарбамоильная группа, и предпочтительны моно-С 1-6 алкилкарбамоильные группы или ди-C1-6-алкилкарбамоильные группы; и моноарилкарбамоильные группы, такие как фенилкарбамоильная группа или 4-метилфенилкарбамоильная группа, и предпочтительны моно-С 6-10-арилкарбамоильные группы. Примеры "замещенных гидроксильных групп" включают алкоксигруппы, такие как метоксигруппа,этоксигруппа, н-пропоксигруппа, н-бутоксигруппа, н-пентилоксигруппа, н-гексилоксигруппа, децилоксигруппа, додецилоксигруппа, лаурилоксигруппа, изопропоксигруппа, изобутоксигруппа, вторбутоксигруппа, трет-бутоксигруппа, 1-этилпропоксигруппа, 1-гексилоксигруппа, 4-метилпентоксигруппа, 3-метилпентоксигруппа, 2-метилпентоксигруппа, 1-метилпентоксигруппа, 3,3-диметилбутоксигруппа, 2,2-диметилбутоксигруппа, 1,1-диметилбутоксигруппа, 1,2-диметилбутоксигруппа, 1,3-диметилбутоксигруппа, 2,3-диметилбутоксигруппа, 1-этилбутоксигруппа или 2-этилбутоксигруппа, и предпочтительны C1-6-алкоксигруппы; циклоалкилоксигруппы, такие как циклопропилметоксигруппа или 2-циклопентилэтоксигруппа, и предпочтительны С 3-8-циклоалкилС 1-6-алкоксигруппы; аралкилоксигруппы, такие как бензилоксигруппа,и предпочтительны С 6-10-арилС 1-6-алкоксигруппы; галогеналкоксигруппы, такие как хлорметоксигруппа,дихлорметоксигруппа, трихлорметоксигруппа, трифторметоксигруппа, 1-фторэтоксигруппа, 1,1 дифторэтоксигруппа, 2,2,2-трифторэтоксигруппа или пентафторэтоксигруппа, и предпочтительны C1-6 галогеналкоксигруппы; алкенилоксигруппы, такие как винилоксигруппа, 1-пропенилоксигруппа, аллилоксигруппа, 1 бутенилоксигруппа, 2-бутенилоксигруппа, 3-бутенилоксигруппа, 1-пентенилоксигруппа, 2-пентенилоксигруппа, 3-пентенил оксигруппа, 4-пентенилоксигруппа, 1-гексенилоксигруппа, 2-гексенилоксигруппа, 3-гексенилоксигруппа, 4-гексенилоксигруппа, 5-гексенилоксигруппа, 1-метил-2-пропенилоксигруппа, 2-метил-2-пропенилоксигруппа, 1-метил-2-бутенилоксигруппа или 2-метил-2-бутенилоксигруппа, и предпочтительны C2-6-алкенилоксигруппы; алкинилоксигруппы, такие как этинилоксигруппа, пропинилоксигруппа, пропаргилоксигруппа, 1 бутинилоксигруппа, 2-бутинилоксигруппа, 3-бутинилоксигруппа, 1-пентинилоксигруппа, 2-пентинилоксигруппа, 3-пентинилоксигруппа, 4-пентинилоксигруппа, 1-гексинилоксигруппа, 1-метил-2 пропинилоксигруппа,2-метил-3-бутинилоксигруппа,1-метил-2-бутинилоксигруппа,2-метил-3 пентинилоксигруппа или 1,1-диметил-2-бутинилоксигруппа,и предпочтительны сигруппа, нафтилоксигруппа, азуренилоксигруппа, инденилоксигруппа, инданилоксигруппа или тетралинилоксигруппа, и предпочтительны С 6-10-арилоксигруппы; арилалкилоксигруппы (аралкилоксигруппы), такие как бензилоксигруппа, фенетилоксигруппа или 2-нафтилметилоксигруппа, и предпочтительны С 6-10-арилС 1-6-алкилоксигруппы; ацилоксигруппы,такие как ацетилоксигруппа,пропионилоксигруппа,нпропилкарбонилоксигруппа, изопропилкарбонилоксигруппа, н-бутилкарбонилоксигруппа, изобутилкарбонилоксигруппа, пентаноилоксигруппа или пивалоилоксигруппа, и предпочтительны C1-7 ацилоксигруппы; алкоксикарбонилалкилоксигруппы, такие как метоксикарбонилметилоксигруппа или 1-метоксикарбонил-1-метилэтилоксигруппа, и предпочтительны C1-6-алкоксикарбонилС 1-6-алкоксигруппы; и триалкилсилилоксигруппы, такие как триметилсилилоксигруппа или трет-бутилдиметилсилилоксигруппа, и предпочтительны три-С 1-6-алкилсилилоксигруппы. Примеры "замещенных аминогрупп" включают алкиламиногруппы, такие как метиламиногруппа,этиламиногруппа, н-пропиламиногруппа, н-бутиламиногруппа, диметиламиногруппа или диэтиламиногруппа, и предпочтительны моно-C1-6-алкиламиногруппы или ди-С 1-6-алкиламиногруппы; моно-C1-6 алкилиденаминогруппы, такие как метилиденаминогруппа или этилиденаминогруппа; моноариламиногруппы, такие как фениламиногруппа или 4-метилфениламиногруппа, и предпочтительны моно-С 6-10 ариламиногруппы; диариламиногруппы, такие как ди-1-нафтиламиногруппа, и предпочтительны диС 6-10-ариламиногруппы; аралкиламиногруппы, такие как бензиламиногруппа, и предпочтительны С 6-10 арилС 1-6-алкиламиногруппы; ациламиногруппы, такие как ацетиламиногруппа, трифторацетиламиногруппа или бензоиламиногруппа, и предпочтительны C1-6-ациламиногруппы; и алкоксикарбониламиногруппы, такие как метоксикарбониламиногруппа или трет-бутоксикарбониламиногруппа, и предпочтительны C1-6-алкоксикарбониламиногруппы. Примеры "замещенных меркаптогрупп" включают алкилтиогруппы, такие как метилтиогруппа или этилтиогруппа, и предпочтительны C1-6-алкилтиогруппы; арилтиогруппы, такие как фенилтиогруппа или 4-метидфенилтиогруппа, и предпочтительны С 6-10-арилтиогруппы; и ацилтиогруппы, такие как ацетилтиогруппа или бензоилтиогруппа, и предпочтительны C1-6-ацилтиогруппы. Примеры "замещенных сульфонильных групп" включают алкилсульфонильные группы, такие как метилсульфонильная группа, этилсульфонильная группа, н-пропилсульфонильная группа, изопропилсульфонильная группа, н-бутилсульфонильная группа, изобутилсульфонильная группа, вторбутилсульфонильная группа, трет-бутилсульфонильная группа, н-пентилсульфонильная группа, изопентилсульфонильная группа, неопентилсульфонильная группа, 1-этилпропилсульфонильная группа, нгексилсульфонильная группа или изогексилсульфонильная группа, и предпочтительны C1-6 алкилсульфонильные группы; галогеналкилсульфонильные группы, такие как трифторметилсульфонильная группа, и предпочтительны С 1-6-галогеналкилсульфонильные группы; арилсульфонильлные группы, такие как фенилсульфонильная группа или 4-метилфенилсульфонильная группа, и предпочтительны С 6-10-арилсульфонильные группы; сульфогруппы; алкоксисульфонильные группы, такие как метоксисульфонильная группа или этоксисульфонильная группа, и предпочтительны C1-6 алкоксисульфонильные группы; сульфамоильные группы; сульфамоильные группы, такие как Nметилсульфамоильная группа, N-этилсульфамоильная группа, N,N-диметилсульфамоильная группа илиN,N-диэтилсульфамоильная группа, и предпочтительны моно-С 1-6-алкилсульфамоильные группы или диC1-6-алкилсульфамоильные группы; и моноарилсульфамоильные группы, такие как фенилсульфамоильная группа или 4-метилфенилсульфамоильная группа, и предпочтительны моно-С 6-10-арилсульфамоильные группы. Примеры "галогеногрупп" включают атом фтора, атом хлора, атом брома и атом иода.R1 и R2 могут вместе образовывать незамещенный или замещенный 5-8-членный цикл или могут образовывать группу =О, группу =CRaRb или группу =N-R'. В данном случае Ra представляет собой атом водорода или незамещенную или замещенную C1-8 алкильную группу. Rb представляет собой атом водорода или незамещенную или замещенную C1-8 алкильную группу. R' представляет собой незамещенную или замещенную гидроксильную группу или незамещенную или замещенную C1-8-алкильную группу. Примеры незамещенных или замещенных С 1-8-алкильных групп в Ra, Rb и R' являются такими же,как примеры "С 1-8-алкильных групп" для указанных выше R1-R3. Примеры замещенных гидроксильных групп в R' являются такими же, как примеры "замещенных гидроксильных групп" для указанных выше R1-R3. Примеры незамещенных или замещенных 5-8-членных циклов, которые могут быть образованы совместно R1 и R2, включают алифатические углеводородные циклы, такие как циклопропановый цикл,циклобутановый цикл, циклопентановый цикл, циклогексановый цикл, циклогептановый цикл или циклооктановый цикл, и предпочтительны С 3-8-циклоалкановые циклы; и ненасыщенные гетероциклы, такие как оксирановый цикл, [1,3]диоксирановый цикл, дигидро-2 Н-пирановый цикл, дигидро-2 Нтиопирановый цикл или тетрагидропиридиновый цикл, и предпочтительны кислородсодержащие 3-5 членные ненасыщенные гетероциклы.X1 соответственно и независимо представляет собой незамещенную или замещенную C1-8 алкильную группу, незамещенную или замещенную С 2-8-алкенильную группу, незамещенную или замещенную С 2-8-алкинильную группу, незамещенную или замещенную гидроксильную группу, галогеногруппу, цианогруппу или нитрогруппу.m представляет число X1 и равен целому числу от 0 до 5. Примеры групп, представленных X1, такие же, как примеры групп, представленных R1-R3. Предпочтительные примеры X1 включают C1-6-алкильные группы, C1-6-галогеналкильные группы,C2-6-алкенильные группы, С 3-8-циклоалкильные группы, гидроксильную группу, C1-6-алкоксигруппы и галогеногруппы.X2 соответственно и независимо представляет собой незамещенную или замещенную C1-8 алкильную группу, незамещенную или замещенную С 2-8-алкенильную группу, незамещенную или замещенную С 2-8-алкинильную группу, незамещенную или замещенную С 3-8-циклоалкильную группу, незамещенную или замещенную С 4-8-циклоалкенильную группу, незамещенную или замещенную С 6-10 арильную группу, незамещенную или замещенную гетероциклическую группу, незамещенную или замещенную C1-8-ацильную группу, незамещенную или замещенную (1-имино)C1-8-алкильную группу, незамещенную или замещенную карбоксильную группу, незамещенную или замещенную карбамоильную группу, незамещенную или замещенную гидроксильную группу, незамещенную или замещенную аминогруппу, незамещенную или замещенную меркаптогруппу, замещенную сульфонильную группу, галогеногруппу, цианогруппу или нитрогруппу.n представляет число X2 и равен целому числу от 0 до 3. Примеры групп, представленных X2, такие же, как примеры групп, представленных R1-R3. Предпочтительные примеры X2 включают C1-6-алкильные группы, C1-6-галогеналкильные группы,C1-6-алкильные группы, С 6-10-арилС 1-6-алкильные группы, С 3-8-циклоалкильные группы, С 6-10-арильные группы, C1-7-ацильные группы, C1-6-алкоксикарбонильные группы, C1-6-алкоксигруппы, аминогруппу,моно-C1-6-алкиламиногруппы, ди-С 1-6-алкиламиногруппы, C1-6-алкоксикарбониламиногруппы, С 1-6 алкилтиогруппы, C1-6-алкилсульфонильные группы, галогеногруппы, цианогруппу и нитрогруппу. В данном случае любой один из R1-R3 и любой один из X2 могут вместе образовывать незамещенный или замещенный 5-8-членный цикл. Примеры 5-8-членных циклов включают ароматические углеводородные циклы, такие как бензольный цикл; и С 5-8-циклоалкеновые циклы, такие как циклопентеновый цикл, циклопентадиеновый цикл,циклогексеновый цикл, циклогептеновый цикл или циклооктеновый цикл.[B, D]. В представляет собой атом углерода или атом азота. Иными словами, В входит в состав пиридинового цикла, в котором "D" конденсирован, или пиразиновый цикл, в котором "D" конденсирован.D представляет собой незамещенный или замещенный X1 5-7-членный углеводородный цикл или незамещенный или замещенный X1 5-7-членный гетероцикл. Примеры 5-7-членных углеводородных циклов включают ароматические углеводородные циклы,такие как бензольный цикл; С 5-7-циклоалкеновые циклы, такие как циклопентеновый цикл, циклогексеновый цикл или циклогептеновый цикл; ароматические 5-7-членные гетероциклы, такие как фурановый цикл, тиофеновый цикл, пирроловый цикл, имидазольный цикл, пиразольный цикл, тиазольный цикл,оксазольный цикл, изоксазольный цикл, пиридиновый цикл, пиразиновый цикл, пиримидиновый цикл,пиридазиновый цикл, азепиновый цикл или диазепиновый цикл; и ненасыщенные 5-7-членные гетероциклы, такие как дигидро-2 Н-пирановый цикл, дигидро-2 Н-тиопирановый цикл или тетрагидропиридиновый цикл. Из них предпочтительными являются ароматические углеводородные циклы, и более предпочтительным является бензольный цикл. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хинолиновый цикл или хиноксалиновый цикл.[А 1, А 2, А 3, А 4]. А 1, А 2, А 3 и А 4 соответственно и независимо представляют собой атом углерода или атом азота. А именно, А 1, А 2, А 3 и А 4 входят в состав бензольного цикла, пиридинового цикла, пиридазинового цикла,пиримидинового цикла, пиразинового цикла или триазинового цикла. Однако в случае, когда В представляет собой атом углерода, А 1-А 4 не все являются атомами углерода. Из них предпочтительным является пиридиновый цикл. Более предпочтителен пиридиновый цикл,в котором А 1 представляют собой атом азота. Никаких особенных ограничений в отношении солей соединения по настоящему изобретению не накладывается, при условии, что они являются приемлемыми для сельского хозяйства или садоводства. Примеры солей включают соли неорганических кислот, таких как хлороводородная кислота или серная кислота; соли органических кислот, таких как уксусная кислота или молочная кислота; соли щелочных металлов, таких как литий, натрий или калий; соли щелочно-земельных металлов, таких как кальций или магний, соли переходных металлов, таких как железо или медь; и соли органических оснований, таких как аммиак, триэтиламин, трибутиламин, пиридин или гидразин. Соединение, представленное вышеуказанной формулой (I), предпочтительно представляет собой соединение, представленное формулой (II) (также называется "соединение (II)"). Соединение, представленное формулой (II), представляет собой соединение, в котором "D" в формуле (I) представляет собой бензольный цикл. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хинолиновый цикл или хиноксалиновый цикл В данном случае R, X1, m, X2, n, А 1, А 2, А 3, А 4 и В в формуле (II) имеют указанные ранее значения. Соединение, представленное вышеуказанной формулой (II), предпочтительно представляет собой соединение, представленное формулой (III) (также называется "соединение (III)"), или соединение, представленное формулой (V) (также называется "соединение (V") Соединение, представленное формулой (III), представляет собой соединение, в котором "А 1" в формуле (II) представляет собой атом азота, и "А 2-А 4" представляют собой атомы углерода. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хинолиновый, хиноксалиновый или пиридиновый цикл. В данном случае R, X1, m, X2, n и В в формуле (III) имеют указанные ранее значения. Соединение, представленное вышеуказанной формулой (III), предпочтительно представляет собой соединение, представленное формулой (IV) (также называется "соединение (IV)")R, X1, m, X2 и n в формуле (IV) имеют указанные ранее значения. Соединение, представленное формулой (IV), представляет собой соединение, в котором "В" в формуле (III) представляет собой атом углерода. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хинолиновый цикл и пиридиновый цикл Соединение, представленное формулой (V), представляет собой соединение, в котором "В" в формуле (II) представляет собой атом азота, и "А 2-А 4" представляют собой атомы углерода. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хиноксалиновый цикл и бензольный или пиридиновый цикл. В данном случае R, X1, m, X2, n и А 1 в формуле (V) имеют указанные ранее значения. Соединение, представленное вышеуказанной формулой (V), предпочтительно представляет собой соединение, представленное формулой (VI) (также называется "соединение (VI)") Соединение, представленное формулой (VI), представляет собой соединение, в котором "А 1" в формуле (V) представляет собой атом азота. А именно, соединение по настоящему изобретению предпочтительно представляет собой соединение, имеющее хиноксалиновый цикл и пиридиновый цикл. В данном случае R, X1, m, X2 и n в формуле (VI) имеют указанные ранее значения. Способы получения соединений по настоящему изобретению Соединения по настоящему изобретению можно получать согласно способам синтеза, указанным ниже. Способ синтеза 1. В приведенных выше формулах R, X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. Q представляет собой атом галогена. Соединение, представленное формулой (I-1) (также называется соединение (I-1 можно получать взаимодействием соединения, представленного формулой (1), с соединением, представленным формулой(2), согласно известным методикам. В способе синтеза 1 7,8-дифтор-3-иодхинолин может быть использован в качестве промежуточного соединения. Способ синтеза 2. В приведенных выше формулах Q, R, X1, m, X2, n, D и А 1-А 4 имеют значения, указанные ранее. Соединение (I-1) можно получать взаимодействием соединения, представленного формулой (3), с соединением, представленным формулой (4), согласно известным методикам. В способе синтеза 2 полезными промежуточными соединениями являются 8-фтор-3 гидроксихинолин, 7,8-дифтор-3-гидроксихинолин, 8-фтор-3-гидрокси-2-метилхинолин или 7,8-дифтор-3 гидрокси-2-метилхинолин. Способ синтеза 3. В приведенных выше формулах X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. R1 и R2 представляют собой незамещенные или замещенные алкильные группы, незамещенные или замещенные алкенильные группы или незамещенные или замещенные алкинильные группы, примеры которых приводятся выше для R1-R3. Hal представляет собой атом галогена. Соединение, представленное формулой (I-3) (также называется соединение (I-3 можно получать взаимодействием 1 эквивалента реактива Гриньяра с соединением, представленным формулой (I-2), которое относится к типу соединения (I) (также называется соединение (I-2. Кроме того, когда во взаимодействие с соединением (I-2) вводят реактив Гриньяра в количестве, превышающим 1 эквивалент, кроме соединения (I-3) образуется соединение, представленное формулой (I-4) (также называется соединение(I-4, и соединение (I-4) можно получить при реакции с 2 эквивалентами реактива Гриньяра. В приведенных выше формулах R2, Hal, X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. G представляет собой удаляемую группу, такую как алкоксигруппа или атом галогена. Соединение, представленное формулой (I-6) (также называется соединение (I-6 можно получать взаимодействием 2 эквивалентов реактива Гриньяра с соединением, представленным формулой (I-5),которое относится к типу соединения (I) (также называется соединение (I-5. Кроме того, когда во взаимодействие с соединением (I-5) вводят реактив Гриньяра в количестве, превышающим 2 эквивалента,кроме соединения (I-6) образуется соединение, представленное формулой (I-7) (также называется соединение (I-7, и соединение (I-7) можно получать при реакции с 3 эквивалентами реактива Гриньяра. Способ синтеза 5. В приведенных выше формулах X1, m, X2, n, D и A1-A4 имеют указанные ранее значения. K1 и K2 представляют собой алкильные группы. Соединение, представленное формулой (I-9) (также называется соединение (I-9 можно получать гидролизом соединения, представленного формулой (I-8) (также называется соединение (I-8 с использованием известных методик. Кроме того, соединение, представленное формулой (I-10) (также называется соединение (I-10, можно синтезировать, позволяя алкилирующему агенту действовать в присутствии основания. Способ синтеза 6. В приведенных выше формулах Hal, R, X1, m, X2, n, D и Al-A4 имеют указанные ранее значения. X1 представляет собой незамещенную или замещенную алкоксигруппу, незамещенную или замещенную алкильную группу, незамещенную или замещенную алкенильную группу или незамещенную или заме- 14023328N-оксид, представленный формулой (I-11) (также называется соединение (I-11, можно получать окислением соединения (I-1) с использованием известных методик, таких как использование окислителя. Соединение, представленное формулой (I-12) (также называется соединение (I-12, можно получать воздействием известного галогенирующего агента, такого как оксихлорид фосфора, на соединение (I-11). Соединение, представленное формулой (I-13) (также называется соединение (I-13, можно синтезировать путем реакции нуклеофильного замещения или реакции сочетания с соединением (I-12) с использованием металлоорганического катализатора. Способ синтеза 7. В приведенных выше формулах R, X1, m, X2, n, D и A1-A4 имеют указанные ранее значения. Q представляет собой галогеногруппу. Соединение, представленное формулой (I-14) (также называется соединение (I-14, можно получать взаимодействием соединения, представленного формулой (5), и соединения, представленного формулой (6), согласно известным методикам. Способ синтеза 8. В приведенных выше формулах Q, R, X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. Соединение (I-14) можно получать взаимодействием соединения, представленного формулой (7), и соединения, представленного формулой (8), согласно известным методикам. Способ синтеза 9. В приведенных выше формулах X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. R1' и R2' представляют собой незамещенные или замещенные алкильные группы, незамещенные или замещенные алкенильные группы или незамещенные или замещенные алкинильные группы, примеры которых приводятся выше для R1-R3. Hal представляет собой галогеногруппу. Соединение, представленное формулой (I-16) (также называется соединение (I-16, можно получать взаимодействием 1 эквивалента реактива Гриньяра (R2'MgHal) с соединением, представленным формулой (I-15), которое относится к типу соединения (I) (также называется соединение (I-15. Кроме того, взаимодействием с соединением (I-15) 2 или больше эквивалентов реактива Гриньяра можно получить соединение, представленное формулой (I-17) (также называется соединение (I-17. В приведенных выше формулах R2', Hal, X1, m, X2, n, D и А 1-А 4 имеют указанные ранее значения. G представляет собой удаляемую группу, такую как алкоксигруппа или галогеногруппа. Соединение, представленное формулой (I-19) (также называется соединение (I-19, можно получать взаимодействием 2 эквивалентов реактива Гриньяра с соединением, представленным формулой (I18), которое относится к типу соединения (I) (также называется соединение (I-18. Кроме того, взаимодействием с соединением (I-19) 3 или более эквивалентов реактива Гриньяра можно получить соединение, представленное формулой (I-20) (также называется соединение (I-20. Соли соединений (I)-(VI) по настоящему изобретению можно получать путем контактирования производного неорганической кислоты, производного органической кислоты, производного щелочного металла, производного щелочно-земельного металла, аммониевого соединения или подобного соединения с соединениями (I)-(VI). В каждом из таких взаимодействий целевое соединение можно эффективно выделить с помощью обычных процедур последующей обработки, используемых в области синтетической органической химии после завершения реакции, и с помощью обычных известных способов разделения и очистки при соответствующей необходимости. Структуру целевого продукта можно определить и подтвердить, например, с помощью спектрального анализа методом 1 Н-ЯМР, ИК-спектрального анализом, анализа методом масс-спектрометрии или элементного анализа. 2) Фунгицид для сельского хозяйства или садоводства. Фунгицид для сельского хозяйства или садоводства по настоящему изобретению содержит в качестве своего активного ингредиента соединение по меньшей мере одного типа, выбранного из группы,состоящей из вышеуказанных азотсодержащих гетероциклических соединений, представленных формулами (I)-(VI), и их солей. Фунгицид по настоящему изобретению обладает превосходной фунгицидной активностью против широкого ряда типов грибов, таких как Oomycetes, Ascomycetes, Deuteromycetes или Basidiomycetes. Фунгицид по настоящему изобретению можно использовать для борьбы с различными болезнями,которые возникают во время выращивания сельскохозяйственных и садовых культур, включая цветущие растения, газонные травы и травы на пастбищах, путем обработки семян, опрыскивания листьев, внесения в почву, применения к водной поверхности или подобным способом. Например, фунгицид по настоящему изобретению можно использовать для борьбы со следующим: сахарная свекла - церкоспорозная пятнистость листьев (Cercospora beticola), корневая гниль aphanomyces (Aphanomyces cochlloides), корневая гниль (Thanatephorus cucumeris) или плесень листвы (Thanatephorus cucumeris); арахис - бурая пятнистость листьев (Mycosphaerella arachidis) или пятнистость листьев (Mysosphaerella berkeleyi); огурцы - настоящая мучнистая роса (Sphaerotheca fuliginea), ложная мучнистая роса (Pseudoperonospora cubensis), черная микосфереллзная гниль (Mycosphaerella melonis), стеблевая гниль (Fusarium oxysporum), склеральная гниль (Sclerotinia sclerotiorum), серая гниль (Botrytis cinerea), антракноз (Colletotrichum obriculare), парша (Cladosporium cucumerinum), коринеспорозная пятнистость листьев (Corynespora cassicola), черная ножка (Pythium debaryanam, Rhizoctonia solani Kuhn) или бактериальная пятнистость (Pseudomonas syringae pv. Lecrymans); томаты - серая гниль (Botrytis cinerea), плесень листвы (Cladosporium fulvum) или фитофтороз (Phytophthora infestans); баклажаны - серая гниль (Botrytis cinerea), черная гниль (Corynespora melongenae), настоящая мучнистая роса (Erysiphe cichoracearum) или плесень листвы (Mycovelloslella nattrassii); земляника - серая плесень (Botrytis cinerea), настоящая мучнистая роса (Sohaerotheca humuli), ан- 16023328 тракноз (Colletotrichum acutatum, Colletotrichum fragariae) или прекращение роста (Phytophthorasquamosa) или ложная мучнистая роса (Peronospora destructor); капуста - кила (Plasmodiophora brassicae), мокрая гниль (Erwinia carotovora) или ложная мучнистая роса (Peronospora parasitica); фасоль обыкновенная - стеблевая гниль (Sclerotinia sclerotiorum) или серая гниль (Botrytis cinerea); яблони - настоящая мучнистая роса (Podosphaera leucotricha), парша (Venturia inaequalis), монилиозberengeriana), антракноз (Glomerella cingulata, Colletotrichum acutatum), пятнистость (Diplocarpon mali),"мухосед" (Zygophiala jamaicensis) или сажистая пятнистость (Gloeodes pomigena); хурма - настоящая мучнистая роса (Phyllactinia kakicola), антракноз (Gloeosporium kaki) или угловатая пятнистость листьев (Cercospora kaki); персики - бурая гниль (Monilinia fructicola), парша (Cladosporium carpophilum) или гниль phomopsisPrunus avium - бурая гниль (Monolinia fructicola); виноград - серая гниль (Botrytis cinerea), настоящая мучнистая роса (Uncinula necator), гломереллзная гниль (Glomerella cingulata, Colletotrichum acutatum), ложная мучнистая роса (Plasmopara viticola),антракноз (Elsinoe ampelina), бурая гниль (Pseudocercospora vitis) или черная гниль (Guignardia bidwellii); груши - парша (Venturia nashicola), ржавчина (Gymnosporangium asiaticum), черная пятнистость (Alternaria kikuchiana), кольцевая гниль (Botryosphaeria berengeriana) или настоящая мучнистая роса (Phyllactinia mali); чай - серая пятнистость листьев (Pestalotia theae) или антракноз (Collectotrichum theae-sinensis); цитрусовые - парша (Elsinoe fawcetti), голубая плесень (Penicillium italicum), леечная плесень (Penicillium digitatum), серая гниль (Botrytis cinerea), меланоз (Diaporthe citri) или рак (Xanthomonas campestrispv. Citri); пшеница - настоящая мучнистая роса (Erysiphe graminis f. sp. tritici), фузариозная гниль (Gibberellazeae), листовая ржавчина (Puccinia recondita), бурая корневая гниль (Pythium iwayamai), снежная плесень(Septoria tritici), септориоз колосковой чешуи (Leptosphaeria nodorum), тифулез (Typhula incarnata), склеротелиоз (Myriosclerotinia borealis) или офиоболз (Gaeumanomyces graminis); ячмень - полосатость (Pyrenophora graminea), окаймленная пятнистость (Rhynchosporium secalis) или пыльная головня (Ustilago tritici, U. nuda); рис - пирикуляриоз (Pyricularia oryzae), ризоктониоз (Rhizoctonia solani), фузариоз (Gibberella fujikuroi), бурая пятнистость (Cochliobolus niyabeanus), полегание (Pythium graminicolum), бактериоз листьев(Xanthomonas oryzae), бактериальное полегание (Burkholderia plantarii), бактериальная желто-бурая пятнистость (Acidovorax avanae) или бактериальная гниль зерна (Burkholderia glumae); табак - склеротиниоз (Sclerotinia sclerotiorum) или плесень owdery (Erysiphe cichoracearum); тюльпаны - серая гниль (Botrytis cinerea); полевица - склеротиниоз (Sclerotinia borealis) или бактериальная серая гниль (Pythium aphanidermatum); ежа сборная - настоящая мучнистая роса (Erysiphe graminis); соя - пурпурное окрашивание (Cercospora kikuchii), ложная мучнистая роса (PeronosporaManshurica) или стеблевая гниль (Phytophthora sojae); или картофель и томаты - фитофтороз (Phytophthora infestans). Кроме того, фунгицид по настоящему изобретению также обладает превосходной фунгицидной активностью против резистентных организмов. Примеры резистентных организмов включают серую гниль(Botrytis cinerea), церкоспорозную пятнистость листьев сахарной свеклы (Cercospora beticola), яблоневую паршу (Venturia inaequalis) и паршу груши (Venturia nashicola), которые обладают резистентностью к бензимидазольным фунгицидам, таким как тиофанат-метил, бемоил или карбендазим; и серую гниль(Botrytis cinerea), которая обладает резистентностью к дикарбоксиимидным бактерицидам (таким как винклозолин, процимидон или ипродион). Примеры болезней, в случае которых применение фунгицида по настоящему изобретению, оказывается, является более предпочтительным, включают паршу яблонь, серую гниль огурцов, настоящую мучнистую росу пшеницы, фитофтороз томатов, листовую ржавчину пшеницы, пирикуляриоз риса и стеблевую гниль огурцов. Кроме того, фунгицид по настоящему изобретению вызывает незначительные химические повреждения, обладает низкой токсичностью для рыбы и теплокровных животных и имеет высокую степень безопасности. Фунгицид по настоящему изобретению можно использовать в той форме, которую можно использовать для сельскохозяйственных химических препаратов, а именно в форме химического препарата для сельского хозяйства, такого как смачивающийся порошок, гранулы, порошок, эмульсия, водный раствор,суспензия или смачивающиеся гранулы. Примеры добавок и носителей, используемых в твердых препаратах, включают растительные порошки, такие как соевый порошок или порошок из зерен пшеницы, минеральные мелкодисперсные порошки, такие как диатомитовая земля, апатит, гипс, тальк, бентонит, пирофилит или глина, и органические или неорганические соединения, такие как бензоат натрия, мочевина или сульфат натрия. Примеры растворителей, используемых в жидких препаратах, включают керосин, ксилол и нефтяные ароматические углеводороды, циклогексан, циклогексанон, диметилформамид, диметилсульфоксид,спирт, ацетон, трихлорэтилен, метилизобутилкетон, минеральное масло, растительное масло и воду. Кроме того, в такие препараты при необходимости можно добавлять поверхностно-активное вещество, для того чтобы получить однородную и устойчивую форму. Никаких особенных ограничений в отношении поверхностно-активных веществ, которые можно добавлять, не накладывается. Примеры таких поверхностно-активных включают неионогенные поверхностно-активные вещества, такие как простые полиоксиэтиленалкилфениловые эфиры, сложные полиоксиэтиленалкиловые эфиры, полиоксиэтилированные эфиры высших жирных кислот, полиоксиэтиленсорбитановые эфиры высших жирных кислот или полиоксиэтилентристирилфениловые эфиры и соли эфиров серной кислоты и полиоксиэтиленалкилфениловых эфиров, алкилбензолсульфонаты, соли эфиров серной кислоты и высших спиртов, алкилнафталинсульфонаты, поликарбоксилаты, лигнинсульфонаты, формальдегидные конденсаты алкилнафталинсульфонатов и сополимеры изобутилена и малеинового ангидрида. Смачивающиеся порошки, эмульсии, текучие средства, водные растворы или смачивающиеся гранулы, полученные вышеуказанным путем, используют, разбрызгивая на растения в форме растворов,суспензий или эмульсий после разбавления соответствующих концентратов водой. Кроме того, порошки и гранулы используют путем распыления непосредственно на растения. Обычно количество активного ингредиента в фунгициде по настоящему изобретению составляет предпочтительно 0,01-90 мас.% и более предпочтительно 0,05-85 мас.% от общей массы препарата. Хотя применяемое количество фунгицида по настоящему изобретению изменяется в соответствии с погодными условиями, формой препарата, временем нанесения, способом нанесения, местом нанесения,болезни, от которой лечат, целевой культуры и подобными факторами, оно обычно составляет 1-1000 г и предпочтительно 10-100 г активного ингредиента на гектар. В случае применения путем разбавления водой смачивающегося порошка, эмульсии, суспензии,водного раствора, смачивающихся гранул или подобной формы используемая концентрация составляет 1-1000 ч./млн и предпочтительно 10-250 ч./млн. Фунгицид по настоящему изобретению также можно смешивать с другими фунгицидами, инсектицидами, акарицидами, регуляторами роста растений или синергистами. Типичные примеры других фунгицидов, инсектицидов, акарицидов и регуляторов роста растений,которые можно использовать, смешивая с фунгицидом по настоящему изобретению, указаны ниже. Фунгициды:(1) фунгициды на основе бензимидазолов: беномил, карбендазим, фуберидазол, тиабендазол, тиофанат-метил и т.п.;(2) фунгициды на основе дикарбоксиимидов: хлозолинат, ипродион, процимидон, винклозолин и т.п.;(4) фунгициды на основе фениламидов: беналаксил, фуралаксил, металаксил, металаксил-М, оксадиксил, офурас и т.п.;(5) фунгициды на основе аминов: альдиморф, додеморф, фенпропиморф, тридеморф, фенпропидин,пипералин, спироксамин и т.п.;(6) фунгициды на основе фосфотиолатов: EDDP, ипробенфос, пиразофос и т.п.;(7) фунгициды на основе дитиоланов: изопротиолан и т.п.;(8) фунгициды на основе карбоксамидов: беноданил, боскалид, карбоксин, фенфурам, флутоланил,фураметпир, мепронил, оксикарбоксин, пентиопирад, тифлузамид и т.п.;(9) фунгициды на основе гидрокси(2-амино)пиримидина: бупиримат, диметиримол, этиримол и т.п.;(11) фунгициды на основе N-фенилкарбаматов: диэтофенкарб и т.п.;(12) фунгициды на основе QoI (ингибиторов Qo): азоксистробин, пикокситробин, пираклостробин,крезоксим-метил, трифлоксистробин, димоксистробин, метоминостробин, оризастробин, фамоксадон,- 18023328(13) фунгициды на основе РР (фенопирролов): фенопиконил, флудиоксонил и т.п.;(14) фунгициды на основе хинолинов: хиноксифен и т.п.;(15) фунгициды на основе АН (ароматических углеводородов): бифенил, хлоронеб, диклоран, хинтозол, текназол, труктофосметил и т.п.;(16) фунгициды на основе MBI-R: фталид, пирохилон, трициклазол и т.п.;(17) фунгициды на основе MBI-D: карпропамид, диклоцимет, феноксанил и т.п.;(18) фунгициды на основе SBI: фенгексамид, пирибутикарб, тербинафин и т.п.;(19) фунгициды на основе фенилмочевины: пенцикурон и т.п.;(20) фунгициды на основе QiI (ингибиторов Qi): циазофамид и т.п.;(21) фунгициды на основе бензамидов: зоксамид и т.п.;(22) фунгициды на основе энопиранурона: бластицидин, милдиомицин и т.п.;(23) фунгициды на основе гексопиранозилов: казугамицин и т.п.;(24) фунгициды на основе глюкопиранозилов: стрептомицин, валидамицин и т.п.;(25) фунгициды на основе цианоацетамидов: цимоксанил и т.п.;(26) фунгициды на основе карбаматов: иодокарб, пропамокарб, протиокарб, поликарбамат и т.п.;(27) фунгициды на основе разъединяющих агентов: бинапакрил, динокап, феримзон, флуазинам и т.п.;(28) фунгициды на основе оловоорганических соединений: ацетат трифенилолова, хлорид трифенилолова, гидроксид трифенилолова и т.п.;(30) фунгициды на основе фталамовой кислоты: теклофталам и т.п.;(31) фунгициды на основе бензотриазинов: триазоксид и т.п.;(32) фунгициды на основе бензолсульфонамидов: флусульфамид и т.п.;(33) фунгициды на основе пиридазинонов: дикломезин и т.п.;(34) фунгициды на основе САА (амидов карбоновых кислот) и подобные: диметоморф, флуморф,бентиаваликарб, ипроваликарб, мандипропамид и т.п.;(35) фунгициды на основе тетрациклинов: окситетрациклин и т.п.;(36) фунгициды на основе тиокарбаматов: метасульфокарб и т.п.;(1) средства на основе органо(тио)фосфатов: ацефат, азаметиофос, азинфос-метил, азинфос-этил,бромофос-этил, бромфенвинфос, BRP, хлорпирифос, хлорпирифос-метил, хлорпирифос-этил, хлорфенвинфос, кадузафос, карбофенотион, хлорэтоксифос, хлормефос, кумафос, цианофенфос, цианофос, CYAP, диазинон, дихлофос, дикротофос, диметоат, дисульфотон, диметон-S-метил, диметилвинфос, диметон-S-метилсульфон, диалифос, диазинон, дихлофентион, диоксабензофос, дисульфотон, этион, этопрофос, этримфос, EPN, фенамифос, фенитротион, фентион, фенсульфотион, флупиразофос, фонофос, формотион, фосметилан, гептенофос, изафос, иодфенфос, изофенфос, изоксатион, ипробенфос, мелатион,мевинфос, метамидофос, митидатион, монокротофос, мекарбам, метакрифос, налед, ометоат, оксидметон-метил, параоксон, паратион, паратион-метил, фентоат, фозалон, фосмет, фосфамид, форат, фоксим,пиримифос-метил, пиримифос-этил, профенофос, протиофос, фостиазат, фосфокарб, пропафос, пропетамфос, протоат, пиридафентион, пираклофос, хиналфос, салитион, сульпрофос, сульфотеп, тетрахлорвинфос, тербуфос, триазофос, трихлорфон, тебупиримфос, темефос, тиометон, вамидотион;(2) средства на основе карбаматов: аланикарб, альдикарб, бендиокарб, бенфуракарб, карбарил, карбофуран, карбосульфан, феноксикарб, фенотиокарб, метиокарб, метомил, оксамил, пиримикарб, пропоксур, тиодикарб, триазамат, этиофенкарб, фенобукарб, MIPC, МРМС, МТМС, пиридафентион, фуратиокарб, ХМС, альдоксикарб, алликсикарб, аминокарб, буфенкарб, бутакарб, бутокарбоксим, бутоксикарбоксим, клоэтокарб, диметилан, форметанат, изопрокарб, метамнатрий, метокарб, промекарб, тиофанокс,триметакарб, ксиликарб;(3) средства на основе пиретроидов: аллетрин, бифентрин, цифлутрин, бета-цифлутрин, цигалотрин, лямбда-цигалотрин, цифенотрин, циперметрин, альфа-циперметрин, бета-циперметрин, дзетациперметрин, дельтаметрин, эсфенвалерат, этофенпрокс, фенпропатрин, фенвалерат, имипротрин, перметрин, праллетрин, пиретрин, пиретрин I, пиретрин II, ресметрин, силафлуофен, флувалинат, тефлутрин, тетраметрин, тралометрин, трансфлутрин, профлутрин, димефлутрин, акринатрин, циклопротрин,нальфенпрокс, флуцитринат, биоаллетрин, биоэтанометрин, биоперметрин, биоресметрин, транспермет- 19023328(13) ингибиторы оксидаз со смешанными функциями: пиперонилбутоксид;(15) микробные пестициды: средства ВТ, патогенные для насекомых вирусные средства, патогенные для насекомых грибковые средства, патогенные для нематод грибковые средства; вид Bacillus, вид(20) стимулируемые магнием ингибиторы АТФазы: тиоциклам, тиосультап, нерейстоксин;(a) средства на основе бензимидазолов: фенбендазол, альбендазол, триклабендазол, оксибендазол;(b) средства на основе салициланилидов: клозантел, оксиклозанид;(c) средства на основе замещенных фенолов: нитроксинил;(d) средства на основе пиримидинов: пирантел;(e) средства на основе имдазотиазолов: левамизол;(f) средства на основе тетрагидропиримидинов: празиквантел;(g) другие антигельминтные средства: циклодиен, риания, клорсулон, метронидазол; регуляторы роста растений: абсцизовая кислота, индолмасляная кислота, униконазол, этихлозат, этефон, клоксифонак, хлормекват, экстракт хлореллы, пероксид кальция, цианамид, дихлорпроп, гиббереллин, даминозид, дециловый спирт, тринексапак-этил, мепикватхлорид, паклобутразол, парафиновый воск, пиперонилбутоксид, пирафлуфен-этил, флурпримидол, прогидроясмон, кальциевая соль прогексадиона, бензиламинопурин,пендиметалин, форхлорфенурон, малеат гидразида калия, 1-нафтилацетоамид, 4-СРА, МСРВ, холин,сульфат оксихинолина, этихлозат, бутралин, 1-метилциклопропен и гидрохлорид авиглицина. Примеры Хотя далее приводится более детальное разъяснение настоящего изобретения со ссылкой на примеры, настоящее изобретение не ограничивается этими примерами. Пример 1. Синтез 3-(2-цианопиридин-3-илокси)-8-фтор-2-метилхинолина Растворяют 4,9 г 8-фтор-3-гидрокси-2-метилхинолина, 3,2 г 3-хлор-2-цианопиридина и 3,8 г карбоната калия в 20 мл N-метилпирролидона и затем перемешивают в течение 3 ч при 130 С. Затем реакционный раствор охлаждают до комнатной температуры и затем добавляют воду и проводят экстракцию этилацетатом. Экстракт промывают крепким рассолом и сушат над сульфатом магния и затем отгоняют растворитель при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле и получают 5,37 г 3-(2-цианопиридин-3-илокси)-8-фтор-2-метилхинолина. Пример 2. Синтез 1-[3-(2-метил-8-фторхинолин-3-илокси)пиридин-2-ил]этанона (соединение а-9) Растворяют 2,51 г 3-(2-цианопиридин-3-илокси)-8-фтор-2-метилхинолина в 30 мл обезвоженного тетрагидрофурана. К раствору при охлаждении льдом по каплям добавляют 3,6 мл 3 М раствора метилмагнийхлорида в тетрагидрофуране и затем реакционный раствор перемешивают в течение 2 ч, продолжая охлаждение льдом. Затем реакционный раствор добавляют к 1N соляной кислоте с последующей нейтрализацией водным раствором бикарбоната натрия и затем смесь экстрагируют этилацетатом. Экстракт промывают крепким рассолом и сушат над сульфатом магния и затем отгоняют растворитель при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле и получают 1,7 г 1-[3-(2-метил-8-фторхинолин-3-илокси)пиридин-2-ил]этанона. Пример 3. Синтез 2-[(8-фтор-2-метилхинолин-3-илокси)пиридин-2-ил]пропан-2-ола (соединение а-7) Растворяют 1,58 г 1-[3-(2-метил-8-фторхинолин-3-илокси)пиридин-2-ил]этанона в 20 мл обезвоженного тетрагидрофурана. К раствору при охлаждении льдом по каплям добавляют 2,7 мл 3 М раствора метилмагнийхлорида в тетрагидрофуране и затем реакционный раствор перемешивают в течение 3 ч,продолжая охлаждение льдом. Затем реакционный раствор добавляют к 1N соляной кислоте с последующей нейтрализацией водным раствором бикарбоната натрия и затем смесь экстрагируют этилацетатом. Экстракт промывают крепким рассолом и сушат над сульфатом магния и затем отгоняют растворитель при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле и получают 1,69 г 2-[(8-фтор-2-метилхинолин-3-илокси)пиридин-2-ил]пропан-2-ола. Пример 4. Синтез 3-[2-(2-метокси-2-пропил)пиридин-3-илокси]-8-фтор-2-метилхинолина (соединение а-16) Растворяют 0,50 г 2-[(8-фтор-2-метилхинолин-3-илокси)пиридин-2-ил]пропан-2-ола и 0,45 г метилиодида в 10 мл диметилфлормамида. К раствору при охлаждении льдом добавляют 64 мг гидрида натрия (60% суспензия в масле) и затем смесь перемешивают в течение 2 ч, продолжая охлаждение льдом. Затем реакционный раствор выливают в смесь воды со льдом и затем смесь экстрагируют этилацетатом. Экстракт промывают крепким рассолом и сушат над сульфатом магния и затем отгоняют растворитель при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле и получают 0,15 г 3-[2-(2-метокси-2-пропил)пиридин-3-илокси]-8-фтор-2-метилхинолина. Пример 5. Синтез 3-[2-(2-этокси-2-пропил)пиридин-3-илокси]-8-фтор-2-метилхинолина (соединение а-56) Растворяют 0,53 г 2-[(8-фтор-2-метилхинолин-3-илокси)пиридин-2-ил]пропан-2-ола в 10 мл хлороформа. К раствору при комнатной температуре добавляют 0,61 г тионилхлорида и затем перемешивают в течение 30 мин при комнатной температуре. Затем растворитель и избыток тионилхлорида отгоняют при пониженном давлении, затем остаток растворяют в этаноле и затем кипятят с обратным холодильником в течение 1 ч. Затем реакционный раствор концентрируют при пониженном давлении, к остатку добавляют воду и затем смесь экстрагируют этилацетатом. Экстракт промывают крепким рассолом и сушат над сульфатом магния и затем отгоняют растворитель при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле и получают 0,19 г 3-[2-(2-этокси-2-пропил)пиридин-3 илокси]-8-фтор-2-метилхинолина. Пример 6. Синтез 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионитрила (соединение а-11). Стадия 1). Синтез 2-(3-бромпиридин-2-ил)-2-метилпропионитрила. Растворяют 2,25 г (3-бромпиридин-2-ил)ацетонитрила в 30 мл диметилформамида. К раствору при 0 С добавляют 1,09 г гидрида натрия (60% суспензия в масле). В продолжение к реакционному раствору добавляют 3,9 г метилиодида и затем раствор перемешивают в течение 1,5 ч. Затем добавляют разбавленную соляную кислоту и затем смесь экстрагируют этилацетатом. Растворитель из органического слоя отгоняют, затем остаток очищают колоночной хроматографией на силикагеле и получают 2,68 г 2-(3 бромпиридин-2-ил)-2-метилпропионитрила. Стадия 2). Синтез 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионитрила Растворяют 1,35 г 2-(3-бромпиридин-2-ил)-2-метилпропионитрила в 6 мл N-метилпирролидона. К раствору добавляют 0,82 г 8-фтор-3-гидроксихинолина, 1,95 г карбоната цезия, 0,18 г дипивалоилметана и 0,50 г хлорида меди(I) и затем смесь перемешивают в течение 23 ч при 130 С. Затем реакционную смесь охлаждают до комнатной температуры, очищают колоночной хроматографией на силикагеле и получают 0,46 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионитрила. Пример 7. Синтез этилового эфира 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионовой кислоты (соединение а-12) К 0,38 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионитрила добавляют 2 мл этанола и 2 мл концентрированной серной кислоты. Смесь перемешивают в течение 6 ч при 100 С. Затем к смеси добавляют насыщенный водный раствор гидрокарбоната натрия для прекращения реакции. Затем полученную смесь экстрагируют этилацетатом и затем растворитель из органического слоя отгоняют. Затем полученный остаток очищают колоночной хроматографией на силикагеле и получают 0,24 г этилового эфира 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионовой кислоты. Пример 8. Синтез 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионовой кислоты (соединение а-19) Растворяют 0,33 г этилового эфира 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2 метилпропионовой кислоты в 1 мл этанола. К раствору добавляют 2 мл 4 N водного раствора гидроксида натрия и затем смесь кипятят с обратным холодильником в течение 48 ч. Затем к реакционной смеси добавляют разбавленную соляную кислоту, затем смесь экстрагируют этилацетатом, растворитель из органического слоя отгоняют и получают 0,25 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионовой кислоты. Растворяют 0,10 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропионовой кислоты и 0,08 диизопропилэтиламина в 1,2 мл диметилформамида. К раствору добавляют 0,3 мл 2,0 М раствора этиламина в тетрагидрофуране и 0,17 г гексафторфосфата О-(бензотриазол-1-ил)-N,N,N',N'тетраметилурония и затем смесь перемешивают в течение 14 ч при комнатной температуре. Затем реакционный раствор экстрагируют этилацетатом и затем отгоняют растворитель из органического слоя. Затем полученный остаток очищают колоночной хроматографией на силикагеле и получают 0,10 г N-этил 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]изобутиламида. Пример 10. Синтез 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропиоальдегида (соединение а-21). Стадия 1). Синтез 2-(3-бромпиридин-2-ил)-2-метилпропиоальдегида. Растворяют 1,8 г 2-(3-бромпиридин-2-ил)-2-метилпропионитрила в 20 мл толуола. К раствору при 0 С добавляют 5,9 мл 25 мас.% раствора гидрида диизобутилалюминия в толуоле. Смесь перемешивают в течение 17 ч при комнатной температуре. Затем к смеси добавляют разбавленную соляную кислоту для растворения непрорегировавшего гидрида диизобутилалюминия. В продолжение к смеси добавляют водный насыщенный раствор гидрокарбоната натрия и затем смесь экстрагируют этилацетатом. Растворитель из органического слоя отгоняют, затем остаток очищают колоночной хроматографией на силикагеле и получают 0,44 г 2-(3-бромпиридин-2-ил)-2-метилпропиоальдегида. Стадия 2). Синтез 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропиоальдегида Растворяют 0,41 г 2-(3-бромпиридин-2-ил)-2-метилпропиоальдегида в 4 мл N-метилпирролидона. К раствору добавляют 0,59 г 8-фтор-3-гидроксихинолина, 1,2 г карбоната цезия, 0,07 г дипивалоилметана и 0,18 г хлорида меди(I) и затем смесь перемешивают в течение 16 ч при 130 С. Затем реакционную смесь охлаждают до комнатной температуры, очищают колоночной хроматографией на силикагеле и получают 0,19 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропиоальдегида. Пример 11. Синтез 3-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-3-метилбутан-2-ола Растворяют 0,10 г 2-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-2-метилпропиоальдегида в 3 мл тетрагидрофурана. К раствору добавляют 0,2 мл 3,0 М раствора метилмагнийхлорида в тетрагидрофуране и затем перемешивают в течение 30 мин при 0 С. Затем к смеси добавляют воду для прекращения реакции. Затем полученную смесь экстрагируют этилацетатом, затем растворитель из органического слоя отгоняют, остаток очищают колоночной хроматографией на силикагеле и получают 0,07 г 3-[3-(8 фторхинолин-3-илокси)пиридин-2-ил]-3-метилбутан-2-ола. Пример 12. Синтез 3-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-3-метилбутан-2-она (соединение а-15) Растворяют 0,07 г 3-[3-(8-фторхинолин-3-илокси)пиридин-2-ил]-3-метилбутан-2-ола в 3 мл дихлорметана. К раствору при 0 С добавляют 0,27 г реагента Десс-Мартина и затем перемешивают в течение 30 мин. Затем реакционный раствор концентрируют, затем остаток очищают колоночной хроматографией на силикагеле и получают 0,04 г 3-[3 -(8-фторхинолин-3-илокси)пиридин-2-ил]-3-метилбутан-2-она. Хотя дальнейшее изложение дает более детальное пояснение получения промежуточных соединений для соединений по настоящему изобретению в ссылочных примерах, получение промежуточных соединений не ограничивается приведенными далее ссылочными примерами. Ссылочный пример 1. Синтез 7,8-дифтор-3-гидрокси-2-метилхинолина. Стадия 1). Синтез 6,7-дифторизатина К 825 мл воды добавляют 15,7 г 2,3-дифторанилина, затем добавляют 24,2 г трихлорацетальдегида,30,8 г гидрохлорида гидроксиламина и 138,6 г безводного сульфата натрия и смесь перемешивают в течение 10 ч при 50 С. После охлаждения до комнатной температуры к смеси добавляют 44 мл 2N соляной кислоты и затем смесь перемешивают в течение 30 мин. Затем кристаллическое вещество удаляют фильтрацией. Полученное кристаллическое вещество сушат, затем добавляют при 70 С к горячей концентрированной серной кислоте и затем смесь перемешивают в течение 1 ч при 80-90 С. Затем реакционный раствор выливают на лед и экстрагируют этилацетатом. Органический слой промывают крепким рассолом и сушат над сульфатом магния, затем отгоняют растворитель при пониженном давлении и получают 26 г сырого 6,7-дифторизатина. Стадия 2). Синтез 7,8-дифтор-3-гидрокси-2-метилхинолина К 200 мл воды добавляют 41 г неочищенного продукта 6,7-дифторизатина и затем при охлаждении льдом добавляют 75,3 г (6 эквивалентов) гидроксида калия, и перемешивают смесь в течение 30 мин. К полученной суспензии при температуре 20-25 С добавляют по каплям 42 г (1,4 эквивалента) бромацетофенона. По завершении прикапывания реакционную смесь перемешивают в течение ночи при комнатной температуре. Затем полученную смесь нейтрализуют концентрированной соляной кислотой. Выпавшее в осадок кристаллическое вещество извлекают фильтрацией и промывают небольшим количеством воды. Полученное кристаллическое вещество сушат и затем добавляют к 100 мл нитробензола за малое время при 130-140 С. По завершении добавления реакционную смесь перемешивают в течение 1 ч при 150 С. После охлаждения реакционной смеси до комнатной температуры выпавшее в осадок кристаллическое вещество промывают хлороформом и получают 26,3 г 7,8-дифтор-3-гидрокси-2-метилхинолина. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, ДМСО-d6)2,57 (с, 3 Н), 7,4-7,7 (м, 3 Н), 10,60 (ушс, 1 Н). 8-Фтор-3-гидрокси-2-метилхинолин получают согласно такому же способу. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, ДМСО-d6)2,56 (с, 3 Н), 7,2-7,6 (м, 4 Н), 10,53 (ушс, 1 Н). Ссылочный пример 2. Синтез 7,8-дифтор-3-гидроксихинолина. Стадия 1). Синтез 7,8-дифторхинолина Загружают 607,7 г (49,57 моль) 80% серной кислоты в 3-л баклажановидную колбу, содержащую мешалку и затем охлаждают до 0 С. Постепенно добавляют в колбу 160,0 г (1,24 моль) 2,3 дифторанилина. По завершении добавления реакционную смесь перемешивают в течение 1 ч при комнатной температуре. Затем к смеси добавляют 1,85 г (12,3 ммоль) иодида натрия и затем колбу нагревают на масляной бане при 150 С. Когда температура жидкости достигнет 150 С, в нее по каплям в течение 1 ч добавляют 125,5 г (1,36 моль) глицерина. По завершении прикапывания реакционную смесь перемешивают в течение 1 ч при 150 С. Далее, температуру масляной бани поднимают до 180 С. Отгоняют воду в течение 2 ч с использованием аппаратуры для перегонки. После подтверждения удаления исходных материалов реакционную смесь нейтрализуют 10N водным раствором гидроксида натрия при охлаждении на бане со смесью воды и льда (внутренняя температура 60-70 С). После нейтрализации реакци- 24023328 онную смесь экстрагируют этилацетатом до возвращения внутренней температуры к комнатной температуре и затем экстракт сушат над сульфатом магния, фильтруют и концентрируют. Полученный сырой продукт реакции очищают колоночной хроматографией на силикагеле (н-гексан: этилацетат) и получают 185,5 г (91%) 7,8-дифторхинолина в форме светло-коричневого твердого вещества. Стадия 2). Синтез 7,8-дифтор-3-иодхинолина Загружают 185,5 г (1,12 моль) 7,8-дифторхинолина, 505,4 г (2,25 моль) N-иодсукцинимида и 927 мл уксусной кислоты в 3-л баклажановидную колбу, содержащую мешалку и затем смесь перемешивают в течение 30 ч при 90 С. После охлаждения полученной смеси выпавшее в осадок кристаллическое вещество отфильтровывают и сушат. Фильтрат концентрируют при пониженном давлении и оставшуюся уксусную кислоту нейтрализуют гидрокарбонатом натрия, после чего смесь экстрагируют этилацетатом. Экстракт сушат над сульфатом магния, фильтруют и концентрируют. Полученный сырой продукт реакции очищают колоночной хроматографией на силикагеле (н-гексан: этилацетат). Полученное вещество объединяют с полученным ранее кристаллическим веществом и получают 227,2 г (70%) 7,8-дифтор-3-иодхинолина в форме светло-коричневого твердого вещества. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, CDCl3)7,39-7,51 (м, 2 Н), 8,55 (м, 1 Н), 9,08 (д, 1 Н, J=2,1 Гц). Стадия 3). Синтез 7,8-дифтор-3-гидроксихинолина(0,078 моль) CuI и 28,1 г (0,156 моль) 1,10-фенантролина. Реакционную смесь нагревают до 100 С на масляной бане и затем смесь перемешивают в течение 24 ч. После охлаждения к смеси добавляют этилацетат и воду и затем органический слой удаляют. Полученный водный слой нейтрализуют концентрированной соляной кислотой. Выпавшее в осадок кристаллическое вещество отфильтровывают и сушат. Фильтрат экстрагируют этилацетатом, затем экстракт сушат над сульфатом магния, фильтруют и концентрируют. Полученный сырой продукт реакции очищают колоночной хроматографией на силикагеле (н-гексан: этилацетат). Полученное вещество объединяют с полученным ранее кристаллическим веществом и получают 133,7 г (95%) 7,8-дифтор-3-гидроксихинолина в форме светло-коричневого твердого вещества. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, CD3OD)7,39-7,60 (м, 3 Н), 8,59 (д, 1H, J=2,4 Гц). 8-Фтор-3-гидроксихинолин получают согласно такому же способу. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, CDCl3)7,16 (м, 1H), 7,34-7,49 (м, 3 Н), 8,71 (д, 1H, J=2,7 Гц), 9,90 (ушс, 1 Н). Ссылочный пример 3. Синтез 7-фтор-3-гидрокси-2-метилхинолина. Стадия 1). Синтез 6-фторизатина К 590 мл воды добавляют 9,6 г 3-фторанилина и затем добавляют 17,2 г моногидрата трихлорацетальдегида, 21,9 г гидрохлорида гидроксиламина и 98,2 г безводного сульфата натрия и смесь перемешивают в течение 5 ч при 50 С. После охлаждения полученной смеси до комнатной температуры и выстаивания в течение ночи к смеси добавляют 31 мл 2N HCl, затем смесь перемешивают в течение 30 мин и затем отфильтровывают кристаллическое вещество. После сушки полученного кристаллического вещества его добавляют к концентрированной серной кислоте, нагретой до 70 С и затем смесь перемешивают в течение 1 ч при 80-90 С. Реакционную смесь выливают на лед и затем экстрагируют этилацетатом и экстракт промывают крепким рассолом. После сушки органического слоя над сульфатом магния отгоняют растворитель при пониженном давлении и получают 7,96 г сырого продукта 6-фторизатина. К 55 мл воды добавляют 7,96 г неочищенного продукта 6-фторизатина и затем при охлаждении льдом добавляют 16,2 г (6 эквивалентов) КОН, и перемешивают смесь в течение 30 мин. К полученной суспензии добавляют по каплям 9,9 г (1,5 эквивалента) бромацетофенона, поддерживая внутреннюю температуру реакционной смеси 20-25 С и затем смесь перемешивают еще в течение ночи при комнатной температуре. Выпавшее в осадок после нейтрализации концентрированной соляной кислотой кристаллическое вещество отфильтровывают и промывают небольшим количеством воды. После соответствующей сушки полученного кристаллического вещества добавляют за малое время 70 мл нитробензола,нагретого до 120-130 С и затем реакционную смесь перемешивают еще в течение 1 ч при 140-150 С. После охлаждения реакционной смеси до комнатной температуры выпавшее в осадок кристаллическое вещество промывают хлороформом и получают 5,4 г 7-фтор-3-гидрокси-2-метилхинолина. Результаты анализа продукта методом ЯМР показаны ниже. 1 Н-ЯМР (300 МГц, ДМСО-d6)2,56 (с, 3 Н), 7,32-7,38 (м, 1H), 7,53-7,57 (м, 1H), 7,80-7,84 (м, 1H). Пример 13. Синтез 3-[2-фтор-6-(5-фторхиноксалин-2-илокси)фенил]-3-метилбутан-2-она 2-Хлор-5-фторхиноксалин, используемый в качестве исходного материала, синтезируют согласно способу, описанному в непатентном документе 1. Растворяют 0,32 г 3-(2-фтор-6-гидроксифенил)-3-метилбутан-2-она и 0,28 г 2-хлор-5 фторхиноксалина в 3 мл диметилформамида. К раствору добавляют 0,25 г карбоната калия и затем смесь перемешивают в течение 2 ч при 100 С. Затем реакционную смесь очищают колоночной хроматографией на силикагеле и получают 0,14 г 3-[2-фтор-6-(5-фторхиноксалин-2-илокси)фенил]-3-метилбутан-2-она. Пример 14. Синтез 2-хлор-6-(5,6,7,8-тетрагидрохиноксалин-2-илокси)бензальдегида Тетрагидрохиноксалон, используемый в качестве исходного материала, синтезируют согласно способу, описанному в патентном документе 5. Растворяют 0,3 г 5,6,7,8-тетрагидрохиноксалин-2-ола в 5 мл диметилформамида. К раствору добавляют 0,1 г гидрида натрия. К реакционному раствору добавляют 0,35 г 2-хлор-6-фторбензальдегида и затем перемешивают в течение 3 ч при 100 С. Затем к реакционному раствору добавляют 1N соляную кислоту. Затем реакционный раствор экстрагируют этилацетатом, органический слой концентрируют и затем очищают колоночной хроматографией на силикагеле и получают 0,26 г 2-хлор-6-(5,6,7,8 тетрагидрохиноксалин-2-илокси)бензальдегида. Пример 15. Синтез 5,6-дифтор-2-[2-(1-метокси-1-метилэтил)пиридин-3-илокси]-3-метилхиноксалина Растворяют 0,17 г 2-хлор-5,6-дифтор-3-метилхиноксалина в 2 мл N-метилпирролидона. К раствору добавляют 0,13 г 2-(1-метокси-1-метилэтил)пиридин-3-ола и 0,11 г карбоната калия и затем перемешивают в течение 3 ч при 100 С. Затем реакционный раствор очищают колоночной хроматографией на силикагеле и получают 0,24 г 5,6-дифтор-2-[2-(1-метокси-1-метилэтил)пиридин-3-илокси]-3-метилхиноксалина. Азотсодержащие гетероциклические соединения, полученные в вышеуказанных примерах, и азотсодержащие гетероциклические соединения, синтезированные согласно способам, схожим с любым из вышеуказанных примеров, приводятся в таблицах 1 и 2. В табл.1 R1, R2, R3, (X1)m и (Х 2)n представляют собой соответствующие группы, указанные в формуле (1-А). В табл.2 R1, R2, R3, (X1)m, А 1-А 4 и (Х 2)n представляют собой соответствующие группы, указанные в формуле (1-В). Кроме того, символ nD, указанный в колонке, озаглавленной "Физические свойства", показывает показатель преломления (и число, показанное подстрочным индексом, указывает температуру измерения
МПК / Метки
МПК: A01N 43/42, C07D 471/04, A01N 43/90, C07D 241/52, A01N 43/60, A01P 3/00, C07D 401/12
Метки: хозяйства, сельского, фунгицид, азотсодержащие, садоводства, гетероциклические, соединения
Код ссылки
<a href="https://eas.patents.su/30-23328-azotsoderzhashhie-geterociklicheskie-soedineniya-i-fungicid-dlya-selskogo-hozyajjstva-ili-sadovodstva.html" rel="bookmark" title="База патентов Евразийского Союза">Азотсодержащие гетероциклические соединения и фунгицид для сельского хозяйства или садоводства</a>












