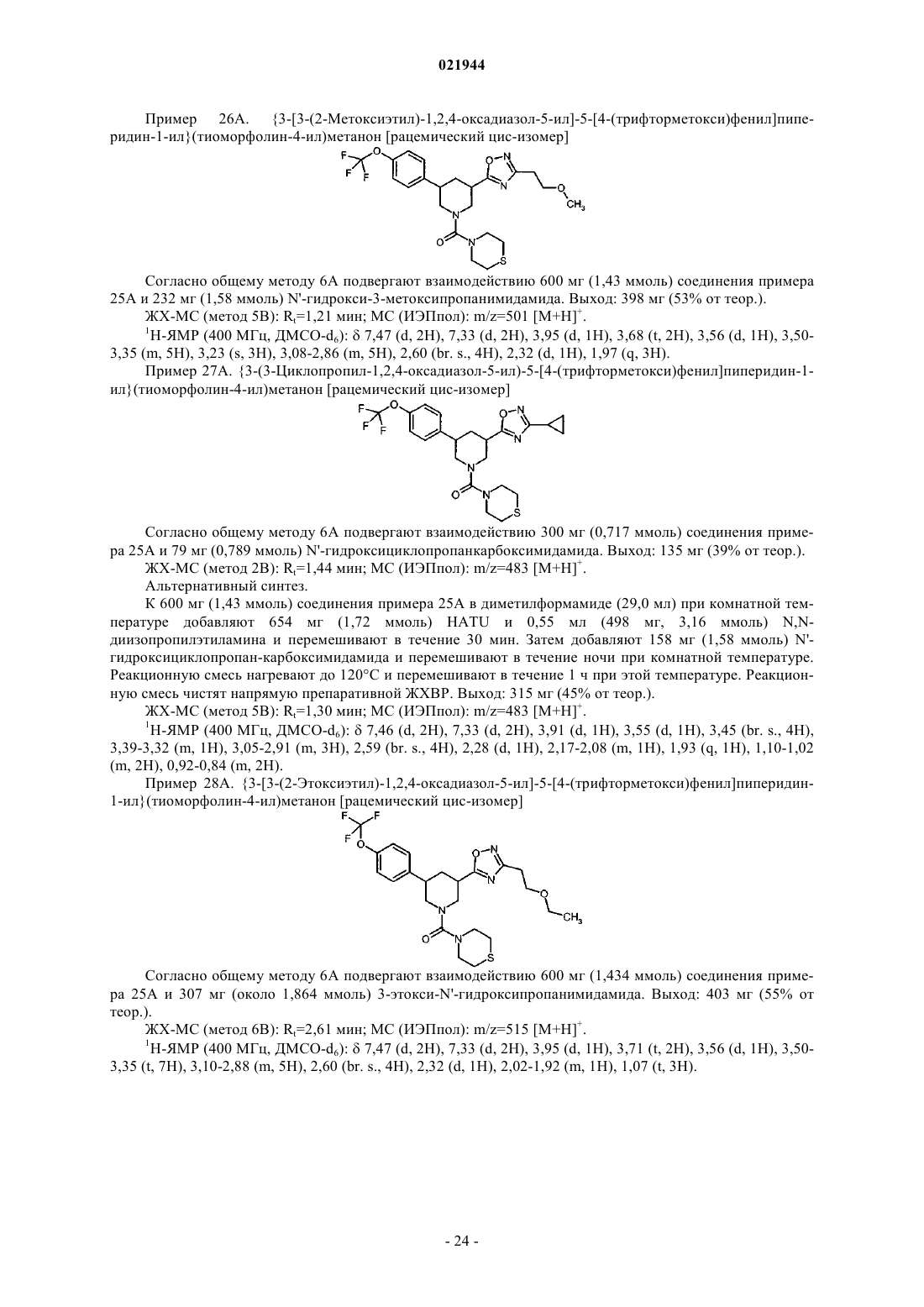
Замещенные пиперидины
Номер патента: 21944
Опубликовано: 30.10.2015
Авторы: Канчо Гранде Еланда, Гердес Кристоф, Циммерманн Катя, Еске Марио, Бухмюллер Анья, Герике Керстен Маттиас, Рериг Зузанне, Гнот Марк Же, Хаймбах Дирк, Бендер Экхард
Формула / Реферат
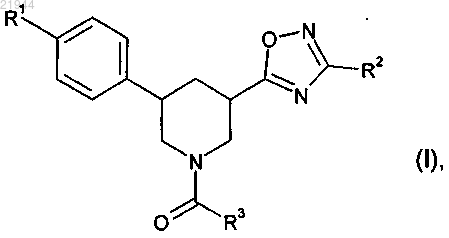
1. Соединение формулы
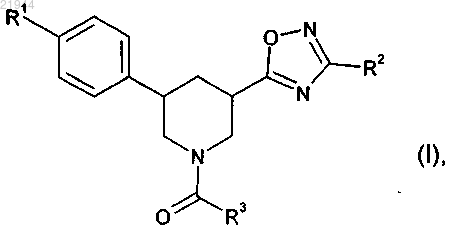
в которой R1 означает трифторметил, 1,1-дифторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, дифторметокси-, трифторметоксигруппу или этил;
R2 означает 2-гидроксиэт-1-ил, 2-метоксиэт-1-ил, 2-этоксиэт-1-ил, циклопропил или 1-метоксициклопроп-1-ил;
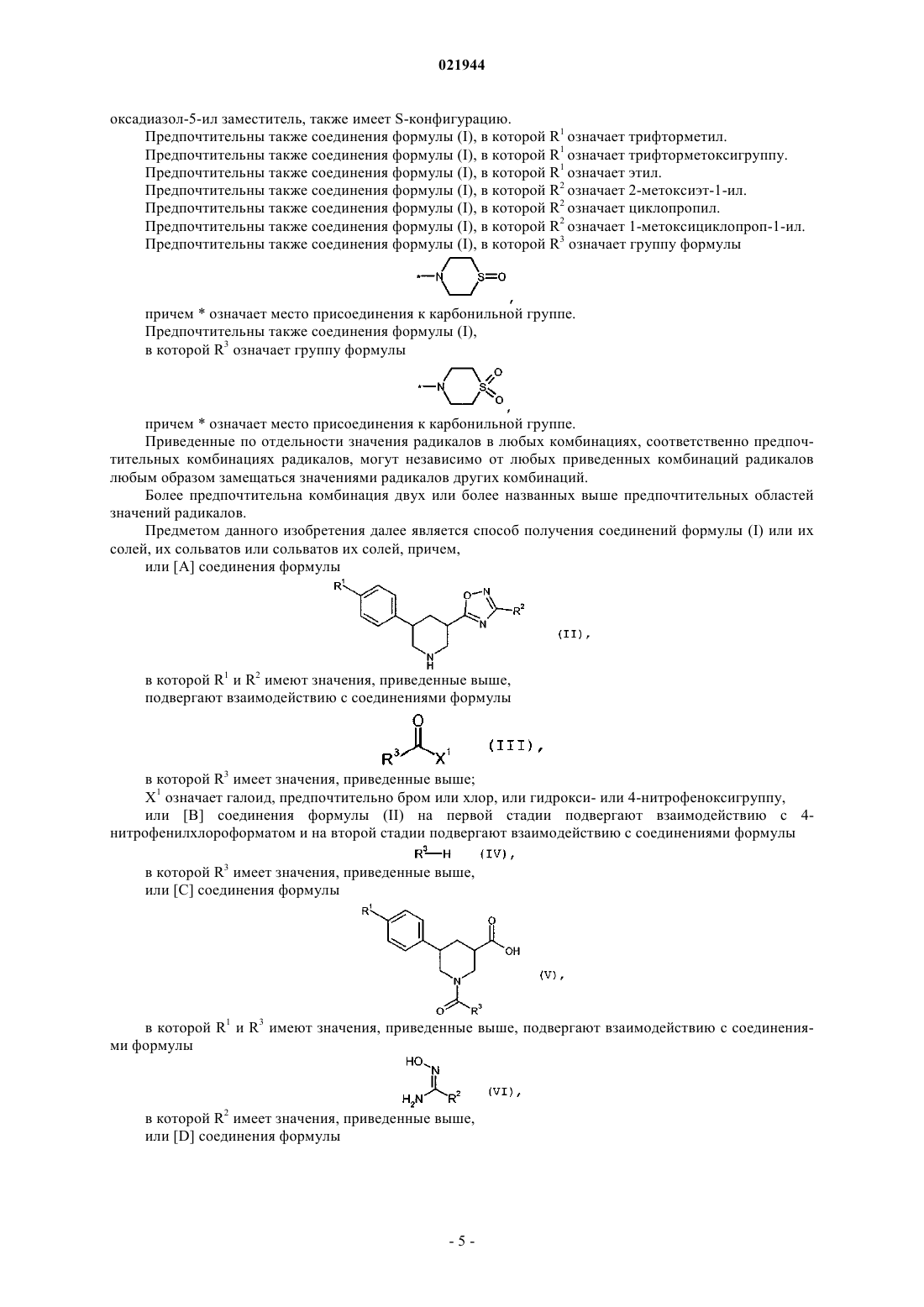
R3 означает группу формулы

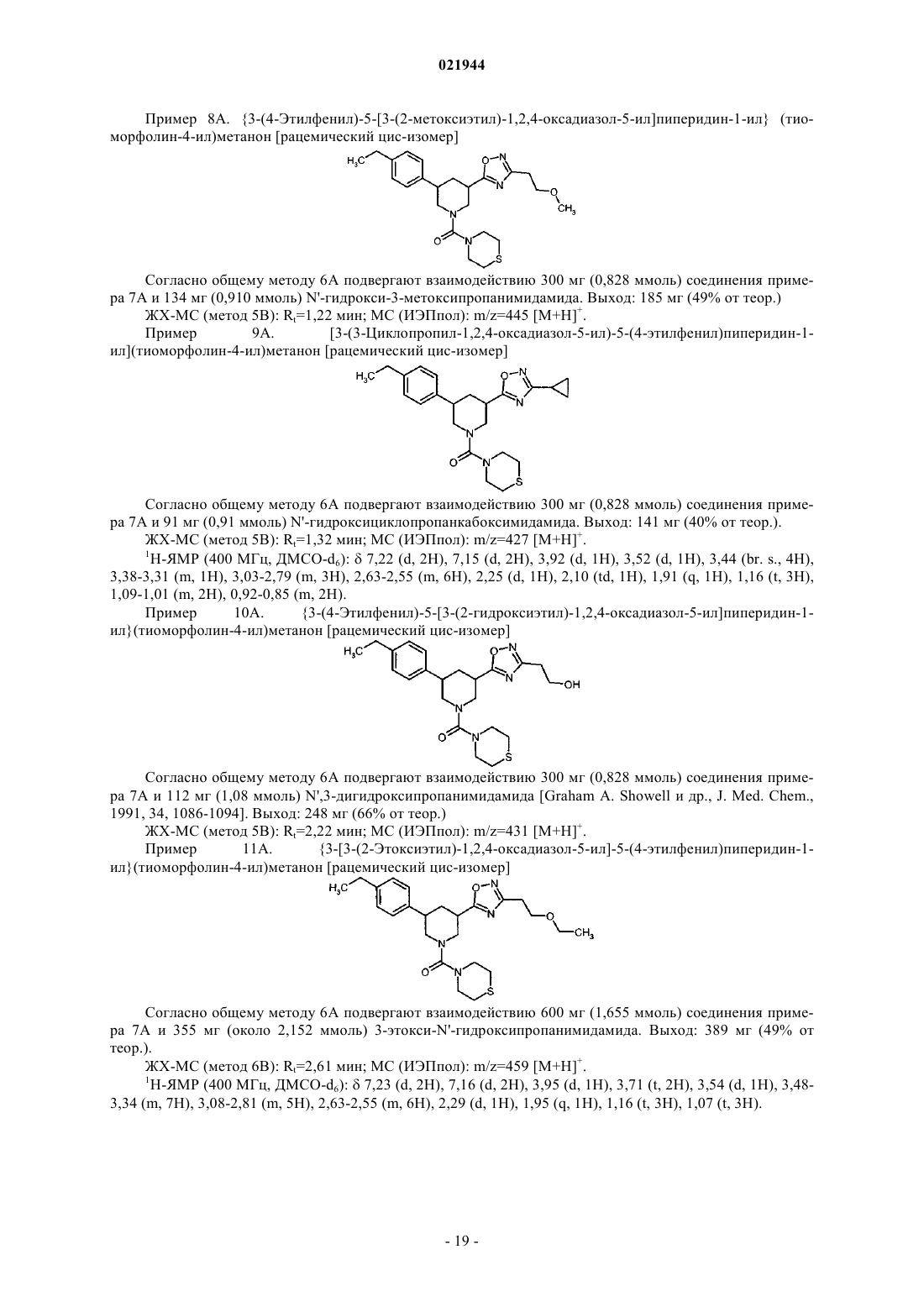
причем * означает место присоединения к карбонильной группе,
или одна из его солей, один из его сольватов или сольватов его солей.
2. Соединение по п.1, отличающееся тем, что
R1 означает трифторметил, 2,2,2-трифторэтил, трифторметоксигруппу или этил;
R2 означает 2-метоксиэт-1-ил, циклопропил или 1-метоксициклопроп-1-ил;
R3 означает группу формулы
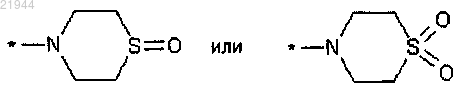
причем * означает место присоединения к карбонильной группе,
или одна из его солей, один из его сольватов или сольватов его солей.
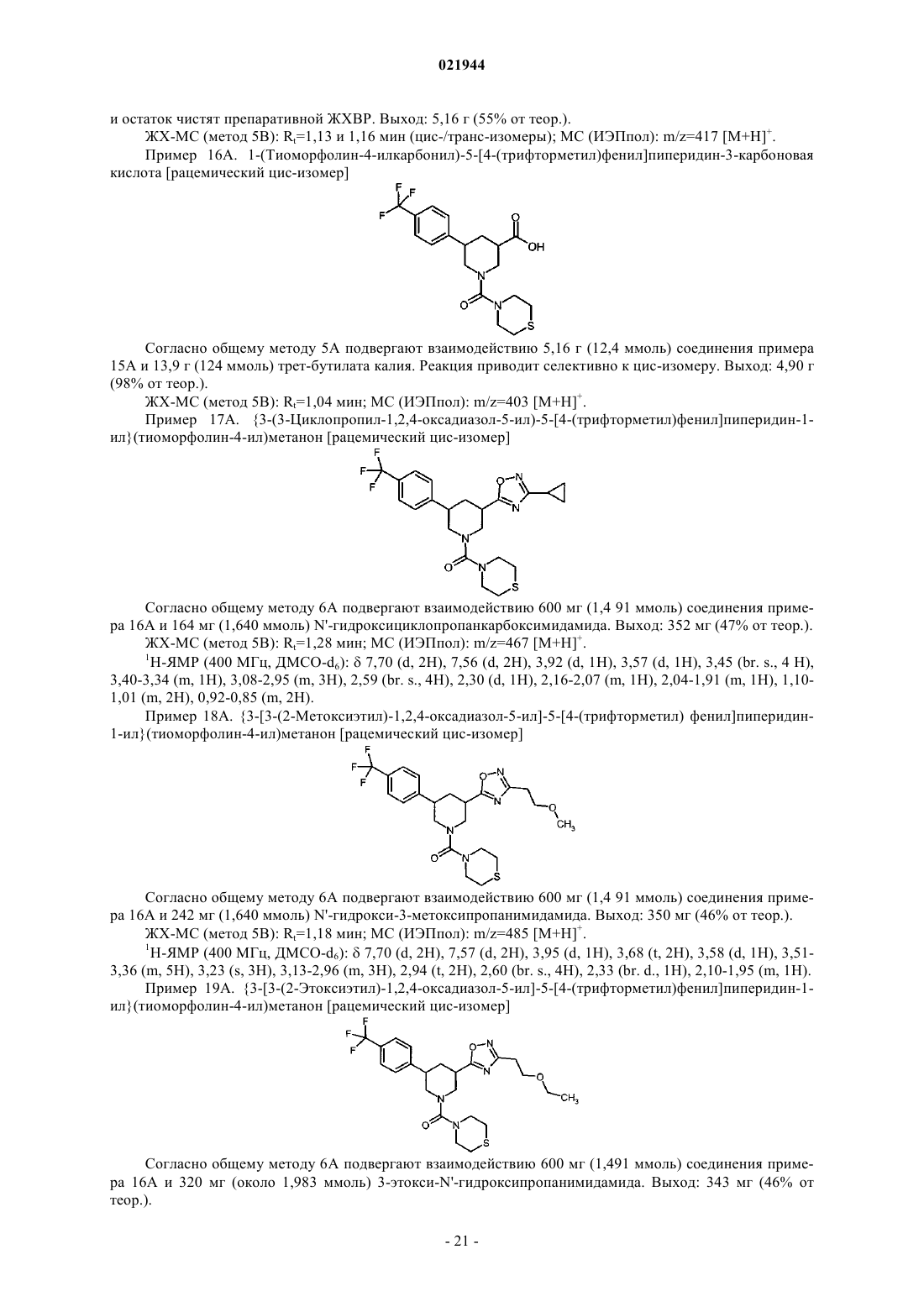
3. Соединение по п.1 или 2, отличающееся тем, что
R1 означает трифторметоксигруппу;
R2 означает 2-метоксиэт-1-ил или циклопропил;
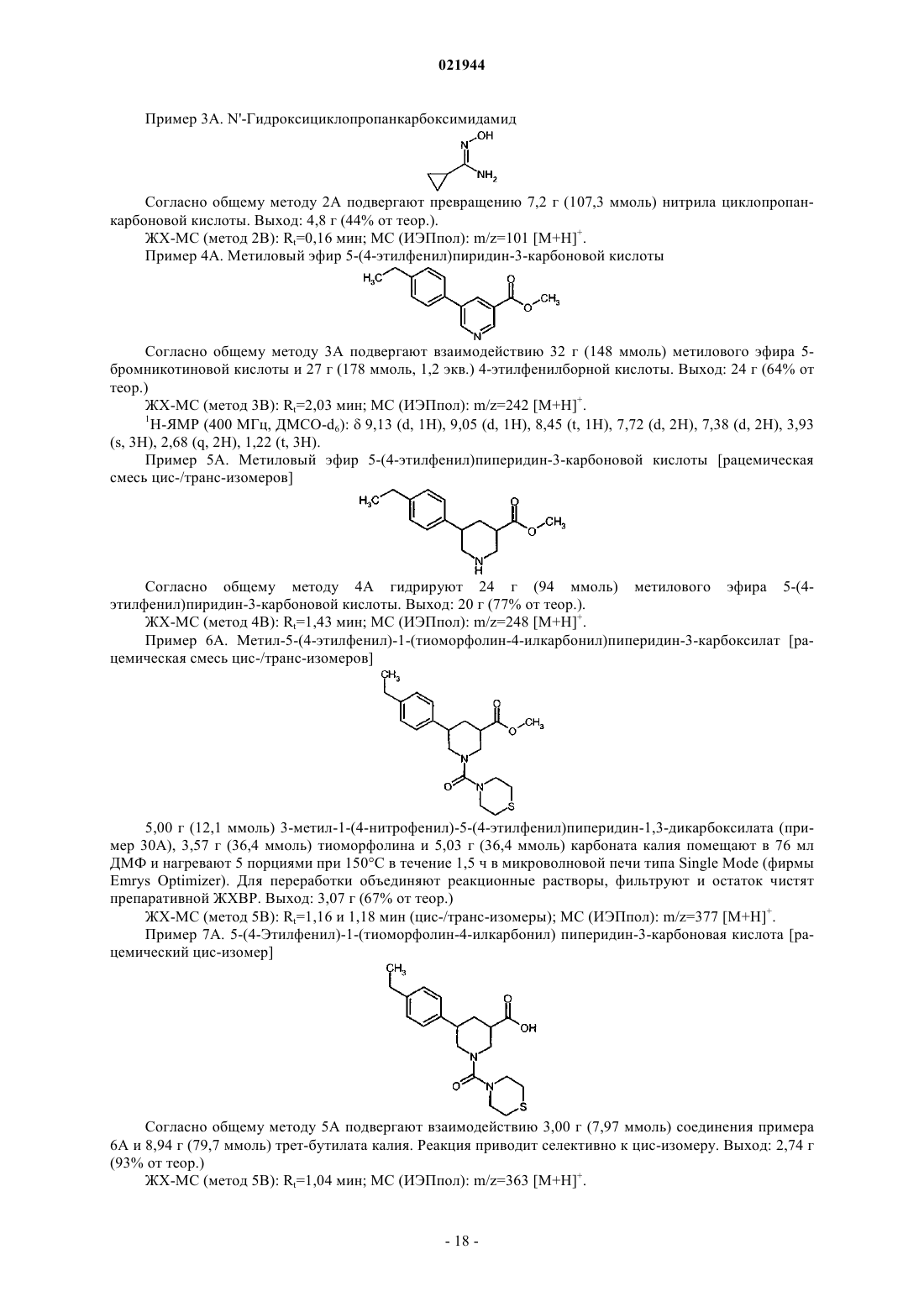
R3 означает группу формулы

причем * означает место присоединения к карбонильной группе,
или одна из его солей, один из его сольватов или сольватов его солей.
4. Соединение по одному из пп.1-3, отличающееся тем, что фенильный заместитель и 1,2,4-оксадиазол-5-ил заместитель, связанные с пиперидиновым кольцом, находятся в цис-положении друг к другу.
5. Соединение по одному из пп.1-4, отличающееся тем, что
R1 означает трифторметоксигруппу,
R2 означает циклопропил,
R3 означает группу формулы
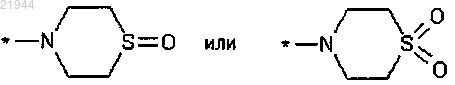
причем * означает место присоединения к карбонильной группе,
или одна из его солей, один из его сольватов или сольватов его солей.
6. Соединение по одному из пп.1-5, отличающееся тем, что атом углерода, к которому присоединен фенильный заместитель, имеет S-конфигурацию и атом углерода, к которому присоединен 1,2,4-оксадиазол-5-ил заместитель, также имеет S-конфигурацию.
7. Способ получения соединения формулы (I) или одной из его солей, одного из его сольватов или сольватов его солей по п.1, отличающийся тем, что соединение формулы
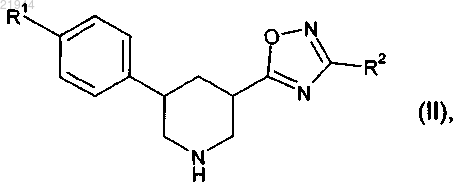
в которой R1 и R2 имеют значения, приведенные в п.1,
подвергают взаимодействию с соединением формулы
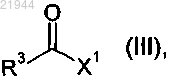
в которой R3 имеет значения, приведенные в п.1;
X1 означает галоид, представляющий собой бром или хлор или гидрокси- или 4-нитрофеноксигруппу.
8. Способ получения соединения формулы (I) или одной из его солей, одного из его сольватов или сольватов его солей по п.1, отличающийся тем, что соединение формулы (II)
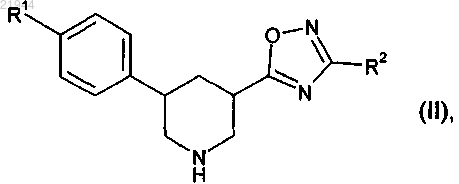
в которой R1 и R2 имеют значения, приведенные в п.1,
на первой стадии подвергают взаимодействию с 4-нитрофенилхлороформатом и на второй стадии подвергают взаимодействию с соединением формулы
в которой R3 имеет значения, приведенные в п.1.
9. Способ получения соединения формулы (I) или одной из его солей, одного из его сольватов или сольватов его солей по п.1, отличающийся тем, что соединение формулы
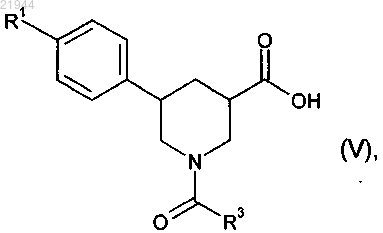
в которой R1 и R3 имеют значения, приведенные в п.1, подвергают взаимодействию с соединением формулы
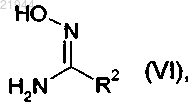
в которой R2 имеет значения, приведенные в п.1.
10. Способ получения соединения формулы (I), в которой R3 означает группу формулы

или одной из его солей, одного из его сольватов или сольватов его солей по п.1,
отличающийся тем, что соединение формулы
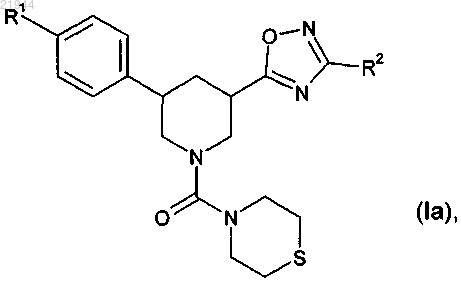
в которой R1 и R2 имеют значения, приведенные в п.1,
подвергают взаимодействию с 0,8-1,1 экв. метахлорпербензойной кислоты.
11. Способ получения соединения формулы (I), в которой R3 означает группу формулы
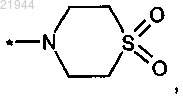
или одной из его солей, одного из его сольватов или сольватов его солей по п.1,
отличающийся тем, что соединение формулы (Ia)
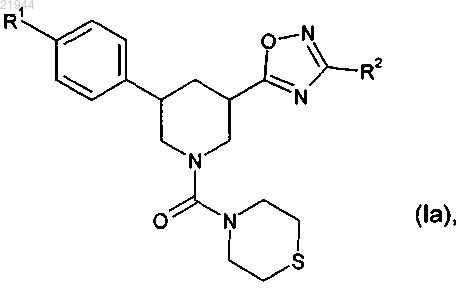
в которой R1 и R2 имеют значения, приведенные в п.1,
подвергают взаимодействию с 2,0-3,0 экв. метахлорпербензойной кислоты.
12. Соединение формулы

в которой R1, R2 и R3 имеют значения, указанные в любом из пп.1-6, для лечения и/или профилактики заболеваний, вызываемых активностью PAR-1-рецептора.
13. Соединение по п.12, где заболевание выбрано из сердечно-сосудистых заболеваний, тромбоэмболических заболеваний и/или опухолевых заболеваний.
14. Соединение формулы

в которой R1, R2 и R3 имеют значения, указанные в любом из пп.1-6, представляющее собой антагонист PAR-1-рецептора.
15. Соединение формулы
в которой R1, R2 и R3 имеют значения, указанные в любом из пп.1-6, для лечения и/или профилактики сердечно-сосудистых заболеваний, тромбоэмболических заболеваний и/или опухолевых заболеваний.
16. Применение соединения по одному из пп.1-6 для предупреждения коагуляции крови in vitro.
17. Фармацевтический препарат для лечения и/или профилактики заболеваний, вызываемых активностью PAR-1-рецептора, содержащий соединение по одному из пп.1-6 в комбинации с инертным, нетоксичным, фармацевтически пригодным вспомогательным веществом.
18. Фармацевтический препарат по п.17, где заболевание выбрано из сердечно-сосудистых заболеваний, тромбоэмболических заболеваний и/или опухолевых заболеваний.
19. Способ лечения и/или профилактики тромбоэмболических заболеваний у людей и животных с использованием антикоагуляторно действующего количества как минимум одного соединения по одному из пп.1-6.
20. Способ лечения и/или профилактики тромбоэмболических заболеваний у людей и животных с использованием антикоагуляторно действующего количества как минимум одного фармацевтического препарата по п.17 или 18.
21. Соединение формулы (I), представляющее собой {3-(3-циклопропил-1,2,4-оксадиазол-5-ил)-5-[4-(трифторметокси)фенил]пиперидин-1-ил}(1,1-диоксидотиоморфолин-4-ил)метанон структурной формулы
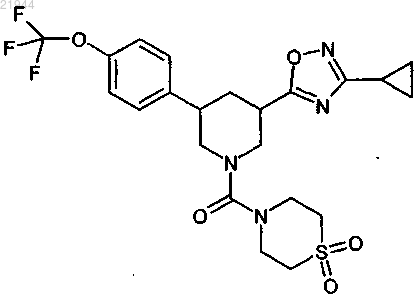
или одна из его солей, один из его сольватов или сольватов его солей.
22. Соединение формулы (I), представляющее собой {3-(3-циклопропил-1,2,4-оксадиазол-5-ил)-5-[4-(трифторметокси)фенил]пиперидин-1-ил}(1,1-диоксидотиоморфолин-4-ил)метанон структурной формулы
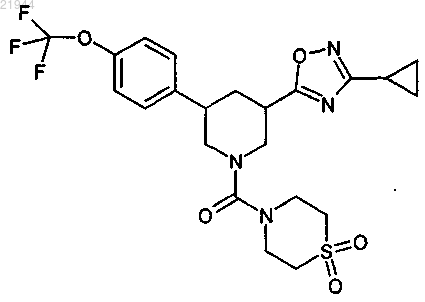
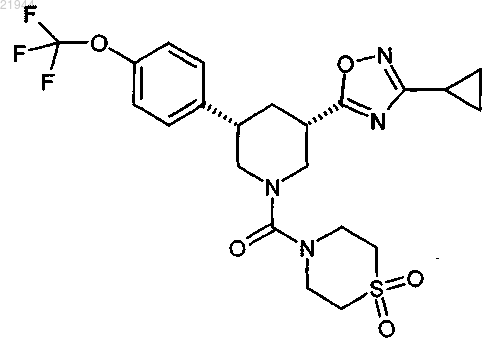
23. Соединение формулы (I) по п.21 или 22 в виде энантиомерно чистого цис-изомера структурной формулы
Текст
Изобретение относится к новым замещенным пиперидинам формулы (I) способу их получения, их применению для лечения и/или профилактики болезней, а также к их применению для получения лекарств для лечения и профилактики болезней, в частности сердечнососудистых болезней и опухолевых болезней.(71)(73) Заявитель и патентовладелец: БАЙЕР ИНТЕЛЛЕКТУЭЛЬ ПРОПЕРТИ ГМБХ (DE) Данное изобретение относится к новым замещенным пиперидинам, способу их получения, их применению для лечения и/или профилактики болезней, а также к их применению для получения лекарств для лечения и профилактики болезней, в частности сердечно-сосудистых болезней и опухолевых болезней. Тромбоциты (кровяные пластинки) представляют собой существенный фактор как в физиологической остановке кровотечения (гемостаз), так и при тромбоэмболических заболеваниях. В особенности в артериальной системе тромбоциты играют центральную роль в комплексном взаимодействии между компонентами крови и стенкой сосуда. Нежелательное активирование тромбоцитов может в результате образования богатых пластинками тромбов приводить к тромбоэмболическим заболеваниям и тромботическим осложнениям с состояниями, представляющими угрозу для жизни. Одним из потенциальных активаторов пластинок является тромбин, протеаза сворачивания крови,который образуется на поврежденных стенках сосуда и, наряду с образованием фибрина, ведет к активированию тромбоцитов, эндотелиальных клеток и мезенхимальных клеток (Vu T.K.H., Hung D.T., WheatonV.I., Coughlin S.R., Cell 1991, 64, 1057-1068). У тромбоцитов in vitro и на моделях животных ингибиторы тромбина замедляют (ингибируют) агрегирование пластинок, соответственно образование богатых пластинками тромбов. Артериальные тромбозы у человека могут успешно предотвращаться или лечиться с помощью ингибиторов тромбоцитной функции, а также ингибиторов тромбина (Bhatt D.L., Topol E.J.,Nat. Rev. Drug Discov. 2003, 2, 15-28). В связи с этим существует большая вероятность того, что антагонисты действия тромбина на кровяные пластинки уменьшают вероятность образования тромбов и наступления клинических последствий, таких как инфаркт миокарда и инсульт. Другие действия тромбина на клетки, например на клетки эндотелия сосудов и клетки гладких мышц сосудов, лейкоциты и фибробласты возможно вызывают воспалительные и пролиферативные заболевания. Клеточные эффекты тромбина передаются, как минимум, отчасти с помощью семейства G-протеинсвязанных рецепторов (протеазой активируемые рецепторы, PARs), прототипом которых является PAR1-рецептор. PAR-1 активируется в результате связывания тромбина и протеолитического расщепления внеклеточно лежащего N-окончания (терминуса). В результате протеолиза высвобождается новый Nтерминус с аминокислотной последовательностью SFLLRN, который в качестве агониста ("связанного лиганда") приводит к внутримолекулярному активированию рецептора и переносу внутриклеточных сигналов. Пептиды, ответвленные от последовательности связанного лиганда, могут быть использованы в качестве агонистов рецептора и приводят на тромбоцитах к активированию и агрегации. Другие протеазы также способны актививировать PAR-1, к ним относятся, например, плазмин, фактор VIIa, фактор Ха, трипсин, активированный протеин С (аРС), триптаза, катепсин G, протеиназа 3, гранзим А, эластаза и матриксметаллопротеаза 1 (ММР-1). В отличие от ингибирования протеазной активности тромбина непосредственными ингибиторами тромбина блокада PAR-1 должна приводить к ингибированию активирования тромбоцитов, не уменьшая способности крови к сворачиванию (антикоагуляция). Антитела и другие селективные PAR-1-антагонисты ингибируют индуцированную тромбином агрегацию тромбоцитов in vitro при низких до средних концентрациях тромбина (Kahn M.L., NakanishiMatsui M., Shapiro M.J., Ishihara H., Coughlin S.R., J. Clin. Invest. 1999, 103, 879-887). Другой тромбиновый рецептор, который возможно оказывает влияние на патофизиологию тромботических процессов,PAR-4, был идентифицирован в тромбоцитах человека и животных. В экспериментальных тромбозах на животных со сравнимым с человеком образцом PAR-экспрессии PAR-1-антагонисты снижают образование богатых пластинками тромбов (Derian C.K., Damiano B.P., Addo M.F., Darrow A.L., D'Andrea M.R.,Nedelman M., Zhang H.-C., Maryanoff B.E., Andrade-Gordon P., J. Pharmacol. Exp. Ther. 2003, 304, 855-861). В последние годы было испытано большое число веществ на ингибирование ими функций пластинок, однако на практике оправдали себя только немногие ингибиторы функции пластинок. В связи с этим существует потребность в фармацевтических средствах, которые специфически ингибируют возросшую реакцию пластинок, не вызывая при этом заметного увеличения риска кровотечения и связанных с ним риском тромбоэмболических осложнений. Эффекты тромбина, которые передаются через рецептор PAR-1, проявляются на течении болезни во время и после оперативного коронарного шунтирования (CABG), а также других операций и, в частности, при операциях с экстракорпоральным (внешним) кровообращением (например, аппарат искусственного кровообращения). В ходе операции, возможно в связи с приемом лекарств перед операцией или во время операции, с веществами, ингибирующими сворачивание крови и/или ингибирующими пластинки, могут происходить осложнения, связанные с кровотечениями. В связи с этим следует, например, прервать прием клопидогреля за несколько дней перед операцией CABG. Кроме того, как упомянуто выше,может (например, по причине длительного контакта между кровью и искусственными поверхностями при применении экстракорпоральной циркуляции или при переливаниях крови) происходить диссеминированное внутрисосудистое сворачивание крови или коагулопатия потребления (DIC), которая вторично может приводить к осложнениям, связанным с кровотечением. В дальнейшем развитии это часто приводит к рестенозу установленных венозных или артериальных байпасов (вплоть до закупорки) по причине тромбоза, интимафиброза, артериосклероза, стенокардии, инфаркта миокарда, сердечной недостаточно-1 021944 сти, аритмий, кратковременных приступов ишемии (TIA) и/или инсульту. Рецептор PAR-1 у человека экспримируют и в других клетках, среди них, например, клетки эндотелия, гладкие мышцы сосудов и клетки опухолей. Злокачественные опухолевые заболевания (рак) имеют высокую частоту заболеваний и связаны, как правило, с высокой смертностью. Современные терапии достигают только у части пациентов полной ремиссии и связаны обычно с тяжелыми побочными последствиями. В связи с этим существует большая потребность в эффективных и надежных методах лечения. PAR-1-рецептор вносит вклад в возникновение, рост, инвазивность и метастазирование рака. Кроме того, экспримированный на клетках эндотелия PAR-1 передает сигналы, которые сливаются в месте роста сосудов ("ангиогенез"), событие, которое незаменимо для возможности роста опухоли свыше примерно 1 мм 3. Ангиогенез также вносит вклад в возникновение и ухудшение других заболеваний, среди них,например, гематопоэтические раковые заболевания, ведущее к слепоте дегенерирование макулы и диабетическая ретинопатия, воспалительные заболевания, такие как ревматоидный артрит и колит. Сепсис (или септикемия) представляет собой часто встречающееся заболевание с высокой летальностью. Первоначальные симптомы сепсиса, как правило, не специфичны (например, температура, плохое самочувствие), при дальнейшем развитии это может, однако, приводить к общему активированию системы сворачивания крови ("диссеминированная внутрисосудистая коагуляция" или "коагулопатия потребления" (DIC с микротромбозированием в различных органах и вторичными осложнениями кровотечений. DIC может проявляться также независимо и в отсутствии сепсиса, например, в рамках операций или при опухолевых заболеваниях. Терапия сепсиса состоит, с одной стороны, в соответствующем устранении инфекционной причины, например, путем оперативной санации очага и антибиоза. С другой стороны, она состоит во временной интенсивной медицинской поддержке поврежденной системы органов. Терапия различных стадий этого заболевания описана, например, в следующей публикации (Dellinger и др., Crit. Care Med. 2004, 32,858-873). Для DIC не существует доказанной эффективной терапии. В связи с этим задача данного изобретения состоит в создании новых PAR-1-антагонистов для лечения таких заболеваний, как, например, заболевания сердечно-сосудистой системы и тромбоэмболические заболевания, а также опухолевых заболеваний у людей и животных. В WO 2006/012226, WO 2006/020598, WO 2007/038138, WO 2007/130898, WO 2007/101270 и US 2006/0004049 описаны структурно похожие пиперидины в качестве 11- HSD1 ингибиторов для лечения среди других диабета, тромбоэмболических заболеваний и инсульта. Предметом данного изобретения являются соединения формулы причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. К соединениям согласно данному изобретению относятся соединения формулы (I) и их соли, сольваты и сольваты солей; охваченные формулой (I) соединения приведенных далее формул и их соли,сольваты и сольваты солей, а также охваченные формулой (I) соединения, приведенные далее в качестве примеров получения и их соли, сольваты и сольваты солей, если только под охваченными формулой (I),далее приведенными соединениями не имеются как раз в виду соли, сольваты и сольваты солей. Соединения согласно данному изобретению могут существовать в зависимости от их структуры в виде стереоизомерных форм (энантиомеры, диастереомеры). В связи с этим изобретение охватывает также энантиомеры или диастереомеры и любые их смеси. Из таких смесей энантиомеров и/или диастереомеров можно выделить известными способами стереоизомерно одинаковые компоненты. Поскольку соединения согласно данному изобретению могут находиться и в таутомерных формах,данное изобретение охватывает также все таутомерные формы. В качестве солей в рамках данного изобретения предпочтительны все физиологически не вызывающие сомнений соли соединений согласно данному изобретению. Охвачены также соли, которые сами по себе не пригодны для фармацевтического применения, однако, например, могут применяться для вы-2 021944 деления или очистки соединений согласно данному изобретению. К физиологически не вызывающим сомнения солям соединений согласно данному изобретению относятся соли присоединения минеральных кислот, карбоновых кислот и сульфоновых кислот, например соли хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, толуолсульфоновой кислоты, бензолсульфоновой кислоты, нафталиндисульфоновой кислоты, уксусной кислоты, трифторуксусной кислоты, пропионовой кислоты, молочной кислоты, винной кислоты, яблочной кислоты, лимонной кислоты, фумаровой кислоты, малеиновой кислоты и бензойной кислоты. К физиологически не вызывающим сомнения солям соединений согласно данному изобретению относятся также соли с обычными основаниями, такие как, например и предпочтительно, соли щелочных металлов (например, натриевые и калиевые соли), соли щелочно-земельных металлов (например, кальциевые и магниевые соли) и аммониевые соли, получаемые с аммиаком или органическими аминами с 116 С-атомами, такими как, например и предпочтительно, этиламин, диэтиламин, триэтиламин, этилдиизо-пропиламин, моноэтаноламин, диэтаноламин, триэтаноламин, дициклогексиламин, диметиламиноэтанол, прокаин, дибензиламин, N-метилморфолин, аргинин, лизин, этилендиамин, N-метилпиперидин и холин. Под сольватами в рамках данного изобретения понимают такие формы соединений согласно данному изобретению, которые образуют в твердом или жидком состоянии комплекс в результате координации молекул растворителя. Гидраты представляют собой особые формы сольватов, у которых происходит координация воды. Наряду с этим, данное изобретение охватывает также пролекарства соединений согласно данному изобретению. Понятие "пролекарство" охватывает соединения, которые сами по себе могут быть биологически активными или неактивными, однако во время нахождения в теле человека могут испытать превращение в соединения согласно данному изобретению (например, метаболически или гидролитически). В формуле группы, которая может означать R3, конечная точка линии, рядом с которой стоит , означает не только атом углерода, соответственно CH2-группу, но и составную часть связи с атомом, с которым связан R3. Предпочтительны соединения формулы (I),в которой R1 означает трифторметил, 1,1-дифторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, дифторметокси-, трифторметоксигруппу или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил, 2,2,2-трифторэтил, трифторметоксигруппу или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил, 2,2,2-трифторэтил или трифторметоксигруппу;R2 означает циклопропил или 1-метоксициклопроп-1-ил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил, трифторметоксигруппу или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны также соединения формулы (I),в которой R1 означает трифторметил или этил; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны соединения формулы (I),в которой R1 означает трифторметоксигруппу; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны соединения формулы (I),в которой R1 означает трифторметоксигруппу; причемозначает место присоединения к карбонильной группе,и их соли, их сольваты и сольваты их солей. Предпочтительны соединения формулы (I),в которой R1 означает трифторметоксигруппу; причемозначает место присоединения к карбонильной группе, и их соли, их сольваты и сольваты их солей. Предпочтительны соединения формулы (I), в которой фенильный заместитель и 1,2,4-оксадиазол-5 ил заместитель, которые присоединены к пиперидиновому кольцу, находятся в цис-положении друг к другу. Предпочтительны также соединения формулы (I), в которой атом углерода, к которому присоединен фенильный заместитель, имеет S-конфигурацию и атом углерода, к которому присоединен 1,2,4-4 021944 оксадиазол-5-ил заместитель, также имеет S-конфигурацию. Предпочтительны также соединения формулы (I), в которой R1 означает трифторметил. Предпочтительны также соединения формулы (I), в которой R1 означает трифторметоксигруппу. Предпочтительны также соединения формулы (I), в которой R1 означает этил. Предпочтительны также соединения формулы (I), в которой R2 означает 2-метоксиэт-1-ил. Предпочтительны также соединения формулы (I), в которой R2 означает циклопропил. Предпочтительны также соединения формулы (I), в которой R2 означает 1-метоксициклопроп-1-ил. Предпочтительны также соединения формулы (I), в которой R3 означает группу формулы причемозначает место присоединения к карбонильной группе. Предпочтительны также соединения формулы (I),в которой R3 означает группу формулы причемозначает место присоединения к карбонильной группе. Приведенные по отдельности значения радикалов в любых комбинациях, соответственно предпочтительных комбинациях радикалов, могут независимо от любых приведенных комбинаций радикалов любым образом замещаться значениями радикалов других комбинаций. Более предпочтительна комбинация двух или более названных выше предпочтительных областей значений радикалов. Предметом данного изобретения далее является способ получения соединений формулы (I) или их солей, их сольватов или сольватов их солей, причем,или [A] соединения формулыX1 означает галоид, предпочтительно бром или хлор, или гидрокси- или 4-нитрофеноксигруппу,или [B] соединения формулы (II) на первой стадии подвергают взаимодействию с 4 нитрофенилхлороформатом и на второй стадии подвергают взаимодействию с соединениями формулы в которой R3 имеет значения, приведенные выше,или [С] соединения формулы в которой R1 и R2 имеют значения, приведенные выше. Соединения формул (Ia)-(Ic) представляют собой частичные подмножества соединений формулы(I). Превращение согласно способу [A] в том случае, когда X1 означает галоид, происходит, как правило, в инертном растворителе, при необходимости в присутствии основания, предпочтительно в температурном интервале от -30 до 50C при нормальном давлении. Инертными растворителями являются, например, тетрагидрофуран, метиленхорид, пиридин, диоксан или диметилформамид, предпочтителен метиленхлорид. Основаниями являются, например, триэтиламин, диизопропилэтиламин или N-метилморфолин,предпочтительны триэтиламин или диизопропилэтиламин. Взаимодействие согласно способу [A] в том случае, когда X1 означает гидроксигруппу, происходит,как правило, в инертном растворителе, в присутствии дегидратизирующего реагента, при необходимости в присутствии основания, предпочтительно в температурном интервале от -30 до 50C, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как дихлорметан или трихлорметан, углеводороды, такие как бензол, нитрометан, диоксан, диметилформамид или ацетонитрил. Также возможно использование смеси растворителей. Более предпочтительны дихлорметан или диметилформамид. В качестве дегидратизирующих реагентов подходят при этом, например, карбодиимиды, такие как,например, N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид, гидрохлорид N-(3-диметиламиноизопропил)-N'-этилкарбодиимида (EDC), N-циклогексилкарбодиимид-N'пропилоксиметил-полистирол (PS-карбодиимид) или карбонильные соединения, такие как карбонилдиимидазол, или 1,2-оксазолиевые соединения, такие как 2-этил-5-фенил-1,2-оксазолий-3-сульфат или 2 трет-бутил-5-метил-изоксазолий-перхлорат, или ациламиносоединения, такие как 2-этокси-1 этоксикарбонил-1,2-дигидрохинолин, или ангидрид пропанфосфоновой кислоты, или изобутилхлороформат,или бис-(2-оксо-3-оксазолидинил)-фосфорилхлорид или бензотриазолилокситри(диметиламино)фосфоний-гексафторфосфат, или О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HBTU), 2-(2-оксо-1-(2 Н)-пиридил)-1,1,3,3-тетраметилуронийтетрафторборат (TPTU) или О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметил-уроний-гексафторфосфат (HATU), или 1-гидроксибензотриазол (HOBt), или бензотриазол-1-илокси-трис-(диметиламино)фосфоний-гексафторфосфат(ВОР), или N-гидроксисукцинимид, или их смеси с основаниями. Основаниями являются, например, карбонаты щелочных металлов, такие как, например, карбонат или гидрокарбонат натрия или калия, или органические основания, такие как триалкиламины, например триэтиламин, N-метилморфолин, N-метилпиперидин, 4-диметиламинопиридин или диизопропилэтиламин. Предпочтительно конденсацию проводят с помощью HATU или EDC в присутствии HOBt. Взаимодействие согласно способу [A], когда X1 означает 4-нитрофеноксигруппу, проводят, как правило, в инертном растворителе, при необходимости в присутствии основания, при необходимости в микроволновой печи, предпочтительно в температурном интервале от 50 до 200C, при давлении от нормального давления до 5 бар. Инертными растворителями являются, например, N-метилпирролидон, диоксан или диметилформамид, предпочтителен N-метилпирролидон. Основаниями являются, например, триэтиламин, диизопропилэтиламин или N-метилморфолин,предпочтительны триэтиламин или диизопропилэтиламин. Соединения формулы (III) известны или могут быть синтезированы известными способами из соответствующих исходных соединений. Взаимодействие на первой стадии согласно способу [B] происходит, как правило, в инертном растворителе, в присутствии основания, предпочтительно в температурном интервале от 0 до 50C, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан, тетрахлорметан или 1,2-дихлорэтан, предпочтителен метиленхлорид. Основаниями являются, например, органические основания, такие как триалкиламины, например триэтиламин, N-метилморфолин, N-метилпиперидин, 4-диметиламинопиридин или диизопропилэтиламин, предпочтителен триэтиламин. Взаимодействие на второй стадии согласно способу [B] происходит, как правило, в инертном растворителе, в присутствии основания, при необходимости в микроволновой печи, предпочтительно в температурном интервале от 50 до 200C, при давлении от нормального давления до 5 бар. Инертными растворителями являются, например, диметилсульфоксид, диметилформамид или Nметилпирролидон, предпочтителен диметилформамид. Основаниями являются, например, карбонаты щелочных металлов, такие как, например, карбонат натрия или калия, предпочтителен карбонат калия. Соединения формулы (IV) известны или могут быть синтезированы известными способами из соответствующих исходных соединений. Взаимодействие согласно способу [C] происходит, как правило, в инертном растворителе, в присутствии дегидратизирующего реагента, при необходимости в присутствии основания, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан или 1,2-дихлорэтан, простые эфиры, такие как диоксан, тетрагидрофуран или 1,2 диметоксиэтан, или другие растворители, такие как ацетон, диметилформамид, диметилацетамид, 2 бутанон или ацетонитрил. Также возможно использование смесей растворителей. Предпочтителен диметилформамид или смесь из диоксана и диметилформамида. В качестве дегидратизирующих реагентов подходят при этом, например, карбодиимиды, такие как,например, N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид, гидрохлорид N-(3-диметиламиноизопропил)-N'-этилкарбодиимида (EDC), N-циклогексилкарбодиимид-N'пропилоксиметил-полистирол (PS-карбодиимид) или карбонильные соединения, такие как карбонилдиимидазол, или 1,2-оксазолиевые соединения, такие как 2-этил-5-фенил-1,2-оксазолий-3-сульфат или 2 трет-бутил-5-метил-изоксазолий-перхлорат, или ациламиносоединения, такие как 2-этокси-1 этоксикарбонил-1,2-дигидрохинолин, или ангидрид пропанфосфоновой кислоты, или изобутилхлороформат,или бис-(2-оксо-3-оксазолидинил)-фосфорилхлорид или бензотриазолилокси-три(диметиламино)фосфоний-гексафторфосфат, или O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HBTU), 2-(2-оксо-1-(2 Н)-пиридил)-1,1,3,3-тетраметилуроний-тетрафторборат (TPTU) или О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметил-уроний-гексафторфосфат (HATU), или 1-гидроксибензотриазол (HOBt), или бензотриазол-1-илокси-трис-(диметиламино)фосфоний-гексафторфосфат(ВОР), или бензотриазол-1-илокси-трис-(пирролидино)фосфоний-гексафторфосфат (PYBOP), или Nгидроксисукцинимид, или их смеси с основаниями. Основаниями являются, например, карбонаты щелочных металлов, такие как карбонат или гидрокарбонат натрия или калия, или органические основания, такие как триалкиламины, например триэтиламин, N-метилморфолин, N-метилпиперидин, 4-диметиламино-пиридин или диизопропилэтиламин, предпочтителен диизопропилэтиламин. Предпочтительно конденсацию проводят с помощью HATU в присутствии диизопропилэтиламина или в виде альтернативы только карбонилдиимидазолом. Соединения формулы (VI) известны или могут быть синтезированы известными способами из соответствующих исходных соединений. Взаимодействие согласно способу [D] проводят, как правило, в инертном растворителе, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя,при нормальном давлении. Метахлорпербензойную кислоту используют предпочтительно в количестве от 0,9 до 1,0 экв. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан или 1,2-дихлорэтан. Предпочтителен метиленхлорид. Взаимодействие согласно способу [E] происходит, как правило, в инертных растворителях, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, при нормальном давлении. Метахлорпербензойную кислоту предпочтительно используют в количестве от 2,3 до 2,6 экв., более предпочтительно в количестве 2,5 экв. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан или 1,2-дихлорэтан. Предпочтителен метиленхлорид. Соединения формулы (II) известны или могут быть получены, когда соединения формулы в которой R1 имеет значения, приведенные выше, на первой стадии подвергают взаимодействию с соединениями формулы (VI) и на второй стадии подвергают взаимодействию с кислотой. Взаимодействие на первой стадии происходит так же, как описано для способа [C]. Взаимодействие на второй стадии происходит, как правило, в инертных растворителях, предпочтительно в температурном интервале от комнатной температуры до 60C, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан, тетрахлорметан или 1,2-дихлорэтан, или простые эфиры, такие как тетрагидрофуран или диоксан, предпочтителен метиленхлорид. Основаниями являются, например, трифторуксусная кислота или хлористый водород в диоксане,предпочтительна трифторуксусная кислота. Соединения формулы (VII) известны или могут быть получены, когда соединения формулыR4 означает метил или этил,на первой стадии подвергают взаимодействию с ди-трет-бутилдикарбоксилатом и на второй стадии подвергают взаимодействию с основанием. Взаимодействие на первой стадии происходит, как правило, в инертных растворителях, в присутствии основания, предпочтительно в температурном интервале от комнатной температуры до 50C, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан, тетрахлорметан или 1,2-дихлорэтан, предпочтителен метиленхлорид. Основаниями являются, например, триэтиламин, диизопропилэтиламин или N-метилморфолин,предпочтителен триэтиламин или диизопропилэтиламин. Взаимодействие на второй стадии происходит, как правило, в инертных растворителях, в присутствии основания, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан, тетрахлорметан или 1,2-дихлорэтан, спирты, такие как метанол или этанол, простые эфиры, такие как диэтиловый эфир, метил-трет-бутиловый эфир, 1,2-диметоксиэтан, диоксан или тетрагидрофуран, или другие растворители, такие как диметилформамид, диметилацетамид, ацетонитрил или пиридин, или смеси растворителей, или смеси растворителей с водой, предпочтительны метанол или метанол с эквивалентом воды, или смесь тетрагидрофурана с водой. Основаниями являются, например, гидроксиды щелочных металлов, такие как гидроксид натрия,лития или калия, или карбонаты щелочных металлов, такие как карбонат цезия, натрия или калия, или алкоголяты, такие как трет-бутилат калия или натрия, предпочтителен гидроксид лития или трет-бутилат калия. Соединения формулы (VIII) известны или могут быть получены, когда гидрируют соединения формулы в которой R1 и R4 имеют значения, приведенные выше. Гидрирование, как правило, проводят с помощью восстановительного средства в инертных растворителях, при необходимости с добавлением кислоты, такой как минеральная кислота и карбоновая кислота, предпочтительна уксусная кислота, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, в интервале давлений от нормального давления до 100 бар, предпочтительно при нормальном давлении или при 50-80 бар. В качестве восстановительного средства предпочтителен водород с палладием на активном угле, с родием на активном угле, с рутением на активном угле или смеси этих катализаторов, или водород с палладием на оксиде алюминия или с родием на оксиде алюминия, или водород с палладием на активном угле и с оксидом платины(IV), предпочтителен водород с палладием на активном угле, или с родием на активном угле, или водород с палладием на активном угле и с оксидом платины(IV). Под давлением можно гидрировать только водородом и с одним оксидом платины(IV). Инертными растворителями являются, например, спирты, такие как метанол, этанол, н-пропанол,изопропанол, н-бутанол или трет-бутанол, или концентрированная уксусная кислота, или метанол с добавкой концентрированной соляной кислотой, предпочтительны метанол или этанол, или концентрированная уксусная кислота, или метанол с добавкой концентрированной соляной кислоты. Соединения формулы (IX) известны или могут быть получены, когда соединения формулы в которых R1 имеет значения, приведенные выше. Взаимодействие происходит, как правило, в инертных растворителях, в присутствии катализатора,при необходимости в присутствии дополнительного реагента, предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, при нормальном давлении. Инертными растворителями являются, например, простые эфиры, такие как диоксан, тетрагидрофуран или 1,2-диметоксиэтан, углеводороды, такие как бензол, ксилол или толуол, или другие растворители, такие как нитробензол, диметилформамид, диметилацетамид, диметилсульфоксид или Nметилпирролидон, при необходимости к этим растворителям добавляют немного воды. Предпочтителен толуол с водой или смесь 1,2-диметоксиэтана, диметилформамида и воды. Катализаторами, например, для условий реакции Сузуки являются обычные палладиевые катализаторы, предпочтительны такие катализаторы, как, например, дихлор-бис-(трифенилфосфин)палладий,тетракистрифенилфосфинпалладий(0), ацетат палладия(II) или бис-(дифенилфосфан-ферроценил)палладий(II)-хлорид. К дополнительным реагентам относятся, например, ацетат калия, карбонат цезия, калия или натрия,гидроксид бария, трет-бутилат калия, фторид цезия, фторид калия или фосфат калия, или их смеси,предпочтительны фторид калия или карбонат натрия или смесь фторида калия и карбоната калия. Соединения формул (X), (XI) и (XIII) известны или могут быть синтезированы известными способами из соответствующих исходных соединений. Соединения формулы (V) известны или могут быть получены, когда соединения формулыR4 означает метил или этил,подвергают взаимодействию с основанием. Взаимодействие происходит, как правило, в инертных растворителях, в присутствии основания,предпочтительно в температурном интервале от комнатной температуры до температуры рефлюкса растворителя, при нормальном давлении. Инертными растворителями являются, например, галоидуглеводороды, такие как метиленхлорид,трихлорметан, тетрахлорметан или 1,2-дихлорэтан, спирты, такие как метанол или этанол, простые эфиры, такие как диэтиловый эфир, метил-трет-бутиловый эфир, 1,2-диметоксиэтан, диоксан или тетрагидрофуран, или другие растворители, такие как диметилформамид, диметилацетамид, ацетонитрил или пиридин, или смеси растворителей, или смеси растворителей с водой, предпочтительны метанол или метанол с одним эквивалентом воды или смесь тетрагидрофурана и воды. Основаниями являются, например, гидроксиды щелочных металлов, такие как гидроксид натрия,лития или калия, или карбонаты щелочных металлов, такие как карбонат цезия, карбонат натрия или карбонат калия, или алкоголяты, такие как трет-бутилат калия или натрия, предпочтителен гидроксид лития или трет-бутилат калия. Соединения формулы (XII) известны или могут быть получены, когда соединения формулы (VIII) подвергают взаимодействию с соединениями формулы (III). Взаимодействие происходит, как описано для способа [A]. В альтернативном способе соединения формулы (XII) можно получить, когда соединения формулы(VIII) на первой стадии подвергают взаимодействию с 4-нитрофенилхлороформатом, а на второй стадии с соединениями формулы (IV). Взаимодействие происходит так же, как описано для способа [B]. Получение соединений формулы (I) можно пояснить следующей схемой реакции: Соединения согласно данному изобретению обнаруживают непредсказуемый, ценный фармакологический и фармакокинетический спектр действия. При этом речь идет о селективных антагонистахPAR-1-рецептора, которые, в частности, действуют в качестве ингибиторов агрегации тромбоцитов, в качестве ингибиторов активирования клеток эндотелия, в качестве ингибиторов пролиферации клеток гладких мышц и в качестве ингибиторов роста опухолей. Для некоторых из названных заболеваний, например сердечно-сосудистых заболеваний с высоким тромбоэмболическим риском, непрерывная защита в результате PAR-1 антагонизма при одновременно простом обращении с лекарством имеет большое значение. PAR-1-антагонисты данного изобретения показывают длительное действие после одноразового орального приема, то есть действие, продолжающееся как минимум 16 ч. В связи с этим они пригодны для применения в качестве лекарств для лечения и/или профилактики заболеваний у людей и животных. Другим предметом данного изобретения является применение соединений согласно данному изобретению для лечения и/или профилактики заболеваний, предпочтительно тромбоэмболических заболеваний и/или тромбоэмболических осложнений. К "тромбоэмболическим заболеваниям" по смыслу данного изобретения относятся, в частности, такие заболевания, как инфаркт сердца с увеличением ST-сегмента (STEMI) и без увеличения ST-сегмента(non-STEMI), стабильная стенокардия (Angina Pectoris), нестабильная стенокардия, реокклюзии и рестенозы после коронарных вмешательств (интервенций, таких как ангиопластия, имплантация стентов или аортокоронарное шунтирование, периферические артериальные заболевания, связанные с закупоркой,легочные эмболии, глубокие венозные тромбозы, тромбозы почечных вен, транзиторические ишемические приступы, а также тромботический и тромбоэмболический мозговой инсульт. Вещества пригодны в связи с этим для предупреждения и лечения кардиогенных тромбоэмболий,таких как, например, ишемия мозга, инсульт (внезапный приступ) и системные тромбоэмболии и ишемии, у пациентов с острыми, интермиттирующими или персистирующими аритмиями сердца, такими как, например, мерцание предсердий, и такими, которые подходят под кардиоверсию, далее у пациентов с заболеваниями сердечных клапанов или с внутрисосидистыми телами, такими как, например, искусственные сердечные клапаны, катетеры, внутриаортная баллонная противопульсация и зонды водителя ритма. Тромбоэмболические осложнения далее появляются при микроангиопатических гемолитических анемиях, при экстракорпоральных системах кровообращения, таких как, например, гемодиализ, гемофильтрация, вспомогательные желудочковые устройства и искусственное сердце, а также при наличии протезов сердечных клапанов. Кроме того, соединения согласно данному изобретению также используют для воздействия на заживление ран, для профилактики и/или лечения атеросклеротических заболеваний сосудов и воспалительных заболеваний, таких как ревматические заболевания опорно-двигательного аппарата, коронарных сердечных заболеваний, сердечной недостаточности, высокого кровяного давления, воспалительных заболеваний, таких как астма, хроническое обструктивное заболевание легких (COPD), воспалительных легочных заболеваний, гломерулонефрит и воспалительных кишечных заболеваний, сверх того также для профилактики и/или лечения болезни Альцгеймера, аутоиммунных заболеваний, болезни Крона и язвенного колита. Наряду с этим, соединения согласно данному изобретению можно также использовать для ингибирования роста опухолей и образования метастазов, при микроангиопатиях, при связанной со старостью дегенерацией желтого пятна сетчатки, при диабетической ретинопатии, диабетической нефропатии и других микроваскулярных (микрососудистых) заболеваниях, а также для предупреждения и лечения тромбоэмболических осложнений, таких как, например, венозные тромбоэмболии, в случае пациентов с опухолями, в частности, таких, которые могут быть связаны с большими хирургическими вмешательствами или с химической или радиационной терапией. Далее соединения согласно данному изобретению пригодны для лечения рака. Раковые заболевания включают среди других: карциномы (среди них рак молочной железы, гепатоцеллюларные карциномы,рак легкого, колоректальный рак, рак толстой кишки и меланомы), липомы (например, липома неХодгкина (Non-Hodgkin) и клетки грибовидного микоза), лейкемии, саркомы, мезотелиомы, рак мозга(например, глиомы), герминомы (например, рак яичка и рак яичника), хориокарцинома, рак легких, рак поджелудочной железы, рак щитовидной железы, рак головы и рак горла, рак эндометрия, рак шейки матки, рак мочевого пузыря, рак желудка и мультиплетная миелома. Кроме того, экспримированный PAR-1 передает клеткам эндотелия сигналы, которые сходятся к росту сосудов ("ангиогенез"), явление, которое необходимо для возможности роста опухолей свыше около 1 мм 3. Индукция ангиогенеза возможна и при других заболеваниях, среди них заболевания ревматического ряда (например, ревматоидные артриты), при легочных заболеваниях (например, фиброз легких,пульмональная гипертония, в частности пульмональноартериальная гипертония, заболевания, характеризующиеся закупоркой легочных сосудов), склероз артерий, разрыв бляшки, диабетическая ретинопатия и влажная дегенерация макулы. Наряду с этим, соединения согласно данному изобретению подходят для лечения сепсиса. Сепсис(или септикемия) является распространенным заболеванием с высокой летальностью. Начальные симптомы сепсиса типичным образом не специфичны (например, температура, плохое самочувствие), дальнейший ход болезни, однако, может приводить к общему активированию системы сворачивания крови("диссеминированной внутрисосудистой коагуляции" или "коагулопатия потребления", в дальнейшем обозначаемая как "DIC") с микротромбозированием в различных органах и с вторичными осложнениями,связанными с кровотечениями. Кроме того, это может приводить к эндотелиальному повреждению с повышенной проницаемостью сосудов и приводить к выходу жидкости и протеинов во внесосудистое пространство. Дальнейшее развитие может приводить к дисфункции или отказу одного из органов (например, почечная недостаточность, печеночная недостаточность, нарушение дыхания, нарушение центральной нервной системы и нарушение сердечно-сосудистой системы вплоть до недостаточности деятельности многих органов). От этого может в принципе пострадать каждый орган, чаще всего дисфункция органа и отказ деятельности наступает у легкого, почки, сердечно-сосудистой системы, системы свертывания крови, центральной нервной системы, эндокринных желез и печени. Сепсис может быть связан с острым синдромом нарушения дыхания ("Acute Respiratory Distress Syndrome", далее обозначаемый какARDS). ARDS может появляться и независимо от сепсиса. "Септический шок" означает наступление понижения кровяного давления, требующее оказания медицинской помощи, и способствует дальнейшему повреждению органа и ухудшению прогноза. Возбудителями болезней могут быть бактерии (грамотрицательные и грамположительные), грибы,вирусы и/или эукариоты. Входной форточкой, соответственно первичными инфекциями, могут быть,например, пневмония, инфекция мочеиспускательных путей, перитонит. Инфекция может быть, но не должна быть обязательно связана с бактериеэмией. Сепсис дефинируется как присутствие инфекции и системного воспалительного ответного синдрома ("systemic inflammatory response syndrome", далее обозначаемого как "SIRS"). SIRS наступает в результате инфекции, а также в результате других состояний, таких как ранения, ожоги, шоки, операции,ишемия, панкреатит, реанимация или опухоли. Согласно решению комитета ACCP/SCCM ConsensusConference Committee от 1992 (Crit. Care Med. 1992, 20, 864-874) описаны необходимые для диагноза"SIRS" симптомы для диагноза и измеряемые параметры (среди которых измененная температура тела,повышенная частота сердечных сокращений, затруднения с дыханием и измененная картина крови). На более поздней(2001) международной конференции по определению сепсиса"SCCM/ESICM/ACCP/ATS/SIS International Sepsis Definitions Conference" критерии в существенной мере сохранены, однако в деталях более уточнены (Levy и др., Crit. Care Med. 2003, 31, 1250-1256).DIC и SIRS могут происходить в рамках сепсиса, а также вследствие операций, опухолевых заболеваний, ожогов и других ранений (повреждений). В случае DIC происходит массовое активирование системы сворачивания крови на поверхности поврежденных клеток эндотелия, поверхностях инородных тел или поврежденной экстраваскулярной ткани. Как следствие происходит сворачивание крови в маленьких сосудах различных органов с гипоксией и последующей дисфункцией органов. Вторично это приводит к расходованию факторов сворачивания крови (например, фактор X, протромбин, фибриноген) и пластинок, в результате чего снижается способность крови к сворачиванию и могут возникнуть тяжелые кровотечения. Соединения согласно данному изобретению могут, наряду с этим, применяться для воспрепятствования (предупреждения) коагуляции ex vivo, например для консервирования продуктов крови и плазмы,для очистки/предварительной обработки катетеров и других медицинских вспомогательных средств и приборов, включая экстракорпоральные кровеносные системы, для покрытия слоем искусственных поверхностей применяемых in vivo или ex vivo медицинских вспомогательных средств и приборов или в случае биологических проб, которые содержат кровяные пластинки. Другим предметом данного изобретения является применение соединения согласно данному изобретению для покрытия слоем медицинских приборов и имплантатов, например катетеры, протезы, стенты или искусственные сердечные клапаны. Соединения согласно данному изобретению при этом могут быть крепко связаны с поверхностью или высвобождаться через определенный промежуток времени,выделяясь из покрывающего слоя носителя в непосредственное окружение для локального действия. Другим предметом данного изобретения является применение соединения согласно данному изобретению для лечения и/или профилактики заболеваний, в частности указанных выше заболеваний. Другим предметом данного изобретения является применение соединений согласно данному изобретению для получения лекарства для лечения и/или профилактики заболеваний, в частности указанных выше заболеваний. Другим предметом данного изобретения является способ лечения и/или профилактики заболеваний,в частности указанных выше заболеваний, путем применения терапевтически эффективного количества соединения согласно данному изобретению. Другим предметом данного изобретения являются лекарства, содержащие одно соединение согласно данному изобретению и одно или несколько других биологически активных веществ, в частности, для лечения и/или профилактики указанных выше заболеваний. В качестве подходящих комбинационных биологически активных веществ, например и предпочтительно, следует назвать блокаторы кальциевого канала, например амлодипин бесилат (например, норваск), фелодипин,дилтиазем, верапамил, нифедипин, никардипин, нисолдипин и беприлил; иомеризин; статины, например аторвастатин, флувастатин, ловастатин, питавастатин, правастатин, росувастатин и симвастатин; ингибиторы абсорбции холестирина, например эзетимибы и AZD4121; ингибиторы протеинов, переносящих холестириловые эфиры ("СЕТР"), например торцетрапиб; низкомолекулярные гепарины, например далтепарин натрий, ардепарин, цертопарин, эноксапарин,парнапарин, тинзапарин, ревипарин и надропарин; другие антикогулянты, например варфарин, маркумар, фондапаринукс; антиаритмики, например дофетилид, ибутилид, метопролол, метопрололтартрат, пропранолол, атенолол, аймалин, дисопирамид, праймалин, прокаинамид, квинидин, спартеин, априндин, лидокаин, мексилетин, токамид, енкамид, флекамид, лоркамид, морицизин, пропафенон, ацебутолол, пиндолол, амиодарон, бретилиум-тозилат, бунафтин, соталол, аденозин, атропин и дигоксин; альфа-адренерговые агонисты, например доксазосин-мезилат, теразосон и празосин; бета-адренерговые блокаторы, например карведилол, пропанолол, тимолол, надолол, атенолол, метопролол, бисопролол, небиволол, бетаксолол, ацебутолол и бисопролол; альдостерон-антагонисты, например эплеренон и спиронолактон; ингибиторы энзимов, конвертирующих ангиотензин ("АСЕ-ингибиторы"), например моэксиприл,гидрохлорид квиналприла, рамиприл, лизиноприл, гидрохлорид беназеприла, эналаприл, каптоприл,спираприл, периндоприл, фосиноприл и трандолаприл; блокаторы ангиотензин II рецептора ("ARBs"), например олмесартан-медоксомил, кандесартан,валсартан, телмисартан, ирбесартан, лосартан и эпросартан; антагонисты эндотелина, например тезосентан, босентан и ситакссентан-натрий; нейтральные ингибиторы эндопептидазы, например кандоксатрил и экадотрил; ингибиторы фосфодиэстеразы, например милриноон, теофиллин, винпоцетин, EHNA (эритро-9-(2 гидрокси-3-нонил)аденин), силденафил, варденафил и тадалафил; фибринолитики, например ретеплаз, алтеплаз и тенектеплаз; прямые ингибиторы тромбинина, например AZD0837, аргатробан, бивалирудин и дабигатран; непрямые ингибиторы тромбинина, например одипарцил; прямые и непрямые ингибиторы фактора Xa, например фондапаринукс-натрий, апиксабан, разаксабан, ривароксабан (BAY 59-7939), KFA-1982, DX-9065a, AVE3247, отамиксабан (XRP0673), AVE6324,SAR377142, идрапаринукс, SSR126517, DB-772d, DT-831j, YM-150, 813893, LY517717 и DU-1766; прямые и непрямые ингибиторы фактора Xa/IIa, например эноксапарин-натрий, AVE5026,SSR128428, SSR128429 и BIBT-986 (таногитран); модуляторы липопротеин-ассоциированной фосфолипазы A2 ("LpPLA2"); диуретики, например хлорталидон, этакриновая кислота, фуросемид, амилорид, хлоротиазид, гидрохлоротиазид, метилхлотиазид и бензтиазид; нитраты, например изосорбид-5-мононитрат; антагонисты тромбоксана, например сератродаст, пикотамид и раматробан; ингибиторы агрегации пластинок, например клопидогрель, тиклопидин, цилостазол, аспирин, абциксимаб, лимапрост, эптифибатид и СТ-50547; ингибиторы циклооксигеназы, например мелоксикам, рофекоксиб и целекоксиб; натриуретические пептиды В-типа, например несиритид и уларитид;NHE-1 ингибиторы, например AVE4454 и AVE4890. Антибиотическая терапия: различные антибиотики или антифунгальные комбинации лекарств имеются в виду, или в виде рассчитанной терапии (перед получением результатов о микробном заражении) или в виде специфической терапии; жидкостная терапия, например кристаллоидальные или коллоидальные жидкости; вазопрессоры, например норепинефрин, допамин или вазопрессин; инотропная терапия, например добутамин; кортикостероиды, например гидрокортизон или флудрокортизон; рекомбинантный человеческий активированный протеин (белок) С, ксигрис; кровяные продукты, например концентраты эритроцитов, концентраты тромбоцитов, эритропиетин или свежезамороженная плазма; механическое машинное дыхание при индуцированном сепсисом остром легочном повреждении ("Acute LungInjury" (ALI соответственно, остром респираторном заболевании ("Acute Respiratory Distress Syndrome"(ARDS, например допустимой гиперкапнии, более низких объемах тидала; успокоение седитативными средствами, например диазепам, лоразепам, мидазолам или пропофол. Опиоиды, например фентанил,гидроморфон, морфин, меперидин или ремифентанил. NSAIDs, например кеторолак, ибупрофен или ацетаминофен. Нейромускулярная блокада, например панкурониум; контроль глюкозы, например инсулин,глюкоза; способы замещения почек, например непрерывная вено-венозная-гемофильтрация или интермиттирующий гемодиализ. Допамин с низкой дозировкой для ренальной защиты; антикоагулянты, например, для профилактики тромбоза или при способах замещения почек, инфракционированные гепарины, гепарины с низким молекулярным весом, гепариноиды, гирудин, бивалирудин или арготробан; бикарбонатная терапия; профилактика стрессовой язвы, например, ингибиторы H2-рецептора, антазида. Лекарства при пролиферативных заболеваниях: урацил, хлорметин, циклофосфамид, ифосфамид,мелфалан, хлорамбуцил, пипоброман, триэтиленэмеламин, триэтиленетиофосфорвамин, бусулфан, кармустин, ломустин, стрептозоцин, дакарбазин, метотрексат, 5-флуороурацил, флоксуридин, цитарабин, бмеркаптопурин, 6-тиогуанин, флударабин фосфат, пентостатин, винбластин, винкристин, виндесин, блеомицин, дактиномицин, даунорубицин, доксорубицин, эпирубицин, идарубицин, паклитаксел, митрамицин, деоксикоформицин, митомицин-C, L-аспаргиназа, интерферон, этопосид, тенипозид 17.альфа.этинилэстрадиол, диэтилстилбестрол, тестостерон, преднизон, флуоксиместерон, пропионат дромостанолона, тестолактон, мегестролацетат, тамоксифен, метилпреднизолон, метилтестостерон, преднизолон,триамцинолон, хлоротрианизен, гидроксипрогестерон, аминоглютетимид, эстранрустин, медроксипрогестеронацетат, леупролид, флутамид, торемифен, госерелин, цисплатин, карбоплатин, гидроксимочевина,амсакрин, прокарбазин, митотан, митоксантрон, левамисол, навелбен, анастразол, летразол, капецитабин,релоксафин, дролоксафин, гексаметилмеламин, оксалиплатин (элоксатин), иресса (гефтимид, Zdl839),КСЕЛОДА (капецитабин), таркева (эрлотиниб), азацитидин (5-азацитидин; 5-AzaC), темозоломид(темодар), гемцитабин (то есть GEMZAR (гемцитабин HCl, вазостатин или комбинация двух или нескольких названных выше веществ. Другим предметом данного изобретения является способ предупреждения коагуляции крови invitro, в частности, в случае консервов крови или биологических проб, которые содержат кровяные пла- 13021944 стинки, отличающийся тем, что добавляют антигоагуляторно действующее количество соединения согласно данному изобретению. Соединения согласно данному изобретению могут действовать системно и/или локально. Для этой цели они могут применяться подходящим образом, например орально, парентерально, пульмонально,назально, подъязычно, язычно, щечно, ректально, накожно, чрескожно, конъюктивально, в уши или в виде имплантанта, соответственно стента. Для этих путей применения соединения согласно данному изобретению могут применяться в подходящих лекарственных формах для приема. Для орального применения подходят формы применения, функционирующие согласно уровню техники, быстро и/или модифицировано высвобождающие соединения согласно данному изобретению, которые содержат соединения согласно данному изобретению в кристаллической и/или аморфной форме,и/или в растворенном виде, такие как, например, таблетки (не покрытые пленкой или покрытые пленкой таблетки, например, с покровами, которые устойчивы к желудочному соку, или с замедленно растворяемыми или нерастворяемыми покровами, которые контролируют высвобождение соединений согласно данному изобретению), быстро распадающиеся в ротовой полости таблетки или пленки/облатки, пленки/лиофилизаты, капсулы (например, твердые или мягкие желатиновые капсулы), драже, грануляты, пилюли, порошки, эмульсии, суспензии, аэрозоли или растворы. Парентеральное применение может происходить так, что избегается ресорбционная стадия (например, внутривенно, внутриартериально, внутрисердечно, интраспинально или интралумбально) или путем включения ресорбции (например, внутримышечно, подкожно, внутрикожно, чрескожно или внутрибрюшно). Для парентерального применения подходят в качестве форм для применения среди прочих инъекционные и инфузионные препараты в виде растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков. Предпочтительным является оральное применение. Для других путей применения пригодны, например, ингаляционные лекарственные формы (среди прочих порошковые ингаляторы, распылители), капли в нос - растворы или спреи, язычные, подъязычные и буккально применяемые таблетки, пленки/облатки или капсулы, суппозитории, препараты для внесения в уши или глаза, вагинальные капсулы, водные суспензии (лосьоны, получаемые при встряхивании смеси), липофильные суспензии, мази, кремы, трансдермальные терапевтические системы (например, пластыри), молочко, пасты, пены, порошки для посыпания, имплантаты или стенты. Соединения согласно данному изобретению могут быть переведены в приведенные формы применения лекарств. Это можно осуществить известным образом путем смешивания с инертными, нетоксичными, фармацевтически пригодными вспомогательными веществами. К таким вспомогательным веществам относятся среди прочих вещества-носители (например, микрокристаллическая целлюлоза, лактоза,маннитол), растворители (например, жидкие полиэтиленгликоли), эмульгаторы и диспергирующие и смачивающие средства (например, додецилсульфат натрия, полиоксисорбитанолеат), связующие средства (например, поливинилпирролидон), синтетические и природные полимеры (например, альбумин), стабилизаторы (например, антиоксиданты, такие как, например, аскорбиновая кислота), красители (например, неорганические пигменты, такие как, например, оксиды железа) и средства, корригирующие вкус и/или запах. Другим предметом данного изобретения являются лекарства, которые содержат как минимум одно соединение согласно данному изобретению, предпочтительно вместе с одним или несколькими инертными нетоксичными, фармацевтически пригодными вспомогательными веществами, а также их применение для названных выше целей. Вообще оказалось предпочтительным, когда при парентеральном применении принимается количество от 5 до 250 мг каждые 24 ч для достижения эффективных результатов. При оральном применении это количество составляет от 5 до 100 мг каждые 24 ч. Однако может возникнуть необходимость отклонения от указанных количеств, а именно в зависимости от веса тела, пути применения, индивидуального поведения по отношению к биологически активному веществу, вида препарата и момента времени, соответственно интервала, в который происходит прием лекарства. Процентные задания в последующих тестах и примерах, если особо не оговорено, даны в виде весовых процентов; доли приведены в виде весовых долей. Соотношение растворителей, условия разбавления и концентрационные задания жидко/жидких растворов относятся в каждом случае к объемам. Обозначение "в/о" означает "вес/объем". Так, например, "10% в/о" означает, что 100 мл раствора или суспензии содержат 10 г вещества. А. Примеры. Сокращения: КДИА - карбонилдиимидазол,d - дублет (в случае ЯМР),ТСХ - тонкослойная хроматография,ПХИ - прямая химическая ионизация (в случае МС),- 14021944dd - двойной дублет (в случае ЯМР),ДМАП - 4-диметиламинопиридин,ДМФ - N,N-диметилформамид,ДМСО - диметилсульфоксид,ДФФА - дифенилфосфоразидат,DSC - дисукцинимидилкарбонат,от теор. - от теоретического (выход),экв. - эквивалент(ы),ИЭП - ионизация электронным пучком (в случае МС),DAD - с помощью диодной матрицы,HATU - O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуроний-гексафторфосфат,ЖХВР - жидкостная хроматография высокого разрешения, высокого давления,ЖХ-МС - жидкостная хроматография, сопряженная с масс-спектрометрометрией,LDA - диизопропиламид лития,m - мультиплет (в случае ЯМР),мин - минута(ы),МС - масс-спектрометрия,ЯМР - спектрометрия ядерного магнитного резонанса,PYBOP - бензотриазол-1-илокси-трис-(пирролидино)-фосфоний-гексафторфосфат,q - квартет (в случае ЯМР),RP - обратимая фаза (в случае ЖХВР),Rt - время удерживания (в случае ЖХВР),s - синглет (в случае ЯМР),t - триплет (в случае ЯМР),ТГФ - тетрагидрофуран,ЖХВР-методы. Метод 1 А. Прибор: HP 1100 с DAD-детектированием; колонка: Kromasil 100 RP-18, 602,1 мм, 3,5 мкм; элюент A: 5 мл перхлорной кислоты (70%)/1 л воды, элюент В: ацетонитрил; градиент: 0 мин 2% В 0,5 мин 2% В 4,5 мин 90% В 6,5 мин 90% В 6,7 мин 2% В 7,5 мин 2% В; поток: 0,75 мл/мин; температура колонки: 30C; УФ-детектирование: 210 нм. ЖХ-МС-методы. Метод 1 В. Тип прибора МС: Micromass ZQ; тип прибора ЖХВР: HP 1100 Series; УФ DAD; колонка: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиент: 0,0 мин 100% А 3,0 мин 10% А 4,0 мин 10% А, печь: 55C; поток: 2 мл/мин; УФ-детектирование: 210 нм. Препаративное разделение энантиомеров. Метод 1D. Фаза: Daicel Chiralpak AD-H, 5 мкм 25020 мм, элюент: изогексан/изопропанол 25:75; поток: 15 мл/мин, температура: 45C; УФ-детектирование: 220 нм. Метод 2D. Фаза: Daicel Chiralpak IA, 5 мкм 25020 мм, элюент: метанол/ацетонитрил 25:75; поток: 15 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 3D. Фаза: Daicel Chiralpak IA, 5 мкм 25020 мм, элюент: метанол/ацетоонитрил 50:50; Fluss: 15 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 4D. Фаза: Daicel Chiralpak IA, 5 мкм 25020 мм; элюент: трет-бутилметиловый эфир/метанол 50:50; поток: 15 мл/мин; температура: 30C; УФ-детектирование: 220 нм. Метод 5D. Фаза: Daicel Chiralpak IA, 5 мкм 25020 мм, элюент: метанол/ацетонитрил 25:75; поток: 15 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 6D. Фаза: Daicel Chiralpak AD-H, 5 мкм 25020 мм, элюент: изогексан/этанол 25:75; поток: 15 мл/мин, температура: 45C; УФ-детектирование: 220 нм. Метод 7D. Фаза: Daicel Chiralpak AD-H, 5 мкм, 25020 мм, элюент: этанол 100%; поток: 15 мл/мин,температура: 45C; УФ-детектирование: 220 нм. Метод 8D. Фаза: Daicel Chiralpak AD-H, 5 мкм, 25020 мм, элюент: изогексан/изопропанол 30:70; поток: 15 мл/мин, температура: 45C; УФ-детектирование: 220 нм. Метод 9D. Фаза: Daicel Chiralpak IA, 5 мкм, 25020 мм, элюент: ацетонитрил/метанол 70:30; поток: 15 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 10D. Фаза: Daicel Chiralpak IA, 5 мкм, 25020 мм, элюент: ацетонитрил/метанол 70:30; поток: 20 мл/мин, температура: 35C; УФ-детектирование: 210 нм. Метод 11D. Фаза: Daicel Chiralpak AD-H, 5 мкм, 25020 мм, элюент: изогексан/этанол 70:30; поток: 15 мл/мин, температура: 40C; УФ-детектирование: 220 нм. Аналитическое разделение энантиомеров. Метод 1E. Фаза: Daicel Chiralpak AD-H, 5 мкм 2504 мм; элюент: изопропанол/изогексан: 75:25; поток: 1 мл/мин; температура: 45C; УФ-детектирование: 220 нм. Метод 2 Е. Фаза: Daicel Chiralpak AD-H, 5 мкм 2504,6 мм; элюент: изогексан/изопропанол 25:75 + 0,2% трифторуксусной кислоты + 1% воды; поток: 1 мл/мин; температура: 45C; УФ-детектирование: 235 нм. Метод 3E. Фаза: Daicel Chiralpak IA, 5 мкм 2504,6 мм; элюент: ацетонитрил/метанол 75:25; поток: 1 мл/мин; температура: 25C; УФ-детектирование: 220 нм. Метод 4 Е. Фаза: Daicel Chiralpak IA, 5 мкм 2504,6 мм; элюент: ацетонитрил/метанол 50:50; поток: 1 мл/мин; температура: 25C; УФ-детектирование: 220 нм. Метод 5 Е. Фаза: Daicel Chiralpak IA, 5 мкм 2504,6 мм; элюент: трет-бутилметиловый эфир/метанол 50:50; поток: 1 мл/мин; температура: 25C; УФ-детектирование: 220 нм. Метод 6 Е. Фаза: Daicel Chiralpak AD-H, 5 мкм, 2504,6 мм, элюент: этанол 100%; поток: 1 мл/мин,температура: 45C; УФ-детектирование: 220 нм. Метод 7 Е. Фаза: Daicel Chiralpak AD-H, 5 мкм, 2504,6 мм, элюент: изогексан/изопропанол 30:70; поток: 1 мл/мин, температура: 45C; УФ-детектирование: 220 нм. Метод 8 Е. Фаза: Daicel Chiralpak IA, 5 мкм, 2504,6 мм, элюент: ацетонитрил/метанол 70:30; поток: 15 мл/мин, температура: 25C; УФ-детектирование: 220 нм. Метод 9 Е. Фаза: Daicel Chiralpak IA, 5 мкм, 2504,6 мм, элюент: ацетонитрил/метанол 70:30; поток: 15 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 10 Е. Фаза: Daicel Chiralpak IA, 5 мкм 2504,6 мм, злюент: ацетонитрил/метанол 70:30; поток: 1 мл/мин, температура: 30C; УФ-детектирование: 220 нм. Метод 11 Е. Фаза: Daicel Chiralpak AD-H, 5 мкм, 2504,6 мм, элюент: изогексан/этанол 25:75 + 0,2% трифторуксусной кислоты + 1% воды; поток: 1 мл/мин, температура: 45C; УФ-детектирование: 220 нм. ГХ-МС-методы. Метод 1F. Прибор: Micromass GCT, GC68 90; колонка: Restek RTX-35, 15 м 2000,33 мкм; постоянный поток с гелием: 0,88 мл/мин; печь: 70C; напуск: 250C; градиент: 70C, 30C/мин 310C (3 мин выдержать). В качестве микроволнового реактора применяют "single mode" прибор типа Emrys Optimizer. Исходные соединения. Общий метод 1 А. Получение N'-гидроксиимидамида. К раствору соответствующего нитрила (1,0 экв.) в этаноле (1,2 мл/ммоль) добавляют при комнатной температуре гидроксиламмонийхлорид (1,5 экв.) и триэтиламин (1,2 экв.). Реакционную смесь перемешивают в течение ночи при комнатной температуре. Для переработки отгоняют этанол в вакууме, к реакционной смеси добавляют насыщенный водный раствор гидрокарбоната натрия и экстрагируют этило- 16021944 вым эфиром уксусной кислоты. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель. Остаток подвергают дальнейшему превращению без дальнейшей очистки. Общий метод 2 А. Получение N'-гидроксиимидамида. К раствору соответствующего нитрила (1,0 экв.) в смеси из этанола (1,9 мл/ммоль) и воды (0,5 мл/ммоль) добавляют при комнатной температуре гидроксиламмонийхлорид (1,08 экв.) и гидроксид натрия (1,12 экв.). Реакционную смесь перемешивают в течение 16 ч при комнатной температуре. Для переработки из реакционной смеси отгоняют растворитель в вакууме, добавляют дихлорметан и фильтруют. Из фильтрата отгоняют растворитель в вакууме и остаток без дальнейшей очистки подвергают превращению. Общий метод 3 А. Сочленение (реакция) Сузуки. К смеси соответствующего бромпиридина в толуоле (1,8 мл/ммоль) в атмосфере аргона при комнатной температуре добавляют тетракис-(трифенилфосфин)палладий (0,02 экв.), раствор соответствующей арилборной кислоты (1,2 экв.) в этаноле (0,5 мл/ммоль) и раствор фтористого калия (2,0 экв.) в воде(0,2 мл/ммоль). Реакционную смесь много часов перемешивают в условиях рефлюкса до почти полного превращения. Добавляют этиловый эфир уксусной кислоты и разделяют фазы, органическую фазу промывают один раз водой и один раз насыщенным водным раствором хлористого натрия, сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Сырой продукт чистят с помощью флэшхроматографии (силикагель-60, элюент: дихлорметан-метанол-смеси). Общий метод 4 А. Гидрирование пиридина. К раствору пиридина в этаноле (9 мл/ммоль) добавляют в атмосфере аргона палладий на активированном угле (увлажненный примерно 50% воды, 0,3 г/ммоль) и гидрируют при температуре 60C в течение ночи в атмосфере водорода при давлении 50 бар. Затем катализатор отфильтровывают через фильтровальный слой и многократно промывают этанолом. Из объединенных фильтратов отгоняют растворитель в вакууме. Общий метод 5 А. Омыление метилового эфира/эпимеризация. К раствору соответствующего метилового эфира (1,0 экв.) в метаноле (35-40 мл/ммоль) добавляют при комнатной температуре трет-бутилат калия (10 экв.). Смесь перемешивают в течение ночи при температуре 60C. При неполном превращении добавляют воду (1,0 экв.) и перемешивают до полного превращения при температуре 60C. Для переработки отгоняют метанол в вакууме, к остатку добавляют воду и, добавляя водный 1 н. раствор соляной кислоты, подкисляют (pH 1). Смесь экстрагируют этиловым эфиром уксусной кислоты, органическую фазу сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Общий метод 6 А. Получение оксадиазола. К раствору соответствующей пиперидин-3-карбоновой кислоты в диметилформамиде (10-20 мл/ммоль) добавляют в атмосфере аргона при комнатной температуре HATU (1,2 экв.), N,Nдиизопропилэтиламин (2,2 экв.) и соответствующий N'-гидроксиимидамид (1.1 экв.). Реакционную смесь перемешивают при комнатной температуре до полного образования промежуточной стадии, после этого продолжают перемешивать при температуре 120C вплоть до образования необходимого продукта из этой промежуточной стадии. После этого реакционную смесь чистят препаративной ЖХВР. Пример 1 А. N'-Гидрокси-3-метоксипропанимидамид Согласно общему методу 1 А подвергают превращению метоксипропионитрила. Выход: 18,1 г (49% от теор., 74% чистоты). ЖХВР (метод 1 А): Rt=0,35 мин; МС (ИЭПпол): m/z=119 [M+H]+. Пример 2 А. 3-Этокси-N'-гидроксипропанимидамид 3 Согласно общему методу 2 А подвергают превращению 5,0 г (50,4 ммоль) 3-этоксипропионитрила. Выход: 0,6 г (8% от теор., 90% чистоты). ЖХВР (метод 1 А): Rt=0,60 мин; МС (ИЭПпол): m/z=133 [M+H]+. Согласно общему методу 2 А подвергают превращению 7,2 г (107,3 ммоль) нитрила циклопропанкарбоновой кислоты. Выход: 4,8 г (44% от теор.). ЖХ-МС (метод 2 В): Rt=0,16 мин; МС (ИЭПпол): m/z=101 [M+H]+. Пример 4 А. Метиловый эфир 5-(4-этилфенил)пиридин-3-карбоновой кислоты Согласно общему методу 3 А подвергают взаимодействию 32 г (148 ммоль) метилового эфира 5 бромникотиновой кислоты и 27 г (178 ммоль, 1,2 экв.) 4-этилфенилборной кислоты. Выход: 24 г (64% от теор.) ЖХ-МС (метод 3 В): Rt=2,03 мин; МС (ИЭПпол): m/z=242 [M+H]+. 1 Согласно общему методу 4 А гидрируют 24 г (94 ммоль) метилового эфира 5-(4 этилфенил)пиридин-3-карбоновой кислоты. Выход: 20 г (77% от теор.). ЖХ-МС (метод 4 В): Rt=1,43 мин; МС (ИЭПпол): m/z=248 [M+H]+. Пример 6 А. Метил-5-(4-этилфенил)-1-(тиоморфолин-4-илкарбонил)пиперидин-3-карбоксилат [рацемическая смесь цис-/транс-изомеров] 5,00 г (12,1 ммоль) 3-метил-1-(4-нитрофенил)-5-(4-этилфенил)пиперидин-1,3-дикарбоксилата (пример 30 А), 3,57 г (36,4 ммоль) тиоморфолина и 5,03 г (36,4 ммоль) карбоната калия помещают в 76 мл ДМФ и нагревают 5 порциями при 150C в течение 1,5 ч в микроволновой печи типа Single Mode (фирмыEmrys Optimizer). Для переработки объединяют реакционные растворы, фильтруют и остаток чистят препаративной ЖХВР. Выход: 3,07 г (67% от теор.) ЖХ-МС (метод 5 В): Rt=1,16 и 1,18 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=377 [M+H]+. Пример 7 А. 5-(4-Этилфенил)-1-(тиоморфолин-4-илкарбонил) пиперидин-3-карбоновая кислота [рацемический цис-изомер] Согласно общему методу 5 А подвергают взаимодействию 3,00 г (7,97 ммоль) соединения примера 6 А и 8,94 г (79,7 ммоль) трет-бутилата калия. Реакция приводит селективно к цис-изомеру. Выход: 2,74 г Согласно общему методу 6 А подвергают взаимодействию 300 мг (0,828 ммоль) соединения примера 7 А и 134 мг (0,910 ммоль) N'-гидрокси-3-метоксипропанимидамида. Выход: 185 мг (49% от теор.) ЖХ-МС (метод 5 В): Rt=1,22 мин; МС (ИЭПпол): m/z=445 [M+H]+. Пример 9 А. Согласно общему методу 6 А подвергают взаимодействию 300 мг (0,828 ммоль) соединения примера 7 А и 91 мг (0,91 ммоль) N'-гидроксициклопропанкабоксимидамида. Выход: 141 мг (40% от теор.). ЖХ-МС (метод 5 В): Rt=1,32 мин; МС (ИЭПпол): m/z=427 [M+H]+. 1 Согласно общему методу 6 А подвергают взаимодействию 300 мг (0,828 ммоль) соединения примера 7 А и 112 мг (1,08 ммоль) N',3-дигидроксипропанимидамида [Graham A. Showell и др., J. Med. Chem.,1991, 34, 1086-1094]. Выход: 248 мг (66% от теор.) ЖХ-МС (метод 5 В): Rt=2,22 мин; МС (ИЭПпол): m/z=431 [M+H]+. Пример 11 А. 3-[3-(2-Этоксиэтил)-1,2,4-оксадиазол-5-ил]-5-(4-этилфенил)пиперидин-1 ил(тиоморфолин-4-ил)метанон [рацемический цис-изомер] Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,655 ммоль) соединения примера 7 А и 355 мг (около 2,152 ммоль) 3-этокси-N'-гидроксипропанимидамида. Выход: 389 мг (49% от теор.). ЖХ-МС (метод 6 В): Rt=2,61 мин; МС (ИЭПпол): m/z=459 [M+H]+. 1 Согласно общему методу 3 А подвергают взаимодействию 28 г (132 ммоль) метилового эфира 5 бромникотиновой кислоты и 30 г (158 ммоль, 1,2 экв.) 4-трифторметилфенилборной кислоты. Выход: 32 г (85% от теор.). ЖХ-МС (метод 4 В): Rt=2,27 мин; МС (ИЭПпол): m/z=282 [M+H]+. Пример 13A. Метиловый эфир 5-[4-(трифторметил)фенил]пиперидин-3-карбоновой кислоты [рацемическая смесь цис-/транс-изомеров] Согласно общему методу 4 А гидрируют 32 г (112 ммоль) метилового эфира 5-[4(трифторметил)фенил]пиридин-3-карбоновой кислоты (пример 12 А). Выход: 26 г (82% от теор.). ЖХ-МС (метод 1B): Rt=1,35 и 1,41 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=288 [M+H]+. 1 20,0 г (69,6 ммоль) метил-5-[4-(трифторметил)фенил]пиперидин-3-карбоксилата (пример 13 А) растворяют в 1,0 л дихлорметана и при температуре 0C добавляют 14,1 г (139 ммоль) триэтиламина. Затем добавляют по каплям 14,0 г (69,6 ммоль) 4-нитрофенил-хлорокарбоната. Реакционную смесь перемешивают в течение 2 ч при температуре 0C и затем в течение 16 ч при комнатной температуре. Для переработки промывают насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Получают 31,3 г сырого продукта, который подвергают взаимодействию без дальнейших операций по очистке. ЖХ-МС (метод 3 В): Rt=2,44 мин и 2,48 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=453 [M+H]+. Пример 15 А. Метил-1-(тиоморфолин-4-илкарбонил)-5-[4-(трифторметил)фенил]пиперидин-3 карбоксилат [рацемическая смесь цис-/транс-изомеров] 10,0 г (22,1 ммоль) 3-метил-1-(4-нитрофенил)-5-[4-(трифторметил)фенил]пиперидин-1,3 дикарбоксилата, 6,84 г (66,3 ммоль) тиоморфолина и 9,17 г (66,3 ммоль) карбоната калия помещают в 150 мл ДМФ и 10 порциями нагревают в течение 1 ч при температуре 150C в микроволновой печи типаSingle Mode (фирмы Emrys Optimizer). Для переработки реакционные растворы объединяют, фильтруют и остаток чистят препаративной ЖХВР. Выход: 5,16 г (55% от теор.). ЖХ-МС (метод 5 В): Rt=1,13 и 1,16 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=417 [M+H]+. Пример 16 А. 1-(Тиоморфолин-4-илкарбонил)-5-[4-(трифторметил)фенил]пиперидин-3-карбоновая кислота [рацемический цис-изомер] Согласно общему методу 5 А подвергают взаимодействию 5,16 г (12,4 ммоль) соединения примера 15 А и 13,9 г (124 ммоль) трет-бутилата калия. Реакция приводит селективно к цис-изомеру. Выход: 4,90 г Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,4 91 ммоль) соединения примера 16 А и 164 мг (1,640 ммоль) N'-гидроксициклопропанкарбоксимидамида. Выход: 352 мг (47% от теор.). ЖХ-МС (метод 5 В): Rt=1,28 мин; МС (ИЭПпол): m/z=467 [M+H]+. 1 Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,4 91 ммоль) соединения примера 16 А и 242 мг (1,640 ммоль) N'-гидрокси-3-метоксипропанимидамида. Выход: 350 мг (46% от теор.). ЖХ-МС (метод 5 В): Rt=1,18 мин; МС (ИЭПпол): m/z=485 [M+H]+. 1 Н-ЯМР (400 МГц, ДМСО-d6):7,70 (d, 2H), 7,57 (d, 2H), 3,95 (d, 1H), 3,68 (t, 2H), 3,58 (d, 1H), 3,513,36 (m, 5H), 3,23 (s, 3H), 3,13-2,96 (m, 3H), 2,94 (t, 2H), 2,60 (br. s., 4H), 2,33 (br. d., 1 Н), 2,10-1,95 (m, 1 Н). Пример 19 А. 3-[3-(2-Этоксиэтил)-1,2,4-оксадиазол-5-ил]-5-[4-(трифторметил)фенил]пиперидин-1 ил(тиоморфолин-4-ил)метанон [рацемический цис-изомер] Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,491 ммоль) соединения примера 16 А и 320 мг (около 1,983 ммоль) 3-этокси-N'-гидроксипропанимидамида. Выход: 343 мг (46% от теор.). Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,491 ммоль) соединения примера 16 А и 201 мг (1,938 ммоль) N',3-дигидроксипропанимидамида. Выход: 494 мг (68% от теор.). ЖХ-МС (метод 5 В): Rt=1,04 мин; МС (ИЭПпол): m/z=471 [M+H]+. Пример 21 А. Метиловый эфир 5-[4-(трифторметокси)фенил]пиридин-3-карбоновой кислоты Согласно общему методу 3A подвергают взаимодействию 23 г (105 ммоль) метилового эфира 5 бромникотиновой кислоты и 26 г (126 ммоль, 1,2 экв.) 4-трифторметоксифенилборной кислоты. Выход: 14 г (41% от теор.). ЖХ-МС (метод 1B): Rt=2,44 мин; МС (ИЭПпол): m/z=298 [M+H]+. Альтернативный синтез. К раствору 26 г (121 ммоль) метилового эфира 5-бромникотиновой кислоты в толуоле (220 мл) в атмосфере аргона при комнатной температуре добавляют 2,8 г (2,4 ммоль) тетракис(трифенилфосфин)палладия и затем добавляют раствор 30 г (146 ммоль) 4-трифторметоксифенилборной кислоты в этаноле (58 мл). После добавления 14 г (243 ммоль) фтористого кальция в воде (58 мл) перемешивают в течение ночи в условиях рефлюкса, затем добавляют еще 0,70 г (0,61 ммоль) тетракис(трифенилфосфин)палладия и перемешивают еще в течение 24 ч в условиях рефлюкса. После нового добавления 1,4 г (1,2 ммоль) тетракис(трифенилфосфин)палладия перемешивают в течение 20 ч в условиях рефлюкса, к реакционному раствору добавляют этиловый эфир уксусной кислоты и промывают водой и насыщенным водным раствором хлористого натрия. Органические фазы сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Остаток чистят на хроматографической колонке К 14 г (45 ммоль) метилового эфира 5-[4-(трифторметокси)фенил]пиридин-3-карбоновой кислоты в этаноле (500 мл) добавляют 17 г увлажненного палладий/уголь-катализатора (10% палладия, 50% воды) и затем гидрируют в течение ночи при температуре 60C и при давлении 50 бар водородной атмосферы. Реакционный раствор фильтруют, остаток после фильтрования промывают этанолом и отгоняют растворитель из фильтрата. Остаток чистят на хроматографической колонке (силикагель, дихлорметан/метанол 600:110:1). Выход: 8 г (59% от теор.). ЖХ-МС (метод 1B): Rt=1,29 мин и 1,33 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=304 [M+H]+; 1 К 8,0 г (26,4 ммоль) метилового эфира 5-(4-(трифторметокси)фенил)пиперидин-3-карбоновой кислоты (пример 22 А) и 5,34 г (26,3 ммоль) триэтиламина в 666 мл дихлорметана медленно добавляют при температуре 0C 5,32 г (26,4 ммоль) 4-нитрофенилхлороформата. Смесь перемешивают в течение 2 ч при комнатной температуре. Для переработки реакционную смесь промывают вначале насыщенным водным раствором гидрокарбоната натрия, а затем водой. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме. Остаток чистят с помощью флэш-хроматографии на силикагеле (растворитель: циклогексан/этиловый эфир уксусной кислоты 1:2 до 1:1). Выход: 7,32 г (54% от теор.). ЖХ-МС (метод 3B): Rt=2,47 мин; МС (ИЭПпол): m/z=469 [M+H]+. Пример 24 А. Метил-1-(тиоморфолин-4-илкарбонил)-5-[4-(трифторметокси)фенил]пиперидин-3 карбоксилат [рацемическая смесь цис-/транс-изомеров] 12,0 г (25,1 ммоль) 3-метил-1-(4-нитрофенил)-5-[4-(трифторметокси)фенил]пиперидин-1,3 дикарбоксилата, 7,77 г (75,3 ммоль) тиоморфолина и 10,4 г (75,3 ммоль) карбоната калия помещают в 180 мл ДМФ и 12 порциями нагревают при температуре 150C в течение 2 ч в микроволновой печи типаSingle Mode (фирмы Emrys Optimizer). Для переработки реакционные растворы объединяют, фильтруют и остаток чистят препаративной ЖХВР. Выход: 7,88 г (73% от теор.). ЖХ-МС (метод 5 В): Rt=1,16 и 1,18 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=433 [M+H]+. 1 К раствору 7,85 г (18,2 ммоль) соединения примера 24 А в метаноле (650 мл) добавляют при комнатной температуре 20,4 г (182 ммоль) трет-бутилата калия. Смесь перемешивают в течение ночи при температуре 60C. Для переработки отгоняют метанол в вакууме, к остатку добавляют воду и, добавляя водный 1 н. раствор соляной кислоты, делают раствор кислым (pH 1). Смесь экстрагируют этиловым эфиром уксусной кислоты, органическую фазу сушат над сульфатом магния, фильтруют и отгоняют растворитель. Реакция дает смесь 85:15 цис/транс-изомеров. Выход: 7,70 г (99% от теор.). ЖХ-МС (метод 5 В): Rt=1,03 мин (транс-изомер) и 1,04 мин (цис-изомер); МС (ИЭПпол): m/z=419 Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,43 ммоль) соединения примера 25 А и 232 мг (1,58 ммоль) N'-гидрокси-3-метоксипропанимидамида. Выход: 398 мг (53% от теор.). ЖХ-МС (метод 5 В): Rt=1,21 мин; МС (ИЭПпол): m/z=501 [M+H]+. 1 Согласно общему методу 6 А подвергают взаимодействию 300 мг (0,717 ммоль) соединения примера 25 А и 79 мг (0,789 ммоль) N'-гидроксициклопропанкарбоксимидамида. Выход: 135 мг (39% от теор.). ЖХ-МС (метод 2 В): Rt=1,44 мин; МС (ИЭПпол): m/z=483 [M+H]+. Альтернативный синтез. К 600 мг (1,43 ммоль) соединения примера 25 А в диметилформамиде (29,0 мл) при комнатной температуре добавляют 654 мг (1,72 ммоль) HATU и 0,55 мл (498 мг, 3,16 ммоль) N,Nдиизопропилэтиламина и перемешивают в течение 30 мин. Затем добавляют 158 мг (1,58 ммоль) N'гидроксициклопропан-карбоксимидамида и перемешивают в течение ночи при комнатной температуре. Реакционную смесь нагревают до 120C и перемешивают в течение 1 ч при этой температуре. Реакционную смесь чистят напрямую препаративной ЖХВР. Выход: 315 мг (45% от теор.). ЖХ-МС (метод 5 В): Rt=1,30 мин; МС (ИЭПпол): m/z=483 [M+H]+. 1 Согласно общему методу 6 А подвергают взаимодействию 600 мг (1,434 ммоль) соединения примера 25 А и 307 мг (около 1,864 ммоль) 3-этокси-N'-гидроксипропанимидамида. Выход: 403 мг (55% от теор.). ЖХ-МС (метод 6 В): Rt=2,61 мин; МС (ИЭПпол): m/z=515 [M+H]+. 1 Согласно общему методу 6 А подвергают взаимодействию 1,00 г (2,390 ммоль) соединения примера 25 А и 323 мг (3,107 ммоль) N',3-дигидроксипропанимидамида. Выход: 848 мг (69% от теор.). ЖХ-МС (метод 6 В): Rt=2,26 мин; МС (ИЭПпол): m/z=487 [M+H]+. Пример 30 А. 3-Метил-1-(4-нитрофенил)-5-(4-этилфенил)пиперидин-1,3-дикарбоксилат [рацемическая смесь цис-/транс-изомеров] 3,0 г (12,1 ммоль) соединения примера 5 А помещают в 30 мл дихлорметана, охлаждают до температуры 0C и добавляют 3,4 мл (2,4 г, 12,1 ммоль) триэтиламина, а также 2,4 г (12,1 ммоль) 4 нитрофенилового эфира хлормуравьиной кислоты. Реакционную смесь медленно нагревают до комнатной температуры и перемешивают в течение 16 ч при комнатной температуре. Промывают многократно водой, сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Остаток чистят на хроматографической колонке на силикагеле (растворитель дихлорметандихлорметан/метанол 100:2). Выход: 4,7 г (83% от теор., 89% чистоты). ЖХВР (метод 1 А): Rt=4,94 мин и 5,00 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=413 [M+H]+. Пример 31 А. 4-Нитрофенилтиоморфолин-4-карбоксилат 7,7 г (74,4 ммоль) тиоморфолина помещают в 100 мл дихлорметана и при охлаждении на ледяной бане добавляют 20,7 мл (15,1 г, 148,8 ммоль) триэтиламина. Добавляют по порциям 10,0 г (49,6 ммоль) нитрофенилового эфира хлормуравьиной кислоты. Реакционную смесь перемешивают в течение 1 ч при комнатной температуре и добавляют воду и этиловый эфир уксусной кислоты. Органическую фазу отделяют, промывают 1 N раствором соляной кислоты, а также насыщенным раствором хлористого натрия,сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Выход: 13,2 г (99% от теор.). ЖХ-МС (метод 5 В): Rt=0,98 мин; МС (ИЭПпол): m/z=269 [M+H]+. 1 Н-ЯМР (400 МГц, ДМСО-d6):8,28 (d, 2H), 7,46 (d, 2H), 3,86 (br. s., 2 Н), 3,72 (br. s., 2H), 2,71 (br. 13,1 г (49,0 ммоль) 4-нитрофенилтиоморфолин-4-карбоксилата помещают в 135 мл дихлорметана и при температуре 0C добавляют порциями 7,6 г (44,1 ммоль) м-хлорпербензойной кислоты. Перемешивают в течение 2 ч при комнатной температуре, добавляют воду и отделяют органическую фазу. Органическую фазу быстро промывают насыщенным водным раствором гидрокарбоната натрия, фильтруют и отгоняют растворитель в вакууме. Сырой продукт чистят препаративной ЖХВР. Выход: 7,8 г (56% от 17,6 г (81,4 ммоль) метилового эфира 5-бромникотиновой кислоты помещают в 375 мл ДМФ в атмосфере аргона, добавляют 26,9 г (105,8 ммоль) 4,4,4',4',5,5,5',5'-октаметил-2,2'-би-1,3,2-диоксаборолана,3,0 г (3,6 ммоль) трис-(дибензилиден-ацетон)дипалладия(0), 1,8 г (6,5 ммоль) трициклогексилфосфина и 32,0 ммоль (325,9 ммоль) ацетата калия. Реакционную смесь перемешивают в течение 20 ч при температуре 100C. Затем отгоняют растворитель в вакууме, к остатку добавляют 40 мл воды и 140 мл третбутилметилового эфира и отделяют органическую фазу. Водную фазу экстрагируют три раза по 80 мл трет-бутилметилового эфира. Объединенные органические экстракты промывают насыщенным водным раствором хлористого натрия, сушат над сульфатом магния, фильтруют и отгоняют растворитель. Остаток растворяют в 360 мл метанола и добавляют 36 мл концентрированной соляной кислоты. Реакционную смесь нагревают 22 ч в условиях рефлюкса и затем 12 ч перемешивают при комнатной температуре. Примерно половину растворителя отгоняют в вакууме, раствор фильтруют и далее концентрируют в вакууме. Маслянистый остаток два раза перекристаллизовывают из ацетона, остаток помещают в 10 мл ацетона и добавляют 100 мл трет-бутилметилового эфира. Через 16 ч образовавшийся осадок отделяют от раствора. Этот осадок перемешивают с 50 мл ацетона, оставляют стоять на 5 недель при комнатной температуре и снова отделяют раствор. Растворы объединяют, отгоняют растворитель и растворяют в 50 мл трет-бутилметилового эфира. Оставляют стоять 5 недель при комнатной температуре и после этого отделяют осадок. Осадок три раза промывают трет-бутилметиловым эфиром и сушат в вакууме в сушильном шкафу. ЖХ-МС (метод 4 В): Rt=0,91 мин; МС (ИЭПпол): m/z=182 [M+H]+. Пример 34A. Метиловый эфир 5-[4-(дифторметокси)фенил]никотиновой кислоты 10,0 г (44,8 ммоль) 4-(дифторметокси)бромбензола подвергают взаимодействию согласно общему методу 3A с 14,6 г (67,3 ммоль) гидрохлорида [5-(метоксикарбонил)пиридин-3-ил]борной кислоты. Высвобождение гидрохлорида достигается дополнительным добавлением 6,80 г (49,3 ммоль) карбоната калия. Выход: 8,6 г (67% от теор.). ЖХ-МС (метод 2 В): Rt=1,15 мин; МС (ИЭПпол): m/z=280 [M+H]+. Пример 35 А. Метиловый эфир 5-[4-(дифторметокси)фенил]пиперидин-3-карбоновой кислоты [рацемическая смесь цис-/транс-изомеров] К раствору 8,6 г (30,9 ммоль) метилового эфира 5-[4-(дифторметокси)фенил]никотиновой кислоты в концентрированной уксусной кислоте (112 мл) добавляют 841 мг палладий/угля (10% палладия) и 1,12 г оксида платины(IV). Затем гидрируют в течение 24 ч при нормальном давлении водородной атмосферы. Из реакционного раствора отгоняют растворитель в вакууме, подкисляют 1 N соляной кислотой(pH 1), экстрагируют диэтиловым эфиром, затем с помощью насыщенного водного раствора гидрокарбоната натрия делают основным (pH10) и многократно экстрагируют этиловым эфиром уксусной кислоты. Объединенные фильтраты сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Выход: 6,6 г (74% от теор.). ЖХ-МС (метод 5 В): Rt=0,65 мин и 0,66 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=286 [M+H]+. 2,2 г (7,7 ммоль) метилового эфира 5-[4-(дифторметокси)фенил]пиперидин-3-карбоновой кислоты растворяют в 14 мл N-метилпирролидона, добавляют 4,0 мл (3,0 г, 23,0 ммоль) N,Nдиизопропилэтиламина и 3,5 г (11,5 ммоль) 4-нитрофенил-тиоморфолин-4-карбоксилат-1,1-диоксида. Реакционную смесь подвергают превращению в течение 7 мин при температуре 180C в микроволновой печи. Затем добавляют воду и этиловый эфир уксусной кислоты, отделяют водную фазу и многократно экстрагируют этиловым эфиром уксусной кислоты. Объединенные органические экстракты промывают водой и насыщенным водным раствором хлористого натрия, сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Остаток растворяют в диэтиловом эфире, фильтруют и фильтрат чистят препаративной ЖХВР. Выход: 2,0 г (51% от теор.). ЖХ-МС (метод 5 В): Rt=0,92 мин и 0,94 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=447 [M+H]+. Пример 37 А. 5-[4-(Дифторметокси)фенил]-1-[(1,1-диоксидотиоморфолин-4-ил)карбонил]пиперидин-3-карбоновая кислота [рацемическая смесь цис-изомеров] Согласно общему методу 4 А подвергают взаимодействию 2,7 г (6,1 ммоль) метилового эфира 5-[4(дифторметокси)фенил]-1-[(1,1-диоксидотиоморфолин-4-ил)карбонил]пиперидин-3-карбоновой кислоты с 6,9 г (61,3 ммоль) трет-бутилата калия. Выход: 2,1 г (77% от теор.). ЖХ-МС (метод 5 В): Rt=0,82 мин; МС (ИЭПпол): m/z=433 [M+H]+. Пример 38 А. Метиловый эфир 5-[4-(дифторметокси)фенил]-1-[(1-оксидо-тиоморфолин-4 ил)карбонил]пиперидин-3-карбоновой кислоты [смесь цис-/транс-изомеров] 2,2 г (7,7 ммоль) метилового эфира 5-[4-(дифторметокси)фенил]пиперидин-3-карбоновой кислоты растворяют в 14 мл N-метилпирролидона, добавляют 4,0 мл (3,0 г, 23,0 ммоль) N,Nдиизопропилэтиламина и 3,3 г (11,5 ммоль) 4-нитрофенил-тиоморфолин-4-карбоксилат-1-оксида. Реакционную смесь подвергают взаимодействию в течение 7 мин при температуре 180C в микроволновой печи. Затем добавляют воду и этиловый эфир уксусной кислоты, водную фазу отделяют и многократно экстрагируют этиловым эфиром уксусной кислоты. Объединенные органические экстракты промывают водой и насыщенным водным раствором хлористого натрия, сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Остаток чистят препаративной ЖХВР. Выход: 2,2 г (59% от теор.). ЖХ-МС (метод 5 В): Rt=0,90 мин и 0,92 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=431 [M+H]+. Согласно общему методу 4 А подвергают взаимодействию 2,7 г (6,3 ммоль) метилового эфира 5-[4(дифторметокси)фенил]-1-[(1-оксидотиоморфолин-4-ил)карбонил]пиперидин-3-карбоновой кислоты с 7,1 г (63,3 ммоль) трет-бутилата калия. Из реакционной смеси отгоняют растворитель в вакууме, остаток суспендируют в воде и делают кислым, добавляя концентрированную соляную кислоту. Осадок отфильтровывают, промывают водой и сушат в вакууме. Выход: 1,1 г (34% от теор.). ЖХ-МС (метод 5 В): Rt=0,75 мин; МС (ИЭПпол): m/z=417 [M+H]+. Пример 40A. 1-Бром-4-(2,2,2-трифторэтил)бензол К раствору 25,0 г (100 ммоль) 4-бромбензилбромида в 1-метил-2-пирролидоне (121 мл) добавляют при комнатной температуре 4,95 г (26,0 ммоль) йодида меди(I) и 37,5 г (195 ммоль) метил-2,2-дифтор-2(фторсульфонил)ацетата. Нагревают до 80C и затем перемешивают в течение ночи. Реакционный раствор выливают в воду и экстрагируют диэтиловым эфиром, а затем органическую фазу сушат над сульфатом натрия. После фильтрования и отгонки растворителя из органической фазы в вакууме остаток чистят на хроматографической колонке (силикагель, циклогексан/этиловый эфир уксусной кислоты 20:1). Выход: 16,1 г (67% от теор.). ГХ-МС (метод 1F): Rt=2,66 мин; МС (ИЭПпол): m/z=240 [M+H]+. Пример 41 А. Метил-5-[4-(2,2,2-трифторэтил)фенил]никотинат К раствору 8,00 г (33,5 ммоль) соединения примера 40 А в толуоле (304 мл) добавляют в атмосфере аргона при комнатной температуре 10,9 г (50,2 ммоль) соединения примера 33 А в этаноле (100 мл) и 5,10 г (36,8 ммоль) карбоната калия. После перемешивания в течение 10 мин добавляют 3,87 г (3,35 ммоль) тетракис(трифенилфосфин)палладия и затем 5,83 г (100 ммоль) фтористого калия в воде (64 мл). Перемешивают в течение 8 ч в условиях рефлюкса, реакционную смесь охлаждают и разбавляют этиловым эфиром уксусной кислоты. Реакционный раствор промывают водой, органическую фазу сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Остаток чистят на хроматографической колонке (силикагель, дихлорметан/метанол 100:180:1). Выход: 9,20 г (69% от теор., 75% чистоты). ЖХ-МС (метод 5 В): Rt=1,06 мин; МС (ИЭПпол): m/z=296 [M+H]+. Пример 42 А. Метил-5-[4-(2,2,2-трифторэтил)фенил]пиперидин-3-карбоксилат [рацемическая смесь цис-/транс-изомеров](192 мл) добавляют 1,94 г палладий/угля (10% палладия) и 2,23 г оксида платины(IV). Затем гидрируют в течение 6 ч при нормальном давлении в атмосфере водорода, после этого добавляют еще 1,00 г палладий/угля (10% палладия) и 2,00 г оксида платины(IV) и гидрируют в течение ночи при нормальном давлении в атмосфере водорода. В заключение добавляют еще 1,00 г палладий/угля (10% палладия) и 3,00 г оксида платины(IV) и гидрируют в течение 24 ч при нормальном давлении в атмосфере водорода. Реак- 28021944 ционный раствор фильтруют через целит, остаток после фильтрования промывают метанол/водой и из объединенных фильтратов отгоняют растворитель в вакууме. Остаток растворяют в дихлорметане и затем промывают 1 N водным раствором карбоната натрия. Органическую фазу сушат над сульфатом натрия, фильтруют и отгоняют растворитель в вакууме. Выход: 6,64 г (85% от теор., 90% чистоты). ЖХ-МС (метод 2 В): Rt=0,83 мин и 0,84 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=302 [M+H]+. Пример 43 А. 3-Метил-1-(4-нитрофенил)-5-[4-(2,2,2-трифторэтил)фенил]пиперидин-1,3 дикарбоксилат [рацемическая смесь цис-/транс-изомеров] К раствору 6,62 г (19,8 ммоль, 90% чистоты) соединения примера 42 А в дихлорметане (211 мл) добавляют 9,65 мл (7,00 г, 69,2 ммоль) триэтиламина, а затем при температуре 0C добавляют 3,99 г (19,8 ммоль) 4-нитрофенилового эфира хлормуравьиной кислоты. Нагревают до комнатной температуры и перемешивают в течение 1 ч. Реакционный раствор промывают насыщенным водным раствором гидрокарбоната натрия и водой, органическую фазу сушат над сульфатом магния, фильтруют и в вакууме отгоняют растворитель. Выход: 10,3 г (91% от теор., 81% чистоты). ЖХ-МС (метод 2 В): Rt=1,40 мин и 1,42 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=467 [M+H]+. Пример 44 А. Метил-1-(тиоморфолин-4-илкарбонил)-5-[4-(2,2,2-трифторэтил)фенил]пиперидин-3 карбоксилат [рацемическая смесь цис-/транс-изомеров](65 мл) добавляют 12,6 мл (13,7 г, 132 ммоль) тиоморфолина и 11,5 мл (8,56 г, 66,2 ммоль) N,Nдиизопропилэтиламина, а затем 5 порциями нагревают при температуре 150C в течение 1 ч в микроволновой печи типа Single Mode (фирмы Emrys Optimizer). Для переработки объединяют реакционные растворы и чистят напрямую препаративной ЖХВР. Выход: 5,63 г (71% от теор.). ЖХ-МС (метод 5 В): Rt=1,13 и 1,16 мин (цис-/транс-изомеры); МС (ИЭПпол): m/z=431 [M+H]+. Пример 45 А. 1-(Тиоморфолин-4-илкарбонил)-5-[4-(2,2,2-трифторэтил)фенил]пиперидин-3 карбоновая кислота [рацемический цис-изомер] К раствору 2,97 г (6,90 ммоль) соединения примера 44 А в метаноле (83 мл) добавляют при комнатной температуре 7,74 г (69,0 ммоль) трет-бутилата калия. Смесь перемешивают в течение ночи при температуре 60C. Для переработки отгоняют метанол в вакууме, к остатку добавляют воду и подкисляют раствор, добавляя раствор водной 1 N соляной кислоты (pH 1). Смесь экстрагируют этиловым эфиром уксусной кислоты, органическую фазу сушат над сульфатом магния, фильтруют и отгоняют растворитель в вакууме. Выход: 2,61 г (76% от теор., 84% чистоты). ЖХ-МС (метод 5 В): Rt=1,02 мин; МС (ИЭПпол): m/z=417 [M+H]+.
МПК / Метки
МПК: C07D 417/14, A61K 31/541
Метки: пиперидины, замещенные
Код ссылки
<a href="https://eas.patents.su/30-21944-zameshhennye-piperidiny.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные пиперидины</a>
Предыдущий патент: Способ изготовления вагинального суппозитория
Следующий патент: Способ прогнозирования эффективности лекарственных соединений для пациента
Случайный патент: Устройство и способ анализа размера, формы и угловатости, а также состава минералов и частиц горных пород