Сульфонамиды в качестве ингибиторов белков семейства bcl-2, предназначенные для лечения рака
Номер патента: 20586
Опубликовано: 30.12.2014
Авторы: Виссер Майкл Скотт, Юсуф Наим, Миллер-Мослин Карен, Тур Бакари-Барри
Формула / Реферат
1. Соединение формулы (I)
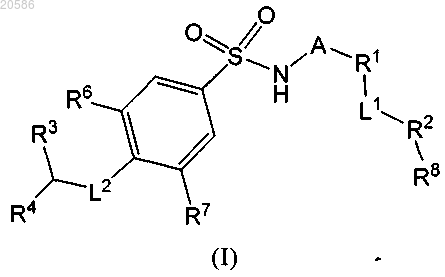
в которой А обозначает двухвалентный бициклический радикал, содержащий насыщенную циклическую структуру и ненасыщенную циклическую структуру, выбранный из
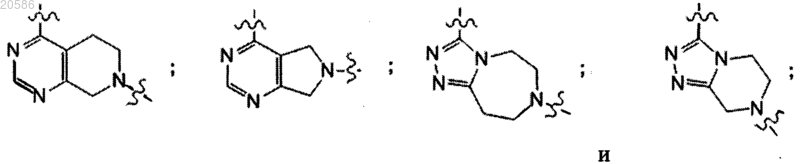
где указанная ненасыщенная циклическая структура присоединена к NH и указанная насыщенная циклическая структура присоединена к R1, где А является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (С1-C6)алкил, галогензамещенный (С1-C6)алкил, CN или NR10R11;
R1 обозначает пиперидинил, пиперазинил, морфолинил, тетрагидрофуранил, циклопропил, циклобутил, циклопентил, циклогексил или фенил, каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей метил, этил, пропил, Cl, F, Br, I или метоксигруппу;
L1 обозначает -CH2-, -СН2СН2- или связь;
L2 обозначает -CH2- или NH;
R2 обозначает фенил, нафтил, пиридинил, пиримидинил или пиридазинил, каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей метил, диметил, этил, пропил, бутил, пентил, гексил, фенил, циклопропил, циклобутил, циклопентил, CF3 или CH2Cl;
R8 обозначает (С1-C6)алкил, (C6-C14)арил, (С3-С14)циклоалкил, галоген или 3-14-членный циклогетероалкил, где любая из указанных выше углеводородных групп необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, (С1-C6)алкил, галогензамещенный (С1-C6)алкил, ОН или NR44R45;
R3 и R4 независимо обозначают (С1-C6)алкил, (С1-C3)алкилен-(C6-C14)арил, (C1-С3)алкилен-(5-14-членный гетероарил), (С1-C3)алкилен-CONR16R17, (C1-C3)алкилен-O-R15, (С1-C3)алкилен-NR13R14, (С1-C3)алкилен-(3-14-членный циклогетероалкил) или (С1-C3)алкилен-S-(С6-С14)арил;
R6 и R7 все независимо обозначают Н, NO2, SO2CF3, SO2(С1-C6)алкил, галогензамещенный (С1-C6)алкил, галоген, (C3-С14)циклоалкил или CN;
R10, R11, R13, R14, R16, R17, R44 и R45 все независимо обозначают Н, (C1-С6)алкил, (С2-C6)алкенил, (C2-C6)алкинил, ОН, -С(О)(С1-C6)алкил, (C1-C6)алкоксигруппу, галоген, (C3-С14)циклоалкил, (С6-С14)арил, 4-14-членный циклогетероалкил или 5-14-членный гетероарил, где каждая из указанных выше углеводородных групп необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, гидроксигруппу, (C1-С6)алкоксигруппу, аминогруппу, (C1-С6)алкиламиногруппу, ди((С1-С6)алкил)аминогруппу или цианогруппу; или
R13 и R14 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил; или
R16 и R17 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил; или
R44 и R45 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил;
R15 независимо обозначает -(С1-С6)алкилен-(С6-С14)арил или -(С1-С6)алкилен-(5-14-членный гетероарил), каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (C1-С6)алкил, галогензамещенный (С1-C6)алкил или CN;
или его фармацевтически приемлемая соль.
2. Соединение формулы (I) по п.1, в которой R1 обозначает пиперидинил, пиперазинил, морфолинил, циклопентил или циклогексил, каждый из которых является незамещенным или содержит следующие заместители: метил, метоксигруппу, Cl или F, или его фармацевтически приемлемая соль.
3. Соединение формулы (I) по п.1, в которой R3 обозначает -СН2-фенил, -СН2СН2-фенил, -СН2СН2СН2-фенил, -СН2-пиридинил, -СН2СН2-пиридинил, -СН2-пиримидинил, -СН2СН2-пиримидинил,
-CH2C(O)NCH3CH3, -CH2C(O)NHCH3, -CH2CH2C(O)NCH3CH3, -CH2-O-CH3, -СН2-О-СН2СН3, -СН2-S-фенил, -СН2СН2-S-фенил или -СН2СН2СН2-S-фенил; R4 обозначает -СН2С(О)СН3, -СН2С(О)СН2СН3,
-СН2СН2С(О)СН3, -CH2-S-CH3, CH2-S-CH2CH3, -CH2-N(CH3)(CH3), -CH2-NHCH3, -CH2-NH2, -СН2-NH-фенил, -СН2-CH2-N(CH3)(CH3), -CH2CH2-NHCH3, -CH2CH2-NH2 или -СН2СН2-NH-фенил, или его фармацевтически приемлемая соль.
4. Соединение формулы (Ib)
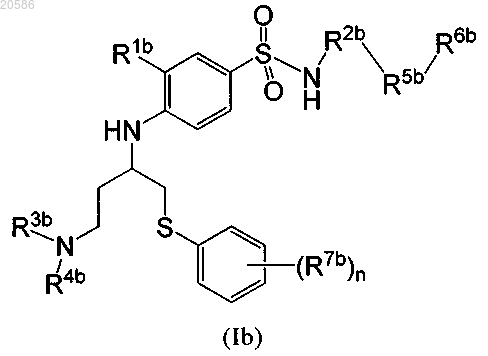
в которой R1b обозначает Н, NO2, SO2CF3, SO2(С1-C6)алкил, галогензамещенный (С1-C6)алкил, галоген, (С3-С14)циклоалкил или CN;
R2b обозначает двухвалентный бициклический радикал, содержащий насыщенную циклическую структуру и ненасыщенную циклическую структуру, выбранный из
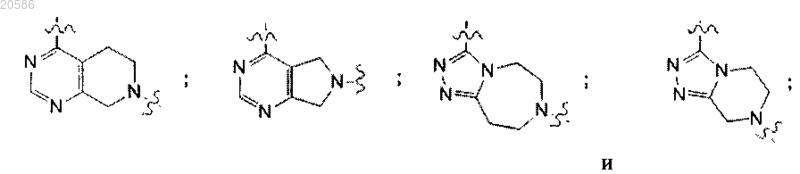
где указанная ненасыщенная циклическая структура присоединена к NH и указанная насыщенная циклическая структура присоединена к R5b, где R2b может быть незамещенным или содержит один или большее количество следующих заместителей: галоген, ОН, (С1-C6)алкил, галогензамещенный (С1-C6)алкил, CN или NH2;
R3b и R4b независимо обозначают Н, (С1-C6)алкил, (C2-C6)алкенил, (С2-C6)алкинил, (С6-С14)арил, 5-14-членный гетероарил, (C3-С14)циклоалкил, галоген или 3-14-членный циклогетероалкил, каждый из которых, если он не обозначает Н, является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей гидроксигруппу, цианогруппу, нитрогруппу, (С1-С8)алкил, (C2-С8)алкенил, (C2-С8)алкинил, (C1-С8)алкоксигруппу, (С2-С8)алкенилоксигруппу, (C2-С8)алкинилоксигруппу, галоген, (С1-С8)алкилкарбонил, карбоксигруппу, (С1-С8)алкоксикарбонил, аминогруппу, (С1-С8)алкиламиногруппу, ди((С1-С8)алкил)аминогруппу, (C1-С8)алкиламинокарбонил, ди((С1-С8)алкил)аминокарбонил, (C1-С8)алкилкарбониламиногруппу, (С1-С8)алкилкарбонил((С1-С8)алкил)аминогруппу, (С1-С8)алкилсульфониламиногруппу, (С1-С8)алкилтиогруппу, (C1-С8)алкилсульфинил, (С1-С8)алкилсульфонил, аминосульфонил, (C1-С8)алкиламиносульфонил или ди((С1-С8)алкил)аминосульфонил, где каждая из указанных выше углеводородных групп необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, гидроксигруппу или (С1-С8)алкоксигруппу;
R5b обозначает 3-8-членный циклогетероалкил, (C3-С8)циклоалкил или (С6-С14)арил, который является незамещенным или содержит следующие заместители: (C1-C6)алкил, галоген, ОН, (С1-C3)алкоксигруппу, NH2 или дейтерий;
R6b обозначает Lb-R8b;
R7b обозначает гидроксигруппу, цианогруппу, нитрогруппу, (С1-С8)алкил, (C2-С8)алкенил, (C2-С8)алкинил, (C2-С8)алкоксигруппу, (C2-С8)алкенилоксигруппу, (C2-С8)алкинилоксигруппу, галоген, (С1-С8)алкилкарбонил, карбоксигруппу, (C1-С8)алкоксикарбонил, аминогруппу, (C1-С8)алкиламиногруппу, ди(C1-С8)алкиламиногруппу, (С1-С8)алкиламинокарбонил, ди((С1-С8)алкил)аминокарбонил, (С1-С8)алкилкарбониламиногруппу, (C1-С8)алкилкарбонил((С1-С8)алкил)аминогруппу, (С1-С8)алкилсульфониламиногруппу, (С1-С8)алкилтиогруппу, (С1-С8)алкилсульфинил, (С1-С8)алкилсульфонил, аминосульфонил, (C1-C8)алкиламиносульфонил или ди((С1-С8)алкил)аминосульфонил, где каждая из указанных выше углеводородных групп необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН или (C1-С8)алкоксигруппу;
Lb обозначает -(С1-C3)алкилен-, -(С2-С4)алкенилен-, -С(О)-, -С(О)О-, -C(O)N(H)-, -(C1-C3)алкил-С(О)-, -(С1-C3)алкил-С(О)О- или связь, где Lb является незамещенным или содержит один или большее количество следующих заместителей: (С1-С4)алкил, галогензамещенный (С1-С4)алкил или (C3-С8)циклоалкил;
R8b обозначает (C6-C14)арил, 5-14-членный гетероарил, 3-8-членный циклогетероалкил или (C3-С14)циклоалкил, каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (С1-C6)алкил, галогензамещенный (С1-C6)алкил или CN;
n равно 0, 1, 2, 3 или 4,
или его фармацевтически приемлемая соль.
5. Способ лечения пролиферативного заболевания, включающий стадию введения нуждающемуся в нем субъекту соединения по п.1 или его фармацевтически приемлемой соли в терапевтически эффективном количестве.
6. Способ лечения по п.5, в котором указанным субъектом является животное и указанным заболеванием является хронический лимфолейкоз.
7. Способ лечения пролиферативного заболевания, включающий стадию введения нуждающемуся в нем субъекту фармацевтической композиции, содержащей в терапевтически эффективном количестве соединение по п.1 или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый инертный наполнитель.
8. Способ лечения по п.7, в котором указанным субъектом является животное и указанным заболеванием является хронический лимфолейкоз.
9. Фармацевтическая композиция, содержащая соединение формулы (I) по любому из пп.1-4 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или инертный наполнитель.
10. Соединение или его фармацевтически приемлемая соль, выбранное из следующих соединений:










Текст
СУЛЬФОНАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ СЕМЕЙСТВА Bcl-2,ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ РАКА В изобретении описаны новые соединения и способы лечения заболевания или нарушения путем антагонистического воздействия на белки семейства Bcl-2 предпочтительно соединениями формулы (I) или их фармацевтически приемлемой солью, а также способы лечения заболевания, нарушения или синдрома, связанные с ингибированием Bcl-2, предпочтительно гиперпролиферативных заболеваний. В изобретении также описаны фармацевтические композиции, содержащие соединения формулы (I) и их фармацевтически приемлемые соли. Область техники, к которой относится изобретение Изобретение относится к сульфонамидам, которые связываются с белками семейства Bcl-2 и ингибируют их. Поэтому настоящее изобретение включает сульфонамиды, содержащие их композиции, способы их применения и способы их получения, где такие соединения обычно применимы в фармакологии в средствах лечения, механизм действия которых основан на ингибировании белков семейства Bcl-2, и более предпочтительно в средствах, предназначенных для лечения пролиферативных заболеваний,включая рак. Уровень техники Белки семейства Bcl-2 являются антиапоптозными белками, связанными с раком и другими заболеваниями. Белки семейства Bcl-2, которые исследуют в качестве мишеней для терапии, включают Bcl-2(BCL2), Bcl-xL (BCL2L1), Bcl-w (BCL2L2), A1 (BCL2A1) и MCL1 (MCL1). При многочисленных раковых заболеваниях экспрессируется один или большее количество белков семейства Bcl-2, что обеспечивает выживание раковых клеток и устойчивость к воздействию химиотерапевтических средств. Например, хромосомная транслокация гена t(14;18), кодирующего белок Bcl-2, t(14;18), является трансформирующим преобразованием в некоторых раковых клетках (Raffeld, et al. Cancer Research 1987, 47(10):253742) и обнаруживается, что выживаемость этих раковых клеток зависит от иммунной РНК, кодирующейBcl-2 (фиг. 1), и они чувствительны к воздействию недавно описанных малых молекул-ингибиторов белков семейства Bcl-2 (Oltersdorf, et al. Nature 2005, 435, 677-681; Deng et al. Cancer Cell 2007, 12(2), 171185). Настоящее изобретение относится к группе соединений, которые ингибируют белки семейства Bcl2 и стимулируют апоптоз раковых клеток по отдельности или в комбинации с другими химиотерапевтическими средствами. Показано, что в дополнение к применению для лечения В-клеточных лимфом антагонисты белков семейства Bcl-2 применимы для лечения раковых заболеваний, при которых экспрессируются представители семейства Bcl-2 или наблюдается нарушение регуляции апоптоза, таких как хронический лимфолейкоз, диффузные крупноклеточные В-клеточные лимфомы, фолликулярные лимфомы, хронический или острый лейкоз, хронический миелолейкоз, лимфоидные злокачественные новообразования Тклеточной или В-клеточной этиологии, мелкоклеточный рак легких, немелкоклеточный рак легких, меланома или другие раковые заболевания кожи, множественная миелома, рак яичников, рак молочной железы, рак толстой кишки, рак желудочно-кишечного тракта (желудка, колоректальный и двенадцатиперстной кишки), рак предстательной железы, рак мочевого пузыря, рак матки, рак шейки матки, саркома, происходящая из мягких тканей, рак поджелудочной железы, рак почки, опухоли головного мозга,печеночно-клеточный рак, рак головы и шеи, рак шейки матки, фибросаркома и другие раковые заболевания. Краткое изложение сущности изобретения Настоящее изобретение относится к соединениям и содержащим их фармацевтическим композициям,которые применимы для лечения заболеваний и/или нарушений, модулируемых ингибированием Bcl-2. Настоящее изобретение относится к соединениям формулы (I) в которой А обозначает двухвалентный бициклический радикал, содержащий насыщенную циклическую структуру и ненасыщенную циклическую структуру, где указанная ненасыщенная циклическая структура присоединена к NH и указанная насыщенная циклическая структура присоединена к R1, где А является незамещенным или содержит один или большее количество следующих заместителей: галоген,ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил, CN или NR10R11;R1 обозначает 3-8-членную циклогетероалкильную группу, (C3-С 8)циклоалкильную группу или (C6C14)арильную группу, которая является незамещенной или содержит следующие заместители: (C1C6)алкил, галоген, OR57, NR58R59 или дейтерий;L1 обозначает (С 1-С 3)алкилен, (С 1-С 4)алкенилен, -С(О)-, -С(О)О-, C(O)N-, -(C1-С 3)алкилен-С(О)-,-(С 1-C3)алкилен-С(О)О- или связь, где L1 является незамещенным или содержит один или большее количество следующих заместителей: (С 1-С 4)алкил, галогензамещенный (C1-C4)галогеналкил или (C3 С 8)циклоалкил;R2 обозначает (C6-C14)арильную группу, 5-14-членную гетероарильную, 3-8-членную циклогетероалкильную группу или (C3-С 14)циклоалкильную группу, каждая из которых является незамещенной или содержит один или большее количество следующих заместителей: галоген, ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил или CN;R8 обозначает (C1-C6)алкил, (C6-C14)арил, (C3-C14)циклоалкил, галоген или 3-14-членный циклогетероалкил, где любая указанная выше углеводородная группа (например, (С 1-C6)алкил, (C6-C14)арил и (C3C14)циклоалкил) необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C6)алкил, галогензамещенный (C1C6)алкил, ОН или NR44R45;R3 и R4 все независимо обозначают Н, (С 1-C6)алкил, -(C1-C6)алкилен-(C6-C14)арил, -(C1-C6)алкилен(5-14-членный гетероарил), -(C1-C6)алкилен-CONR16R17, -(С 1-С 6)алкилен-О-R15, -(Cl-C6)алкилен-NR13R14,-(С 1-С 3)алкилен-(3-14-членный циклогетероалкил), -(C1-C3)алкилен-S-(С 6-С 14)арильную группу, -(C1C6)алкилен-COR18, -(С 1-С 6)алкилен-С(О)О-R19, -(С 1-С 6)алкилен-О-С(О)-R20, -(C1-C3)алкилен-S-R21, -(С 1C3)алкилен-SOR22 или -(C1-C3)алкилен-SO2R23;R6 и R7 все независимо обозначают Н, NO2, -SO2CF3, -SO2(C1-C6)алкил, галогензамещенный (С 1C6)алкил, галоген, (C3-С 14)циклоалкил или CN;R10, R11, R13, R14, R16, R17, R44, R45, R46, R47, R49, R50, R57, R58 и R59 все независимо обозначают Н, (С 1C6)алкил, (С 2-C6)алкенил, (С 2-C6)алкинил, ОН, -С(О)-(C1-C6)алкил, (C1-C6)алкоксигруппу, галоген, (C3 С 14)циклоалкил, (С 6-С 14)арил, 4-14-членный циклогетероалкил или 5-14-членный гетероарил, где каждая из указанных выше углеводородных групп (например, (C1-C6)алкил, (C2-С 6)алкенил, (C2-C6)алкинил, (C3 С 14)циклоалкил, (С 6-C14)арил и (C1-С 6)алкильные фрагменты -С(О)-(C1-C6)алкила и (C1C6)алкоксигруппы) необязательно содержит один или большее количество следующих заместителей: галоген, гидроксигруппу, (С 1-C6)алкоксигруппу, аминогруппу, (C1-С 6)алкиламиногруппу, диС 1C6)алкил)аминогруппу или цианогруппу; илиR13 и R14 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным; илиR16 и R17 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным; илиR58 и R59 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным; илиR44 и R45 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным; илиR46 и R47 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным; илиR49 и R50 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил или 5-14-членный гетероарил, каждый из которых является замещенным или незамещенным;R15, R18, R19, R20, R22, R23, R48, R51, R52, R53, R55 и R56 все независимо обозначают -(C1-C6)алкилен-(С 6 С 14)арил или -(C1-C6)алкилен-(5-14-членный гетероарил), каждый из которых является незамещенным или содержит один или большее количество следующих заместителей: галоген, ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил или CN;R21 и R54 все независимо обозначают (C6-C14)арил, 5-14-членный гетероарил, -(C1-C6)алкилен-(С 6 С 14)арил или -(С 1-C6)алкилен-(5-14-членный гетероарил), каждый из которых является незамещенным или содержит один или большее количество следующих заместителей: галоген, ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил или CN; или их фармацевтически приемлемой соли. В одном варианте осуществления настоящее изобретение включает соединения формулы (I), в которой А обозначает двухвалентный бициклический радикал, содержащий насыщенную циклическую структуру и ненасыщенную циклическую структуру, где указанная ненасыщенная циклическая структура присоединена к NH и указанная насыщенная циклическая структура присоединена к R1, где А является незамещенным или содержит один или большее количество следующих заместителей: галоген, ОН,(C1-C6)алкил (например, метил, этил, пропил или бутил), галогензамещенный (C1-C6)алкил (например,CF3, CH2CF3) или CN. В предпочтительном варианте осуществления А обозначаетY1 и Y2 все независимо обозначают -CR30R31-, -CR32R33-CR34R35-, -NR36-, -CR37R38-NR39-, -O-, -S-,40 41X обозначает СН или N;R29, R30, R31, R32, R33, R34, R35, R36, R37, R38, R39, R40, R41, R42 и R43 все независимо обозначают Н, (С 1C6)алкил, галоген, галогензамещенный (C1-С 6)алкил или (C3-C14)циклоалкил; предпочтительно, если R29,R30, R31, R32, R33, R34, R35, R36, R37, R38, R39, R40, R41, R42 и R43 все независимо обозначают Н, метил, этил,пропил, F, Cl, CF3, циклопропил, циклобутил, циклопентил или циклогексил,или его фармацевтически приемлемую соль. В другом варианте осуществления настоящее изобретение включает соединения формулы (I), в которой А обозначает и по меньшей мере один из G1, G2 и G3 обозначает N;R30, R31, R32, R33, R34 и R35 все независимо обозначают Н, метил, этил, пропил, Cl, F или CF3; или их фармацевтически приемлемую соль. В предпочтительном варианте осуществления G1, G2 и G3 все независимо обозначают СН, С-СН 3, CCN, C-NR10R11, C-CF3, C-F, C-Cl или N. В другом предпочтительном варианте осуществления G1 и G3 обозначают N. В другом варианте осуществления Y1 и Y2 все независимо обозначают -СН 2-, -СН 2-СН 2-, -NH-,-NCH3-, -CH2NH-, -О-, -S-, -СН 2-О- или -CH2-S-. В еще одном предпочтительном варианте осуществления Y1 обозначает -СН 2 СН 2- и Y2 обозначает-СН 2-. В другом варианте осуществления X обозначает СН. В другом предпочтительном варианте осуществления X обозначает N. В другом варианте осуществления X обозначает N и N присоединен к атому углерода гетероарила или циклогетероалкила в R1 и L1 обозначает связь. В другом варианте осуществления, где X обозначает СН, X присоединен к гетероатому гетероарила или циклогетероалкила в R1 и L1 обозначает связь. В другом варианте осуществления настоящее изобретение включает соединения формулы (I), в которой два из G1, G2 и G3 обозначают N и оставшийся G обозначает CR29;X обозначает N. В другом варианте осуществления настоящее изобретение включает соединения формулы (I), в которой В еще одном варианте осуществления настоящее изобретение включает соединения формулы (I), в которой А обозначает где X обозначает СН или N;R29, R30, R31, R32, R33, R34, R35 и R60 все независимо обозначают Н, метил, этил, пропил, Cl, F или CF3; или их фармацевтически приемлемую соль. В другом варианте осуществления А обозначает каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (С 1-С 6)алкил (например, метил, этил, пропил или бутил), галогензамещенный (С 1-C6)алкил (например, CF3), CN илиNR10R11. В одном варианте осуществления R1 обозначает 3-8-членный циклогетероалкил (например, пиперидинил, пиперазинил, морфолинил или тетрагидрофуранил), (C3-С 8)циклоалкил (например, циклопропил,циклобутил, циклопентил или циклогексил) или (С 6-C14)арил (например, фенил или нафтил), каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей (C1-C6)алкил (например, метил, этил, пропил, бутил или пентил), галоген, NR58R59 (например, NH2, NHCH3 или NCH3CH3), дейтерий или OR57, где R57 обозначает (C1-C6)алкил или Н. В еще одном варианте осуществления настоящее изобретение включает соединения формулы (I), в которой R1 обозначает пиперидинил, пиперазинил, морфолинил, тетрагидрофуранил, циклопропил, циклобутил, циклопентил, циклогексил или фенил, который является незамещенным или содержит следующие заместители: метил, этил, пропил, Cl, F, Br, I или метоксигруппу. В другом варианте осуществленияR1 обозначает пиперидинил, пиперазинил, морфолинил, циклопентил или циклогексил, каждый из которых является незамещенным или содержит следующие заместители: метил, метоксигруппу, Cl или F. В другом варианте осуществления R1 обозначает пиперидинил, пиперазинил или циклогексил, каждый из которых является незамещенным или содержит следующие заместители: метил, этил, F, Cl или Br. В другом варианте осуществления R1 обозначает пиперидинил, который является незамещенным или содержит следующие заместители: метил или F. В другом варианте осуществления L1 обозначает (C1-C3)алкилен (например, метилен, этилен или пропилен), (C1-C4)алкенилен (например, =С-, -С=С-, -С=С-С- или -С-С=С-; -С(О)-, -С(О)О-, -C(O)N-),-С 1-С 3)алкил)-С(О)- (например, -СН 2 С(О)-, -СН 2 СН 2 С(О)- или СН 2-СН 2-СН 2-С(О)-), (C1-С 3-алкил)С(О)О- (например, -СН 2 С(О)О-, -СН 2 СН 2 С(О)О- или СН 2-СН 2-СН 2-С(О)О-) или связь, где L1 является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей (C1-С 4)алкил (например, метил, этил, пропил или бутил), галогенза-4 020586 мещенный (C1-С 4)алкил (например, CF3 или CH2CF3) или (C3-С 8)циклоалкил (например, циклопропил,циклобутил, циклопентил или циклогексил). В другом варианте осуществления L1 обозначает метилен, этилен, пропилен, =С-, -С=С-, -С=С-С-,-С(О)-, -С(О)О-, C(O)N-, -CH2C(O)-, -СН 2 С(О)О- или связь, где L1 является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей метил, этил или CF3. В другом варианте осуществления L1 обозначает метилен, этилен или связь. В другом варианте осуществления L1 обозначает метилен. В другом варианте осуществления L2 обозначает (C1-C3)алкилен (например, метилен, этилен или пропилен), NR9, -О- или -S-, где R9 обозначает Н, (С 1-С 6)алкил (например, метил, этил, пропил или бутил), -(C1-C3)алкилен-(С 6-С 14)арил (например, -СН 2-фенил, -СН 2 СН 2-фенил или СН 2 СН 2 СН 2-фенил), -(С 1 С 3)алкилен-(5-14-членный гетероарил) (например, -СН 2-пиридинил, -СН 2 СН 2-пиридинил, -СН 2 пиримидинил или -СН 2 СН 2-пиримидинил), -(С 1-C3)алкилен-CONR46R47 (например, -CH2C(O)NCH3CH3,-CH2C(O)NHCH3, -CH2CH2C(O)NCH3CH3 или -CH2CH2C(O)NHCH3), -(С 1-С 3)алкилен-O-R48 (например,-СН 2-О-СН 3, -СН 2-О-СН 2 СН 3, -СН 2 СН 2-О-СН 3 или -СН 2 СН 2-О-СН 2 СН 3), -(С 1-C3)алкилен-NR49R50, -(С 1C3)алкилен-(3-14-членный циклогетероалкил) (например, -СН 2-пиперидинил, -СН 2 СН 2-пиперидинил или-С(О)СН 2 СН 2 СН 2-пиперидинил). В другом варианте осуществления L2 обозначает -СН 2- или NR9, где R9 обозначает Н, метил или этил. В другом варианте осуществления L2 обозначает -СН 2- или -NH-. В другом варианте осуществления L2 обозначает -NH-. В еще одном варианте осуществления настоящее изобретение включает соединения формулы (I), в которой L1 обозначает -СН 2-, -СН 2 СН 2- или связь; L2 обозначает -СН 2- или NH. В одном варианте осуществления R2 обозначает (C6-C14)арил (например, фенил или нафтил), 5-14 членный гетероарил (например, пиридинил, пиримидинил или пиридазинил), 3-8-членный циклогетероалкил (например, пиперидинил, пиперазинил, морфолинил или тетрагидрофуранил) или (С 3 С 14)циклоалкил (например, циклопропил, циклобутил, циклопентил, циклогексил или частично насыщенный циклогексил (циклогексенил или циклогексадиенил, каждый из которых является незамещенным или содержит один или большее количество следующих заместителей: галоген, ОН, -(C1-С 6)алкил,галогензамещенный -(C1-С 3)алкил (предпочтительно CF3); или CN. В другом варианте осуществления настоящее изобретение включает соединения формулы (I), в которой R2 обозначает фенил, нафтил, пиридинил, пиримидинил или пиридазинил, каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей метил, диметил, этил, пропил, бутил, пентил, гексил, фенил,циклопропил, циклобутил, циклопентил, CF3 или CH2Cl. В другом варианте осуществления R2 обозначает фенил, циклогексил или частично насыщенный циклогексил, где R2 является незамещенным или содержит один или большее количество заместителей, независимо выбранных из группы, включающей метил, диметил, ОН, F, Cl или Br. В другом варианте осуществления R2 обозначает фенил. В другом варианте осуществления R3 и R4 все независимо обозначают Н, (С 1-C6)алкил, -(С 1C6)алкилен-(С 6-C14)арил (например, -СН 2-фенил, -СН 2 СН 2-фенил, -СН 2 СН 2 СН 2-фенил, -СН 2 СН 2 СН 2 СН 2 фенил или -СН 2 СН 2 СН 2 СН 2 СН 2-фенил), -(C1-C6)алкилен-(5-14-членный гетероарил) (например,-СН 2 СН 2 СН 2 СН 2-пиридинил или -СН 2 СН 2 СН 2 СН 2-пиримидинил), -(С 1-С 6)алкилен-С(О)NR16R17 (например, -CH2CH2CH2CH2C(O)NCH3CH3, -CH2CH2CH2CH2C(O)NHCH3 или -CH2CH2CH2CH2C(O)NH2), -(С 1 С 6)алкилен-О-R15 (например, -бутил-О-СН 3 или -бутил-О-СН 2 СН 3), -(C1-C6)алкилен-NR13R14 (например,-бутил-N(CH3)(CH3), -бутил-NHCH3, -бутил-NH2, -бутил-NH-фенил или -бутил-N(CH3)(CH3, -(С 1C6)алкилен-(3-14-членный циклогетероалкил) (например, -бутилпиперидинил), -(C1-C3)алкилен-S-(С 6 С 14)арильную группу, -(C1-C6)алкилен-COR18, -(C1-С 6)алкилен-С(O)OR19, -(C1-С 6)алкилен-О-С(О)-R20,(С 1-С 3)алкилен-S-R21, -(С 1-С 3)алкилен-SOR22 или -(C1-С 3)алкилен-SO2R23. В предпочтительном варианте осуществления R3 и R4 все независимо обозначают Н, (С 1-C6)алкил-CH2CH2S(O)OCH2CH3). В другом варианте осуществления R3 и R4 независимо обозначают (C1-С 6)алкил, (C1-С 3)алкил-(С 6C14)арил, -(С 1-С 3)алкилен-(5-14-членный гетероарил), -(С 1-С 3)алкилен-С(O)-NR16R17, -(C1-С 3)алкилен-OR15, -(C1-С 3)алкилен-NR13R14, -(С 1-С 3)алкил-(3-14-членный циклогетероалкил) или -(C1-С 3)алкил-S-(С 6C14)арил. В одном варианте осуществления R3 и R4 все независимо обозначают -СН 2-фенил, -СН 2 СН 2-фенил,-СН 2 СН 2 СН 2-фенил, -СН 2-пиридинил, -СН 2 СН 2-пиридинил, -СН 2-пиримидинил, -СН 2 СН 2-пиримидинил,-CH2C(O)NCH3CH3, -CH2C(O)NHCH3, -CH2CH2C(O)NCH3CH3, -CH2-O-CH3, -СН 2-О-СН 2 СН 3, -CH2-Sфенил, -СН 2 СН 2-S-фенил, -СН 2 СН 2 СН 2-S-фенил, -СН 2 С(О)СН 3, -СН 2 С(О)СН 2 СН 3, -СН 2 СН 2 С(О)СН 3,-CH2-S-CH3, -CH2-S-CH2CH3, -СН 2-N(CH3)(CH3), -CH2-NHCH3, -CH2-NH2, СН 2-NH-фенил, -CH2-CH2N(CH3)(CH3), -CH2CH2-NHCH3, -CH2CH2-NH2 или -СН 2 СН 2-NH-фенил. В еще одном варианте осуществления R3 обозначает -СН 2-фенил, -СН 2 СН 2-фенил, -CH2CH2CH2 фенил,-СН 2-пиридинил,-CH2CH2-пиридинил,-СН 2-пиримидинил,-СН 2 СН 2-пиримидинил,-CH2C(O)NCH3CH3, -CH2C(O)NHCH3, -CH2CH2C(O)NCH3CH3, -СН 2-О-СН 3, -СН 2-О-СН 2 СН 3, -CH2-Sфенил, -СН 2 СН 2-S-фенил, -СН 2 СН 2 СН 2-S-фенил; R4 обозначает -СН 2 С(О)СН 3, -СН 2 С(О)СН 2 СН 3,-СН 2 СН 2 С(О)СН 3, -CH2-S-СН 3, -CH2-S-CH2CH3, -CH2-N(CH3)(CH3), -CH2-NHCH3, -CH2-NH2, CH2-NHфенил, -CH2-CH2-N(CH3)(CH3), -CH2CH2-NHCH3, -CH2CH2-NH2 или -CH2CH2-NH-фенил. В другом варианте осуществления R3 обозначает -СН 2-фенил, -СН 2 СН 2-фенил, -СН 2 СН 2 СН 2-фенил,-СН 2-S-фенил, -СН 2 СН 2-S-фенил или -СН 2 СН 2 СН 2-S-фенил. В другом варианте осуществления R4 обозначает -CH2-N(CH3)(CH3), -CH2-NHCH3, -CH2-NH2, -CH2-NH-фенил, -CH2-CH2-N(CH3)(CH3), -CH2CH2NHCH3, -CH2CH2-NH2 или -СН 2 СН 2-NH-фенил. В другом варианте осуществления R3 обозначает -СН 2-Sфенил или -СН 2 СН 2-S-фенил. В другом варианте осуществления R4 обозначает -CH2-N(CH3)(CH3), -CH2NHCH3, -СН 2-NH2, -СН 2-NH-фенил или -CH2-CH2-N(CH3)(CH3). В одном варианте осуществления R8 обозначает (C1-C6)алкил (предпочтительно метил, этил, пропил, бутил, пентил или гексил), (С 6-C14)арил (предпочтительно нафтил или фенил), (С 3-C14)циклоалкил(предпочтительно циклопропил, циклобутил, циклопентил или циклогексил), галоген или 3-14-членный циклогетероалкил (предпочтительно пиперидинил, пиперазинил, морфолинил или тетрагидрофуранил),где любая указанная выше углеводородная группа (например, (C1-C6)алкил, (C6-C14)арил и (С 3C14)циклоалкил) необязательно содержит следующие заместители: галоген, (C1-C6)алкил (предпочтительно метил, этил, пропил или бутил), галогензамещенный (C1-С 6)алкил (предпочтительно CF3), ОН илиNR44R45. В другом варианте осуществления R8 обозначает метил, этил, пропил, бутил, нафтил, фенил, циклопропил, циклобутил, циклопентил, циклогексил, F, Br, пиперидинил или пиперазинил, где любая указанная выше углеводородная группа (например, метил, этил, пропил, бутил, нафтил, фенил, циклопропил, циклобутил, циклопентил и циклогексил) содержит следующие заместители: F, Cl, Br, метил, этил,пропил или CF3. В другом варианте осуществления R8 обозначает фенил, который является незамещенным или содержит следующие заместители: F, Cl, Br, метил, этил, пропил или CF3. В одном варианте осуществления R6 и R7 все независимо обозначают Н, NO2, SO2CF3, SO2-(C1 С 6)алкил (предпочтительно SO2CH3 или SO2CH2CH3), галогензамещенный (С 1-C6)алкил (предпочтительно CF3), галоген, (C3-С 14)циклоалкил (предпочтительно циклопропил, циклобутил, циклопентил или циклогексил) или CN. В другом варианте осуществления один из R6 и R7 обозначает Н и другой выбран из группы, включающей NO2, SO2CF3, SO2CH3, SO2CH2CH3, CF3, Cl или F. В другом варианте осуществления один из R6 и R7 обозначает Н и другой выбран из группы, включающей NO2 или SO2CF3. В другом варианте осуществления оба R6 и R7 обозначают Н. В одном варианте осуществления R10, R11, R13, R14, R16, R17, R46, R47, R49 и R50 все независимо обозначают Н, (C1-C6)алкил (предпочтительно метил, этил, пропил или бутил), (С 2-C6)алкенил (предпочтительно этенил или пропенил), (С 2-С 6)алкинил, ОН, -С(О)-(C1-C6)алкил (предпочтительно -С(О)метил,-6 020586-С(О)этил или -С(О)пропил), (С 1-C6)алкоксигруппу (предпочтительно метоксигруппу, этоксигруппу или пропоксигруппу), галоген, (C3-C14)циклоалкил (предпочтительно циклопропил, циклобутил, циклопентил или циклогексил), (С 6-C14)арил (предпочтительно фенил), 4-14-членный циклогетероалкил (предпочтительно пиперидинил, пиперазинил, морфолинил или тетрагидрофуранил) или 5-14-членный гетероарил (предпочтительно пиридинил, пиримидинил или пиридазинил), где каждая из указанных выше углеводородных групп (например, (С 1-C6)алкил, (С 2-C6)алкенил, (С 2-C6)алкинил, (C3-С 14)циклоалкил и (C6C14)арил и (C1-C6)алкильный фрагмент -C(O)-(C1-С 6)алкила и (C1-C6)алкоксигруппы) необязательно содержит один или большее количество заместителей, выбранных из группы, включающей галоген, гидроксигруппу, (С 1-C6)алкоксигруппу, аминогруппу, (C1-C6)алкиламиногруппу, диC1-C6)алкил)аминогруппу или цианогруппу. В другом варианте осуществления R13 и R14 вместе с N, к которому они присоединены, образуют 48-членную циклогетероалкильную группу (предпочтительно пиперидинил или пиперазинил) или 5-14 членный гетероарил (предпочтительно пиридинил или пиримидинил), каждый из которых является замещенным или незамещенным; или R16 и R17 вместе с N, к которому они присоединены, образуют 4-8-членный циклогетероалкил(предпочтительно пиперидинил или пиперазинил) или 5-14-членный гетероарил (предпочтительно пиридинил или пиримидинил), каждый из которых является замещенным или незамещенным. В одном варианте осуществления R15, R18, R19, R20, R22, R23, R44, R45, R48, R51, R52, R53, R55 и R56 все независимо обозначают -(С 1-C6)алкилен-(С 6-С 14)арил (предпочтительно -CH2-фенил, -CH2CH2-фенил или-CH2CH2CH2-фенил) или -(С 1-C6)алкилен-(5-14-членный гетероарил), (предпочтительно -CH2-пиридинил,-CH2CH2-пиридинил, -CH2-пиримидинил или -CH2CH2-пиримидинил), каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (C1-C6)алкил (предпочтительно метил, этил, пропил или бутил), галогензамещенный (C1-C6)алкил (предпочтительно CF3) или CN.R21 и R54 все независимо обозначают (C6-C14)арил (предпочтительно фенил или нафтил), 5-14 членный гетероарил, -(C1-C6)алкил-(С 6-С 14)арил (предпочтительно -CH2-фенил, -CH2CH2-фенил или-CH2CH2CH2-фенил) или (С 1-C6)алкилен-(5-14-членный гетероарил) (предпочтительно -CH2-пиридинил,-CH2CH2-пиридинил, -CH2-пиримидинил или -CH2CH2-пиримидинил), каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (С 1-C6)алкил (предпочтительно метил, этил или пропил),галогензамещенный (С 1-C6)алкил (предпочтительно CF3) или CN. В другом варианте осуществления настоящее изобретение включает соединения формулы (Ib) или их фармацевтически приемлемую соль,в которой R1b обозначает Н, NO2, SO2CF3, SO2(С 1-C6)алкил, галогензамещенный (С 1-С 6)алкил, галоген, (C3-C14)циклоалкильную группу или CN;R2b обозначает двухвалентный бициклический радикал, содержащий насыщенную циклическую структуру и ненасыщенную циклическую структуру, где указанная ненасыщенная циклическая структура присоединена к NH и указанная насыщенная циклическая структура присоединена к R5b, где R2b является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (C1-C6)алкил, галогензамещенный (С 1-C6)алкил, CN или NH2;R3b и R4b все независимо обозначают Н, (С 1-C6)алкил, (С 2-C6)алкенил, (С 2-С 6)алкинил, (C6C14)арильную группу, 5-14-членную гетероарильную группу, (C3-C14)циклоалкильную группу, галоген или 3-14-членную циклогетероалкильную группу, каждая из которых, если она не обозначает Н, может быть незамещенной или содержит один или большее количество следующих заместителей: гидроксигруппу, цианогруппу, нитрогруппу, (C1-С 8)алкил, (C2-С 8)алкенил, (C2-С 8)алкинил, (C1-С 8)алкоксигруппу,(C2-С 8)алкенилоксигруппу, (С 2-С 8)алкинилоксигруппу, галоген, (C1-С 8)алкилкарбонил, карбоксигруппу,(С 1-С 8)алкоксикарбонил, аминогруппу, (C1-С 8)алкиламиногруппу, диС 1-С 8)алкил)аминогруппу, (С 1 С 8)алкиламинокарбонил, диC1-С 8)алкил)аминокарбонил, (C1-С 8)алкилкарбониламиногруппу, (C1 С 8)алкилкарбонилС 1-С 8)алкил)аминогруппу,(C1-С 8)алкилсульфониламиногруппу,(C1 С 8)алкилтиогруппу,(C1-С 8)алкилсульфинил,(C1-С 8)алкилсульфонил,аминосульфонил,(C1C8)алкиламиносульфонил или ди(C1-С 8)алкиламиносульфонил, где каждая из указанных выше углеводо-7 020586 родных групп (например, (C1-С 8)алкил, (С 2-С 8)алкенил, (С 2-С 8)алкинил и (C1-С 8)алкильные, (С 2 С 8)алкенильные и (С 2-С 8)алкинильные фрагменты (С 2-С 8)алкоксигруппы, (С 2-С 8)алкенилоксигруппы,(С 2-С 8)алкинилоксигруппы,(C1-С 8)алкилкарбонила,(C1-С 8)алкоксикарбонила,(C1 С 8)алкиламиногруппы,ди(C1-С 8)алкиламиногруппы,(C1-С 8)алкиламинокарбонила,диC1 С 8)алкил)аминокарбонила,(С 1-С 8)алкилкарбониламиногруппы,(C1-С 8)алкилкарбонилC1 С 8)алкил)аминогруппы,(С 1-С 8)алкилсульфониламиногруппы,(С 1-С 8)алкилтиогруппы,(С 1 С 8)алкилсульфинила,(C1-С 8)алкилсульфонила,(C1-С 8)алкиламиносульфонила и диС 1 С 8)алкил)аминосульфонила) необязательно содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН или (C1-С 8)алкоксигруппу;R5b обозначает 3-8-членный циклогетероалкил, (C3-С 8)циклоалкил или (С 6-С 14)арил, который является незамещенным или содержит следующие заместители: (С 1-C6)алкил, галоген, ОН, (С 1C3)алкоксигруппу, NH2 или дейтерий;R7b обозначает гидроксигруппу, цианогруппу, нитрогруппу, (C1-С 8)алкил, (C2-С 8)алкенил, (C2 С 8)алкинил, (C2-С 8)алкоксигруппу, (С 2-С 8)алкенилоксигруппу, (С 2-С 8)алкинилоксигруппу, галоген, (C1 С 8)алкилкарбонил, карбоксигруппу, (C1-С 8)алкоксикарбонил, аминогруппу, (C1-С 8)алкиламиногруппу,ди(C1-С 8)алкиламиногруппу,(C1-С 8)алкиламинокарбонил,диC1-С 8)алкил)аминокарбонил,(С 1 С 8)алкилкарбониламиногруппу,(C1-С 8)алкилкарбонилС 1-С 8)алкил)аминогруппу,(C1 С 8)алкилсульфониламиногруппу,(С 1-С 8)алкилтиогруппу,(C1-С 8)алкилсульфинил,(С 1 С 8)алкилсульфонил,аминосульфонил,(C1-С 8)алкиламиносульфонил или диС 1 С 8)алкил)аминосульфонил, где каждая из указанных выше углеводородных групп (например, (C1 С 8)алкил, (C2-С 8)алкенил, (С 2-С 8)алкинил и (С 1-С 8)алкильные, (С 2-С 8)алкенильные и (C2-С 8)алкинильные фрагменты (С 2-С 8)алкоксигруппы, (С 2-С 8)алкенилоксигруппы, (С 2-С 8)алкинилоксигруппы, (C1 С 8)алкилкарбонила, (C1-С 8)алкоксикарбонила, (C1-С 8)алкиламиногруппы, ди(С 1-С 8)алкиламиногруппы,(C1-С 8)алкиламинокарбонила, диС 1-С 8)алкил)аминокарбонила, (C1-С 8)алкилкарбониламиногруппы, (C1 С 8)алкилкарбонилC1-С 8)алкил)аминогруппы,(С 1-С 8)алкилсульфониламиногруппы,(C1 С 8)алкилтиогруппы, (С 1-С 8)алкилсульфинила, (C1-С 8)алкилсульфонила, (C1-С 8)алкиламиносульфонила и диС 1-С 8)алкил)аминосульфонила) необязательно содержит один или большее количество заместителей,каждый из которых независимо выбран из группы, включающей галоген, ОН или (C1-С 8)алкоксигруппу;Lb обозначает -(C1-С 3)алкилен-, -(С 2-С 4)алкенилен-, -С(О)-, -С(О)О-, -C(O)N(H)-, -(C1-C3)алкилС(О)-, -(С 1-C3)алкил-С(О)О- или связь, где Lb является незамещенным или содержит один или большее количество следующих заместителей: (C1-С 4)алкил, галогензамещенный (C1-C4)алкил или (C3 С 8)циклоалкил;R8b обозначает (C6-C14)арил, 5-14-членный гетероарил, 3-8-членный циклогетероалкил или (C3 С 14)циклоалкил, каждый из которых является незамещенным или содержит один или большее количество заместителей, каждый из которых независимо выбран из группы, включающей галоген, ОН, (С 1C6)алкил, галогензамещенный (С 1-C6)алкил или CN;n равно 0, 1, 2, 3 или 4. В одном варианте осуществления настоящее изобретение дополнительно включает соединения формулы (Ib), в которой R2b определен, как А в формуле (I). В другом варианте осуществления настоящее изобретение включает соединения формулы (Ib), в которой n равно 0, 1 или 2. В другом варианте осуществления n равно 0. В другом варианте осуществления настоящее изобретение включает соединения формулы (Ib), в которой R3b и R4b все независимо обозначают Н, (C1-C6)алкил (предпочтительно метил, этил или пропил),(С 2-C6)алкенил, (C2-С 6)алкинил, (С 6-C14)арил (предпочтительно фенил), 5-14-членную гетероарильную группу (предпочтительно пиридинил или пиримидинил), (C3-С 14)циклоалкил (предпочтительно циклопропил, циклобутил, циклопентил или циклогексил) или галоген (предпочтительно F, Cl или Br). или их фармацевтически приемлемую соль. Более предпочтительными являются соединения, такие как или их фармацевтически приемлемая соль. Другим объектом настоящего изобретения является фармацевтическая композиция, которая содержит соединение, предлагаемое в настоящем изобретении, и фармацевтически приемлемый носитель или инертный наполнитель. Фармацевтическая композиция необязательно содержит по меньшей мере одно дополнительное фармацевтическое средство (подходящие фармацевтические средства описаны ниже в настоящем изобретении). Еще одним объектом настоящего изобретения является способ ингибирования активности Bcl-2,включающий стадию введения нуждающемуся в нем субъекту (i) соединения, предлагаемого в настоящем изобретении, в терапевтически эффективном количестве или (ii) фармацевтической композиции,содержащей соединение, предлагаемое в настоящем изобретении, и по меньшей мере один фармацевтически приемлемый инертный наполнитель. Кроме того, настоящее изобретение включает способ лечения пролиферативного заболевания,включающий стадию введения нуждающемуся в нем субъекту (i) соединения, предлагаемого в настоящем изобретении, в терапевтически эффективном количестве или (ii) фармацевтической композиции,содержащей соединение, предлагаемое в настоящем изобретении, и по меньшей мере один фармацевтически приемлемый инертный наполнитель. Альтернативно, способ лечения пролиферативного заболевания или ингибирования активности Bcl2 может включать комбинированную терапию, которая включает стадию (стадии) введения:(i) первой композиции, содержащей соединение, предлагаемое в настоящем изобретении, и фармацевтически приемлемый носитель или инертный наполнитель;(ii) второй композиции, содержащей по меньшей мере одно дополнительное фармацевтическое средство и фармацевтически приемлемый носитель или инертный наполнитель; где указанное по меньшей мере одно дополнительное фармацевтическое средство представляет собой противораковое средство, химиотерапевтическое средство или антипролиферативное соединение. Первую композицию и вторую композицию можно вводить одновременно или последовательно в любом порядке. Настоящее изобретение также относится к введению соединения, предлагаемого в настоящем изобретении, или фармацевтической композиции, содержащей соединение, предлагаемое в настоящем изобретении, для применения в терапии. Предпочтительно, если заболевание, нарушение или синдром у субъекта являются гиперпролиферативными, где указанным субъектом является животное, включая людей, и заболевание выбрано из группы, включающей рак и воспаление. Настоящее изобретение также включает фармацевтическую композицию, содержащую (i) соединение, предлагаемое в настоящем изобретении, и (ii) фармацевтически приемлемый носитель или инертный наполнитель. Кроме того, настоящее изобретение включает фармацевтическую композицию, содержащую соединение, предлагаемое в настоящем изобретении, в комбинации со вторым активным средством и фармацевтически приемлемый носитель или инертный наполнитель. Определения. При использовании в настоящем изобретении "алкил" означает обладающий линейной или разветвленной цепью углеводород (CnH2n+1). Алкильные фрагменты, содержащие от 1 до 5 атомов углерода, называются "низш. алкилами", примеры включают, но не ограничиваются только ими, метил, этил, нпропил, изопропил, н-бутил, втор-бутил, трет-бутил, изобутил, н-пентил, изопентил и неопентил. Термин"алкилен" означает алкильный фрагмент, содержащий два центра связывания. Алкиленовая группа может быть линейной (например, -(СН 2)-, -(СН 2)2-, -(СН 2)3-, -(СН 2)4- и т.п.) или разветвленной (например,-СН(СН 3)-, -С(СН 3)2-, -СН 2 СН(СН 3)-, -СН(СН 3)-СН 2-, -С(СН 3)2-СН 2- и т.п.). Подходящими алкиленовыми фрагментами являются такие же, как описанные выше для алкила, но содержащие два центра связывания вместо только одного."Галогензамещенный алкил" означает алкильную группу, замещенную галогенидными группами,например фторидными группами. Например, если заместителем является фтор, то обычными галогеналкильными группами являются трифторалкильная,2,2,2-трифторэтильная или 2,2,2,1,1 пентафторэтильная группы. Обычно галогензамещенный (C1-C6)алкил содержит до 7 замещающих атомов галогена, которые могут быть одинаковыми или разными. Пергалогеналкил означает алкильную группу, в которой все атомы водорода замещены галогеном (например, трифторметил). Термин "алкенил" означает одновалентную группу, образованную из углеводорода, содержащего по меньшей мере одну двойную углерод-углеродную связь. Например, винил, проп-1-енил, проп-2-енил,2-метилпроп-2-енил, 3-метилбут-2-енил и т.п. Термин "алкенилен" означает алкенильный фрагмент, содержащий два центра связывания, например -СН 2-СН=СН-СН 2-. Подходящими алкениленовыми фрагментами являются такие же, как описанные выше для алкенила, но содержащие два центра связывания вместо только одного. Термин "алкинил" означает одновалентную группу, образованную из углеводорода, содержащего по меньшей мере одну тройную углерод-углеродную связь. Термин "С 2-C6-алкинил" означает одновалентную группу, образованную из углеводорода, содержащего от 2 до 6 атомов углерода, и содержащую по меньшей мере одну тройную углерод-углеродную связь. Термин "алкоксигруппа" означает группу, в которой алкильная группа присоединена к кислороду,где алкил является таким, как определено выше. Термин "циклоалкил" означает моноциклическое, бициклическое или спироциклическое полностью или частично насыщенное карбоциклическое кольцо. Циклоалкил может присоединяться с помощью любого элемента кольца. Подходящие циклоалкильные группы включают циклопропил, циклобутил,циклопентил, циклогексил, циклогептил или циклооктил. Частично насыщенное моноциклическое кольцо включает такие фрагменты, как циклогексенил, циклопропенил, циклобутенил, циклопентенил, циклогексадиенил и т.п. Термин "циклоалкилен" означает полностью насыщенное карбоциклическое кольцо(кольца), обладающее двумя положениями присоединения. Карбоциклическое кольцо может представлять собой отдельное кольцо, бициклическое кольцо или спироциклическое кольцо, где два центра связывания бициклического кольца и спироциклического кольца могут находиться в одном кольце или в разных кольцах. См., например, приведенную ниже иллюстрацию. Термин "арил" означает ароматические фрагменты, представляющие собой отдельное кольцо (например, фенил) или конденсированную кольцевую систему (например, нафталин, антрацен, фенантрен и т.п.). Типичная арильная группа представляет собой 6-14-членное ароматическое карбоциклическое кольцо (кольца). Конденсированная ароматическая кольцевая система также может включать фенил,сконденсированный с частично или полностью насыщенным циклоалкилом. Например, 2,3 дигидроинденил, 1,2,3,4-тетрагидронафталинил, 1,2-дигидронафталинил, 2,3-дигидронафталинил, 9,10 дигидроантраценил, флуоренил и т.п. Термин "арилен" означает карбоциклический ароматический фрагмент, содержащий два центра связывания. Подходящие арилены включают группы, описанные выше для арильного фрагмента, с тем отличием, что они содержат два центра связывания, а не один. Например, 1,2-фенилен, 1,3-фенилен, 1,4 фенилен, 1,3-нафтилен, 1,4-нафтилен, 1,5-нафтилен, 1,6-нафтилен, 1,7-нафтилен, 2,3-нафтилен, 2,4 нафтилен, 2,5-нафтилен, 2,6-нафтилен, 2,7-нафтилен, 3,4-нафтилен, 3,5-нафтилен, 3,6-нафтилен, 3,7 нафтилен и т.п. Два центра связывания конденсированной ариленовой системы могут находиться в одном кольце или в разных кольцах. Термин "гетероарил" означает моноциклическую или конденсированную кольцевую систему, в которой моноциклическое и по меньшей мере одно из бициклических конденсированных колец является ароматическим кольцом, содержащим (а) от 1 до 4 атомов азота или (b) один атом кислорода или серы или (с) 1 атом кислорода или 1 атом серы и 1 или 2 атома азота, и конденсированное кольцо может представлять собой арильную группу, другой гетероарил, насыщенный или частично насыщенный циклоалкил или насыщенный или частично насыщенный гетероцикл. Гетероарил необязательно может содержать от 1 до 3 элементов кольца, выбранных из группы, включающей О, S или N. Гетероарил может присоединяться с помощью любого элемента кольца. Подходящие моноциклические гетероарильные группы включают пиридил, тиенил, фуранил, пирролил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил и тетразолил. Подходящие конденсированные гетероарильные группы включают индолил, бензофуранил, хинолил, изохинолил, индазолил, индолинил,- 16020586 изоиндолил, индолизинил, бензимидазолил и хинолинил. Термин "гетероарилен" означает бирадикальную гетероарильную моноциклическую или конденсированную кольцевую систему, в которой кольцо(кольца) обладают двумя положениями присоединения, которые могут находиться в одном кольце или, в случае конденсированной кольцевой системы, в разных кольцах. Термин "циклогетероалкил" или "гетероцикл" означает неароматическое кольцо (кольца), которое является частично или полностью насыщенным и может существовать в виде отдельного кольца, бициклического кольца или спироциклического кольца, содержащего 1 или 2 элемента кольца, выбранных из группы, включающей N(R27), О или S(O)r. Циклогетероалкил необязательно может содержать от 1 до 3 элементов кольца, каждый из которых независимо выбран из группы, включающей С(=О), N(R28)q, О илиS(O)r, где R27 или R28 обозначает Н или (С 1-C6)алкил, q равно 0-1, r равно 0-2. Циклогетероалкил может присоединяться с помощью любого элемента кольца. Подходящие гетероциклоалкильные группы включают [1,3]диоксолан, [1,4]диоксан, оксиранил, азиридинил, оксетанил, азетидинил, тетрагидрофуранил,пирролидинил, тетрагидропиранил, пиперидинил, морфолиновую группу, тиоморфолинил, пиперазинил,азепинил, оксапинил, оксазепинил и диазепинил. Термин "циклогетероалкилен" означает бирадикальный гетероцикл, обладающий двумя положениями присоединения. Гетероциклическое кольцо может представлять собой отдельное кольцо, бициклическое кольцо или спироциклическое кольцо, где два центра связывания бициклического кольца и спироциклического кольца могут находиться в одном кольце или в разных кольцах. См., например, приведенную ниже иллюстрацию."Галоген" может означать фтор, хлор, бром или йод. Следует понимать, что обозначение С(О) означает группу -С=О, которая может входить в кетон,альдегид или кислоту или производное кислоты. Аналогичным образом, S(O) означает группу -S=O. Выражение "терапевтически эффективное количество" означает количество соединения, предлагаемого в настоящем изобретении, которое (i) лечит или предупреждает конкретное заболевание, патологическое состояние или нарушение, (ii) ослабляет, смягчает или устраняет один или большее количество симптомов конкретного заболевания, патологического состояния или нарушения, или (iii) предупреждает или задерживает начало одного или большего количества симптомов конкретного заболевания, патологического состояния или нарушения, описанного в настоящем изобретении. Термин "животное" означает людей (мужчин или женщин), домашних животных (например, собак,кошек и лошадей), животных, являющихся источником пищи, животных в зоопарках, морских животных, птиц и животных других аналогичных видов. "Съедобные животные" означают животных, являющихся источником пищи, таких как коровы, свиньи и домашняя птица. Предпочтительным животным является человек. Выражение "фармацевтически приемлемый" показывает, что вещество или композиция должны быть химически и/или токсикологически совместимы с другими ингредиентами, входящими в препарат,или с животным, которое ими лечат. Термины "лечение", "лечить" включает предупредительное, т.е. профилактическое, и паллиативное лечение. Термин "соединения, предлагаемые в настоящем изобретении" (если специально не указано иное) означает соединения формулы (I) и (Ib) и их соли, а также все стереоизомеры (включая диастереоизомеры и энантиомеры), таутомеры и изотопно-меченые соединения (включая дейтерозамещенные), а также образованные вследствие их природы (например, полиморфные формы, сольваты и/или гидраты). Для задач настоящего изобретения гидраты и сольваты считаются композициями, содержащими соединение,предлагаемое в настоящем изобретении, и инертный наполнитель (например, воду или растворитель). Подробное описание изобретения Соединения, предлагаемые в настоящем изобретении, можно синтезировать путями, которые включают методики, аналогичные хорошо известным в химической науке, в частности, с учетом описания,приведенного в настоящем изобретении. Исходные вещества обычно можно приобрести у таких фирм,как Aldrich Chemicals (Milwaukee, Wis.) или легко получить по методикам, хорошо известным специалистам в данной области техники (например, получить по методикам, описанным в публикациях Louis F.Fieser and Mary Fieser, Reagents for Organic Synthesis, v. 1-19, Wiley, New York (1967-1999 ed.) или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая дополнения (также доступные в виде баз данных Beilstein в Интернете. Для иллюстративных целей на схемах реакций, представленных ниже, приведены возможные пути синтеза соединений, предлагаемых в настоящем изобретении, а также основных промежуточных продук- 17020586 тов. Более подробное описание отдельных стадий реакций приведено ниже в разделе "Примеры". Специалисты в данной области техники должны понимать, что для синтеза соединений, предлагаемых в настоящем изобретении, можно использовать другие методики синтеза. Хотя на схемах приведены и ниже обсуждены конкретные исходные вещества и реагенты, легко можно использовать другие исходные вещества и реагенты и/или условия проведения реакций и получить множество производных. Кроме того,многие соединения, полученные по описанным ниже методикам, можно дополнительно модифицировать с учетом настоящего раскрытия по обычным химическим методикам, хорошо известным специалистам в данной области техники. Для получения соединений, предлагаемых в настоящем изобретении, может потребоваться защита дальних функциональных групп (например, первичной или вторичной аминогруппы) в промежуточных продуктах. Необходимость такой защиты зависит от природы дальних функциональных групп и условий проведения методик получения. Подходящие защитные группы аминогруппы (NH-Pg) включают ацетил,трифторацетил,трет-бутоксикарбонил(CBz) и 9 флуоренилметиленоксикарбонил (Fmoc). Необходимость такой защиты легко определит специалист в данной области техники. Общее описание защитных групп и их применения приведено в публикации Т.W. Greene, Protective Groups in Organic Synthesis, John WileySons, New York, 1991. Приведенная ниже схема 1 показывает, как можно получить соединения формулы (I) или (Ib). Специалисты в данной области техники должны знать, как изменить условия и/или исходные вещества для получения других полезных производных. Схема 1 Соединения формулы (I) можно получить путем проводимого сначала катализируемого металлом перекрестного сочетания сульфонамидов типа II с гетероарилгалогенидами типа III (Hal обычно обозначает Cl или Br и Pg обозначает защитную группу) с получением гетероарилсульфонамидов типа IV. Например,перекрестное сочетание можно провести с использованием трис(дибензилиденацетон)дипалладия(0) (также называющегося, как Pd2(dba)3), 2-(2-дициклогексилфосфанилфенил)-N,N-диметиланилина (также известного, как DavePhos), карбоната цезия в диоксане при повышенных температурах (например, примерно при 180 С). Альтернативно, перекрестное сочетание можно провести с использованием йодида меди, карбоната цезия и N,N-диметилциклогексан-1,2 диамина в толуоле примерно при 90 С. После этого защитную группу азота можно удалить при условиях, подходящих для конкретной защитной группы, использующейся для получения промежуточных продуктов типа V. Затем промежуточные продукты типа V можно подвергнуть восстановительному аминированию или кетонами типа VI и после удаления защитной группы получить промежуточные продукты типа VII, или кетонами типа IX и получить соединения формулы (I). Второе восстановительное аминирование аминов типа VII карбониль- 18020586 ными соединениями типа VIII также дает соединения формулы (I). Например, восстановительное аминирование можно провести с использованием цианоборогидрида натрия или триацетоксиборогидрида натрия при условиях, хорошо известных специалистам в данной области техники. Следует понимать, что для иллюстрации общей схемы переменная А, описанная в формуле изобре тения, представлена в виде и переменная R1, описанная в формуле изобретения, пред ставлена в виде Соединения можно выделить и использовать в виде самого соединения или в виде его соли. При использовании в настоящем изобретении термины "соль" или "соли" означают соль присоединения с кислотой или соль присоединения с основанием соединения, предлагаемого в настоящем изобретении."Соли", в частности, включают "фармацевтически приемлемые соли". Термин "фармацевтически приемлемые соли" означает соли, которые сохраняют биологическую эффективность и свойства соединений,предлагаемых в настоящем изобретении, и которые обычно не являются нежелательными в биологическом или ином отношении. Во многих случаях соединения, предлагаемые в настоящем изобретении, могут образовывать соли с кислотой и/или основанием вследствие наличия аминогрупп и/или карбоксигрупп или аналогичных им групп. Фармацевтически приемлемые соли присоединения с кислотами можно образовать с неорганическими кислотами и с органическими кислотами, например, ацетат, аспартат, бензоат, безилат, бромид/гидробромид, бикарбонат/карбонат, бисульфат/сульфат, камфорсульфонат, хлорид/гидрохлорид,хлортеофиллонат, цитрат, этандисульфонат, фумарат, глюцептат, глюконат, глюкуронат, гиппурат, гидройодид/йодид, изетионат, лактат, лактобионат, лаурилсульфат, малат, малеат, малонат, манделат, мезилат, метилсульфат, нафтоат, напзилат, никотинат, нитрат, октадеканоат, олеат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрофосфат, полигалактуронат, пропионат, стеарат, сукцинат, сульфосалицилат, тартрат, тозилат и трифторацетат. Неорганические кислоты, из которых можно образовать соли, включают, например, хлористоводородную, бромисто-водородную, серную, азотную, фосфорную кислоты и т.п. Органические кислоты, из которых можно образовать соли, включают, например, уксусную, пропионовую, гликолевую, щавелевую, малеиновую, малоновую, янтарную, фумаровую, винную, лимонную, бензойную, миндальную, метансульфоновую, этансульфоновую, толуолсульфоновую, сульфосалициловую кислоты и т.п. Фармацевтически приемлемые соли присоединения с основанием можно образовать с неорганическими и органическими основаниями. Неорганические основания, из которых можно образовать соли, включают, например, соли аммония и металлов групп I-XII Периодической системы. В некоторых вариантах осуществления соли образованы из натрия, калия, аммония, кальция, магния, железа, серебра, цинка и меди; особенно предпочтительные соли включают соли аммония, калия, натрия, кальция и магния. Органические основания, из которых можно образовать соли, включают, например, первичные,вторичные и третичные амины, замещенные амины, включая природные замещенные амины, циклические амины, основные ионообменные смолы и т.п. Некоторые органические амины включают изопропиламин, бензатин, холин, диэтаноламин, диэтиламин, лизин, меглумин, пиперазин и трометамин. Фармацевтически приемлемые соли, предлагаемые в настоящем изобретении, можно синтезировать из исходного соединения, основного или кислотного фрагмента по обычным химическим методикам. Обычно такие соли можно получить по реакции свободных кислотных форм этих соединений со стехиометрическим количеством соответствующего основания (такого как гидроксид, карбонат, бикарбонат и т.п. Na, Ca, Mg или K) или по реакции свободных основных форм этих соединений со стехиометрическим количеством соответствующей кислоты. Такие реакции обычно проводят в воде, или в органическом растворителе, или в их смеси. Обычно, если это возможно, желательно использование неводных сред, таких как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечни дополнительных подходящих солей приведены, например, в публикациях "Remington's Pharmaceutical Sciences", 20th ed.,Mack Publishing Company, Easton, Pa., (1985); и "Handbook of Pharmaceutical Salts: Properties, Selection,and Use" by Stahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002). В объем настоящего изобретения входят все фармацевтически приемлемые изотопно-меченые соединения, предлагаемые в настоящем изобретении, т.е. соединения формулы (I) и (Ib), в которых один или большее количество атомов заменены на атомы, обладающие таким же атомным номером, но атомной массой или массовым числом, отличающимся от атомной массы или массового числа, обычно обнаруживающихся в природе. Примеры изотопов, подходящих для включения в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такие как 36 О и 18 О, фосфора, такие как 32 Р, и серы, такие как 35S. Некоторые изотопно-меченые соединения формулы (I) и (Ib), например, содержащие радиоактивный изотоп, применимы для исследования распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы тритий, т.е. 3 Н, и углерод-14, т.е. 14 С, являются особенно подходящими для этой цели вследствие легкости их включения и простых средств детектирования. Замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2 Н, может привести к некоторым терапевтическим преимуществам, обусловленным большей метаболической стабильностью, например увеличенным периодом полувыведения in vivo или возможностью использования меньших доз, и, следовательно, при некоторых обстоятельствах может быть предпочтительным. Замещение изотопами, испускающими позитроны, такими как 11 С, 18F, 15 О и 13N, может быть полезно для изучения занятости рецепторов субстрата с помощью позитронной эмиссионной томографии(ПЭТ). Изотопно-меченые соединения формулы (I) и (Ib) обычно можно получить по стандартным методикам, известным специалистам в данной области техники, или по методикам, аналогичным описанным в приведенных ниже примерах и синтезах, с использованием подходящих изотопно-меченых реагентов вместо использовавшегося ранее не содержащего изотопа реагента. Специалисты в данной области техники должны понимать, что соединения, предлагаемые в настоящем изобретении, могут содержать хиральные центры и поэтому могут существовать в различных изомерных формах. При использовании в настоящем изобретении термин "изомеры" означает разные соединения, которые обладают одной и той же молекулярной формулой, но различаются по расположению и конфигурации атомов. Кроме того, при использовании в настоящем изобретении термин "оптический изомер" означает любую из разных стереоизомерных конфигураций, которые могут существовать для данного соединения, предлагаемого в настоящем изобретении, и включает геометрические изомеры. Следует понимать, что заместитель может быть присоединен к атому углерода, являющемуся хиральным центром. Поэтому настоящее изобретение включает энантиомеры, диастереоизомеры и рацематы соединения."Энантиомеры" представляют собой пару стереоизомеров, которые являются зеркальными изображениями, не налагающимися друг на друга. Смесь двух энантиомеров состава 1:1 называется "рацемической" смесью. Этот термин используется для обозначения рацемической смеси, если это является подходящим."Диастереоизомеры" являются стереоизомерами, которые содержат не менее двух асимметрических атомов, но которые не являются зеркальными изображениями друг друга. Абсолютную стереохимическую конфигурацию описывают с помощью R-S системы Кана-Ингольда-Прелога. Если соединение является чистым энантиомером, то стереохимическую конфигурацию каждого хирального атома углерода можно описать, как R или S. Разделенные соединения, абсолютная конфигурация которых не установлена, можно описать с помощью символов (+) или (-) в зависимости от направления, в котором они вращают плоскость поляризации света при длине волны линии D натрия (право- и левовращающие). Некоторые соединения, описанные в настоящем изобретении, содержат один или большее количество асимметрических центров и поэтому могут образовывать энантиомеры, диастереоизомеры и другие стереоизомерные формы, абсолютную стереохимическую конфигурацию которых можно обозначить, как (R)- или(S)-. Если не указано иное, то соединения, предлагаемые в настоящем изобретении, включают все такие возможные изомеры, включая рацемические смеси, оптически чистые формы и смеси промежуточного состава. Оптически активные (R)- и (S)-изомеры можно получить с помощью хиральных синтонов или хиральных реагентов или выделить по обычным методикам. Если соединение содержит двойную связь,то заместители могут находиться в Е- или Z-конфигурации. Если соединение представляет собой дизамещенный циклоалкил, то заместители циклоалкила могут находиться в цис- или транс-конфигурации. Предполагается, что в объем настоящего изобретения входят все таутомерные формы. Соединения, предлагаемые в настоящем изобретении, которые содержат группы, способные выступать в качестве доноров и/или акцепторов водородных связей, могут образовывать совместные кристаллы с подходящими веществами, образующими совместные кристаллы. Эти совместные кристаллы можно получить из соединений, предлагаемых в настоящем изобретении, по известным методикам совместной кристаллизации. Такие методики включают измельчение, нагревание, совместную возгонку, совместное плавление или взаимодействие в растворе соединения, предлагаемые в настоящем изобретении, с веществами, образующими совместные кристаллы, при условиях кристаллизации с выделение образовавшихся таким образом совместных кристаллов. Подходящие вещества, образующие совместные кристаллы,включают описанные в WO 2004/078163. Следовательно, настоящее изобретение также относится к совместным кристаллам, включающим соединение, предлагаемое в настоящем изобретении. Соединение формулы (I) или (Ib) также с успехом можно применять в комбинации с другими антипролиферативными соединениями. Такие антипролиферативные соединения включают, но не ограничиваются только ими, ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; соединения, активные по отношению к микротрубочкам; алкилирующие соединения; соединения, которые индуцируют процессы дифференциации клеток; ингибиторы циклооксигеназы; ингибиторы ММР; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, предназначенные для избирательного воздействия/уменьшения активности протеин- или липидкиназы и другие антиангиогенные соединения; соединения, которые предназначены для избирательного воздействия/уменьшения или ингибирования активности протеин- или липидфосфатазы; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; бисфосфонаты; модификаторы биологического ответа; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеосомы; соединения, применяющиеся при лечении злокачественных заболеваний крови; которые предназначены для избирательного воздействия,уменьшения или ингибирования активности Flt-3; ингибиторы Hsp90, ингибиторы кинезинового белка веретена, ингибиторы PI3K, ингибиторы RAF, средства, связывающие EDG, противолейкозные соединения, ингибиторы рибонуклеотидредуктазы, ингибиторы S-аденозилметиониндекарбоксилазы, антипролиферативные антитела или другие химиотерапевтические соединения. Кроме того, альтернативно или в дополнение их можно применять в комбинации с другими методиками борьбы с опухолями, включая хирургию, применение ионизирующего излучения, фотодинамическую терапию, имплантаты, например,совместно с кортикостероидами, гормонами, или их можно применять в качестве радиосенсибилизаторов. Кроме того, в противовоспалительное и/или антипролиферативное лечение включают комбинации с противовоспалительными лекарственными веществами. Также возможна комбинация с антигистаминными лекарственными веществами, бронхорасширяющими лекарственными средствами, нестероидными противовоспалительными лекарственными средствами или антагонистами хемокиновых рецепторов. Некоторые более предпочтительные терапевтические средства, вместе с которыми можно использовать соединение формулы (I) или (Ib), включают доксорубицин, доцетаксел, 5FU, камптотецин, эрлотиниб,паклитаксел, карбоплатин, этопозид и гемцитабин. Соединения, предлагаемые в настоящем изобретении, применимы в качестве профилактических и терапевтических средств лечения заболеваний или нарушений, связанных с гиперактивностью Bcl-2. Таким образом, другим объектом настоящего изобретения является способ лечения заболевания или патологического состояния, связанного с гиперактивностью Bcl-2 или заболевания или патологического состояния, модулируемого с помощью Bcl-2, включающий введение соединения формулы (I) или (Ib) или его фармацевтически приемлемой соли в терапевтически эффективном количестве. Другим объектом настоящего изобретения является способ лечения пролиферативного заболеваний, такого как рак, включающий введение формулы (I), (Ib) или его фармацевтически приемлемой соли в терапевтически эффективном количестве. Примеры типов рака включают, но не ограничиваются только ими, рак молочной железы, колоректальный рак, рак яичников, рак поджелудочной железы или рак предстательной железы,хронический лимфолейкоз, диффузные крупноклеточные В-клеточные лимфомы, фолликулярные лимфомы, хронический или острый лейкоз, хронический миелолейкоз, лимфоидные злокачественные новообразования Т-клеточной или В-клеточной этиологии, рак легких, такой как мелкоклеточный рак легких и немелкоклеточный рак легких, меланома или другие раковые заболевания кожи, множественная миелома, рак яичников, рак желудочно-кишечного тракта (желудка, колоректальный и двенадцатиперстной кишки), рак мочевого пузыря, рак матки, рак шейки матки, саркома, происходящая из мягких тканей, рак почки, опухоли головного мозга, печеночно-клеточный рак, рак головы и шеи, рак шейки матки, фибросаркома и другие раковые заболевания. Настоящее изобретение дополнительно поясняется, но не ограничивается приведенными ниже типичными примерами, которые предназначены для иллюстрации настоящего изобретения, и их не следует рассматривать, как ограничивающие. Примеры Структуру конечных продуктов, описанных в настоящем изобретении, можно подтвердить с помощью стандартных аналитических методик, например с помощью спектрометрических и спектроскопических методик (например, МС, ЯМР, ВЭЖХ). Времена удерживания, приведенные ниже в примерах, определены с помощью системы Agilent 1100 HPLC; колонка Inertsil ODS3 1003 мм С 18; скорость потока 1,0 мл/мин; градиентный режим 5-95% ацетонитрил/вода с добавлением 0,1% муравьиной кислоты. Соединения очищают по стандартным методикам, например, с помощью кристаллизации, флэшхроматографии или ВЭЖХ с обращенной фазой. Приведенные ниже аббревиатуры обладают указанными значениями в представленных ниже примерах. ДХЭ - 1,2-дихлорэтан; ДИПЭА - диизопропилэтиламин; ДМА - диметилацетамид; ДМЭ - 1,2-диметоксиэтан; ДМФ - диметилформамид; экв. - эквиваленты; ВЭЖХ - высокоэффективная жидкостная хроматография; ВР-МС - масс-спектрометрия высокого разрешения; МС - масс-спектрометрия; ЯМР - ядерный магнитный резонанс; ТФЭ - твердофазная экстракция; ВПР - времяпролетная масс-спектрометрия. Получение ключевых промежуточных продуктов. Синтез промежуточных продуктов типа II(18,8 мл) нагревали при 100 С в течение 6 ч. Реакционную смесь охлаждали до комнатной температуры и разбавляли смесью EtOAc/гептаны (1:1, 50 мл). Этот раствор промывали водой, слои разделяли и водный слой экстрагировали смесью EtAc/гептаны (1:1) (50 мл 3). Объединенные органические слои промывали водой, сушили над MgSO4, концентрировали и получали искомое соединение в виде желтого твердого вещества (965 мг, выход 82%). МС (ИЭР - ионизация электрораспылением) m/е (М+Н+): 512,2. Искомое соединение получали из 4-фтор-3-(трифторметилсульфонил)бензолсульфонамида и (R)-3 морфолин-4-ил-1-фенилсульфанилметилпропиламина по методике, описанной для промежуточного продукта 4. МС (ИЭР) m/е (М+Н+): 553,6. Промежуточный продукт 6. Искомое соединение получали из 4-фтор-3-(трифторметил)бензолсульфонамида и (R)-N1,N1 диметил-4-фенилсульфанилбутан-1,3-диамина по методике, описанной для промежуточного продукта 4. Промежуточный продукт 7. Искомое соединение получали из 4-фтор-3-(циано)бензолсульфонамида и (R)-N1,N1-диметил-4 фенилсульфанилбутан-1,3-диамина по методике, описанной для промежуточного продукта 4. Промежуточный продукт 8. Искомое соединение получали из 3,4,5-трифторбензолсульфонамида и (R)-N1,N1-диметил-4 фенилсульфанилбутан-1,3-диамина по методике, описанной для промежуточного продукта 4. Промежуточный продукт 9. 4-R)-3-Диметиламино-1-фенилсульфанилметилпропиламино)-3-нитробензолсульфонамид Промежуточный продукт 9 получали, как описано в публикации Wendt, M.D., et al., in J. Med. Chem. 2006, 49, 1165-1181. Синтез промежуточных продуктов типа III(1,0 г). Полученную суспензию перемешивали в течение 16 ч в атмосфере водорода. Реакционную смесь фильтровали через целит, концентрировали и получали светло-желтое твердое вещество (2,9 г). Его сразу растворяли в CH2Cl2 (100 мл), обрабатывали Вос-ангидридом (4,4 г, 20,2 ммоль) и ДИПЭА (4,3 г, 33,6 ммоль) и перемешивали в течение 16 ч при комнатной температуре. Органические вещества последовательно промывали с помощью HCl (1 н.), водой и рассолом, сушили над сульфатом магния, фильтровали,концентрировали и получали 1-трет-бутиловый эфир,4-этиловый эфир 3-оксопиперидин-1,4 дикарбоновой кислоты в виде прозрачного масла (4,8 г, выход 100%). МС (ИЭР) m/e (M+H+): 271,36. Стадия В. 1-трет-Бутиловый эфир,4-этиловый эфир 3-оксопиперидин-1,4-дикарбоновой кислоты(4,6 г, 16,8 ммоль) растворяли в EtOH (90 мл) и последовательно добавляли этоксид натрия (2,3 г, 33,6 ммоль) и формамидингидрохлорид (2,0 г, 25,2 ммоль). Полученную суспензию нагревали при 70 С и перемешивали в течение 5 ч и затем реакционную смесь охлаждали до комнатной температуры и концентрировали. Остаток растворяли в насыщенном растворе хлорида аммония и экстрагировали этилацетатом. Значение рН водной фазы доводили до 5,5 концентрированной АсОН и еще несколько раз экстрагировали этилацетатом. Объединенные органические слои последовательно промывали водой и рассолом, сушили, концентрировали и получали трет-бутиловый эфир 4-гидрокси-5,8-дигидро-6 Н-пиридо[3,4d]пиримидин-7-карбоновой кислоты в виде коричневого твердого вещества (1,8 г, выход 42%). МС (ИЭР) m/e (M+H+)=251,28. Стадия С. Смесь трет-бутилового эфира 4-гидрокси-5,8-дигидро-6 Н-пиридо[3,4-d]пиримидин-7 карбоновой кислоты (1,4 г, 5,6 ммоль) и трифенилфосфина (2,9 г, 11,1 ммоль) перемешивали в ДХЭ (41 мл) до образования прозрачного раствора и затем добавляли тетрахлорид углерода (1,6 мл, 16,7 ммоль). Реакционную смесь нагревали при 70 С и перемешивали в течение 2,5 ч. Летучие вещества удаляли в вакууме и неочищенное вещество непосредственно очищали с помощью флэш-хроматографии на силикагеле (0-50% EtOAc/гептаны) и получали искомое соединение в виде почти белого твердого вещества Стадия А. Этоксид натрия получали путем объединения металлического натрия (0,5 г, 21,8 ммоль) и этанола (33 мл). При температуре окружающей среды добавляли трифторацетамидин (1,35 г, 12,0 ммоль), затем порциями в течение 15 мин сразу добавляли этил-1-бензил-3-оксо-4 пиперидинкарбоксилатгидрохлорид (2,92 г, 9,81 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч и затем нагревали при 80 С в течение 16 ч. Затем реакционную смесь охлаждали до температуры окружающей среды и растворитель удаляли в вакууме. Полученное темно-красное вспененное твердое вещество переносили в диэтиловый эфир (40 мл) и 1 н. водный раствор NaOH (40 мл). Слои разделяли и водный слой промывали с помощью Et2O (40 мл). Объединенные органические слои экстрагировали с помощью 1 н. NaOH (10 мл). Объединенные водные слои охлаждали до 0 С и подкисляли до рН 7 концентрированной HCl. Осаждалось желтовато-коричневое твердое вещество, которое выделяли медленным фильтрованием. Сушка на фильтре в течение ночи давала 7-бензил-2(трифторметил)-5,6,7,8-тетрагидропиридо[3,4-d]пиримидин-4-ол (2,35 г, выход 78%). МС (ИЭР) m/e (М+Н)+=310,4. Стадия В. К 7-бензил-2-(трифторметил)-5,6,7,8-тетрагидропиридо[3,4-d]пиримидин-4-олу (0,47 г,1,52 ммоль), частично растворенному в метаноле (20 мл), добавляли гидроксид палладия на угле (70 мг,влажный, 20 мас.% в пересчете на массу сухого вещества). Реакционную смесь перемешивали в течение 20 ч во встряхивающем устройства Парра при давлении водорода, равном 50 фунт-сила/дюйм 2. Затем реакционную смесь фильтровали через слой целита, элюируя метанолом (400 мл). Фильтрат концентрировали в вакууме и получали 2-(трифторметил)-5,6,7,8-тетрагидропиридо[3,4-d]пиримидин-4-ол в виде светло-бежевого твердого вещества (255 мг, выход 77%). 1 Н ЯМР (400 МГц, MeOD)част./млн 4,09 (s, 2 Н), 3,48 (t, J=6,32 Гц, 2 Н), 2,78 (t, J=6,32 Гц, 2 Н). Стадия С. При перемешивании к смеси 2-(трифторметил)-5,6,7,8-тетрагидропиридо[3,4d]пиримидин-4-ола (0,246 г, 1,122 ммоль) с тетрагидрофураном (11 мл) добавляли раствор ди-третбутилдикарбоната (0,269 г, 1,235 ммоль) в тетрагидрофуране (11 мл). Смесь перемешивали при температуре окружающей среды в течение 16 ч и затем концентрировали в вакууме. Неочищенный остаток очищали с помощью флэш-хроматографии на силикагеле (элюент: от 0 до 7% метанол/дихлорметан) и получали трет-бутил-4-гидрокси-2-(трифторметил)-5,6-дигидропиридо[3,4-d]пиримидин-7(8 Н)-карбоксилат в виде светло-желтого вспененного твердого вещества (0,306 г, выход 85%). МС (ИЭР) m/e (M-H)-=318,3. Стадия D. трет-Бутил-4-гидрокси-2-(трифторметил)-5,6-дигидропиридо[3,4-d]пиримидин-7(8 Н)карбоксилат (5,12 г, 16,05 ммоль) объединяли с трифенилфосфином (8,42 г, 32,1 ммоль) и перемешивали в дихлорэтане (160 мл) при температуре окружающей среды в течение 15 мин и затем добавляли тетрахлорид углерода (7,41 г, 48,1 ммоль). Реакционную смесь перемешивали при 70 С в течение 3 ч, охлаждали до комнатной температуры и концентрировали в вакууме. Неочищенный остаток очищали с помощью флэш-хроматографии на силикагеле (элюируя в градиентном режиме смесью от 0 до 3% метанол/ДХМ (дихлорметан и получали искомое соединение в виде прозрачного масла (5,22 г, выход 86%). МС (ИЭР) m/e (M-H)-=336,3. Промежуточный продукт 12. трет-Бутиловый эфир 3-бром-4,5,7,8-тетрагидро-1,2,3 а,6-тетраазаазулен-6-карбоновой кислоты Стадия А. При перемешивании к раствору трет-бутил-5-оксо-1,4-диазепан-1-карбоксилата (1000 мг,4,67 ммоль) в дихлорметане (10 мл) в атмосфере азота добавляли триметилоксонийтетрафторборат (690 мг, 4,67 ммоль) и реакционную смесь перемешивали в течение 16 ч. Затем гидразинформиат (280 мг, 4,67 ммоль) в дихлорметане (8 мл) добавляли и реакционную смесь перемешивали в течение еще 16 ч. Затем реакционную смесь концентрировали при пониженном давлении, повторно суспендировали в метаноле(10 мл) и кипятили с обратным холодильником в течение 16 ч. Реакционную смесь концентрировали,очищали с помощью флэш-хроматографии на силикагеле (0-50% 2 н. NH3 в метаноле в CH2Cl2) и получали трет-бутиловый эфир 4,5,7,8-тетрагидро-1,2,3 а,6-тетраазаазулен-6-карбоновой кислоты (680 мг, выход 61%). МС [m/z; (M+1)+]: 319,3. Стадия В. К суспензии трет-бутилового эфира 4,5,7,8-тетрагидро-1,2,3 а,6-тетраазаазулен-6 карбоновой кислоты (200 мг, 0,839 ммоль) в воде добавляли 10 н. NaOH до образования прозрачного раствора. Затем медленно добавляли Br2 (0,432 мл, 8,39 ммоль), поддерживая значение рН 12 путем добавления концентрированного раствора NaOH. Реакционную смесь перемешивали при температуре окружающей среды в течение 16 ч. Затем реакционную смесь подкисляли до рН 4 с помощью 6 М HCl. Органические вещества трижды экстрагировали с помощью CH2Cl2. Объединенные органические слои промывали рассолом, сушили над Na2SO4, фильтровали, концентрировали при пониженном давлении и получали искомое соединение в виде белого твердого вещества (185 мг, выход 70%). 1H ЯМР (400 МГц, ДМСО-d6)част./млн 1,43 (s, 9 Н), 3,05 (br. s., 2 Н), 3,54 (br. s., 2H), 3,63-3,71 (m,2H), 4,10 (br. s., 2H). Общая методика катализируемого Pd перекрестного сочетания сульфонамидов II с гетероарилхлоридами III В высушенный в сушильном шкафу флакон объемом 20 мл с тефлоновой крышкой помещали(DavePhos) (0,03 экв.). Затем флакон закрывали и продували азотом. Добавляли диоксан (1,5 мл) и полученную суспензию перемешивали в течение 15 мин в атмосфере азота. Добавляли раствор сульфонамида(1 экв.) и гетероарилхлорида (1 экв.) в диоксане (1,0 мл/ммоль II). Через 5 мин смесь помещали в микроволновую печь и нагревали при 180 С в течение 30 мин. Затем растворитель фильтровали через слой сульфата магния, промывая с помощью CH2Cl2. Фильтрат концентрировали и получали оранжевое твер- 25020586 дое вещество. Это твердое вещество повторно растворяли в CH2Cl2 и полученный раствор промывали насыщенным водным раствором NaHCO3, затем рассолом. Объединенные водные слои дважды экстрагировали с помощью CH2Cl2 и один раз с помощью EtOAc. Объединенные органические слои сушили надMgSO4, концентрировали и неочищенный остаток очищали с помощью флэш-хроматографии на силикагеле (градиентный режим: от 0 до 40% метанол/CH2Cl2). Промежуточный продукт 13. трет-Бутиловый эфир 4-4-[4-R)-3-морфолин-4-ил-1-фенилсульфанилметилпропиламино)-3 трифторметансульфонилбензолсульфониламино]-5,8-дигидро-6 Н-пиридо[3,4d]пиримидин-7 илпиперидин-1-карбоновой кислоты С использованием общей методики 4-R)-3-морфолин-4-ил-1-фенилсульфанилметилпропиламино)3-трифторметансульфонилбензолсульфонамид (616 мг, 1,1 ммоль) и трет-бутиловый эфир 4-хлор-5,8 дигидро-6 Н-пиридо[3,4-d]пиримидин-7-карбоновой кислоты (300 мг, 1,1 ммоль) давали искомое соединение (600 мг, выход 68%). МС (ИЭР) m/e (М+Н+): 787,4. Промежуточные продукты 14-18, указанные ниже, получали с помощью перекрестного сочетания сульфонамидов II с гетероарилхлоридами III по описанной выше общей методике. Промежуточный продукт 14.(54,8 мг,0,181 ммоль),4-R)-3-морфолин-4-ил-1-фенилсульфанилметилпропиламино)-3 трифторметансульфонилбензолсульфонамид (100 мг, 0,181 ммоль), (1S,2S)-N,N'-диметилциклогексан 1,2-диамин (07,71 мг, 0,054 ммоль), карбонат цезия (100 мг, 0,307 ммоль) и йодид меди(I) (5,16 мг, 0,027 ммоль) добавляли в сосуд для микроволновой печи, затем добавляли толуол (2 мл). Реакционную смесь дегазировали в течение 15 мин в атмосфере азота и затем нагревали при 90 С в течение 14 ч. Неочищенное вещество непосредственно очищали с помощью флэш-хроматографии на силикагеле (0-25% 7 н. ам- 27020586 миака в метаноле в CH2Cl2) и получали искомое соединение (130 мг, выход 92%). МС [m/z; (M+1)+]: 776,5. Промежуточный продукт 20. трет-Бутиловый эфир 3-[4-R)-3-морфолин-4-ил-1-фенилсульфанилметилпропиламино)-3 трифторметансульфонилбензолсульфониламино]-4,5,7,8-тетрагидро-1,2,3 а,6-тетраазаазулен-6 карбоновой кислоты(0,011 мл, 0,146 ммоль), карбонат цезия (269 мг, 0,825 ммоль) и йодид меди(I) (13,87 мг, 0,073 ммоль) добавляли в сосуд для микроволновой печи, затем добавляли толуол (8 мл). Реакционную смесь дегазировали в течение 15 мин в атмосфере азота, герметизировали и затем нагревали обычным образом при 90 С в течение 14 ч. Неочищенное вещество непосредственно очищали с помощью флэш-хроматографии на силикагеле (0-15% 2 н. NH3 в метаноле в CH2Cl2) и получали искомое соединение (170 мг, выход 44%). МС [m/z; (M+1)+]: 790,5. Промежуточный продукт 21. Стадия А. трет-Бутил-4-гидрокси-5 Н-пирроло[3,4-d]пиримидин-6(7 Н)-карбоксилат (300 мг, 1,264 ммоль) и (1H-бензо[d][1,2,3]триазол-1-илокси)-трис-(диметиламино)фосфонийгексафторфосфат(V) (671 мг, 1,517 ммоль) перемешивали в ацетонитриле (10 мл). К этой взвеси добавляли 2,3,4,6,7,8,9,10 октагидропиримидо[1,2-а]азепин (289 мг, 1,897 ммоль). Реакционную смесь перемешивали 1,5 ч. Растворители удаляли в вакууме и получали трет-бутил-4-(1H-бензо[d][1,2,3]триазол-1-илокси)-5 Нпирроло[3,4-d]пиримидин-6(7 Н)-карбоксилат, который использовали на следующей стадии без дополнительной очистки. Стадия В. трет-Бутил-4-(1H-бензо[d][1,2,3]триазол-1-илокси)-5 Н-пирроло[3,4-d]пиримидин-6(7 Н)карбоксилат(448 мг,1,264 ммоль),(R)-4-(4-морфолино-1-(фенилтио)бутан-2-иламино)-3(трифторметилсульфонил)бензолсульфонамид (910 мг, 1,643 ммоль) и карбонат калия (524 мг, 3,79 ммоль) объединяли в N,N-диметилформамиде (6,3 мл) и перемешивали в течение 1,5 ч при 85 С и затем в течение 2,5 ч при 95 С. Затем реакционную смесь охлаждали до комнатной температуры и перемешивали в течение 16 ч. Реакционную смесь обрабатывали водой (30 мл) и обрабатывали ультразвуком. Темно-коричневое твердое вещество прилипало к колбе. Твердое вещество несколько раз промывали водой и затем несколько раз диэтиловым эфиром. Затем этот остаток отрабатывали метанолом (15 мл) и образовавшийся почти белый осадок удаляли фильтрованием. Темно-коричневый фильтрат концентрировали в вакууме и получали коричневое твердое вещество. Промывочные растворы, содержащие воду и эфир, объединяли и разбавляли дополнительным количеством воды и эфира. Слои разделяли и органический слой сушили над сульфатом натрия, фильтровали и концентрировали. Этот остаток объединяли с коричневым твердым веществом, очищали с помощью флэш-хроматографии на силикагеле (от 0 до 10% метанол/этилацетат, затем от 0 до 30% метанол/дихлорметан) и получали искомое соединение (199 мг,выход 13%). МС (ИЭР) m/e (М+Н)+=773,5. Общая методика удаления защитной группы Boc из аминов IV. Амин (1 экв.) растворяли в CH2Cl2 (5 мл/ммоль) и колбу охлаждали до 0 С. Медленно добавляли хлористо-водородную кислоту (2 н. в диэтиловом эфире, 4 экв.) и затем реакционную смесь перемешивали в течение 3 ч при комнатной температуре. Растворитель удаляли в вакууме и к остатку добавлялиCH2Cl2 (20 мл). Полученный раствор промывали насыщенным водным раствором NaHCO3 и рассолом. Объединенные водные слои дважды экстрагировали с помощью CH2Cl2 и один раз с помощью EtOAc. Органические слои объединяли, сушили над MgSO4 и концентрировали. Дополнительную очистку не проводили. Промежуточный продукт 22. С использованием общей методики трет-бутиловый эфир 4-4-[4-R)-3-морфолин-4-ил-1 фенилсульфанилметилпропиламино)-3-трифторметансульфонилбензолсульфониламино]-5,8-дигидро 6 Н-пиридо[3,4-d]пиримидин-7-илпиперидин-1-карбоновой кислоты (300 мг, 0,38 ммоль) давал искомое соединение (170 мг, 50%). МС (ИЭР) m/e (М+Н+): 687,3. Промежуточные продукты 23-28 получали путем удаления защитной группы из аминов IV по описанной выше общей методике. Промежуточный продукт 23.
МПК / Метки
МПК: A61P 35/00, A61K 31/519, C07D 471/04, C07C 311/20
Метки: bcl-2, белков, семейства, предназначенные, качестве, ингибиторов, сульфонамиды, лечения, рака
Код ссылки
<a href="https://eas.patents.su/30-20586-sulfonamidy-v-kachestve-ingibitorov-belkov-semejjstva-bcl-2-prednaznachennye-dlya-lecheniya-raka.html" rel="bookmark" title="База патентов Евразийского Союза">Сульфонамиды в качестве ингибиторов белков семейства bcl-2, предназначенные для лечения рака</a>