Соединения-антагонисты рнк для модуляции активности бета-катенина
Формула / Реферат
1. Олигомер длиной 16-18 нуклеиновых оснований, способный ингибировать экспрессию гена бета-катенина, который включает в себя непрерывную последовательность длиной 16-18 нуклеиновых оснований, где указанная непрерывная последовательность нуклеиновых оснований является на 100% гомологичной соответствующей области SEQ ID NO: 192, и где указанный олигомер представляет собой одноцепочечную молекулу.
2. Олигомер по п.1, где непрерывная последовательность нуклеиновых оснований не содержит несовпадений с соответствующим участком SEQ ID NO: 192.
3. Олигомер по п.1 или 2, где последовательность нуклеиновых оснований олигомера состоит из непрерывной последовательности нуклеиновых оснований.
4. Олигомер по любому из пп.1-3, где непрерывная последовательность нуклеиновых оснований включает в себя нуклеотидные аналоги, такие как нуклеотиды с модифицированным сахаром, выбранные из группы, состоящей из молекул закрытой нуклеиновой кислоты (LNA); молекул 2'-O-алкил-РНК, молекул 2'-ОМе-РНК, молекул 2'-амино-ДНК и молекул 2'-фтор-ДНК.
5. Олигомер по п.4, где нуклеотидные аналоги представляют собой LNA.
6. Олигомер по п.4 или 5, который представляет собой гэпмер.
7. Олигомер по любому из пп.1-6, который ингибирует экспрессию гена или мРНК бета-катенина в клетке, которая экспрессирует ген или мРНК бета-катенина.
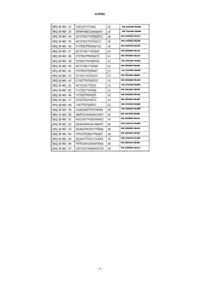
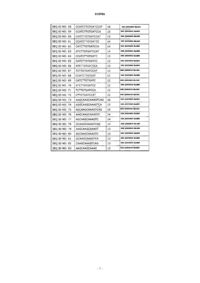
8. Олигомер по любому из пп.1-7, где последовательность нуклеиновых оснований указанного олигомера состоит из SEQ ID NO: 103 или SEQ ID NO: 151.
9. Олигомер по любому из пп.1-8, где олигомер представляет собой SEQ ID NO: 171
где строчные буквы представляют собой звенья ДНК, выделенные жирным шрифтом заглавные буквы представляют собой звенья бета-D-окси-LNA, все С LNA представляют собой 5'-метилцитозин и подстрочная буква "s" представляет собой фосфоротиоатную связь.
10. Конъюгат, включающий в себя олигомер по любому из пп.1-9 и по меньшей мере один ненуклеотидный или неполинуклеотидный фрагмент, ковалентно соединенный с указанным олигомером.
11. Фармацевтическая композиция, включающая в себя олигомер по любому из пп.1-9 или конъюгат по п.10 и фармацевтически приемлемые разбавитель, носитель, соль или адъювант.
12. Применение олигомера по любому из пп.1-9 или конъюгата по п.10 в качестве лекарственного средства для лечения гиперпролиферативного заболевания, такого как рак.
13. Применение олигомера по любому из пп.1-9, или конъюгата, как определено в п.10, для производства лекарственного средства для лечения гиперпролиферативного заболевания, такого как рак.
14. Применение по п.12 или 13, где олигомер представляет собой олигомер, определенный в п.9.
15. Способ in vitro ингибирования бета-катенина в клетке, которая экспрессирует бета-катенин, где указанный способ включает в себя введение олигомера по любому из пп.1-9 или конъюгата по п.10 в указанную клетку таким образом, чтобы ингибировать бета-катенин в указанной клетке.
Текст
СОЕДИНЕНИЯ-АНТАГОНИСТЫ РНК ДЛЯ МОДУЛЯЦИИ АКТИВНОСТИ БЕТАКАТЕНИНА Изобретение относится к олигомерным соединениям (олигомерам), мишенью которых в клетке является мРНК бета-катенина и которые вызывают уменьшение экспрессии бета-катенина. Уменьшение экспрессии бета-катенина является полезным при ряде медицинских нарушений,таких как гиперпролиферативные заболевания, включая рак. Изобретение предоставляет терапевтические композиции, включающие в себя олигомеры, и методы модулирования экспрессии бета-катенина с применением указанных олигомеров, включая методы лечения. Область техники, к которой относится изобретение Настоящее изобретение относится к олигомерным соединениям (олигомерам), мишенью которых в клетке является мРНК бета-катенина и которые вызывают уменьшение экспрессии бета-катенина. Уменьшение экспрессии бета-катенина является полезным при ряде медицинских нарушений, таких как гиперпролиферативные заболевания, включая рак. Изобретение предоставляет терапевтические композиции, включающие в себя олигомеры, и методы модулирования экспрессии бета-катенина с применением указанных олигомеров, включая методы лечения. Уровень техники изобретения Бета-катенин (также известный как кадгерин-ассоциированный белок и -катенин) является членом семейства катенинов, цитозольных белков и главным игроком сигнального пути, инициируемого белками Wnt, медиаторами нескольких процессов. Бета-катенин подвергается фосфорилированию после стимуляции факторами роста, приводящему к уменьшению клеточной адгезии. Как было показано, роль бета-катенина в развитии рака регулируется продуктом экспрессии генаAPC (аденоматозный полипоз толстой кишки). Опухолевый супрессор, белок APC связывается с бетакатенином, в то же время показано, что бета-катенин взаимодействует с факторами транскрипции Tcf иLef. По результатам работы Morin et al. белок APC подавляет транскрипционную активацию, опосредованную бета-катенином и Tcf-4 при колоректальном раке. Указанные результаты показывают, что регуляция бета-катенина является ключевой для опухоль-супрессивного эффекта APC и что данная регуляция может быть нарушена мутациями APC или бета-катенина. Об обнаружении мутаций бета-катенина в различных раковых клеточных линиях сообщается в нескольких исследованиях, и аномально высокие количества бета-катенина были обнаружены в клеточных линиях меланомы.Morin et al. показали, что мутации бета-катенина, которые повреждали участки фосфорилирования,делали клетки нечувствительными к APC-опосредованной понижающей регуляции бета-катенина, и что данный нарушенный механизм являлся ключевым в колоректальном онкогенезе (Morin et al., Science,1997, 275, 1787-1790). Патент США 6066500, Bennett et al. описывает антисмысловые соединения,композиции и методы модулирования экспрессии бета-катенина. Учитывая свидетельства участия бетакатенина в развитии рака, сохраняется потребность в агентах, способных эффективно ингибировать функции бета-катенина. Сущность изобретения Изобретение предоставляет олигомер длиной 10-50 нуклеиновых оснований, который включает в себя непрерывную последовательность нуклеиновых оснований общей длиной 10-50 нуклеиновых оснований, где указанная непрерывная последовательность нуклеиновых оснований является по меньшей мере на 80% гомологичной соответствующему участку нуклеиновой кислоты, которая кодирует бетакатенин млекопитающих. Изобретение предоставляет олигомер длиной 10-50 нуклеиновых оснований, который включает в себя непрерывную последовательность нуклеиновых оснований общей длиной 10-50 нуклеиновых оснований, где указанная непрерывная последовательность нуклеиновых оснований является по меньшей мере на 80% гомологичной соответствующему участку последовательности нуклеиновых кислот, выбранной из группы, состоящей из SEQ ID NO: 173 и SEQ ID NO: 174-193. Изобретение предоставляет олигомеры длиной 10-50 нуклеиновых оснований, которые включают в себя непрерывную последовательность нуклеиновых оснований общей длиной 10-50 нуклеиновых оснований, где указанная непрерывная последовательность нуклеиновых оснований является по меньшей мере на 80% гомологичной соответствующему участку последовательности нуклеиновых кислот, выбранных из группы, состоящей из SEQ ID NO: 1-132. Далее изобретение предоставляет конъюгат, включающий в себя олигомер в соответствии с изобретением, например конъюгат, который в дополнение к последовательности нуклеиновых оснований олигомера включает в себя по меньшей мере один ненуклеотидный (т.е. ненуклеиновые основания) или неполинуклеотидный фрагмент, ковалентно соединенный с олигомером изобретения. Ненуклеотидный или неполинуклеотидный фрагмент может состоять или включать в себя стериновую группу, например холестерин или другой фрагмент, который способствует проникновению в клетку. Изобретение предоставляет конъюгат, включающий в себя олигомер согласно изобретению, например конъюгат, который в дополнение к последовательности нуклеиновых оснований олигомера включает в себя полимерный конъюгат, содержащий положительно заряженные молекулы, например полиэтиленгликоль (ПЭГ), т.е. олигомер согласно изобретению может по желанию быть пегилированным. Изобретение предоставляет фармацевтическую композицию, включающую в себя олигомер или,как определено, конъюгат изобретения, и фармацевтически приемлемые разбавитель, носитель, соль или адъювант. Далее изобретение предусматривает олигомер в соответствии с изобретением для применения в медицине. Изобретение далее предусматривает применение олигомера изобретения для производства лекарственного средства для лечения одного или более заболеваний, упоминаемых в описании, например заболевания, выбранного из гиперпролиферативных заболеваний, например заболеваний, упоминаемых в описании, например рака. Изобретение далее предусматривает олигомер согласно изобретению для применения в лечении одного или более заболеваний, упоминаемых в описании, например рака. Также предоставлены фармацевтические и другие композиции, содержащие олигомер или конъюгат изобретения. Далее предоставлены способы уменьшения экспрессии бета-катенина в клетках или тканях, включающие в себя контактирование указанных клеток или тканей in vitro или in vivo с одним или более олигомерами, конъюгатами или композициями изобретения. Также раскрыты методы лечения животного или человека, предположительно имеющего или склонного к заболеванию или состоянию, ассоциированному с экспрессией или повышенной экспрессией бета-катенина, путем введения указанному животному или человеку терапевтически или профилактически эффективного количества одного или более олигомеров, конъюгатов или композиций изобретения. Далее предоставляются способы применения олигомеров для ингибирования экспрессии бетакатенина и для лечения заболеваний, ассоциированных с активностью бета-катенина. Изобретение предусматривает способ лечения заболевания или нарушения, например заболевания или нарушения, упоминаемых в описании, например гиперпролиферативного заболевания, такого как рак, указанный способ включает в себя введение олигомера, конъюгата или фармацевтической композиции согласно изобретению пациенту, который в этом нуждается. Изобретение предусматривает способ ингибирования или уменьшения экспрессии бета-катенина в клетке или ткани, указанный способ включает в себя стадию контактирования указанной клетки или ткани с олигомером, конъюгатом или с фармацевтической композицией согласно изобретению, так что экспрессия бета-катенина ингибируется или уменьшается. Изобретение предусматривает способ запускания апоптоза в клетке, например в раковой клетке,указанный способ включает в себя стадию контактирования указанной клетки или ткани с олигомером,конъюгатом или с фармацевтической композицией согласно изобретению, так что экспрессия бетакатенина ингибируется или уменьшается и/или запускается апоптоз. Изобретение далее предусматривает олигомер, который включает в себя или состоит из непрерывной последовательности нуклеиновых оснований, которая является по меньшей мере на 80% гомологичной участку, соответствующему последовательности, выбранной из группы, состоящей изSEQ ID NO: 1-132 и SEQ ID NO: 174-193, например последовательности, выбранной из группы, состоящей из SEQ ID NO: 189, 192, 58 и 103. Изобретение далее предусматривает олигомер, который включает в себя или состоит из непрерывной последовательности нуклеиновых оснований, которая соответствует эквивалентной последовательности, представленной в последовательности, выбранной из SEQ ID NO: 174-193, напримерSEQ ID NO: 189 или 192. Изобретение далее предусматривает олигомер, который включает в себя или состоит из последовательности, выбранной из группы, состоящей из SEQ ID NO: 133-174, например SEQ ID NO: 168 или 171,или которая включает в себя или состоит из непрерывной последовательности нуклеиновых оснований,которая соответствует указанной последовательности. Связанные случаи. Следующие родственные заявки включены в настоящее описание посредством ссылок:US 60/915371 и US 61/023244. Краткое описание чертежей Фиг. 1. Последовательности-мишени бета-катенина, которые соответствуют олигонуклеотиднымSEQ ID NO: 1, 16, 17, 18, 33, 34, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 73, 88, 103 и 118 соответственно, показаны толстым шрифтом и подчеркнуты, показывая их положение в транскрипте бета-катенина (номер доступа в Генбанк NM001904 - SEQ ID NO: 173). Фиг. 2. Экспрессия бета-катенина, нормализованная по ГАФДГ, через 24 ч после трансфекции клеток SW480. Фиг. 3. Содержание белка бета-катенина в клетках SW480, трансфицированных олигонуклеотидами в концентрации 1 и 5 нМ, измеренное с помощью вестерн-блоттинга. В качестве контроля нагрузки использовали окрашивание тубулина и в качестве скремблированного контроля (scrambled control) использовали олигонуклеотид SEQ ID NO: 194. Фиг. 4. Клеточная пролиферация, измеренная с помощью теста MTS в клетках НСТ 116, трансфицированных олигонуклеотидами в концентрации 25 нМ, измеренными как OD490 в различные временные точки после трансфекции. В качестве контролей применяли мнимо трансфицированные клетки и клетки,трансфицированные SEQ ID NO: 194 (скремблированный контроль scrambled control). Фиг. 5. Экспрессия мРНК бета-катенина в сравнении с контролем, обработанным физиологическим раствором, в печени мышей, измеренная с помощью количественной ПЦР после i.v. обработки нуклеотидом 325 мг/кг. Экспрессия бета-катенина была нормализована по ГАФДГ и результаты были нанесены на график в сравнении с контролем, обработанным физиологическим раствором. Подробное описание изобретения Олигомер. Настоящее изобретение использует олигомерные соединения (обозначаемые в описании как олигомеры) для применения в модулировании функции молекул нуклеиновой кислоты, молекул, кодирующих бета-катенин млекопитающих, например нуклеиновой кислоты бета-катенина, показанной вSEQ ID NO: 173, и встречающихся в природе аллельных вариантов таких молекул нуклеиновой кислоты,кодирующих бета-катенин млекопитающих. Термин "олигомер" в контексте настоящего изобретения относится к молекуле, образованной с помощью ковалентной связи двух или более нуклеиновых оснований (т.е. олигонуклеотид). В описании каждое отдельное нуклеиновое основание также может быть обозначено как мономер или молекула. Олигомер состоит или включает в себя непрерывную последовательность длиной 10-50 нуклеиновых оснований. Олигомер может включать в себя природные нуклеотидные молекулы, например, рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или аналогов нуклеиновой кислоты или их смесей, которые упоминаются в описании, предпочтительно включающих в себя закрытую нуклеиновую кислоту (LNA). Таким образом, термин включает в себя олигомер, состоящий из встречающихся в природе нуклеиновых оснований, сахаров и связей между нуклеиновыми основаниями, а также олигомеры, имеющие нуклеиновые основания, не встречающиеся в природе, которые функционируют сходным образом или имеют специфические улучшенные свойства. Полностью или частично модифицированные или замещенные олигомеры часто являются более предпочтительными по сравнению с нативными формами ввиду нескольких желаемых свойств таких олигомеров, например способности проникать через клеточную мембрану, хорошей устойчивости к вне- и/или внутриклеточным нуклеазам и высокой аффинности и специфичности к нуклеиновой кислоте мишени. LNA-аналог является особенно предпочтительным, например, в отношении упомянутых выше свойств. Таким образом, в особенно предпочтительном воплощении олигомер согласно изобретению создают из молекул нуклеотида и аналога нуклеотида, например молекул LNA или из различных групп молекул аналогов нуклеотидов, чтобы создать олигонуклеотид длиной 10-50, предпочтительно 10-25 нуклеиновых оснований, более предпочтительно 10-16 нуклеиновых оснований и еще более предпочтительно 12-16 нуклеиновых оснований. В различных воплощениях олигомер изобретения не включает в себя РНК (молекулы). Предпочтительно соединение согласно изобретению представляет собой линейную молекулу или синтезируется в виде линейной молекулы. Олигомер представляет собой одноцепочечную молекулу и предпочтительно не содержит коротких участков, например по меньшей мере 3, 4 или 5 непрерывных нуклеиновых основания, которые комплементарны эквивалентным участкам внутри того же самого олигомера (т.е. дуплексы), в этом отношении олигомер (по существу) не является двухцепочечным. В различных воплощениях олигомер в основном не является двухцепочечным, например не является siPHK. Олигомер включает в себя или состоит из непрерывной последовательности нуклеиновых оснований. В различных воплощениях олигомер изобретения может полностью состоять из непрерывного участка нуклеиновых оснований. В различных воплощениях последовательность нуклеиновых оснований олигомера состоит из непрерывной последовательности нуклеиновых оснований. Мишень. Термин "нуклеиновая кислота-мишень", применяемый в описании, относится к ДНК, кодирующей полипептид бета-катенина млекопитающих, например бета-катенин человека, например SEQ ID NO: 173,к нуклеиновым кислотам, кодирующим бета-катенин, или их вариантам, встречающимся в природе, и РНК-нуклеиновым кислотам, происходящим из них, предпочтительно мРНК, например пре-мРНК, хотя предпочтительна зрелая мРНК. В различных воплощениях, например в случае применения в исследовании или в диагностике, "нуклеиновая кислота-мишень" может представлять собой кДНК или синтетический олигонуклеотид, полученный из упомянутой выше ДНК или РНК нуклеиновой кислоты-мишени. Олигомерное соединение согласно изобретению предпочтительно способно к гибридизации с нуклеиновой кислотой-мишенью. Термин "нуклеиновая кислота-мишень" может быть в различных воплощениях, например экзонами генов человека, имеющими номера доступа Х 89579, Х 89593, Х 89592, Х 89591, Х 89588, Х 89585, Х 89584 и Х 89578), или мРНК бета-катенина млекопитающих, например SEQ ID NO: 173. Примеры других мРНК бета-катенина млекопитающих включают в себя без ограничения мРНК, имеющие номера доступаNM 214367 (мРНК бета-катенина свиньи); ВС 119949, ВТ 030683 (мРНК бета-катенина коровы). Следует различать, что упомянутые выше номера доступа относятся к последовательности кДНК, а не к последовательности мРНК непосредственно - последовательность зрелой мРНК может быть получена непосредственно из последовательности кДНК - остатки тимина (Т) должны быть замещены остатками урацила(U). Применяемый в описании термин "гибридизация" обозначает водородное связывание, которое может быть уотсон-криковским, хугстеновским, обратным хугстеновским водородным связыванием и т.д. между комплементарными нуклеотидными/нуклеиновыми основаниями. Уотсон и Крик показали при-3 018986 близительно 50 лет назад, что дезоксирибонуклеиновая кислота (ДНК) состоит из двух цепочек, которые удерживаются вместе в конфигурации спирали водородными связями, образующимися между расположенными напротив друг друга комплементарными нуклеиновыми основаниями из двух цепочек. Четыре нуклеиновых основания, обычно обнаруживаемых в ДНК, представляют собой гуанин (G), аденин (А),тимин (Т) и цитозин (С), из них нуклеиновое основание G образует пару с С, и нуклеиновое основание А образует пару с Т. В РНК нуклеиновое основание тимин замещается нуклеиновым основанием урацил(U), которое аналогично нуклеиновому основанию Т и образует пару с А. Химические группы в нуклеиновых основаниях, которые участвуют в образовании стандартного дуплекса, составляют уотсонкриковскую поверхность. Хугстен показал через два года, что пуриновые нуклеиновые основания (G и А) дополнительно к их уотсон-криковской поверхности имеют хугстеновскую поверхность, которая может быть распознана с внешней стороны дуплекса и использована для связывания пиримидиновых нуклеотидов водородной связью с образованием тройной спиральной структуры. Особенно предпочтительно, что соединения изобретения способны гибридизироваться с нуклеиновой кислотой-мишенью, например мРНК. Соответственно олигомер или конъюгат изобретения способен к ингибированию, например, к подавлению экспрессии гена бета-катенина. В различных воплощениях олигомеры изобретения связываются с нуклеиновой кислотой-мишенью и вызывают ингибирование экспрессии по меньшей мере на 10% или 20% по сравнению с нормальным уровнем экспрессии, более предпочтительно по меньшей мере ингибирование на 30, 40, 50, 60, 70, 80, 90 или 95% по сравнению с нормальным уровнем экспрессии. В некоторых воплощениях указанную модуляцию наблюдают в случае применения 1-25 нМ олигомера или конъюгата изобретения. В том же самом или в другом воплощении ингибирование экспрессии составляет меньше чем 100%, например меньше чем 98% ингибирование, меньше чем 95% ингибирование,меньше чем 90% ингибирование, меньше чем 80% ингибирование, например меньше чем 70% ингибирование. Модуляция уровня экспрессии может быть определена путем измерения уровней белка, например,с помощью методов, таких как SDS-PAGE с последующим вестерн-блоттингом, с примененим соответствующих антител, вызванных против белка-мишени. Альтернативно, модуляция, например ингибирование, уровней экспрессии может быть определена путем измерения мРНК, например, с помощью нозерн-блоттинга или количественной ПЦР-РВ. В случае измерения с помощью уровней мРНК уровень ингибирования или понижающей регуляции при применении соответствующей дозы, например 1-25 нМ,составляет в различных воплощениях обычно 10-20% от нормальных уровней в отсутствие соединения изобретения. Таким образом, изобретение предоставляет способ понижающей регуляции или ингибирования экспрессии белка и/или мРНК бета-катенина в клетке, которая экспрессирует белок и/или мРНК бета-катенина, указанный способ включает в себя введение олигомера или конъюгата согласно изобретению в указанную клетку для понижающей регуляции или ингибирования экспрессии белка и/или мРНК бета-катенина в указанной клетке. Соответственно, клетка представляет собой клетку млекопитающего,например клетку человека. Введение может осуществляться в различных воплощениях in vitro. Введение может осуществляться в различных воплощениях in vivo. Термин "нуклеиновая кислота-мишень", применяемый в описании, относится к ДНК, кодирующей полипептид бета-катенина млекопитающих, например бета-катенина человека, напримерSEQ ID NO: 173, к нуклеиновым кислотам, кодирующим бета-катенин, или их вариантам, встречающимся в природе, и РНК-нуклеиновым кислотам, происходящим из них, предпочтительно мРНК, например пре-мРНК, хотя предпочтительна зрелая мРНК. В различных воплощениях, например в случае применения в исследовании или в диагностике, "нуклеиновая кислота-мишень" может представлять собой кДНК или синтетический олигонуклеотид, полученный из упомянутой выше ДНК или РНК нуклеиновой кислоты-мишени. Олигомерное соединение согласно изобретению предпочтительно способно к гибридизации с нуклеиновой кислотой-мишенью. Термин "их варианты, встречающиеся в природе" относится к вариантам полипептида или последовательности нуклеиновой кислоты бета-катенина, которые встречаются в природе в определенной таксонометрической группе, например млекопитающих, например мышь, обезьяна и предпочтительно человек. Обычно при ссылке на "встречающиеся в природе варианты" полинуклеотида, термин также может охватывать любой аллельный вариант геномной ДНК, кодирующей бета-катенин, который находят в хромосоме Chr 3: 41.22 - 41.26 Mb с помощью хромосомной транслокации или дупликации, и РНК, например, мРНК, получаемая из него. При упоминании "специфической полипептидной последовательности" термин также включает в себя, например, встречающиеся в природе формы белка, которые могут быть процессированы, например, путем ко- или посттрансляционных модификаций, например расщепление сигнального пептида, протеолитическое расщепление, гликозилирование и т.д. Термин "по меньшей мере один" включает в себя целые числа, которые больше или равны 1, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 и т.д. В различных воплощениях, например, если имеют в виду нуклеиновую кислоту или белок - мишени соединения изобретения, термин "по меньшей мере один" включает в себя термины "по меньшей мере два", "по меньшей мере три" и "по меньшей мере четыре", также термин "по меньшей мере два" может включать в себя термины "по меньшей мере три" и "по меньшей мере четыре". Последовательности. Олигомеры изобретения могут иметь своей мишенью мРНК бета-катенина человека, и, например,они включают в себя или состоят из непрерывной последовательности нуклеиновых оснований, которая соответствует нуклеотидной последовательности, представленной в SEQ ID NO: 173, или последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-132, где указанный олигомер (или его часть, состоящая из непрерывных нуклеиновых оснований) может при желании включать в себя одно,два или три несовпадения по сравнению с указанной выбранной последовательностью. В различных воплощениях олигонуклеотидные последовательности состоят из или включают в себя последовательность из 10-16 (непрерывных) нуклеиновых оснований. Примеры олигонуклеотидных последовательностей,включающих в себя 16 нуклеиновых оснований, показаны в SEQ ID NO: 1, 16, 17, 18, 33, 34, 49, 50, 51,52, 53, 54, 55, 56, 57, 58, 73, 88, 103 и 118. Более короткие последовательности могут быть получены на основании представленных последовательностей. Более длинные последовательности могут включать в себя все или по меньшей мере 10 нуклеиновых оснований из соответствующей SEQ ID NO. Таблица 1 Антисмысловые олигонуклеотидные последовательности (мотивы) Изобретение далее предоставляет последовательности-мишени в гене бета-катенина, в частности последовательности, соответствующие (т.е. обратно комплементарные) SEQ ID NO: 1-132, где антисмысловые олигонуклеотиды (олигомеры), соответствующие указанным последовательностям-мишеням,способны к понижающей регуляции бета-катенина. Например, последовательности-мишени, которые соответствуют антисмысловым олигонуклеотидным последовательностям SEQ ID NO: 1, 16, 17, 18, 33,34, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 73, 88, 103 и 118 соответственно, показаны на фиг. 1 (выделены толстым шрифтом и подчеркнуты, с соответствующими олиго SEQ ID NO, показанными выше). Олигомер изобретения, соответственно, может включать в себя или состоять из или быть получен из (например, включать в себя соответствующую непрерывную последовательность нуклеиновых оснований, обнаруживаемую в указанной SEQ ID) последовательности, выбранной из SEQ ID NO: 174-193. Предпочтительно последовательность включает в себя последовательность из 10-16 нуклеиновых оснований. Примеры последовательностей, включающих в себя 16 нуклеиновых оснований, показаны вSEQ ID, выбранной из группы, состоящей из SEQ ID NO: 1, 16, 17, 18, 33, 34, 49, 50, 51, 52, 53, 54, 55, 56,57, 58, 73, 88, 103 и 118. Последовательности, которые имеют меньше нуклеиновых оснований, например 10, 11, 12, 13, 14 или 15, могут, таким образом, иметь непрерывную последовательность нуклеиновых оснований, которая соответствует субпоследовательности, например, по меньшей мере из 8, по меньшей мере из 9, по меньшей мере из 10, по меньшей мере из 11, по меньшей мере из 12, по меньшей мере из 13, по меньшей мере из 14 или 15 непрерывных нуклеиновых оснований, обнаруживаемых вSEQ ID NO: 1, 16, 17, 18, 33, 34, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 73, 88, 103 и 118. Следовательно, более короткие последовательности могут быть получены на основании указанных последовательностей. Более длинные последовательности могут включать в себя все или по меньшей мере 10 нуклеиновых оснований из последовательностей, представленных в качестве примеров SEQ ID NO. Обычно хотя бы часть последовательности олигонуклеотида представлена в SEQ ID, выбранной из SEQ ID NO: 1, 16, 17,18, 33, 34, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 73, 88, 103 и 118, в таком случае оставшаяся часть последовательности олигонуклеотида является гомологичной соответствующим нуклеотидам, фланкирующим указанную SEQ ID: Два вызывающих интерес мотива последовательности представляют собойSEQ ID NO 58 и SEQ ID NO: 103. Также раскрыты конкретные структуры олигомеров изобретения, например олигомеров, показанных в SEQ ID NO: 133-152, в особенности SEQ ID NO: 133, 134, 135, 136, 138, 141, 148, 149, 150, 151 и 152. Также раскрыты конкретные структуры LNA-олигонуклеотидов, например LNA-олигонуклеотидов,показанных в SEQ ID NO: 153-172, в особенности SEQ ID NO: 153, 154, 155, 156, 158, 161, 168, 169, 170,171 и 172. В предпочтительных воплощениях олигомеры изобретения рассматривают как эффективные ингибиторы мРНК и экспрессии белка бета-катенина. В определенных воплощениях олигомер может включать в себя или состоять из непрерывной последовательности нуклеиновых оснований, которые полностью комплементарны (абсолютно комплементарны) эквивалентному участку нуклеиновой кислоты, который кодирует бета-катенин млекопитающих. Однако в некоторых воплощениях олигомер может включать в себя 1, 2, 3 или 4 (или более) несовпадений, и в то же время гибридизоваться с последовательностью-мишенью и по-прежнему адекватно связываться с мишенью и проявлять желаемый эффект, т.е. понижающую регуляцию мишени. Несовпадения могут быть компенсированы, например, с помощью увеличения длины олигомерой последовательности нуклеиновых оснований и/или увеличения числа нуклеотидых аналогов, например LNA, представленных в последовательности нуклеиновых оснований. В различных воплощениях непрерывная последовательность нуклеиновых оснований включает в себя не более чем 3, например не более чем 2 несовпадения с последовательностью-мишенью, например с соответствующим участком нуклеиновой кислоты, который кодирует бета-катенин млекопитающих. В различных воплощениях непрерывная последовательность нуклеиновых оснований включает в себя не более чем одно несовпадение с последовательностью-мишенью, например соответствующий участок нуклеиновой кислоты, который кодирует бета-катенин млекопитающих. Последовательность нуклеиновых оснований олигомеров изобретения или непрерывная последовательность нуклеиновых оснований является предпочтительно по меньшей мере на 80% гомологичной соответствующей последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-132, например по меньшей мере на 85%,по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%,по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%,по меньшей мере на 98%, по меньшей мере на 99% гомологичной, например на 100% гомологичной(идентичной). Последовательность нуклеиновых оснований олигомеров изобретения или непрерывная последовательность нуклеиновых оснований является предпочтительно по меньшей мере на 80% гомологичной соответствующей последовательности, представленной в SEQ ID NO: 173, например по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99%, гомологичной, например на 100% гомологич-9 018986 ной (идентичной). Последовательность нуклеиновых оснований олигомеров изобретения или непрерывная последовательность нуклеиновых оснований является предпочтительно по меньшей мере на 80% комплементарной субпоследовательности, представленной в SEQ ID NO: 173, например по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96% комплементарной, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99%, например на 100% комплементарной (абсолютно комплементарной). В различных воплощениях олигомер (или его часть из непрерывных нуклеиновых оснований) выбран из или включает в себя одну из последовательностей, выбранных из группы, состоящей изSEQ ID NO: 1-132 или SEQ ID NO: 174-193, или субпоследовательность по меньшей мере из 10 непрерывных нуклеиновых оснований из данных последовательностей, где указанный олигомер (или его часть из непрерывных нуклеиновых оснований) может по желанию включать в себя одно, два или три несовпадения по сравнению с указанной выбранной последовательностью. В различных воплощениях субпоследовательность может состоять из 11, 12, 13, 14, 15, 16, 17, 18,19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 непрерывных нуклеиновых оснований, например 10-15, 12-25,12-22, например 12-18 нуклеиновых оснований. Соответственно, в различных воплощениях субпоследовательность имеет такую же длину, как непрерывная последовательность нуклеиновых оснований олигомера изобретения. Однако следует понимать, что в различных воплощениях последовательность нуклеиновых оснований олигомера может включать в себя дополнительные 5'- или 3'-нуклеиновые основания, например независимо 1, 2, 3, 4 или 5 дополнительных нуклеиновых оснований по 5'- и/или по 3'-концу, которые некомплементарны последовательности-мишени. В этом отношении олигомер изобретения может в различных воплощениях включать в себя непрерывную последовательность нуклеиновых оснований, которая фланкирована по 5'- и/или по 3'-концу дополнительными нуклеиновыми основаниями. В различных воплощениях 3'-конец непрерывной последовательности нуклеиновых оснований фланкирован 1, 2 или 3 молекулами ДНК или РНК. При твердофазном синтезе олигомеров часто применяют 3' ДНК молекулы. В различных воплощениях, которые могут быть одними и теми или различными, 5'-конец непрерывной последовательности нуклеиновых оснований фланкирован 1, 2 или 3 молекулами ДНК или РНК. В различных воплощениях дополнительные 5'- или 3'-нуклеиновые основания представляют собой встречающиеся в природе нуклеотиды, например ДНК или РНК. В различных воплощениях дополнительные 5'- или 3'-нуклеиновые основания могут представлять собой участок D, который упоминается в описании в контексте гэпмерных олигомеров (gapmer oligomers). В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 1 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 16 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 17 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 18 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 33 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 34 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 49 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 50 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 51 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 52 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 53 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 54 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 55 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 56 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 57 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 58 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 73 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 88 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 103 или ее субпоследовательность. В различных воплощениях олигомер согласно изобретению состоит или включает в себя последовательность нуклеиновых оснований согласно SEQ ID NO: 118 или ее субпоследовательность. При определении "гомологии" или "комплементарности" между олигомерами изобретения (или непрерывной последовательностью нуклеиновых оснований) и нуклеиновой кислотой, которая кодирует бета-катенин млекопитающих, например последовательности, раскрытые в описании, определение гомологии может быть осуществлено с помощью простого выравнивания соответствующей последовательности нуклеиновых оснований соединения изобретения и соответствующего участка нуклеиновой кислоты,которая кодирует бета-катенин млекопитающих (или нуклеиновой кислоты-мишени), или их комплементарных последовательностей, и гомологию определяют путем подсчета числа оснований, которые выровнены, деления на общее число непрерывных нуклеиновых оснований в соединении (олигомере) изобретения и умножения на 100. При указанном сравнении, если имеются разрывы, предпочтительно, чтобы данные разрывы представляли собой только несовпадения, а не области, где число нуклеиновых оснований внутри разрыва отличается в последовательности нуклеиновых оснований изобретения и в нуклеиновой кислоте-мишени. Аминокислотная и полинуклеотидная гомология может быть определена с помощью алгоритма(белок), или полной ДНК-последовательности нуклеотидных/нуклеиновых оснований. Данные выравнивания также могут быть применены для идентификации участков нуклеиновых кислот, кодирующих бета-катенин человека и различных видов млекопитающих, например обезьяны, мыши и/или крысы, где есть достаточные по протяженности отрезки комплементарности нуклеиновых кислот, для разрешения структуры олигонуклеотидов, которые имеют своей мишенью нуклеиновую кислоту-мишень бетакатенина человека и соответствующие нуклеиновые кислоты, представленные в различных видах млекопитающих, например олигомеры, которые состоят из или включают в себя участки по меньшей мере из 10, например по меньшей мере 12, например по меньшей мере 14, например по меньшей мере 16, например по меньшей мере 18, например из 11, 12, 13, 14, 15, 16, 17 или 18 непрерывных нуклеиновых оснований, которые на 100% комплементарны эквивалентным участкам нуклеиновой кислоты, кодирующей бета-катенин человека, и нуклеиновой кислоты (кислот), кодирующей бета-катенин различных видов млекопитающих. В различных воплощениях олигомер изобретения включает в себя или состоит из непрерывной последовательности нуклеиновых оснований, которая является по меньшей мере на 80%, например по меньшей мере на 85%, например по меньшей мере на 90%, например по меньшей мере на 95%, например по меньшей мере на 98%, например по меньшей мере на 99% или на 100% гомологичной соответствующему участку нуклеиновой кислоты, кодирующей бета-катенин человека, и нуклеиновой кислоты (кислот), кодирующей бета-катенин различных видов млекопитающих, например нуклеиновой кислоты,кодирующей бета-катенин мыши (т.е. на 80-100% комплементарный эквивалентному участку человека и последовательности мыши). Предпочтительно непрерывная последовательность нуклеиновых оснований олигомера является на 100% комплементарной эквивалентному участку мРНК бета-катенина человека. Термины "соответствующий" и "соответствует" относятся к сравнению последовательности нуклеиновых оснований олигомера или непрерывной последовательности нуклеиновых оснований и эквивалентной нуклеотидной последовательности i) обратной комплементарной последовательности нуклеиновой кислоты-мишени, например мРНК, которая кодирует белок бета-катенин, например SEQ ID NO: 173,и/или ii) последовательности нуклеотидов, предоставленных в описании, например группа, состоящая изSEQ ID NO: 1-132 или SEQ ID NO: 174-193. Нуклеотидные аналоги сравнивают непосредственно с их эквивалентом или с соответствующими нуклеотидами. Термины "соответствующий нуклеотидный аналог" и "соответствующий нуклеотид" предназначены для того, чтобы показать, что нуклеиновое основание в нуклеотидном аналоге и встречающийся в природе нуклеотид являются идентичными. Например, если молекула 2-дезоксирибозы нуклеотида связана с аденином, "соответствующий нуклеотидный аналог" содержит молекулу пентозы (отличающуюся от 2-дезоксирибозы), связанную с аденином. Длина. Олигомер включает в себя или состоит из непрерывной последовательности нуклеиновых оснований общей длиной 10-50 нуклеиновых оснований, например 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21,22, 23, 24, 25, 26, 27, 28, 29 или 30 непрерывных нуклеиновых оснований. В различных воплощениях олигомеры включают в себя или состоят из непрерывной последовательности нуклеиновых оснований общей длиной 10-25, 10-24, 12-25, 12-24 или 10-22, например 12-18, например 13-17 или 12-16, например 13, 14, 15, 16 непрерывных нуклеиновых оснований. В различных воплощениях олигомеры включают в себя или состоят из непрерывной последовательности нуклеиновых оснований общей длиной 10, 11, 12,13 или 14 непрерывных нуклеиновых оснований. В различных воплощениях олигомер согласно изобретению состоит не более чем из 22 нуклеиновых оснований, например не более чем 20 нуклеиновых оснований, например не более чем 18 нуклеиновых оснований, например 15, 16 или 17 нуклеиновых оснований. В различных воплощениях олигомер изобретения включает в себя меньше чем 20 нуклеиновых оснований. Нуклеотиды и нуклеотидные аналоги. Термин "нуклеотид", применяемый в описании, относится к гликозиду, включающему в себя сахарную часть, основную часть и ковалентно связанную фосфатную группу, и охватывает встречающиеся в природе нуклеотиды, например ДНК или РНК, предпочтительно ДНК. Не встречающиеся в природе нуклеотиды, содержащие модифицированные сахарные и/или основные части, обозначены в описании как "нуклеотидные аналоги". Термин "нуклеиновое основание" охватывает природные (ДНК- или РНКтипа) нуклеотиды, а также нуклеотидные аналоги. Не встречающиеся в природе нуклеотиды включают в себя нуклеотиды, которые имеют модифицированные сахарные части, например, бициклические нуклеотиды или 2' модифицированные нуклеотиды,например, 2' замещенные нуклеотиды."Нуклеотидные аналоги" представляют собой варианты природных нуклеотидов, например ДНКили РНК-нуклеотидов на основе модификаций в сахарной и/или в основной частях. Аналоги в принципе могут быть просто "молчащими" или "эквивалентными" природным нуклеотидам в контексте олигонуклеотида, т.е. могут не иметь функционального эффекта на путь воздействия олигонуклеотида при ингибировании экспрессии гена-мишени. Указанные "эквивалентные" аналоги тем не менее могут быть полезны, если, например, они являются более простыми или дешевыми в получении, или более стабильными при хранении или при получении, или представляют собой таг или метку. Предпочтительно, однако,аналоги будут обладать функциональным эффектом на путь воздействия олигонуклеотида при ингибировании экспрессии; например, путем создания повышенной аффинности связывания с мишенью и/или повышенной устойчивости к внутриклеточным нуклеазам и/или облегчения транспорта внутрь клетки. Термин "нуклеиновое основание" применяют в качестве общего термина, который охватывает нуклеотиды и нуклеотидные аналоги. Последовательность нуклеиновых оснований представляет собой последовательность, которая включает в себя по меньшей мере два нуклеотида или нуклеотидные аналоги. В различных воплощениях последовательность нуклеиновых оснований может включать в себя только нуклеотиды, например, молекулы ДНК, в альтернативном воплощении последовательность нуклеиновых оснований может включать в себя только нуклеотидные аналоги, например молекулы LNA, или в различных воплощениях последовательность нуклеиновых оснований может включать в себя молекулы нуклеотидов и нуклеотидных аналогов. Термин "нуклеиновая кислота" обозначает молекулу, образованную путем ковалентной связи двух или более нуклеотидов. Термины "нуклеиновая кислота" и "полинуклеотид" применяют в описании взаимозаменяемо. Термин "основная часть" нуклеинового основания охватывает основания встречающихся в природе,а также не встречающихся в природе нуклеиновых оснований. Таким образом, основная часть включает в себя не только известные пуриновые и пиримидиновые гетероциклы, но также гетероциклические аналоги и их таутомеры. Примеры таких основных частей включают в себя без ограничения аденин, гуанин,цитозин, тимидин, урацил, ксантин, гипоксантин, 5-метилцитозин, изоцитозин, псевдоизоцитозин,5-бромурацил, 5-пропинилурацил, 6-аминопурин, 2-аминопурин, инозин, диаминопурин и 2-хлор-6 аминопурин. В различных воплощениях по меньшей мере одно из нуклеиновых оснований, представленных в олигомере, включает в себя модифицированное основание, например, выбранное из группы, состоящей из 5-метилцитозина, изоцитозина, псевдоизоцитозина, 5-бромурацила, 5-пропинилурацила,6-аминопурина, 2-аминопурина, инозина, диаминопурина и 2-хлор-6-аминопурина. Конкретные примеры нуклеозидных/нуклеотидных аналогов описаны, например, FreierAltmann; Таким образом, олигомер может включать в себя или состоять из простой последовательности встречающихся в природе нуклеотидов - предпочтительно 2'-деоксинуклеотидов (обычно обозначаемых в описании как "ДНК"), но также возможны рибонуклеотиды (обычно обозначаемые в описании как"РНК"), или комбинация таких встречающихся в природе нуклеотидов и одного или более не встречающихся в природе нуклеотидов, т.е. нуклеотидных аналогов. Данные нуклеотидные аналоги могут соответственно усиливать аффинность олигомера к последовательности-мишени. Примеры подходящих и предпочтительных нуклеотидных аналогов описаны в WO 2007/031091,которые включены посредством ссылки или упоминаются в описании. Одна предпочтительная модификация нуклеотида включает в себя нуклеотиды, где сахарная часть модифицирована для получения 2'-замещенной группы или для создания соединенной мостиковой связью (закрытая нуклеиновая кислота - LNA) структуры, которая усиливает аффинность связывания и возможно также обеспечивает некоторое возрастание нуклеазной устойчивости; замена обычной фосфодиэфирной внутринуклеотидной связи на связь, более устойчивую к нуклеазной атаке, например, на фосфоротиоатную или боранофосфатную связи - указанные две связи расщепляются РНКазой Н - также делает возможным указанный путь антисмыслового ингибирования при модуляции экспрессии бета-катенина. Включение в олигомер нуклеотидных аналогов, усиливающих аффинность, например LNA или 2'-замещенных сахаров, может обеспечить необходимое уменьшение размера специфически связывающегося олигомера, а также может снизить верхний предел размера олигомера, до того как произойдет неспецифическое или аберрантное связывание. В различных воплощениях олигомер включает в себя по меньшей мере 2 нуклеотидных аналога. В некоторых воплощениях олигомер включает в себя 3-8 нуклеотидных аналога, например 6 или 7 нуклеотидных аналогов. В некоторых предпочтительных воплощениях по меньшей мере один из нуклеотидных аналогов представляет собой закрытую нуклеиновую кислоту (LNA); например, по меньшей мере 3 или по меньшей мере 4, или по меньшей мере 5, или по меньшей мере 6, или по меньшей мере 7, или 8 нуклеотидных аналогов могут быть LNA. В некоторых воплощениях все нуклеотидные аналоги могут бытьLNA. Следует понимать, что при ссылке на мотив предпочтительной нуклеотидной последовательности или на нуклеотидную последовательность, которая состоит только из нуклеотидов, олигомеры изобретения, которые определяют с помощью указанной последовательности, могут включать в себя соответствующий нуклеотидный аналог вместо одного или более нуклеотидов, представленных в указанной по- 13018986 следовательности, например, молекулы LNA или другие нуклеотидные аналоги, которые повышают стабильность дуплекса/Tm для олигомер/дуплекс-мишень (т.е. нуклеотидные аналоги, усиливающие аффинность). В различных воплощениях любые несовпадения между нуклеотидной последовательностью олигомера и последовательностью-мишенью встречаются предпочтительно в участках за пределами нуклеотидных аналогов, усиливающих аффинность (например, участки А и С), например, в участке В, который упоминается в описании, и/или в участке D, который упоминается в описании, и/или в сайте немодифицированных, например, нуклеотидов ДНК в олигонуклеотиде, и/или в участках, которые представляют собой 5'- или 3'-конец непрерывной последовательности нуклеиновых оснований. Примеры указанной модификации нуклеотида включают в себя изменение сахарной части для получения 2'-замещенной группы или для создания соединенной мостиковой связью (закрытая нуклеиновая кислота) структуры, которая усиливает аффинность связывания и также может обеспечивать увеличение устойчивости к нуклеазам. Предпочтительный нуклеотидный аналог представляет собой LNA, например окси-LNA (например,бета-D-окси-LNA и альфа-L-окси-LNA), и/или амино-LNA (например, бета-D-амино-LNA и альфа-L-амино-LNA), и/или тио-LNA (например, бета-D-тио-LNA и альфа-L-тио-LNA), и/или ENA (например, бета-D-ENA и альфа-L-ENA). В различных воплощениях молекулы LNA представляют собой бета-D-окси-LNA. В некоторых воплощениях нуклеотидные аналоги, представленные в олигомере изобретения (например, в участках А и С, упоминаемых в описании), независимо выбраны, например, из молекул 2'-O-алкил-РНК, молекул 2'-амино-ДНК, молекул 2'-фтор-ДНК, молекул LNA, молекул арабинонуклеиновой кислоты (ANA), молекул 2'-фтор-ANA, молекул HNA, молекул INA (интеркалирующая нуклеиновая кислота - Christensen, 2002. Nucl. Acids. Res. 2002, 30: 4918-4925, включено в описание посредством ссылки) и молекул 2'MOE. В различных воплощениях имеется только один из упомянутых выше типов нуклеотидных аналогов, представленных в олигомере изобретения или в его непрерывной последовательности нуклеиновых оснований. В различных воплощениях нуклеотидные аналоги представляют собой 2'-O-метоксиэтил-РНК(2'-MOE), мономеры 2'-фтор-ДНК или LNA-нуклеотидные аналоги, и, как указанный олигонуклеотид изобретения, могут включать в себя нуклеотидные аналоги, которые независимо выбраны из трех аналогов, или могут включать в себя только один тип аналога, выбранный из трех типов. В различных воплощениях по меньшей мере один из указанных нуклеотидных аналогов представляет собой 2'-MOE-РНК,например 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидных молекул 2'-MOE-РНК. В различных воплощениях по меньшей мере один из указанных нуклеотидных аналогов представляет собой 2'-фтор-ДНК, например 2,3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидных молекул 2'-фтор-ДНК. В различных воплощениях олигомер согласно изобретению включает в себя по меньшей мере одну молекулу закрытой нуклеиновой кислоты (LNA), например 1, 2, 3, 4, 5, 6, 7 или 8 молекул LNA, например 3-7 или 4-8 молекул LNA или 3, 4, 5, 6 или 7 молекул LNA. В различных воплощениях все нуклеотидные аналоги представляют собой LNA. В некоторых воплощениях олигомер может включать в себя бета-D-окси-LNA и одну или более из следующих молекул LNA: тио-LNA, амино-LNA, окси-LNA и/илиENA либо в конфигурации бета-D, либо в конфигурации альфа-L, либо в их комбинации. В различных воплощениях все молекулы LNA-цитозина представляют собой 5'метил-цитозин. В различных воплощениях изобретения олигомер может включать в себя молекулы LNA и ДНК. Предпочтительно общее число молекул LNA и ДНК составляет 10-25, предпочтительно 10-20, еще более предпочтительно 12-16. В различных воплощениях изобретения последовательность нуклеиновых оснований олигомера, например непрерывная последовательность, нуклеиновых оснований состоит по меньшей мере из одной LNA и оставшиеся нуклеотидные молекулы представляют собой молекулы ДНК. В различных воплощениях олигомер включает в себя только нуклеотидные аналоги LNA и встречающиеся в природе нуклеотиды(например, РНК или ДНК, наиболее предпочтительно нуклеотиды ДНК), по желанию с модифицированными соединяющими группами, например с фосфоротиоатными группами. В различных воплощениях по меньшей мере одно из нуклеиновых оснований, представленных в олигомере, имеет модифицированное основание, выбранное из группы, состоящей из 5-метилцитозина,изоцитозина, псевдоизоцитозина, 5-бромурацила, 5-пропинилурацила, 6-аминопурина, 2-аминопурина,инозина, диаминопурина и 2-хлор-6-аминопурина.LNA. Термин "LNA" относится к бициклическому нуклеотидному аналогу, известному как "закрытая нуклеиновая кислота". Термин может относиться к мономеру LNA или, в случае применения в контексте"олигонуклеотида LNA" или "олигомера" LNA, может относиться к олигомеру, содержащему один или более таких бициклических нуклеотидных аналогов. Применяемая в олигомерах изобретения LNA предпочтительно имеет структуру с общей формулой I где X выбирают из -O-, -S-, -N(RN)-, -C(R6R6)-; В выбирают из водорода, при желании замещенного С 1-4 алкокси, при желании замещенногоC1-4 алкил, при желании замещенного C1-4 ацилокси, нуклеиновых оснований, интеркаляторов ДНК, фотохимически активных групп, термохимически активных групп, хелатообразующих групп, "репортерных" групп и лигандов; Р обозначает положение радикала для внутринуклеотидной связи с последующим мономером или 5'-концевую группу, такая внутринуклеотидная связь или 5'-концевая группа по желанию включает в себя замещающую группу R5 или в равной степени применимую замещающую группу R5; Р обозначает внутринуклеотидную связь с предыдущим мономером или 3'-концевую группу;-С(R )=C(Rb)-, -C(Ra)=N-, -O-, -Si(Ra)2-, -S-, -SO2-, -N(Ra)- и C=Z,где Z выбран из -O-, -S- и -N(Ra)- и Ra и Rb, каждый независимо, выбраны из водорода, по желанию замещенного на С 1-12 алкил, по желанию замещенного на С 2-12 алкенил, по желанию замещенного на С 2-12 алкинил,гидрокси,C1-12 алкокси,С 2-12 алкоксиалкил,С 2-12 алкенилокси,карбокси,C1-12 алкоксикарбонил, C1-12 алкилкарбонил, формил, арил, арилоксикарбонил, арилокси, арилкарбонил,гетероарил, гетероарилоксикарбонил, гетероарилокси, гетероарилкарбонил, амино, моно- и ди(С 1-6 алкил)амино, карбамоил, моно- и ди(C1-6 алкил)аминокарбонил, амино-С 1-6 алкиламинокарбонил,монои ди(C1-6 алкил)амино-С 1-6 алкиламинокарбонил,C1-6 алкилкарбониламино,карбамидо,C1-6 алканоилокси, сульфоно, C1-6 алкилсульфонилокси, нитро, азидо, сульфанил, C1-6 алкилтио, галоген,интеркаляторы ДНК, фотохимически активные группы, термохимически активные группы, хелатирующие группы, "репортерные" группы и лиганды, где арил и гетероарил могут быть по желанию замещены и где два геминальных заместителя Ra и Rb вместе могут обозначать по желанию замещенный метилен(=CH2); и каждый из заместителей R1, R2, R3, R5, R5, R6 и R6, которые представлены, выбран независимо из водорода, по желанию замещенного на C1-12 алкил, по желанию замещенного на С 2-12 алкенил, по желанию замещенного на С 2-12 алкинил, гидрокси, C1-12 алкокси, С 2-12 алкоксиалкил, С 2-12 алкенилокси, карбокси,С 1-12 алкоксикарбонил, C1-12 алкилкарбонил, формил, арил, арилоксикарбонил, арилокси, арилкарбонил,гетероарил, гетероарилоксикарбонил, гетероарилокси, гетероарилкарбонил, амино, моно- и ди(C1-6 алкил)амино, карбамоил, моно- и ди(С 1-6 алкил)аминокарбонил, амино-С 1-6 алкиламинокарбонил,монои ди(С 1-6 алкил)амино-С 1-6 алкиламинокарбонил,C1-6 алкилкарбониламино,карбамидо,C1-6 алканоилокси, сульфоно, C1-6 алкилсульфонилокси, нитро, азидо, сульфанил, C1-6 алкилтио, галоген,интеркаляторы ДНК, фотохимически активные группы, термохимически активные группы, хелатирующие группы, "репортерные" группы и лиганды, где арил и гетероарил могут быть по желанию замещены и где два геминальных заместителя вместе могут обозначать оксо, тиоксо, имино или по желанию замещенный метилен или вместе могут образовывать спиробирадикал, состоящий из алкиленовой цепи из 1-5 атомов углерода, которая по желанию прерывается и/или заканчивается одним или более гетероатомами/группами, выбранными из -O-, -S- и -(NRN)-, где RN выбран из водорода и C1-4 алкила и где два соседних (негименальных) заместителя могут обозначать дополнительную связь, давая в результате двойную связь; и RN в тех случаях, когда представлен и не вовлечен в бирадикал, выбран из водорода иC1-4 алкила и их основных солей и кислых солей добавления. В различных воплощениях R5 выбран из H, -CH3, -CH2-CH3,-CH2-O-CH3 и -CH=CH2. В различных воплощениях R4 и R2 вместе обозначают бирадикал, выбранный из -С(RaRb)-О,a b-С(R R )-С(RcRd)-О, -С(RaRb)-C(RcRd)-С(ReRf)-О, -C(RaRb)-O-C(RcRd)-, -С(RaRb)-O-C(RcRd)-О, -С(RaRb)С(RcRd)-, -С(RaRb)-С(RcRd)-С(ReRf)-, -С(Ra)=C(Rb)-С(RcRd)-, -С(RaRb)-N(Rc)-, -С(RaRb)-С(RcRd)-N(Rc)-,-С(RaRb)-N(Rc)-O и -C(RaRb)-S-, -С(RaRb)-C(RcRd)-S-, где Ra, Rb, Rc, Rd, Re и Rf, каждый независимо, выбраны из водорода, по желанию замещенного на C1-12 алкил, по желанию замещенного на С 2-12 алкенил, по желанию замещенного на С 2-12 алкинил, гидрокси, C1-12 алкокси, C2-12 алкоксиалкил, С 2-12 алкенилокси, карбокси, С 1-12 алкоксикарбонил, С 1-12 алкилкарбонил, формил, арил, арилоксикарбонил, арилокси, арилкарбонил, гетероарил, гетероарилоксикарбонил, гетероарилокси, гетероарилкарбонил, амино, моно- и ди(С 1-6 алкил)амино, карбамоил, моно- и ди(C1-6 алкил)аминокарбонил, амино-С 1-6 алкиламинокарбонил,монои ди(C1-6 алкил)амино-С 1-6 алкиламинокарбонил,C1-6 алкилкарбониламино,карбамидо,C1-6 алканоилокси, сульфоно, C1-6 алкилсульфонилокси, нитро, азидо, сульфанил, C1-6 алкилтио, галоген,ДНК интеркаляторы, фотохимически активные группы, термохимически активные группы, хелатирующие группы, "репортерные" группы и лиганды, где арил и гетероарил могут быть по желанию замещены и где два геминальных заместителя Ra и Rb вместе могут обозначать по желанию замещенный метилен- 15018986 В другом воплощении R4 и R2 вместе обозначают бирадикал, выбранный из -CH2-O-, -CH2-S-,-CH2-NH-, -CH2-N(CH3)-, -CH2-CH2-O-, -CH2-CH(CH3)-, -CH2-CH2-S-, -CH2-CH2-NH-, -CH2-CH2-CH2-,-CH2-CH2-CH2-O-, -CH2-CH2-CH(CH3)-, -CH=CH-CH2-, -CH2-O-CH2-O-, -CH2-NH-O-, -CH2-N(CH3)-O-,-CH2-O-CH2-, -CH(CH3)-O-, -CH(CH2-O-CH3)-O-. Для всех хиральных центров асимметричные группы могут быть обнаружены либо в R, либо в S ориентации. Предпочтительно LNA, используемый в олигомере изобретения, включает в себя по меньшей мере одну молекулу LNA согласно любой из формулZ и Z независимо выбраны из межнуклеотидой связи, концевой группы или защитной группы; В представляет собой часть молекулы, которая соответствует встречающемуся или не встречающемуся в природе нуклеотидному основанию; иRH выбран из водорода и С 1-4 алкила. Особенно предпочтительные молекулы LNA показаны на схеме 2. Схема 2 Термин "тио-LNA" включает в себя закрытое нуклеиновое основание (LNA), в котором Y в общей формуле, представленной выше, выбран из S или -CH2-S-. Тио-LNA может быть представлен как в бетаD, так и в альфа-L конфигурации. Термин "амино-LNA" включает в себя закрытые нуклеиновые основания (LNA), в которых Y в общей формуле, представленной выше, выбран из -N(H)-, N(R)-, CH2-N(H)- и -CH2-N(R)-, где R выбран из водорода и C1-4 алкила. Амино-LNA может быть представлен как в бета-D, так и в альфа-L конфигурации. Термин "окси-LNA" включает в себя закрытое нуклеиновое основание (LNA), в котором Y в общей формуле, представленной выше, представляет собой -O- или -CH2-O-. Окси-LNA может быть представлен как в бета-D, так и в альфа-L конфигурации. Термин "ENA" включает в себя закрытое нуклеиновое основание (LNA), в котором Y в общей формуле, представленной выше, представляет собой -CH2-O- (где атом кислорода -CH2-O- присоединяется в 2'-положение относительно основания В). В предпочтительном воплощении LNA выбран из бета-D-окси-LNA, альфа-L-окси-LNA, бета-Dамино-LNA и бета-D-тио-LNA, в особенности бета-D-окси-LNA. В контексте настоящего описания термин "С 1-4 алкил" обозначает линейную или разветвленную насыщенную углеводную цепь, где цепь содержит от одного до четырех атомов углерода, например метил,этил, н-пропил, изопропил, н-бутил, изобутил, сек-бутил и трет-бутил. Распознавание РНКазой Н. Очевидно, что олигомерное соединение может действовать через неопосредуемую РНКазой деградацию мишени мРНК, например, путем стерической блокировки трансляции или другими способами,однако предпочтительные олигомеры изобретения способны распознаваться эндорибонуклеазами(РНКазами), например РНКазой Н. В различных воплощениях указанный олигомер или непрерывная последовательность нуклеиновых оснований включает в себя участок по меньшей мере из 6, например по меньшей мере из 7 последовательных нуклеотидов или молекул нуклеиновых оснований, например по меньшей мере 8 или по меньшей мере 9 последовательных молекул нуклеиновых оснований (остатков), включая 7, 8, 9, 10, 11, 12, 13,14, 15 или 16 последовательных нуклеотидов или нуклеиновых оснований, который при формировании дуплекса с комплементарной мишенью РНК способен распознаваться РНКазой. Непрерывная последовательность, способная распознаваться РНКазой, может представлять собой участок В, упоминаемый в контексте гэпмера, который описан в настоящем документе. В различных воплощениях размер непрерывной последовательности, которая способна распознаваться РНКазой, например участок В, может быть больше, например, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 молекул нуклеиновых оснований. Европейская патентная заявка ЕР 1222309 предоставляет методы определения активности РНКзы Нin vitro, которые могут быть применены для определения способности распознаваться РНКазой Н. Олигомер считают способным распознаваться РНКазой Н, если при наличии комплементарной РНК-мишени начальная скорость РНКазы Н, измеренная в пмоль/л/мин, составляет по меньшей мере 1%, например по меньшей мере 5%, например по меньшей мере 10% или меньше чем 20% от скорости, определяемой с применением эквивалентного только ДНК-олигонуклеотида, не имеющего замен в 2'-положении, с фосфоротиоатными соединяющими группами между всеми нуклеотидами в олигонуклеотиде, с применением методологии, предоставленной в примере 91-95 в ЕР 1222309. В различных воплощениях олигомер считают, по существу, неспособным к распознаванию РНКазой Н, если при наличии комплементарной мишени РНК, начальная скорость РНКазы Н, измеренная в пмоль/л/мин, составляет меньше 1%, например меньше 5%, например меньше 10 или меньше 20% от скорости, определяемой с применением эквивалентного только ДНК олигонуклеотида, не имеющего замен в 2'-положении, с фосфоротиоатными соединяющими группами между всеми нуклеотидами в олигонуклеотиде, с применением методологии, предоставленной в примере 91-95 в ЕР 1222309. В других воплощениях олигомер считают способным распознаваться РНКазой Н, если при наличии комплементарной мишени РНК и РНКазы Н, начальная скорость РНКазы Н, измеренная в пмоль/л/мин,составляет по меньшей мере 20%, например по меньшей мере 40%, например по меньшей мере 60%, например по меньшей мере 80% от начальной скорости, определяемой с эквивалентным только ДНКолигонуклеотидом (т.е. имеющим такую же последовательность оснований, но содержащим только молекулы ДНК), без замен в 2'-положении, с фосфоротиоатными соединяющими группами между всеми нуклеотидами в олигонуклеотиде, с применением методологии, предоставленной в примере 91-95 в ЕР 1222309. Обычно участок олигомера, который образует непрерывную последовательность нуклеиновых оснований, при образовании дуплекса с комплементарной мишенью РНК, способный распознаваться РНКазой, состоит из нуклеотидных молекул, которые образуют ДНК/РНК-подобный дуплекс с мишенью РНК и могут включать в себя молекулы ДНК и молекулы LNA, которые находятся в альфа-L конфигурации, особенно предпочтительной является альфа-L-окси LNA. Олигомер изобретения может включать в себя последовательность нуклеиновых оснований, которая содержит нуклеотиды и нуклеотидные аналоги, и может быть в форме гепмэра (a gapmer), хедмера(a headmer) или миксмера (a mixmer). Хедмером называют непрерывную последовательность аналогов нуклеотидов на 5'-конце, которые не распознаются РНКазой, за которыми в направлении к 3'-концу следует непрерывная последовательность молекул ДНК или модифицированных нуклеотидов (аналогов), распознаваемых и расщепляемых РНКазой (например, по меньшей мере 7 таких нуклеотидов), и тейлмером называют непрерывную последовательность ДНК или модифицированных нуклеотидов (аналогов), распознаваемых и расщепляемых РНКазой на 5'-конце (например, по меньшей мере 7 таких нуклеотидов), за которыми следует в направлении к 3'-концу непрерывная последовательность нераспозноваемых РНКазой нуклеотидных аналогов. Другие "химерные" олигомеры, называемые в изобретении "миксмерами" состоят из сочетания чередующихся i) ДНК или модифицированных нуклеотидов, распознаваемых и расщепляемых РНКазой,и ii) аналогов нуклеотидов, не распознаваемых РНКазой. Кроме того, некоторые аналоги нуклеотидов могут опосредовать связывание и расщепление РНКазы, такой как РНКаза Н. Поскольку активность РНКазы вызывается определенным участком -L-LNA, для конструкции гэпмера могут потребоваться небольшие участки (например, гэпы - или участок В) ДНК или модифицированных нуклеотидов, распознаваемых и расщепляемых РНКазой, и в конструкцию миксмера может быть внесена большая гибкость. Структура гэпмера. Предпочтительно олигомер изобретения представляет собой гэпмер. Гэпмерный олигомер представляет собой олигомер, который включает в себя непрерывный участок нуклеотидов или нуклеиновых оснований, распознаваемый РНКазой, например РНКазой Н, например участок по меньшей мере из 6 или 7 ДНК-нуклеотидов, называемый в описании участок В, где участок В фланкирован по 5'- и 3'-концам участками нуклеотидных аналогов, например нуклеотидных аналогов, усиливающих аффинность, например 1-6 нуклеотидных аналогов по 5'- и 3'-концам непрерывного участка нуклеотидов, который рас- 17018986 познается РНКазой, указанные участки обозначают как участки А и С соответственно. Предпочтительно гэпмер включает в себя (поли)нуклеотидную последовательность формулы (от 5' к 3'), А-В-С, или по желанию A-B-C-D или D-A-B-C, где участок А (5'-участок) состоит или включает в себя по меньшей мере один нуклеотидный аналог, например по меньшей мере одну молекулу LNA, например 1-6 нуклеотидных аналогов, например молекул LNA, и участок В состоит или включает в себя по меньшей мере пять последовательных нуклеотидов или нуклеиновых оснований, способных распознаваться РНКазой (при образовании дуплекса с комплементарной молекулой РНК, например мРНКмишень), например ДНК-нуклеотиды, и участок С (3'-участок) состоит или включает в себя по меньшей мере один нуклеотидный аналог, например по меньшей мере одну молекулу LNA, например 1-6 нуклеотидных аналогов, например молекул LNA, и участок D, если представлен, состоит или включает в себя 1,2 или 3 нуклеотидные молекулы, например, ДНК-нуклеотиды. В различных воплощениях участок А состоит из 1, 2, 3, 4, 5 или 6 нуклеотидных аналогов, например молекул LNA, например 2-5 нуклеотидных аналога, например 2-5 молекулы LNA, например 3 или 4 нуклеотидных аналога, например 3 или 4 молекулы LNA; и/или участок С состоит из 1, 2, 3, 4, 5 или 6 нуклеотидных аналогов, например молекул LNA, например 2-5 нуклеотидных аналога, например 2-5 молекулы LNA, например 3 или 4 нуклеотидных аналога, например 3 или 4 молекулы LNA. В различных воплощениях В состоит или включает в себя 5, 6, 7, 8, 9, 10, 11 или 12 последовательных нуклеотидов или нуклеиновых оснований, которые способны распознаваться РНКазой, или 6-10,или 7-9, например 8 последовательных нуклеотидов или нуклеиновых оснований, которые способны распознаваться РНКазой. В различных воплощениях участок В состоит или включает в себя по меньшей мере одну молекулу ДНК-нуклеотида, например 1-12 молекул ДНК, предпочтительно 4-12 молекул ДНК,более предпочтительно 6-10 молекул ДНК, например 7-10 молекул ДНК, наиболее предпочтительно 8, 9 или 10 молекул ДНК. В различных воплощениях участок А состоит из 3 или 4 нуклеотидных аналогов, например LNA,участок В состоит из 7, 8, 9 или 10 молекул ДНК и участок С состоит из 3 или 4 нуклеотидных аналогов,например LNA. Такие структуры включают в себя (А-В-С) 3-10-3, 3-10-4, 4-10-3, 3-9-3, 3-9-4, 4-9-3, 3-83, 3-8-4, 4-8-3, 3-7-3, 3-7-4, 4-7-3 и далее могут включать в себя участок D, который может иметь одну или 2 нуклеотидных молекулы, например молекулы ДНК. Другие структуры гэпмера раскрыты в WO 2004/046160, и они включены в описание посредством ссылки. Предварительная заявка США 60/977409, включенная в описание посредством ссылки, имеет отношение к "коротким" гэпмерным олигомерам, которые в различных воплощениях могут быть гэпмерным олигомером согласно настоящему изобретению. В различных воплощениях олигомер состоит из непрерывной последовательности нуклеиновых оснований общей длиной 10, 11, 12, 13 или 14 молекул нуклеиновых оснований, где непрерывная последовательность нуклеиновых оснований представляет собой по формуле (5'-3'), А-В-С, или по желанию A-BC-D или D-A-B-C, где А состоит из 1, 2 или 3 молекул нуклеотидных аналогов, например молекул LNA; В состоит из 7, 8 или 9 непрерывных молекул нуклеотидов или нуклеиновых оснований, которые способны распознаваться РНКазой при образовании дуплекса с комплементарной молекулой РНК (например, мишень мРНК); и С состоит из 1, 2 или 3 молекул нуклеотидных аналогов, например молекул LNA. Если представлен, участок D состоит из одной молекулы ДНК. В различных воплощениях А состоит из 1 молекулы LNA. В различных воплощениях А состоит из 2 молекул LNA. В различных воплощениях А состоит из 3 молекул LNA. В различных воплощениях С состоит из 1 молекулы LNA. В различных воплощениях С состоит из 2 молекул LNA. В различных воплощениях С состоит из 3 молекул LNA. В различных воплощениях В состоит из 7 нуклеотидных молекул. В различных воплощениях В состоит из 8 нуклеотидных молекул. В различных воплощениях В состоит из 9 нуклеотидных молекул. В различных воплощениях участок В включает в себя 1-9 молекул ДНК, например 2, 3, 4, 5, 6, 7 или 8 молекул ДНК. В различных воплощениях участок В состоит из молекул ДНК. В различных воплощениях участок В включает в себя по меньшей мере одну молекулу LNA,которая имеет альфа-L-конфигурацию, например 2, 3, 4, 5, 6, 7, 8 или 9 молекул LNA в альфа-Lконфигурации. В различных воплощениях В включает в себя по меньшей мере одну молекулу альфа-Lокси-LNA или где все молекулы LNA в альфа-L-конфигурации представляют собой альфа-L-окси-LNAмолекулы. В различных воплощениях число нуклеотидов, представленных в А-В-С, выбирают из группы, состоящей из (молекул нуклеотидных аналогов - участок В - молекул нуклеотидных аналогов): 1-8-1,1-8-2, 2-8-1, 2-8-2, 3-8-3, 2-8-3, 3-8-2, 4-8-1, 4-8-2, 1-8-4, 2-8-4, или 1-9-1, 1-9-2, 2-9-1, 2-9-2, 2-9-3, 3-9-2, 19-3, 3-9-1, 4-9-1, 1-9-4, или 1-10-1, 1-10-2, 2-10-1, 2-10-2, 1-10-3, 3-10-1. В различных воплощениях число нуклеотидов в А-В-С выбрано из группы, состоящей из: 2-7-1, 1-7-2, 2-7-2, 3-7-3, 2-7-3, 3-7-2, 3-7-4 и 4-73. В различных воплощениях участки А и С состоят из двух молекул LNA, каждый, и участок В состоит из 8 или 9 нуклеотидных молекул, предпочтительно молекул ДНК. Другие структуры гэпмеров включают в себя структуры, где участок А и/или С состоит из 3, 4, 5 или 6 нуклеотидных аналогов, например нуклеотидных аналогов, выбранных из группы, состоящей из 2'O-метоксиэтил-РНК (2'MOE) и 2'-фтор-ДНК мономеров, и участок В состоит из 8, 9, 10, 11 или 12 нуклеотидов, например молекул ДНК (или нуклеиновых оснований), например 5-10-5 и 4-12-4 гэпмерные структуры. Другие структуры гэпмеров раскрыты в международном патенте WO 2007/146511A2, который включен в описание посредством ссылки. Соединяющие группы. Термины "соединяющая группа" или "межнуклеотидная связь" обозначают группу, способную ковалентно соединить вместе два нуклеотида или нуклеиновых основания, два нуклеотидных аналога, и нуклеотид и нуклеотидный аналог и т.д. Специфические и предпочтительные примеры включают в себя фосфатные группы и фосфоротиоатные группы. Нуклеиновые основания олигомера изобретения или его непрерывная последовательность нуклеиновых оснований соединены посредством соединяющих групп. Соответственно каждое нуклеиновое основание соединяется с соседним 3'-нуклеиновым основанием через соединяющую группу. Соответствующие соединяющие группы включают в себя группы, которые перечислены в международном патенте WO 2007/031091, например соединяющие группы, перечисленные в первом параграфе на странице 34 международного патента WO 2007/031091 (который включен в описание посредством ссылки). В различных воплощениях предпочтительно заменить обычную фосфодиэфирную связывающую группу на группу, более устойчивую к нуклеазной атаке, например на фосфоротиоатную или боранофосфатную группы, указанные две связи расщепляются РНКазой Н, а также обеспечивают указанный путь антисмыслового ингибирования для уменьшения экспрессии гена-мишени. Соответствующие серосодержащие соединяющие группы (S), содержащие группы связывания,предоставляемые в настоящем документе, могут быть предпочтительными. Фосфоротиоатные соединяющие группы также являются предпочтительными, особенно в гэпмерном участке (В) гэпмеров. Фосфоротиоатные связи также могут быть применены во фланкирующих участках (А и С, и для связывания А или С с D, и внутри участка D в соответствующих случаях). Участки А, В и С могут, однако, включать в себя соединяющие группы, другие чем фосфоротиоат,например фосфодиэфирные соединяющие группы, особенно если, например, применение нуклеотидных аналогов защищает соединяющие группы внутри участков А и С от эндонуклеазной деградации, например, если участки А и С содержат нуклеотиды LNA. Соединяющие группы в олигомере могут представлять собой фосфодиэфиры, фосфоротиоат или боранофосфат при условии, что возможно расщепление РНКазой Н РНК-мишени. Фосфоротиоат является предпочтительным ввиду увеличения нуклеазной устойчивости и по другим причинам, например простоте получения. В одном аспекте олигомера изобретения нуклеотиды и/или нуклеотидные аналоги соединяются друг с другом посредством фосфоротиоатных групп. Следует понимать, что включение фосфодиэфирных связей, например одной или двух связей, в другой фосфоротиоатный олигомер, особенно между или рядом с молекулами нуклеотидных аналогов(обычно в участок А и/или С) может изменить биодоступность и/или биораспределение олигомера, см.WO 2008/053314, включенный в описание посредством ссылки. В некоторых воплощениях, например в воплощениях, упоминаемых выше, где это применимо и специально не указано, все остальные соединяющие группы представляют собой либо фосфодиэфир,либо фосфоротиоат, либо их смесь. В некоторых воплощениях все группы межнуклеотидной связи представляют собой фосфоротиоат. При упоминании специфических гэпмерных олигонуклеотидных последовательностей, например последовательностей, предоставляемых в описании, следует понимать, что в различных воплощениях,если связи представляют собой фосфоротиоатные связи, то могут быть применены альтернативные связи, например связи, раскрытые в описании, например фосфатные (фосфодиэфирные) связи, особенно для связей между нуклеотидными аналогами, например молекулами LNA. Аналогично при упоминании специфических гэпмерных олигонуклеотидных последовательностей, например последовательностей, предоставляемых в описании, если С-остатки помечены, как 5'метил-модифицированный цитозин, то в различных воплощениях, один или более С, представленные в олигомере, могут представлять собой немодифицированные С-остатки. Олигомерные соединения. Олигомеры изобретения могут быть выбраны из группы, состоящей из SEQ ID NO: 133-152, которые показаны в табл. 2. В табл. 2 приведены структуры олигомеров SEQ ID NO: 133-152, заглавные буквы обозначают молекулы нуклеотидных аналогов и подстрочная буква "s" означает фосфоротиоатную связь. Строчные буквы представляют собой нуклеотидные (ДНК) молекулы. Отсутствие "s" (если имеется) обозначает фосфодиэфирную связь. Конъюгаты. В настоящем контексте термин "конъюгат" обозначает гетерогенную молекулу, образованную путем ковалентного соединения ("конъюгации") олигомера, который описан в настоящем документе, с одним или более ненуклеотидом/ненуклеотидным аналогом (т.е. ненуклеиновое основание), или неполинуклеотидные молекулы. Примеры ненуклеотидных или неполинуклеотидных молекул включают в себя макромолекулярные агенты, например белки, цепи жирных кислот, остатки сахаров, гликопротеины,полимеры или их комбинации. Обычно белки могут представлять собой антитела к белку-мишени. Типичные полимеры могут представлять собой полиэтиленгликоль. Таким образом, в различных воплощениях олигомер изобретения может включать в себя полинуклеотидный участок, т.е. участок из нуклеотидов/нуклеиновых оснований, который обычно состоит из непрерывной последовательности нуклеиновых оснований, и другой ненуклеотидный участок. При ссылке на олигомер изобретения, состоящий из непрерывной последовательности нуклеиновых оснований, соединение может включать в себя компоненты, не являющиеся нуклеотидами/нуклеиновыми основаниями, например конъюгатный компонент. В различных воплощениях изобретения олигомерное соединение соединено с лигандами/конъюгатами, которые могут быть применены, например, для увеличения клеточного захвата олигомерных соединений. Международный патент WO 2007/031091 предоставляет соответствующие лиганды и конъюгаты, которые включены в описание посредством ссылки. Изобретение также предоставляет конъюгат, включающий в себя соединение согласно изобретению, которое описано в настоящем документе, и по меньшей мере одну ненуклеотидную или неполинуклеотидную молекулу, ковалентно присоединенную к указанному соединению. Таким образом, в различных воплощениях, где соединение изобретения состоит из заданной нуклеиновой кислоты или последовательности нуклеиновых оснований, которая раскрыта в описании, соединение также может включать в себя по меньшей мере одну ненуклеотидную или неполинуклеотидную молекулу (например, не содержащую один или более нуклеотидов или нуклеотидных аналогов), ковалентно присоединенную к ука- 20018986 занному соединению. Конъюгаты могут увеличивать активность, клеточное распределение или клеточный захват олигомера изобретения. Указанные молекулы включают в себя без ограничения антитела, полипептиды, молекулы липидов, например молекулу холестерина, холевую кислоту, простой тиоэфир, например гексил-sтритилтиол, тиохолестерин, алифатическую цепь, например додекантиол или ундециловые остатки,фосфолипиды, например дигексадецил-рац-глицерин или триэтиламмоний 1,2-ди-о-гексадецил-рацглицеро-В-h-фосфонат, полиамин или полиэтиленгликолевая цепь, адамантануксусная кислота, пальмитиловый фрагмент, октадециламин, или молекулу гексиламинокарбонилоксихолестерина. Олигомеры изобретения также могут быть конъюгированы с активными лекарственными субстанциями, например с аспирином, ибопруфеном сульфамидным препаратом, противодиабетическим, антибактериальным препаратом или с антибиотиком. В определенных воплощениях конъюгированная часть представляет собой стирол, например холестерин. В различных воплощениях конъюгированная часть включает в себя или состоит из положительно заряженного полимера, например из положительно заряженных пептидов длиной, например, 1-50, например 2-20, например 3-10 аминокислотных остатков и/или полиалкиленоксида, например полиэтиленгликоля (PEG) или полипропиленгликоля, см. международный патент WO 2008/034123, который включен в описание посредством ссылки. Соответственно, положительно заряженный полимер, например полиалкиленоксид, может быть присоединен к олигомеру изобретения через линкер, например отделяемый линкер, описание которого приведено в международном патенте WO 2008/034123. Активированные олигомеры. Термин "активированный олигомер", применяемый в описании, относится к олигомеру изобретения, который ковалентно связан (т.е. функционализирован) по меньшей мере с одной функциональной молекулой, которая обеспечивает ковалентное связывание олигомера с одной или более конъюгированными молекулами, т.е. молекулами, которые не являются нуклеиновыми кислотами или мономерами, для формирования конъюгатов, описываемых в настоящем документе. Обычно функциональная молекула включает в себя химическую группу, которая способна к ковалентному связыванию с олигомером, например, через 3'-гидроксильную группу или экзоциклическую NH2-группу аденинового основания, спейсер, который предпочтительно представляет собой гидрофильную и терминальную группу, которая способна к связыванию с конъюгированной молекулой (например, амино, сульфгидрильная или гидроксильная группа). В некоторых воплощениях указанная терминальная группа не защищена и, например,является NH2-группой. В других воплощениях терминальная группа защищена, например, любой подходящей защитной группой, например, группами, описанными в "Protective Gpoups in Organic Synthesis".Theodora W. Greene and Peter G.M. Wuts, 3rd edition (John WileySons, 1999). Примеры подходящих гидроксильных защитных групп включают в себя сложные эфиры, например эфир уксусной кислоты, аралкильные группы, например бензил, дифенилметил или трифенилметил и тетрагидропиранил. Примеры подходящих аминопротективных групп включают в себя бензил, альфа-метилбензил, дифенилметил,трифенилметил, бензилоксикарбонил, трет-бутоксикарбонил и ацильные группы, например трихлорацетил или трифторацетил. В некоторых воплощениях функциональная молекула является саморазрушаемой. В других воплощениях функциональная молекула является биодеградируемой. См., например, патент США 7087229, который во всей полноте включен посредством ссылки в настоящее описание. В некоторых воплощениях олигомеры изобретения функционализированы по 5'-концу, чтобы сделать возможным ковалентное присоединение конъюгированной молекулы к 5'-концу олигомера. В других воплощениях олигомеры изобретения могут быть функционализированы по 3'-концу. В других воплощениях олигомеры изобретения могут быть функционализированы по скелету молекулы или по гетероциклическому основанию молекулы. В других воплощениях олигомеры изобретения могут быть функционализированы по более чем одному положению, независимо выбранному из 5'-конца, 3'-конца, скелета молекулы и основания. В некоторых воплощениях активированные олигомеры изобретения синтезируют путем введения в состав во время синтеза одного или более мономеров, которые ковалентно присоединяют к функциональной молекуле. В других воплощениях активированные олигомеры изобретения синтезируют с мономерами, которые не были функционализированы, и олигомер функционализируют после завершения синтеза. В некоторых воплощениях олигомеры функционализируют связанным сложным эфиром, содержащим аминоалкильный линкер, где алкильная часть имеет формулу (CH2)w, где w представляет собой целое число в пределах от 1 до 10, предпочтительно 6, где алкильная часть алкиламиногруппы может быть неразветвленной цепью или разветвленной цепью, и где функциональная группа присоединена к олигомеру посредством сложноэфирной группы (-O-C(O)-(CH2)wNH). В других воплощениях олигомеры функционализируют связанным сложным эфиром, содержащим(CH2)w-сульфгидрильный (SH) линкер, где w представляет собой целое число в пределах от 1 до 10,предпочтительно 6, где алкильная часть алкиламиногруппы может быть неразветвленной цепью или разветвленной цепью, и где функциональная группа присоединена к олигомеру посредством сложноэфирной группы (-O-C(O)-(CH2)wSH). В некоторых воплощениях сульфгидрилактивированные олигонуклеотиды конъюгируют с полимерными молекулами, например полиэтиленгликолем или пептидами (путем образования дисульфидной связи). Активированные олигомеры, содержащие связанные сложные эфиры, которые описаны выше, могут быть синтезированы любым способом, известным в данной области техники, и в частности способами, раскрытыми в публикации РСТWO 2008/034122 и примеров в нем, которые во всей полноте включены в настоящее описание посредством ссылки. В других воплощениях олигомеры изобретения функционализируют путем введения сульфгидрильной, амино или гидроксильной группы в олигомер посредством функционализирующего реагента,главным образом, как описано в патентах США 4962029 и 4914210, т.е., по существу, неразветвленный реагент, имеющий фосфорамидит на одном конце, связанный через цепочку гидрофильного спейсера с противоположным концом, который включает в себя защищенную или незащищенную сульфгидрильную, амино или гидроксильную группу. Такие реагенты, прежде всего, реагируют с гидроксильными группами олигомера. В некоторых воплощениях такие активированные олигомеры имеют функционализирующий реагент, соединенный с 5'-гидроксильной группой олигомера. В других воплощениях активированные олигомеры имеют функционализирующий реагент, соединенный с 3'-гидроксильной группой. В других воплощениях активированные олигомеры изобретения имеют функционализирующий реагент, соединенный с гидроксильной группой на скелете олигомера. В других воплощениях олигомер изобретения функционализируют более чем одним из функционализирующих реагентов, описанных в патенте США 4962029 и 4914210, которые во всей полноте включены в настоящее описание посредством ссылки. Способы синтезирования таких функционализирующих реагентов и введения их в мономеры и олигомеры раскрыты в патентах США 4962029 и 4914210. В некоторых воплощениях 5'-конец олигомера, связанного на твердой фазе, функционализируют производным диенилфосфорамидита с последующей конъюгацией депротектированного олигомера, например с аминокислотой или пептидом посредством реакции циклоприсоединения Дильса-Альдера. В различных воплощениях включение в олигомер мономеров, содержащих модификации в 2'-положении сахара,например 2'-карбаматзамещенный сахар или 2'-(О-пентил-Nфталимидо)дезоксирибоза, способствует ковалентному присоединению конъюгированных молекул к сахарам олигомера. В других воплощениях олигомер с аминосодержащим линкером в 2'-положении одного или более мономеров получают с применением реагента, такого как, например, 5'-диметокситритил 2'-O-(е-фталимидиламинопентил)-2'-деоксиаденозин-3'-N,N-диизопропилцианоэтоксифосфорамидит. См., например, Manoharan, et al., Tetrahedron Letters, 1991, 34, 7171. В других воплощениях олигомеры изобретения могут иметь аминосодержащие функциональные молекулы в нуклеиновом основании, включая аминогруппы, расположенные на N6 пурина, на экзоциклическом N2 гуанина, или в положениях N4 или 5 цитозина. В одном воплощении указанная функционализация может быть достигнута путем применения коммерческого реагента, который является уже функционализированным при синтезе олигомера. Некоторые функциональные молекулы являются коммерчески доступными, например, гетеробифункциональные и гомобифункциональные связывающие молекулы доступны в Pierce Co. (Rockford, III). Другие коммерчески доступные связывающие группы представляют собой реагенты 5'-аминомодификатор С 6 и 3'-аминомодификатор, доступные в Glen Research Corporation (Sterling, Va.). Также 5'-аминомодификатор С 6 доступен в ABI (Applied Biosystems Inc., Foster City, Calif.) как аминолинк-2, и также 3'-аминомодификатор доступен в Clontech Laboratories Inc. (Palo Alto, Calif.). Композиции. Олигомер изобретения может быть применен в фармацевтических формулах и композициях. Соответственно, такие композиции включают в себя фармацевтически приемлемый разбавитель, носитель,соль или адъювант. Международный патент WO 2007/031091 предоставляет подходящие и предпочтительные фармацевтически приемлемые растворители, носители и адъюванты, которые включены в описание посредством ссылки. Подходящие дозировки, формулы, пути введения, композиции, лекарственные формы, комбинации с другими терапевтическими агентами, формулами пролекарств также представлены в международном патенте WO 2007/031091, который также включен в описание посредством ссылки. Применяемый в описании термин "фармацевтически приемлемые соли" относится к солям, которые сохраняют желаемую биологическую активность установленных в настоящем описании соединений и проявляют минимальные нежелательные токсические эффекты. Не ограничивающие примеры таких солей могут быть получены с органической аминокислотой и солями присоединения основания, образованными с катионами металлов, например цинка, кальция, висмута, бария, магния, алюминия, меди, кобальта, никеля, кадмия, натрия, калия и т.п., или с катионом, полученным из аммиака,N,N-дибензилэтилендиамина, D-глюкозамина, тетраэтиламмония или этилендиамина; или (с) с комбинациями (а) и (b); например соль танната цинка и т.п. Применения. Олигомеры изобретения могут быть применены в качестве исследовательских реагентов, например,для диагностики, лечения и профилактики. В исследовании данные олигомеры могут быть применены для специфического ингибирования экспрессии или синтеза белка бета-катенина (обычно путем деградации или ингибирования мРНК и предотвращения тем самым образования белка) в клетках и у экспериментальных животных, тем самым,облегчая функциональный анализ мишени или оценки применимости в качестве мишени для терапевтического воздействия. В диагностике олигомеры могут быть применены для обнаружения и количественного анализа экспрессии бета-катенина в клетках и тканях с помощью нозерн-блоттинга, гибридизации in situ или сходных методов. В лечении животного или человека, которые предположительно имеют заболевание или нарушение,которые можно лечить путем модуляции экспрессии бета-катенина, животное или человека лечат введением олигомерных соединений, например эффективного количества олигомера (или его конъюгата) согласно настоящему изобретению. Далее предоставлены способы лечения млекопитающего, например лечения человека, который предположительно имеет или подвержен заболеванию или состоянию, ассоциированному с экспрессией бета-катенина, путем введения терапевтически или профилактически эффективного количества одного или более олигомеров или композиций изобретения. Изобретение также обеспечивает применение соединений или конъюгата изобретения, которые описаны, в получении медикамента для лечения нарушения, упоминаемого в описании, или в способе лечения нарушения, упоминаемого в описании. Изобретение также относится к олигомеру, композиции или конъюгату, которые описаны в настоящем документе, для применения в качестве медикамента. Соответственно, при ссылке на способы изобретения введение олигомера или конъюгата изобретения выполняют путем введения эффективного количества олигомера или конъюгата, например, количества,которое является эффективным для обеспечения лечения или количества, которое является эффективным для ингибирования или подавления экспрессии бета-катенина в клетке или в клетках. Изобретение также предоставляет способ лечения нарушения, как описано в настоящем документе,указанный способ включает в себя введение соединения согласно изобретению, как описано в настоящем документе, и/или конъюгата согласно изобретению, и/или фармацевтической композиции согласно изобретению пациенту, который в этом нуждается. В различных воплощениях олигомер или его конъюгат вызывает желаемый терапевтический эффект у человека, например, путем образования водородной связи с нуклеиновой кислотой-мишенью. Олигомер или его конъюгат вызывает снижение (ингибирование) экспрессии мишени путем образования водородной связи (гибридизации) с мРНК мишени, вызывая тем самым уменьшение экспрессии гена. Также предусматривается, что олигомерные соединения и конъюгаты, раскрытые в описании, могут иметь нетерапевтические применения, например диагностические применения. Медицинские показания. Нарушение, упоминаемое в описании, выбирают в различных воплощениях из группы, состоящей из гиперпролиферативного заболевания, такого как рак, выбранный из группы, состоящей из колоректального рака, гепатоцеллюлярного рака, рака эндометрия, злокачественной меланомы, рака яичников,рака поджелудочной железы, рака гипофиза, рака пищевода, рака легких, рака молочной железы, рака почек, рака гематопоэтической системы, рака шейки матки, рака ЦНС, рака костей, рака желчевыводящих путей и рака надпочечников. В различных воплощениях нарушение, которое упоминается в описании, представляет собой рак,выбранный из группы, состоящей из колоректального рака, гепатоцеллюлярного рака, рака эндометрия и злокачественной меланомы. В различных воплощениях нарушение, которое упоминается в описании, представляет собой рак,выбранный из группы, состоящей из рака печени и рака почек. Олигомеры и другие композиции согласно изобретению могут быть применены для лечения состояний, ассоциированных с повышенной экспрессией или экспрессией видоизмененной версии бетакатенина. Изобретение далее обеспечивает применение соединения изобретения в получении или в производстве медикамента для лечения заболевания, нарушения или состояния, упоминаемого в описании. Изобретение далее относится к применению соединения, композиции или конъюгата, как определено в описании, для производства медикамента для лечения аномальных уровней бета-катенина или экспрессии мутантных форм бета-катенина (например, аллельные варианты, такие как варианты, ассоциированные с одним из заболеваний, упоминаемых в описании). Один аспект изобретения направлен на способ лечения млекопитающего, имеющего или подверженного состояниям, ассоциированным с аномальными уровнями бета-катенина, включающий в себя введение млекопитающему терапевтически эффективного количества олигомера, имеющего своей мишенью бета-катенин, например олигомера, который включает в себя одну или более молекулу LNA. Поэтому способы изобретения могут быть применены для лечения или профилактики заболеваний, вызван- 23018986 ных аномальными уровнями бета-катенина. Альтернативно утверждается, что, кроме того, в различных воплощениях изобретение направлено на способ лечения аномальных уровней бета-катенина, указанный способ включает в себя введение олигомера изобретения, или конъюгата изобретения, или фармацевтической композиции изобретения пациенту, который в этом нуждается. Заболевание или нарушение, которое упоминается в описании, может быть ассоциировано в различных воплощениях с мутацией гена бета-катенина или гена, белковый продукт которого ассоциирован или взаимодействует с бета-катенином. Следовательно, в различных воплощениях мРНК-мишень представляет собой мутированную форму последовательности бета-катенина. Вызывающий интерес аспект изобретения направлен на применение описываемого олигомера (соединения) или описываемого конъюгата для приготовления медикамента для лечения заболевания, нарушения или состояния, упоминаемого в описании. Изобретение также относится к олигомеру, композиции или конъюгату, которые упоминаются в описании, для применения в качестве медикамента. Кроме того, изобретение относится к способу лечения субъекта, имеющего заболевание или состояние, например заболевание или состояние, упоминаемое в описании, указанный способ включает в себя введение соединения согласно изобретению, как описано в настоящем документе, и/или конъюгата согласно изобретению, и/или фармацевтической композиции согласно изобретению пациенту, который в этом нуждается. Соответствующие дозировки, рецептуры, пути введения, композиции, лекарственные формы, комбинации с другими терапевтическими агентами рецептуры пролекарств также представлены в международном патенте WO 2007/031091, который включен в настоящее описание посредством ссылки. Изобретение также предоставляет фармацевтическую композицию, включающую в себя соединение или конъюгат, как описано в настоящем документе, или конъюгат и фармацевтически приемлемый разбавитель,носитель или адъювант. Международный патент WO 2007/031091 предоставляет подходящий и предпочтительный фармацевтически приемлемый разбавитель, носитель и адъюванты, которые включены в описание посредством ссылки. Способы изобретения предпочтительно применяют для лечения или профилактики заболеваний,вызванных аномальными уровнями бета-катенина. Далее описываемое в настоящем документе изобретение охватывает способ предотвращения или лечения заболевания, включающий в себя введение терапевтически эффективного количества олигомера,модулирующего бета-катенин, человеку, который нуждается в указанном лечении. Изобретение далее охватывает применение короткого периода введения олигонуклеотидного соединения, модулирующего бета-катенин (олигомер или конъюгат). Альтернативно утверждается, что, кроме того, в различных воплощениях изобретение направлено на способ лечения аномальных уровней бета-катенина, указанный способ включает в себя введение олигомера изобретения, или конъюгата изобретения, или фармацевтической композиции изобретения пациенту, который в этом нуждается, и далее включает в себя введение следующего агента или следующего активного ингредиента. Указанное следующее введение может быть таким, что следующий агент или следующий активный ингредиент конъюгирован с соединением изобретения, представлен в фармацевтической композиции или введен в отдельной рецептуре. Изобретение также относится к олигомеру, композиции или конъюгату, которые определены в описании, для применения в качестве медикамента. Изобретение далее относится к применению соединения, композиции или конъюгата, которые определены в описании, для производства медикамента для лечения аномальных уровней бета-катенина или экспрессии мутантных форм бета-катенина (например, аллельных вариантов, таких как аллельные варианты, ассоциированные с одним из заболеваний, упомянутых в описании). Кроме того, изобретение относится к способу лечения субъекта, имеющего заболевание или состояние, такое как заболевание или состояние, упомянутое в описании. Пациент, который нуждается в лечении, представляет собой пациента, имеющего или возможно имеющего заболевание или нарушение. В различных воплощениях термин "лечение", используемый в описании, относится к лечению существующего заболевания (например, заболевания или нарушения, которые упоминаются в описании) или к предотвращению заболевания, т.е. к профилактике. Поэтому следует понимать, что лечение, упоминаемое в описании, в различных воплощениях может быть профилактическим. Заболевание или нарушение, упоминаемое в описании, в различных воплощениях может быть ассоциировано с мутацией в гене бета-катенина или в гене, белковый продукт которого ассоциирован с бетакатенином, например ген APC. Следовательно, в различных воплощениях мРНК-мишень представляет собой видоизмененную форму последовательности бета-катенина, например, она может включать в себя одну или более точечную мутацию, например SNP, ассоциированные с раком. Примеры таких заболеваний, где мутации в гене бета-катенина или в гене APC приводят к аномальным уровням активности бета-катенина, включают в себя:(1) колоректальный рак, APC и бета-катенин, оба мутированы более чем в 70% всех случаев (Powell(2) гепатоцеллюлярный рак, бета-катенин мутирован более чем в 25% случаев (de La Coste A.,PNAS, 1998);(4) злокачественная меланома, бета-катенин мутирован 10% случаев (Rubinfeld et al., Science,1997). Другие примеры указанных заболеваний включают в себя рак яичников, поджелудочной железы,гипофиза, пищевода, легких, молочной железы, почек, гемопоэтической системы, шейки матки, ЦНС,костей, желчных путей и надпочечников. Было показано, что мутации гена бета-катенина или гена APC ассоциированы с указанными заболеваниями (каталог соматических мутаций при раке доступен на Вебстранице Института Сандера (Великобритания) http://www.sanger.ac.uk/). Упоминаемый в соответствии с изобретением рак может быть выбран из упомянутых выше форм рака. Другие воплощения. Следующие воплощения также относятся к описанию и краткому изложению изобретения и могут быть совмещены с воплощениями изобретения, упоминаемыми в описании, включая воплощение, упоминаемое в формуле изобретения. 1. Антисмысловой олигонуклеотид (например, олигомер), способный к связыванию с последовательностью-мишенью гена бета-катенина SEQ ID NO: 173 или его аллелями и к угнетению экспрессии бета-катенина, указанный олигонуклеотид включает в себя последовательность из 10-50 нуклеиновых оснований, соответствующую последовательности-мишени. 2. Антисмысловой олигонуклеотид воплощения 1, где последовательность-мишень выбрана из участков гена бета-катенина, показанных SEQ ID NO: 1-132 или их аллельных вариантов. 3. Олигонуклеотид воплощения 1 или воплощения 2, включающий в себя последовательность из 1016 нуклеиновых оснований, показанных в SEQ ID NO: 1, 16, 17, 18, 33, 34, 49, 50, 51, 52, 53, 54, 55, 56,57, 58, 73, 88, 103 и 118 или их аллельные варианты. 4. Олигонуклеотид по любому из воплощений 1-3, включающий в себя последовательности, показанные как SEQ ID NO: 1-132. 5. Олигонуклеотид любого из предшествующих воплощений, показанный с помощьюSEQ ID NO: 133-172. 6. Олигонуклеотид по любому из предшествующих воплощений, где указанная последовательность нуклеиновых оснований включает в себя межнуклеотидные связи, независимо выбранные из фосфодиэфирной, фосфоротиоатной и боранфосфатной связи. 7. Олигонуклеотид по любому из предшествующих воплощений, где по меньшей мере два из указанных нуклеиновых основания представляют собой нуклеотидные аналоги. 8. Олигонуклеотид по воплощению 5, где указанная последовательность нуклеиновых оснований включает в себя в 5'-3' направлении (i) участок А: фрагмент из 2-4 нуклеотидных аналогов, за которым следует (ii) участок В: фрагмент из 6-11 нуклеотидов или нуклеотидных аналогов, отличающихся от нуклеотидных аналогов участка А, за которым следует (iii) участок С: фрагмент из 2-4 нуклеотидных аналогов, и за которым следует по желанию (iv) участок D: один или два нуклеотида. 9. Олигонуклеотид по воплощению 8, где участок А включает в себя по меньшей мере одну фосфодиэфирную связь между двумя молекулами нуклеотидных аналогов и/или молекулой нуклеотидного аналога и молекулой нуклеинового основания участка В. 10. Олигонуклеотид по воплощению 8 или воплощению 9, где участок С включает в себя по меньшей мере одну фосфодиэфирную связь между двумя молекулами нуклеотидных аналогов и/или молекулой нуклеотидного аналога и молекулой нуклеинового основания участка B. 11. Олигонуклеотид по любому из воплощений 1-6, где все межнуклеотидные связи являются фосфоротиоатными. 12. Олигонуклеотид по любому из воплощений 7-11, где указанные молекулы нуклеотидных аналогов независимо выбраны из 2'-O-алкил-РНК, 2'-амино-ДНК, 2'-фтор-ДНК, закрытой нуклеиновой кислоты (LNA), арабинонуклеиновой кислоты (ANA), 2'-фтор-ANA, HNA, INA и 2'-MOE. 13. Олигонуклеотид по воплощению 12, где нуклеотидные аналоги независимо выбраны из 2'-MOE-РНК, 2'-фтор-ДНК и LNA. 14. Олигонуклеотид по воплощению 13, где по меньшей мере один из указанных нуклеотидных аналогов представляет собой закрытую нуклеиновую кислоту (LNA). 15. Олигонуклеотид по воплощению 14, где все нуклеотидные аналоги представляют собой LNA. 16. Олигонуклеотид по любому из воплощений 12-15, где LNA выбрана из бета-D-окси-LNA, альфа-L-окси-LNA, бета-D-амино-LNA и бета-D-тио-LNA. 17. Конъюгат, включающий в себя олигонуклеотид любого из предшествующих воплощений и по меньшей мере одну ненуклеотидную или неполинуклеотидную молекулу, ковалентно соединенную с указанным олигонуклеотидом. 18. Конъюгат по воплощению 17, где указанная ненуклеотидная или неполинуклеотидная молекула состоит или включает в себя стериновую группу, например холестерин. 19. Фармацевтическая композиция, включающая в себя олигонуклеотид по любому из воплощений 1-16 или конъюгат по воплощению 17 или по воплощению 18 и фармацевтически приемлемый дилюент,носитель или адъювант. 20. Олигонуклеотид или конъюгат по любому из воплощений 1-18 для применения в качестве медикамента. 21. Применение олигонуклеотида или конъюгата по любому из воплощений 1-18 для получения медикамента для лечения аномальных уровней бета-катенина, или заболевания, или состояния, для которого показано подавление экспрессии бета-катенина. 22. Применение по воплощению 21, где указанное заболевание или состояние представляет собой рак. 23. Способ лечения субъекта, имеющего рак, указанный способ включает в себя стадию введения фармацевтической композиции, олигонуклеотида или конъюгата по любому из воплощений 1-19 субъекту, который в этом нуждается. 24. Применение или способ любого из воплощений 21-23, где рак выбран из колоректального рака,гепатоцеллюлярного рака, рака эндометрия, злокачественной меланомы, рака яичников, рака поджелудочной железы, рака гипофиза, рака пищевода, рака легких, рака молочной железы, рака почек, рака гематопоэтической системы, рака шейки матки, рака ЦНС, рака костей, рака желчевыводящих путей и рака надпочечников. 25. Последовательность-мишень внутри гена бета-катенина, где антисмысловой олигонуклеотид,соответствующий указанной последовательности-мишени, способен подавлять экспрессию бетакатенина. 26. Последовательность-мишень воплощения 25, где последовательность-мишень выбрана из участков гена бета-катенина, комплементарных SEQ ID NO: 1-132 или их аллельным вариантам. 27. Способ подавления экспрессии бета-катенина в клетке, включающий в себя контактирование клетки с олигонуклеотидом по любому из воплощений 1-16. Примеры Пример 1. Синтез мономера. Мономерные элементы структуры LNA и производные получают, следуя опубликованным процедурам и ссылкам, цитируемым в настоящем описании, см. международный патент WO 07/031081 и ссылки, цитируемые в описании. Пример 2. Синтез олигонуклеотидов. Олигонуклеотиды синтезируют по способу, описанному в международном патенте WO 07/031081. В табл. 1 показаны примеры антисмысловых олигонуклеотидных мотивов изобретения. Пример 3. Структура олигонуклеотидов. Согласно изобретению конструируют серии олигомеров, мишенью которых являются различные участки бета-катенина человека, с применением опубликованной последовательности с номером доступа Генбанка NM001904, которая представлена в описании как SEQ ID NO: 173. В табл. 2 показаны структуры олигомеров изобретения. В табл. 3 показаны 24-членные мотивы последовательностей, из которых могут быть сконструированы олигомеры изобретения, толстым шрифтом изображены 16-членные мотивы последовательностей, которые показаны в табл. 1. Пример 4. Модель in vitro: клеточная культура. Воздействие антисмысловых олигонуклеотидов на экспрессию нуклеиновой кислоты - мишени может быть проверено на любом типе клеток из предоставляемого многообразия типов клеток, при условии, что нуклеиновая кислота-мишень представлена в измеряемых концентрациях. Мишень может быть экспрессирована эндогенно или с помощью транзиторной или стабильной трансфекции нуклеиновой кислоты, кодирующей указанную нуклеиновую кислоту. Уровень экспрессии нуклеиновой кислотымишени может быть определен по стандартной методике с применением, например, анализа нозернблоттинг, ПЦР в режиме реального времени, тестов защиты от РНКазы. Следующие типы клеток предоставлены в иллюстративных целях, и другие типы клеток могут быть применены по стандартной методике при условии, что в выбранном типе клеток экпрессируется мишень. Клетки культивируют в соответствующей среде, как описано ниже, и сохраняют при 37C, влажности 95-98% и 5% СО 2. Клетки пересевают 2-3 раза в неделю по стандартной методике.SW480: клеточную линию колоректального рака человека SW480 культивируют в среде L-15(Leibovitz) + 10% эмбриональная бычья сыворотка (FBS) + Glutamax I + пен/стреп. НСТ 116: клеточную линию колоректального рака человека НСТ 116 культивируют в модифицированной среде МакКоя 5 а (Sigma) + 10% эмбриональная бычья сыворотка (FBS) + Glutamax I + пен./стреп. Пример 5. Модель in vitro: обработка антисмысловым олигонуклеотидом. Клетки обрабатывают олигонуклеотидом с применением катионной липосомной композицииLipofectAMINE 2000 (Gibco) в качестве трансфекционного переносчика. Клетки высевают в 6-луночные клеточные культуральные планшеты (NUNC) и обрабатывают при слиянии 75-90% колоний. Применяемые концентрации олигонуклеотидов изменяются в пределах от 1 до 25 нМ в конечной концентрации. Приготовление состава олигонуклеотид-липидных комплексов выполняют согласно описанию производителя с применением среды OptiMEM (Gibco), свободной от сыворотки, и с конечной концентрацией липидов 10 мкг/мл LipofectAMINE 2000. Клетки инкубируют при 37 С в течение 4 ч и останавливают обработку путем удаления культуральной среды, содержащей олигонуклеотиды. Отмывают клетки и добавляют среду, содержащую сыворотку. После обработки олигонуклеотидами клеткам дают восстановиться в течение 20 ч, перед тем как они будут собраны для анализа РНК. Пример 6. Модель in vitro: экстракция РНК и синтез кДНК. Для выделения РНК из клеточных линий применяют набор RNeasy mini kit (Qiagen, каталожный номер 74104) согласно протоколу производителя. Синтез первой цепи проводят с применением реагентов для обратной траскриптазы от Ambion, согласно инструкциям производителя. Для каждой пробы 0,5 мкг общей РНК доводят (10,8 мкл) свободной от РНКазы H2O и смешивают с 2 мкл произвольных декамеров (50 мкМ) и 4 мкл смеси дНТФ (2,5 мМ каждый дНТФ) и нагревают до 70 С в течение 3 мин, после чего пробы быстро охлаждают на льду. После охлаждения проб на льду 2 мкл 10 буфера RT, 1 мкл MMLV обратной траскриптазы (100 U/ мкл) и 0,25 мкл ингибитора РНКазы(10 Ед/мкл) добавляют к каждой пробе с последующей инкубацией при 42 С в течение 60 мин, инактивацией фермента нагреванием при 95 С в течение 10 мин и затем образец охлаждают до 4 С. Пример 7. Модель in vitro: анализ ингибирования олигонуклеотидами экспрессии бета-катенина с помощью ПЦР в режиме реального времени. Антисмысловая модуляция экспрессии бета-катенина может быть проверена с помощью ряда способов, известных в данной области техники. Например, уровни мРНК бета-катенина могут быть количественно измерены, например, с помощью анализа нозерн-блоттинг, конкурентной полимеразной цепной реакции (ПЦР) или ПЦР в режиме реального времени. В настоящее время предпочтительным является количественная ПЦР в режиме реального времени. Анализ РНК может быть проведен на общей клеточной РНК или на мРНК. Методы выделения РНК и анализ РНК, например анализ нозерн-блоттинг, являются общепринятыми в данной области техники и описываются, например, в Current Protocols inMolecular Biology, John Wiley and Sons. Количественный анализ в режиме реального времени (ПЦР) может быть удобно выполнен с применением коммерчески доступной системы детектирования Multi-Color Real Time PCR Detection System,имеющейся в наличии в Applied Biosystem. Количественный анализ ПЦР в режиме реального времени уровней мРНК бета-катенина. Содержание в образце мРНК бета-катенина человека определяют количественно с помощью реактива для анализа the human ABI Prism Pre-Developed TaqMan Assay Reagent (Applied Biosystems, каталожный номер Hs00170025ml) согласно инструкции производителя. Количество мРНК глицеральдегид-3-фосфат дегидрогеназы (ГАФДГ) используют в качестве внутреннего контроля для нормализации любого отклонения в приготовлении образца. Содержание в образце мРНК ГАФДГ человека определяют количественно с помощью реактива для анализа the human GAPDH ABI Prism Pre-Developed TaqMan Assay Reagent (Applied Biosystems, каталожный номер 4310884E) согласно инструкции производителя. Количественная ПЦР в режиме реального времени представляет собой метод, хорошо известный в данной области техники, и он описан, например,Heid et al. Real time quantitative PCR, Genome Research (1996), 6: 986-994. ПЦР в режиме реального времени. кДНК из синтеза первой цепи, выполненного, как описано в примере 8, разводят в 2-20 раз и анализируют с помощью количественной ПЦР в режиме реального времени с применением Taqman 7500 FAST от Applied Biosystems. Праймеры и зонд смешивают с 2 общей реакционной смеси Taqman Fast Universal PCR master mix (2) (Applied Biosystems, каталожный номер 4364103) и добавляют к 4 мкл кДНК до конечного объема 10 мкл. Каждый образец анализируют в триплетах. Стандартные кривые для анализов строят путем проведения количественного анализа 2-кратных разведений кДНК, которые были приготовлены на материале, выделенном из клеточной линии, которая экспрессирует представляющую интерес РНК. Для контроля, не содержащего матрицы, вместо кДНК применяют стерильную H2O. Программа ПЦР: 95 С в течение 30 с, с последующими 40 циклами при 95 С, 3 с, 60 С, 30 с. Относительные количества последовательности мРНК-мишени определяют из рассчитанного порогового цикла с применением программы Applied Biosystems Fast System SDS Software, версия 1.3.1.21. Пример 8. Анализ in vitro: антисмысловое ингибирование экспрессии бета-катенина человека олигонуклеотидами. Оценивают способность олигонуклеотидов, показанных в табл. 2, снижать мРНК бета-катенина в концентрациях 1, 5 и 25 нМ в клетках SW480 (см. фиг. 2). Данные представлены в табл. 4 в виде процента угнетения мРНК бета-катенина относительно фиктивно трансфицированных клеток при 5 нМ. Строчные буквы означают молекулы ДНК, выделенные жирным шрифтом заглавные буквы означают молекулы -D-окси-LNA. Все LNA С представляют собой 5'-метил С. Подстрочный индекс "s" означает фосфоротиоатную связь. Как показано в табл. 4, олигонуклеотиды SEQ ID NO: 153, 154, 155, 156, 158, 161, 168, 169, 170, 171 и 172 демонстрируют приблизительно 74% или выше ингибирование экспрессии мРНК бета-катенина при 5 нМ в данных экспериментах и, таким образом, являются предпочтительными. Также предпочтительными являются олигонуклеотиды, основанные на иллюстративных антисмысловых олигопоследовательностях, например, отличающиеся по длине (короче или длиннее) и/или по составу нуклеиновых оснований (например, тип и/или соотношение аналоговых единиц), которые также обеспечивают хорошее ингибирование экспрессии бета-катенина. Пример 9. Анализ in vitro: анализ вестерн-блоттинг уровней белка бета-катенина. Воздействие in vitro олигомерных соединений на уровни белка бета-катенина в трансфицированных клетках определяют с помощью анализа вестерн-блоттинг. Клетки SW480, 200000 клеток, трансфицированных олигонуклеотидами, как описано в примере 5, собирают и лизируют в лизирующем буфере RIPA(50 мМ Трис-HCl pH 7,4, 150 мМ NaCl, 1 мМ ЭДТА, 1% Тритон Х-100, 0,1% SDS, 1% деоксихолат натрия), дополненном смесью ингибиторов протеаз (Roche). Концентрации общего белка измеряют с помощью набора ВСА protein assay kit (Pierce). Общий белок, 50 мкг, разделяют на 3-8% трис-ацетатных гелях и собирают на мембраны PVDF согласно инструкциям производителя (Invitrogen). После инкубации в течение ночи в блокирующем буфере (PBS-T, дополненный 5% порошка молока с пониженным содержанием жира), мембраны инкубируют в течение ночи с антителом против бета-катенина (BDTransduction laboratories). В качестве контроля загрузки определяют тубулин с помощью моноклональных антител производства Neomarker. Затем мембраны инкубируют с вторичными антителами и белки бета-катенин или тубулин вызуализируют с помощью набора для хемилюменисцентной детекции ECL+(Amersham), см. фиг. 3. Пример 10. Подсчет пролиферирующих жизнеспособных клеток (тест MTS). Клетки линии колоректального рака HCTl16 высевают с плотностью 200000 клеток на лунку в 6-луночный планшет с модифицированной средой МакКоя 5 а (Sigma M8403) + 2 мМ Glutamax I (Gibco 35050-038) + 10% FBS (Brochrom 193575010) + 25 мкг/мкл гентамицина (Sigma G1397 50 мг/мл) за день
МПК / Метки
МПК: C12N 15/11, A61K 31/7088
Метки: активности, бета-катенина, соединения-антагонисты, модуляции, рнк
Код ссылки
<a href="https://eas.patents.su/30-18986-soedineniya-antagonisty-rnk-dlya-modulyacii-aktivnosti-beta-katenina.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения-антагонисты рнк для модуляции активности бета-катенина</a>
Предыдущий патент: Новый антиген, ассоциированный с новообразованными сосудами опухолевых метастазов
Следующий патент: Композиция для улучшения жизнеспособности растения
Случайный патент: Производные гигромицина а в качестве антибактериальных агентов