Селективные модуляторы рецепторов эстрогена для лечения вазомоторных симптомов
Номер патента: 16613
Опубликовано: 30.06.2012
Авторы: Уоллас Оуэн Брендан, Дэлли Роберт Дин, Додж Джеффри Алан, Фрэнк Скотт Алан, Шеферд Тимоти Алан, Хинклин Рональд Джей
Формула / Реферат
1. Соединение формулы (I)
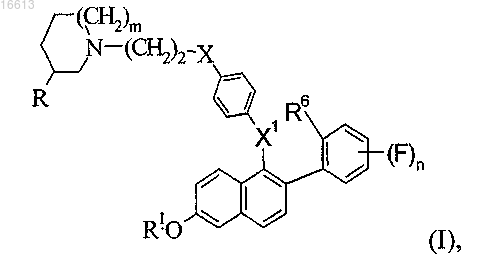
где m равно 0, 1 или 2;
n равно 1, 2, 3 или 4;
R представляет собой Н или метил при условии, что если m равно 1 или 2, то R должен представлять собой Н, и если m равно 0, то R должен представлять собой метил;
R1 представляет собой Н, SO2(н-С4-С6-алкил) или COR2;
X представляет собой О или NR3;
X1 представляет собой О, СН2 или С=O;
R6 представляет собой Н или F,
R2 представляет собой C1-С6-алкил; C1-C6-алкокси; NR5R5a; фенокси или фенил, необязательно замещенный галогеном;
R3 независимо представляет собой Н или С1-С6-алкил и
R5 и R5a независимо представляют собой Н, C1-С6-алкил или фенил;
или его фармацевтическая кислотно-аддитивная соль; причем указанное соединение формулы (I) не является
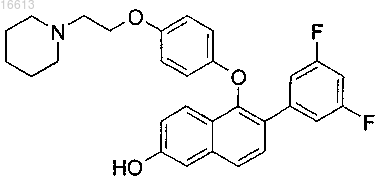
2. Соединение по п.1, отличающееся тем, что m равно 1 или 2, R1 представляет собой Н или COR2, R2 представляет собой C1-C4-алкил, NHCH3 или фенил, X представляет собой О, X1 представляет собой О или СН2.
3. Соединение по п.1 или 2, отличающееся тем, что R1 представляет собой Н.
4. Соединение по любому из пп.1-3, отличающееся тем, что m равно 1, R6 представляет собой Н или F и X1 представляет собой О.
5. Соединение по любому из пп.1-4, отличающееся тем, что общее количество атомов фтора при n и R6 составляет 1, 2 или 3.
6. Соединение по любому из пп.1-4, отличающееся тем, что общее количество атомов фтора при n и R6 составляет 1 или 2.
7. Соединение по любому из пп.1-6, отличающееся тем, что R6 представляет собой Н, n равно 2 и соответствующие заместители, являющиеся фтором, находятся в положениях 3 и 5.
8. Соединение по любому из пп.1-4, отличающееся тем, что R6 представляет собой Н, n равно 1 и соответствующий заместитель фтор находится в положении 4.
9. Применение соединения по любому из пп.1-8 для лечения одного или более вазомоторных симптомов.
10. Применение по п.9, отличающееся тем, что лечат один симптом и этот симптом представляет собой приливы.
11. Применение соединения по пп.1-8 для получения лекарственного средства для лечения одного или более вазомоторных симптомов.
12. Применение по п.11, отличающееся тем, что лечат один симптом и этот симптом представляет собой приливы.
13. Соединение формулы (II)
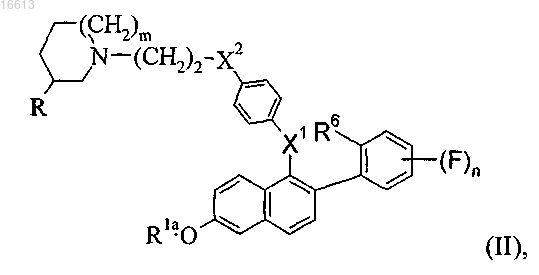
где m равно 0, 1 или 2;
n равно 1, 2, 3 или 4;
R представляет собой Н или метил при условии, что если m равно 1 или 2, то R должен представлять собой Н, и если m равно 0, то R должен представлять собой метил;
R1a представляет собой Н, SO2CH3, SO2(н-С4-С6-алкил), COR2, C1-С6-алкил или бензил;
X1 представляет собой О, СН2 или С=O;
X2 представляет собой О или NR7;
R6 представляет собой Н или F,
R2 представляет собой С1-С6-алкил; C1-С6-алкокси; NR5R5a; фенокси или фенил, необязательно замещенный галогеном;
R5 и R5a независимо представляют собой Н, C1-С6-алкил или фенил;
R7 представляет собой Н, C1-С6-алкил или CO2(C1-С6-алкил) при условии, что если R1a представляет собой Н, SO2(н-С4-С6-алкил) или COR2, то X2 представляет собой NR7 и R7 представляет собой СО2(C1-С6-алкил);
или его кислотно-аддитивная соль; причем соединение формулы (II) не является
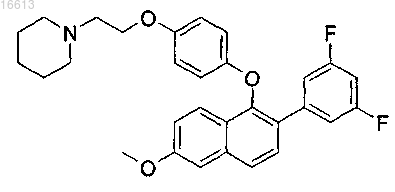
14. Соединение по п.13, отличающееся тем, что n равно 2 и соответствующие заместители, являющиеся фтором, находятся в положениях 3 и 5.
Текст
СЕЛЕКТИВНЫЕ МОДУЛЯТОРЫ РЕЦЕПТОРОВ ЭСТРОГЕНА ДЛЯ ЛЕЧЕНИЯ ВАЗОМОТОРНЫХ СИМПТОМОВ Данное изобретение относится к селективному модулятору рецепторов эстрогена формулы (I) или его фармацевтической соли с кислотой, полезных для лечения вазомоторных симптомов.(71)(73) Заявитель и патентовладелец: ЭЛИ ЛИЛЛИ ЭНД КОМПАНИ (US)"Вазомоторные симптомы", т.е. приливы, ночное потоотделение, сухость влагалища, нарушения сна, тошнота и перепады настроения, обычно возникают у женщин в период менопаузы. Фактически,вазомоторные симптомы будут возникать у большинства женщин в период менопаузы, причем значительный процент таких женщин будут страдать от этих симптомов в течение более 5 лет (Psychosom.Med. 1965, 27, 266; Med. Gynecol. Soc. 1969, 4, 268). К приливам особенно склонны женщины, которые подвергаются двусторонней овариоэктомии, радиотерапии или лечению агонистами гонадотропинвысвобождающего гормона (Br. J. Obstet. Gynaecol. 1977, 84, 769). Сообщалось также о возникновении вазомоторных симптомов у мужчин после лечения агонистом гонадотропин-высвобождающего гормона(N. Engl. J. Med. 1981, 305, 663) или после орхидэктомии (Urology 1980, 16, 620). Несмотря на то что вазомоторные симптомы уже сотни лет рассматриваются как связанное с менопаузой недомогание, точный механизм их возникновения неизвестен. Однако широко распространено мнение об их связи со снижением уровней эстрогена (вследствие природной менопаузы или других причин). Интересно, что женщины с низкими уровнями эстрогена вследствие дискенезии яичников обычно не страдают вазомоторными симптомами, за исключением случаев, когда они сначала получали гормонзаместительную терапию (ГЗТ), а затем прекратили ее (Clin. Endocrinol. (Oxf.) 1985, 22, 293), что указывает на синдром отмены эстрогенов как возможную базовую причину вазомоторной нестабильности. В настоящее время ГЗТ представляет собой предпочтительный стандарт лечения вазомоторных симптомов с эффективностью 80% у женщин, которые начинают лечение, что дополнительно поддерживает гипотезу о роли эстрогенов в этиологии данных состояний. Приливы характеризуются ощущением тепла, которое возникает в груди и распространяется в направлении шеи и головы, часто сопровождаясь потоотделением, сердцебиением и покраснением кожи. Приступы длятся от 30 с до 10 мин. Считается, что сами по себе приливы являются центрально опосредованными и представляют собой результат временного ослабления жесткого механизма терморегуляции в гипоталамусе (обзор см. в Can. J. Physiol. Pharmacol. 1987, 65, 1312). Регулирование процесса терморегуляции может включать, среди прочего, катехоламины, эстроген, тестостерон, опиоиды и серотонин (обзор см. в Мауо Clin. Proc. 2002, 77, 1207). Фактически, соединения, которые модулируют сигнальный путь каждого из этих гормонов/нейромедиаторов, оценивали с точки зрения лечения приливов. См., например, Ann. Intern. Med. 2000, 132, 788; Br. Med. J. 1974, i, 409; Maturitas, 1978, 1, 21; Med. J.Obstet. Gynecol. 1999, 94, 225; Br. J. Obstet. Gynecol. 1998, 105, 904; Neurology 2000, 54, 2161; Obstet. Gynecol. 1998, 72, 688; J. Clin. Oncol. 1998, 16, 495; J. Clin. Oncol. 2001, 19, 2739 и J. Nutr. 2001, 131 (11,supl), 3095s. Несмотря на большое количество существующих средств для лечения приливов, все они имеют недостаток низкой эффективности, их применение сопровождается неприемлемыми побочными эффектами или же они противопоказаны для определенных групп пациентов. Например, ГЗТ не рекомендуется женщинам с раком молочной железы, раком матки, раком яичников и венозной тромбоэмболией в анамнезе. Недавно полученные данные указывают на то, что ГЗТ может быть непригодной для женщин с заболеванием коронарной артерии. Негормональные средства терапии обычно не обладают полной эффективностью (например, клонидин) и/или вызывают побочные эффекты (например, венлафаксин, габапентин). В течение последних 10 лет появилось большое число публикаций, раскрывающих селективные модуляторы рецепторов эстрогена (SERM), например патенты США 5484795, 5484798, 5510358,5998401 и WO 96/09040. Многие из указанных SERM продемонстрировали полезный эффект в качестве агонистов эстрогена в костной и сердечно-сосудистой системах с сопутствующим полезным эффектом в качестве антагонистов эстрогена в молочных железах. Небольшая, особенно полезная подгруппа этих соединений также продемонстрировала действие антагонистов эстрогена или не эстрогенное воздействие на матку. Однако реальное применение SERM для лечения вазомоторных симптомов также было затруднено из-за проблем с эффективностью. Например, во время фазы III клинических исследований ралоксифена для лечения/профилактики постменопаузального остеопороза его применение сопровождалось небольшим повышением частоты приливов по сравнению с плацебо, а относительно тамоксифена известна его способность вызывать приливы более чем у 50% пациентов (Arch. Intern. Med. 1991, 151, 1842). Таким образом, остается неудовлетворенной медицинская потребность в средствах для лечения вазомоторных симптомов, которые преодолевали бы слабые стороны существующих средств лечения. Особенно существует потребность в лекарственном средстве, которое обладало бы положительными характеристиками ранее раскрытых SERM, таких как ралоксифен (т.е. позитивное воздействие на костную и сердечно-сосудистую системы, матку и молочные железы), но одновременно облегчало бы вазомоторные симптомы.-1 016613 Данное изобретение относится к соединению формулы (I)R представляет собой Н или метил при условии, что если m равно 1 или 2, то R должен представлять собой Н, и если m равно 0, то R должен представлять собой метил;R3 независимо представляет собой Н или С 1-С 6-алкил иR5 и R5a независимо представляют собой Н, С 1-С 6-алкил или фенил; или его фармацевтически кислотно-аддитивной соли; причем указанное соединение формулы (I) не является Данное изобретение также относится к применению соединения формулы (I) или его фармацевтической соли с кислотой для лечения одного или более вазомоторных симптомов. Данное изобретение также относится к применению соединения формулы (I) или его фармацевтической соли с кислотой для производства лекарственного средства для лечения одного или более вазомоторных симптомов. Данное изобретение также относится к соединению формулы (II)R представляет собой Н или метил при условии, что если m равно 1 или 2, то R должен представлять собой Н, и если m равно 0, то R должен представлять собой метил;R5 и R5a независимо представляют собой Н, C1-C6-алкил или фенил;R7 представляет собой Н, С 1-С 6-алкил или CO2(C1-C6-алкил) при условии, что если R1a представляет собой Н, SO2 (н-С 4-С 6-алкил) или COR2, то X2 представляет собой NR7 и R7 представляет собой CO2 (C1 С 6-алкил); или его кислотно-аддитивной соли; причем соединение формулы (II) не является полезному в качестве промежуточного соединения для получения соединения формулы (I). Если не указано иное, в данном описании термин "соединение формулы (I)" включает его фармацевтические соли с кислотой. Соединения по настоящему изобретению содержат один или более хиральных центров и могут существовать в различных стереоизомерных конфигурациях. Как результат существования данных хиральных центров, соединения по настоящему изобретению существуют в виде рацематов, смесей энантиомеров и индивидуальных энантиомеров, а также в виде диастереомеров и смесей диастереомеров. Все такие рацематы, энантиомеры и диастереомеры находятся в объеме данного изобретения. Следующие термины определены ниже для целей данного изобретения, как раскрыто и заявлено в данном описании и формуле. Термин "гало" означает фтор, хлор, бром или йод. Термин "С 1-С 6-алкил" означает неразветвленный,разветвленный или циклический углеводородный остаток, содержащий от 1 до 6 атомов углерода, например метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил, пентил, циклопентил, гексил, циклогексил и т.п. Такие остатки, как циклобутилметиленил и циклопропилметиленил также включены в рамки C1-C6-алкильной группы. Термин "C1-C4-алкил" конкретно означает метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, третбутил, циклопропилметил и циклобутил. Термин "н-С 4-С 6-алкил" конкретно означает н-бутил, н-пентил и н-гексил. Группа "С 1-С 6-алкокси" представляет собой С 1-С 6-алкильный остаток, связанный через оксисвязь. Термин "фармацевтический" в данном описании как прилагательное означает, по существу, безвредный (не оказывающий вредного действия)."Фармацевтическая соль с кислотой" представляет собой соль, образованную путем взаимодействия соединения формулы (I) в форме свободного основания с фармацевтической кислотой, такой как описано в Encyclopedia of Pharmaceutical Technology, editors James Swarbrick and James C. Boylan, vol. 13, 1996,Preservation of Pharmaceutical Products to Salt Forms of Drugs and Absorption". Конкретные формы солей включают, но не ограничиваются ими, ацетат, бензоат, бензолсульфонат, 4-хлорбензолсульфонат; цитрат; этансульфонат; фумарат; d-глюконат; d-глюкуронат; глутарат; гликолят; гиппурат; гидрохлорид; 2 гидроксиэтансульфонат; dl-лактат; малеат; d-малат; l-малат; малонат; d-манделат; l-манделат; метансульфонат; 1,5-нафталиндисульфонат; 2-нафталинсульфонат; фосфат; салицилат; сукцинат; сульфат; dтартрат; l-тартрат и п-толуолсульфонат. Термин "лечащий" и "лечить" в данном описании означает облегчение, уменьшение, профилактику,подавление, ограничение, замедление, остановку или обращение прогресса или выраженности патологического состояния или его последствий, описанных в данном описании. Термин "предупреждение" означает уменьшение вероятности того, что реципиент, принимающий соединение формулы (I), будет подвергаться, или в дальнейшем подвергаться, или у него будет развиваться любое из патологических состояний или их последствий, приведенных в данном описании."Вазомоторный симптом" представляет собой состояние, выбранное из следующего перечня: приливы, ночное потоотделение, сухость влагалища, нарушения сна, тошнота и перепады настроения; причем указанное состояние является результатом снижения уровня циркулирующего эндогенного эстрогена, которое возникает у женщины после прекращения или уменьшения менструаций в результате естественных, хирургических или других процессов. Термин "женщина, которая нуждается в этом" означает женщину, страдающую указанным патологическим состоянием, или женщину с риском такого состояния, установленным медицинским диагнозом,т.е. определенным наблюдающим врачом. Термин "эффективное количество" в данном описании означает количество соединения формулы(I), способное лечить описанные в описании состояния. Предпочтительные соединения и воплощения изобретения Некоторые соединения по настоящему изобретению являются особенно интересными и предпочтительными. Следующий перечень определяет несколько групп предпочтительных соединений. Следует понимать, что каждый из пунктов списка может сочетаться с другими пунктами списка с образованием дополнительных групп предпочтительных соединений. А именно соединение, где m равно 1 или 2, R1 представляет собой Н или COR2, R2 представляет собой С 1-С 4-алкил, NHCH3 или фенил, X представляет собой О, X1 представляет собой О или СН 2. Соединение, где R1 представляет собой Н. Соединение, где m равно 1, R6 представляет собой Н или F и X1 представляет собой О.-3 016613 Соединение, где общее количество атомов фтора при n и R6 составляет 1, 2 или 3. Соединение, где общее количество атомов фтора при n и R6 составляет 1 или 2. Соединение, где R6 представляет собой Н, n равно 2 и соответствующие заместители, являющиеся фтором, находятся в положениях 3 и 5. Соединение, где R6 представляет собой Н, n равно 1 и соответствующий заместитель фтор находится в положении 4. Соединение формулы (I) предпочтительно применяется при лечении приливов. Соединение формулы (I) предпочтительно вводится в рецептуру дозированной лекарственной формы, т.е. в индивидуальный носитель для доставки, например в таблетку или капсулу, перед введением женщине-реципиенту. Соединение формулы (I) предпочтительно вводится перорально. Синтез Соединение формулы (I) может быть получено согласно следующей схеме (где R8a представляет собой R8, H или F), подготовительным примерам и примерам. Схема 1 На схеме 1 соединение формулы V взаимодействует с соединением формулы IV в обычных условиях реакции Сузуки или Штилле, т.е. когда один из заместителей "А" или "D" представляет собой остаток бороновой кислоты/эфира или алкилстаннана, а другой является уходящей группой, например хлором,бромом, йодом, или сульфонатной группой, такой как трифторметилсульфонат, с получением соединения формулы VI (если R8a представляет собой R8 из формулы III). Если в соединении формулы VI X1 представляет собой СО, кетогруппа может быть восстановлена в стандартных условиях, например, с использованием борана, с получением соответствующего бензилового спирта. Такой восстановленный продукт может быть подвергнут циклизации в стандартных условиях, например, если R8a представляет собой F, в условиях основного катализа трет-бутоксидом калия, или если R8a не является F, в условиях кислотного катализа с помощью HCl, с получением соответствующего соединения формулы (I) или (II). Если R1a представляет собой SO2CH3, С 1-С 6-алкил или бензил (предпочтительно метил, бензил илиSO2CH3), указанные защитные гидроксигруппы могут быть удалены в стандартных условиях (см., например, методики в последнем издании Greene, Protective Groups in Organic Synthesis, John WileySons,New York, N.Y.) с получением соединения формулы (I), где R1 представляет собой Н. Аналогично, еслиX2 представляет собой NR7 и R7 представляет собой CO2(C1-С 6-алкил), указанная защитная аминогруппа также может быть удалена, как показано Greene. Соединения формулы (I), где R1 представляет собой Н,могут быть далее преобразованы, используя стандартную методику ацилирования или сульфонилирования, с получением соединения формулы (I), где R1 представляет собой COR2 или SO2(н-С 4-С 6-алкил). Соединения формулы IV могут быть получены, как показано ниже, или с помощью методик, кото-4 016613 рые аналогичны известным из уровня техники. Соединения формулы V, как правило, являются коммерчески доступными или могут быть получены с помощью методик, легко доступных обычному специалисту в области органического синтеза, или с помощью показанных ниже способов. Подготовительные примеры и примеры Условия хирального разделения. Все подготовительные условия подразумевают использование колонки Chiralpak AD. Условия А: 3:2 гептан/IPA (изофталевая кислота) мас./0,2% диметилэтиламина (DMEA), 830 см,365 нм, 350 мл/мин. Условия В: 3:2 гептан/IPA мас./0,2% DMEA, 830 см, 365 нм, 350 мл/мин. Условия С: 80/10/10 гептан/3 А/МеОН мас./0,2% DMEA, 834 см, 260 нм, 375 мл/мин. Условия D: 75/15/10 гептан/IPA/MeOH мас./0,2% DMEA, 834 см, 260 нм, 375 мл/мин. Условия Е: 70/30 гептан/IPA мас./0,2% DMEA, 834 см, 260 нм, 375 мл/мин. Условия F: 4:1 гептан/IPA мас./0,2% DMEA, 830 см, 350 нм, 350 мл/мин. Условия G: 3:1 гептан/IPA мас./0,2% DMEA, 833 см, 340 нм, 375 мл/мин. Условия Н: 3:1 гептан/IPA мас./0,2% DMEA, 833 см, 340 нм, 375 мл/мин. Условия I: 3:1 гептан/IPA мас./0,2% DMEA, 833 см, 360 нм, 375 мл/мин. Условия J: 4:1 гептан/IPA мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Условия K: 70/30 гептан/IPA мас./0,2% DMEA, 834 см, 320 нм, 350 мл/мин. Условия L: 100% 3 А мас./0,2% DMEA, 830 см, 260 нм, 300 мл/мин. Условия М: 70/30 гептан/IPA мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Условия N: 70/30 гептан/IPA мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Условия О: 65/35 3 А/гептан мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Условия Р: 100% 3 А мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Условия Q: 70/30 гептан/IPA мас./0,2% DMEA, 830 см, 260 нм, 350 мл/мин. Подготовительный пример 1. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2 иловый эфир трифторметансульфоновой кислоты К диметилформамиду (ДМФА, 250 мл) при комнатной температуре добавляют 6-метоксинафталин 2-ол (20 г, 114,8 ммоль) с последующим добавлением N-бромсукцинимида (NBS, 21,5 г, 120 ммоль) в течение 30 мин. Через 45 мин разбавляют водой (800 мл), собирают осадок и сушат с получением 25,5 г(K2CO3, 40,0 г, 290 ммоль) и бензилбромид (49,6 г, 290 ммоль). Смесь перемешивают при комнатной температуре в течение 1 ч. Добавляют воду (400 мл) для осаждения продукта. Осадок собирают и промывают на фильтре гептаном (3125 мл), затем сушат с получением 83,7 г 2-бензилокси-1-бром-6 метоксинафталина (86,2%). Объединяют толуол (200 мл), 2-бензилокси-1-бром-6-метоксинафталин (30 г, 87,4 ммоль), 4-(2 пиперидин-1-илэтокси)фенол (23,2 г, 105 ммоль) и карбонат цезия (34,4 г 105 ммоль) и кипятят смесь с обратным холодильником. Порцию толуола (100 мл) удаляют. К реакционной смеси добавляют этилацетат (390 мг, 4,37 ммоль) и комплекс меди с трифлатом бензола (2,20 г, 4,37 ммоль) и перемешивают в течение 5 мин. Растворитель удаляют дистилляцией, нагревают полученный остаток до 174 С и выдерживают 1,5 ч. Остаток растворяют в смеси этилацетата (200 мл) и водного HCl (1 N, 90 мл). Фазы разделяют и концентрируют органическую фазу до получения остатка. Остаток хроматографируют на колонке с получением 12,4 г 1-2-[4-(2-бензилокси-6-метоксинафталин-1-илокси)фенокси]этилпиперидина(30%). 1-2-[4-(2-Бензилокси-6-метоксинафталин-1-илокси)фенокси]этилпиперидин (12,4 г, 25,5 ммоль) добавляют к смеси метанол/этилацетат (1:1, 490 мл) и нагревают до образования раствора. Нагревание прекращают и добавляют формиат аммония (4,83 г, 76,6 ммоль) и Pd(OH)2 на углероде (20 мас.%, 1,58 г,1,12 ммоль). Кипятят с обратным холодильником в течение 50 мин, затем смесь фильтруют. Фильтрат концентрируют с получением 9,9 г 6-метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-ола(98,5%). Дихлорметан (290 мл), триэтиламин (3,08 г, 30,4 ммоль) и 6-метокси-1-[4-(2-пиперидин-1 илэтокси)фенокси]нафталин-2-ол (9,2 г, 23,4 ммоль) охлаждают до -50 С и добавляют ангидрид трифторметансульфоновой кислоты (7,26 г, 25,7 ммоль). Полученную смесь перемешивают при -50 С в течение 2 ч, затем дают смеси нагреться до комнатной температуры и перемешивают еще в течение 1 ч. Добавляют рассол (150 мл) и отделяют органическую фазу. Органический слой промывают NaHCO3, затем-5 016613 сушат и концентрируют до получения остатка. Остаток кристаллизуют в смеси этиловый эфир/гексаны с получением 11,2 г указанного в заголовке соединения (90,9%). Пример 1. 1-(2-4-[2-(2,6-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидин 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,0 г, 1,9 ммоль) растворяют в 20 мл ДМФА. К этому раствору добавляют 2,6 дифторфенилбороновую кислоту (0,6 г, 3,8 ммоль), фосфат калия (2,42 г, 11,4 ммоль) и тетракис(трифенилфосфин)палладий(0) (0,44 г, 0,38 ммоль) и нагревают до 100 С, выдерживая при этой температуре 18 ч. Смесь охлаждают и фильтруют, очищают на колонке с интенсивным катионным обменом(strong cation exchange, SCX), элюируя примеси метанолом, затем элюируя продукт 2 N аммиаком в метаноле. Затем очищают на колонке с силикагелем, элюируя градиентом 50-100% смеси метиленхлорид/гексан, содержащей 1% изопропиламина, с получением 300 мг (32%) указанного в заголовке соединения. Пример 2. Гидрохлорид 6-(2,6-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2 ола. 1-(2-4-[2-(2,6-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидин (300 мг, 0,61 ммоль) растворяют в 20 мл метиленхлорида и охлаждают на льду. К полученной смеси добавляют 2,0 мл трибромида бора с вихревым перемешиванием и дают нагреться до комнатной температуры. Полученную смесь выливают в двухфазную смесь, состоящую из насыщенного бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой промывают рассолом и сушат над молекулярными ситами 3. Проводят дальнейшую очистку, используя хроматографию с обращенной фазой, с получением 138 мг указанного в заголовке соединения (48%). Переводят в гидрохлорид и лиофилизуют. 1 Н-ЯМР (CDCl3,300 МГц)7,92 (д, J=9,0 Гц, 1 Н); 7,59 (д, J=8,4 Гц, 1 Н); 7,35 (д, J=8,4 Гц, 1 Н); 7,20-7,17 (м, 2 Н); 7,03 (дд,J=9,0, 2,1 Гц, 1 Н); 6,85-6,80 (м, 2 Н); 6,52 (с, 4 Н); 3,95 (т, J=5,7 Гц, 2 Н); 2,73 (т, J=6,0 Гц, 2 Н); 2,52-2,52 (м,4 Н); 1,64-1,59 (м, 4 Н); 1,46-1,44 (м, 2 Н). Пример 3. Гидрохлорид 1-(2-4-[2-(2-фторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина В круглодонную колбу объемом 100 мл, высушенную в печи, загружают 6-метокси-1-[4-(2 пиперидин-1-илэтокси)фенокси]нафталин-2-иловый эфир трифторметансульфоновой кислоты (300 мг,0,57 ммоль) и помещают в атмосферу азота. Твердое вещество растворяют в ацетонитриле (10 мл) и добавляют 2-фторфенилбороновую кислоту (240 мг, 1,71 ммоль), трициклогексилфосфин (48 мг, 0,17 ммоль), ацетат палладия (38 мг, 0,17 ммоль) и фторид цезия (780 мг, 5,14 ммоль). Доводят температуру раствора до 85 С и перемешивают в течение 1 ч. Раствор фильтруют через слой целита, промывают ацетонитрилом и концентрируют в вакууме. Сырой продукт очищают с использованием радиальной хроматографии, получая 295 мг (110%) указанного в заголовке соединения в форме свободного основания. Свободное основание растворяют в 3 мл эфира и добавляют 0,8 мл 1 N HCl. Немедленно сушат с получением 305 мг указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=472 (M-Cl). Пример 4. Гидрохлорид 6-(2-фторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-ола. В круглодонную колбу объемом 100 мл помещают гидрохлорид 1-(2-4-[2-(2-фторфенил)-6 метоксинафталин-1-илокси]феноксиэтил)пиперидина (290 мг, 0,57 ммоль) в 5 мл безводного CH2Cl2 и охлаждают до 0 С в атмосфере азота. Добавляют 2,90 мл (2,90 ммоль) 1 M раствора BBr3 в CH2Cl2 и контролируют реакцию с помощью ES-MS. После перемешивания в течение 1 ч реакционную смесь выливают в холодный насыщенный раствор водного бикарбоната натрия и метиленхлорида (150 мл). Органический слой сушат над сульфатом натрия и концентрируют в вакууме. Сырой продукт очищают с использованием радиальной хроматографии, элюируя 8% МеОН/CH2Cl2, с получением 137 мг (52%) указанного в заголовке соединения в виде свободного основания. Гидрохлорид получают добавлением 0,8 мл 1 N раствора HCl в Et2O: масс-спектр (распыление ионов) m/z=458 (M-Cl). 1-(2-4-[2-(2,4-дифторфенил)-6-метоксинафталин-1-илокси]фенок Смешивают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-иловый эфир трифторметансульфоновой кислоты (2,99 г, 5,70 ммоль), 2,4-дифторбензолбороновую кислоту (2,70 г, 17,09 ммоль), ацетат палладия(II) (0,13 г, 0,57 ммоль), трициклогексилфосфин (240 мг, 0,85 ммоль), фторид цезия (7,79 г, 51,25 ммоль) и ацетонитрил (70 мл) и нагревают при 90 С. Через 10 мин охлаждают до комнатной температуры, фильтруют и удаляют растворитель в вакууме. Растворяют в дихлорметане и промывают 1 N водной хлористо-водородной кислотой, насыщенным водным раствором бикарбоната натрия, насыщенным водным раствором хлорида натрия, сушат с помощью сульфата магния, фильтруют и удаляют растворитель в вакууме. Остаток хроматографируют на силикагеле с использованием смеси дихлорметан/метанол и добавляют 1 М хлористый водород в эфире (10 мл), получая 3,0 г (100%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=488 (M-Cl). Пример 6. Гидрохлорид 6-(2,4-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2 ола. Гидрохлорид 1-(2-4-[2-(3,4-дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина(3,00 г, 5,70 ммоль) растворяют в дихлорметане (90 мл) и охлаждают на ледяной бане. Добавляют трибромид бора (1 М в дихлорметане, 18,0 мл, 18,0 ммоль) и перемешивают в течение 2,5 ч. Добавляют метанол (20 мл), нагревают до комнатной температуры и удаляют растворитель в вакууме. Растворяют в дихлорметане с минимальным количеством метанола, промывают насыщенным водным раствором бикарбоната натрия и удаляют растворитель в вакууме. Кристаллизуют в смеси этилацетат/дихлорметан и отфильтровывают твердое вещество с получением указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в смеси дихлорметан/метанол, добавляют 1 М хлористый водород в эфире (10 мл) и удаляют растворитель в вакууме с получением 2,68 г (92%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=476 (M-Cl). Пример 7. Гидрохлорид 1-(2-4-[2-(2,5-дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина Смешивают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-иловый эфир трифторметансульфоновой кислоты (154 мг, 0,29 ммоль), 2,5-дифторфенилбороновую кислоту (139 мг, 0,88 ммоль), комплекс [1,1'-бис-(дифенилфосфин)ферроцен)дихлорпалладия(II) с дихлорметаном (1:1) (239 мг, 0,29 ммоль), фторид цезия (400 мг, 2,63 ммоль) и ацетонитрил (6 мл), перемешивают и нагревают до 90 С. Через 4 ч охлаждают до комнатной температуры и удаляют растворитель в вакууме. Остаток суспендируют в этиловом эфире и обрабатывают ультразвуком, фильтруют и удаляют растворитель в вакууме. Сырую смесь хроматографируют на силикагеле со смесями дихлорметан/метанол, объединяют содержащие продукт фракции, добавляют 1 M хлористый водород в эфире (1 мл) и удаляют растворитель в вакууме с получением 140 мг указанного в заголовке соединения: масс-спектр (распыление ионов)(133 мг, 0,25 ммоль) растворяют в дихлорметане (5 мл), охлаждают на ледяной бане и добавляют трибромид бора (1 М в дихлорметане, 0,76 мл, 0,76 ммоль). Дают медленно нагреться до комнатной температуры в течение 18 ч, гасят насыщенным водным раствором бикарбоната натрия, органический слой сушат сульфатом магния, фильтруют и хроматографируют на силикагеле со смесями дихлорметан/метанол. Объединяют фракции, содержащие продукт, добавляют 1 M хлористый водород в эфире (1 мл) и удаляют растворитель в вакууме с получением 108 мг (83%) указанного в заголовке соединения: масс-спектр В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-иловый эфир трифторметансульфоновой кислоты (800 мг, 1,52 ммоль), 3,4,5-трифторбензолбороновую кислоту (804 мг, 4,57 ммоль), фторид цезия (1,1 г, 7,6 ммоль) и продувают азотом. В отдельную колбу помещают ацетат палладия(II) (34 мг, 0,15 ммоль), трициклогексилфосфин (64 мг, 0,23 ммоль) и продувают азотом. Добавляют дегазированный ацетонитрил и обрабатывают ультразвуком в атмосфере азота в течение 10 мин. К смеси твердых веществ добавляют раствор катализатора и погружают колбу в масляную баню с температурой 80 С на 10 мин. Охлаждают до комнатной температуры и фильтруют через целит. Концентрируют и снова растворяют в метиленхлориде. Промывают насыщенным водным раствором бикарбоната натрия, разделяют фазы, сушат, фильтруют и концентрируют. Остаток очищают над силикагелем,элюируя 0-5% метанолом в метиленхлориде, с получением 720 мг (93%) указанного в заголовке соединения: масс-спектр (распыление ионов) 508,3 (М+Н). Пример 10. Гидрохлорид 6-(3,4,5-трифторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин 2-ола. 1-(2-4-[6-Метокси-2-(3,4,5-трифторфенил)нафталин-1-илокси]феноксиэтил)пиперидин (720 мг,1,4 ммоль) растворяют в метиленхлориде (15 мл). Добавляют 2 M HCl в эфире (1,4 мл, 2,8 ммоль) и концентрируют в вакууме. Остаток растворяют в метиленхлориде (15 мл) и по каплям добавляют трибромид бора (0,53 мл, 5,6 ммоль) при температуре 0 С в атмосфере азота. Через 45 мин выливают в холодный насыщенный водный раствор бикарбоната натрия и экстрагируют метиленхлоридом. Органический слой концентрируют и остаток очищают на силикагеле, элюируя 0-12% метанолом в метиленхлориде, с получением 554 мг (80%) указанного в заголовке соединения в виде свободного основания. Свободное основание (554 мг, 1,1 ммоль) растворяют в этилацетате (6 мл) и эфире (12 мл). Добавляют 2 M HCl в эфире(1,1 мл, 2,2 ммоль) и собирают осадок. Сушат в вакуумной печи при 50 С в течение ночи с получением 467 мг (79%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=494,3 (M-Cl). Пример 11. 1-(2-4-[2-(2,3-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидин С использованием методики, описанной в примере 9, осуществляют взаимодействие 6-метокси-1[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-илового эфира трифторметансульфоновой кислоты (3,5 г, 6,67 ммоль), 3,5-дифторбензолбороновой кислоты (3,1 г, 19,6 ммоль), фторида цезия (9,2 г, 60,4 ммоль), ацетата палладия(II) (145 мг, 0,64 ммоль) и трициклогексилфосфина (290 мг, 1,03 ммоль) с получением 3,3 г (100%) указанного в заголовке соединения: масс-спектр (распыление ионов) 490,3 (М+Н). Пример 14. Гидрохлорид 6-(3,5-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2 ола. С использованием такой же методики, как и в случае гидрохлорида 6-(3,4,5-трифторфенил)-5-[4-(2-8 016613 пиперидин-1-илэтокси)фенокси]нафталин-2-ола,осуществляют взаимодействие 1-(2-4-[2-(3,5 дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина (3,8 г, 7,9 ммоль), 2 М HCl в эфире (7,9 мл, 15,8 ммоль) и трибромида бора (3,7 мл, 39,2 ммоль) с получением 2,6 г (64%) указанного в заголовке соединения после хроматографии на силикагеле: масс-спектр (распыление ионов) 476,3 (М-Cl). Пример 15. Гидрохлорид 6-(3,4-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2 ола В круглодонную колбу объемом 250 мл, высушенную в печи, загружают 6-метокси-1-тетралон (3,0 г, 17,0 ммоль) и помещают в атмосферу азота. Твердое вещество растворяют в толуоле (30 мл) и добавляют 1-бром-3-фторбензол (4,7 мл, 42,6 ммоль), трет-бутоксид натрия (6,5 г, 68,1 ммоль), ацетат палладия (76 мг, 0,34 ммоль) и рацемический BINAP (212 мг, 0,34 ммоль). Раствор нагревают до 115 С и перемешивают в течение 18 ч. Раствор разбавляют холодной 5 N HCl (50 мл) и этилацетатом (200 мл). Органический слой отделяют и сушат над сульфатом натрия, фильтруют через слой целита и концентрируют в вакууме. Сырой продукт очищают с использованием радиальной хроматографии, получая 3,4 г(74%) указанного в заголовке соединения. Этот продукт используют без дальнейшей очистки: массспектр (распыление ионов) m/z=267 (M-H). 2-(3-Фторфенил)-6-метоксинафталин-1-ол (3,36 г, 12,5 ммоль) растворяют в N-метил-2 пирролидиноне (NMP) (10 мл) и добавляют гидрид натрия (500 мг, 60% дисперсия в масле, 12,5 ммоль) при комнатной температуре. После перемешивания в течение 1 ч этот раствор добавляют к раствору 4 фторбензальдегида (2,4 мл, 22,5 ммоль) в NMP (10 мл), который был нагрет до 185 С. Перемешивание продолжают в течение 2,5 ч. Реакционную смесь охлаждают до комнатной температуры, добавляют буфер с рН 7 (50 мл) и экстрагируют этилацетатом (2100 мл). Органические экстракты промывают водой и фильтруют через пробку силикагеля. Сырой продукт очищают с использованием радиальной хроматографии, получая 2,50 г (54%) указанного в заголовке соединения, которое используют без дальнейшей очистки: масс-спектр (распыление ионов) m/z=371 (M-Н). В круглодонную колбу объемом 100 мл помещают 4-[2-(3-фторфенил)-6-метоксинафталин-1 илокси]бензальдегид (2,5 г, 6,71 ммоль) и этилацетат (5 мл). При комнатной температуре добавляют 2 мл 35% пероксида водорода. К полученному раствору медленно добавляют 2 мл концентрированной серной кислоты. Смесь нагревают приблизительно до 40 С и затем охлаждают до комнатной температуры, при которой перемешивают в течение 2 ч. Реакционную смесь разбавляют водой и этилацетатом (100 мл) и органический слой сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Сырой продукт очищают с использованием радиальной хроматографии, элюируя СН 2 С 12, с получением 540 мг (22%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=359 (M-H). Пример 16. Гидрохлорид 1-(2-4-[2-(3-фторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина К 4-[2-(3-фторфенил)-6-метоксинафталин-1-илокси]фенолу (180 мг, 0,50 ммоль) в 10 мл безводного ДМФА добавляют гидрид натрия (60 мг, 60% дисперсия в масле, 1,50 ммоль) и раствор перемешивают в течение 30 мин при комнатной температуре. Добавляют гидрохлорид 1-(2-хлорэтил)пиперидина (138 мг,0,75 ммоль) и перемешивают реакционную смесь в течение 3 дней. Реакционную смесь разбавляют метиленхлоридом, промывают насыщенным раствором бикарбоната натрия (1), рассолом (1), экстрагируют органический слой и сушат над сульфатом натрия. Сырой продукт очищают с использованием радиальной хроматографии, элюируя 4% МеОН/CH2Cl2, с получением 234 мг (99%) указанного в заголовке соединения в виде свободного основания. Гидрохлорид образуют, добавляя 0,8 мл 1 N раствора HCl вEt2O: масс-спектр (распыление ионов) m/z=472 (M-Cl). Пример 17. Гидрохлорид 6-(3-фторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-ола. В круглодонную колбу объемом 100 мл помещают гидрохлорид 1-(2-4-[2-(3-фторфенил)-6 метоксинафталин-1-илокси]феноксиэтил)пиперидина (245 мг, 0,48 ммоль) и охлаждают до 0 С в атмосфере азота. Добавляют 1,45 мл 1 М раствора BBR3 в CH2Cl2 и контролируют протекание реакции с помощью ES-MS. После перемешивания в течение 1 ч реакционную смесь выливают в холодную смесь насыщенного водного раствора бикарбоната натрия и метиленхлорида (150 мл). Органический слой сушат над сульфатом натрия и концентрируют в вакууме. Сырой продукт очищают с использованием радиальной хроматографии, элюируя 4% МеОН/CH2Cl2, с получением 139 мг (63%) указанного в заголовке соединения в виде свободного основания. Гидрохлорид образуют, добавляя 0,8 мл 1 N раствора HCl в Бром (107 мл, 2,08 моль) добавляют в раствор 6-бензилокси-3,4-дигидро-2 Н-нафталин-1-она (250 г,0,99 моль) в хлороформе (2 л) при 5 С в течение 1,5 ч. Добавляют раствор тиосульфата натрия (250 мл),гася реакционную смесь при 0 С. Добавляют этилацетат (1 л) и разделяют слои. Водный слой экстрагируют с помощью CH2Cl2 (500 мл) и органические слои объединяют, промывают водным раствором бикарбоната натрия и рассолом. Сушат с помощью сульфата натрия и концентрируют в вакууме. Остаток растирают при добавлении 10% этилацетата в гексане (600 мл) с получением твердого вещества. Твердое вещество отфильтровывают и сушат с получением 405 г (100%) 6-бензилокси-2,2-дибром-3,4-дигидро 2 Н-нафталин-1-она. 1 М метоксид натрия (215 мл, 0,99 моль) добавляют к раствору 6-бензилокси-2,2-дибром-3,4 дигидро-2 Н-нафталин-1-она (205 г, 0,5 моль) в метаноле (1,3 л). Суспензию нагревают до растворения. Реакционную смесь охлаждают до 0 С и добавляют 1 N HCl (540 мл). Добавляют Н 2 О (3 л) и охлаждают до 3 С с получением твердого вещества. Твердое вещество отфильтровывают и сушат с получением 152 г (92%) 6-бензилокси-2-бромнафталин-1-ола. Гидрид натрия (24 г, 0,6 ммоль) добавляют порциями к раствору 6-бензилокси-2-бромнафталин-1 ола (179 г, 0,54 моль) в ТГФ (3,0 л) при 0 С. Добавляют метансульфонилхлорид (47 мл, 0,61 моль) в течение 45 мин и перемешивают реакционную смесь в течение 1,5 ч при 10 С. Добавляют раствор бикарбоната натрия (500 мл) и воду (500 мл). Слои разделяют и экстрагируют водный слой этилацетатом(2500 мл). Органические слои объединяют и промывают рассолом (200 мл). Сушат с помощью сульфата магния, фильтруют и концентрируют в вакууме. Остаток растирают при добавлении 20% этилацетата в гексане (1 л) с получением твердого вещества. Фильтруют, промывают твердое вещество толуолом(2200 мл) и сушат твердое вещество с получением 176 г (80%) 6-бензилокси-2-бромнафталин-1-илового эфира метансульфоновой кислоты. 6-Бензилокси-2-бромнафталин-1-иловый эфир метансульфоновой кислоты (10,0 г, 24,4 ммоль), 4 фторфенилбороновую кислоту (10,2 г, 72,9 ммоль), карбонат натрия (7,8 г, 73,6 ммоль) и тетракистрифенилфосфинпалладий (2,8 г, 2,4 ммоль) перемешивают в смеси толуола (300 мл), этанола (60 мл) и воды(40 мл). Смесь нагревают при 100 С в течение 12 ч. Суспензию охлаждают и фильтруют через слой целита. Растворитель выпаривают в вакууме. Остаток промывают раствором бикарбоната натрия и рассолом. Сушат с помощью сульфата магния и концентрируют в вакууме. Остаток очищают на силикагеле,элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (0-10%), с получением 10,1 г(98%) 6-бензилокси-2-(4-фторфенил)нафталин-1-илового эфира метансульфоновой кислоты. 6-Бензилокси-2-(4-фторфенил)нафталин-1-иловый эфир метансульфоновой кислоты (5,2 г, 12,3 ммоль) растворяют в 5 M гидроксиде натрия (12 мл, 60 ммоль), ТГФ (86 мл) и МеОН (86 мл). Нагревают при 50 С в течение 1 ч. Охлаждают и добавляют этилацетат (100 мл). Органический слой промывают 1 NHCl, насыщенным раствором бикарбоната натрия и рассолом. Сушат с помощью сульфата магния и концентрируют в вакууме с получением 3,4 г (89%) 6-бензилокси-2-(4-фторфенил)нафталин-1-ола. Гидрид натрия (400 мг, 10 ммоль) добавляют в раствор 6-бензилокси-2-(4-фторфенил)нафталин-1 ола в NMP (40 мл). Полученную суспензию алкоксида добавляют в раствор 4-фторбензальдегида (2 мл,19 ммоль) в NMP (30 мл) при 165 С. Нагревают при температуре 165 С в течение 1 ч. Охлаждают и добавляют буферный раствор (рН 7, 10 мл). Добавляют диэтиловый эфир (1 л). Слои разделяют и промывают водный слой диэтиловым эфиром (2200 мл). Органические слои объединяют, сушат с помощью сульфата магния и концентрируют в вакууме. Остаток хроматографируют на колонке Biotage, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (0-10%), с получением 2,9 г (70%) 4-[6 бензилокси-2-(4-фторфенил)нафталин-1-илокси]бензальдегида. В раствор Н 2 О 2 (1 мл, 9,7 ммоль) и 4-[6-бензилокси-2-(4-фторфенил)нафталин-1 илокси]бензальдегида при 0 С добавляют по каплям 18 М H2SO4 (1 мл, 16,8 ммоль) и перемешивают при- 10016613 комнатной температуре в течение 12 ч. Добавляют H2O (20 мл) и CH2Cl2 (100 мл). Слои разделяют и экстрагируют водный слой CH2Cl2 (250 мл). Органические слои объединяют, сушат с помощью сульфата магния и концентрируют в вакууме с получением 1,88 г (73%) указанного в заголовке соединения; массспектр (распыление ионов: m/z=435,1 (M-H). Пример 18. 1-(2-4-[6-Бензилокси-2-(4-фторфенил)нафталин-1-илокси]феноксиэтил)пиперидин 4-[6-Бензилокси-2-(4-фторфенил)нафталин-1-илокси]фенол (5,20 г, 11,91 ммоль) растворяют в ДМФА (60 мл) в атмосфере N2 и добавляют NaH (1,43 г, 35,74 ммоль, 60 мас.%). Раствор перемешивают в течение 0,5 ч при комнатной температуре и затем добавляют гидрохлорид 1-(2-хлорэтил)пиперидина(3,29 г, 17,87 ммоль). Раствор продолжают перемешивать и затем добавляют воду (300 мл). Водный слой экстрагируют с помощью CH2Cl2 (3300 мл) и затем органические слои объединяют. Органический слой сушат с помощью Na2SO4, затем фильтруют, концентрируют и очищают колоночной флэшхроматографией (силикагель, 0-4% MaOH:NH4OH (10/1, об./об.)/CH2Cl2) с получением 6,5 г (99%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=548,3 (М+Н). Пример 19. Гидрохлорид 6-(4-Фторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-ола. 1-(2-4-[6-Бензилокси-2-(4-фторфенил)нафталин-1-илокси]феноксиэтил)пиперидин (6,5 г, 11,87 ммоль) растворяют в смеси МеОН/ТГФ (200 мл, об./об.=1/1) в атмосфере N2. Добавляют Pd/C (0,65 г,10%) и трижды заменяют N2 на Н 2. Реакционную смесь перемешивают в течение 2 ч, затем отфильтровывают Pd/C. Растворитель удаляют и остаток очищают колоночной хроматографией (силикагель, 2-8%MeOH:NH4OH (10/1, об./об.)/CH2Cl2) с получением 2,93 г (54%) указанного в заголовке соединения в виде свободного основания. Свободное основание (2,93 г, 6,41 ммоль) растворяют в CH2Cl2 (100 мл) и охлаждают до -78 С. Добавляют HCl (10 мл, 2,0 М в Et2O) и перемешивают раствор в течение 10 мин. Растворитель удаляют при пониженном давлении и температуре 40 С в течение ночи, затем в вакууме с получением 3,17 г (100%) указанного в заголовке соединения; масс-спектр (распыление ионов) m/z=458,2(44 г, 0,22 ммоль) в ТГФ (600 мл) и ДМФА (100 мл) при комнатной температуре добавляют гидрид натрия (18 г, 0,45 моль). Нагревают до 60 С и выдерживают в течение 30 мин. Раствор выливают в воду со льдом. Разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой сушат с помощью сульфата магния, фильтруют и концентрируют при пониженном давлении с получением коричневого масла. Масло растворяют в этилацетате (500 мл) и метаноле (500 мл). Добавляют формиат аммония (100 г, 1,59 моль) и палладий-на-угле (10 г, 9,4 ммоль). Смесь кипятят с обратным холодильником в течение 30 мин. Добавляют формиат аммония (100 г, 1,59 моль) и палладий-на-угле (10 г, 9,4 ммоль). Реакционную смесь нагревают в течение 30 мин. Полученную суспензию фильтруют через слой целита и элюируют этилацетатом (500 мл). Растворитель выпаривают при пониженном давлении и добавляют воду (100 мл). Смесь разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой промывают насыщенным раствором бикарбоната натрия (2200 мл), сушат сульфатом магния, фильтруют и выпаривают растворитель при пониженном давлении с получением 31 г (64%) 4-(2-азепан-1-илэтокси)фенола. Смешивают 2-бензилокси-1-бром-6-метоксинафталин (31 г, 90 ммоль), 4-(2-азепан-1 илэтокси)фенол (31 г, 132 ммоль), медную бронзу (12 г, 189 ммоль), карбонат калия (25 г, 181 ммоль) и пиридин (400 мл). Реакционную смесь кипятят с обратным холодильником в течение 85 ч. Охлаждают,остаток фильтруют через целит и элюируют метанолом и метиленхлоридом (500 мл, 1:5 об./об.). Растворитель выпаривают при пониженном давлении и остаток хроматографируют на колонке с силикагелем,элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (0-10%), с получением 19 г (43%) 1-2-[4-(2-бензилокси-6-метоксинафталин-1-илокси)фенокси]этилазепана. 1-2-[4-(2-Бензилокси-6-метоксинафталин-1-илокси)фенокси]этилазепан (19 г, 38 ммоль) растворяют в этилацетате (500 мл) и метаноле (600 мл). Смесь нагревают до получения прозрачного раствора. Охлаждают до комнатной температуры. Добавляют формиат аммония (30 г, 476 ммоль) и палладий-наугле (2 г, 1,9 ммоль). Кипятят с обратным холодильником в течение 30 мин. Добавляют формиат аммония (7 г, 111 ммоль) и палладий-на-угле (0,7 г, 0,7 ммоль). Кипятят с обратным холодильником в течение- 11016613 30 мин. Полученную суспензию фильтруют через слой целита и элюируют этилацетатом (500 мл). Растворитель выпаривают при пониженном давлении и добавляют воду (100 мл). Смесь разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой промывают насыщенным раствором бикарбоната натрия (2200 мл), сушат с помощью сульфата магния, фильтруют и выпаривают растворитель при пониженном давлении с получением 15,1 г (97%) 1-[4-(2-азепан-1-илэтокси)фенокси]-6 метоксинафталин-2-ола. Трифторметансульфоновый ангидрид (7 мл, 42 ммоль) добавляют в раствор 1-[4-(2-азепан-1 илэтокси)фенокси]-6-метоксинафталин-2-ола (15 г, 37 ммоль), триэтиламина (20 мл) и метиленхлорида(500 мл) при -50 С. Реакционную смесь нагревают до комнатной температуры и перемешивают при этой температуре в течение 1 ч. Реакционную смесь охлаждают до -78 С и добавляют рассол (20 мл). Реакционную смесь нагревают до комнатной температуры. Слои разделяют и промывают органический слой насыщенным раствором бикарбоната натрия (100 мл) и рассолом. Органический слой сушат с помощью сульфата магния, фильтруют и выпаривают растворитель при пониженном давлении. Остаток хроматографируют на колонке с силикагелем, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (0-10%), с получением 20 г (99%) 1-[4-(2-азепан-1-илэтокси)фенокси]-6 метоксинафталин-2-илового эфира трифторметансульфоновой кислоты. Пример 20. 1-(2-4-[2-(3,5-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепан 1-[4-2-Азепан-1-илэтокси)фенокси]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (435 мг, 0,80 ммоль), фторид цезия (864 мг, 5,7 ммоль) и 1,3-дифторбензолбороновую кислоту(383 мг, 2,4 ммоль) растворяют в сухом ацетонитриле (5 мл) и перемешивают в течение 10 мин. В отдельной колбе суспендируют ацетат палладия (18 мг, 0,08 ммоль) и трициклогексилфосфин (33 мг, 0,12 ммоль) в сухом ацетонитриле (15 мл) и обрабатывают ультразвуком в атмосфере азота в течение 10 мин. Содержимое обеих колб объединяют и нагревают реакционную смесь при 60 С в течение 15 мин. Реакционную смесь охлаждают и фильтруют через слой целита, затем концентрируют в вакууме. Сырой продукт очищают хроматографией на силикагеле, используя градиент 1-3% метанола в дихлорметане, с получением 400 мг (98%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=504,2(М+Н). Пример 21. Гидрохлорид 5-[4-(2-азепан-1-илэтокси)фенокси]-6-(3,5-дифторфенил)нафталин-2-ола. 1-(2-4-[2-(3,5-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепан (583 мг, 1,2 ммоль) растворяют в дихлорметане (10 мл). Охлаждают до 0 С, добавляют 2 М HCl (1,2 мл, 2,3 ммоль) и перемешивают при комнатной температуре в течение 15 мин. Концентрируют в вакууме. Соль снова растворяют в дихлорметане (10 мл) и охлаждают до 0 С. Добавляют по каплям трибромид бора (972 мг, 3,5 ммоль) и доводят до комнатной температуры. Реакционную смесь перемешивают в течение 1,5 ч и выливают в смесь льда, насыщенного бикарбоната натрия (10 мл) и метанола (10 мл). Экстрагируют дихлорметаном, экстракты объединяют и промывают водой и насыщенным раствором бикарбоната натрия. Сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Очищают хроматографией на силикагеле, используя градиент 1-4% метанола в дихлорметане, с получением 366 мг (65%) указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в 10 мл дихлорметана и добавляют 2 М HCl (0,8 мл), перемешивают в течение 10 мин и концентрируют в вакууме с получением 343 мг (88%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=490,3 (MCl). Пример 22. 1-(2-4-[2-(3,4-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепан Смешивают ацетат палладия (33 мг, 0,15 ммоль), трициклогексилфосфин (61 мг, 0,22 ммоль) и ацетонитрил (6 мл). Смесь обрабатывают ультразвуком в течение 5 мин. Смешивают 1-[4-(2-азепан-1 илэтокси)фенокси]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (787 мг, 1,46 ммоль), фторид цезия (2,00 г, 13,2 ммоль), 3,4-дифторфенилбороновую кислоту (692 мг, 4,38 ммоль) и ацетонитрил (16 мл). В реакционный сосуд добавляют обработанную ультразвуком суспензию Pd/Pcy3 и нагревают при 90 С в течение 30 мин. Охлаждают до комнатной температуры, фильтруют через слой целита и выпаривают растворитель. Остаток растворяют в этилацетате (40 мл) и промывают насыщенным NaHCO3 (10 мл). Слои разделяют, органический слой промывают рассолом (10 мл), сушат с помощью MgSO4, фильтруют и концентрируют в вакууме. Остаток хроматографируют на колонке с SiO2,- 12016613 элюируя продукт метанолом в дихлорметане (0-5%), с получением 630 мг (86%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=504,2 (М+Н). Пример 23. Гидрохлорид 5-[4-(2-азепан-1-илэтокси)фенокси]-6-(3,4-дифторфенил)нафталин-2-ола. 1-(2-4-[2-(3,4-Дифторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепан (630 мг, 1,25 ммоль) растворяют в дихлорметане (20 мл). Добавляют 2 М HCl в диэтиловом эфире (1 мл, 2,0 ммоль). Перемешивают в течение 5 мин. Полученную взвесь концентрируют и сушат в вакууме. Остаток разбавляют дихлорметаном (20 мл) и продувают азотом. Раствор охлаждают до 0 С на внешней ледяной бане. Добавляют BBr3 (0,4 мл, 4,3 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и выливают в смесь насыщенного водного раствора NaHCO3 (20 мл), льда (5 г) и метанола (5 мл). Разбавляют дихлорметаном (20 мл), разделяют слои, промывают органический слой рассолом(10 мл), сушат с помощью MgSO4, фильтруют и концентрируют в вакууме. Остаток хроматографируют на колонке с SiO2, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (от 0 до 5%), с получением указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в диэтиловом эфире (5,0 мл), этилацетате (6,0 мл) и метаноле (1,0 мл) и добавляют 2 M HCl (1 мл, 2,0 ммоль) в диэтиловом эфире. Остаток собирают на фильтровальную бумагу, промывают диэтиловым эфиром и сушат в вакууме (2 мм рт. ст.) с получением 310 мг (47%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=490,3 (M-Cl). Пример 24. Гидрохлорид 1-(2-4-[2-(3-фторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепана Данное соединение получают, следуя описанной выше методике получения 1-(2-4-[2-(3 фторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)пиперидина, с использованием гидрохлорида 2(гексаметиленимино)этилхлорида, получая 100% выход свободного основания указанного в заголовке соединения после радиальной хроматографии. Гидрохлорид образуют, добавляя 0,8 мл 1 M раствора HCl в Et2O: масс-спектр (распыление ионов) m/z=486 (М-Cl). Пример 25. Гидрохлорид 5-[4-(2-азепан-1-илэтокси)фенокси]-6-(3-фторфенил)нафталин-2-ола. Данное соединение получают, следуя описанной выше методике получения гидрохлорида 6-(3 фторфенил)-5-[4-(2-пиперидин-1-илэтокси)фенокси]нафталин-2-ола с использованием в качестве исходного соединения гидрохлорида 1-(2-4-[2-(3-фторфенил)-6-метоксинафталин-1-илокси]феноксиэтил)азепана, получая указанное в заголовке соединение в виде свободного основания с выходом 52% после радиальной хроматографии. Гидрохлорид образуют, добавляя 0,8 мл 1 M раствора HCl в Et2O: масс-спектр (распыление ионов) m/z=472 (M-Cl). Пример 26. 1-(2-4-[6-Бензилокси-2-(4-фторфенил)нафталин-1-илокси]феноксиэтил)азепан Гидрид натрия (324 мг, 8,0 ммоль) добавляют к раствору 4-[6-бензилокси-2-(4 фторфенил)нафталин-1-илокси]фенола (1,18 г, 2,7 ммоль) в ДМФА (10 мл) и перемешивают в течение 20 мин при комнатной температуре. Добавляют гидрохлорид 2-(гексаметиленимино)этилхлорида (1,07 г, 5,4 ммоль) и перемешивают при комнатной температуре в течение 12 ч. Добавляют Н 2 О (10 мл) и диэтиловый эфир (100 мл). Слои разделяют и промывают водный слой диэтиловым эфиром (250 мл). Органические слои объединяют, сушат с помощью сульфата магния и концентрируют в вакууме. Остаток очищают на силикагеле, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (от 0 до 10%),с получением 1,0 г указанного в заголовке соединения (66%): масс-спектр (распыление ионов) m/z=562,3(20 мл) и этилацетата (12 мл). Кипятят с обратным холодильником в течение 1 ч. Полученную суспензию охлаждают и фильтруют через слой целита. Растворитель выпаривают, разбавляют CH2Cl2 и промываютH2O (20 мл). Органический слой сушат с помощью сульфата магния и концентрируют в вакууме с получением свободного основания указанного в заголовке соединения. Свободное основание растворяют в этилацетате (2 мл), диэтиловом эфире (2 мл) и MeOH (0,1 мл). Добавляют 2 M HCl (1 мл, 20 ммоль), полученную взвесь концентрируют и сушат в вакууме с получением указанного в заголовке соединения- 13016613 Подготовительный пример 5. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2 иловый эфир трифторметансульфоновой кислоты В сухой круглодонной колбе, оборудованной мешалкой, датчиком температуры и подводом азота,растворяют 2,6-диметоксинафталин (1,0 экв.) в CH2Cl2 (5 об.экв.) при комнатной температуре. Раствор охлаждают до 0 С на ледяной бане и добавляют 4-(2-пиперидин-1-илэтокси)бензоилхлорид (1,1 экв.). Добавляют хлорид алюминия (2,0 экв.). Как только определят, что реакция завершилась, реакционную смесь медленно гасят 1 N NaOH и разбавляют добавлением воды и CH2Cl2. Водный слой промывают(120 мл) CH2Cl2. Органические экстракты объединяют, промывают рассолом и сушат (Na2SO4). Сырой продукт перекристаллизовывают из метанола с получением (2,6-диметоксинафталин-1-ил)-[4-(2 пиперидин-1-илэтокси)фенил]метанона (средний выход 68%).(10 об.экв.) в трехгорлой круглодонной колбе, оборудованной дополнительной воронкой для выравнивания давления, мешалкой и источником азота. Колбу охлаждают на ледяной бане, содержащей рассол, и по каплям добавляют 1,0 M раствор BCl3 в CH2Cl2 (1,2 экв.). Реакционный раствор становится темнокрасным, и температура сначала повышается до 5 С. В течение 1 ч все исходные вещества вступают в реакцию, что подтверждается данными ТСХ (эфир/петролейный эфир, 1:1). Реакционную смесь гасят метанолом (5 экв.) и дают нагреться до комнатной температуры. Органический раствор разбавляютCH2Cl2 (1 об.экв.) и добавляют к 1,0 М раствору NaHCO3 (5 об.экв.), затем перемешивают в течение 1 ч. Водный и органический слои разделяют. Водный слой промывают CH2Cl2 (1 об.) и органические слои объединяют, промывают насыщенным раствором NH4Cl и сушат над Na2SO4. Продукт очищают колоночной хроматографией (50/1 силикагель), элюируя смесью CH2Cl2/гексаны (3:1), с получением (2 гидрокси-6-метоксинафталин-1-ил)-[4-(2-пиперидин-1-илэтокси)фенил]метанона (типичный выход 87%). В трехгорлой круглодонной колбе, оборудованной мешалкой и источником азота, растворяют (2 гидрокси-6-метоксинафталин-1-ил)-[4-(2-пиперидин-1-илэтокси)фенил]метанон в CH2Cl2 (10 об.) и охлаждают до 0 С на ледяной бане с рассолом. Добавляют пиридин (1,3 экв.). Добавляют трифторметансульфонилхлорид (1,2 экв.) с помощью шприца в течение 15 мин. Через 15 мин реакционную смесь гасят водой (10 об.), промывают 1 N HCl (5 об.), промывают 1,0 N NaHCO3 и сушат над Na2SO4. Концентрируют до получения указанного в заголовке соединения с количественным выходом. Продукт используют без дальнейшей очистки. Пример 28. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (12,4 г, 23,0 ммоль) и 2,4-дифторфенилбороновую кислоту (7,0 г, 4 6,0 ммоль) растворяют в дегазированном диметоксиэтане (620 мл). Добавляют 2 M водный раствор карбоната натрия (73 мл, 14 5 ммоль) и перемешивают при комнатной температуре в атмосфере азота в течение 5 мин. Добавляют ацетат палладия(II) (520 мг, 2,3 ммоль) и трифенилфосфин (1,2 г, 4,6 ммоль) и погружают колбу в масляную баню при температуре 85 С. Перемешивают в течение 40 мин и охлаждают до комнатной температуры. Выливают в насыщенный водный раствор бикарбоната натрия и дважды экстрагируют метиленхлоридом. Объединенные органические слои сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Полученное масло очищают на колонках с интенсивным катионным обменом (SCX)[2-(2,4-Дифторфенил)-6-метоксинафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (10,8 г, 21,5 ммоль) растворяют в метиленхлориде (200 мл). Добавляют 2 М HCl в эфире (21,5 мл, 43 ммоль) и концентрируют в вакууме. Пену снова растворяют в метиленхлориде (200 мл) и охлаждают до 0 С в атмосфере азота. Медленно добавляют трибромид бора (10,1 мл, 107 ммоль) и перемешивают при 0 С в течение 30 мин. Реакционную смесь медленно выливают в насыщенный водный раствор бикарбоната натрия и экстрагируют 20% изофталевой кислотой (IPA) в хлороформе. Органический слой сушат над сульфатом натрия, фильтруют и концентрируют в вакууме с получением 10,5 г (100%) указанного в за- 14016613 головке соединения в виде свободного основания. 1H-ЯМР (CDCl3)7,72 (д, J=8,6 Гц, 1H), 7,49 (д, J=8,6 Гц, 3 Н), 7,35 (д, J=8,4 Гц, 1 Н), 7,18 (т, J=7,8 Гц, 1 Н), 7,14 (д, J=1,9 Гц, 1H), 6,96 (дд, J=9,2, 2,3 Гц, 1 Н),6,74-6,62 (м, 2 Н), 6,58 (д, J=8,6 Гц, 2 Н), 4,08 (т, J=5,9 Гц, 2 Н), 2,79 (т, J=5,6 Гц, 2 Н), 2,55 (уш.с, 4 Н), 1,63(уш.с, 4 Н), 1,45 (м, 2 Н). Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 1,0 М хлористо-водородной кислоты и лиофилизуют смесь с получением указанного в заголовке соединения. Пример 30. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (4,51 г, 8,4 ммоль) растворяют в ацетонитриле (140 мл). Добавляют Pd(OAc)2 (0,28 г, 1,3 ммоль), трициклогексилфосфин (0,59 г, 2,1 ммоль), фторид цезия (11,4 г, 75,6 ммоль) и 2,5 дифторбензолбороновую кислоту (2,56 г, 16,2 ммоль). Колбу заполняют азотом и реакционную смесь нагревают до 90 С. Реакционную смесь нагревают в течение 1 ч и затем охлаждают до комнатной температуры. Добавляют воду (400 мл) и экстрагируют водный слой метиленхлоридом (3400 мл). Органические слои объединяют и сушат сульфатом натрия, фильтруют, концентрируют и очищают колоночной флэш-хроматографией (0-4% MeOH:NH4OH, (10/1, об./об.)/CH2Cl2) с получением 2,42 г (68%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=502,3 (М+Н). Пример 31. Гидрохлорид [2-(2,5-дифторфенил)-6-гидроксинафталин-1-ил]-[4-(2-пиперидин-1 илэтокси)фенил]метанона.(M+H). Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 5 М хлористо-водородной кислоты и лиофилизуют смесь с получением указанного в заголовке соединения. Пример 32. 6-(2,4-Дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир метансульфоновой кислоты[2-(2,4-Дифторфенил)-6-гидроксинафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (540 мг, 1,11 ммоль) и метансульфонилхлорид (254 мг, 2,22 ммоль) растворяют в 10 мл ацетонитрила и добавляют триэтиламин (224 мг, 2,22 ммоль). Смесь перемешивают в течение 5 дней при комнатной температуре. Добавляют эквивалентные количества сульфонилхлорида и триэтиламина и перемешивают в течение 30 мин. Смесь упаривают досуха, остаток растворяют в метаноле и пропускают через колонку с интенсивным катионным обменом (SCX). Колонку промывают метанолом и элюируют продукт 2 N аммиаком в метаноле с получением 433 мг (69%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=566 (M+H). Пример 33. В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (2,0 г, 3,7 ммоль), 2,6-дифторфенилбороновую кислоту (1,17 г, 7,4 ммоль), тетракис(трифенилфосфин)палладий(0) (855 мг, 0,7 4 ммоль) и фосфат калия (4,7 г, 22,2 ммоль),добавляют 100 мл сухого ДМФА и нагревают в атмосфере азота при 100 С в течение 2 ч. Реакционную смесь охлаждают и фильтруют. Очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем, элюируя градиентом 0-10%[2-(2,6-Дифторфенил-6-метоксинафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (1,5 г,3,0 ммоль) растворяют в 500 мл метиленхлорида и охлаждают на льду. К полученному раствору добавляют порциями трибромид бора (6,0 мл, 63 ммоль) с вихревым перемешиванием между добавлениями. Дают нагреться до комнатной температуры и перемешивают в течение 1 ч. Выливают в двухфазную систему, состоящую из органического слоя хлороформ/изопропанол 3:1 и водного слоя - насыщенного раствора бикарбоната натрия. Слои разделяют и сушат органический слой с помощью молекулярных сит 3. Очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид. Выход чистого продукта составляет 600 мг (44%). 1 Н-ЯМР (CD3OD, 400 МГц)7,87 (д, J=8,0 Гц, 1 Н); 7,56(д, J=8,4 Гц, 2 Н); 7,49 (д, J=9,2 Гц, 1 Н); 7,33 (д, J=8,8 Гц, 1 Н); 7,27-7,25 (м, 1 Н); 7,23-7,21 (м, 1 Н); 7,06 (дд,J=8,8, 2,4 Гц, 1 Н); 6,86-6,79 (м, 4 Н); 4,14 (т, J=5,6 Гц, 2 Н); 2,76 (т, J=5,6 Гц, 2 Н); 2,53-2,53 (м, 4 Н); 1,651,59 (м, 4 Н); 1,50-1,46 (м, 2 Н). Подготовительный пример 6. 6-Бензилокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2 иловый эфир трифторметансульфоновой кислоты 6-Гидрокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (9,00 г, 17,2 ммоль) растворяют в ТГФ (540 мл). Перемешивают раствор при 0 С в атмосфере азота и добавляют бензиловый спирт (2,78 г, 25,8 ммоль), полимер-PPh3 (8,60 г, 25,8 ммоль) и двухвалентный радикал (DIAD) (5,21 г, 25,8 ммоль). Реакционную смесь продолжают перемешивать в течение 2 ч при комнатной температуре. Добавляют воду (1000 мл) и экстрагируют водный слой CH2Cl2(3500 мл). Органические слои объединяют и сушат с помощью Na2SO4, фильтруют, концентрируют и очищают колоночной флэш-хроматографией (силикагель, 0-4% MeOH:NH4OH (10/1, об./об.)/CH2Cl2) с получением 10,0 г (96%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=614,1 6-Бензилокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,00 г, 1,63 ммоль) растворяют в 20 мл ацетонитрила, добавляют 2 фторбензолбороновую кислоту (0,46 г, 3,26 ммоль) и транс[дихлор-бис-(трифенилфосфин)]палладий(II)(0,23 г, 0,33 ммоль) и обрабатывают ультразвуком в течение короткого промежутка времени. Далее добавляют фторид цезия (2,23 г, 14,67 ммоль) и нагревают до 75 С в течение 1 ч. Добавляют целит и фильтруют. Растворитель концентрируют в вакууме, растворяют остаток в метаноле и очищают с помощью картриджа с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с выделением 550 мг указанного в заголовке соединения (60%). Пример 36. Гидрохлорид[6-Бензилокси-2-(2-фторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-ил)этокси)фенил]метанон (0,55 г,0,98 ммоль) растворяют в 25 мл этанола и после продувания азотом добавляют 10% палладий-на-угле (60 мг) и водород (1 атм.). Через 12 ч фильтруют через целит и растворитель концентрируют в вакууме,очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с выделением 350 мг указанного в заголовке соединения (76%). Превращают в гидрохлорид с получением указанного в заголовке соединения.[6-Метокси-2-(2,4,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фе 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (752 мг, 1,4 ммоль), 2,4,6-трифторфенилбороновую кислоту (4 93 мг, 2,8 ммоль), фосфат калия (1,8 г, 8,4 ммоль) и тетракис(трифенилфосфин)палладий (324 мг, 0,3 ммоль) растворяют в сухом ДМФА (25 мл) и нагревают при 100 С в течение 20 мин, Реакционную смесь очищают на колонке с интенсивным катионным обменом (SCX) с получением 674 мг (93%) указанного в заголовке соединения: масс-спектр (распыление ионов): m/z=520,2 (M+H). Пример 38. [6-Гидрокси-2-(2,4,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон.[6-Метокси-2-(2,4,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (670 мг,1,3 ммоль) растворяют в дихлорметане (10 мл). Охлаждают до 0 С, добавляют 2 М HCl (1,3 мл, 2,6 ммоль) и перемешивают при комнатной температуре в течение 15 мин. Концентрируют в вакууме. Соль растворяют в дихлорметане (10 мл) и охлаждают до 0 С. Добавляют по каплям трибромид бора (1,1 г, 3,9 ммоль) и доводят до комнатной температуры. Реакционную смесь перемешивают в течение 1,5 ч и затем выливают в смесь льда, насыщенного раствора бикарбоната натрия (10 мл) и метанола (10 мл). Экстрагируют дихлорметаном, экстракты объединяют и промывают водой и насыщенным раствором бикарбоната натрия. Сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Очищают хроматографией на силикагеле с использованием градиента 1-3% метанола в дихлорметане, получая 454 мг (70%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=506,3 (М+Н). Подготовительный пример 7. 6-Метансульфонилокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты 6-Гидрокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (12,5 г, 24 ммоль) суспендируют в сухом метиленхлориде (100 мл). Добавляют диизопропилэтиламин (8,3 мл, 48 ммоль). Медленно добавляют метансульфонилхлорид (2,7 мл, 36 ммоль). Через 20 мин реакционную смесь выливают в насыщенный водный раствор бикарбоната натрия и экстрагируют метиленхлоридом. Органический слой промывают водой, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме с получением 14,2 г (99%) указанного в заголовке соединения. Пример 39. [6-Гидрокси-2-(2,3,5-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон 6-Метансульфонилокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (7,0 г, 11,6 ммоль) растворяют в дегазированном ацетонитриле (100 мл). Добавляют фторид цезия (9,1 г, 58 ммоль) и бис-(ацетат)-бис-(трифенилфосфин)палладий (0,87 г, 1,2 ммоль) с последующим добавлением бис-(неопентилгликолят)дибора (3,1 г, 13,9 ммоль) и погружают колбу в масляную баню при температуре 75 С в атмосфере азота. Через 15 мин к реакционной смеси добавляют 1-бром-2,3,5-трифторбензол (4,9 г, 23,2 ммоль) и бис-(ацетат)-бис-(трифенилфосфин)палладий(200 мг) и перемешивают при 75 С в течение 2,5 ч. Реакционную смесь охлаждают до комнатной температуры и фильтруют через целит. Фильтрат концентрируют в вакууме и растворяют остаток в метаноле(100 мл). Добавляют KOH (5 г) и перемешивают при комнатной температуре в течение ночи. Реакционную смесь выливают в насыщенный водный раствор хлорида аммония и экстрагируют метиленхлоридом. Органический слой сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Очищают на силикагеле (от 0 до 6% метанола в метиленхлориде) с получением 3,7 г (64%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=506,3 (М+Н).[6-Метокси-2-(2,3,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фе Осуществляют взаимодействие 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2 илового эфира трифторметансульфоновой кислоты (1,81 г, 3,37 ммоль) с 2-бром-1,3,4-трифторбензолом(0,79 г, 1,52 ммоль) деметилируют с помощью BBr3 по методике, сходной с описанной для получения 2(2,4-дифторфенил)-6-гидроксинафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанона, получая 0,67 г (88%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=506,3 (M+H). Пример 42. [6-Метокси-2-(2,3,4-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (2,13 г, 4,0 ммоль), 2,3,4-трифторфенилбороновую кислоту (1,0 г, 5,7 ммоль), трансдихлор-бис-(трифенилфосфин)палладий(II) (561 мг, 0,8 ммоль) и фторид цезия (5,5 г, 36 ммоль) и добавляют 50 мл ацетонитрила. Смесь нагревают при 80 С в течение 4 ч. Смесь охлаждают и фильтруют, затем очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с диоксидом кремния, элюируя смесью 2% 2 N аммиак/метанол/метиленхлорид, с получением 880 мг (43%) указанного в заголовке соединения. 1 Н-ЯМР(880 мг, 1,69 ммоль) растворяют в 100 мл метиленхлорида и охлаждают на льду. Добавляют 4,0 мл неразбавленного трибромида бора с вихревым перемешиванием и перемешивают на ледяной бане в течение 30 мин. Смеси дают нагреться до комнатной температуры и перешивают в течение еще 1 ч. Смесь осторожно выливают в двухфазную систему, состоящую из насыщенного раствора бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой отделяют, сушат над молекулярными ситами 3 и выпаривают с получением 800 мг слегка загрязненного продукта. Очищают на колонке с силикагелем,элюируя 3% метанолом в метиленхлориде, с получением 635 мг (74%) указанного в заголовке соединения. 1 Н-ЯМР (CD3OD, 400 МГц)7,89 (д, J=8,8 Гц, 1 Н); 7,69-7,42 (м, 4 Н); 7,45-7,42 (м, 1 Н); 7,31 (д, J=2,4 Гц, 1 Н); 7,14 (дд, J=9,2, 2,4 Гц, 1 Н); 7,02-6,87 (м, 3 Н); 4,20 (т, J=5,6 Гц, 2 Н); 2,84 (т, J=5,6 Гц, 2 Н); 2,592,59 (м, 4 Н); 1,71-1,65 (м, 4 Н); 1,56-1,53 (м, 2 Н). Пример 44. В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (2,0 г, 3,7 ммоль), 2,3-дифторфенилбороновую кислоту (1,17 г, 7,4 ммоль), дихлорид бис-(трифенилфосфин)палладия (518 мг, 0,74 ммоль) и фторид цезия (5,06 г, 33,3 ммоль) и добавляют 250 мл дегазированного ацетонитрила. Смесь нагревают при 85 С в течение 2 ч, затем охлаждают и отфильтровывают любые твердые вещества. Очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем,- 18016613 элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 1,3 г (70%) указанного в заголовке соединения. 1 Н-ЯМР (CD3OD, 400 МГц)7,92 (д, J=8,8 Гц, 1 Н); 7,54 (дд, J=8,4, 4,0 Гц, 3 Н); 7,43 дд, J=8,4, 1,6 Гц, 1 Н); 7,31 (д, J=2,8 Гц, 1 Н); 7,09 (дд, J=9,2, 2,4 Гц, 1 Н); 7,05-6,92 (м, 3 Н); 6,79 (д, J=8,8 Гц, 2 Н); 4,10 (т, J=5,6 Гц, 2 Н); 3,93 (с, 3 Н); 2,73 (т, J=5,2 Гц, 2 Н); 2,50-2,50 (м, 4 Н); 1,62-1,57 (м, 4 Н); 1,481,43 (м, 2 Н). Пример 45.[2-(2,3-дифторфенил)-6-гидроксинафталин-1-ил]-[4-(2-пиперидин-1 илэтокси)фенил]метанон (1,3 г, 2,6 ммоль) и добавляют 200 мл метиленхлорида с последующим добавлением 25 мл HCl в эфире, после чего упаривают досуха. Полученное твердое вещество растворяют в 200 мл метиленхлорида и охлаждают раствор на льду. К полученному раствору добавляют трибромид бора(4,0 мл, 42,4 ммоль) при вихревом перемешивании. Раствор перемешивают при комнатной температуре в течение 1 ч до момента, когда все исходные вещества прореагируют. Выливают в двухфазную смесь,состоящую из насыщенного раствора бикарбоната натрия в качестве водной фазы и смеси хлороформ/изопропанол 3:1 в качестве органической фазы, и экстрагируют с использованием делительной воронки. Органический слой отделяют и сушат над молекулярными ситами 3. Очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, и собирают первую фракцию,которая содержит продукт, с получением 400 мг (32%) указанного в заголовке соединения. 1 Н-ЯМР(CD3OD, 400 МГц)7,84 (д, J=8,4 Гц, 1 Н); 7,55 (д, J=9,2 Гц, 2 Н); 7,50 (д, J=8,8 Гц, 1 Н); 7,40 (дд, J=9,2, 1,6 Гц, 1 Н); 7,25 (д, J=2,4 Гц, 1 Н); 7,10-7,03 (м, 2 Н); 6,99-6,95 (м, 2 Н); 6,83 (д, J=9,2 Гц, 2 Н); 4,12 (т, J=5,2 Гц,2 Н); 2,76-2,73 (м, 2 Н); 2,58-2,52 (м, 4 Н); 1,64-1,58 (м, 4 Н); 1,49-1,45 (м, 2 Н). Подготовительный пример 8. 6-Гидрокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2 иловый эфир трифторметансульфоновой кислоты 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (240 г, 430 ммоль) растворяют в дихлорэтане (1,5 л). Охлаждают до 0 С. Реакционную смесь продувают хлористым водородом (36 г, 1 моль). Трихлорид бора (250 г, 2,1 моль) конденсируют в дополнительной воронке с кожухом и по каплям добавляют к реакционной смеси. Перемешивают в течение 48-72 ч. Реакционную смесь осторожно добавляют к смеси 5 М гидроксида натрия (700 мл), воды(500 мл) и дихлорметана (1 л) при 0 С. Доводят рН до 7 с помощью 50% водного раствора гидроксида натрия. Разбавляют 1 М бикарбонатом натрия (1,7 л) и дихлорметаном (500 мл). Органический слой отделяют. Промывают водой с дихлорметаном (1 л). Органические слои объединяют и сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Продукт суспендируют в дихлорметане (200 мл) с получением 196,2 г (87%) указанного в заголовке соединения. Пример 46. Гидрохлорид В колбу помещают 6-гидрокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (500 мг, 0,96 ммоль) и добавляют 10 мл воды вместе с 2 мл 1,2 диметоксиэтана. К полученной смеси добавляют 3-фторфенилбороновую кислоту (270 мг, 1,91 ммоль),трансдихлор-бис-(трифенилфосфин)палладий(II) (130 мг, 0,19 ммоль) и карбонат натрия (920 мг, 8,64 ммоль). Смесь нагревают до 80 С и выдерживают в течение 1 ч. Смесь охлаждают и фильтруют, очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Концентрируют и очищают на колонке с силикагелем, элюируя градиентом 0-10% 2 N аммиака в смеси метанол/метиленхлорид. Концентрируют и превращают в гидрохлорид. 1 Н-ЯМР (CDCl3, 300 МГц)7,76 (д,J=8,7 Гц, 1 Н); 7,52-7,41 (м, 5 Н); 7,21-6,96 (м, 4 Н); 6,89-6,86 (м, 1 Н); 6,52 (д, J=9,0 Гц, 2 Н); 4,09-4,05 (т,2 Н); 2,78-2,78 (м, 2 Н); 2,56 (с, 4 Н); 1,67-1,63 (м, 4 Н); 1,48-1,46 (м, 2 Н). Подготовительный пример 9. 1-[4-(2-Азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты 4-(2-Азепан-1-илэтокси)бензоилхлорид (79,4 г, 249 ммоль) и 2,6-диметоксинафталин (37,8 г, 201 ммоль) растворяют в дихлорметане (800 мл). Охлаждают до -5 С и добавляют трихлорид алюминия (134 г, 1 моль). Нагревают до комнатной температуры и перемешивают в течение ночи. Добавляют охлажденную воду (1,5 л) и энергично перемешивают в течение 1 ч. Смесь декантируют, отделяя остаток и органический слой. Водный слой промывают дихлорметаном (500 мл). Объединяют с остатком из реакционного сосуда и промывают насыщенным водным раствором бикарбоната натрия (1 л). После длительного перемешивания (2 ч) органический слой отделяют и водный слой промывают дихлорметаном (300 мл). Органические слои объединяют и добавляют DARCO (30 г), силикагель (30 г) и сульфат магния. Фильтруют и концентрируют в вакууме с получением 72,4 г [4-(2-азепан-1-илэтокси)фенил]-(2-гидрокси-6 метоксинафталин-1-ил)метанона (73%).[4-(2-Азепан-1-илэтокси)фенил]-(2-гидрокси-6-метоксинафталин-1-ил)метанон (41,0 г, 88,0 ммоль) и триэтиламин (28,8 г, 284 ммоль) растворяют в дихлорметане (400 мл). Охлаждают до -60 С и добавляют трифторметансульфоновый ангидрид (39,8 г, 141 ммоль) в дихлорметане (100 мл). Нагревают до комнатной температуры и перемешивают. Разбавляют насыщенным водным раствором бикарбоната натрия(500 мл) и отделяют органический слой. Водный слой промывают дихлорметаном (200 мл). Органические слои объединяют и промывают насыщенным водным раствором хлорида натрия. Сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают колоночной хроматографией с использованием колонки с силикагелем, элюируя линейным градиентом, который начинается с дихлорметана и заканчивается смесью дихлорметан/метанол 30:1, с получением 48,6 г указанного в заголовке соединения (96%). Альтернативный синтез 1-[4-(2-азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-илового эфира трифторметансульфоновой кислоты. Гидрид натрия (18 г, 0,45 моль) добавляют к раствору 4-бензилоксифенола (41 г, 0,20 моль) и гидрохлорида 2-(гексаметиленимино)этилхлорида (44 г, 0,22 ммоль) в ТГФ (600 мл) и ДМФА (100 мл) при комнатной температуре. Нагревают до 60 С и выдерживают 30 мин. Раствор выливают в смесь воды и льда. Разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой сушат с помощью сульфата магния, фильтруют и концентрируют при пониженном давлении с получением коричневого масла. Полученное масло растворяют в этилацетате (500 мл) и метаноле (500 мл). Добавляют формиат аммония(100 г, 1,59 моль) и палладий-на-угле (10 г, 9,4 ммоль). Кипятят с обратным холодильником в течение 30 мин. Добавляют формиат аммония (100 г, 1,5 9 моль) и палладий-на-угле (10 г, 9,4 ммоль). Реакционную смесь нагревают в течение 30 мин. Суспензию фильтруют через слой целита и элюируют этилацетатом(500 мл). Растворитель выпаривают при пониженном давлении и добавляют воду (100 мл). Смесь разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой промывают насыщенным раствором бикарбоната натрия (2200 мл), сушат с помощью сульфата магния, фильтруют и выпаривают растворитель при пониженном давлении с получением 31 г (64%) 4-(2-азепан-1-илэтокси)фенола. Смешивают 2-бензилокси-1-бром-6-метоксинафталин (31 г, 90 ммоль), 4-(2-азепан-1 илэтокси)фенол (31 г, 132 ммоль), медную бронзу (12 г, 189 ммоль), карбонат калия (25 г, 181 ммоль) и пиридин (400 мл). Реакционную смесь кипятят с обратным холодильником в течение 85 ч. Остаток охлаждают и отфильтровывают через целит, элюируют метанолом и метиленхлоридом (500 мл, 1:5 об./об.). Растворитель выпаривают при пониженном давлении и остаток хроматографируют на колонке с силикагелем, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (от 0 до 10%), с получением 19 г (43%) 1-2-[4-(2-бензилокси-6-метоксинафталин-1-илокси)фенокси]этилазепана. 1-2-[4-(2-Бензилокси-6-метоксинафталин-1-илокси)фенокси]этилазепан (19 г, 38 ммоль) растворяют в этилацетате (500 мл) и метаноле (600 мл). Смесь нагревают до получения прозрачного раствора. Охлаждают до комнатной температуры. Добавляют формиат аммония (30 г, 476 ммоль) и палладий-наугле (2 г, 1,9 ммоль). Кипятят с обратным холодильником в течение 30 мин. Добавляют формиат аммония (7 г, 111 ммоль) и палладий-на-угле (0,7 г, 0,7 ммоль). Кипятят с обратным холодильником в течение 30 мин. Суспензию фильтруют через слой целита и элюируют этилацетатом (500 мл). Растворитель выпаривают при пониженном давлении и добавляют воду (100 мл). Смесь разбавляют этилацетатом (500 мл) и разделяют слои. Органический слой промывают насыщенным раствором бикарбоната натрия(2200 мл), сушат с помощью сульфата магния, фильтруют и выпаривают растворитель при пониженном давлении с получением 15,1 г (97%) 1-[4-(2-азепан-1-илэтокси)фенокси]-6-метоксинафталин-2-ола. Трифторметансульфоновый ангидрид (7 мл, 42 ммоль) добавляют в раствор 1-[4-(2-азепан-1 илэтокси)фенокси]-6-метоксинафталин-2-ола (15 г, 37 ммоль), триэтиламина (20 мл) и метиленхлорида(500 мл) при -50 С. Реакционную смесь нагревают до комнатной температуры и перемешивают при этой температуре в течение 1 ч. Реакционную смесь охлаждают до -78 С и добавляют рассол (20 мл). Реакци- 20016613 онную смесь нагревают до комнатной температуры. Слои разделяют и органический слой промывают насыщенным раствором бикарбоната натрия (100 мл) и рассолом. Органический слой сушат с помощью сульфата магния, фильтруют и растворитель выпаривают при пониженном давлении. Остаток хроматографируют на колонке с силикагелем, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (от 0 до 10%), с получением 20 г (99%) 1-[4-(2-азепан-1-илэтокси)фенокси]-6 метоксинафталин-2-илового эфира трифторметансульфоновой кислоты. Пример 47. [4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,4,6-трифторфенил)нафталин-1-ил]метанон 1-[4-(2-Азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (990 мг, 1,8 ммоль), 2,4,6-трифторфенилбороновую кислоту (634 мг, 3,6 ммоль), фосфат калия(25 мл) и нагревают при 100 С в течение 3 ч. Реакционную смесь очищают на колонке SCX и хроматографией на силикагеле, используя градиент 1-3% метанола в дихлорметане, с получением 320 мг (35%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=534 (M+Н). Пример 48.[4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,4,6-трифторфенил)нафталин-1-ил]метанон (634 мг,1,2 ммоль) растворяют в дихлорметане (10 мл). Охлаждают до 0 С, добавляют HCl (2 М в эфире, 1,2 мл,2,4 ммоль) и перемешивают при комнатной температуре в течение 15 мин. Концентрируют в вакууме. Соль растворяют в дихлорметане (10 мл) и охлаждают до 0 С. Добавляют по каплям трибромид бора(949 мг, 3,6 ммоль) и доводят до комнатной температуры. Реакционную смесь перемешивают в течение 1,5 ч и выливают в смесь льда, насыщенного раствора бикарбоната натрия (20 мл) и метанола (20 мл). Экстрагируют дихлорметаном, экстракты объединяют и промывают водой и насыщенным раствором бикарбоната натрия. Сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Очищают хроматографией на силикагеле, используя градиент 1-3% метанола в дихлорметане, с получением 350 мг (57%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=520 (M+H). Пример 49. [4-(2-Азепан-1-илэтокси)фенил]-[2-(2-фторфенил)-6-метоксинафталин-1-ил]метанон 1-[4-(2-Азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (1,68 г, 3,05 ммоль) растворяют в 30 мл ацетонитрила и добавляют 2-фторбензолбороновую кислоту (0,85 г, 6,10 ммоль), транс[дихлор-бис-(трифенилфосфин)]палладий(II) (0,43 г, 0,61 ммоль) и обрабатывают ультразвуком в течение короткого промежутка времени. Далее добавляют фторид цезия (4,17 г, 27,45 ммоль) и нагревают при 75 С в течение 1 ч. Добавляют целит и фильтруют. Растворитель концентрируют в вакууме, растворяют в метаноле и очищают с помощью картриджа с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем,элюируя градиентом 0-10% смеси метанол/метиленхлорид, с выделением 1,10 г указанного в заголовке соединения (72%). Пример 50. Гидрохлорид [4-(2-азепан-1-илэтокси)фенил]-[2-(2-фторфенил)-6-гидроксинафталин-1 ил]метанона.[4-(2-Азепан-1-илэтокси)фенил]-[2-(2-фторфенил)-6-метоксинафталин-1-ил]метанон (550 мг, 1,11 ммоль) растворяют в 20 мл метиленхлорида и охлаждают на ледяной бане. Добавляют трибромид бора(1,5 мл) и доводят до комнатной температуры. Выливают в двухфазный раствор насыщенного бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой отделяют, промывают водой и сушат над ситами 3. Выпаривают растворитель и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с выделением 268 мг указанного в заголовке соединения в виде свободного основания (50%). Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 5 М хлористо-водородной кислоты и смесь лиофилизуют с получением указанного в заголовке соединения.[4-(2-Азепан-1-илэтокси)фенил]-[2-(2-фторфенил)-6-гидроксинафталин-1-ил]метанон (223 мг, 0,48 ммоль) растворяют в 15 мл тетрагидрофурана. К полученному раствору добавляют 5 мл триэтилборгидрида лития (1 М раствор в тетрагидрофуране). Реакционную смесь разбавляют водой, экстрагируют этилацетатом и концентрируют. Полученный остаток (спиртовой продукт) растворяют в 20 мл метиленхлорида и добавляют триэтилсилан (0,06 мл, 0,40 ммоль) и 1,5 мл трифторуксусной кислоты. Реакционную смесь концентрируют и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 70 мг (31%) указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 5 M хлористо-водородной кислоты и смесь лиофилизуют с получением указанного в заголовке соединения. Пример 52. [4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,3,6-трифторфенил)нафталин-1-ил]метанон Осуществляют взаимодействие 1-[4-(2-азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-илового эфира трифторметансульфоновой кислоты (1,48 г, 2,67 ммоль) с 2-бром-1,3,4-трифторбензолом (1,13 г,5,35 ммоль) по методике, сходной с описанной для получения [6-гидрокси-2-(2,3,5 трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанона, с получением 0,66 г (46%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=534,4 (М+Н). Пример 53.[4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,3,6-трифторфенил)нафталин-1-ил]метанон (0,66 г,1,24 ммоль) деметилируют с помощью BBr3 по методике, сходной с получением [4-(2-азепан-1 илэтокси)фенил]-[6-гидрокси-2-(2,4,6-трифторфенил)нафталин-1-ил]метанона, получая 0,53 г (82%) указанного в заголовке соединения. Аналитические данные, полученные для соответствующей соли HCl: масс-спектр (распыление ионов) m/z=520,3 (M-Cl). Пример 54. 4-(2-Азепан-1-илэтокси)фенил]-[2-(2,4-дифторфенил)-6-метоксинафталин-1-ил]метанон Осуществляют взаимодействие 1-[4-(2-азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-илового эфира трифторметансульфоновой кислоты (1,4 г, 2,5 ммоль) и 2,4-дифторфенилбороновой кислоты (1,2 г,7,6 ммоль) по методике, описанной для получения [2-(2,4-дифторфенил)-6-метоксинафталин-1-ил]-[4-(2 пиперидин-1-илэтокси)фенил]метанона, с получением 1,1 г (85%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=516,3 (M+H). Пример 55. Гидрохлорид[4-(2-Азепан-1-илэтокси)фенил]-[2-(2,4-дифторфенил)-6-метоксинафталин-1-ил]метанон (1,1 г, 2,1 ммоль) деметилируют с помощью BBr3 (1,0 мл, 10,5 ммоль) по методике, описанной для получения [2(2,4-дифторфенил)-6-гидроксинафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанона. Очищают на силикагеле (от 0 до 5% метанола в метиленхлориде) с получением 790 мг (75%) указанного в заголовке соединения в виде свободного основания: масс-спектр (распыление ионов) m/z=502,3 (M+H). Превращают в гидрохлорид. Пример 56. [4-(2-Азепан-1-илэтокси)фенил]-[2-(2,6-дифторфенил)-6-метоксинафталин-1-ил]метанон- 22016613 В колбу помещают 1-[4-(2-азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (3,9 г, 7,06 ммоль), 2,6-дифторфенилбороновую кислоту (2,23 г, 14,12 ммоль), фосфат калия (9,0 г, 42,20 ммоль) и тетракис(трифенилфосфин)палладий(0) (1,63 г, 1,40 ммоль) с последующим добавлением 125 мл сухого ДМФА. Смесь нагревают в атмосфере азота при 100 С в течение 90 мин. Охлаждают, фильтруют, выпаривают растворитель и очищают на картридже с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Затем очищают на колонке с силикагелем, элюируя 0-10% метанолом в метиленхлориде. Выход составляет 2,5 г (70%). 1 Н-ЯМР (CDCl3, 400 МГц)7,90 (д, J=8,4 Гц, 1 Н); 7,66-7,61 (м, 3 Н); 7,39 (д, J=8,4 Гц, 1 Н); 7,23-7,22 (м, 1 Н); 7,18-7,08 (м, 2 Н); 6,79-6,74 (м, 4 Н); 4,08-4,05 (т, 2H); 3,95 (с, 3 Н); 2,96-2,89 (т, 2 Н); 2,78-2,75 (м, 4 Н); 1,66-1,59 (м, 8 Н). Пример 57. [4-(2-Азепан-1-илэтокси)фенил]-[2-(2,6-дифторфенил)-6-гидроксинафталин-1-ил]метанон.[4-(2-Азепан-1-илэтокси)фенил]-[2-(2,6-дифторфенил)-6-метоксинафталин-1-ил]метанон (2,5 г, 4,8 ммоль) преобразуют в гидрохлорид и помещают в колбу в виде твердой соли. Продукт растворяют в 200 мл метиленхлорида и охлаждают на льду. К полученной смеси добавляют трибромид бора (5,0 мл, 53,0 ммоль) при вихревом перемешивании. Реакционную смесь перемешивают при комнатной температуре в течение 1 ч и выливают в двухфазную систему насыщенного раствора бикарбоната натрия и органического слоя, состоящего из смеси хлороформ/изопропанол 3:1. Встряхивают, чтобы экстрагировать продукт, отделяют органический слой, сушат над молекулярными ситами 3 и выпаривают растворитель в вакууме. Очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид,с получением 1,3 г (54%) указанного в заголовке соединения. 1 Н-ЯМР (CDCl3, 400 МГц)7,79-7,74 (д,1 Н); 7,58 (д, J=8,4 Гц, 2 Н); 7,50 (д, J=8,8 Гц, 1 Н); 7,33-7,30 (д, 1 Н); 7,17 (д, J=2,4 Гц, 1 Н); 7,16-7,08 (м,1 Н); 6,99-6,95 (дд, 1 Н); 6,77-6,73 (м, 2 Н); 6,68 (д, J=9,2 Гц, 2 Н); 4,11 (т, J=6,0 Гц, 2 Н); 3,05-2,99 (т, 2 Н); 2,90-2,84 (м, 4 Н); 1,71-1,71 (м, 4 Н); 1,63-1,60 (м, 4 Н). Пример 58. [4-(2-Азепан-1-илэтокси)фенил]-[2-(2,5-дифторфенил)-6-метоксинафталин-1-ил]метанон 1-[4-(2-Азепан-1-илэтокси) бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (2,00 г, 3,63 ммоль) растворяют в 5 мл дегазированного ацетонитрила, добавляют 2,5 дифторфенилбороновую кислоту (1,15 г, 7,26 ммоль), транс[дихлор-бис-(трифенилфосфин)]палладий(II)(0,51 г, 0,73 ммоль) и обрабатывают ультразвуком в течение короткого промежутка времени. Далее добавляют фторид цезия (4,96 г, 32,76 ммоль) и нагревают до 75 С, выдерживая при этой температуре 1 ч. Добавляют целит и фильтруют. Растворитель концентрируют в вакууме, остаток растворяют в метаноле и очищают на картридже с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле,с получением 1,74 г (93%) указанного в заголовке соединения. Пример 59.[4-(2-Азепан-1-илэтокси)фенил]-[2-(2,5-дифторфенил)-6-метоксинафталин-1-ил]метанон (1,74 г,3,37 ммоль) растворяют в 20 мл метиленхлорида и охлаждают на льду. К полученному раствору добавляют 2,0 мл трибромида бора (5,3 г, 21,2 ммоль) и дают нагреться до комнатной температуры. Полученную смесь выливают в двухфазный раствор насыщенного бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой отделяют, промывают водой и сушат над ситами 3. Растворитель выпаривают и остаток очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид. Растворитель выпаривают, получая 780 мг (46%) указанного в заголовке соединения. 1 Н-ЯМР (CDCl3, 300 МГц)7,79 (д, J=8,7 Гц, 1 Н); 7,60-7,55 (м, 3 Н); 7,41 (дд, J=8,7, 1,8 Гц, 1 Н); 7,267,21 (м, 1 Н); 7,04-6,82 (м, 4 Н); 6,71-6,68 (м, 2 Н); 4,14-4,14 (м, 2 Н); 3,03-2,97 (м, 2 Н); 2,95-2,88 (м, 4 Н); 1,73-1,58 (м, 8 Н). Пример 60. [4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,3,5-трифторфенил) нафталин-1 ил]метанон 1-[4-(2-Азепан-1-илэтокси)бензоил]-6-метоксинафталин-2-иловый эфир трифторметансульфоновой кислоты (2,60 г, 6,53 ммоль) растворяют в 200 мл ацетонитрила и к полученной смеси добавляют бис(пинаколоато)дибор (1,5 г, 7,96 ммоль), бис-(трициклогексилфосфин)палладий(0) (0,72 г, 1,50 ммоль) и фторид цезия (7,33 г, 67,0 ммоль). Реакционную смесь нагревают до 100 С и выдерживают до тех пор,- 23016613 пока данные ЖХ/МС не покажут, что все исходные вещества прореагировали. К полученной смеси добавляют 1-бром-2,3,5-трифторбензол (2,00 г, 13,06 ммоль) и еще 720 мг палладиевого катализатора, затем нагревают при 80 С в течение 24 ч. Реакционную смесь фильтруют, концентрируют и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 1,85 г[4-(2-Азепан-1-илэтокси)фенил]-[6-метокси-2-(2,3,5-трифторфенил)нафталин-1-ил]метанон (2,85 г,5,34 ммоль) растворяют в 50 мл метиленхлорида и охлаждают до 0 С. Добавляют трибромид бора (3,0 мл, 31,7 ммоль) и дают нагреться до комнатной температуры. Полученную смесь выливают в двухфазную систему насыщенного раствора бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой промывают рассолом и сушат над молекулярными ситами 3. Концентрируют с получением 2,63 г (95%) указанного в заголовке соединения. Подготовительный пример 10. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2 иловый эфир трифторметансульфоновой кислоты(2,6-Диметоксинафталин-1-ил)-[4-(2-пиперидин-1-илэтокси)фенил]метанон (56,0 г, 123 ммоль) растворяют в хлороформе (500 мл). Охлаждают до 0 С. Добавляют трихлорид бора (150 мл, 150 ммоль, 1 М раствор в дихлорметане) и перемешивают в течение 2 ч. Нагревают до комнатной температуры и перемешивают в течение 1,5 ч. После охлаждения до 0 С добавляют еще трихлорид бора (50 мл, 50 ммоль). Нагревают до комнатной температуры и перемешивают в течение ночи. Осторожно добавляют лед и насыщенный водный раствор бикарбоната натрия. Органический слой отделяют и водный слой трижды промывают смесью дихлорметан/изопропанол 3:1. Концентрируют в вакууме и полученный остаток растворяют в дихлорметане. Сушат над сульфатом натрия, декантируют и концентрируют в вакууме. Суспендируют в эфире и фильтруют, промывают гексанами с получением 49,4 г (2-гидрокси-6 метоксинафталин-1-ил)-[4-(2-пиперидин-1-илэтокси)фенил]метанона (99%).(2-Гидрокси-6-метоксинафталин-1-ил)-[4-(2-пиперидин-1-илэтокси)фенил]метанон (12 г, 29,6 ммоль) растворяют в тетрагидрофуране (200 мл). Добавляют алюмогидрид лития (3,0 г, 78,0 ммоль) и реакционную смесь кипятят с обратным холодильником. Дают остыть до комнатной температуры и добавляют лед. Доводят рН смеси до 7 с помощью 5 М хлористо-водородной кислоты. Разбавляют водой(500 мл). Смесь промывают четыре раза дихлорметаном (по 500 мл каждый раз). Органические слои объединяют, сушат над сульфатом натрия, декантируют и концентрируют в вакууме с получением 1 гидрокси-[4-(2-пиперидин-1-илэтокси)фенил]метил-6-метоксинафталин-2-ола. Полученное вещество повторно растворяют в хлороформе и добавляют трифторуксусную кислоту(5,0 мл, 64,9 ммоль) и триэтилсилан (10,0 мл, 62,6 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 1 ч. Охлаждают до комнатной температуры и разбавляют насыщенным водным раствором бикарбоната натрия (300 мл). Органический слой экстрагируют и водный слой промывают трижды дихлорметаном (по 300 мл каждый раз). Органические экстракты объединяют, сушат над сульфатом натрия, декантируют и концентрируют в вакууме. Выделяют остаток, содержащий 6-метокси-1-[4(2-пиперидин-1-илэтокси)бензил]нафталин-2-ол. Остаток очищают на колонке с интенсивным катионным обменом (SCX), элюируя примеси метанолом, затем элюируя продукт 2 N аммиаком в метаноле. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-ол растворяют в дихлорэтане (300 мл) и добавляют N-фенил-бис-(трифторметансульфонимид) (15,0 г, 42,0 ммоль). Добавляют триэтиламин (20 мл, 143,5 ммоль) и кипятят с обратным холодильником в течение 6 ч. Концентрируют в вакууме и полученный остаток очищают колоночной хроматографией с использованием колонки с силикагелем, элюируя линейным градиентом, который начинается с дихлорметана и заканчивается смесью дихлорметан/метанол 20:1, с получением 13,6 г указанного в заголовке соединения (88%). Пример 62. 1-(2-4-[2-(2,5-Дифторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,0 г, 1,91 ммоль) и добавляют 20 мл дегазированного ацетонитрила. К полученному раствору добавляют 2,5-дифторфенилбороновую кислоту (0,6 г, 3,82 ммоль), трансдихлор-бис-(трифенилфосфин)палладий(II) (270 мг, 0,38 ммоль) и фторид цезия (2,61 г, 17,2 ммоль). В- 24016613 течение короткого промежутка времени смесь обрабатывают ультразвуком и нагревают до 75 С. Через 3 ч добавляют небольшое количество кислоты, катализатор и фторид цезия и кипятят в течение ночи. Утром смесь фильтруют и очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид. Концентрируют с получением 430 мг (46%) указанного в заголовке продукта. 1 НЯМР (CDCl3, 300 МГц)7,85 (д, J=9,3 Гц, 1 Н); 7,73 (д, J=8,7 Гц, 1 Н); 7,33 (д, J=8,4 Гц, 1 Н); 7,18 (д, J=2,7 Гц, 1 Н); 7,11-6,89 (м, 4 Н); 6,86-6,82 (м, 2 Н); 6,73-6,69 (м, 2 Н); 4,34-4,19 (д, Н); 4,04-3,99 (т, 2 Н); 3,93 (с,3 Н); 2,72 (т, J=6,3 Гц, 2 Н); 2,47 (т, J=5,1 Гц, 4 Н); 1,58 (квин., J=5,4 Гц, 4 Н); 1,46-1,41 (м, 2 Н). Пример 63. Гидрохлорид 6-(2,5-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2 ола. 1-(2-4-[2-(2,5-Дифторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин растворяют в 20 мл ацетонитрила и охлаждают на ледяной бане. Добавляют 1,5 мл трибромида бора при вихревом перемешивании и дают нагреться до комнатной температуры. Полученную смесь выливают в двухфазную смесь насыщенного раствора бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой промывают водой и сушат над молекулярными ситами 3. Органический слой концентрируют и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид. Растворитель выпаривают и соединение превращают в гидрохлорид, получая 369 мг (82%) указанного в заголовке соединения. 1 Н-ЯМР (CDCl3, 300 МГц)7,77 (д, J=8,7 Гц, 1 Н); 7,61 (д, J=8,1 Гц, 1 Н); 7,28-7,25 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,00 г, 1,91 ммоль) растворяют в 20 мл дегазированного ацетонитрила и добавляют 2,4 дифторфенилбороновую кислоту (0,60 г, 3,82 ммоль), транс[дихлор-бис-(трифенилфосфин)]палладий(II)(0,27 г, 0,38 ммоль) и обрабатывают ультразвуком в течение короткого промежутка времени. Добавляют фторид цезия (2,61 г, 17,19 ммоль) и нагревают до 75 С, выдерживая при этой температуре в течение 1 ч. Добавляют целит и фильтруют. Растворитель концентрируют в вакууме, остаток растворяют в метаноле и очищают на картридже с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле,с выделением указанного в заголовке соединения. Пример 65. Гидрохлорид 6-(2,4-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2 ола. 1-(2-4-[2-(2,4-Дифторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин (0,72 г, 1,48 ммоль) растворяют в 30 мл метиленхлорида и охлаждают на льду. К полученному раствору добавляют 2,0 мл трибромида бора (21,2 ммоль) и дают нагреться до комнатной температуры. Выливают в двухфазный раствор насыщенного бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой отделяют, промывают водой и сушат над ситами 3. Растворитель выпаривают и остаток очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид. Растворитель выпаривают с получением 300 мг (43%) указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 5 М хлористо-водородной кислоты и смесь лиофилизуют с получением указанного в заголовке соединения. Пример 66. 1-(2-4-[2-(4-Фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,0 г, 1,91 ммоль), 4-фторфенилбороновую кислоту (3,8 г, 3,8 ммоль), транс[дихлор-бис(трифенилфосфин)]палладий(II) (266 мг, 0,38 ммоль) и фторид цезия (2,6 г, 17,1 ммоль) растворяют в 125 мл дегазированного ацетонитрила и нагревают при 85 С в течение 8 ч. Охлаждают, фильтруют и очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Выпаривают до состояния масла и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид: масс-спектр (распыление ионов) m/z=470 (М+Н).- 25016613 Пример 67. Гидрохлорид 6-(4-фторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-ола. 1-(2-4-[2-(4-Фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин (500 мг, 1,06 ммоль) растворяют в 250 мл метиленхлорида и охлаждают на льду. К полученной смеси добавляют 1,0 мл трибромида бора при вихревом перемешивании и дают смеси нагреться до комнатной температуры. Через 1 ч добавляют еще 1,0 мл трибромида бора, затем через 30 мин добавляют еще 0,5 мл бромида и снова перемешивают в течение 30 мин. Реакционную смесь выливают в двухфазную систему насыщенного раствора бикарбоната натрия и органического слоя, состоящего из смеси хлороформ/изопропанол 3:1. Встряхивают в делительной воронке, отделяют органический слой и сушат над молекулярными ситами 3. Растворитель выпаривают и очищают остаток на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 300 мг (62%) свободного основания указанного в заголовке соединения. Свободное основание превращают в соль, растворяя его в ацетонитриле и добавляя хлористо-водородную кислоту, и полученный раствор лиофилизуют. Пример 68. 1-(2-4-[2-(2-Фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,0 г, 1,9 ммоль), 2-фторфенилбороновую кислоту (532 мг, 3,8 ммоль), транс[дихлор-бис(трифенилфосфин)]палладий(II) (266 мг, 0,38 ммоль) и фторид цезия (2,6 г, 17,1 ммоль) растворяют в 150 мл дегазированного ацетонитрила и нагревают при 85 С в течение 2 ч. Реакционную смесь охлаждают,фильтруют и очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Концентрируют и очищают остаток на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 560 мг (63%) указанного в заголовке соединения: массспектр (распыление ионов) m/z=470 (M+Н). Пример 69. Гидрохлорид 6-(2-фторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-ола. 1-(2-4-[2-(2-Фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин (560 мг, 1,2 ммоль) растворяют в 250 мл ацетонитрила и охлаждают на льду. Добавляют 2,0 мл трибромида бора при вихревом перемешивании, перемешивают в течение 1 ч и дают нагреться до комнатной температуры. Реакционную смесь выливают в двухфазную систему, содержащую насыщенный раствор бикарбоната натрия и органический слой, состоящий из смеси хлороформ/метанол 3:1. Встряхивают в делительной воронке, отделяют органический слой и сушат над молекулярными ситами. Растворитель выпаривают и остаток очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Растворитель выпаривают до состояния масла и очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 220 мг (48%) указанного в заголовке соединения в виде свободного основания. Превращают в гидрохлорид растворением в ацетонитриле и добавлением хлористо-водородной кислоты и последующей лиофилизацией. Пример 70. 1-(2-4-[2-(3-Фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин В колбу помещают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (2,0 г, 3,82 ммоль), 3-фторфенилбороновую кислоту (1,07 г, 7,64 ммоль), трансдихлор-бис-(трифенилфосфин)палладий(II) (536 мг, 0,7 6 ммоль) и фторид цезия (5,2 г, 34,4 ммоль) вместе со 100 мл дегазированного ацетонитрила и нагревают при 85 С в течение 4 ч или до тех пор, пока весь исходный трифлат не прореагирует. Реакционную смесь охлаждают, фильтруют и очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Выход сырого продукта составляет 1,5 г (83%). Сырой продукт далее очищают на колонке с диоксидом кремния, элюируя 3% метанолом в метиленхлориде, с получением 1,1 г указанного в заголовке соединения(дд, J=6,4, 2,4 Гц, 2 Н); 4,34 (с, 2 Н); 4,07 (т, J=6,0 Гц, 2 Н); 3,93 (с, 3 Н); 2,81 (т, J=6,0 Гц, 2 Н); 2,57-2,57 (м,4 Н); 1,67-1,61 (м, 4 Н); 1,48-1,46 (м, 2 Н). Пример 71. Гидрохлорид 6-(3-фторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-ола. В колбу помещают 1-(2-4-[2-(3-фторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин (1,1 г, 2,3 ммоль), растворенный в 250 мл метиленхлорида и охлажденный на льду. При перемешивании порциями добавляют 6,0 мл неразбавленного трибромида бора и реакционную смесь пере- 26016613 мешивают на льду в течение 1 ч и затем при комнатной температуре в течение 2 ч. Выливают в двухфазную смесь, содержащую насыщенный раствор бикарбоната натрия и органическую фазу, состоящую из смеси хлороформ/изопропанол 3:1. Соединение экстрагируют в органическую фазу с использованием делительной воронки, разделяют фазы и сушат органический слой над молекулярными ситами 3. Выпаривают и очищают остаток на колонке с силикагелем, элюируя 3% метанолом в метиленхлориде. Переводят в гидрохлорид и лиофилизуют с получением 650 мг (57%) указанного в заголовке соединения. 1 Н-ЯМР (данные для свободного основания) (CDCl3, 400 МГц)7,73 (д, J=9,6 Гц, 1 Н); 7,61 (д, J=8,0 Гц,1 Н); 7,32-7,30 (м, 1 Н); 7,28-7,24 (м, Н); 7,15 (д, J=2,0 Гц, 1 Н); 7,04-6,94 (м, 4 Н); 6,79 (д, J=8,4 Гц, 2 Н); 6,62-6,59 (м, 2 Н); 4,28 (с, 2 Н); 4,13 (т, J=5,6 Гц, 2 Н); 2,92-2,92 (м, 2 Н); 2,72-2,64 (м, 4 Н); 1,74 (д, J=4,8 Гц,4 Н); 1,51-1,51 (м, 2 Н). Пример 72. 1-(2-4-[6-Метокси-2-(2,3,4,5-тетрафторфенил)нафталин-1-илметил]феноксиэтил)пиперидин 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (259 мг, 0,49 ммоль), бис-(пинаколато)дибор (151 мг, 0,59 ммоль), бис(трициклогексилфосфин)палладий(0) (75 мг, 0,11 ммоль) и фторид цезия (764 мг, 5,03 ммоль) растворяют в 20 мл дегазированного ацетонитрила и нагревают до 100C в атмосфере азота в герметично укупоренном сосуде. Реакция завершается в течение 10 мин. Охлаждают и добавляют 1-бром-2,3,4,5 тетрафторбензол (224 мг, 0,99 ммоль) вместе с 10 мл ацетонитрила, герметично укупоривают сосуд, продувают азотом и нагревают при 80 С в течение 2 ч. Охлаждают, фильтруют и очищают на колонке с интенсивным катионным обменом (SCX), элюируя 2 N аммиаком в метаноле. Растворитель выпаривают и полученное масло очищают на колонке с силикагелем, элюируя 3% метанолом в метиленхлориде, с получением 188 мг (73%) указанного в заголовке соединения. Пример 73. Гидрохлорид 5-[4-(2-пиперидин-1-илэтокси)бензил]-6-(2,3,4,5-тетрафторфенил)нафталин-2-ола. 1-(2-4-[6-Метокси-2-(2,3,4,5-тетрафторфенил)нафталин-1-илметил]феноксиэтил)пиперидин (180 мг, 0,34 ммоль) растворяют в 50 мл метиленхлорида и охлаждают на льду. Добавляют 2,0 мл трибромида бора и перемешивают на льду в течение 1 ч. Полученную смесь выливают в двухфазную систему, состоящую из насыщенного раствора бикарбоната натрия и органического слоя, содержащего смесь хлороформ/изопропанол 3:1. Встряхивают в делительной воронке, органический слой отделяют, промывают его рассолом и сушат над молекулярными ситами. Растворитель выпаривают и остаток очищают на колонке с силикагелем, элюируя сначала чистым метиленхлоридом, затем 3% метанолом в метиленхлориде. Очистку повторяют с получением 45 мг указанного в заголовке соединения в виде свободного основания (26%). Свободное основание переводят в гидрохлорид растворением в ацетонитриле, добавлением трет-Бутиловый эфир (4-бромфенил)карбаминовой кислоты (3,0 г, 11,0 ммоль) растворяют в N,Nдиметилформамиде (30 мл). Добавляют гидрид натрия (1,1 г, 27,6 ммоль) и перемешивают при комнатной температуре. Добавляют 1-(2-хлорэтилпиперидин)моногидрохлорид (3,0 г, 16,5 ммоль). Перемешивают в течение ночи при комнатной температуре и затем в течение ночи при 60 С. Охлаждают до комнатной температуры и разбавляют этилацетатом и водой. Органический слой отделяют и водный слой промывают этилацетатом. Органические фракции объединяют и промывают насыщенным водным раствором хлорида натрия. Сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают колоночной хроматографией с использованием колонки с силикагелем, элюируя линейным градиентом, который начинается с дихлорметана и заканчивается смесью дихлорметан/метанол 9:1, с получением 1,2 г указанного в заголовке соединения. 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,50 г, 2,86 ммоль) растворяют в 50 мл ацетонитрила и добавляют 2,6 дифторфенилбороновую кислоту (0,90 г, 5,73 ммоль), тетракис(трифенилфосфин)палладий(0) (0,66 г,0,57 ммоль). Затем добавляют фосфат калия (3,64 г, 17,16 ммоль) и нагревают при 80 С в течение 1 ч. Добавляют целит и фильтруют. Растворитель концентрируют в вакууме до получения темного масла,которое растворяют в метаноле и очищают на картридже с интенсивным катионным обменом (SCX),элюируя 2 N аммиаком в метаноле. Далее очищают на колонке с силикагелем, элюируя градиентом 010% смеси метанол/метиленхлорид. Растворитель выпаривают с получением 800 мг (58%) указанного в заголовке соединения. Пример 75. Гидрохлорид 6-(2,6-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2 ола. 1-(2-4-[2-(2,6-Дифторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин (800 мг,1,64 ммоль) растворяют в 20 мл метиленхлорида и охлаждают на ледяной бане. К полученному раствору добавляют 2,0 мл трибромида бора (21,2 ммоль) и дают нагреться до комнатной температуры. Выливают смесь в двухфазный раствор насыщенного бикарбоната натрия и смеси хлороформ/изопропанол 3:1. Органический слой отделяют, промывают водой и сушат над ситами 3. Растворитель выпаривают и остаток очищают на колонке с силикагелем, элюируя градиентом 0-10% смеси метанол/метиленхлорид, с получением 670 мг (86%) указанного в заголовке соединения в виде свободного основания. Свободное основание растворяют в смеси ацетонитрил/вода 1:1. Добавляют соответствующее количество 5 M хлористо-водородной кислоты и смесь лиофилизуют с получением указанного в заголовке соединения. Пример 76. 1-(2-4-[2-(2,3-Дифторфенил)-6-метоксинафталин-1-илметил]феноксиэтил)пиперидин С использованием методики, описанной для получения 1-(2-4-[6-метокси-2-(2,3,4,5 тетрафторфенил)нафталин-1-илметил]феноксиэтил)пиперидина, получают указанное в заголовке соединение с выходом 49%: масс-спектр (распыление ионов) m/z=488 (M+H). Пример 77. Гидрохлорид 6-(2,3-дифторфенил)-5-[4-(2-пиперидин-1-илэтокси)бензил]нафталин-2 ола. С использованием методики, описанной для получения гидрохлорида 5-[4-(2-пиперидин-1 илэтокси)бензил]-6-(2,3,4,5-тетрафторфенил)нафталин-2-ола, получают указанное в заголовке соединение с выходом 39%: масс-спектр (распыление ионов) m/z=474 (M+H). Пример 78. [6-Гидрокси-2-(2,3,5-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон 6-Метансульфонилокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (10,0 г, 16,6 ммоль) растворяют в дегазированном ацетонитриле (100 мл). Добавляют фторид цезия (13,0 г, 83,0 ммоль) и бис-(ацетат)-бис-(трифенилфосфин)палладий (1,2 г, 1,7 ммоль) с последующим добавлением бис-(неопентилгликолят)дибора (4,5 мг, 19,9 ммоль) и погружают колбу в масляную баню при 75 С в атмосфере азота. Через 15 мин к реакционной смеси добавляют 1 бром-2,3,5-трифторбензол (7,0 г, 33,2 ммоль) и бис-(ацетат)-бис-(трифенилфосфин)палладий (500 мг) и перемешивают при 75 С в течение 2,5 ч. Охлаждают до комнатной температуры и фильтруют через целит. Фильтрат концентрируют в вакууме и остаток снова растворяют в метаноле (100 мл). ДобавляютKOH (4 г) и перемешивают при комнатной температуре в течение ночи. Реакционную смесь выливают в насыщенный водный раствор хлорида аммония и экстрагируют метиленхлоридом. Органический слой сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Очищают на 5 колонках с интенсивным катионным обменом (SCX) (загружают в метаноле и элюируют 2 М NH3 в метаноле), полу- 28016613 чая 8,4 г (100%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=506,4 (M+H). Пример 79. 5-Гидрокси-[4-(2-пиперидин-1-илэтокси)фенил]метил-6-(2,3,5-трифторфенил)нафталин-2-ол. В колбу, которую продувают азотом, помещают (R)-(+)-,-дифенил-2-пирролидинметанол (630 мг, 2,49 ммоль), растворяют в 1 М ВН 3-тетрагидрофуране (ТГФ) (66 мл, 66 ммоль) и нагревают до 45 С в атмосфере азота. [6-Гидрокси-2-(2,3,5-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (8,3 г, 16,6 ммоль) растворяют в ТГФ (75 мл) и добавляют по каплям с помощью шприцевого насоса к раствору борана в течение 2,5 ч. Медленно добавляют этаноламин (20 мл, 332 ммоль) и нагревают при 45 С в течение 2 ч. Реакционную смесь выливают в насыщенный водный раствор хлорида аммония и дважды экстрагируют метиленхлоридом. Объединенные органические слои промывают водой, сушат над сульфатом натрия, фильтруют и концентрируют. Полученный остаток растворяют в метиленхлориде (20 мл) и дают медленно осесть. Осадок собирают с выходом 4,3 г (51%) указанного в заголовке соединения с ИЭ 99%. Маточный раствор очищают над силикагелем (элюируя 1-6% метанолом в метиленхлориде) с получением 2,0 г (общий выход 75%) указанного в заголовке соединения с ИЭ 91%. Масс-спектр (распыление ионов): m/z=508,3 6-Метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (752 мг, 1,4 ммоль), 2,4,6-трифторфенилбороновую кислоту (493 мг, 2,8 ммоль), фосфат калия (1,8 г, 8,4 ммоль) и тетракис(трифенилфосфин)палладий (324 мг, 0,3 ммоль) растворяют в сухом диметилформамиде (ДМФА, 25 мл) и нагревают при 100 С в течение 20 мин. Реакционную смесь очищают на колонке с интенсивным катионным обменом (SCX) с получением 674 мг (93%) указанного в заголовке соединения. Масс-спектр (распыление ионов): m/z=520,2 (M+H). Альтернативно, смешивают 6-метокси-1-[4-(2-пиперидин-1-илэтокси)бензоил]нафталин-2-иловый эфир трифторметансульфоновой кислоты (1,93 г, 3,60 ммоль), фторид цезия (5,0 г, 33 ммоль), бис(неопентилгликолят)дибор (1/0 г, 4,4 ммоль), бис-(трициклогексилфосфин)палладий (0,50 г, 0,75 ммоль) и ацетонитрил (50 мл). Смесь нагревают до 90 С, выдерживая при этой температуре 20 мин, с получением раствора темного цвета. Добавляют 2-бром-1,3,5-трифторбензол (5 г, 23,7 ммоль) и нагревают при 90 С в течение 2 ч. Добавляют бис-(трициклогексилфосфин) палладий (0,50 г, 0,75 ммоль) и 2-бром 1,3,5-трифторбензол (5,0 г, 23 ммоль) и нагревают при 90 С в течение 4 ч. Охлаждают до комнатной температуры и фильтруют через слой целита, затем растворитель выпаривают. Остаток очищают на силикагеле, элюируя продукт метанолом в дихлорметане (0-5%), с получением 1,30 г (67%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=520,2 (М+Н). Пример 83. [6-Гидрокси-2-(2,4,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон.[6-Метокси-2-(2,4,6-трифтрофенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (670 мг,1,3 ммоль) растворяют в дихлорметане (10 мл). Охлаждают до 0 С, добавляют 2 M HCl (1,3 мл, 2,6 ммоль) и перемешивают при комнатной температуре в течение 15 мин. Концентрируют в вакууме. Соль растворяют в дихлорметане (10 мл) и охлаждают до 0 С. Добавляют по каплям трибромид бора (1,1 г, 3,9 ммоль) и доводят до комнатной температуры. Реакционную смесь перемешивают в течение 1,5 ч и выливают в смесь льда, насыщенного раствора бикарбоната натрия (10 мл) и метанола (10 мл). Экстрагируют дихлорметаном, объединяют экстракты и промывают водой и насыщенным раствором бикарбоната натрия. Сушат с помощью сульфата натрия, фильтруют и концентрируют в вакууме. Очищают хроматографией на силикагеле, используя градиент 1-3% метанола в дихлорметане, с получением 454 мг (70%) указанного в заголовке соединения. Масс-спектр (распыление ионов): m/z=506,3 (М+Н). Альтернативно, [6-метокси-2-(2,4,6-трифторфенил)нафталин-1-ил]-[4-(2-пиперидин-1-илэтокси)фенил]метанон (1,90 г, 3,67 ммоль) растворяют в дихлорметане (10 мл). Добавляют 2 М HCl в диэтиловом эфире (4,0 мл, 80 ммоль). Полученную суспензию концентрируют и сушат в вакууме. Остаток разбавляют дихлорметаном (30 мл) и гасят азотом. Раствор охлаждают до 0 С на внешней ледяной бане. Добавляют трибромид бора (1 мл, 11 ммоль). Через 60 мин реакционную смесь выливают в смесь льда (20 г),метанола (10 мл) и насыщенного раствора бикарбоната натрия (20 мл). Экстрагируют дихлорметаном(100 мл). Слои разделяют, органический слой промывают рассолом (20 мл), сушат с помощью сульфата магния, фильтруют и концентрируют в вакууме. Остаток очищают на силикагеле, элюируя продукт ступенчатым градиентом смеси метанол/дихлорметан (0-10%), с получением 1,6 г (87%) указанного в заголовке соединения: масс-спектр (распыление ионов) m/z=506,2 (M+H).
МПК / Метки
МПК: A61P 15/12, C07D 335/04, A61K 31/4523, A61K 31/4453, C07D 311/78, C07D 295/08, C07D 221/18, A61K 31/55
Метки: вазомоторных, лечения, рецепторов, симптомов, селективные, модуляторы, эстрогена
Код ссылки
<a href="https://eas.patents.su/30-16613-selektivnye-modulyatory-receptorov-estrogena-dlya-lecheniya-vazomotornyh-simptomov.html" rel="bookmark" title="База патентов Евразийского Союза">Селективные модуляторы рецепторов эстрогена для лечения вазомоторных симптомов</a>
Предыдущий патент: Неводные или водные концентраты действующего вещества с гербицидным действием, их применение и способ борьбы с нежелательным ростом растений
Следующий патент: Соединения для лечения гепатита с
Случайный патент: Катализатор на носителе и способ получения амина


































