8-сульфонил-1,3,4,8-тетрагидро-2н-[1,4]оксазепино[6,7-e]индольные производные и их использование в качестве 5-нт6 рецепторных лигандов
Номер патента: 16456
Опубликовано: 30.05.2012
Авторы: Рингберг Эрик, Линдквист Бенгт, Хаммер Кристин, Бертс Веи, Брандт Петер, Рингом Руне, Хенрикссон Софиа
Формула / Реферат
1. Соединение формулы (I)
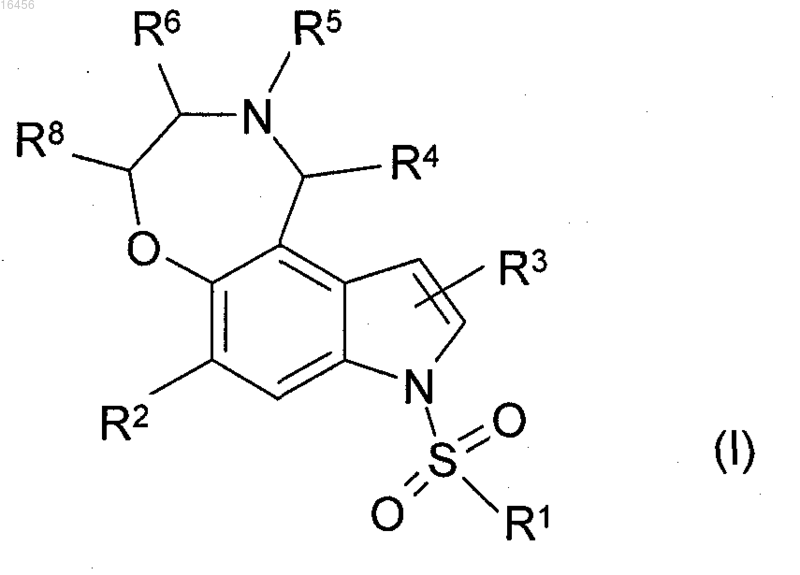
в которой R1 выбирают из фенила, нафтила, пиридинила, изоксазолила, имидазолила, 1,4-бензодиоксинила, бензофуранила, фуранила, 1,3-бензотиазолила, хроманила, тиенила и бензотиенила, каждый из которых необязательно независимо замещен в одном или двух положениях заместителем, выбранным из:
(a) галогена,
(b) C1-3алкила,
(c) фтор-С1-3алкила,
(d) C1-3алкокси,
(e) фтор-С1-3алкокси,
(f) C1-3алкилсульфонила,
(g) -CN и
(h) фенила;
R2 представляет водород, галоген, C1-3алкил, С1-3алкокси;
R3 представляет водород, галоген, С1-3алкил, 1-гидрокси-С1-3алкил, С1-3алкилкарбонил или циклопропилгидрокси-С1-3алкил;
R4 выбирают из водорода или С1-3алкила;
R5 выбирают из водорода, С1-3алкила или фтор-С1-3алкила;
R6 представляет водород;
R8 представляет водород или
R5 и один из R6 и R8 вместе с атомами азота и углерода, к которым они присоединены, образуют пирролидиновое кольцо, а другой из R6 и R8 является водородом;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где
R1 выбирают из фенила, нафтила, пиридинила, изоксазолила, имидазолила, 1,4-бензодиоксинила, бензофуранила, фуранила, 1,3-бензотиазолила, хроманила, тиенила и бензотиенила, каждый из которых необязательно независимо замещен в одном или двух положениях заместителем, выбранным из:
(a) фтора,
(b) хлора,
(c) С1-3алкила,
(d) трифторметила,
(e) метокси,
(f) трифторметокси,
(g) метилсульфонила,
(h) -CN и
(i) фенила;
R2 представляет водород, фтор, метил или метокси;
R3 представляет водород, хлор, метил, 1-гидроксиэтил, 1-гидрокси-1-метилэтил, ацетил, изобутирил или циклопропилгидроксиметил;
R4 выбирают из водорода, метила и изопропила;
R5 выбирают из водорода, метила, этила, изопропила и 2-фторэт-1-ила или
R6 представляет водород;
R8 представляет водород или
R5 и один из R6 и R8 вместе с атомами азота и углерода, к которым они присоединены, образуют пирролидиновое кольцо, а другой из R6 и R8 является водородом.
3. Соединение по п.1 или 2, где
R1 выбирают из фенила, 1-нафтила, 2-нафтила, 3-пиридинила, 4-изоксазолила, 4-имидазолила, 1,4-бензодиоксин-6-ила, 2-бензофуранила, 3-фурила, 1,3-бензотиазол-6-ила, 6-хроменила, 2-тиенила, 3-тиенила, 2-бензотиенила и 3-бензотиенила, каждый из которых необязательно независимо замещен в соответствии с п.1 или 2.
4. Соединение по п.3, которое выбирают из
2,5-метилен-9-(фенилсульфонил)-1,2,3,4,5,9-гексагидро[1,5]оксазоцино[3,2-е]индола;
2,4-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-изопропил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-этил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(2,3-дигидро-1,4-бензодиоксин-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3,4-диметоксифенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1-бензофуран-2-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,5-диметил-3-фурил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1,3-бензотиазол-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-{[4-(метилсульфонил)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-изопропилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,2-диметил-3,4-дигидро-2Н-хромен-6-ил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-хлор-4-фторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3,4-дихлорфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-фторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,6-дифторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-{[4-(трифторметокси)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-(2-нафтилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3-хлор-4-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4,5-дихлор-2-тиенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,4-дихлорфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-{[4-фтор-3-(трифторметил)фенил]сульфонил}-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-(2-тиенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-[(4-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метокси-5-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3-фтор-4-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1-бензотиен-3-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8- [(4-метоксифенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-{[4-(трифторметил)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-метил-8-[(4-пропилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
3-хлор-4-[(2-метил-1,2,3,4-тетрагидро-8Н-[1,4]оксазепино[6,7-е]индол-8-ил)сульфонил]бензонитрила;
8-[(2,5-диметил-3-тиенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-[(2-метил-1,2,3,4-тетрагидро-8Н-[1,4]оксазепино[6,7-е]индол-8-ил)сульфонил]бензонитрила;
2-метил-1-[2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индол-9-ил]пропан-1-она;
1-[2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индол-9-ил]этанона;
9-хлор-2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-[2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индол-9-ил]пропан-2-ола;
циклопропил[2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индол-9-ил]метанола;
1-[2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индол-9-ил]этанола;
10-хлор-2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(7aR)-3-(фенилсульфонил)-3,7а,8,9,10,12-гексагидро-7Н-пиррол[2',1':3,4][1,4]оксазепино[6,7-е]индола;
(7aS)-3-(фенилсульфонил)-3,7а,8,9,10,12-гексагидро-7Н-пиррол[2',1':3,4][1,4]оксазепино[6,7-е]индола;
(3S)-3-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(3S)-2,3-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2,7-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
6-метокси-2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
2-(2-фторэтил)-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метокси-5-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,4-дихлорфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-{[3-(трифторметил)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3,4-диметоксифенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(2-нафтилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метокси-4-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-пропилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-изопропилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1-бензофуран-2-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,5-диметил-3-тиенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(3-фтор-4-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-метоксифенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,5-диметил-3-фурил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(4-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(2-тиенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-{[2-(трифторметокси)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(бифенил-3-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-{[2-(трифторметил)фенил]сульфонил}-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1-бензотиен-2-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-(1-нафтилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(5-фтор-2-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(3R)-3-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(3R)-2,3-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
6-метокси-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
9-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(4-фторфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
3-[(10-хлор-1,2,3,4-тетрагидро-8Н-[1,4]оксазепино[6,7-е]индол-8-ил)сульфонил]бензонитрила;
10-хлор-8-(пиридин-3-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-хлорфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(1S)-1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
(1R)-1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-(фенилсульфонил)-3,8-дигидро-4Н-[1,4]оксазепино[6,7-е]индола;
6-фтор-1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
6-метокси-1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-хлорфенил)сульфонил]-6-метокси-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
6-метокси-1-метил-8-[(2-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,6-дифторфенил)сульфонил]-6-метокси-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
6-метокси-8-[(2-метокси-5-метилфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,4-дихлорфенил)сульфонил]-6-метокси-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-изопропил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-изопропил-2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1,2-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-1-метил-8-(фенилсульфонил)-3,8-дигидро-4Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-1-метил-8-(пиридин-3-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-1-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-1,2-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(2-метокси-5-метилфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(2-метокси-5-метилфенил)сульфонил]-1,2-диметил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(2-фторфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(2-фторфенил)сульфонил]-1,2-диметил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(3-фторфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
10-хлор-8-[(3-фторфенил)сульфонил]-1,2-диметил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-(пиридин-3-илсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-хлорфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-[(2-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2H-[1,4]оксазепино[6,7-е]индола;
8-[(2,6-дифторфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,4-дихлорфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метокси-5-метилфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2-метокси-4-метилфенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,5-диметил-3-тиенил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(2,5-диметил-3-фурил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-(2-тиенилсульфонил)-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
1-метил-8-[(5-метилизоксазол-4-ил)сульфонил]-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола;
8-[(1,2-диметил-1Н-имидазол-4-ил)сульфонил]-1-метил-1,3,4,8-тетрагидро-2Н-[1,4]оксазепино[6,7-е]индола.
5. Фармацевтическая композиция для лечения или профилактики расстройства, связанного с 5-НТ6 рецептором, содержащая соединение по любому из пп.1-4 в качестве активного ингредиента в сочетании с фармацевтически приемлемым разбавителем или носителем.
Текст
Настоящее изобретение относится к соединениям формулы (I), в которой А, X и R1-R9 представляют, как описано в данном изобретении; фармацевтическим композициям, содержащим упомянутые соединения; к способам их приготовления и к применению данных соединений в качестве лекарственных средств против расстройств, связанных с 5-НТ 6 рецептором 016456 Область техники, к которой относится изобретение Настоящее изобретение относится к новым соединениям, к фармацевтическим композициям, содержащим данные соединения, к способам их приготовления, а также к использованию данных соединений для приготовления лекарственного средства против расстройств, связанных с 5-НТ 6 рецептором. Уровень техники Ожирение является состоянием, характеризующимся увеличением содержания жира, приводящим к избыточному весу тела по сравнению с общепринятыми нормами. Ожирение является самым важным расстройством, связанным с питанием, в западном мире и представляет основную проблему для здоровья во всех промышленных странах. Данное расстройство приводит к увеличению смертности в результате увеличения числа случаев заболеваний, таких как сердечно-сосудистые заболевания, расстройства пищеварения, болезни органов дыхания, рак и диабет 2 типа. Поиск соединений, которые снижают вес тела,продолжается в течение многих десятилетий. Одним из направлений исследований была активация серотонинэргических систем, как прямая активация серотониновых рецепторных подтипов, так и ингибирование обратного захвата серотонина. Однако точная требуемая структура рецепторного подтипа неизвестна. Серотонин (5-гидрокситриптамин или 5-НТ), главный нейромедиатор периферической и центральной нервной системы, регулирует широкий диапазон физиологических и патологических функций, включая тревогу, регуляцию сна, агрессию, питание и депрессию. Обнаружено и клонировано множество подтипов серотониновых рецепторов. Один из них, 5-НТ 6 рецептор, был клонирован несколькими группами в 1993 г. (Ruat, M. et al. (1993), Biochem. Biophys. Res. Commun. 193: 268-276; Sebben, M.et al. (1994), NeuroReport. 5: 2553-2557). Данный рецептор безусловно связывается с аденилилциклазой и проявляет сродство к антидепрессантам, таким как клозапин. Недавно сообщалось о действии 5-НТ 6 антагониста и 5-НТ 6 антисмысловых олигонуклеотидов для того, чтобы снизить потребление крысами пищи (Bentley, J.С. et al. (1999), Br. J. Pharmacol. Suppl. 126, P66; Bentley, J.C. et al. (1997), J.Psychopharmacol. Suppl. A64, 255; Woolley M.L. et al. (2001), Neuropharmacology. 41: 210-219). Были обнаружены соединения с повышенным сродством и селективностью по отношению к 5-НТ 6 рецептору, например, в WO 00/34242 и у Isaac, M. et al. (2000), 6-Bicyclopiperazinyl-1-arylsulphonylindolesChemistry Letters. 13: 3355-3359 (2003), Expert Opinion Therapeutic Patents. 12(4): 513-527 (2002). Описание изобретения Неожиданно было найдено, что соединения настоящего изобретения проявляют сродство к 5-НТ 6 рецептору при наномолярных концентрациях. Соединения настоящего изобретения и их фармацевтически приемлемые соли обладают активностью антагониста 5-НТ 6 рецептора, агониста и частичного агониста, предпочтительно активностью антагониста и считают, что их можно использовать для лечения или профилактики ожирения и диабета 2 типа для того, чтобы добиться снижения веса тела и замедления набора веса тела так же, как для лечения или профилактики расстройств центральной нервной системы,таких как тревога, депрессия, приступ панического расстройства, расстройства памяти, когнитивные расстройства, эпилепсия, расстройства сна, мигрень, анорексия, булимия, компульсивное переедание, обсессивно-компульсивные расстройства, психозы, болезнь Альцгеймера, болезнь Паркинсона, хорея Гентингтона и/или шизофрения, приступ панического расстройства, синдром дефицита внимания с гиперактивностью (ADHD), наркотическая абстиненция (например, злоупотребление амфетамином, кокаиновая абстиненция и/или никотиновая), нейродегенеративные расстройства, характеризующиеся ослабленным ростом нейронов, и боль. Снижения веса тела и замедления набора веса тела (например, лечение нарушений веса тела) достигают наряду с прочим снижением потребления пищевых продуктов. Как используется в данном описании, термин "нарушения веса тела" относится к нарушениям, вызванным дисбалансом между потребляемой и расходуемой энергией, приводящим к ненормальному (например, избыточному) весу тела. Такие нарушения веса тела включают, но не ограничиваются ими, ожирение, избыточную массу тела, анорексию, кахексию, резистентность к инсулину и диабет. Настоящее изобретение относится к соединению формулы (I) в которой R1 выбирают из фенила, нафтила, пиридинила, изоксазолила, имидазолила,1,4-бензодиоксинила, бензофуранила, фуранила, 1,3-бензотиазолила, хроманила, тиенила и бензотиенила, каждый из которых необязательно независимо замещен в одном или двух положениях заместителем,выбранным из:R4 выбирают из водорода или C1-3 алкила;R5 и один из R6 и R8 вместе с атомами азота и углерода, к которым они присоединены, образуют пирролидиновое кольцо, а другой из R6 и R8 является водородом; или его фармацевтически приемлемой соли. Предпочтительны соединения формулы (I), где R1 выбирают из фенила, нафтила, пиридинила, изоксазолила, имидазолила, 1,4-бензодиоксинила, бензофуранила, фуранила, 1,3-бензотиазолила, хроманила, тиенила и бензотиенила, каждый из которых необязательно независимо замещен в одном или двух положениях заместителем, выбранным из:R5 и один из R6 и R8 вместе с атомами азота и углерода, к которым они присоединены, образуют пирролидиновое кольцо, а другой из R6 и R8 является водородом. Ещ более предпочтительны соединения формулы (I), где R1 выбирают из фенила, 1-нафтила,2-нафтила, 3-пиридинила, 4-изоксазолила, 4-имидазолила, 1,4-бензодиоксин-6-ила, 2-бензофуранила,3-фурила, 1,3-бензотиазол-6-ила, 6-хроменила, 2-тиенила, 3-тиенила, 2-бензотиенила и 3-бензотиенила,каждый из которых необязательно независимо замещен в соответствии с п.1 или 2. Наиболее предпочтительны следующие соединения формулы (I): 2,5-метилен-9-(фенилсульфонил)-1,2,3,4,5,9-гексагидро[1,5]оксазоцино[3,2-е]индол; 2,4-диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 2-изопропил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 2-этил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 2-метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 8-(2,3-дигидро-1,4-бензодиоксин-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол; 8-[(3,4-диметоксифенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 8-(1-бензофуран-2-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 8-[(2,5-диметил-3-фурил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 8-(1,3-бензотиазол-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 2-метил-8-[4-(метилсульфонил)фенил]сульфонил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7 е]индол; 8-[(4-изопропилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол; 8-[(2,2-диметил-3,4-дигидро-2 Н-хромен-6-ил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол; 8-[(2-хлор-4-фторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол;-4 016456 и их фармацевтически приемлемые соли. Соединения формулы (I) могут быть агонистами, частичными агонистами или антагонистами 5-НТ 6 рецептора. Предпочтительно соединения действуют как частичные агонисты или антагонисты 5-НТ 6 рецептора. Более предпочтительно соединения действуют как антагонисты 5-НТ 6 рецептора. Термин "частичный агонист 5-НТ 6 рецептора" относится к соединению, которое связывается с человеческим 5-НТ 6 рецептором и не вызывает полный антагонизм образования сАМР, вызванное 5-НТ, в испытании на внутреннюю активность, описанном в данном изобретении (см. "Биологические испытания"). Примеры расстройств, связанных с 5-НТ 6 рецептором, включают ожирение и диабет 2 типа, расстройства центральной нервной системы, такие как тревога, депрессия, приступ панического расстройства, расстройства памяти, когнитивные расстройства, эпилепсия, расстройства сна, мигрень, анорексия,булимия, компульсивное переедание, обсессивно-компульсивные расстройства, психозы, болезнь Альцгеймера, болезнь Паркинсона, хорея Гентингтона, шизофрения, синдром дефицита внимания с гиперактивностью (ADHD), наркотическая абстиненция (например, злоупотребление амфетамином, кокаиновая абстиненция и/или никотиновая), нейродегенеративные расстройства, характеризующиеся ослабленным ростом нейронов, и боль. Другим объектом настоящего изобретения является фармацевтическая композиция, содержащая соединение формулы (I) в качестве активного ингредиента, в комбинации с фармацевтически приемлемым разбавителем или носителем. Эта композиция предназначена для лечения или профилактики расстройства, связанного с 5-НТ 6 рецептором. Химические структуры в схемах в данном описании изображают переменные, которые таким образом определяют соизмеримо с определениями химических групп (частиц, атомов и т.д.) соответствующего положения в формулах соединений в данном описании, обозначены ли они тем же самым именем переменной (например, R1, R2, R, R1, X и т.д.) или нет. Химические реагенты, используемые в описанных в данном изобретении синтетических подходах,включают, например, растворители, реагенты, катализаторы и реагенты для введения и удаления защитных групп. Способы, описанные выше, могут также дополнительно включать стадии как перед, так и после стадий, описанных специально в данном изобретении, чтобы ввести или удалить подходящие защитные группы для того, чтобы в конце концов позволить синтезировать соединения. Кроме того, можно проводить различные синтетические стадии в альтернативной последовательности или порядке, чтобы получить требуемые соединения. Превращения в синтетической химии, пригодные для синтеза подходящих соединений, известны в данной области техники и включают, например,превращения, описанные в R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989);Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John WileySons (1995) и последующих их изданиях. Способы проведения реакций, описанных выше, хорошо известны специалистам в данной области техники. Необходимые исходные вещества для приготовления соединений формулы (I) являются или известными, или могут быть приготовлены по аналогии с приготовлением известных соединений. Соединения формулы (I) могут содержать один или более хиральных атомов углерода и их, следовательно, можно получить в форме оптических изомеров, например в виде чистого энантиомера, или в виде смеси энантиомеров (рацемата), или в виде смеси, содержащей диастереомеры. Разделение смесей оптических изомеров, чтобы получить чистые энантиомеры, является хорошо известным и может, например, достигаться фракционной кристаллизацией солей с оптически активными (хиральными) кислотами или хроматографическим разделением на хиральных колонках. Все возможные изомерные формы(чистые энантиомеры, диастереомеры, таутомеры, рацемические смеси и неравные смеси двух энантиомеров) описанных соединений включены в объем данного изобретения. Когда соединения, описанные в данном изобретении, содержат олефиновые двойные связи геометрической асимметрии, подразумевается, что они включают оба транс- и цис- (Е- и Z-) геометрических изомера. Соединения формулы (I) можно использовать как таковые или, по необходимости, в виде их фармакологически приемлемых солей (соли присоединения основания или кислоты). Подразумевают, что упомянутые выше фармакологически приемлемые соли присоединения включают терапевтически активные нетоксические формы солей присоединения кислоты или основания, которые способны образовывать соединения. Соединения, которые обладают основными свойствами, можно превратить в фармацевтически приемлемые кислотно-аддитивные соли обработкой основной формы подходящей кислотой. Примеры кислот включают неорганические кислоты, такие как хлористо-водородная, бромисто-водородная,йодисто-водородная, серная, фосфорная кислоты; и органические кислоты, такие как муравьиная, уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, гликолевая, малеиновая, малоновая,щавелевая, бензолсульлфокислота, толуолсульфокислота, метансульфокислота, трифторуксусная, фумаровая, янтарная, яблочная, винная, лимонная, салициловая, п-аминосалициловая, памовая, бензойная,аскорбиновая кислоты и подобные. Примерами солей присоединения оснований являются соли натрия,калия, кальция и соли с фармацевтически приемлемыми аминами, такими как, например, аммиак, алкиламины, бензатин, и аминокислотами, такими как, например, аргинин и лизин. Термин "соль присоеди-5 016456 нения", как используется в данном описании, также включает сольваты, которые способны образовывать соединения и их соли, такие как, например, гидраты, алкоголяты и подобные. Для клинического использования соединения данного изобретения формулируют в фармацевтические рецептуры для перорального, ректального, парентерального или других режимов введения. Фармацевтические рецептуры обычно приготавливают смешиванием активного вещества или его фармацевтически приемлемой соли с общепринятыми фармацевтическими вспомогательными веществами. Примерами вспомогательных веществ являются вода, желатин, аравийская камедь, лактоза, микрокристаллическая целлюлоза, крахмал, крахмалгликолят натрия, гидрофосфат кальция, стеарат магния, тальк, коллоидный диоксид кремния и подобные. Такие рецептуры могут также включать другие фармакологически активные агенты и общепринятые вспомогательные вещества, такие как стабилизаторы, смачивающие агенты, эмульгаторы, ароматизирующие вещества, буферы и подобные. Обычно количество активных соединений составляет 0,1-95 вес.% препарата, предпочтительно 0,2-20 вес.% в препаратах для парентерального использования и более предпочтительно 1-50 вес.% в препаратах для перорального приема. Рецептуры можно, кроме того, приготавливать известными способами, такими как гранулирование,компрессия, микроинкапсулирование, нанесение покрытия распылением и т.д. Рецептуры можно приготовить общепринятыми способами в дозовых формах в виде таблеток, капсул, гранул, порошков, сиропов, суспензий, суппозиториев или инъекций. Жидкие рецептуры можно приготовить растворением или суспендированием активного вещества в воде или других подходящих средах. Таблетки и гранулы можно приготовить общепринятым способом. Доза конкретного соединения и частота приема доз будет изменяться в зависимости от факторов,включая активности конкретного применяемого соединения, метаболической стабильности и продолжительности действия данного соединения, возраста пациента, веса тела, общего состояния здоровья, пола,диеты, способа и продолжительности введения, скорости экскреции, сочетания с другими лекарственными средствами, сложности лечимого состояния и пациента, подвергнутого лечению. Дневная доза может,например, варьироваться от 0,001 до приблизительно 100 мг на килограмм веса тела, принимаемая в виде одной или множества доз, например от приблизительно 0,01 до приблизительно 25 мг каждая. Обычно такая доза дается перорально, но может также быть выбран парентеральный прием. Косметические композиции обладают активностью ингредиентов, смешанных с разбавителем,вспомогательным веществом или носителем, приспособленным для перорального приема, и могут содержать, например, воду, желатин, лактозу, крахмал, тальк, вазелин, аравийскую камедь, полиалкиленгликоли и стеарат магния. Косметические композиции могут быть в форме таблеток, порошков, гранул,пастилок, желатиновых капсул, суспензий или растворов. Таблетки, порошки, гранулы, пастилки или желатиновые капсулы могут содержать связующие вещества, наполнители, порошкообразные носители; растворы или суспензии могут содержать разбавители, растворители и загустители. Определения Следующие определения будут применяться во всем описании и прилагаемой формуле изобретения. Если не указано особо, термин "C1-6 алкил" обозначает прямую или разветвленную алкильную группу, имеющую от 1 до 6 атомов углерода. Примеры упомянутого C1-6 алкила включают метил, этил,н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил и гексил с прямой и разветвленной цепью. Для частей диапазона "C1-6 алкил" предполагаются все их подгруппы, такие как C1-5 алкил,C1-4 алкил, C1-3 алкил, C1-2 алкил, С 2-6 алкил, С 2-5 алкил, С 2-4 алкил, С 2-3 алкил, С 3-6 алкил, С 4-5 алкил и т.д. Также "арил-С 1-6 алкил" относится к C1-6 алкильной группе, замещенной арильной группой. Примеры включают бензил, 2-фенилэтил, 1-фенилэтил и 1-нафтилметил. Если не указано особо, "фтор-С 1-6 алкил" относится к C1-6 алкильной группе, замещенной одним или более атомов фтора. Примеры упомянутого фтор-С 1-6 алкила включают 2-фторэтил, фторметил, трифторметил и 2,2,2-трифторэтил. Если не указано особо, термин "гидрокси-С 1-4 алкил" обозначает прямую или разветвленную алкильную группу, в которой ее атом водорода замещен на ОН. Примеры упомянутого гидрокси-C1-4 алкила включают гидроксиметил, 2-гидроксиэтил, 2-гидроксипропил и 2-гидрокси-2-метилпропил. Если не указано особо, термин "C1-6 алкокси" обозначает прямую или разветвленную алкоксигруппу, имеющую от 1 до 6 атомов углерода. Примеры упомянутого C1-6 алкокси включают метокси, этокси,н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси и гексокси с прямой и разветвленной цепью. Для частей диапазона "С 1-6 алкокси" предполагаются все их подгруппы,такие как C1-5 алкокси, C1-4 алкокси, C1-3 алкокси, С 1-2 алкокси, С 2-6 алкокси, С 2-5 алкокси, С 2-4 алкокси,С 2-3 алкокси, С 3-6 алкокси, С 4-5 алкокси и т.д. Если не указано особо, "фтор-С 1-6 алкокси" относится к C1-6 алкоксигруппе, замещенной одним или более атомами фтора. Примеры упомянутого фтор-С 1-6 алкокси включают трифторметокси, дифторметокси, монофторметокси, 2-фторэтокси, 2,2,2-трифторэтокси и 1,1,2,2-тетрафторэтокси.-6 016456 Если не указано особо, термин "С 1-4 алкокси-С 2-4 алкил" обозначает прямую или разветвленную алкоксигруппу, имеющую от 1 до 4 атомов углерода, связанную с алкильной группой, имеющей от 1 до 4 атомов углерода. Примеры упомянутого С 1-4 алкокси-С 2-4 алкила включают метоксиметил, этоксиметил,изопропоксиметил, н-бутоксиметил и трет-бутоксиметил. Для частей диапазона "C1-4 алкокси-С 2-4 алкил" предполагаются все их подгруппы, такие как С 1-3 алкокси-С 2-4 алкил, С 1-4 алкокси-С 2-3 алкил, С 1-2 алкоксиС 2-3 алкил, С 2-4 алкокси-С 2-4 алкил, С 2-3 алкокси-С 2-4 алкил, С 2-4 алкокси-С 2-3 алкил и т.д. Если не указано особо, термин "С 2-6 алкенил" обозначает прямую или разветвленную алкенильную группу, имеющую от 2 до 6 атомов углерода. Примеры упомянутого С 2-6 алкенила включают винил, аллил, 2,3-диметилаллил, 1-бутенил, 1-пентенил и 1-гексенил. Для частей диапазона "С 2-6 алкенил" предполагаются все их подгруппы, такие как С 2-5 алкенил, С 2-4 алкенил, С 2-3 алкенил, С 3-6 алкенил, С 4-5 алкенил и т.д. Также "арил-С 2-6 алкенил" относится к С 2-6 алкенильной группе, замещенной арильной группой. Примеры упомянутого арил-С 2-6 алкенила включают стирил и циннамил. Если не указано особо, термин "фтор-С 2-6 алкенил" обозначает прямую или разветвленную алкенильную группу, имеющую от 2 до 6 атомов углерода, замещенную одним или более атомами фтора. Примеры упомянутого фтор-С 2-6 алкенила включают 1-фторвинил, 1,2-дифторвинил, трифторвинил и 2-фтор-2-пропен-1-ил. Если не указано особо, термин "С 3-4 алкинил" обозначает прямую или разветвленную алкинильную группу, имеющую от 3 до 4 атомов углерода. Примеры упомянутого С 3-4 алкинила включают 1-пропинил,2-пропинил, 1-бутинил, 2-бутинил и 1-метилпроп-2-ин-1-ил. Если не указано особо, термин "С 3-7 циклоалкил" обозначает циклическую алкильную группу,имеющую размер кольца от 3 до 7 атомов углерода. Упомянутый циклоалкил включает циклопропил,циклобутил, циклопентил, циклогексил и циклогептил. Для частей диапазона "С 3-7 циклоалкил" предполагаются все их подгруппы, такие как С 3-6 циклоалкил, С 3-5 циклоалкил, С 3-4 циклоалкил, С 4-7 циклоалкил,С 4-бциклоалкил, С 4-5 циклоалкил, C5-7 циклоалкил, С 6-7 циклоалкил и т.д. Если не указано особо, термин "метил-С 3-7 циклоалкил" обозначает С 3-7 циклоалкильную группу, замещенную одной или более метильными группами. Примеры упомянутого "метил-С 3-7 циклоалкила" включают 4-метилциклогексил, 3,3-диметилциклопентил и 1-метилциклопропил. Если не указано особо, термин "метил-С 3-7 циклоалкокси" обозначает С 3-7 циклоалкоксигруппу, замещенную одной или более метильными группами. Примеры упомянутого "метил-С 3-7 циклоалкокси" включают 4-метилциклогексилокси, 3,3-диметилциклопентилокси и 1-метилциклопропилокси. Если не указано особо, термин "фтор-С 3-7 циклоалкил" обозначает С 3-7 циклоалкильную группу,замещенную 1 или 2 атомами фтора. Примеры упомянутого "фтор-С 3-7 циклоалкила" включают 2,2-дифторциклопропил и 4-фторциклогексил. Если не указано особо, термин "фтор-С 3-7 циклоалкокси" обозначает С 3-7 циклоалкоксигруппу,замещенную 1 или 2 атомами фтора. Примеры упомянутого "фтор-С 3-7 циклоалкокси" включают 2,2-дифторциклопропилокси и 4-фторциклогексилокси. Если не указано особо, термин "арил" относится к углеводородной кольцевой системе из одного,двух или трех, предпочтительно из одного или двух колец, имеющей по меньшей мере одно ароматическое кольцо и имеющей 6-14, предпочтительно 6-10 атомов углерода. Примерами арилов являются фенил, пенталенил, инденил, инданил, 1,2,3,4-тетрагидронафтил, 1-нафтил, 2-нафтил, флуоренил и антрил. Арильные кольца могут быть необязательно замещенными. Также арилокси относится к арильной группе, связанной с атомом кислорода. Арильная группа может быть соединена с остатком молекулы через любой пригодный кольцевой атом, находится ли кольцевой атом в ароматическом кольце или в частично насыщенном кольце. Термин "гетероарил" относится к моно- или бициклической ароматической кольцевой системе,только одно кольцо должно быть ароматическим и упомянутая гетероарильная частица может быть соединена с остатком молекулы через атом углерода или азота в любом кольце и имеющей от 5 до 10 кольцевых атомов (моно- или бициклическая), в которой один или более кольцевых атомов являются отличными от углерода, такими как азот, сера, кислород и селен. Примеры таких гетероарильных колец включают фурильную, пирролильную, тиенильную, оксазолильную, изоксазолильную, имидазолильную, тиазолильную, изотиазолильную, пиридинильную, пиримидинильную, пиразинильную, хроманильную, хиназолинильную, индолильную, изоиндолильную, индолинильную, изоиндолинильную, индазолильную,пиразолильную, пиридазинильную, хинолинильную, изохинолинильную, бензофуранильную, дигидробензофуранильную, бензодиоксолильную, бензодиоксинильную, бензотиенильную, бензимидазолильную, бензотиазолильную, бензотиадиазолильную и бензотриазолильную группы. Если бициклическое гетероарильное кольцо является замещенным, оно может быть замещено в любом кольце. Если не указано особо, термин "гетероциклил" относится к неароматической (например, частично или полностью насыщенной) моно- или бициклической кольцевой системе, имеющей 4-10 атомов углерода по меньшей мере с одним гетероатомом, таким как О, N или S, и оставшиеся кольцевые атомы являются атомами углерода. Предпочтительно "гетероциклил" относится к полностью насыщенной неароматической моноциклической кольцевой системе с 4-7 кольцевыми атомами и в которой один или два атома являются гетероатомами, выбранными из О, N и S, и оставшиеся кольцевые атомы являются ато-7 016456 мами углерода. Примеры гетероциклических групп включают пиперидильную, тетрагидропиранильную,тетрагидрофуранильную, азепинильную, азетидинильную, пирролидинильную, морфолинильную, имидазолинильную, тиоморфолинильную, пиранильную, диоксанильную и пиперазинильную группы. При наличии в гетероциклической группе атом серы может быть необязательно в окисленной форме (например, S=O или O=S=O). Если не указано особо, термин "карбоциклил" относится к неароматической (например, частично или полностью насыщенной) моноциклической кольцевой системе, имеющей 3-6 кольцевых углеродных атомов. Примеры карбоциклических колец включают циклопропан, циклобутан, циклопентан, циклогексан, циклопентен, циклогексен. Если не указано особо, термин "галоген" будет обозначать фтор, хлор, бром или йод. Термин"Необязательный" или "необязательно" обозначает то, что впоследствии описанное явление или условие может не иметь места и что данное описание включает примеры, когда явление или условие имеет место и примеры, когда оно не имеет места."Фармацевтически приемлемые" обозначает то, что они являются пригодными для приготовления фармацевтической композиции и они обычно являются безопасными, нетоксичными и ни биологически,ни в остальном нежелательными и включают те, что являются пригодными для ветеринарного использования, так же как для фармацевтического использования на человеке."Лечение", как используется в данном изобретении, включает профилактику упомянутых расстройств или состояний, или улучшение состояния, или устранение расстройства, как только оно зафиксировано."Эффективное количество" относится к количеству соединения, которое оказывает терапевтическое действие на субъект, подвергнутый лечению. Терапевтическое действие может быть объективным (например, измеренным с помощью некоторых исследований или маркеров) или субъективным (например,субъект дает показания или чувствует действие). Ссылка на соединение "формулы (I)" в вариантах осуществления данного изобретения также включает соединения любой формулы, изображенной в данном описании. Термин "пролекарственные формы" относится к фармакологически приемлемому производному,такому как эфир или амин, и указанное производное подвергается биотрансформации в теле, чтобы образовать активное лекарственное средство. Ссылаемся на Goodman and Gilman's, The Pharmacological basisChemistry of Drug Design and Drug Action" by Richard B. Silverman. Chapter 8, p. 352 (Academic Press, Inc. 1992. ISBN 0-12-643730-0). Комбинации заместителей и переменные величины, представленные в данном изобретении, являются только теми, что приводят в результате к образованию стабильных соединений. Термин "стабильный", как используется в данном описании, относится к соединениям, которые обладают стабильностью, достаточной, чтобы делать возможным производство, и которая поддерживает целостность соединения в течение достаточного периода времени для того, чтобы оно было пригодным для целей, описанных в данном изобретении (например, терапевтического введения субъекту для лечения 5-НТ 6-опосредованного заболевания или расстройства (включая те, что представлены в данном изобретении), ожирения, диабета 2 типа). Перечисление списка химических групп в любом определении переменной величины в данном изобретении включает определение данной переменной величины как любой единичной группы или комбинации перечисленных групп. Перечисление варианта осуществления для переменной величины в данном изобретении включает данный вариант осуществления как любой единичный вариант осуществления или в комбинации с любыми другими вариантами осуществления или их частями.CV - коэффициент вариации,DCM - дихлорметан,DMSO - диметилсульфоксид,EDTA - этилендиаминтетрауксусная кислота,EGTAэтилен-бис-(оксиэтиленнитрило)тетрауксусная кислота,ESI - электроспрей-ионизация,HEPES - 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота,ВЭЖХ - высокоэффективная жидкостная хроматография,LSD - диэтиламид лизергиновой кислоты,MeCN - ацетонитрил,SPA - сцинтилляционный анализ сближения,TFA - трифторуксусная кислота,THF - тетрагидрофуран,UV - ультрафиолетовое излучение,MeOH - метанол,BnBr - бензилбромид,DCE - 1,2-дихлорэтан,TMAD - (Е)-N,N,N',N'-тетраметилдиазен-1,2-дикарбоксамид. Примеры В настоящее время данное изобретение будет проиллюстрировано следующими неограничивающими примерами. Конкретные примеры, представленные ниже, следует истолковывать просто как иллюстративные и не ограничивающие оставшуюся часть описания каким бы то ни было образом. Без дополнительных уточнений считают, что специалисты в данной области техники могут на основании данного описания использовать настоящее изобретение в его максимально полном объеме. Все ссылки и публикации, цитируемые в данном изобретении, вводятся, таким образом, полностью с помощью ссылки. Способы. Спектры 1 Н ядерного магнитного резонанса (ЯМР) и 13 С ЯМР спектры записывали на BrukerInova 400 спектрометре при 400,0 и 100,5 МГц соответственно, или, альтернативно, на Bruker NMR 500 спектрометре при 500,1 и 125,1 МГц соответственно, или альтернативно, на JEOL eclipse 270 спектрометре при 270,0 и 67,5 МГц соответственно. Все спектры записывали, используя остаточный растворитель в качестве внутреннего стандарта. Аналитическую ВЭЖХ/МС проводили, используя Agilent 1100/1200 серий жидкостной хроматограф/масс-селективный детектор (МСД) (Singel Quadrupole) (1946A/1946C/1956C/6110), оснащенный электроспрей. Препаративную ВЭЖХ/МС проводили на Waters/Micromass Platform ZQ системе и препаративную ВЭЖХ/UV проводили на Gilson системе. Препаративную флэш-хроматографию осуществляли на Merck силикагеле 60 (230-400 меш). Соединения называли, используя ACD Name 6.0, за исключением соединения в примере 1 - 2,5-метилен-9(фенилсульфонил)-1,2,3,4,5,9-гексагидро[1,5]оксазоцино[3,2-е]индола. Реакции с использованием микроволн проводили на Personal Chemistry Smith Creator, используя 0,5-2 мл или 2-5 мл Smith Process пробирки, снабженные алюминиевой крышкой и септой.Chlorothricins. Helv. Chim. Acta. 1970, 53, 1544-1547). Промежуточное соединение 2. 5-(Бензилокси)-4-бром-1 Н-индол. К суспензии измельченного K2CO3 (11,4 г, 83,0 ммоль) в сухом ацетоне (150 мл) добавляли региосмесь бромфенолов (промежуточное соединение 1, 12,4 г, 53,5 ммоль) и BnBr (9,42 г, 55,1 ммоль) и смесь кипятили с обратным холодильником в течение 2 ч. Реакционную смесь фильтровали и фильтрат упаривали при пониженном давлении, чтобы получить масло, которое использовали в следующей стадии без дополнительной очистки. Сырой бензиловый эфир растворяли в сухом DMF (100 мл) и добавляли диметилацеталь диметилформамида (13,0 г, 109 ммоль),и реакционную смесь грели при 90 С в течение двух дней. Каждый день в течение следующих трех дней добавляли при 90 С порцию диметилацеталя диметилформамида (1,0 г, 8,0 ммоль). Растворитель удаляли при пониженном давлении и черно-красный маслянистый остаток растворяли в уксусной кислоте (20 мл). Вязкий раствор аккуратно добавляли к хорошо перемешиваемой суспензии железного порошка (9,15 г, 164 ммоль) в теплой уксусной кислоте(60 мл) в течение 10 мин. Густую реакционную смесь кипятили с обратным холодильником в течение 1 ч, твердые остатки отфильтровывали и фильтрат упаривали при пониженном давлении. Черный остаток растворяли в теплом CHCl3 (350 мл), добавляли 50 г силикагеля с последующим добавлением гептана(350 мл). Смесь фильтровали через слой силикагеля и растворитель упаривали. Черный остаток очищали- 24016456 флэш-хроматографией на силикагеле, используя петролейный эфир/EtOAc 90:10 в качестве элюента, чтобы получить заявленное в заголовке соединение (4,0 г) в виде темно-зеленого масла. МС m/z 302/304 [М+Н]+. Промежуточное соединение 3. 4-Бром-5-(бензилокси)-1-(фенилсульфонил)-1 Н-индол. К раствору 4-бром-5-бензилокси-1 Н-индола (промежуточное соединение 2, 3,85 г, 12,7 ммоль) в(0,41 г, 1,3 ммоль) и 3 М NaOH (13 мл, 39 ммоль) и смесь энергично перемешивали при комнатной температуре в течение 30 мин. Органическую фазу промывали водой и соляным раствором, сушили (MgSO4) и концентрировали досуха, чтобы получить заявленное в заголовке соединение (5,7 г) в виде твердого остатка. МС m/z 442/444 [М+Н]+. Промежуточное соединение 4. 5-(Бензилокси)-1-(фенилсульфонил)-1 Н-индол-4-карбальдегид. К теплому раствору 4-бром-5-бензилокси-1-(фенилсульфонил)-1 Н-индола (промежуточное соединение 3, 4,74 г, 10,7 ммоль) в толуоле (100 мл) добавляли трибутилвинилолово (6,80 г, 21,4 ммоль) иPd(PPn3)2Cl2 (0,37 г, 0,50 ммоль). Раствор кипятили с обратным холодильником в течение 2 ч и добавляли еще Pd(PPh3)2Cl2 (0,20 г, 0,30 ммоль) и реакционную смесь кипятили с обратным холодильником в течение ночи. Добавляли чайную ложку силикагеля и смесь фильтровали через слой силикагеля. Растворитель удаляли при пониженном давлении и полученное в результате масло растирали петролейным эфиром, чтобы получить полукристаллическую массу (3,6 г), которую растворяли в диоксане (110 мл) и добавляли 2,6-лутидин (2,00 г, 18,7 ммоль) и OsO4 (0,24 г, 0,94 ммоль). Смесь перемешивали при комнатной температуре в течение 5 мин. К темному раствору добавляли раствор периодата натрия (8,02 г,37,5 ммоль) в воде (35 мл) и полученную в результате суспензию перемешивали в течение 30 мин. Добавляли большее количество диоксана (40 мл) и смесь фильтровали. Фильтрат упаривали, чтобы получить темно-красное масло. Сырой продукт очищали флэш-хроматографией на силикагеле, используя петролейный эфир/EtOAc 90:10 и затем 80:20 в качестве элюента, чтобы получить заявленное в заголовке соединение (2,44 г) в виде желтого твердого остатка. МС m/z 392 [М+Н]+. Пример 1. 2,5-Метилен-9-(фенилсульфонил)-1,2,3,4,5,9-гексагидро[1,5]оксазоцино[3,2-е]индол. К раствору 5-(бензилокси)-1-(фенилсульфонил)-1 Н-индол-4-карбальдегида (промежуточное соединение 4, 100 мг, 0,250 ммоль) в DCE (3 мл) добавляли 3-гидроксипирролидин (33 мг, 0,38 ммоль) и триацетоксиборгидрид натрия (0,16 г, 0,77 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли при пониженном давлении и остаток растворяли в MeOH (2 мл) и добавляли Pd/C 10 вес.% (0,020 г, 0,019 ммоль) и смесь продували газообразным N2. Добавляли формиат аммония (0,050 г, 0,80 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли при пониженном давлении и остаток растворяли в CHCl3/H2O и смесь промывали водой и соляным раствором, сушили (MgSO4) и растворитель удаляли при пониженном давлении, чтобы получить 4-[(3-гидроксипирролидин-1-ил)метил]-1-(фенилсульфонил)-1 Н-индол-5-ол (85 мг) в виде масла. МС m/z 373 [М+Н]+. Это масло (85 мг, 0,23 ммоль) растворяли в сухом DCM (3 мл) и добавляли трифенилфосфин(179 мг, 0,680 ммоль) с последующим добавлением 1,1'-азо-бис-(N,N-диметилформамида) (118 мг,0,680 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь упаривали и сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 pH 10 CH3CN), чтобы получить заявленное в заголовке соединение (8,0 мг) в виде коричневого масла. МС m/z 355 [М+Н]+. Пример 2. 2,4-Диметил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индолтрифторацетат. К раствору 5-(бензилокси)-1-(фенилсульфонил)-1 Н-индол-4-карбальдегида (промежуточное соединение 4, 0,050 г, 0,12 ммоль) в DCE (3 мл) добавляли 1-амино-2-пропанол (0,020 г, 0,27 ммоль) и триацетоксиборгидрид натрия (0,080 г, 0,38 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли формальдегид (37 вес.% в Н 2 О, 0,10 мл, 1,2 ммоль) и триацетоксиборгидрид натрия (0,10 г, 0,48 ммоль) и смесь перемешивали при комнатной температуре в течение 1 ч. Растворитель удаляли при пониженном давлении и остаток растворяли в MeOH (2 мл). Добавляли 10 вес.% Pd/C (0,020 г, 0,019 ммоль) и смесь продували газообразным N2. Добавляли формиат аммония(0,050 г, 0,80 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли при пониженном давлении, полутвердый остаток растворяли в CHCl3/H2O и смесь промывали водой и соляным раствором, сушили (MgSO4) и растворитель удаляли при пониженном давлении. Сырое вещество растворяли в сухом DCM (1 мл) и добавляли трифенилфосфин (8,0 мг,0,030 ммоль) с последующим добавлением 1,1'-азо-бис-(N,N-диметилформамида) (5,2 мг, 0,030 ммоль) и- 25016456 смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь упаривали и сырой продукт очищали препаративной ВЭЖХ (АСЕ С 8, 0,1% TFA - CH3CN), чтобы получить заявленное в заголовке соединение (7,4 мг) в виде трифторацетатной соли. МС m/z 357 [М+Н]+. Пример 3. 2-Изопропил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индолтрифторацетат. К раствору 5-(бензилокси)-1-(фенилсульфонил)-1 Н-индол-4-карбальдегида (промежуточное соединение 4, 0,033 г, 0,084 ммоль) в DCE (2,5 мл) добавляли N-изопропилэтаноламин (0,017 г, 0,17 ммоль) и триацетоксиборгидрид натрия (0,036 г, 0,17 ммоль) и смесь грели в герметически закрытой пирекструбке при 40 С в течение ночи. Растворитель удаляли при пониженном давлении и остаток растворяли в MeOH (2 мл). Добавляли 10 вес.% Pd/C (0,020 г, 0,019 ммоль) и смесь продували газообразным N2. Добавляли формиат аммония (0,021 г, 0,34 ммоль) и реакционную смесь перемешивали при 40 С в течение ночи. Реакционную смесь фильтровали через слой hydromatrix, используя DCM в качестве элюента, и фильтрат упаривали. Сырое вещество растворяли в сухом DCM (1 мл) и добавляли трифенилфосфин(0,044 г, 0,017 ммоль) с последующим добавлением 1,1'-азо-бис-(N,N-диметилформамида) (0,029 г,0,017 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь упаривали и сырой продукт очищали препаративной ВЭЖХ (АСЕ С 8, 0,1% TFA - CH3CN), чтобы получить заявленное в заголовке соединение (5,2 мг) в виде бесцветного масла в виде трифторацетатной соли. МС m/z 371 [М+Н]+. Пример 4. 2-Этил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индолтрифторацетат. К раствору 5-(бензилокси)-1-(фенилсульфонил)-1 Н-индол-4-карбальдегида (промежуточное соединение 4, 0,033 г, 0,084 ммоль) в DCE (2,5 мл) добавляли N-этилэтаноламин (0,015 г, 0,17 ммоль) и тригидроксиборгидрид натрия (0,036 г, 0,17 ммоль) и смесь грели в герметически закрытой пирекс-трубке при 40 С в течение ночи. Растворитель удаляли при пониженном давлении и остаток растворяли в MeOH(2 мл), добавляли 10 вес.% Pd/C (0,010 г, 0,0095 ммоль) и смесь продували газообразным N2. Добавляли формиат аммония (0,021 г, 0,34 ммоль) и реакционную смесь перемешивали при 40 С в течение ночи. Реакционную смесь фильтровали через слой hydromatrix, используя DCM в качестве элюента, и фильтрат упаривали. Сырое вещество растворяли в сухом DCM (1 мл) и добавляли трифенилфосфин (0,044 г,0,017 ммоль) с последующим добавлением 1,1'-азо-бис-(N,N-диметилформамида) (0,029 г, 0,017 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь упаривали и сырой продукт очищали препаративной ВЭЖХ (АСЕ С 8, 0,1% TFA - CH3CN), чтобы получить заявленное в заголовке соединение (0,8 мг) в виде бесцветного масла в виде трифторацетатной соли. МС m/z 357 [М+Н]+. Промежуточное соединение 5. 4-[(2-Гидроксиэтил)метиламино]метил-1 Н-индол-5-ол. Суспендировали в этаноле (10 мл) параформальдегид (0,060 г, 2 ммоль) и 2-метиламиноэтанол(0,15 г, 2,0 ммоль) и грели при 50 С в течение 20 мин. Раствор охлаждали до комнатной температуры и добавляли 5-гидроксииндол (0,27 мг, 2,0 ммоль). Раствор перемешивали в атмосфере N2 при комнатной температуре в течение ночи. Раствор упаривали, чтобы получить заявленное в заголовке соединение(441 мг), которое использовали на следующей стадии без дополнительной очистки. МС m/z 221 [М+Н]+. Промежуточное соединение 6. 2-Метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. 4-[(2-Гидроксиэтил)метиламино]метил-1 Н-индол-5-ол (промежуточное соединение 5, 0,44 г,2,0 ммоль), 1,1'-азо-бис-(N,N-диметилформамид) (0,52 мг, 3,0 ммоль) и трифенилфосфин (0,79 мг,3,0 ммоль) растворяли в THF (10 мл) и перемешивали при комнатной температуре в течение ночи. Смесь упаривали и сырое вещество очищали флэш-хроматографией на силикагеле, используя градиент MeOHэтилацетат, 4-32% MeOH, чтобы получить 136 мг заявленного в заголовке соединения. МС m/z 203 [М+Н]+. Пример 5. 2-Метил-8-(фенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. В пробирку, содержащую 2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол (промежуточное соединение 6, 0,250 г, 1,24 ммоль) и гидрид натрия (60% в минеральном масле, 0,100 г,2,50 ммоль), добавляли DMF (15 мл). Смесь перемешивали в течение 20 мин при комнатной температуре перед добавлением бензолсульфонилхлорида (0,327 г, 1,85 ммоль). Реакционную смесь перемешивали в течение 30 мин перед добавлением 2 М HCl (0,5 мл) и смесь разбавляли 1 М Na2CO3 и диэтиловым эфиром. Органическую фазу промывали водой, сушили (MgSO4) и упаривали. Сырой продукт растворяли вDCM (2 мл) и добавляли гексан (20 мл). Смесь оставляли в течение ночи и светло-желтые кристаллы фильтровали и промывали гексаном, чтобы получить заявленное в заголовке соединение (202 мг) в виде светло-желтого твердого остатка.- 26016456 МС m/z 343 [М+Н]+. Общая методика для приготовления соединений примеров 6-34. 2-Метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол (промежуточное соединение 6, 0,010 г,0,050 ммоль) растворяли в сухом DMF (0,2 мл) и добавляли гидрид натрия (60% в минеральном масле,0,6 мг, 0,1 ммоль). Реакционную смесь встряхивали при комнатной температуре в течение 10 мин и добавляли необходимое количество сульфонилхлорида (0,1 ммоль в 0,15 мл сухого DMF). Реакционную смесь встряхивали при комнатной температуре в течение 10-20 мин и затем реакцию прекращали добавлением 1 мл смеси метанола и уксусной кислоты (1:1). Сырые продукты очищали, как описано ниже. Пример 6. 8-(2,3-Дигидро-1,4-бензодиоксин-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2, 3-дигидро-1,4-бензодиоксин-6-сульфонилхлорид (0,023 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (11 мг). МС m/z 401 [М+Н]+. Пример 7. 8-[(3,4-Диметоксифенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 3,4-диметоксибензолсульфонилхлорид (0,024 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (10,9 мг). МС m/z 403 [М+Н]+. Пример 8. 8-(1-Бензофуран-2-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 1-бензофуран-2-сульфонилхлорид (0,022 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (5,5 мг). МС m/z 383 [М+Н]+. Пример 9. 8-[(2,5-Диметил-3-фурил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2,5-диметил-3-фурансульфонилхлорид (0,019 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (11,4 мг). МС m/z 361 [М+Н]+. Пример 10. 8-(1,3-Бензотиазол-6-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 1,3-бензотиазол-6-сульфонилхлорид (0,023 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (7,1 мг). МС m/z 400 [М+Н]+. Пример 11. 2-Метил-8-[4-(метилсульфонил)фенил]сульфонил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7 е]индол. Сульфонилхлорид: 4-метилсульфонилбензолсульфонилхлорид (0,025 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (9,5 мг). МС m/z 421 [М+Н]+. Пример 12. 8-[(4-Изопропилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-изопропилбензол-1-сульфонилхлорид (0,022 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (10,7 мг). МС m/z 385 [М+Н]+. Пример 13. 8-[(2,2-Диметил-3,4-дигидро-2 Н-хромен-6-ил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2,2-диметил-6-хромансульфонилхлорид (0,026 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (9,6 мг). МС m/z 427 [М+Н]+. Пример 14. 8-[(2-Хлор-4-фторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2-хлор-4-фторбензолсульфонилхлорид (0,023 г, 0,10 ммоль).- 27016456 Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (10,3 мг). МС m/z 395 [М+Н]+. Пример 15. 8-[(3,4-Дихлорфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 3,4-дихлорбензолсульфонилхлорид (0,025 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12,2 мг). МС m/z 412 [М+Н]+. Пример 16. 8-[(4-Фторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-фторбензолсульфонилхлорид (0,019 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12,8 мг). МС m/z 361 [М+Н]+. Пример 17. 8-[(2,6-Дифторфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2,6-дифторбензолсульфонилхлорид (0,021 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (11,2 мг). МС m/z 379 [М+Н]+. Пример 18. 2-Метил-8-[4-(трифторметокси)фенил]сульфонил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7 е]индол. Сульфонилхлорид: 4-(трифторметокси)бензол-1-сульфонилхлорид (0,026 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (16,8 мг). МС m/z 427 [М+Н]+. Пример 19. 2-Метил-8-(2-нафтилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2-нафталинсульфонилхлорид (0,023 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (19,8 мг). МС m/z 393 [М+Н]+. Пример 20. 8-[(3-Хлор-4-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 3-хлор-4-метилбензолсульфонилхлорид (0,023 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (2,2 мг). МС m/z 391 [М+Н]+. Пример 21. 8-[(4,5-Дихлор-2-тиенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2,3-дихлортиофен-5-сульфонилхлорид (0,025 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (11,5 мг). МС m/z 418 [М+Н]+. Пример 22. 8-[(5-Хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 5-хлор-3-метилбензо(b)тиофен-2-сульфонилхлорид (0,028 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (9 мг). МС m/z 447 [М+Н]+. Пример 23. 8-[(2,4-Дихлорфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2,4-дихлорбензолсульфонилхлорид (0,025 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (9 мг). МС m/z 412 [М+Н]+.- 28016456 Пример 24. 8-[4-Фтор-3-(трифторметил)фенил]сульфонил-2-метил-1,3,4,8-тетрагидро-2 Н[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-фтор-3-трифторметилбензолсульфонилхлорид (0,026 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (4 мг). МС m/z 429 [М+Н]+. Пример 25. 2-Метил-8-(2-тиенилсульфонил)-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 2-тиенилсульфонилхлорид (0,018 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (2 мг). МС m/z 349 [М+Н]+. Пример 26. 2-Метил-8-[(4-метилфенил)сульфонил]-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-толуолсульфонилхлорид (0,019 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12 мг). МС m/z 357 [М+Н]+. Пример 27. 8-[(2-Метокси-5-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7 е]индол. Сульфонилхлорид: 2-метокси-5-метилбензолсульфонилхлорид (0,022 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12 мг). МС m/z 387 [М+Н]+. Пример 28. 8-[(3-Фтор-4-метилфенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 3-фтор-4-метилбензолсульфонилхлорид (0,021 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12 мг). МС m/z 375 [М+Н]+. Пример 29. 8-(1-Бензотиен-3-илсульфонил)-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 1-бензотиофен-3-сульфонилхлорид (0,023 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (12 мг). МС m/z 399 [М+Н]+. Пример 30. 8-[(4-Метоксифенил)сульфонил]-2-метил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-метоксибензолсульфонилхлорид (0,021 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (6,2 мг). МС m/z 373 [М+Н]+. Пример 31. 2-Метил-8-[4-(трифторметил)фенил]сульфонил-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7 е]индол. Сульфонилхлорид: 4-(трифторметил)бензолсульфонилхлорид (0,024 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (11,6 мг). МС m/z 411 [М+Н]+. Пример 32. 2-Метил-8-[(4-пропилфенил)сульфонил]-1,3,4,8-тетрагидро-2 Н-[1,4]оксазепино[6,7-е]индол. Сульфонилхлорид: 4-пропилбензолсульфонилхлорид (0,022 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), чтобы получить заявленное в заголовке соединение (13 мг). МС m/z 385 [М+Н]+. Пример 33. 3-Хлор-4-[(2-метил-1,2,3,4-тетрагидро-8 Н-[1,4]оксазепино[6,7-е]индол-8 ил)сульфонил]бензонитрил. Сульфонилхлорид: 2-хлор-4-цианобензолсульфонилхлорид (0,024 г, 0,10 ммоль). Сырой продукт очищали препаративной ВЭЖХ (XTerra C18, 50 мМ NH4HCO3 рН 10 - CH3CN), что- 29
МПК / Метки
МПК: C07D 498/04, C07D 498/18, A61K 31/553
Метки: производные, качестве, использование, лигандов, 5-нт6, рецепторных, 8-сульфонил-1,3,4,8-тетрагидро-2н-[1,4]оксазепино[6,7-e]индольные
Код ссылки
<a href="https://eas.patents.su/30-16456-8-sulfonil-1348-tetragidro-2n-14oksazepino67-eindolnye-proizvodnye-i-ih-ispolzovanie-v-kachestve-5-nt6-receptornyh-ligandov.html" rel="bookmark" title="База патентов Евразийского Союза">8-сульфонил-1,3,4,8-тетрагидро-2н-[1,4]оксазепино[6,7-e]индольные производные и их использование в качестве 5-нт6 рецепторных лигандов</a>
Предыдущий патент: Мягкие капсулы, содержащие палоносетрона гидрохлорид, имеющие улучшенную стабильность и биологическую доступность
Следующий патент: Аналог тиофена для лечения вирусной инфекции гепатита с
Случайный патент: Способ удаления и отверждения диоксида углерода из потока текучей среды и устройство разделения текучей среды












