Макроциклические ингибиторы вируса гепатита с
Номер патента: 15131
Опубликовано: 30.06.2011
Авторы: Самуэльссон Бенгт Бертил, Рабуассон Пьер Жан-Мари Бернар, Тахри Абделлах, Де Кок Херман Аугустинус, Бельфраге Анна Карин Гертруд Линнеа, Нильссон Карл Магнус, Вендевилль Сандрин Мари Элен, Пелькман Микаэль, Ху Лили, Сюрлеро Доминик Луи Нестор Гилейн, Симмен Кеннет Алан, Йоханссон Пер-Ола Микаэль, Иванов Владимир, Росенквист Оса Анника Кристина
Формула / Реферат
1. Соединение формулы
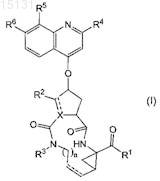
его N-оксид, соль или стереоизомер, где
каждая пунктирная линия (изображенная как ----) означает необязательную двойную связь;
X представляет собой N, СН, и когда X образует двойную связь, он представляет собой С;
R1 представляет собой -OR7, -NH-SO2R8;
R2 представляет собой водород, и когда X представляет собой С или СН, R2 также может представлять собой С1-6алкил;
R3 представляет собой водород, C1-6алкил, С1-6алкоксиС1-6алкил, С3-7циклоалкил;
R4 представляет собой арил или Het;
n равно 3, 4, 5 или 6;
R5 представляет собой галоген, C1-6алкил, гидрокси, C1-6алкокси, полигалогенС1-6алкил, фенил или Het;
R6 представляет собой C1-6алкокси или диметиламино;
R7 представляет собой водород; арил; Het; С3-7циклоалкил, необязательно замещенный C1-6алкилом; или C1-6 алкил, необязательно замещенный С3-7циклоалкилом, арилом или Het;
R8 представляет собой арил; Het; С3-7циклоалкил, необязательно замещенный C1-6алкилом; или C1-6алкил, необязательно замещенный С3-7циклоалкилом, арилом или Het;
арил в качестве группы или части группы представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями, выбранными из галогена, гидрокси, нитро, циано, карбоксильной группы, C1-6алкила, C1-6алкокси, C1-6алкоксиС1-6алкила, C1-6алкилкарбонила, амино, моно- или ди-С1-6алкиламино, азидо, меркапто, полигалогенС1-6алкила, полигалогенС1-6алкокси, С3-7циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-C1-6алкилпиперазинила, 4-С1-6алкилкарбонилпиперазинила и морфолинила; где морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя C1-6 алкильными радикалами;
Het в качестве группы или части группы представляет собой 5- или 6-членный насыщенный, частично ненасыщенный или полностью ненасыщенный гетероцикл, содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из атома азота, атома кислорода и атома серы, причем указанный гетероцикл является необязательно конденсированным с бензольным кольцом; где указанный Het в целом является необязательно замещенным одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы заместителей, включающей галоген, гидрокси, нитро, циано, карбоксильную группу, C1-6алкил, C1-6алкокси, C1-6алкоксиС1-6алкил, C1-6алкилкарбонил, амино, моно- или ди-C1-6алкиламино, азидо, меркапто, полигалогенС1-6алкил, полигалогенС1-6алкокси, С3-7циклоалкил, пирролидинил, пиперидинил, пиперазинил, 4-С1-6алкилпиперазинил, 4-C1-6алкилкарбонилпиперазинил и морфолинил; где морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя C1-6 алкильными радикалами.
2. Соединение по п.1, где соединение имеет формулу (I-c), (I-d) или (I-е)
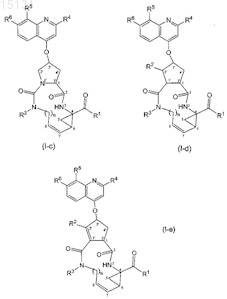
3. Соединение по любому из пп.1-2, в котором R4 выбран из группы, включающей фенил, пиридин-4-ил
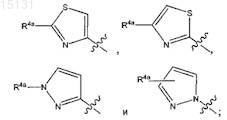
где R4a, каждый независимо, представляет собой водород, галоген, C1-6алкил, амино или моно- или диС1-6 алкиламино.
4. Соединение по любому из пп.1-3, где R5 представляет собой метил, этил, изопропил, трет-бутил, фтор, хлор или бром и R6представляет собой метокси.
5. Соединение по любому из пп.1-4, где
(a) R1представляет собой -O-R7, где R7представляет собой C1-6алкил или водород;
(b) R1представляет собой -NHS(=O)2R8, где R8представляет собой метил, циклопропил или фенил; или
(c) R1представляет собой -NHS(=O)2R8, где R8представляет собой циклопропил, замещенный метилом.
6. Соединение по п.5, где R1 представляет собой -NHS(=O)2R8, где R8 представляет собой метил, циклопропил или фенил.
7. Соединение по любому из пп.1-6, где n равно 4 или 5.
8. Соединение по любому из пп.1-7, где n равно 4.
9. Соединение по любому из пп.1-8, где R3 представляет собой водород или С3-6алкил.
10. Соединение по п.9, где R3 представляет собой водород или метил.
11. Соединение по любому из пп.1-2, где R4 представляет собой радикал
![]()
где атом азота, там где это возможно, может содержать заместитель R4a или связь с остальной частью молекулы; каждый из R4a в любом из R4 заместителей может быть выбран из заместителей, указанных в п.1 в качестве возможных заместителей для Het.
12. Соединение по любому из пп.1-2, где R4 выбран из группы, включающей
![]()
где каждый R4a представляет собой водород, галоген, C1-6алкил, амино, моно- или диC1-6алкиламино, пирролидинил, пиперидинил, морфолинил, пиперазинил, 4-С1-6алкилпиперазинил; и где морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя C1-6алкильными радикалами.
13. Соединение по п.12, где в радикалах (q-1), (q-2), (q-3) или (q-4) каждый R4a независимо представляет собой водород, галоген, С1-6алкил, амино или моно- или диC1-6алкиламино.
14. Соединение по любому из пп.1-13, где R6 представляет собой метокси.
15. Соединение по п.1, которое имеет структуру
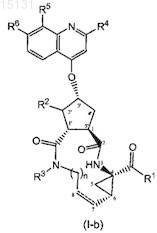
16. Соединение по п.15, в котором R2 представляет собой водород и между атомами углерода 7 и 8 присутствует двойная связь.
17. Соединение по п.1, где соединение формулы (I) представляет собой
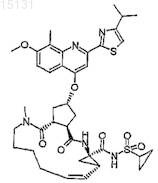
18. Соединение по п.1, где соединение формулы (I) представляет собой
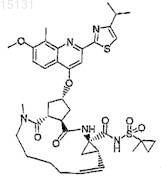
19. Соединение по п.1, где соединение формулы (I) представляет собой
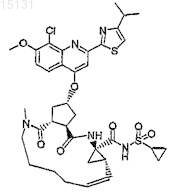
20. Соединение по п.1, где соединение формулы (I) представляет собой
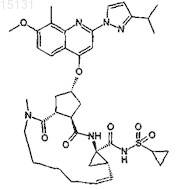
21. Соединение по любому из пп.1-20, которое не является N-оксидом или солью.
22. Соединение по любому из пп.1-21, которое не является N-оксидом.
23. Комбинация, включающая:
(a) соединение по любому из пп.1-22 или его фармацевтически приемлемую соль и
(b) ритонавир или его фармацевтически приемлемую соль.
24. Комбинация, включающая:
(a) соединение по любому из пп.1-22 или его фармацевтически приемлемую соль и
(b) интерферон-a, пегилированный интерферон-a и/или рибавирин.
25. Фармацевтическая композиция, включающая носитель и в качестве активного ингредиента противовирусно эффективное количество соединения по любому из пп.1-22.
26. Соединение по любому из пп.1-22 для применения в качестве лекарственного средства.
27. Соединение по любому из пп.1-22 для ингибирования репликации HCV.
28. Способ получения соединения по любому из пп.1-22, включающий:
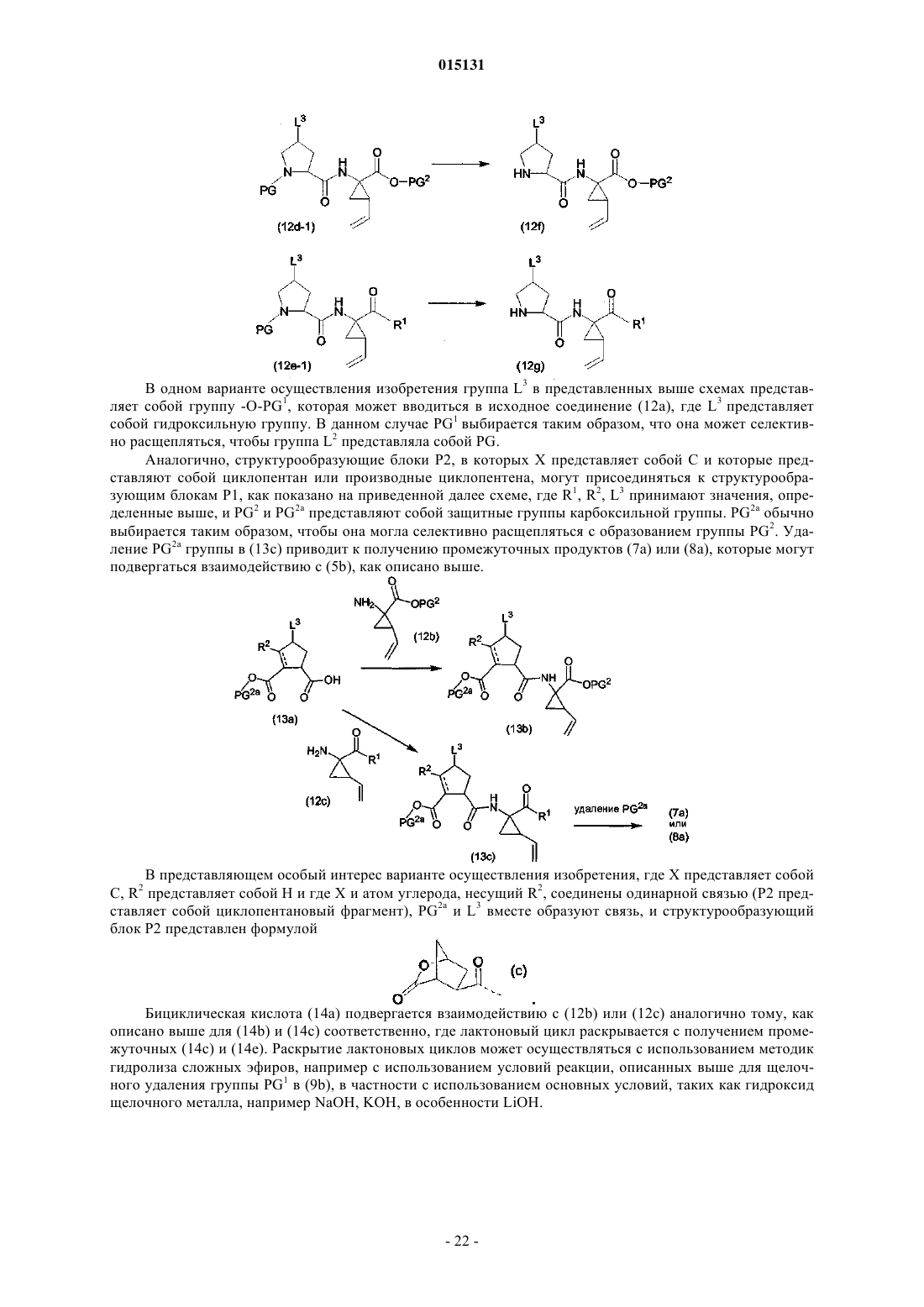
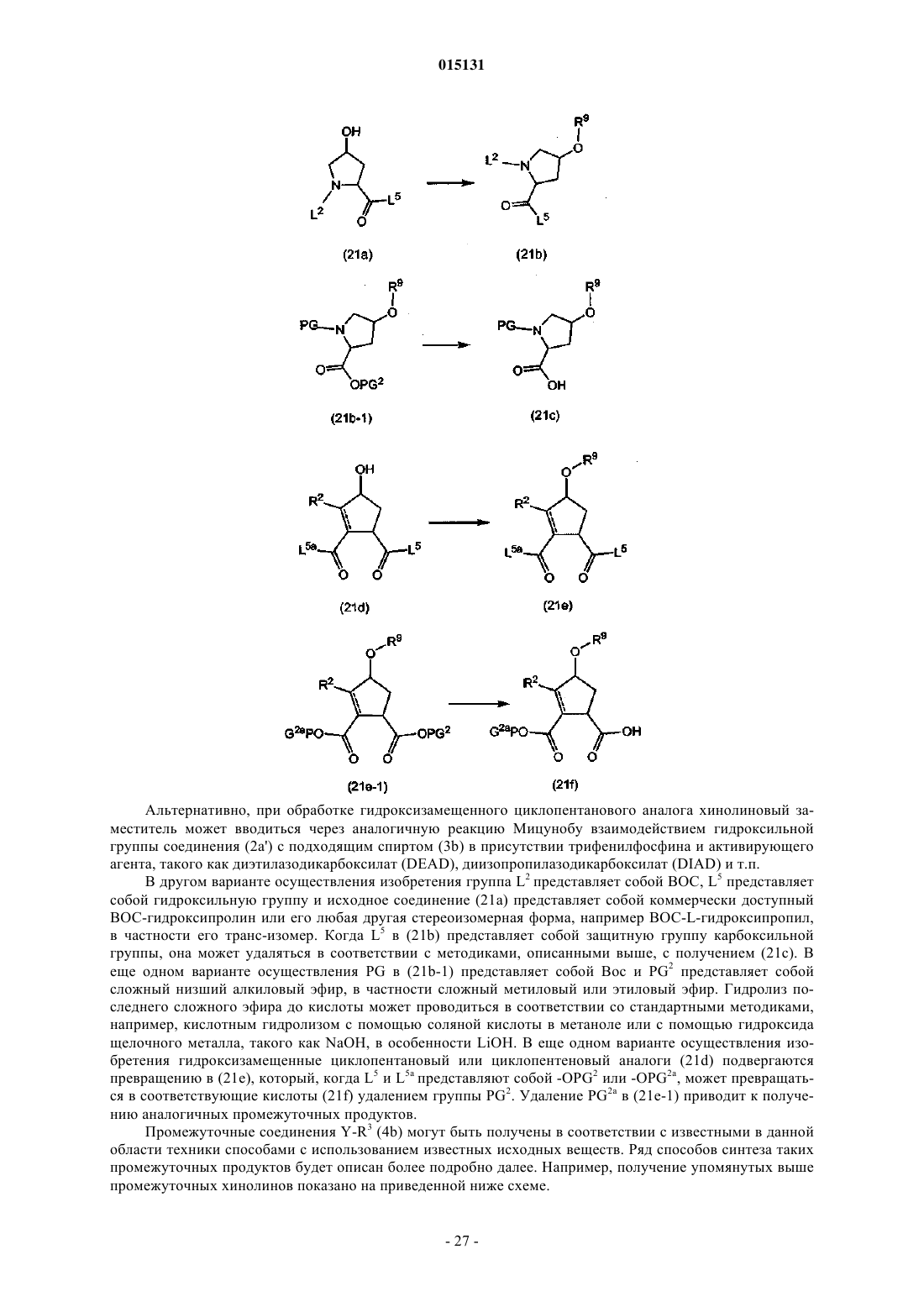
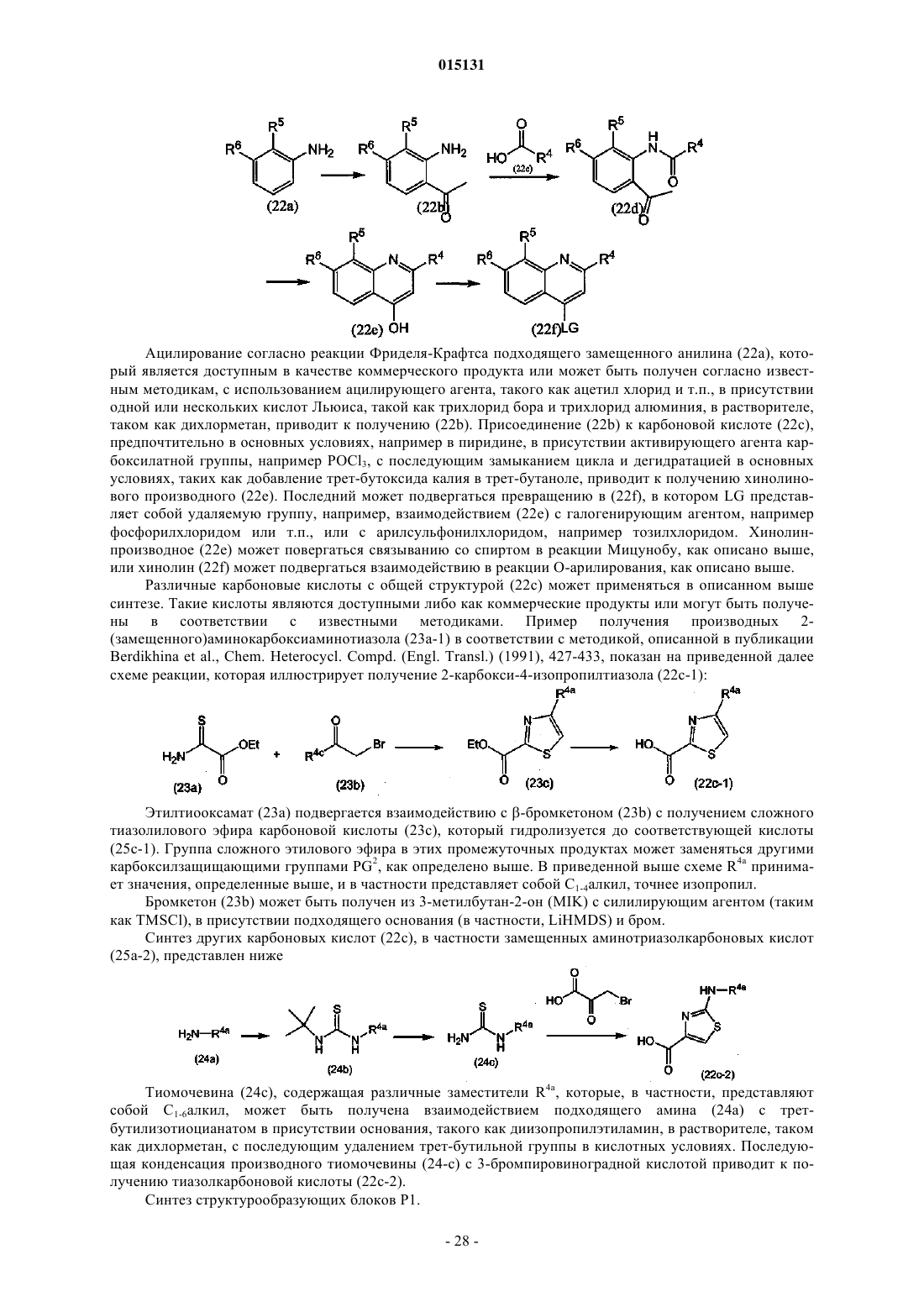
(а) получение соединения формулы (I), в котором связь между С7 и C8является двойной связью и которое представляет собой соединение формулы (I-i), посредством образования двойной связи между С7и C8 посредством реакции олефинового метатезиса с одновременной циклизацией в макроцикл, как показано на приведенной далее схеме реакции
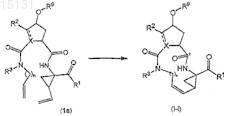
где в приведенной выше и приведенных далее схемах реакций R9представляет собой радикал
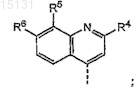
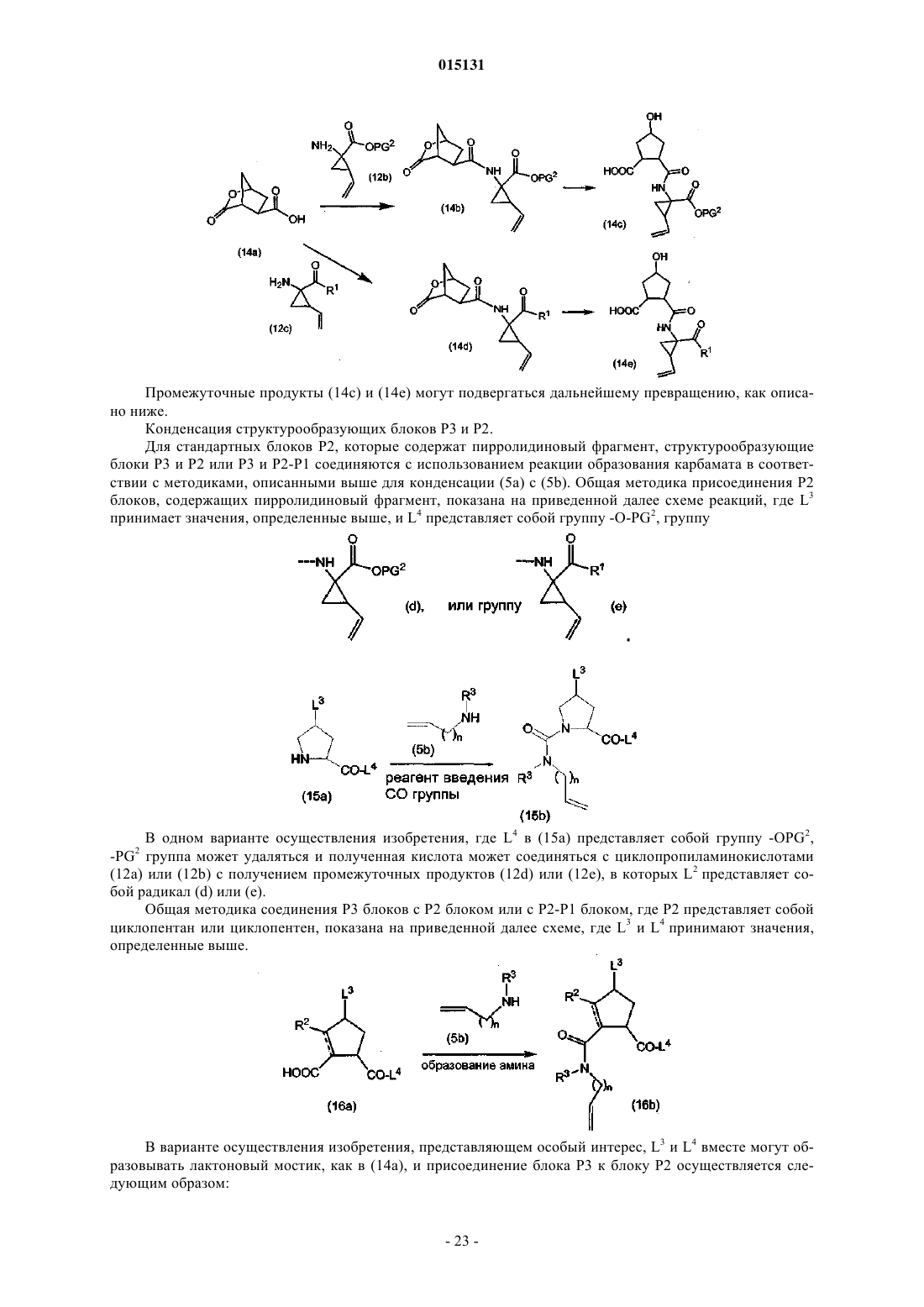
(b) превращение соединения формулы (I-i) в соединение формулы (I), в котором связь между С7 и С8в макроцикле представляет собой одинарную связь, т.е. в соединение формулы (I-j)
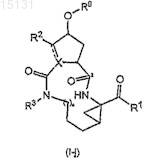
восстановлением С7-С8двойной связи в соединениях формулы (I-j);
(с) получение соединения формулы (I), где R1 представляет собой -NHSO2R8, причем указанное соединение представлено формулой (I-k-1), посредством образования амидной связи между промежуточным соединением (2а) и сульфониламином (2b), или получение соединения формулы (I), где R1 представляет собой -OR7, то есть соединения (I-k-2), посредством образования сложноэфирной связи между промежуточным соединением (2а) и спиртом (2с), как показано на приведенной далее схеме, где G представляет собой группу
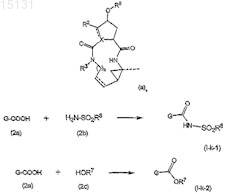
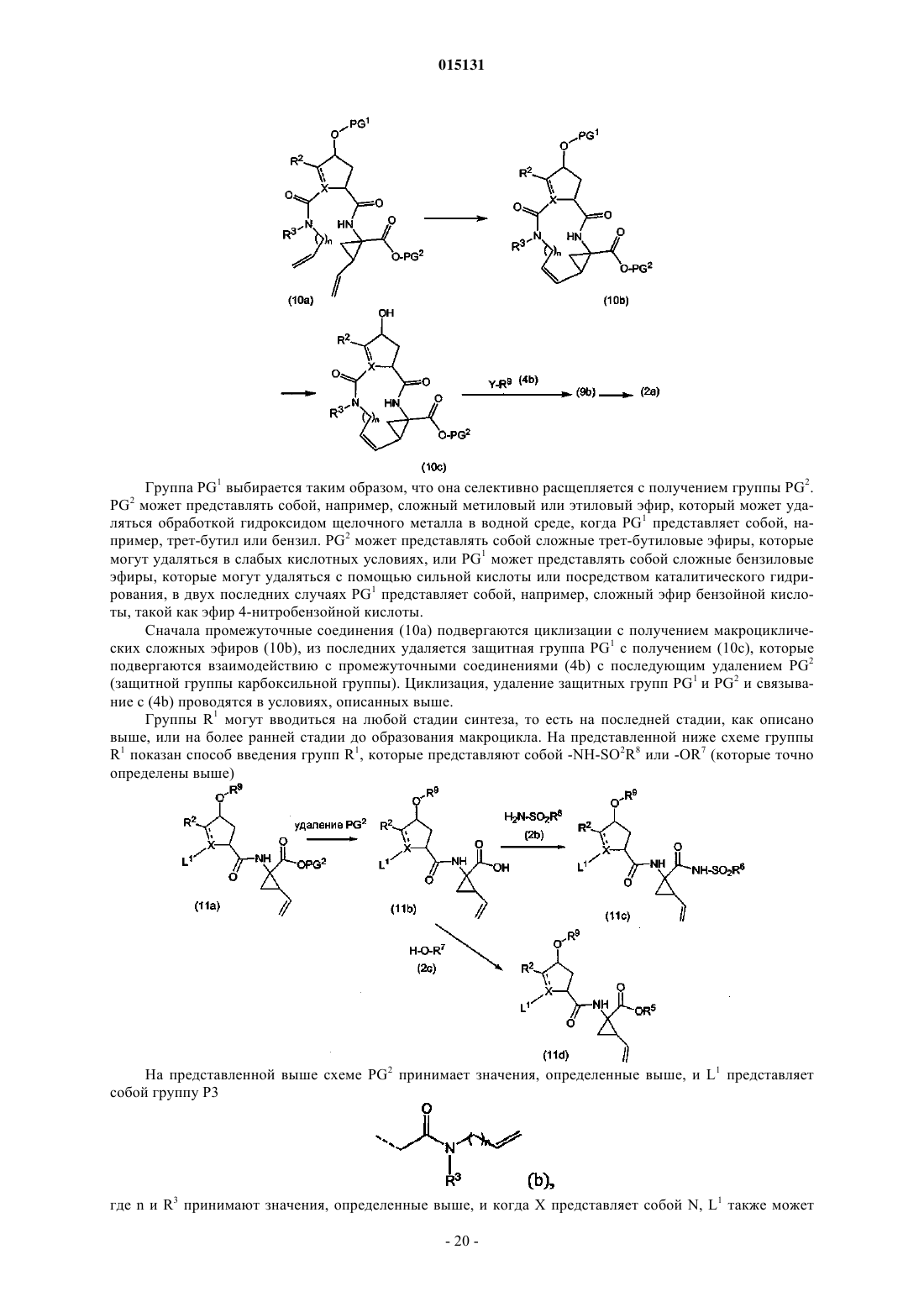
(d) получение соединения формулы (I), где R3 представляет собой водород, указанное соединение представлено формулой (I-1), из соответствующего азот-защищенного промежуточного соединения (3а), где PG представляет собой защитную группу атома азота
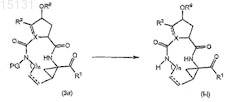
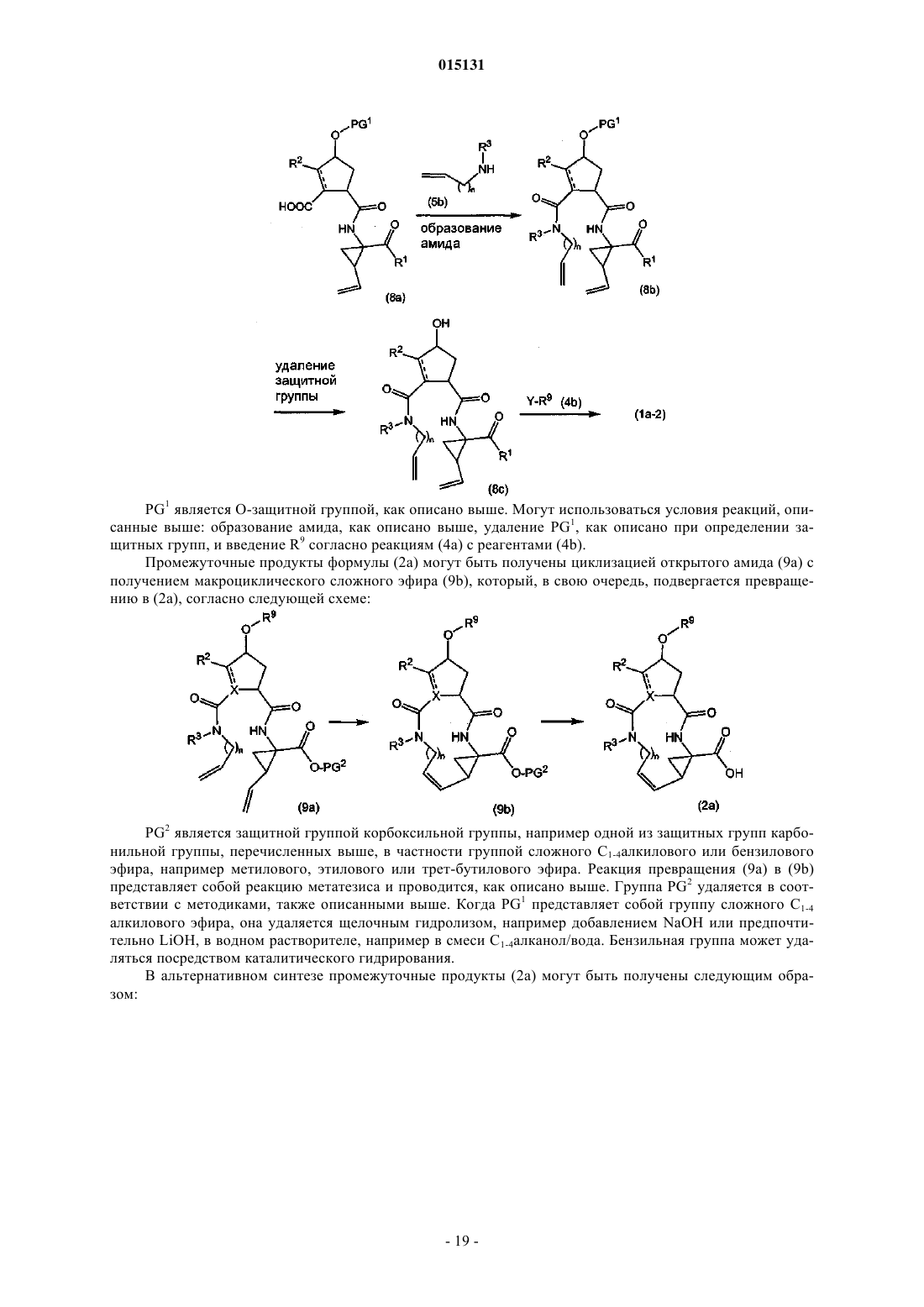
(е) взаимодействие промежуточного продукта (4а) с промежуточным продуктом (4b), как показано на приведенной далее схеме реакции

где Y в (b) представляет собой гидроксильную или удаляемую группу и где, когда Y представляет собой гидроксильную группу, взаимодействие (4а) с (4b) представляет собой реакцию Мицунобу; а когда Y представляет собой удаляемую группу, взаимодействие (4а) с (4b) представляет собой реакцию замещения;
(f) превращение соединений формулы (I) друг в друга посредством реакции трансформации функциональной группы или
(g) получение солевой формы взаимодействием свободной формы соединения формулы (I) с кислотой или основанием.
Текст
МАКРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ВИРУСА ГЕПАТИТА С Изобретатель: Рабуассон Пьер Жан-Мари Бернар, Де Кок Херман Аугустинус, Ху Лили, Вендевилль Сандрин Мари Элен, Тахри Абделлах,Сюрлеро Доминик Луи Нестор Гилэйн,Симмен Кеннет Алан (BE), Нильссон Карл Магнус, Самуэльссон Бенгт Бертил, Росенквист Оса Анника Кристина, Иванов Владимир, Пелькман Микаэль, Бельфраге Анна Карин Гертруд Линнеа, Йоханссон Пер-Ола Микаэль (SE) Представитель: Медведев В.Н. (RU) где каждая пунктирная линия представляет собой необязательную двойную связь; X представляет собой N, СН и, когда X образует двойную связь, он представляет собой С; R1 представляет собой -OR7, -NH-SO2R8; R2 представляет собой водород,и когда X представляет собой С или СН, R2 также может представлять собой C1-6 алкил; R3 представляет собой водород, C14 5 6 алкил, С 1-6 алкоксиС 1-6 алкил, С 3-7 циклоалкил; R представляет собой арил или Het; n равно 3, 4, 5 или 6; R представляет собой галоген, C1-6 алкил, гидрокси, C1-6 алкокси, фенил или Het; R6 представляет собой C1-6 алкокси или диметиламино; R7 представляет собой водород; арил; Het; С 3-7 циклоалкил, необязательно замещенный C1-6 алкилом; или C1-6 алкил, необязательно замещенный С 3-7 циклоалкилом, арилом или Het; R8 представляет собой арил; Het; С 3-7 циклоалкил, необязательно замещенный C1-6 алкилом; или C1-6 алкил, необязательно замещенный С 3-7 циклоалкилом, арилом или Het; арил представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями; Het представляет собой 5- или 6 членный насыщенный, частично ненасыщенный или полностью ненасыщенный гетероцикл, содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из атома азота, атома кислорода и атома серы, причем указанный гетероцикл является необязательно замещенным одним, двумя или тремя заместителями; предлагаются также фармацевтические композиции, содержащие соединения формулы (I), и способы получения соединений формулы (I). Кроме того, предлагаются биологически доступные комбинации ингибиторов HCV формулы (I) с ритонавиром. 015131 Настоящее изобретение относится к макроциклическим соединениям, обладающим ингибиторной активностью в отношении репликации вируса гепатита С (HCV). Оно также относится к композициям,включающим указанные соединения в качестве активных ингредиентов, а также способам получения указанных соединений и композиций. Вирус гепатита С является основной причиной распространенного во всем мире хронического заболевания печени, и данный вирус стал основным предметом серьезных медицинских исследований.HCV является представителем семейства вирусов Flaviviridae рода гепацивирусов (hepacivirus) и тесно связан с родом флавивирусов (flavivirus), который включает ряд вирусов, вовлеченных в заболевания людей, такие как вирус лихорадки денге и вирус желтой лихорадки, и с семейством вирусов животныхpestivirus, которое включает вирус вирусной диареи крупного рогатого скота (bovine viral diarrhea virus BVDV). HCV представляет собой вирус с кодирующей однонитевой линейной РНК с геномом из примерно 9600 оснований. Геном включает как 5', так и 3' нетранслируемые области, которые образуют вторичные структуры РНК, и центральную открытую рамку считывания, которая кодирует единственный полипротеин из примерно 3010-3030 аминокислот. Полипротеин кодирует десять генных продуктов, которые генерируются из предшественника полипротеина посредством ряда согласованных одновременных и посттрансляционных эндопротеолитических расщеплений, опосредуемых протеазами организмахозяина и вируса. Структурные белки вируса включают основной белок, представляющий собой нуклеокапсидный белок, и два оболочечных гликопротеина Е 1 и Е 2. Неструктурные (NS) белки отвечают за некоторые существенные ферментативные функции вируса (геликаза, полимераза, протеаза), а также представляют собой белки неизвестной функции. Репликация генома вируса опосредована РНКзависимой РНК-полимеразой, представленной неструктурным белком 5b (NS5B). Было показано, что помимо полимеразы функции геликазы и протеазы вируса, которые закодированы в бифункциональномNS3 белке, являются существенными для репликации HCV РНК. Помимо NS3 сериновой протеазы, HCV также кодирует металлопротеиназу в NS2 области. После первичной острой инфекции у большей части инфицированных пациентов развивается хронический гепатит, поскольку HCV реплицируется предпочтительно в гепатоцитах, но не является непосредственно цитопатическим. В частности, оказалось, что отсутствие активной реакции Т-лимфоцитов и высокая предрасположенность вируса к мутации способствуют высокому показателю хронической инфекции. Хронический гепатит может развиться до фиброза печени, приводящего к циррозу, заболеванию печени последней стадии и гепатоклеточному раку (hepatocellular carcinoma - НСС), что делает его основной причиной трансплантаций печени. Существует 6 основных генотипов и более 50 подтипов HCV, которые отличаются географическим распространением. HCV типа 1 является генотипом, преобладающим в Европе и США. Значительная генетическая гетерогенность HCV имеет важные диагностические и клинические проявления, что, вероятно, объясняет трудности в разработке вакцины и невосприимчивость к терапевтическому лечению. Передача HCV может происходить через контакт с зараженной кровью или продуктами, полученными из такой крови, например после переливания крови или внутривенного применения лекарственных препаратов. Применение диагностических тестов при проверке крови привело к тенденции снижения посттрансфузионного заражении HCV. Однако при медленном развитии заболевания печени до конечной стадии те инфекции, которые уже имеют место, будут представлять собой серьезную медицинскую и экономическую проблему в течение десятков лет. Существующие в настоящее время терапевтические методы лечения HCV основаны на (пегилированном) -интерфероне (IFN-) в сочетании с рибавирином. Данная комбинированная терапия приводит к получению устойчивого вирусологического ответа у более 40% пациентов, инфицированных вирусами генотипа 1, и приблизительно у 80% пациентов, инфицированных вирусами генотипов 2 и 3. Помимо ограниченной эффективности в отношении HCV типа 1 такая комбинированная терапия дает значительные побочные эффекты и плохо переносится многими пациентами. Основные побочные эффекты включают симптомы, напоминающие симптомы заболевания гриппом, гематологические отклонения и невропсихиатрические симптомы. Такие образом, существует потребность в более эффективных, удобных и хорошо переносимых способах лечения. В последнее время в качестве возможных клинических лекарственных средств привлекают внимание два пептидомиметических ингибитора протеазы HCV, а именно BILN-2061, описанный в WO 00/59929, и VX-950, описанный в WO 03/87092. Ряд аналогичных ингибиторов протеазы HCV также был описан в периодических научных изданиях и патентной литературе. Стало очевидно, что постоянное введение BILN-2061 или VX-950 приводит к появлению селективных мутантов HCV, которые являются устойчивыми к соответствующему лекарственному средству, так называемых мутантов, ускользнувших от лекарственного средства. Эти мутанты, устойчивые к лекарственным средствам, содержат характеристические мутации в геноме протеазы HCV, в частности D168V, D168A и/или A156S. Таким образом, существует потребность в дополнительных лекарственных средствах с разными моделями резистентности для обеспечения пациентов, испытывающих недостаток в лекарственных средствах, и поэтому комбинированная терапия с применением нескольких лекарственных средств, вероятно, в будущем-1 015131 будет нормой даже при лечении лекарственными средствами первого выбора. Испытания с лекарственными средствами для лечения ВИЧ, в частности ингибиторами протеазы ВИЧ, также показали, что субоптимальные фармакокинетические свойства и сложные схемы приема лекарственных средств быстро приводят к случайным нарушениям режима приема. Это, в свою очередь,означает, что самое низкое значение 24-часовой концентрации (минимальная концентрация в плазме крови) для соответствующих лекарственных средств в режиме лечения ВИЧ зачастую выходит за предел нижнего значения IC90 или ED90 в течение больших временных отрезков дня. Считается, что минимальное значение 24-часовой концентрации, равное, по меньшей мере, IC50, точнее IC90 или ED90, является существенным для замедления развития мутантов, резистентных к лекарственным средствам. Наличие необходимых фармакокинетических свойств и нужного метаболизма лекарственных веществ для обеспечения нужных уровней минимальной концентрации в плазме является строгим ограничением для разработки лекарственных средств. Выраженная пептидомиметическая природа ингибиторов протеазы HCV предшествующего уровня техники с множеством пептидных связей приводит к фармакокинетическим ограничениям в эффективных схемах приема лекарственных средств. Таким образом, существует потребность в ингибиторах HCV, с помощью которых можно преодолеть трудности применения используемых в настоящее время терапевтических лекарственных средств для лечения HCV, такие как побочные эффекты, ограниченная эффективность, развитие резистентности и неблагоприятные результаты вследствие случайного нарушения схемы приема лекарственного средства. Настоящее изобретение относится к ингибиторам HCV более высокого качества по одному или нескольким из перечисленных далее связанных фармакологических свойств, то есть эффективности, сниженной цитотоксичности, улучшенным фармакокинетическим свойствам, улучшенному профилю резистентности, приемлемой дозировке и содержанию в таблетках (pill burden). Кроме того, соединения согласно настоящему изобретению являются соединениями с относительно низкой молекулярной массой и легко синтезируются из исходных веществ, которые являются коммерчески доступными или могут легко синтезироваться согласно известным в данной области техники методикам синтеза. В WO 05/010029 описываются аза-пептидные макроциклические ингибиторы сериновой протеазы гепатита С, фармацевтические композиции, включающие вышеупомянутые соединения для введения субъекту, страдающему HCV инфекцией, и способы лечения HCV инфекции у субъекта введением фармацевтической композиции, включающей указанные соединения. Настоящее изобретение относится к ингибиторам репликации HCV, которые могут быть представлены формулой (I) и их N-оксидам, солям и стереоизомерам, где каждая пунктирная линия (изображенная как ) означает необязательную двойную связь;X представляет собой N, СН, и когда X образует двойную связь, он представляет собой С;R2 представляет собой водород, и когда X представляет собой С или СН, R2 также может представлять собой C1-6 алкил;R4 представляет собой арил или Het;R8 представляет собой арил; Het; С 3-7 циклоалкил, необязательно замещенный С 1-6 алкилом; или С 1-6 алкил, необязательно замещенный С 3-7 циклоалкилом, арилом или Het; арил в качестве группы или части группы представляет собой фенил, необязательно замещенный-2 015131 одним, двумя или тремя заместителями, выбранными из галогена, гидрокси, нитро, циано, карбоксильной группы, C1-6 алкила, С 1-6 алкокси, С 1-6 алкоксиС 1-6 алкила, С 1-6 алкилкарбонила, амино, моно- или ди-С 1-6 алкиламино, азидо, меркапто, полигалогенС 1-6 алкила, полигалогенС 1-6 алкокси, С 3-7 циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-C1-6 алкилпиперазинила, 4-С 1-6 алкилкарбонилпиперазинила и морфолинила; где морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя С 1-6 алкильными радикалами;Het в качестве группы или части группы представляет собой 5- или 6-членный насыщенный, частично ненасыщенный или полностью ненасыщенный гетероцикл, содержащий от 1 до 4 гетероатомов,каждый из которых независимо выбран из атома азота, атома кислорода и атома серы, причем указанный гетероцикл является необязательно конденсированным с бензольным кольцом; и Het в целом является необязательно замещенным одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы заместителей, включающей галоген, гидрокси, нитро, циано, карбоксильную группу, С 1-6 алкил, С 1-6 алкокси, С 1-6 алкоксиС 1-5 алкил, С 1-6 алкилкарбонил, амино, моно- или ди-С 1-6 алкиламино, азидо,меркапто, полигалогенС 1-6 алкил, полигалогенС 1-6 алкокси, С 3-7 циклоалкил, пирролидинил, пиперидинил,пиперазинил, 4-С 1-6 алкилпиперазинил, 4-С 1-6 алкилкарбонилпиперазинил и морфолинил; где морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя С 1-6 алкильными радикалами. Изобретение также относится к способам получения соединений формулы (I), их N-оксидов, аддитивных солей, четвертичных аминов, комплексов с металлами и стереохимических изомерных форм,промежуточных продуктов и к применению промежуточных продуктов для получения соединений формулы (I). Изобретение относится к соединениям формулы (I), как таковым, их N-оксидам, аддитивным солям,четвертичным аминам, комплексам с металлами и стереохимическим изомерным формам для применения в качестве лекарственного средства. Изобретение относится также к фармацевтическим композициям, включающим носитель и противовирусно эффективное количество соединения формулы (I), которые описаны выше. Фармацевтические композиции могут содержать комбинации упомянутых выше соединений с другими противо-HCV средствами. Изобретение относится также к упомянутым фармацевтическим композициям для введения субъекту, страдающему HCV инфекцией. Изобретение относится также к применению соединения формулы (I) или его N-оксида, аддитивной соли, четвертичного амина, комплекса с металлами или его стереохимически изомерных форм для производства лекарственного средства для ингибирования репликации HCV. Или изобретение относится к способу ингибирования репликации HCV в организме теплокровного животного, причем указанный способ включает введение эффективного количества соединения формулы (I) или его пролекарства, Nоксида, аддитивной соли, четвертичного амина, комплекса с металлами или стереохимически изомерных форм. За исключением особо оговоренных случаев в представленном описании используются следующие определения. Термин галоген представляет собой общее название фтора, хлора, брома и йода. Термин полигалогенС 1-6 алкил, используемый для определения группы или части группы, например полигалогенС 1-6 алкоксигруппы, означает моно- или полигалогензамещенный С 1-6 алкил, в частности С 1-6 алкил, замещенный одним, двумя, тремя, четырьмя, пятью, шестью или большим количеством атомов галогена, такой как метил или этил, содержащий один или несколько атомов фтора, например дифторметил, трифторметил, трифторэтил. Предпочтительным является трифторметил. Данный термин включает также перфторС 1-6 алкильные группы, например пентафторэтил. В случае, когда к алкильной группе, определенной термином полигалогенС 1-6 алкил, присоединено более одного атома галогена,атомы галогена могут быть одинаковыми или отличаться друг от друга. Термин С 1-4 алкил, используемый для определения группы или части группы, означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 4 атомов углерода, такие как, например, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-1-пропил; термин С 1-6 алкил включает С 1-4 алкильные радикалы и их высшие гомологи, содержащие 5 или 6 атомов углерода, такие как, например, 1-пентил, 2-пентил, 3-пентил, 1-гексил, 2-гексил, 2-метил-1-бутил, 2-метил-1 пентил, 3-этил-1-бутил, 3-метил-2-пентил и т.п. Среди групп, определенных термином С 1-6 алкил, особый интерес представляет С 1-4 алкил. Термин С 2-6 алкенил, используемый для определения группы или части группы, означает углеводородные радикалы с прямой или разветвленной цепью, содержащие насыщенные углерод-углеродные связи и по меньшей мере одну двойную связь и включающие от 2 до 6 атомов углерода, такие как, например, этенил (или винил), 1-пропенил, 2-пропенил (или аллил), 1-бутенил, 2-бутенил, 3-бутенил, 2 метил-2-пропенил, 2-пентенил, 3-пентенил, 2-гексенил, 3-гексенил, 4-гексенил, 2-метил-2-бутенил, 2 метил-2-пентенил и т.п. Среди групп, определенных термином С 2-6 алкенил, особый интерес представляет С 2-4 алкенил. Термин С 2-6 алкинил, используемый для определения группы или части группы, означает углево-3 015131 дородные радикалы с прямой или разветвленной цепью, содержащие насыщенные углерод-углеродные связи и по меньшей мере одну тройную связь и включающие в себя от 2 до 6 атомов углерода, такие как,например, этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 2-пентинил, 3-пентинил,2-гексинил, 3-гексинил и т.п. Среди групп, определенных термином С 2-6 алкинил, особый интерес представляет С 2-4 алкинил. Термин С 3-7 циклоалкил включает циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Термин С 1-6 алкандиил означает двухвалентные насыщенные углеводородные радикалы с прямой и разветвленной цепью, содержащие 1 до 6 атомов углерода, такие как, например, метилен, этилен, 1,3 пропандиил, 1,4-бутандиил, 1,2-пропандиил, 2,3-бутандиил, 1,5-пентандиил, 1,6-гександиил и т.п. Среди групп, определенных термином С 1-6 алкандиил, особый интерес представляет С 1-4 алкандиил. Термин С 1-6 алкокси означает С 1-6 алкилокси, в котором C1-6 алкил представляет собой группу, определенную выше. Использованный выше в описании элемент (=O) или оксо образует карбонильный фрагмент, когда указанный элемент присоединен к атому углерода, сульфоксидный фрагмент, когда данный элемент присоединен к атому серы, и сульфонильный фрагмент, когда два указанных элемента присоединены к атому серы. Всякий раз, когда цикл или циклическая система замещены оксогруппой, атом углерода, к которому присоединена оксогруппа, является насыщенным атомом углерода. Радикал, обозначенный как Het, представляет собой гетероцикл, который определен в данном описании и формуле изобретения. Предпочтительными среди Het-радикалов являются моноциклические радикалы. Примеры Het включают, например, пирролидинил, пиперидинил, морфолинил, тиоморфолинил,пиперазинил, пирролил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазинолил, изоотиазинолил,тиазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил (включая 1,2,3-триазолил, 1,2,4 триазолил), тетразолил, фуранил, тиенил, пиридил, пиримидил, пиридазинил, триазинил и т.п. Среди групп, определенных термином Het, интерес представляют ненасыщенные радикалы, в особенности радикалы, обладающие ароматическими свойствами. Особый интерес представляют Het-радикалы, содержащие один или два атома азота. Каждый из Het-радикалов, упомянутых в данном и следующих абзацах, может быть необязательно замещен заместителями, число и вид которых указаны в определениях соединений формулы (I) или любой из подгрупп соединений формулы (I). Некоторые из Het-радикалов, упомянутых в данном и следующих далее абзацах, могут быть замещены одним, двумя или тремя гидроксильными заместителями. Такие гидроксизамещенные циклы могут существовать в виде таутомерных форм, содержащих кетогруппы. Например, 3-гидроксипиридазиновый фрагмент может существовать в его таутомерной форме как 2 Н-пиридазин-3-он. Когда Het представляет собой пиперазинил, он предпочтительно является замещенным в положении 4 заместителем, присоединенным к атому азота через атом углерода, например, 4 С 1-6 алкилом, 4-полигалогенС 1-6 алкилом, С 1-6 алкоксиС 1-6 алкилом, С 1-6 алкилкарбонилом, С 3-7 циклоалкилом.Het-радикалы, представляющие интерес, включают, например, пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, пирролил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил (включая 1,2,3-триазолил, 1,2,4-триазолил),тетразолил, фуранил, тиенил, пиридил, пиримидил, пиридазинил, пиразолил, триазинил, или любой из таких гетероциклов, конденсированный с бензольных кольцом, такой как индолил, индазолил (в частности, 1 Н-индазолил), индолинил, хинолинил, тетрагидрохинолинил (в частности, 1,2,3,4 тетрагидрохинолинил), изохинолинил, тетрагидроизохинолинил (в частности, 1,2,3,4-тетрагидроизохинолинил), хиназолинил, фталазинил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензоксадиазолил, бензотиадиазолил, бензофуранил, бензотиенил.Het-радикалы пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, 4 замещенный пиперазинил предпочтительно присоединены через атом азота (т.е. представляют собой 1 пирролидинил, 1-пиперидинил, 4-тиоморфолинил, 4-морфолинил, 1-пиперазинил, 4-замещенный 1 пиперазинил). Следует отметить, что положения используемых в определениях радикалов на любом фрагменте молекул могут быть произвольными до тех пор, пока при этом молекула является химически стабильной. За исключением особо оговоренных случаев радикалы, используемые в определениях переменных,включают все возможные изомеры. Например, термин пиридил включает 2-пиридил, 3-пиридил и 4 пиридил; термин пентил включает 1-пентил, 2-пентил и 3-пентил. Когда любая переменная встречается более одного раза в любой составляющей, каждое определение является независимым. Подразумевается, что всякий раз, когда далее используется термин соединения формулы (I) , термин настоящие соединения или аналогичные термины, они включают соединения формулы (I), их пролекарства, N-оксиды, аддитивные соли, четвертичные амины, комплексы с металлами и стереохимически-4 015131 изомерные формы. Один вариант осуществления изобретения включает соединения формулы (I) или любую подгруппу соединений формулы (I), описанную в изобретении, а также их N-оксиды, соли в качестве возможных стереоизомерных форм. Другой вариант осуществления изобретения включает соединения формулы (I) или любую подгруппу соединений формулы (I), описанную в изобретении, а также их соли в качестве их возможных стереоизомерных форм. Соединения формулы (I) содержат несколько центров хиральности и существуют в виде стереохимически изомерных форм. Термин стереохимически изомерные формы, когда используется в данном описании, означает все возможные соединения, образованные такими же атомами, соединенными в такой же последовательность, но имеющие отличные друг от друга трехмерные структуры, которые не являются взаимозаменяемыми и которыми могут обладать соединения формулы (I). Что касается примеров, в которых для описания абсолютной конфигурации хирального атома в заместителе используются символы (R) или (S), при таком описании принимается во внимание все соединение, а не отдельно заместитель. За исключением особо оговоренных случаев химическое обозначение соединения включает все возможные стереохимически изомерные формы, которыми могло обладать указанное соединение. Указанная смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанного соединения. Подразумевается, что все стереохимически изомерные формы соединений согласно настоящему изобретению как в чистой форме, так и в форме смесей, включены в объем настоящего изобретения. Чистые стереоизомерные формы соединений и промежуточных продуктов, которые упомянуты в описании, определены как изомеры, по существу, свободные от других энантиомерных или диастереомерных форм такой же основной молекулярной структуры указанных соединений или промежуточных продуктов. В частности, термин стереоизомерно чистые относится к соединениям или промежуточным продуктам со стереомерным избытком по меньшей мере от 80% (т.е. минимум 90% одного изомера и максимум 10% других возможных изомеров) до 100% (т.е. 100% одного изомера и отсутствие другого),предпочтительно к соединениям или промежуточным продуктам со стереоизомерным избытком от 90 до 100%, более предпочтительно со стереизомерным избытком от 94 до 100% и наиболее предпочтительно со стереоизомерным избытком от 97 до 100%. Термин энантиомерно чистые и диастереомерно чистые следует понимать аналогично, но в отношении энантиомерного избытка и диастеремерного избытка соответственно данной смеси. Чистые стереизомерные формы соединений и промежуточных продуктов согласно настоящему изобретению могут быть получены с применением методик, известных в данной области техники. Например, энантиомеры могут разделяться селективной кристаллизацией их диастереомерных солей с оптически активными кислотами или основаниями. Примерами таких кислот являются винная кислота,дибензоилвинная кислота, дитолуоилвинная кислота и камфорсульфоновая кислота. Альтернативно,энантиомеры могут разделяться хроматографическими методами с использованием хиральных стационарных фаз. Указанные чистые стереохимически изомерные формы также могут быть получены из соответствующих чистых стереохимически изомерных форм подходящих исходных веществ при условии,что реакция протекает стереоспецифически. Предпочтительно, если желательно получение специфического стереоизомера, указанное соединение будет синтезироваться стереспецифическими способами получения. В данных способах полезно будет применение энантиомерно чистых исходных веществ. Диастереомерные рацематы соединений формулы (I) могут быть получены отдельно удобными способами. Подходящими способами физического разделения, которые могут успешно применяться, являются, например, селективная кристаллизация и хроматография, например колоночная хроматография. Для некоторых соединений формулы (I), их пролекарств, N-оксидов, солей, сольватов, четвертичных аминов или комплексов с металлами и промежуточных продуктов, используемых при их получении,абсолютная стереохимическая конфигурация не была установлена экспериментально. Специалист данной области техники может определить абсолютную конфигурацию таких соединений, используя методы, известные в данной области техники, например дифракцию рентгеновских лучей. Подразумевается, что настоящее изобретение включает все изотопы атомов, встречающихся в настоящих соединениях. Изотопы включают атомы с таким же атомным числом, но другими массовыми числами. В качестве общего примера, но без ограничения данным примером, можно привести изотопы водорода, которые включают тритий и дейтерий. Изотопы углерода включают С-13 и С-14. Термин пролекарство, когда используется в данном описании, означает фармакологически приемлемые производные, такие как сложные эфиры, амиды и фосфаты, продукт биологического превращения которых in vivo представляет собой активное лекарственное средство, которое определено в описании соединений формулы (I). Общее определение пролекарств дано Goodman и Gilman в монографии:The Pharmacological Basis of Therapeutics, 8th ed, McGraw-Hill, Int. Ed. 1992, "Biotransformation of Drugs",p. 13-15 - которая введена в данное описание в виде ссылки. Предпочтительно, пролекарства обладают прекрасной растворимостью в воде, повышенной биодоступностью и легко метаболизируются в активные ингибиторы in vivo. Пролекарста соединений согласно настоящему изобретению могут быть полу-5 015131 чены модификацией функциональных групп настоящего соединения таким образом, что полученные модифицированные соединения расщепляются либо в результате простой манипуляции, либо в условияхin vivo с получением исходного соединения. Предпочтительными являются фармацевтически приемлемые сложноэфирные пролекарства, которые могут гидролизоваться in vivo и которые получены из соединений формулы (I), содержащих гидроксильную или карбоксильную группу. Способный гидролизоваться in vivo сложный эфир представляет собой сложный эфир, который подвергается гидролизу в организме человека или животного с получение исходной кислоты или исходного спирта. Подходящие фармацевтически приемлемые сложные эфиры для карбоксисоединений включают C1-6 алкоксиметиловые эфиры, например метоксиметиловый эфир,С 1-6 алканоилоксиметиловые эфиры, например пивалоилоксиметиловый, фталидиловый эфиры, С 3-8 циклоалкоксикарбонилоксиС 1-6 алкиловые эфиры, например 1-циклогексилкарбонилоксиэтиловый эфир; 1,3 диоксолен-2-онилметиловые эфиры, например 5-метил-1,3-диоксолен-2-онилметиловый эфир; и С 1-6 алкоксикарбонилоксиэтиловые эфиры, например 1-метоксикарбонилоксиэтиловый эфир, который может быть получен на любой карбоксильной группе в соединениях согласно настоящему изобретению. Способный гидролизоваться in vivo сложный эфир соединения формулы (I), содержащего гидроксильную группу, включает неорганические сложные эфиры, такие как фосфаты, и простые ацилоксиалкиловые эфиры и родственные соединения, которые в результате гидролиза сложного эфираin vivo разлагаются с получением исходной гидроксильной группы. Примеры простых ацилоксиалкиловых эфиров включают ацетоксиметоксиэфир и 2,2-диметилпропионилоксиметоксиэфир. Примеры групп, образующих с гидроксильной группой способный гидролизоваться in vivo сложный эфир, включают алканоил, бензоил, фенилацетил и замещенные бензоил и фенилацетил, алкоксикарбонил (для получения сложных карбонатов), диалкилкарбамоил и N-(диалкиламиноэтил)-Nалкилкарбамоил (для получения карбаматов), диалкиламиноацетил и карбоксиацетил. Примеры заместителей в составе бензоила включают морфолино и пиперазино, присоединенные через атом азота цикла с помощью метиленовой группы в положении 3 или 4 бензоильного кольца. Солями соединений формулы (I), подходящими для терапевтического применения, являются соли,в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут найти применение, например для получения или очистки фармацевтически приемлемого соединения. Все соли, как фармацевтически приемлемые, так и фармацевтически не приемлемые, включены в объем настоящего изобретения. Подразумевается, что фармацевтически приемлемые кислотно- и основно-аддитивные соли, которые упомянуты выше, включают терапевтически активные нетоксичные кислотно- и основноаддитивные солевые формы, которые могут образовывать соединения формулы (I). Фармацевтически приемлемые кислотно-аддитивные соли могут быть получены стандартным способом обработкой основной формы такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогеноводородные кислоты, например соляная кислота или бромисто-водородная кислота, серную, азотную, фосфорную и т.п. кислоты или органические кислоты, такие как, например,уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.е. этандиовая), малоновая, янтарная (т.е. бутандиовая), малеиновая, фумаровая, яблочная (т.е. гидроксибутандиовая), винная,лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая,салициловая, п-аминосалициловая, памовая и т.п. кислоты. И наоборот, указанные солевые формы могут превращаться в форму свободного основания при обработке подходящим основанием. Соединения формулы (I), содержащие кислотный протон, также могут превращаться в нетоксичные аддитивные солевые формы металлов или амино-аддитивные солевые формы при обработке подходящими органическими или неорганическими основаниями. Подходящие основные солевые формы включают, например, аммониевые соли, соли щелочных или щелочно-земельных металлов, например соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например бензатином,N-метил-D-глюкамином, гидрабаминовые соли и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. Термин аддитивная соль, который упомянут выше, также включает сольваты, которые могут образовывать соединения формулы (I), а также их соли. Такими сольватами являются, например, гидраты,алкоголяты и т.п. Термин четвертичный амин, который использовался в описании выше, означает четвертичные аммониевые соли, которые соединения формулы (I) могут образовывать в результате взаимодействия основного азота в соединении формулы (I) и соединения, способствующего образованию четвертичного соединения, такого как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например метилйодид или бензилйодид. Могут также использоваться другие реагенты с легко удаляемыми группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-толуолсульфонат. Четвертичный амин содержит положительно заряженный атом азота. Термин фармацевтически приемлемые противоионы включает хлор, бром, йод, трифторацетат и-6 015131 ацетат. Выбранный противоион может вводиться с использованием ионно-обменных смол. Подразумевается, что N-оксидные формы настоящих соединений включают соединения формулы(I), в которых один или несколько атомов азота окислены до так называемого N-оксида. Следует принять во внимание, что соединения формулы могут обладать способностью связывания металлов, а также хелатообразующими и комплексообразующими свойствами и, следовательно, могут существовать в виде комплексов с металлами или хелатов с металлами. Подразумевается, что такие металлсодержащие производные соединений формулы (I) включены в объем настоящего изобретения. Некоторые соединения формулы (I) также могут существовать в таутомерной форме. Подразумевается, что такие формы, хотя подробно не показаны на приведенной выше формуле, включены в объем настоящего изобретения. Как указывалось выше, соединения формулы (I) содержат несколько асимметрических центров. Для более удобной ссылки на каждый из этих асимметрических центров будет использоваться система нумерации, которая показана на представленной ниже структурной формуле Асимметрические центры находятся в положениях 1, 4 и 6 макроцикла, а также при атоме углерода в положении 3' в 5-членном цикле, при атоме углерода в положении 2', когда R2 заместитель представляет собой С 1-6 алкил, и при атоме углерода в положении 1', когда X представляет собой СН. Каждый из этих асимметрических центров может существовать в R или S конфигурации. Стереохимия при атоме в положении 1 предпочтительно соответствует стереохимии конфигурацииL-аминокислоты, т.е. L-пролина. Когда X представляет собой СН, 2 карбонильные группы, расположенные в положениях 1' и 5' циклопентанового цикла, предпочтительно находятся в транс-конфигурации. Карбонильный заместитель в положении 5' предпочтительно находится в конфигурации, которая соответствует конфигурации Lпролина. Карбонильные группы, расположенные в положениях 1' и 5', предпочтительно располагаются,как показано ниже на представленной структурной формуле Соединения формулы (I) включают циклопропильную группу, как показано на структурном фрагменте, представленном ниже где С 7 представляет собой атом углерода в положении 7, и атомы углерода в положениях 4 и 6 являются асимметрическими атомами углерода циклопропанового кольца. Несмотря на другие возможные асимметрические центры на других участках соединений формулы(I), присутствие этих двух асимметрических центров означает, что соединения могут существовать в виде смесей диастереомеров, таких как диастереомеры соединений формулы (I), в которых атом углерода в положении 7 находится либо в син-конфигурации по отношению к карбонилу или в син-конфигурации по отношению к амидогруппе, как показано ниже. Один вариант осуществления изобретения относится к соединениям формулы (I), в которых атом углерода в положении 7 находится в син-конфигурации относительно карбонила. Другой вариант осуществления изобретения относится к соединениям формулы (I), в которых конфигурация при атоме углерода в положении 4 представляет собой R-конфигурацию. Особую подгруппу соединений формулы (I) составляют соединения, в которых атом углерода в положении 7 находится в син-конфигурации относительно карбонила, и конфигурация при атоме углерода в положении 4 представляет собой Rконфигурацию. Соединения формулы (I) могут также включать пролиновый остаток (когда X представляет собойN), либо циклопентильный или циклопентенильный остаток (когда X представляет собой СН или С). Предпочтительными являются соединения формулы (I), в которых заместитель в положении 1 (или 5') и заместитель в положении 3' находится в транс-конфигурации. В частности интерес представляют соединения формулы (I), где положение 1 соотвеиствует конфигурации L-пролина и заместитель в положении 3' находится в транс-конфигурации относительно положения 1. Предпочтительно соединения формулы(I) имеют стереохимию, представленную ниже на структурах формул (Ia) и (Ib) Один вариант осуществления настоящего изобретения относится к соединениям формулы (I) или формулы (Ia) или любой подгруппе соединений формулы (I), которые соответствую одному или нескольким из следующих условий:(b) X представляет собой атом азота;(c) двойная связь находится между атомами углерода в положениях 7 и 8. Другой вариант осуществления настоящего изобретения относится к соединениям формулы (I) или формул (Ia), (Ib) или любой подгруппе соединений формулы (I), которые соответствуют одному или нескольким из следующих условий:(c) двойная связь находится между атомами углерода в положениях 7 и 8. Особую подгруппу соединений формулы (I) составляют соединения, представленные следующими структурными формулами: Среди соединений формулы (I-c) и (I-d) соединения, имеющие стереохимическую конфигурацию соединений формул (Ia) и (Ib), соответственно, представляют особый интерес. Двойная связь между атомами углерода в положениях 7 и 8 в соединениях формулы (I) или в любой подгруппе соединений формулы (I) может иметь цис- или транс-конфигурацию. Предпочтительно двойная связь между атомами углерода в положениях 7 и 8 имеет цис-конфигурацию, как показано на формулах (I-c) и (I-d). Двойная связь между атомами углерода в положениях 1' и 2' может присутствовать в соединениях формулы (I) или в любой подгруппе соединений формулы (I), как показано в формуле (I-е), представленной ниже Еще одну особую подгруппу соединений формулы (I) составляют соединения, представленные приведенными ниже структурными формулами-9 015131 Среди соединений формулы (I-f), (I-g) или (I-h) соединения, имеющие стереохимическую конфигурацию соединений формул (Ia) и (Ib), соответственно, представляют особый интерес. В формулах (Ia), (Ib), (Ic), (Id), (Ie), (If), (Ig) и (Ih), когда это применимо, X, n, R1, R2, R3, R4, R5 и R6 принимают значения, указанные в определениях соединений формулы (I) или любой из подгрупп соединений формулы (I), специально определенных в описании. Следует представлять, что, как подразумевается, определенные выше подгруппы соединений формул (Ia), (Ib), (Ic), (Id) , (Ie), (If), (Ig) или (Ih), а также любая другая подгруппа, определенная в описании,включает также любые N-оксиды, аддитивные соли, четвертичные амины, комплексы с металлами и стереохимически изомерные формы таких соединений. Когда в соединениях формулы (I) или любой подгруппе соединений формулы (I) n равно 2, фрагмент -СН 2-, заключенный в скобки с индексом n, соответствует этандиилу. Когда в соединениях формулы (I) или любой подгруппе соединений формулы (I) n равно 3, фрагмент -СН 2-, заключенный в скобки с индексом n, соответствует пропандиилу. Когда в соединениях формулы (I) или любой подгруппе соединений формулы (I) n равно 4, фрагмент -СН 2-, заключенный в скобки с индексом n, соответствует бутандиилу. Когда в соединениях формулы (I) или любой подгруппе соединений формулы (I) n равно 5, фрагмент -СН 2-, заключенный в скобки с индексом n, соответствует пентандиилу. Когда в соединениях формулы (I) или любой подгруппе соединений формулы (I) n равно 6, фрагмент -СН 2-, заключенный в скобки с индексом n, соответствует гександиилу. Особую подгруппу соединений формулы (I) составляют соединения, в которых n равно 4 или 5. Вариантами осуществления изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых(a) R1 представляет собой -OR7, в частности, где R7 представляет собой С 1-6 алкил, такой как метил,этил или трет-бутил (или изобутил), и наиболее предпочтительно где R7 представляет собой водород;(c) R1 представляет собой -NHS(=O)2R8, в частности, где R8 представляет собой С 3-7 циклоалкил, замещенный С 1-6 алкилом, предпочтительно, где R8 представляет собой циклопропил, циклобутил, циклопентил или циклогексил, каждый из которых является замещенным С 1-4 алкилом, то есть метилом, этилом, пропилом, изопропилом, бутилом, трет-бутилом или изобутилом. Другими вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), где R1 представляет собой -NHS(=O)2R8, в частности,где R8 представляет собой циклопропил, замещенный C1-4 алкилом, то есть метилом, этилом, пропилом или изопропилом. Дополнительными вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), где R1 представляет собой -NHS(=O)2R8, в частности, где R8 представляет собой 1-метилциклопропил. Дополнительными вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых(b) R2 представляет собой C1-6 алкил, предпочтительно метил. Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых(a) X представляет собой N, С (где X присоединен через двойную связь) или СН (где X присоединен через одинарную связь) и R2 представляет собой водород;(b) X представляет собой С (где X присоединен через двойную связь) и R2 представляет собой С 1-6 алкил, предпочтительно метил. Дополнительными вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых(c) R3 представляет собой С 1-6 алкоксиС 1-6 алкил или С 3-7 циклоалкил. Предпочтительными вариантами осуществления изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых R3 представляет собой водород или C1-6 алкил, более предпочтительно водород или метил. Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 представляет собой арил или Het, каждый из которых независимо необязательно замещен любым из заместителей Het или арила, упомянутых в определениях соединений формулы (I) или любой из подгрупп соединений формулы (I); или конкретно указанный арил или Het, каждый независимо, является необязательно замещенным С 1-6 алкилом, галогеном, амино, моноили ди-C1-6 алкиламино, пирролидинилом, пиперидинилом, морфолинилом, пиперазинилом, 4-С 1-6 алкилпиперазинилом; или в которых морфолинильная и пиперидинильная группы могут быть необязательно замещены одним или двумя С 1-6 алкильными радикалами.- 10015131 Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 представляет собой радикал где, когда это возможно, атом азота может нести на себе R4a заместитель или связь с остатком молекулы; каждый R4a в любом из R4 заместителей может выбираться из заместителей, перечисленных в качестве возможных заместителей для Het, как указано в определениях соединений формулы (I) или любой из подгрупп соединений формулы (I); точнее, каждый R4a может представлять собой водород, атом галогена, С 1-6 алкил, амино, или моноили ди-С 1-6 алкиламино, пирролидинил, пиперидинил, морфолинил, пиперазинил, 4-С 1-6 алкилпиперазинил; где морфолинилльная и пиперидинильная группы могут быть необязательно замещены одним или двумя С 1-6 алкильными радикалами; точнее, каждый R4a независимо представляет собой водород, атом галогена, С 1-6 алкил, амино, моноили ди-С 1-6 алкиламино; где R4a замещен по атому азота и предпочтительно представляет собой заместитель, содержащий атомы углерода, который присоединен к атому азота через атом углерода или один из его атомом углерода; и где в данном случае R4a предпочтительно представляет собой С 1-6 алкил. Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), где R4 представляет собой фенил или пиридил (в частности, 4 пиридил), каждый из которых может быть замещен 1, 2 или 3 заместителями, выбранными из заместителей, перечисленных для арила в определениях соединений формулы (I) или любой из подгрупп соединений формулы (I). В частности, указанный фенил или пиридил является замещенным 1-3 (или 1-2 или одним) заместителями, которые выбраны из галогена, С 1-6 алкила или C1-6 алкокси. Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых R5 представляет собой атом галогена или C1-6 алкил,предпочтительно метил, этил, изопропил, трет-бутил, фтор, хлор или бром, включая полигалогенС 1-6 алкил. Вариантами осуществления настоящего изобретения являются соединения формулы (I) или любой из подгрупп соединений формулы (I), в которых R6 представляет собой C1-6 алкокси или диС 1-6 алкиламино; предпочтительно R6 представляет собой метокси или диметиламино; более предпочтительно R6 представляет собой метокси. Соединения формулы (I) состоят из трех структурообразующих блоков Р 1, Р 2 и Р 3. Структурообразующий блок Р 1 дополнительно содержит хвостовую часть Р 1'. Карбонильная группа, помеченная звездочкой в соединении (I-c), представленном ниже, может составлять часть структурообразующего блока Р 2 или структурообразующего блока Р 3. По химическим соображениям структурообразующий блок Р 2 соединений формулы (I), в которых X представляет собой С, содержит карбонильную группу, присоединенную в положении 1'. Соединение структурообразующих блоков Р 1 с Р 2, Р 2 с Р 3, Р 2 с Р' (когда R1 представляет собой-NH-SO2R8 или -OR7) включает образование амидной связи. Соединение блоков Р 1 и Р 3 включает образование двойной связи. Соединение структурообразующих блоков P1, P2 и Р 3 с получением соединений(I-i) или (I-j) может выполняться в любой последовательности. Одна из стадий включает циклизацию,посредством которой образуется макроцикл. Представленные ниже соединения (I-i) представляют собой соединения формулы (I), в которых атомы углерода С 7 и С 8 соединены двойной связью, а соединения (I-j) представляют собой соединения формулы (I), в которых атомы углерода С 7 и С 8 соединены одинарной связью. Соединения формулы (I-j) могут быть получены из соответствующих соединений формулы (I-I) восстановлением двойной связи в макроцикле. Следует отметить, что в соединениях формулы (I-c) образование амидной связи между блоками Р 2 и Р 3 может проходить по двум положениям карбамоильного фрагмента. В образовании первой амидной связи принимает участие атом азота пироллидинового цикла и соседний карбонил (помеченный звездочкой). В образовании альтернативной амидной связи протекает с участием помеченного звездочкой карбонила и -NHR3 группы. Осуществимо образование обеих амидных связей между стандартными блоками Р 2 и Р 3. Подразумевается, что методики синтеза, описанные далее, в равной степени применимы для рацематов, стереохимически чистых промежуточных или конечных продуктов и для любых стереоизомерных смесей. Рацематы или стереохимические смеси могут разделяться на стереоизомерные формы на любой стадии методик синтеза. В одном варианте осуществления изобретения промежуточные и конечные продукты имеют стерехимию, точно определенную выше в описаниях соединений формулы (Ia) и (Ib). Для простоты структурного изображения соединений формулы (I) или промежуточных продуктов группа представлена как R9, а пунктирная линия представляет собой связь, присоединяющую указанную группу,представленную как R9, к остальной части молекулы. В одном варианте осуществления изобретения соединения (I-i) получают посредством образования сначала амидных связей и последующим образованием мостиковой двойной связи между Р 3 и Р 1 с одновременной циклизацией и получением макроцикла. В предпочтительном варианте осуществления изобретения соединения, в которых двойная связь между С 7 и С 8 представляет собой двойную связь и которые представляют собой соединения формулы (Ii), как определено выше, могут быть получены в соответствии со следующей схемой реакции: Образование макроцикла может проводиться через реакцию олефинового метатезиса в присутствии подходящего металлического катализатора, такого как, например, катализатора на основе Ru, описанного в публикациях Miller, S.J., Blackwell, H.E., Grubbs, R.H. J. Am. Chem. Soc. 118, (1996), 9606-9614; Kingsbury, J.S., Harrity, J.P.A., Bonitatebus, P.J., Hoveyda, A.H., J. Am. Chem. Soc. 121, (1999), 791-799; и Huanget al., J. Am. Chem. Soc. 121, (1999), 2674-2678; например катализатора Ховейды-Краббса. Могут использоваться стабильные на воздухе катализаторы на основе рутения, такие как хлорид бис(трициклогексилфосфин)-3-фенил-1 Н-инден-1-илиденрутения (Neolyst M1) или дихлорид бис(трициклогексилфосфин)(фенилтиометилен)рутения (IV). Другими катализаторами, которые могут применяться, являются катализаторы Граббса первого и второго поколения, т.е. бензилиден- 12015131 бис(трициклогексилфосфин)дихлоррутений и (1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден) дихлор(фенилметилен)(трициклогексилфосфин)рутений соответственно. Особый интерес представляют катализаторы Ховейды-Граббса первого и второго поколения, которыми являются дихлор(оизопропоксифенилметилен)(трициклогексилфосфин)рутений (II) и 1,3-бис(2,4,6-триметилфенил)-2 имидазолидинилиден)дихлор-(о-изопропоксифенилметилен)рутений соответственно. Для указанной реакции также могут использоваться и другие катализаторы, содержащие другие переходные металлы, такие как Мо. Реакция метатезиса может проводиться в подходящем растворителе, таком как, например, простые эфиры, например ТГФ, диоксан; галогенированные углеводороды, например дихлорметан, CHCl3, 1,2 дихлорэтан и т.п., углеводороды, например толуол. В предпочтительном варианте осуществления изобретения реакция метатезиса проводится в толуоле. Данные реакции проводятся при повышенных температурах в атмосфере азота. Соединения формулы (I), в которых связь между С 7 и С 8 в макроцикле представляет собой одинарную связь, т.е. соединения формулы (I-j) могут быть получены из соединений формулы (I-i) восстановлением двойной связи С 7-С 8 в соединениях формулы (I-i). Такое восстановление может проводиться посредством каталитического гидрирования водородом в присутствии катализатора на основе благородного металла, такого как, например, Pt, Pd, Ph, Ru или никель Ренея. Интерес представляют катализаторыPh на алюминии. Реакция гидрирования предпочтительно проводится в растворителе, таком как, например, спирт, в частности метанол, этанол, или простой эфир, такой как ТГФ, или их смеси. К указанным растворителям или смесям растворителей может также добавляться вода.R1 группа может присоединяться к структурообразующему блоку Р 1 на любой стадии синтеза, т.е. до или после циклизации либо до или после циклизации и восстановления, как описано выше. Соединения формулы (I), в которых R1 представляет собой -NHSO2R8, т.е. соединения, представленные формулой(I-k-1), могут быть получены присоединением группы R1 к Р 1 посредством образования амидной связи между обоими фрагментами. Аналогично, соединения формулы (I), в которых R1 представляет собой-OR7, т.е. соединения (I-k-2), могут быть получены присоединением группы R1 к Р 1 с образованием сложноэфирной связи. В одном варианте осуществления изобретения группы -OR5 вводятся на последней стадии синтеза соединений (I), как показано на приведенных далее схемах реакции, где G представляет собой группу Промежуточное соединение (2 а) может соединяться с амином (2b) посредством реакции образования амида, такой как любая реакция образования амидной связи, методики которых описаны ниже. В частности, (2 а) может подвергаться обработке конденсирующим реагентом, например N,N'-карбонилдиимидазол (N,N'-карбонилдиимидазол - CDI), EEDQ, IIDQ, EDCI или гексафторфосфатом бензотриазол-1 илокси-трис-пирролидинофосфония (коммерчески доступен как РуВОР), в растворителе, таком как простой эфир, например ТГФ, или галогенированный углеводород, например дихлорметан, хлороформ,дихлорэтан, и подвергается взаимодействию с желательным сульфонамидом (2b) предпочтительно после взаимодействия (2 а) с конденсирующим реагентом. Реакции (2 а) с (2b) предпочтительно проводятся в присутствии основания, например триалкиламина, такого как триэтиламин или диизопропилэтиламин,или 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU). Промежуточное соединение (2 а) может также подвергаться превращению в активированную форму, например в активированную форму общей формулы G-CO-Z,где Z представляет собой атом галогена, или остаток активного сложного эфира, например Z, представляет собой арилоксигруппу, такую как фенокси, п-нитрофенокси, пентафторфенокси, трихлорфенокси,пентахлорфенокси и т.п.; или Z может представлять собой остаток смешанного ангидрида. В одном ва- 13015131 рианте осуществления изобретения G-CO-Z представляет собой хлорангидрид (G-CO-Cl) или смешанный ангидрид кислоты (G-CO-O-CO-R или G-CO-O-CO-OR, где в последней формуле R представляет собой, например, С 1-4 алкил, такой как метил, этил, пропил, изопропил, бутил, трет-бутил, изобутил, или бензил). Активированная форма G-CO-Z подвергается взаимодействию с сульфонамидом (2b). Активация группы карбоновой кислоты в (2 а), как описано в представленных выше реакциях, может приводить к реакции внутренней циклизации с получением промежуточного азалактона формулы где X, R2, R3, R9, n принимают значения, описанные выше, и где стереогенные центры могут иметь стереохимическую конфигурацию, описанную выше, например конфигурацию (Ia) или (Ib). Промежуточные соединения (2 а-1) могут выделяться из реакционной смеси с использованием стандартной методологии, и выделенное промежуточное соединение (2 а-1) затем подвергается взаимодействию с (2b), или реакционная смесь, содержащая (2 а-1), может подвергаться дальнейшему взаимодействию с (2b) без выделения (2 а-1). В одном варианте осуществления настоящего изобретения, где взаимодействие с конденсирующим агентом проводится в растворителе, не смешивающимся с водой, реационная смесь, содержащая (2 а-1), может промываться водой или слабо подщелоченной водой для удаления всех растворимых в воде побочных продуктов. Полученный таким образом промытый раствор может затем подвергаться взаимодействию с (2b) без дополнительных стадий очистки. С другой стороны, выделение промежуточных продуктов (2 а-1) может обеспечить некоторые преимущества в том, что выделенный продукт после необязательной дополнительной очистки может подвергаться взаимодействию с (2b) с получением меньшего количества побочных продуктов и более легкой обработки реакционной смеси. Промежуточный продукт (2 а) может подвергаться связыванию со спиртом (2 с) посредством реакции образования сложного эфира (реакции этерификации). Например, (2 а) и (2 с) подвергаются взаимодействию с удалением воды физическим способом, например азеотропной отгонкой воды, или химическим способом посредством применения дегидратирующего агента. Промежуточное соединение (2 а) может также превращаться в активированную форму G-CO-Z, такую как упомянутые выше активированные формы, и последовательно подвергаться взаимодействию со спиртом (2 с). Реакции этерификации предпочтительно проводятся в присутствии основания, такого как карбонат или гидрокарбонат щелочного металла, например гидрокарбонат натрия или калия, или третичного амина, такого как амины, перечисленные при описании реакций образования амидов, в частности триалкиламина, например триэтиламина. Растворители, которые могут применяться в реациях этерификации, включают простые эфиры,такие как ТГФ; галогенированные углеводороды, такие как дихлорметан, CH2Cl2; углеводороды, такие как толуол; полярные апротонные растворители, такие как ДМФА, ДМСО, ДМА; и т.п. растворители. Соединения формулы (I), в которых R3 представляет собой водород, то есть соединения (I-1), могут быть получены удалением защитной группы PG из соответствующего промежуточного продукта (3 а),содержащего группу, защищающую атом азота, как показано на приведенной далее схеме реакции. Защитная группа PG, в частности, представляет собой любую группу из групп, применяющихся для защиты атома азота, которые описаны далее, и может удаляться с использованием методик, также описанных далее. Исходные соединения (3 а) в описанной выше реакции могут быть получены в соответствии с методиками получения соединений формулы (I), но при использовании промежуточных соединений, в которых группа R3 представляет собой PG.- 14015131 Соединения формулы (I) также могут быть получены взаимодействием промежуточного соединения (4 а) с промежуточным соединением (4b), как представлено на приведенной далее схеме реакции, где различные радикалы принимают значения, описанные вышеY в (4b) представляет собой гидроксильную или удаляемую группу LG, такую как галогенид, например бромид или хлорид, или арилсульфонильную группу, например мезилат, трифторметансульфонат или тозилат и т.п. В одном варианте осуществления изобретения взаимодействие (4 а) с (4b) представляет собой реакцию О-арилирования, и Y представляет собой удаляемую группу. Данная реакция может проводиться в соответствии с методиками, описанными в публикации Е.М. Smith et al., J. Med. Chem. (1988), 31, 875885. В частности, данная реакция проводится в присутствии основания, предпочтительно сильного основания, в инертном по отношению к реакции растворителе, например одном из растворителей, рекомендованных для реакции образования амидной связи. В варианте осуществления изобретения, заслуживающем особого внимания, исходное соединение(4 а) подвергается взаимодействию с (4b) в присутствии основания, которое является достаточно сильным для того, чтобы отщепить водород из гидроксильной группы, например, гидрида щелочного металла,такого как LiH или гидрид натрия, или алкоксида щелочного металла, такого как метоксид или этоксид натрия или калия, трет-бутоксид калия, в инертном по отношению к реакции растворителе, таком как полярный апротонный растворитель, например ДМА, ДМФ и т.п. Образующийся алкоголят подвергается взаимодействию с арилирующим агентом (4b), где Y представляет собой подходящую удаляемую группу, как указано выше. Превращение (4 а) в (I) с использованием реакции О-арилирования данного типа не изменяет стереохимической конфигурации при атоме углерода, несущем гидроксильную группу. Альтернативно, взаимодействие (4 а) с (4b) также может проводиться посредством реакции Мицунобу (Mitsunobu, 1981, Synthesis, January, 1-28; Rano et al., Tetrahedron Lett., 1995, 36, 22, 3779-3792;Krchnak et al., Tetrahedron Lett., 1995, 36, 5, 6193-6196; Richter et al., Tetrahedron Lett., 1994, 35, 27, 47054706). Данная реакция включает обработку промежуточного соединения (4 а) с помощью (4b), где Y представляет собой гидроксильную группу, в присутствии трифенилфосфина и активирующего агента,такого как диалкилазокарбоксилат, например диэтилазодикарбоксилат (diethyl azodicarboxylate DEAD),диизопропилазодикарбоксилат (diisopropyl azodicarboxylate - DIAD) и т.п. Реакция Мицунобу изменяет стереохимическую конфигурацию при атоме углерода, несущем гидроксильную группу. В соответствии с другой альтернативой для получения соединений формулы (I) сначала проводится реакция получения амидной связи между структурообразующими блоками Р 2 и Р 1 и последовательно присоединением структурообразующего блока Р 3 к фрагменту Р 1 в Р 1-Р 2 и образованием карбаматной или сложноэфирной связи между Р 3 и фрагментом Р 2 в Р 2-Р 1-Р 3 с одновременным замыканием цикла. В соответствии с еще одной альтернативной методикой синтеза проводится реакция образования амидной связи между стандартными блоками Р 2 и Р 3 с последующим присоединением стандартного блока Р 1 к фрагменту Р 3 в Р 3-Р 2 и образованием последней амидной связи между Р 1 и Р 2 в Р 1-Р 3-Р 2 с одновременным замыканием цикла. Структурообразующие блоки Р 1 и Р 3 могут соединяться с образованием Р 1-Р 3 последовательности. Если это необходимо, двойная связь, соединяющая Р 1 и Р 3, может подвергаться восстановлению. Полученная таким образом последовательность Р 1-Р 3, восстановленная или невосстановленная, может присоединяться к структурообразующему блоку Р 2, и полученная таким образом последовательность Р 1-Р 3 Р 2 затем подвергается циклизации через образование амидной связи. Структурообразующие блоки Р 1 и Р 3 в любом из описанных выше подходов могут соединяться посредством образования двойной связи, например, с помощью реакции олефинового метатезиса, описанной далее, или реакции Виттига. Если нужно, образованная таким образом двойная связь может подвергаться восстановлению, аналогично превращению (I-i) в (I-j), описанному выше. Двойная связь также может восстанавливаться на более поздней стадии, т.е. после присоединения третьего стандартного блока или после образования макроцикла. Структурообразующие блоки Р 2 и Р 1 соединяются посредством образования амидной связи, и Р 3 и Р 2 соединяются посредством образования фрагмента карбамата или сложного эфира. Хвостовой фрагмент Р 1' может присоединяться к структурообразующему блоку Р 1 на любой стадии- 15015131 синтеза соединений формулы (I), например, до или после соединения структурообразующих блоков Р 2 и Р 1; до или после присоединения стандартного блока Р 3 к Р 1; либо до или после замыкания цикла. Сначала могут быть получены отдельные структурообразующие блоки, и затем полученные блоки могут соединяться вместе, или, альтернативно, предшественники структурообразующих блоков могут соединяться вместе и модифицироваться на более поздней стадии синтеза с получением молекулы желательного строения. Функциональные группы, находящиеся в каждом из структурообразующих блоков, могут защищаться для предотвращения побочных реакций. Образование амидных связей может осуществляться с использованием стандартных методик, которые применялись, например, для соединения аминокислот в синтезе пептидов. Последний включает в себя связывание карбоксильной группы одного реагента с аминогруппой другого реагента с образованием мостиковой амидной связи. Образование амидной связи может проводиться взаимодействием исходных веществ в присутствии конденсирующего агента или посредством превращения карбоксильной функциональной группы в активную форму, такую как активированный сложный эфир, смешанный ангидрид или хлорангидрид или бромангидрид карбоновой кислоты. Общее описание таких реакций конденсации и реагентов, используемых в них, приводится в стандартных учебниках по химии пептидов,таких как, например, М. Bodanzsky, "Peptide Chemistry", 2nd rev. ed., Springer-Verlag, Berlin, Germany,(1993). Примеры реакций конденсации с образованием амидной связи включают азидный метод, метод с использованием смешанного ангидрида угольной и карбоновой кислоты (изобутилхлорформиата), метод с использованием карбодиимида (дициклогексилкарбодиимида, диизопропилкарбодиимида или растворимого в воде карбодиимида, такого как N-этил-N'-[(3-диметиламино)пропил]карбодиимида), метод с использованием активированного сложного эфира (например, п-нитрофенилового, п-хлорфенилового,трихлорфенилового, пентахлорфенилового, пентафторфенилового, N-гидроксисукцинимидо- и т.п. сложных эфиров), метод с использованием K-реагента Вудварда, метод с использованием 1,1 карбонилдиимидазола (CDI или N,N'-карбонилдиимидазола), методы с использованием фосфорсодержащих реагентов или окислительно-восстановительные методы. Эффективность некоторых из этих методов может быть повышена добавлением подходящих катализаторов, например, в карбодиимидном способе добавлением 1-гидроксибензотриазола, DBU (1,8-диазабицикло[5.4.0]ундец-7-ен) или 4-DMAP. Дополнительными конденсирующими агентами являются гексафторфосфат (бензотриазол-1 илокси)трис-(диметиламино)фосфония - сам по себе или в присутствии 1-гидроксибензотриазола или 4DMAP; или тетрафторборат 2-(1 Н-бензотриазол-1-ил)-N,N,N',N'-тетраметилурония или гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N'N'-тетраметилурония. Такие реакции конденсации могут проводиться в растворе (в жидкой фазе) или на твердой фазе. Предпочтительно образование амидной связи проводится с применением N-этилоксикарбонил-2 этилокси-1,2-дигидрохинолинаN-изобутилоксикарбонил-2-изобутилокси-1,2 дигидрохинолина (IIDQ). В отличие от классической методики с применением ангидрида при применении EEDQ и IIDQ не требуются ни основание, ни низкие температуры реакции. Обычно методика синтеза включает в себя взаимодействие эквимолярных количеств карбоксильного и аминного компонентов в органическом растворителе (может применяться большой перечень растворителей). Затем добавляется избыток EEDO или IIDQ и смесь перемешивается при комнатной температуре. Реакции конденсации предпочтительно проводятся в инертном растворителе, таком как галогенированные углеводороды, например дихлорметан, хлороформ, поляроные апротонные растворители, такие как ацетонитрил, диметилформамид, диметилацетамид, ДМСО, НМРТ, простые эфиры, такие как тетрагидрофуран (ТГФ). Во многих примерах реакции конденсации проводились в присутствии подходящего основания, такого как третичный амин, например триэтиламин, диизопропилэтиламин (DIPEA), N-метилморфолин, Nметилпирролидин, 4-DMAP или 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU). Температура реакции может находиться в интервале от 0 до 50 С и время реакции может находиться в интервале от 15 мин до 24 ч. Функциональные группы в структурообразующих блоках, соединенных вместе, могут защищаться для предупреждения образования нежелательных связей. Подходящие защитные группы, которые могут применяться, приведены, например, в изданиях Greene, "Protective Groups in Organic Chemystry", JohnYork (1987). Карбоксильные группы могут защищаться посредством образования группы сложного эфира, которая может расщепляться с получением карбоновой кислоты. Защитные группы, которые могут использоваться, включают: 1) сложные алкиловые эфиры, такие как метиловый, триметилсилиловый и третбутиловый; 2) сложные арилалкиловые эфиры, такие как бензиловый и замещенный бензиловый; или 3) сложные эфиры, которые могут расщепляться под действием мягкого основания или мягких восстановителей, таких как сложные трихлорэтиловый и фенациловый эфиры. Аминогруппы могут защищаться различными N-защитными группами, такими как: 1) ацильные группы, например формил, трифторацетил, фталил и п-толуолсульфонил;- 16015131 2) ароматические карбаматные группы, такие как бензилоксикарбонил (Cbz или Z) и замещенные бензилоксикарбонилы, и 9-флуоренилметилоксикарбонил (Fmoc); 3) алифатические карбаматные группы, например трет-бутилоксикарбонил (Boc), этоксикарбонил,диизопропилметоксикарбонил и аллилоксикарбонил; 4) циклические алкилкарбаматные группы, например циклопентилоксикарбонил и адамантилоксикарбонил; 5) алкильные группы, например трифенилметил, бензил или замещенный бензил, например 4 метоксибензил; 6) триалкилсилил, например триметилсилил или трет-бутилдиметилсилил; и 7) тиолсодержащие группы, например фенилтиолкарбонил и дитиасукциноил. Защитными группами аминогруппы, представляющими особый интерес, являются Boc и Fmoc. Предпочтительно защитная группа аминогруппы отщепляется перед следующей стадией конденсации. Удаление N-защитных групп может проводиться в соответствии с известными в данной области техники методиками. Когда используется Вос-группа, такими способами удаления являются обработка трифторуксусной кислотой, чистой или в дихлорметане, или HCl в диоксане или в этилацетате. Образующаяся аммониевая соль затем подвергается нейтрализации либо перед конденсацией, либо непосредственно с помощью основных растворов, таких как водные буферы, или третичные амины в дихлорметане, ацетонитриле или диметилформамиде. Когда используется группа Fmoc, такими реагентами являются пиперидин или замещенный пиперидин в диметилформамиде, но может использоваться любой вторичный амин. Удаление защиты проводится при температуре в интервале от 0 С до комнатной температуры,обычно приблизительно 15-25 С или 20-22 С. Другие функциональные группы, которые могут затрагиваться в реакциях конденсации структурообразующих блоков, также могут защищаться. Например, гидроксильные группы могут защищаться с образованием незамещенных или замещенных простых бензиловых эфиров, например 4 метоксибензилового эфира, сложного незамещенного или замещенного бензоилового эфира, например 4 нитробензоилового эфира, или введением триалкилсилильных групп (например, триметилсилильной или трет-бутилдиметилсилильной). Дополнительные аминогруппы также могут защищаться защитными группами, которые могут подвергаться селективному расщеплению. Например, когда в качестве -аминозащитной группы используется Boc, подходящими защитными группами боковых цепей являются следующие группы: птолуолсульфонильные (тозильные) фрагменты могут применяться для защиты дополнительных аминогрупп; простые бензиловые (Bn) эфиры могут применяться для защиты гидроксильных групп; и сложные бензиловые эфиры могут использоваться для защиты дополнительных карбоксильных групп. Или, когда для защиты -аминогрупп выбрана Fmoc, приемлемыми обычно являются производные трет-бутильных групп. Например, Boc может использоваться для дополнительных аминогрупп; простые трет-бутиловые эфиры для гидроксильных групп; и сложные трет-бутиловые эфиры для дополнительных карбоксильных групп. Любая из защитных групп может удаляться на любой стадии методики синтеза, но предпочтительно защитные группы любой из функциональностей, не задействованных в реакционных стадиях, удаляются после завершения образования макроцикла. Удаление защитных групп может осуществляться любым способом, который определяется выбором защитных групп и которые хорошо известны специалисту данной области техники. Промежуточные продукты формулы (1 а), где X представляет собой N, то есть промежуточные продукты, представленные формулой (1 а-1), могут быть получены исходя из промежуточных соединений(5 а), которые подвергаются взаимодействию с алкенамином (5b) в присутствии карбонилирующего агента, как показано на представленной далее схеме реакции Карбонилирующие (СО) агенты включают фосген или производные фосгена, такие как карбонилдиимидазол (CDI) и т.п. В одном варианте осуществления изобретения (5 а) подвергается взаимодействию с реагентом введения СО группы в присутствии подходящего основания и растворителя, которые- 17015131 могут представлять собой основание и растворители, используемые в реакциях образования амидной связи, как описано выше. В варианте осуществления изобретения, представляющем особый интерес, основание представляет собой гидрокарбонат, например NaHCO3, или третичный амин, такой как триэтиламин и т.п., и растворитель представляет собой простой эфир или галогенированный углеводород, например ТГФ, CH2Cl2, CHCl3 и т.п. После этого к полученным таким образом промежуточным соединениям (1 а-1) добавляется амин (5b), как показано на представленной выше схеме. Альтернативный способ, в котором используются аналогичные условия реакций, включает сначала взаимодействие реагента введения СО группы с алкенамином (5b) и затем взаимодействие полученного таким образом промежуточного продукта с (5 а). Альтернативно, промежуточные соединения (1 а-1) могут быть получены следующим образом:PG1 является О-защитной группой, которая может представлять собой любую из групп, указанных выше, и в частности представляет собой бензоильную или замещенную бензоильную группу, такую как 4-нитробензоил. В последнем случае данная группа может удаляться взаимодействием с гидроксидом щелочного металла (LiOH, NaOH, KOH), в особенности, когда PG1 представляет собой 4-нитробензоил, с помощью LiOH в водной среде, включающей в себя воду и растворимый в воде органический растворитель, такой как алканол (метанол, этанол) и ТГФ. Промежуточные соединения (6 а) подвергаются взаимодействию с (5b) в присутствии карбонилирующего агента, аналогичного описанным выше соединениям, и данное взаимодействие приводит к получению промежуточных соединения (6 с). Из полученных соединений удаляются защитные группы, в частности, с использованием условий реакций, описанных выше. Полученный спирт (6d) подвергается взаимодействию с промежуточными продуктами (4b), как определено выше при описании взаимодействия (4 а) с (4b), и указанное взаимодействие приводит к получению промежуточных продуктов (1 а-1). Промежуточные соединения формулы (1 а), в которых X представляет собой С, то есть соединения,представленные формулой (1 а-2), могут быть получены с помощью реакции образования амида, исходя из промежуточных соединений (7 а), которые подвергаются взаимодействию с амином (5b), как показано на представленной далее схеме реакции, с использованием условий реакций получения амидов, которые описаны выше. Альтернативно, промежуточные соединения (1 а-1) могут быть получены следующим образом:PG1 является О-защитной группой, как описано выше. Могут использоваться условия реакций, описанные выше: образование амида, как описано выше, удаление PG1, как описано при определении защитных групп, и введение R9 согласно реакциям (4 а) с реагентами (4b). Промежуточные продукты формулы (2 а) могут быть получены циклизацией открытого амида (9 а) с получением макроциклического сложного эфира (9b), который, в свою очередь, подвергается превращению в (2 а), согласно следующей схеме:PG2 является защитной группой корбоксильной группы, например одной из защитных групп карбонильной группы, перечисленных выше, в частности группой сложного С 1-4 алкилового или бензилового эфира, например метилового, этилового или трет-бутилового эфира. Реакция превращения (9 а) в (9b) представляет собой реакцию метатезиса и проводится, как описано выше. Группа PG2 удаляется в соответствии с методиками, также описанными выше. Когда PG1 представляет собой группу сложного C1-4 алкилового эфира, она удаляется щелочным гидролизом, например добавлением NaOH или предпочтительно LiOH, в водном растворителе, например в смеси С 1-4 алканол/вода. Бензильная группа может удаляться посредством каталитического гидрирования. В альтернативном синтезе промежуточные продукты (2 а) могут быть получены следующим образом: Группа PG1 выбирается таким образом, что она селективно расщепляется с получением группы PG2.PG может представлять собой, например, сложный метиловый или этиловый эфир, который может удаляться обработкой гидроксидом щелочного металла в водной среде, когда PG1 представляет собой, например, трет-бутил или бензил. PG2 может представлять собой сложные трет-бутиловые эфиры, которые могут удаляться в слабых кислотных условиях, или PG1 может представлять собой сложные бензиловые эфиры, которые могут удаляться с помощью сильной кислоты или посредством каталитического гидрирования, в двух последних случаях PG1 представляет собой, например, сложный эфир бензойной кислоты, такой как эфир 4-нитробензойной кислоты. Сначала промежуточные соединения (10 а) подвергаются циклизации с получением макроциклических сложных эфиров (10b), из последних удаляется защитная группа PG1 с получением (10 с), которые подвергаются взаимодействию с промежуточными соединениями (4b) с последующим удалением PG2(защитной группы карбоксильной группы). Циклизация, удаление защитных групп PG1 и PG2 и связывание с (4b) проводятся в условиях, описанных выше. Группы R1 могут вводиться на любой стадии синтеза, то есть на последней стадии, как описано выше, или на более ранней стадии до образования макроцикла. На представленной ниже схеме группыR1 показан способ введения групп R1, которые представляют собой -NH-SO2R8 или -OR7 (которые точно определены выше) 2 На представленной выше схеме PG2 принимает значения, определенные выше, и L1 представляет собой группу Р 3- 20015131 представлять собой азот-защитную группу (PG, как определено выше), когда X представляет собой С, L1 также может представлять собой группу COOPG2a, где группа PG2a представляет собой защитную группу карбоксильной группы, аналогичную PG2, но где группа PG2a селективно расщепляется с получением группы PG2. В одном варианте осуществления группа PG2a представляет собой трет-бутил, и PG2 представляет собой метил или этил. Промежуточные соединения (11 с) и (11d), где L1 представляет собой группу (b), соответствуют промежуточным соединениям (1 а) и могут подвергаться дальнейшим превращениям, как описано выше. Конденсация структурообразующих блоков Р 1 и Р 2. Структурообразующие блоки Р 1 и Р 2 конденсируют с использованием реакции получения амида в соответствии с методиками, описанными выше. Структурообразующий блок Р 1 может содержать защитную группу карбоксильной группы PG2 (как в (12b, или он может быть присоединен к Р 1' группе (как в(12 с. L2 представляет собой N-защитную группу (PG) или группу (b), которая подробно описана выше.L3 представляет собой гидроксильную группу, -OPG1 или группу -O-R9, которые подробно описаны выше. Когда в любой из приведенных далее схем реакций L3 представляет гидроксильную группу, перед каждой реакционной стадией она может защищаться с образованием группы -OPG1 и, если это желательно, последующим удалением защиты с получением свободной гидроксильной функциональной группы. Аналогично, как описано выше, гидроксильная функция может превращаться в группу -O-R9. В методике представленной выше схемы циклопропильная аминокислота (12b) или (12 с) конденсируется с кислотной функциональной группой структурообразующего блока Р 2 (12 а) с образованием амидного мостика с соответствии с методиками, описанными выше. Таким образом получают промежуточные продукты (12d) или (12 е). Когда в указанных промежуточных продуктах L2 представляет собой группу (b), образующиеся продукты представляют собой последовательности Р 3-Р 2-Р 1, которые содержат некоторые из промежуточных продуктов (11 с) или (11d), полученные в соответствии с представленной ранее схемой реакции. Удаление группы, защищающей кислотную группу в (12d) с использованием условий, подходящих для используемой защитной группы, с последующим связыванием с амином H2NSO2R8 (2b) или с HOR7 (2 с), как описано выше, снова приводит к получению промежуточных продуктов(12 е), в которых -COR1 представляет собой амидные или сложноэфирные группы. Когда L2 представляет собой N-защитную группу, он может удаляться с получением промежуточных продуктов (5 а) или (6 а). В одном варианте осуществления изобретения PG в данной реакции представляет собой ВОС группу, и PG2 представляет собой метил или этил. Когда дополнительная группа L3 представляет собой гидроксильную группу, исходное соединение (12 а) представляет собой Boc-L-гидроксипролин. В варианте осуществления изобретения, представляющем особый интерес, PG представляет собой ВОС, PG2 представляет собой метил или этил и L3 представляет собой -O-R8. В еще одном варианте осуществления изобретения L2 представляет собой группу (b), и указанные реакции включают присоединение Р 1 к Р 2-Р 3, что приводит к получению промежуточных продуктов (1 а-1) или (1 а), описанных выше. В еще одном варианте осуществления изобретения L2 представляет собой N-защитную группу PG, которая точно описана выше, и реакция связывания приводит к получению промежуточных продуктов (12d-l) или (12 е-1), из которых группа PG может удаляться с использованием условий реакции, описанных выше, с получением промежуточных продуктов (12-f) или (12-g) соответственно, которые включают промежуточные продукты (5 а) и (6 а), которые описаны выше В одном варианте осуществления изобретения группа L3 в представленных выше схемах представляет собой группу -O-PG1, которая может вводиться в исходное соединение (12 а), где L3 представляет собой гидроксильную группу. В данном случае PG1 выбирается таким образом, что она может селективно расщепляться, чтобы группа L2 представляла собой PG. Аналогично, структурообразующие блоки Р 2, в которых X представляет собой С и которые представляют собой циклопентан или производные циклопентена, могут присоединяться к структурообразующим блокам Р 1, как показано на приведенной далее схеме, где R1, R2, L3 принимают значения, определенные выше, и PG2 и PG2a представляют собой защитные группы карбоксильной группы. PG2a обычно выбирается таким образом, чтобы она могла селективно расщепляться с образованием группы PG2. Удаление PG2a группы в (13 с) приводит к получению промежуточных продуктов (7 а) или (8 а), которые могут подвергаться взаимодействию с (5b), как описано выше. В представляющем особый интерес варианте осуществления изобретения, где X представляет собой С, R2 представляет собой Н и где X и атом углерода, несущий R2, соединены одинарной связью (Р 2 представляет собой циклопентановый фрагмент), PG2a и L3 вместе образуют связь, и структурообразующий блок Р 2 представлен формулой Бициклическая кислота (14 а) подвергается взаимодействию с (12b) или (12 с) аналогично тому, как описано выше для (14b) и (14 с) соответственно, где лактоновый цикл раскрывается с получением промежуточных (14 с) и (14 е). Раскрытие лактоновых циклов может осуществляться с использованием методик гидролиза сложных эфиров, например с использованием условий реакции, описанных выше для щелочного удаления группы PG1 в (9b), в частности с использованием основных условий, таких как гидроксид щелочного металла, например NaOH, KOH, в особенности LiOH. Промежуточные продукты (14 с) и (14 е) могут подвергаться дальнейшему превращению, как описано ниже. Конденсация структурообразующих блоков Р 3 и Р 2. Для стандартных блоков Р 2, которые содержат пирролидиновый фрагмент, структурообразующие блоки Р 3 и Р 2 или Р 3 и Р 2-Р 1 соединяются с использованием реакции образования карбамата в соответствии с методиками, описанными выше для конденсации (5 а) с (5b). Общая методика присоединения Р 2 блоков, содержащих пирролидиновый фрагмент, показана на приведенной далее схеме реакций, где L3 принимает значения, определенные выше, и L4 представляет собой группу -O-PG2, группу В одном варианте осуществления изобретения, где L4 в (15 а) представляет собой группу -OPG2,-PG группа может удаляться и полученная кислота может соединяться с циклопропиламинокислотами(12 а) или (12b) с получением промежуточных продуктов (12d) или (12 е), в которых L2 представляет собой радикал (d) или (е). Общая методика соединения Р 3 блоков с Р 2 блоком или с Р 2-Р 1 блоком, где Р 2 представляет собой циклопентан или циклопентен, показана на приведенной далее схеме, где L3 и L4 принимают значения,определенные выше. 2 В варианте осуществления изобретения, представляющем особый интерес, L3 и L4 вместе могут образовывать лактоновый мостик, как в (14 а), и присоединение блока Р 3 к блоку Р 2 осуществляется следующим образом: Бициклический лактон (14 а) подвергается взаимодействию с (5b) в соответствии с реакцией образования амида с получением амида (16 с), в которой лактоновый мостик расщепляется с получением (16d). Условия реакций образования амида и расщепления лактона описаны выше или далее. Промежуточный продукт (16d), в свою очередь, может присоединяться к Р 1 группе, как описано выше. Реакции, представленные на приведенных выше схемах, проводятся в соответствии с методиками,описанными выше для взаимодействий (5 а), (7 а) или (8 а) с (5b) и, в частности, описанные выше взаимодействия, где L4 представляет собой группу (d) или (е), соответствуют взаимодействиям (5 а), (7 а) или(8 а) с (5b), как описано выше. Структурообразующие блоки Р 1, Р 1', Р 2 и Р 3, используемые для получения соединений формулы(I), могут быть получены исходя из известных в данной области промежуточных продуктов. Ряд таких методов синтеза описан далее более подробно. В частности, сначала могут быть получены отдельные структурообразующие блоки, которые затем могут соединяться вместе, или, альтернативно, предшественники стандартных блоков могут соединяться вместе и подвергаться модификации на более поздней стадии с получением молекулы желательного строения. Для предотвращения побочных реакций функциональности в каждом из стандартных блоков могут быть защищены. Синтез структурообразующих блоков Р 2. Структурообразующие блоки Р 2 содержат пирролидиновый, циклопентановый или циклопентеновый фрагмент, замещенный группой -O-R4. Структурообразующие блоки Р 2, содержащие пирролидиновый фрагмент, могут быть получены из коммерчески доступного гидроксипролина. Получение структурообразующих блоков Р 2, которые содержат циклопентановое кольцо, может осуществляться в соответствии с представленной ниже схемой. Бициклическая кислота (17b) может быть получена, например, из 3,4-бис(метоксикарбонил)циклопентанона (17 а), как описано в публикации Rosenquist et al., Acta Chem. Scand. 46 (1992) 1127-1129. Первая стадия данной методики включает восстановление кето-группы с помощью восстановителя, такого как борогидрид натрия, в растворителе, таком как метанол, с последующим гидролизом сложных эфиров и, наконец, замыканием цикла с получением бициклического лактона (17b) в соответствии с методиками получения лактонов, в частности с применением уксусного ангидрида в присутствии слабого основания,такого как пиридин. Функциональная группа карбоновой кислоты в (17b) затем может защищаться введением подходящей защитной группы карбоксила, такой как группа PG2, которая определена выше, с получением, таким образом, бициклического сложного эфира (17 с). В частности, группа PG2 является кислотно-лабильной, такой как трет-бутильная группа, и вводится, например, посредством обработки изобутеном в присутствии кислоты Льюиса или ди-трет-бутилдикарбонатом в присутствии основания,такого как третичный амин, например диметиламинопиридил или триэтиламин, в растворителе, таком- 24015131 как дихлорметан. Раскрытие лактона в (17 с) с использованием условий реакции, описанной выше, в частности гидроксида лития, приводит к получению кислоты (17d), которая может далее использоваться в реакциях конденсации со структурообразующими блоками Р 1. Свободная кислотная группа в (17d) также может быть защищена, предпочтительно защитной группой для кислоты PG2a, которая может селективно расщепляться с получением PG2, и гидроксильная функция может подвергаться превращению в группу -OPG1 или в группу -O-R9. Продуктами, полученными в результате удаления группы PG2, являются промежуточные продукты (17g) и (17i), которые соответствуют промежуточным продуктам (13 а) или (16 а), описанным выше. Промежуточные продукты со специфической стереохимией могут быть получены разделением промежуточных продуктов в описанной выше последовательности реакции. Например, (17b) может разделяться согласно известным в данной области техники методикам, например образованием солевой формы с оптически активным основанием или хиральной хроматографией, и полученные стереоизомеры могут подвергаться дальнейшим превращениям, как описано выше. Группы ОН и СООН в (17d) находятся в цис-положении. Транс-аналоги могут быть получены инверсией стереохимии на атоме углерода,несущем ОН функцию, с помощью специфических реагентов в реакциях введения OPG1 или O-R9, которые инвертируют стереохимию, например применением реакции Мицунобу. В одном варианте осуществления изобретения промежуточные продукты (17d) соединяются с блоками P1 (12b) или (12 с), и данные реакции сочетания соответствуют реакции присоединения (13 а) или(16 а) с такими же блоками Р 1 в этих же условиях. Последовательное введение -O-R9, как описано выше,и затем удаление защитной группы кислоты PG2 приводит к получению промежуточных продуктов (8 а 1), которые представляют собой подгруппу промежуточных продуктов (7 а) или часть промежуточных продуктов (16 а). Продукты реакции удаления PG2 могут далее подвергаться реакции конденсации со структурообразующим блоком Р 3. В одном варианте осуществления изобретения PG2 в (17d) представляет собой трет-бутил, который может удаляться в кислотных условиях, например, с помощью трифторуксусной кислоты Ненасыщенный структурообразующий блок Р 2, т.е. циклопентеновое кольцо, может быть получен,как показано на схеме, представленной ниже Реакция бромирования-элиминирования 3,4-бис(метоксикарбонил)циклопентанона (17 а) в соответствии с методикой, описанной в публикации Dolby et al., J. Org. Chem. 36 (1971) 1277-1285, с последующим восстановлением кето-функциональности таким восстановителем, как борогидрид натрия, приводит к получению циклопентенола (19 а). Селективный гидролиз сложного эфира с использованием, например,гидроксида лития в растворителе, таком как смесь диоксана и воды, приводит к получению гидроксизамещенного сложного моноэфирного циклопентенола (19b). Ненасыщенный структурообразующий блок Р 2, в котором R2 может быть отличным от атома водорода, может быть получен, как показано на схеме, представленной ниже. Окисление коммерчески доступного 3-метил-3-бутен-1-ола (20 а), в частности, с помощью окислителя, такого как хлорхромат пиридиния, приводит к получению (20b), который подвергается превращению в соответствующий сложный метиловый эфир, например, обработкой ацетилхлоридом в метаноле, и последующему бромированию бромом с получением сложного -бром эфира (20 с). Сложный эфир (20 е) предпочтительно представляет собой трет-бутиловый эфир, который может быть получен из соответствующей коммерчески доступной кислоты (20d), например, обработкой ди-трет-бутилдикарбонатом в присутствии основания, такого как диметиламинопиридин. Промежуточный (20 е) подвергается обработке основанием, таким как диизопропиламид лития, в растворителе, таком как тетрагидрофуран, и подвергается взаимодействию с (20 с) для получения сложного алкенилового диэфира (20f). Циклизация (20f) реакцией олефинового метатезиса, проводимая как описано выше, приводит к получению циклопентенового производного (20g). Стереоселективное эпоксидирование (20g) может проводиться с использованием метода асимметрического эпоксидирования Джакобсена для получения эпоксида (20h). И, наконец, реакция раскрытия эпоксида в основных условиях, например, добавлением основания, в частности DBN (1,5-диазабицикло-[4.5.0]нон-5-ена), приводит к получению спирта (20i). Двойная связь в промежуточном (20i) может необязательно подвергаться восстановлению, например, каталитическим гидрированием с использованием катализатора, такого как палладий на углероде, с получением соответствующего циклопентанового соединения. Группа сложного трет-бутилового эфира может удаляться с получением соответствующей группы кислоты, которая затем присоединяется к структурообразующему блоку Р 1. Группа -R9 может вводиться в пирролидиновое, циклопентановое или циклопентеновое кольца на любой удобной стадии синтеза соединений согласно настоящему изобретению. В одном варианте сначала в указанные циклы вводится группа -R9 и затем добавляются другие желательные структурообразующие блоки, т.е. Р 1 (необязательно с Р 1'-хвостом) и Р 3, с последующим образованием макроцикла. В другом варианте сначала соединяются структурообразующие блоки Р 2, не содержащие -O-R9 заместителя, с каждым из Р 1 и Р 3 и затем присоединяется -R9 группа до или после образования макроцикла. В последней методике фрагменты Р 2 содержат гидроксильную группу, которая может быть защищена с помощью защищающей гидроксильную группу группы PG1. Группа -R9 может вводиться в структурообразующие блоки Р 2 взаимодействием гидроксизамещенных (21 а) или (21b) с промежуточными (4b), как описано выше в синтезе (I) исходя из (4 а). Данные реакции представлены на схемах ниже, где L2 принимает значения, указанные выше, и L5 и L5a независимо представляют собой гидроксильную группу, группу -OPG2 или -OPG2a, защищающую карбоксильную группу, или L5 может также представлять собой группу Р 1, такую как группа (d) или (е), которые описаны выше, или L5a также может представлять собой группу Р 3, такую как группа (b), которая описана выше. Группы PG2 и PG2a представляют собой группы, описанные выше. Когда группы L5 и L5a представляют собой PG2 или PG2a, они могут подбираться таким образом, чтобы каждая группа была способна селективно расщепляться с получением другой. Например, одна из групп L5 и L5a может представлять собой метильную или этильную группу, а другая - бензильную или трет-бутиловую группу. В одном варианте осуществления изобретения в (21 а) L2 представляет собой PG и L5 представляет собой -OPG2, или в (21d) L5a представляет собой -OPG2 и L5 представляет собой -OPG2, и группы PG2 удаляются, как описано выше. Альтернативно, при обработке гидроксизамещенного циклопентанового аналога хинолиновый заместитель может вводиться через аналогичную реакцию Мицунобу взаимодействием гидроксильной группы соединения (2 а') с подходящим спиртом (3b) в присутствии трифенилфосфина и активирующего агента, такого как диэтилазодикарбоксилат (DEAD), диизопропилазодикарбоксилат (DIAD) и т.п. В другом варианте осуществления изобретения группа L2 представляет собой ВОС, L5 представляет собой гидроксильную группу и исходное соединение (21 а) представляет собой коммерчески доступный ВОС-гидроксипролин или его любая другая стереоизомерная форма, например BOC-L-гидроксипропил,в частности его транс-изомер. Когда L5 в (21b) представляет собой защитную группу карбоксильной группы, она может удаляться в соответствии с методиками, описанными выше, с получением (21 с). В еще одном варианте осуществления PG в (21b-1) представляет собой Boc и PG2 представляет собой сложный низший алкиловый эфир, в частности сложный метиловый или этиловый эфир. Гидролиз последнего сложного эфира до кислоты может проводиться в соответствии со стандартными методиками,например, кислотным гидролизом с помощью соляной кислоты в метаноле или с помощью гидроксида щелочного металла, такого как NaOH, в особенности LiOH. В еще одном варианте осуществления изобретения гидроксизамещенные циклопентановый или циклопентеновый аналоги (21d) подвергаются превращению в (21 е), который, когда L5 и L5a представляют собой -OPG2 или -OPG2a, может превращаться в соответствующие кислоты (21f) удалением группы PG2. Удаление PG2a в (21 е-1) приводит к получению аналогичных промежуточных продуктов. Промежуточные соединения Y-R3 (4b) могут быть получены в соответствии с известными в данной области техники способами с использованием известных исходных веществ. Ряд способов синтеза таких промежуточных продуктов будет описан более подробно далее. Например, получение упомянутых выше промежуточных хинолинов показано на приведенной ниже схеме. Ацилирование согласно реакции Фриделя-Крафтса подходящего замещенного анилина (22 а), который является доступным в качестве коммерческого продукта или может быть получен согласно известным методикам, с использованием ацилирующего агента, такого как ацетил хлорид и т.п., в присутствии одной или нескольких кислот Льюиса, такой как трихлорид бора и трихлорид алюминия, в растворителе,таком как дихлорметан, приводит к получению (22b). Присоединение (22b) к карбоновой кислоте (22 с),предпочтительно в основных условиях, например в пиридине, в присутствии активирующего агента карбоксилатной группы, например POCl3, с последующим замыканием цикла и дегидратацией в основных условиях, таких как добавление трет-бутоксида калия в трет-бутаноле, приводит к получению хинолинового производного (22 е). Последний может подвергаться превращению в (22f), в котором LG представляет собой удаляемую группу, например, взаимодействием (22 е) с галогенирующим агентом, например фосфорилхлоридом или т.п., или с арилсульфонилхлоридом, например тозилхлоридом. Хинолинпроизводное (22 е) может повергаться связыванию со спиртом в реакции Мицунобу, как описано выше,или хинолин (22f) может подвергаться взаимодействию в реакции О-арилирования, как описано выше. Различные карбоновые кислоты с общей структурой (22 с) может применяться в описанном выше синтезе. Такие кислоты являются доступными либо как коммерческие продукты или могут быть получены в соответствии с известными методиками. Пример получения производных 2(замещенного)аминокарбоксиаминотиазола (23 а-1) в соответствии с методикой, описанной в публикацииBerdikhina et al., Chem. Heterocycl. Compd. (Engl. Transl.) (1991), 427-433, показан на приведенной далее схеме реакции, которая иллюстрирует получение 2-карбокси-4-изопропилтиазола (22 с-1): Этилтиооксамат (23 а) подвергается взаимодействию с -бромкетоном (23b) с получением сложного тиазолилового эфира карбоновой кислоты (23 с), который гидролизуется до соответствующей кислоты(25 с-1). Группа сложного этилового эфира в этих промежуточных продуктах может заменяться другими карбоксилзащищающими группами PG2, как определено выше. В приведенной выше схеме R4a принимает значения, определенные выше, и в частности представляет собой С 1-4 алкил, точнее изопропил. Бромкетон (23b) может быть получен из 3-метилбутан-2-он (MIK) с силилирующим агентом (таким как TMSCl), в присутствии подходящего основания (в частности, LiHMDS) и бром. Синтез других карбоновых кислот (22 с), в частности замещенных аминотриазолкарбоновых кислот Тиомочевина (24 с), содержащая различные заместители R4a, которые, в частности, представляют собой С 1-6 алкил, может быть получена взаимодействием подходящего амина (24 а) с третбутилизотиоцианатом в присутствии основания, такого как диизопропилэтиламин, в растворителе, таком как дихлорметан, с последующим удалением трет-бутильной группы в кислотных условиях. Последующая конденсация производного тиомочевины (24-с) с 3-бромпировиноградной кислотой приводит к получению тиазолкарбоновой кислоты (22 с-2). Синтез структурообразующих блоков Р 1.- 28015131 Циклопропанаминокислота, используемая в получении Р 1 фрагмента, является коммерчески доступной или может быть получена в соответствии с известными в данной области техники методиками. В частности, аминовинилциклопропилэтиловый эфир (12b) может быть получен в соответствии с методикой, описанной в WO 00/9543, или, как показано на приведенной далее схеме, где PG2 представляет собой защитную группу карбоксильной группы, как определено выше Обработка имина (25 а), который доступен в качестве коммерческого продукта или может быть легко получен, 1,4-дигалогенбутеном в присутствии основания приводит к получению (25b), гидролиз которого дает циклопропиламинокислоту (12b), содержащую аллильный заместитель, син-ориентированный относительно карбоксильной группы. Разделение энантиомерной смеси (12b) приводит к получению(12b-1). Разделение проводится с использованием известных методик, таких как ферментативное разделение; кристаллизация с хиральной кислотой; химическая дериватизация; или хиральная колоночная хроматография. Промежуточные продукты (12b) или (12b-1) могут присоединяться к подходящим производным Р 2, как описано выше. Структурообразующие блоки Р 1 для получения соединений согласно общей формуле (I), где R1 представляет собой -OR7 или -NH-SO2R8, могут быть получены взаимодействием аминокислот (23 а) с подходящим спиртом или амино соответственно в стандартных условиях образования сложного эфира или амида. Циклопропиламинокислоты (23 а) получают введением N-защитной группы PG и удалением PG2, и аминокислоты (а) подвергают превращению в амиды (12 с-1) или сложные эфиры (12 с-2), которые представляют собой подгруппы промежуточных продуктов (12 с), как показано на приведенной далее схеме реакций, где PG принимает значения, определенные выше. Взаимодействие (26 а) с амином (2b) проходит в соответствии с методикой образования амида. Аналогичное взаимодействие с (2 с) представляет собой реакцию образования сложных эфиров. Оба этих взаимодействия могут проводиться в соответствии с методиками, описанными выше. Такая реакция приводит к получению промежуточных продуктов (26b) или (26 с), аминозащитная группа из которых удаляется в соответствии со стандартными способами, например, описанными выше. Это, в свою очередь,приводит к получению целевого промежуточного соединения (12-с). Исходные вещества (26 а) могут быть получены из описанных выше промежуточных соединений (12b) введением сначала N-защитной групп PG и последующим удалением группы PG2. В одном варианте осуществления изобретения взаимодействие (26 а) с (2b) проводится обработкой аминокислоты конденсирующим агентом, например N,N'-карбонилдиимидазолом (CDI) и т.п., в растворителе, таком как ТГФ, с последующим взаимодействием с (2b) в присутствии основания, такого как 1,8 диазабицикло[5.4.0]ундец-7-ен (DBU). Альтернативно, аминокислота может обрабатываться (2b) в присутствии основания, такого как диизопропилэтиламин, с последующей обработкой конденсирующим агентом, таким как гексафторфосфат бензотриазол-1-илокси-трис-пирролидинофосфония (коммерчески
МПК / Метки
МПК: C07D 245/04, C07K 5/078, C07D 487/04, A61P 31/14, A61K 31/33, A61K 38/05, C07K 5/06
Метки: вируса, ингибиторы, макроциклические, гепатита
Код ссылки
<a href="https://eas.patents.su/30-15131-makrociklicheskie-ingibitory-virusa-gepatita-s.html" rel="bookmark" title="База патентов Евразийского Союза">Макроциклические ингибиторы вируса гепатита с</a>
Предыдущий патент: Пиперидиновые агонисты gpcr
Следующий патент: Лекарственное средство для лечения вирусных инфекций
Случайный патент: Способ добычи газа, газового конденсата и нефти (варианты)