Соль глюкуроновой кислоты и соединения пиперазина
Номер патента: 14942
Опубликовано: 29.04.2011
Авторы: Мирмехраби Махмуд, Дешмух Субодх С., Дайорио Кристофер Р., Фавзи Махди Б., Али Кадум, Эрнсперджер Эрик С., Шах Саед Музафар
Формула / Реферат
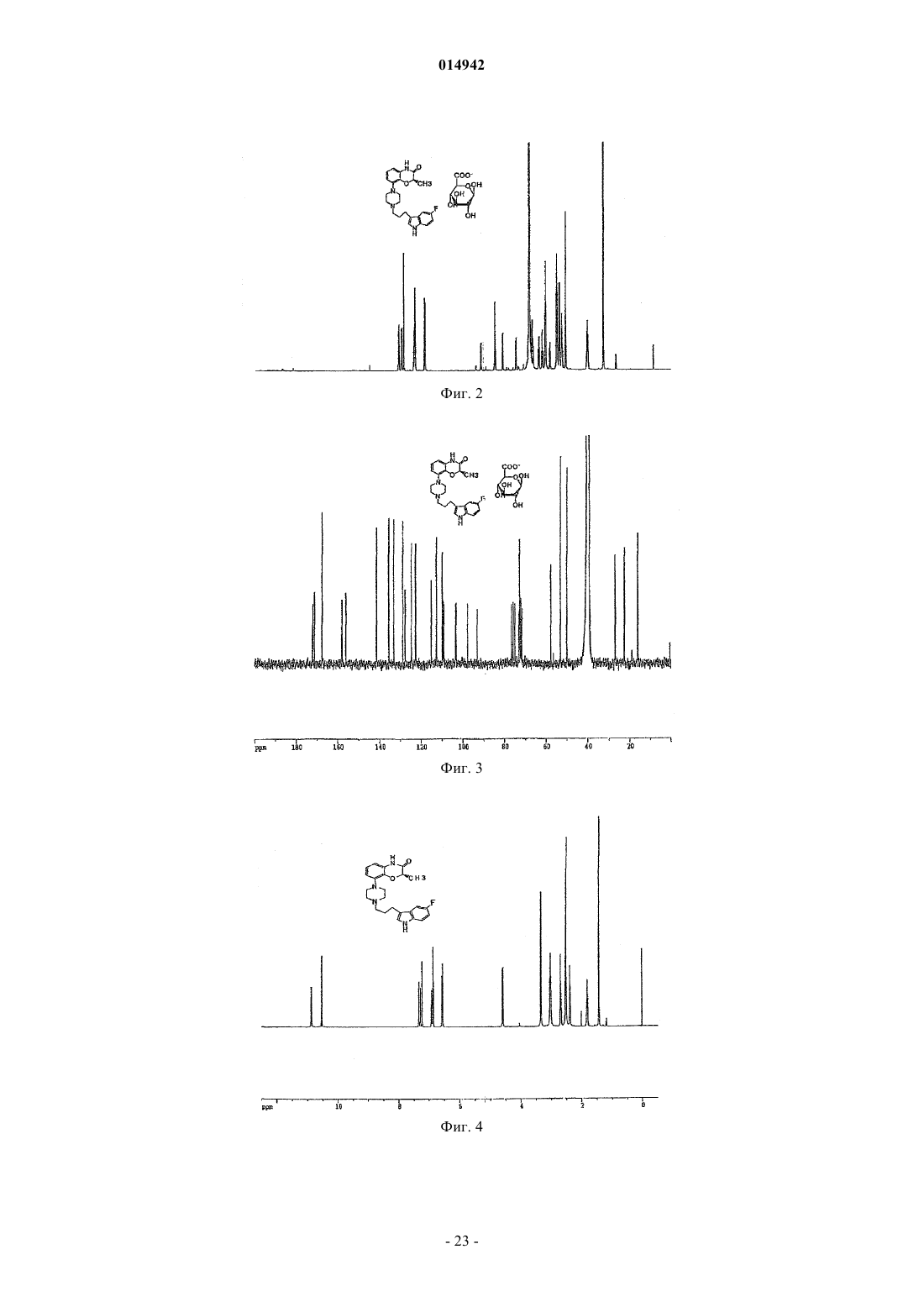
1. Соединение 2
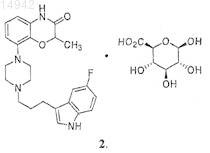
2. Соединение по п.1, где указанное соединение находится в твердой форме.
3. Соединение по п.2, где указанное соединение является кристаллическим веществом.
4. Соединение по п.3, где указанное соединение является кристаллическим твердым веществом, по существу, свободным от аморфного соединения 2.
5. Соединение по п.1, где указанное соединение, по существу, свободно от примесей.
6. Способ получения соединения 2
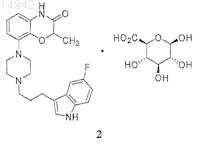
включающий стадии получения соединения 1
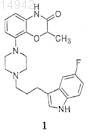
объединения соединения 1 с глюкуроновой кислотой в подходящем растворителе; и
необязательно стадию выделения соединения 2.
7. Способ по п.6, где указанный подходящий растворитель представляет собой протонный растворитель, полярный апротонный растворитель или их смесь.
8. Способ получения соединения 2
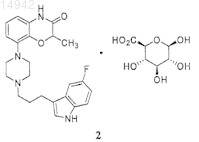
включающий стадии объединения соединения 1
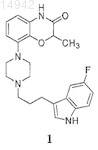
с подходящим растворителем и нагревания, чтобы получить раствор;
добавления глюкуроновой кислоты к указанному раствору; и
необязательно стадию выделения соединения 2.
9. Фармацевтически приемлемая композиция, предназначенная для лечения или уменьшения тяжести одного и более расстройства, выбранного из болезни Паркинсона, психозов, включая шизофрению, манию, психотическую депрессию, биполярное расстройство, депрессии, стресса/тревоги, болезни Альцгеймера, болезни Гентингтона, панического расстройства, обсессивно-компульсивного расстройства, расстройства пищевого поведения, наркомании, социальных фобий, агрессивности или беспокойства, мигрени, склеродермии, феномена Рейно, рвоты, желудочно-кишечного расстройства, связанного с регуляцией перистальтики, синдрома беспокойных ног или нарушений секреции пролактина, возникших вследствие опухолей гипофиза, содержащая соединение по п.1 и фармацевтически приемлемый носитель, адъювант или растворитель.
10. Композиция по п.9, где указанная композиция представляет собой инъекционный состав для внутрисосудистого введения.
11. Композиция по п.9, где указанная композиция представляет собой инъекционный состав для внутримышечного введения.
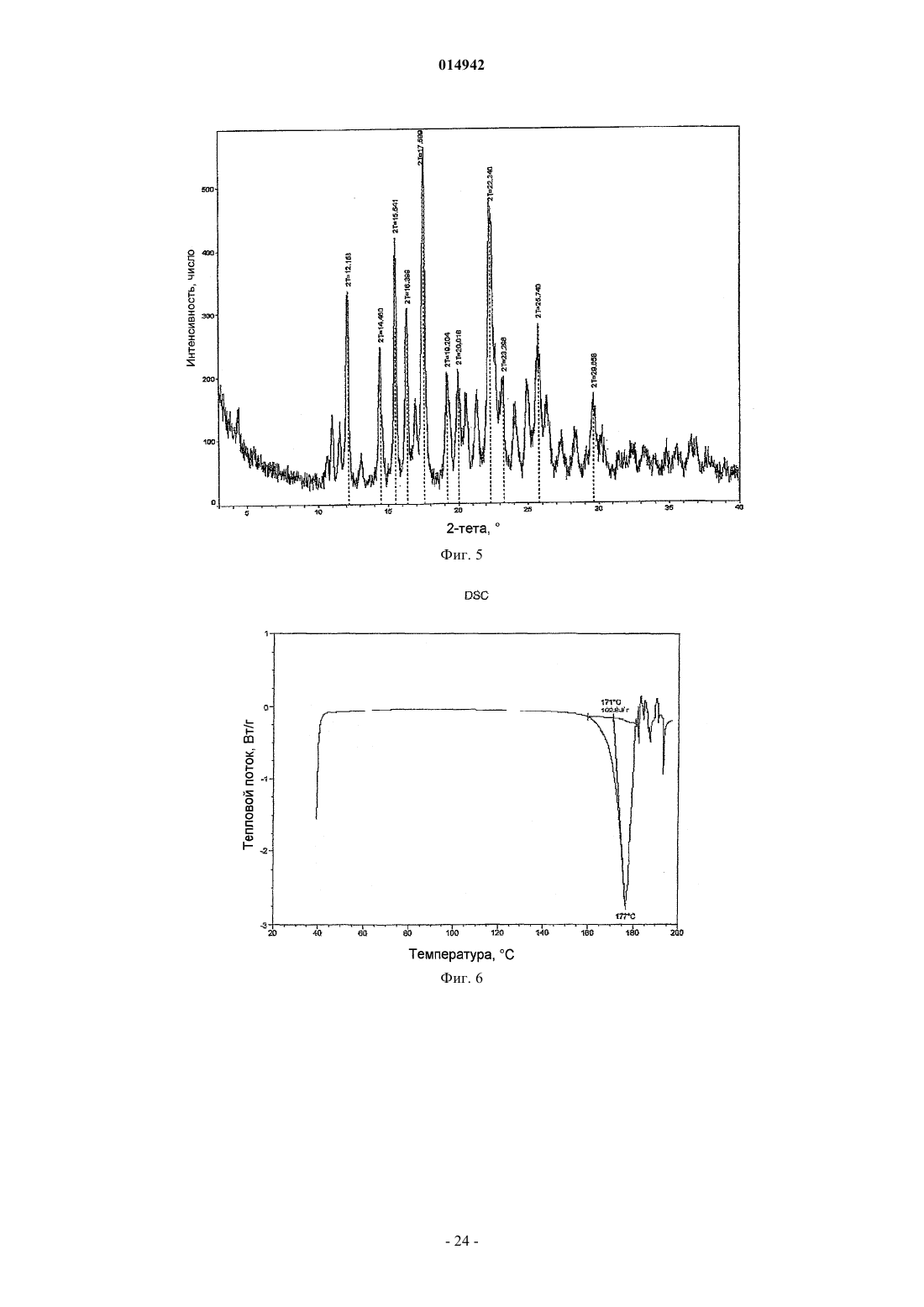
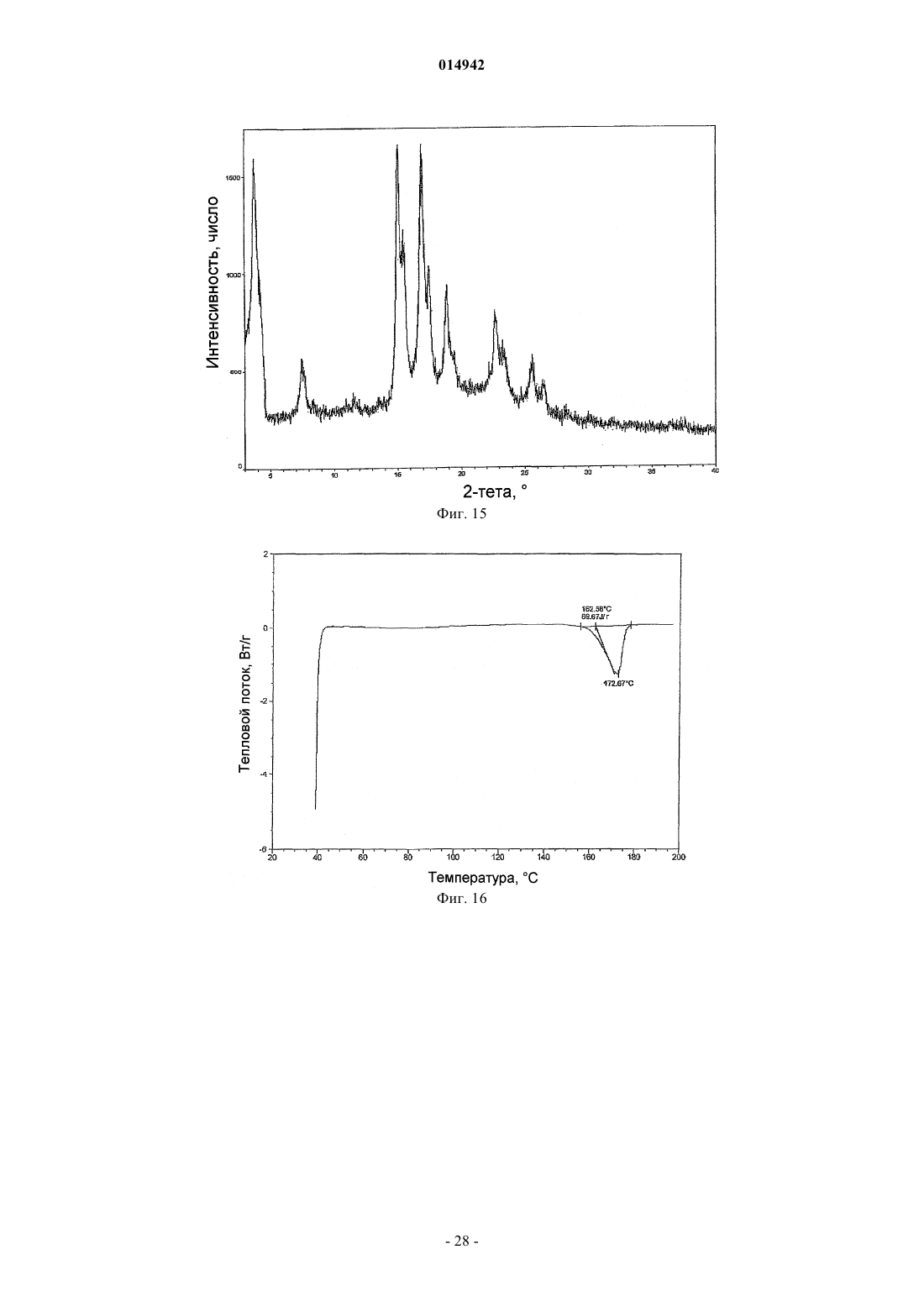
12. Кристаллическое соединение по п.3, где указанное соединение находится в форме I, имеющей на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 17,5; 22,5; 19,9; 3,9 и 12,2°.
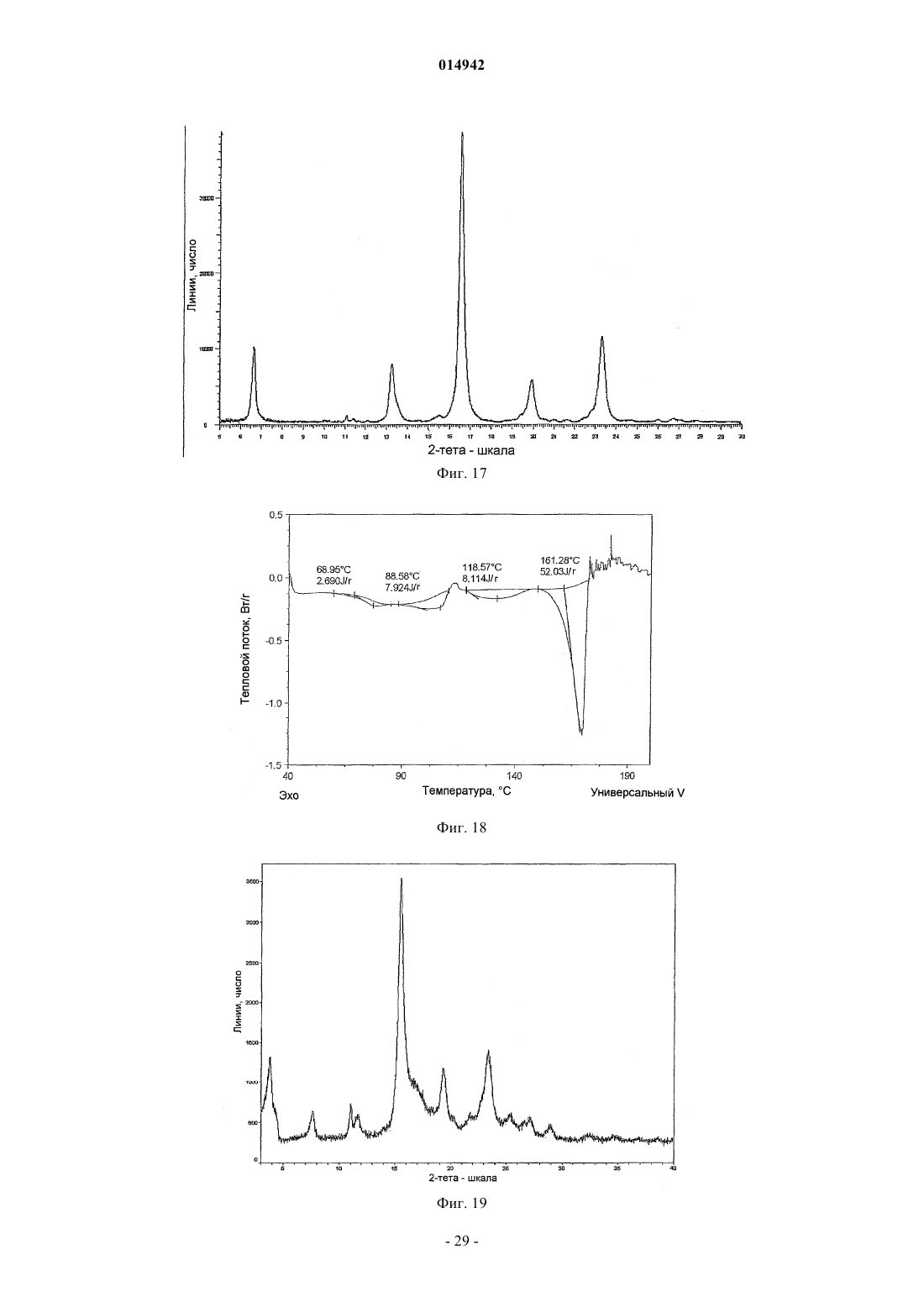
13. Кристаллическое соединение по п.3, где указанное соединение находится в форме II, имеющей на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 18,7°.
14. Кристаллическое соединение по п.3, где указанное соединение представляет собой гидрат соединения 2.
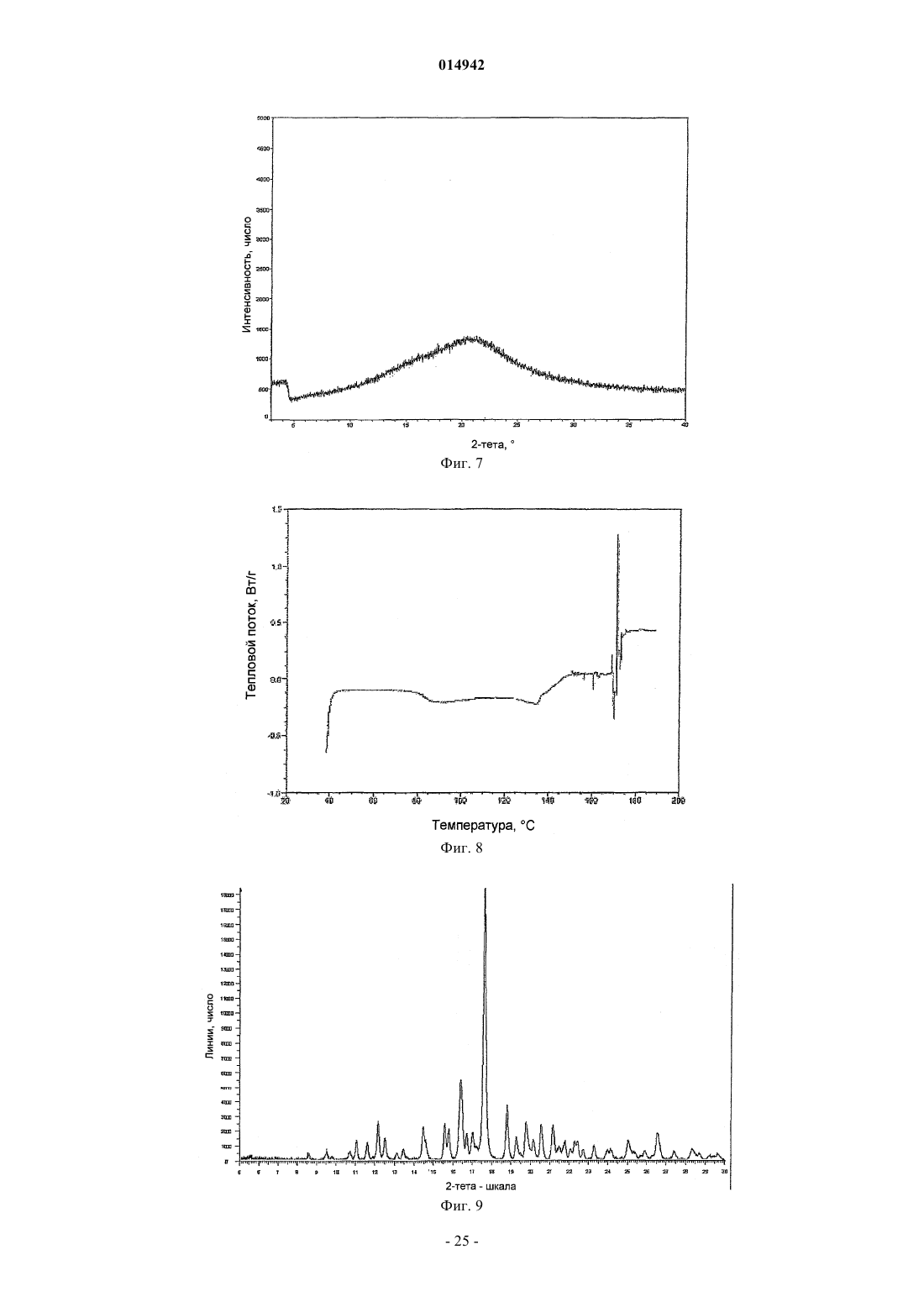
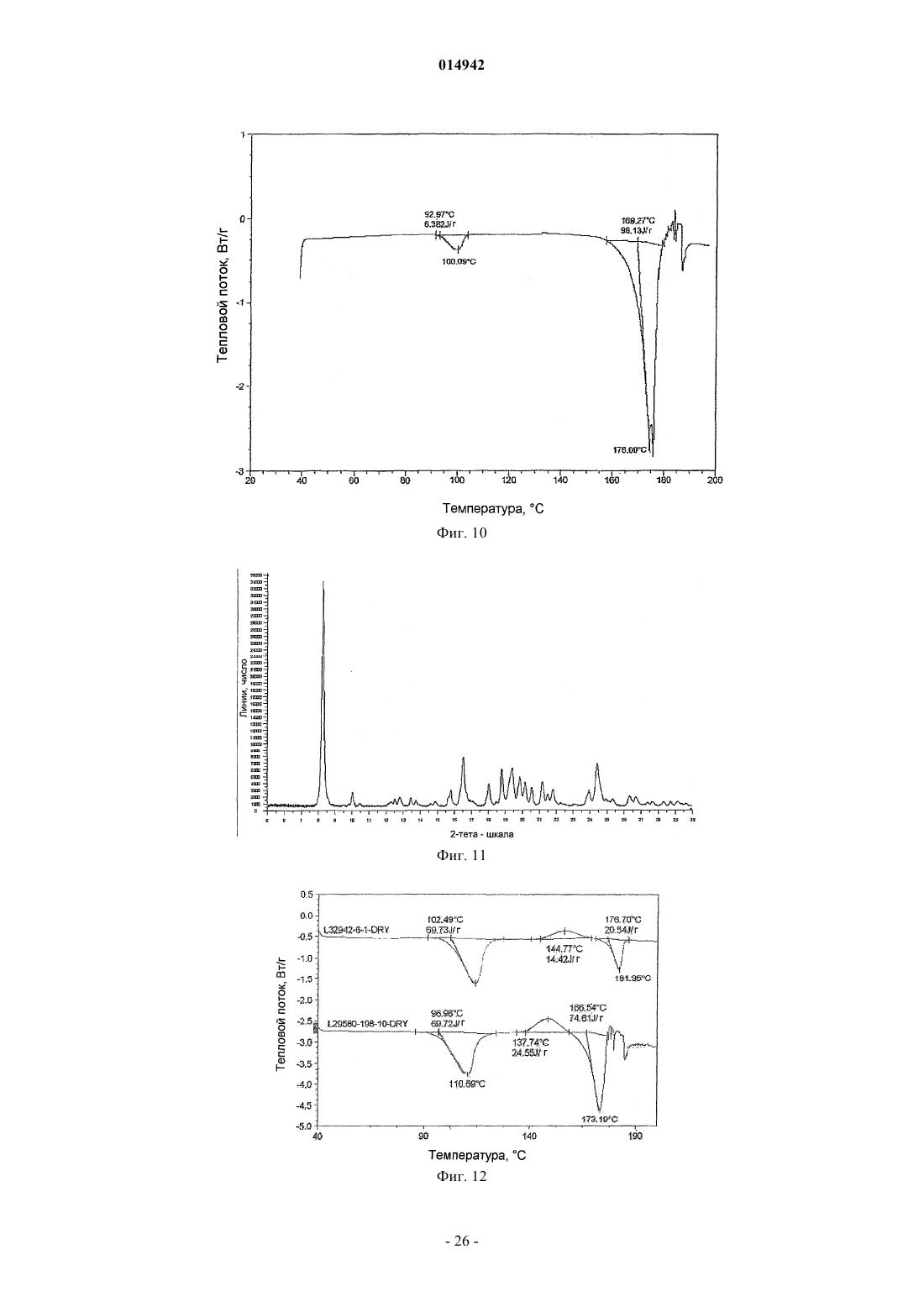
15. Кристаллическое соединение по п.14, где указанный гидрат выбран из гидрата I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 9,49; 16,40 и 17,61°, или гидрата II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 8,252; 10,015; 16,511 и 24,42°.
16. Кристаллическое соединение по п.3, где указанное соединение представляет собой сольват соединения 2.
17. Кристаллическое соединение по п.16, где указанный сольват выбран из
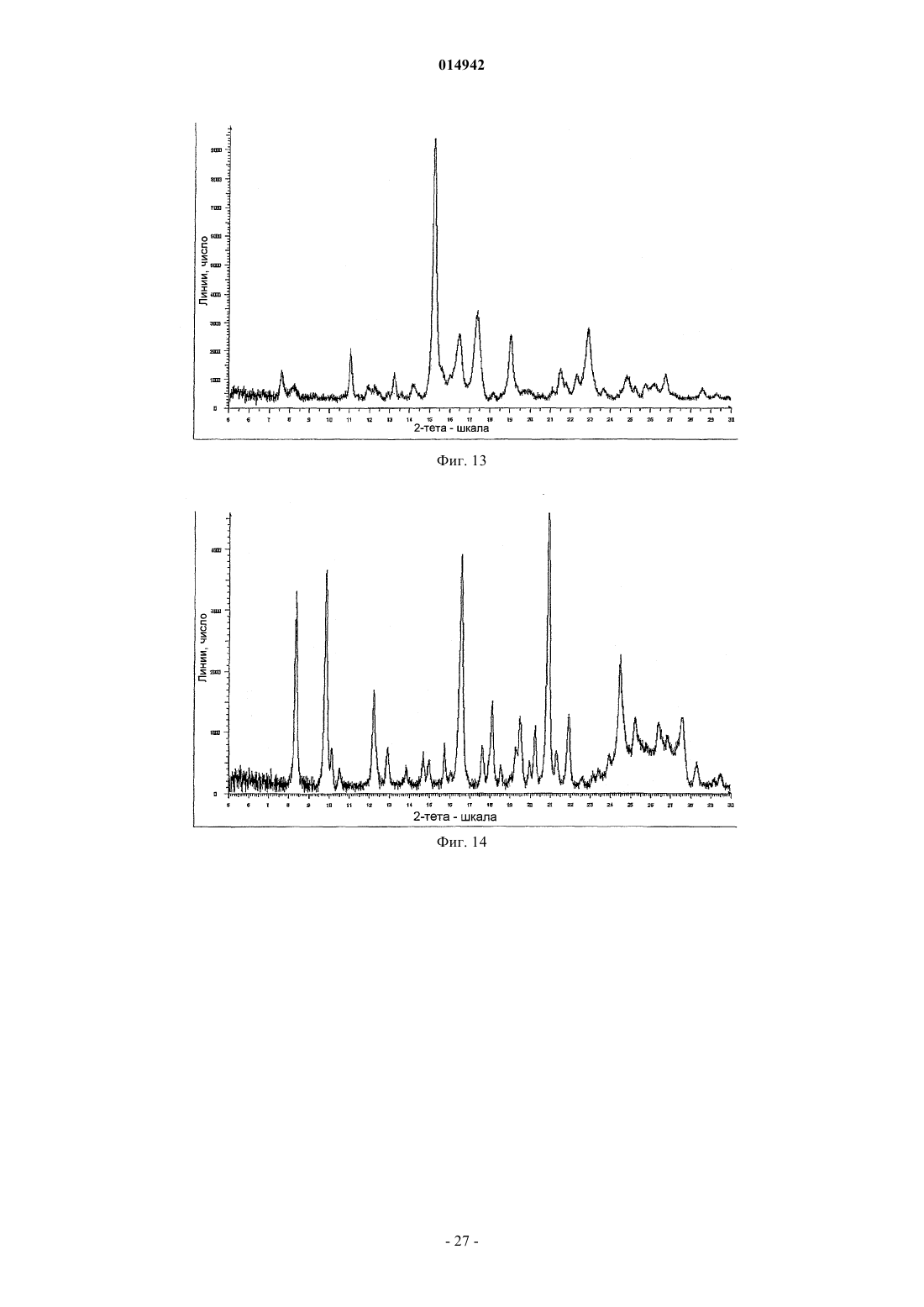
метанолята, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 11,048; 15,211; 17,363; 19,047 и 22,897°,
этанолята I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 8,32; 9,81; 16,56; 20,88 и 24,47°,
этанолята II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 15,09 и 16,9°,
изопропанолята I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 6,59; 13,23; 16,55 и 23,31°,
изопропанолята II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 3,79; 15,54 и 23,32°, или
ацетоната, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 11,04; 15,20; 15,47 и 20,81°.
Текст
СОЛЬ ГЛЮКУРОНОВОЙ КИСЛОТЫ И СОЕДИНЕНИЯ ПИПЕРАЗИНА Настоящее изобретение относится к солевой форме и ее композициям, применимым в качестве модулятора одного или более GPCR, которая проявляет необходимые для этого характеристики. Настоящее изобретение также относится к способам получения указанной солевой формы,которая является производным 8-4-[3-(5-фтор-1 Н-индол-3-ил)пропил]пиперазин-1-ил)-2-метил 4 Н-бензо[1,4]оксазин-3-она и глюкуроновой кислоты. Дешмух Субодх С., Али Кадум, Дайорио Кристофер Р., Эрнсперджер Эрик С., Фавзи Махди Б., Шах Саед Музафар (US),Мирмехраби Махмуд (CA) 014942 Перекрестная ссылка на родственную заявку В настоящей заявке испрашивается приоритет согласно предварительной заявке на патент США с регистрационным номером 60/716167, поданной 12 сентября 2005 г., которая тем самым включена в настоящее описание во всей полноте посредством ссылки. Область, к которой относится изобретение Настоящее изобретение относится к солям и их композициям, предназначенным для использования в качестве модуляторов одного или нескольких GPCR. Уровень техники Семейство рецепторов, сопряженных с G-белками (GPCR), самое крупное из известных семейств генов: оно составляет более 1% генома человека и участвует в широком диапазоне биологических функций (включая различные аутокринные, паракринные и эндокринные процессы). Надсемейство GPCR также является семейством генов, которое в наибольшей степени используется в фармацевтической промышленности для создания терапевтических соединений. GPCR были разделены на родопсиноподобныеGPCR, секретиноподобные GPCR, рецепторы цАМФ, грибковые рецепторы половых феромонов и семейство метаботропных глутаматных рецепторов. Родопсиноподобные GPCR представляют собой широко распространенное семейство белков, которое включает рецепторы гормонов, нейромедиаторов и света, все из которых преобразуют внеклеточные сигналы посредством взаимодействия с белками, связывающими нуклеотид гуанин (G). Хотя строение и характер активирующих их лигандов варьируют в широких пределах, аминокислотная последовательность родопсиноподобных GPCR очень похожа и, как полагают, имеет общий структурный остов, содержащий 7 трансмембранных (ТМ) стягивающих спиралей; родопсиноподобные GPCR спарены с внутриклеточными G-белками, которые при связывании рецептора с агонистом отделяются от рецептора и запускают или ингибируют сигнальные механизмы с участием вторичных мессенджеров. См.: Lander et al. Nature 409:860 (2001); Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001). Семейство родопсиноподобных GPCR включает несколько классов рецепторов, которые в разной степени распределены по центральной нервной системе (ЦНС) и многим периферическим участкам; эти рецепторы участвуют в ряде состояний ЦНС и психоневрологических состояний. Среди этих рецепторов находятся дофаминовые (D) рецепторы и 6 из 7 главных подтипов серотониновых (5 гидрокситриптаминовых, 5 НТ) рецепторов (подтипы рецепторов 5HT1,2 и 4-7 представляют собойGPCR, в то время как подтип рецепторов 5 НТ 3-управляемый лигандом Na+/K+ ионный канал). Дофаминовые нейроны в ЦНС позвоночных участвуют в инициировании и выполнении движений,поддержке эмоциональной стабильности и регуляции функций гипофиза. Связывание дофамина с внеклеточной связывающей бороздой D-рецепторов активирует G-белки: рецепторы подтипов D1 и D5 (D1 подобные) связаны со стимулирующими G-белками, в то время как рецепторы подтипов 2-4 (D2 подобные) связаны с ингибирующими G-белками. D2-подобные рецепторы обнаружены во всех отделах головного мозга, а также в гладких мышцах и пресинаптических нервных окончаниях; при связывании с агонистом D2-подобные рецепторы ингибируют передачу нервных импульсов. Конкретно, рецепторы D2 в большом количестве и широко распространены в полосатом теле, лимбической системе, таламусе, гипоталамусе и гипофизе. Связывание антагониста с D2-рецепторами ингибирует связывание агонистов и тем самым предотвращает ингибирование расположенных далее сигнальных механизмов. АнтагонистыD2-рецепторов используются в лечении психозов (например, шизофрении, мании, психотической депрессии и биполярного расстройства), а также могут применяться для кратковременного седативного воздействия при агрессивности или беспокойстве (например, амисульприд, клозапин, галоперидол, немонаприд, пимозид, ремоксиприд, спиперон, сульпирид) и могут применяться для лечения наркомании, в то время как агонисты D2-рецепторов используются для лечения болезни Паркинсона и подавления секреции пролактина, вызванной опухолями гипофиза (например, апоморфин, бромокриптин, дигидроэрготамин, пирибедил, квинпирол), и для лечения синдрома беспокойных ног (например, прамипексол, ропинирол). См. Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McQraw Hill Companies, Inc.Lancet, 346:743-749, (1995); Hietala. The Lancet, 346:1130-1131 (1995); Kemppainen et al. Eur. J. Neurosci.,18:149-154 (2003). 5-Гидрокситриптамин повсеместно встречается у растений и животных. 5-Гидрокситриптамин является важным нейромедиатором и местным гормоном ЦНС и кишечника; 5-гидрокситриптамин участвует в очень большом количестве физиологических и патофизиологических путей. Связывание 5 гидрокситриптамина с внеклеточной связывающей бороздой 5 НТ-рецепторов активирует G-белки; известно, что подтип рецепторов 5HT1 сопряжен с ингибирующими G-белками, в то время как подтипы 2,4, 6 и 7 со стимулирующими G-белками. Известно, что подтипы 5HT1-рецептора (описано по меньшей мере 5) прежде всего встречаются в кровеносных сосудах головного мозга, где они опосредуют нейральное ингибирование и вазоконстрикцию. Специфичные агонисты 5 НТ 1-рецепторов используются в лечении мигрени (например, суматриптан) и стресса/тревоги (например, буспирон), в то время как антагонисты рекомендованы для лечения психозов (например, спиперон, метиотепин). Кроме того, регуляция-1 014942 подтипов 5 НТ 1-рецептора участвует в развитии наркомании, болезни Альцгеймера, болезни Паркинсона,депрессии, рвоты и расстройств пищевого поведения. Подтипы 5 НТ 2-рецептора (известно по меньшей мере 3) обнаружены во всех отделах ЦНС и во многих периферических участках, где они оказывают возбуждающее действие на нейроны и гладкие мышцы. Антагонисты 5 НТ 2-рецепторов используются в лечении мигрени (например, метисергид); они также показали потенциал в лечении склеродермии и феномена Рейно (например, кетансерин). 5 НТ 3-рецепторы, как известно, главным образом находятся в периферической нервной системе, и их антагонисты используются как противорвотные средства (например,ондасетрон, трописетрон). 5 НТ 4-рецепторы обнаружены в головном мозге, а также сердце, мочевом пузыре и желудочно-кишечном тракте (ЖКТ). В пределах ЖКТ они вызывают возбуждение нейронов и опосредуют стимулирующее действие 5 НТ на перистальтику. Специфичные антагонисты 5 НТ 4 рецепторов (например, метоклопрамид) используются для лечения желудочно-кишечных расстройств. Подтипы 5 НТ-рецепторов 5 (известно по меньшей мере 5), 6 и 7 также обнаружены во всех отделах ЦНС и могут быть потенциальными целями для низкомолекулярных средств. В частности, подтип рецептора 5 НТ 7 принимает участвие в развитии депрессии, психозов, болезни Паркинсона, болезни Альцгеймера,болезни Гентингтона, мигрени, стресса/тревоги, расстройств пищевого поведения и рвоты. См. Basic andBehavioral Reviews, 14:3547 (1990). Действие 5 НТ в синапсах ограничено его повторным захватом через пресинаптическую мембрану,опосредованным Na+/K+. Ингибиторы обратного захвата 5 НТ (например, циталопрам, кломипрамин, флуоксетин, флувоксамин, индатралин, циметидин) используются в лечении депрессии, стресса/тревоги, панического расстройства, обсессивно-компульсивного расстройства, расстройств пищевого поведения и социофобий и могут оказаться применимыми для лечения мигрени, психозов, болезни Альцгеймера, болезни Паркинсона, заболевания Гентингтона, наркомании, расстройств пищевого поведения, склеродермии и феномена Рейно, желудочно-кишечных расстройств, связанных с регуляцией перистальтики, и/или рвоты. См.(1999); и, кроме того, ссылки в предыдущих абзацах. Соответственно, желательно получить соединения, которые модулируют GPCR, в форме, подходящей для введения пациенту, который нуждается в лечении любого из вышеупомянутых расстройств. В частности, было бы желательно, чтобы такие соединения имели дополнительные особенности, такие как хорошая растворимость, стабильность, легкость приготовления лекарственной формы и так далее. Сущность изобретения В настоящее время обнаружено, что новая форма соли по настоящему изобретению и ее композиции применимы в качестве модулятора одного или нескольких GPCR и имеют необходимые для этого характеристики. В целом, эта форма соли и ее фармацевтически приемлемые композиции применимы для лечения или уменьшения тяжести ряда заболеваний или расстройств, включающих, но не ограниченных перечисленными, болезнь Паркинсона, психозы (например шизофрению, манию, психотическую депрессию и биполярное расстройство), депрессию, стресс/тревогу, болезнь Альцгеймера, болезнь Гентингтона, паническое расстройство, обсессивно-компульсивное расстройство, расстройства пищевого поведения, наркоманию, социальные фобии, агрессивность или беспокойство, мигрень, склеродермию и феномен Рейно, рвоту, желудочно-кишечные расстройства, связанные с регуляцией перистальтики, синдром беспокойных ног и нарушения секреции пролактина, возникшие вследствие опухолей гипофиза. Краткое описание чертежей На фиг. 1 изображена порошковая рентгенограмма для формы I соединения 2; на фиг. 2 - 1 Н-спектр ЯМР соединения 2; на фиг. 3 - 13 С-спектр ЯМР соединения 2; на фиг. 4 - 1 Н-спектр ЯМР соединения 1; на фиг. 5 - порошковая рентгенограмма для формы I соединения 2;-2 014942 на фиг. 6 изображена термограмма ДСК для формы I соединения 2; на фиг. 7 - порошковая рентгенограмма для аморфного соединения 2; на фиг. 8 - термограмма ДСК для аморфного соединения 2; на фиг. 9 - порошковая рентгенограмма для гидрата I соединения 2; на фиг. 10 - термограмма ДСК для гидрата I соединения 2; на фиг. 11 - порошковая рентгенограмма для гидрата соединения 2; на фиг. 12 - термограмма ДСК для гидрата I (верхний график) и гидрата II (нижний график) соединения 2; на фиг. 13 - порошковая рентгенограмма для метанолята соединения 2; на фиг. 14 - порошковая рентгенограмма для этанолята I соединения 2; на фиг. 15 - порошковая рентгенограмма для этанолята II соединения 2; на фиг. 16 - термограмма ДСК для этанолята II соединения 2; на фиг. 17 - порошковая рентгенограмма для изопропанолята I (+ ДМФА) соединения 2; на фиг. 18 - термограмма ДСК для изопропанолята I (+ ДМФА) соединения 2; на фиг. 19 - порошковая рентгенограмма для изопропанолята II соединения 2; на фиг. 20 - термограмма ДСК для изопропанолята II соединения 2; на фиг. 21 - порошковая рентгенограмма для ацетоната соединения 2. Подробное описание изобретения Общее описание некоторых особенностей изобретения: В заявке РСТ/ЕР/00/08190 (номер международной публикации WO 01/14330) описаны различные содержащие индол производные пиперазина, включая соединение 1 (8-4-[3-(5-фтор-1 Н-индол-3-ил)пропил]-пиперазин-1-ил-2-метил-4 Н-бензо[1,4]оксазин-3-он), которые проявляют антагонистическую активность по отношению к D2-рецепторам и ингибирующую активность в отношении обратного захвата 5 НТ в терапевтических моделях. Кроме того, соединение 1 активно в отношении терапевтических моделей, которые чувствительны к имеющим клиническое значение нейролептикам, антидепрессантам и транквилизаторам, а также активно при болезни Паркинсона. Соответственно, соединение 1 применимо для лечения болезни Паркинсона, психозов (например, шизофрении, мании, психотической депрессии и биполярного расстройства),депрессии, стресса/тревоги, панического расстройства, болезни Альцгеймера, обсессивнокомпульсивного расстройства, расстройств пищевого поведения, наркомании, социальной фобии, агрессивности или беспокойства, мигрени, склеродермии и феномена Рейно, рвоты, желудочно-кишечных расстройств, связанных с регуляцией перистальтики, синдрома беспокойных ног и применимо для подавления секреции пролактина, возникшей вследствие опухолей гипофиза. Кроме того, соединение 1 отличается слабой способностью вызывать каталепсию у грызунов и, следовательно, с меньшей вероятностью будет вызывать экстрапирамидные побочные эффекты, чем существующие нейролептики. См.WO 01/14330; van der Heyden and Bradford. Behav. Brain Res. 31:61 (1988); van der Poel et al. Psychopharmacology, 97:147 (1989); и Ungerstedt. Acta Physiol. Scand. 82: (suppl. 367) 69 (1971). Было бы желательно получить соединение 1 в форме соли, которая в отличие от соединения 1 обладает такими характеристиками, как улучшенная растворимость в воде, стабильность и легкость приготовления лекарственной формы. В частности, улучшенная растворимость в воде выгодна, поскольку улучшает растворение в желудочно-кишечном тракте (ЖКТ), тем самым повышая всасывание и биодоступность. Улучшенная биодоступность позволила бы применять более низкую дозу, что, в свою очередь,реже вызывало бы такие побочные желудочно-кишечные эффекты, как тошнота или рвота. Более низкая доза также позволила бы разработать более мелкую лекарственную форму (например таблетку, капсулу),что было бы выгодно с точки зрения технологии лекарственного средств и улучшило бы соблюдение пациентом режима лечения (пациенты предпочитают принимать более мелкие таблетки или капсулы). Кроме того, лекарственная форма, которую нужно принимать 1 раз в сутки, улучшила бы соблюдение пациентом режима лечения по сравнению с многократным приемом препарата в течение суток - это соображение важно для соответствующей популяции пациентов, таких как больные шизофренией и другими психозами. Соответственно, настоящее изобретение относится к соли глюкуроновой кислоты и соединения 1, находящейся в форме, подходящей для лекарственной формы с пролонгированным действием; у такой формы были бы дополнительные преимущества - снижение частоты побочных эффектов со-3 014942 стороны верхних отделов ЖКТ, таких как тошнота или рвота, за счет ограничения количества лекарственного средства, высвобождаемого в этих отделах, и за счет обхода рецепторов верхних отделов ЖКТ,которые отвечают за указанные эффекты. Один вариант осуществления настоящего изобретения относится к соли глюкуроновой кислоты соединения 1, представленной соединением 2 Среднему специалисту в данной области техники будет ясно, что глюкуроновая кислота и соединение 1 соединены ионной связью с образованием соединения 2. Предполагается, что соединение 2 может существовать в виде ряда физических форм. Например, соединение 2 может находиться в растворе, суспензии или в твердой форме. В определенных вариантах осуществления соединение 2 находится в твердой форме. Если соединение 2 находится в твердой форме, указанное соединение может быть аморфным,кристаллическим или представлять собой их смесь. Примеры твердых форм более подробно описаны ниже. Как используется в настоящем описании, несмотря на структуру соединения 2, изображенную выше, фраза соль глюкуроновой кислоты и родственные термины относятся к соли D-глюкуроновой кислоты, соли L-глюкуроновой кислоты, соли DL-глюкуроновой кислоты или их смеси. В определенных вариантах осуществления соединение 2 представляет собой соль D-глюкуроновой кислоты. В других вариантах осуществления соединение 2 представляет собой соль D-глюкуроновой кислоты, которая, по существу, свободна от соли L-глюкуроновой кислоты, где по существу свободна означает, что соединение не содержит существенного количества соли L-глюкуроновой кислоты. В определенных вариантах осуществления по меньшей мере приблизительно 95 мас.% соединения 2 присутствует в виде соли Dглюкуроновой кислоты. В других вариантах осуществления изобретения по меньшей мере приблизительно 99 мас.% соединения 2 присутствует в виде соли D-глюкуроновой кислоты. Средний специалист в данной области техники признает, что глюкуроновая кислота может существовать в циклической форме, которая изображена выше, или в форме открытого цикла. Соответственно,в настоящем изобретении учитывается, что соль глюкуроновой кислоты соединения 2 включает и циклическую соль глюкуроновой кислоты, и формы соли глюкуроновой кислоты с открытым циклом. Другие варианты осуществления настоящего изобретения относятся к соединению 2, по существу свободному от примесей. Как используется в данном описании, термин по существу свободный от примесей означает, что соединение не содержит существенного количества постороннего вещества. Такое постороннее вещество может включать избыток глюкуроновой кислоты, избыток соединения 1, остатки растворителей или любые другие примеси, которые могут образовываться в ходе получения и/или очистки соединения 2. В определенных вариантах осуществления присутствует по меньшей мере приблизительно 95 мас.% соединения 2. В других вариантах осуществления изобретения присутствует по меньшей мере приблизительно 99 мас.% соединения 2. В одном варианте осуществления соединение 2 присутствует в количестве по меньшей мере приблизительно 97; 97,5; 98,0; 98,5; 99; 99,5; 99,8 мас.%, где процентное содержание вычислено в расчете на общую массу композиции. Согласно другому варианту осуществления соединение 2 содержит не более приблизительно 2,0% площади ВЭЖХ общего количества органических примесей и в определенных вариантах осуществления не более приблизительно 1,5% площади ВЭЖХ общего количества органических примесей в расчете на общую площадь высокоэффективной жидкостной хроматограммы. В других вариантах осуществления соединение 2 содержит не более приблизительно 0,6% площади ВЭЖХ любой одной примеси и в определенных вариантах осуществления - не более приблизительно 0,5% площади ВЭЖХ любой одной примеси относительно общей площади высокоэффективной жидкостной хроматограммы. Подразумевается, что строение, изображенное для соединения 2, также включает все изомерные(например, энантиомерные или конформационные) формы. Например, в это изобретение включены какR-, так и S-конфигурации при стереогенном атоме углерода. Поэтому отдельные стереохимические изомеры, а также энантиомерные и конформационные смеси настоящего изобретения включены в объем изобретения. Кроме того, все таутомерные формы соединения 2 включены в объем настоящего изобретения. Кроме того, также подразумевается, что структуры, изображенные в настоящем описании, включают соединения, которые отличаются только присутствием одного атома и более, обогащенного изотопами. Например, соединения, имеющие данное строение, за исключением замены водорода дейтерием или тритием или замены углерода на углерод, обогащенный 13 С или 14 С, включены в объем настоящего-4 014942 изобретения. Твердые формы соединения 2 Обнаружено, что соединение 2 может существовать в виде ряда твердых форм. Такие формы включают чистые кристаллические формы, также известные как полиморфы, сольваты, гидраты и аморфные формы. Все такие формы рассматриваются в настоящем изобретении. Определенные варианты осуществления настоящего изобретения относятся к соединению 2 как к смеси одной твердой формы и более,выбранной из полиморфов, сольватов, гидратов и аморфных форм соединения 2. Как используется в данном описании, термин полиморф относится к различным кристаллическим структурам (несольватированных форм), в которых соединение может кристаллизоваться. Как используется в данном описании, термин сольват относится к кристаллической форме со стехиометрическим или нестехиометрическим количеством растворителя, включенного в кристаллическую структуру. Сходным образом термин гидрат относится к кристаллической форме со стехиометрическим или нестехиометрическим количеством воды, включенной в кристаллическую структуру. В определенных вариантах осуществления соединение 2 представляет собой кристаллическое твердое вещество. В других вариантах осуществления соединение 2 представляет собой кристаллическое твердое вещество, по существу свободное от аморфного соединения 2. Как используется в настоящем описании, термин по существу свободный от аморфного соединения 2 означает, что соединение не содержит существенного количества аморфного соединения 2. В определенных вариантах осуществления присутствует по меньшей мере приблизительно 95 мас.% кристаллического соединения 2. В других вариантах осуществления изобретения присутствует по меньшей мере приблизительно 99 мас.% кристаллического соединения 2. В определенных вариантах осуществления соединение 2 представляет собой чистую кристаллическую форму и, следовательно, не содержит воды или растворителя, включенного в кристаллическую структуру. Обнаружено, что соединение 2 может существовать по меньшей мере в двух различных чистых кристаллических формах или полиморфах. Две такие полиморфные формы упоминаются в настоящем описании как форма I и форма II. Определенные варианты осуществления настоящего изобретения относятся к форме I соединения 2. В одном аспекте форма I соединения 2 имеет порошковую дифракционную рентгенограмму, по существу схожую с изображенной на фиг. 1 или 5. В другом варианте осуществления форма I соединения 2 отличается тем, что имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 17,5; 22,5; 19,9; 3,9 и 12,2. Как используется в настоящем описании, термин около, если используется в отношении значения угла 2-тета, относится к установленному значению 2-тета 0,1. Способы получения формы I соединения 2 описаны ниже. Другие варианты осуществления настоящего изобретения относятся к форме II соединения 2. В одном варианте осуществления форма II соединения 2 имеет характерный пик на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 18,7. Способы получения формы II соединения 2 описаны ниже. Другой вариант осуществления настоящего изобретения относится к соединению 2 в виде аморфного твердого вещества. Порошковая дифракционная рентгенограмма аморфного соединения 2 изображена на фиг. 7. Аморфные твердые вещества известны специалисту в данной области техники, и их обычно получают такими способами, среди прочих, как лиофилизация, плавление и осаждение из надкритической жидкости. Другие способы получения аморфного соединения 2 описаны в данном описании ниже. Обнаружено, что соединение 2 может существовать по меньшей мере в двух гидратированных формах. Две гидратированные формы упоминаются в настоящем описании как гидрат I и гидрат II. Определенные варианты осуществления настоящего изобретения относятся к гидрату I соединения 2. В одном варианте осуществления гидрат I отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 9,49; 16,40 и 17,61. Согласно одному аспекту гидрат I соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 9. Способы получения гидрата I соединения 2 описаны ниже. В табл. 1 (ниже) приведены пики дифракционной рентгенограммы для гидрата I соединения 2, где каждое значение представляет собой угол 2-тета.-5 014942 Таблица 1. Наблюдаемые пики дифракционной рентгенограммы для гидрата I соединения 2 Определенные варианты осуществления настоящего изобретения относятся к гидрату II соединения 2. В одном варианте осуществления гидрат II отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 8,252; 10,015; 16,511 и 24,42. Согласно одному аспекту гидрат II соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 11. Способы получения гидрата II соединения 2 описаны ниже. В табл. 2 (ниже) приведены пики дифракционной рентгенограммы для гидрата II соединения 2, где каждое значение представляет собой угол 2-тета. Таблица 2. Наблюдаемые пики дифракционной рентгенограммы для гидрата II соединения 2 Обнаружено, что соединение 2 может существовать в виде ряда кристаллических форм. Определенные варианты осуществления настоящего изобретения относятся к кристаллическому метаноляту соединения 2. В одном аспекте изобретения метанолят соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 13. Согласно другому варианту осуществления метанолят соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 11,048; 15,211; 17,363; 19,047 и 22,897. Способы получения метанолята соединения 2 описаны ниже. В табл. 3 (ниже) приведены пики дифракционной рентгенограммы для метанолята соединения 2,где каждое значение представляет собой угол 2-тета.-6 014942 Таблица 3. Наблюдаемые пики дифракционной рентгенограммы для метанолята соединения 2 В других вариантах осуществления кристаллические соединения 2 получают в виде этанолята. Идентифицированы две формы этанолята соединения 2. Согласно одному аспекту кристаллический этанолят соединения 2 представляет собой этанолят I и имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 14. В другом варианте осуществления этанолят I соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 8,32; 9,81; 16,56; 20,88 и 24,47. Способы получения этанолята I соединения 2 описаны ниже. В табл. 4 (ниже) приведены пики дифракционной рентгенограммы для этанолята I соединения 2,где каждое значение представляет собой угол 2-тета. Таблица 4. Наблюдаемые пики дифракционной рентгенограммы для этанолята I соединения 2 В определенных вариантах осуществления кристаллический этанолят соединения 2 представляет собой этанолят II и имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 15. В другом варианте осуществления этанолят II соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 15,09 и 16,9. Способы получения этанолята II соединения 2 описаны ниже. В табл. 5 (ниже) приведены пики дифракционной рентгенограммы для этанолята II соединения 2,где каждое значение представляет собой угол 2-тета.-7 014942 Таблица 5. Наблюдаемые пики дифракционной рентгенограммы для этанолята II соединения 2 В других вариантах осуществления кристаллическое соединение 2 получают в виде изопропанолята соединения 2. Идентифицированы две формы изопропанолята соединения 2. Согласно одному аспекту кристаллический изопропанолят соединения 2 представляет собой изопропанолят I, который содержит ДМФА. Согласно одному аспекту изопропанолят I соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 17, и/или термограмму ДСК, изображенную на фиг. 18. В другом варианте осуществления изопропанолят I соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 6,5 9; 13,2 3; 16,55 и 23,31. Способы получения изопропанолята I соединения 2 описаны ниже. В табл. 6 (ниже) приведены пики дифракционной рентгенограммы для изопропанолята I (+ ДМФА) соединения 2, где каждое значение представляет собой угол 2-тета. Таблица 6. Наблюдаемые пики дифракционной рентгенограммы для изопропанолята I (+ ДМФА) соединения 2 Согласно другому аспекту кристаллический изопропанолят соединения 2 представляет собой изопропанолят II, который не содержит ДМФА. Согласно одному аспекту изопропанолят II соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 19. В другом варианте осуществления изопропанолят II соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 3,79/ 15,54 и 23,32. Способы получения изопропанолята II соединения 2 описаны ниже. В табл. 7 (ниже) приведены пики дифракционной рентгенограммы для изопропанолята II соединения 2, где каждое значение представляет собой угол 2-тета. Таблица 7. Наблюдаемые пики дифракционной рентгенограммы для изопропанолята II соединения 2 В других вариантах осуществления кристаллическое соединение 2 получают в виде ацетоната. Согласно одному аспекту ацетонат соединения 2 имеет порошковую дифракционную рентгенограмму, по существу подобную изображенной на фиг. 21. В другом варианте осуществления ацетоната соединения 2 отличается тем, что он имеет один пик и более на порошковой дифракционной рентгенограмме, выбранный из пиков в области значений 2-тета около 11,04; 15,20; 15,47 и 20,81. Способы получения ацетоната соединения 2 описаны ниже. В табл. 8 (ниже) приведены пики дифракционной рентгенограммы для ацетоната соединения 2, где каждое значение представляет собой угол 2-тета.-8 014942 Таблица 8. Наблюдаемые пики дифракционной рентгенограммы для ацетоната соединения 2 Определенные варианты осуществления настоящего изобретения относятся к форме I соединения 2,включающей одну дополнительную твердую форму соединения 2 и более. Другие варианты осуществления настоящего изобретения относятся к форме I соединения 2, включающей одну или более форм II,гидрата соединения 2, сольвата соединения 2 или аморфного соединения 2. Общие способы получения соединения 2 Соединение 1 получают способами, подробно описанными в публикации РСТ WO 01/14330, которая тем самым полностью включена в данное описание посредством ссылки. Другой аспект настоящего изобретения относится к способу получения соединения 2 включающему стадии получения соединения 1 объединения соединения 1 с глюкуроновой кислотой в подходящем растворителе; и необязательно стадию выделения соединения 2. Подходящий растворитель может сделать растворимым один компонент реакционной смеси и более, или, альтернативно, подходящий растворитель может облегчить взбалтывание суспензии одного компонента реакционной смеси и более. Примерами подходящих растворителей, применимых по настоящему изобретении, служит протонный растворитель, полярный апротонный растворитель или их смеси. В определенных вариантах осуществления подходящие растворители включают простой эфир,сложный эфир, спирт, кетон или их смесь. В определенных вариантах осуществления подходящим растворителем является метанол, этанол, изопропанол или ацетон, где указанный растворитель безводный или находится в комбинации с водой или гептаном. В других вариантах осуществления подходящие растворители включают тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метилтрет-бутиловый простой эфир, трет-бутанол, н-бутанол и ацетонитрил. В другом варианте осуществления подходящий растворитель представляет собой безводный этанол. Другой вариант осуществления настоящего изобретения относится к способу получения соедине-9 014942 ния 2 включающему стадии объединения соединения 1 с подходящим растворителем и необязательно нагревания, чтобы получить его раствор; добавления глюкуроновой кислоты к указанному раствору; и необязательно стадию выделения соединения 2. Как описано для общего случая выше, соединение 1 растворяют в подходящем растворителе, необязательно при нагревании. В определенных вариантах осуществления соединение 1 растворяют при температуре приблизительно 60 С. В других вариантах осуществления соединение 1 растворяют при температуре приблизительно 40 С. В других вариантах осуществления соединение 1 растворяют при температуре от приблизительно 40 до приблизительно 60 С. В других вариантах осуществления соединение 1 растворяют при температуре кипения растворителя. В других вариантах осуществления соединение 1 растворяют без нагревания. В определенных вариантах осуществления раствор соединения 1 фильтруют перед добавлением глюкуроновой кислоты. В других вариантах осуществления раствор соединения 1 не фильтруют до добавления глюкуроновой кислоты. В определенных вариантах осуществления, в которых раствор соединения 1 был нагрет до любой температуры от приблизительно 40 до приблизительно 60 С, раствор затем охлаждают до любой более низкой температуры от приблизительно 20 до приблизительно 40 С перед добавлением глюкуроновой кислоты. В определенных вариантах осуществления, в которых раствор соединения 1 был нагрет до любой температуры от приблизительно 40 до приблизительно 60 С, раствор затем не охлаждают до более низкой температуры перед добавлением глюкуроновой кислоты. В определенных вариантах осуществления к соединению 1 добавляют приблизительно 1 эквивалент глюкуроновой кислоты, чтобы получить соединение 2. В других вариантах осуществления к соединению 1 добавляют менее 1 эквивалента глюкуроновой кислоты, чтобы получить соединение 2. В других вариантах осуществления к соединению 1 добавляют более 1 эквивалента глюкуроновой кислоты, чтобы получить соединение 2. В других вариантах осуществления к соединению 1 добавляют от приблизительно 1,0 до приблизительно 1,2 эквивалента глюкуроновой кислоты, чтобы получить соединение 2. В других вариантах осуществления к соединению 1 добавляют от приблизительно 0,9 до приблизительно 1,1 эквивалента глюкуроновой кислоты, чтобы получить соединение 2. В других вариантах осуществления к соединению 1 добавляют от приблизительно 0,99 до приблизительно 1,01 эквивалента глюкуроновой кислоты, чтобы получить соединение 2. Следует понимать, что глюкуроновая кислота может быть добавлена к смеси соединения 1 и подходящего растворителя в любой подходящей форме. Например, глюкуроновая кислота может быть добавлена в форме твердого вещества или в виде раствора или суспензии в подходящем растворителе. Подходящий растворитель может быть тем же самым подходящим растворителем, что и растворитель, объединенный с соединением 1, или может быть другим растворителем. Согласно одному варианту осуществления глюкуроновую кислоту добавляют в форме твердого вещества. В определенных вариантах осуществления глюкуроновую кислоту объединяют с подходящим растворителем перед добавлением к соединению 1. Согласно другому варианту осуществления глюкуроновую кислоту добавляют в виде раствора в подходящем растворителе. В других вариантах осуществления подходящий растворитель, в котором растворяют глюкуроновую кислоту, является полярным протонным или полярным апротонным растворителем. Такие растворители включают воду, спирты, эфиры и кетоны. Примеры таких растворителей включают воду, метанол, этанол, изопропанол, ацетон, тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метил-трет-бутиловый простой эфир, трет-бутанол, н-бутанол и ацетонитрил.- 10014942 В определенных вариантах осуществления подходящий растворитель выбран из перечисленных выше и является безводным. Согласно одному варианту осуществления глюкуроновую кислоту растворяют в воде. В определенных вариантах осуществления полученную в результате смесь, содержащую соединение 2, охлаждают. В определенных вариантах осуществления, в которых смесь, содержащая соединение 2, нагрета выше приблизительно 20 С, раствор охлаждают до приблизительно 20 С. В других вариантах осуществления смесь, содержащую соединение 2, охлаждают ниже 20 С. В определенных вариантах осуществления соединение 2 осаждается из смеси. В другом варианте осуществления соединение 2 кристаллизуется из смеси. В других вариантах осуществления соединение 2 кристаллизуется из раствора после его затравливания (то есть добавления к раствору кристаллов соединения 2). Кристаллическое или аморфное соединение 2 может осаждаться из реакционной смеси, или его могут получать удалением части или всего растворителя такими способами, как испарение, перегонка,фильтрация (например, нанофильтрация, ультрафильтрация), обратный осмос, абсорбция и реакция, путем добавления антирастворителя, такого как гептан, путем охлаждения или различными комбинациями этих способов. Как описано для общего случая выше, соединение 2 необязательно выделяют. Следует понимать,что соединение 2 может быть выделено любыми подходящими физическими методами, известными среднему специалисту в данной области техники. В определенных вариантах осуществления осажденное твердое соединение 2 отделяют от супернатанта фильтрацией. В других вариантах осуществления осажденное твердое соединение 2 отделяют от супернатанта декантированием супернатанта. В определенных вариантах осуществления осажденное твердое вещество соединения 2 отделяют от супернатанта фильтрацией. В определенных вариантах осуществления выделенное соединение 2 сушат на воздухе. В других вариантах осуществления выделенное соединение 2 сушат под пониженным давлением, необязательно при повышенной температуре. Другой вариант осуществления настоящего изобретения относится к способу получения соединения 2 включающему стадии объединения соединения 1 с подходящим растворителем и нагревания, чтобы получить его раствор; добавления водного раствора глюкуроновой кислоты к указанному раствору и необязательно выделения соединения 2. В определенных вариантах осуществления способ получения соединения 2 дополнительно включает стадию перегонки реакционной смеси. Согласно другому аспекту настоящего изобретения реакционную смесь перегоняют во время добавления дополнительного растворителя, такого, что содержание воды снижается. В других вариантах осуществления способ дополнительно включает стадию охлаждения полученной в результате взвеси, содержащей соединения 2, и выделения соединения 2 подходящими физическими методами. В одном варианте осуществления молярное отношение глюкуроновой кислоты к полученному соединению 1 составляет от приблизительно 0,5 до приблизительно 1,0. В других вариантах осуществления отношение глюкуроновой кислоты к полученному соединению 1 составляет от приблизительно 0,8 до приблизительно 2,0. В определенных вариантах осуществления отношение составляет от приблизитель- 11014942 но 0,9 до приблизительно 1,2. В других вариантах осуществления отношение составляет от приблизительно 0,94 до приблизительно 1,06. В других вариантах осуществления отношение составляет от приблизительно 0,94 до приблизительно 0,95. Применение соединений и фармацевтически приемлемых композиций Как отмечалось выше, настоящее изобретение относится к соединению 2, которое применимо в качестве модулятора D-рецепторов, 5 НТ-рецепторов, модулятора обратного захвата 5 НТ и синтеза простагландинов и демонстрирует полезность в клинически релевантных моделях психозов, депрессии,стресса/тревоги и болезни Паркинсона. В определенных вариантах осуществления настоящее соединение применимо в качестве модулятора одного и более подтипа D2-рецепторов, обратного захвата 5 НТ или синтеза простагландинов. В других вариантах осуществления настоящее соединение применимо для лечения психозов, депрессии, стресса/тревоги и болезни Паркинсона. Соответственно, другой аспект настоящего изобретения относится к фармацевтически приемлемым композициям, где эти композиции содержат соединение 2 и необязательно фармацевтически приемлемый носитель, вспомогательное вещество или растворитель. В определенных вариантах осуществления эти композиции необязательно дополнительно содержат одно дополнительное терапевтическое средство и более. Как отмечалось выше, фармацевтически приемлемые композиции по настоящему изобретению дополнительно содержат фармацевтически приемлемый носитель, вспомогательное вещество или растворитель, который, как используется в настоящем описании, включает любой и все растворители, разбавители или другие жидкие носители, средства, облегчающие получение дисперсии или суспензии, поверхностно-активные вещества, изотонические средства, загустители или эмульгаторы, консерванты, твердые связующие, смазывающие вещества и тому подобное, которые подходят для конкретной желаемой лекарственной формы. Различные носители, используемые в приготовлении фармацевтически приемлемых композиций, и известные методы их получения раскрыты в Remington's Pharmaceutical Sciences, SixteenthEdition, E.W. Martin (Mack Publishing Co., Easton, Pa., 1980). За исключением случаев, когда любая обычная среда носителя несовместима с солью по изобретению, например из-за возникновения нежелательного биологического эффекта или иного вредного взаимодействия с любым другим компонентом(ами) фармацевтически приемлемой композиции, считается, что ее применение включено в объем настоящего изобретения. Некоторые примеры веществ, которые могут служить фармацевтически приемлемыми носителями, включают, но не ограничиваются этим, ионообменные вещества, оксид алюминия, стеарат алюминия, лецитин, белки сыворотки, например сывороточный альбумин человека, буферные вещества,например фосфаты, глицин, сорбиновую кислоту или сорбат калия, частичные смеси глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как сульфат протамина, гидроксифосфат натрия, гидроксифосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния,трисиликат магния, поливинилпирролидон, полиакрилаты, воски, блок-сополимеры полиэтиленаполиоксопропилена, ланолин, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный и картофельный крахмал; целлюлозу и ее производные, такие как натрийкарбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; измельченный в порошок трагакант; солод; желатин; тальк; наполнители, такие как масло какао и воски для изготовления суппозиториев; масла, такие как масло арахиса, хлопковое масло; масло сафлора; кунжутное масло; оливковое масло; кукурузное масло и масло сои; гликоли, такие как пропиленгликоль или полиэтиленгликоль; сложные эфиры,такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический раствор хлорида натрия; раствор Рингера; этиловый спирт и растворы фосфатных буферов, а также другие нетоксичные совместимые смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, разделительные средства, покровные вещества, подсластители, вкусовые и ароматизирующие добавки, консерванты и антиоксиданты также могут присутствовать в композиции на усмотрение разработчика рецептур. Еще один аспект относится к способу лечения или уменьшения тяжести расстройства, связанному с модулированием D-рецепторов, 5 НТ-рецепторов, модулированием обратного захвата 5 НТ и синтеза простагландинов, и/или для лечения или уменьшения тяжести психозов, депрессии, стресса/тревоги и/или болезни Паркинсона, предусматривающему введение эффективного количества соединения 2 или его фармацевтически приемлемой композиции субъекту, которому этому требуется. В определенных вариантах осуществления настоящего изобретения эффективное количество соединения или фармацевтически приемлемой композиции представляет собой такое количество, которое эффективно для лечения или уменьшения тяжести расстройства, связанного с модулированием D-рецепторов, 5 НТ-рецепторов, модулированием обратного захвата 5 НТ и синтеза простагландинов, и/или для лечения или уменьшения тяжести психозов, депрессии, стресса/тревоги и/или болезни Паркинсона. В других вариантах осуществления эффективное количество соединения представляет собой количество, которое действует как модулятор одного D-рецептора и более, 5 НТ-рецепторов, обратного захвата 5 НТ и синтез простагландинов. Эффективное количество соединения может достичь желаемого терапевтического и/или профилактического эффекта, например, количество, которое приводит к предупреждению или ослаблению симптомов,- 12014942 связанных с заболеванием, связанным с модулированием одного D-рецептора и более, рецептора 5 НТ,обратного захвата 5 НТ и синтеза простагландинов и/или с психозом, депрессией, стрессом/тревогой и/или болезнью Паркинсона. Согласно способу по настоящему изобретению соединение и композиции могут вводиться с использованием любого количества и любого пути введения, эффективного для лечения или уменьшении тяжести расстройства, связанного с одним D-рецептором и более, 5 НТ-рецепторами, обратным захватом 5 НТ и синтезом простагландинов, и/или для лечения или уменьшения тяжести психозов, депрессии,стресса/тревоги и/или болезни Паркинсона. Точное требуемое количество у разных субъектов будет меняться в зависимости от биологического вида, возраста и общего состояния субъекта, тяжести инфекции,конкретного средства, его способа введения и тому подобного. Из соли по изобретению предпочтительно готовят лекарственную форму, разделенную на дозы (например, таблетка, капсула или ампула) для простоты введения и единообразия дозировки. Выражение лекарственная форма, разделенная на дозы, как используется в настоящем описании, относится к физически дискретной единице средства, подходящей для пациента, который будет подвергаться лечению. Однако необходимо понимать, что общее суточное применение соли и композиций по настоящему изобретению будет определяться лечащим врачом согласно обоснованному медицинскому суждению. Конкретный эффективный уровень дозы для любого конкретного пациента или организма будет зависеть от ряда факторов, включая расстройство, которое подвергается лечению, и его тяжесть; активность конкретного используемого соединения; конкретную используемую композицию; возраст, массу тела, общее состояние здоровья, пол и питание пациента; время введения, путь введения и скорость экскреции конкретного используемого соединения; продолжительность лечения; лекарственные средства, используемые в комбинации или одновременно с конкретным используемым соединением, и тому подобные факторы, известные в области медицины. Термин пациент, как используется в настоящем описании, означает животное, предпочтительно млекопитающее, и наиболее предпочтительно человека. Фармацевтически приемлемые композиции по настоящему изобретению могут вводиться людям и другим животным перорально, через нос, ректально, парентерально, интерцистернально, во влагалище,интраперитонально, местно (посредством порошков, мазей или капель), буккально или тому подобными путями, в зависимости от тяжести инфекции, которая подвергается лечению. В определенных вариантах осуществления соль по изобретению может вводиться перорально или парентерально в дозе от приблизительно 0,01 до приблизительно 50 мг/кг и предпочтительно от приблизительно 1 до приблизительно 25 мг/кг массы тела субъекта в сутки, один раз в день или более, чтобы получить желаемый терапевтический эффект. Жидкие лекарственные формы для перорального или назального введения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, аэрозоли, гели, сиропы и эликсиры,но не ограничиваются этим. Помимо активной соли, жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области техники, например воду или другие растворители, солюбилизирующие компоненты и эмульгаторы, например этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3 бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное масло, масло зародышей пшеницы, оливковое, касторовое масло и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры сорбитана и жирных кислот и их смеси. Помимо инертных разбавителей пероральные композиции также могут содержать вспомогательные вещества,например увлажнители, эмульгаторы и суспендирующие средства, подсластители, вкусовые и ароматические добавки. Аэрозольные составы типично содержат раствор или тонкую суспензию активного вещества в физиологически приемлемом водном или неводном растворителе и обычно присутствуют в количестве одной или многих доз в стерильной форме в герметичном контейнере, который может иметь форму картриджа или заправки для использования в аэрозольном аппарате. Альтернативно герметичный контейнер может быть единичным дозатором, таким как назальный ингалятор с одной дозой, или аэрозольным дозатором с дозирующим клапаном, предназначенным для ликвидации после того, как содержимое контейнера будет исчерпано. Если лекарственная форма содержит распылитель аэрозоля, она будет содержать фармацевтически приемлемый газ-вытеснитель. Аэрозольные лекарственные формы также могут принимать форму насоса-распылителя. Препараты для инъекций, например стерильные водные или масляные суспензии для инъекций, могут быть приготовлены согласно известному уровню техники, используя подходящие увлажнители и суспендирующие средства. Стерильный препарат для инъекций также может быть стерильным раствором для инъекций, суспензией или эмульсией в нетоксичном парентерально приемлемом разбавителе или растворителе, например раствором в 1,3-бутандиоле. Среди приемлемых разбавителей и растворителей, которые могут использоваться, находятся вода, раствор Рингера, U.S.Р. и изотонический раствор хлорида натрия. Кроме того, в качесте растворителя или среды для суспензии традиционно используются стерильные нелетучие масла. Для этой цели может использоваться любое мягкое нелетучее масло, включая синтетические моно- и диглицериды. Кроме того, для получения препаратов для инъекций исполь- 13014942 зуются жирные кислоты, такие как олеиновая кислота. Составы для инъекций могут стерилизоваться, например, посредством фильтрации через фильтр,задерживающий бактерии, или путем включения стерилизующих веществ в стерильные твердые композиции, которые перед применением могут растворяться или диспергироваться в стерилизованной воде или другой стерильной инъекционной среде. Выгодно, чтобы соединение 2, которое описано в настоящем описании, имело повышенную растворимость в воде. Соответственно, настоящее соединение применимо для внутрисосудистого и внутримышечного введения. Не желая быть связанными какой-либо конкретной теорией, считается, что повышенная растворимость соединения 2 позволила бы уменьшить объем инъекции, что ослабило бы боль и дискомфорт для пациента. Соответственно, настоящее изобретение также относится к составу для инъекций для внутрисосудистого или внутримышечного введения. Чтобы продлить действие соединения по настоящему изобретению, часто желательно замедлить всасывание соединения из места подкожной или внутримышечной инъекции. Этого можно достичь при помощи жидкой суспензии кристаллического или аморфного вещества со слабой растворимостью в воде. Скорость всасывания соединения к тому же зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера и формы кристаллов. Альтернативно отсроченное всасывание парентерально введенной формы соединения достигается путем растворения или суспендирования соединения в масляном растворителе. Инъекционные депо-формы получают путем создания микроинкапсулированных матриц соединения в поддающихся биологическому разложению полимерах, таких как полилактидполигликолид. Скоростью высвобождения соединения можно управлять в зависимости от соотношения соединения и полимера и природы конкретного используемого полимера. Примеры других поддающихся биологическому разложению полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъекционные депо-составы также получают путем заключения соединения в липосомы или микроэмульсии, которые совместимы с тканями организма. Типичные парентеральные композиции состоят из раствора или суспензии соединения или физиологически приемлемой соли в стерильном водном или неводном носителе, или парентерально приемлемом масле, например полиэтиленгликоле, поливинилпирролидоне, лецитине, арахисовом масле или кунжутном масле. Альтернативно раствор может быть лиофилизирован и затем воссоздан с помощью подходящего растворителя непосредственно перед введением. Удобно, если композиции для ректального или влагалищного введения находятся в форме суппозиториев, пессариев, влагалищных таблеток, пен или клизм. Композиции для ректального или влагалищного введения предпочтительно представляют собой суппозитории, которые можно получить смешиванием соли по настоящему изобретению с подходящими нераздражающими наполнителями или носителями,такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые при комнатной температуре являются твердыми веществами, а при температуре тела - жидкостями, и поэтому плавятся в полости прямой кишки или влагалища и высвобождают активное соединение. Твердые лекарственные формы для перорального приема включают капсулы, таблетки, пилюли,порошки и гранулы. В таких твердых лекарственных формах активное соединение смешано по меньшей мере с одним инертным фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или гидроксифосфат кальция и/или а) наполнителями, такими как крахмал, лактоза, сахароза,глюкоза, маннит и кремниевая кислота, b) связующими, такими как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и камедь акации, с) увлажнителями, такими как глицерин,d) разрыхлителями, такими как как агар-агар, карбонат кальция, картофельный крахмал или крахмал тапиоки, альгиновая кислота, определенные силикаты и карбонат натрия, е) средствами, задерживающими растворение, такими как парафин, f) ускорителями всасывания, такими как четвертичные соли аммония,д) смачивателями, такими как цетиловый спирт и моностеарат глицерина, h) абсорбентами, такими как каолин и бентонит и i) смазывающими веществами, такими как тальк, стеарат кальция, стеарат магния,твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль лекарственная форма также может содержать буферные вещества. Композиции, подходящие для буккального или подъязычного применения, включают таблетки,таблетки для рассасывания и пастилки, в которых активный ингредиент смешан с носителем, таким как сахар и аравийская камедь, трагакант или желатин и глицерин. Твердые композиции подобного типа также могут применяться в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких наполнителей, как лактоза или молочный сахар,а также высокомолекулярные полиэтиленгликоли и тому подобного. На твердые лекарственные формы в виде таблеток, драже, капсул, пилюль и гранул можно нанести покрытия и оболочки, такие как кишечнорастворимые покрытия и другие покрытия, известные в области технологии лекарственных форм. Они могут необязательно содержать замутняющие компоненты, а также могут состоять из композиции, которая высвобождает активный ингредиент(ы) исключительно или предпочтительно в определенной части кишечника, необязательно отсроченно. Примеры композиций, которые могут использоваться, включают полимерные вещества и воски. Твердые композиции подобного типа также могут использоваться в каче- 14014942 стве наполнителей в мягких и твердых желатиновых капсулах с использованием таких наполнителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и тому подобного. Соединения 2 также могут находиться в микроинкапсулированной форме с одним наполнителем и более, как отмечено выше. На твердые лекарственные формы в виде таблеток, драже, капсул, пилюль и гранул можно нанести покрытия и оболочки, такие как кишечнорастворимые покрытия и другие покрытия, известные в области технологии лекарственных форм. В таких твердых лекарственных формах соединение 2 может быть смешано по меньшей мере с одним инертным разбавителем, таким как сахароза,лактоза или крахмал. Такие лекарственные формы также могут содержать, в соответствии с обычной практикой, дополнительные вещества, отличающиеся от инертных разбавителей, например смазывающие вещества для таблетирования и другие вещества, облегчающие таблетирование, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль лекарственные формы также могут содержать буферные вещества. Они могут необязательно содержать замутняющие компоненты, а также могут состоять из композиции, которая высвобождает активный ингредиент(ы) исключительно или предпочтительно в определенной части кишечника, необязательно отсроченно. Примеры композиций, которые могут использоваться, включают полимерные вещества и воски. Композиции для перорального приема могут быть предназначены для защиты активного ингредиента от разрушения в тот период, когда он проходит через пищеварительный тракт, например с помощью внешнего покрытия, нанесенного на таблетку или капсулу. В другом варианте осуществления соединение 2 находится в композиции с пролонгированным (или отсроченным или замедленным) высвобождением. Эта композиция с отсроченным высвобождением содержит соединение 2 в комбинации с компонентом замедленного высвобождения. Эта композиция делает возможным прицельное высвобождение соединения 2 в нижних отделах ЖКТ; например в тонкой кишке, толстой кишке, ободочной и/или прямой кишке. В определенных вариантах осуществления композиция с замедленным высвобождением, содержащая соединения 2, кроме того, содержит кишечнорастворимое или зависимое от рН покрытие, такое как фталаты ацетата целлюлозы и другие фталаты (например, фталат поливинилацетата, метакрилаты (Eudragits. Альтернативно композиция с замедленным высвобождением обеспечивает контролируемое высвобождение в тонкой и/или ободочной кишке благодаря чувствительным к рН покрытию из метакрилата,чувствительному к рН полимерным микросферам или полимерам, которые разрушаются за счет гидролиза. Композиция с замедленным высвобождением может быть получена с использованием гидрофобных или гелеобразующих наполнителей или покрытий. Кроме того, доставка в ободочную кишку может быть обеспечена с помощью покрытий, которые расщепляются бактериальными ферментами, таких как амилоза или пектин, с помощью зависимых от рН полимеров, пробок из гидрогеля, набухающих со временем (Pulsincap), покрытий из гидрогеля с зависимостью от времени и/или акриловой кислоты, связанной с азоароматическими связями покрытий. В определенных вариантах осуществления композиции с замедленным высвобождением по настоящему изобретению содержат гипромеллозу, микрокристаллическую целлюлозу и смазывающее вещество. Из смеси соединения 2, гипромеллозы и микрокристаллической целлюлозы может быть приготовлена таблетка или капсула для перорального приема. В определенных вариантах осуществления смесь гранулируют и прессуют в таблетки. В других вариантах осуществления композиции с замедленным высвобождением по настоящему изобретению находятся в виде состава, состоящего из множества частиц. Смесь соединения 2 и подходящего полимера гранулируют, чтобы получить шарики, на которые наносят покрытие. В определенных вариантах осуществления шарики имеют защитную оболочку, состоящую из нефункционального покрытия. В других вариантах осуществления шарики сначала покрыты защитной оболочкой из нефункционального покрытия, а затем - функциональным покрытием. Как используется в настоящем описании, термин нефункциональное покрытие означает покрытие, которое не влияет на скорость высвобождения лекарственного средства. Примеры нефункционального покрытия включают гидроксипропилцеллюлозу, гипромеллозу или поливиниловый спирт. В определенных вариантах осуществления нефункциональное покрытие представляет собой Opadry Clear,который содержит гидроксипропилметилцеллюлозу и полиэтиленгликоль. Как используется в настоящем описании, термин функциональное покрытие означает покрытие,которое влияет на скорость высвобождения лекарственного средства из лекарственной формы. Примеры функционального покрытия включают этилцеллюлозу и производные полиметакрилата (Eudragits). Соответственно, другой вариант осуществления относится к составу, состоящему из множества частиц и содержащему ядро шарика, содержащее соединение 2, нефункциональное изолирующее покрытие и функциональное изолирующее покрытие. Лекарственные формы для местного или чрескожного введения соединения по настоящему изобретению включают мази, пасты, кремы, лосьоны, гели, порошки, растворы, аэрозоли, средства для ингаляции или пластыри. Активный компонент в стерильных условиях смешивают с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферами, которые могут требоваться.- 15014942 Офтальмический состав, ушные капли и глазные капли также рассматриваются как входящие в объем настоящего изобретения. Кроме того, в настоящем изобретении рассматривается применение чрескожных пластырей, которые обладают дополнительным преимуществомобеспечивают контролируемую доставку соединения в организм. Такие лекарственные формы могут быть получены путем растворения или при распределении соединения в соответствующей среде. Средства, усиливающие всасывание, также могут использоваться, чтобы увеличить проникновение соединения через кожу. Скоростью можно управлять, либо предусмотрев мембрану, контролирующую скорость, либо распределив соединение в полимерной матрице или геле. В зависимости от способа введения композиции могут содержать от 0,1 до 99% (мас./мас.), предпочтительно 0,1-60% (мас./мас.), более предпочтительно 0,2-20 мас.% и наиболее предпочтительно 0,2512% (мас./мас.) соединения 2. Как описано для общего случая выше, соль по настоящему изобретению применима в качестве модуляторов одного D-рецептора и более, 5 НТ-рецепторов, модуляторов обратного захвата 5 НТ и синтеза простагландинов, и, следовательно, изобретение дополнительно относится к способу лечения (например,паллиативного, лечебного, профилактического) или уменьшения тяжести заболевания или расстройства,связанного с модулированием одного D-рецептора и более, 5 НТ-рецепторов, модулированием обратного захвата 5 НТ и синтеза простагландинов. В одном варианте осуществления соединение 2 является модулятором одного D-рецептора и более,5 НТ-рецепторов, модуляторов обратного захвата 5 НТ и синтеза простагландинов, и, таким образом, не желая быть связанным какой-либо конкретной теорией, настоящее соединение и композиции особенно применимы для лечения или уменьшения тяжести заболевания, состояния или расстройства, при которых модулирование одного D-рецептора и более, 5 НТ-рецепторов, модулирование обратного захвата 5 НТ и синтеза простагландинов участвует в развитии заболевания, состояния или расстройства. Если модулирование одного D-рецептора и более, 5 НТ-рецепторов, модуляторов обратного захвата 5 НТ и синтеза простагландинов участвует в развитии конкретного заболевания, состояния или расстройства, то заболевание, состояние или расстройство может также называться заболеванием, опосредованным рецептором D, рецептором 5 НТ, обратным захватом 5 НТ или синтезом простагландинов или симптомом заболевания. В определенных вариантах осуществления соли и композиции по настоящему изобретению обеспечивают способ лечения или уменьшения тяжести одного расстройства и более, включая болезнь Паркинсона, психозы (например, шизофрению, манию, психотическую депрессию и биполярное расстройство),депрессию, стресс/тревогу, болезнь Альцгеймера, болезнь Гентингтона, паническое расстройство, обсессивно-компульсивное расстройство, расстройства пищевого поведения, наркоманию, социофобии, агрессивность или беспокойство, мигрень, склеродермию и феномен Рейно, рвоту, желудочно-кишечные расстройства, связанные с регуляцией перистальтики, синдром беспокойных ног и нарушения секреции пролактина, возникшие в результате опухолей гипофиза, но не ограничиваются этим, где указанный способ предусматривает введение пациенту соединения 2 или его композиции. Также следует понимать, что соль и фармацевтически приемлемые композиции по настоящему изобретению могут использоваться в комбинированном лечении, то есть соединение 2 и его композиции могут вводиться одновременно, перед или после одного и более лекарственного средства или медицинских процедур. Конкретная комбинация методов лечения (лекарственных средств или процедур) для использования в комбинированном режиме будет учитывать совместимость желаемых лекарственных средств и/или процедур и желаемый терапевтический эффект, который будет достигнут. Также следует понимать, что используемые методы лечения могут обеспечить желаемый эффект для одного и того же расстройства (например, соединение по изобретению может вводиться одновременно с другим средством, используемым для лечения того же расстройства) или они могут обеспечивать различные эффекты(например, контроль над любыми побочными эффектами). Как используется в данном описании, дополнительные терапевтические средства, которые обычно вводятся для лечения или профилактики конкретного заболевания, или условия, называются соответствующими заболеванию или состоянию, которое подвергается лечению. Количество дополнительного терапевтического средства, присутствующего в композициях этого изобретения, не будет превышать количество, которое обычно вводилось бы в композициях, содержащих это терапевтическое средство в качестве единственного активного вещества. В определенных вариантах осуществления количество дополнительного терапевтического средства в раскрытых в настоящий момент композициях будет колебаться приблизительно от 50 до 100% количества, которое обычно присутствует в композициях, содержащих это средство в качестве единственного активного вещества. Другой аспект по изобретению относится к модулированию D-рецепторов, 5 НТ-рецепторов, модулированию обратного захвата 5 НТ и активности синтеза простагландинов в биологической пробе или у пациента, причем данный способ предусматривает введение пациенту соединения 2 или его композиции или контакт биологической пробой с соединением 2 или его композицией. Термин биологическая проба, как используется в настоящем описании, включает культуры клеток или их экстракты; биопсийный- 16014942 материал, полученный от млекопитающего, или экстракты биопсийного материала; и кровь, слюну, мочу, кал, сперму, слезы или другие жидкости организма или их экстракты, но не ограничивается этим. Модулирование D-рецепторов, 5 НТ-рецепторов, модулирование обратного захвата 5 НТ и активности синтеза простагландинов в биологической пробе применимы для ряда целей, которые известны специалисту в данной области техники. Примеры таких целей включают биологические анализы, но не ограничены этим. Количество соединения 2, эффективного для лечения расстройства, как изложено выше, зависит от природы и тяжести расстройства, подвергающегося лечению, и массы пациента, которому требуется лечение. Однако разовая доза для взрослого массой 70 кг обычно будет содержать 0,01-100 мг, например 0,1-50 мг, предпочтительно от 0-5 до 16 мг соединения по изобретению в сутки. Разовые дозы могут вводиться один раз в сутки и более, например 2, 3 или 4 раза в сутки, обычно 1-3 раза в сутки, более предпочтительно 1 или 2 раза в сутки. Следует понимать, что вышеприведенные диапазоны доз регулируют введение соединения 2 взрослому. Количество, которое будет вводиться, например, ребенку, может быть определено медицинским работником или специалистом в данной области и может быть ниже или равняться дозе для взрослого. Разовая доза предпочтительно предоставляется в форме капсулы или таблетки. Все особенности каждого из аспектов изобретения относятся ко всем другим аспектам с учетом необходимых изменений. Для более полного понимания изобретения, описанного в настоящем описании, приведены следующие примеры. Следует понимать, что эти примеры приведены исключительно для иллюстративных целей и не должны рассматриваться как ограничивающие это изобретение каким-либо образом. Примеры Общие процедуры Порошковые дифракционные рентгенограммы были получены на Rigaku Miniflex Diffraction System(Rigaku MSG Inc.). Пробы порошка помещали на полированный кремниевый держатель с нулевым фоном. В качестве источника рентгеновского излучения использовали нормальнофокусную медную рентгеновскую трубку на 0,45 кВт, оборудованную Ni K фильтром, сканирующую со скоростью 2/мин угол 2-тета от 3,00 до 40,00. Данные обрабатывали с помощью программного обеспечения Jade 6,0. Спектры протонного ядерно-магнитного резонанса (1 Н ЯМР) получали на Bruker model AvanceDRX-500 МГц ЯМР-спектрометре, снабженном 5-миллиметровым QNP-зондом. Около 5-25 мг каждого соединения растворяли в 0,6 мл ДМСО-d6 (99,9% D), содержащего 0,05% TMS в качестве внутреннего стандарта. Спектры 1 Н ЯМР записывали при 500,133 МГц, используя 30 импульсы с задержкой импульса 20 с, 32k экспериментальные точки, 64 скана. Экспоненциальное окно функции с 0,3 Гц расширением линий применяли к 16k экспериментальным точкам, чтобы обработать данные без нулевого заполнения,и TMS принимали за 0,00 м.д. Количественный 13 С ЯМР-спектр получали при 125,7 МГц, используя инвертированное подавление взаимодействий, 30 импульс и задержку 8 с. Данные DSC получали на дифференциальном сканирующем калориметре ТА Q1000. Прибор нагревал пробу на 40-200 С со скоростью 10/мин в потоке азота 50 мл/мин. Пример 1. Получение соединения 2 (форма I) Соединение 1 (500 мг) суспендировали в 20 мл безводного этанола и нагревали до 60 С, чтобы получить прозрачный раствор. Раствор фильтровали через фильтр с диаметром пор 0,45 мкм и охлаждали до 40 С. К этому раствору добавляли 275 мг (1,2 экв.) глюкуроновой кислоты. Получали жидкую белую взвесь. Взвесь охлаждали до 20 С и перемешивали магнитной мешалкой в течение 16 ч. Взвесь фильтровали и полученную в результате твердую фазу высушивали на воздухе при комнатной температуре и анализировали с помощью рентгеновской дифракции (см. фиг. 1) и оптической микроскопии; было обнаружено, что это кристаллическое соединение 2. На фиг. 2 изображен 1 Н ЯМР-спектр, полученный для соединения 2. На фиг. 3 изображен 13 С ЯМР-спектр, полученный для соединения 2, и на фиг. 4 изображен 1 Н ЯМР-спектр, полученный для соединения 1. Пример 2. Получение соединения 2 (форма I) с помощью реакционной перегонки из этанола/водыD-глюкуроновую кислоту (4,6 г) добавляли к 25 мл воды и растворяли при комнатной температуре. Соединение 1 (10 г) добавляли в 320 мл безводного этанола и нагревали до 50-70 С, чтобы получить прозрачный раствор. Подготовленный водный раствор глюкуроновой кислоты (1 экв.) добавляли к раствору свободного основания и раствору этанола. Раствор оставался прозрачным; затем его охлаждали естественным путем до комнатной температуры и перемешивали в течение 16 ч. Полученный в результате раствор азеотропно перегонялся при 78 С. Примерно 400 мл безводного этанола добавляли обратно в раствор, 200 мл каждые 0,5 ч во время перегонки. Во время перегонки осаждалось белое твердое вещество. Перегонку останавливали после перегонки 600 мл раствора и оставляли 150 мл белой взвеси. Взвесь фильтровали и сушили в течение ночи при 50 С под вакуумом, что давало соединение 2. Конечный продукт (12 г, выход 8 4%) был кристаллическим, что было показано порошковой рентгеновской дифракцией (фиг. 5) и ДСК (фиг. 6). Ниже, в табл. 9 приведены пики рентгеновской диффракции, наблюдаемые для формы I соединения 2, где каждое значение представляет собой угол 2-тета в градусах.- 17014942 Таблица 9. Наблюдаемые пики рентгеновской дифракции для соединения 2 (форма I) Пример 3. Получение соединения 2 (форма I) гетерогенной реакцией в этаноле Соединение 1 (500 мг) растворяли в 70 мл безводного этанола при комнатной температуре. 230 мг глюкуроновой кислоты (1,0 экв.) добавляли к раствору свободного основания, чтобы получить взвесь. Взвесь перемешивали в течение 16 ч при комнатной температуре, а затем фильтровали. Твердую фазу сушили под вакуумом при 50 С, чтобы получить соединение 2. Конечный продукт (235 мг, выход 32,2%) был характеризован рентгеновской дифракцией, ДСК и ЯМР-спектроскопией. Пример 4. Получение соединения 2 (форма I) гетерогенной реакцией при 60 С в этаноле Соединение 1 (400 мг) суспендировали в 13 мл безводного этанола и нагревали до 60 С, чтобы получить прозрачный раствор. Раствор фильтровали через фильтр с размером пор 0,45 мкм и охлаждали до 40 С. К этому раствору добавляли 202 мг (1,1 экв.) глюкуроновой кислоты. Получали жидкую белую взвесь. Взвесь охлаждали до 20 С и перемешивали магнитной мешалкой в течение 16 ч. Взвесь фильтровали и полученную в результате твердую фазу (22 4 мг, 38%) сушили при 50 С под вакуумом. Пример 5. Общий способ получения соединения 2 (форма I) Добавить 25,3 кг этанола к 1 кг соединения 1 и нагреть смесь до 60 С. Добавить 2 кг воды к 0,46 кг глюкуроновой кислоты; перемешивать до растворения всей кислоты в воде. Добавить раствор глюкуроновой кислоты к раствору свободного основания. Проверить раствор на прозрачность. Охладить раствор до 50 С. Профильтровать реакционный раствор при 50 С через фильтр с порами 0,5 мкм. Охладить реакционный раствор до 24 С и медленно перемешивать в течение 16 ч. Нагреть реакционный раствор до 78 С, чтобы начать перегонку. Перегнать 15,8 кг раствора, добавить 15,8 кг этанола, перегнать 15,8 кг раствора, добавить 15,8 кг этанола и, наконец, перегнать 20 л раствора (перегнали 60 л, добавили 40 л,объем оставшегося раствора 15,5 л). Охладить реакционную смесь до 20 С в течение 1 ч и выдерживать реакционную смесь при 20 С в течение 1 ч. Профильтровать маточный раствор и осадок на фильтре дважды промыть 4,0 кг (общее количество 8 кг) этанола. Сушить осадок на фильтре при 50 С под вакуумом в течение 12 ч. Пример 6. Альтернативный способ получения соединения 2 (форма I) из ацетонитрила В другом способе получения формы I аморфное соединение 2 суспендировали в ацетонитриле при комнатной температуре в течение 3 дней. Аморфное твердое вещество превратилось в чистую кристаллическую форму соединения 2 (форму I). Пример 7. Получение аморфного соединения 2 Способ А: 0,92 г D-глюкуроновой кислоты добавляли к 5 мл воды и растворяли при комнатной температуре. 2 г свободного основания SLV-314 (32797-94-01) добавляли в 20 мл ацетона и нагревали до 40-50 С, чтобы получить прозрачный раствор. К этому раствору добавляли подготовленный водный раствор глюкуроновой кислоты (1 экв.) и перемешивали. Раствор оставался прозрачным, затем его охлаждали естественным путем до комнатной температуры и перемешивали в течение 16 ч. Полученный в результате раствор перегоняли при 56 С. Во время перегонки 50 мл ацетона возвращали назад в раствор с двумя интервалами. Белое твердое вещество кратковременно появлялось во время перегонки, а затем растворялось. Перегонку останавливали после отгонки 35 мл раствора и оставляли 35 мл прозрачного раствора. Растворитель выпаривали в сушилке при 50 С под вакуумом, что давало светло-коричневое сухое аморфное твердое вещество, характеристики которого исследовали с помощью порошковой рентгеновской дифракции (фиг. 7) и ДСК (фиг. 8). Способ В. Соединение 2 растворяли в 32 объемах этанола и 4 объемах воды при повышенной температуре. Растворитель выпаривали при атмосферном давлении при нагревании до температуры кипения с обрат- 18014942 ным холодильником. Получали гель. Гель высушивали под вакуумом при 50 С. Получали аморфное твердое вещество. Пример 8. Получение соединения 2 (форма II) Форма I соединения 2 превращается в форму II при образовании суспензии формы I в ряде растворителей. Превращение происходит со временем при комнатной температуре или при повышенной температуре. Форму I ресуспендировали в толуоле, ацетоне, tBME, ацетонитриле или изопропилацетате при комнатной температуре или при 50 С в течение одной или двух недель. Обнаружено, что повышенная температура ускоряет превращение. Образование формы II мониторировали по характерному пику при 18,7 2-тета на порошковых дифракционных рентгенограммах. Пример 9. Получение гидрата I соединения 2 Соединение 2, форма I, ресуспендировали в воде более 2 недель при комнатной температуре или 50 С. Полное превращение происходило очень медленно, чтобы получить указанное в заголовке соединение в виде смеси формы I и гидрата I, характеристики которых определяли с помощью порошковой дифракционной рентгенографии и ДСК. См. фиг. 9 и 10. Пример 10. Получение гидрата II соединения 2 Аморфное соединение 2 растворяли в 6 объемах воды при комнатной температуре и позволяли соединению кристаллизоваться при комнатной температуре. Полученную в результате суспензию перемешивали в течение ночи и указанное в заголовке соединение собирали фильтрацией, и его характеристики определяли с помощью порошковой дифракционной рентгенографии и ДСК. См. фиг. 11 и 12, соответственно. Пример 11. Получение сольватов соединения 2 Метанолят Аморфное соединение 2 растворяли в 6 объемах метанола при комнатной температуре и позволяли кристаллизоваться при комнатной температуре. Полученную в результате смесь размешивали в течение ночи и твердый метанолят собирали фильтрацией. См. фиг. 13. Обнаружено, что метанолят неустойчив при сушке и превращается в форму I. Этанолят Соединение 1 растворяли в 32 объемах этанола 1J1 при повышенной температуре. Одномоментно добавляли стехиометрическое количество глюкуроновой кислоты, растворенной в 3-4 объемах воды. Образование зародышей начиналось немедленно. Полученную в результате смесь перемешивали на льду в течение 30 мин, затем оставляли на ночь без перемешивания. Указанное в заголовке соединение собирали фильтрацией, и оно было охарактеризовано с помощью порошковой дифракционной рентгенографии как этанолят I. См. фиг. 14. В процессе сушки этанолят I превращался в форму I. Альтернативно второй этанолят соединения 2, этанолят II, получали, растворяя аморфное соединение 2 в 6 объемах этанола 1J1 (этанол-этилацетат). Смесь перемешивали в течение ночи, и этанолят II собирали фильтрацией. На фиг. 15 изображена порошковая дифракционная рентгенограмма этанолята II,и на фиг. 16 изображена термограмма ДСК этанолята II. Изопропанолят Соединение 2 растворяли в 10 объемах ДМФА при комнатной температуре. 60 объемов IPA добавляли в течение 10 мин. Полученную в результате смесь перемешивали в течение 30 мин. ИзопропанолятI соединения собирали фильтрацией и его характеристики определяли с помощью порошковой дифракционной рентгенографии и ДСК. См. фиг. 17 и 18. Влажный осадок на фильтре показывал изопропанолят+ ДМФА. Высушивание пробы разрушало строение до аморфного соединения, которое содержало растворитель. Альтернативно второй изопропанолят, изопропанолят II соединения 2, получали, суспендируя аморфное соединение 2 в IPA при комнатной температуре в течение 2 или 3 дней. См. фиг. 19 и 20, которые представляют собой порошковую дифракционную рентгенограмму и термограмму ДСК соответственно. Ацетонат Соединение 1 растворяли в 32 объемах ацетона при повышенной температуре. Одномоментно добавляли стехиометрическое количество глюкуроновой кислоты, растворенной в 3-4 объемах воды. Немедленно начиналось образование зародышей. Полученную в результате смесь перемешивали на льду в течение 30 мин, затем оставляли на ночь без перемешивания. Указанное в заголовке соединение собирали фильтрацией. На фиг. 21 изображена порошковая дифракционная рентгенограмма ацетоната. При высушивании ацетонат соединения 2 превращался в форму I. Пример 12. Интеграцию сигналов от глюкуроновой кислоты сравнивали с уникальным пиком соединения 1(фиг. 4), чтобы получить молярное соотношение глюкуроновой кислоты к соединению 1. Наблюдаемое соотношение кислоты к соединению 1 колебалось от 0,94 до 0,95. Сравнительная равновесная растворимость гидрохлорида, гидробромида и глюкуроната соединения 1 указаны в табл. 10.- 19014942 Таблица 10. Сравнительная равновесная растворимость солей соединения 1 Пример 12. Получение пролонгированных составов Состав А. Пролонгированный состав для таблеток получали из соединения 2 (30% мас./мас.), микрокристаллической целлюлозы (29% мас./мас.), гипромеллозы (40% мас./мас.) и стеарата магния (1% мас./мас.) путем смешивания соединения 2, части микрокристаллической целлюлозы, гипромеллозы и некоторого количества стеарата магния с последующей сухой грануляцией смеси посредством уплотнения на вальцах. Полученные в результате компактные гранулы распределяли по размерам с помощью размола и/или просеивания. Их смешивали с оставшейся микрокристаллической целлюлозой, и гранулят смазывали остающимся стеаратом магния и прессовали в таблетки. Состав В. Другим примером пролонгированной лекарственной формы служит состав, состоящий из множества частиц с ядром из соединения 2 (70% мас./мас.) и микрокристаллической целлюлозы (30% мас./мас.). Ядро получали путем объединения компонентов и гранулирования их с водой в планетарном смесителе. Затем, используя систему Nica, полученную в результате влажную массу экструдировали через 1,0 миллиметровое сито. Экструдат затем переносили в сферонизатор и вращали при около 700 об./мин до получения сферических шариков (2-3 мин). Затем влажные шарики сушили в кипящем слое до содержания влаги 2-5%. Высушенные шарики пропускали через сито с ячейками размером 18 меш, чтобы удалить слишком крупные шарики. После этого шарики покрывали изолирующей оболочкой, состоящей изOpadry Clear (5% мас./мас.) и воды (95% мас./мас.). Это было осуществлено, во-первых, за счет монтажа на аппарате с кипящим слоем колонки Wurster и в нижней части аппарата - системы сопел для распыления, затем нанесения изолирующего слоя из Opadry при температуре на входе примерно 60 С, скорости подачи раствора покрытия 5-10 г/мин, давлении атомизации 1-2 бар. Желаемая температура продукта составляла 38-43 С. После того как масса увеличивалась примерно на 2% за счет изолирующего слоя,наносили слои этилцеллюлозы. Этот слои состоял из Surelease (водной дисперсии этилцеллюлозы с содержанием твердых веществ 25%; 5 мас.%) и воды (95 мас.%), и его наносили подобным образом, как и изолирующий слой до увеличения массы на 3-8%. После того как слой этилцеллюлозы был нанесен,шарики сушили еще 5-10 мин. Затем шарики удаляли и просеивали через сито с ячейками размером 18 меш, чтобы удалить агломераты и слишком крупные частицы. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение 2 2. Соединение по п.1, где указанное соединение находится в твердой форме. 3. Соединение по п.2, где указанное соединение является кристаллическим веществом. 4. Соединение по п.3, где указанное соединение является кристаллическим твердым веществом, по существу, свободным от аморфного соединения 2. 5. Соединение по п.1, где указанное соединение, по существу, свободно от примесей. 6. Способ получения соединения 2 включающий стадии получения соединения 1 объединения соединения 1 с глюкуроновой кислотой в подходящем растворителе; и необязательно стадию выделения соединения 2. 7. Способ по п.6, где указанный подходящий растворитель представляет собой протонный растворитель, полярный апротонный растворитель или их смесь. 8. Способ получения соединения 2 включающий стадии объединения соединения 1 с подходящим растворителем и нагревания, чтобы получить раствор; добавления глюкуроновой кислоты к указанному раствору; и необязательно стадию выделения соединения 2. 9. Фармацевтически приемлемая композиция, предназначенная для лечения или уменьшения тяжести одного и более расстройства, выбранного из болезни Паркинсона, психозов, включая шизофрению,манию, психотическую депрессию, биполярное расстройство, депрессии, стресса/тревоги, болезни Альцгеймера, болезни Гентингтона, панического расстройства, обсессивно-компульсивного расстройства,расстройства пищевого поведения, наркомании, социальных фобий, агрессивности или беспокойства,мигрени, склеродермии, феномена Рейно, рвоты, желудочно-кишечного расстройства, связанного с регуляцией перистальтики, синдрома беспокойных ног или нарушений секреции пролактина, возникших вследствие опухолей гипофиза, содержащая соединение по п.1 и фармацевтически приемлемый носитель, адъювант или растворитель. 10. Композиция по п.9, где указанная композиция представляет собой инъекционный состав для внутрисосудистого введения. 11. Композиция по п.9, где указанная композиция представляет собой инъекционный состав для внутримышечного введения. 12. Кристаллическое соединение по п.3, где указанное соединение находится в форме I, имеющей на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 17,5; 22,5; 19,9; 3,9 и 12,2. 13. Кристаллическое соединение по п.3, где указанное соединение находится в форме II, имеющей на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области- 21014942 значений 2-тета около 18,7. 14. Кристаллическое соединение по п.3, где указанное соединение представляет собой гидрат соединения 2. 15. Кристаллическое соединение по п.14, где указанный гидрат выбран из гидрата I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 9,49; 16,40 и 17,61, или гидрата II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 8,252; 10,015; 16,511 и 24,42. 16. Кристаллическое соединение по п.3, где указанное соединение представляет собой сольват соединения 2. 17. Кристаллическое соединение по п.16, где указанный сольват выбран из метанолята, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 11,048; 15,211; 17,363; 19,047 и 22,897,этанолята I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 8,32; 9,81; 16,56; 20,88 и 24,47,этанолята II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 15,09 и 16,9,изопропанолята I, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 6,59; 13,23; 16,55 и 23,31,изопропанолята II, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 3,79; 15,54 и 23,32, или ацетоната, имеющего на порошковой дифракционной рентгенограмме один или более пиков, выбранных из пиков в области значений 2-тета около 11,04; 15,20; 15,47 и 20,81.
МПК / Метки
МПК: C07D 413/12, A61K 31/538, A61P 25/18
Метки: кислоты, пиперазина, соль, соединения, глюкуроновой
Код ссылки
<a href="https://eas.patents.su/30-14942-sol-glyukuronovojj-kisloty-i-soedineniya-piperazina.html" rel="bookmark" title="База патентов Евразийского Союза">Соль глюкуроновой кислоты и соединения пиперазина</a>
Предыдущий патент: Агенты для предупреждения и лечения нарушений, включающих модулирование ryr рецепторов
Следующий патент: Способ получения покрывной композиции
Случайный патент: Способ снижения содержания ацетальдегида в формованных из расплава полиэфирах, изделие из полиэфира, способ его изготовления и композиция для его изготовления