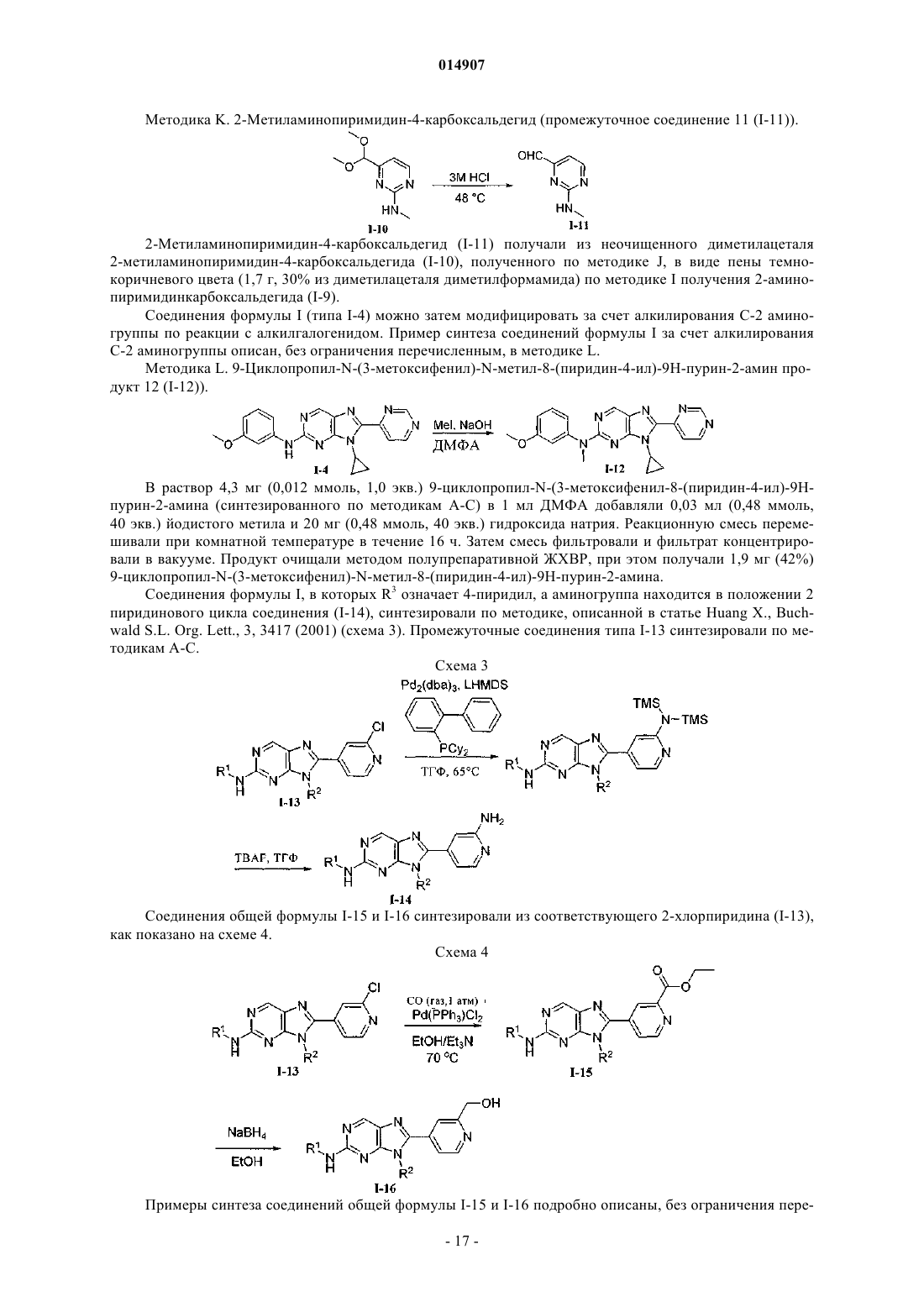
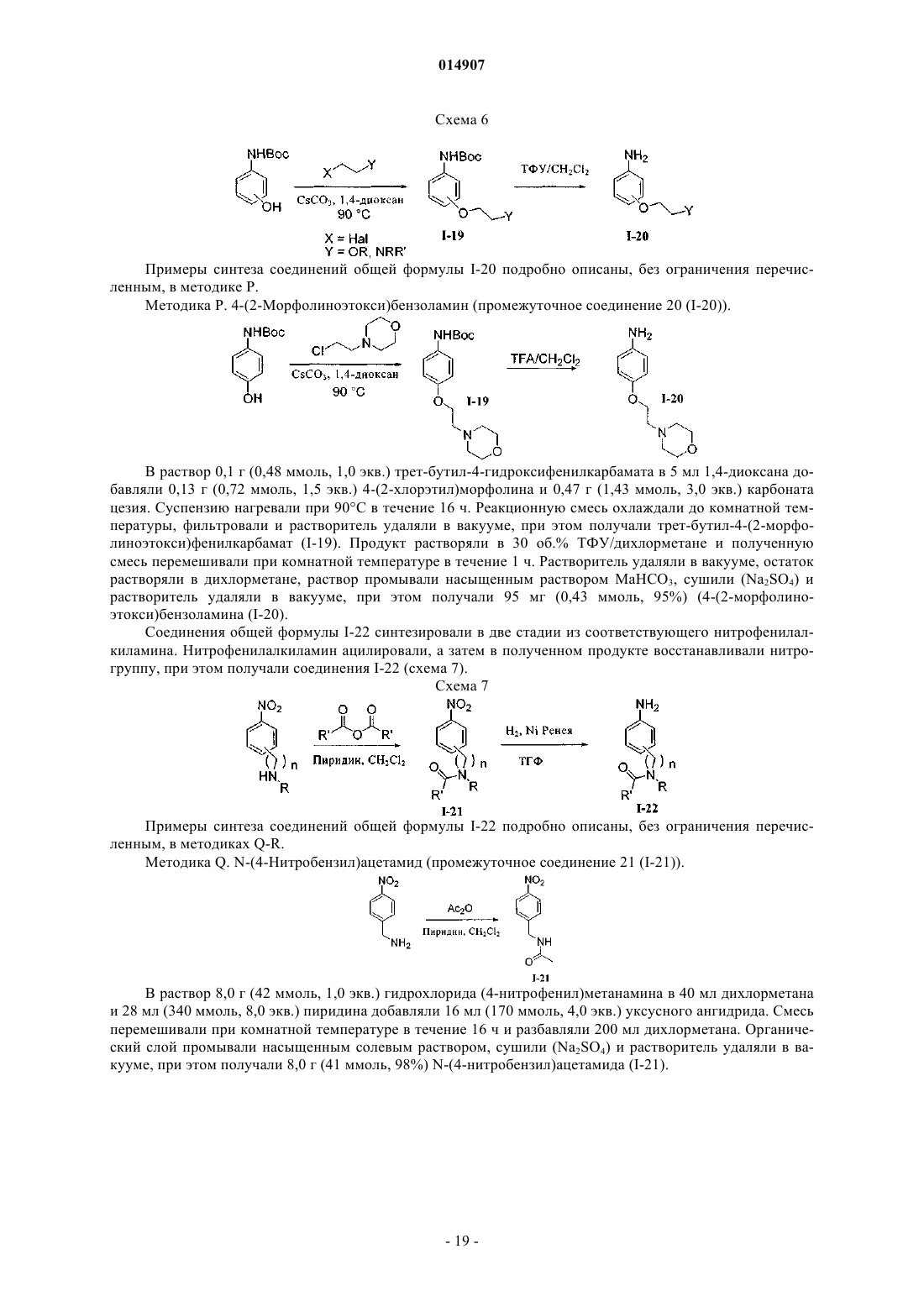
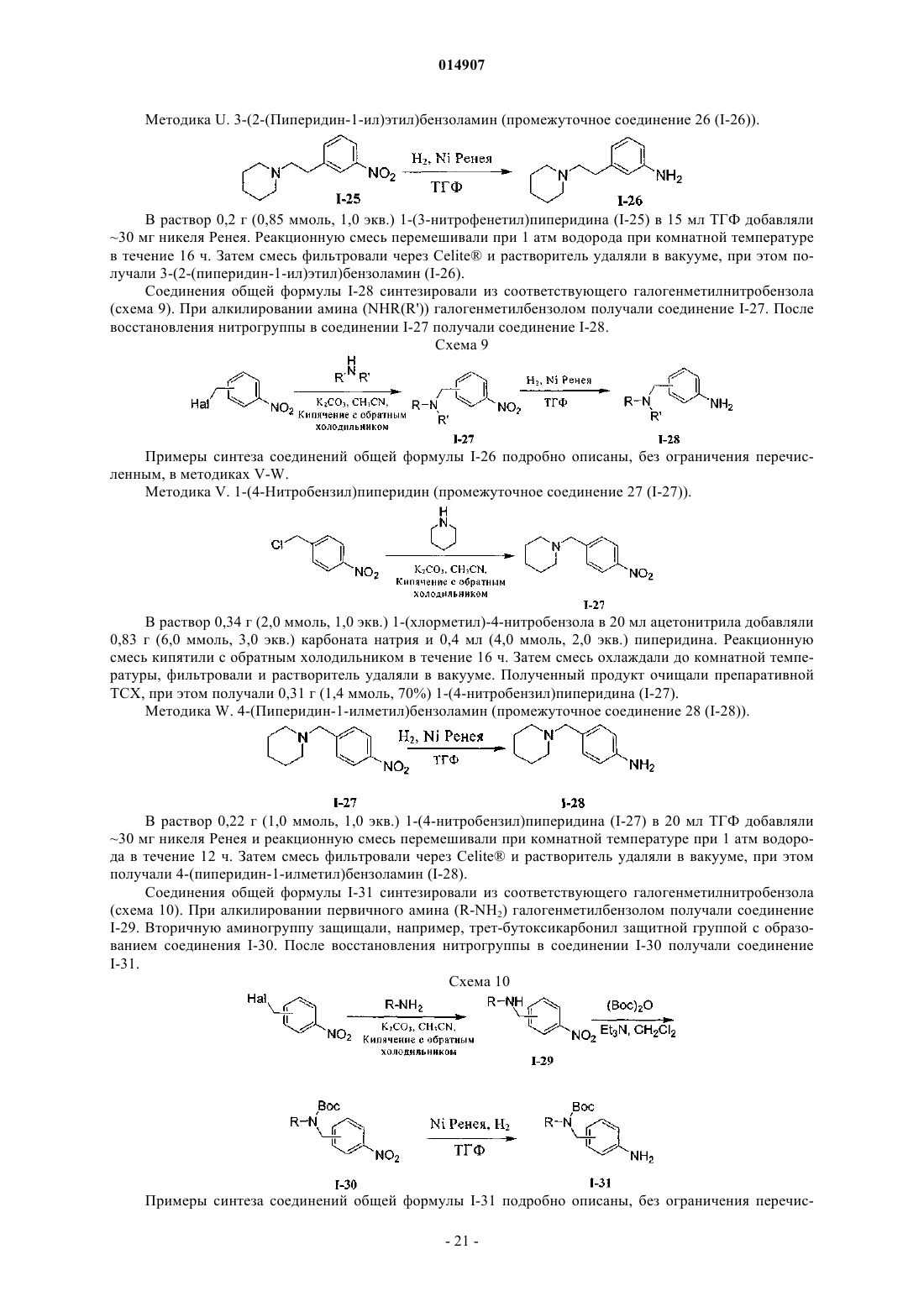
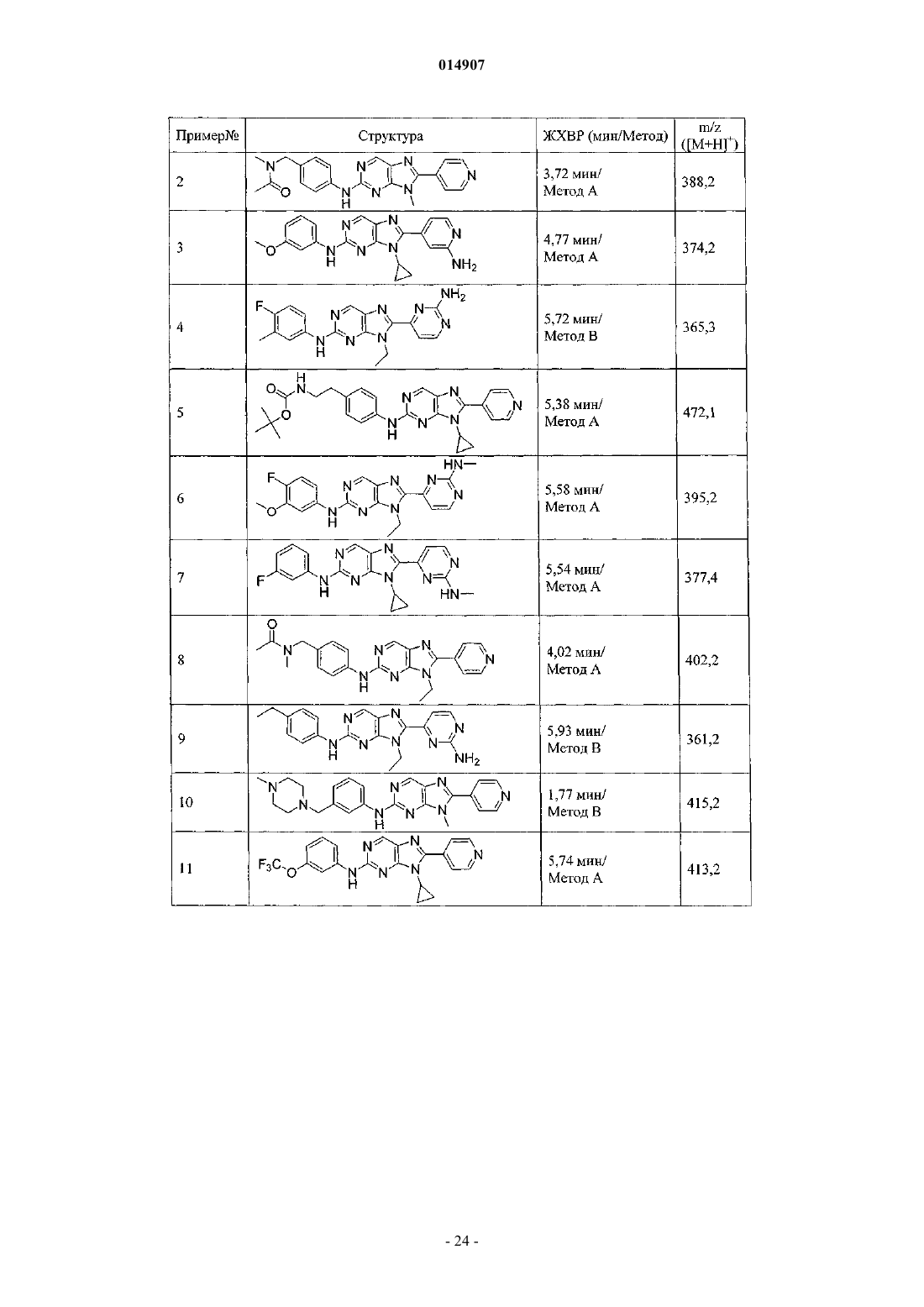
Ингибиторы mnk2 на основе 8-гетероарилпурина для лечения метаболических нарушений
Номер патента: 14907
Опубликовано: 28.02.2011
Авторы: Чжан Цоань Ц., Метцгер Аксель, Хендерсон Айан, Хуссейн Захид, Ахмед Гульзар, Брессиа Марк-Ралей, Диллер Дейвид Дж., Кул Эндрью Г.
Формула / Реферат
1. Соединение формулы I
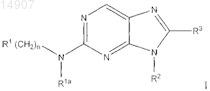
где R1выбирают из группы, включающей арил, гетероарил, C1-C10-алкил, замещенный арил, замещенный гетероарил и замещенный C1-C10-алкил;
n выбирают из группы, включающей 0, 1 и 2;
R1a означает водород или метил;
R2 выбирают из группы, включающей водород, C1-C6-алкил и C1-C6-алкил, замещенный группой CN, C1-C6-алкокси или фтор; а
R3 выбирают из группы, включающей арил, замещенный одной или двумя группами C1-C6-алкокси, и гетероарил, необязательно замещенный одним-тремя заместителями, выбранными из группы, включающей C1-C6-алкил, гидроксил, гидрокси-C1-C6-алкил, C1-C6-алкокси, амино, C1-C6-алкиламино, ди(C1-C6)алкиламино и ациламино, C1-C6-алкоксикарбонил и галоген, где термины
"арил" означает 5- или 6-членное моноциклическое, 9- или 10-членное бициклическое или 13- или 14-членное трициклическое ароматическое кольцо,
"гетероарил" означает 5- или 6-членное моноциклическое, 9- или 10-членное бициклическое или 13- или 14-членное трициклическое ароматическое кольцо, содержащее один, два или три гетероатома, выбранные из О, N и S, а
"замещенный алкил, арил, циклоалкил, гетероциклил", если не указано иначе, означают алкил, арил, циклоалкил или гетероциклил, где до трех атомов водорода в каждом остатке заменены на группу галоген, C1-C6-алкил, галоген-C1-C6-алкил, галоген-C1-C6-алкокси, гидрокси, C1-C6-алкокси.
2. Соединение по п.1, где R3 выбирают из группы, включающей гетероарил, необязательно замещенный одним-тремя заместителями, выбранными из группы, включающей C1-C6-алкил, гидрокси, C1-C6-алкокси, амино, C1-C6-алкиламино, ди(C1-C6-алкил)амино и ациламино.
3. Соединение по п.2, где R1 выбирают из группы, включающей арил, гетероарил и C1-C10-алкил, каждый необязательно замещенный одним-тремя заместителями, выбранными из группы, включающей C1-C6-алкил, галоген, C1-C6-алкокси, галоген-C1-C6-алкил, гидрокси, циано, нитро, амино, C1-C6-алкиламино, ди(C1-C6-алкил)амино, амино-C1-C6-алкил, C1-C6-алкиламино-C1-C6-алкил, ди(C1-C6-алкил)амино-С1-С6-алкил, меркапто, C1-C6-алкилтио, C1-C6-алкилсульфинил, C1-C6-алкилсульфонил, ациламино и ациламино-C1-C6-алкил, окса-C1-C6-алкил, гетероциклил-C1-C6-алкил, ди(C1-C6-алкил)амино-C1-C6-алкокси, (C1-C6-алкил)(ацил)амино-C1-C6-алкил, трифторметокси, ациламино-C1-C6-алкокси, гетероциклил-C1-C6-алкокси.
4. Соединение по п.2, где R1 означает фенил, замещенный одним заместителем, выбранным из группы, включающей метилендиокси, галоген, С1-C6-алкил, аминометил, C1-C6-алкиламинометил, ди(C1-C6-алкил)аминометил, окса-C1-C6-алкил, ди(C1-C6-алкил)амино-C1-C6-алкокси, (C1-C10-алкил)(ацил)амино-C1-C6-алкил, трифторметокси, ациламино-C1-C6-алкокси, гетероциклил-C1-C6-алкокси, и
![]()
где группа ![]() означает азотсодержащий гетероцикл, а q равно 1-3.
означает азотсодержащий гетероцикл, а q равно 1-3.
5. Соединение по п.2, где R1 означает фенил или фенил, замещенный группой метилендиокси, C1-C6-алкил, галоген, C1-C6-алкил, аминометил, C1-C6-алкиламинометил, ди(C1-C6-алкил)аминометил, ациламино и ациламино-C1-C6-алкил.
6. Соединение по п.2, где R1 означает тиенил, а n равно 2.
7. Соединение по п.2, где R1 означает C1-C6-алкил, а n равно 0.
8. Соединение по п.2, где R1a означает H.
9. Соединение по п.2, где n равно 0.
10. Соединение по п.2, где R2 выбирают из группы, включающей C1-C3-алкил, фтор(C1-C3)алкил и циано(С1-С3)алкил.
11. Соединение по п.2, где R2 выбирают из группы, включающей циклопропил, изопропил, 2-цианоэтил, этил, трифторэтил, водород и метил.
12. Соединение по п.2, где R3 выбирают из группы, включающей азотсодержащий гетероарил и замещенный азотсодержащий гетероарил.
13. Соединение по п.12, где R3 означает группу формулы II
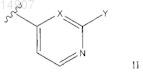
где X выбирают из группы, включающей CH, C-галоген и азот;
Y выбирают из группы, включающей H, галоген, NH2, NHMe, NHEt, HMe2, NHAc, OH, OMe, OEt, Me и Et.
14. Соединение по п.13, где Y выбирают из группы, включающей H, NH2 и NHMe.
15. Соединение по п.1, где R3 означает замещенный фенил.
16. Соединение по п.13, где R3 выбирают из группы, включающей 4-пиридинил, 2-аминопиримидин-4-ил и 2-(метиламино)пиримидин-4-ил.
17. Соединение по п.13, где R3 выбирают из группы, включающей 4-пиридил, 4-пиримидинил, 4-(2-аминопиримидил) и 4-(2-аминопиридинил).
18. Соединение по п.2, где
R1 выбирают из группы, включающей фенил и фенил, замещенный группой C1-C6-алкокси, галоген, амино-C1-C6-алкил или ациламино-C1-C6-алкил;
n выбирают из группы, включающей 0, 1 и 2;
R1a означает водород;
R2 выбирают из группы, включающей циклопропил, изопропил, этил, 2-цианоэтил, водород и метил; а
R3 выбирают из группы, включающей 4-пиридил, 4-пиримидинил, 4-(2-аминопиримидил) и 4-(2-аминопиридинил).
19. Фармацевтическая композиция, включающая соединение по любому из пп.1-18 и фармацевтически приемлемый носитель.
20. Способ профилактики или лечения диабета типа 2, включающий введение фармацевтической композиции по п.19 пациенту, который нуждается в такой профилактике или лечении.
21. Способ профилактики или лечения метаболических нарушений, включающий введение фармацевтической композиции по п.19 пациенту, который нуждается в такой профилактике или лечении.
22. Способ по п.21, где нарушение означает ожирение.
23. Способ профилактики или лечения нарушений питания, кахексии, сахарного диабета, остеоартрита, желчных конкрементов, приступов апноэ во сне, нейродегенеративных нарушений и рака, включающий введение фармацевтической композиции по любому из пп.1-18 пациенту, который нуждается в такой профилактике или лечении.
24. Способ ингибирования активности Mnk2, включающий обработку Mnk2-активной клетки любым соединением по любому из пп.1-18.
25. Применение соединения по любому из пп.1-18 при получении лекарственного средства, предназначенного для профилактики или лечения метаболических нарушений, диабета, ожирения и лейкоза.
26. Способ ингибирования активности Mnk1, включающий обработку Mnk1-активной клетки любым соединением по любому из пп.1-18.
27. Способ ингибирования активности Flt-3, включающий обработку Flt-3-активной клетки любым соединением по любому из пп.1-18.
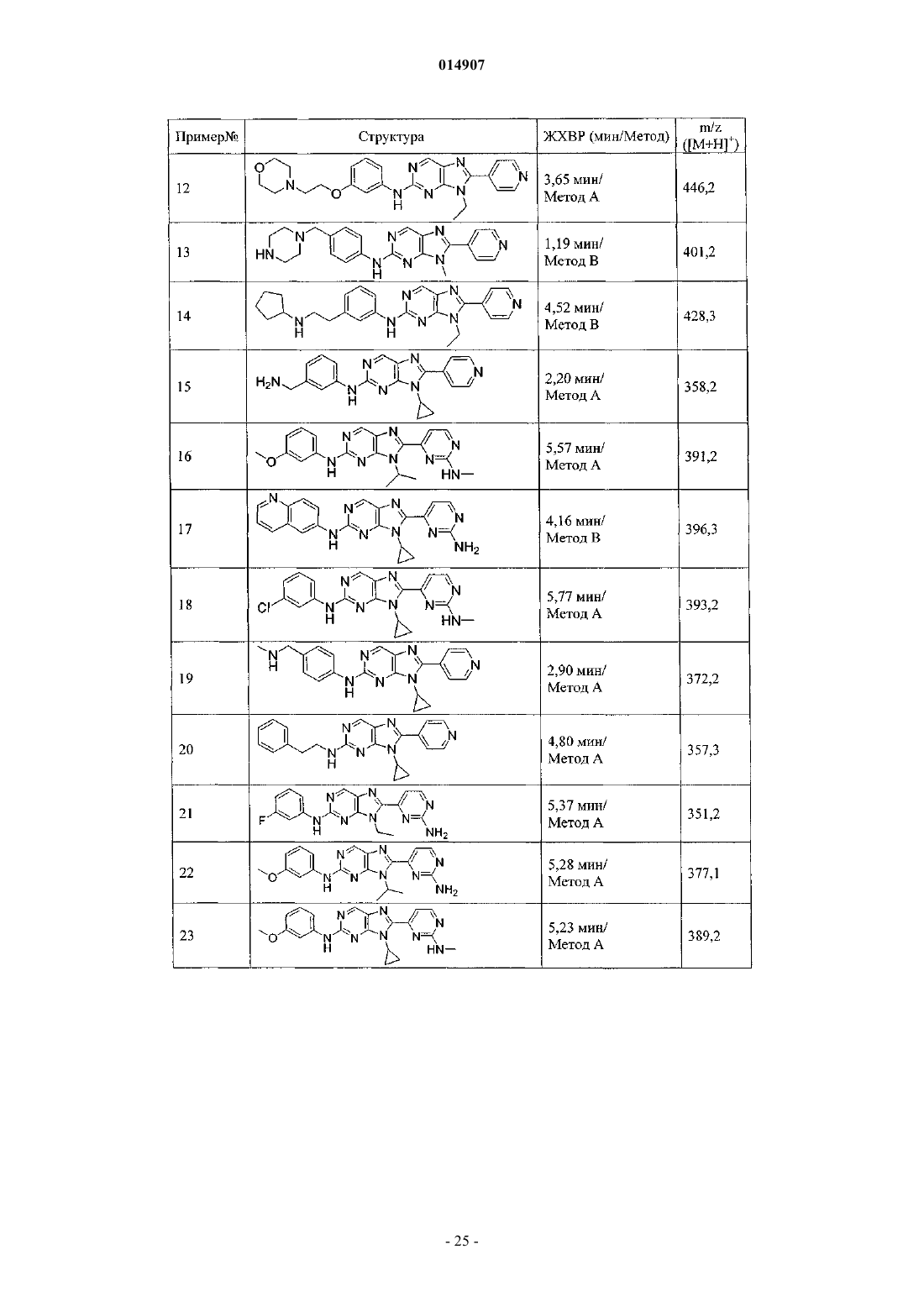
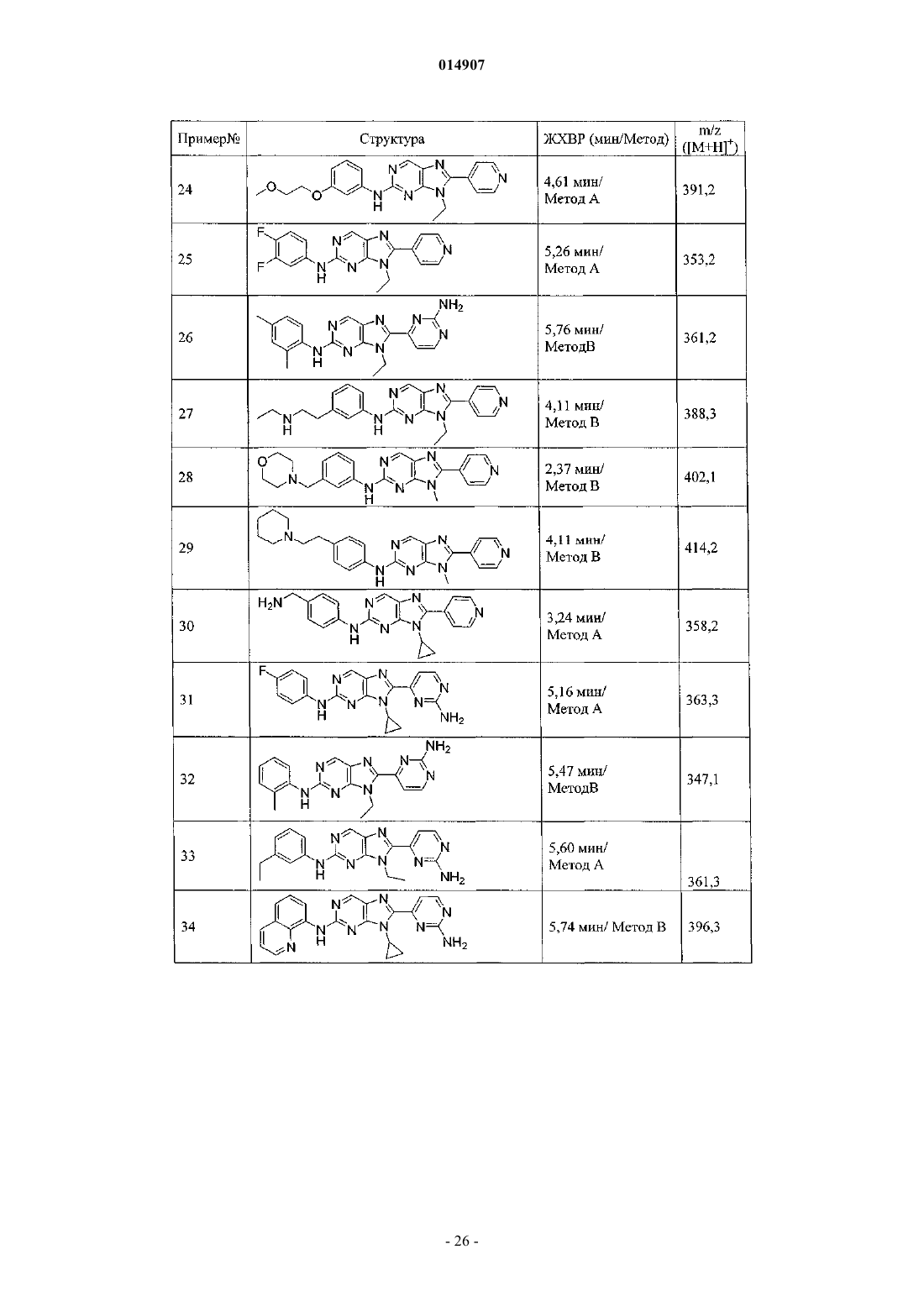
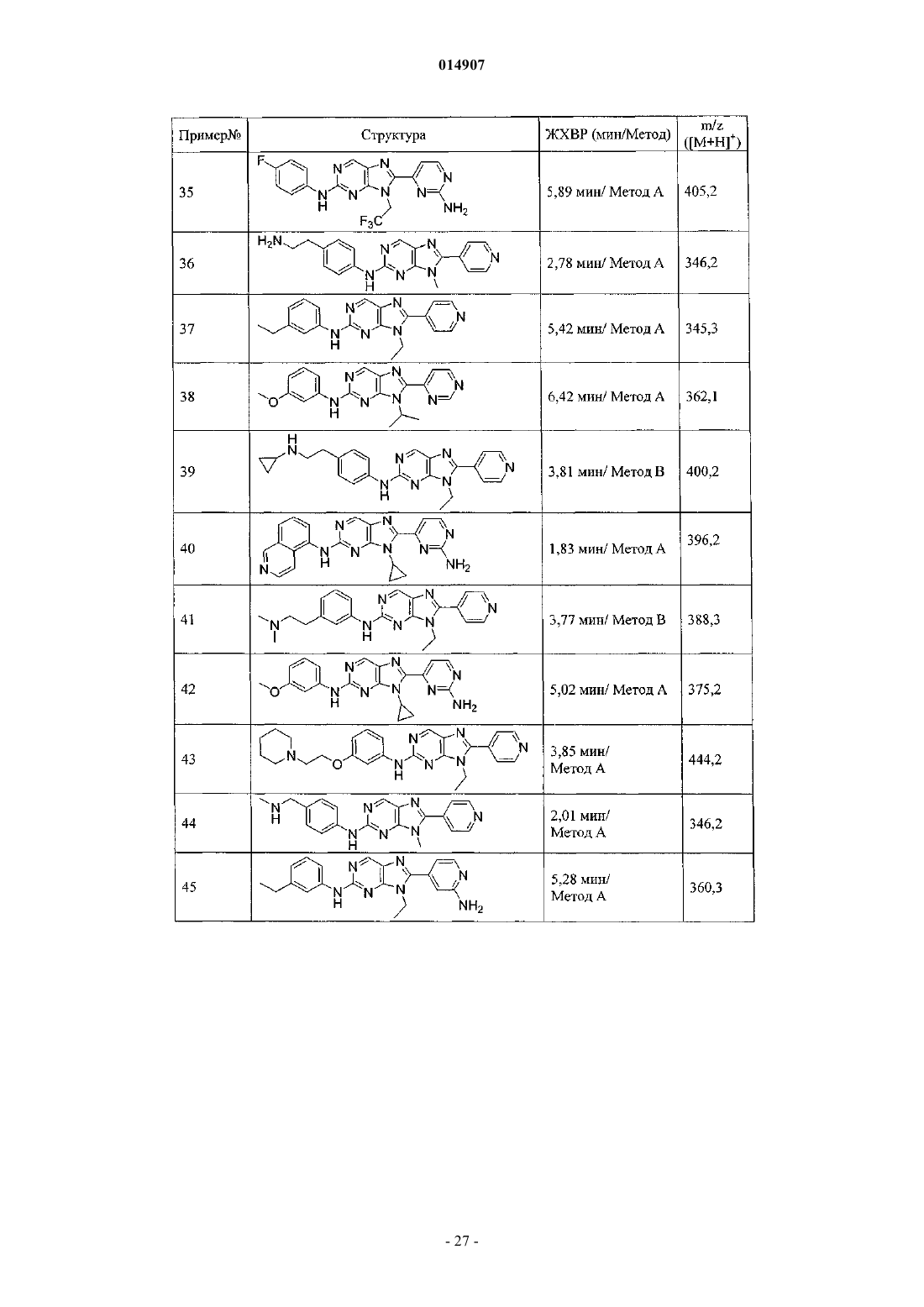
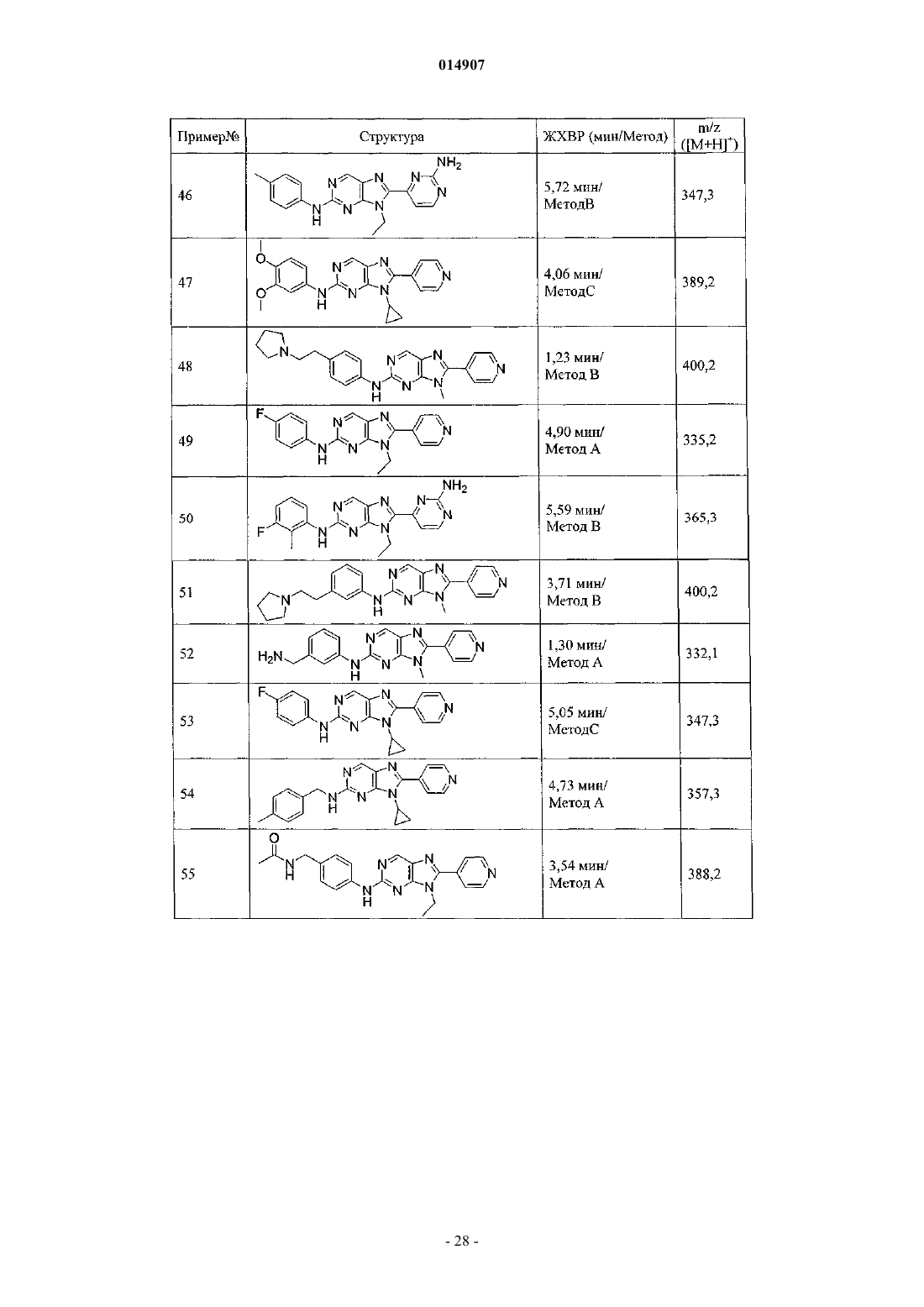
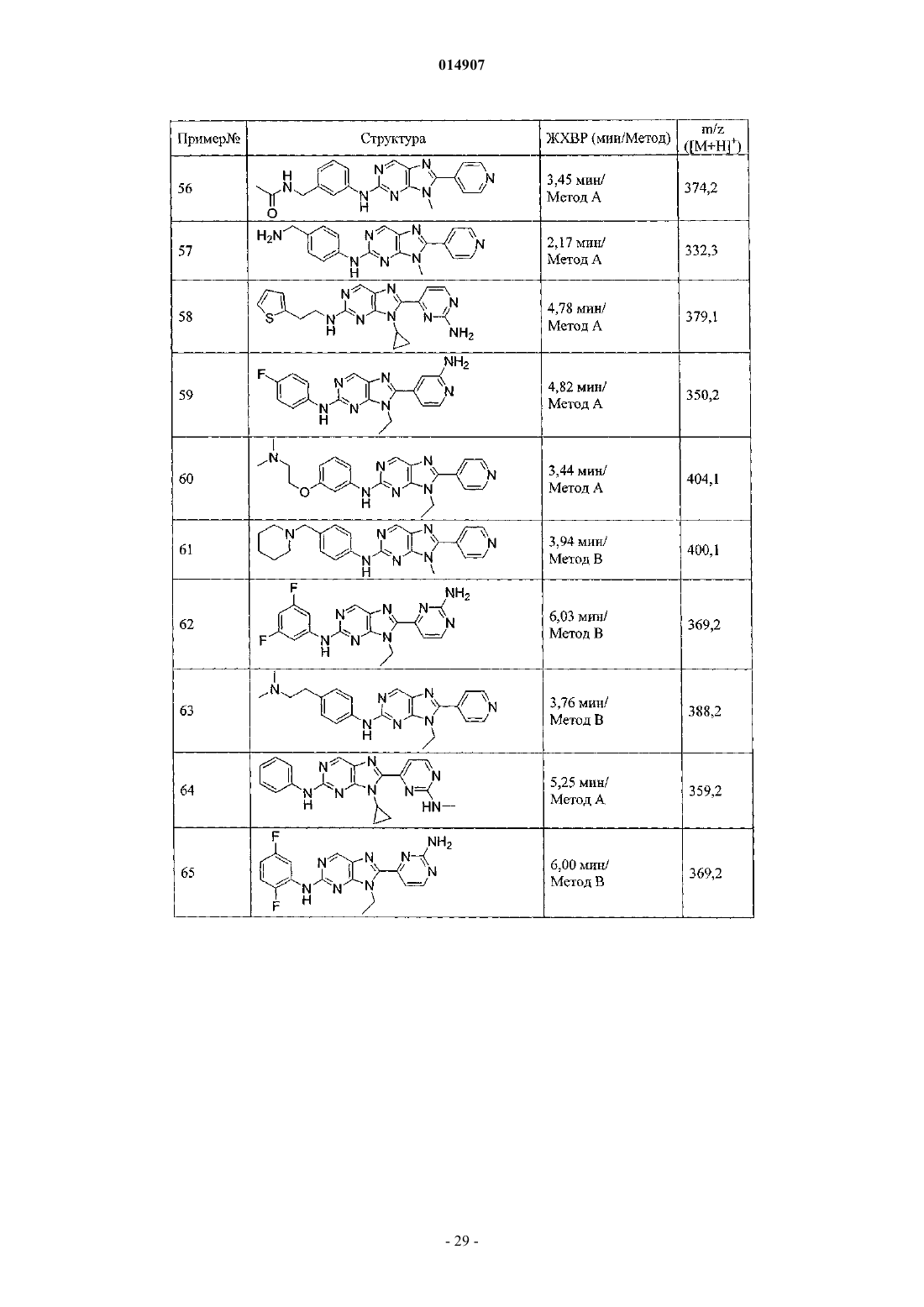
28. Соединение по п.1, выбранное из группы, включающей
9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-N-метатолил-9Н-пурин-2-амин,
N-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)-N-метилацетамид,
8-(2-аминопиридин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-3-метилфенил)-9Н-пурин-2-амин,
трет-бутиловый эфир 4-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетилкарбаминовой кислоты,
9-этил-N-(4-фтор-3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(3-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
N-(4-(9-этил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)-N-метилацетамид,
8-(2-аминопиримидин-4-ил)-9-этил-N-(4-этилфенил)-9Н-пурин-2-амин,
9-метил-N-(3-((4-метилпиперазин-1-ил)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-8-(пиридин-4-ил)-N-(3-(трифторметокси)фенил)-9Н-пурин-2-амин,
9-этил-N-(3-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(пиперазин-1-илметил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3-(2-(циклопентиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3-(аминометил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-изопропил-N-(3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)хинолин-6-амин,
N-(3-хлорфенил)-9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(4-((метиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-фенетил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фторфенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-изопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
9-циклопропил-N-(3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(3-(2-метоксиэтокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3,4-дифторфенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,4-диметилфенил)-9-этил-9Н-пурин-2-амин,
9-этил-N-(3-(2-(этиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(3-(морфолинометил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(2-(пиперидин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(аминометил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(4-фторфенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-ортотолил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(3-этилфенил)-9Н-пурин-2-амин,
N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)хинолин-8-амин,
8-(2-аминопиримидин-4-ил)-N-(4-фторфенил)-9-(2,2,2-трифторэтил)-9Н-пурин-2-амин,
N-(4-(2-аминоэтил)фенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(3-этилфенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-изопропил-N-(3-метоксифенил)-8-(пиримидин-4-ил)-9Н-пурин-2-амин,
N-(4-(2-(циклопропиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)изохинолин-5-амин,
N-(3-(2-(диметиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
9-этил-N-(3-(2-(пиперидин-1-ил)этокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-((метиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-9-этил-N-(3-этилфенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-паратолил-9Н-пурин-2-амин,
9-циклопропил-N-(3,4-диметоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-8-(пиридин-4-ил)-N-(4-(2-(пирролидин-1-ил)этил)фенил)-9Н-пурин-2-амин,
9-этил-N-(4-фторфенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фтор-2-метилфенил)-9Н-пурин-2-амин,
9-метил-8-(пиридин-4-ил)-N-(3-(2-(пирролидин-1-ил)этил)фенил)-9Н-пурин-2-амин,
N-(3-(аминометил)фенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(4-фторфенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-метилбензил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(9-этил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)ацетамид,
N-(3-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)ацетамид,
N-(4-(аминометил)фенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-9-этил-N-(4-фторфенил)-9Н-пурин-2-амин,
N-(3-(2-(диметиламино)этокси)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(пиперидин-1-илметил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3,5-дифторфенил)-9-этил-9Н-пурин-2-амин,
N-(4-(2-(диметиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-N-фенил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,5-дифторфенил)-9-этил-9Н-пурин-2-амин,
9-циклопропил-N-(3-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3,4-дифторфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,3-дифторфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(4-фторфенил)-9-метил-9Н-пурин-2-амин,
трет-бутиловый эфир 4-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензилкарбаминовой кислоты,
9-циклопропил-N-(2,4-диметоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(3-(2-(пиперидин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(2-аминоэтил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(3-((этиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-метатолил-9Н-пурин-2-амин,
N-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетил)ацетамид,
8-(2-аминопиримидин-4-ил)-N-(3,4-диметилфенил)-9-этил-9Н-пурин-2-амин,
N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9-(2,2,2-трифторэтил)-9Н-пурин-2-амин,
N-(3-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)ацетамид,
(4-(2-(4-фторфениламино)-9-метил-9Н-пурин-8-ил)пиридин-2-ил)метанол,
N-(4-((циклопентиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2-хлор-5-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
N-(4-фторфенил)-9-метил-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(3-метоксифенил)-8-(пиримидин-4-ил)-9Н-пурин-2-амин,
N1-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)-N4,N4-диметилбензол-1,4-диамин,
9-метил-8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,3-диметилфенил)-9-этил-9Н-пурин-2-амин,
N-(2,3-дигидробензо[b][1,4]диоксин-6-ил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
3-(2-(3-метоксифениламино)-8-(пиримидин-4-ил)-9Н-пурин-9-ил)пропаннитрил,
9-этил-N-(3-этилфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-((этиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(2-морфолиноэтил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-хлорпиридин-4-ил)-9-циклопропил-N-фенил-9Н-пурин-2-амин,
9-циклопропил-8-(1-метил-1Н-пиррол-2-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фтор-4-метилфенил)-9Н-пурин-2-амин,
9-метил-N-(4-((4-метилпиперазин-1-ил)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3,5-диметилфенил)-9-этил-9Н-пурин-2-амин,
9-метил-N-(4-(морфолинометил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3-((диметиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-9-этил-N-(4-фтор-3-метоксифенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3-хлорфенил)-9-этил-9Н-пурин-2-амин,
N-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетил)-N-метилацетамид,
8-(2-аминопиримидин-4-ил)-N-(4-хлор-2-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
9-циклопропил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(2-фторфенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-(2-(этиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-((изопропиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(2-(4-метилпиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(3-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
N-(4-фторфенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-фенил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,3-дигидро-1H-инден-5-ил)-9-этил-9Н-пурин-2-амин,
9-этил-N-(4-(2-метоксиэтокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3-(аминометил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3-((циклопентиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
3-этил-N-(4-((метиламино)метил)фенил)-2-(пиридин-4-ил)-3H-имидазо[4,5-b]пиридин-5-амин,
N-(4-(2-(циклопентиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(3-(2-(пиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(2-фторфенетил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-8-(пиридин-4-ил)-N-(3,4,5-триметоксифенил)-9Н-пурин-2-амин,
9-метил-8-(пиридин-4-ил)-N-(4-(пирролидин-1-илметил)фенил)-9Н-пурин-2-амин,
9-циклопропил-N-(3-этилфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
8-(6-аминопиридин-3-ил)-9-этил-N-(4-фторфенил)-9Н-пурин-2-амин,
N1-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)-N3,N3-диметилбензол-1,3-диамин,
N-(3-((циклопропиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,4-дифторфенил)-9-этил-9Н-пурин-2-амин,
9-циклопропил-N-(3,5-диметоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетил)ацетамид,
N-(4-(9-этил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетил)-N-метилацетамид,
N-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)ацетамид,
9-этил-N-(4-(2-(пиперидин-1-ил)этокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(2-метоксиэтокси)фенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-хлорпиридин-4-ил)-9-изопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-9-изопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
9-этил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-N-(3,4-дифторфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2-хлорфенил)-9-этил-9Н-пурин-2-амин,
9-метил-N-(3-(пиперидин-1-илметил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(6-аминопиридин-3-ил)-9-этил-N-(3-этилфенил)-9Н-пурин-2-амин,
N-(4-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)-N-метилацетамид,
9-циклопропил-8-(пиридин-3-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
N-(2,2-диметилбензо[d][1,3]диоксол-5-ил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенетил)-N-метилацетамид,
9-циклопропил-8-(тиазол-2-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,6-дифторфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(2-фтор-4-метилфенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(4-хлорфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3-хлор-4-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
9-метил-N-(3-(2-(4-метилпиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(3-((изопропиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9Н-пурин-2-ил)хинолин-5-амин,
N-(2-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)фенокси)этил)ацетамид,
8-(2-хлорпиридин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,5-диметилфенил)-9-этил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-2-метилфенил)-9Н-пурин-2-амин,
N-(4-((циклопропиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(2-этилфенил)-9Н-пурин-2-амин,
N-(4-метоксифенил)-9-метил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-8-(пиримидин-4-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-3-метоксифенил)-9Н-пурин-2-амин,
9-циклопропил-8-(1-метил-1H-имидазол-5-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
N-(бензо[d][1,3]диоксол-5-ил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(2-(диметиламино)этокси)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(бензо[d]тиазол-6-ил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-фтор-3-метоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(2,3-дигидро-1Н-инден-4-ил)-9-этил-9Н-пурин-2-амин,
N-(3-(2-(циклопропиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-этил-N-(4-(2-(изопропиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3-хлор-2-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
3-(8-(2-аминопиримидин-4-ил)-2-(3-метоксифениламино)-9Н-пурин-9-ил)пропаннитрил,
8-(2-аминопиридин-4-ил)-N-(4-фторфенил)-9-метил-9Н-пурин-2-амин,
N-(4-фторфенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-хлорфенил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-этилфенил)-9Н-пурин-2-амин,
9-этил-N-(4-((метиламино)метил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-фторфенил)-8-(пиридин-4-ил)-9-(2,2,2-трифторэтил)-9Н-пурин-2-амин,
N-(3-(9-этил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)ацетамид,
9-метил-8-(пиридин-4-ил)-N-(3-(пирролидин-1-илметил)фенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(5-фтор-2-метилфенил)-9Н-пурин-2-амин,
8-(2-хлорпиридин-4-ил)-9-циклопропил-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(5-хлор-2-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
9-метил-N-(3-(2-морфолиноэтил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(2-метоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-хлорпиридин-4-ил)-9-этил-N-(3-этилфенил)-9Н-пурин-2-амин,
9-циклопропил-N-(3-метоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(2-метоксифенетил)-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
этиловый эфир 4-(2-(4-фторфениламино)-9-метил-9Н-пурин-8-ил)пиколиновой кислоты,
8-(2-аминопиримидин-4-ил)-N-(2-хлор-4-фторфенил)-9-циклопропил-9Н-пурин-2-амин,
N-(4-(2-аминоэтил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9H-пурин-2-амин,
N-циклопентил-9-циклопропил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-фторфенил)-9Н-пурин-2-амин,
9-циклопропил-8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
8-(2-аминопиридин-4-ил)-9-циклопропил-N-фенил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-N-(3-хлорфенил)-9-циклопропил-9Н-пурин-2-амин,
N-(4-(аминометил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(4-(9-метил-8-(пиридин-4-ил)-9Н-пурин-2-иламино)бензил)-2,2,2-трифторацетамид,
9-этил-N-(3-(2-(изопропиламино)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
N-(3,4-дифторфенил)-9-этил-8-(2-(метиламино)пиримидин-4-ил)-9Н-пурин-2-амин,
9-метил-N-(3-(пиперазин-1-илметил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-изобутил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-этил-8-(2-(метиламино)пиримидин-4-ил)-N-метатолил-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-циклопропил-N-фенил-9Н-пурин-2-амин,
9-циклопропил-8-(1H-пиррол-2-ил)-N-(2-(тиофен-2-ил)этил)-9H-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фторфенил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-метатолил-9Н-пурин-2-амин,
9-метил-N-(4-(2-(пиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9Н-пурин-2-амин,
N-(4-((диметиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9Н-пурин-2-амин,
9-циклопропил-N-(4-метоксифенил)-8-(пиридин-4-ил)-9Н-пурин-2-амин,
8-(2-аминопиримидин-4-ил)-9-этил-N-(5,6,7,8-тетрагидронафталин-1-ил)-9Н-пурин-2-амин.
Текст
ИНГИБИТОРЫ Mnk2 НА ОСНОВЕ 8-ГЕТЕРОАРИЛПУРИНА ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКИХ НАРУШЕНИЙ В изобретении описаны соединения формулы которые являются ингибиторами Mnk2 и которые можно использовать для лечения и профилактики метаболических нарушений, таких как ожирение и диабет. 014907 Область техники, к которой относится изобретение Настоящее изобретение относится к ингибиторам Mnk2 на основе 8-гетероарилпурина, которые можно использовать для лечения и профилактики метаболических заболеваний. Предпосылки создания изобретения Одним из главных гормонов, воздействующих на метаболические процессы, является инсулин, который синтезируется в -клетках островков Лангерганса поджелудочной железы. Инсулин, главным образом, регулирует направление метаболизма, сдвигая многие процессы в направлении хранения субстратов и предотвращения их деградации (см., например, обзоры Shepherd P.R. и др. Biochem. J., 333, 471-490(1998), Alessi D.R. и Downes С.Р. Biochim. Biophys. Acta, 1436, 151-164 (1998. Предполагается, что инсулин принимает участие в транспорте глюкозы и аминокислот, а также ключевых минеральных веществ, таких как калий, магний и фосфат, из кровотока в клетки. Предполагается также, что инсулин регулирует в клетках многие ферментативные реакции, которые включают синтез макромолекул из небольших структурных фрагментов. Недостаточность функции инсулина (при сахарном диабете) может вызвать серьезные нарушения таких процессов, как (1) хранение глюкозы в форме гликогена и окисление глюкозы для выработки энергии, (2) синтез из жирных кислот и их предшественников и его хранение, а также завершение процесса окисления жирных кислот и (3) синтез белка из аминокислот. Существуют два варианта диабета. Тип 1 означает инсулинозависимый сахарный диабет (IDDM,раньше называемый юношеским диабетом), при котором необходимо введение инсулина. При этом заболевании инсулин не секретируется поджелудочной железой и, следовательно, пациенту требуется вводить инсулин. Диабет типа 2, т.е. инсулиннезависимый сахарный диабет (NIDDM), на клиническом уровне характеризуется гипергликемией, резистентностью к инсулину и обычно ассоциируется с ожирением. Диабет типа 2 представляет собой гетерогенную группу нарушений, при которых гипергликемия обычно развивается за счет нарушенной секреции инсулина в ответ на глюкозу и пониженной эффективности действия инсулина при стимулировании захвата глюкозы скелетными мышцами и при ограничении продуцирования глюкозы в печени (инсулинорезистентность). Еще до развития диабета у пациента отсутствует начальная секреция инсулина в ответ на глюкозу и секретируется относительно большое количество проинсулина. При развитом диабете может наблюдаться нормальный уровень инсулина в плазме крови натощак, а у пациентов с диабетом типа 2 даже повышеннный уровень, однако секреция инсулина, стимулированная глюкозой, остается явно пониженной. Пониженный уровень инсулина обычно влечет за собой снижение инсулин-опосредованного захвата глюкозы и отсутствие торможения продуцирования глюкозы в печени. Гомеостаз глюкозы зависит от баланса между продуцированием глюкозы в печени и утилизацией глюкозы инсулинозависимыми тканями, такими как жировая ткань и мышцы, и инсулинонезависимыми тканями, такими как мозг и почки. При диабете типа 2 транспорт глюкозы в жировую ткань и мышцы является пониженным, а продуцирование глюкозы в печени повышенным из-за инсулинорезистентности в тканях. Рецепторные тирозинкиназы (RTK) представляют собой класс рецепторов клеточных мембран. Лигандами RTK являются пептидные/белковые гормоны, включающие фактор роста нервной ткани (NGF),тромбоцитарный фактор роста (PDGF), эпидермальный фактор роста (EGF) и инсулин. Связывание лиганда с RTK стимулирует активность эндогенной рецепторной протеинтирозинкиназы, которая затем запускает каскад передачи сигнала, приводящий к изменениям клеточной физиологии и программы генной экспрессии. Сигнальный путь RTK характеризуется широким спектром функций, включая регуляцию пролиферации и дифференциации клеток, стимулирование выживания клеток и модуляцию клеточного метаболизма. Рецептор тромбоцитарного фактора роста (PDGFR) и Fms-подобная тирозинкиназа 3 (FLT-3) принимают участие в ряде патологических процессов, прежде всего различных типов рака, и, следовательно,считаются мишенями при разработке лекарственных средств. Оба белка являются членами класса III семейства рецепторных тирозинкиназ (RTK), который также включает рецепторы фактора стволовых клеток (с-KIT) и колонийстимулирующего фактора 1 (CSF1R). Рецептор PDGF принимает участие в процессе ранозаживления и регуляции гомеостаза соединительной ткани. Указанный рецептор экспрессируется ранними стволовыми клетками, тучными клетками, миелоидными клетками, мезенхимальными клетками и клетками гладкой мускулатуры. Сверхактивность/сверхэкспрессия PDGFR ассоциируется со злокачественными процессами, а также с различными заболеваниями, которые сопровождаются избыточным клеточным ростом, такими как атеросклероз и фиброз. Рецептор FLT-3 играет ключевую роль в поддержании процессов пролиферации и дифференциации при гемопоэзе. FLT-3 экспрессируется клеткамипредшественниками нормальных миелоидных и лимфоидных клеток, а также лейкозными клетками. Ингибирование тирозинкиназной активности рецептора является основным механизмом, представляющим интерес при разработке противолейкозных лекарственных средств. Указанный новый подход к лечению острого миелоидного лейкоза (АМЛ) основан на данных о том, что конститутивная активация рецептораFLT-3 играет важную роль в развитии агрессивного гематологического злокачественного роста, для которого в настоящее время отсутствуют эффективные методы лечения (см., например, Markovic А. et al.Ras представляет собой ГТФ-связывающий белок-переключатель, который действует подобно ключевой сигнальной молекуле в путях, которые инициируются при активации RTK. В общем случае, Rasопосредованная RTK в клетках млекопитающих использует высококонсервативный путь передачи сигнала, в котором активированный Ras индуцирует киназный каскад, кульминацией которого является активация киназы MAP (митоген-активируемой протеинкиназы). Указанная серин/треонинкиназа, которая может проникать в ядро, фосфорилирует множество различных белков, включая факторы транскрипции,регулирующие экспрессию белков, которые, как полагают, играют важную роль в клеточном цикле и процессе дифференциации. Продукты гена Mnk1 и Mnk2 мыши ("киназа, взаимодействующая с киназой MAP" или "киназа, интегрирующая сигнал киназы MAP" 1 и 2) являются серин/треонинкиназами, состоящими из одного домена, последовательности которых гомологичны на 72% (Waskiewicz A.J. et al. ЕМВО J., 16, 1909-1920(1997), GenBank,Y11091 и Y11092). Описана также Mnk1 человека (Fukunaga R. et al. ЕМВО J., 16,1921-1933 (1999), GenBank,АВ 000409). Все три указанных белка были идентифицированы благодаря их способности прочно связываться с киназами MAP. Обе киназы Mnk1 и 2 связываются с внеклеточными регуляторными киназами ERK1 и ERK2, a Mnk1 также связывается со стресс-активируемой киназой р 38. В качестве одного из физиологических субстратов Mnk1 и Mnk2 идентифицирован эукариотический фактор инициации 4 Е (eIF4E) (Scheper G.C. et al. Mol. Cell. Biol., 21, 743-754 (2001. По данным Harris и др. (Blood, 104(5), 1314-1323 (2004, некоторые eIF, такие как eIF4E, селективно усиливают экспрессию рост-стимулирующих мРНК (например, циклина D) и мРНК, ассоциированных с метастазированием (например, эндотелиального фактора роста сосудов), и, следовательно, контроль трансляции за счет регуляции eIF может играть важную роль в подавлении роста опухоли. Идентифицирован ген Mnk2 человека и охарактеризован с использованием дрожжевой двухгибридной системы, в которой белок Mnk2 взаимодействует с лигандсвязывающим доменом рецептора эстрогена (ER) (Slentz-Kesler K. et al. Genomics, 69, 63-71 (2000. Установлено, что ген Mnk2 человека включает два сплайсированных по С-концевому фрагменту, обозначенных Mnk2a (GenBank,AF237775) и Mnk2b (GenBank,AF237776). Установлено, что две изоформы кодируют идентичную аминокислотную последовательность из первых 385 аминокислот и отличаются только концевым экзоном, кодирующим 80 дополнительных аминокислотных остатков в Mnk2a и 29 остатков в Mnk2b. Установлено также, что Mnk2 селективно взаимодействует с рецептором эстрогена (ER) в отличие от ERI и что это взаимодействие специфично для Mnk2b в отличие от Mnk2a или Mnk1. В WO 02/103361 сообщается, что Mnk2 принимает участие в сигнальном пути инсулина, и предлагается метод идентификации модулятора захвата глюкозы. В WO 03/037362 сообщается, что киназыMnk, прежде всего Mnk2 (Mnk2a и Mnk2b), принимают участие в регуляции массы тела и теплообразовании и, следовательно, могут ассоциироваться с метаболическими заболеваниями, такими как ожирение, а также с сопутствующими нарушениями, такими как нарушение питания, кахексия, сахарный диабет, гипертензия, коронарная болезнь сердца, гиперхолестеринемия, дислипидемия, остеоартрит, желчные конкременты, приступы апноэ во сне, нейродегенеративные нарушения и нарушения, связанные с защитой от активных форм кислорода (АФК), такие как сахарный диабет, нейродегенративные нарушения и рак, например рак репродуктивных органов. Согласно WO 2005/003785 киназы Mnk являются перспективными мишенями для противовоспалительной терапии. Ожирение представляет собой одно из наиболее распространенных во всем мире нарушений массы тела. Ожирение определяется как масса тела, которая на 20% превышает идеальную массу тела. Заболевание ассоциируется с повышенным риском сердечно-сосудистого заболевания, гипертензии, диабета,гиперлипидемии и повышенным уровнем смертности. Ожирение означает состояние, которое развивается по множеству причин и характеризуется повышенным уровнем инсулина в плазме крови натощак и повышенной секрецией инсулина в ответ на пероральный прием глюкозы. В работе Worch и др. (Oncogene, 23, 9162-9172 (2004 установлено, что при остром миелоидном лейкозе (AML) экспрессия белка Mnk1 индуцируется в клеточных линиях продуктами транслокации,PML-RAR, PLZF-RAR и AML1-ETO при стабилизации белка Mnk1. Ингибирование Mnk1 усиливало дифференциацию гемопоэтических клеток. При анализе образцов костного мозга пациентов с AML установлено, что в 25 из 99 образцов экспрессия белка Mnk1 локализована в цитоплазме и у таких пациентов экспрессия Mnk1 ассоциируется с экспрессией онкогена, белка с-Мус. Соединения, которые ингибируют Mnk2, представляют интерес для профилактики и лечения заболеваний и нарушений, ассоциированных с регуляцией массы тела и теплообразованием. В заявке PCTWO 03/037362 и цитированных документах описаны низкомолекулярные соединения, ингибирующиеMnk2, такие как соединение CGP57380, которые можно использовать для профилактики и лечения метаболических заболеваний, таких как ожирение и диабет. Существует четкая корреляция между ожирением и диабетом типа 2. Диабет типа 2, известный также как сахарный, наиболее часто развивается при ожирении пациентов. Это заболевание характеризуется гипогликемией из-за нарушенной чувствительности к инсулину в сочетании с неспособностью организма компенсировать повышенное продуцирование инсулина, а не из-за фактической недостаточности секреции инсулина, наблюдаемой при диабете типа 1. Диабет типа 2 и ожирение характеризуются сверхэкспрессией Mnk2. Следовательно, ингибирование Mnk2 можно использовать при лечении и профилактике этих двух широко распространенных заболеваний. Ряд данных свидетельствует о том, что Mnk2 модулирует сигнальный путь RAS/киназа MAP и, следовательно, модулирует ответную реакцию на инсулин и гомеостаз глюкозы. В организме млекопитающих сверхэкспрессия Mnk2b влечет за собой нарушение передачи сигнала киназой MAP и захвата глюкозы (WO 02/103361). Сверхэкспрессия Mnk2b снижает захват глюкозы в адипоцитах мыши и нейронных клетках человека in vitro. Захват глюкозы линией нейронных клеток можно увеличить за счет нокдауна эндогенного Mnk2 с использованием РНК-интерференции. На основании приведенных данных для специалиста в данной области очевидно, что ингибитор Mnk2 является перспективным агентом при снижении уровня глюкозы в крови. Краткое изложение сущности изобретения Настоящее изобретение относится к соединениям 8-гетероарилпурина, используемым для ингибирования Mnk2 с целью лечения и профилактики метаболических нарушений. Одним объектом изобретения являются соединения формулы I, которые ингибируют Mnk2. В указанных соединениях R1 выбирают из группы, включающей арил, гетероарил и C1-C10-алкил,замещенный арил, замещенный гетероарил и замещенный C1-C10-алкил. R1a означает водород или метил,a R2 выбирают из группы, включающей водород, C1-C6-алкил и C1-C6-алкил, замещенный группой CN,(низш.)алкокси и фтор. R3 выбирают из группы, включающей арил, замещенный одной или двумя группами алкокси, и гетероарил, необязательно замещенный одним-тремя заместителями, выбранными из группы, включающей (низш.)алкил, гидроксил, (низш.)алкокси, амино, алкиламино, диалкиламино и ациламино, алкоксикарбонил и галоген. Другим объектом изобретения являются фармацевтические композиции, включающие фармацевтически приемлемый носитель и соединение формулы I. Еще одним объектом изобретения являются способы лечения и профилактики метаболических нарушений (таких как ожирение), диабета типа 2, заключающиеся в том, что соединения по изобретению вводят пациенту, который нуждается в такой профилактике или лечении. Другим объектом изобретения является способ профилактики или лечения нарушений питания, кахексии, сахарного диабета, остеоартрита, желчных конкрементов, приступов апноэ во сне, нейродегенеративных нарушений и рака, заключающийся в том, что фармацевтическую композицию по любому из пп.1-18 вводят пациенту, который нуждается в такой профилактике или лечении. Кроме того, изобретение относится к способу ингибирования активности Mnk2, который заключается в том, что Mnk2-активные клетки обрабатывают любым из заявленных соединений, а также к способу ингибирования активности Mnk1, который заключается в том, что Mnk1-активные клетки обрабатывают любым из заявленных соединений. Кроме того, изобретение относится к способу ингибирования активности Flt-3, который заключается в том, что Flt-3-активные клетки обрабатывают любым из заявленных соединений. Подробное описание изобретения Документы, цитированные в описании, включены в текст заявки в качестве ссылки в полном объеме в каждом случае в той же степени, как если бы каждый документ цитировался отдельно. Определения терминов Термины и названия заместителей, используемые в описании заявки, имеют следующие значения. Термин "алкил" включает углеводородные радикалы с прямой, разветвленной или циклической це-3 014907 пью или их комбинации. Если не указано иное, алкил содержит 10 или менее атомов углерода,(низш.)алкил означает алкильные группы, содержащие 1, 2, 3, 4, 5 и 6 атомов углерода. Примеры группы(низш.)алкилгруппы включают метил, этил, пропил, изопропил, бутил, втор- и трет-бутил и т.п. Предпочтительными являются группы алкил и алкилен, содержащие C10 или менее (например, С 1, С 2, С 3, С 4,С 5, С 6, С 7, С 8, С 9, C10) атомов углерода, наиболее предпочтителен (низш.)алкил. Циклоалкил означает подгруппу алкил и включает циклические углеводородные группы, содержащие 3, 4, 5, 6, 7 и 8 атомов углерода. Примеры группы циклоалкил включают циклопропил, циклобутил, циклопентил, норборнил,адмантил и т.п. Группа C1-C20-алкил (например, C1 ,С 2, С 3, С 4, С 5, C6, С 7, С 8, С 9, C10) включает алкил, циклоалкил,алкенил, алкинил, арил и их комбинации. Примеры включают бензил, фенетил, циклогексилметил, камфорил и нафтилэтил. Алкокси означает группы, содержащие 1, 2, 3, 4, 5, 6, 7 или 8 атомов углерода, с прямой, разветвленной или циклической цепью, и их комбинации, присоединенные к основному фрагменту через атом кислорода. Примеры включают метокси, этокси, пропокси, изопропокси, циклопропилокси, циклогексилокси и т.п. Группа (низш.)алкокси означает группы, содержащие от одного до четырех атомов углерода,предпочтительно метокси. В настоящем описании алкокси и (низш.)алкокси включают метилендиокси и этилендиокси. Ацил означает группы, содержащие 1, 2, 3, 4, 5, 6, 7 и 8 атомов углерода с прямой, разветвленной или циклической цепью или их комбинации, насыщенные, ненасыщенные и ароматические и их комбинации, присоединенные к основному фрагменту через карбонильную группу. В ацильной группе один или более атомов углерода заменены на атом азота, кислорода или серы, если группа присоединена к основному фрагменту через группу карбонил. Примеры включают формил, ацетил, пропионил, изобутирил, трет-бутоксикарбонил, бензоил, бензилоксикарбонил и т.п. Группа (низш.)ацил означает группы,содержащие от одного до четырех атомов углерода. Арил и гетероарил означают ароматические или гетероароматические циклы, в том числе в качестве заместителей. Гетероарил содержит один, два или три гетероатома, выбранных из O, N или S. Оба радикала означают моноциклические 5- или 6-членные ароматические или гетероароматические циклы,бициклические 9- или 10-членные ароматические или гетероароматические циклы и трициклические 13 или 14-членные ароматические или гетероароматические циклы. Бициклические и трициклические арильные группы, которые, по меньшей мере, частично являются ароматическими, но не все циклы являются ароматическими. Ароматические 6, 7, 8, 9, 10, 11, 12, 13 и 14-членные карбоциклические циклы включают, например, бензол, нафталин, индан, тетралин и флуорен, а 5, 6, 7, 8, 9 и 10-членные ароматические гетероцикличекие циклы включают, например, имидазол, пиридин, индол, тиофен, бензопиранон,тиазол, фуран, бензимидазол, хинолин, изохинолин, хиноксалин, пиримидин, пиразин, тетразол и пиразол. Арилалкил означает алкил, присоединенный к арильному циклу. Примерами являются бензил, фенетил и т.п. Термин "гетероцикл" означает моноциклический, бициклический или трициклический остаток, содержащий 1-13 атомов углерода и 1-4 гетероатома, выбранные из группы, включающей азот, кислород или серу. Гетероцикл конденсирован с ароматическим углеводородным радикалом. Пригодные примеры включают пирролил, пиридинил, пиразолил, триазолил, пиримидинил, пиридазинил, оксазолил, тиазолил, имидазолил, индолил, тиофенил, фуранил, тетразолил, 2-пирролинил, 3-пирролинил, пирролидинил,1,3-диоксоланил, имидазолинил, имидазолидинил, пиразолинил, пиразолидинил, изоксазолил, изотиазолил, 1,2,3-оксадиазолил, 1,2,3-триазолил, 1,3,4-тиадиазолил, 2H-пиранил, 4H-пиранил, пиперидинил,1,4-дитианил, тиоморфолинил, пиразинил, пиперазинил, 1,3,5-триазинил, 1,2,5-тритианил, бензо(b)тиофенил, бензимидазолил, хинолинил и т.п. Азотсодержащий гетероцикл означает гетероцикл, содержащий в цикле по меньшей мере один атом азота и, кроме того, может включать дополнительные атомы азота и других гетероатомов. Примеры включают пиперидин, пиперазин, морфолин, пирролидин и тиоморфолин. Азотсодержащий гетероарил означает подгруппу азотсодержащих гетероциклов, примеры включают пиридин, пиррол и тиазол. Замещенный алкил, арил, циклоалкил, гетероциклил и т.п. означает алкил, арил, циклоалкил или гетероциклил, где до трех атомов водорода в каждом остатке заменены на группы галоген, алкил, галогеналкил, галогеналкокси, гидрокси, (низш.)алкокси, в настоящем описании включает метилендиокси и этилендиокси, оксаалкил, карбокси, карбоалкокси (алкоксикарбонил), карбоксамидо (алкиламинокарбонил), циано, карбонил, нитро, амино, гидроксиалкил, алкиламино, диалкиламино, аминоалкил, (алкил)(арил)аминоалкил, алкиламиноалкил (включая циклоалкиламиноалкил), диалкиламиноалкил, диалкиламиноалкокси, гетероциклилалкокси, меркапто, алкилтио, алкилсульфинил, алкилсульфонил, ациламино, ациламиноалкил, ациламиноалкокси, амидино, фенил, бензил, гетероарил, гетероциклилалкил,фенокси, бензилокси или гетероарилокси. Галогеналкил означает группу алкил, в которой один или более атомов водорода заменены на галоген. Примеры включают трифторметил, трифторметокси, трихлорэтил и дифторметил. Оксаалкил означает алкил, в котором один или более атомов углерода (и связанных с ними атомов водорода) заменены на атом кислорода. Примеры включают метоксипропокси, 3,6,9-триоксадецил и т.п.-4 014907 Термин оксаалкил имет значение, принятое в данной области техники (см. справочник Naming and Indexing of Chemical Substances for Chemical Abstracts, 196 и, без ограничения перечисленным, 127(а), опубликованный Американским химическим обществом), т.е. означает соединения, в которых атом кислорода связан простой связью с соседними атомами (с образованием простоэфирных связей). Термин "галоген "означает фтор, хлор, бром или йод. Термин "пролекарство" означает соединение, которое превращается в активное соединение in vivo. Обычно пролекарство превращается в лекарственное средство в печени или крови млекопитающего за счет ферментативного гидролиза. Соединения по настоящему изобретению могут существовать в форме, включающей радиоактивную метку, т.е. соединения могут содержать один или более атомов, атомная масса или массовое число которых отличается от атомной массы или массового числа природных изотопов. Радиоизотопы водорода, углерода, фосфора, серы и фтора включают 3 Н, 14 С, 32 Р, 35S и 18F соответственно. Соединения, которые содержат такие радиоизотопы и/или радиоизотопы других атомов, включены в объем настоящего изобретения. Благодаря простым способам получения и детектирования предпочтительны радиоизотопы 3 Н и 14 С. Соединения формулы I по настоящему изобретению и их пролекарства, содержащие радиоактивную метку, получают известными методами. Обычно соединения с радиоактивной меткой получают по методикам, описанным в примерах и показанным на схемах, при замене обычного реагента на доступный реагент, содержащий радиоактивную метку. Термин "способы лечения или профилактики" означает уменьшение интенсивности симптомов заболевания, предотвращение или ослабление симптомов и/или побочных действий, ассоциированных с нарушением метаболизма липидов. Термин "профилактика", используемый в описании заявки, означает введение лекарственного средства заблаговременно с целью предотвратить или смягчить острый приступ(заболевания) или при хроническом заболевании с целью уменьшить вероятность развития или тяжесть патологического состояния. Для лечащего врача (для которого предназначены заявленные способы лечения) представляется очевидным, что термин "профилактика" не следует воспринимать как абсолютно надежное мероприятие. В медицине этот термин означает профилактическое введение лекарственного средства с целью существенно уменьшить вероятность развития или тяжесть патологического состояния,и это определение включено в пункты формулы изобретения. Подразумевается, что термин "лечение" пациента, используемый в описании заявки, включает и профилактику заболевания. Документы, цитированные в описании, включены в текст заявки в качестве ссылки в полном объеме в каждом случае в той же степени, как если бы каждый документ цитировался отдельно. Термин "млекопитающее" используется в соответствии с общепринятым значением. Термин "млекопитающее" включает, например, мышей, хомяков, крыс, крупный рогатый скот, овец, свиней, коз, лошадей, обезьян, собак (например, семейства Canis), кошек, кроликов, морских свинок и приматов, включая человека. Соединения можно использовать для лечения или профилактики диабета типа 2 и ассоциированных метаболических нарушений, таких как ожирение. Связь функции Mnk2 и таких нарушений описана в РСТ заявках WO 02/103361 и 03/037362, которые включены в описание заявки в качестве ссылки. Если в R1 и R2 присутствуют асимметрические центры, соединения могут образовывать энантиомеры, диастереомеры и другие стереоизомерные формы. Каждый хиральный центр характеризуется абсолютной стереохимической структурой, т.е. находится в (R)- или (S)-конфигурации. Настоящее изобретение включает все возможные изомеры, а также их рацемические и оптически чистые формы. Оптически активные (R)- и (S)-изомеры получают с использованием хиральных синтонов или хиральных реагентов или изомеры разделяют соответствующими методами. Если соединения по изобретению содержат олефиновые двойные связи или другие центры геометрической асимметрии и, если не указано иное, подразумевается, что соединения включают E и Z геометрические изомеры. Подразумевается также, что изобретение включает все таутомерные формы. Конфигурацию любой углерод-углеродной двойной связи изображают только для удобства и подразумевается, что она не означает конкретную конфигурацию, т.е. углерод-углеродную двойную связь произвольно представляют в Е-конфигурации, но указанная структура может означать Z-, Е-конфигурацию или их смесь в любой пропорции. Термины "защита" и "деблокирование" функциональных групп также известны специалисту в данной области и используются в контексте способов получения соединений, которые включают последовательную обработку рядом реагентов. В связи с этим защитная группа означает группу, которая используется с целью блокировать функциональную группы на одной из стадий синтеза и исключить ее нежелательное участие в реакции. Защитная группа блокирует участие функциональной группы в реакции на данной стадии синтеза, а затем удаляется с образованием свободной функциональной группы. Удаление или "деблокирование" проводят после завершения реакции или реакций, в которых может принимать участие данная функциональная группа. Таким образом, если последовательность используемых реагентов известна, специалист в данной области может выбрать и использовать такие группы, которые пригодны в качестве "защитных групп". Сокращения Me, Et, Ph, Tf, Ts и Ms означают метил, этил, фенил, трифторметансульфонил, толуол-5 014907 сульфонил и метансульфонил соответственно. Подробный перечень сокращений, используемых в органической химии, приводится в первом издании каждого тома Journal of Organic Chemistry. Этот перечень,который обычно имеет форму таблицы, озаглавленной "Перечень стандартных сокращений", включен в описание в качестве ссылки. Соединения формулы I можно вводить в виде неочищенных химических соединений, однако предпочтительно их получают в виде фармацевтической композиции. Поэтому еще одним объектом настоящего изобретения является фармацевтическая композиция, включающая соединение формулы I в смеси с одним или более фармацевтически приемлемым носителем и необязательно с одним или более другим терапевтическим ингредиентом. Носитель (носители) является "приемлемым" в том смысле, что он совместим с другими ингредиентами в составе препарата и безопасен для реципиента. Препараты включают композиции, пригодные для перорального, парентерального (включая подкожное, внутрикожное, внутримышечное, внутривенное и внутрисуставное), ректального и местного(включая дермальное, трансбуккальное, подъязычное и внутриглазное) введения. Наиболее пригодный способ введения зависит от состояния и нарушения у реципиента. Обычно препараты получают в виде стандартных лекарственных форм по любому из способов, известных в фармацевтике. Все способы включают стадию смешивания соединения формулы I с фармацевтически приемлемым носителем, который может включать один или более дополнительных ингредиентов. В общем случае препараты получают равномерным и тщательным смешиванием активного ингредиента с жидкими носителями или тонкоизмельченными твердыми носителями либо с тем и другим, а затем при необходимости продукт перерабатывают в требуемые лекарственные формы. Препараты по настоящему изобретению, пригодные для перорального введения, получают в виде дискретных изделий, таких как капсулы, пакетики или таблетки, каждое из которых содержит определенное количество активного ингредиента в виде порошка или гранул, в виде раствора или суспензии в водной или неводной среде или в жидкой эмульсии масло-в-воде или вода-в-масле. Активный ингредиент может также присутствовать в форме шарика, электуария или пасты. Таблетки получают прессованием или формованием под давлением необязательно в смеси с одним или более дополнительных ингредиентов. Прессованные таблетки получают прессованием активного ингредиента в свободнотекучей форме, такой как порошок или гранулы, необязательно в смеси со связующим агентом, замасливателем, инертным разбавителем, поверхностно-активным или диспергирующим агентом, в соответствующей таблетирующей машине. Формованные таблетки получают формованием под давлением смеси порошкообразного соединения, увлажненного инертным жидким разбавителем в пригодной таблетирующей машине. На таблетки необязательно наносят покрытие или надсечку и перерабатывают для получения лекарственной формы с пролонгированным, замедленным или регулируемым высвобождением активного ингредиента. Фармацевтические композиции могут включать "фармацевтически приемлемый инертный носитель" и подразумевается, что указанное определение включает один или более инертный эксципиент,такой как крахмалы, полиолы, гранулирующие агенты, микрокристаллическая целлюлоза, разбавители,замасливатели, связующие агенты, дезинтегрирующие агенты и т.п. При необходимости на таблетки заявленной композиции наносят стандартное водное или неводное покрытие. "Фармацевтически приемлемый носитель" включает также материалы, регулирующие высвобождение агента. Кроме того, композиции по настоящему изобретению необязательно включают другие терапевтические ингредиенты, разрыхлители, консерванты, подсластители, красители, ароматизаторы, осушители,пластификаторы и т.п. Любой такой необязательный ингредиент является совместимым с соединением по изобретению для обеспечения стабильности состава. Интервал доз для взрослого человека обычно составляет от 0,005 мг до 10 г/сутки при пероральном введении. Таблетки или другие лекарственные формы обычно содержат соединение по изобретению в количестве, которое является эффективным в дозе или при введении нескольких таких доз, например,содержащих от 5 до 500 мг, обычно приблизительно от 10 до 200 мг. Точное количество соединения,введенное пациенту, определяется лечащим врачом. Однако используемая доза зависит от ряда факторов, включающих возраст и пол пациента, конкретное нарушение, подлежащее лечению, и тяжесть такого нарушения. Для специалиста в данной области представляется очевидным, что термин "соединение" включает соли, сольваты и комплексы включения указанного соединения. Термин "сольват" означает соединение формулы I в твердом состоянии, кристаллическая решетка которого включает молекулы пригодного растворителя. Растворитель, пригодный для терапевтического введения, является физиологически переносимым в составе введенной дозы. Примерами растворителей,пригодных для терапевтического введения, являются этанол и вода. Если растворителем является вода,сольват называется гидратом. В общем случае сольваты образуются при растворении соединения в соответствующем растворителе и выделении сольвата при охлаждении раствора или при добавлении антирастворителя. Сольват обычно высушивают или растворитель удаляют в виде азеотропной смеси при комнатной температуре. Примеры комплексов включения описаны в монографии Remington: The Science-6 014907 Наиболее часто используются комплексы включения с циклодекстринами, и все циклодекстриновые комплексы, природные и синтетические, включены в пункты формулы изобретения. Термин "фармацевтически приемлемая соль" означает соли фармацевтически приемлемых нетоксичных кислот или оснований, включающих неорганические кислоты и основания и органические кислоты и основания. Если соединения по настоящему изобретению являются основаниями, соли получают с использованием фармацевтически приемлемых нетоксичных кислот, включающих неорганические и органические кислоты. Пригодные фармацевтически приемлемые кислотно-аддитивные соли соединений по настоящему изобретению включают уксусную, бензолсульфоновую (безилат), бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористо-водородную, изэтионовую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную,паратолуолсульфоновую кислоты и т.п. Если соединения содержат кислотные группы, пригодные фармацевтически приемлемые основно-аддитивные соли соединений по настоящему изобретению включают соли металлов, такие как соли алюминия, кальция, лития, магния, калия, натрия и цинка, или соли органических оснований, таких как хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин (N-метилглюкамин) и прокаин. Соединения формулы I являются ингибиторами Mnk2. Следовательно, указанные соединения можно использовать для лечения и профилактики диабета типа 2 и метаболических нарушений, таких как ожирение, а также ассоциированных нарушений, таких как нарушение питания, кахексия, гипертензия,коронарная болезнь сердца, гиперхолестеринемия, дислипидемия, остеоартрит, желчные конкременты,приступы апноэ во сне, нейродегенеративные нарушения, рак и другие заболевания и нарушения. Согласно настоящему изобретению некоторые производные 8-гетероарилпурина ингибируют киназы Mnk2a и Mnk2b, взаимодействующие с киназой MAP. Кроме того, авторами неожиданно установлено, что соединения по изобретению обладают также активностью в отношении Mnk1. По результатам испытаний соединения по изобретению обладают активностью одного порядка в отношении Mnk1 и Mnk2 (в испытаниях использовали Mnk2a), т.е. обычно соотношение активностей в отношении Mnk1/Mnk2 составляет от 1:20 до 20:1. Согласно WO 2005/003785 киназы Mnk (включая Mnk1 и Mnk2) являются перспективными мишенями для противовоспалительной терапии. Поскольку соединения по изобретению являются высокоэффективными ингибиторами Mnk2, а также Mnk1, как описано выше, их также можно использовать при противовоспалительной терапии. Предположение о том, что Mnk1 является перспективной мишенью для противовоспалительной терапии, подтверждается также данными Buxad и др. (Immunity, 23, 177-189 (2005, согласно которым другим субстратом Mnk1 является гетерогенный ядерный рибонуклеопротеин A1 (hnRNP), который принимает участие в синтезе TNF. Соединения по изобретению можно использовать при лечении или профилактике нарушения или состояния, ассоциированного с активностью Mnk1, Mnk2a, Mnk2b и/или FLT-3, такого как метаболические заболевания, например ожирение, а также ассоциированных нарушений, таких как нарушение питания, кахексия, сахарный диабет, гипертензия, коронарная болезнь сердца, гиперхолестеринемия, дислипидемия, гиперлипидемия, гипергликемия, остеоартрит, желчные конкременты и приступы апноэ во сне,и нарушений, связанных с защитой от активированных форм кислорода (АФК), таких как сахарный диабет, нейродегенеративные нарушения и рак, например рак репродуктивных органов, лейкоз, например острый миелоидный лейкоз (AML), и воспалительных состояний. Кроме того, соединения по изобретению можно также использовать при лечении по профилактике нарушений, ассоциированных с сигнальным путем инсулина. Примером такого нарушения является диабет типа 2. В одном объекте изобретения R3 выбирают из группы, включающей гетероарил, необязательно замещенный одним-тремя заместителями, выбранными из группы, включающей (низш.)алкил, гидрокси,(низш.)алкокси, амино, алкиламино, диалкиламино и ациламино. В другом объекте изобретения R1 выбирают из группы, включающей арил, гетероарил и C1-C10-алкил, каждый из которых необязательно замещен одним-тремя заместителями, выбранными из группы, включающей (низш.)алкил, галоген,(низш.)алкокси, галогеналкил, гидрокси, циано, нитро, амино, алкиламино, диалкиламино, аминоалкил,алкиламиноалкил, диалкиламиноалкил, меркапто, алкилтио, алкилсульфинил, алкилсульфонил, сульфон,ациламино, оксаалкил, гетероциклилалкил, диалкиламиноалкокси, (алкил)(ацил)аминоалкил, трифторметокси, ациламиноалкокси, гетероциклилалкокси и ациламиноалкил. В еще одном объекте изобретения R1 означает фенил, замещенный одним заместителем, выбранным из группы, включающей метилендиокси,галоген, алкил, аминометил, алкиламинометил, диалкиламинометил, оксаалкил, диалкиламиноалкокси,(алкил)(ацил)аминоалкил, трифторметокси, ациламиноалкокси, гетероциклилалкокси и где группа означает азотсодержащий гетероцикл, a q равно 1-3.R1 может также означать фенил или фенил, замещенный группой метилендиокси, (низш.)алкил, галоген, алкил, аминометил, алкиламинометил, диалкиламинометил, ациламино и ациламиноалкил, или если R1 означает тиенил, то n равно 2. В еще одном варианте R1 означает (низш.)алкил, а n равно 0. Кроме того, R1a может означать H. В одном объекте изобретения R2 означает C1-C3-алкил, фтор(C1-C3)алкил и циано(C1-C3)алкил. В другом объекте изобретения R2 выбирают из группы, включающей циклопропил,изопропил, 2-цианоэтил, этил, трифторэтил, водород и метил, a R3 выбирают из группы, включающей азотсодержащий гетероарил и замещенный азотсодержащий гетероарил. В еще одном объекте R3 означает группу формулы IIH, галоген, NH2, NHMe, NHEt, HMe2, NHAc, OH, OMe, OEt, Me и Et. В другом объекте R3 означает замещенный фенил или R3 выбирают из группы, включающей 4-пиридинил, 2-аминопиримидин-4-ил и 2-(метиламино)пиримидин-4-ил, или R3 выбирают из группы, включающей 4-пиридил, 4-пиримидинил,4-(2-аминопиримидил) и 4-(2-аминопиридинил). В другом варианте R1 означает фенил и фенил, замещенный группой алкокси, (низш.)алкил, галоген, аминоалкил или ациламиноалкил, n выбирают из группы, включающей 0, 1 и 2, R1a означает водород, R2 означает циклопропил, изопропил, этил, 2-цианоэтил,трифторэтил, водород и метил. В другом объекте R3 выбирают из группы, включающей 4-пиридил, 4 пиримидинил, 4-(2-аминопиримидил) и 4-(2-аминопиридинил). Настоящее изобретение также относится к способам профилактики или лечения диабета типа 2 и метаболических нарушений, таких как ожирение, благодаря обработке Mnk2-активных клеток соединениями общей формулы I, указанной выше. Другим объектом изобретения являются соединения по изобретению для применения в терапии,например для профилактики или лечения метаболических нарушений, диабета, ожирения, лейкоза, и для получения лекарственного средства, предназначенного для профилактики или лечения метаболических нарушений, диабета, ожирения и лейкоза. Кроме того, соединение формулы I выбирают из группы, включающей 9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-N-метатолил-9 Н-пурин-2-амин,N-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)-N-метилацетамид,8-(2-аминопиридин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-3-метилфенил)-9 Н-пурин-2-амин,трет-бутиловый эфир 4-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетилкарбаминовой кислоты,9-этил-N-(4-фтор-3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(3-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,N-(4-(9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)-N-метилацетамид,8-(2-аминопиримидин-4-ил)-9-этил-N-(4-этилфенил)-9 Н-пурин-2-амин,9-метил-N-(3-4-метилпиперазин-1-ил)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-8-(пиридин-4-ил)-N-(3-(трифторметокси)фенил)-9 Н-пурин-2-амин,9-этил-N-(3-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(4-(пиперазин-1-илметил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3-(2-(циклопентиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3-(аминометил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-изопропил-N-(3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)хинолин-6-амин,N-(3-хлорфенил)-9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(4-метиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-фенетил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фторфенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-изопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,9-циклопропил-N-(3-метоксифенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(3-(2-метоксиэтокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3,4-дифторфенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,4-диметилфенил)-9-этил-9 Н-пурин-2-амин,9-этил-N-(3-(2-(этиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(3-(морфолинометил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,-8 014907 9-метил-N-(4-(2-(пиперидин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(аминометил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(4-фторфенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-ортотолил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(3-этилфенил)-9 Н-пурин-2-амин,N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)хинолин-8-амин,8-(2-аминопиримидин-4-ил)-N-(4-фторфенил)-9-(2,2,2-трифторэтил)-9 Н-пурин-2-амин,N-(4-(2-аминоэтил)фенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(3-этилфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-изопропил-N-(3-метоксифенил)-8-(пиримидин-4-ил)-9 Н-пурин-2-амин,N-(4-(2-(циклопропиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)изохинолин-5-амин,N-(3-(2-(диметиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,9-этил-N-(3-(2-(пиперидин-1-ил)этокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(4-метиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-9-этил-N-(3-этилфенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-паратолил-9 Н-пурин-2-амин,9-циклопропил-N-(3,4-диметоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-8-(пиридин-4-ил)-N-(4-(2-(пирролидин-1-ил)этил)фенил)-9 Н-пурин-2-амин,9-этил-N-(4-фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фтор-2-метилфенил)-9 Н-пурин-2-амин,9-метил-8-(пиридин-4-ил)-N-(3-(2-(пирролидин-1-ил)этил)фенил)-9 Н-пурин-2-амин,N-(3-(аминометил)фенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(4-фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-метилбензил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)ацетамид,N-(3-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)ацетамид,N-(4-(аминометил)фенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-9-этил-N-(4-фторфенил)-9 Н-пурин-2-амин,N-(3-(2-(диметиламино)этокси)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(4-(пиперидин-1-илметил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3,5-дифторфенил)-9-этил-9 Н-пурин-2-амин,N-(4-(2-(диметиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9H-пурин-2-амин,9-циклопропил-8-(2-(метиламино)пиримидин-4-ил)-N-фенил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,5-дифторфенил)-9-этил-9 Н-пурин-2-амин,9-циклопропил-N-(3-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3,4-дифторфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,3-дифторфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(4-фторфенил)-9-метил-9 Н-пурин-2-амин,трет-бутиловый эфир 4-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензилкарбаминовой кислоты,9-циклопропил-N-(2,4-диметоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(3-(2-(пиперидин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(2-аминоэтил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(3-этиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-метатолил-9 Н-пурин-2-амин,N-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетил)ацетамид,8-(2-аминопиримидин-4-ил)-N-(3,4-диметилфенил)-9-этил-9 Н-пурин-2-амин,N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9-(2,2,2-трифторэтил)-9 Н-пурин-2-амин,N-(3-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)ацетамид,(4-(2-(4-фторфениламино)-9-метил-9 Н-пурин-8-ил)пиридин-2-ил)метанол,N-(4-циклопентиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2-хлор-5-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,N-(4-фторфенил)-9-метил-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(3-метоксифенил)-8-(пиримидин-4-ил)-9 Н-пурин-2-амин,N1-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)-N4,N4-диметилбензол-1,4-диамин,9-метил-8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,3-диметилфенил)-9-этил-9 Н-пурин-2-амин,N-(2,3-дигидробензо[b][1,4]диоксин-6-ил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,3-(2-(3-метоксифениламино)-8-(пиримидин-4-ил)-9 Н-пурин-9-ил)пропаннитрил,-9 014907 9-этил-N-(3-этилфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-этиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(4-(2-морфолиноэтил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-хлорпиридин-4-ил)-9-циклопропил-N-фенил-9 Н-пурин-2-амин,9-циклопропил-8-(1-метил-1H-пиррол-2-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(3-фтор-4-метилфенил)-9 Н-пурин-2-амин,9-метил-N-(4-4-метилпиперазин-1-ил)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3,5-диметилфенил)-9-этил-9 Н-пурин-2-амин,9-метил-N-(4-(морфолинометил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3-диметиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-9-этил-N-(4-фтор-3-метоксифенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3-хлорфенил)-9-этил-9 Н-пурин-2-амин,N-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетил)-N-метилацетамид,8-(2-аминопиримидин-4-ил)-N-(4-хлор-2-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,9-циклопропил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(2-фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-(2-(этиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-изопропиламино)метил)фенил)-8-(пиридин-4-ил)-9H-пурин-2-амин,9-метил-N-(4-(2-(4-метилпиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(3-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,N-(4-фторфенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-фенил-8-(пиридин-4-ил)-9H-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,3-дигидро-1H-инден-5-ил)-9-этил-9 Н-пурин-2-амин,9-этил-N-(4-(2-метоксиэтокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3-(аминометил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3-циклопентиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,3-этил-N-(4-метиламино)метил)фенил)-2-(пиридин-4-ил)-3H-имидазо[4,5-b]пиридин-5-амин,N-(4-(2-(циклопентиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(3-(2-(пиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(2-фторфенетил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-8-(пиридин-4-ил)-N-(3,4,5-триметоксифенил)-9 Н-пурин-2-амин,9-метил-8-(пиридин-4-ил)-N-(4-(пирролидин-1-илметил)фенил)-9 Н-пурин-2-амин,9-циклопропил-N-(3-этилфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,8-(6-аминопиридин-3-ил)-9-этил-N-(4-фторфенил)-9 Н-пурин-2-амин,N1-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)-N3,N3-диметилбензол-1,3-диамин,N-(3-циклопропиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,4-дифторфенил)-9-этил-9 Н-пурин-2-амин,9-циклопропил-N-(3,5-диметоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетил)ацетамид,N-(4-(9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетил)-N-метилацетамид,N-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)ацетамид,9-этил-N-(4-(2-(пиперидин-1-ил)этокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(2-метоксиэтокси)фенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-хлорпиридин-4-ил)-9-изопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-9-изопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,9-этил-N-(4-(2-(метиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-(2-морфолиноэтокси)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-N-(3,4-дифторфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2-хлорфенил)-9-этил-9 Н-пурин-2-амин,9-метил-N-(3-(пиперидин-1-илметил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(6-аминопиридин-3-ил)-9-этил-N-(3-этилфенил)-9 Н-пурин-2-амин,N-(4-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)-N-метилацетамид,9-циклопропил-8-(пиридин-3-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,N-(2,2-диметилбензо[d][1,3]диоксол-5-ил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенетил)-N-метилацетамид,9-циклопропил-8-(тиазол-2-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,6-дифторфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(2-фтор-4-метилфенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(4-хлорфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3-хлор-4-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,- 10014907 9-метил-N-(3-(2-(4-метилпиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(3-изопропиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(8-(2-аминопиримидин-4-ил)-9-циклопропил-9 Н-пурин-2-ил)хинолин-5-амин,N-(2-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)фенокси)этил)ацетамид,8-(2-хлорпиридин-4-ил)-9-циклопропил-N-(3-метоксифенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,5-диметилфенил)-9-этил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-2-метилфенил)-9 Н-пурин-2-амин,N-(4-циклопропиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(2-этилфенил)-9 Н-пурин-2-амин,N-(4-метоксифенил)-9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-8-(пиримидин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фтор-3-метоксифенил)-9 Н-пурин-2-амин,9-циклопропил-8-(1-метил-1H-имидазол-5-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,N-(бензо[d][1,3]диоксол-5-ил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(2-(диметиламино)этокси)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(бензо[d]тиазол-6-ил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-фтор-3-метоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(2,3-дигидро-1H-инден-4-ил)-9-этил-9 Н-пурин-2-амин,N-(3-(2-(циклопропиламино)этил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-фторфенил)-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-этил-N-(4-(2-(изопропиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3-хлор-2-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,3-(8-(2-аминопиримидин-4-ил)-2-(3-метоксифениламино)-9 Н-пурин-9-ил)пропаннитрил,8-(2-аминопиридин-4-ил)-N-(4-фторфенил)-9-метил-9 Н-пурин-2-амин,N-(4-фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-хлорфенил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-этилфенил)-9 Н-пурин-2-амин,9-этил-N-(4-метиламино)метил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-фторфенил)-8-(пиридин-4-ил)-9-(2,2,2-трифторэтил)-9 Н-пурин-2-амин,N-(3-(9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)ацетамид,9-метил-8-(пиридин-4-ил)-N-(3-(пирролидин-1-илметил)фенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(5-фтор-2-метилфенил)-9 Н-пурин-2-амин,8-(2-хлорпиридин-4-ил)-9-циклопропил-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(5-хлор-2-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,9-метил-N-(3-(2-морфолиноэтил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(2-метоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-хлорпиридин-4-ил)-9-этил-N-(3-этилфенил)-9H-пурин-2-амин,9-циклопропил-N-(3-метоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(2-метоксифенетил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,этиловый эфир 4-(2-(4-фторфениламино)-9-метил-9 Н-пурин-8-ил)пиколиновой кислоты,8-(2-аминопиримидин-4-ил)-N-(2-хлор-4-фторфенил)-9-циклопропил-9 Н-пурин-2-амин,N-(4-(2-аминоэтил)фенил)-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-циклопентил-9-циклопропил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-(3-фторфенил)-9 Н-пурин-2-амин,9-циклопропил-8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиридин-4-ил)-9-циклопропил-N-фенил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-N-(3-хлорфенил)-9-циклопропил-9 Н-пурин-2-амин,N-(4-(аминометил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(4-(9-метил-8-(пиридин-4-ил)-9 Н-пурин-2-иламино)бензил)-2,2,2-трифторацетамид,9-этил-N-(3-(2-(изопропиламино)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,N-(3,4-дифторфенил)-9-этил-8-(2-(метиламино)пиримидин-4-ил)-9 Н-пурин-2-амин,9-метил-N-(3-(пиперазин-1-илметил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-изобутил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-этил-8-(2-(метиламино)пиримидин-4-ил)-N-метатолил-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-циклопропил-N-фенил-9 Н-пурин-2-амин,9-циклопропил-8-(1H-пиррол-2-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-(4-фторфенил)-9 Н-пурин-2-амин,8-(2-аминопиримидин-4-ил)-9-этил-N-метатолил-9 Н-пурин-2-амин,9-метил-N-(4-(2-(пиперазин-1-ил)этил)фенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин,N-(4-диметиламино)метил)фенил)-9-этил-8-(пиридин-4-ил)-9 Н-пурин-2-амин,9-циклопропил-N-(4-метоксифенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин,- 11014907 8-(2-аминопиримидин-4-ил)-9-этил-N-(5,6,7,8-тетерагидронафталин-1-ил)-9 Н-пурин-2-амин. Композиции можно вводить отдельно или в комбинации с другим агентом, лекарственным средством или гормоном и любым приемлемым способом. Фармацевтические композиции для применения по изобретению включают активные ингредиенты в количестве, эффективном для достижения требуемой цели. Эффективная доза также определяется специалистом в данной области. Наряду с лечением диабета типа 2 и метаболических нарушений, например ожирения, такую фармацевтическую композицию можно использовать для лечения кахексии, остеоартрита, желчных конкреций, приступов апноэ во сне, нейродегенеративных нарушений и рака. В описании примеров используются следующие сокращения:AcOH - уксусная кислота,CDCl3 - дейтерированный хлороформ,CD3OD - дейтерированный метанол,(CD3)2SO - дейтерированный диметилсульфоксид, - химический сдвиг относительно сигнала тетраметилсилана,DMA - N,N-диметилацетамид,ДМСО - диметилсульфоксид,Et - этил,Et3N - триэтиламин,EtOAc - этилацетат,ESI - ионизация электрораспылением,1 Н ЯМР - протонный ядерно-магнитный резонанс,iPr2Net - диизопропилэтиламин,MeOH - метанол (CH3OH),MHz - мегагерц,Ph - фенил,ТФУ - трифторуксусная кислота,ТГФ - тетрагидрофуран. Анализ биологической активности Анализ киназы Mnk1 in vitro (HTRF) Ингибирующую активность в отношении Mnk1 определяли с использованием рекомбинантной полноразмерной Mnk1 человека, включающей N-концевую GST-метку (глутатион-S-трансфераза,GST-Mnk2A). Гибридный белок экспрессировали в клетках Sf9 и очищали с использованием колонки,содержащей глутатион-сефарозу 4 FF. Для определения активности Mnk1 in vitro использовали анализ флуоресценции с разрешением во времени в гомогенной среде (HTRF). В указанном анализе использовали биотинилированный 18-членный пептид, который является частью аминокислотной последовательности фактора транскрипции CREB (биотин-AGAGKRREILSRRPSYRK, фирма NeoMPS). Количество фосфорилированного CREB-пептида оценивали методом HTRF с использованием в качестве донора конъюгата европия (Eu3+) и фосфоспецифичных антител (CREB Ser133, фирма Cisbio International), а в качестве акцептора, меченного стрептавидином, - XL665 (сшитого аллофикоцианина, StrepXLent, фирма CisbioInternational). При проведении анализа использовали реакционную смесь для определения киназы(БСА в буферном растворе следующего состава: 50 мМ HEPES, рН 7,6, 0,25 мМ MnCl2, 1 мМ дитиотреит (DTT) и 0,001% Твин 20. Реакционную смесь для определения киназы инкубировали в течение 30 мин при комнатной температуре. Реакцию останавливали при добавлении конъюгата криптата Eu3+ и фосфоспецифичных антител (CREB Ser133), содержащего 0,6 М фторид калия. Реакцию останавливали при конечной концентрации фторида калия 0,3 М. Стадию детектирования проводили при добавлении стрептавидина/XL665. Конечная концентрация донора и акцептора составляла 0,2 и 42 нМ соответственно. Реагенты для детектирования растворяли в буферном растворе следующего состава: 50 мМ Hepes,pH 7,0, 0,6 М фторид калия и 0,1% БСА. Смесь инкубировали в течение 1 ч при комнатной температуре,а затем анализировали на планшете-ридере (Wallac Victor2 V) методом HTRF при длине волны возбуждения 340 нМ и длине волны испускания криптата Eu3+и акцептора XL665 615 и 665 нМ соответственно. Данные HTRF представляют собой соотношение интенсивности флуоресценции при 665 нМ и флуоресценции при 615 нМ, поскольку такое отношение не зависит от оптических свойств среды при указанной длине волны возбуждения. Для оценки величины IC50 получали 10-мМ исходные растворы анализируемых соединений в 100% ДМСО. Соединения добавляли в смесь для определения киназы в разведении 1:100 и обычно анализировали в серийном разведении (11 концентраций) и в трехкратном повторе в каждой точке. По данным анализа соотношение активностей соединений в отношении Mnk1 и Mnk2a составляет от 11:0,1, т.е. приблизительно от 10:1 до 1:10. Таким образом, можно считать, что соединения по настоящему изобретению обладают активностями в отношении Mnk1 и Mnk2a, соотношение которых составляет от 1:20 до 20:1.- 12014907 Материалы Ингибирующую активность в отношении Mnk2a определяли с использованием рекомбинантной полноразмерной Mnk2a человека, включающей N-концевую GST-метку (глутатион-S-трансфераза,GST-Mnk2A). Гибридный белок экспрессировали в клетках Sf9 и очищали с использованием колонки,содержащей глутатион-сефарозу FF, в сочетании с последующей гель-фильтрацией. Реагенты для анализа флуоресценции с разрешением во времени в гомогенной среде включали биотинилированный CREBпептид (биотинил-Ala-Gly-Ala-Gly-Lys-Arg-Arg-Glu-Ile-Leu-Ser-Arg-Arg-Pro-Ser-Tyr-Arg-Lys, фирмаNeoMPS, Strasbourg, Франция), конъюгат криптата европия и меченых антител антифосфо-CREB(Ser133) (фирма CisUS, Bedford, MA) и Strept/XLent (фирма CisUS). Буферный раствор включал HEPES(БСА), аденозинтрифосфат, дитиотреит, фторид калия и диметилсульфоксид (ДМСО, фирма SigmaAldrich, St. Louis, МО). Анализ проводили в 1536-луночных планшетах белого цвета (фирма Nunc). Ингибирующую активность в отношении FLT-3 оценивали с использованием рекомбинантного цитоплазматического домена (аминокислоты 564-958) FLT-3 человека, содержащего С-концевую гистидиновую метку, экспрессированного в клетках насекомого и активированного in vitro за счет аутофосфорилирования (фирма Invitrogen, Carlsbad, CA). Реагенты для анализа флуоресценции с разрешением во времени в гомогенной среде включали биотинилированный поли(Glu,Ala,Tyr)пептид (фирма Sigma-Aldrich,St. Louis, МО), содержащие метку европия антитела антифосфотирозин (РТ 66, фирма PerkinElmer,Waltham, MA) и StreptXLent (фирма CisUS, Bedford, MA). Буферный раствор включал HEPES (фирмаBioWhittaker/Cambrex, Walkersville, MD), хлорид магния, ортованадат натрия, бычий сывороточный албумин (БСА), аденозинтрифосфат, дитиотреит, тритон Х-100, этилендиаминтетрауксусную кислоту(ЭДТА) и диметилсульфоксид (ДМСО, фирма Sigma-Aldrich, St. Louis, МО). Анализ проводили в 384-луночных планшетах черного цвета (фирма Corning-Costar). Определение ингибирования Mnk2 Анализируемые соединения серийно разбавляли 100% ДМСО до конечной концентрации (50), а затем разбавляли (25) концентрированным (2) раствором АТФ/CREB-субстрат в буферном растворе для анализа (50 мМ HEPES, pH 7,6, 0,25 мМ MnCl2, 1 мМ дитиотреит, 0,05% БСА). В лунках планшета смешивали 2 мкл раствора соединения/АТФ/CREB-субстрата с 2 мкл буферного раствора для анализа. Конечная концентрация реагентов составляла 160 нМ CREB-пептид, 0,5 мкМ АТФ и 0,06 нМ ферментаMnk2a, 2% ДМСО. Киназную реакцию проводили в течение 30 мин при 25 С. Для детектирования использовали растворы (по 2 мкл каждого) следующего состава: 2 мкг/мл стрепт-XLent (партия 8) и криптат/антитела антифосфо-CREB (0,14 мкг/мл, партия 4) в буферном растворе для анализа (50 мМHEPES, рН 7,0, 0,6 М KF, 0,1% БСА). В каждую лунку добавляли по 2 мкл растворов для детектирования и реакционную смесь инкубировали в течение 4-16 ч. Флуоресценцию с разрешением по времени измеряли при двух комбинациях длин волн (340/671 и 340/618 нМ) на планшет-ридере Perkin Elmer, Boston,MA). Данные аппроксимировали с использованием уравнения сигмоидальной зависимости от дозы с переменной крутизной (пакет программ GraphPad Prism и GraphPad Software, San Diego, CA). Определение ингибирования FLT-3 Анализируемые соединения серийно разбавляли 100% ДМСО до конечной концентрации (100), а затем разбавляли реакционной смесью следующего состава: буферный раствор для анализа (50 мМHEPES, рН 7,6, 0,2 мМ Na3VO4, 10 мМ MrCl2, 1 мМ дитиотреит, 0,01% БСА, 0,01% тритон X-100),0,12 мкг/мл FLT-3, 1,4 мкг/мл биотинилированный поли(Glu,Ala,Tyr), 3 мкМ АТФ и 1% ДМСО. Объем реакционной смеси составлял 21 мкл (7 мкл раствора анализируемого соединения в буферном растворе/3,3% ДМСО, 7 мкл раствора фермента и 7 мкл биотин-поли(Glu,Ala,Tyr)/АТФ). Киназную реакцию проводили в течение 1 ч в темноте при 25 С. Для детектирования в каждую лунку добавляли по 10 мкл раствора реагентов следующего состава: 2 мкг/мл стрепт-XLent/0,8 мкг/мл Eu-РТ 66 в 50 мМ HEPES,рН 7,6, 12 мМ EDTA, 0,05% БСА. Смесь инкубировали в течение 1 ч в темноте при 25 С и измеряли флуоресценцию с разрешением по времени в гомогенной среде на планшет-ридере Victor V (фирмаPerkin Elmer, Waltham, MA) при 340/665 и 340/615 нМ. Данные аппроксимировали с использованием уравнения сигмоидальной зависимости от дозы с переменной крутизной (пакет программ GraphPad Prism и GraphPad Software, San Diego, CA). В указанных условиях стауроспорин ингибировал FLT-3 при величине IC50 0,5 нМ. Примеры Пример 1. Синтез производных аминопурина. Соединения формулы I синтезировали обычным органическим синтезом, известным специалисту в данной области техники. Примеры синтеза соединений формулы I показаны, без ограничения перечисленным, ниже на схеме 1 Соединения формулы I получали из коммерческого препарата 2,4-дихлор-5-нитропиримидина по схеме, включающей четыре стадии. Первичный амин (R2-NH2) N-арилировали по реакции с 2,4-дихлор 5-нитропиримидином с образованием смеси (обычно 10:1) региоизомеров, которые разделяли экспрессхроматографией. Затем преобладающий региоизомер (соответствующий замещению по С-4, I-1) модифицировали, присоединяя второй первичный амин (R1-NH2) по C-2 (I-2), и после восстановления нитрогруппы получали промежуточный продукт I-3. Соединение I-3 конденсировали с альдегидом при нагревании в DMA, при этом получали соответствующее производное пурина I-4. Соединения формулы I получали по аналогичным методикам. Методика А. 2-Хлор-N-циклопропил-5-нитропиримидин-4-амин (продукт 1 (I-1. В 10,0 г (53 ммоль, 1,0 экв.) 2,4-дихлор-5-нитропиримидина в 40 мл ТГФ при -78 С добавляли 22 мл(120 ммоль, 2,2 экв.) N,N-диизопропилэтиламина и 3,7 мл (53 ммоль, 1,0 экв.) циклопропиламина. Реакционную смесь перемешивали при -78 С в течение 30 мин, затем нагревали до комнатной температуры и перемешивали в течение еще 1 ч. Растворитель удаляли в вакууме, при этом получали твердое вещество желтого цвета. Продукт очищали экспресс-хроматографией (элюент: 15% EtOAc/гексан), при этом получали 8,8 г (8,1 ммоль, 77%) 2-хлор-N-циклопропил-5-нитропиримидин-4-амина (I-1) в виде твердого вещества желтого цвета. Методика В. N4-Циклопропил-N2-(2-(тиофен-2-ил)этил)пиримидин-2,4,5-триамин (промежуточное соединение 3 (I-3. В раствор 0,2 г (0,93 ммоль, 1,0 экв.) 2-хлор-N-циклопропил-5-нитропиримидин-4-амина (I-1) в 5 мл ТГФ добавляли 0,19 мл (1,4 ммоль, 1,5 экв.) триэтиламина и 0,14 г (1,1 ммоль, 1,2 экв.) 2-тиофенэтиламина. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и добавляли 2 мл ТГФ. Затем добавляли раствор 1,0 г (5,7 ммоль, 85% тех., 6,0 экв.) гидросульфита натрия и 1,0 г(12 ммоль, 13 экв.) гидрокарбоната натрия в 10 мл воды и смесь интенсивно перемешивали при комнатной температуре в течение 1 ч. Смесь разбавляли 20 мл EtOAc и промывали 10 мл насыщенного солевого раствора. Органический слой сушили (Na2SO4) и растворитель удаляли в вакууме, при этом получали 0,16 г неочищенного N4-циклопропил-N2-(2-(тиофен-2-ил)этил)пиримидин-2,4,5-триамина (I-3). Методика С. 9-Циклопропил-8-(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амин (промежуточное соединение 4 (I-4. В раствор 0,032 г (0,12 ммоль, 1,0 экв.) N4-циклопропил-N2-(2-(тиофен-2-ил)этил)пиримидин-2,4,5 триамина (I-3) в 5 мл DMA добавляли 0,05 мл (0,38 ммоль, 3,2 экв.) 4-пиридинкарбоксальдегида. Смесь перемешивали при 140 С в течение 16 ч и растворитель удаляли в вакууме. Продукт очищали экспрессхроматографией (элюент: EtOAc), при этом получали 0,015 г (0,04 ммоль, 35%) 9-циклопропил-8(пиридин-4-ил)-N-(2-(тиофен-2-ил)этил)-9 Н-пурин-2-амина (I-4) в виде твердого вещества желтого цвета. В другом варианте соединения формулы I получали 4-стадийным синтезом из коммерческого препарата 2,4-дихлор-5-нитропиримидина (схема 2) по модифицированной методике, включающей синтез- 14014907 промежуточного 2-хлорпурина (I-6). Первичный амин (R2-NH2) N-арилировали 2,4-дихлор-5-нитропиримидином с образованием соединения I-1 (см. выше). Затем в соединении I-1 восстанавливали нитрогруппу и из соединения I-5 по реакции с альдегидом в DMA при 140 С получали промежуточный 2-хлорпурин (I-6). 2-Аминопурин получали по реакции соединения I-6 с амином (R1-NH2) в присутствииBINAP, Pd2(dba)3 и трет-t-BuONa при 160 С. Примеры синтеза соединений формулы I подробно описаны,без ограничения перечисленным, в методиках D-F. Схема 2 В раствор 10,0 г (50 ммоль, 1,0 экв.) 2-хлор-N-этил-5-нитропиримидин-4-амина (I-1) в 300 мл ТГФ добавляли 4,0 г никеля Ренея. Раствор перемешивали при 1 атм водорода при комнатной температуре в течение 12 ч. Реакционную смесь фильтровали через Celite и слой сорбента промывали 100 мл ТГФ. Растворитель удаляли в вакууме, при этом получали 8,0 г (46 ммоль, 92%) 2-хлор-N4-этилпиримидин-4,5 диамина (I-5). Методика Е. 2-Хлор-9-этил-8-(пиридин-4-ил)-9 Н-пурин (промежуточное соединение 6 (I-6.AcOH/DMA добавляли 6,0 мл (65 ммоль, 1,3 экв.) 4-пиридинкарбоксальдегида и смесь нагревали при 140 С в течение 14 ч. Смесь охлаждали до комнатной температуры и растворитель удаляли в вакууме. Продукт очищали препаративной ЖХВР, при этом получали 2,0 г (7,7 ммоль, 15%) 2-хлор-9-этил-8(пиридин-4-ил)-9 Н-пурина (I-6). Методика F. Получение промежуточного соединения 4 (I-4). В раствор 60 мг (0,23 ммоль, 1,0 экв.) 2-хлор-9-этил-8-(пиридин-4-ил)-9 Н-пурина (I-6) в 3 мл 1,4-диоксана добавляли 0,46 ммоль (2,0 экв.) первичного амина (R1-NH2), а затем 10 мг (0,016 ммоль,0,07 экв.) BINAP, 10 мг (0,01 ммоль, 0,05 экв.) Pd2(dba)3 и 30 мг (0,31 ммоль, 1,4 экв.) трет-BuONa. Реакционную смесь нагревали в микроволновом реакторе при температуре смеси 160 С в течение 40 мин. Смесь фильтровали и фильтрат концентрировали в вакууме. Полученный продукт очищали препаративной ЖХВР, при этом получали соединение I-4. Пиримидинкарбоксальдегиды, которые не являются коммерческими препаратами, синтезировали методами, известными в данной области техники. Примеры синтеза таких пиримидинкарбоксальдегидов подробно описаны, без ограничения перечисленным, в методиках G-K.(10 ммоль, 1,0 экв.) диоксида селена. Полученную смесь нагревали при 100 С в течение 5 ч, а затем охлаждали до комнатной температуры. В смесь добавляли еще 0,25 г (2,3 ммоль, 0,23 экв.) диоксида селена и реакционную смесь нагревали при 100 С в течение еще 1 ч. Затем смесь охлаждали до комнатной температуры и фильтровали через Celite. Слой целита промывали 200 мл этилацетата и фильтрат концентрировали в вакууме. Полученное масло темно-коричневого цвета суспендировали в 200 мл дихлорметана и фильтровали. Растворитель удаляли в вакууме, при этом получали 0,3 г (2,8 ммоль, 28%) пиримидин-4-карбоксальдегида (I-7) в виде масла темно-коричневого цвета. Методика H. Диметилацеталь 2-аминопиримидин-4-карбоксальдегида (промежуточное соединение 8 (I-8. Раствор 5,5 мл (41 ммоль, 1,0 экв.) диметилацеталя диметилформамида и 5,0 мл (41 ммоль, 1,0 экв.) диметилацеталя пируватальдегида нагревали при 100 С в течение 16 ч. Метанол удаляли в вакууме, при этом получали масло коричневого цвета. В раствор 4,3 г (45 ммоль, 1,1 экв.) гидрохлорида гуанидина в 10 мл воды добавляли раствор 1,8 г (45 ммоль, 1,1 экв.) гидроксида натрия в 5 мл воды. Полученный раствор добавляли в указанное выше масло и смесь перемешивали при комнатной температуре в течение 48 ч. Смесь фильтровали, при этом получали 2,5 г (15 ммоль, 36%) диметилацеталя 2-аминопиримидин 4-карбоксальдегида (I-8). Методика I. 2-Аминопиримидин-4-карбоксальдегид (промежуточное соединение 9 (I-9. Раствор 2,5 г (15 ммоль, 1,0 экв.) диметилацеталя 2-аминопиримидин-4-карбоксальдегида (I-8) в 16 мл (48 ммоль, 3,2 экв.) 3 М HCl нагревали при 48 С в течение 14 ч. Смесь охлаждали до комнатной температуры и разбавляли 50 мл EtOAc. Водный слой нейтрализовали при добавлении NaHCO3, а затем экстрагировали EtOAc (550 мл). Объединенные органические экстракты сушили (Na2SO4) и растворитель удаляли в вакууме, при этом получали 0,69 г (5,6 ммоль, 37%) 2-аминопиримидин-4 карбоксальдегида (I-9) в виде твердого вещества желтого цвета. Методика J. Диметилацеталь 2-метиламинопиримидин-4-карбоксальдегида (промежуточное соединение 10 (I-10. Раствор 5,5 мл (41 ммоль, 1,0 экв.) диметилацеталя диметилформамида и 5,0 мл (41 ммоль, 1,0 экв.) диметилацеталя пируватальдегида нагревали при 100 С в течение 16 ч. Метанол удаляли в вакууме, при этом получали масло коричневого цвета. В раствор 15 мл этоксида натрия (21% раствор в этаноле,41 ммоль, 1,0 экв.) добавляли 4,5 г (41 ммоль, 1,0 экв.) гидрохлорида метилгуанидина, смесь перемешивали в течение 10 мин, а затем добавляли 15 мл раствора полученного масла в безводном этаноле. Смесь кипятили с обратным холодильником в течение 24 ч, охлаждали до комнатной температуры и фильтровали. Растворитель удаляли в вакууме, при этом получали диметилацеталь 2-метиламинопиримидин-4 карбоксальдегида (I-10) в виде масла темно-коричневого цвета, которое использовали на следующей стадии без дополнительной очистки. 2-Метиламинопиримидин-4-карбоксальдегид (I-11) получали из неочищенного диметилацеталя 2-метиламинопиримидин-4-карбоксальдегида (I-10), полученного по методике J, в виде пены темнокоричневого цвета (1,7 г, 30% из диметилацеталя диметилформамида) по методике I получения 2-аминопиримидинкарбоксальдегида (I-9). Соединения формулы I (типа I-4) можно затем модифицировать за счет алкилирования С-2 аминогруппы по реакции с алкилгалогенидом. Пример синтеза соединений формулы I за счет алкилирования С-2 аминогруппы описан, без ограничения перечисленным, в методике L. Методика L. 9-Циклопропил-N-(3-метоксифенил)-N-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амин продукт 12 (I-12. В раствор 4,3 мг (0,012 ммоль, 1,0 экв.) 9-циклопропил-N-(3-метоксифенил-8-(пиридин-4-ил)-9 Нпурин-2-амина (синтезированного по методикам А-С) в 1 мл ДМФА добавляли 0,03 мл (0,48 ммоль,40 экв.) йодистого метила и 20 мг (0,48 ммоль, 40 экв.) гидроксида натрия. Реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Затем смесь фильтровали и фильтрат концентрировали в вакууме. Продукт очищали методом полупрепаративной ЖХВР, при этом получали 1,9 мг (42%) 9-циклопропил-N-(3-метоксифенил)-N-метил-8-(пиридин-4-ил)-9 Н-пурин-2-амина. Соединения формулы I, в которых R3 означает 4-пиридил, а аминогруппа находится в положении 2 пиридинового цикла соединения (I-14), синтезировали по методике, описанной в статье Huang X., Buchwald S.L. Org. Lett., 3, 3417 (2001) (схема 3). Промежуточные соединения типа I-13 синтезировали по методикам А-С. Схема 3 Соединения общей формулы I-15 и I-16 синтезировали из соответствующего 2-хлорпиридина (I-13),как показано на схеме 4. Схема 4 Примеры синтеза соединений общей формулы I-15 и I-16 подробно описаны, без ограничения пере- 17014907 численным, в методиках M-N. Методика M. Этиловый эфир 4-(2-(4-фторфениламино)-9-метил-9 Н-пурин-8-ил)пиколиновойкислоты (продукт 15 (I-15. В суспензию 0,8 г (2,3 ммоль, 1,0 экв.) 8-(2-хлорпиридин-4-ил)-N-(4-фторфенил)-9-метил-9 Н-пурин 2-амина (I-13) в 20 мл EtOH и 10 мл триэтиламина добавляли 160 мг (0,23 ммоль, 0,10 экв.) Pd(PPh3)Cl2. Смесь нагревали при 70 С в течение 18 ч при постоянном насыщении CO. Летучие компоненты удаляли в вакууме и полученный остаток фракционировали экспресс-хроматографией (элюент: EtOAc/гексан),при этом получали 42 мг соединения I-15 и 700 мг исходного соединения I-13. Методика N. (4-(2-(4-Фторфениламино)-9-метил-9 Н-пурин-8-ил)пиридин-2-ил)метанол (продукт 16 В раствор 30 мг (0,077 ммоль, 1,0 экв.) этилового эфира 4-(2-(4-фторфениламино)-9-метил-9 Нпурин-8-ил)пиколиновой кислоты (I-15) в 3 мл этанола добавляли 58 мг (1,5 ммоль, 20 экв.) боргидрида натрия и смесь перемешивали при комнатной температуре в течение 16 ч. Летучие компоненты удаляли в вакууме и полученный остаток фракционировали полупрепаративной ЖХВР, при этом получали 0,9 мг(3%) (4-(2-(4-фторфениламино)-9-метил-9 Н-пурин-8-ил)пиридин-2-ил)метанола (I-16). Соединения формулы I, типа соединения I-4, в которых R2 означает водород, синтезировали за счет включения 2,4-диметоксибензила (в положение R2) по методикам А-С с образованием соединения I-17. После дебензилирования соединения I-17 при обработке кислотой получали соединение I-18 (схема 5). Схема 5 Примеры синтеза соединений общей формулы I-18 подробно описаны, без ограничения перечисленным, в методике O. Методика О. N-(4-Фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амин (продукт 18 (I-18. Раствор 46 мг (0,1 ммоль, 1,0 экв.) 9-(2,4-диметоксибензил)-N-(4-фторфенил)-8-(пиридин-4-ил)-9 Нпурин-2-амина (I-17) в 0,6 мл дихлорметана и 2,4 мл ТФУ перемешивали при комнатной температуре в течение 4 ч. Затем в смесь порциями добавляли 1 мл Et3SiH и полученную реакционную смесь перемешивали при комнатной температуре в течение еще 1 ч. Летучие компоненты удаляли в вакууме и полученный остаток фракционировали полупрепаративной ЖХВР, при этом получали 7,3 мг (24%) N-(4 фторфенил)-8-(пиридин-4-ил)-9 Н-пурин-2-амина (I-18). Амины и анилины, которые не являются коммерческими препаратами, синтезировали методами,известными в данной области техники. Примеры синтеза таких аминов и анилинов для включения в состав группы R1 в соединениях формулы I подробно описаны, без ограничения перечисленным, ниже. Требуемые соединения синтезировали из таких нестандартных аминов и анилинов по методикам, показанным на предыдущих схемах. Соединения общей формулы I-20 синтезировали в две стадии из соответствующих N-Boc-аминофенолов, которые сначала O-алкилировали при взаимодействии с алкилгалогенидами, а затем в полученном соединении I-19 удаляли защитную группу с образованием соединения I-20 (схема 6). Примеры синтеза соединений общей формулы I-20 подробно описаны, без ограничения перечисленным, в методике P. Методика P. 4-(2-Морфолиноэтокси)бензоламин (промежуточное соединение 20 (I-20. В раствор 0,1 г (0,48 ммоль, 1,0 экв.) трет-бутил-4-гидроксифенилкарбамата в 5 мл 1,4-диоксана добавляли 0,13 г (0,72 ммоль, 1,5 экв.) 4-(2-хлорэтил)морфолина и 0,47 г (1,43 ммоль, 3,0 экв.) карбоната цезия. Суспензию нагревали при 90 С в течение 16 ч. Реакционную смесь охлаждали до комнатной температуры, фильтровали и растворитель удаляли в вакууме, при этом получали трет-бутил-4-(2-морфолиноэтокси)фенилкарбамат (I-19). Продукт растворяли в 30 об.% ТФУ/дихлорметане и полученную смесь перемешивали при комнатной температуре в течение 1 ч. Растворитель удаляли в вакууме, остаток растворяли в дихлорметане, раствор промывали насыщенным раствором MaHCO3, сушили (Na2SO4) и растворитель удаляли в вакууме, при этом получали 95 мг (0,43 ммоль, 95%) (4-(2-морфолиноэтокси)бензоламина (I-20). Соединения общей формулы I-22 синтезировали в две стадии из соответствующего нитрофенилалкиламина. Нитрофенилалкиламин ацилировали, а затем в полученном продукте восстанавливали нитрогруппу, при этом получали соединения I-22 (схема 7). Схема 7 Примеры синтеза соединений общей формулы I-22 подробно описаны, без ограничения перечисленным, в методиках Q-R. Методика Q. N-(4-Нитробензил)ацетамид (промежуточное соединение 21 (I-21. В раствор 8,0 г (42 ммоль, 1,0 экв.) гидрохлорида (4-нитрофенил)метанамина в 40 мл дихлорметана и 28 мл (340 ммоль, 8,0 экв.) пиридина добавляли 16 мл (170 ммоль, 4,0 экв.) уксусного ангидрида. Смесь перемешивали при комнатной температуре в течение 16 ч и разбавляли 200 мл дихлорметана. Органический слой промывали насыщенным солевым раствором, сушили (Na2SO4) и растворитель удаляли в вакууме, при этом получали 8,0 г (41 ммоль, 98%) N-(4-нитробензил)ацетамида (I-21). В раствор 4,0 г (21 ммоль, 1,0 экв.) N-(4-нитробензил)ацетамида (I-21) в 100 мл ТГФ добавляли каталитическое количество никеля Ренея и смесь перемешивали при 1 атм водорода при комнатной температуре в течение 16 ч. Затем смесь фильтровали через Celite, слой сорбента промывали 100 мл ТГФ и растворитель удаляли в вакууме, при этом получали 3,4 г (21 ммоль, 100%) N-(4-аминобензил)ацетамида(I-22). Соединения общей формулы I-26 синтезировали из соответствующего нитрофенилалкилового спирта (схема 8). Первичный спирт (I-23) мезилировали с образованием соединения I-24, из которого алкилированием амина (NHR(R' получали соединение I-25. После восстановления нитрогруппы в соединении I-25 получали соединение I-26. Схема 8 Примеры синтеза соединений общей формулы I-26 подробно описаны, без ограничения перечисленным, в методиках S-U. Методика S. 3-Нитрофенетилметансульфонат (промежуточное соединение 24 (I-24. В раствор 1,6 г (10 ммоль, 1,0 экв.) 2-(3-нитрофенил)этилового спирта (I-23) (ред) в 20 мл дихлорметана добавляли 2,8 мл (20 ммоль, 2,0 экв.) триэтиламина. Затем добавляли раствор 1,7 г (10 ммоль,1,0 экв.) ангидрида метансульфоновой кислоты в 10 мл дихлорметана и смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь промывали насыщенным солевым раствором,органический слой сушили (Na2SO4) и растворитель удаляли в вакууме. Полученные остаток фракционировали экспресс-хроматографией, при этом получали 2,2 г (9,0 ммоль, 90%) 3-нитрофенетилметансульфоната (I-24). Методика T. 1-(3-Нитрофенетил)пиперидин (промежуточное соединение 25 (I-25. В смесь 0,49 г (2,0 ммоль, 1,0 экв.) 3-нитрофенетилметансульфоната (I-24) и 0,55 г (6,0 ммоль,3,0 экв.) карбоната калия в 20 мл ацетонитрила добавляли 0,4 мл (4,0 ммоль, 2,0 экв.) пиперидина. Реакционную смесь кипятили с обратным холодильником при перемешивании в течение 16 ч. Затем смесь охлаждали до комнатной температуры, фильтровали и растворитель удаляли в вакууме. Продукт очищали препаративной ТСХ, при этом получали 0,35 г (1,5 ммоль, 75%) 1-(3-нитрофенетил)пиперидина (I-25). В раствор 0,2 г (0,85 ммоль, 1,0 экв.) 1-(3-нитрофенетил)пиперидина (I-25) в 15 мл ТГФ добавляли 30 мг никеля Ренея. Реакционную смесь перемешивали при 1 атм водорода при комнатной температуре в течение 16 ч. Затем смесь фильтровали через Celite и растворитель удаляли в вакууме, при этом получали 3-(2-(пиперидин-1-ил)этил)бензоламин (I-26). Соединения общей формулы I-28 синтезировали из соответствующего галогенметилнитробензола(схема 9). При алкилировании амина (NHR(R' галогенметилбензолом получали соединение I-27. После восстановления нитрогруппы в соединении I-27 получали соединение I-28. Схема 9 Примеры синтеза соединений общей формулы I-26 подробно описаны, без ограничения перечисленным, в методиках V-W. Методика V. 1-(4-Нитробензил)пиперидин (промежуточное соединение 27 (I-27. В раствор 0,34 г (2,0 ммоль, 1,0 экв.) 1-(хлорметил)-4-нитробензола в 20 мл ацетонитрила добавляли 0,83 г (6,0 ммоль, 3,0 экв.) карбоната натрия и 0,4 мл (4,0 ммоль, 2,0 экв.) пиперидина. Реакционную смесь кипятили с обратным холодильником в течение 16 ч. Затем смесь охлаждали до комнатной температуры, фильтровали и растворитель удаляли в вакууме. Полученный продукт очищали препаративной ТСХ, при этом получали 0,31 г (1,4 ммоль, 70%) 1-(4-нитробензил)пиперидина (I-27). Методика W. 4-(Пиперидин-1-илметил)бензоламин (промежуточное соединение 28 (I-28. В раствор 0,22 г (1,0 ммоль, 1,0 экв.) 1-(4-нитробензил)пиперидина (I-27) в 20 мл ТГФ добавляли 30 мг никеля Ренея и реакционную смесь перемешивали при комнатной температуре при 1 атм водорода в течение 12 ч. Затем смесь фильтровали через Celite и растворитель удаляли в вакууме, при этом получали 4-(пиперидин-1-илметил)бензоламин (I-28). Соединения общей формулы I-31 синтезировали из соответствующего галогенметилнитробензола(схема 10). При алкилировании первичного амина (R-NH2) галогенметилбензолом получали соединениеI-29. Вторичную аминогруппу защищали, например, трет-бутоксикарбонил защитной группой с образованием соединения I-30. После восстановления нитрогруппы в соединении I-30 получали соединение Примеры синтеза соединений общей формулы I-31 подробно описаны, без ограничения перечис- 21014907 ленным, в методиках X-Z. После завершения синтеза в соединениях общей формулы I-31 удаляли трет-бутоксикарбонил защитные группы, при этом получали соединения формулы I. Методика X. N-(4-Нитробензил)этанамин (промежуточное соединение 29 (I-29. В смесь 0,34 г (2,0 ммоль, 1,0 экв.) 1-(хлорметил)-4-нитробензола и 1,38 г (10 ммоль, 5,0 экв.) карбоната натрия в 20 мл ацетонитрила добавляли 0,33 г (4,0 ммоль, 2,0 экв.) гидрохлорида этиламина и реакционную смесь кипятили с обратным холодильником в течение 16 ч. Затем смесь охлаждали до комнатной температуры, фильтровали и растворитель удаляли в вакууме, при этом получали 0,18 г В раствор 0,18 г (1,0 ммоль, 1,0 экв.) N-(4-нитробензил)этанамина (I-29) и 0,28 мл (2,0 ммоль,2,0 экв.) триэтиламина в 20 мл дихлорметана добавляли 0,44 г (2,0 ммоль, 2,0 экв.) ди-трет-бутилдикарбоната и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Полученный раствор промывали 1 М раствором NaHCO3 и насыщенным солевым раствором. Органический слой сушили (Na2SO4) и растворитель удаляли в вакууме. Полученный продукт очищали препаративной ТСХ,при этом получали 0,25 г (0,9 ммоль, 89%) трет-бутил-4-нитробензил(этил)карбамата (I-30). Методика Z. трет-Бутил-4-нитробензил(этил)карбамат (промежуточное соединение 31 (I-31. В раствор 0,15 г (0,53 ммоль, 1,0 экв.) трет-бутил-4-нитробензил(этил) карбамата (I-30) в 10 мл ТГФ добавляли 30 мг никеля Ренея и реакционную смесь перемешивали при комнатной температуре при 1 атм водорода в течение 12 ч. Затем реакционную смесь фильтровали через Celite и растворитель удаляли в вакууме, при этом получали трет-бутил-4-нитробензил(этил)карбамат (I-31). Анализ методом ЖХВР Метод А. Система: Waters Millenium 2690/996PDA, колонка: Phenomonex Luna, 3 мкм, С 8,504,6 мм, элюент: градиент вода (0,1% ТФУ)/ацетонитрил, скорость элюирования: 1 мл/мин. Программа элюирования: 0-1 мин, 10% вода (0,1% ТФУ)/ацетонитрил,1-7 мин, линейный градиент: вода (0,1% ТФУ)/ацетонитрил, от 10 до 90%,7-9 мин, 90% вода (0,1% ТФУ)/ацетонитрил,9-10 мин, линейный градиент: вода (0,1% ТФУ)/ацетонитрил, от 90 до 10%,10-12 мин, 10% вода (0,1% ТФУ)/ацетонитрил. Метод В. Система: Waters Millenium 2690/996PDA, колонка: Phenomenex Columbus, 5 мкм, С 18, 1002,00 мм,элюент: градиент вода (0,1% ТФУ)/ацетонитрил, скорость элюирования: 0,4 мл/мин. Программа элюирования: 0-0,5 мин, 10% вода (0,05% ТФУ)/ацетонитрил,0,5-5,5 мин, линейный градиент: вода (0,05% ТФУ)/ацетонитрил, от 10 до 90%,5,5-7,5 мин, 90% вода (0,05% ТФУ)/ацетонитрил,7,5-8 мин, линейный градиент: вода (0,05% ТФУ)/ацетонитрил, от 90 до 10%,8-10 мин, 10% вода (0,05% ТФУ)/ацетонитрил. Метод С. Система: Waters Millenium 2695/996PDA, колонка: Phenomenex Columbus, 3 мкм, C18, 504,6 мм,элюент: градиент вода (0,1% ТФУ)/ацетонитрил, скорость элюирования: 1,1 мл/мин. Программа элюирования: 0-1 мин, 10% вода (0,1% ТФУ)/ацетонитрил,- 22014907 1-8 мин, линейный градиент: вода (0,1% ТФУ)/ацетонитрил, от 10 до 90%,8-9 мин, 90% вода (0,1% ТФУ)/ацетонитрил,9-12 мин, линейный градиент: вода (0,1% ТФУ)/ацетонитрил, от 90 до 10%,10-12 мин, 10% вода (0,1% ТФУ)/ацетонитрил. Масс-спектрометрия Масс-спектрометрию проводили с использованием системы Thermo-electron LCQ classic или Applied Biosciences PE Sciex API150ex. Жидкостную хроматографию/масс-спектрометрию проводили с использованием системы Waters Millenium 2690/996PDA, сопряженной с системой Thermo-electron LCQAVANCE 300 или Bruker 400 МГц AVANCEII 400. Примеры Типичные примеры соединений приводятся ниже в табл. 1. При ингибировании Mnk2 соединения характеризуются величинами IC5010 мкМ. Таблица 1
МПК / Метки
МПК: C07D 473/32, A61K 31/52, A61P 3/00
Метки: метаболических, основе, ингибиторы, нарушений, лечения, 8-гетероарилпурина
Код ссылки
<a href="https://eas.patents.su/30-14907-ingibitory-mnk2-na-osnove-8-geteroarilpurina-dlya-lecheniya-metabolicheskih-narushenijj.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы mnk2 на основе 8-гетероарилпурина для лечения метаболических нарушений</a>
Предыдущий патент: 5-(арилсульфонил)пиразолопиперидины
Следующий патент: Композиции, обладающие свойствами регуляторов роста растения
Случайный патент: Таблетки циталопрама гидробромида