Антибактериальные агенты
Номер патента: 11808
Опубликовано: 30.06.2009
Авторы: Эрвин Элис, Вагман Аллан, Пфистер Кейт Б., Клайн Тони, Шавар Рибхи, Ябаннавар Аша, Андерсон Нейлз Х., Бауман Джейсоен, Харвуд Эрик, Нг Саймон, Мдлули Кхисимузи
Формула / Реферат
1. Соединение формулы
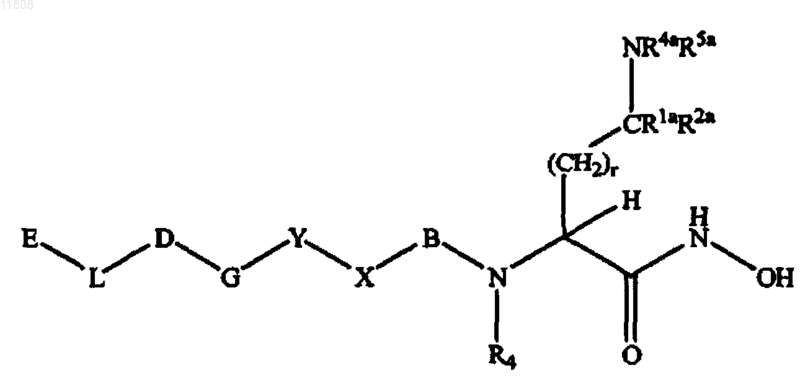
или его стереоизомер, или фармацевтически приемлемая соль, где E отсутствует или выбирают из группы, состоящей из
(1) H,
(2) C1-С6-алкила; C1-С6-алкила, замещенного одним или более ОН, F, Cl, Br, I, CN, COOH, NH2, N(CH3)2, N(CH2CH3)3+, NHC(O)CH3, C(O)NHOH, C(O)NH2, N(CH(CH3)2)2, OCH3, NHC(O)OCCH3, NHC(NH)NH2, NHSO2CH3, OCH2CH3, или оксо; циклопропила; циклопропила, замещенного фенилом; циклобутила; циклопентила, циклогексила; циклогексила, замещенного одним или более NH2 или C1-С6-алкилом; -(C1-С6-алкил)циклогексила; циклогептила; бициклогептила; -(C1-C6-алкил)бициклогептила;
-(C1-С6-алкил)бициклогептила, где бициклогептил замещен одним или более C1-С6-алкилом; циклооктила; -(C1-С6-алкил)трициклодецила; -(C1-С6-алкил)пиперидинила; -(C1-C6-алкил)пиперидинила, где пиперидинил замещен одним или более ацетилом, C(O)NH2, CF3, фенилом или пиперидинилом; -(C1-C6-алкил)пиперазинила; -(C1-С6-алкил)пиперазинила, где пиперазинил замещен одним или более C1-С6-алкилом, фенилом или фенилом, замещенным одним или более F, Cl, Br, или I; -(C1-C6-алкил)пиридила;
-(C1-С6-алкил)тиенила; -(C1-C6-алкил)бензотиенила; -(C1-С6-алкил)имидазолила; -(С1-С6-алкил)морфолинила; -(C1-C6-алкил)азепанила; -(C1-С6-алкил)пирролидинила; -(C1-C6-алкил)пирролидинила, где пирролидинил замещен одним или более оксо, диметиламино, амино, ацетиламино или NHC(O)CF3; -(C1-C6-алкил)фенила; или -(C1-С6-алкил)фенила, где фенил замещен одним или более F, Cl, Br, I, ОН, SCH3, SO2CH3, SCF3, CF3, NO2, NH2, N(CH3)2, OCH3, OCF3, или C1-С6-алкила;
(3) С2-С6-алкенила, или С2-С6-алкенила, замещенного одним или более F, Cl, Br или фенилом;
(4) фенила или фенила, замещенного одним или более F, Cl, Br, I, ОН, NH2, NO2, OC6H5, OCH3, OCF3, OPO(OH)2, CN, CNOH, SO2CH3, SCH3, CF3 или C1-С6-алкилом;
(5) бензимидазолила; бензотиенила; пиперазинила; пиперазинила, замещенного одним или более С1-С6-алкилом или фенилом; пирролидинила; пирролидинила, замещенного одним или более NH2, NHC(O)CF3 или N(CH3)2; ацетиламинопирролидинила; морфолинила; азепанила; пиразолила; тиадиазолила; имидазолила; тетрагидропиримидинила; пирролидинонила; пиперидинила; пиперидинила, замещенного одним или более ацетилом, пиперидинилом, CF3, фенилом или фенилом, замещенным одним или более F, Cl, Br, I, C(O)NH2 или ацетилом; и
(6) тиенила; тиенила, замещенного CHNOH; пиридила или пиридила, замещенного одним или более C1-С6-алкилом, F, Cl, Br, I, ОН, COOH или OCH3;
L отсутствует или выбирают из группы, состоящей из
(1) C1-С6-алкила,
(2) -(NH)0-1-(CH2)jNR3L-(CH2)k-,
(3) -(NH)0-1-C(R1L,R2L)-NR3L-C(R1L,R2L)-,
(4) -C(R1L,R2L)-O-C(R1L,R2L)-,
(5) -(CH2)jNR3L-C(R1L,R2L)-CONH-(CH2)k-,
(6) -CO-C(R1L,R2L)-NHCO-,
(7) -CONH- и
(8) -NHCO-,
где R1L, R2L и R3L независимо выбирают из группы, состоящей из
(a) H,
(b) циклопропила, C1-С6-алкила или C1-С6-алкила, замещенного F, Cl, Br, I, ОН, NH2, CN, COOH, OCH3, OCH2CH3, N(CH3)2, NHC(O)OCCH3 или NHC(O)CH3;
(c) C1-С6-алкила, замещенного фенилом; или фенила, замещенного одним или более F, Cl, Br, I, OCH3, CF3, OCF3 или С1-С6-алкилом,
(d) C1-С6-алкила, замещенного одним или более пирролидинилом, морфолинилом, азепинилом, карбоксамидпирролидинилом, ацетиламинопирролидинилом, диметиламинопирролидинилом, аминопирролидинилом или пиперидинилом, и
(e) C1-С6-алкила, замещенного пиридилом или имидазолилом,
или R1L и R3L вместе с атомами, к которым они присоединены, могут образовывать пирролидиновое или пиперидиновое кольцо;
j представляет собой целое число от 0 до 4; и
k представляет собой целое число от 0 до 4;
D отсутствует или выбирают из группы, состоящей из
(1) С3-С8-циклоалкила,
(2) фенила или фенила, замещенного одним или более F, Cl, Br, I, CF3, NO2, ОН, OCH3, OCF3, ОС(О)(C1-С6-алкилом), гидроксиамино-2-оксоэтилокси, метилсульфониламино, аминоацетиламино, метилсульфониламинометилом, диметиламино, диэтиламино, фенилсульфониламино или C1-С6-алкилом; и
(3) тиенила; пиразинила; пиридила; пиридила, замещенного одним или более F, Cl, Br или I; пиримидинила или пиримидинила, замещенного амино;
G отсутствует или выбирают из группы, состоящей из
(1) -(CH2)i-O-(CH2)i-,
(2) -(CH2)i-S-(CH2)i-,
(3) -(CH2)i-NRg-(CH2)i-,
(4) -С(=O)-,
(5) -NHC(=O)-,
(6) -C(=O)NH-,
(7) -(CH2)iNHCH2C(=O)NH-,
(8) -CуC-,
(9) -CуC-CуC- и
(10) -C=C-;
где Rg представляет собой H или C1-С6-алкил; и
i представляет собой целое число от 0 до 4;
Y выбирают из группы, состоящей из
(1) С3-С8-циклоалкила,
(2) флуоренила; фенила или фенила, замещенного одним или более F, Cl, Br, I, CN, CF3, SCH2(C6H5), SCH3, NH2, NHSO2CH3, CH2NHSO2CH3, NHSO2(C6H5), NHSO2(C6H4Br), N2(C6H5), ОН, OCF3, CHO, С3-С4алкенилом, С3-С4алкенилом, замещенным одним или более F или С1-С4алкокси;
(3) пирролидинила; фуранила; бензодиоксоила; хроменила; бензофуранила; тиенила или тиенила, замещенного одним или более F, Cl, Br, I или ОН; и
(4) пиридинила; пиридинила, замещенного одним или более F, Cl, Br, I, COOH или CF3; пиримидинила, замещенного одним или более NH2 или ОСН3; или хинолинила;
X выбирают из группы, состоящей из
(1) -(C=O)-,
(2) -C1-С6-алкил-(C=O)-, где алкил незамещен или замещен NH2,
(3) -С2-С6-алкенил-(C=O)-,
(4) -С2-С6-алкинил-(C=O)- и
(5) -CH2-;
В отсутствует или
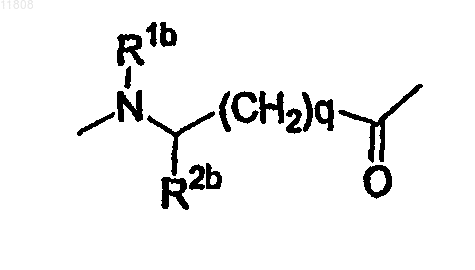
где R1b и R2b независимо выбирают из группы, состоящей из
(a) H,
(b) C1-С6-алкила или C1-С6-алкила, замещенного одним или более NH2, CN, COOH, ОН, оксо, ацетиламино или C(O)NH2;
(c) С2-С6-алкинила,
(d) фенила или фенила, замещенного ОН;
(e) имидазолила;
(f) C1-С6-алкила, замещенного фенилом или фенилом, замещенным ОН; и
(g) C1-С6-алкила, замещенного имидазолилом;
или R1b и R2b вместе с атомами, к которым они присоединены, могут образовывать тетрагидроизохинолинил, пиперазинил, пирролидинил или пирролидинил, замещенный ОН; и
q представляет собой целое число от 0 до 4;
R4 представляет собой H или C1-С6-алкил,
R1a, R2a, R4a и R5a независимо выбирают из группы, состоящей из
(a) H;
(b) циклобутила; C1-С6-алкила; C1-С6-алкила, замещенного одним или более оксо, -NHC(О)О(C1-С6-алкилом), -S(C1-С6-алкилом), замещенным одним или более ОН или COOH, NH2, -NH(C1-С6-алкилом),
-NH(C1-C6-алкилом), где алкил замещен одним или более NH2, имидазолилом, NHC(О)О(С1-С6-алкилом), COOH, C(O)NH2, С(О)О(C1-С6-алкилом), С(О)NH-(C1-С6-алкилом), где алкил замещен NH2, фенилом или фенилом, замещенным ОСН3;
(c) -C(O)O-(C1-С6-алкила); -C(O)NH2; -C(NH)NH2; -С(О)-морфолинила; -С(О)-(C1-С6-алкил)морфолинила; -С (О)-пиридинила, где пиридинил замещен одним или более ОН, -С(О)-фенилом, где фенил замещен одним или более ОН;
(d) тетрагидрофуранила, пиперидинила, замещенного C1-С6-алкилом;
(e) С2-С6-алкенила;
(f) C1-С6-алкила, замещенного фенилом, замещенного ОСН3; и
(g) C1-С6-алкила, замещенного пирролидинилом, пиперидинилом, замещенным C1-С6-алкилом, или пиперазинилом, замещенным C1-C6-алкилом;
r представляет собой целое число от 0 до 4;
где В отсутствует, или E, L, G и B отсутствуют, или E, L и G отсутствуют, или E, L и В отсутствуют, или E, L, D, G и В отсутствуют.
2. Соединение по п.1, где В отсутствует,
R4 представляет собой H, и
R1a, R2a, R4a и R5a независимо выбирают из группы, состоящей из
(a) H и
(b) C1-С6-алкила; циклобутила; C1-С6-алкила, замещенного одним или более оксо, -NHC(О)О(C1-С6-алкилом), -S(С1-С6-алкилом), замещенным одним или более ОН или COOH, NH2, -NH(C1-С6-алкилом),
-NH(C1-C6-алкилом), где алкил замещен одним или более NH2, имидазолилом, NHC(O)O(C1-C6-алкилом), COOH, C(O)NH2, С(О)О(C1-С6-алкилом), С(О)NH-(C1-С6-алкилом), где алкил замещен NH2, фенилом или фенилом, замещенным OCH3; и C1-С6-алкила, замещенного пирролидинилом.
3. Соединение по п.1, имеющее формулу III
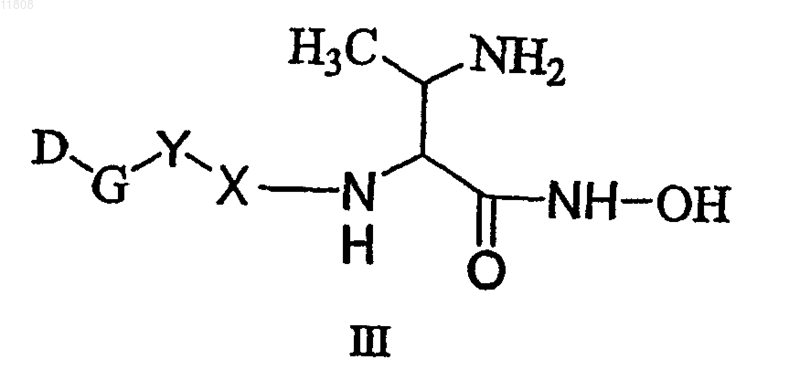
или его стереоизомер, или фармацевтически приемлемая соль, где D-G-Y, взятые вместе, выбирают из группы, состоящей из
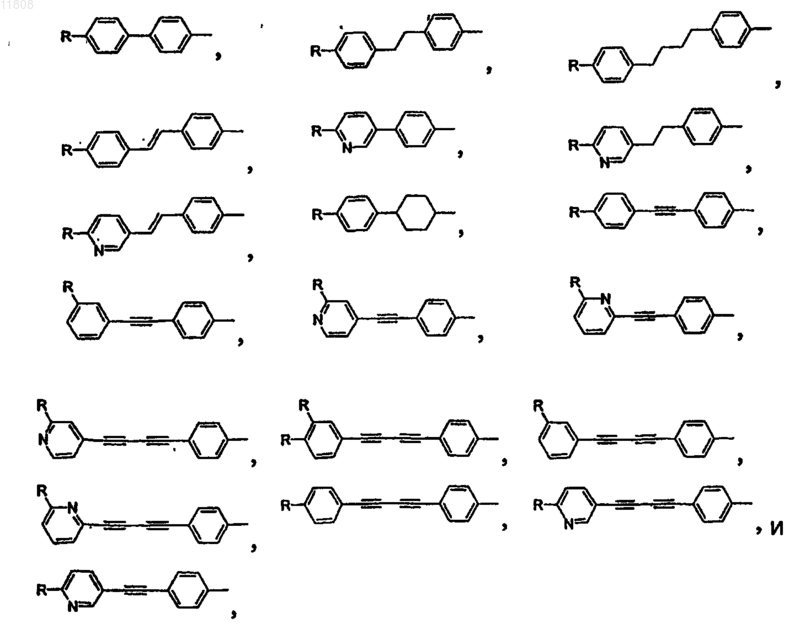
или
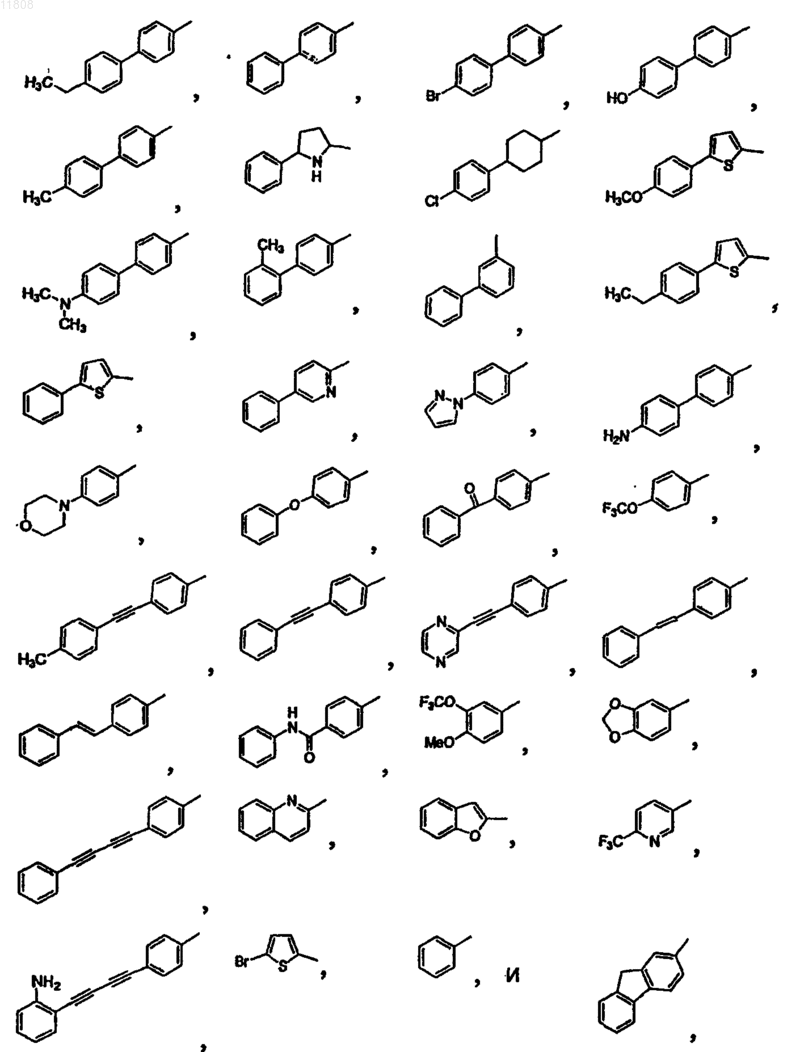
где R выбирают из группы, состоящей из -CH3, -С2Н5, -CH2OH, -ОН, -OCH3, -OC2H5, -OCF3, -CN, -NO2,
-CO2H, -CO2CH3, -CONH2, -NH2, -F, -Cl, -Br, -CF3, -N(CH3)2, -NHSO2CH3 и -NHCOCH3; и
X выбирают из групп, состоящих из
(1) -(C=O)-,
(2) -С1-С6-алкил-(C=O)- и
(3) -С2-С6-алкенил-(C=O)-.
4. Соединение по п.1, имеющее формулу V
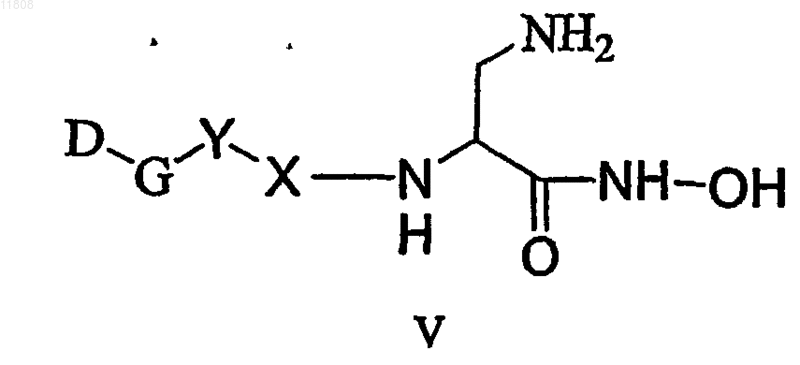
или его стереоизомер, или фармацевтически приемлемая соль, где D-G-Y, взятые вместе, выбирают из группы, состоящей из
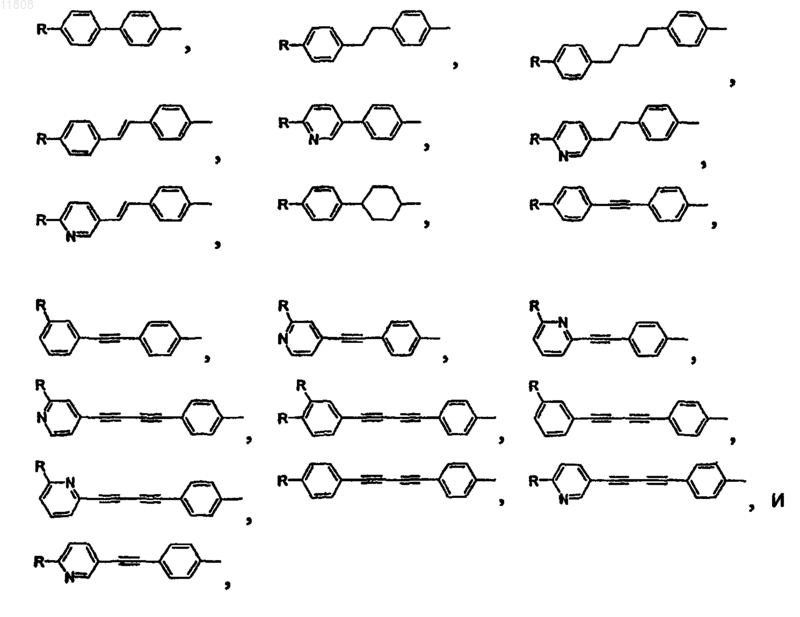
или

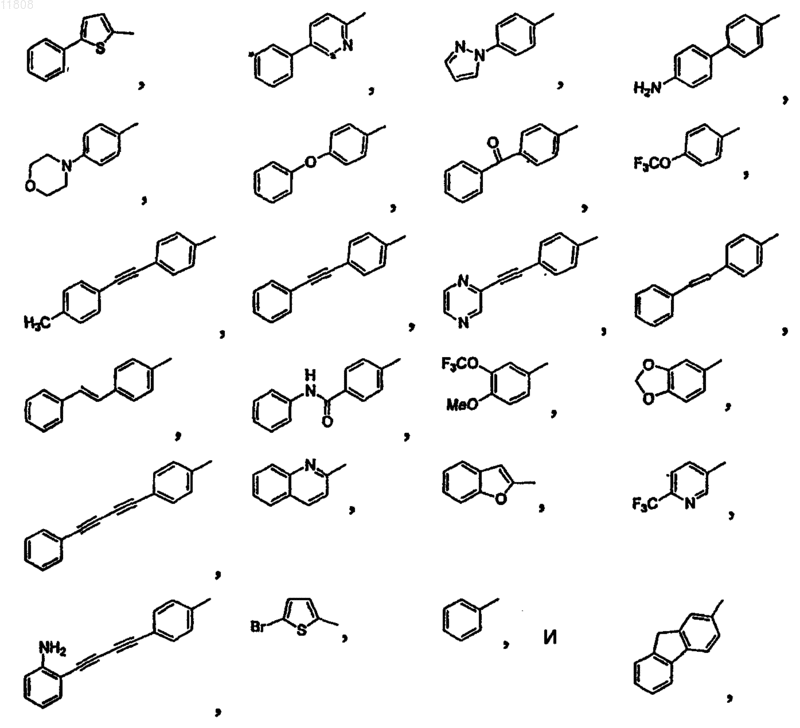
где R выбирают из группы, состоящей из -CH3, -C2H5, -CH2OH, -ОН, -OCH3, -OC2H5, -OCF3, -CN, -NO2,
-CO2H, -CO2CH3, -CONH2, -NH2, -F, -Cl, -Br, -CF3, -N(CH3)2, -NHSO2CH3 и -NHCOCH3;
X выбирают из группы, состоящей из
(1) -(C=O)-,
(2) -C1-С6-алкил-(C=O)- и
(3) -С2-С6-алкенил-(C=O)-.
5. Соединение по п.1, имеющее формулу VII
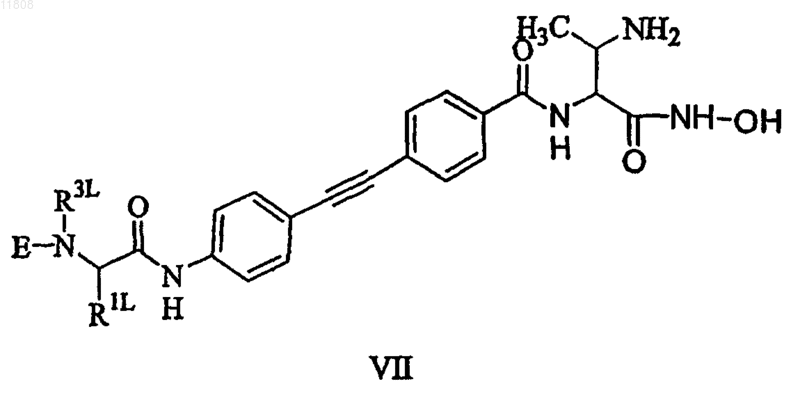
или его стереоизомер, или фармацевтически приемлемая соль, где E отсутствует или выбирают из группы, состоящей из C1-С6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br или I; циклопропила, циклобутила и C1-С6-алкила, замещенного пиридилом; и R1L и R3L оба представляют собой H.
6. Соединение по п.1, имеющее формулу IX

или его стереоизомер, или фармацевтически приемлемая соль, где E отсутствует или выбирают из группы, состоящей из
(1) H;
(2) циклопропила; циклобутила; циклопентила, циклогексила; циклогептила; бициклогептила; C1-С6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С6-алкокси, ди(C1-C6-алкил)амино, циано или циклогексилом;
(3) фенила или фенила, замещенного одним или более F, Cl, Br или I; C1-С6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С6-алкилом или C1-С6-алкокси; и
(4) пиридинила, пиразинила или C1-С6-алкила, замещенного пиридинилом или тиофенилом;
или Е и R3L вместе с атомами, к которым они присоединены, могут образовывать пирролидинил, азепанил, имидазолил, морфолино, пиперидинил, пиперазинил или пиперазинил, замещенный C1-С6-алкилом;
R1L, R3L независимо выбирают из группы, состоящей из
(1) H;
(2) С1-С6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С6-алкокси, ди(C1-С6-алкил)амино, циано или циклогексилом;
(3) C1-С6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С6-алкилом или C1-С6-алкокси; и
(4) C1-С6-алкила, замещенного пиридинилом или тиофенилом.
7. Соединение по п.1, имеющее формулу X
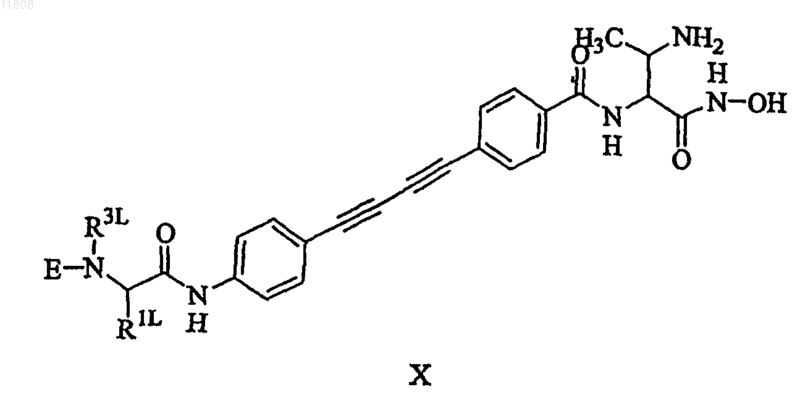
или его стереоизомер, или фармацевтически приемлемая соль, где E отсутствует или выбирают из группы, состоящей из
(1) H;
(2) циклопропила; циклобутила; циклопентила; циклогексила; циклогептила; бициклогептила; C1-С6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С6-алкокси, ди(C1-C6-алкил)амино, циано или циклогексилом;
(3) фенила или фенила, замещенного одним или более F, Cl, Br или I; C1-С6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С6-алкилом или C1-C6-алкокси; и
(4) пиридинила, пиразинила или C1-С6-алкила, замещенного пиридинилом или тиофенилом;
или E и R3L вместе с атомами, к которым они присоединены, могут образовывать пирролидинил, азепанил, имидазолил, морфолино,пиперидинил, пиперазинил или пиперазинил, замещенный C1-C6-алкилом;
R1L, R3L независимо выбирают из группы, состоящей из
(1) H;
(2) C1-С6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С6-алкокси, ди(C1-С6-алкил)амино, циано или циклогексилом;
(3) C1-С6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С6-алкилом или C1-C6-алкокси; и
(4) C1-С6-алкила, замещенного пиридинилом или тиофенилом.
8. Фармацевтическая композиция, включающая соединение по одному из пп.1-7 и фармацевтически приемлемое вспомогательное вещество.
9. Фармацевтическая композиция, включающая соединение по одному из пп.1-7, второй агент и фармацевтически приемлемое вспомогательное вещество, причем вторым агентом является антибактериальный агент, антиэндотоксин или ингалируемый не антибактериальный агент для лечения инфекции дыхательных путей.
10. Способ лечения инфекции, включающий введение пациенту, нуждающемуся в этом, эффективного количества соединения по одному из пп.1-7.
11. Способ лечения инфекции, включающий введение пациенту, нуждающемуся в этом, эффективного количества соединения по одному из пп.1-7 и эффективного количества второго агента, причем вторым агентом является антибактериальный агент, антиэндотоксин или ингалируемый не антибактериальный агент для лечения инфекции дыхательных путей.
Текст
011808 Настоящий патент заявляет преимущество приоритета следующих предварительных патентных заявок США, серийный номер 60/438523, опубликованной 8 января 2003 г.; серийный номер 60/466974,опубликованной 30 апреля 2003 г.; и серийный номер 60/520211, опубликованной 13 ноября 2003 г.; каждая из которых включена в данное описание в виде ссылки полностью. Настоящее изобретение относится в основном к лечению инфекций, вызываемых грамотрицательными бактериями. В частности, изобретение, раскрытое в данном описании, относится к лечению грамотрицательных инфекций ингибированием активности УДФ-3-О-(R-3-гидроксидеканоил)-N-ацетилглюкозаминдеацетилазы (LpxC). Настоящее изобретение относится к низкомолекулярным ингибиторамLpxC, фармацевтическим композициям, содержащим такие ингибиторы, способам лечения пациентов такими фармацевтическими композициями и способам получения таких фармацевтических композиций и ингибиторов. Ингибиторы могут быть использованы для лечения грамотрицательных инфекций у пациентов отдельно или в комбинации с другими антибактериальными агентами. На протяжении последних нескольких десятилетий количество случаев антимикробной устойчивости и ее связь с серьезными инфекционными заболеваниями увеличивается с тревожной скоростью. Увеличивающаяся распространенность устойчивости среди внутрибольничных патогенов является особенно тревожащей. Из более чем 2 миллионов внутрибольничных инфекций, появляющихся каждый год в Соединенных Штатах, от 50 до 60% вызваны штаммами бактерий, устойчивых к антибактериальным препаратам. Такая высокая степень устойчивости повышает заболеваемость, смертность и затраты, связанные с внутрибольничными инфекциями. В Соединенных Штатах считают, что внутрибольничные инфекции способствуют или вызывают более чем 77000 смертей в год и стоят приблизительно от 5 до 10 миллиардов долларов ежегодно. Среди грамположительных организмов наиболее важными устойчивыми патогенами являются метициллин-(оксациллин-)устойчивый золотистый стафилококк, -лактам устойчивые и устойчивые ко многим лекарственным средствам пневмококки и ванкомицинустойчивые энтерококки. Важные причины грамотрицательной устойчивости включают -лактамазы широкого спектра (ESBL) у Klebsiella pneumoniae, Escherichia coli и Proteus mirabilis, -лактамазная устойчивость высокого уровня к цефалоспоринам третьего поколения (Amp С) среди видов Enterobacter и Citrobacterfreundii и гены множественной лекарственной устойчивости, наблюдаемые у Pseudomonas aeruginosa,Acinetobacter и Stenotrophomonas maltophilia (Jones RN 2001 Chest 119 (supplement) 397S-404S: Resistancepatterns among nosocomial pathogens: Trends over the past few years). Проблема устойчивости к антибактериальным препаратам заключается в существовании бактериальных штаммов, устойчивых к множеству антибактериальных препаратов. Например, выделенная Pseudomonas aeruginosa, устойчивая к фторхинолонам, является практически всегда устойчивой к другим антибактериальным препаратам (Sahm D.F. et al. 2001, Antimicrobial Agents and Chemotherapy 45, 267-274:Evaluation of current activities of fluoroquinolones against gram-negative bacilli using centralized in vitro testing and electronic surveillance.) Следовательно, существует необходимость в новых антибактериальных препаратах, в частности,антибактериальных препаратах с новыми механизмами действия. Большинство попыток открытия антибактериальных препаратов в фармацевтической промышленности направлено на разработку лекарственных средств против грамположительных бактерий. Однако также существует необходимость в новых грамотрицательных антибактериальных препаратах. Грамотрицательные бактерии являются в общем более устойчивыми к большому количеству антибактериальных препаратов и химиотерапевтических агентов, чем грамположительные бактерии. Исследование антибактериальных препаратов природного происхождения, о которых сообщают в последнее время, показало, что у более чем 90% отсутствует активность в отношении Escherichia coli, хотя они активны против грамположительных бактерий. Наружная мембрана грамотрицательных бактерий вносит свой вклад в такую внутреннюю устойчивость, действуя как эффективный барьер проницаемости, так как узкие пористые каналы ограничивают проникновение гидрофильных растворов, и низкая текучесть липополисахаридного листка замедляет диффузию внутрь липофильных растворов. Второй механизм делает вклад во внутреннюю устойчивость грамотрицательных бактерий. В недавних исследованиях было показано, что насосы, выделяющие множество лекарственных препаратов, иногда с необычно широкой специфичностью, действуют как второй фактор создания общей внутренней устойчивости грамотрицательных бактерий. Когда их уровень экспрессии повышен как следствие физиологической регуляции или генетических нарушений, они могут часто давать впечатляющий уровень устойчивости к множеству антибактериальных агентов. (Nikaido H 1998efflux pumps). Исторически большая часть разработок антибактериальных агентов была относительно эмпирической. Активные соединения обычно находили посредством скрининга почвы, сточных вод, воды и других естественных веществ для определения организмов, продуцирующих антибактериальные агенты или посредством скрининга различных химических соединений. Когда обнаруживали главный кандидат и определяли его химическую структуру, создавали ряд аналогов для определения оптимального соединения для последующей химической разработки. Более рациональный подход включает определение новых-1 011808 целей, таких как гены или ферментные функции, ответственных за ключевую клеточную основную активность. Когда это сделано, ингибиторы или блокаторы функции или продукта гена могут быть разработаны. С целью определения потенциальных мишеней для новых грамотрицательных антибактериальных агентов проводили исследования, имеющие целью определение всех основных и важных генов Pseudomonas aeruginosa. Среди этих основных идентифицированных генов был lрхС, который кодирует фермент уридилдифосфо-3-O-(R-гидроксидеканоил)-N-ацетилглюкозаминдеацетилазу (LpxC). Этот фермент является первой совершаемой стадией в синтезе липида А, липидного компонента липополисахарида,который является основным компонентом грамотрицательных бактерий. Следовательно, он привлекателен для новых антибактериальных препаратов. Чтобы быть применимыми в качестве антибактериальных агентов, ингибиторы LpxC должны не только ингибировать ферментативную активность LpxC множества бактерий, но должны разрушать механизмы внутренней устойчивости грамотрицательных бактерий,как описано выше: они должны проникать сквозь наружную мембрану и быть относительно нечувствительными к насосам, откачивающим множество лекарственных средств. Исследователи идентифицировали несколько соединений с антибактериальной активностью, которые имеют целью биосинтез липида A. WO 97/42179, выданный Patchett et al., раскрывает соединения формулы Соединения обладают активностью в отношении определенных грамотрицательных организмов,например, Escherichia coli, но не активны в отношении других важных в медицине грамотрицательных бактерий, например, Pseudomonas aeruginosa. Последующие исследования обнаружили, что первичной причиной их неактивности в отношении определенных, важных в медицине грамотрицательных бактерий, является их плохая способность ингибировать LpxC P. aeruginosa; отток главными насосами, откачивающими множество лекарственных средств, или неспособность проникать через наружную мембрану не были критическими факторами.Jackman et al., в J.Biol.Chem. (vol. 2 75, по. 15, April 14, 2000, pps. 11002-11009), обсуждает механизм биосинтеза липида А в контексте грамотрицательных бактерий, раскрывает новый класс ингибиторовLpxC, содержащих гидроксамат. Wyckoff et al., в Trends in Microbiology (vol. 6, no. 4, April 1998, pps. 154159), обсуждает роль LpxC в биосинтезе липида А и его роль в регуляции. Wyckoff et al. описывают некоторые оксазолингидроксамовые кислоты, которые ингибируют бактериальный рост. Однако Wyckoffet al. также обсуждают недостатки доступных ингибиторов деацетилазы в качестве бактерицидных агентов в отношении Pseudomonas, и что больше работы требуется осуществить в области техники. Следовательно, существует увеличивающаяся необходимость в ингибиторах LpxC, которые обладают активностью в качестве бактерицидных агентов в отношении грамотрицательных бактерий. Соответственно, задачей настоящего изобретения является обеспечение соединений и комбинаций таких соединений для применения в получении антибактериальных препаратов и других фармацевтических средств, способных ингибировать грамотрицательные бактериальные инфекции. Патентная публикация США No. 2001/0053555 (патентная заявка США серийный 08/958638),опубликованная 20 декабря 2001, соответствующая WO 98/18754, опубликованному 7 мая 1998, описывает комбинаторную библиотеку гидроксиламина, гидроксамовой кислоты, гидроксимочевины и гидроксилсульфонамидных соединений, предназначенных для того, чтобы быть применимыми в качестве ингибиторов металлопротеаз. Патент США No. 6281245, продолжение частично U.S. 08/958638 заявляет способ ингибирования фермента деформилазы введением одного из гидроксиламиновых соединений из комбинаторной библиотеки, как описано в патентной публикации США 2001/0053555 и соответствующем WO 98/18754. Относящимся к вышеописанным патентным заявкам является WO 99/57097,опубликованный 11 ноября 1999, который описывает способ твердофазного синтеза гидроксиламиновой библиотеки соединений. WO 00/61134 (выданный British Biotech Pharmaceuticals Limited), опубликованный 19 октября 2000, описывает соединения формулы Соединения являются применимыми в качестве антибактериальных агентов, о которых считают,что они имеют бактерицидную активность, по меньшей мере, частично из-за внутриклеточного ингибирования бактериального полипептида деформилазы. В более раннем выданном British Biotech Pharmaceuticals Limited WO 99/39704, опубликованном 12 августа 1999, описаны соединения формулы Соединения являются пригодными в качестве антибактериальных агентов в отношении грамотрицательных и грамположительных бактерий. В последнее время De Novo Pharmaceuticals LTD описали в WO 02/50081, опубликованном 27 июня 2002, антибактериальные и антипротозойные агенты, имеющие формулы, показанные ниже: Патентная публикация обсуждает, что антибактериальная активность обусловлена, по меньшей мере, частично, внутриклеточным ингибированием бактериальной полипептиддеформилазы. Настоящее изобретение относится к новым соединениям, фармацевтическим композициям, включающим соединения, способам ингибирования УДФ-3-O-(R-3-гидроксидеканоил)-N-ацетилглюкозаминдеацетилазы (LpxC), и способам лечения грамотрицательных бактериальных инфекций. В одном варианте воплощения изобретение относится к соединениям формулы I или их стереоизомерам, фармацевтически приемлемым солям, сложным эфирам и пролекарствам,где E отсутствует или выбран из группы, состоящей из(1) H,(2) C1-С 6-алкила; C1-С 6-алкила, замещенного одним или более ОН, F, Cl, Br, I, CN, COOH, NH2, N(CH3)2, N(CH2CH3)3+, NHC(O)CH3, C(O)NHOH, C(O)NH2, N(CH(CH3)2)2, OCH3, NHC(O)OCCH3,NHC(NH)NH2, NHSO2CH3, OCH2CH3 или оксо; циклопропила; циклопропила, замещенного фенилом; циклобутила; циклопентила, циклогексила; циклогексила, замещенного одним или более NH2 или C1-С 6 алкилом; -(C1-С 6-алкил)циклогексила; циклогептила; бициклогептила; -(C1-С 6-алкил)бициклогептила;-(C1-С 6-алкил)бициклогептила, где бициклогептил замещен одним или более C1-С 6-алкилом; циклооктила; -(C1-С 6-алкил)трициклодецила; -(C1-C6-алкил)пиперидинила; -(C1-С 6-алкил)пиперидинила, где пиперидинил замещен одним или более ацетилом, C(O)NH2, CF3, фенилом или пиперидинилом; -(C1-С 6 алкил)пиперазинила; -(C1-C6-алкил)пиперазинила, где пиперазинил замещен одним или более C1-С 6 алкилом, фенилом или фенилом, замещенным одним или более F, Cl, Br или I; -(C1-С 6-алкил) пиридила; (C1-С 6-алкил)тиенила; -(C1-С 6-алкил)бензотиенила; -(C1-С 6-алкил)имидазолила; -(C1-C6-алкил)морфолинила; -(C1-С 6-алкил)азепанила; -(C1-C6-алкил)пирролидинила; -(C1-С 6-алкил)пирролидинила, где пирролидинил замещен одним или более оксо, диметиламино, амино, ацетиламино или NHC(O)CF3; -(C1-С 6 алкил)фенила; или -(C1-C6-алкил)фенила, где фенил замещен одним или более F, Cl, Br, I, ОН, SCH3,SO2CH3, SCF3, CF3, NO2, NH2, N(CH3)2, OCH3, OCF3 или C1-С 6-алкила;(3) С 2-С 6-алкенила или С 2-С 6-алкенила, замещенного одним или более F, Cl, Br или фенилом;(4) фенила или фенила, замещенного одним или более F, Cl, Br, I, ОН, NH2, NO2, OC6H5, OCH3,OCF3, OPO(OH)2, CN, CNOH, SO2CH3, SCH3, CF3 или C1-С 6-алкилом;(5) бензимидазолила; бензотиенила; пиперазинила; пиперазинила, замещенного одним или болееC1-С 6-алкилом или фенилом; пирролидинила; пирролидинила, замещенного одним или более NH2,NHC(O)CF3 или N(CH3)2; ацетиламинопирролидинила; морфолинила; азепанила; пиразолила; тиадиазолила; имидазолила; тетрагидропиримидинила; пирролидинонила; пиперидинила; пиперидинила, замещенного одним или более ацетилом, пиперидинилом, CF3, фенилом или фенилом, замещенным одним или более F, Cl, Br, I, C(O)NH2 или ацетилом; и(6) тиенила; тиенила, замещенного CHNOH; пиридила или пиридила, замещенного одним или болееL отсутствует или выбирают из группы, состоящей изR1L, R2L и R3L независимо выбирают из группы, состоящей из(c) C1-С 6-алкила, замещенного фенилом; или фенила, замещенного одним или более F, Cl, Br, I,OCH3, CF3, OCF3 или C1-С 6-алкилом,(d) C1-С 6-алкила, замещенного одним или более пирролидинилом, морфолинилом, азепинилом,карбоксамидпирролидинилом, ацетиламинопирролидинилом, диметиламинопирролидинилом, аминопирролидинилом или пиперидинилом, и(e) C1-С 6-алкила, замещенного пиридилом или имидазолилом, илиR1L и R3L, вместе с атомами, к которым они присоединены, могут образовывать пирролидиновое или пиперидиновое кольцо;j представляет собой целое число от 0 до 4; иk представляет собой целое число от 0 до 4;D отсутствует или выбирают из группы, состоящей из(1) С 3-С 8-циклоалкила,(2) фенила; или фенила, замещенного одним или более F, Cl, Br, I, CF3, NO2, ОН, OCH3, OCF3,ОС(О)(C1-С 6-алкилом), гидроксиамино-2-оксоэтилокси, метилсульфониламино, аминоацетиламино, метилсульфониламинометилом, диметиламино, диэтиламино, фенилсульфониламино или C1-С 6-алкил; и(3) тиенила; пиразинила; пиридила; пиридила, замещенного одним или более F, Cl, Br или I; пиримидинила; или пиримидинила, замещенного амино;G отсутствует или выбирают из группы, состоящей изRg представляет собой H или C1-С 6-алкил; и i представляет собой целое число от 0 до 4; Y выбирают из группы, состоящей из(1) С 3-С 8-циклоалкила,(2) флуоренила; фенила; или фенила, замещенного одним или более F, Cl, Br, I, CN, CF3,SCH2(C6H5), SCH3, NH2, NHSO2CH3, CH2NHSO2CH3, NHSO2(C6H5), NHSO2(C6H4Br), N2(C6H5), OH, OCF3,CHO, С 3-С 4 алкенилом, С 3-С 4 алкенилом, замещенным одним или более F, или С 1-С 4 алкокси;(3) пирролидинила; фуранила; бензодиоксоила; хроменила; бензофуранила; тиенила; или тиенила,замещенного одним или более F, Cl, Br, I или ОН; и(4) пиридинила; пиридинила, замещенного одним или более F, Cl, Br, I, COOH или CF3; пиримидинила, замещенного одним или более NH2 или OCH3; или хинолинила;(1) -(C=O)-,(2) -C1-С 6-алкил-(C=O)-, где алкил незамещен или замещен NH2,(3) -С 2-С 6-алкенил-(C=O)-,(4) -С 2-С 6-алкинил-(C=O) - и где R1b и R2b независимо выбирают из группы, состоящей из(a) H,(b) C1-С 6-алкила или C1-С 6-алкила, замещенного одним или более NH2, CN, COOH, ОН, оксо, ацетиламино или C(O)NH2;(f) C1-С 6-алкила, замещенного фенилом или фенилом, замещенным ОН; иq представляет собой целое число от 0 до 4;R4 представляет собой H или C1-С 6-алкил,R1a, R2a, R4a и R5a независимо выбирают из группы, состоящей из(b) циклобутила; C1-С 6-алкила; C1-С 6-алкила, замещенного одним или более оксо, -NHC(О)О(C1-С 6 алкилом), -S(C1-C6-алкилом), замещенным одним или более ОН или COOH, NH2, -NH(C1-С 6-алкилом),-NH(C1-С 6-алкилом), где алкил замещен одним или более NH2, имидазолилом, NHC(О)О(C1-С 6-алкилом),COOH, C(O)NH2, С(О)О(C1-С 6-алкилом), С(О)NH-(C1-С 6-алкилом), где алкил замещен NH2, фенилом или фенилом, замещенным OCH3;(c) -C(O)O-(C1-С 6-алкила); -C(O)NH2; -C(NH)NH2; -C(O)-морфолинила; -C(O)-(C1-С 6-алкил)морфолинила; -C(O)-пиридинила, где пиридинил замещен одним или более ОН, -С(О)-фенилом, где фенил замещен одним или более ОН;r представляет собой целое число от 0 до 4; где В отсутствует, или E, L, G и В отсутствуют, или E, L и G отсутствуют, или E, L и В отсутствуют, или E, L, D, G и В отсутствуют. В одном аспекте, изобретение относится к способу ингибирования фермента деацетилазы грамотрицательных бактерий, таким образом влияя на рост бактерий, включающий введение пациенту, нуждающемуся в таком ингибировании, соединения формулы I. В другом аспекте, изобретение относится к способу ингибирования LpxC, таким образом модулируя вирулентность бактериальной инфекции, включающий введение пациенту, нуждающемуся в таком ингибировании, соединения формулы I. В другом аспекте, изобретение относится к способу лечения субъекта с грамотрицательной бактериальной инфекцией, включающий введение субъекту, нуждающемуся в этом, антибактериально эффективного количества соединения формулы I с фармацевтически приемлемым носителем. В предпочтительном варианте воплощения способа лечения субъектом является млекопитающее и, в некоторых вариантах, человек. В другом аспекте, изобретение относится к способу введения достаточного для ингибирования количества соединения формулы I к ферментирующим или неферментирующим грамотрицательным бактериям. В предпочтительном варианте воплощения способа введения ингибирующего количества соединения формулы I к ферментирующим или неферментирующим грамотрицательным бактериям грамотрицательные бактерии выбирают из группы, состоящей из Pseudomonas aeruginosa, Stenotrophomonasmaltophila, Burkholderia cepacia, Alcaligenes xylosoxidans, Acinetobacter, Enterobacteriaceae, виды Haemophilus и Neisseria. В другом варианте воплощения изобретение относится к способу введения ингибирующего количества соединения формулы I грамотрицательным бактериям, таким как Enterobacteriaceae, которые выбирают из группы, состоящей из организмов, таких как Serratia, Proteus, Klebsiella, Enterobacter, Citrobacter,Salmonella, Providencia, Morganella, Cedecea, и видов Edwardsiella и Escherichia coli. Другой вариант воплощения изобретения относится к фармацевтической композиции, включающей эффективное количество соединения формулы I с его фармацевтически приемлемым носителем. Фармацевтические композиции по настоящему изобретению включают любое из соединений, описанных выше, в комбинации с фармацевтически приемлемым носителем. Другой вариант воплощения изобретения относится к способу совместного введения соединения формулы I с другими терапевтическими агентами, которые выбирают за их особенную полезность в отношении состояний, которые лечат. Например, соединение формулы I является пригодным в комбинации с другими антибактериальными агентами. Соединение формулы I усиливает чувствительность грамотрицательных бактерий к существующим классам антибактериальных средств. Комбинации раскрытых в настоящее время соединений с другими антибактериальными агентами находятся в объеме настоящего изобретения. Такие антибактериальные агенты включают, но не ограничены, эритромицин, рифампицин, налидиксовую кислоту,карбенициллин, бацитрацин, циклосерин, фосфомицин и ванкомицин. Подробное описание Настоящее изобретение относится к новым соединениям, способам ингибирования LpxC у грамотрицательных бактерий и новым способам лечения бактериальных инфекций. Соединения, представленные в данном описании, могут входить в состав фармацевтических композиций и лекарственных препа-5 011808 ратов, которые являются пригодными в способах по изобретению. Изобретение также относится к применению соединений в получении лекарственных препаратов и фармацевтических композиций, применению соединений в ингибировании LpxC и применению соединений в лечении бактериальных инфекций у субъекта. Следующие сокращения и определения используют в описании настоящего патента:LpxC представляет собой сокращение, которое употребляется для УДФ-3-О-(R-3-гидроксидеканоил)-N-ацетилглюкозаминдеацетилазы. Обычно, ссылка на определенный элемент, такой как водород или H, обозначает включение всех изотопов такого элемента. Например, если R-группа определена как включающая водород или H, она также включает дейтерий и тритий. Термин алкил относится к алкильным группам, которые не содержат гетероатомов. Следовательно термин включает линейные алкильные группы, такие как метил, этил, пропил, бутил, пентил, гексил,гептил, октил, нонил, децил, ундецил, додецил и подобные. Термин также включает изомеры с разветвленной цепью алкильных групп с линейной цепью, включая, но не ограничиваясь, следующие, которые представлены в виде примера: -CH(CH3)2, -CH(CH3)(CH2CH3), -СН(СН 2 СН 3)2, -C(CH3)3, -С(СН 2 СН 3)3,-СН 2 СН(СН 3)2,-CH2CH(CH3)(CH2CH3),-CH2CH(CH2CH3)2,-CH2C(CH3)3,-CH2C(CH2CH3)3,-CH(CH3)CH(CH3)(CH2CH3), -CH2CH2CH(CH3)2, -CH2CH2CH(CH3)(CH2CH3), -CH2CH2CH(CH2CH3)2,-CH2CH2C(CH3)3,-СН 2 СН 2 С(СН 2 СН 3)3,-CH(CH3)CH2CH(CH3)2,-CH(CH3)CH(CH3)CH(CH3)2,-CH(CH2CH3)CH(CH3)CH(CH3)(CH2CH3) и другие. Термин также включает циклические алкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил и такие кольца, замещенные линейными и разветвленными алкильными группами, как определено выше. Таким образом, термин алкильные группы включает первичные алкильные группы, вторичные алкильные группы и третичные алкильные группы. Предпочтительные алкильные группы включают линейные и разветвленные алкильные группы и циклические алкильные группы, имеющие от 1 до 12 атомов углерода. Термин замещенный алкил относится к алкильной группе, как определено выше, в которой одна или более связей с углеродом(ами) или водородом(ами) замещены атомами не водорода и не углерода,такими как, но не ограничиваясь, атом галогена, такой как F, Cl, Br и I; атом кислорода в группах, таких как гидроксильные группы, алкоксигруппы, арилоксигруппы и группы сложных эфиров; атом серы в группах, таких как тиоловые группы, алкил- и арилсульфидные группы, сульфоновые группы, сульфонильные группы и сульфоксидные группы; атом азота в группах, таких как амины, амиды, алкиламины,диалкиламины, ариламины, алкилариламины, диариламины, N-оксиды, имиды и енамины; атом кремния в группах, таких как в триалкилсилильные группы, диалкиларилсилильные группы, алкилдиарилсилильные группы, и триарилсилильные группы; и другие гетероатомы в различных других группах. Замещенные алкильные группы включают группы, в которых одна или более связей с атомом углерода или водорода замещены связью более высокого порядка (например, двойной или тройной связью) с гетероатомом, такие как кислород в OKCO-, карбонильных, карбоксильных и эфирных группах; азот в группах,таких как имины, оксимы, гидразоны и нитрилы. Замещенные алкильные группы, кроме того, включают алкильные группы, в которых одна или более связей с атомами углерода или водорода замещены связью с арильной, гетероциклической группой или циклоалкильной группой. Предпочтительные замещенные алкильные группы включают, среди других, алкильные группы, в которых одна или более связей с атомом углерода или водорода замещены одной или более связями с атомами фтора. Другой предпочтительной замещенной алкильной группой является трифторметильная группа и другие алкильные группы,которые содержат трифторметильную группу. Другие предпочтительные замещенные алкильные группы включают группы, в которых одна или более связей с атомом углерода или водорода замещены связью с атомом кислорода, так что замещенная алкильная группа содержит гидроксильную, алкокси или арилоксигруппу. Другие предпочтительные замещенные алкильные группы включают алкильные группы, которые имеют аминовую, или замещенную или незамещенную алкиламиновую, диалкиламиновую, ариламиновую, (алкил)(арил)аминовую, диариламиновую, гетероциклиламиновую, дигетероциклиламиновую,(алкил)(гетероциклил)аминовую или (арил)(гетероциклил)аминовую группу. Термин алкенил относится к линейным, разветвленным и циклическим группам, таким как описанные в отношении алкильных групп, как определено выше, кроме того по меньшей мере одна двойная связь существует между двумя атомами углерода. Примеры включают, но не ограничены, винил,-CH=C(H)(CH3), -CH=C(CH3)2, -C(CH3)=C(H)2, -С(CH3)=С(H)(CH3), -С(CH2CH3)=СН 2, циклогексенил,циклопентенил, циклогексадиенил, бутадиенил, пентадиенил и гексадиенил среди остальных. Термин замещенный алкенил имеет то же значение в отношении алкенильных групп, которое имеют замещенные алкильные группы в отношении к незамещенным алкильным группам. Замещенная алкенильная группа включает алкенильные группы, в которых не углеродный или не водородный атом связан с углеродом, связанным двойной связью с другим углеродом, и таковые, в которых не углеродный или не водородный атомы связаны с углеродом, не включенным в двойную связь с другим углеродом. Термин алкинил относится к группам с линейной или разветвленной цепью, таким как описанные в отношении алкильных групп, как определено выше, кроме того по меньшей мере одна тройная связь-6 011808 существует между двумя атомами углерода. Примеры включают, но не ограничены -CC(H), -CC(CH3),-CC(CH2CH3), -C(H2)CC(H), -C(H)2CC(CH3) и -C(H)2CC(CH2CH3) среди остальных. Термин замещенный алкинил имеет то же значение в отношении алкинильных групп, что и замещенные алкильные группы относительно незамещенных алкильных групп. Замещенные алкинильные группы включают алкинильные группы, в которых не углеродный или не водородный атом связан с углеродом, связанным тройной связью с другим углеродом, и такие, в которых не углеродный или не водородный атом связан с углеродом, не включенным в тройную связь с другим углеродом. Термин гетероциклил относится к ароматическим и неароматическим циклическим соединениям,включающим моноциклические, бициклические и полициклические циклические соединения, такие как,но не ограничиваясь, хинуклидинил, содержащие 3 или более членов кольца, из которых один или более представляет собой гетероатом, такой как, но не ограничиваясь N, O и S. Хотя термин незамещенный гетероциклил включает конденсированные гетероциклические кольца, такие как бензимидазолил, он не включает гетероциклические группы, которые имеют другие группы, такие как алкильные или галогеновые группы, связанные с одним из членов кольца, как соединения, такие как 2-метилбензимидазолил,являются замещенными гетероциклическими группами. Примеры гетероциклических групп включают,но не ограничены, ненасыщенные 3-8-членные кольца, содержащие от 1 до 4 атомов азота, такие как, но не ограничиваясь, пирролил, пирролинил, имидазолил, пиразолил, пиридил, дигидропиридил, пиримидил, пиразинил, пиридазинил, триазолил (например, 4 Н-1,2,4-триазолил, 1H-1,2,3-триазолил, 2H-1,2,3 триазолил, и др.), тетразолил (например, 1 Н-тетразолил, 2 Н-тетразолил, и др.); насыщенные от 3 до 8 членов кольца, содержащие от 1 до 4 атомов азота, такие как, но не ограничиваясь, пирролидинил, имидазолидинил, пиперидинил, пиперазинил; конденсированные ненасыщенные гетероциклические группы,содержащие от 1 до 4 атомов азота, такие как, но не ограничиваясь, индолил, изоиндолил, индолинил,индолизинил, бензимидазолил, хинолил, изохинолил, индазолил, бензотриазолил; ненасыщенные 3-8 членные кольца, содержащие от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, такие как, но не ограничиваясь, оксазолил, изоксазолил, оксадиазолил (например, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил,1,2,5-оксадиазолил, и др.); насыщенные 3-8-членные кольца, содержащие от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, такие как, но не ограничиваясь, морфолинил; ненасыщенные конденсированные гетероциклические группы, содержащие от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, например,бензоксазолил, бензоксадиазолил, бензоксазинил (например, 2 Н-1,4-бензоксазинил и др.); ненасыщенные 3-8-членные кольца, содержащие от 1 до 3 атомов серы и от 1 до 3 атомов азота, такие как, но не ограничиваясь, тиазолил, изотиазолил, тиадиазолил (например, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,3,4 тиадиазолил, 1,2,5-тиадиазолил, и др.); насыщенные 3-8-членные кольца, содержащие от 1 до 2 атомов серы и от 1 до 3 атомов азота, такие как, но не ограничиваясь, тиазолодинил; насыщенные и ненасыщенные 3-8-членные кольца, содержащие от 1 до 2 атомов серы, такие как, но не ограничиваясь, тиенил, дигидродитиенил, дигидродитионил, тетрагидротиофен, тетрагидротиопиран; ненасыщенные конденсированные гетероциклические кольца, содержащие от 1 до 2 атомов серы и от 1 до 3 атомов азота, такие как,но не ограничиваясь, бензотиазолил, бензотиадиазолил, бензотиазинил (например, 2H-1,4-бензотиазинил, и др.), дигидробензотиазинил (например, 2 Н-3,4-дигидробензотиазинил, и др.), ненасыщенные 38-членные кольца, содержащие атомы кислорода, такие как, но не ограничиваясь, фурил; ненасыщенные конденсированные гетероциклические кольца, содержащие от 1 до 2 атомов кислорода, такие как бензодиоксолил (например, 1,3-бензодиоксоил, и др.); ненасыщенные 3-8-членные кольца, содержащие атом кислорода и от 1 до 2 атомов серы, такие как, но не ограничиваясь, дигидрооксатиенил; насыщенные 3-8 членные кольца, содержащие от 1 до 2 атомов кислорода и от 1 до 2 атомов серы, такие как 1,4-оксатиан; ненасыщенные конденсированные кольца, содержащие от 1 до 2 атомов серы, такие как бензотиенил,бензодитиенил; и ненасыщенные конденсированные гетероциклические кольца, содержащие атомы кислорода и от 1 до 2 атомов серы, такие как бензоксатиенил. Гетероциклические группы также включают группы, описанные выше, в которых один или более атомов S в кольце являются связанными двойной связью с одним или двумя атомами кислорода (сульфоксиды и сульфоны). Например, гетероциклические группы включают тетрагидротиофен, тетрагидротиофеноксид и тетрагидротиофен 1,1-диоксид. Предпочтительные гетероциклические группы содержат 5 или 6 членов кольца. Более предпочтительные гетероциклические группы включают морфолин, пиперазин, пиперидин, пирролидин, имидазол, пиразол,1,2,3-триазол, 1,2,4-триазол, тетразол, тиоморфолин, тиоморфолин, в котором атом S тиоморфолина связан с одним или более атомами О, пиррол, гомопиперазин, оксазолидин-2-он, пирролидин-2-он, оксазол,хинуклидин, тиазол, изоксазол, фуран и тетрагидрофуран. Термин замещенный гетероциклил относится к гетероциклической группе, как определено выше,в которой один из членов кольца связан с не водородным атомом, таким как описано выше в отношении замещенных алкильных групп и замещенных арильных групп. Примеры включают, но не ограничиваются, 2-метилбензимидазолил, 5-метилбензимидазолил, 5-хлорбензтиазолил, 1-метилпиперазинил и 2-хлорпиридил среди остальных. Термин арил относится к арильным группам, которые не содержат гетероатомов. Таким образом,термин включает, но не ограничивается, группы, такие как фенил, бифенил, антраценил, нафтенил в ка-7 011808 честве примера. Хотя термин незамещенный арил включает группы, содержащие конденсированные кольца, такие как нафталин, она не включает арильные группы, которые имеют другие группы, такие как алкильные или галогеновые группы, связанные с одним из членов кольца, так арильные группы, такие как толил, рассматриваются в данном описании как замещенные арильные группы, как описано ниже. Предпочтительной замещенной арильной группой является фенил. Однако незамещенные арильные группы могут быть связаны с одним или более атомом(ами) углерода, атомом(ами) кислорода, атомом(ами) азота и/или атомом(ами) серы в основном соединении. Термин замещенная арильная группа имеет такое же значение в отношении незамещенных арильных групп, которое замещенные алкильные группы имеют в отношении незамещенных алкильных групп. Однако замещенные арильные группы также включают арильные группы, в которых один из ароматических углеродов связан с одним из не углеродных или не водородных атомов, описанных выше, и также включает арильные группы, в которых один или более ароматических углеродов арильной группы связаны с замещенной и/или незамещенной алкильной, алкенильной или алкинильной группой, как определено в данном описании. Это включает связанные расположения, в которых два атома углерода арильной группы связаны с двумя атомами алкильной, алкенильной, или алкинильной группы для определения сшитой системы колец (например, дигидронафтил или тетрагидронафтил). Таким образом, термин замещенный арил включает, но не ограничивается, толил и гидроксифенил среди остальных. Предпочтительные заместители включают линейные и разветвленные алкильные группы, -CH3, -C2H5,-CH2OH, -ОН, -OCH3, -OC2H5, -OCF3, -CN, -NO2, -CO2H, -CO2CH3, -CONH2, -NH2, -F, -Cl, Br, -CF3,-N(CH3)2, -NHSO2CH3, -NHCOCH3. Термин гетероарил, как используется в данном описании, относится к циклическому или бициклическому ароматическому радикалу, имеющему от пяти до десяти атомов в каждом кольце, из которых один атом циклического или бициклического кольца выбирают из S, О и N; ноль, один или два атома кольца являются дополнительными гетероатомами, независимо выбираемыми из S, О и N; и оставшиеся атомы кольца являются углеродом, радикал объединен с остальной частью молекулы посредством любого из атомов в кольце, такой как, например, пиридил, пиразинил, пиримидинил, пирролил, пиразолил,имидазолил, тиазолил, оксазолил, изооксазолил, тиадиазолил, оксадиазолил, тиофенил, фуранил, хинолинил, изохинолинил, и нафтиридинил, и подобные. Термин замещенный гетероарил, как используется в данном описании, относится к гетероарильной группе, как определено в настоящем описании, замещенной независимым замещением одного, двух или трех атомов водорода на нем Cl, Br, F, I, ОН, CN, C1-С 3-алкилом, C1-С 6-алкокси, С 1-С 6-алкокси, замещенным арилом, галогеналкилом, тиоалкокси, амино, алкиламино, диалкиламино, меркапто, нитро,карбоксальдегидом, карбокси, алкоксикарбонилом и карбоксамидом. Кроме того, любой заместитель может быть арильной, гетероарильной или гетероциклоалкильной группой. Предпочтительные заместители включают линейные и разветвленные алкильные группы, -CH3, -C2H5, -CH2OH, -ОН, -OCH3, -OC2H5,-OCF3, -CN, -NO2, -CO2H, -CO2CH3, -CONH2, -NH2, -F, -Cl, Br, -CF3, -N(CH3)2, -NHSO2CH3, -NHCOCH3. Термин биарил относится к группе или заместителю, с которым связаны две арильные группы,которые не конденсированы друг с другом. Примеры биарильных соединений включают, например, фенилбензол, дифенилдиазен, 4-метилтио-1-фенилбензол, феноксибензол, (2-фенилэтинил)бензол, дифенилкетон, (4-фенилбута-1,3-диинил)бензол, фенилбензиламин, (фенилметокси)бензол, и подобные. Предпочтительные необязательно замещенные биарильные группы включают 2-(фениламино)-N-[4-(2 фенилэтинил)фенил]ацетамид, 1,4-дифенилбензол, N-[4-(2-фенилэтинил)фенил]-2-[бензиламино]ацетамид, 2-амино-N-[4-(2-фенилэтинил)фенил]пропанамид, 2-амино-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(циклопропиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-(этиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-[(2-метилпропил)амино]-N-[4-(2-фенилэтинил)фенил]ацетамид, 5-фенил-2 Н-бензо[d] 1,3-диоксолин, 2-хлор-1-метокси-4-фенилбензол, 2-[(имидазолилметил)амино]-N-[4-(2-фенилэтинил)фенил]ацетамид, 4-фенил-1-феноксибензол, N-(2-аминоэтил)[4-(2-фенилэтинил)фенил]карбоксамид, 2-[(4 фторфенил)метил]амино-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-[(4-метилфенил)метил]амино-N-[4(2-фенилэтинил)фенил]ацетамид, 4-фенил-1-(трифторметил)бензол, 1-бутил-4-фенилбензол, 2-(циклогексиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-(этилметиламино)-N-[4-(2-фенилэтинил)фенил] ацетамид, 2-(бутиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, N-[4-(2-фенилэтинил)фенил]-2-(4-пиридиламино)ацетамид,N-[4-(2-фенилэтинил)фенил]-2-(хинуклидин-3-иламино)ацетамид,N-[4-(2 фенилэтинил)фенил]пирролидин-2-илкарбоксамид, 2-амино-3-метил-N-[4-(2-фенилэтинил)фенил]бутанамид, 4-(4-фенилбута-1,3-диинил)фениламин, 2-(диэтиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил] ацетамид, 2-(этиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил]ацетамид, 4-этил-1-фенилбензол, 1-[4-(2 фенилэтинил)фенил]этан-1-он,N-(1-карбамоил-2-гидроксипропил)[4-(4-фенилбута-1,3-диинил)фенил] карбоксамид, N-[4-(2-фенилэтинил)фенил]пропанамид, 4-метоксифенилфенилкетон, фенил-N-бензамид,(трет-бутокси)-N-[(4-фенилфенил)метил]карбоксамид, 2-(3-фенилфенокси)этангидроксамовая кислота, 3 фенилфенилпропаноат, 1-(4-этоксифенил)-4-метоксибензол и [4-(2-фенилэтинил)фенил]пиррол. Термин гетероариларил относится к биарильной группе, где одна из арильных групп является гетероарильной группой. Примеры гетероариларильных групп включают, например, 2-фенилпиридин, фенилпиррол, 3-(2-фенилэтинил)пиридин, фенилпиразол, 5-(2-фенилэтинил)-1,3-дигидропиримидин-2,4-8 011808 дион, 4-фенил-1,2,3-тиадиазол, 2-(2-фенилэтинил)пиразин, 2-фенилтиофен, фенилимидазол, 3-(2 пиперазинилфенил)фуран, 3-(2,4-дихлорфенил)-4-метилпиррол и подобные. Предпочтительные необязательно замещенные гетероариларильные группы включают 5-(2-фенилэтинил)пиримидин-2-иламин, 1 метокси-4-(2-тиенил)бензол, 1-метокси-3-(2-тиенил)бензол, 5-метил-2-фенилпиридин, 5-метил-3 фенилизоксазол,2-[3-(трифторметил)фенил]фуран,3-фтор-5-(2-фурил)-2-метокси-1-проп-2-фенилбензол, (гидроксиимино) (5-фенил(2-тиенилметан, 5-[(4-метилпиперазинил)метил]-2-фенилтиофен, 2(4-этилфенил)тиофен, 4-метилтио-1-(2-тиенил)бензол, 2-(3-нитрофенил)тиофен, (трет-бутокси)-N-[(5 фенил(3-пиридилметил]карбоксамид, гидрокси-N-[(5-фенил(3-пиридилметил]амид, 2-(фенилметилтио)пиридин и бензилимидазол. Термин гетероарилгетероарил относится к биарильной группе, где обе арильные группы являются гетероарильными группами. Примеры гетероарилгетероарильных групп включают, например, 3 пиридилимидазол, 2-имидазолилпиразин и подобные. Предпочтительные необязательно замещенные гетероарилгетероарильные группы включают 2-(4-пиперазинил-3-пиридил)фуран, диэтил(3-пиразин-2 ил(4-пиридиламин и диметил 2-[2-(5-метилпиразин-2-ил)этинил](4-пиридил)амин. Термин необязательно замещенный относится к необязательному замещению водорода одним или более одновалентными или двухвалентными радикалами. Необязательно замещенные группы включают описанные в настоящем описании для каждой группы, в которой представлено особое определение для замещения. Кроме того, подходящие замещающие группы включают, например, гидроксил, нитро,амино, имино, циано, галоген, тио, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино,имидино, гуанидино, сульфонамидо, карбоксил, формил, алкил, замещенный алкил, галоген-низший алкил, низший алкокси, галоген-низший алкокси, низший алкоксиалкил, алкилкарбонил, арилкарбонил,аралкилкарбонил, гетероарилкарбонил, гетероаралкилкарбонил, алкилтио, аминоалкил, цианоалкил, бензил, пиридил, пиразолил, пиррол, тиофен, имидазолил и подобные. Характерные замещенные амидино и гетероциклоамидиногруппы включают, например, показанные ниже. Такие амидино и гетероциклоамидиногруппы далее могут быть замещены, как очевидно специалисту, обладающему умениями в области техники органической и медицинской химии в связи с настоящим описанием. Характерные замещенные алкилкарбониламино, алкилоксикарбониламино, аминоалкилоксикарбониламино и арилкарбониламиногруппы включают, например, представленные ниже. Такие группы могут быть далее замещенными, как очевидно специалисту. Характерные замещенные аминокарбонильные группы включают, например, представленные ниже. Они могут быть далее замещенными гетероциклогруппами и гетероарильными группами, как очевидно специалисту. Предпочтительные аминокарбонильные группы включают N-(2-цианоэтил)карбоксамид, N(3-метоксипропил)карбоксамид, N-циклопропилкарбоксамид, N-(2-гидроксиизопропил)карбоксамид,метил 2-карбониламино-3-гидроксипропаноат, N-(2-гидроксипропил)карбоксамид, N-(2-гидроксиизопропил)карбоксамид, N-[2-гидрокси-1-(гидроксиметил)этил]карбоксамид, N-(2-карбониламиноэтил) ацетамид, N-(2-(2-пиридил)этил)карбоксамид, N-(2-пиридилметил)карбоксамид, N-(оксолан-2-илметил) карбоксамид, N-(4-гидроксипирролидин-2-ил)карбоксамид, N-[2-(2-гидроксиэтокси)этил]карбоксамид,N-(4-гидроксициклогексил)карбоксамид, N-[2-(2-оксо-4-имидазолинил)этил]карбоксамид, N-(карбониламинометил)ацетамид, N-(3-пирролидинилпропил)карбоксамид, N-[1-(карбониламинометил)пирролидин-3-ил]ацетамид, N-(2-морфолин-4-илэтил)карбоксамид, N-[3-(2-оксопирролидинил)пропил]карбоксамид, 4-метил-2-оксопиперазинкарбальдегид, N-(2-гидрокси-3-пирролидинилпропил)карбоксамид, N(2-гидрокси-3-морфолин-4-илпропил)карбоксамид, N-2-[(5-циано-2-пиридил)амино]этилкарбоксамид,3-(диметиламино)пирролидинкарбальдегид,N-[(5-метилпиразин-2-ил)метил]карбоксамид,2,2,2 трифтор-N-(1-формилпирролидин-3-ил)ацетамид,Характерные замещенные алкоксикарбонильные группы включают, например, представленные ниже. Такие алкоксикарбонильные группы могут быть далее замещены гетероциклогруппами и гетероарильными группами, как очевидно специалисту в области техники органической и медицинской химии в связи с настоящим описанием. Термин защищенная в отношении к гидроксильным группам, аминогруппам и сульфгидрильным группам относится к формам таких функциональных групп, которые защищены от нежелательных реакций защитной группой, известной специалисту в области техники, такой как установленные в ProtectiveGroups in Organic Synthesis, Greene, T.W.; Wuts, P. G. M., John WileySons, New York, NY, (3rd Edition,1999), которые могут быть добавлены или удалены с использованием методик, изложенных в данном описании. Примеры защищенных гидроксильных групп включают, но не ограничиваясь, силиловые эфиры, такие как полученные реакцией гидроксильной группы с реагентом, таким как, но не ограничиваясь,трет-бутилдиметилхлорсилан, триметилхлорсилан, триизопропилхлорсилан, триэтилхлорсилан; замещенные метиловые и этиловые эфиры, такие как, но не ограничиваясь, метоксиметиловый эфир, метилтиометиловый эфир, бензилоксиметиловый эфир, трет-бутоксиметиловый эфир, 2-метоксиэтоксиметиловый эфир, тетрагидропираниловые эфиры, 1-этоксиэтиловый эфир, аллиловый эфир, бензиловый эфир; сложные эфиры, такие как, но не ограничиваясь, бензоилформиат, формиат, ацетат, трихлорацетат и трифторацетат. Примеры защищенных аминогрупп включают, но не ограничиваясь, амиды, такие как формамид, ацетамид, трифторацетамид и бензамид; имиды, такие как фталимид и дитиосукцинимид; и другие. Примеры защищенных сульфгидрильных групп включают, но не ограничиваясь, тиоэфиры, такие как S-бензиловый тиоэфир, и S-4-пиколиловый тиоэфир; замещенные S-метиловые производные,такие как гемитио, дитио и аминотиоацетали; и другие. Термин фармацевтически приемлемая соль включает соль с неорганическим основанием, органическим основанием, неорганической кислотой, органической кислотой или основной или кислой аминокислотой. В качестве соли неорганических оснований изобретение включает, например, щелочные металлы, такие как натрия или калий; щелочно-земельные металлы, такие как кальций и магний или алюминий; и аммиак. В качестве соли органических оснований изобретение включает, например, триметиламин, триэтиламин, пиридин, пиколин, этаноламин, диэтаноламин и триэтаноламин. В качестве соли неорганических кислот настоящее изобретение включает, например, соли соляной кислоты, гидроборной кислоты, азотной кислоты, серной кислоты и фосфорной кислоты. В качестве соли органических кислот настоящее изобретение включает, например, соли муравьиной кислоты, уксусной кислоты, трифторуксусной кислоты, фумаровой кислоты, щавелевой кислоты, винно-каменной кислоты, малеиновой кислоты, лимонной кислоты, янтарной кислоты, яблочной кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты и п-толуолсульфоновой кислоты. В качестве соли основных аминокислот настоящее изобретение включает, например, аргинин, лизин и орнитин. Кислые аминокислоты включают, например, аспарагиновую кислоту и глутаминовую кислоту. Как используется в данном описании, термин фармацевтически приемлемый сложный эфир относится к сложным эфирам, которые гидролизуются in vivo и включают эфиры, которые легко разрушаются в человеческом организме, оставляя исходное соединение или его соль. Подходящие группы сложных эфиров включают, например, полученные из фармацевтически приемлемых алифатических карбоновых кислот, особенно алкановых, алкеновых, циклоалкановых и алкандикарбоновых кислот, в которых каждый алкильный или алкенильный компонент преимущественно имеет не более чем 6 атомов углерода. Характерные примеры определенных сложных эфиров включают, но не ограничиваются, формиаты,- 10011808 ацетаты, пропионаты, бутираты, акрилаты и этилсукцинаты. Термин фармацевтически приемлемые пролекарства, как используется в данном описании, относится к таким пролекарствам соединений по настоящему изобретению, которые являются, с точки зрения специалиста, подходящими для применения в контакте с тканями человека и низших млекопитающих без нежелательной токсичности, раздражения, аллергического ответа и подобного, соответствующим разумному соотношению польза/риск и эффективным для предназначенного использования, а также цвиттерионным формам, где возможно, соединений по изобретению. Термин пролекарство относится к соединениям, которые быстро преобразуются in vivo с получением исходного соединения по вышеуказанной формуле, например, гидролизом в крови. Полное обсуждение представлено в T. Higuchi и V.Stella, Pro-drugs as Novel Delivery Systems, Vol. 14 of the A.C.S. Symposium Series, и in Edward B. Roche,ed., Bioreversible Carriers in Drug Design, American Pharmaceutical Association и Pergamon Press, 1987, оба из которых включены в данное описание в виде ссылки. Термин антибактериальный агент относится к агентам, синтезированным или модифицированным в лаборатории, которые обладают и бактерицидной или бактериостатической активностью. Активный агент в таком смысле будет ингибировать рост P. aeruginosa и других грамотрицательных бактерий. Термин ингибирование роста указывает, что скорость увеличения количества популяции определенной бактерии снижается. Следовательно, термин включает ситуации, в которых бактериальная популяция увеличивается, но со сниженной скоростью, а также ситуации, когда рост популяции остановлен, а также ситуации, когда количество бактерий в популяции снижено или популяция даже уничтожена. Если используется исследование активности фермента для скрининга ингибиторов, можно производить модификации в потреблении/выделении, растворимости, полужизни и др. соединений с целью корреляции ингибирования фермента с ингибированием роста. Активность антибактериальных агентов не обязательно ограничена бактериями, но также может включать активность в отношении паразитов, вирусов и грибов. Настоящее изобретение также включает меченные изотопами ингибиторы LpxC, которые являются структурно идентичными описанным выше при том, что один или более атомов являются замещенными атомом, имеющим атомную массу или массовое число, отличное от атомной массы или массового числа,обычно обнаруживаемого в природе. Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора и хлора,такие как 2H, 3H, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F и 36Cl, соответственно. Соединения по настоящему изобретению, их пролекарства и фармацевтически приемлемые соли указанных соединений и указанных пролекарств, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, находятся в объеме настоящего изобретения. Определенные меченные изотопами соединения по настоящему изобретению, например, те, в которые включены радиоактивные изотопы, такие как 3H и 14C, являются применимыми в исследованиях лекарственных средств и/или распределения в тканях субстратов. Меченные тритием, т.е. 3H, и углеродом-14, т.е. 14C, изотопы являются особенно предпочтительными из-за простоты их получения и определяемости. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может давать определенные терапевтические преимущества, возникающие в результате более высокой метаболической стабильности, например, увеличенной in vivo полужизни или сниженной дозы и, следовательно, может быть предпочтительным в некоторых обстоятельствах. Меченные изотопами соединения по настоящему изобретению и их пролекарства могут обычно быть получены проведением известных или ссылочных методик и замещением легко доступного меченного изотопом реагента реагентом, не меченным изотопом. Настоящее изобретение относится к новым соединениям, фармацевтическим композициям, включающим соединения, способам ингибирования УДФ-3-O-(R-3-гидроксидеканоил)-N-ацетилглюкозаминдеацетилазы (LpxC), и способам лечения грамотрицательных бактериальных инфекций. В одном варианте воплощения изобретения настоящее изобретение относится к соединениям формулы I или их стереоизомерам, фармацевтически приемлемым солям, сложным эфирам и пролекарствам,где E отсутствует или выбран из группы, состоящей из(1) H,(2) C1-С 6-алкила; C1-С 6-алкила, замещенного одним или более ОН, F, Cl, Br, I, CN, COOH, NH2,N(CH3)2, N(CH2CH3)3+, NHC(O)CH3, C(O)NHOH, C(O)NH2, N(CH(CH3)2)2, OCH3, NHC(O)OCCH3,NHC(NH)NH2, NHSO2CH3, OCH2CH3 или оксо; циклопропила; циклопропила, замещенного фенилом; циклобутила; циклопентила, циклогексила; циклогексила, замещенного одним или более NH2 или C1-С 6 алкилом; -(C1-С 6-алкил)циклогексила; циклогептила; бициклогептила; -(C1-С 6-алкил)бициклогептила;-(C1-С 6-алкил)бициклогептила, где бициклогептил замещен одним или более C1-С 6-алкилом; циклоокти- 11011808 ла; -(С 1-С 6-алкил)трициклодецила; -(C1-C6-алкил)пиперидинила; -(C1-С 6-алкил)пиперидинила, где пиперидинил замещен одним или более ацетилом, C(O)NH2, CF3, фенилом или пиперидинилом; -(C1-С 6 алкил)пиперазинила; -(C1-C6-алкил)пиперазинила, где пиперазинил замещен одним или более C1-С 6 алкилом, фенилом или фенилом, замещенным одним или более F, Cl, Br или I; -(C1-С 6-алкил)пиридила;-(C1-С 6-алкил)тиенила; -(C1-С 6-алкил)бензотиенила; -(С 1-С 6-алкил)имидазолила; -(C1-C6-алкил)морфолинила; -(C1-С 6-алкил)азепанила; -(C1-C6-алкил)пирролидинила; -(C1-С 6-алкил)пирролидинила, где пирролидинил замещен одним или более оксо, диметиламино, амино, ацетиламино или NHC(O)CF3; -(C1-С 6 алкил)фенила; или -(C1-C6-алкил)фенила, где фенил замещен одним или более F, Cl, Br, I, ОН, SCH3,SO2CH3, SCF3, CF3, NO2, NH2, N(CH3)2, OCH3, OCF3 или C1-С 6-алкила;(3) С 2-С 6-алкенила или С 2-С 6-алкенила, замещенного одним или более F, Cl, Br, или фенилом;(4) фенила или фенила, замещенного одним или более F, Cl, Br, I, ОН, NH2, NO2, OC6H5, OCH3,OCF3, OPO(OH)2, CN, CNOH, SO2CH3, SCH3, CF3 или C1-С 6-алкилом;(5) бензимидазолила; бензотиенила; пиперазинила; пиперазинила, замещенного одним или болееC1-С 6-алкилом или фенилом; пирролидинила; пирролидинила, замещенного одним или более NH2,NHC(O)CF3, или N (CH3)2; ацетиламинопирролидинила; морфолинила; азепанила; пиразолила; тиадиазолила; имидазолила; тетрагидропиримидинила; пирролидинонила; пиперидинила; пиперидинила, замещенного одним или более ацетилом, пиперидинилом, CF3, фенилом или фенилом, замещенным одним или более F, Cl, Br, I, C(O)NH2 или ацетилом; и(6) тиенила; тиенила, замещенного CHNOH; пиридила; или пиридила, замещенного одним или более C1-С 6-алкилом, F, Cl, Br, I, ОН, COOH или OCH3;L отсутствует или выбирают из группы, состоящей из(8) -NHCO-,где R1L, R2L и R3L независимо выбирают из группы, состоящей из(c) C1-С 6-алкила, замещенного фенилом; или фенила, замещенного одним или более F, Cl, Br, I,OCH3, CF3, OCF3 или C1-С 6-алкилом,(d) C1-С 6-алкила, замещенного одним или более пирролидинилом, морфолинилом, азепинилом,карбоксамидпирролидинилом, ацетиламинопирролидинилом, диметиламинопирролидинилом, аминопирролидинилом или пиперидинилом, и(е) C1-С 6-алкила, замещенного пиридилом или имидазолилом,или R1L и R3L, вместе с атомами, к которым они присоединены, могут образовывать пирролидиновое или пиперидиновое кольцо;j представляет собой целое число от 0 до 4; иk представляет собой целое число от 0 до 4;D отсутствует или выбирают из группы, состоящей из(1) С 3-С 8-циклоалкила,(2) фенила; или фенила, замещенного одним или более F, Cl, Br, I, CF3, NO2, ОН, OCH3, OCF3,ОС(О)(C1-С 6-алкилом), гидроксиамино-2-оксоэтилокси, метилсульфониламино, аминоацетиламино, метилсульфониламинометилом, диметиламино, диэтиламино, фенилсульфониламино или C1-С 6-алкил; и(3) тиенила; пиразинила; пиридила; пиридила, замещенного одним или более F, Cl, Br или I; пиримидинила; или пиримидинила, замещенного амино;G отсутствует или выбирают из группы, состоящей изi представляет собой целое число от 0 до 4;(1) С 3-С 8-циклоалкила,(2) флуоренила; фенила; или фенила, замещенного одним или более F, Cl, Br, I, CN, CF3,SCH2(C6H5), SCH3, NH2, NHSO2CH3, CH2NHSO2CH3, NHSO2(C6H5), NHSO2(C6H4Br), N2(C6H5), ОН, OCF3,CHO, С 3-С 4-алкенилом, С 3-С 4-алкенилом, замещенным одним или более F, или С 1-С 4 алкокси;(3) пирролидинила; фуранила; бензодиоксоила; хроменила; бензофуранила; тиенила; или тиенила,замещенного одним или более F, Cl, Br, I или ОН; и(4) пиридинила; пиридинила, замещенного одним или более F, Cl, Br, I, COOH или CF3; пиримидинила, замещенного одним или более NH2 или OCH3; или хинолинила;(1) -(C=O)-,(2) -C1-С 6-алкил-(C=O)-, где алкил незамещен или замещен NH2,(3) -С 2-С 6-алкенил-(C=O)-,(4) -С 2-С 6-алкинил-(C=O) - и где R1b и R2b независимо выбирают из группы, состоящей из(a) H,(b) C1-С 6-алкила или C1-С 6-алкила, замещенного одним или более NH2, CN, COOH, ОН, оксо, ацетиламино или C(O)NH2;(f) C1-С 6-алкила, замещенного фенилом или фенилом, замещенным ОН; иq представляет собой целое число от 0 до 4;R4 представляет собой H или C1-С 6-алкил,R1a, R2a, R4a и R5a независимо выбирают из группы, состоящей из(b) циклобутила; C1-С 6-алкила; C1-С 6-алкила, замещенного одним или более оксо, -NHC(О)О(C1-С 6 алкилом), -S(C1-C6-алкилом), замещенным одним или более ОН или COOH, NH2, -NH(C1-С 6-алкилом),-NH(C1-C6-алкилом), где алкил замещен одним или более NH2, имидазолилом, NHC(O)O(C1-С 6-алкилом),COOH, C(O)NH2, С(О)О(C1-С 6-алкилом), С(О)NH-(C1-С 6-алкилом), где алкил замещен NH2, фенилом или фенилом, замещенным ОСН 3;(c) -С(O)O-(С 1-С 6-алкила); -C(O)NH2; -C(NH)NH2; -C(O)-морфолинила; -C(O)-(C1-С 6-алкил)морфолинила; -C(O)-пиридинила, где пиридинил замещен одним или более ОН, -С(О)-фенилом, где фенил замещен одним или более ОН;r представляет собой целое число от 0 до 4; где В отсутствует, или E, L, G и B отсутствуют, или E, L и G отсутствуют, или E, L и В отсутствуют, или E, L, D, G и B отсутствуют. В другом варианте воплощения настоящее изобретение относится к соединениям формулы III(3) -С 2-С 6-алкенил-(C=O)-. В другом варианте воплощения настоящее изобретение относится к соединениям формулы V или их стереоизомерам, фармацевтически приемлемым солям или сложным эфирам, где D-G-Y,взятые вместе, выбирают из группы, состоящей из(3) -С 2-С 6-алкенил-(C=O)-. В другом варианте воплощения настоящее изобретение относится к соединениям формулы VII или их стереоизомерам или фармацевтически приемлемым солям, где E отсутствует или выбран из группы, состоящей из C1-С 6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br или I; циклопропила, циклобутила; и C1-С 6-алкила, замещенного пиридилом; иR1L и R3L оба представляют собой H. В другом варианте воплощения настоящее изобретение относится к соединениям формулы IX или их стереоизомерам или фармацевтически приемлемым солям, где E отсутствует или выбран из группы, состоящей из(1) H,(2) циклопропила; циклобутила; циклопентила, циклогексила; циклогептила; бициклогептила; C1 С 6-алкила, незамещенного или замещенного одним или более гидрокси, С 1-С 6-алкокси, ди(С 1-С 6-алкил) амино, циано или циклогексилом;(3) фенила; или фенила, замещенного одним или более F, Cl, Br или I; C1-С 6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С 6-алкилом или C1-С 6 алкокси; и(4) пиридинила, пиразинила или C1-С 6-алкила, замещенного пиридинилом или тиофенилом; или E и R3L, вместе с атомами, к которым они присоединены, могут образовывать пирролидинил,азепанил, имидазолил, морфолино, пиперидинил, пиперазинил или пиперазинил, замещенный C1-С 6 алкилом;R1L, R3L независимо выбирают из группы, состоящей из(2) C1-С 6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С 6-алкокси, ди(3) C1-С 6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl,Br, I, C1-С 6-алкилом или C1-С 6-алкокси; и(4) C1-С 6-алкила, замещенного пиридинилом или тиофенилом. В другом варианте воплощения настоящее изобретение относится к соединениям формулы X или их стереоизомерам или фармацевтически приемлемым солям, где E отсутствует или выбран из группы, состоящей из(2) циклопропила; циклобутила; циклопентила; циклогексила; циклогептила; бициклогептила; C1 С 6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С 6-алкокси, ди(C1-C6- 16011808 алкил)амино, циано или циклогексилом;(3) фенила; или фенила, замещенного одним или более F, Cl, Br или I; C1-С 6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl, Br, I, C1-С 6-алкилом или C1-С 6 алкокси; и(4) пиридинила, пиразинила или C1-С 6-алкила, замещенного пиридинилом или тиофенилом; или E и R3L, вместе с атомами, к которым они присоединены, могут образовывать пирролидинил,азепанил, имидазолил, морфолино, пиперидинил, пиперазинил или пиперазинил, замещенный C1-С 6 алкилом;R1L, R3L независимо выбирают из группы, состоящей из(2) C1-С 6-алкила, незамещенного или замещенного одним или более гидрокси, C1-С 6-алкокси, ди(3) C1-С 6-алкила, замещенного фенилом, который незамещен или замещен одним или более F, Cl,Br, I, C1-С 6-алкилом, или C1-С 6-алкокси; и(4) C1-С 6-алкила, замещенного пиридинилом или тиофенилом. В другом аспекте изобретение относится к ингибированию LpxC, таким образом модулируя вирулентность бактериальной инфекции, включающему введение пациенту, нуждающемуся в таком ингибировании, соединения формулы I. В некоторых вариантах воплощения способа ингибирования LpxC с использованием соединения формулы I значение ИК 50 соединения составляет менее или равное 10 мкМ в отношении LpxC. В других таких вариантах воплощения значение ИК 50 составляет менее чем или равное 1 мкМ, составляет менее чем или равное 0,1 мкМ, составляет менее чем или равное 0,050 мкМ, составляет менее чем или равное 0,030 мкМ, составляет менее чем или равное 0,025 мкМ, или составляет менее чем или равное 0,010 мкМ. В одном аспекте изобретение относится к способу лечения субъекта, включающему введение субъекту антибактериально эффективного количества соединения формулы I, вместе с фармацевтически приемлемым носителем. В предпочтительном варианте воплощения способа лечения субъектом является млекопитающее и в некоторых вариантах воплощения - человек. В другом аспекте изобретение относится к способу введения ингибирующего количества соединения формулы I к ферментирующим или неферментирующим грамотрицательным бактериям. В предпочтительном варианте воплощения способа введения ингибирующего количества соединения формулы I ферментирующим или неферментирующим грамотрицательным бактериям, грамотрицательные бактерии выбирают из группы, состоящей из Pseudomonas aeruginosa, Stenotrophomonas maltophila,Burkholderia cepacia, Alcaligenes xylosoxidans, Acinetobacter, Enterobacteriaceae, Haemophilus, виды Neisseria. В другом варианте воплощения изобретение относится к способу введения ингибирующего количества соединения формулы I грамотрицательным бактериям, таким как Enterobacteriaceae, которые выбирают из группы, состоящей из микроорганизмов, таких как Serratia, Proteus, Klebsiella, Enterobacter,Citrobacter, Salmonella, Providencia, Morganella, Cedecea и виды Edwardsiella и Escherichia coli. Другой вариант воплощения изобретения относится к фармацевтической композиции, включающей эффективное количество соединения по формуле I с его фармацевтически приемлемым носителем. Фармацевтические композиции по настоящему изобретению, которые включают любое из соединений, описанных выше в комбинации с фармацевтически приемлемым носителем. Другой вариант воплощения изобретения относится к способу совместного введения соединения формулы I с другими терапевтическими агентами, которые выбирают за их определенную применимость в отношении состояний, которые подвергаются лечению. Например, соединение формулы I является применимым в комбинации с другими антибактериальными агентами. Соединение формулы I увеличивает чувствительность бактерий к существующим классам антибактериальных препаратов. Комбинации настоящих описанных соединений с другими антибактериальными агентами находятся в объеме настоящего изобретения. Такие антибактериальные агенты включают, но не ограничиваются, эритромицин, рифампицин, налидиксовую кислоту, карбенициллин,бацитрацин, циклосерин, фосфомицин и ванкомицин. Следующим аспектом изобретения является применение ингибиторов LpxC для лечения инфекции,особенно бактериальной инфекции. Бактериальная инфекция, подвергаемая лечению соединениями по изобретению, может быть первичной инфекцией или соинфекцией, вызываемой видами бактерий и одним или более дополнительными инфекционными агентами, выбираемыми из группы, состоящей из бактерий, вирусов, паразитов и грибов. Термин лечение, как используется в настоящем описании, относится к реверсии, облегчению, ингибированию прогрессирования или предотвращению расстройства или состояния, к которому такой термин применяется, или одного или более симптомов такого расстройства или состояния. Термин лечение, как используется в настоящем описании, относится к действию лечения, как лечение определено непосредственно выше. Соединения по изобретению могут быть использованы для лечения состояний, вызванных бактери- 17011808 альной продукцией эндотоксина и, в частности, грамотрицательными бактериями и бактериями, которые используют LpxC в биосинтезе липополисахарида (ЛПС (LPS или эндотоксина. Соединения по изобретению также являются применимыми в состояниях, которые вызываются или усиливаются бактериальной продукцией липида А и ЛПС или эндотоксина, таких как сепсис, септический шок, системное воспаление, локализованное воспаление, хронические обструктивные заболевания легких (ХОБЛ) и обострение хронического бронхита (ОХБ). Для таких состояний лечение включает введение соединения по изобретению или комбинации соединений по изобретению, необязательно со вторым агентом, где второй агент представляет собой второй антибактериальный агент или второй неантибактериальный агент. Для сепсиса, септического шока, системного воспаления, местного воспаления, хронических обструктивных заболеваний легких (ХОБЛ) и обострений хронического бронхита (ОХБ), предпочтительные вторые неантибактериальные агенты включают антиэндотоксины, включая антитела, связывающие рецептор эндотоксина, антитела, связывающие эндотоксин, антитела, связывающие анти-CD14-белок,антитела, связывающие антилипополисахарид и ингибиторы тирозинкиназ. В лечении серьезных или хронических инфекций дыхательного тракта соединения по настоящему изобретению также могут быть использованы со вторыми неантибактерильными агентами, вводимыми посредством ингаляции. Предпочтительные неантибактериальные агенты, используемые в таком лечении, включают противовоспалительные стероиды, нестероидные противовоспалительные средства, бронхорасширяющие средства, муколитики, противоастматические лекарственные средства и поверхностноактивные вещества жидкости легких, в частности, неантибактериальный агент может быть выбран из группы, состоящей из альбутерола, сальбутерола, будесонида, беклометазона, дексаметазона, недокромила, беклометазона, флутиказона, флунизолида, триамцинолона, ибупрофена, рофекоксиба, напроксена,целекоксиба, недокромила, ипратропия, метапротеренола, пирбутерола, сальметерола, бронхорасширяющих средств, муколитиков, сальфактанта, берактанта, порактанта-альфа, сурфаксина и пульмозима(также называемого дорназ-альфа). Соединения по изобретению могут быть использованы отдельно или в комбинации со вторым антибактериальным агентом для лечения серьезных или хронических инфекций дыхательного тракта,включая серьезные инфекции легких и внутрибольничные инфекции, такие как вызываемые Enterobacteraerogenes, Enterobacter cloacae, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Proteus mirabilis,Serratia marcescens, Stenotrophomonas maltophilia, Pseudomonas aeruginosa, Burkholderia cepacia, Acinetobacter calcoaceticus, Alcaligenes xylosoxidans, Flavobacterium meningosepticum, Providencia stuartii и Citrobacter freundi, общественные инфекции легких, такие как вызванные Haemophilus influenzae, видами Legionella, Moraxella catarrhalis, Branhamella catarrhalis, видами Enterobacter, видами Acinetobacter, видамиKlebsiella, и видами Proteus, и инфекции, вызванные другими видами бактерий, такими как виды Neisseria, виды Shigella, виды Salmonella, Helicobacter pylori, Vibrionaceae и виды Bordetella, а также инфекции,вызванные видами Brucella species, Francisella tularensis и/или Yersinia Pestis. При использовании для лечения инфекций, вызываемых грамотрицательными бактериями, соединения по настоящему изобретению могут быть использованы для повышения чувствительности грамотрицательных бактерий к действию второго агента. Когда соединения по настоящему изобретению используют в комбинации со вторым антибактериальным агентом, неограничивающие примеры антибактериальных агентов могут быть выбраны из следующих групп:(3) монобактамы, такие как пенициллин G, пенициллин V, метициллин, оксациллин, клоксациллин,диклоксациллин, нафциллин, ампициллин, амоксициллин, карбенициллин, тикарциллин, мезлоциллин,пиперациллин, азлоциллин, темоциллин, цепалотин, цефапирин, цефрадин, цефалоридин, цефазолин,цефамандол, цефуроксим, цефалексин, цефпрозил, цефаклор, лоракарбеф, цефокситин, цефинетазол, цефотаксим, цефтизоксим, цефтриаксон, цефоперазон, цефтазидим, цефиксим, цефподоксим, цефтибутен,цефдинир, цефпиром, цефепим и азтреонам;(4) хинолоны, такие как налидиксовая кислота, оксолиновая кислота, норфлоксацин, пефлоксацин,эноксацин, офлоксацин, левофлоксацин, ципрофлоксацин, темафлоксацин, ломефлоксацин, флероксацин, грепафлоксацин, спарфлоксацин, тровафлоксацин, клинафлоксацин, гатифлоксацин, моксифлоксацин, ситафлоксацин, ганефлоксацин, гемифлоксацин и пазуфлоксацин;(8) рифамицины, такие как рифампицин (также называемый рифампин), рифапентин, рифабутин,безоксазинорифамицин и рифаксимин;(9) линкозамиды, такие как линкомицин и клиндамицин;(10) гликопептиды, такие как ванкомицин и тейкопланин;(11) стрептограмины, такие как хинупристин и дафлопристин;(14) триметоприм и бацитрацин. Второй антибактериальный агент может вводиться в комбинации с соединениями по настоящему изобретению, причем второй антибактериальный агент вводят перед, одновременно или после введения соединения или соединений по настоящему изобретению. Когда является желательным одновременное введение соединения по изобретению со вторым агентом и путь введения является одинаковым, тогда соединение по изобретению может составлять со вторым агентом одну лекарственную форму. Примером лекарственной формы, содержащей соединение по изобретению и второй агент, является таблетка или капсула. При использовании для лечения серьезных или хронических инфекций дыхательного тракта соединения по изобретению могут быть использованы отдельно или в комбинации со вторым антибактериальным агентом, вводимым посредством ингаляции. В случае ингаляции предпочтительный второй антибактериальный агент выбирают из группы, состоящей из тобрамицина, гентамицина, азтреонама, ципрофлоксацина, полимиксина, колистина, колимицина, азитромицина и кларитромицина. Фармацевтические композиции Фармацевтические композиции по настоящему изобретению включают терапевтически эффективное количество соединения по настоящему изобретению вместе с одним или более фармацевтически приемлемыми носителями. Как используется в данном описании, термин фармацевтически приемлемый носитель обозначает нетоксический, инертный твердый, полутвердый или жидкий наполнитель, разбавитель, инкапсулирующее вещество или рецептурную добавку любого типа. Некоторыми примерами веществ, которые могут служить в качестве фармацевтически приемлемых носителей, являются сахара,такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; вспомогательные вещества, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло; сафлоровое масло; кунжутное масло; оливковое масло; кукурузное масло и соевое масло; гликоли; такие как пропиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные агенты, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатный буферный раствор, а также другие нетоксические совместимые смазывающие агенты, такие как лаурилсульфат натрия и стеарат магния, а также красящие агенты, высвобождающие средства, глазировочные средства (покрытия), подслащающие, вкусовые и ароматизирующие агенты, консерванты и антиоксиданты также могут присутствовать в композиции в соответствии с мнением разработчика рецептур. Фармацевтические композиции по настоящему изобретению могут вводиться людям и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, интраперитонеально, местно (как в виде порошков, мазей или капель),буккально или в виде орального или назального спрея или жидкого аэрозоля или композиции сухого порошка для ингаляций. Жидкие лекарственные формы для перорального введения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В добавление к активным соединениям жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в области техники, такие как, например, вода или другие растворители, солюбилизирующие компоненты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности,хлопковое, арахисовое, кукурузное, проростковое, оливковое, касторовое и кунжутное масла), глицерин,тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры сорбита и жирных кислот и их смеси. Кроме инертных разбавителей пероральные композиции могут также включать добавки, такие как увлажняющие агенты, эмульгирующие и суспендирующие агенты, подслащающие, вкусовые и ароматизирующие агенты. Инъекционные препараты, например, стерильные инъекционные водные или масляные суспензии могут быть приготовлены в соответствии с известной методикой с использованием подходящих диспергирующих или увлажняющих агентов и суспендирующих агентов. Стерильные инъекционные препараты могут также быть стерильными инъекционными растворами, суспензиями или эмульсиями в нетоксичном приемлемом для парентерального применения разбавителе или растворителе, например, как раствор в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, которые могут применяться, находятся вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно используют в качестве растворителя или суспендирующей среды. С этой целью любое- 19011808 легкое нелетучее масло может применяться, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, используют в получении инъекционных препаратов. Инъекционные композиции могут быть стерилизованы, например, фильтрацией через фильтр,удерживающий бактерии, или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъекционной среде перед использованием. С целью продления эффекта лекарственного средства часто желательно замедлить всасывание лекарственного средства из подкожной или внутримышечной инъекции. Это может быть достигнуто использованием кристаллического или аморфного вещества с плохой растворимостью в воде. Итак, скорость всасывания лекарственного средства зависит от его скорости растворения, которая, в свою очередь,может зависеть от размера кристаллов и кристаллической формы. Альтернативно, замедленное всасывание вводимого парентерально лекарственного средства может достигаться растворением или суспендированием лекарственного средства в масляном носителе. Инъекционные депо-формы сделаны путем создания микроинкапсулированных матриц лекарственного средства в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от соотношения лекарственного средства и полимера и природы определенного используемого полимера, скорость высвобождения лекарственного средства может регулироваться. Примеры других биоразлагаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъекционные композиции депо также могут быть получены заключением лекарственного средства в липосомы или микроэмульсии, которые совместимы с тканями тела. Композициями для ректального или вагинального введения являются предпочтительно суппозитории, которые могут быть получены смешиванием соединений по настоящему изобретению с подходящими нераздражающими вспомогательными веществами или носителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, который является твердым при температуре окружающей среды, но жидким при температуре тела и, следовательно, тает в прямой кишке или полости влагалища и высвобождает активное соединение. Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли,порошки и гранулы. В таких твердых лекарственных формах активное соединение смешивают с по меньшей мере одним инертным, фармацевтически приемлемым вспомогательным веществом или носителем, таким как цитрат натрия или фосфат дикальция и/или а) наполнителями или модифицирующими агентами, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, b) вяжущими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и акация, с) смачивающими веществами, такими как глицерин, d) разрыхляющими агентами, такими как агар-агар, карбонат кальция, картофельный или тапиока крахмал, альгиновая кислота,определенные силикаты и карбонат натрия, е) агентами, замедляющими растворение, такими как парафин, f) ускорителями абсорбции, такими как соединения четвертичного аммония, g) увлажняющими агентами, такими как, например, ацетиловый спирт и моностеарат глицерина, h) поглотителями, такими как каолин и бентонитовая глина, и i) смазывающими веществами, такими как тальк, стеарат кальция,стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль лекарственная форма может также включать буферные агенты. Твердые композиции подобного типа также могут использоваться в качестве заполнения мягких и твердых наполненных желатиновых капсул с использованием таких вспомогательных веществ, как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и подобных. Твердые лекарственные формы таблетки, драже, капсулы, пилюли и гранулы могут быть получены с оболочками и кожурой, такими как оболочка, растворяющаяся в кишечнике, и другие оболочки, хорошо известные в области приготовления фармацевтических препаратов. Они могут необязательно содержать рентгеноконтрастные агенты и также могут быть композицией, которая высвобождает активный ингредиент(ы) только, или предпочтительно, в определенной части кишечного тракта, необязательно,пролонгировано. Примеры встроенных композиций, которые могут использоваться, включают полимерные вещества и воски. Твердые композиции подобного типа также могут применяться в качестве наполнителей мягких и твердых наполненных желатиновых капсул с использованием таких вспомогательных веществ, как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и подобных. Активные соединения также могут быть в микроинкапсулированной форме с одним или более вспомогательными веществами, как отмечено выше. Твердые лекарственные формы таблетки, драже,капсулы, пилюли и гранулы могут быть получены с оболочками и кожурой, такими как кишечнорастворимые оболочки, оболочки, контролирующие высвобождение, и другие оболочки, хорошо известные в области приготовления фармацевтических препаратов. В таких твердых лекарственных формах активное соединение может быть смешано по меньшей мере с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы также могут включать, как в обычной практике, дополнительные вещества, иные, чем инертные разбавители, например, таблетирующие смазывающие вещества и другие таблетирующие добавки, такие как стеарат магния и микрокристаллическая- 20011808 целлюлоза, в случае капсул, таблеток и пилюль лекарственные формы также могут включать буферные агенты. Они могут необязательно содержать рентгеноконтрастные агенты и также могут быть композицией, которая высвобождает активный ингредиент(ы) только, или предпочтительно, в определенной части кишечного тракта, необязательно, с задержкой. Примеры герметизирующих композиций, которые могут быть использованы, включают полимерные вещества и воски. Лекарственные формы для местного или трансдермального введения соединения по настоящему изобретению включают мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, ингаляции или пластыри. Активный компонент смешан в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферами, что может потребоваться. Глазные композиции, ушные капли и подобные также рассматриваются как находящиеся в рамках настоящего изобретения. Мази, пасты, кремы и гели могут содержать, в добавление к активному соединению по настоящему изобретению, вспомогательные вещества, такие как животные и растительные жиры, масла, воски, парафины, крахмал, трагакант, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, кремниевая кислота, тальк и оксид цинка или их смеси. Композиции по изобретению могут также быть приготовлены для доставки в виде жидкого аэрозоля или ингаляционного сухого порошка. Композиции жидкого аэрозоля могут быть распылены преимущественно до размера частиц, которые могут быть доставлены в концевые и дыхательные бронхиолы,где находятся бактерии у пациентов с бронхиальными инфекциями, такими как хронический бронхит и пневмония. Патогенные бактерии обычно присутствуют на всем протяжении дыхательных путей до бронхов, бронхиол и паренхимы легких, особенно в концевых и дыхательных бронхиолах. При обострении инфекции бактерии также могут присутствовать в альвеолах. Композиции жидких аэрозолей и ингаляционных сухих порошков являются предпочтительно доставляемыми на всем протяжении эндобронхиального древа до концевых бронхиол и, в конечном счете, в ткань паренхимы. Аэрозольные композиции по изобретению могут доставляться с использованием устройства, создающего аэрозоль, такого как форсунка, вибрирующая полупроницаемая мембрана или ультразвуковой распылитель, предпочтительно выбираемого, чтобы образовывались частицы аэрозоля, имеющие средний массовый диаметр преимущественно от 1 до 5 мкм. Кроме того, композиция предпочтительно имеет сбалансированную ионную силу осмолярности и концентрацию хлоридов и наименьший аэрозольный объем, способный доставить эффективную дозу соединений по изобретению в участок инфекции. Кроме того, аэрозольная композиция предпочтительно не ухудшает отрицательно функционирование дыхательных путей и не вызывает нежелательных побочных эффектов. Аэрозольные устройства, подходящие для введения аэрозольных композиций по изобретению,включают, например, форсунку, вибрирующую полупроницаемую мембрану, ультразвуковые распылители и подключенные к источнику питания ингаляторы сухих порошков, которые способны распылять композицию по изобретению в аэрозольные частицы размером преимущественно в диапазоне размеров 1-5 мкм. Преимущественно в настоящей заявке значения по меньшей мере 70%, но предпочтительно более чем 90% всех образующихся аэрозольных частиц находятся в диапазоне от 1 до 5 мкм. Воздушный распылитель работает посредством давления воздуха для разрушения жидкого раствора до аэрозольных капель. Распылители с вибрирующей полупроницаемой мембраной работают посредством использования быстро вибрирующей полупроницаемой мембраны для продавливания капель растворителя через полупроницаемую мембрану. Ультразвуковой распылитель работает посредством пьезоэлектрического кристалла, который разделяет жидкость на маленькие аэрозольные капли. Множество подходящих устройств являются доступными, включая, например, AeroNeb и AeroDose распылители с вибрирующей полупроницаемой мембраной (AeroGen, Inc., Sunnyvale, California), Sidestream7 распылители (Medic-AidLtd., West Sussex, England), Pari LC7 и Pan LC Star7 воздушные распылители (Pari Respiratory Equipment,Inc., Richmond, Virginia) и Aerosonic (DeVilbiss Medizinische Produkte (Deutschland) GmbH, Heiden, Germany) и UltraAire7 (Omron Healthcare, Inc., Vernon Hills, Illinois) ультразвуковые распылители. Соединения по изобретению также могут быть приготовлены для использования в качестве порошков для местного использования и спреев, которые могут содержать, в добавление к соединениям по настоящему изобретению вспомогательные вещества, такие как лактоза, тальк, кремниевая кислота, гидроксид алюминия, силикаты кальция и порошок полиамида или смеси таких веществ. Спреи могут дополнительно содержать обычные пропелленты, такие как хлорфторуглеводороды. Трансдермальные пластыри имеют дополнительное преимущество обеспечения регулируемой доставки соединения в организм. Такие лекарственные формы могут быть получены путем растворения или диспергирования соединения в соответствующей среде. Усилители всасывания также могут быть использованы для увеличения тока соединения через кожу. Скорость может регулироваться обеспечением мембраны, регулирующей скорость, или диспергированием соединения в полимерной матрице или геле. В соответствии со способами лечения по настоящему изобретению, бактериальные инфекции лечат или предотвращают у пациента, такого как человек или низшее млекопитающее, путем введения пациенту терапевтически эффективного количества соединения по изобретению, в таких количествах и в течение такого времени, как необходимо для достижения желаемого результата. Терапевтически эффектив- 21011808 ным количеством соединения по изобретению обозначают достаточное количество соединения для лечения бактериальных инфекций, с приемлемым соотношением польза/риск, применимым к любому медицинскому лечению. Однако надо понимать, что общее суточное потребление соединений и композиций по настоящему изобретению будет решаться наблюдающим врачом в рамках существующего медицинского суждения. Уровень специфической терапевтически эффективной дозы для любого определенного пациента будет зависеть от множества факторов, включая расстройство, подвергаемое лечению, и тяжесть расстройства; активность специфического применяемого соединения; возраст, массу тела, общее состояние здоровья, пол и питание пациента; время введения, путь введения и скорость экскреции специфического применяемого соединения; длительность лечения; лекарственные средства, используемые в комбинации или совпадающие со специфическим применяемым соединением; и подобных факторов,хорошо известных в медицинской области техники. Общая суточная доза соединений по настоящему изобретению, вводимая человеку или другому млекопитающему в однократной или разделенных дозах, может быть в количестве, например, от 0,01 до 50 мг/кг массы тела или обычно от 0,1 до 25 мг/кг массы тела. Композиции отдельных доз могут содержать такие количества или их доли для получения суточной дозы. В общем, схемы лечения в соответствии с настоящим изобретением включают введение пациенту, нуждающемуся в таком лечении, от около 10 мг до около 2000 мг соединения(й) по настоящему изобретению в день однократно или в нескольких дозах. Способы приготовления препаратов хорошо известны в области техники и описаны, например, вRemington: The Science и Practice of Pharmacy, Mack Publishing Company, Easton, Pa., 19th Edition (1995). Фармацевтические композиции для использования в настоящем изобретении могут быть в форме стерильных, апирогенных жидких растворов или суспензий, покрытых оболочкой капсул, суппозиториев,лиофилизированных порошков, трансдермальных пластырей или других форм, известных в области техники. Набор, как используется в настоящей заявке, включает контейнер для содержания фармацевтических композиций и также может включать разделенные контейнеры, такие как разделенный флакон или разделенный пленочный пакет. Контейнер может быть в любом обычном виде или форме, как известно в области техники, который сделан из фармацевтически приемлемого материала, например, бумажная или картонная коробка, стеклянный или пластиковый флакон или баночка, повторно закрывающийся пакет(например, для хранения запасного блока таблеток для замены в другой контейнер) или блистерная упаковка с отдельными дозами для выдавливания из упаковки в соответствии со схемой лечения. Применяемый контейнер может зависеть от точной используемой лекарственной формы, например, обычная картонная коробка, как правило, не используется для хранения жидкой суспензии. Является осуществимым, чтобы более чем один контейнер мог использоваться вместе с отдельной упаковкой для продажи стандартной лекарственной формы. Например, таблетки могут содержаться во флаконе, который в свою очередь содержится в коробке. Примером такого набора является так называемая блистерная упаковка. Блистерные упаковки хорошо известны в упаковочной промышленности и широко используются для упаковки фармацевтических стандартных лекарственных форм (таблетки, капсулы и подобные). Блистерные упаковки обычно состоят из листа относительно плотного материала, покрытого пленкой из предпочтительно прозрачного пластикового материала. Во время процесса упаковки в пластиковой пленке формируют углубления. Углубления имеют размер и форму отдельных таблеток или капсул, которые будут упакованы, или могут иметь размер или форму для накопления множества таблеток и/или капсул, которые будут упакованы. Затем таблетки или капсулы помещают в углубления соответственно, и лист относительно плотного материала закрепляют на пластиковой пленке, на стороне пленки, которая противоположна направлению, в котором формируют углубления. В результате, таблетки или капсулы являются отдельно закрытыми или совместно закрытыми, по желанию, в углублениях между пластиковой пленкой и листом. Предпочтительно, прочность листа является таковой, что таблетки или капсулы могут быть удалены из блистерной упаковки применяемым ручным давлением на углубления, таким образом образуются отверстия в листе в месте углубления. Таблетка или капсула может затем быть удалена через указанное отверстие. Может быть желательным обеспечить памяткой, содержащей информацию и/или инструкции для врача, фармацевта или другого представителя здравоохранения или субъекта, например, в форме чисел рядом с таблетками или капсулами, таким образом, что числа соответствуют дням схемы лечения, в которые таблетки или капсулы, помеченные таким образом, должны быть приняты, или карты, которая содержит такой же тип информации. Другим примером такой памятки является календарь, напечатанный на карточке, например, как следующее Первая неделя, Понедельник, Вторник и др Вторая неделя,Понедельник, Вторник и др. Другие варианты памяток будут без труда выражены. Суточной дозой может быть одна таблетка или капсула или несколько таблеток или капсул для приема в заданный день. Когда набор содержит отдельные композиции, суточная доза одной или более композиций набора может состоять из одной таблетки или капсулы, тогда как суточная доза другой одной или более композиций набора может состоять из нескольких таблеток или капсул. Другим специфическим вариантом воплощения набора является дозирующее устройство, разрабо- 22011808 танное для дозирования суточных доз по одной в момент времени, в порядке их предписанного применения. Предпочтительно дозирующее устройство снабжено памяткой, так чтобы облегчить согласие со схемой лечения. Примером такой памятки является механический счетчик, который показывает количество суточных доз, которое было дозировано. Другим примером такой памятки является микрочип памяти на батарейках, в сочетании с жидкокристаллическим индикатором или звуковым сигналом напоминания, который, например, читает дату, когда была принята последняя суточная доза, и/или напоминает,когда следующая доза должна быть принята. Наборы по настоящему изобретению также могут включать, в добавление к ингибиторам LpxC, одно или более дополнительных фармацевтически активных соединений. Предпочтительно, дополнительным соединением является другой ингибитор LpxC или другое соединение, применимое при бактериальных инфекциях. Дополнительные соединения могут вводиться в такой же лекарственной форме, как ингибитор LpxC или в различных лекарственных формах. Подобным образом дополнительные соединения могут вводиться в то же время, что и ингибитор LpxC, или в различное время. Композиции настоящих соединений также могут быть использованы в комбинации с другими известными антибактериальными агентами сходного спектра действия для (1) синергического усиления лечения тяжелых грамотрицательных инфекций, охватываемых спектром настоящего соединения, или(2) добавления покрытия при тяжелых инфекциях, при которых во многих микроорганизмах предполагают, что другой агент отличного спектра может потребоваться в добавление к настоящему соединению. Потенциальные агенты включают представители аминогликозидов, пенициллинов, цефалоспоринов,фторхинолонов, макролидов, гликопептидов, липопептидов и оксазолидинонов. Лечение может включать введение композиции, включающей оба активных агента, или введение соединений по изобретению с последующим или предшествующим введением дополнительного активного антибактериального агента. Способы идентификации и очистки Ссылаясь на примеры, которые следуют ниже, соединения по настоящему изобретению идентифицируют высокоэффективной жидкостной хроматографией (ВЭЖХ) с использованием хроматографической системы Waters Millenium с модулем разделения 2690 (Milford, Massachusetts). Аналитическими колонками были Alltima C-18 обращенной фазы, 4,6250 мм от Alltech (Deerfield, Illinois). Использовали градиентное элюирование, обычно начиная с 5% ацетонитрила/95% воды и увеличивая до 100% ацетонитрила в течение 40 мин. Все растворители содержали 0,1% трифторуксусную кислоту (ТФУ). Соединения определяли по поглощению ультрафиолетового излучения (УФ) при 220 или 254 нм. Растворители ВЭЖХ были от Burdick и Jackson (Muskegan, Michigan), или Fisher Scientific (Pittsburg, Pennsylvania). В некоторых случаях чистоту оценивали тонкослойной хроматографией (ТЖХ) с использованием силиконовых планшетов на стеклянном или пластиковом основании, таких как, например, гибкие листы BakerFlex Silica Gel 1B2-F. Результаты ТЖХ легко определяли визуально в ультрафиолетовом свете или с использованием хорошо известных методик окрашивания парами йода и различных других. Масс-спектрометрический анализ проводили на одном или двух приборах ЖХМС: система Waters(Alliance HT ВЭЖХ и масс-спектрометр Micromass ZQ; колонка: Eclipse XDB-C18, 2,150 мм; система растворителей: 5-95% (или 35-95%, или 65-95%, или 95-95%) ацетонитрил в воде с 0,05% ТФУ; скорость потока 0,8 мл/мин; диапазон молекулярной массы 500-1500; напряжение конуса 20 В; температура колонки 40C) или система Hewlett Packard (Series 1100 ВЭЖХ; колонка: Eclipse XDB-C18, 2,150 мм; система растворителей: 1-95% ацетонитрил в воде с 0,05% ТФУ; скорость потока 0,4 мл/мин; диапазон молекулярной массы 150-850; напряжение конуса 50 В; температура колонки 30C). Все массы представлены как массы протонированных исходных ионов. ГХМС анализ проводили на приборе Hewlet Packard (газовый хроматограф НР 6890 Series с Mass Selective Detector 5973; объем впрыскивателя: 1 мкл; исходная температура: 50C; окончательная температура колонки: 250 С; время линейного нарастания: 20 мин; скорость тока газа: 1 мл/мин; колонка: 5% фенилметилсилоксан, модель НР 190915-443, размеры: 30,0 м 25 м 0,25 м). Анализ ядерного магнитного резонанса (ЯМР) проводили с помощью Varian 300 МГц ЯМР (PaloAlto, California). Спектральная опорная точка была или TMS, или известный химический сдвиг растворителя. Некоторые образцы соединений запускали при повышенной температуре (например, 75C) для получения повышенной растворимости образца. Чистоту некоторых соединений по изобретению оценивали элементным анализом (Desert Analytics,Tuscon, Arizona). Температуру плавления определяли на приборе Laboratory Devices Mel-Temp (Holliston, Massachusetts). Препаративное разделение проводили с использованием хроматографической системы Flash 40 иKP-Sil, 60A (Biotage, Charlottesville, Virginia) , или флэш-колоночной хроматографии с использованием в качестве наполнителя силикагеля (230-400 ячеек), или ВЭЖХ с использованием колонки с обращенной фазой C-18. Типичными растворителями, используемыми для системы Flash 40 Biotage и флэшколоночной хроматографии, были дихлорметан, метанол, этилацетат, гексан, ацетон, водный гидроксиа- 23011808 мин и триэтиламин. Типичными растворителями, применяемыми для ВЭЖХ с обращенной фазой, были различные концентрации ацетонитрила и воды с 0,1% трифторуксусной кислотой. Соединения по настоящему изобретению могут быть легко синтезированы с использованием способов, описанных в данном описании или других способов, которые хорошо известны в области техники. Например, синтез гидроксамовых кислот или подобных материалов, имеющих множество заместителей,широко описан в Kline Т., Andersen N.H., Harwood E.A., Bowman J., Malanda A., Endsley S., Erwin A.L.,Doyle M., Fong S., Harris A.L., Mendelsohn В., Mdluli K., Raetz C.R., Stover C.K. , Witte P.R., YabannavarLett., 2000, 2, 3289-3292; Fernandez, X., Fellous, R., Dunach, E., Novel Synthesis of 2-Thioazolines, Tetrahedron Lett., 2000, 41, 3381-3384. Wipf, P., Miller, C.P., Venkatraman, S., Fritch, P., C. Thiolysis of Oxazolinenes: A New, Selective Method for the Direct Conversion of Peptide Oxazolines into Thiazolines, Tetrahedron Lett., 1995, 36, 6395-6398, которые включены в данное описание в виде ссылки. Синтез других негидроксаматных соединений или обычно цинксвязывающих групп описан в Pirrung, M.С, Tumey, L.N., Raetz, C.R.H., Jackman, J.E., Snehalatha, K., McClerren, A.L., Fierke, C.A. , Gantt,S.L., Rusche, K.M., Inhibition of the Antibacterial Target UDP-(3-O-acyl)-N-acetylglucosamine DeacetylaseDesign (1996), 2 (6), 624-661; Skotnicki, J.S., DiGrandi, M.J., Levin, J.I., Chemical and Screening Sciences,Wyeth Research, New York, NY, USA. Current Opinion in Drug DiscoveryDevelopment (2003), 6 (5), 742759. Вышеизложенное может быть лучше понятно со ссылками на следующие примеры, которые представлены для иллюстрации и не ограничивают рамки идеи изобретения. Примеры Далее представлены сокращения, используемые в примерах:PPh3: трифенилфосфин; ОФ-ВЭЖХ: высокоэффективная жидкостная хроматография с обращенной фазой;Trt-Br: трет-бутилбромид. Номенклатура для соединений примеров обеспечивается с использованием программного обеспечения ACD Name версии 5.07 software (ноябрь 14, 2001), доступной от Advanced Chemistry Development,Inc. Некоторые из соединений и исходных веществ названы с использованием стандартной номенклатуры IUPAC. Синтез аналогов N-ароилтреонина и образование гидроксамата. Пример 1. Синтез 3-бром-4-фтор-N-(1S,2R)-2-гидрокси-1-[(гидроксиамино)карбонил]пропилбензамида (3). Получение метилового эфира (2S,3R)-2-(3-бром-4-фторбензоиламино)-3-гидроксимасляной кислоты (2). Диизопропилэтиламин (6,8 мл, 39,0 ммоль) добавляли к перемешиваемому раствору 3-бром-4 фторбензойной кислоты 1 (2,152 г, 9,83 ммоль), гидрохлорида метилового эфира L-треонина (1,968 г,11,6 ммоль), EDCI (2,218 г, 11,6 ммоль) и HOBt (1,410 г, 10,4 ммоль) в безводном ДМФ (60 мл) при 0C в атмосфере N2. Раствор перемешивали при 0C в течение 1 ч и при комнатной температуре в течение 20 ч. Раствор разбавляли EtOAc (300 мл) и промывали 1,0 M HCl (280 мл), насыщенным NaHCO3 (280 мл),H2O (480 мл), сушили над MgSO4, фильтровали и концентрировали в вакууме для получения бесцветного сиропа, который отвердевал при отстаивании с выходом 3,280 г (100%) метилового эфира (2S,3R)-2(3-бром-4-фторбензоиламино)-3-гидроксимасляной кислоты 2 в виде твердого вещества белого цвета,т.п.73-74C. MC(ES+) m/z 333,9 (C12H13BrFNO4+H требуется 334,00). Получение 3-бром-4-фтор-N-(1S,2R)-2-гидрокси-1-[(гидроксиамино)карбонил]пропилбензамида К раствору гидрохлорида гидроксиламина (66 мг, 0,95 ммоль) в безводном MeOH (2,0 мл) при 0C в атмосфере N2 добавляли метоксид натрия (25 мас.% в MeOH, 360 мг, 1,67 ммоль). Осадок образовался немедленно, и мутный белый раствор перемешивали в течение 10 мин при 0C. Добавляли раствор метил(2,0 мл) и реакционную смесь перемешивали 2 ч при 0C и затем нагревали постепенно до комнатной температуры в течение ночи (всего 17 ч). Добавляли водную 1,0 M HCl (10 мл) и раствор экстрагировали 4:1 хлорформом/изопропиловым спиртом (420 мл). Органические слои собирали, сушили над Na2SO4 и концентрировали для получения розовой пены. Сырое твердое вещество растирали с диэтиловым эфиром(28 мл) и сушили в вакууме для получения 3-бром-4-фтор-N-(1S,2R)-2-гидрокси-1-[(гидроксиамино) карбонил]пропилбензамида 3 в виде белой пены: т.п.152-153 С. Rf (10:1 CH2Cl2/МеОН на силикагеле)=0,53. Получение гидроксаматов. Пример 2. Синтез 4-бензоил-N-(1S,2R)-2-гидрокси-1-[(гидроксиамино)карбонил]пропилбензамида. Методика. К раствору гидрохлорида гидроксиламина (121 мг, 1,74 ммоль) в безводном MeOH (2,0 мл) при 0C в атмосфере N2 добавляли метоксид натрия (25 мас.% в MeOH, 680 мг, 3,14 ммоль). Немедленно наблюдали осадок и мутный белый раствор перемешивали в течение 10 мин при 0C. Добавляли раствор метилMeOH (3,0 мл) и реакционную смесь перемешивали 3 ч при 0C, затем нагревали постепенно до температуры окружающей среды в течение ночи (всего 18 ч). Добавляли водную 0,5 M HCl (20 мл) и раствор экстрагировали 5:1 хлорформом/изопропиловым спиртом (440 мл). Органические слои объединяли,сушили над Na2SO4 и концентрировали для получения оранжевой пены. Очистка хроматографией на силикагеле (с увеличением полярности элюента от 30:1 CH2Cl2/МеОН до 15:1 CH2Cl2/МеОН) давала 228 мг(710 мкл, 4,07 ммоль) при перемешивании. Охлаждающую баню удаляли через 1 ч и реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч и затем разбавляли EtOAc (200 мл). Органический слой промывали 1,0 M HCl (260 мл), насыщенный NaHCO3 (260 мл) и H2O (560 мл),сушили над MgSO4 и концентрировали для получения 493 мг (92%) бесцветного масла 2R,3R)-3 гидрокси-1-[4-(трифторметокси)фенил]карбонилпирролидин-2-ил)-N-(фенилметокси)карбоксамида(2), которое медленно выкристаллизовывалось при отстаивании. Rf (25:1 CH2Cl2/МеОН)=0,35. Получение (2R,3R)-3-гидрокси-1-[4-(трифторметокси)фенил]карбонилпирролидин-2-карбогидроксамовой кислоты (2). Методика. К раствору 2R,3R)-3-гидрокси-1-[4-(трифторметокси)фенил]карбонилпирролидин-2-ил)-N(фенилметокси)карбоксамида (1) (143 мг, 0,337 ммоль) в EtOH (10 мл) добавляли 20% Pd(OH)2/C (50 мг). Раствор очищали газообразным водородом (приблизительно 0,5 л из 1 л баллона) и затем перемешивали в атмосфере H2 (баллонное давление). Анализ ТЖХ не показал исходного вещества через один час. Раствор разбавляли EtOAc (10 мл) и фильтровали через целит, промывали 20:1 EtOAc/EtOH (50 мл). Раствор концентрировали и сушили в вакууме для получения 90 мг (80%) (2R,3R)-3-гидрокси-1-[4-(трифторметокси)фенил]карбонилпирролидин-2-карбогидроксамовой кислоты (2) в виде липкой белой пены: т.п.64-65 С. Rf (10:1 CH2Cl2/МеОН)=0,29. Синтез аналогов N-бензилтреонина восстановительным аминированием. Пример 4. Синтез (2S,3R)-3-гидрокси-2-[(4-фенилфенил)метил]аминобутангидроксамовой кислоты (3). Триэтиламин (1,70 мл, 12,1 ммоль) добавляли к перемешиваемой суспензии гидрохлорида метилового эфира L-треонина (1,030 г, 6,07 ммоль) и 4-бифенилкарбоксальдегида (1,104 г, 6,06 ммоль) в ТГФ(25 мл) . Через 20 мин добавляли NaBH(OAc)3 и суспензию перемешивали в течение 20 ч. Реакцию отслеживали ТЖХ (50:1 DCM/MeOH, Rf=0,4). Реакционную смесь гасили насыщенным NaHCO3 (50 мл),экстрагировали EtOAc (2120 мл), сушили над MgSO4, фильтровали и концентрировали с получением желтого масла. Очистка хроматографией на силикагеле (150:1 DCM/MeOH) давала 1,220 г (выход 67%,чистота 98%) метилового эфира (2S,3R)-2-[(бифенил-4-илметил)амино]-3-гидроксимасляной кислоты 2 в виде бледно-желтого масла. ВЭЖХ (260 нм, 34 мин ток) 14,2 мин; MCHP(ES+) m/z 299,9 (C18H21NO3 + H требует 300,10). Соединение 3 затем образовывалось добавлением NH2OH в MeOH/NaOMe при 0C, с нагреванием до температуры окружающей среды в течение нескольких часов. ЖХМС MH+ 301,15. Общие способы получения фенилбензойных кислот и фенилбензоатных эфиров (см. пример 5 ниже). Стандартная методика. 1 экв. арилгалогена (1) добавляли к 1,2 экв. (2) и Pd(dppf)Cl2 в ТГФ, затем добавляли воду и перемешивали 8 ч при комнатной температуре. После завершения реакции (обычно после ночи) реакционные смеси разбавляли этилацетатом (5-10 мл) и водой (1 мл). Органический слой отделяли и промывали NaHCO3 (23 мл), водой (13 мл), солевым раствором (13 мл), сушили над Na2SO4, фильтровали и концентрировали в 8 мл стеклянном сосуде. Остаток растворяли в ДМСО и вводили на приготовительную колонку ВЭЖХ с обратной фазой для получения 80% выхода. Методики Suzuki с использованием катализатора Pd(dppf)Cl2-DCM и растворителя ДМФ. Стандартная методика. Галоидированный арен 1 и бороновую кислоту 2 отвешивали и помещали в реакционную колбу. ДМФ барботировали аргоном в течение 5-10 мин, затем добавляли ТЭА и реакционную смесь слегка барботировали аргоном. Твердый катализатор Pd(dppf)Cl2 добавляли одной порцией. Флакон заполняли аргоном, плотно запечатывали и перемешивали или встряхивали при 80 С. После достижения завершения (в течение ночи), реакционную смесь фильтровали и вводили на подготовительную колонку ВЭЖХ с- 28011808 обратной фазой (выход 80%). Синтез аналогов метил DAP. Пример 5. 3-(R)-Амино-2-(S) -[(4'-этилбифенил-4-карбонил)амино]бутилгидроксамовая кислота (8). Получение метилового эфира N-трифенилметилаллотреонина (2). Для подобных методик см.: Righi, P.; Scardovi, N.; Marotta, E.; ten Holte, P.; Zwanenburg, B. OrganicLetters 2002, 4(4), 497-500. Раствор трифенилбромметана (3,2 г, 10,0 ммоль) в CHCl3 (40 мл) добавляли по каплям к перемешиваемому раствору HCl соли метилового эфира аллотреонина (1) (2,0 г, 12,0 ммоль) и DIEA (5,2 мл, 30,0 ммоль) в CHCl3 (60 мл) при комнатной температуре в атмосфере N2. За реакцией можно было наблюдать ТЖХ, элюируя EtOAc/гексан (40:60) (Rf=0,3). После перемешивания в течение 12 ч реакционную смесь концентрировали до коричневого масла. Сырой продукт разбавляли EtOAc (170 мл) и промывали 0,2 N лимонной кислотой (250 мл), водой (250 мл), солевым раствором (50 мл) , сушили (Na2SO4), фильтровали и концентрировали при пониженном давлении с получением 3,73 г (выход 85%, чистота 95%) твердого желтого вещества. ВЭЖХ (220 нм, 41 мин ток) 30,90 мин; ВЭЖХ (220 нм, 17 мин ток) 14,86 мин; ЖХМС: ЖХ (214 нм) 3,06 мин, MC(ES+) m/z 376,2 (C24H25NO3 + H требует 376,18). Получение метилового эфира 3-(R)-азидо-2-(S)-(тритиламино)масляной кислоты (3). Для подобных методик см.: Matsuda, A.; Yasuoka, I; Sasaki, Т.; Ueda, T. J. Med. Chem. 1991, 34, 999- 29011808 1002. Раствор чистого DEAD (2,9 мл, 17,8 ммоль) в ТГФ (5 мл) медленно добавляли по каплям к перемешиваемому раствору метилового эфира трет-аллотреонина (2) (4,1 г, 10,9 ммоль) и PPh3 (2,9 г, 10,9 ммоль) в ТГФ (40 мл) при 0C в атмосфере N2. Через 3 мин добавляли раствор DPPA (6,4 мл, 29,7 ммоль) в ТГФ (5 мл) к оранжево-желтому реакционному раствору при 0C. Через 1 ч реакционной смеси позволяли нагреться до комнатной температуры. Через 40 ч реакция достигала завершения по ТЖХ(гексан/DCM/EtOAc (64:20:16) (Rf=0,6 и ЖХМС. Желтый раствор концентрировали для получения 18 г сырого вещества, которое очищали колоночной хроматографией, элюируя гексан/EtOAc (88:12) получая 3,5 г 70% чистоты продукта после выпаривания. Продукт снова очищали (для удаления тритилового спирта и кротилового побочного продукта, образующегося во время реакции элиминации) колоночной хроматографией, элюируя гексан/DCM/EtOAc (76:20:4), получая 1,65 г (выход 38%) бледно-желтого масла после концентрирования и сушки в вакууме. Обратить внимание, что тритиловая защитная группа должна гидролизоваться при воздействии ТФУ во время перегонки образца на ВЭЖХ. Альтернативно, реакцию можно проводить в сухом DCM. Реакционную смесь с использованием 5,44 г (14,5 ммоль) метилового эфира trt-алло-треонина (2) в DCM (100 мл) с PPh3 (3,8 г, 14,5 ммоль),чистого DEAD (3,4 мл, 21,8 ммоль) в DCM (5 мл) и DPPA (6,3 мл, 24,0 ммоль) в DCM (10 мл) смешивали, следуя методике, описанной выше. Через 3 дня реакция не прогрессировала далее по ТЖХ и ЖХМС. После такой же обработки получали 2,97 г продукта с выходом 51%. ВЭЖХ (220 нм, 41 мин ток) 40,5 мин; ВЭЖХ (220 нм, 17 мин ток) 16,32 мин; ЖХМС: ЖХ (214 нм) 3,7 мин, MC(ES+) m/z 401,2(C24H25N3O2 + H требует 401,15). Получение HCl соли метилового эфира 2-(S)-амино-3-(R)-азидомасляной кислоты (4). Раствор Trt-азидо-Thr-ОМе (3) (4,8 г, 12,0 ммоль) растворяли в 95% растворе ТФУ/DCM (60 мл) при комнатной температуре при перемешивании. Через 2,5 ч реакция завершалась по ЖХМС. Яркий желтый раствор разбавляли 0,5 N водным HCl (300 мл). Водный слой экстрагировали DCM (2x30 мл) и затем лиофилизировали досуха. Белое твердое вещество растворяли в AcCN/воде (50:50) (100 мл) и опять лиофилизировали досуха для получения густого порошка и удаляли ТФУ, насколько возможно. Продукт азидо-Thr (4), 2,26 г (выход 97%, чистота 95%) твердого вещества белого цвета получали в виде солиHCl. ВЭЖХ (220 нм, 41 мин ток) 7,91 мин; ВЭЖХ (220 нм, 17 мин ток) 3,36 мин; ЖХМС: ЖХ (214 нм) 0,48 мин, MC(ES+) m/z 159,3 (C5H10N4O2 + H требует 159,08). Получение метилового эфира 3-(R)-азидо-2-(S)-[(4'-этилбифенил-4-карбонил)амино]масляной кислоты (6).EDCHCl (249 мг, 1,3 ммоль) добавляли к перемешиваемому бесцветному раствору азидо-ThrOMeHCl (4) (195 мг, 1,0 ммоль), HOBT (158 мг, 1,0 ммоль), 4'-этилбифенил-4-карбоновой кислоты (5)(226 мг, 1,0 ммоль) и DIEA (0,44 мл, 2,5 ммоль) в DCM (10 мл) при комнатной температуре в атмосфере
МПК / Метки
МПК: C07C 233/00, A61P 31/04, A61K 31/16, A61K 31/165
Метки: антибактериальные, агенты
Код ссылки
<a href="https://eas.patents.su/30-11808-antibakterialnye-agenty.html" rel="bookmark" title="База патентов Евразийского Союза">Антибактериальные агенты</a>
Предыдущий патент: Азолидинонвинильные производные конденсированного бензола
Следующий патент: Пиримидиновые соединения, их применение в качестве а 2b-селективных антагонистов и способ их получения
Случайный патент: Вращающееся устройство для создания давления












