Тетраазабензо[е]азуленовые производные и их аналоги
Номер патента: 10888
Опубликовано: 30.12.2008
Авторы: Эллиотт Ричард Луис, Хаммонд Марлис, Камерон Кимберли О'киф
Формула / Реферат
1. Соединение формулы (I)
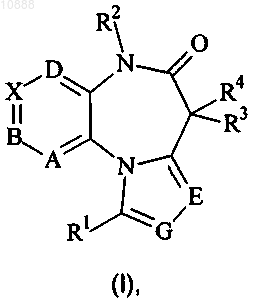
где каждый из А, В, X и D представляет собой -C(R5)-; и каждый из Е и G представляет собой -N-,
R1 выбран из группы, состоящей из (С2-С6)алкила, группировок галогензамещенный (С1-C6)алкил-, (C6-C10)арила, группировок (C6-C10)арил(С1-C6)алкил-, гетероарил-А, гетероарил-А(С1-C6)алкил- и полностью насыщенный (C3-С7)циклоалкил(С1-C6)алкил-, и когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (C3-С7)циклоалкила;
где гетероарил-А выбран из группы, состоящей из тиенила, индолила, 2-пиридила, фуранила, хинолинила, изохинолинила, бензотиофенила и бензофуранила,
арил, гетероарил-А или полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из галогено, (C1-C3)алкокси-, группировки галогензамещенный (С1-С3)алкокси-, -OH, (C1-C3)алкила и группировки галогензамещенный (C1-C3)алкил-;
R2 представляет собой -CH2C(O)N(R6)(R7);
один из R3 и R4 представляет собой H, (С1-С6)алкил, (C1-C6)алкокси-, а другой из R3 и R4 представляет собой -C(R8)(R9)(R10); или
R3 и R4 вместе образуют =CHR11;
каждый R5 независимо выбран из группы, состоящей из H, (C1-C6)алкокси-, -OH и галогено;
один из R6 и R7 представляет собой (C3-C6)алкил или полностью насыщенный (C3-С7)циклоалкил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (С1-C3)алкокси-, (С1-C6)алкила и (С1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (C1-С3)алкокси- и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-С6)алкил-, галогензамещенный (С1-C3)алкокси-, (С1-C6)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила, 3- или 4-пиридила, пиримидила, оксазолила и фуранила;
два из R8, R9 и R10 независимо представляют собой H, а оставшийся из R8, R9 и R10 представляет собой фенил или гетероарил-С, где гетероарил-С выбран из группы, состоящей из индол-2-ила, индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; указанный фенил или гетероарил-С возможно замещены по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (С1-C6)алкокси-, F, Cl, -CN, -OH, -CO2H, тетразола и галогензамещенного (C1-C6)алкокси-; и
R11 представляет собой фенил или гетероарил-С, где гетероарил-С выбран из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; указанный фенил или гетероарил-С возможно замещены по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (C1-C6)алкокси-, F, Cl, -CN, -OH, -CO2H, тетразола и галогензамещенного (C1-C6)алкокси-;
его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли.
2. Соединение по п.1 формулы (III)
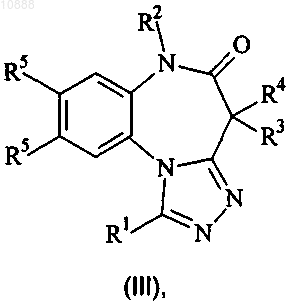
где R1, R2, R3, R4 и R5 являются такими, как определено в п.1;
или его фармацевтически приемлемая соль.
3. Соединение по п.1 или 2, где
один из R3 и R4 представляет собой H, (С1-C3)алкил или (C1-C3)алкокси-, а другой из R3 и R4 представляет собой -C(R8)(R9)(R10) или
R3 и R4 вместе образуют =CHR11;
R1 выбран из группы, состоящей из (С2-С6)алкила, -CF3, фенила, группировок фенил(С1-C3)алкил-, гетероарил-А, гетероарил-А(С1-C3)алкил-, и группировки полностью насыщенный(С3-С7)циклоалкил(С1-C3)алкил-, и, когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (C3-С7)циклоалкила,
где гетероарил-А выбран из группы, состоящей из тиенила и 2-пиридила;
фенил, гетероарил-А, полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из F, Cl, (C1-C3)алкокси-,
-OH, (C1-C3)алкила и -CF3;
или его фармацевтически приемлемая соль.
4. Соединение по любому из пп.1-3, где каждый R5 представляет собой H;
один из R6 и R7 представляет собой (C3-C6)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок F- или Cl-замещенный (C1-C3)алкил-, F- или Cl-замещенный (С1-С3)алкокси-, (C1-C4)алкила и (C1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок F- или Cl-замещенный (C1-C3)алкил-, F-или Cl-замещенный (C1-C3)алкокси-, (С1-С4)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила, 3- или 4-пиридила и пиримидила;
два из R8, R9 и R10 представляют собой H, а оставшийся из R8, R9 и R10 представляет собой гетероарил-С, выбранный из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; причем указанный гетероарил-С возможно замещен по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (C1-C3)алкокси-, F, Cl, -CN, -OH, -CO2H, тетразола и F-замещенного (C1-C3)алкокси-; и
R11 представляет собой гетероарил-С, выбранный из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; причем указанный гетероарил-С возможно замещен по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (C1-C3)алкокси-, F, Cl, -CN, -OH,
-CO2H, тетразола и F-замещенного (C1-C3)алкокси-;
или его фармацевтически приемлемая соль.
5. Соединение по любому из пп.1-4 формуыы (IV)
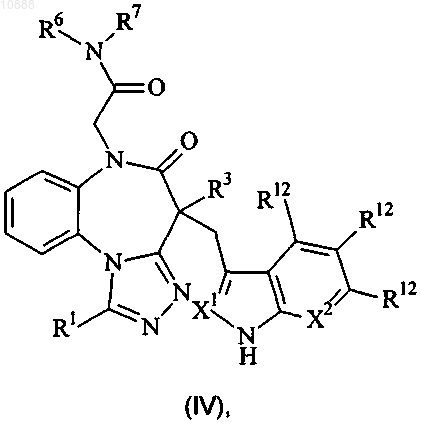
где R3 представляет собой H или (C1-C3)алкил;
X1 представляет собой -CH- и X2 представляет собой -N- или -C(R12)- или X1 представляет собой -N- и X2 представляет собой -C(R12)-; и
каждый R12 независимо выбран из группы, состоящей из H, F и Cl; при условии, однако, что не более трех R12 иные, чем H;
или его фармацевтически приемлемая соль.
6. Соединение по любому из пп.1-5, где
R1 представляет собой фенил или 2-пиридил, или, когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 также может представлять собой полностью насыщенный (С5-C7)циклоалкил, где фенил, 2-пиридил или полностью насыщенный (С5-С7)циклоалкил возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из F, Cl, (C1-C3)алкокси-, -OH, (C1-C3)алкила и -CF3;
R3 представляет собой H;
один из R6 и R7 представляет собой (C3-C6)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок F-замещенный (С1-C3)алкил-, F-замещенный (C1-C3)алкокси-, (C1-C4)алкила и (C1-C3)алкокси-; фенилметил-, возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из -OH и -ОСН3; или 3- или 4-пиридил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок F-замещенный (С1-C3)алкил-, F-замещенный (C1-C3)алкокси-, (C1-C4)алкила и (C1-C3)алкокси-;
или его фармацевтически приемлемая соль.
7. Соединение по любому из пп.1-6, где
R1 представляет собой фенил или циклогексил, когда ни один из R6 и R7 не представляет собой фенилметил-, где фенил возможно замещен 1-3 атомами F или группой -OH;
один из R6 и R7 представляет собой (C3 или С4)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH,F, Cl, -CF3, -OCF3, (С1-С4)алкила и (С1-C3)алкокси-; фенилметил-; или 3- или 4-пиридил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из
-OH, F, Cl, -CF3, -OCF3, (С1-С4)алкила и (С1-C3)алкокси-;
или его фармацевтически приемлемая соль.
8. Соединение формулы (V)
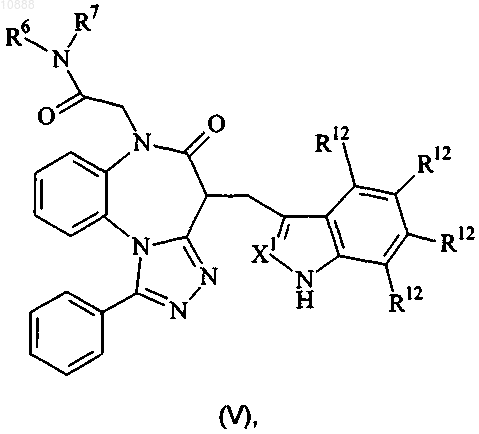
где X1 представляет собой -CH- или -N-; и
один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1 или 2 атомами F; фенилметил-; или 3- или 4-пиридил, возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -OCH3 и -OCH2CH3; и каждый R12 независимо представляет собой H или F; при условии, однако, что не более трех R12 представляют собой F;
или его фармацевтически приемлемая соль.
9. Соединение по п.8, где X1 представляет собой -CH-; один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой фенил или фенилметил-; и каждый R12 представляет собой H; или его фармацевтически приемлемая соль.
10. Соединение по п.8, где X1 представляет собой -CH-; один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой 3-пиридил, возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -OCH3 и -OCH2CH3; и каждый R12 представляет собой H; или его фармацевтически приемлемая соль.
11. Соединение N-бензил-2-[4-(1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропилацетамид или его фармацевтически приемлемая соль.
12. Соединение (-)N-бензил-2-[4-(1Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропилацетамид.
13. Соединение формулы (F-1)
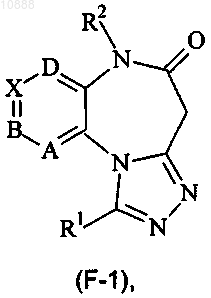
где каждый из А, В, X и D представляет собой -C(R5)-,
R1 выбран из группы, состоящей из (С2-С6)алкила, группировок галогензамещенный (С1-C6)алкил-, (C6-C10)арила, группировок (C6-C10)арил(С1-C6)алкил-, гетероарил-А, гетероарил-А(C1-C6)алкил- и полностью насыщенный (C3-С7)циклоалкил(C1-C6)алкил-, и когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (C3-С7)циклоалкила;
где гетероарил-А выбран из группы, состоящей из тиенила, индолила, 2-пиридила, фуранила, хинолинила, изохинолинила, бензотиофенила и бензофуранила,
арил, гетероарил-А или полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из галогено, (C1-C3)алкокси-, группировки галогензамещенный (C1-C3)алкокси-, -OH, (C1-C3)алкила и группировки галогензамещенный (C1-C3)алкил-;
R2 представляет собой -CH2C(O)N(R6)(R7);
каждый R5 независимо выбран из группы, состоящей из H, (С1-С6)алкокси-, -OH и галогено;
один из R6 и R7 представляет собой (C3-C6)алкил или полностью насыщенный (C3-С7)циклоалкил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (С1-C6)алкил-, галогензамещенный (C1-С3)алкокси-, (С1-C6)алкила и (C1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, группировок галогензамещенный (С1-С6)алкил-, галогензамещенный (C1-C3)алкокси- и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (C1-C3)алкокси-, (C1-C6)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила, 3- или 4-пиридила, пиримидила, оксазолила и фуранила;
или его соль.
Текст
010888 Область изобретения Это изобретение относится к соединениям формулы (I) и промежуточным соединениям, применимым для получения соединений. Соединения формулы (I) представляют собой агонисты рецептора холецистокинина-А (CCK-A) и, следовательно, являются полезными, например, для контроля массы и лечения ожирения и связанных с ним заболеваний. Предшествующий уровень техники Ожирение представляет собой основную тревогу для здравоохранения, ввиду его увеличивающегося распространения и ассоциирующихся с ним рисков для здоровья. Кроме того, ожирение может влиять на качество жизни человека посредством ограниченной подвижности и уменьшенной физической выносливости, а также посредством социальной, научной дискриминации и дискриминации по работе. Ожирение и избыточная масса обычно определяются индексом массы тела (ИМТ), который сопоставляется с общим содержанием жира в организме и служит в качестве оценки риска некоторых заболеваний. ИМТ рассчитывают путем деления массы организма в килограммах на рост в квадратных метрахEvidence Report, Washington, DC: U.S. Department of Health and Human Services, NIH publication no. 984083 (1998). В недавних исследованиях было обнаружено, что ожирение и ассоциирующиеся с ним риски для здоровья не ограничены взрослыми, а часто поражают детей и подростков в удивительной степени. В соответствии с данными Центра по контролю за заболеваниями (Center for Disease Control) процент детей и подростков, определяемых как имеющих избыточную массу организма, увеличился более чем вдвое с начала 1970-х годов, и приблизительно 15% детей и подростков в настоящее время имеют избыточную массу. Факторы риска сердечного заболевания, такие как высокий уровень холестерина и высокое кровяное давление, возникают с большей частотой у детей и подростков с избыточной массой по сравнению с субъектами такого же возраста, имеющими нормальную массу. Кроме того, частота диабета 2 типа, ранее рассматриваемого как заболевание взрослых, резко увеличилась у детей и подростков. Состояния с избыточной массой и ожирением тесно связаны с диабетом 2 типа. Недавно было приблизительно подсчитано, что подростки с избыточной массой имеют 70%-ную вероятность вырасти во взрослых людей с избыточной массой или ожирением. Вероятность увеличивается до 80%, если по меньшей мере один из родителей страдает от избыточной массы или ожирения. Самое прямое следствие избыточной массы,ощущаемое самим ребенком, является социальная дискриминация. Возможные неблагоприятные последствия избыточной массы или ожирения для здоровья заключаются в том, что страдающие от них индивиды имеют увеличенный риск заболеваний (сопутствующих заболеваний), таких как гипертензия, дислипидемия, диабет 2 типа (инсулиннезависимый), инсулинорезистентность, интолерантность к глюкозе, гиперинсулинемия, ишемическая болезнь сердца, стенокардия,застойная сердечная недостаточность, инсульт, желчные конкременты, холецистит, желчно-каменная болезнь, подагра, остеоартрит, обструктивное апноэ во сне и респираторные проблемы, заболевание желчного пузыря, некоторые формы рака (например, эндометрия, молочной железы, предстательной железы и ободочной кишки) и психологические расстройства (такие, как депрессия, расстройства приема пищи, расстройство схемы тела и низкая самооценка). Отрицательные последствия ожирения для здоровья делают его второй ведущей причиной преждевременной смертности в Соединенных Штатах Америки и оказывают значительное экономическое и психологическое воздействие на общество. См. McGinnisM., Foege W.H., "Actual Causes of Death in the United States", JAMA, 270, 2207-12 (1993). В настоящее время ожирение рассматривают как хроническое заболевание, требующее лечения для уменьшения ассоциирующихся с ним рисков для здоровья. Хотя потеря массы представляет собой важный исход лечения, одна из важнейших задач лечения ожирения заключается в улучшении сердечнососудистых и метаболических показателей для уменьшения связанной с ожирением заболеваемости и смертности. Показано, что 5-10%-ная потеря массы тела может значительно улучшить метаболические показатели, такие как уровень глюкозы в крови, кровяное давление и концентрации липидов. Следовательно, полагают, что умышленное уменьшение массы тела на 5-10% может уменьшить заболеваемость и смертность. Доступные в настоящее время лекарства, предписываемые для лечения ожирения, обычно уменьшают массу главным образом вследствие вызывания чувства насыщения или уменьшения абсорбции жира, входящего в рацион питания. Насыщения достигают путем увеличения синаптических уровней норэпинефрина, серотонина или обоих. Например, стимуляция подтипов 1 В, 1D и 2 С серотониновых рецепторов и 1- и 2-адренергических рецепторов уменьшает прием пищи путем регулирования насыщения. См. Bray G.A., "The New Era of Drug Treatment. Pharmacologic Treatment of Obesity: Symposium Overview", Obes Res., 3 (suppl 4), 415s-7s (1995). Адренергические агенты (например, диэтилпропион, бензфетамин, фендиметразин, мазиндол и фентермин) действуют путем модуляции центральных норэпинефриновых и дофаминовых рецепторов благодаря тому, что способствуют высвобождению катехоламина. Более старые адренергические лекарства для уменьшения массы (например, амфетамин, метамфетамин и-1 010888 фенметразин), которые в значительной степени вовлечены в дофаминовые пути, больше не рекомендуются ввиду риска злоупотребления ими. Два серотонергических агента фенфлюрамин и дексфенфлюрамин, которые использовались для регуляции аппетита, больше не доступны для применения. Холецистокинин (CCK) представляет собой кишечно-мозговой пептид, действующий в качестве желудочно-кишечного гормона, нейромедиатора и нейромодулятора в центральной и периферической нервной системах. Холецистокинин представляет собой пептид, который существует во множестве активных форм различной длины (например, CCK-58; CCK-39; CCK-33; CCK-8 и CCK-4) с различными формами, преобладающими у различных видов. Холецистокинин-58 представляет собой основную молекулярную форму в кишечнике человека, собаки и кошки, но не свиньи, крупного рогатого скота или крысы. См., например, G. A. Eberlien, V. E. Eysselein and H. Goebell, 1988, Peptides 9, pp. 993-998. Периферические эффекты CCK, где О-сульфатированный октапептид CCK-8S, как полагают, представляет собой преобладающую форму, сконцентрированы на его роли в качестве желудочно-кишечного фактора насыщения. Показано, что CCK высвобождается из 1-клеток слизистой оболочки двенадцатиперстной кишки и тощей кишки в ответ на прием пищи, в частности в ответ на жир или белок в пище. ВысвободившийсяCCK инициирует множество реакций, согласованных для того, чтобы способствовать перевариванию и регуляции приема пищи, включая опорожнение желчного пузыря, регуляцию высвобождения пищеварительных ферментов из поджелудочной железы, контроль опорожнения желудка путем регуляции пилорического сфинктера, а также нейрональную передачу сигналов в ЦНС (центральная нервная система) через вагусные афферентные нейроны. В ЦНС CCK обнаружен во множестве анатомических локализаций, включая кору головного мозга,гиппокамп, перегородку, миндалевидную железу, обонятельную луковицу, гипоталамус, таламус, парабрахиальное ядро, ядро шва, черное вещество, вентральный мезенцефалон, ядро одиночного пути, вентральный мозг и спинной мозг. См., например, Т. Hokfelt et al., 1988, J. Chem. Neuroanat. 1, pp. 11-52; J.J.Press, Oxford. Полагают, что нейрональный CCK опосредует множество процессов в ЦНС, включая модуляцию дофаминергической нейротрансмиссии и анксиогенные эффекты, а также влияет на познавательную способность и ноцицепцию. См., например, J.N. Crawley and R.L. Corwin, 1994, Peptides, 15:731-755; N.S.Opinion on Investigational Drugs (2000), 9(1), 129-146. Показано, что холецистокинин опосредует различные гормональные и нейромодуляторные функции посредством двух подтипов рецепторов: подтипов CCK-A (CCK1) и CCK-В (CCK2) (См., например,G.N. Woodruff and J. Hughes, Annu. Rev. Pharmacol. Toxicol. (1991), 31: 469-501), оба из которых секвенированы и клонированы из крыс (См., например, S.A. Wank et al. (1992) Proc. Natl. Acad. Sci. USA, 89,8691-8695) и людей (См., например, J.R. Pisegna et al., 1992, Biochem. Biophys. Res. Commun. 189, pp. 296303). Оба подтипа рецепторов CCK-A и CCK-В относятся к суперсемейству из семи трансмембранных рецепторов, связанных с G-белком. Нуклеотидные последовательности периферического рецептораSci. 713, pp. 49-66. Рецептор CCK-A преимущественно локализован на периферии, включающей ацинарные клетки поджелудочной железы, пилорический сфинктер, желчный пузырь и вагусные афференты, где он опосредует панкреатическую экзокринную секрецию, опустошение желудка и сокращение желчного пузыря,и передает сигналы о насыщении после приема пищи в центральную нервную систему (ЦНС). Дополнительно, рецептор CCK-A обнаружен в дискретных областях в ЦНС, включающих ядро одиночного пути,область пострема (area postrema) и дорсально-медиальный гипоталамус. Рецептор CCK-В локализован преимущественно в ЦНС, и менее преимущественно на периферии. Множество исследований свидетельствуют о том, что CCK опосредует эффект насыщения через рецептор CCK-A, который передает сигнал о насыщении после приема пищи через вагусные афференты в центральную нервную систему (ЦНС). См., например, G.P. Smith et al., Science 213 (1981) pp. 10361037; и J.N. Crawley et al., J. Pharmacol. Exp. Ther., 257 (1991) pp. 1076-1080. Например, сообщали о том,что CCK и агонисты CCK могут уменьшать прием корма животными, включающими крыс (См., например, J. Gibbs, R.C. Young and G.P. Smith, 1973, J. Comp. Physiol. Psychol. 84:488-95), собак и приматовHirosue et al., 1993, Am. J. Physiol. 265:R481-R486; и K.Е. Asin et al., 1992, Pharmacol. Biochem. Behav. 42:699-704), и что это аноректическое действие опосредовано через рецептор CCK-A, локализованный на вагусных афферентных волокнах (См., например, С.Т. Dourish, 1992, в Multiple cholecystokinin receptorsDourish, S.J. Cooper, S.D. Iversen and L.L. Iversen, editors, Oxford University Press, New York, NY, pp. 166182; J.N. Crawley and R.L. Corwin, 1994, Peptides, 15:731-755; и G.P. Smith et al., 1981, Science 213, pp. 1036-1037). Другие линии доказательств, поддерживающих вовлечение рецептора CCK-A в регуляцию приема пищи, включают факт, что крысы OLETF (лишенные рецептора CCK-A) нечувствительны к анорексигенному действию CCK. Кроме того, сообщали о том, что селективные антагонисты CCK-A, но не антагонисты CCK-В, блокируют аноректические действия CCK и аналогов CCK и увеличивают прием корма животными (См., например, G. Hewson et al., 1988, Br. J. Pharmacol. 93:79-84; R.D. Reidelberger и M.F.(См., например, О.М. Wolkowitz et al.,1990, Biol. Psychiatry, 28:169-173). Наконец, было сообщено, что инфузия CCK или селективных агонистов CCK-A уменьшает размер потребляемого корма и потребления калорий животными, включающими людей (См., например, L. Degen et al., Peptides (New York, NY) (2001), 22(8), 1265-1269; H.R. Kissileff et al., Am J Clin Nutr 34 (1981),pp. 154-160; A. Ballinger et al., Clin Sci 89 (1995), 375-381; и R.J. Lieverse et al., Gastroenterology 106(1994), 1451-1454). В литературе сообщалось о разработке непептидных агонистов CCK-A. Например, Sanofi в патенте США 5798353 сообщил, что некоторые 3-ациламино-5-(полизамещенный фенил)-1,4-бензодиазепин 2-оны действуют в качестве агонистов CCK-A. Сообщалось, что некоторые 1,5-бензодиазепиноны представляют собой агонисты CCK-A, обладающие аноректической активностью у грызунов (См., например,Е.Е. Sugg et al., (1998) Pharmaceutical Biotechnology 11 (Integration of Pharmaceutical Discovery and Development): 507-524). R.G. Sherrill et al. в BioorganicMedicinal Chemistry Letters (2001), 11(9), 1145-1148 раскрывают некоторые 1,4-бензодиазепины в качестве агонистов периферического рецептора CCK-A,обладающие аноректической активностью в моделях кормления крыс. Серии 3-(1H-индазол-3-илметил)1,5-бензодиазепинов обсуждаются B.R. Henke et al. в J. Med. Chem. (1997), 40(17), 2706-2725 и J. Med.Chem. (1996), 39(14), 2655-2658 в качестве перорально активных агонистов CCK-A. Хотя исследования продолжаются, все еще существует потребность в более эффективном и безопасном терапевтическом лечении для уменьшения или профилактики набора массы. Краткое изложение сущности изобретения Настоящее изобретение относится к соединению формулы (I) где каждый из A, B, X и D представляет собой -C(R5)-; и каждый из Е и G представляет собой -N-,R1 выбран из группы, состоящей из (C2-C6)алкила, группировок галогензамещенный (C1-C6)алкил-,(C6-C10)арила, группировок (C6-C10)арил(С 1-C6)алкил-, гетероарил-А, гетероарил-А(С 1-C6)алкил- и полностью насыщенный (C3-С 7)циклоалкил(С 1-С 6)алкил-, и когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (С 3-С 7)циклоалкила; где гетероарил-А выбран из группы, состоящей из тиенила, индолила, 2-пиридила, фуранила, хинолинила, изохинолинила, бензотиофенила и бензофуранила,арил, гетероарил-А или полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из галогено, (C1C3)алкокси-, группировки галогензамещенный (C1-C3)алкокси-, -OH, (C1-C3)алкила и группировки галогензамещенный (C1-C3)алкил-;R2 представляет собой -CH2C(O)N(R6)(R7); один из R3 и R4 представляет собой H, (C1-C6)алкил, (C1-C6)алкокси-, а другой из R3 и R4 представляет собой -C(R8)(R9)(R10); или R3 и R4 вместе образуют =CHR11; каждый R5 независимо выбран из группы, состоящей из H, (С 1-C6)алкокси-, -OH и галогено; один из R6 и R7 представляет собой (C3-С 6)алкил или полностью насыщенный (C3-С 7)циклоалкил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (С 1-С 3)алкокси-, (C1-C6)алкила и (C1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH,группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (C1-C3)алкокси- и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (С 1-C6)алкил-, галогензамещенный(C1-С 3)алкокси-, (С 1-C6)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила, 3- или 4-пиридила, пиримидила, оксазолила и фуранила; два из R8, R9 и R10 независимо представляют собой H, а оставшийся из R8, R9 и R10 представляет собой фенил или гетероарил-С, где гетероарил-С выбран из группы, состоящей из индол-2-ила, индол-3 ила, индазол-3-ила и 7-азаиндол-3-ила; указанный фенил или гетероарил-С возможно замещены по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (С 1-С 6)алкокси-,F, Cl, -CN, -OH, -CO2H, тетразола и галогензамещенного (C1-C6)алкокси-; иR11 представляет собой фенил или гетероарил-С, где гетероарил-С выбран из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; указанный фенил или гетероарил-С возможно замещены по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (C1C6)алкокси-, F, Cl, -CN, -OH, -CO2H, тетразола и галогензамещенного (C1-C6)алкокси-; его фармацевтически приемлемой соли, или сольвату, или гидрату указанного соединения или указанной соли. Предпочтительное воплощение изобретения относится к соединению формулы (III) где R1, R2, R3, R4 и R5 являются такими, как определено выше для соединения формулы (I); или его фармацевтически приемлемой соли. Предпочтительными являются вышеописанные соединения по изобретению, где один из R3 и R4 представляет собой H, (C1-C3)алкил или (С 1-С 3)алкокси-, а другой из R3 и R4 представляет собой -C(R8)(R9)(R10); илиR1 выбран из группы, состоящей из (С 2-C6)алкила, -CF3, фенила, группировок фенил(С 1-С 3)алкил-,гетероарил-А, гетероарил-А(C1-C3)алкил-, и группировки полностью насыщенный(C3-С 7)циклоалкил(С 1C3)алкил-, и когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (C3-С 7)циклоалкила; где гетероарил-А выбран из группы, состоящей из тиенила и 2-пиридила; фенил, гетероарил-А, полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из F, Cl, (С 1-С 3)алкокси-,-OH, (C1-C3)алкила и -CF3; или их фармацевтически приемлемая соль. Более предпочтительными являются вышеописанные соединения по изобретению, где каждый R5 представляет собой H; один из R6 и R7 представляет собой (С 3-С 6)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы,состоящей из -OH, F, Cl, группировок F- или Cl-замещенный (С 1-С 3)алкил-, F- или Cl-замещенный (С 1C3)алкокси-, (С 1-С 4)алкила и (С 1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок F- или Cl-замещенный (C1-C3)алкил-, F- или Cl-замещенный (C1-C3)алкокси-,(C1-C4)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила,3- или 4-пиридила и пиримидила; два из R8, R9 и R10 представляют собой H, а оставшийся из R8, R9 и R10 представляет собой гетероарил-С, выбранный из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила; причем указанный гетероарил-С возможно замещен по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (С 1-C3)алкокси-, F, Cl, -CN, -OH, -CO2H, тетразола и F-замещенного (С 1C3)алкокси-; иR11 представляет собой гетероарил-С, выбранный из группы, состоящей из индол-3-ила, индазол-3 ила и 7-азаиндол-3-ила; причем указанный гетероарил-С возможно замещен по атому(ам) углерода 1-3 заместителями, независимо выбранными из группы, состоящей из (C1-C3)алкокси-, F, Cl, -CN, -OH,-CO2H, тетразола и F-замещенного (C1-C3)алкокси-; или их фармацевтически приемлемая соль. Также предпочтительным воплощением изобретения является соединение формулы (IV)X1 представляет собой -N-, и X2 представляет собой -C(R12)-; и каждый R12 независимо выбран из группы, состоящей из H, F и Cl; при условии, однако, что не более трех R12 иные, чем H; или его фармацевтически приемлемая соль. Более предпочтительными являются вышеописанные соединения по изобретению, гдеR1 представляет собой фенил или 2-пиридил, или когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 также может представлять собой полностью насыщенный (С 5-С 7)циклоалкил, где фенил, 2-пиридил или полностью насыщенный (С 5-С 7)циклоалкил возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из F, Cl, (C1-C3)алкокси-, -OH, (C1-C3)алкила и -CF3;R3 представляет собой H; один из R6 и R7 представляет собой (C3-С 5)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы,состоящей из -OH, F, Cl, группировок F-замещенный (С 1-C3)алкил-, F-замещенный (C1-C3)алкокси-, (C1 С 4)алкила и (C1-C3)алкокси-; фенилметил-, возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из -OH и -OCH3; или 3- или 4-пиридил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, группировок Fзамещенный (C1-C3)алкил-, F-замещенный (C1-C3)алкокси-, (C1-C4)алкила и (С 1-C3)алкокси-; или их фармацевтически приемлемая соль. Еще более предпочтительными являются вышеописанные соединения по изобретению, гдеR1 представляет собой фенил, или циклогексил, когда ни один из R6 и R7 не представляет собой фенилметил-, где фенил возможно замещен 1-3 атомами F или группой -OH; один из R6 и R7 представляет собой (C3 или С 4)алкил с разветвленной цепью, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, F, Cl, CF3, -OCF3, (С 1-С 4)алкила и (C1-C3)алкокси-; фенилметил-; или 3- или 4 пиридил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из-OH, F, Cl, -CF3, -OCF3, (С 1-С 4)алкила и (C1-C3)алкокси-; или их фармацевтически приемлемая соль. Согласно изобретению предложено также соединение формулы (V) где X1 представляет собой -CH- или -N-; и один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1 или 2 атомами F; фенилметил-; или 3- или 4-пиридил, возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -ОСН 3 и -ОСН 2 СН 3; и каждый R12 независимо представляет собой H или F; при условии, однако, что не более трех R12 представляют собой F; или его фармацевтически приемлемая соль.-5 010888 Предпочтительным воплощением указанного соединения является соединение, гдеX1 представляет собой -CH-; один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой фенил или фенилметил-; и каждый R12 представляет собой H; или его фармацевтически приемлемая соль. Также предпочтительным воплощением указанного соединения является соединение, гдеX1 представляет собой -CH-; один из R6 и R7 представляет собой изопропил, а другой из R6 и R7 представляет собой 3-пиридил,возможно замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl,-ОСН 3 и -ОСН 2 СН 3; и каждый R12 представляет собой H; или его фармацевтически приемлемая соль. Наиболее предпочтительным воплощением соединений по изобретению является N-бензил-2-[4(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропилацетамид; или его фармацевтически приемлемая соль. Еще более предпочтительным воплощением соединений по изобретению является N-бензил-2-[4(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропилацетамид. Кроме того, согласно изобретению предложено промежуточное соединение формулы (F-1) где каждый из А, В, X и D представляет собой -C(R5)-;R1 выбран из группы, состоящей из (С 2-C6)алкила, группировок галогензамещенный (С 1-C6)алкил-,(C6-C10)арила, группировок (C6-C10)арил(C1-C6)алкил-, гетероарил-А, гетероарил-А(C1-C6)алкил- и полностью насыщенный (C3-С 7)циклоалкил(С 1-C6)алкил-, и когда ни один из R6 и R7 не представляет собой фенилметил-, тогда R1 выбран из указанной группы и полностью насыщенного (С 3-С 7)циклоалкила; где гетероарил-А выбран из группы, состоящей из тиенила, индолила, 2-пиридила, фуранила, хинолинила, изохинолинила, бензотиофенила и бензофуранила,арил, гетероарил-А или полностью насыщенная циклоалкильная группа или часть группы возможно замещены 1-3 заместителями, независимо выбранными из группы, состоящей из галогено, (C1C3)алкокси-, группировки галогензамещенный (C1-C3)алкокси-, -OH, (C1-C3)алкила и группировки галогензамещенный (C1-C3)алкил-;R2 представляет собой -CH2C(O)N(R6)(R7); каждый R5 независимо выбран из группы, состоящей из H, (C1-C6)алкокси-, -OH и галогено; один из R6 и R7 представляет собой (С 3-C6)алкил или полностью насыщенный (C3-С 7)циклоалкил, а другой из R6 и R7 представляет собой фенил, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (С 1-C3)алкокси-, (C1-C6)алкила и (C1-C3)алкокси-; фенилметил-, где фенильная группировка возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH,группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (C1-C3)алкокси- и (C1-C3)алкокси-; или гетероарил-В, возможно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из -OH, галогено, группировок галогензамещенный (C1-C6)алкил-, галогензамещенный (C1C3)алкокси-, (C1-C6)алкила и (C1-C3)алкокси-; и где указанный гетероарил-В выбран из группы, состоящей из тиенила, 3- или 4-пиридила, пиримидила, оксазолила и фуранила; или его соль. Когда в соединениях по изобретению R1 представляет собой фенил, то наиболее предпочтительно он не замещен, но если замещен, то наиболее предпочтительно замещен 1-3 атомами F или группой -OH. Каждый R5 в формуле (I) независимо предпочтительно выбран из группы, состоящей из H, -OH и F; еще более предпочтительно из H и F. Наиболее предпочтительно, каждый R5 представляет собой H. Предпочтительно один из R6 и R7 в формуле (I) представляет собой (C3-C6)алкил с разветвленной цепью; более предпочтительно (C3-C5)алкил с разветвленной цепью; еще более предпочтительно (C3 или С 4)алкил с разветвленной цепью; и наиболее предпочтительно изопропил. Другой из R6 и R7 в формуле (I) предпочтительно представляет собой фенил, фенилметил- или гетероарил-В, где фенильная группа, фенильная часть фенилметильной группы или группа гетероарил-В-6 010888 возможно замещена, как указано выше. Предпочтительно, фенильная группа R6 или R7 возможно замещена 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -CF3, -OCF3, -CH3 и (С 1-С 3)алкокси-. Еще более предпочтительно, фенильная группа возможно замещена 1 или 2 атомами F. Когда один из R6 и R7 представляет собой возможно замещенную фенильную группу, тогда она предпочтительно представляет собой незамещенный фенил или 4-F-фенил. Предпочтительно, фенильная группировка фенилметильной группы R6 или R7 возможно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из -OH и (C1-C3)алкокси-. Более предпочтительно, фенильная группировка возможно замещена 1 или 2 заместителями, независимо выбранными из группы, состоящей из -OH и -OCH3. Наиболее предпочтительно, фенильная группировка фенилметильной группы не замещена. Наиболее предпочтительно, группа гетероарил-В в качестве R6 или R7 возможно замещена 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -CF3, -OCF3, -CH3 и(С 1-С 3)алкокси-. Еще более предпочтительно, группа гетероарил-В возможно замещена 1 или 2 заместителями, независимо выбранными из группы, состоящей из F, Cl и (C1-C3)алкокси-. Еще более предпочтительно, гетероарил-В возможно замещен 1 или 2 заместителями, независимо выбранными из группы,состоящей из Cl, -OCH3 и -OCH2CH3. В особенно предпочтительном воплощении гетероарил-В замещен одним заместителем, выбранным из группы, описанной выше, обычно или предпочтительно, в частности, -OCH3. Гетероарил-В в качестве R6 или R7 предпочтительно выбран из группы, состоящей из тиенила, 3 или 4-пиридила и пиримидила. Более предпочтительно, он представляет собой 3- или 4-пиридильную группу, в частности 3-пиридильную группу, которая может быть незамещенной или предпочтительно замещенной, как описано выше. Когда 3-пиридильная группа монозамещена, она предпочтительно замещена по С-6. В особенно предпочтительном воплощении гетероарильная группа представляет собой 6 метоксипирид-3-ил. В предпочтительном воплощении один из R3 и R4 в формуле (I) представляет собой H, (C1-C3)алкил или (С 1-C3)алкокси-; более предпочтительно H или (C1-C3)алкил, например -CH3; наиболее предпочтительно H. Другой из R3 и R4 в формуле (I) представляет собой -C(R8)(R9)(R10). Для -C(R8)(R9)(R10) в соединениях формулы (I) два из R8, R9 и R10 предпочтительно представляет собой H, а оставшийся из R8, R9 и R10 представляет собой группу гетероарил-С, предпочтительно выбранную из группы, состоящей из индол-3-ила, индазол-3-ила и 7-азаиндол-3-ила. Более предпочтительно, гетероарил-С представляет собой индол-3-ильную или индазол-3-ильную группу; наиболее предпочтительно индол-3-ильную группу. Группа гетероарил-С возможно замещена по атому(ам) углерода, который(е) предпочтительно расположен(ы) на фенильном или пиридильном кольце группы гетероарил-С,1-3 заместителями; предпочтительно 1 или 2 заместителями; более предпочтительно 1 заместителем. Заместители независимо выбраны, предпочтительно, из группы, состоящей из (C1-C3)алкокси-, F, Cl, -CN,-OH, -CO2H, тетразола и F-замещенного (C1-C3)алкокси- (например, -OCF3); более предпочтительно от F и Cl. Еще более предпочтительно, группа гетероарил-С возможно замещена 1, или 2, или 3 (предпочтительно 1) атомами F. Наиболее предпочтительно, гетероарил не замещен. В альтернативном воплощении R3 и R4 вместе образуют =CHR11. В этом воплощении, если R3 и R4 в формуле (I) взяты вместе, то R11 является таким же, как "другие" из R8, R9 и R10, как определено выше и ниже, обычно и предпочтительно. Предпочтительные соединения по настоящему изобретению включают 2-[4-(6-фтор-1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид,2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-(6-метоксипиридин-3-ил)ацетамид,2-[4-(5-фтор-1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид,2-[1-циклогексил-4-(1 Н-индол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид,2-[1-(3-гидроксифенил)-4-(1H-индол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид,N-бензил-2-[8,9-дифтор-4-(5-фтор-1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,2-[1-(3-гидроксифенил)-4-(1 Н-индол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропил-N-фенилацетамид,N-бензил-2-[8,9-дифтор-4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,N-бензил-2-[8,9-дифтор-4-(6-фтор-1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,-7 010888N-изопропил-2-[5-оксо-1-фенил-4-(1 Н-пирроло[2,3-b]пиридин-3-илметил)-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-фенилацетамид,N-бензил-2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен 6-ил]-N-изопропилацетамид,N-(6-хлорпиридин-3-ил)-2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,N-(6-этоксипиридин-3-ил)-2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,2-[4-(1 Н-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-(6-метоксипиридин-3-ил)ацетамид,2-[4-(1H-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид,N-бензил-2-[8,9-дифтор-4-(1 Н-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,N-бензил-2-[4-(1H-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,2-[4-(1H-индол-3-илметил)-4-метил-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-фенилацетамид,2-[1-(2-фторфенил)-4-(1 Н-индазол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен 6-ил]-N-изопропил-N-фенилацетамид,2-[1-(3-фторфенил)-4-(1H-индазол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен 6-ил]-N-изопропил-N-фенилацетамид,2-[1-циклогексил-4-(1H-индазол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-фенилацетамид,2-[1-(4-фторфенил)-4-(1H-индазол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен 6-ил]-N-изопропил-N-фенилацетамид,N-(4-фторфенил)-2-[4-(1 Н-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид,2-[4-(1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид,2-[4-(1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид,2-[1-циклогексил-4-(1 Н-индол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-фенилацетамид,2-[1-(2-фторфенил)-4-(1 Н-индол-3-илметил)-5-оксо-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6 ил]-N-изопропил-N-фенилацетамид, и 2-[4-(1 Н-индол-3-илметилен)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид; или их фармацевтически приемлемую соль. Подмножество таких предпочтительных соединений включает 2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид;N-бензил-2-[4-(1 Н-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил]-N-изопропилацетамид; и 2-[4-(1H-индазол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-фенилацетамид; 2-[4-(1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-Nизопропил-N-(6-метоксипиридин-3-ил)ацетамид; или их фармацевтически приемлемую соль. Еще одно подмножество таких предпочтительных соединений включает энантиомеры-8 010888 или их фармацевтически приемлемую соль. В изобретении также раскрыто промежуточное соединение формулы (D) или его соль, представляющее собой промежуточное соединение, также полезное при получении соединений формулы (I) где А, В, X, D, R1 и R2 являются такими, как определено выше для соединений формулы (I), обычно и предпочтительно;R представляет собой (С 1-C6)алкил или (С 3-С 6)циклоалкил; предпочтительно (C1-C4)алкил; более предпочтительно прямоцепочечный (С 1-С 4)алкил, такой как -CH3 или -CH2CH3. Формула (D-1), где R является таким, как определено выше для формулы (D), и R7 является таким,как определено выше для соединений формулы (I), обычно и предпочтительно, представляет предпочтительную подгруппу формулы (D) Формула (F-1a), где R7 является таким, как определено выше для соединений формулы (I), обычно и предпочтительно, представляет предпочтительную подгруппу формулы (F-1). В настоящем изобретении также раскрыт способ получения соединения формулы (С) включающий приведение соединения формулы (А) в контакт с соединением формулы (В) в присутствии кислотного катализатора, где A, B, X и D являются такими, как определено выше для формулы (I), обычно и предпочтительно. Каждый R независимо представляет собой (C1-C6)алкил или (C3-C6)циклоалкил; предпочтительно (C1-C4)алкил; более предпочтительно прямоцепочечный (C1-C4)алкил, такой как -CH3 или -CH2CH3. Кислотный катализатор может представлять собой неорганическую кислоту, например соляную кислоту или серную кислоту; органическую сульфоновую кислоту, например бензолсульфоновую кислоту или пара-толуолсульфоновую кислоту; или карбоновую кислоту, например уксусную кислоту. Уксусная кислота является предпочтительным катализатором. Способ обычно осуществляют в присутствии растворителя, предпочтительно апротонного растворителя, такого как ДМФ, ацетон, метилэтилкетон, этилацетат, метиленхлорид, хлороформ, диоксан, ТГФ,толуол или ксилолы. Более предпочтительно растворитель представляет собой углеводородный растворитель, такой как толуол или ксилол(ы); в особенности ксилол(ы). Способ может быть осуществлен при температуре окружающей среды, такой как приблизительно 25 С, или при повышенной температуре, обычно в интервале от приблизительно 50 С до температуры дефлегмации, причем предпочтительный интервал заканчивается приблизительно 150 или 200 С. Способ может быть осуществлен при атмосферном давлении или при избыточном давлении, например до 1,01325, 2,0265, 3,03975, 4,053 или 5,06625 МПа (10, 20, 30, 40 или 50 атм). В предпочтительном воплощении лабораторного масштаба раствор соединения формулы (В) в апротонном растворителе добавляют к нагретому раствору соединения формулы (А) и кислотному катализатору в апротонном растворителе в реакционном сосуде, и все нагревают при повышенной температуре в соответствии с описанным более подробно в получениях (3A) и (3B) в разделе примеры. Продукт (С) в предпочтительных условиях может быть выделен из реакционной смеси простым фильтрованием. Также раскрыт способ получения соединения формулы (D), соединения формулы (Е), соединения формулы (F-1) или соединения формулы (I-1) включающий превращение соединения формулы (С), получаемого способом, описанным выше, в соединение формулы (D), соединение формулы (Е), соединение формулы (F-1) или соединение формулы (I-1),где A, B, X, D, R, R1, R2, R3 и R4 являются такими, как определено выше, обычно и предпочтительно. Это изобретение также относится к солям и сольватам, включая гидраты, соединений по изобретению. Соединения по изобретению и промежуточные соединения, основные по природе, способны образовывать широкое разнообразие солей с различными неорганическими и органическими кислотами. Кислоты, которые могут быть использованы для получения фармацевтически приемлемых солей присоединения кислоты таких соединений, представляют собой такие кислоты, которые образуют нетоксичные соли присоединения кислоты, т.е. соли, содержащие фармакологически приемлемые анионы. Некоторые из соединений по изобретению и промежуточных соединений являются кислыми по природе и способны образовывать соли с различными основаниями. Предпочтительными являются соли натрия и калия. Соединения по настоящему изобретению могут существовать в форме пролекарств. Соединения формулы (I), имеющие свободные карбокси-, амино- или гидроксигруппы, могут быть превращены в,например, сложные эфиры или амиды, действующие в качестве пролекарств. Соединение формулы (I) может входить в состав фармацевтической композиции. Такая композиция может также содержать по меньшей мере один дополнительный фармацевтический агент, который предпочтительно представляет собой средство против ожирения. Дополнительный фармацевтический агент также может представлять собой агент, полезный в лечении заболевания, сопутствующего основному- 10010888 показанию применения композиции. Композиция предпочтительно содержит терапевтически эффективное количество соединения формулы (I) или терапевтически эффективное количество комбинации соединения формулы (I) и дополнительного фармацевтического агента. Также композиция предпочтительно содержит фармацевтически приемлемый эксципиент, разбавитель или носитель. Соединения формулы (I) также могут быть использованы в способе лечения заболевания, состояния или расстройства, модулируемого агонистом рецептора CCK-A у животных, включающем введение животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, или сольвата или гидрата указанного соединения или указанной соли. Соединение формулы (I) может быть использовано самостоятельно или в комбинации по меньшей мере с одним дополнительным фармацевтическим агентом, предпочтительно средством против ожирения, или агентом, полезным в лечении заболевания, сопутствующего заболеванию, состоянию или расстройству. Заболевания, состояния или расстройства, модулируемые агонистом рецептора CCK-A у животных,включают ожирение, избыточный вес и желчные конкременты. Также вероятно могут быть улучшены заболевания, сопутствующие таким заболеваниям, состояниям или расстройствам. Соответственно, соединения по изобретению могут быть использованы в способе лечения ожирения у животного, включающем введение животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I), его фармацевтически приемлемой соли, или сольвата,или гидрата указанного соединения или указанной соли. Соединение формулы (I) может быть использовано самостоятельно или в комбинации по меньшей мере с одним дополнительным фармацевтическим агентом, предпочтительно средством против ожирения. Соединения по изобретению также могут быть использованы в способе регулирования массы животного, включающем введение животному соединения формулы (I), его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли в количестве, регулирующем массу организма. Соединение формулы (I) может быть использовано самостоятельно или в комбинации по меньшей мере с одним дополнительным фармацевтическим агентом, предпочтительно средством против ожирения. Соединения по изобретению могут быть использованы в способе уменьшения приема пищи животным, включающем введение животному соединения формулы (I), его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли в количестве, уменьшающем прием пищи. Соединение формулы (I) может быть использовано самостоятельно или в комбинации по меньшей мере с одним дополнительным фармацевтическим агентом, предпочтительно средством против ожирения. Соединения по изобретению также могут быть использованы в способе профилактики желчных конкрементов у животного, включающем введение животному соединения формулы (I), его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли в количестве, предотвращающем образование желчных конкрементов. Соединение формулы (I) может быть использовано самостоятельно или в комбинации по меньшей мере с одним дополнительным фармацевтическим агентом, предпочтительно агентом, полезным в лечении или профилактике желчных конкрементов. Соединения по настоящему изобретению могут входить в состав фармацевтического набора для применения потребителем в лечении ожирения. Набор содержит (а) подходящую лекарственную форму,содержащую соединение формулы (I), и (б) указания, описывающие способ применения лекарственной формы для лечения или профилактики ожирения. Набор также может представлять собой комбинацию раздельных фармацевтических композиций. Такой фармацевтический набор содержит:(а) первую фармацевтическую композицию, содержащую соединение формулы (I),(б) вторую фармацевтическую композицию, содержащую второе соединение, полезное для лечения ожирения, профилактики желчных конкрементов или лечения заболевания, сопутствующего ожирению; и(в) контейнер, содержащий первую и вторую композиции. Как правило, набор также включает указания по введению отдельных компонентов. Особенно благоприятной является форма набора, когда отдельные компоненты предпочтительно вводят в различных лекарственных формах или с различными интервалами введения доз. Одним из примеров такого набора по настоящему изобретению является так называемая блистерная упаковка. Блистерные упаковки широко используются в фармацевтической промышленности для упаковки стандартных лекарственных форм (таблетки, капсулы и тому подобного). Блистерные упаковки обычно состоят из листа относительно жесткого материала, покрытого фольгой, предпочтительно, прозрачного пластичного материала. В процессе упаковки в пластиковой фольге формируют углубления. Углубления имеют размер и форму упаковываемых таблеток или капсул. Затем таблетки или капсулы помещают в углубления и листом относительно жесткого материала запаивают пластиковую фольгу со стороны, противоположной направлению, в котором формируют углубления. В результате таблетки или- 11010888 капсулы запаивают в углубления между пластиковой фольгой и листом. Предпочтительно, прочность листа такова, что таблетки или капсулы могут быть удалены из блистерной упаковки вручную путем нажатия на углубления, в результате чего в листе образуется отверстие на месте углубления. Затем таблетка или капсула может быть извлечена через отверстие. Может быть желательным обеспечение набора памяткой, например, в форме номеров за таблетками или капсулами, где номера соответствуют суткам схемы приема таблеток или капсул, которые должны быть приняты. Еще один пример такой памятки представляет собой календарь, напечатанный на наборе,например, следующим образом: "Первая неделя, понедельник, вторник,и так далее Вторая неделя,понедельник, вторник," и так далее. Очевидны и другие варианты памяток. "Суточная доза" может представлять собой одну таблетку или капсулу или несколько пилюль или капсул, которые следует принять в указанные сутки. Кроме того, суточная доза соединений по настоящему изобретению может состоять из таблетки или капсулы, тогда как суточная доза второго соединения может состоять из нескольких таблеток или капсул и наоборот. Памятка должна отражать это. Определения Используемые здесь следующие термины, если не указано иначе, имеют значения, приписанные им. Термин "алкил" означает прямоцепочечный или разветвленный углеводородный радикал, имеющий общую формулу CnH2n+1. Например, термин "(C1-C6)алкил" относится к одновалентной, прямоцепочечной или разветвленной насыщенной алифатической группе, содержащей от 1 до 6 атомов углерода (например, метилу, этилу, н-пропилу, изопропилу, н-бутилу, изобутилу, втор-бутилу, трет-бутилу, нпентилу, 1-метилбутилу, 2-метилбутилу, 3-метилбутилу, неопентилу, 3,3-диметилпропилу, гексилу, 2 метилпентилу и тому подобному). Аналогично, алкильная часть группы, например алкокси, ацилильной,алкиламино, диалкиламино или алкилтиогруппы, имеет такое же значение, как указано выше. "Галогензамещенный алкил" относится к алкильной группе, замещенной одним или более чем одним атомом галогена (например, -CH2Cl, -CHF2, -CF3, -C2F5 и т.п.). Аналогично, такие термины, как "F-замещенный алкил" или "Cl-замещенный алкил" означают алкильную группу, замещенную одним или более чем одним атомом фтора или хлора, соответственно. Термин "ацил" относится к алкил-, циклоалкил-, гетероцикл-, арил- и гетероарилзамещенным карбонильным группам. Например, ацил включает группы, такие как (C1-C6)алканоил (например, формил,ацетил, пропионил и т.п.), (C3-C6)циклоалкилкарбонил (например, циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил и т.п.), гетероциклилкарбонил (например, пирролидинилкарбонил, пирролид-2-он-5-карбонил, пиперидинилкарбонил, пиперазинилкарбонил, тетрагидрофуранилкарбонил и т.п.), ароил (например, бензоил) и гетероароил (например, тиофенил-2-карбонил, тиофенил-3-карбонил,фуранил-2-карбонил, фуранил-3-карбонил, 1 Н-пирроил-2-карбонил, 1H-пирроил-3-карбонил, бензо[b]тиофенил-2-карбонил и т.д.). Термин "галогено" обозначает F, Cl, Br или I. Предпочтительно, галогено представляет собой F, Cl или Br; более предпочтительно F или Cl."Ar" означает арил. Термин "арил" относится к ароматическим группировкам, имеющим единичную (например, фенилу) или конденсированную кольцевую систему (например, нафталину, антрацену, фенантрену и т.д.). Типичная арильная группа представляет собой 6-10-членную ароматическую карбоциклическую кольцевую систему. Если не указано иначе, арильная группа может быть присоединена к химическому объекту или химической группировке посредством любого из атомов углерода в ароматической кольцевой системе. Арильная часть (т.е. ароматическая группировка) группы (например, арилалкила) имеет такое же значение, как указано выше. Термин "частично или полностью насыщенное карбоциклическое кольцо" (также названное как"частично или полностью насыщенный циклоалкил") относится к неароматическим кольцам, которые являются или частично, или полностью гидрированными и могут существовать в виде единичного кольца, бициклического кольца или спирального кольца. Если не указано иначе, карбоциклическое кольцо обычно представляет собой 3-8-членное кольцо (предпочтительно 3-6-членное кольцо). Например, частично или полностью насыщенные карбоциклические/циклоалкильные кольца включают такие группы,как циклопропил, циклопропенил, циклобутил, циклобутенил, циклопентил, циклопентенил, циклопентадиенил, циклогексил, циклогексенил, циклогексадиенил, норборнил (бицикло[2,2,1]гептил), норборненил, бицикло[2,2,2]октил и т.п. Если не указано иначе, карбоциклическая группа может быть присоединена к химическому объекту или химической группировке посредством любого из атомов углерода в циклоалкильной кольцевой системе. Циклоалкильная часть группы (например, циклоалкилалкильной,циклоалкиламино и т.д.) имеет такое же значение, как указано выше. Термин "частично или полностью насыщенное гетероциклическое кольцо" (также названное как"частично или полностью насыщенный гетероцикл" или "частично или полностью насыщенный гетероциклил") относится к неароматическим кольцам, которые являются или частично или полностью гидрированными, содержат по меньшей мере один кольцевой гетероатом и могут существовать в виде единичного кольца, бициклического кольца или спирального кольца. Если не указано иначе, гетероциклическое- 12010888 кольцо обычно представляет собой 4-7-членное кольцо, содержащее 1-4 гетероатома (предпочтительно 1 или 2 гетероатома), независимо выбранные из серы, кислорода или азота. Гетероциклические кольца включают такие группы, как эпокси, азиридинил, пиранил, тетрагидрофуранил, пирролидинил, Nметилпирролидинил, имидазолидинил, пиперидинил, пиперазинил, пиразолидинил, морфолино, тетрагидротиенил, тетрагидротиенил 1,1-диоксид и т.п. Если не указано иначе, гетероциклическая группа может быть присоединена к химическому объекту или химической группировке посредством любого из кольцевых атомов в гетероциклической кольцевой системе. Гетероциклическая часть группы (например,гетероциклилалкильной) имеет такое же значение, как указано выше. Термин "гетероарил" относится к ароматическим группировкам, содержащим по меньшей мере один гетероатом (например, кислород, серу, азот или их комбинации) в 5-10-членной ароматической кольцевой системе (например, пиридилу, пиразолилу, индолилу, индазолилу, азаиндолилу, тиенилу, фуранилу, бензофуранилу, оксазолилу, изоксазолилу, имидазолилу, тетразолилу, пиримидилу, пиразинилу,пиридазинилу, тиазолилу, изотиазолилу, хинолинилу, изохинолинилу, бензотиофенилу и т.д.). Гетероароматическая группировка может состоять из одного кольца или конденсированной кольцевой системы. Типичное единичное гетероарильное кольцо представляет собой 5-6-членное кольцо, содержащее от одного до трех гетероатомов, независимо выбранных из кислорода, серы и азота, а типичная конденсированная гетероарильная кольцевая система представляет собой 9-10-членную кольцевую систему, содержащую от одного до четырех гетероатомов, независимо выбранных из кислорода, серы и азота. Если не указано иначе, гетероарильная группа может быть присоединена к химическому объекту или химической группировке посредством любого из атомов в ароматической кольцевой системе (например, имидазол-1 иле, имидазол-2-иле, имидазол-4-иле, имидазол-5-иле). Гетероарильная часть группы (например, гетероарилалкильной) имеет такое же значение, как указано выше. Термин "сольват" относится к молекулярному комплексу соединения с одной или более чем одной молекулой растворителя. Для сольватов соединения формулы (I) (включая пролекарства и их фармацевтически приемлемые соли) молекулы растворителя представляют собой молекулы, обычно используемые в фармацевтике, про которые известно, что они безвредны для реципиента, например воду, этанол и т.п. Термин "гидрат" относится к сольвату, в котором молекула растворителя представляет собой воду. Термин "защитная группа" или "Pg" относится к заместителю, обычно используемому для блокирования или защиты конкретной функциональной группы, в то время как другие функциональные группы соединения реагируют. Например, "аминозащитная группа" представляет собой заместитель, присоединенный к аминогруппе, который блокирует или защищает в соединении функциональную аминогруппу. Подходящие аминозащитные группы включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС),бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Аналогично, "гидроксизащитная группа" относится к заместителю на гидроксигруппе, который блокирует или защищает функциональную гидроксигруппу. Подходящие гидроксизащитные группы включают ацетил и силил. "Карбоксизащитная группа" относится к заместителю, блокирующему или защищающему функциональную карбоксильную группу, такую как эфирная группа. Обычные карбоксизащитные группы включают-CH2CH2SO2Ph,цианоэтил,2-(триметилсилил)этил,2-(триметилсилил)этоксиметил,2-(паратолуолсульфонил)этил, 2-(пара-нитрофенилсульфенил)этил, 2-(дифенилфосфино)этил, нитроэтил и т.п. Общее описание защитных групп и их применение см. в Т. W. Greene, Protective Groups in Organic Synthesis, John WileySons, New York, 1991. Выражение "пролекарства" означает соединения, являющиеся предшественниками лекарства, которые после введения высвобождают лекарство in vivo посредством некоторых химических или физиологических способов (например, пролекарство превращается в желаемую форму лекарства путем приведения до физиологического значения pH или путем действия фермента). Фраза "фармацевтически приемлемый" означает, что вещество или композиция химически и/или токсикологически совместимо(а) с другими ингредиентами, содержащимися в препарате, и/или с животным, которое лечат ими. Фраза "терапевтически эффективный" предназначена для оценки количества агента для применения в лечении заболевания, состояния или расстройства, которое (1) лечит или предотвращает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более чем один симптом конкретного заболевания, состояния или расстройства или (3) предотвращает или замедляет начало одного или более чем одного симптома описанного здесь конкретного заболевания, состояния или расстройства. Термины "лечение", "лечить" и "процесс лечения" охватывает как превентивное, т.е. профилактическое, так и паллиативное лечение. Термин "животное" означает людей, а также других теплокровных членов животного мира, обладающих гомеостатическим механизмом, включая млекопитающих (например, животных-спутников, животных в зоопарках и животных как источников пищи) и птиц. Некоторыми примерами животныхспутников являются собачьи (например, собаки), кошачьи (например, кошки) и лошади; некоторыми примерами животных как источников пищи являются свиньи, коровы, овцы, домашние птицы и т.п. Предпочтительно, животным является млекопитающее. Предпочтительно, млекопитающим является че- 13010888 ловек, животное-спутник или животное как источник пищи. Наиболее предпочтительно, животным является человек. Термин "соединения по настоящему изобретению" и тому подобное (если специально не установлено иначе) обычно и предпочтительно означает соединения формул (I), как определено выше (включая все воплощения), их пролекарства, фармацевтически приемлемые соли соединений и/или пролекарств, и гидраты или сольваты соединений, солей и/или пролекарств, а также все стереоизомеры, атропоизомеры,таутомеры и изотопно-меченные производные соединений формулы (I). Подробное описание Обычно соединения по настоящему изобретению могут быть получены способами, описанными здесь, или другими способами, находящимися в пределах знаний специалиста в области медицинской химии, включающими способы, аналогичные описанным в области техники для получения соединений,подобных или аналогичных соединениям по настоящему изобретению, или обладающих заместителями,подобными или такими же, как заместители соединений по настоящему изобретению. Некоторые промежуточные соединения и способы получения настоящих соединений предложены в качестве дополнительных признаков настоящего изобретения и проиллюстрированы следующими схемами реакций. Эти способы могут быть осуществлены последовательными или конвергентными путями синтеза. Другие способы описаны в экспериментальной части. Способы очистки включают кристаллизацию и нормально-фазовую или обращенно-фазовую хроматографию. В представленном ниже обсуждении, относящемся к схемам реакций, использованы некоторые обычные сокращения и акронимы, которые включают AcOH (уксусную кислоту), ДМФ (диметилформамид), ДМСО (диметилсульфоксид), NH4OAc (ацетат аммония), NMP (N-метилпирролидон), OTS (паратолуолсульфонилокси), Pg (защитную группу) и ТГФ (тетрагидрофуран). Схема I ниже иллюстрирует один из способов получения соединений формулы (I), где Е и G оба представляют собой -N-. В структурах на схеме I ниже А, В, X, D, R, R1, R2, R3 и R4 являются такими, как определено выше, обычно и предпочтительно. Схема I- 14010888 В соответствии со схемой I соединение формулы (С) получают путем сочетания диамина формулы(А) с соответствующим бис-алкоксиакрилатом формулы (В), таким как этиловый эфир 3,3 диэтоксиакриловой кислоты, например, путем нагревания двух соединений в подходящем растворителе,таком как толуол или ксилол(ы), в присутствии кислотного катализатора, такого как уксусная кислота. Диамины формулы (А) имеются в продаже, могут быть получены способами, описанными в литературе,или могут быть получены способами, аналогичными описанным в литературе для аналогичных соединений, или способами, находящимися в объеме знаний специалистов в области медицинской химии, из доступных исходных веществ. Иминоэфир формулы (С) затем N-алкилируют алкилирующим агентом R2L, где L представляет собой уходящую группу, такую как Cl, Br, I или OTs (например, Br как в 2-бром-N-изопропил-Nфенилацетамиде), с использованием инертного растворителя, такого как NMP или ДМФ, и основания,такого как гексаметилдисилазид лития или гидрид натрия, при температуре от приблизительно -20 С до приблизительно 70 С в течение от приблизительно 2 до приблизительно 48 ч с получением Nалкилированного иминоэфира формулы (D). Альтернативно, соединение формулы (С) алкилируют в описанных выше условиях алкилирующим агентом L-CH2CO2Pg (где L представляет собой уходящую группу, и Pg представляет собой защитную группу), таким как сложный эфир 2-галогенуксусной кислоты (например, бензиловый эфир 2 бромуксусной кислоты), и удаляют сложноэфирную защитную группу с получением соответствующей карбоновой кислоты, т.е. соединения формулы (D), где R2 представляет собой -CH2COOH. Соединениекарбоновую кислоту затем сочетают с амином HNR6R7 с использованием стандартных способов амидного сочетания с получением соединения формулы (D), где R2 представляет собой -CH2C(O)N(R6)(R7). Соединение формулы (D), где R2 представляет собой -CH2C(O)N(R6)(R7), затем превращают в триазиновое производное формулы (F-1) путем конденсации соединения формулы (D) с ацилгидразидом общей формулы R1CONHNH2 в органическом растворителе, таком как ледяная уксусная кислота или толуол, при температуре, находящейся в диапазоне от приблизительно 0 С до температуры дефлегмации. Альтернативно, соединение формулы (С) превращают в триазин формулы (Е) в описанных выше условиях для образования триазинового кольца. Соединение формулы (Е) затем N-алкилируют с образованием соединения формулы (F-1) в соответствии со способом, описанным выше для алкилирования соединения формулы (С). Соединение формулы (F-1) алкилируют по атому углерода С-3 с использованием подходящего электрофила, такого как (R8)(R9)(R10)C-галогенид или -тозилат (например, R3L, где R3 представляет собой -C(R8)(R9)(R10), и L представляет собой уходящую группу, такую как Cl, Br, I или OTs), подходящего основания, такого как гексаметилдисилазид лития или гидрид натрия, и инертного растворителя, такого как ДМФ, NMP или ТГФ, при температуре, находящейся в диапазоне от приблизительно -20 С до приблизительно 70 С, с получением моноалкилированного продукта формулы (I-1), где R3 представляет собой -C(R8)(R9)(R10), и R4 представляет собой H. Повторяя эту методику с соответствующим основанием и алкилирующим агентом (например, R4L, где R4 представляет собой алкил или циклоалкил, и L представляет собой уходящую группу, такую как Cl, Br, I или OTs) получают соединение формулы (I-1), где R3 представляет собой -C(R8)(R9)(R10), и R4 представляет собой алкил или циклоалкил. Соединения, где один из R3 и R4 представляет собой галогено, выходящие за рамки заявленной формулы (I), но приводимые здесь в качестве дополнительной иллюстрации, могут быть получены аналогичным образом: путем образования аниона при С-3 с использованием сильного основания, такого как гексаметилдисилазид лития или гидрид натрия, в инертном растворителе, таком как ДМФ, NMP или ТГФ, при температуре, находящейся в диапазоне от приблизительно -78 С до комнатной температуры, и последующего захвата аниона подходящим галогенирующим агентом (например, Br2, Cl2, трифторидом (диэтиламино)серы(DAST) или бис-(тетрафторборатом) 1-(хлорметил)-4-фтор-1,4-диазониабицикло[2,2,2]октана (Selectfluor, поставляется Air Products and Chemicals, Inc., 7201 Hamilton Boulevard, Allentown, PA с получением С-3 галогенированного соединения. Аналогично, захват аниона С-3 подходящим окислителем, таким как 2-(фенилсульфонил)-3-фенилоксазиридин или оксодипероксимолибден(пиридин) (триамид гексаметилфосфорной кислоты) (MoOPh), позволяет получить С-3 гидроксисоединение, которое затем может быть превращено в С-3 алкоксисоединение путем О-алкилирования с алкилгалогенидом и подходящим основанием в стандартных условиях. Альтернативно, соединение формулы (F-1) конденсируют с альдегидом R11CHO, таким как индол 3-карбоксальдегид, в органическом растворителе, таком как толуол или ксилол(ы), предпочтительно в присутствии основания, такого как пиперидин, при температуре, находящейся в диапазоне от комнатной температуры до температуры дефлегмации, с получением соответствующего альфа-бета ненасыщенного промежуточного соединения (т.е. где R3 и R4 вместе образуют =CHR11), которое может быть восстановлено в стандартных условиях (например, Zn-AcOH; H2, Pd-C) с получением соединения формулы (I-1),где один из R3 и R4 представляет собой H, а другой из R3 и R4 представляет собой -CH2R10 (R11 является таким же, как R10). Схема II ниже иллюстрирует один из способов получения соединений формулы (I), где Е представляет собой -N-, и G представляет собой -C(R5)-. Эти соединения выходят за рамки формулы (I) согласно- 15010888 настоящему изобретению, но схема их получения приведена здесь в качестве дополнительной иллюстрации. В структурах на схеме II ниже А, В, X, D, R, R1, R2, R3, R4 и R5 являются такими, как определено выше, обычно и предпочтительно. Схема II В соответствии со схемой II амидин формулы (G) получают путем обработки иминоэфира формулы(С) NH3 или источником аммиака (например, NH4OAc). Затем амидин конденсируют в стандартных условиях, например, с бромкетоном формулы R1CH(Br)C(O)R5, с получением имидазола формулы (Н). Альтернативно, иминоэфир формулы (С) может быть конденсирован с альфа-аминокетоном формулыH2NCH(R5)C(O)R1 с получением имидазола формулы (Н) (См., например, М. Langlois et al., J. Heterocycl.Chem. (1982), 19(1), 193-200). Имидазол формулы (Н) затем подвергают N1-алкилированию (т.е. введению заместителя R2) с использованием методик, аналогичных описанным выше для N-алкилирования соединения формулы (С) или (Е) в схеме I, с получением N-алкилированного имидазола формулы (F-2). Это соединение затем алкилируют по C3 с использованием условий, аналогичных описанным для превращения соединения формулы (F-1) в соединение формулы (I-1) в схеме I с получением соединения формулы (I-2) схемы II. Схема III ниже иллюстрирует один из способов получения соединений формулы (I), где Е представляет собой -C(R5)- и G представляет собой -N-. Эти соединения выходят за рамки формулы (I) согласно настоящему изобретению, но схема их получения приведена здесь в качестве дополнительной иллюстрации. В структурах на схеме III ниже А, В, X, D, R, R1, R2, R3, R4 и R5 являются такими, как определено выше, обычно и предпочтительно. Соединения формулы (I-3) могут быть синтезированы способами, аналогичными представленным в химической и патентной литературе для похожих или аналогичных соединений (См., например, "Diazepine derivatives," Neth. Appl., NL 7803585 (1978); Armin Walser, "Imidazodiazepine derivatives," Ger.Often., DE 2813549 (1978); и Armin Walser and Rodney Ian Fryer, "Imidazo[1,5-a][1,5]benzodiazepines" U.S. 4080323 (1978. Таким образом, соединение формулы (D) конденсируют с анионом нитроалкана (который может быть образован обработкой нитроалкана сильным основанием, таким как гексаметилдисилазид лития, гидрид натрия, трет-бутоксид калия или диизопропиламид лития, в апротонном органическом растворителе, таком как ТГФ, ДМСО или ДМФ, например), при температуре, находящейся в диапазоне от приблизительно -30 С до приблизительно 100 С, с получением соединения формулы (J). Это соединение затем восстанавливают с использованием металлического катализатора, такого как палладий, платина или никель, в присутствии водорода с получением соединения формулы (K). Соединение формулы (K) ацилируют с использованием подходящего ацилирующего агента для введения R1CO-, например, ацилгалогенида/основания или карбоновой кислоты/связующего агента (например,гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида(EDCl),N,Nкарбонилдиимидазола), с получением соединения формулы (L), которое затем подвергают воздействию в стандартных дегидратирующих условиях циклизации с получением соединения формулы (М). Окисление соединения формулы (М) с получением соединения формулы (F-3) осуществляют с использованием окислителя, такого как диоксид марганца или перманганат калия. Соединение формулы (F-3) может быть превращено в соединение формулы (I-3) способом, аналогичным описанному для превращения соединения формулы (F-1) в соединение формулы (I-1) на схеме I. Обычные способы и/или методики разделения и очистки, известные специалисту в данной области техники, могут быть использованы для выделения соединений по настоящему изобретению, а также различных связанных с ними промежуточных соединений. Такие методики хорошо известны специалистам- 17010888 в данной области техники и могут включать, например, все типы хроматографии (жидкостную хроматографию высокого давления (ЖХВД), колоночную хроматографию с использованием обычных адсорбентов, таких как силикагель, и тонкослойную хроматографию), перекристаллизацию и дифференциальные(т.е. жидкость-жидкость) способы экстракции. Соединения по настоящему изобретению могут быть выделены и использованы сами по себе или в форме их фармацевтически приемлемых солей, сольватов и/или гидратов. Термин "соли" включает как неорганические, так и органические соли. Эти соли могут быть получены in situ во время конечного выделения и очистки соединения, или путем отдельного взаимодействия соединения с подходящей органической или неорганической кислотой или основанием и выделения соли, полученной таким образом. Соли промежуточных соединений не обязательно должны быть фармацевтически приемлемыми. Типичные фармацевтически приемлемые соли присоединения кислоты настоящих соединений включают хлористо-водородную, бромисто-водородную, йодисто-водородную соли, нитрат, сульфат,бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, кислый цитрат,тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат,сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, паратолуолсульфонат, памоат, пальмитат, малонат, стеарат, лаурат, малат, борат, гексафторфосфат, нафтилат,глюкогептонат, лактобионат и лаурилсульфонат и т.п. Предпочтительной солью соединений является хлористо-водородная соль. Соли, образуемые основаниями, включают катионы на основе щелочных и щелочно-земельных металлов, таких как натрий, литий, калий, кальций, магний и т.п., а также катионы аммония, четвертичного аммония и 1, 2 или 3 аминопроизводных, в том числе катионы аммония, тетраметиламмония и тетраэтиламмония и катионы, полученные из метиламина, этиламина, диметиламина, триметиламина, триэтиламина и т.п., но не ограничиваясь ими. См., например, Berge, et al., J. Pharm. Sci., 66, 1-19 (1977). Соединения формулы (I) могут существовать в форме пролекарств. Используемый здесь термин(I) или фармацевтически приемлемой соли, гидрата или сольвата соединения. Превращение может быть осуществлено при помощи различных механизмов, таких как гидролиз в крови. Обсуждение применения пролекарств предложено Т. Higuchi and W. Stella, "Prodrugs as Novel Delivery Systems," Vol. 14 of theChem. 1996, 39, 10. Например, если соединение по настоящему изобретению содержит функциональную группу карбоновой кислоты, то пролекарство может включать сложный эфир, образуемый путем замещения атома водорода кислотной группы такой группой, как (C1-C8)алкил, (C2-C12)алканоилоксиметил, 1(алканоилокси)этил, имеющий от 4 до 9 атомов углерода, 1-метил-1-(алканоилокси)этил, имеющий от 5 до 10 атомов углерода, алкоксикарбонилоксиметил, имеющий от 3 до 6 атомов углерода, 1(алкоксикарбонилокси)этил, имеющий от 4 до 7 атомов углерода, 1-метил-1-(алкоксикарбонилокси)этил,имеющий от 5 до 8 атомов углерода, N-(алкоксикарбонил)аминометил, имеющий от 3 до 9 атомов углерода, 1-(N-(алкоксикарбонил)амино)этил, имеющий от 4 до 10 атомов углерода, 3-фталидил, 4 кротонолактонил, гамма-бутиролактон-4-ил, ди-N,N-(С 1-С 2)алкиламино(C2-C3)алкил (такой, как диметиламиноэтил), карбамоил-(C1-C2)алкил, N,N-ди(С 1-С 2)алкилкарбамоил-(C1-C2)алкил и пиперидин-,пирролидин- или морфолин(С 2-С 3)алкил. Аналогично, если соединение по настоящему изобретению содержит спиртовую функциональную группу, то пролекарство может быть получено путем замещения атома водорода спиртовой группы такой группой,как(C1-C6)алканоилоксиметил,1-C1-C6)алканоилокси)этил,1-метил-1-C1-C6)алканоилокси)этил, (C1-С 6)алкоксикарбонилоксиметил, N-(С 1-C6)алкоксикарбониламинометил, сукциноил, (C1-C6)алканоил, -амино-(C1-C4)алканоил, арилацил и -аминоацил, или -аминоациламиноацил,где каждая -аминоацильная группа независимо выбрана из встречающегося в природе кольца Lаминокислот, P(O)(OH)2, P(O)(O(C1-C6)алкил)2 или гликозила (радикал, являющийся результатом удаления гидроксильной группы с гемиацетальной формы углеводорода). Если соединение по настоящему изобретению содержит аминофункциональную группу, то пролекарство может быть получено путем замещения атома водорода в аминогруппе группой, такой как Rкарбонил-; RO-карбонил-; (R')(R)N-карбонил-, где R и R', каждый независимо, представляют собой (C1C10)алкил, (C3-С 7)циклоалкил или бензил; или R-карбонил представляет собой природный -аминоацил или природный -аминоацил-природный -аминоацил; -C(OH)C(O)OY', где Y' представляет собой H,(C1-C6)алкил или бензил; -C(OY0)Y1, где Y0 представляет собой (C1-C4)алкил, и Y1 представляет собой(С 1-C6)алкил,карбокси(C1-C6)алкил,амино(С 1-С 4)алкил или моно-Nили ди-N,N-(C1C6)алкиламиноалкил; или -C(Y2)Y3, где Y2 представляет собой H или метил, и Y3 представляет собой моно-N- или ди-N,N-(C1-C6)алкиламино, морфолино, пиперидин-1-ил или пирролидин-1-ил. Множество соединений по настоящему изобретению и некоторые промежуточные соединения содержат один или более чем один асимметричный или хиральный центр (например, атом углерода С-3,- 18010888 имеющий R3 и R4 в формуле (I, следовательно, такие соединения существуют в различных стереоизомерных формах (например, энантиомеры и диастереоизомеры). Множество соединений по настоящему изобретению также демонстрируют атропоизомерию. Все стереоизомерные формы промежуточных соединений и соединений по настоящему изобретению, а также их смеси, включающие рацемические и диастереоизомерные смеси, которые обладают свойствами, полезными в лечении обсуждающихся здесь состояний, или представляют собой промежуточные соединения, полезные при получении соединений,обладающих такими свойствами, образуют часть настоящего изобретения. Обычно один из энантиомеров биологически является более активным по сравнению с другим энантиомером. Однако менее активный энантиомер может быть превращен в рацемическую смесь посредством эпимеризации при стереоцентре С-3 с использованием сильного основания, такого как, например, метоксид натрия в метаноле. Затем рацемическая смесь может быть разделена на каждый энантиомер с использованием стандартных условий, таких как расщепление или хиральная хроматография. Дополнительно, настоящее изобретение охватывает все геометрические изомеры и атропоизомеры. Например, если промежуточное соединение или соединение по настоящему изобретению содержит двойную связь или конденсированное кольцо, то в объеме изобретения содержатся как цис-, так и транс-формы, а также смеси. Диастереоизомерные смеси могут быть разделены на индивидуальные диастереоизомеры на основе их физико-химических различий способами, хорошо известными специалистам в данной области техники, такими как хроматография и/или фракционная кристаллизация. Энантиомеры могут быть разделены путем использования колонки для хиральной ЖХВД. Они также могут быть разделены путем превращения энантиомерной смеси в диастереоизомерную смесь взаимодействием с соответствующим оптически активным соединением (например, хиральным вспомогательным веществом, таким как хиральный спирт или хлорангидрид Мошера), разделения диастереоизомеров и превращения (например, путем гидролиза) индивидуальных диастереоизомеров в соответствующие чистые энантиомеры. Соединения по настоящему изобретению и промежуточные соединения могут существовать в несольватированной, а также сольватированной формах с растворителями, такими как вода, этанол, изопропиловый спирт и тому подобное, и сольватированные и несольватированные формы включены в объем изобретения. Сольваты для применения в способах по изобретению должны быть с фармацевтически приемлемыми растворителями. Ряд соединений по настоящему изобретению и их промежуточные соединения демонстрируют таутомерию и таким образом могут существовать в различных таутомерных формах при определенных условиях. Термин "таутомер" или "таутомерная форма" относится к структурным изомерам с различными значениями энергии, которые взаимопревращаемы посредством низкоэнергетического барьера. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимные превращения путем миграции протона, такие как кето-енольные и имино-енаминовые изомеризации. Конкретный пример протонного таутомера представляет собой имидазольную группировку, где водород может мигрировать между атомами азота кольца. Валентные таутомеры включают взаимные превращения путем реорганизации некоторых электронов связи. Все такие таутомерные формы (например, все кетоенольные и имино-енаминовые формы) находятся в объеме изобретения. Изображение любой конкретной таутомерной формы в любой из структурных формул здесь не предназначено для того, чтобы быть ограничивающим по отношению к этой форме, а означает, что она является представителем целого ряда таутомеров. Настоящее изобретение также охватывает изотопно-меченные соединения, идентичные соединениям формулы (I) или их промежуточным соединениям, но за исключением того, что один или более чем один атом заменен атомом, имеющим атомную массу или массовое число, которые отличаются от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, которые могут быть включены в промежуточные соединения или соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, йода и хлора, такие как 2H, 3H, 11 С, 13 С, 14 С, 13N,15N, 15O, 17O, 18O, 31P, 32P, 35S, 18F, 123I, 125I и 36Cl, соответственно. Соединения по настоящему изобретению, их пролекарства и фармацевтически приемлемые соли, гидраты и сольваты указанных соединений и указанных пролекарств, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, находятся в объеме настоящего изобретения. Некоторые изотопно-меченные соединения по настоящему изобретению (например, соединения,меченные 3 Н и 14 С) являются полезными в анализах распределения соединения и/или субстрата в тканях. Тритиевые (т.е. 3 Н) и углерод-14 (т.е. 14 С) изотопы особенно предпочтительны ввиду легкости их получения и обнаружения. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий (т.е. 2 Н),может давать некоторые терапевтические преимущества, являющиеся результатом большей метаболической стабильности (например, увеличенный период полувыведения in vivo или уменьшенная потребность в дозе) и, следовательно, может быть предпочтительным в некоторых обстоятельствах. Позитронизлучающие изотопы, такие как 15O, 13N, 11 С и 18F, являются полезными для исследований путем позитронно-эмиссионной томографии (ПЭТ) для исследования оккупации рецепторов субстратом. Изотопномеченные соединения по настоящему изобретению, как правило, могут быть получены, следуя методикам, аналогичным описанным в приведенных здесь схемах и/или в примерах путем замещения реагента- 19010888 не меченного изотопом на реагент, меченный изотопом. Соединения по настоящему изобретению полезны, например, для лечения заболеваний, состояний и расстройств, модулируемых рецепторами холецистокинина А (например, агонистами рецептора CCK-A). Такие заболевания, состояния и расстройства включают ожирение и желчные конкременты, а также не связанные с ожирением состояния с избыточной массой и состояния с нормальной массой, где контроль или регулирование массы желательны для предотвращения ожирения или состояния с избыточной массой в результате развития, или только для поддержания оптимальной, здоровой массы организма. Соединения по настоящему изобретению также полезны в лечении или профилактике заболеваний, состояний и расстройств, которые являются клиническими последствиями ожирения или сопутствуют ему, таких как гипертензия, дислипидемия, диабет 2 типа (инсулиннезависимый), инсулинорезистентность, интолерантность к глюкозе, гиперинсулинемия, ишемическая болезнь сердца, стенокардия, застойная сердечная недостаточность, инсульт, желчные конкременты, холецистит, желчно-каменная болезнь, подагра, остеоартрит, обструктивное апноэ во сне и респираторные проблемы, заболевание желчного пузыря,некоторые формы рака (например, эндометрия, молочной железы, предстательной железы и ободочной кишки) и психологические расстройства (такие, как депрессия, расстройства приема пищи, расстройство схемы тела и низкая самооценка). Дополнительно, настоящие соединения полезны при лечении любого состояния, при котором желательно снизить массу или уменьшить прием пищи. Поэтому, в настоящем изобретении предложены способы лечения или профилактики таких заболеваний, состояний и/или расстройств, модулируемых агонистами рецептора CCK-A, у животного, включающие введение животному, нуждающемуся в таком лечении, соединения формулы (I), предпочтительно его терапевтически эффективного количества. Настоящие соединения обычно вводят в форме фармацевтической композиции. Соответственно, в настоящем изобретении также предложены фармацевтические композиции, содержащие терапевтически эффективное количество соединения формулы (I) в смеси с фармацевтически приемлемым эксципиентом, разбавителем или носителем, а также способы применения таких композиций в лечении заболеваний, состояний и/или расстройств, которые модулируются агонистами рецептора CCK-A у животного,или их клинических последствий или сопутствующих им заболеваний, включающие введение животному, нуждающемуся в таком лечении, такой фармацевтической композиции. Соединения формулы (I) и содержащие их композиции также полезны в изготовлении лекарственного средства для упомянутых здесь терапевтических применений. Соединения по настоящему изобретению можно вводить пациенту в дозах, находящихся в диапазоне от приблизительно 0,1 до приблизительно 3000 мг в сутки. Доза для человека обычно находится в диапазоне от приблизительно 1 до приблизительно 1000 мг в сутки; чаще от приблизительно 1 до приблизительно 400 или 500 мг в сутки; предпочтительно от приблизительно 1 до приблизительно 200 или 250 мг в сутки; более предпочтительно от приблизительно 1 до приблизительно 75 или 100 мг в сутки; типично от приблизительно 1 до приблизительно 50 или 60 мг в сутки. Конкретная доза и диапазон дозы,которые могут быть использованы, зависят от множества факторов, включая возраст и массу пациента,путь введения, тяжесть заболевания, состояния и/или расстройства, которые лечат, и фармакологическую активность вводимого соединения. Определение диапазонов доз и оптимальных доз для конкретного пациента находятся в объеме знаний специалиста в данной области техники. Соединения по этому изобретению могут быть использованы в комбинациях с другими фармацевтическими агентами (иногда названными здесь как "комбинация") для лечения упомянутых здесь заболеваний, состояний и/или расстройств или сопутствующих им заболеваний. Поэтому в настоящем изобретении также предложены способы лечения, включающие введение соединений по настоящему изобретению в комбинации с другими фармацевтическими агентами. Подходящие фармацевтические агенты, которые могут быть использованы в комбинированном аспекте настоящего изобретения, включают средства против ожирения, такие как антагонисты каннабиноидного рецептора-1 (СВ-1) (такие, как римонабант), ингибиторы 11-гидроксистероидной дегидрогеназы-1 (11-HSD тип 1), агонисты пептида YY (PYY) и PYY (такие, как PYY3-36), агонисты рецептора меланокортина-4 (MCR-4), ингибиторы обратного захвата моноамина (такие, как сибутрамин), симпатомиметики, агонисты 3-адренергического рецептора, агонисты дофаминового рецептора (такие, как бромкриптин), аналоги рецептора меланоцит-стимулирующего гормона (такие, как раскрытые в патенте США 6716810), агонисты рецептора 5-гидрокситриптамина 2 с (5 НТ 2 с), антагонисты меланинконцентрирующего гормона, лептин (белок ОВ), агонисты лептинового рецептора, галаниновые антагонисты, ингибиторы липазы (такие, как тетрагидролипстатин, т.е. орлистат), агонисты бомбезинового рецептора,антагонисты рецептора нейропептида-Y (NPY) (например, антагонисты рецептора NPY Y5), тиреомиметики, дегидроэпиандростерон, агонисты или антагонисты глюкокортикоидного рецептора, антагонисты орексинового рецептора, агонисты рецептора глюкагон-подобного пептида-1, цилиарные нейротрофические факторы (такие, как Axokine, поставляемый Regeneron Pharmaceuticals, Inc., Tarrytown, NY andProcterGamble Company, Cincinnati, ОН), антагонисты человеческого агутисвязанного белка (AGRP),антагонисты грелинового рецептора, антагонисты или обратные агонисты гистаминового рецептора 3,- 20010888 агонисты рецептора нейромедина U, ингибиторы секреции МТР/АроВ, блокаторы кальциевых Т-каналов(такие, как зонизамид), антагонисты опиоидного рецептора (такие, как обсуждаемые в РСТ публикациях заявок на патентыWO 03/101963 и WO 2004/026305) и т.п. Предпочтительные антагонисты рецептора NPY включают антагонисты рецептора NPY Y5, такие как спиросоединения, раскрытые в патентах США 6566367; 6649624; 6638942; 6605720; 6495559; 6462053; 6388077; 6335345 и 6326375; публикациях заявок на патенты США 2002/0151456 и 2003/036652 и РСТ публикациях заявок на патентыWO 03/010175; WO 03/082190 и WO 02/048152. Все из цитированных выше источников включены здесь путем ссылки. Предпочтительные средства против ожирения включают орлистат (патенты США 5274143; 5420305; 5540917 и 5643874), сибутрамин (патент США 4929629), бромкриптин (патенты США 3752814 и 3752888), эфедрин, лептин, псевдоэфедрин, зонизамид (патент США 4172896) и пептидYY3-36, или его аналог, или производное (публикация заявки на патент США 2002/0141985 и РСТ публикация заявки на патентWO 03/026591). Все из цитированных выше источников включены здесь путем ссылки. Соединения по этому изобретению также могут быть использованы в комбинации с другими фармацевтическими агентами (например, агентами, снижающими уровень холестерина липопротеидов низкой плотности (ЛПНП-холестерина), агентами, снижающими уровень триглицеридов) для лечения упомянутых здесь заболеваний/состояний. Например, настоящие соединения могут быть использованы в комбинации с ингибитором 3-гидрокси-3-метилглютарил-коэнзим A (HMG-CoA) редуктазы (таким, как аторвастатин, симвастатин, флувастатин, правастатин, церивастатин, розувастатин или питавастатин),ингибитором HMG-CoA синтазы, ингибитором экспрессии гена HMG-CoA редуктазы, ингибитором сквален-синтетазы/эпоксидазы/циклазы, ингибитором синтеза холестерина, ингибитором абсорбции холестерина (таким, как эзетимиб), ингибитором белка-переносчика эфиров холестерина (СЕТР) (таким,как торцетрапиб), модулятором рецептора, активируемого пероксисомальным пролифератором (PPAR),или другим агентом, снижающим уровень холестерина, таким как фибрат, ниацином, ионообменной смолой, антиоксидантом, ингибитором ацил-коэнзим А холестерин ацилтрансферазы (АСАТ) (таким, как авазимиб, CS-505 (Sankyo) и эфлуцимиб) или агентом, усиливающим секрецию желчных кислот. Другие фармацевтические агенты, полезные на практике в комбинированном аспекте изобретения, включают ингибиторы обратного захвата желчных кислот, ингибиторы илеального транспортера желчных кислот,ингибиторы АСС, антигипертензивные агенты (такие, как Norvasc), антибиотики, антидиабетические средства (такие, как метформин, фенформин или буформин), активаторы PPAR, агенты, увеличивающие секрецию инсулина (такие, как сульфонилмочевины и глиниды), инсулин, ингибиторы альдозоредуктазы(ARI) (например, зополрестат), ингибиторы сорбитолдегидрогеназы (SDI) и противовоспалительные агенты, такие как аспирин или, предпочтительно, противовоспалительный агент, который ингибирует циклооксигеназу-2 (Сох-2) в большей степени, чем циклооксигеназу-1 (Сох-1), такой как целекоксибRN 202409-33-4) или люмиракокосиб (CAS RN 220991-20-8). Соединения по настоящему изобретению также могут быть введены в комбинации с встречающимися в природе веществами для уменьшения уровней холестерина плазмы. Эти встречающиеся в природе вещества обычно называют "нутрицевтиками" (nutraceutical), и они включают, например, чесночный экстракт, экстракты растения Hoodia и ниацин. Форма ниацина с замедленным высобождением имеется в продаже под торговым названием Niaspan. Niacin также может быть объединен с другими терапевтическими агентами, такими как ловастатин, который представляет собой ингибитор HMG-СоА редуктазы. Это комбинированная терапия известна как Advicor (Kos Pharmaceuticals Inc.). Соединения формулы (I) по настоящему изобретению также могут быть использованы в комбинации с антигипертензивными агентами. Предпочтительные антигипертензивные агенты включают блокаторы кальциевых каналов, такие как Cardizem, Adalat, Calan, Cardene, Covera, Dilacor, DynaCirc, Procardia XL, Sular, Tiazac, Vascor, Verelan, Isoptin, Nimotop, Norvasc, и Plendil; ингибиторы ангиотензин-превращающего фермента (АСЕ), такие как Accupril, Altace, Captopril,Lotensin, Mavik, Monopril, Prinivil, Univasc, Vasotec и Zestril. Диабеты (в особенности II типа), инсулинорезистентность, нарушение толерантности к глюкозе или тому подобное можно лечить путем введения терапевтически эффективного количества соединения формулы (I), предпочтительно в комбинации с одним или более чем одним агентом (например, инсулином), полезным в лечении диабетов. В качестве второго агента в комбинации с соединением формулы (I) по настоящему изобретению может быть использован любой ингибитор гликогенфосфорилазы. Термин ингибитор гликогенфосфорилазы относится к соединениям, которые ингибируют биопревращение гликогена в глюкозо-1-фосфат,катализируемое ферментом гликогенфосфорилазой. Такая активность ингибирования гликогенфосфорилазы легко определяется при помощи стандартных анализов, хорошо известных в области техники (например, J. Med. Chem. 41 (1998), 2934-2938). Ингибиторы гликогенфосфорилазы, представляющие здесь- 21010888 интерес, включают ингибиторы, раскрытые в РСТ публикациях заявок на патенты WO 96/39384 и WO 96/39385. Цитированные выше источники включены здесь путем ссылки. Ингибиторы альдозоредуктазы также могут быть полезными на практике в комбинированном аспекте настоящего изобретения. Эти соединения ингибируют биопревращение глюкозы в сорбит, катализируемое ферментом альдозоредуктазой. Ингибирование альдозоредуктазы легко определяется при помощи стандартных анализов (например, J. Malone, Diabetes, 29:861-864 (1980) "Red Cell Sorbitol, an Indicator of Diabetic Control", источник включен здесь путем ссылки). Множество ингибиторов альдозоредуктазы известно специалистам в данной области техники. Цитированные выше источники включены здесь путем ссылки. В комбинации с соединением формулы (I) по настоящему изобретению может быть использован любой ингибитор сорбитолдегидрогеназы. Термин ингибитор сорбитолдегидрогеназы относится к соединениям, которые ингибируют биопревращение сорбита во фруктозу, катализируемое ферментом сорбитолдегидрогеназой. Такая активность ингибирования сорбитолдегидрогеназы легко определяется с использованием стандартных анализов, известных в области техники (например, Analyt. Biochem (2000) 280: 329-331). Ингибиторы сорбитолдегидрогеназы, представляющие интерес, включают ингибиторы,раскрытые в патенте США 5728704 и 5866578. Цитированные выше источники включены здесь путем ссылки. В комбинированном аспекте настоящего изобретения может быть использован любой ингибитор глюкозидазы. Такие соединения ингибируют ферментативный гидролиз сложных углеводов гликозидгидралазами, такими как амилаза или мальтаза, в биодоступные простые сахара, например глюкозу. Быстрое метаболическое действие глюкозидаз, в особенности после потребления высоких уровней углеводов, приводит в результате к состоянию алиментарной гипергликемии, которая у тучных субъектов или диабетиков приводит к усиленной секреции инсулина, увеличенному синтезу жиров и уменьшению разрушения жира. После таких гипергликемий часто возникает гипогликемия вследствие присутствия увеличенных уровней инсулина. Кроме того, известно, что химус, оставшийся в желудке, способствует продукции желудочного сока, который инициирует или благоприятствует развитию гастрита или язв двенадцатиперстной кишки. Соответственно, известно, что ингибиторы гликозидазы являются полезными в ускорении прохождения углеводов через желудок и ингибировании абсорбции глюкозы из кишечника. Кроме того, превращение углеводов в липиды жировой ткани и последующее включение пищевого жира в отложения жировой ткани соответственно уменьшается или замедляется, наряду с сопутствующей выгодой от уменьшения или профилактики возникающих в результате вредных аномалий. Такая активность ингибирования глюкозидазы легко определяется специалистом в данной области техники в соответствии со стандартными анализами (например, Biochemistry (1969) 8: 4214, источник включен здесь путем ссылки). Типичный предпочтительный ингибитор глюкозидазы включает ингибитор амилазы. Ингибитор амилазы представляет собой ингибитор глюкозидазы, ингибирующий ферментативное разрушение крахмала или гликогена в мальтозу. Такая активность ингибирования амилазы легко определяется с использованием стандартных анализов (например, Methods Enzymol. (1955) 1: 149, источник включен здесь путем ссылки). Выгода от ингибирования такого ферментативного разрушения заключается в уменьшении количеств биодоступных сахаров, включая глюкозу и мальтозу, и сопутствующих вредных состояний, возникающих от них. Предпочтительные ингибиторы глюкозидазы включают акарбозу, адипозин, воглибозу, миглитол,эмиглитат, камиглибозу, тендамистат, трестатин, прадимицин-Q и сальбостатин. Ингибитор глюкозидазы акарбоза и различные производные аминосахаров, родственные ей, раскрыты в патентах США 4062950 и 4174439 соответственно. Ингибитор глюкозидазы адипозин раскрыт в патенте США 4254256. Ингибитор глюкозидазы воглибоза, 3,4-дидезокси-4-2-гидрокси-1-(гидроксиметил)этил]амино]-2-С-(гидроксиметил)-D-эпиинозит, и различные N-замещенные псевдоаминосахара, родственные ей, раскрыты в патенте США 4701559. Ингибитор глюкозидазы миглитол, (2R,3R,4R,5S)-1-(2 гидроксиэтил)-2-(гидроксиметил)-3,4,5-пиперидинтриол, и различные 3,4,5-тригидроксипиперидины,родственные ему, раскрыты в патенте США 4639436. Ингибитор глюкозидазы эмиглитат, этил-пара[2-[(2R,3R,4R,5S)-3,4,5-тригидрокси-2-(гидроксиметил)пиперидин]этокси]бензоат, различные производные, родственные ему, и его фармацевтически приемлемые соли присоединения кислоты раскрыты в патенте США 5192772. Ингибитор глюкозидазы MDL-25637, 2,6-дидезокси-7-OD-глюкопиранозил 2,6-имино-D-глицеро-L-глюкогептит, различные гомодисахариды, родственные ему, и его фармацевтически приемлемые соли присоединения кислоты раскрыты в патенте США 4634765. Ингибитор глюкозидазы камиглибоза,сесквигидрат метил-6-дезокси-6-[(2R,3R,4R,5S)-3,4,5-тригидрокси-2(гидроксиметил)пиперидин]D-глюкопиранозида, производные дезоксинойиримицина, родственные ей, ее различные фармацевтически приемлемые соли и синтетические способы ее получения раскрыты в патентах США 5157116 и 5504078. Ингибитор глюкозидазы сальбостатин и различные псевдосахариды, родственные ему, раскрыты в патенте США 5091524. Все цитированные выше источники включены здесь путем ссылки.- 22010888 Представляющие интерес ингибиторы амилазы раскрыты в патенте США 4451455, патенте США 4623714 (AI-3688 и различные циклические полипептиды, родственные ему) и патенте США 4273765 (трестатин, состоящий из смеси трестатина А, трестатина В и трестатина С, и различные трегалозосодержащие аминосахара, родственные ему). Все цитированные выше источники включены здесь путем ссылки. Доза дополнительного фармацевтического агента обычно зависит от множества факторов, включая состояние здоровья субъекта, которого лечат, желаемую длительность лечения, природу и тип сопутствующего лечения, если оно имеет место, и частоту лечения и природу желаемого действия. Как правило,диапазон доз дополнительного фармацевтического агента составляет от приблизительно 0,001 до приблизительно 100 мг на килограмм массы тела субъекта в сутки, предпочтительно от приблизительно 0,1 до приблизительно 10 мг на килограмм массы тела субъекта в сутки. Однако в зависимости от возраста и массы субъекта, которого лечат, планируемого пути введения, конкретного вводимого средства против ожирения и тому подобного также может потребоваться некоторое изменение общего диапазона доз. Определение диапазонов доз и оптимальных доз для конкретного пациента также находится в объеме знаний специалиста в данной области техники, получающего выгоду от настоящего описания. В соответствии со способами лечения по изобретению соединение по настоящему изобретению или комбинацию вводят субъекту, нуждающемуся в таком лечении, предпочтительно в форме фармацевтической композиции. В комбинированном аспекте изобретения соединение по настоящему изобретению и другой(ие) фармацевтический(ие) агент(ы) могут быть введены или раздельно, или в фармацевтической композиции, содержащей оба из них. Обычно является предпочтительным, чтобы такое введение было пероральным. Если комбинацию соединения по настоящему изобретению и по меньшей мере одного другого фармацевтического агента вводят вместе, то такое введение может быть последовательным по времени или одновременным. Одновременное введение комбинаций лекарств обычно является предпочтительным. При последовательном введении соединение по настоящему изобретению и дополнительный фармацевтический агент могут быть введены в любом порядке. Обычно является предпочтительным, чтобы такое введение было пероральным. Особенно предпочтительно, чтобы такое введение было пероральным и одновременным. Если соединение по настоящему изобретению и дополнительный фармацевтический агент вводят последовательно, то введение каждого из них может быть осуществлено при помощи одного и того же или различных способов. Соответственно, соединение по настоящему изобретению или комбинация могут быть введены пациенту раздельно или вместе в любой общепринятой лекарственной форме для перорального, ректального, трансдермального, парентерального (например, внутривенного, внутримышечного или подкожного),интрацистернального, интравагинального, внутрибрюшинного, местного (например, в форме порошка,мази, крема, спрея или лосьона), трансбуккального или назального (например, в форме спрея, капель или ингалируемой форме) введения. Соединения по изобретению или комбинации обычно вводят в смеси с одним или более чем одним подходящим фармацевтическим эксципиентом, разбавителем или носителем, известным в области техники и выбранным в соответствии с планируемым путем введения и стандартной фармацевтической практикой. Соединение по изобретению или комбинация могут быть приготовлены с предоставлением лекарственной формы с немедленным, замедленным, модифицированным, длительным, импульсным или контролируемым высвобождением в зависимости от желаемого пути введения и специфичности профиля высвобождения, соответствующего терапевтическим потребностям. Фармацевтические композиции содержат соединение по изобретению или комбинацию в количестве, как правило, находящемся в диапазоне от приблизительно 1 до приблизительно 75, 80, 85, 90 или даже 95% (по массе) от массы композиции, обычно в диапазоне от приблизительно 1, 2 или 3 до приблизительно 50, 60 или 70%, чаще в диапазоне от приблизительно 1, 2 или 3 до менее чем 50%, таком как приблизительно 25, 30 или 35%. Способы приготовления различных фармацевтических композиций с определенным количеством активного соединения известны специалистам в данной области техники. Например, см. Remington: ThePractice of Pharmacy, Lippincott Williams and Wilkins, Baltimore MD, 20th ed. 2000. Композиции, подходящие для парентеральной инъекции, обычно включают фармацевтически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии, и стерильные порошки для растворения в стерильных растворах или дисперсиях для инъекции. Примеры подходящих водных и неводных носителей или разбавителей (включая растворители и основу) включают воду, этанол, полиолы (пропиленгликоль, полиэтиленгликоль, глицерин и т.п.), их подходящие смеси, триглицериды, включающие растительные масла, такие как оливковое масло и инъецируемые органические сложные эфиры, такие как этилолеат. Предпочтительный носитель представляет собой Miglyol (торговое название): сложный эфир каприловой/каприновой кислоты с глицерином или пропиленгликолем (например, Miglyol 812, Miglyol 829, Miglyol 840), поставляемый Condea Vista Co., Cranford, NJ. Соответствующую текучесть можно поддерживать, например, путем использования оболочки, такой как ле- 23010888 цитин, путем поддержания требуемого размера частиц в случае дисперсий и путем использования поверхностно-активных веществ. Эти композиции для парентеральной инъекции также могут содержать эксципиенты, такие как консерванты, увлажнители, эмульгаторы и диспергирующие агенты. Предотвращения загрязнения композиций микроорганизмами можно достигнуть при помощи различных антибактериальных и противогрибковых агентов, например парабенов, хлорбутанола, фенола, сорбиновой кислоты и тому подобного. Также может быть желательным включение изотонических агентов, например сахаров, хлорида натрия и тому подобного. К пролонгированной абсорбции инъецируемых фармацевтических композиций может привести использование агентов, способных замедлять абсорбцию, например, моностеарата алюминия и желатина. Твердые лекарственные формы для перорального введения включают капсулы, таблетки, жевательные резинки, лепешки, пилюли, порошки и препараты в виде множества частиц (гранул). В таких твердых лекарственных формах соединение по настоящему изобретению или комбинацию смешивают по меньшей мере с одним инертным эксципиентом, разбавителем или носителем. Подходящие эксципиенты, разбавители или носители включают такие материалы, как цитрат натрия или дикальция фосфат,и/или (а) заполнители или наполнители (например, микрокристаллическую целлюлозу (доступную какAvicel от FMC Corp.), крахмалы, лактозу, сахарозу, маннит, кремниевую кислоту, ксилит, сорбит, декстрозу, гидрофосфат кальция, декстрин, альфа-циклодекстрин, бета-циклодекстрин, полиэтиленгликоль,среднецепочечные жирные кислоты, оксид титана, оксид магния, оксид алюминия и т.п.); (б) связывающие вещества (например, карбоксиметилцеллюлозу, метилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, желатин, гуммиарабик, этилцеллюлозу, поливиниловый спирт, пуллулан,прежелатинизированный крахмал, агар, трагакант, альгинаты, желатин, поливинилпирролидон, сахарозу,акацию и т.п.); (в) увлажнители (например, глицерин и т.п.); (г) разрыхлители (например, агар-агар, карбонат кальция, картофельный крахмал или крахмал тапиоки, альгиновую кислоту, некоторые сложные силикаты, карбонат натрия, лаурилсульфат натрия, натрия крахмал гликолят (поставляемый какExplotab от Edward Mendell Co.), поперечно-сшитый поливинилпирролидон, натриевую кроскармеллозу А-типа (поставляемую как Ac-di-sol), калиевый полиакрилин (ионообменную смолу) и тому подобное; (д) замедлители растворения (например, парафин и т.п.); (е) ускорители абсорбции (например, соединения четвертичного аммония и т.п.); (ж) смачивающие вещества (например, цетиловый спирт, глицеринмоностеарат и т.п.); (з) адсорбенты (например, каолин, бентонит и т.п.) и/или (и) смазывающие вещества (например, тальк, стеарат кальция, стеарат магния, стеариновую кислоту, полиоксилстеарат(polyoxyl stearate), цетанол, тальк, гидрированное касторовое масло, сахарозные эфиры жирной кислоты,диметилполисилоксан, микрокристаллический воск, желтый пчелиный воск, белый пчелиный воск, твердые полиэтиленгликоли, лаурилсульфат натрия и т.п.). В случае капсул и таблеток лекарственные формы также могут содержать буферные агенты. Твердые композиции похожего типа также можно применять в качестве наполнителей в мягких или твердых желатиновых капсулах с использованием таких эксципиентов, разбавителей или носителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п. Твердые лекарственные формы, такие как таблетки, драже, капсулы и гранулы могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие, хорошо известные в области техники. Они также могут содержать светонепроницаемые агенты, а также могут представлять собой такую композицию, которая высвобождает соединение по настоящему изобретению и/или дополнительный фармацевтический агент замедленным образом. Примерами инкапсулирующих композиций, которые могут быть использованы, являются полимерные вещества и воски. Также лекарство может находиться в микроинкапсулированной форме, если это целесообразно, с одним или более чем одним из упомянутых выше эксципиентов, разбавителей или носителей. Для таблеток активный агент обычно составляет меньше чем 50% (по массе) препарата, например меньше чем приблизительно 10%, например 5% или 2,5% по массе. Преобладающая часть препарата включает эксципиенты, разбавители или носители, такие как наполнители, разрыхлители, смазывающие вещества и возможно корригенты. Композиция этих эксципиентов хорошо известна в области техники. Часто наполнители/разбавители включают смеси двух или более чем двух из следующих компонентов: микрокристаллическую целлюлозу, маннит, лактозу (любую/все типы), крахмал и дикальция фосфат. Смеси эксципиента, разбавителя или носителя обычно составляют меньше чем приблизительно 98% от препарата и предпочтительно меньше чем приблизительно 95%, например приблизительно 93,5%. Предпочтительные разрыхлители включают Ac-di-sol, Explotab, крахмал и лаурилсульфат натрия. Если присутствует разрыхлитель, то он обычно составляет меньше чем приблизительно 10% от препарата или меньше чем приблизительно 5%, например, приблизительно 3%. Если присутствует смазывающее вещество, то оно обычно составляет меньше чем приблизительно 5% от препарата или меньше чем приблизительно 3%, например приблизительно 1%. Предпочтительное смазывающее вещество представляет собой стеарат магния. Таблетки могут быть приготовлены при помощи стандартных способов таблетирования, например- 24010888 прямого прессования или влажного, сухого гранулирования или гранулирования из расплава, способа затвердевания расплава и экструзии. Ядра таблеток могут быть моно- или многослойными и могут быть покрыты соответствующими оболочками, известными в области техники. Жидкие лекарственные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры. Кроме соединения по настоящему изобретению или комбинации жидкая лекарственная форма может содержать инертные эксципиенты, разбавители или носители, обычно используемые в области техники, такие как воду или другие растворители, солюбилизаторы и эмульгаторы, например этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (например, хлопковое масло, арахисовое масло, масло из зародышей кукурузы, оливковое масло, касторовое масло, кунжутное масло и т.п.), Miglyol (поставляемый CONDEA Vista Co., Cranford, NJ.), глицерин,тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры сорбита и жирных кислот или смеси этих веществ и т.п. Помимо таких инертных эксципиентов, разбавителей или носителей композиция также может включать смачивающие вещества, эмульгаторы и/или суспендирующие агенты и подсластители, корригенты и/или ароматизирующие добавки. Жидкие формы соединений по изобретению для перорального введения или комбинации включают растворы, в которых активное соединение полностью растворено. Примеры растворителей включают все фармацевтически признанные растворители, подходящие для перорального введения, в частности, растворители, в которых соединения по изобретению демонстрируют хорошую растворимость, например,полиэтиленгликоль, полипропиленгликоль, пищевые масла и глицерильные и глицеридные системы. Глицерильные и глицеридные системы могут включать, например, следующие марочные товары (и соответствующие немарочные товары): Captex 355 ЕР (глицерилтрикаприлат/капрат, от Abitec, Columbus ОН), Crodamol GTC/C (среднецепочечный триглицерид, от Croda, Cowick Hall, UK) или Labrafac CCMaisine 35-1 (глицерилмоноолеат, от Gattefosse). Особенный интерес представляют среднецепочечные(приблизительно C8-C10) триглицеридные масла. Эти растворители часто составляют преобладающую часть композиции, т.е. больше чем приблизительно 50%, обычно больше чем приблизительно 80%, например приблизительно 95, 97 или 99%. Другие эксципиенты, разбавители или носители могут быть также включены с растворителями, в основном в качестве агентов, маскирующих вкус, вкусовых агентов и корригентов, антиоксидантов, стабилизаторов, модификаторов плотности и вязкости, солюбилизаторов и т.п. Кроме соединения по настоящему изобретению или комбинации суспензии дополнительно могут содержать эксципиенты, разбавители или носители, такие как суспендирующие агенты, например, этоксилированные изостеариловые спирты, полиоксиэтиленсорбит и сложные эфиры сорбита, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант или смеси этих веществ и т.п. Композиции для ректального или вагинального введения предпочтительно содержат суппозитории,которые могут быть приготовлены путем смешивания соединения по настоящему изобретению или комбинации с подходящими не вызывающими раздражения эксципиентами, разбавителями или носителями,такими как масло какао, полиэтиленгликоль или воск суппозиториев, которые являются твердыми при обычной комнатной температуре, но жидкими при температуре тела, и, таким образом, плавятся в прямой кишке или вагинальной полости, тем самым высвобождая активный(е) компонент(ы). Лекарственные формы для местного введения соединений по настоящему изобретению или комбинаций включают мази, кремы, лосьоны, порошки и спреи. Лекарства смешивают с фармацевтически приемлемым эксципиентом, разбавителем или носителем и любыми консервантами, буферными агентами или пропеллентами, которые могут потребоваться или могут быть желательны. Для любого из настоящих соединений, которое плохо растворимо в воде, например, меньше чем приблизительно 1 мкг/мл, жидкие композиции в солюбилизирующих неводных растворителях, таких как среднецепочечные триглицеридные масла, обсуждавшиеся выше, представляют собой предпочтительные лекарственные формы. Твердые аморфные дисперсии, включая дисперсии, образуемые при помощи сушки распылением, также представляют собой предпочтительную лекарственную форму для плохо растворимых соединений по изобретению. Под "твердой аморфной дисперсией" подразумевают твердый материал, в котором по меньшей мере часть плохорастворимого соединения находится в аморфной форме и диспергирована в водорастворимом полимере. Под "аморфным" подразумевают, что плохораствормое соединение не является кристаллическим. Под "кристаллическим" подразумевают, что соединение демонстрирует дальний порядок в трех измерениях из по меньшей мере 100 повторяющихся единиц в- 25010888 каждом измерении. Таким образом, предполагается, что термин аморфный включает не только вещество,которое, по существу, не имеет порядка, а также вещество, которое может иметь некоторую небольшую степень порядка, при этом порядок меньше чем в трех измерениях и/или только на короткие расстояния. Аморфное вещество может быть охарактеризовано при помощи методик, известных в области техники,такими как дифракция рентгеновских лучей на порошке (ДРЛП), кристаллография, твердотельный ядерный магнитный резонанс (ЯМР) или термическими способами, такими как дифференциальная сканирующая калориметрия (ДСК). Предпочтительно, по меньшей мере основная часть (т.е. по меньшей мере приблизительно 60 мас.%) плохорастворимого соединения в твердой аморфной дисперсии является аморфным. Соединение может находиться в твердой аморфной дисперсии в относительно чистых аморфных доменах или областях, в виде твердого раствора соединения, гомогенно распределенного в полимере, или любой комбинации этих состояний или тех состояний, которые находятся между ними. Предпочтительно, твердая аморфная дисперсия является по существу гомогенной, так что аморфное соединение по возможности гомогенно диспергировано в полимере. Используемый здесь термин "по существу гомогенный" означает,что часть соединения, которая присутствует в относительно чистых аморфных доменах или областях в твердой аморфной дисперсии, относительно небольшая, имеет порядок меньше чем приблизительно 20 мас.%; предпочтительно меньше чем приблизительно 10 мас.% от общего количества лекарства. Водорастворимые полимеры, подходящие для применения в твердых аморфных дисперсиях, должны быть инертными с той точки зрения, что они не вступают в химическую реакцию с плохорастворимым соединением неблагоприятным образом, являются фармацевтически приемлемыми и обладают, по меньшей мере, некоторой растворимостью в водном растворе при физиологически значимых pH (например, 1-8). Полимер может быть нейтральным или ионизируемым и должен обладать растворимостью в воде по меньшей мере 0,1 мг/мл в по меньшей мере части диапазона pH 1-8. Водорастворимые полимеры, подходящие для применения в настоящем изобретении, могут быть целлюлозными или нецеллюлозными. Полимеры могут быть нейтральными или ионизируемыми в водном растворе. Из них предпочтительными являются ионизируемые и целлюлозные полимеры, причем ионизируемые целлюлозные полимеры являются более предпочтительными. Типичные водорастворимые полимеры включают сукцинат ацетат гидроксипропилметилцеллюлозы (HPMCAS), гидроксипропилметилцеллюлозу (НРМС), фталат гидроксипропилметилцеллюлозы(НРМСР), карбоксиметилэтилцеллюлозу (СМЕС), фталат ацетат целлюлозы (САР), тримеллитат ацетат целлюлозы (CAT), поливинилпирролидон (PVP), гидроксипропилцеллюлозу (НРС), метилцеллюлозу(МС), блок-сополимеры этиленоксида и пропиленоксида (РЕО/РРО, также известные как полоксамеры),и их смеси. Особенно предпочтительные полимеры включают HPMCAS, НРМС, НРМСР, СМЕС, CAP,CAT, PVP, полоксамеры и их смеси. Наиболее предпочтителен HPMCAS. Смотри публикацию европейской заявки на патент 0901786 А 2, описание которой включено здесь путем ссылки. Твердые аморфные дисперсии могут быть получены любым из способов получения твердых аморфных дисперсий, которые приводят в результате к по меньшей мере основной части (по меньшей мере 60%) плохорастворимого соединения в аморфном состоянии. Такие способы включают механические, термические способы и способы растворения. Типичные механические способы включают измельчение и экструзию; способы плавления включают высокотемпературное плавление, модифицированное растворителем плавление и способы затвердевания расплава; а способы растворения включают осаждение при помощи осадителя, покрытие распылением и сушку распылением. См., например, следующие патенты США, подходящие описания которых включены здесь путем ссылки 5456923 и 5939099, описывающие дисперсии, образующиеся способами экструзии;5340591 и 4673564, описывающие дисперсии, образующиеся способами измельчения; и 5707646 и 4894235, описывающие дисперсии, образующиеся при помощи затвердевания расплава. В предпочтительном способе твердая аморфная дисперсия образуется путем сушки распылением, как раскрыто в публикации европейской заявки на патент 0901786 А 2. В этом способе соединение и полимер растворяют в растворителе, таком как ацетон или метанол, а затем растворитель быстро удаляют из раствора путем сушки распылением с образованием твердой аморфной дисперсии. Могут быть получены твердые аморфные дисперсии, содержащие до 99 мас.% соединения, например 1, 5, 10, 25, 50, 75, 95 или 98 мас.% в соответствии с желаемым. Твердая дисперсия может быть использована в виде самой лекарственной формы или может служить в качестве продукта, используемого при получении (manufacturing-use-product) (ПИП) других лекарственных форм, таких как капсулы, таблетки, растворы или суспензии. Пример водной суспензии представляет собой водную суспензию высушенной распылением дисперсии соединение/HPMCAS-HF(1:1, мас./мас.), содержащую 2,5 мг/мл соединения в 2% полисорбате-80. Твердые дисперсии для применения в таблетке или капсуле обычно смешаны с другими эксципиентами или адъювантами, как правило,обнаруживаемыми в таких лекарственных формах. Например, типичный наполнитель для капсул содержит высушенную распылением дисперсию соединение/HPMCAS-HF (2:1, мас./мас.) (60%), лактозу ("fastAqoat-HF соответственно, от Shin-Etsu Chemical Co., LTD, Tokyo, Japan. Обычно предпочтительными являются полимеры более высокого качества MF и HF. Для применения фармацевтическая композиция может быть упакована множеством путей, зависящих от способа, используемого для введения лекарства. Как правило, распространяемое средство включает контейнер, содержащий фармацевтический препарат в подходящей форме. Подходящие контейнеры хорошо известны специалистам в данной области техники и включают такие материалы, как бутыли(пластиковые и стеклянные), саше, ампулы, полиэтиленовые пакеты, металлические цилиндры и т.п. Контейнер также может включать защитное устройство для предотвращения неосторожного доступа к содержимому упаковки. Кроме того, контейнер содержит наклеенную этикетку, которая описывает содержимое контейнера. Этикетка также может включать соответствующие предупреждения. Применение в ветеринарии. В следующих абзацах описаны примеры препаратов, доз и т.д., полезные для животных, не являющихся человеком. Введение соединений по настоящему изобретению и комбинаций соединений по настоящему изобретению со средствами против ожирения может быть осуществлено перорально или не перорально. Соединение по настоящему изобретению или комбинацию соединения по настоящему изобретению со средством против ожирения вводят в таком количестве, чтобы достичь эффективной дозы. Обычно суточная доза, которую перорально вводят животному, составляет между приблизительно 0,01 и приблизительно 1000 мг/кг массы тела, например между приблизительно 0,01 и приблизительно 300 мг/кг, или между приблизительно 0,01 и приблизительно 100 мг/кг, или между приблизительно 0,01 и приблизительно 50 мг/кг, или между приблизительно 0,01 и приблизительно 25 мг/кг, или между приблизительно 0,01 и приблизительно 10 мг/кг, или между приблизительно 0,01 и приблизительно 5 мг/кг массы тела. Соединение по настоящему изобретению (или комбинация) может быть легко приготовлено в питьевой воде так, что терапевтическая доза соединения проглатывается вместе с суточным потреблением воды. Соединение может быть отмерено непосредственно в питьевую воду, предпочтительно в форме жидкости, водорастворимого концентрата (такого, как водный раствор водорастворимой соли). Соединение по настоящему изобретению (или комбинация) также может быть легко добавлено непосредственно в корм: как таковые, или в форме добавки в корм для животного, также называемой как предварительно приготовленная смесь или концентрат. Предварительно приготовленную смесь или концентрат соединения в эксципиенте, разбавителе или носителе обычно используют для включения в корм агента. Подходящие эксципиенты, разбавители или носители являются жидкими или твердыми, в соответствии с желаемым, такими как вода, различные виды муки, такие как мука из люцерны, соевая мука,жмых от переработки хлопковых семян, мука из жмыха льняного семени, мука из сердцевины кукурузного початка и кукурузная мука, меласса, мочевина, костная мука и минеральные смеси, такие как обычно используемые для кормления домашних птиц. Особенно эффективный эксципиент, разбавитель или носитель представляет собой сам соответствующий корм для животного; т.е. небольшую часть такого корма. Носитель облегчает равномерное распределение соединения в конечном корме, с которым смешивают предварительно приготовленную смесь. Предпочтительно, соединение тщательно смешивают с предварительно приготовленной смесью, а затем кормом. В этой связи соединение может быть диспергировано или растворено в подходящей масляной основе, такой как соевое масло, кукурузное масло,хлопковое масло и тому подобном, или в летучем органическом растворителе, и затем смешано с носителем. Понятно, что доли соединения в концентрате могут широко варьироваться, так как количество соединения в конечном корме может быть установлено путем смешивания соответствующей части предварительно приготовленной смеси с кормом с получением желаемого уровня соединения. Высокоэффективные концентраты могут быть смешаны производителем корма с белковым носителем, таким как соевый шрот и другие виды муки, как описано выше, для приготовления концентрированных добавок, которые подходят для непосредственного питания животного. В таких случаях животным дают возможность потреблять обычную диету. Альтернативно, такие концентрированные добавки могут быть добавлены непосредственно в корм для получения сбалансированного по питательности конечного корма, содержащего терапевтически эффективный уровень соединения по настоящему изобретению. Смеси тщательно смешивают при помощи стандартных способов, таких как смешивание в смесителе с двойным корпусом для обеспечения гомогенности. Если добавку используют в качестве верхнего слоя корма, то это также помогает обеспечивать равномерность распределения соединения через верх покрытого корма. Питьевую воду и корм, эффективный для увеличения отложения нежирного мяса и для улучшения отношения нежирного мяса к жирному, обычно готовят путем смешиваниясоединения по настоящему изобретению с достаточным количеством корма для животного с получением приблизительно от 10-3 до 500 млн-1 соединения в корме или воде. Предпочтительный лечебный корм для свиней, крупного рогатого скота, овец и коз обычно содержит от приблизительно 1 до приблизительно 400 г соединения по настоящему изобретению (или комби- 27010888 нации) на тонну корма, оптимальное количество для этих животных обычно составляет от приблизительно 50 до приблизительно 300 г на тонну корма. Предпочтительные корма для домашних птиц и комнатных животных обычно содержат от приблизительно 1 до приблизительно 400 г, предпочтительно от приблизительно 10 до приблизительно 400 г соединения по настоящему изобретению (или комбинации) на тонну корма. Соединения по настоящему изобретению могут быть введены животному парентерально. Для парентерального введения полезны гранулы или стандартные инъецируемые растворы или суспензии. Обычно парентеральное введение включает инъекцию достаточного количества соединения по настоящему изобретению (или комбинации) с получением животным от приблизительно 0,01 до приблизительно 20 мг лекарства/кг массы тела/сутки. Предпочтительная доза для домашних птиц, свиней, крупного рогатого скота, овец, коз и комнатных животных находится в диапазоне от приблизительно 0,05 до приблизительно 10 мг лекарства/кг массы тела/сутки. Соединения по настоящему изобретению (или комбинация) могут быть получены в форме гранулы и введены в виде имплантата, обычно под кожу головы или уха животного, для которого добиваются увеличения отложения нежирного мяса и улучшения отношения нежирного мяса к жирному. Гранулы, содержащие эффективное количество соединения по настоящему изобретению, фармацевтическую композицию или комбинацию, могут быть получены путем смешивания соединения по настоящему изобретению или комбинации с разбавителем, таким как карбовакс, карнаубский воск и тому подобным, и для улучшения процесса гранулирования может быть добавлено смазывающее вещество,такое как стеарат магния или кальция. Безусловно, понятно, что более чем одна гранула может быть введена животному для достижения желательного уровня дозы, обеспечивающего увеличение отложения нежирного мяса и улучшение желаемого отношения нежирного мяса к жирному мясу. Кроме того, периодически в течение лечения животного ему можно вводить имплантаты для поддержания соответствующего уровня лекарства в организме животного. Также соединения по настоящему изобретению могут быть введены животным, не являющимся человеком, например животным-спутникам, таким как собаки, кошки и лошади, и животным как источникам пищи, перорально в тех же самых лекарственных формах, какие используют для людей, например таблетках, капсулах, растворах, суспензиях, пастах, порошках и так далее. Препараты в виде паст могут быть получены путем диспергирования лекарства в фармацевтически приемлемом масле, таком как арахисовое масло, кунжутное масло, кукурузное масло и т.п. Настоящее изобретение имеет несколько благоприятных ветеринарных особенностей. Для владельца комнатного животного или ветеринара, который желает усилить худобу и/или уменьшить нежелательный жир у питомца, в настоящем изобретении предложены способы, при помощи которых это можно осуществить. Для тех, кто разводит домашних птиц, коров и свиней, использование способа по настоящему изобретению позволяет получить более худых животных, которые продаются по более высоким ценам в мясной отрасли. Воплощения по настоящему изобретению проиллюстрированы следующими примерами. Тем не менее, специалисту в данной области техники понятно, что воплощения изобретения не ограничены конкретными деталями этих примеров, поскольку известны другие их варианты, или очевидные в свете настоящего описания. Примеры Если не указано иначе, исходные вещества обычно имеются в продаже от таких поставщиков, какPharmaceuticals (London, England), или могут быть получены способами, известными специалистам со средним уровнем знаний в области техники, из легкодоступных веществ. Общие экспериментальные методики Спектры ЯМР регистрировали на Varian Unity 400 (поставляемом Varian Inc., Palo Alto, CA) при комнатной температуре при 400 и 500 МГц 1 Н, соответственно. Химические сдвиги выражены в миллионных доляхотносительно оставшегося растворителя в качестве внутреннего стандарта. Формы пиков обозначены в соответствии со следующим: s, синглет; d, дублет; t, триплет; q, квартет; m, мультиплет; br s, шир. синглет; v br s, очень шир. синглет; br m, шир. мультиплет. В некоторых случаях приведены только типичные пики 1 Н ЯМР. Масс-спектры регистрировали путем прямого анализа потока с использованием положительного и отрицательного режимов сканирования химической ионизации при атмосферном давлении (ХИАД). Для проведения экспериментов использовали масс-спектрометр Waters APcI/MC модель ZMD, оборудованный жидкостной системой Gilson 215. Масс-спектрометрический анализ также осуществляли при помощи градиентного хроматографического разделения для обращенно-фазовой жидкостной хроматографии высокого давления (ЖХВД). Молекулярные массы регистрировали при помощи положительного и отрицательного режимов сканирова- 28010888 ния ионизации распылением электронов (ИРЭ). Для проведения экспериментов использовали массспектрометр Waters/Micromass ESI/MC модель ZMD или LCZ (Waters Corp., Milford, MA), оборудованный жидкостной системой Gilson 215 (Gilson, Inc., Middleton, WI) и HP 1100 DAD (Hewlett Packard). В тех случаях, когда указана интенсивность хлор- или бромсодержащих ионов, это означает, что наблюдали предполагаемое соотношение интенсивностей (приблизительно 3:1 для 35Cl/37Cl-содержащих ионов и 1:1 для 79Br/81Br-содержащих ионов), и приведен лишь ион с меньшей молекулярной массой. Оптические вращения определяли на поляриметре PerkinElmer 241 (поставляемом PerkinElmer Inc.,Wellesley, MA) с использованием натриевой D-линии (=589 нм) при указанной температуре, и они представлены в следующем виде: []Dтемп, концентрация (с=г/100 мл) и растворитель. Колоночную хроматографию осуществляли с использованием или силикагеля Baker (40 мкм, J.T.Baker, Phillipsburg, NJ), или силикагеля 50 (ЕМ Sciences, Gibbstown, NJ) в стеклянных колонках, в колонках Biotage (Biotage, Inc., Charlottesville, USA) или с использованием комбинированной системы флэш-разделения Isco Combiflash Separation System при низком давлении азота. Радиальную хроматографию осуществляли с использованием Chromatotron (Harrison Research). Выбранные методы очистки осуществляли с использованием препаративной жидкостной хроматографии Shimadzu. Хиральные разделения проводили с использованием колонки Chirlapak AD, (S,S)-Whelk-O 1 или Chiralcel OD. Ссылки на "энантиомер 1" или "энантиомер 2" относятся только к последовательности, в которой соединения элюируются из колонки. В следующем ниже рассмотрении были использованы некоторые обычные сокращения и акронимы,включающие AcOH (уксусная кислота), DMAP (4-диметиламинопиридин), ДМФ (диметилформамид),Et2O (диэтиловый эфир), EtOAc (этилацетат), EtOH (этанол), Et3N (триэтиламин), KHMDS (гексаметилдисилазан калия), MeOH (метанол), NaBH(OAc)3 (триацетоксиборгидрид натрия), NaHMDS (гексаметилдисилазан натрия), ТФУ (трифторуксусная кислота), ТГФ (тетрагидрофуран). Пример 1(A). Получение 2-[4-(6-фтор-1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамида. Стадия А. 2-[4-(6-Фтор-1H-индол-3-илметилен)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид. К раствору N-изопропил-N-(6-метоксипиридин-3-ил)-2-(5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетраазабензо[е]азулен-6-ил)ацетамида (получение 11) (150 мг, 0,311 ммоль) и 6-фтор-1H-индол-3 карбальдегида (61 мг, 0,373 ммоль) в толуоле (20 мл) добавляли пиперидин (100 мкл). Реакционный сосуд снабжали ловушкой Дина-Старка, содержащей толуол и 4 молекулярные сита, и нагревали с обратным холодильником в течение 24 ч. Раствор охлаждали до комнатной температуры и разбавляли водой. Водный раствор промывали EtOAc (3) и объединенные органические экстракты сушили (MgSO4),фильтровали и концентрировали. Остаток очищали хроматографией среднего давления, элюируя градиентом растворителя (от 10% EtOAc в гексанах до 100% EtOAc) с получением 158 мг 2-[4-(6-фтор-1Hиндол-3-илметилен)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N(6-метоксипиридин-3-ил)ацетамида. МС 628,3 (М+1), 626,2 (M-1). Стадия Б. (2-[4-(6-Фтор-1H-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид). К раствору 2-[4-(6-фтор-1H-индол-3-илметилен)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамида (158 мг, 0,252 ммоль) в MeOH(20 мл) добавляли формиат аммония (463 мг, 7,34 ммоль) и палладий (10%) на древесном угле (112 мг). Реакционную смесь нагревали с обратным холодильником в течение 24 ч. Суспензию подвергали горячему фильтрованию, ополаскивали 10% MeOH в CH2Cl2 (3) и CH2Cl2 (3). Объединенные органические фильтраты концентрировали и остаток очищали хроматографией среднего давления, элюируя градиентом растворителя (от 2% MeOH в CH2Cl2 до 8% MeOH в CH2Cl2) с получением 110 мг 2-[4-(6-фтор-1Hиндол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6 метоксипиридин-3-ил)ацетамида. Стадия А. 2-[4-(1H-Индол-3-илметилен)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид. В соответствии с методикой, описанной для примера 1 (А), стадия A, N-изопропил-N-(6 метоксипиридин-3-ил)-2-(5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил)ацетамид(получение 11) (293 мг, 0,608 ммоль) конденсировали с 1H-индол-3-карбальдегидом (106 мг, 0,729 ммоль). Очистка хроматографией среднего давления с элюированием градиентом растворителя (от 2%MeOH в CH2Cl2 до 10% MeOH в CH2Cl2) позволила получить 286 мг 2-[4-(1H-индол-3-илметилен)-5 оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3 ил)ацетамида. 1 Н ЯМР (CD3OD)8,25 (s) и 7,90 (s, общий 1 Н), 8,16 (s, 1H), 7,58-7,67 (m, 4H), 7,37-7,53 (m, 6 Н),7,07-7,17 (m, 3H), 6,94 (m, 2 Н), 4,90 (m, 1 Н), 4,55 (m, 1 Н), 4,25 (m, 1 Н), 3,96 (m, 4 Н), 1,10 (m, 6 Н); МС 610,8 (М+1), 608,5 (M-1). Стадия Б. 2-[4-(1 Н-Индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен 6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид. В соответствии с методикой, описанной для примера 1(A), стадия Б, 2-[4-(1 Н-индол-3-илметилен)5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин 3-ил)ацетамид (276 мг, 0,453 ммоль) восстанавливали и очищали хроматографией среднего давления,элюируя градиентом растворителя (от CH2Cl2 до 5% MeOH в CH2Cl2) с получением 86 мг 2-[4-(1Hиндол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6 метоксипиридин-3-ил)ацетамида в виде рацемической смеси. 1 Н ЯМР (CD3OD)8,08 (d, 1H), 7,61 (m, 3H), 7,39-7,53 (m, 6H), 7,25 (d, 1H), 7,12 (m, 2H), 7,00 (m,1H), 6,90 (m, 3H), 4,78 (m, 1H), 4,55 (m, 1H), 4,15 (m, 1H), 3,95 (s, 3H), 3,89 (m, 1H), 3,67-3,80 (m, 2H), 1,01(m, 6H); МС 612,2 (М+1), 610,5 (M-1). Стадия В. (-)2-[4-(1H-Индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид, энантиомер 1. Рацемический продукт со стадии Б, 2-[4-(1 Н-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро 2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамид(217 мг,0,355 ммоль), разделяли на его энантиомеры хроматографией высокого давления с использованием колонки Chiralpak AD (5 см 50 см), элюируя гептаном в EtOH (75:12) со скоростью потока 85 мл/мин, с получением энантиомера 1, имеющего время удерживания 7,04 мин. Энантиомер растворяли в EtOAc, и органический слой промывали водой (1) и рассолом (1). Органический экстракт сушили (MgSO4),фильтровали и концентрировали с получением 85 мг 2-[4-(1H-индол-3-илметил)-5-оксо-1-фенил-4,5 дигидро-2,3,6,10b-тетраазабензо[е]азулен-6-ил]-N-изопропил-N-(6-метоксипиридин-3-ил)ацетамида
МПК / Метки
МПК: C07D 519/00, A61K 31/551, C07D 487/14, A61P 43/00, C07D 487/04
Метки: тетраазабензо[е]азуленовые, аналоги, производные
Код ссылки
<a href="https://eas.patents.su/30-10888-tetraazabenzoeazulenovye-proizvodnye-i-ih-analogi.html" rel="bookmark" title="База патентов Евразийского Союза">Тетраазабензо[е]азуленовые производные и их аналоги</a>
Предыдущий патент: Тетрагидроиндазольные модуляторы каннабиноидов
Следующий патент: Комбинированная схема дозирования эритропоэтина
Случайный патент: Абсорбент












