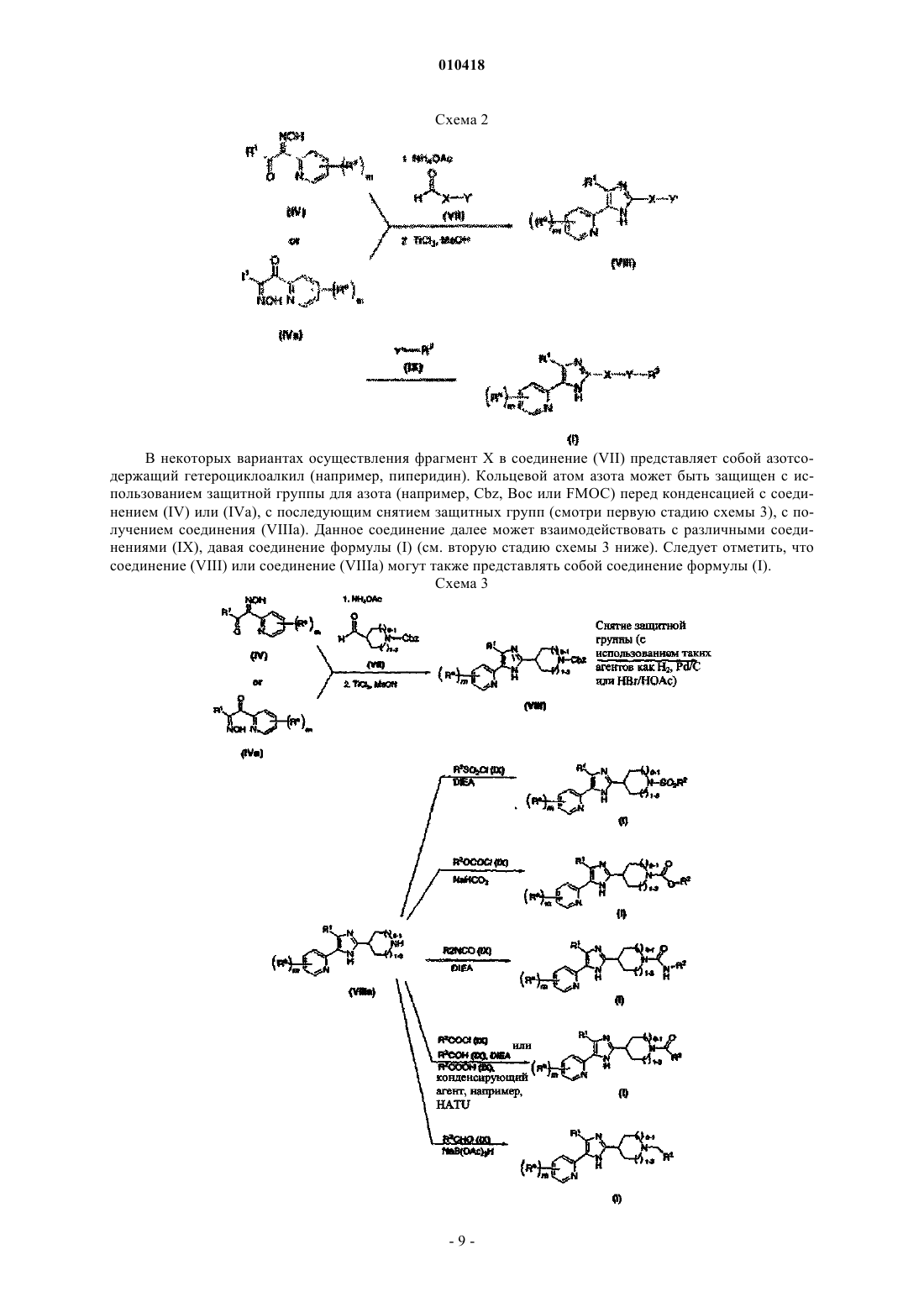
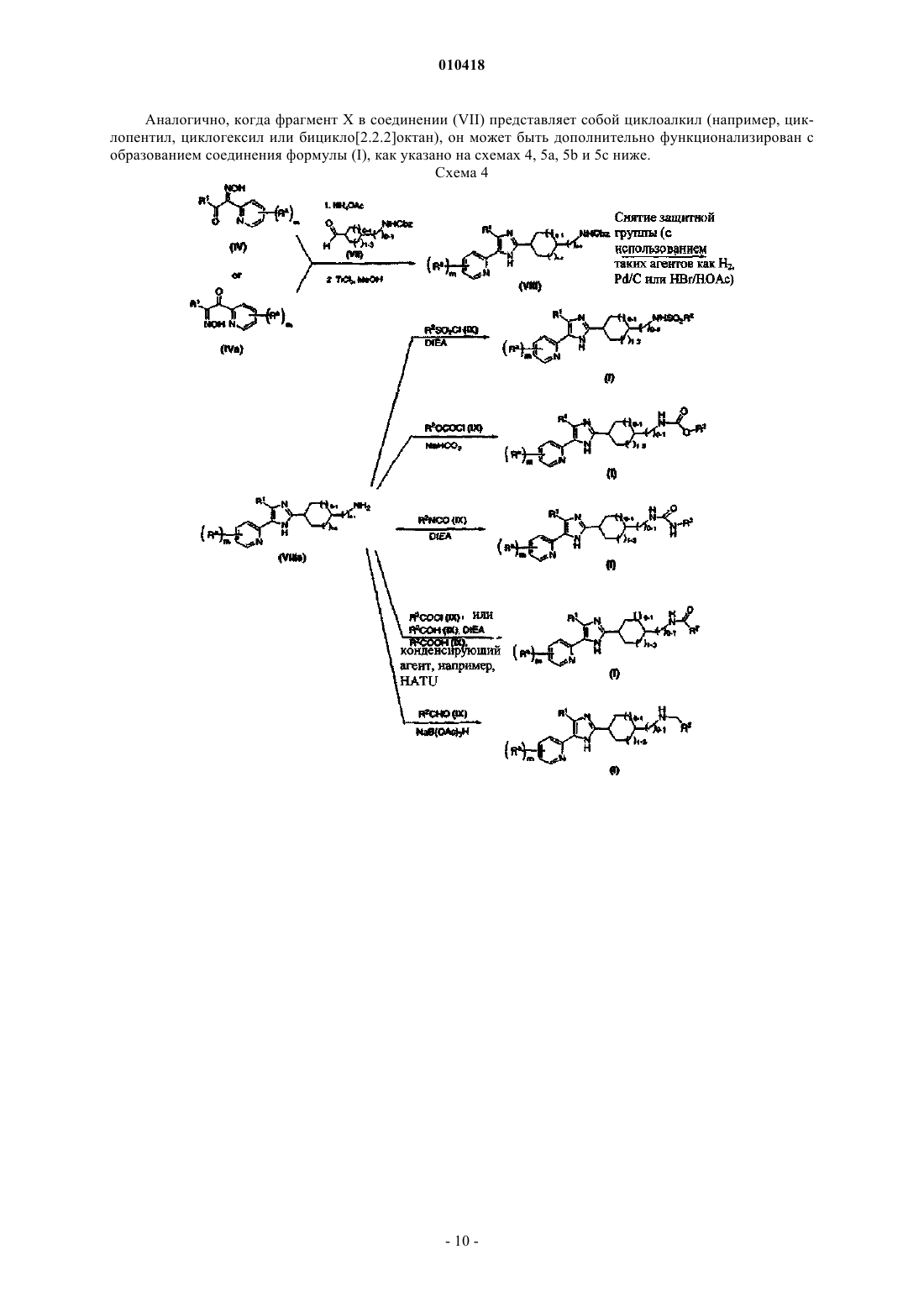
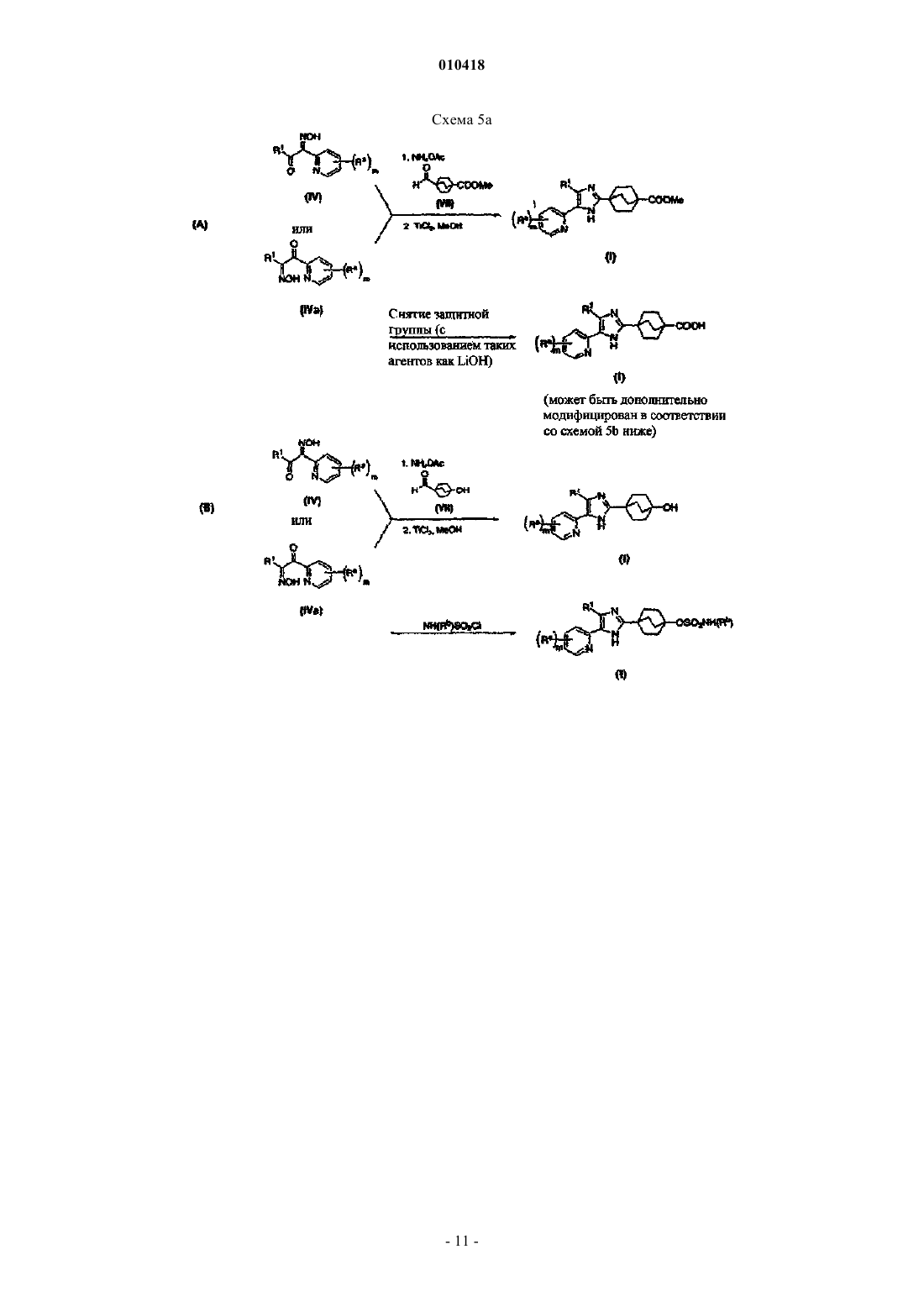
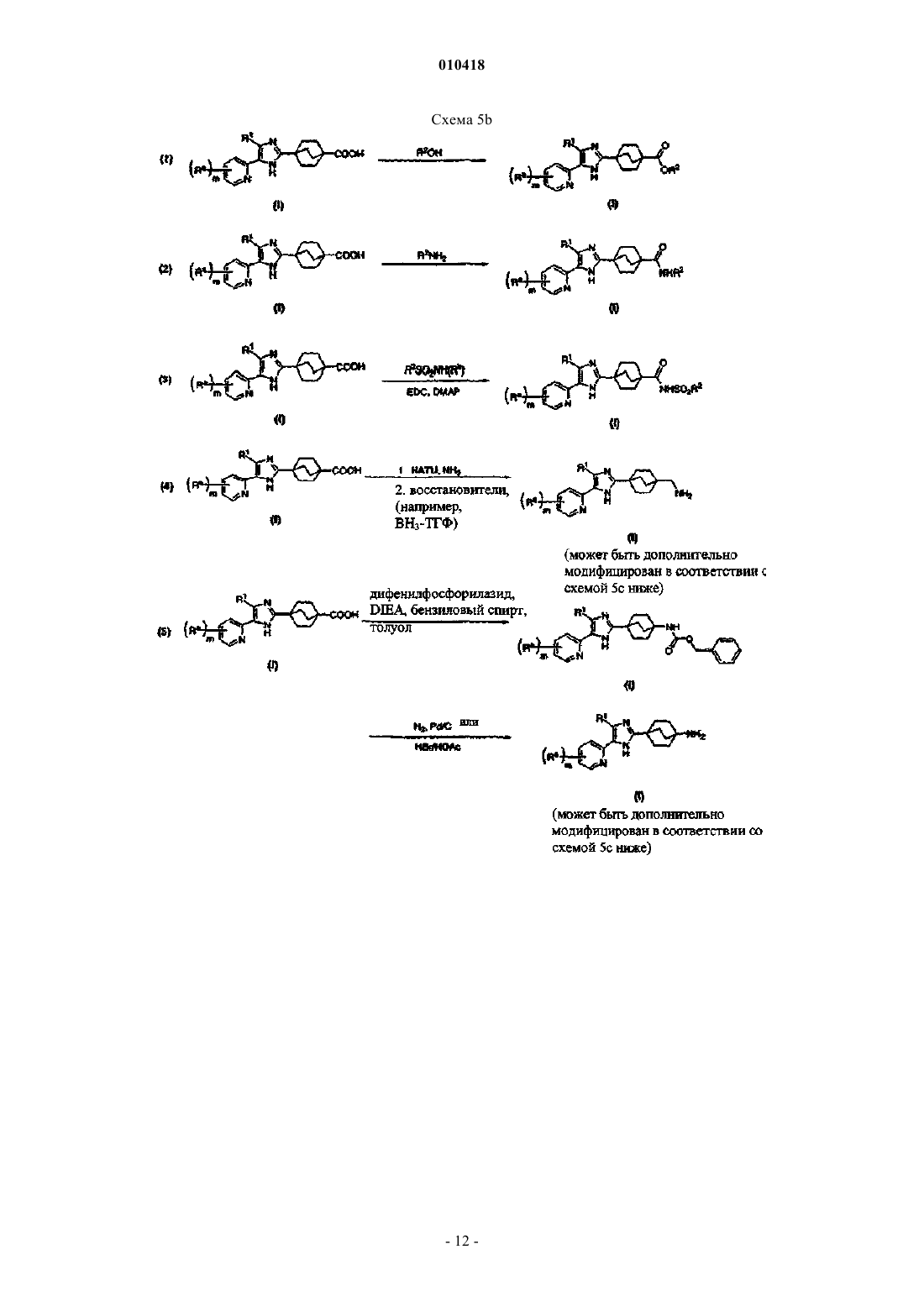
Тризамещённые гетероарилы и способы их получения и применения
Номер патента: 10418
Опубликовано: 29.08.2008
Авторы: Чуацюй Клаудио, Сунь Лихун, Петтер Расселл К., Ли Вен-Чернг, Шань Фэн, Чжэн Чжунли
Формула / Реферат
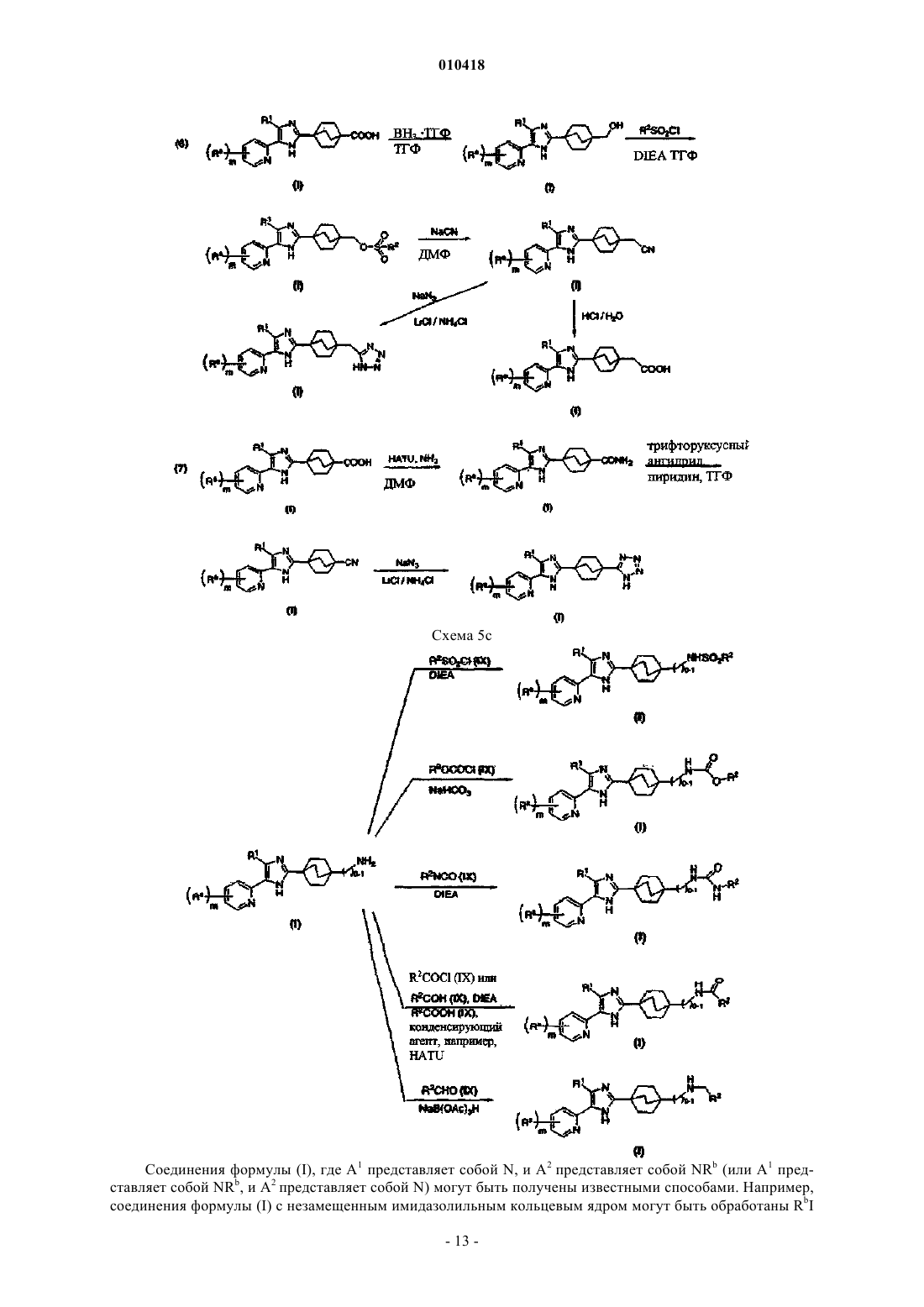
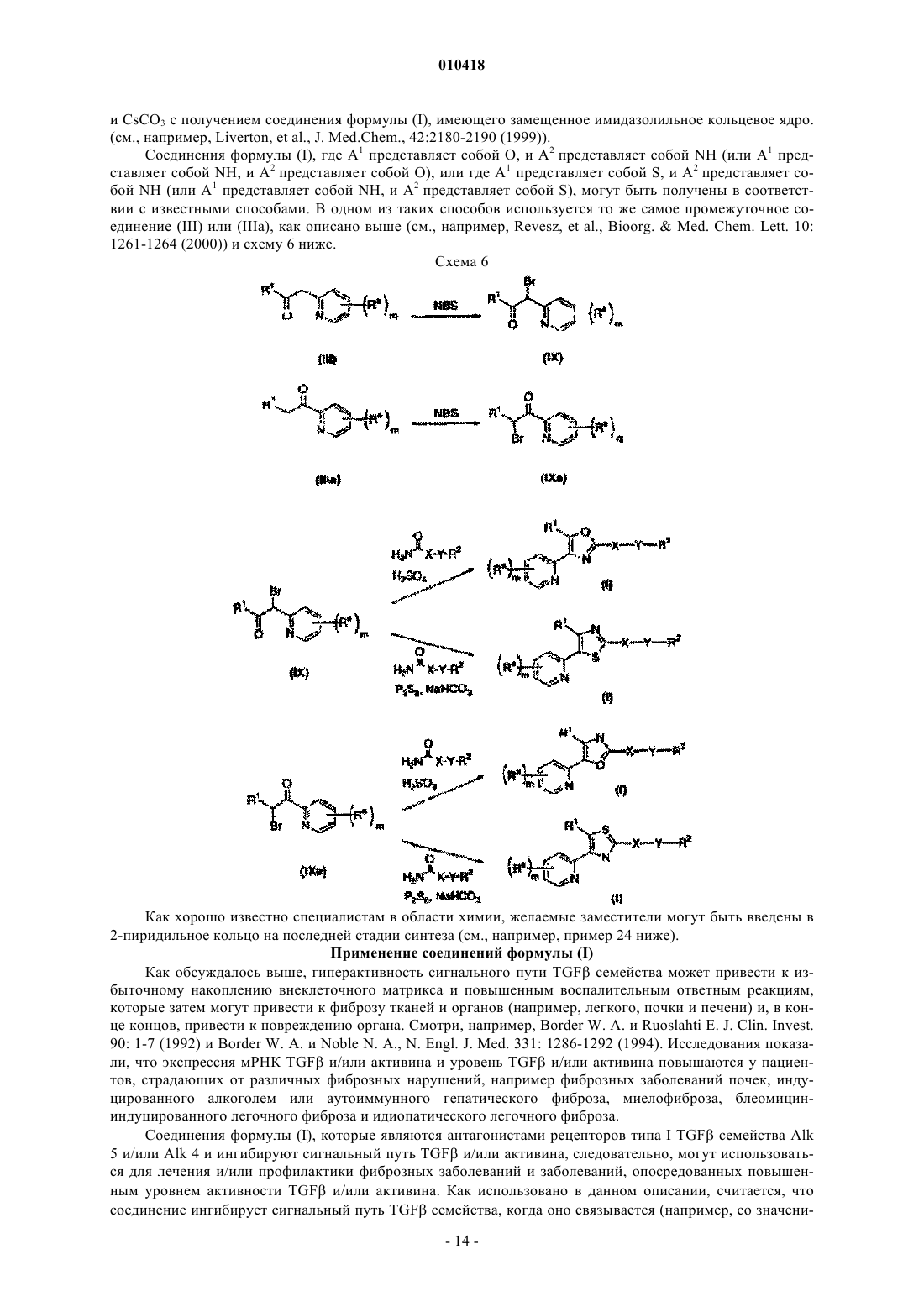
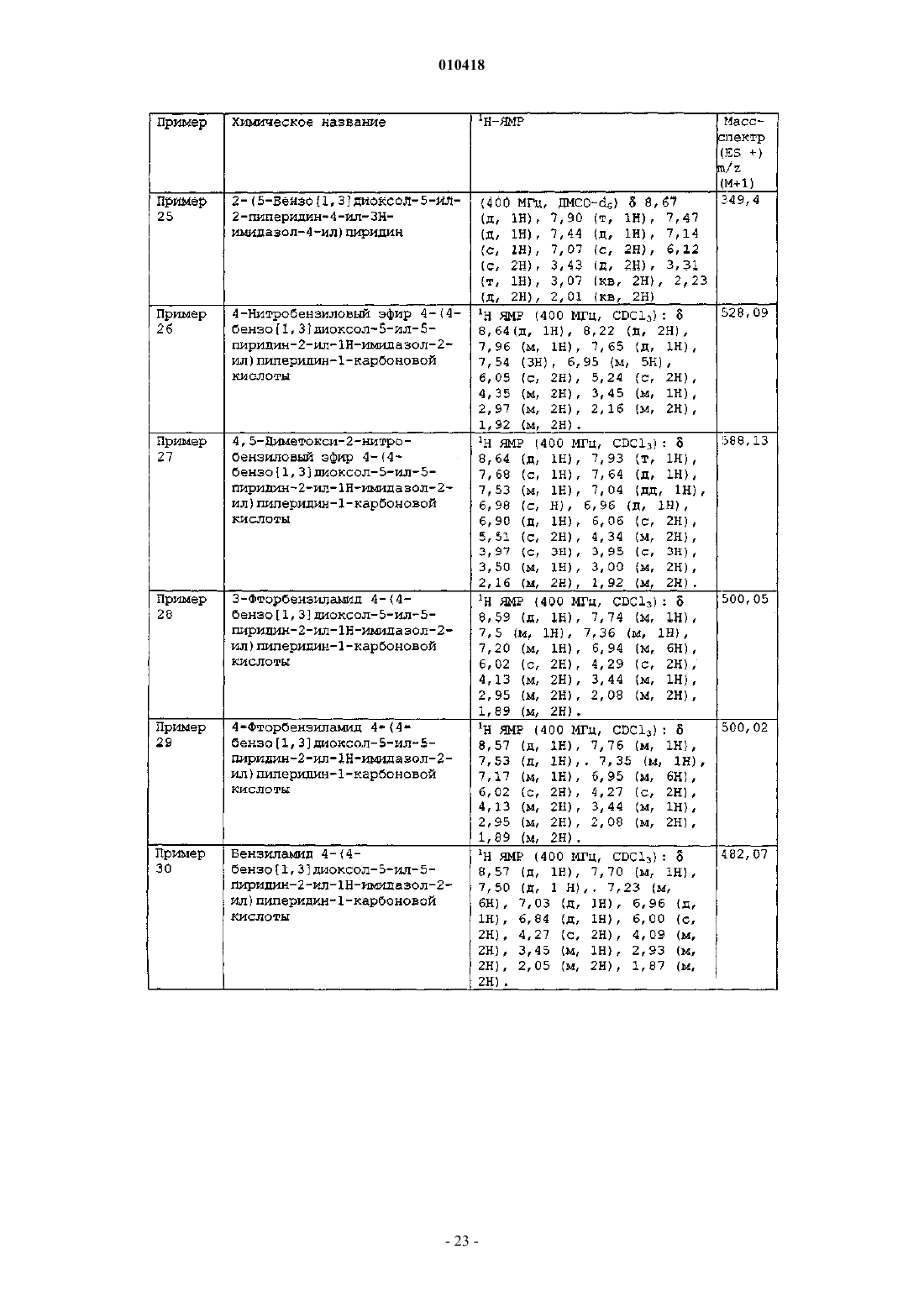
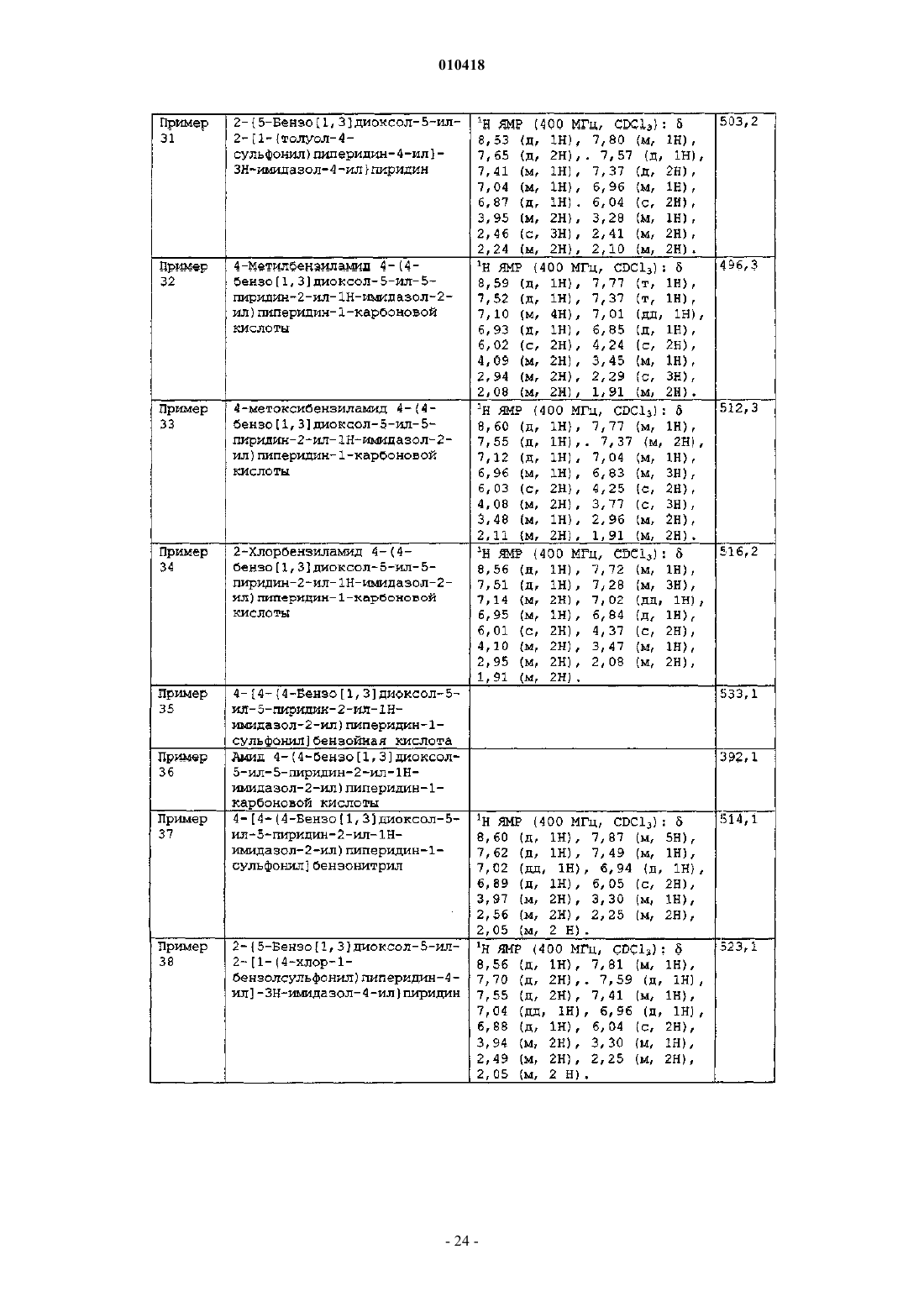
1. Соединение следующей формулы
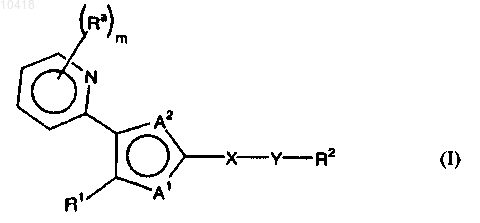
или его N-оксид, или фармацевтически приемлемая соль,
где R1 представляет собой арил, гетероарил, аралкил или гетероаралкил,
каждый Ra независимо представляет собой алкил, алкенил, алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, оксо, тиоксо, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, алкилсульфониламино, алкоксикарбонил, алкилкарбонилокси, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил, гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, арил, арилокси, арилсульфанил, ароил, гетероарил, гетероарилокси, гетероарилсульфанил или гетероароил;
X представляет собой пиперидинил, пиперазинил, пирролидинил, тетрагидрофуран, циклогексил, циклопентил, бицикло[2.2.1]гептан, бицикло[2.2.2]октан, бицикло[3.2.1]октан, 2-оксабицикло[2.2.2]октан, 2-азабицикло[2.2.2]октан, 3-азабицикло[3.2.1]октан или 1-азабицикло[2.2.2]октан;
Y представляет собой связь, -С(О)-, -С(O)-O-, -O-С(O)-, -S(O)p-O-, -O-S(O)p-, -C(O)-N(Rb)-, -N(Rb)-C(O)-, -O-C(O)-N(Rb)-, -N(Rb)-C(O)-O-, -O-S(O)p-N(Rb)-, -N(Rb)-S(O)p-O-, -N(Rb)-C(O)-N(Rc)-, -N(Rb)-S(O)p-N(Rc)-, -C(O)-N(Rb)-S(O)p-, -S(O)p-N(Rb)-C(O)-, -C(O)-N(Rb)-S(O)p-N(Rc)-, -C(O)-O-S(O)P-N(Rb)-,
-N(Rb) -S(O)p-N(Rc)-C(O)-, -N(Rb)-S(O)p-OC(O)-, -S(O)p-N(Rb)-, -N(Rb)-S(O)p-, -N(Rb)-, -S(O)p-, -O-, -S- или -(C(Rb)(Rc))q-, где каждый из Rb и Rc независимо представляет собой водород, гидрокси, алкил, алкокси, амино, арил, аралкил, гетероциклоалкил, гетероарил или гетероаралкил; р равен 1 или 2 и q составляет 1-4;
R2 представляет собой водород, алкил, алкенил, алкинил, циклоалкил, (циклоалкил)алкил, циклоалкенил, (циклоалкенил)алкил, арил, аралкил, арилалкенил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероциклоалкенил, (гетероциклоалкенил)алкил, гетероарил, гетероаралкил или (гетероарил)алкенил;
каждый из А1 и А2 независимо представляет собой O, S, N или NRb, при условии, что по крайней мере один из А1 и А2 представляет собой N; и
m равно 0, 1, 2 или 3, при условии, что когда m_ 2, две смежных Ra группы могут быть объединены вместе с образованием 4-8-членного необязательно замещенного циклического фрагмента;
и где термин "алкил", как группа или как часть других групп, относится к необязательно замещенной насыщенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 1-8 атомов углерода; термин "алкенил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода и по крайней мере одну двойную связь; термин "алкинил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода и по крайней мере одну тройную связь; термин "арил", как группа или как часть других групп, относится к необязательно замещенным фенилу, нафтилу или бензоконденсированной группе, содержащей 2-3 кольца, представляющих собой С4-8 карбоциклические фрагменты; термин "аралкил" относится к алкильной группе, которая замещена арильной группой, где алкил и арил являются такими, как определено выше; термин "циклоалкил", как группа или как часть других групп, относится к необязательно замещенному алифатическому карбоциклическому кольцу из 3-10 атомов углерода; термин "циклоалкенил", как группа или как часть других групп, относится к необязательно замещенному неароматическому карбоциклическому кольцу из 3-10 атомов углерода, содержащему одну или несколько двойных связей; термин "гетероциклоалкил", как группа или как часть других групп, относится к необязательно замещенной 3-10-членной насыщенной кольцевой структуре, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероциклоалкенил", как группа или как часть других групп, относится к необязательно замещенной 3-10-членной неароматической кольцевой структуре, имеющей одну или более двойных связей, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероарил", как группа или часть других групп, относится к необязательно замещенной моноциклической, бициклической или трициклической кольцевой структуре, имеющей 5-15 кольцевых атомов, где один или несколько из кольцевых атомов представляет собой гетероатом, например N, О или S, и где одно или более колец в бициклической или трициклической структуре является ароматическим; термин "циклический фрагмент" включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых определен выше; термин "ацил" относится к формильной группе или группе алкил-С(=O)-, где "алкил" определен выше; термин "амино" относится к группе -NRXRY, где каждый из RX и RY независимо представляет собой водород, алкил, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил, каждый из которых определен выше, причем когда термин "амино" не относится к терминальной группе, он представлен группой -NRX-, где RX имеет такое же значение, как определено выше; термин "карбамоил" относится к группе, имеющей структуру -O-CO-NRXRY или -NRX-CO-O-RZ, где RX и RYопределены выше, a RZ может представлять собой алкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероаралкил, где указанные термины определены выше; термин "сульфокси" относится к группам -O-SO-RZ или -SO-O-RX, где RX определен выше; термин "сульфамоил" относится к структуре -S(O)2-NRXRY или -NRX-S(O)2-RZ, где RX, RY и RZ определены выше; термин "сульфамид" относится к структуре -NRX-S(О)2-NRYRZ, где RX, RY и RZ определены выше; термин "остаток мочевины" относится к структуре -NRX-CO-NRYRZ, а термин "остаток тиомочевины" относится к структуре -NRX-CS-NRYRZ, где RX, RY и RZ определены выше.
2. Соединение по п.1, где X представляет собой пиперидинил, пиперазинил или пирролидинил.
3. Соединение по п.2, где пиперидинил, пиперазинил или пирролидинил связаны с Y через кольцевой атом азота.
4. Соединение по п.3, где Y представляет собой связь, -С(O)O-, -C(O)-N(Rb)-, -S(O)2- или -S(О)2-N(Rb)-, где Rb представляет собой водород или C1-4 алкил.
5. Соединение по п.1, где X представляет собой циклогексил, циклопентил или бицикло[2.2.2]октан.
6. Соединение по п.5, где Y представляет собой -N(Rb)-C(O)-, -N(Rb)-S(O)2-, -C(O)-, -С(O)-O-, -O-С(O)-, -C(O)-N(Rb)-, -S(O)p-, -O-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O- или -N(Rb)-C(O)-N(Rc)-.
7. Соединение по п.1, где Y представляет собой -N(Rb)-C(O)-, -N(Rb)-S(O)2-, -С(O)-, -С(O)-O-, -O-С(O)-, -C(O)-N(Rb)-, -S(O)p-, -O-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O-, -N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc)- или -C(O)-O-S(O)p-N(Rb)-.
8. Соединение по п.1, где R2 представляет собой водород, C1-6 алкил, арил, гетероарил, арил-С1-4 алкил или гетероарил-С1-4 алкил.
9. Соединение по п.1, где R2 представляет собой водород, C1-4алкил, фенил, пиридил, имидазолил, фуранил, тиенил, триазолил, тетразолил, бензил, фенилэтил, бензимидазолил, бензотиазолил, нафтилметил, нафтилэтил или -C1-2алкилпиридил, каждый из которых необязательно является замещенным одним или несколькими заместителями, выбранными из группы, состоящей из фтора, хлора, трифторметила, метила, этила, аминокарбонила, алкилкарбониламино, сульфамолила, алкоксикарбонила и алкилкарбонилокси.
10. Соединение по п.1, где R2 представляет собой водород, метил, этил, н-бутил, трет-бутил, бензил или пиридилметил.
11. Соединение по п.1, где R1 представляет собой арил или гетероарил.
12. Соединение по п.1, где R1 представляет собой замещенный фенил, инданил или гетероарил, выбранный из группы, состоящей из бензо[1,3]диоксолила, бензо[b]тиофенила, бензооксадиазолила, бензотиадиазолила, бензоимидазолила, бензооксазолила, бензотиазолила, 2-оксобензооксазолила, пиридила, пиримидинила, 2,3-дигидробензо[1,4]диоксила, 2,3-дигидробензофурила, 2,3-дигидро-бензо[b]тиофенила, 3,4-дигидробензо[1,4]оксазинила, 3-оксобензо[1,4]оксазинила, 1,1-диоксо-2,3-дигидробензо[b]тиофенила, [1,2,4]триазоло[1,5-а]пиридила, [1,2,4]триазоло[4,3-а]пиридила, хинолинила, хиноксалинила, хиназолинила, изохинолинила и циннолинила.
13. Соединение по п.1, где m равно 0-2.
14. Соединение по п.1, где Ra является замещенным в 6 положении.
15. Соединение по п.1, где Ra представляет собой C1-4алкил, C1-4алкокси, C1-4алкилтио, галоген, амино, аминокарбонил или алкоксикарбонил.
16. Соединение по п.1, где А1 представляет собой N, и А2 представляет собой NRb, или А1 представляет собой NRb, и А2 представляет собой N; где Rb представляет собой водород или C1-4алкил.
17. Соединение по п.1, где m равно 0-2, R1 представляет собой арил или гетероарил; R2 представляет собой водород, C1-6алкил, арил, гетероарил, -C1-4алкил-арил или -C1-4алкил-гетероарил; и Y представляет собой -N(Rb)-С(О)-, -N(Rb)-S(О)2-, -С(О)-, -С(O)-O-, -О-С(О)-, -C(O)-N(Rb)-, -S(O)p-, -О-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-С(О)-O-, -N(Rb)-С(О)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc)- или -C(O)-O-S(O)p-N(Rb)-.
18. Соединение по п.1, где m равно 0-2; R1 представляет собой арил или гетероарил; R2 представляет собой водород, C1-6алкил, арил, гетероарил, -C1-4алкил-арил или -C1-4алкил-гетероарил; X представляет собой пиперидинил, пиперазинил, пирролидинил, тетрагидрофуран, циклогексил, циклопентил, бицикло[2.2.1]гептан, бицикло[2.2.2]октан, бицикло[3.2.1]октан, 2-оксабицикло[2.2.2]октан, 2-аза-бицикло[2.2.2]октан, 3-азабицикло[3.2.1]октан или 1-азабицикло[2.2.2]октан; и Y представляет собой
-N(Rb)-С(О)-, -N(Rb)-S(O)2-, -C(O)-, -С(O)-O-, -О-С(О)-, -C(O)-N(Rb)-, -S(O)p-, -О-, -S(О)2N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O-, -N(Rb)-C-(O)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc)- или -С(О)-O-S(О)p-N(Rb)-.
19. Соединение по п.1, где m равно 0-2; R1 представляет собой арил или гетероарил; R2 представляет собой водород, C1-6алкил, арил, гетероарил, -C1-4алкил-арил или -C1-4алкил-гетероарил и X-Y- представляет собой
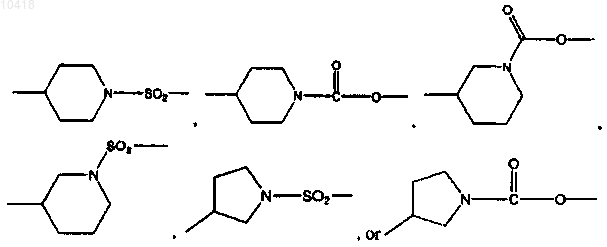
20. Соединение по п.19, где А1 представляет собой N, и А2 представляет собой NH, или А1 представляет собой NH, и А2 представляет собой N.
21 Соединение по п.20, где R1 представляет собой замещенный фенил.
22. Соединение по п.21, где R2 представляет собой водород, C1-4алкил, бензил или пиридилметил.
23. Соединение по п.22, где m равно 1, и Ra является замещенным в 6 положении.
24. Соединение по п.1, где m равно 0-2; R1 представляет собой арил или гетероарил; R2 представляет собой водород, C1-6алкил, арил, гетероарил, арил-С1-4алкил или гетероарил-С1-4алкил; X представляет собой циклогексил, циклопентил или бицикло[2.2.2]октан; и Y представляет собой -N(Rb)-С(О)-, -N(Rb)-S(O)2-, -C(O)-, -С(O)-O-, -O-С(O)-, -C(O)-N(Rb)-, -S(O)p-, -O-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O-,
-N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc)- или -C(O)-O-S(O)p-N(Rb)-, где каждый из Rb и Rc независимо представляет собой водород или C1-4алкил.
25. Соединение по п.24, где А1 представляет собой N, и А2 представляет собой NH, или А1 представляет собой NH, и А2 представляет собой N.
26. Соединение по п.25, где R1 представляет собой замещенный фенил.
27. Соединение по п.26, где R2 представляет собой водород, C1-4алкил, бензил или пиридилметил.
28. Соединение по п.27, где m равно 1, и Ra является замещенным в 6 положении.
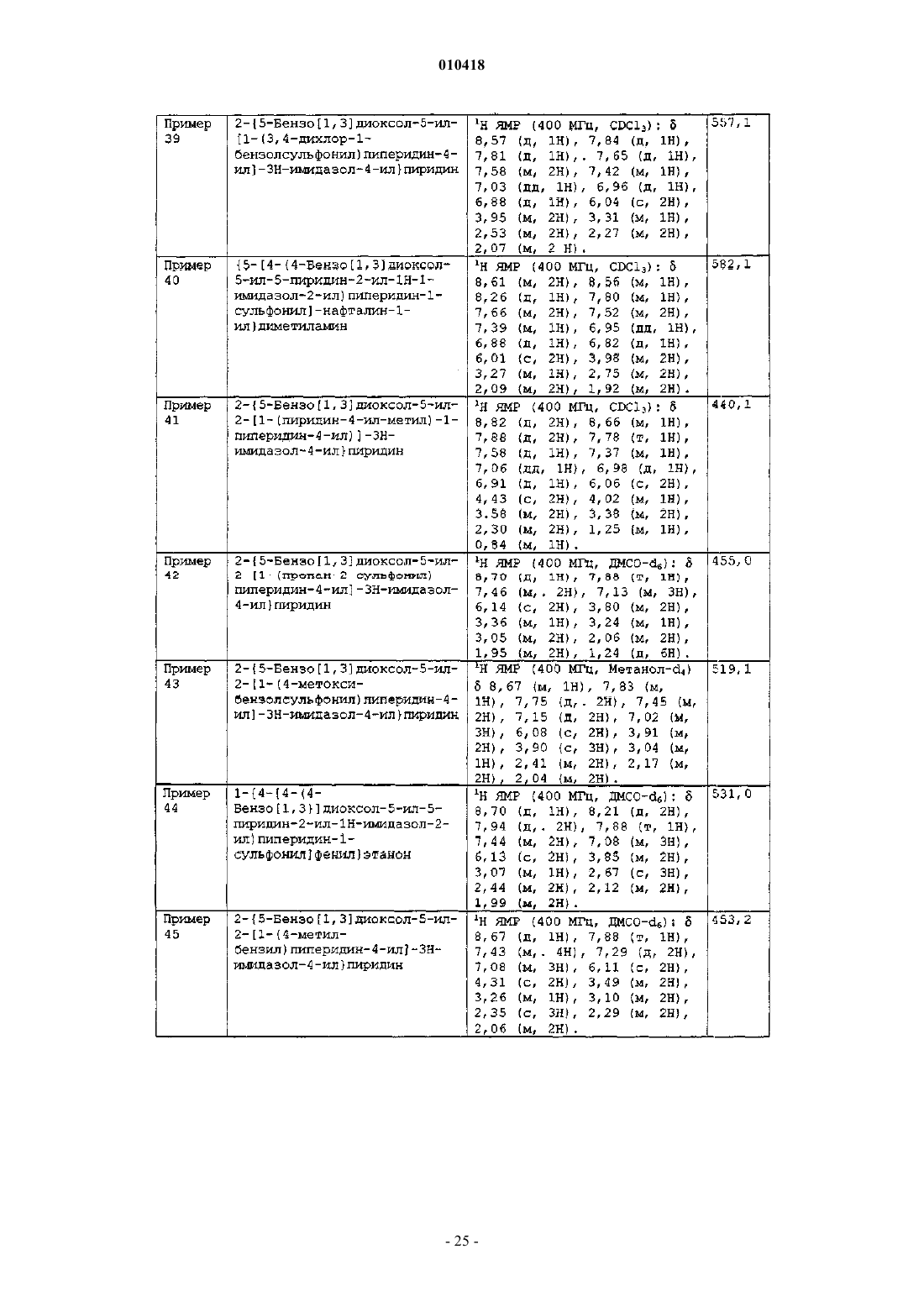
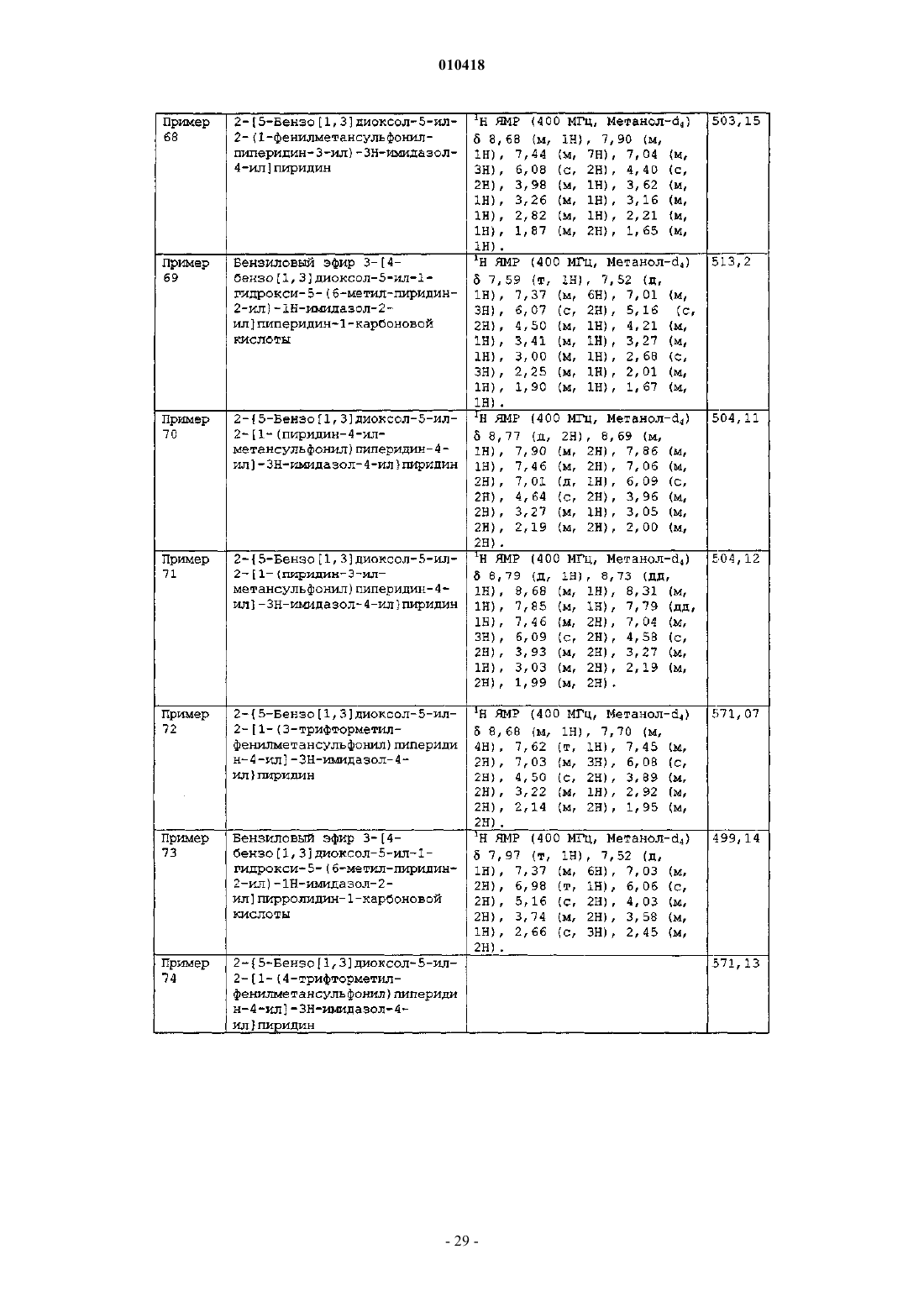
29. Соединение по п.1, выбранное из группы, состоящей из
4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]бензойной кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дихлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-фторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-этансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-3-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-4-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензю[1,3]диоксол-5-ил-2-[1-(тиофен-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(1-метил-1Н-имидазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(5-метилизоксазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-фенилметансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида бутан-1-сульфоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-пиридин-2-илметансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида 1-метил-1Н-имидазол-4-сульфоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(тиофен-3-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-этилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метанола;
амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонитрила;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-этилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-С-пиридин-2-ил-метансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[4-(1Н-тетразол-5-ил)бицикло[2.2.2]окт-1-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида 1-метил-1Н-имидазол-4-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-3-сульфоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметиловый эфир метансульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетонитрила;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}уксусной кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}-С-пиридин-2-илметансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нитрофенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
1-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}-7,7-диметилбицикло[2.2.1]гептан-2-она;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
метиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}фениламина;
(1-метил-5-метилсульфанил-1Н-[1,2,4]триазол-3-ил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
диметиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(3-хлорфенил)метанона;
4-[5-бензо[1,3]диоксол-5-ил-4-(6-циклопропилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метоксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}карбаминовой кислоты;
гидразида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}ацетамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-фенил-метансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида бутан-1-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида пропан-2-сульфоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-пиридин-2-ил-метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}метансульфонамида;
метилового эфира 4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метилового эфира 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октанола;
амида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}сульфамида;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-иловый эфир сульфаминовой кислоты;
бензилового эфира {4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}бензолсульфонамида;
метилового эфира 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(3-метил-4-оксю-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}ацетамида;
метилового эфира 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2] октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}метансульфонамида;
2,2,2-трифтор-N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}ацетамида;
амида 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида;
метилового эфира 4-[4-(5-фтор-6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-нитробензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(толуол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нитрофенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,4-дихлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
бензилового эфира 3-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 3-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-4-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-илпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-3-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-илпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-трифторметилфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
бензилового эфира 3-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пирролидин-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-трифторметилфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
{4-[2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-5-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-ил}-(4-метокси-бензил)амина;
4-[2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-5-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-иламина;
метилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(5-метил-2-трифторметилфуран-3-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[2-(1-фенилметансульфонилпиперидин-4-ил)-5-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-илфторида;
(4-метоксибензил)-{4-[5-(6-метилпиридин-2-ил)-2-(1-фенилметансульфонилпиперидин-4-ил)-1Н-имидазол-4-ил]пиридин-2-ил}амина;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}карбаминовой кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-бромпиридина;
1-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-3-фенилпропан-1-она;
N-4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-С-фенилметансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтенсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,4-дихлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}-С-фенилметансульфонамида;
(пиридин-2-илметил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(фуран-2-илметил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпирролидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пирролидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(1-метил-1Н-имидазол-4-сульфонил)пирролидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпирролидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
этиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бутиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты изопропиламида;
(3-имидазол-1-ил-пропил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}пирролидин-1-илметанона;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты диэтиламида;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексиламина;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(4-фтор-фенил)метанона;
N-{4-[4-бензо[1,3]диоксо-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-пиридин-4-ил-метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-2,2,2-трифторацетамида;
бензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-(5-бензо[1,3]диоксол-5-ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина;
2-хлорбензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
4,5-диметокси-2-нитробензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
3-фторбензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
4-фторбензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
бензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
4-метилбензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
4-метоксибензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2,4-дихлорбензиламшфр 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-хлорбензиламида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
амида 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]бензонитрила;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,4-дихлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
{5-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]нафталин-1-ил}диметиламина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-пиридин-4-илметилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-метоксибензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
1-{4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]фенил}этанона;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фуран-2-илметилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-метилбензил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-фтор-5-трифторметилбензил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-циклогексилметилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
этилового эфира 2-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-илметил]циклопропанкарбоновой кислоты;
трет-бутилового эфира 2-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-илметил]пирролидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2,2-диметил-[1,3]диоксолан-4-илметил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
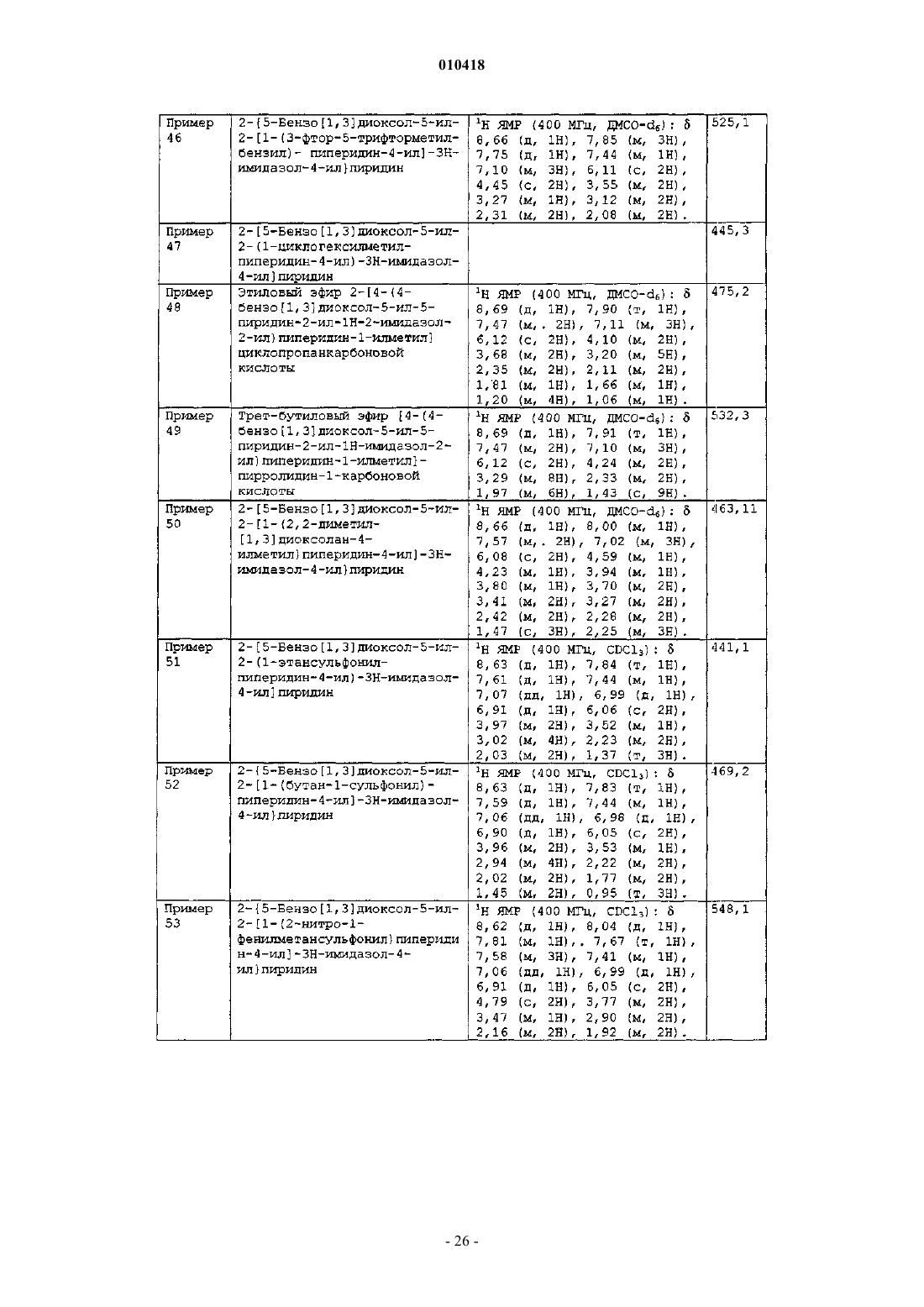
1-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-ил]-2-метилпропан-2-ола;
2-(6-амино-3-имино-3H-ксантен-9-ил)-4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбонил]бензойной кислоты;
1-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-ил]этанона;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-этансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтенсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
1-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонилметил]-7,7-диметилбицикло[2,2,1]гептан-2-она;
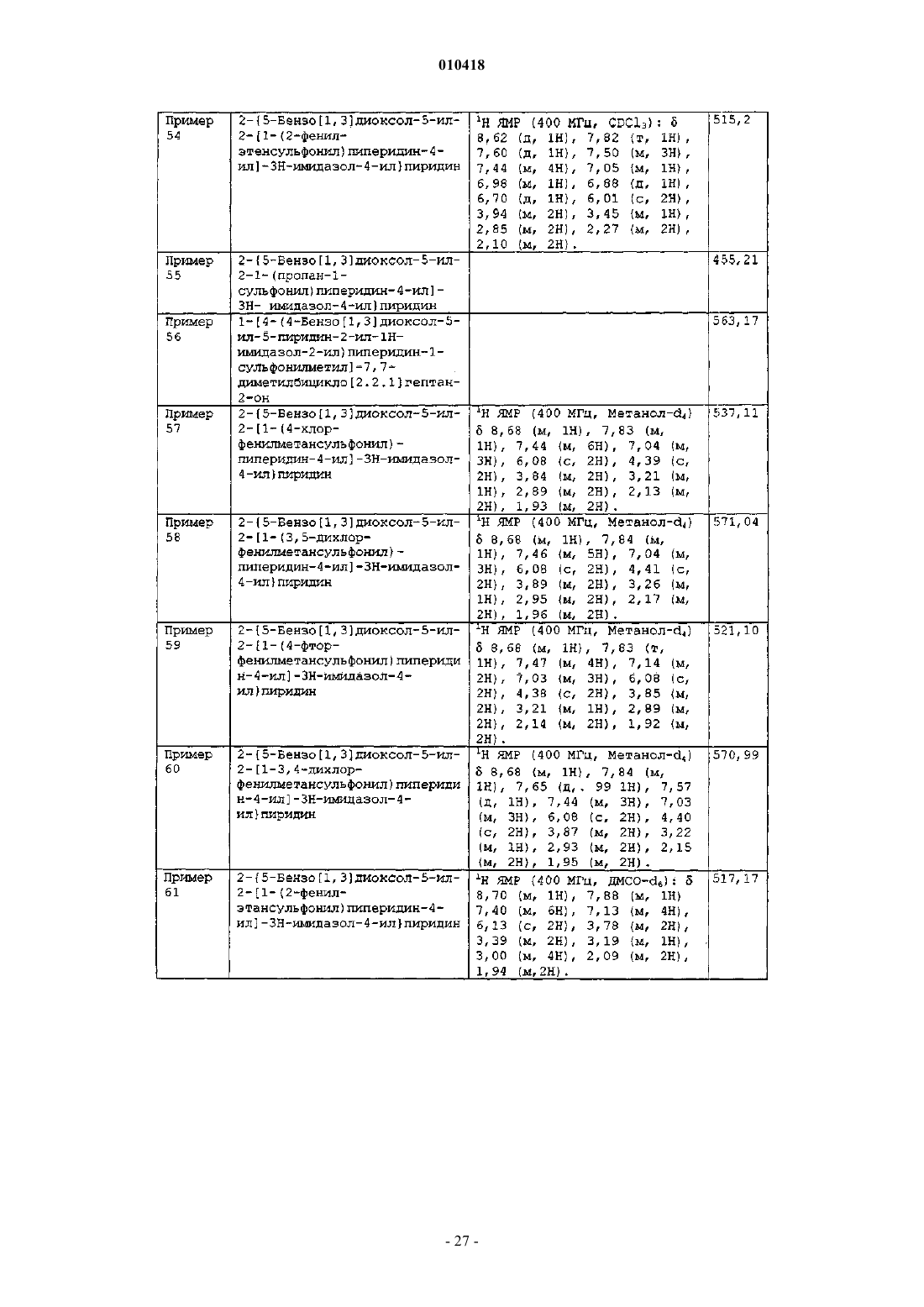
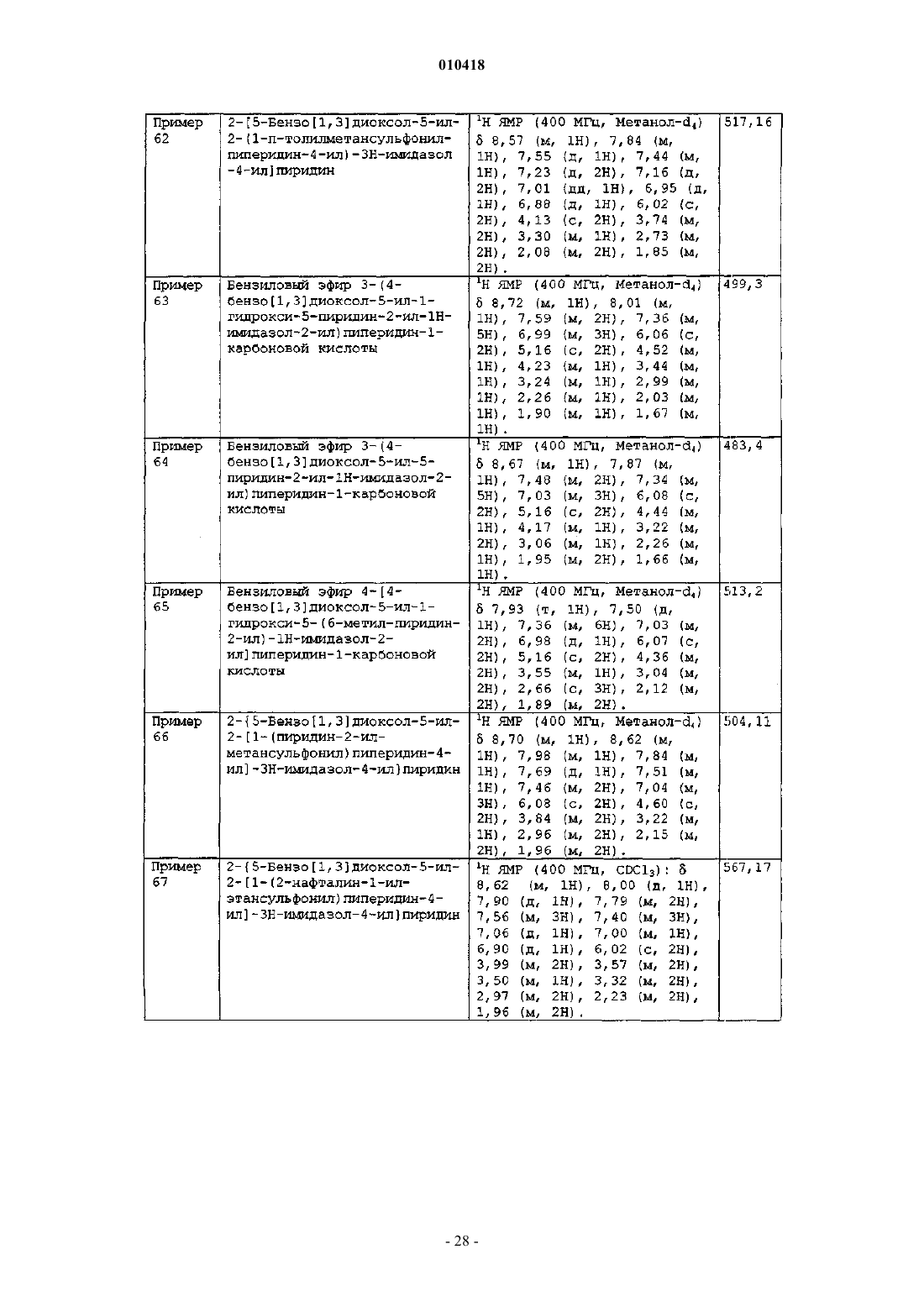
2-[5-бензо[1,3]диоксол-5-ил-2-(1-п-толилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
бензилового эфира 3-(4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-метоксибензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нафталин-1-ил-этансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-3-ил)-3H-имидазол-4-ил]пиридина;
бензилового эфира 3-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 3-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пирролидин-1-карбоновой кислоты;
бензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-бистрифторметилфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бифенил-4-сульфонил)пиперидин-4-ил]-5Н-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-феноксибензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бифенил-4-илметансульфонил)пиперидин-4-ил]-5Н-имидазол-4-ил}пиридина;
бензилового эфира 4-[5-бензо[1,3]диоксол-5-ил-1-метил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-1-метил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
бензилового эфира 4-[4-(2-хлорпиридин-4-ил)-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-илпиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-феноксифенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
бензилового эфира 4-[4-(2-фторпиридин-4-ил)-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[5-бензо[1,3]диоксол-5-ил-1-гидрокси-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-бромпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-трифторметилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[5-бензо[1,3]диоксол-5-ил-4-(6-бромпиридин-2-ил)-1-гидрокси-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-иламина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бифенил-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-феноксибензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
бензиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
3-хлор-4-фторбензиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пирролидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нафталин-2-ил-этансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
циклогексиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты дипропиламида;
(2-гидрокси-1-метил-2-фенилэтил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(1Н-бензоимидазол-2-ил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(пиридин-4-илметил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бензотиазол-2-иламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(5,7-дифторбензотиазол-2-ил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(4-метоксифенил)метанона и
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}карбаминовой кислоты.
30. Соединение по п.1, где указанное соединение выбирают из группы, состоящей из
4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]бензойной кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дихлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-фторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензю[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-ил-метансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-этансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-3-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-4-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(тиофен-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(1-метил-1Н-имидазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(5-метилизоксазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-фенилметансульфонамида;
бутан-1-сульфоновой кислоты {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-пиридин-2-ил-метансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида 1-метил-1Н-имидазол-4-сульфоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(тиофен-3-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-этилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метанола;
амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонитрила;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-этилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-С-пиридин-2-ил-метансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[4-(1Н-тетразол-5-ил)бицикло[2.2.2]окт-1-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида-1-метил-1Н-имидазол-4-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-3-сульфоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметиловый эфир метансульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетонитрила;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}уксусной кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}-С-пиридин-2-ил-метансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нитрофенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
1-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}-7,7-диметилбицикло[2.2.1]гептан-2-она;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
метиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}фениламина;
(1-метил-5-метилсульфанил-1Н-[1,2,4]триазол-3-ил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
диметиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(3-хлорфенил)метанона;
4-[5-бензо[1,3]диоксол-5-ил-4-(6-циклопропилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метоксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}карбаминовой кислоты;
гидразида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}ацетамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-фенил-метансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида бутан-1-сульфоновой кислоты;
пропан-2-сульфоновой кислоты {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-пиридин-2-ил-метансульфонамида;
N-4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}метансульфонамида;
метилового эфира 4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метилового эфира 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октанола;
амида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}сульфамида;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илового эфира сульфаминовой кислоты;
бензилового эфира {4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}бензолсульфонамида;
метилового эфира 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил)циклогексил}ацетамида;
метилового эфира 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}метансульфонамида;
2,2,2-трифтор-N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}ацетамида;
амида 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида;
метилового эфира 4-[4-(5-фтор-6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-нитробензилового эфира 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(толуол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нитрофенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,4-дихлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
бензилового эфира 3-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
3-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты бензилового эфира;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-4-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-илпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-3-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-илпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-трифторметилфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
бензилового эфира 3-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пирролидин-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3-трифторметилфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
{4-[2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-5-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-ил}-(4-метоксибензил)амина;
4-[2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-5- (6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-иламина;
метилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(5-метил-2-трифторметилфуран-3-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[2-(1-фенилметансульфонилпиперидин-4-ил)-5-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил]пиридин-2-илфторида;
(4-метоксибензил)-(4-[5-(6-метилпиридин-2-ил)-2-(1-фенилметансульфонилпиперидин-4-ил)-1Н-имидазол-4-ил]пиридин-2-ил}амина;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}карбаминовой кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-бромпиридина;
1-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-3-фенилпропан-1-она;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-С-фенилметансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтенсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,4-дихлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}-С-фенилметансульфонамида;
(пиридин-2-илметил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(фуран-2-илметил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпирролидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пирролидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(1-метил-1Н-имидазол-4-сульфонил)пирролидин-3-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпирролидин-3-ил)-3H-имидазол-4-ил]-6-метилпиридина;
этиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бутиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
изопропиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
(3-имидазол-1-илпропил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}пирролидин-1-ил-метанона;
диэтиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексиламина;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(4-фторфенил)метанюэр;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-пиридин-4-ил-метансульфонамида и
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-2,2,2-трифторацетамида.
31. Соединение по п.1, где указанное соединение выбирают из группы, состоящей из
4-[4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1Н-имидазол-2-ил)пиперидин-1-сульфонил]бензойной кислоты;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дихлорфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-фторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-ил-метансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}пиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-2-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-этансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(бутан-1-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-3-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пиридин-4-илметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(3,5-дифторфенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(тиофен-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(1-метил-1Н-имидазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(5-метилизоксазол-4-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-фенилметансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида бутан-1-сульфоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}-С-пиридин-2-илметансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексил}амида 1-метил-1Н-имидазол-4-сульфоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(тиофен-3-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
бензилового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-этилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метанола;
амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(пропан-2-сульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонитрила;
2-[5-бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]-6-этилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}-С-пиридин-2-ил-метансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[4-(1Н-тетразол-5-ил)бицикло[2.2.2]окт-1-ил]-3H-имидазол-4-ил}-6-метилпиридина;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-2-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида 1-метил-1Н-имидазол-4-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}амида тиофен-3-сульфоновой кислоты;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-фенилэтансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметилового эфира метансульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетонитрила;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}уксусной кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илметил}-С-пиридин-2-ил-метансульфонамида;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(2-нитрофенилметансульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
1-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}-7,7-диметилбицикло[2.2.1]гептан-2-она;
2-{5-бензо[1,3]диоксол-5-ил-2-[1-(4-хлорбензолсульфонил)пиперидин-4-ил]-3H-имидазол-4-ил}-6-метилпиридина;
метиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
2-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-сульфонилметил}фениламина;
(1-метил-5-метилсульфанил-1Н-[1,2,4]триазол-3-ил)амида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
диметиламида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]пиперидин-1-ил}-(3-хлорфенил)метанона;
4-[5-бензо[1,3]диоксол-5-ил-4-(6-циклопропилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метоксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[5-бензо[1,3]диоксол-5-ил-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
бензилового эфира {4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}карбаминовой кислоты;
гидразида 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}ацетамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-фенилметансульфонамида;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида бутан-1-сульфоновой кислоты;
{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}амида пропан-2-сульфоновой кислоты;
N-{4-[4-бензю[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]циклогексилметил}-С-пиридин-2-ил-метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1-имидазол-2-ил]циклогексил}метансульфонамида;
метилового эфира 4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(6-метилпиридин-2-ил)-4-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
метилового эфира 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октанола;
амида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-циклопропилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}сульфамида;
4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-илового эфира сульфаминовой кислоты;
бензилового эфира {4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}карбаминовой кислоты;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}метансульфонамида;
N-{4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбонил}бензолсульфонамида;
метилового эфира 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}ацетамида;
метилового эфира 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
гидроксиамида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
амида 4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}метансульфонамида;
2,2,2-трифтор-N-{4-[4-(6-метилпиридин-2-ил)-5-хиноксалин-6-ил-1Н-имидазол-2-ил]циклогексил}ацетамида;
амида 4-[5-(3-метил-4-оксо-3,4-дигидрохиназолин-6-ил)-4-(6-метилпиридин-2-ил)-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}метансульфонамида;
N-{4-[5-(6-метилпиридин-2-ил)-4-хиноксалин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]окт-1-ил}ацетамида и
метилового эфира 4-[4-(5-фтор-6-метилпиридин-2-ил)-5-[1,2,4]триазоло[1,5-а]пиридин-6-ил-1Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты.
32. Соединение следующей формулы
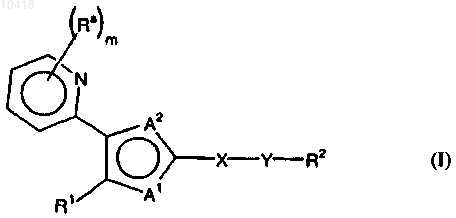
или его N-оксид, или фармацевтически приемлемая соль,
где R1 представляет собой арил, аралкил или гетероаралкил,
каждый Ra независимо представляет собой алкил, алкенил, алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, оксо, тиоксо, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, алкилсульфониламино, алкоксикарбонил, алкилкарбонилокси, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил, гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, арил, арилокси, арилсульфанил, ароил, гетероарил, гетероарилокси, гетероарилсульфанил или гетероароил;
X представляет собой циклоалкил или гетероциклоалкил;
Y представляет собой связь, -С(О)-, -С(O)-O-, -O-С(O)-, -S(O)p-O-, -O-S(O)p-, -C(O)-N(Rb)-, -N(Rb)-C(O)-, -O-C(O)-N(Rb)-, -N(Rb)-C(O)-O-, -O-S(O)p-N(Rb)-, -N(Rb)-S(O)p-O-, -N(Rb)-C(O)-N(Rc)-, -N(Rb)-S(O)p-N(Rc)-, -C(O)-N(Rb)-S(O)p-, -S(O)p-N(Rb)-C(O)-, -C(O)-N(Rb)-S(O)p-N(Rc)-, -C(O)-O-S(O)p-N(Rb)-,
-N(Rb)-S(O)p-N(Rc)-C(O)-, -N(Rb)-S(O)p-OC(O)-, -S(O)p-N(Rb)-, -N(Rb)-S(O)p-, -N(Rb)-, -S(O)p-, -O-, -S- или
-(C(Rb)(Rc))q-, где каждый из Rb и Rc независимо представляет собой водород, гидрокси, алкил, алкокси, амино, арил, аралкил, гетероциклоалкил, гетероарил, или гетероаралкил; р равен 1 или 2 и q составляет 1-4;
R2 представляет собой водород, алкил, алкенил, алкинил, циклоалкил, (циклоалкил)алкил, циклоалкенил, (циклоалкенил)алкил, арил, аралкил, арилалкенил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероциклоалкенил, (гетероциклоалкенил)алкил, гетероарил, гетероаралкил или (гетероарил)алкенил;
каждый из А1 и А2 независимо представляет собой О, S, N или NRb при условии, что по крайней мере один из А1 и А2 представляет собой N; и
m равно 0, 1, 2 или 3 при условии, что когда m_ 2, две смежных Ra группы могут быть объединены вместе с образованием 4-8-членного необязательно замещенного циклического фрагмента;
и где термин "алкил", как группа или как часть других групп, относится к необязательно замещенной насыщенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 1-8 атомов углерода; термин "алкенил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода и по крайней мере одну двойную связь; термин "алкинил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода и по крайней мере одну тройную связь; термин "арил", как группа или как часть других групп, относится к необязательно замещенным фенилу, нафтилу или бензоконденсированной группе, содержащей 2-3 кольца, представляющих собой С4-8 карбоциклические фрагменты; термин "аралкил" относится к алкильной группе, которая замещена арильной группой, где алкил и арил являются такими, как определено выше; термин "циклоалкил", как группа или как часть других групп, относится к необязательно замещенному алифатическому карбоциклическому кольцу из 3-10 атомов углерода; термин "циклоалкенил", как группа или как часть других групп, относится к необязательно замещенному неароматическому карбоциклическому кольцу из 3-10 атомов углерода, содержащему одну или несколько двойных связей; термин "гетероциклоалкил", как группа или как часть других групп, относится к необязательно замещенной 3-10-членной насыщенной кольцевой структуре, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероциклоалкенил", ъръ группа или как часть других групп, относится к необязательно замещенной 3-10-членной неароматической кольцевой структуре, имеющей одну или более двойных связей, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероарил", как группа или часть других групп, относится к необязательно замещенной моноциклической, бициклической или трициклической кольцевой структуре, имеющей 5-15 кольцевых атомов, где один или несколько из кольцевых атомов представляет собой гетероатом, например N, О или S, и где одно или более колец в бициклической или трициклической структуре является ароматическим; термин "циклический фрагмент" включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых определен выше; термин "ацил" относится к формильной группе или группе алкил-С(=O)-, где "алкил" определен выше; термин "амино" относится к группе -NRXRY, где каждый из RX и RY независимо представляет собой водород, алкил, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил, каждый из которых определен выше, причем когда термин "амино" не относится к терминальной группе, он представлен группой -NRX-, где RX имеет такое же значение, как определено выше; термин "карбамоил" относится к группе, имеющей структуру -O-CO-NRXRY или -NRX-CO-O-RZ, где RX и RY определены выше, a RZ может представлять собой алкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероаралкил, где указанные термины определены выше; термин "сульфокси" относится к группам -O-SO-RX или -SO-O-RX, где RX определен выше; термин "сульфамоил" относится к структуре -S(О)2-NRXRY или -NRX-S(O)2-RZ, где RX, RY и RZ определены выше; термин "сульфамид" относится к структуре -NRX-S(О)2-NRYRZ, где RX, RY и RZ определены выше; термин "остаток мочевины" относится к структуре -NRX-CO-NRYRZ, а термин "остаток тиомочевины" относится к структуре -NRX-CS-NRYRZ, где RX, RY и RZ определены выше.
33. Соединение следующей формулы
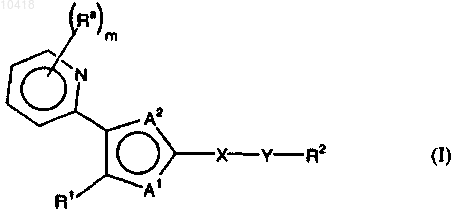
или его N-оксид, или фармацевтически приемлемая соль,
где R1 представляет собой бензо[1,3]диоксолил, [1,2,4]триазоло[1,5-а]пиридинил или [1,2,4,]триазоло[4,3-а]пиридинил,
каждый Ra независимо представляет собой алкил, алкенил, алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, оксо, тиоксо, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, алкилсульфониламино, алкоксикарбонил, алкилкарбонилокси, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил, гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, арил, арилокси, арилсульфанил, ароил, гетероарил, гетероарилокси, гетероарилсульфанил или гетероароил;
X представляет собой циклоалкил или гетероциклоалкил;
Y представляет собой связь, -С(О)-, -С(O)-O-, -O-С(O)-, -S(O)p-O-, -O-S(O)p-, -C(O)-N(Rb)-, -N(Rb)-C(O)-, -O-C(O)-N(Rb)-, -N(Rb)-C(O)-O-, -O-S(O)p-N(Rb)-, -N(Rb)-S(O)p-O-, -N(Rb)-C(O)-N(Rc)-, -N(Rb)-S(O)p-N(Rc)-, -C(O)-N(Rb)-S(O)p-, -S(O)p-N(Rb)-C(O)-, -C(O)-N(Rb)-S(O)p-N(Rc)-, -C(O)-O-S(O)p-N(Rb)-,
-N(Rb)-S(O)p-N(Rc)-C(O)-, -N(Rb)-S(O)p-OC(O)-, -S(O)p-N(Rb)-, -N(Rb)-S(O)p-, -N(Rb)-, -S(O)p-, -O-, -S- или -(С(Rb)(Rc))q-, где каждый из Rb и Rc независимо представляет собой водород, гидрокси, алкил, алкокси, амино, арил, аралкил, гетероциклоалкил, гетероарил или гетероаралкил; р равен 1 или 2 и q составляет 1-4;
R2 представляет собой водород, алкил, алкенил, алкинил, циклоалкил, (циклоалкил)алкил, циклоалкенил, (циклоалкенил)алкил, арил, аралкил, арилалкенил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероциклоалкенил, (гетероциклоалкенил)алкил, гетероарил, гетероаралкил или (гетероарил)алкенил;
каждый из А1 и А2 независимо представляет собой О, S, N или NRb, при условии, что по крайней мере один из А1 и А2 представляет собой N; и
m равно 0, 1, 2 или 3, при условии, что когда m_ 2, две смежных Ra группы могут быть объединены вместе с образованием 4-8-членного необязательно замещенного циклического фрагмента;
и где термин "алкил", как группа или как часть других групп, относится к необязательно замещенной насыщенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 1-8 атомов углерода; термин "алкенил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода, и по крайней мере одну двойную связь; термин "алкинил", как группа или как часть других групп, относится к необязательно замещенной алифатической углеводородной группе, которая может быть линейной или разветвленной и содержит 2-8 атомов углерода и по крайней мере одну тройную связь; термин "арил", как группа или как часть других групп, относится к необязательно замещенным фенилу, нафтилу или бензоконденсированной группе, содержащей 2-3 кольца, представляющих собой C4-8карбоциклические фрагменты; термин "аралкил" относится к алкильной группе, которая замещена арильной группой, где алкил и арил являются такими, как определено выше; термин "циклоалкил", как группа или как часть других групп, относится к необязательно замещенному алифатическому карбоциклическому кольцу из 3-10 атомов углерода; термин "циклоалкенил", как группа или как часть других групп, относится к необязательно замещенному неароматическому карбоциклическому кольцу из 3-10 атомов углерода, содержащему одну или несколько двойных связей; термин "гетероциклоалкил", как группа или как часть других групп, относится к необязательно замещенной 3-10-членной насыщенной кольцевой структуре, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероциклоалкенил", как группа или как часть других групп, относится к необязательно замещенной 3-10-членной неароматической кольцевой структуре, имеющей одну или более двойных связей, в которой один или несколько кольцевых атомов представляют собой гетероатом, например N, О или S; термин "гетероарил", как группа или часть других групп, относится к необязательно замещенной моноциклической, бициклической или трициклической кольцевой структуре, имеющей 5-15 кольцевых атомов, где один или несколько из кольцевых атомов представляет собой гетероатом, например N, О или S, и где одно или более колец в бициклической или трициклической структуре является ароматическим; термин "циклический фрагмент" включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых определен выше; термин "ацил" относится к формильной группе или группе алкил-С(=O)-, где алкил определен выше; термин "амино" относится к группе -NRXRY, где каждый из RX и RY независимо представляет собой водород, алкил, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил шыш гетероаралкил, каждый из которых определен выше, причем когда термин "амино" не относится к терминальной группе, он представлен группой -NRX-, где RX имеет такое же значение, как определено выше; термин "карбамоил" относится к группе, имеющей структуру -O-CO-NRxRy или -NRX-CO-O-RZ, где RX и RY определены выше, a RZ может представлять собой алкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероаралкил, где указанные термины определены выше; термин "сульфокси" относится к группам -O-SO-RX или -SO-O-RX, где RX определен выше; термин "сульфамоил" относится к структуре -S(O)2-NRXRY или -NRX-S(О)2-RZ, где RX, RY и RZ определены выше; термин "сульфамид" относится к структуре -NRX-S(О)2-NRYRZ, где RX, RY и RZ определены выше; термин "остаток мочевины" относится к структуре -NRX-CO-NRYRZ, а термин "остаток тиомочевины" относится к структуре -NRX-CS-NRYRZ, где RX, RY и RZ определены выше.
34. Фармацевтическая композиция, содержащая соединение по п.1 или 32, 33 и фармацевтически приемлемый носитель.
35. Фармацевтическая композиция, содержащая соединение по п.29 и фармацевтически приемлемый носитель.
36. Способ ингибирования TGFb сигнального пути у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.1 или 32, 33.
37. Способ ингибирования TGFb сигнального пути у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.29.
38. Способ ингибирования TGFb рецептора типа I в клетке, включающий контактирование указанной клетки с эффективным количеством соединения по п.1 или 32, 33.
39. Способ ингибирования TGFb рецептора типа I в клетке, включающий контактирование указанной клетки с эффективным количеством соединения по п.29.
40. Способ снижения накопления избытка внеклеточного матрикса, индуцированного TGFb, у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.1 или 32, 33.
41. Способ снижения накопления избытка внеклеточного матрикса, индуцированного TGFb, у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.29.
42. Способ лечения и профилактики фиброзного состояния у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.1 или 32, 33.
43. Способ лечения и профилактики фиброзного состояния у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.29.
44. Способ по п.42 или 43, где фиброзное состояние выбирают из группы, состоящей из склеродермы, идиопатического легочного фиброза, гломерулонефрита, диабетической нефропатии, экзематозного нефрита, индуцированной повышенным кровяным давлением нефропатии, глазного рубцевания, рубцевания роговицы, фиброза печени, фиброза желчных путей, легочного фиброза, почечного фиброза, рестеноза, индуцированного лучевой терапией фиброза, индуцированного химиотерапией фиброза, острого повреждения легкого, постинфарктного сердечного фиброза, фибросклероза, фиброзных злокачественных новообразований, фиброидов, фибромы, фиброаденом и фибросарком.
45. Способ ингибирования метастазов опухолевых клеток у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.1 или 32, 33.
46. Способ ингибирования метастазов опухолевых клеток у субъекта, включающий введение указанному субъекту эффективного количества соединения по п.29.
47. Способ лечения раковых новообразований, опосредованных сверхэкспрессией TGFb, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения по п.1 или 32, 33.
48. Способ лечения раковых новообразований, опосредованных сверхэкспрессией TGFb, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения по п.29.
49. Способ по п.47 или 48, где указанные раковые новообразования выбирают из группы, состоящей из раковых новообразований легкого, молочной железы, печени, желчных путей, желудочно-кишечного тракта, головы и шеи, поджелудочной железы, простаты и шейки матки, множественной миеломы, меланомы, глиомы и глиобластомы.
Текст
TGF (Трансформирующий фактор роста ) - член большого семейства димерных полипептидных факторов роста, которое включает, например, активины, ингибины, белки остеогенеза (BMPs), факторы роста и дифференциации (GDFs) и ингибирующие муллериан вещества (MIS), TGF существует в трех изоформах (TGF1, TGF2 и TGF3) и присутствует в большинстве клеток наряду со своими рецепторами. Каждая изоформа экспрессируется как тканеспецифическим, так и эволюционно регулируемым образом. Каждая изоформа TGF синтезируется в виде белка-предшественника, который внутриклеточно расщепляется на С-концевую область (латентно-связанный пептид (LAP и N-концевую область, известную как зрелый или активный TGF. LAP обычно нековалентно связан со зрелым TGF перед выделением из клетки. Комплекс LAP-TGF не может связываться с TGF рецепторами и не являестя биологически активным. TGF обычно высвобождается (и активируется) из комплекса по множеству механизмов, включая, например, взаимодействие с тромбоспондином-1 или плазмином. После активации TGF связывается с высокой аффинностью с рецептором II типа (TGFRII), конститутивно активной серин/треонинкиназой. Лигандсвязанный рецептор II типа фосфорилирует рецептор TGF типа I (Alk 5) в глицин/серин обогащенном домене, что позволяет рецептору I типа сформироваться и фосфорилировать ниже данного участка последовательности сигнальные молекулы Smad2 илиSmad3 затем могут образовывать комплекс с Smad4, и весь целиком гетеро-Smad комплекс перемещается в ядро и регулирует транскрипцию различных TGF-отвечающих генов. См., например, Massague, J. Ann.Rev. Biochem. Med. 67: 773 (1998). Активины также являются членами TGF надсемейства, которые отличаются от TGF тем, что они являются гомо- или гетеродимерами активина a или b. Активины передают сигнал аналогично TGF,то есть посредством связывания с конститутивной серин-треониновой киназой рецептора, активиновым рецетором II типа (ActRIIB) и активирования серин-треонинового рецептора I типа Alk 4, для фосфорилирования Smad2 или Smad3. Последующее образование гетеро-Smad комплекса также приводит к активин-индуцированной регуляции генной транскрипции. Действительно, TGF и родственные факторы, такие как активин, регулируют большой набор клеточных процессов, например, приостановку клеточного цикла в эпителиальных и гематопоэтических клетках, контроль пролиферации и дифференциации мезенхимальных клеток, рекрутинг воспалительных клеток, иммуноподавление, заживление ран и продуцирование внеклеточного матрикса. См., например,Massage, J.Ann. Rev. Cell. Biol. 6: 594-641 (1990); Roberts, А. В. и Sporn M. B. PeptideGrowth Factors иTheir Receptors, 95:419-472, Berlin: Springer-Verlag (1990); Roberts, А. В. и Sporn M. B. Growth Factors 8: 19 (1993); и Alexandrow, M. G., Moses, H. L. Cancer Res. 55; 1452-1457 (1995). Гиперактивность TGF сигнального пути лежит в основе многих заболеваний человека (например, избыточное накопление внеклеточного матрикса, аномально высокий уровень воспалительных ответных реакций, фиброзные заболевания и прогрессирующие злокачественные новообразования). Аналогично, активиновая передача сигнала и сверхэкспрессия активина связана с патологическими нарушениями, которые включают накопление внеклеточного матрикса и фиброз (см., например, Matsuse, T. et al., Am. J. Respir. Cell Mol. Biol. 13: 17-24(1995); Inoue, S. et al., Biochem. Biophys. Res. Comm. 205: 441-448 (1994); Matsuse, T. et al., Am. J. Pathol. 148: 707-713 (1996); De Bleser et al., Hepatology 26: 905-912 (1997); Pawlowski, J. E., et al., J. Clin. Invest. 100: 639-648 (1997); Sugiyama, M. et al., Gastroenterology 114: 550-558 (1998); Munz, B. et al., EMBOJ. 18: 5205-5215 (1999, воспалительные ответные реакции (см., например, Rosendahl, A. et al., Am. J. Repir.Cell Mol. Biol. 25: 60-68 (2001, кахексию или общее истощение (см. Matzuk, M. M. et al., Proc. Nat. Acad.al., Endocrinology 141: 2319-27 (2000, заболевания или патологические ответные реакции центральной нервной системы (смотри Logan, A. et al., Eur. J. Neurosci. 11: 2367-2374 (1999); Logan, A. et al., Exp. Neurol. 159: 504-510 (1999); Masliah, E. et al., Neurochem. Int. 39: 393-400 (2001); De Groot, C. J. A. et al., J.(см. Dahly, A. J. et al., Am. J. Physio. Regul. Integr. Comp, Physio, 283; R757-67 (2002. Исследования показали, что TGF и активин могут действовать синергетически, индуцируя продуцирование внеклеточного матрикса (см., например, Sugiyama, M. et al., Gastroenterology 114: 550-558, (1998. Таким образом,желательно разработать модуляторы (например, антагонисты) для членов семейства TGF с целью профилактики и/или лечения заболеваний, включающий в себя данный сигнальный путь. Краткое изложение сущности изобретения Данное изобретение основано на том открытии, что соединения формулы (I) неожиданно оказались сильными антагонистами рецепторов типа I семейства TGF, Alk 5 и/или Alk 4. Таким образом, соединения формулы (I) могут использоваться при профилактике и/или лечении заболеваний, таких как фиброз (например, почечный фиброз, легочный фиброз и фиброз печени), прогрессирующий рак или других заболеваний, при которых желательно снижение сигнальной активности се-1 010418 мейства TGF. В одном аспекте изобретение характеризует соединение формулы I:R1 может представлять собой арил, гетероарил, аралкил или гетероаралкил. Каждый Ra независимо может представлять собой алкил, алкенил, алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, оксо, тиоксо, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил,алкилсульфонил, аминокарбонил, алкилкарбониламино, алкилсульфониламино, алкоксикарбонил, алкилкарбонилокси, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил, гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, арил, арилокси, арилсульфанил, ароил, гетероарил, гетероарилокси, гетероарилсульфанил или гетероароил. X может представлять собой циклоалкил или гетероциклоалкил. Y может представлять собой связь, -С(О)-, -С(O)-O-, -O-С(O)-, -S(O)p-O-, -O-S(O)p-, -C(O)-N(Rb)-, -N(Rb)-C(O)-, -OC(O)-N(Rb)-, -N(Rb)-C(O)-O-, -O-S(O)p-N(Rb)-, -N(Rb)-S(O)p-O-, -N(Rb)-C(O)-N(Rc)-, -N(Rb)-S(O)p-N(Rc)-,-C(O)-N(Rb)-S(O)p-, -S(O)p-N(Rb)-C(O)-, -C(O)-N(Rb)-S(O)p-N(Rc)-, -C(O)-O-S(O)p-N(Rb)-, -N(Rb)-S(O)pN(Rc)-C(O)-, -N(Rb)-S(O)p-O-C(O)-, -S(O)p-N(Rb)-, -N(Rb)-S(O)p-, -N(Rb)-, -S(O)p-, -O-, -S- или -(C(Rb)(Rcq, где каждый из Rb и Rc независимо представляет собой водород, гидрокси, алкил, алкокси, амино, арил,аралкил, гетероциклоалкил, гетероарил, или гетероаралкил. р может составлять 1 или 2, и q может составлять 1-4. R2 может представлять собой водород, алкил, алкенил, алкинил, циклоалкил, (циклоалкил)алкил, циклоалкенил, (циклоалкенил)алкил, арил, аралкил, арилалкенил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероциклоалкенил, (гетероциклоалкенил)алкил, гетероарил, гетероаралкил или (гетероарил)алкенил. Каждый из А 1 и А 2, независимо, может представлять собой О, S, N или NRb при условии, что, по крайней мере, один из А 1 и А 2 может представлять собой N. m может быть равно 0, 1, 2 или 3, т.е. 2-пиридильное кольцо может быть незамещенным или замещенным 1-3 Ra группами. Отметим, что когда m 2, две смежных Ra группы могут быть объединены вместе с образованием 4-8-членного необязательно замещенного циклического фрагмента. То есть 2-пиридильное кольцо может быть конденсированным с циклическим фрагментом с образованием фрагмента, например 7 Н-[2]пириндинила, 6,7-дигидро-5 Н-[1]пириндинила, 5,6,7,8 тетрагидрохинолинила,5,7-дигидрофуро[3,4-b]пиридинила или 3,4-дигидро-1 Н-тиопирано[4,3c]пиридинила, который необязательно может быть замещенным одним или несколькими заместителями,такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеналкил, такой как трифторметил),алкенил, алкинил, циклоалкил, гетероциклоалкил, алкокси, арил, гетероарил, арилокси, гетероарилокси,ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилтио, сульфокси, сульфамоил, оксо или карбамоил. В одном варианте осуществления X может представлять собой 4-8-членный моноциклический циклоалкил или гетероциклоалкил, или X может представлять собой 4-8-членный бициклический циклоалкил или гетероциклоалкил. Например, X может представлять собой циклогексил, циклопентил, пиперидинил, пиперазинил, пирролидинил, тетрагидрофуран, бицикло[2.2.1]гептан, бицикло[2.2.2]октан, бицикло[3,2.1]октан, 2-оксабицикло[2.2.2]октан, 2-азабицикло[2.2.2]октан, 3-азабицикло[3.2.1]октан или 1 азабицикло[2.2.2]октан. В одном варианте осуществления X может представлять собой пиперидинил, пиперазинил или пирролидинил; каждый из которых может быть связанным с фрагментом Y через соответствующий свой атом азота; и Y может представлять собой связь, -С(O)O-, -C(O)-N(Rb)-, -S(O)2- или -S(O)2-N(Rb)-, где Rb может представлять собой водород или C1-4 алкил. В одном варианте осуществления X может представлять собой циклогексил, циклопентил или бицикло[2.2.2]октан; и Y может представлять собой -N(Rb)-С(О)-, -N(Rb)-S(О)2-, -С(O)-, -С(O)-O-, -O-С(O)-,-C(O)-N(Rb)-, -S(O)p-, -O-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O-, -N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb)-S(O)pN(Rc)- или -C(O)-O-S(O)p-N(Rb)-. Каждый из Rb, Rc и р был определен выше. В варианте осуществления Y может представлять собой -N(Rb)-C(O)-, -N(Rb)-S(O)2-, -С(O)-, -С(O)O-, -O-С(O)-, -C(O)-N(Rb)-, -S(O)p-, -O-, -S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O-, -N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb) -S(O)p-N(Rc) - или -C(O)-O-S(O)p-N(Rb)-. Каждый из Rb, Rc и р был определен выше. В одном варианте осуществления R2 может представлять собой водород, C1-6 алкил (например, метил, этил, н-бутил, или трет-бутил), арил (например, фенил), гетероарил (например, пиридил), арил-С 1-4 алкил (например, бензил) или гетероарил-C1-4 алкил (например, пиридилметил). В варианте осуществления R2 может представлять собой C1-4 алкил, фенил, пиридил, имидазолил, фуранил, тиенил, триазолил,-2 010418 тетразолил, бензил, фенилэтил, бензимидазолил, бензотиазолил, нафтилметил, нафтилэтил или -C1-2 алкилпиридил (т.е. пиридил-C1-2 алкил); каждый из которых независимо может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из фтора, хлора, трифторметила, метила, этила, аминокарбонила, алкилкарбониламино, сульфамоила, алкоксикарбонила и алкилкарбонилокси. В варианте осуществления R1 может представлять собой арил или гетероарил, например, R1 может представлять собой замещенный фенил, необязательно замещенный инданил или необязательно замещенный гетероарил, выбранный из группы, состоящей из бензо[1,3]диоксолила, бензо[b]тиофенила, бензоксадиазолила, бензотиадиазолила, бензоимидазолила, бензооксазолила, бензотиазолила, 2-оксобензооксазолила, пиридила, пиримидинила, 2,3-дигидробензо[1,4]диоксила, 2,3-дигидробензофурила, 2,3-дигидробензо[b]тиофенила,3,4-дигидробензо[1,4]оксазинила, 3-оксобензо[1,4]оксазинила, 1,1-диоксо-2,3-дигидро-бензо[b]тиофенила,[1,2,4]триазоло [1,5-а]пиридила, [1,2,4]триазоло[4,3-а]пиридила, хинолинила, хиноксалинила, хиназолинила,изохинолинила и циннолинила. В варианте осуществления m может составлять 0-2. В варианте осуществления Ra может представлять собой C1-4 алкил, C1-4 алкокси, C1-4 алкилтио, галоген, амино, оксо, аминокарбонил или алкоксикарбонил. В одном варианте осуществления Ra может быть замещенным в 6-положении. В варианте осуществления А 1 может представлять собой N, и А 2 может представлять собой NRb,или А 1 может представлять собой NRb, и А 2 может представлять собой N; где Rb может представлять собой водород или C1-4 алкил. В варианте осуществления m может составлять 0-2; R1 может представлять собой арил или гетероарил; 2R может представлять собой водород, C1-6 алкил, арил, гетероарил, -C1-4 алкиларил, или -C1-4 алкилгетероарил;X может представлять собой 4-8-членный моноциклический или бициклический циклоалкил или гетероциклоалкил (например, пиперидинил, пиперазинил, пирролидинил, тетрагидрофуран, циклогексил, циклопентил,бицикло[2.2.1]гептан,бицикло[2.2.2]октан,бицикло[3.2.1]октан,2-оксабицикло[2.2.2]октан,2 азабицикло[2.2.2]октан, 3-азабицикло[3.2.1]октан или 1-азабицикло[2.2.2]октан); и Y может представлять собой -N(Rb)-С(O)-, -N(Rb)-S(O)2-, -С(О)-, -С(O)-O-, -О-С(О)-, -C(O)-N(Rb)-, -S(O)p-, -О-, -S(O)2-N([Rb)-, -N(Rb)-, N(Rb)-C(O)-O-, -N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc)-, или -C(O)-O-S(O)p-N(Rb)-. В варианте осуществления, m может составлять 0-2; R1 может представлять собой арил (например,замещенный фенил) или гетероарил; R2 может представлять собой водород, C1-6 алкил (например, C1-4 алкил), арил, гетероарил, -C1-4 алкиларил (например, бензил) или -C1-4 алкилгетероарил (например, пиридилметил); X может представлять собой циклогексил, циклопентил, или бицикло[2.2.2]октан; и Y может представлять собой -N(Rb)-C(O)-, -N(Rb)-S(O)2-, -C(O)-, -C(O)-O-, -O-C(O)-, -C(O)-N(Rb)-, -S(O)p-, -O-, S(O)2-N(Rb)-, -N(Rb)-, -N(Rb)-C(O)-O- или -N(Rb)-C(O)-N(Rc)-, -C(O)-N(Rb)-S(O)p-N(Rc) -или -C(O)-OS(O)p-N(Rb)-, где каждый из Rb и Rc независимо может представлять собой водород или C1-4 алкил; А 1 может представлять собой N, и А 2 может представлять собой NH, или А 1 может представлять собой NH,и А 2 может представлять собой N; m может равным 1; и Ra может быть замещенным в 6-положении. Для соединений формулы (I), где m равен 1, Ra обычно может быть замещен в 6-положении. В варианте осуществления m может составлять 0-2; R1 может представлять собой арил (например,замещенный фенил) или гетероарил; R2 может представлять собой водород, C1-6 алкил (например, C1-4 алкил), арил, гетероарил, -C1-4 алкиларил (например, бензил) или -C1-4 алкилгетероарил (например, пиридилметил); -X-Y-может представлять собой А 1 может представлять собой N, и А 2 может представлять собой NH, или А 1 может представлять собой NH, и А 2 может представлять собой N; m может быть равным 1; и Ra может быть замещенным в 6 положении. Некоторые примеры соединений формулы (I) показаны ниже в примерах 5-215.N-оксидное производное или фармацевтически приемлемая соль каждого из соединений формулы(1) также включены в объем данного изобретения. Например, кольцевой атом азота имидазольного центрального кольца или азотсодержащий гетероциклический заместитель могут образовывать оксид в присутствии подходящего окислителя, такого как м-хлорпербензойная кислота или H2O2. Соединение формулы (I), которое является кислотным по своей природе (например, имеет карбоксильную или фенольную гидроксильную группу) может образовывать фармацевтически приемлемую соль, такую как соль натрия, калия, кальция или золота. Также в объем изобретения входят соли, образо-3 010418 ванные с фармацевтически приемлемыми аминами, такими как аммиак, алкиламины, гидроксиалкиламины и N-метилгликамин. Соединение формулы (I) может быть обработано кислотой с образованием кислотно-аддитивных солей. Примеры таких кислот включают хлористо-водородную кислоту, бромистоводородную кислоту, иодисто-водородную кислоту, серную кислоту, метансульфоновую кислоту, фосфорную кислоту, п-бромметилсульфоновую кислоту, угольную кислоту, янтарную кислоту, лимонную кислоту, бензойную кислоту, щавелевую кислоту, малоновую кислоту, салициловую кислоту, яблочную кислоту, фумаровую кислоту, аскорбиновую кислоту, малеиновую кислоту, уксусную кислоту и другие минеральные и органические кислоты, хорошо известные специалистам в данной области. Кислотноаддитивные соли могут быть получены обработкой соединения формулы (I) в виде свободного основания достаточным количеством кислоты (например, хлористоводородной кислоты) с получением кислотно-аддитивной соли (например, гидрохлоридной соли). Кислотно-аддитивная соль может быть преобразована обратно в свободное основание путем обработки соли подходящим разбавленным водным раствором основания (например, гидроксида натрия, бикарбоната натрия, карбоната калия или аммиака). Соединения формулы (I) также могут быть в виде ахиральных соединений, рацемических смесей, оптически активных соединений, чистых диастереомеров или смеси диастереомеров. Соединения формулы (I) проявляют неожиданно высокую аффинность к рецепторам типа I семейства TGF, например Alk 5 и/или Alk 4, со значениями IC50 и Ki меньше, чем 10 мкМ в условиях, описанных ниже в примерах 215 и 217, соответственно. Некоторые соединения формулы (I) проявляют значения IC50 и Ki меньше, чем 1 мкМ (как, например, ниже 50 нМ). Соединения формулы (I) также могут быть модифицированы путем присоединения подходящих функциональных групп для усиления селективных биологических свойств. Такие модификации известны в данной области и включают те, которые повышают биологическое проникновение в данную биологическую систему (например, кровь, лимфатическая система, центральная нервная система), повышают пероральную доступность, повышают растворимость для введения путем инъекции, изменяют метаболизм и/или изменяют скорость выведения. Примеры таких модификаций включают, но не ограничиваются указанным, этерификацию с использованием полиэтиленгликолей, получение производных с использованием пиволатов или заместителей на основе жирных кислот, превращение в карбаматы, гидроксилирование ароматических колец и введение гетероатомных заместителей в ароматические кольца. Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение формулы (I) (или комбинацию двух или более соединений формулы (I и по крайней мере один фармацевтически приемлемый носитель. Настоящее изобретение также относится к лекарственной композиции, включающей любое из соединений формулы (I), само по себе или в комбинации, вместе с подходящим эксципиентом. Изобретение также относится к способу ингибирования рецепторов I типа семейства TGF, Alk 5 и/или Alk 4, (например, со значениями IC50 меньше, чем 10 мкМ; например, меньше, чем 1 мкМ; и, например, меньше, чем 5 нМ) в клетке, включая стадию контактирования клетки с эффективным количеством одного или нескольких соединений формулы (I). В объем изобретения также входит способ ингибирования TGF и/или активинового сигнального пути в клетке или у субъекта (например, млекопитающего, такого как человек), включающий стадию контактирования клетки или введения субъекту эффективного количества одного или нескольких соединений формулы (I). Также в объем настоящего изобретения входит способ лечения субъекта или профилактики субъекта от состояния, характеризуемого или являющегося результатом повышенного уровня активности TGF и/или активина. Способ включает стадию введения субъекту эффективного количества одного или нескольких соединений формулы (I). Состояния включают, например, накопление избытка внеклеточного матрикса, фиброзное состояние (например, гломерулонефрит, диабетическая нефропатия, гипертензивная нефропатия, экзематозная нефропатия или нефрит, индуцированный гепатитом цирроз, фиброз желчных путей, склеродерма, легочный фиброз, постинфарктный сердечный фиброз, фибросклероз,фиброзные злокачественные новообразования, фиброиды, фиброма, фиброаденома или фибросаркома),TGF-индуцированные метастазы опухолевых клеток; и карциномы (например, карцинома легкого, молочной железы, печени, желчных путей, желудочно-кишечного тракта, головы и шеи, поджелудочной железы, простаты, шейки матки, а также множественная миелома, меланома, глиома или глиобластома). Как использовано в данном описании, выражение "алкильная" группа относится к насыщенной алифатической углеводородной группе, содержащей 1-8 (например, 1-6 или 1-4) атомов углерода. Алкильная группа может быть линейной или разветвленной. Примеры алкильной группы включают, но не ограничиваются указанным, метил, этил, пропил, изопропил, бутил, изобутил, вторбутил, трет-бутил, нпентил, н-гептил и 2-этилгексил. Алкильная группа необязательно может быть замещенной одним или несколькими заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси,гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси,сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкил-, алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарил-4 010418 карбониламино, гетероаралкилкарбониламино, остаток мочевины, остаток тиомочевины, сульфамоил,сульфамид, алкоксикарбонил или алкилкарбонилокси. Как использовано в данном описании выражение "алкенильная" группа относится к алифатической углеродной группе, которая содержит 2-8 (например, 2-6 или 2-4) атомов углерода и по крайней мере одну двойную связь. Как и алкильная группа, алкенильная группа может быть линейной или разветвленной. Примеры алкенильной группы включают, но не ограничиваются указанным, аллил, изопропенил, 2 бутенил и 2-гексенил. Алкенильная группа необязательно может быть замещенной одним или несколькими заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино,гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино,гетероаралкилкарбониламино, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид, алкоксикарбонил или алкилкарбонилокси. Как использовано в данном описании, выражение "алкинильная" группа относится к алифатической углеродной группе, которая содержит 2-8 (например, 2-6 или 2-4) атомов углерода и по крайней мере одну тройную связь. Алкинильная группа может быть линейной или разветвленной. Примеры алкинильной группы включают, но не ограничиваются указанным, пропаргил и бутинил. Алкинильная группа не обязательно может быть замещенной одним или несколькими заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино,нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкил-карбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, остаток мочевины, остаток тиомочевины, сульфамоил, сульфамид алкоксикарбонил или алкилкарбонилокси. Как использовано в данном описании, выражение "амино" группа относится к группе -NRXRY, где каждый из RX и RY независимо представляет собой водород, алкил, циклоалкил, (циклоалкил)алкил,арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил. Когда термин-NRX-. RX имеет такое же значение, как определено выше. Как использовано в данном описании, выражение арильная группа относится к фенилу, нафтилу или бензоконденсированной группе, содержащей 2-3 кольца. Например, бензоконденсированная группа включает фенил, конденсированный с одним или двумя C4-8 карбоциклическими фрагментами, например 1,2,3,4-тетрагидронафтил, инданил или флуоренил. Арил необязательно замещен одним или двумя заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеналкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино,арилкарбониламино,аралкилкарбониламино,(гетероциклоалкил)карбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина,тиомочевина, сульфамоил, сульфамид, оксо или карбамоил. Как использовано в данном описании, выражение аралкильная группа относится к алкильной группе (например, C1-4 алкильной группе), которая замещена арильной группой. Как алкил, так и арил являются такими, как определено выше. Примером аралкильной группы является бензил. Как использовано в данном описании, выражение "циклоалкильная" группа относится к алифатическому карбоциклическому кольцу из 3-10 (например, 4-8) атомов углерода. Примеры циклоалкильных групп включают циклопропил, циклопентил, циклогексил, циклогептил, адамантил, норборнил, кубил,октагидроинденил, декагидронафтил, бицикло[3.2.1]октил, бицикло[2.2.2]октил, бицикло[3.3.1]нонил и бицикло[3.2.3]нонил. Выражение "циклоалкенильная" группа, как оно использовано в данном описании,относится к неароматическому карбоциклическому кольцу из 3-10 (например, 4-8) атомов углерода, содержащему одну или несколько двойных связей. Примеры циклоалкенильных групп включают циклопентенил, 1,4-циклогексадиенил, циклогептенил, циклооктенил, гексагидроинденил, октагидронафтил,бицикло[2.2.2]октенил и бицикло[3.3.1]ноненил. Циклоалкильная или циклоалкенильная группы необязательно могут быть замещены одним или несколькими заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеналкил, такой как трифторметил), алкенил, алкинил, циклоалкил,(циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкил-5 010418 карбониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо, или карбамоил. Как использовано в данном описании, выражение "гетероциклоалкильная" группа относится к 3-10 членной (например, 4-8-членной) насыщенной кольцевой структуре, в которой один или несколько кольцевых атомов представляют собой гетероатом, например, N, О или S. Примеры гетероциклоалкильной группы включают пиперидинил, пиперазинил, тетрагидропиранил, тетрагидрофурил, диоксоланил, оксазолидинил, изооксазолидинил, морфолинил, октагидробензофурил, октагидрохроменил, октагидротиохроменил, октагидроиндолил, октагидропиридинил, декагидрохинолинил, октагидробензо[b]тиофенил,2-окса-бицикло[2.2.2]октил, 1-азабицикло [2 .2.2]октил, 3-аза-бицикло[3.2.1] октил и 2,6 диоксатрицикло[3.3.1. О 3,7] нонил. Выражение "гетероциклоалкенильная" группа, как оно использовано в данном описании, относится к 3-10-членной (например, 4-8-членной) неароматической кольцевой структуре, имеющей одну или более двойных связей, где один или несколько кольцевых атомов представляет собой гетероатом, напримерN, О или S. Гетероциклоалкильная или гетероциклоалкенильная группа необязательно может быть замещена одним или несколькими заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеналкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро,карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил) алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо, или карбамоил. Выражение "гетероарильная" группа, как оно использовано в данном описании, относится к моноциклической, бициклической или трициклической кольцевой структуре, имеющей 5-15 кольцевых атомов, где один или несколько из кольцевых атомов представляет собой гетероатом, например N, О или S,и где одно или более колец в бициклической или трициклической структуре является ароматическим. Некоторыми примерами гетероарила являются пиридил, фурил, пирролил, тиенил, тиазолил, оксазолил,имидазолил, индолил, тетразолил, бензофурил, бензтиазолил, ксантен, тиоксантен, фенотиазин, дигидроиндол и бензо[1,3]диоксол. Гетероарил необязательно является замещенным одним или несколькими заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеналкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил) алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, (гетероциклоалкил) карбониламино,(гетероциклоалкил) алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил,сульфамид, оксо или карбамоил. Выражение "гетероаралкильная" группа, как использовано в данном описании, относится к алкильной группе (например, C1-4 алкильной группе), которая замещена гетероарильной группой. Как "алкил", так и "гетероарил" были определены выше. Как использовано в данном описании, циклический фрагмент включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых был определен ранее. Как использовано в данном описании, выражение "ацильная" группа относится к формильной группе или группе алкил-С(=O)-, где "алкил" был определен ранее. Примерами ацильных групп являются ацетил и пивалоил. Как использовано в данном описании, выражение "карбамоильная" группа относится к группе,имеющей структуру -O-CO-NRxRy или -NRx-CO-O-Rz, где Rx и Ry были определены ранее, a Rz может представлять собой алкил, арил, аралкил, гетероциклоалкил, гетероарил, или гетероаралкил. Как использовано в данном описании, выражения "карбокси" и "сульфо" группа относятся к группам -СООН и -SO3H, соответственно. Как использовано в данном описании, выражение "алкоксильная" группа относится к группе алкилО-, где "алкил" был определен ранее. Как использовано в данном описании, выражение "сульфокси" группа относится к группам -O-SORx или -SO-O-Rx, где Rx был определен ранее. Как использовано в данном описании, выражение "галоген" или группа "галогена" относится к фтору, хлору, брому или йоду. Как использовано в данном описании, выражение "сульфамоильная" группа относится к структуре S(O)2-NRXRY или -NRX-S(O)2-RZ, где RX, RY и RZ были определены выше. Как использовано в данном описании, выражение "сульфамидная" группа относится к структуре -6 010418NRX-S(O)2-NRYRZ, где RX, RY и RZ были определены выше. Как использовано в данном описании, выражение группа мочевины относится к структуре -NRXCO-NRYRZ, а выражение группа "тиомочевины" относится к структуре -NRX-CS-NRYRZ. RX, RY и RZ были определены выше. Как использовано в данном описании, выражение эффективное количество определяется как количество, требуемое для оказания терапевтического действия на пациента, которого лечат, и обычно оно определяется с учетом возраста, площади поверхности, веса и состояния пациента. Взаимосвязь дозировок для животных и людей (из расчета на миллиграммы на квадратный метр поверхности площади тела) описаны в публикации Freireich et al., Cancer Chemother. Rep., 50: 219 (1966). Площадь поверхности тела может быть приблизительно определена из расчета роста и веса пациента. См., например, Scientific Tables, Geigy Pharmaceuticals, Ardsley, New York, 537 (1970). Как использовано в данном описании, выражение пациент относится к млекопитающему, включая человека. Выражение антагонист, как оно использовано в данном описании, относится к молекуле, которая связывается с рецептором без активации рецептора. Он конкурирует с эндогенным лигандом(ами) или субстратом(ами) за сайт(ы) связывания на рецепторе и, таким образом, ингибирует способность рецептора передавать внутриклеточный сигнал в ответ на связывание с эндогенным лигандом. Поскольку соединения формулы (I) представляют собой антагонисты TGF рецептора типа I (Alk 5) и/или активинового рецептора типа I (Alk 4), данные соединения полезны для ингибирования последствий TGF и/или активиновой трансдукции сигнала, таких как продуцирование внеклеточного матрикса(например, коллагена и фибронектина), дифференциация стромальных клеток в миофибробласты и стимуляция или миграция воспалительных клеток. Таким образом, соединения формулы (I) ингибируют патологические воспалительные и фиброзные ответные реакции и обладают терапевтической применимостью для лечения и/или профилактики нарушений или заболеваний, при которых желательно понижение активности TGF и/или активина (например, различные типы фиброза или прогрессирующий рак). Кроме того соединения формулы (I) могут использоваться для изучения и исследования роли TGF рецептора типа I (Alk 5) и/или активинового рецептора типа I (Alk 4), такой как их роль в клеточных процессах, например сигнальной трансдукции, продуцировании внеклеточного матрикса, дифференциации стромальных клеток в миофибробласты и стимулировании и миграции воспалительных клеток. Если не указано другого, все технические и научные термины, использованные в данном описании,имеют те же значения, которые обычно понятны специалистами в данной области, к которой принадлежит изобретение. Все отмеченные публикации, патентные заявки, патенты и другие ссылки включены в данное описание посредством ссылки во всей своей полноте. Кроме того, материалы, способы и примеры являются только иллюстративными и не предназначены для ограничения. Другие отличительные особенности и преимущества изобретения будут очевидны из следующего подробного описания и формулы изобретения. Подробное описание изобретения В общем, изобретение относится к соединениям формулы (I), которые проявляют неожиданно высокую аффинность к рецепторам семейства TGF типа I, Alk 5 и/или Alk 4. Синтез соединений формулы (I). Соединения формулы (I) могут быть получены рядом известных способов из коммерчески доступных или известных исходных веществ. В одном способе соединения формулы (I), где А 1 представляет собой N, и А 2 представляет собой NH, или А 1 представляет собой NH, и А 2 представляет собой N, получают в соответствии с представленными ниже схемой 1 а или схемой 1b. Конкретно, на схеме 1 а необязательно замещенный 2-метилпиридин(II) депротонируют с использованием LDA перед взаимодействием с метоксиметиламидомR1-(61 метилпиридил)кетона (III). R является таким, как определено ранее (см. ниже пример 3 В). Метоксиметиламид может быть получен взаимодействием соответствующего хлорангидрида кислоты (т.е., R1-COCl) с гидрохлоридом N,O-диметилгидроксиламина (см. ниже пример 2). Затем R1-(6-метилпиридил)кетон(III) может быть обработан нитритом натрия в уксусной кислоте с получением -кетооксима (IV), который можно подвергнуть дальнейшему взаимодействию с подходящим замещенным (и необязательно защищенным) альдегидом (VI) в присутствии ацетата аммония, давая соединение формулы (I). В другом способе описанные выше соединения формулы (I) могут быть получены в соответствии с приведенной далее схемой 1b. Конкретно, R1-замещенный пиридин-2-карбальдегид (IIa) первоначально подвергают взаимодействию с анилином и дифенилфосфитом с образованием конечного N,Р-ацеталя,который может в дальнейшем связываться с R1-замещенным альдегидом с образованием (R1 метил)пиридилкетона (IIIa). См., например, Journet et al., Tetrahedron Lett., 39: 1717-1720 (1998) и пример 3 С ниже. Обработка (R1-метил) пиридилкетона (IIIa) нитритом натрия в уксусной кислоте приводит к кетооксиму (IVa), который можно подвергнуть дальнейшему взаимодействию с подходящим замещенным (и необязательно защищенным) альдегидом (VI) в присутствии ацетата аммония, давая соединение формулы (I), как описано выше на схеме 1 а. Схема 1b Если соединение (VI) находится в защищенной форме, для полученного в результате соединения можно использовать подходящие агенты для снятия защитных групп после реакции конденсации соединения (IV) или (IVa) с соединением (VI), получая соединение формулы (I) (см., например, подходящие защитные группы в Т. W. Greene, Protective Groups in Organic Synthesis, John WileySons, Inc., NewYork (1981. Альтернативно, соединение формулы (I) может быть получено взаимодействием промежуточного соединения (IV) или (IVa) с альдегидом (VII) с получением следующего промежуточного соединения(VIII), которое далее может взаимодействовать с соединением (IX), давая соединение формулы (I). Отметим, что фрагменты Y' и Y" представляют собой предшественники фрагмента Y. (см. ниже схему 2). Кроме того, желаемые замещения в Ra могут быть получены, например, путем выбора подходящего промежуточного соединения (IIa) (см. ниже пример 3A). В некоторых вариантах осуществления фрагмент X в соединение (VII) представляет собой азотсодержащий гетероциклоалкил (например, пиперидин). Кольцевой атом азота может быть защищен с использованием защитной группы для азота (например, Cbz, Boc или FMOC) перед конденсацией с соединением (IV) или (IVa), с последующим снятием защитных групп (смотри первую стадию схемы 3), с получением соединения (VIIIa). Данное соединение далее может взаимодействовать с различными соединениями (IX), давая соединение формулы (I) (см. вторую стадию схемы 3 ниже). Следует отметить, что соединение (VIII) или соединение (VIIIa) могут также представлять собой соединение формулы (I). Схема 3-9 010418 Аналогично, когда фрагмент X в соединении (VII) представляет собой циклоалкил (например, циклопентил, циклогексил или бицикло[2.2.2]октан), он может быть дополнительно функционализирован с образованием соединения формулы (I), как указано на схемах 4, 5 а, 5b и 5 с ниже. Схема 4 Соединения формулы (I), где А 1 представляет собой N, и А 2 представляет собой NRb (или А 1 представляет собой NRb, и А 2 представляет собой N) могут быть получены известными способами. Например,соединения формулы (I) с незамещенным имидазолильным кольцевым ядром могут быть обработаны RbI- 13010418 и CsCO3 с получением соединения формулы (I), имеющего замещенное имидазолильное кольцевое ядро.(см., например, Liverton, et al., J. Med.Chem., 42:2180-2190 (1999. Соединения формулы (I), где А 1 представляет собой О, и А 2 представляет собой NH (или А 1 представляет собой NH, и А 2 представляет собой О), или где А 1 представляет собой S, и А 2 представляет собой NH (или А 1 представляет собой NH, и А 2 представляет собой S), могут быть получены в соответствии с известными способами. В одном из таких способов используется то же самое промежуточное соединение (III) или (IIIa), как описано выше (см., например, Revesz, et al., Bioorg.Med. Chem. Lett. 10: 1261-1264 (2000 и схему 6 ниже. Схема 6 Как хорошо известно специалистам в области химии, желаемые заместители могут быть введены в 2-пиридильное кольцо на последней стадии синтеза (см., например, пример 24 ниже). Применение соединений формулы (I) Как обсуждалось выше, гиперактивность сигнального пути TGF семейства может привести к избыточному накоплению внеклеточного матрикса и повышенным воспалительным ответным реакциям,которые затем могут привести к фиброзу тканей и органов (например, легкого, почки и печени) и, в конце концов, привести к повреждению органа. Смотри, например, Border W. А. и Ruoslahti E. J. Clin. Invest. 90: 1-7 (1992) и Border W. А. и Noble N. A., N. Engl. J. Med. 331: 1286-1292 (1994). Исследования показали, что экспрессия мРНК TGF и/или активина и уровень TGF и/или активина повышаются у пациентов, страдающих от различных фиброзных нарушений, например фиброзных заболеваний почек, индуцированного алкоголем или аутоиммунного гепатического фиброза, миелофиброза, блеомицининдуцированного легочного фиброза и идиопатического легочного фиброза. Соединения формулы (I), которые являются антагонистами рецепторов типа I TGF семейства Alk 5 и/или Alk 4 и ингибируют сигнальный путь TGF и/или активина, следовательно, могут использоваться для лечения и/или профилактики фиброзных заболеваний и заболеваний, опосредованных повышенным уровнем активности TGF и/или активина. Как использовано в данном описании, считается, что соединение ингибирует сигнальный путь TGF семейства, когда оно связывается (например, со значени- 14010418 ем IC50 меньшим, чем 10 мкМ; таким как меньше 1 мкМ и, например, меньше, чем 5 нМ) с рецептором пути (например, Alk 5 и/или Alk 4), конкурируя таким образом с эндогенным лигандом(ами) или субстратом(ами) за сайт связывания на рецепторе и снижая способность рецептора передавать межклеточный сигнал в ответ на связывание с эндогенным лигандом или субстратом. Вышеуказанные нарушения или заболевания включают любое состояние, характеризуемое (а) присутствием аномально высокого уровня TGF и/или активина; и/или (b) избыточным накоплением внеклеточного матрикса; и/или (с) повышенным количеством и синтетической активностью миофибробластов. Данные нарушения или заболевания включают, но не ограничиваются указанным, фиброзные состояния, такие как склеродерма,идиопатический легочный фиброз, гломерулонефрит, диабетическая нефропатия, экзематозная нефропатия, индуцированная гипертензией нефропатия, рубцевание глазного яблока или роговицы, фиброз печени или желчных путей, острое повреждение легких, легочный фиброз, постинфарктный сердечный фиброз, фибросклероз, фиброзные злокачественные новообразования, фиброиды, фиброма, фиброаденома и фибросаркома. Другие фиброзные состояния, для которых профилактическое лечение с использованием соединений формулы (I) может иметь терапевтическое значение, включают фиброз, индуцированный лучевой терапией, фиброз, индуцированный химиотерапией и хирургически индуцированное рубцевание, включая хирургические спайки, ламинектому и коронарный рестеноз. Также установлено, что повышенная TGF активность проявляется у пациентов с прогрессирующим раком. Исследования показали, что на поздних стадиях различных видов рака как опухолевые клетки, так и стромальные клетки в опухоли обычно сверхэкспрессируют TGF. Это приводит к стимуляции ангиогенеза и подвижности клеток, подавлению иммунной системы и повышенному взаимодействию опухолевых клеток с внеклеточным матриксом. Смотри, например, Hojo, M. et al., Nature 397: 530-534(1999). В результате опухолевые клетки становятся более инвазивными и метастазируют в отдаленные органы. Смотри, например, Maehara, Y. et al., J. Clin. Oncol. 17: 607-614 (1999) и Picon, A. et al., CancerEpidemiol. Biomarkers Prev. 7: 497-504 (1998). Таким образом, соединения формулы (I), которые являются антагонистами рецепторов типа I TGF семейства и ингибируют сигнальные пути TGF, также могут использоваться для лечения и/или профилактики поздних стадий различных видов рака, при которых сверхэкспрессируется TGF. Такие поздние стадии рака включают карциномы легкого, молочной железы, печени, желчных путей, желудочно-кишечного тракта, головы и шеи, поджелудочной железы, простаты, шейки матки, а также множественную миелому, меланому, глиому или глиобластому. Важно, и это следует отметить, что вследствие хронической и в некоторых случаях локализованной природы нарушений или заболеваний, опосредованных сверхэкспрессией TGF и/или активина (например, фиброза или злокачественных новообразований), лечение небольшими молекулами (как, например,лечение, описанное в данном изобретении) имеет преимущество в случае продолжительного лечения. Соединения формулы (I) не только полезны для лечения нарушений или заболеваний, опосредованных высокими уровнями активности TGF и/или активина, данные соединения также можно использовать для профилактики тех же самых нарушений или заболеваний. Известно, что полиморфизм, ведущий к повышенному продуцированию TGF и/или активина, связан с фиброзом и гипертензией. Действительно, высокие уровни TGF в сыворотке крови коррелируют с развитием фиброза у пациентов с раком молочной железы, которые получали лучевую терапию, с хроническим заболеванием трансплантатпротив-хозяина, идиопатическим интерстициальным пневмонитом, закупоркой вен у реципиентов трансплантатов и перитонеальным фиброзом у пациентов, подвергающихся постоянному амбулаторному перитонеальному диализу. Таким образом, уровни TGF и/или активина в сыворотке крови и мРНК TGF и/или активина в ткани может быть измерено и использоваться в качестве диагностических или прогностических маркеров для нарушений или заболеваний, опосредованных сверхэкспрессией TGF и/или активина, и полиморфизмы в гене для TGF, который определяет продуцирование TGF и/или активина,также могут использоваться для предсказания подверженности к таким нарушениями или заболеваниям. Смотри, например, Blobe, G. С. et al., N. Engl. J. Med. 342 (18): 1350-1358 (2000); Matsuse, T. et al., Am. J.(1998). Введение соединений формулы (I) Как определено выше эффективное количество представляет собой количество, требуемое для оказания терапевтического действия на пациента, которого лечат. Для соединения формулы (I) эффективное количество может колебаться, например, от примерно 1 до примерно 150 мг/кг (например, от примерно 1 до примерно 100 мг/кг). Эффективные дозы также будут изменяться, как понятно специалистам в данной области, в зависимости от пути введения, используемого эксципиента и возможности совместного использования с другим терапевтическим лечением, включая применение других терапевтических агентов и/или лучевой терапии. Соединения формулы (I) можно вводить любым путем, подходящим для введения фармацевтических соединений, включая, но не ограничиваясь указанным, пилюли, таблетки, капсулы, аэрозоли, суп- 15010418 позитории, жидкие композиции для приема внутрь или инъекции или для применения в качестве глазных или ушных капель, пищевых добавок и местных препаратов. Фармацевтически приемлемые композиции включают водные растворы активного агента в изотоническом физиологическом растворе, 5%-ном растворе глюкозы или другом хорошо известном фармацевтически приемлемом эксципиенте. Солюбилизирующие агенты, такие как циклодекстрины, или другие солюбилизирующие агенты,хорошо известные специалистам в данной области, могут использоваться в качестве фармацевтических эксципиентов для доставки терапевтических соединений. Что касается пути введения, композиции могут вводиться перорально, интраназально, чрескожно, внутрикожно, вагинально, внутриушно, путем внутриглазного введения, буккально, ректально, через слизистую оболочку или посредством ингаляции, имплантации (например, хирургической) или путем внутривенного введения. Композицию можно вводить животному (например, млекопитающему, такому как человек, не являющийся человеком примат, лошадь, собака, корова, свинья, овца, коза, кошка, мышь, крыса, морская свинка, кролик, хомяк, песчанка или хорек, или птице, или рептилии, такой как ящерица). Необязательно соединения формулы (I) могут вводиться в сочетании с одним или несколькими другими агентами, которые ингибируют TGF сигнальный путь или используются для лечения соответствующих патологических нарушений (например, фиброза или прогрессирующего рака) за счет использования различных механизмов действия. Примеры таких агентов включают ингибиторы ангиотензинконвертирующего фермента, нестероидные и стероидные противовоспалительные агенты, а также агенты, которые антагонизируют связывание лиганда или активацию TGF рецепторов, например антитела против TGF и против TGF-рецепторов, или антагонисты TGF рецепторов типа II. Изобретение будет дополнительно описано в следующих примерах, которые не ограничивают объем изобретения, представленный в формуле изобретения. Синтез иллюстративных промежуточных соединений (IIa), (III), (IIIa), (IV), (V) и (VII) описан ниже в примерах 1-4. Пример 1. Бензиловый эфир (4-формилциклогексил)карбаминовой кислоты (VII) Синтез указанного в заголовке соединения описан ниже в частях (а)-(с).(a) 4-Бензилоксикарбониламиноциклогексанкарбоновая кислота Бензилхлорформиат (2,2 мл, 15,4 ммоль) добавляли к раствору 4-аминоциклогексанкарбоновой кислоты (2 г, 14,0 ммоль) в смеси 1,4-диоксана (5 мл) и насыщенного водного раствора бикарбоната натрия(5 мл). Смесь перемешивали при 0 С в течение 3 ч. Диоксан удаляли при пониженном давлении. Остаток распределяли между этилацетатом и водой. Этилацетатный раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали, и концентрировали, получая 2,3 г (59%) 4 бензилоксикарбониламиноциклогексанкарбоновую кислоту в виде желтого масла. Масс-спектр (ESP-)(b) Бензиловый эфир (4-(метоксиметилкарбамоил)циклогексил)карбаминовой кислоты К раствору 4-бензилоксикарбониламиноциклогексанкарбоновой кислоты (2,3 г, 8,3 ммоль) в дихлорметане (20 мл) медленно добавляли оксалилхлорид (0,796 мл, 9,1 ммоль). Смесь перемешивали при комнатной температуре в атмосфере азота в течение 1 ч. Растворитель удаляли при пониженном давлении. К остатку после реакции добавляли гидрохлорид N,O-диметилгидроксиламина (0,971 г, 9,96 ммоль) в безводном пиридине (10 мл). Смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении и остаток распределяли между этилацетатом и водой. Этилацетатный раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали, получая 1,0 г (38%) бензилового эфира (4-(метоксиметилкарбамоил)циклогексил)карбаминовой кислоты в виде желтого масла. 1(с) Бензиловый эфир (4-формилциклогексил) карбаминовой кислоты Диизобутилалюминийгидрид (1,0 М раствор, 6,24 мл, 6,24 ммоль) медленно добавляли к раствору бензилового эфира (4-(метоксиметилкарбамоил)циклогексил)карбаминовой кислоты (1,0 г, 3,12 ммоль) в безводном ТГФ (20 мл) при -78 С. Смесь перемешивали при -78 С в течение 1 ч. Добавляли воду (2 мл) при 0 С. Смесь распределяли между этилацетатом и водой. Этилацетат промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали, получая 0,60 г (74%) бензилового эфира (4-формилциклогексил)карбаминовой кислоты в виде желтого масла. 1 Н ЯМР (400 МГц,CDCl3)9,66 (с, 1 Н), 7,36 (5 Н), 3,63 (м, 1 Н), 2,38 (м, 1 Н), 1,77 (м, 4 Н), 1,18 (м, 4 Н). Пример 2. Метоксиметиламид бензо[1,3]диоксол-5-карбоновой кислоты (V) Гидроксид натрия (12,0 г, 300 ммоль) в воде (15 мл) медленно добавляли к раствору пиперонилхлорида (5,55 г, 30 ммоль) и гидрохлорида N,О-диметилгидроксиламина (3,53 г, 36 ммоль) в ацетонитриле(200 мл). Смесь перемешивали при комнатной температуре в течение 0,5 ч. Ацетонитрил удаляли при пониженном давлении, и остаток распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. Ко- 16010418 лоночная хроматография на силикагеле при элюировании смесью этилацетат:гексан (30:70) давала 5,5 г(88%) указанного в заголовке соединения в виде желтого масла. Масс-спектр (ES+) m/z 210,1 (М+1). 1H ЯМР (400 МГц, CDCl3)7,34 (м, 1 Н), 7,26 (д, 1 Н, J = 1,3 Гц), 6,86 (д, 1 Н, J = 8,1 Гц), 6,05 (с, 2 Н), 3,61 (с,3H), 3,38 (с, 3H). Пример 3A. 6-Циклопропилпиридин-2-карбальдегид (IIa) Синтез указанного в заголовке соединения описан ниже в частях (а)-(с).(a) 2-Бром-6-[1,3]диоксолан-2-илпиридин Смесь 6-бромпиридин-2-карбальдегида (2,0 г, 10,75 ммоль), этиленгликоля (3 мл, 53,75 ммоль) и каталитического количества TsOH в толуоле (50 мл) нагревали при кипении с обратным холодильником с ловушкой Дина-Старка в течение 1,5 ч, охлаждали до комнатной температуры и концентрировали в вакууме. Остаток очищали на колонке с силикагелем с использованием 2% EtOAc в CH2Cl2, получая 2 бром-6-[1,3]диоксолан-2-илпиридин в виде бесцветной жидкости (1,97 г, 80%).(b) 2-Циклопролил-6-[1,3] диоксолан-2-илпиридин К раствору ZnCl2 в ТГФ (0,5 М, 25 мл) добавляли по каплям раствор циклопропилмагнийбромида(0,5 М, 25 мл) при -78 С в атмосфере азота. Реакционную смесь затем оставляли нагреваться до комнатной температуры и перемешивали в течение часа. Затем вышеуказанную смесь переносили в герметически закрытую ампулу с 2-бром-6-[1,3]диоксолан-2-илпиридином (1,9 г, 8,25 ммоль, см. выше подраздел(а и Pd(PPh3)4 (0,4 г, 0,35 ммоль). ТСХ показала в основном образование продукта и некоторое количество исходного вещества. Затем смесь нагревали при 120 С в течение 2 ч и охлаждали до комнатной температуры и затем обрабатывали EtOAc и насыщенным раствором хлорида аммония и сушили надMgSO4. Остаток от концентрирования очищали на колонке с силикагелем с использованием 5% EtOAc в(с) 6-Циклопропилпиридин-2-карбальдегид Смесь 2-циклопропил-6-[1,3]диоксолан-2-илпиридина (0,9 г, см. выше подраздел (b и каталитического количества гидрата TsOH в смеси ацетона (10 мл) и воды (2 мл) нагревали при кипении с обратным холодильником в течение ночи до тех пор, пока большая часть исходных веществ не расходовалась по данным ТСХ. Затем смесь охлаждали до комнатной температуры и концентрировали. Остаток растворяли в диэтиловом эфире и промывали насыщенным раствором карбоната натрия и затем водой, а затем сушили над MgSO4 и концентрировали. Концентрат очищали на колонке с силикагелем с использованием 100% CH2Cl2, получая 6-циклопропилпиридин-2-карбальдегид в виде яркой жидкости (0,65 г, 94%). 1H ЯМР (CDCl3, 300 МГц)9,90 (с, 1 Н), 7,58 (м, 2 Н), 7,23 (м, 1 Н), 2,01 (м, 1 Н), 1,02-0,92 (м, 4 Н). Указанный в заголовке альдегид превращали в соответствующий N,Р-ацеталь для получения кетона в соответствии со схемой 1b выше. Пример 3B. 1-Бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этанон (III) н-Бутиллитий (2,5 М в гексане, 13,8 мл, 34,4 ммоль) медленно добавляли к раствору диизопропиламина (4,53 мл, 32,3 ммоль) в безводном ТГФ (50 мл) при -78 С. После перемешивания в течение 0,1 ч смесь оставляли нагреваться до 0 С. Перемешивание продолжали в течение 0,5 ч. Затем смесь охлаждали до -78 С и медленно добавляли 2,6-лутидин (3,76 мл, 32,3 ммоль). Смесь оставляли нагреваться до 0 С и перемешивали в течение 0,5 ч. Затем смесь охлаждали до -78 С, после чего медленно добавляли метоксиметиламид бензо[1,3] диоксол-5-карбоновой кислоты (4,5 г, 21,5 ммоль; см. пример 2 выше) в безводном ТГФ (10 мл). Смесь перемешивали при -78 С в течение 0,5 ч, при 0 С в течение 0,5 ч и при комнатной температуре в течение 2 ч. Смесь затем гасили водным раствором хлорида аммония и экстрагировали этилацетатом. Экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия,фильтровали и концентрировали. После очистки с использованием колоночной хроматографии на силикагеле (элюент: этилацетат (2): гексан (8, получали 4,8 г (87%) 1-бензо[1,3]диоксол-5-ил-2-(6 метилпиридин-2-ил)этанона В виде желтого твердого вещества. Масс-спектр (ESP+) m/z 256,1 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,56 (т, 1 Н, J = 7,5 Гц), 7,39 (дд, 1 Н, J = 1,8 Гц, 8,3 Гц), 7,30 (дд, 1 Н, J = 0,5 Гц, 1,8 Гц), 6,93 (м, 1 Н), 6,83 (м, 2 Н), 5,98 (с, 2 Н), 4,87 (с, 2 Н), 2,50 (с, 3H). Пример 3 С. (6-Метилпиридин-2-ил)-2-[1,2,4]триазоло[1,5-а]пиридин-6-илэтанон (IIIa) Синтез указанного в заголовке соединения описан ниже в частях (а) и (b).(а) [1,2,4]Триазоло[1,5-а]пиридин-6-карбальдегид К раствору 6-иод-[1,2,4]триазоло[1,5-а]пиридина (5,0 г, 20 ммоль; получен из 2-амино-5 иодпиридина (Aldrich-Sigma, St. Louis, МО) в соответствии с WO 01/62756) в безводном ТГФ (300 мл) при 0 С медленно добавляли раствор изопропилмагнийбромида в ТГФ (1 М, 31 мл, 31 ммоль). Полученную молочную суспензию перемешивали при 0 С. Через час к суспензии добавляли при 0 С ДМФ (6 мл,50 ммоль) и суспензию оставляли нагреваться до комнатной температуры и перемешивали дополнительно в течение 4 ч. Затем при комнатной температуре добавляли 100 мл воды и перемешивали в течение 1 ч. Полученную смесь экстрагировали диэтиловым эфиром и промывали насыщенным раствором Na2CO3. Экстракты сушили над MgSO4 и концентрировали. Остаток очищали на тонком слое силикагеля с использованием EtOAc, получая [1,2,4]триазоло[1,5-а] пиридин-6-карбальдегид в виде светло-желтого(b) 1-(6-Метилпиридин-2-ил)-2-[1,2,4]триазоло[1,5-а]пиридин-6-илэтанон К раствору [1,2,4]триазоло[1,5-а]пиридин-6-карбальдегида (3 г, 20 ммоль; см. подраздел (а) выше) и дифенилового эфира [(6-метилпиридин-2-ил)фениламинометил]фосфоновой кислоты (8,8 г, 20 ммоль; получен из 6-метилпиридин-2-карбоксальдегида (Aldrich-Sigma, St. Louis, МО) в соответствии с Tetrahedron Lett. 39: 1717-1720 (1998 в смеси ТГФ (40 мл) и iPrOH (10 мл) добавляли Cs2CO3 (8,6 г, 26 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. К вышеуказанной смеси добавляли по каплям раствор 3 н HCl (30 мл) и перемешивали в течение 1 ч. Затем смесь разбавляли МТВЕ (метилтрет-бутиловым эфиром) и экстрагировали дважды 1 н HCl. Водный экстракт нейтрализовали примерно 50% KOH до рН 7-8, при этом образовывался осадок. Осадок собирали, промывали водой и сушили, получая 1-(6-метилпиридин-2-ил)-2-[1,2,4]триазоло[1,5-а]пиридин-6-илэтанон в виде не совсем белого твердого вещества (2,9 г). Фильтраты экстрагировали EtOAc, сушили над MgSO4 и концентрировали. Остаток перекристаллизовывали из смеси iPrOH/H2O, получая дополнительную порцию целевого продукта (0,6 г). ESP+, m/e 253. 1H ЯМР (CDCl3, 300 МГц)8,6 (с, 1 Н), 8,29 (с, 1 Н), 7,87 (д, 1 Н), 7,72 (т, 1 Н),7,70 (д, 1 Н), 7,53 (дд, 1 Н), 7,36 (д, 1 Н), 4,61 (с, 2 Н), 2,66 (с, 3H). Пример 4. 1-Бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион 2-оксим (IV) Нитрит натрия (0,405 г, 5,88 ммоль) добавляли к раствору 1-бензо [1,3]диоксол-5-ил-2-(6 метилпиридин-2-ил)этанона (1,0 г, 3,92 ммоль; см. выше пример 3B) в смеси НОАс/ТГФ/H2O (6:4:1, 22 мл). Смесь перемешивали при 0 С в течение 1 ч и затем при комнатной температуре в течение 1 ч. Растворитель удаляли при пониженном давлении. Остаток растворяли в воде и добавляли NaOH (3H), до тех пор, пока значение рН не превышало 8. Водный раствор затем экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали, получая 0,90 г (81%) 1-бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион 2 оксима в виде желтого вспененного вещества. Масс-спектр (ESP+) m/z 285,1 (М+1). 1H ЯМР (CDCl3, 300 МГц)7,49 (м, 4 Н), 7,09 (д, 1 Н, J = 7,5 Гц), 6,81 (д, 1 Н, J = 7,8 Гц), 6,04 (с, 2 Н), 2,43 (с, 3H). Синтез иллюстративных соединений формулы (I) описан далее в примерах 5-24. Пример 5. Бензиловый эфир 4-(4-бензо[1,3]диоксол-5-ил-5-(6-метил-пиридин-2-ил)-1 Н-имидазол-2 ил)пиперидин-1-карбоновой кислоты 4-Формил-N-Cbz-пиперидин (0,297 г, 1,2 ммоль) добавляли к раствору 1-бензо[1,3]диоксол-5-ил-2(6-метилпиридин-2-ил)этан-1,2-дион 2-оксима (0,280 г, 1,0 ммоль, см. пример 4) и ацетата аммония (1,54 г, 20,0 ммоль) в уксусной кислоте (10 мл). Смесь нагревали при кипении с обратным холодильником в течение 2 ч. Растворитель удаляли при пониженном давлении. Реакционную смесь затем гасили смесью аммиак/лед. Водный раствор экстрагировали этилацетатом. Экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,12 г (23%) гидроксиимидазола в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 513,2 (M+1). Вышеуказанный гидроксиимидазол (0,50 г, 0,98 ммоль) добавляли к раствору TiCl3/HCl (10%, 5 мл) и метанолу (20 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,16 г (33%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 497,3 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,71 (т, 1 Н, J = 7,8 Гц), 7,35 (м, 6 Н), 7,26 (д, 1 Н, J = 7,8 Гц), 7,01 (м,3H), 6,07 (с, 2 Н), 5,16 (с, 2 Н), 4,35 (м, 2 Н), 3,36 (м, 1 Н), 3,03 (м, 2 Н), 2,64 (с, 3H), 2,11 (м, 2 Н), 1,87(м, 2 Н). Пример 6. Бензиловый эфир 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1 Н-имидазол-2 ил)пиперидин-1-карбоновой кислоты Бензиловый эфир 4-(4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-пиридин-2-ил-1 Н-имидазол-2 ил)пиперидин-1-карбоновой кислоты (0,9 г, 1,8 ммоль), который был получен из 4-формил-N-Cbzпиперидина и 1-бензо[1,3]диоксол-5-ил-2-(пиридин-2-ил)этан-1,2-дион 2-оксима по методике, аналогичной описанной в примере 5, добавляли к раствору TiCl3/HCl (10%, 15 мл) и метанолу (20 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. Колоночная хроматография на силикагеле с использованием смеси метанол:дихлорметан (5:95) давала 0,52 г (60%) указанного в заголовке соединения в виде желтого вспененного вещества. Масс-спектр (ESP+) m/z 483,02 (М+1). 1H ЯМР (400 МГц, CDCl3)8,50 (м, 1 Н), 7,50 (м, 2 Н), 7,34 (м, 5 Н), 7,09 (м, 3H), 6,85 (д, 1 Н, J = 7,9 Гц),6,00 (с, 2 Н), 5,14 (с, 2 Н), 4,29 (м, 2 Н), 3,00 (м, 3H), 2,10 (м, 2 Н), 1,81 (м, 2 Н). Пример 7. Бензиловый эфир 3-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2 ил]пиперидин-1-карбоновой кислоты Бензиловый эфир 3-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2- 18010418 ил]пиперидин-1-карбоновой кислоты (0,50 г, 0,98 ммоль), который был получен из 3-формил-N-Cbzпиперидина и 1-бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион-2-оксима по методике,аналогичной описанной в примере 5, добавляли к раствору TiCl3/HCl (10%, 5 мл) и метанолу (20 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,15 г (30%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 497,2 (М+1). 1H ЯМР (400 МГц,Метанол-d4)7,78 (т, 1 Н, J = 7,9 Гц), 7,34 (м, 7 Н), 7,01 (м, 3H), 6,08 (с, 2 Н), 5,16 (с, 2 Н), 4,41 (м, 1 Н), 4,15(м, 1 Н), 3,22 (м, 2 Н), 3,10 (м, 1 Н), 2,66 (с, 3H), 2,26 (м, 1 Н), 1,92 (м, 2 Н), 1,64 (м, 1 Н). Пример 8. Бензиловый эфир 3-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2 ил]пирролидин-1-карбоновой кислоты Бензиловый эфир 3-[4-бензо[1,3]диоксол-5-ил-1-гидрокси-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2 ил]пирролидин-1-карбоновой кислоты (0,180 г, 0,361 ммоль), который был получен из 3-формил-N-Cbzпирролидина и 1-бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион 2-оксима по методике,аналогичной описанной в примере 5, добавляли к раствору TiCl3/HCl (10%, 2 мл) и метанолу (10 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,03 г (17%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 483,14 (M+1). 1H ЯМР (400 МГц,Метанол-d4)7,84 (т, 1 Н, J = 8,0 Гц), 7,37 (м, 7 Н), 7,01 (м, 3H), 6,07 (с, 2 Н), 5,16 (с, 2 Н), 4,01 (м, 1 Н), 3,83(м, 1 Н), 3,74 (м, 1 Н), 3,55 (м, 1 Н), 2,68 (с, 3H), 2,50 (м, 1 Н), 2,36 (м, 1 Н). Пример 9. 2-(5-Бензо[1,3]диоксол-5-ил-2-пиперидин-4-ил-3H-имидазол-4-ил)-6-метилпиридин Палладий на активированном угле (0,010 г) добавляли к раствору бензилового эфира 4-(4 бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты(0,100 г, 0,20 ммоль; см. пример 5) в метаноле (5 мл). Реакционную смесь перемешивали в атмосфере водорода в течение 4 ч. Смесь затем фильтровали и концентрировали, получая 0,070 г (97%) указанного в заголовке соединения в виде желтого масла. Масс-спектр (ESP+) m/z 363,2 (M+1). Масс-спектр (ESP+)(0,050 г, 0,14 ммоль; см. пример 9) в безводном ТГФ (3 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении, и остаток растворяли в 1 мл ДМСО. Раствор в ДМСО фильтровали и вводили в колонку препаративной ВЭЖХ. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,005 г (7%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 517,2 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,73 (т, 1 Н, J = 7,7 Гц), 7,42 (м, 5 Н), 7,33 (д, 1 Н, J = 7,3 Гц), 7,27 (д, 1 Н, J = 7,3 Гц),6,07 (с, 2 Н), 4,40 (с, 2 Н), 3,82 (м, 2 Н), 3,19 (м, 1 Н), 2,85 (м, 2 Н), 2,66 (с, 3H), 2,10 (м, 2 Н), 1,92 (м, 2 Н). Пример 11. 2-[5-Бензо[1,3]диоксол-5-ил-2-(1-фенилметансульфонил-пиперидин-4-ил)-3H-имидазол 4-ил]пиридин-Толуолсульфонилхлорид (0,023 г, 0,12 ммоль) и диизопропилэтиламин (0,026 мл, 0,15 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5-ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,035 г,0,10 ммоль, в 3 мл безводного ТГФ), который получали из бензилового эфира 4-(4-бензо[1,3]диоксол-5 ил-5-пиридин-2-ил-1 Н-имидазол-2-ил)пиперидин-1-карбоновой кислоты по методике, аналогичной описанной в примере 9. Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении, и остаток растворяли в 1 мл ДМСО. Раствор в ДМСО фильтровали и вводили в колонку препаративной ВЭЖХ. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,005 г (10%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 503,1 (М + 1). 1 Н ЯМР (400 МГц, Метанол-d4)8,67 (м, 1 Н), 7,82(м, 1 Н), 7,42 (м, 7 Н), 7,02 (м, 3H), 6,07 (с, 2 Н), 4,38 (с, 2 Н), 3,81 (м, 2 Н), 3,17 (м, 1 Н), 2,85 (м, 1 Н), 2,10 (м,2 Н), 1,90 (м, 2 Н). Пример 12. 2-[5-Бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4 ил]пиридин Метансульфонилхлорид (0,009 мл, 0,12 ммоль) и диизопропилэтиламин (0,026 мл, 0,15 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5-ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,035 г,- 19010418 0,10 ммоль; получен, как описано в примере 11) в безводном ТГФ (3 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении и остаток растворяли в 1 мл ДМСО. Раствор в ДМСО фильтровали и вводили в колонку препаративной ВЭЖХ. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,012 г (28%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 427,1 (M+1). 1H ЯМР (400 МГц, CDCl3)8,65 (м, 1 Н), 7,83 (м, 1 Н), 7,56 (м, 1 Н), 7,45 (м, 1 Н), 7,03 (дд, 1 Н, J = 1,8 Гц, 8,1 Гц), 6,97 (д, 1 Н, J = 1,8 Гц), 6,88 (д, 1 Н, J = 8,1Hz), 6,05 (с, 2 Н), 3,91 (м, 2 Н), 3,47 (м, 1 Н), 2,89 (м, 2 Н),2,84 (с, 3H), 2,22 (м, 2 Н), 2,11 (м, 2 Н). Пример 13. 2-[5-Бензо[1,3]диоксол-5-ил-2-(1-метансульфонилпиперидин-4-ил)-3H-имидазол-4-ил]6-метилпиридин Метансульфонилхлорид (0,009 мл, 0,12 ммоль) и диизопропилэтиламин (0,026 мл, 0,15 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5-ил-2-пиперидин-4-ил-3H-имидазол-4-ил)-6-метилпиридина(0,036 г, 0,10 ммоль; см. пример 9) в безводном ТГФ (3 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении, и остаток растворяли в 1 мл ДМСО. Раствор в ДМСО фильтровали и вводили в колонку препаративной ВЭЖХ. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,011 г (25%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 441,2 (M+1). 1 Н ЯМР (400 МГц, Метанол-d4)7,74 (т, 1 Н, J=7,9 Гц), 7,34 (м, 1 Н), 7,28 (м,1 Н), 7,03 (м, 3H), 6,08 (с, 2 Н), 3,92 (м, 2 Н),3,25 (м, 1 Н), 2,94 (м, 2 Н), 2,90 (с, 3H), 2,66 (с, 3H), 2,23 (м, 2 Н), 2,03 (м, 2 Н). Пример 14. 2-Хлорбензиловый эфир 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1 Н-имидазол-2 ил)пиперидин-1-карбоновой кислоты 2-Хлорбензилхлорформиат (0,011 мл, 0,070 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5 ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,021 г, 0,059 ммоль; получен, как описано в примере 11) в смеси ТГФ (3 мл) и 2 М водного раствора бикарбоната натрия (0,3 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Смесь распределяли между этилацетатом и водой. Органический раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,026 г(70%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 517,03 (M+1). 1H ЯМР (400 МГц, CDCl3)8,60 (м, 1 Н), 7,81 (м, 1 Н), 7,60 (д, 1 Н, J = 8,2 Гц), 7,39 (м, 3H),7,27 (м, 2 Н), 7,07 (дд, 1 Н, J = 8,1, 1,8 Гц), 6,99 (д, 1 Н, J = 1,8 Гц), 6,90 (д, 1 Н, J = 8,1 Гц), 6,05 (с, 2 Н), 5,24(с, 2 Н), 4,36 (м, 2 Н), 3,48 (м, 1 Н), 2,98 (м, 2 Н), 2,17 (м, 2 Н), 1,86 (м, 2 Н). Пример 15. 2,4-Дихлорбензиламид 4-(4-бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1 Н-имидазол-2 ил)пиперидин-1-карбоновой кислоты 2,3-Дихлорбензилизоцианат (0,009 мл, 0,07 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5 ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,021 г, 0,059 ммоль; получен, как описано в примере 11) и диизопропилэтиламина (0,031 мл, 0,177 ммоль) в безводном ТГФ (5 мл). Смесь перемешивали при комнатной температуре в течение 2 ч и распределяли между этилацетатом и водой. Органический раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,016 г(41%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 550,2 (M+1). 1 Н ЯМР (400 МГц, CDCl3)8,58 (м, 1 Н), 7,80 (м, 1 Н), 7,56 (д, 1 Н, J = 8,2 Гц), 7,39 (м, 1 Н),7,32 (д, 1 Н, J = 2,1 Гц), 7,25 (д, 1 Н, J = 8,2 Гц), 7,14 (дд, 1 Н, J = 8,2, 2,0 Гц), 7,03 (дд, 1 Н, J = 8,1, 1,8 Гц),6,95 (д, 1 Н, J = 1,6 Гц), 6,87 (д, 1 Н, J = 8,0 Гц), 6,04 (с, 2 Н), 4,38 (с, 2 Н), 4,11 (м, 2 Н), 3,48 (м, 1 Н), 2,99 (м,2 Н), 2,14 (м, 2 Н), 1,92 (м, 2 Н). Пример 16. 1-[4-(4-Бензо[1,3]диоксол-5-ил-5-пиридин-2-ил-1 Н-имидазол-2-ил)пиперидин-1 ил]этанон Уксусный ангидрид (0,011 мл, 0,12 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5-ил-2 пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,035 г, 0,10 ммоль; получен, как описано в примере 11) и диизопропилэтиламина (0,021 мл, 0,12 ммоль) в безводном ТГФ (3 мл). Смесь перемешивали при комнатной температуре в течение 18 ч и распределяли между этилацетатом и водой. Органический раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,010 г (26%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 391,2 (M+1). 1H ЯМР (400 МГц, Метанол-d4)8,59 (м, 1 Н), 7,73 (м, 1 Н), 7,34 (м, 2 Н), 6,94 (м, 3H), 5,98 (с, 2 Н), 4,83 (с,3H), 4,60 (м, 2 Н), 4,01 (м, 2 Н), 3,28 (м, 3H), 2,69 (м, 2 Н). Пример 17. 2-[5-Бензо[1,3]диоксол-5-ил-2-(1-фуран-2-ил-метилпиперидин-4-ил)-3H-имидазол-4 ил]пиридин Триацетоксиборгидрид натрия (0,030 г, 0,14 ммоль) добавляли к раствору 2-(5-бензо[1,3]диоксол-5 ил-2-пиперидин-4-ил-3H-имидазол-4-ил)пиридина (0,035 г, 0,10 ммоль; получен, как описано в примере 11) и фуран-2-карбальдегида (0,0083 мл, 0,10 ммоль) в дихлорметане (5 мл). Смесь перемешивали при комнатной температуре в течение 18 ч, фильтровали и концентрировали. ВЭЖХ очистка с использовани- 20010418 ем элюирования смесью ацетонитрил:вода давала 0,010 г (23%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 429,1. 1H ЯМР (400 МГц, ДМСО-d6)8,67(м,1 Н), 7,87 (м, 2 Н), 7,44 (м, 2 Н), 7,09 (м, 3H), 6,73 (д, 1 Н, J = 3,2 Гц), 6,60 (м, 1 Н), 6,12 (с, 2 Н), 4,45 (с, 2 Н),3,54 (м, 2 Н), 3,26 (м, 1 Н), 3,11 (м, 2 Н), 2,33 (м, 2 Н), 2,06 (м, 2 Н). Пример 18. Бензиловый эфир 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол 2-ил]циклогексилкарбаминовой кислоты Бензиловый эфир (4-формилциклогексил)карбаминовой кислоты (0,133 г, 0,507 ммоль; см. пример 1 выше) добавляли к раствору 1-бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион 2-оксима(0,120 г, 0,422 ммоль; см. пример 4) и ацетата аммония (0,651 г, 8,44 ммоль) в уксусной кислоте (5 мл). Смесь нагревали при кипении с обратным холодильником в течение 2 ч и растворитель удаляли при пониженном давлении. Реакционную смесь затем гасили смесью аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,035 г (16%) гидроксиимидазола в виде желтого твердого вещества. Массспектр (ESP+) m/z 527,2 (M+1). Вышеуказанный гидроксиимидазол (0,100 г, 0,190 ммоль) добавляли к раствору TiCl3/HCl (10%, 2 мл) и метанолу (10 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,015 г(15%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 511,2 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,68 (м, 1 Н), 7,33 (м, 6 Н), 7,22 (м, 1 Н), 7,01 (м, 3H), 6,07 (с,2 Н), 5,08 (с, 2 Н), 3,52(м, 1 Н), 3,09(м, 1 Н), 2,66 (с, 3H), 2,16 (м, 3H), 1,98 (м, 1 Н), 1,83 (м, 2 Н), 1,44 (м, 2 Н). Пример 19. 4-[4-Бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил]циклогексиламин Палладий на активированном угле (0,017 г) добавляли к раствору бензилового эфира 4-[4 бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил]циклогексилкарбаминовой кислоты(смотри пример 18; 0,370 г, 0,725 ммоль) в метаноле (5 мл). Реакционную смесь перемешивали в атмосфере водорода в течение 4 ч. Затем смесь фильтровали и концентрировали, получая 0,250 г (92%) указанного в заголовке соединения в виде желтого масла. Масс-спектр (ESP+) m/z 377,2 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,80 (т, 1 Н, J = 7,8 Гц), 7,36 (м, 2 Н), 7,01 (м, 3H), 6,07 (с, 2 Н), 3,47 (м, 1 Н), 3,32 (м,1 Н), 2,29 (м, 2 Н), 2,03 (м, 4 Н), 1,90 (м, 2 Н). Пример 20.-Толуолсульфонилхлорид (0,023 г, 0,12 ммоль) и диизопропилэтиламин (0,026 мл, 0,15 ммоль) добавляли к раствору 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2 ил]циклогексиламина (см. пример 19; 0,038 г, 0,10 ммоль) в безводном ТГФ (3 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Растворитель удаляли при пониженном давлении и остаток растворяли в 1 мл ДМСО. Раствор ДМСО фильтровали и вводили в колонку препаративной ВЭЖХ. ВЭЖХ очистка с использованием элюирования смесью ацетонитрил:вода давала 0,005 г (9%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 531,1(М+1). 1H ЯМР (400 МГц, Метанол-d4)7,67 (м, 1 Н), 7,41 (м, 6 Н), 7,30 (м, 1 Н), 7,22 (м, 1 Н), 7,01 (м, 2 Н),6,07 (с, 2 Н), 4,34 (с, 2 Н), 3,05 (м, 2 Н), 2,63 (с, 3H), 2,13 (м, 2 Н), 1,95 (м, 2 Н), 1,72 (м, 2 Н), 1,43 (м, 2 Н). Пример 21. Метиловый эфир 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2 ил]бицикло[2.2.2]октан-1-карбоновой кислоты Метиловый эфир 4-формилбицикло[2.2.2]октан-1-карбоновой кислоты (0,284 г, 1,0 ммоль) добавляли к раствору 1-бензо[1,3]диоксол-5-ил-2-(6-метилпиридин-2-ил)этан-1,2-дион 2-оксима (см. пример 4; 0,215 г, 1,1 ммоль) и ацетата аммония (1,54 г, 20 ммоль) в уксусной кислоте (5 мл). Смесь нагревали при кипении с обратным холодильником в течение 2 ч. Растворитель удаляли при пониженном давлении. Реакционную смесь затем гасили смесью аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия,фильтровали и концентрировали, получая 0,300 г (65%) гидроксиимидазола в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 462,3 (M+1). Вышеуказанный гидроксиимидазол (0,250 г, 0,54 ммоль) добавляли к раствору TiCl3/HCl (10%, 3 мл) и метанолу (10 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Для гашения реакции добавляли смесь аммиак/лед. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка с элюированием смесью ацетонитрил:вода давала 0,100 г (42%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 446,2 (M+1). 1H ЯМР (400 МГц, Метанол-d4)7,72 (т, 1 Н, J = 7,8 Гц), 7,34- 21010418 Пример 22. 4-[4-Бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил]бицикло[2.2.2]октан-1 карбоновая кислота Моногидрат гидроксида лития (0,020 г, 0,487 ммоль) добавляли к раствору метилового эфира 4-[4 бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты (см. пример 21; 0,150 г, 0,325 ммоль) в смеси ТГФ/МеОН/H2O (2/1/1, 4 мл). Смесь перемешивали в течение 3 ч. Растворитель удаляли. Остаток разбавляли водой (30 мл). К раствору добавляли лимонную кислоту для получения рН ниже 7. Водный раствор экстрагировали этилацетатом. Этилацетатный экстракт промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали, получая 0,140 г (99%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр (ESP+) m/z 432,2 (М+1). 1 Н ЯМР (400 МГц, Метанол-d4)7,72 (м, 1 Н), 7,33 (д, 1 Н, J = 7,7 Гц), 7,22 (д, 1 Н, J=7,7 Гц), 6,98 (м, 3H), 6,05 (с, 2 Н), 2,64 (с, 3H), 2,11(м, 6 Н), 1,99(м, 6 Н). Пример 23. Бензиловый эфир 4-[4-бензо[1,3]диоксол-5-ил-5-(6-метилпиридин-2-ил)-1 Н-имидазол 2-ил]бицикло[2.2.2]окт-1-илкарбаминовой кислоты Дифенилфосфорилазид (0,070 мл, 0,324 ммоль) добавляли к раствору 4-[4-бензо[1,3]диоксол-5-ил 5-(6-метилпиридин-2-ил)-1 Н-имидазол-2-ил]бицикло[2.2.2]октан-1-карбоновой кислоты (см. пример 22; 0,140 г, 0,324 ммоль) и диизопропилэтиламина (0,068 мл, 0,39 ммоль) в толуоле (5 мл). Смесь перемешивали в течение 2 ч. К смеси добавляли бензиловый спирт (0,067 мл, 0,648 ммоль). Смесь перемешивали при комнатной температуре в течение 18 ч. Растворитель удаляли. Смесь распределяли между этилацетатом и водой. Органический раствор промывали насыщенным раствором соли, сушили над сульфатом натрия, фильтровали и концентрировали. ВЭЖХ очистка при элоюировании смесью ацетонитрил:вода давала 0,002 г (1%) указанного в заголовке соединения в виде желтого твердого вещества. Масс-спектр(ESP+) m/z 537,4 (М+1). 1H ЯМР (400 МГц, Метанол-d4)7,71 (м, 1 Н), 7,33 (м, 5 Н), 7,22 (м, 2 Н), 6,97 (м,3H), 6,05 (с, 2 Н), 5,02 (с, 2 Н), 2,63 (с, 3H), 2,17 (м, 6 Н), 2,06(м, 6 Н). Пример 24. Бензиловый эфир 4-[4-бензо[1,3]диоксол-5-ил-5-(6-этилпиридин-2-ил)-1 Н-имидазол-2 ил]пиперидин-1-карбоновой кислоты К раствору бензинового эфира 4-[4-бензо[1,3]диоксол-5-ил-5-(6-бромпиридин-2-ил)-1 Н-имидазол 2-ил]пиперидин-1-карбоновой кислоты (полученного согласно схеме 1b из 6-бромпиперидин-2 карбальдегида в качестве исходного вещества; 100 мг, 0,18 ммоль) в ДМФ (1 мл) и триэтиламине (2 мл) в атмосфере азота добавляли PdCl2(PPh3)2 (2 мг, 0,005 ммоль) и CuI (2 мг, 0,01 ммоль), с последующим добавлением триметилсилилацетилена (30 мкл, 0,20 ммоль). Смесь перемешивали при комнатной температуре в течение 4 ч до тех пор, пока ЖХ-масс-спетроскопия не показала завершение взаимодействия. Добавляли диэтиловый эфир (30 мл) и осадок отфильтровывали. Прозрачный раствор промывали насыщенным водным раствором NH4Cl, затем 0,5 М раствором EDTA и водой, а затем сушили (MgSO4). Концентрирование давало желтый сироп, который растворяли в ТГФ (20 мл). Раствор охлаждали до 0 С и добавляли фторид тетрабутиламмония (2 мл, 1 М в ТГФ). Смесь перемешивали при комнатной температуре в течение 30 мин, до тех пор, пока ЖХ-масс-спектроскопия не показала, что силильная группа удалена полностью. Реакционную смесь затем концентрировали в вакууме и пропускали через короткую колонку с силикагелем, элюируя смесью этилацетат/дихлорметан (1:1). Очищенное вещество растворяли в этаноле (20 мл) и добавляли PtO2 (50 мг). Смесь перемешивали в атмосфере водорода (1 атм) при комнатной температуре в течение 3 дней до тех пор пока ЖХ-масс-спектр не показал, что в основном прошло превращение алкина в соответствующий алкан. Твердые вещества отфильтровывали и фильтраты концентрировали и очищали препаративной ВЭЖХ, получая указанное в заголовке соединение (3 мг,3%) в виде соли с трифторуксусной кислотой. Масс-спектр (EPS+: 511,3 (МН+. 1H ЯМР (400 МГц,MeOH-d4)7,60 (т, 1 Н), 7,39-7,29 (м, 5 Н), 7,23 (д, 1 Н), 7,13 (д, 1 Н), 6,93 (дд, 1 Н), 6,91 (дд, 1 Н), 6,81 (д,1 Н), 5,95 (с, 2 Н), 5,14 (с, 2 Н), 4,28 (д (ушир.), 2 Н), 3,04 (м, 1 Н), 3,02 (ушир., 2 Н), 2,79 (кв, 2 Н), 2,00 (д(ушир.), 2 Н), 1,85 (ддд, 2 Н), 1,28 (т, 3H). Соединения, перечисленные в следующей таблице, были синтезированы аналогично описанным выше способам и примерам. В таблицу включены данные масс-спектроскопии для данных соединений.
МПК / Метки
МПК: C07D 405/14, C07D 409/14, C07D 401/14, C07D 409/04, C07D 401/04, A61K 31/517, C07D 405/04, A61K 31/395, A61K 31/435, A61K 31/36, A61K 31/41
Метки: способы, тризамещённые, гетероарилы, применения, получения
Код ссылки
<a href="https://eas.patents.su/30-10418-trizameshhyonnye-geteroarily-i-sposoby-ih-polucheniya-i-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Тризамещённые гетероарилы и способы их получения и применения</a>