Применение ингибиторов дипептидилпептидазы
Формула / Реферат
1. Способ лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, воспалительного заболевания кишечника, болезни Крона, индуцированного химиотерапией энтерита, мукозита слизистой оболочки полости рта, синдрома укороченной кишки, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), метаболического ацидоза, кетоза, регуляции аппетита, ожирения, диабетической нейропатии, диабетической ретинопатии, болезни почек, гиперлипидемии, артериосклероза, гипертонии, инфаркта миокарда, стенокардии, церебрального инфаркта, апоплексии головного мозга и метаболического синдрома, включающий
введение пациенту суточной дозы, составляющей от 1 до 250 мг/сутки, соединения I, где соединение I имеет формулу
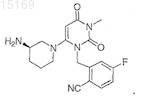
2. Способ по п.1, в котором суточная доза соединения I, вводимая пациенту, составляет от 5 до 100 мг.
3. Способ по п.1, в котором суточная доза соединения I, вводимая пациенту, составляет 6,25 мг.
4. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки.
5. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в виде однократной дозы.
6. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в течение периода времени, составляющего по меньшей мере 30 суток.
7. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в течение периода времени, составляющего по меньшей мере 60 суток.
8. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки утром.
9. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки утром перед первым приемом пищи пациентом в этот день.
10. Способ по любому из пп.1-9, в котором введение осуществляют путем, выбранным из группы, состоящей из перорального, парентерального, внутрибрюшинного, внутривенного, внутриартериального, трансдермального, подъязычного, внутримышечного, ректального, трасбуккального, интраназального, липосомного, ингаляционного, вагинального, внутриглазного, введения путем локальной доставки, подкожного, введения в жировую ткань, внутрисуставного, внутрибрюшинного и интратекального введения.
11. Способ по любому из пп.1-9, в котором введение осуществляют перорально.
12. Способ по любому из пп.1-11, в котором введение осуществляют для лечения патологического состояния пациента, представляющего собой диабет типа I или типа II.
13. Способ по любому из пп.1-11, в котором указанный пациент имеет диабет типа II.
14. Способ по любому из пп.1-11, в котором указанный пациент находится в преддиабетическом состоянии.
15. Способ по любому из пп.1-14, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, отличными от соединения I, для лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), диабетической нейропатии, диабетической ретинопатии и метаболического синдрома.
16. Способ лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), диабетической нейропатии, диабетической ретинопатии и метаболического синдрома, включающий
введение суточной дозы, составляющей от 1 до 250 мг/сутки, соединения I пациенту в комбинации с одним или несколькими антидиабетическими соединениями, отличными от соединения I, где соединение I имеет формулу
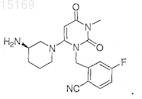
17. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину и усилителей секреции инсулина.
18. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из ингибиторов протеинтирозинфосфатазы, ингибиторов глутаминфруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо-6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецепторов глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, активаторов глюкокиназы, агонистов рецептора GLP-1, агонистов рецептора GLP-2, модуляторов UCP, модуляторов RXR, ингибиторов GSK-3, модуляторов PPAR, инсулина и a2-адренергических антагонистов.
19. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из ингибиторов GSK-3, агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-альфа, антидиабетических ванадийсодержащих соединений и бигуанидов.
20. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из (S)-(3,4-дигидро-2-(фенилметил)-2Н-1-бензопиран-6-ил)метилтиазолидин-2,4-диона, 5-{[4-(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метил}тиазолидин-2, 4-диона, 5-{[(4-(1-метилциклогексил)метокси)фенил]метил}тиазолидин-2,4-диона, 5-{[4-(2-(1-индолил)этокси)фенил]метил}тиазолидин-2,4-диона, 5-{4-[2-(5-метил-(2-фенил-4-оксазолил)этокси)]бензил}тиазолидин-2,4-диона, 5-(2-нафтилсульфонил)тиазолидин-2,4-диона, бис{4-[(2,4-диоксо-5-тиазолидинил)метил]фенил}метана, 5-{4-[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензил}тиазолидин-2,4-диона, 5-[4-(1-фенил-1-циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-[4-(2-(2,3-дигидроиндол-1-ил)этокси)фенилметил]тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-(5-фенилсульфонил)тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2,4-диона, 5-{[4-(2-(метил-2-пиридиниламино)этокси)фенил]метил}тиазолидин-2,4-диона, 5-{[4-(2-(5-этил-2-пиридил)этокси)фенил]метил}тиазолидин-2,4-диона, 5-{[2-(2-нафтил)бензоксазол-5-ил]метил}тиазолидин-2,4-диона и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида, включая их любые фармацевтически приемлемые соли.
21. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с метформином, включая его любые фармацевтически приемлемые соли.
22. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими производными сульфонилмочевины.
23. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида, толазамида, глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли.
24. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бета-клеток и кратковременно действующих стимуляторов секреции инсулина.
25. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с инсулином.
26. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими агонистами GLP-1.
27. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими агонистами GLP-2.
28. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с экстендатидом.
29. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из репаглинида, митиглинида и натеглинида, включая их любые фармацевтически приемлемые соли.
30. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими ингибиторами альфа-глюкозидазы.
31. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы, состоящей из акарбозы, воглибозы и миглитола, включая их любые фармацевтически приемлемые соли.
32. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с розиглитазоном, включая его любые фармацевтически приемлемые соли.
33. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с пиоглитазоном, включая его любые фармацевтически приемлемые соли.
34. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с метформином и пиоглитазоном, включая их любые фармацевтически приемлемые соли.
35. Способ по любому из пп.33 и 34, в котором пиоглитазон представляет собой пиоглитазон-HCl.
36. Способ по любому из пп.1-35, в котором соединение I вводят в виде свободного основания.
37. Способ по любому из пп.1-35, в котором соединение I вводят в виде фармацевтически приемлемой соли.
38. Способ по любому из пп.1-35, в котором соединение I вводят в виде сукцинатной соли.
39. Фармацевтическая композиция, приготовленная в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит 2,5, 5, 6,25, 20, 25, 50 или 75 мг соединения I, где соединение I имеет формулу
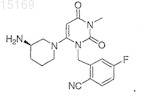
40. Фармацевтическая композиция по п.39, в которой указанная стандартная лекарственная форма содержит 6,25 мг соединения I.
41. Фармацевтическая композиция по любому из пп.39-40, в которой указанная стандартная лекарственная форма дополнительно содержит одно или несколько антидиабетических соединений, отличных от соединения I.
42. Фармацевтическая композиция, приготовленная в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит от 1 до 250 мг соединения I и одно или несколько антидиабетических соединений, отличных от соединения I, где соединение I имеет формулу
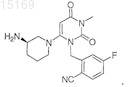
43. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину и усилителей секреции инсулина.
44. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из ингибиторов протеинтирозинфосфатазы, ингибиторов глутаминфруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо-6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецепторов глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, инсулина и a2-адренергических антагонистов.
45. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из ингибиторов GSK-3, агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-альфа, антидиабетических ванадийсодержащих соединений и бигуанидов.
46. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из (S)-(3,4-дигидро-2-(фенилметил)-2Н-1-бензопиран-6-ил)метилтиазолидин-2,4-диона, 5-{[4-(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метил}тиазолидин-2,4-диона, 5-{[4-(1-метилциклогексил)метокси) фенил]метил}тиазолидин-2,4-диона, 5-{[4-(2-(1-индолил)этокси)фенил]метил}тиазолидин-2,4-диона, 5-{4-[2-(5-метил-2-фенил-4-оксазолил)этокси]бензил}тиазолидин-2,4-диона, 5-(2-нафтилсульфонил)тиазолидин-2,4-диона, бис{4-[(2,4-диоксо-5-тиазолидинил)метил]фенил}метана, 5-{4-[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензил}тиазолидин-2,4-диона, 5-[4-(1-фенил-1-циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-{[4-(2-(2,3-дигидроиндол-1-ил)этокси)фенилметил)тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-(5-фенилсульфонил)тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2, 4-диона, 5-{[4-(2-(метил-2-пиридиниламино)этокси)фенил]метил}тиазолидин-2,4-диона, 5-{[2-(2-нафтил)бензоксазол-5-ил]метил}тиазолидин-2,4-диона и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида, включая их любые фармацевтически приемлемые соли.
47. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит метформин, включая его любые фармацевтически приемлемые соли.
48. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит производное сульфонилмочевины.
49. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида, толазамида, глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли.
50. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бета-клеток и кратковременно действующих стимуляторов секреции инсулина.
51. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит инсулин.
52. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько агонистов GLP-1.
53. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько агонистов GLP-2.
54. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит экстендатид.
55. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из репаглинида, митиглинида и натеглинида, включая их любые фармацевтически приемлемые соли.
56. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько ингибиторов альфа-глюкозидазы.
57. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы, состоящей из акарбозы, воглибозы и миглитола, включая их любые фармацевтически приемлемые соли.
58. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит розиглитазон, включая его любые фармацевтически приемлемые соли.
59. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит пиоглитазон, включая его любые фармацевтически приемлемые соли.
60. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит метформин и пиоглитазон, включая их любые фармацевтически приемлемые соли.
61. Фармацевтическая композиция по любому из пп.59 и 60, в которой пиоглитазон представляет собой пиоглитазон-НС1.
62. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма предназначена для перорального введения.
63. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой твердый препарат, предназначенный для перорального введения.
64. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой таблетку или капсулу, предназначенную для перорального введения.
65. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой препарат длительного высвобождения, предназначенный для перорального введения.
66. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде свободного основания.
67. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде фармацевтически приемлемой соли.
68. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде сукцинатной соли.
69. Набор, содержащий
несколько доз фармацевтической композиции по любому из пп.39-68 и
инструкции, которые содержат одну или несколько форм информации, выбранных из группы, состоящей из указания патологического состояния, в случае которого необходимо вводить фармацевтическую композицию, информации о хранении фармацевтической композиции, информации о дозах и инструкций по введению фармацевтической композиции.
70. Изделие, содержащее
несколько доз фармацевтической композиции по любому из пп.39-68 и
упаковочные материалы.
71. Изделие по п.70, в котором упаковочный материал включает контейнер для хранения нескольких доз фармацевтической композиции.
72. Изделие по п.71, в котором контейнер имеет этикетку, на которой указана одна или несколько форм информации из группы, состоящей из информации о патологическом состоянии, в случае которого необходимо вводить соединение, информации о хранении, информации о дозах и/или инструкций по введению композиции.
73. Применение фармацевтической композиции по любому из пп.39-68 для лечения диабета типа II.
74. Применение фармацевтической композиции по любому из пп.39-68 для лечения диабета типа I.
75. Применение фармацевтической композиции по любому из пп.39, 40 и 62-68 для лечения лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, воспалительного заболевания кишечника, болезни Крона, индуцированного химиотерапией энтерита, мукозита слизистой оболочки полости рта, синдрома укороченной кишки, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), метаболического ацидоза, кетоза, регуляции аппетита, ожирения, диабетической нейропатии, диабетической ретинопатии, болезни почек, гиперлипидемии, артериосклероза, гипертонии, инфаркта миокарда, стенокардии, церебрального инфаркта, апоплексии головного мозга и метаболического синдрома.
Текст
(71)(73) Заявитель и патентовладелец: ТАКЕДА ФАРМАСЬЮТИКАЛ КОМПАНИ ЛИМИТЕД (JP) Предлагаются фармацевтические композиции, содержащие 2-[6-(3-аминопиперидин-1-ил)-3 метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1-илметил]-4-фторбензонитрил и его фармацевтически приемлемые соли, а также наборы и изделия, содержащие фармацевтические композиции,а также способы применения фармацевтических композиций. Композиции могут быть использованы для лечения диабета. 015169 Область техники, к которой относится изобретение Изобретение относится к способу введения соединений, используемых для ингибирования дипептидилпептидазы IV, а также к способам лечения, основанным на указанном введении. Уровень техники Дипептидилпептидаза IV (согласно номенклатуре ферментов IUBMB ЕС.3.4.14.5) является мембранным белком типа II, который в литературе имеет широкое множество названий, включая DPP4, DP4,DAP-IV, FAP, белок 2, образующий комплекс с аденозиндезаминазой, белок, связывающий аденозиндезаминазу (ADAbp), дипептидиламинопептидаза IV; Xaa-Pro-дипептидиламинопептидаза; Gly-Proнафтиламидаза; постпролиндипептидиламинопептидаза IV; лимфоцитарный антиген CD26; гликопротеин GP110; дипептидилпептидаза IV; глицилпролинаминопептидаза; глицилпролинаминопептидаза; Xпролилдипептидиламинопептидаза; pep X; лейкоцитарный антиген CD26; глицилпролилдипептидиламинопептидаза; дипептидилпептидгидролаза; глицилпролиламинопептидаза; дипептидиламинопептидазаIV; DPP IV/CD26; аминоацилпролилдипептидиламинопептидаза; инициирующая Т-клетки молекула Тр 103; X-PDAP. Дипептидилпептидаза IV в настоящем описании упоминается как "DPP-IV".DPP-IV является неклассической сериновой аминодипептидазой, которая отщепляет дипептиды Хаа-Pro с аминоконца (N-конца) полипептидов и белков. Также сообщалось, что зависимое от DPP-IV медленное высвобождение дипептидов типа X-Gly или X-Ser происходит в случае некоторых встречающихся в природе пептидов.DPP-IV конститутивно экспрессируется на эпителиальных и эндотелиальных клетках множества разных тканей (кишечник, печень, легкое, почка и плацента), а также выявляется в жидкостях организма.DPP-IV также экспрессируется на циркулирующих Т-лимфоцитах, и было показано, что DPP-IV тождественна антигену клеточной поверхности CD-26.DPP-IV ответственна за метаболическое расщепление некоторых эндогенных пептидов (GLP-1 (736), глюкагон) in vivo и проявляет протеолитическую активность против ряда других пептидов (GHRH,NPY, GLP-2, VIP) in vitro.GLP-1 (7-36) является 29-аминокислотным пептидом, полученным в результате посттрансляционного процессинга проглюкагона в тонком кишечнике. GLP-1 (7-36) оказывает множество воздействий invivo, включая стимуляцию секреции инсулина, ингибирование секреции глюкагона, усиление чувства насыщения и замедление опорожнения желудка. На основании физиологического профиля полагают, что действия GLP-1 (7-36) полезны для предотвращения и лечения диабета типа II и, вероятно, ожирения. Например, обнаружено, что экзогенное введение GLP-1 (7-36) (непрерывная инфузия) пациентам с диабетом является эффективным в указанной популяции пациентов. К сожалению, GLP-1 (7-36) быстро распадается in vivo и, как было показано, имеет короткое время полужизни in vivo (t1/2=1,5 мин). На основании исследования генетически выведенных нокаутированных по DPP-IV мышей и на основании исследований in vivo/in vitro с использованием избирательных ингибиторов DPP-IV показано,что DPP-IV является основным ферментом, расщепляющим GLP-1 (7-36) in vivo. GLP-1 (7-36) эффективно расщепляется ферментом DPP-IV до GLP-1 (9-36), который, как предполагается, действует в качестве физиологического антагониста GLP-1 (7-36). Поэтому полагают, что ингибирование DPP-IV in vivo применимо для повышения эндогенных уровней GLP-1 (7-36) и уменьшения образования его антагонистаGLP-1 (9-36). Таким образом, считают, что ингибиторы DPP-IV являются средствами, применимыми для предотвращения, замедления прогрессирования и/или лечения состояний, опосредованных DPP-IV, в частности диабета, и более конкретно сахарного диабета типа 2, диабетической дислипидемии, состояний нарушения толерантности к глюкозе (IGT), состояний нарушения уровня глюкозы в плазме натощак(IFG), метаболического ацидоза, кетоза, регуляции аппетита и ожирения. Показано, что несколько соединений ингибируют DPP-IV. Однако все еще существует потребность в новых ингибиторах DPP-IV и способах введения указанных ингибиторов для лечения заболевания. Сущность изобрения Предлагается способ, включающий введение суточной дозы от 1 до 250 мг/сут соединения I пациенту, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В одном варианте вводят суточную дозу 2,5, 5, 6,25, 10, 20, 25, 50,75 или 100 мг соединения I. В другом варианте один раз в неделю вводят дозу 2,5, 5, 6,25, 10, 20, 25, 50,75 или 100 мг соединения I. В одном варианте введение осуществляют 1 раз в сутки и необязательно могут осуществлять 1 раз в сутки в виде однократной дозы. Необязательно введение осуществляют 1 раз в сутки в течение периода времени, составляющего по меньшей мере 30 дней, и необязательно в течение периода времени, составляющего по меньшей мере 60 дней. В одном варианте введение осуществляют 1 раз в сутки утром и необязательно осуществляют 1 раз в сутки утром до первого приема пищи пациентом в этот день. В одном варианте введение осуществляют 1 раз в неделю и необязательно могут осуществлять 1 раз в неделю в виде однократной дозы. Необязательно введение осуществляют 1 раз в неделю в течение периода времени, составляющего по меньшей мере 30 дней, и необязательно в течение периода времени,составляющего по меньшей мере 60 дней.-1 015169 В одном варианте введение осуществляют 1 раз в неделю утром и необязательно осуществляют 1 раз в неделю утром перед первым приемом пищи пациентом в этот день. Введение можно осуществлять различными путями введения, включая, без ограничения, путь, выбранный из группы, состоящей из перорального, парентерального, внутрибрюшинного, внутривенного,внутриартериального, трансдермального, подъязычного, внутримышечного, ректального, трасбуккального, интраназального, липосомного, ингаляционного, вагинального, внутриглазного, введения путем локальной доставки, подкожного, введения в жировую ткань, внутрисуставного, внутрибрюшинного и интратекального введения. В одном конкретном варианте введение осуществляют перорально. Соединение I можно использовать для лечения ряда заболеваний. В одном варианте введение соединения I осуществляют для лечения указанного патологического состояния у пациента, как диабет типа I или типа II. В другом варианте введение соединения I осуществляют для лечения преддиабетического состояния пациента. В еще одном варианте введение соединения I осуществляют для лечения воспалительного заболевания кишечника, болезни Крона, индуцированного химиотерапией энтерита, мукозита слизистой оболочки полости рта или синдрома укороченной кишки. В другом варианте введение соединения I осуществляют для лечения пациента, страдающего от состояний, опосредованных DPP-IV, таких как диабет и более конкретно сахарный диабет типа 2; диабетическая дислипидемия; нарушение толерантности к глюкозе (IGT); нарушение уровня глюкозы в плазме натощак (IFG); метаболический ацидоз; кетоз; регуляция аппетита; ожирение; осложнения, связанные с диабетом, включая диабетическую нейропатию, диабетическую ретинопатию и болезнь почек; гиперлипидемия, включая гипертриглицеридемию, гиперхолестеринемию, низкий уровень ЛПВП и постпрандиальную гиперлипидемию; артериосклероз; гипертония; инфаркт миокарда, стенокардия, церебральный инфаркт, апоплексия головного мозга и метаболический синдром. Также предлагается способ введения соединения I в комбинации с одним или несколькими антидиабетическими или инкретиновыми соединениями, отличными от соединения I. В одном варианте осуществляют такой способ комбинированной терапии, при котором пациенту вводят суточную дозу от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В одном варианте суточную дозу 2,5, 5, 6,25,10, 20, 25, 50, 75 или 100 мг соединения I вводят пациенту в комбинации с одним или несколькими антидиабетическими соединениями, отличными от соединения I. В одном варианте осуществляют такой способ комбинированной терапии, при котором пациенту один раз в неделю вводят дозу, составляющую от 1 до 250 мг соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединенияI. В одном варианте пациенту один раз в неделю вводят дозу 2,5, 5, 6,25, 10, 20, 25, 50, 75 или 100 мг, 150 или 200 мг соединения I в комбинации с одним или несколькими антидиабетическими соединениями,отличными от соединения I. Следует отметить, что в настоящем изобретении предлагается несколько разных диапазонов доз для конкретных антидиабетических соединений и инкретинов. Подразумевается, что в объем настоящего изобретения включены комбинации лекарственных средств, охватывающие любой из описанных диапазонов соединения I в комбинации с любыми описанными в настоящем описании диапазонами доз для других антидиабетических соединений или инкретинов. Комбинация соединения I с одним или несколькими антидиабетическими соединениями, отличными от соединения I, обеспечивает превосходные эффекты, такие как 1) усиление терапевтических эффектов соединения I и/или антидиабетических соединений; 2) уменьшение побочных эффектов соединения I и/или антидиабетических соединений; и 3) уменьшение дозы соединения I и/или антидиабетических соединений. Одно или несколько антидиабетических соединений или инкретинов, вводимых в комбинации с соединением I, необязательно могут быть выбраны из группы, состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину и усилителей секреции инсулина. Одно или несколько антидиабетических соединений или инкретинов, вводимых в комбинации с соединением I, также необязательно могут быть выбраны из группы, состоящей из ингибиторов протеинтирозинфосфатазы, ингибиторов глутамин-фруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо 6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецепторов глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, активаторов глюкокиназы, агонистов рецептора GLP-1, агонистов рецептора GLP-2, модуляторов UCP, модуляторовRXR, ингибиторов GSK-3, модуляторов PPAR, метформина, инсулина и антагонистов 2 адренергических рецепторов. Одно или несколько антидиабетических соединений или инкретинов, вводимых в комбинации с соединением I, также необязательно могут быть выбраны из группы, состоящей из ингибиторов GSK-3,агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-2 015169 альфа, антидиабетических ванадийсодержащих соединений и бигуанидов. Одно или несколькими антидиабетических соединений или инкретинов, вводимых в комбинации с соединением I, также необязательно могут представлять собой тиазолидиндионы, выбранные из группы,состоящей из (S)-(3,4-дигидро-2-(фенилметил)-2 Н-1-бензопиран-6-ил)метилтиазолидин-2,4-диона, 5-[4(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метилтиазолидин-2,4-диона,5-[(4-(1-метилциклогексил)метокси)фенил]метилтиазолидин-2,4-диона, 5-[4-(2-(1-индолил)этокси)фенил]метилтиазолидин-2,4-диона, 5-4-[(2-(5-метил-2-фенил-4-оксазолил)этокси)]бензилтиазолидин-2,4-диона, 5-(2 нафтилсульфонил)тиазолидин-2,4-диона, бис 4-[(2,4-диоксо-5-тиазолидинил)метил]фенилметана, 5-4[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензилтиазолидин-2,4-диона, 5-[4-(1-фенил-1-циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-[4-(2-(2,3-дигидроиндол-1-ил)этокси)фенилметилтиазолидин-2,4-диона,5-[(3-(4-хлорфенил)-2-пропинил)-5-фенилсульфонил]тиазолидин-2,4 диона,5-[3-(4-хлорфенил])-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2,4-диона,5-[4-(2(метил-2-пиридиниламино)этокси)фенил]метилтиазолидин-2,4-диона, 5-[4-(2-(5-этил-2-пиридил)этокси)фенил]метилтиазолидин-2,4-диона, 5-[4-3,4-дигидро-6-гидрокси-2,5,7,8-тетраметил-2 Н-1-бензопиран-2-ил)метокси)фенил]метилтиазолидин-2,4-диона, 5-[6-(2-фторбензилокси)нафталин-2-илметил] тиазолидин-2,4-диона, 5-[2-(2-нафтил)бензоксазол-5-ил]метилтиазолидин-2,4-диона и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают метформин. В одном конкретном варианте метформин в указанной комбинации включает одну или несколько его фармацевтически приемлемых солей. В другом конкретном варианте метформин в указанной комбинации включает HCl-соль метформина. В еще одном конкретном варианте метформин в указанной комбинации вводят в суточной дозе, составляющей от 125 до 2550 мг. В еще одном варианте метформин в указанной комбинации вводят в суточной дозе, составляющей от 250 до 2550 мг. В другом варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают одно или несколько производных сульфонилмочевины. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут быть выбраны из группы, состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида, толазамида, глипизида, карбутамида,гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают глимепирид. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут быть выбраны из группы, состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бета-клеток и кратковременно действующих стимуляторов секреции инсулина. В другом варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают инсулин. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой один или несколько агонистов GLP-1, включая, например, экстендатид. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой один или несколько агонистов GLP-2, включая, например, рекомбинантный GLP-2 человека. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой одно или несколько антидиабетических производных Dфенилаланина. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут быть выбраны из группы, состоящей из репаглинида, митиглинида и натеглинида, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают гидрат кальциевой соли митиглинида. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой один или несколько ингибиторов альфа-глюкозидазы. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут быть выбраны из группы, состоящей из акарбозы, воглибозы и миглитола,включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I, включают воглибозу. В другом варианте воглибозу в указанной комбинации вводят в суточной дозе от 0,1 до 1 мг. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой розиглитазон, включая его любые фармацевтически при-3 015169 емлемые соли. В одном варианте розиглитазон в указанной комбинации представляет собой малеатную соль розиглитазона. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой тезаглитазар, мураглитазар или навеглитазар, включая их любые фармацевтически приемлемые соли. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут представлять собой пиоглитазон, включая его любые фармацевтически приемлемые соли. В одном варианте пиоглитазон в указанной комбинации представляет собой HCl-соль пиоглитазона. В другом варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 7,5 до 60 мг. В еще одном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 15 до 45 мг. Одно или несколько антидиабетических соединений, вводимых в комбинации с соединением I,также необязательно могут включать метформин и пиоглитазон. В одном варианте пиоглитазон в указанной комбинации представляет собой одну или несколько его фармацевтически приемлемых солей. В другом варианте пиоглитазон в указанной комбинации представляет собой HCl-соль пиоглитазона. В еще одном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 7,5 до 60 мг. В еще одном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 15 до 45 мг. В другом варианте каждого из указанных выше вариантов метформин в указанной комбинации представляет собой одну или несколько его фармацевтически приемлемых солей. В одном конкретном варианте метформин в указанной комбинации представляет собой HCl-соль метформина. В другом конкретном варианте метформин в указанной комбинации вводят в суточной дозе от 125 до 2550 мг. В еще одном варианте метформин в указанной комбинации вводят в суточной дозе от 250 до 2550 мг. Что касается каждого из указанных выше вариантов осуществления и их вариаций, то соединение I можно вводить в виде свободного основания или в виде его фармацевтически приемлемой соли. В конкретных вариантах соединение I вводят в виде HCl-соли, метансульфоната, сукцината, бензоата, толуолсульфоната, R-(-)манделата или бензолсульфонатной соли соединения I. Также предлагаются фармацевтические композиции. В одном варианте предлагается фармацевтическая композиция, которую получают в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В конкретных вариантах фармацевтическая композиция содержит 2,5, 5, 6,25, 10, 20, 25, 50, 75 или 100 мг соединения I. В одном варианте предлагается фармацевтическая композиция, которую готовят в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит от 1 мг/неделю до 250 мг/неделю соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В конкретных вариантах фармацевтическая композиция содержит 2,5, 5, 6,25, 10, 20, 25, 50, 75 или 100 мг соединения I, вводимых один раз в неделю. В другом варианте предлагается фармацевтическая композиция, которая содержит соединение I и одно или несколько антидиабетических или инкретиновых соединений, отличных от соединения I, в стандартной лекарственной форме. Необязательно соединение I присутствует в стандартной лекарственной форме в количестве от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I,необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В конкретных вариантах фармацевтическая композиция содержит 2,5, 5, 6,25, 10, 20, 25, 50, 75 или 100 мг соединения I. Комбинация соединения I с одним или несколькими антидиабетическими соединениями, отличными от соединения I, обеспечивает превосходные действия, такие как 1) усиление терапевтических действия соединения I и/или антидиабетических соединений; 2) уменьшение побочных действий соединения I и/или антидиабетических соединений; и 3) уменьшение дозы соединения I и/или антидиабетических соединений. Согласно указанному выше варианту одно или несколько антидиабетических соединений, входящих в фармацевтическую композицию, необязательно могут быть выбраны из группы, состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину, инкретинов и усилителей секреции инсулина. Также согласно указанному выше варианту одно или несколько антидиабетических соединений,входящих в состав фармацевтической композиции, необязательно могут быть выбраны из группы, состоящей из ингибиторов протеинтирозинфосфатаз, ингибиторов глутаминфруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо-6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецептора глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, активаторов глюкокиназы, агонистов рецептора GLP-1, агонистов рецептора GLP-2,модуляторов UCP, модуляторов RXR, ингибиторов GSK-3, модуляторов PPAR, метформина, инсулина и-4 015169 антагонистов 2-адренергических рецепторов. Также согласно указанному выше варианту одно или несколько антидиабетических соединений,входящих в состав фармацевтической композиции, необязательно могут быть выбраны из группы, состоящей из ингибиторов GSK-3, агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-альфа, антидиабетических ванадийсодержащих соединений и бигуанидов. Также согласно указанному выше варианту одно или несколько антидиабетических соединений,входящих в состав фармацевтической композиции, необязательно могут представлять собой тиазолидиндионы, выбранные из группы, состоящей из (S)-3,4-дигидро-2-(фенилметил)-2 Н-1-бензопиран-6-ил)метил)тиазолидин-2,4-диона, 5-[4-(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метилтиазолидин-2,4-диона, 5-[(4-(1-метилциклогексил)метокси)фенил]метилтиазолидин-2,4-диона, 5-[4-(2-(1 индолил)этокси)фенил]метилтиазолидин-2,4-диона, 5-4-[(2-(5-метил-2-фенил-4-оксазолил)этокси)]бензилтиазолидин-2,4-диона,5-(2-нафтилсульфонил)тиазолидин-2,4-диона,бис 4-[(2,4-диоксо-5 тиазолидинил)метил]фенилметана,5-4-[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензил тиазолидин-2,4-диона, 5-[4-(1-фенил-1-циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-[42-(2,3-дигидроиндол-1-ил)этокси]фенилметилтиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]5-фенилсульфонилтиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил) тиазолидин-2,4-диона, 5-[4-(2-(метил-2-пиридиниламино)этокси)фенил]метилтиазолидин-2,4-диона, 5[4-(2-(5-этил-2-пиридил)этокси)фенил]метилтиазолидин-2,4-диона,5-[(4-(3,4-дигидро-6-гидрокси 2,5,7,8-тетраметил-2 Н-1-бензопиран-2-ил)метокси)фенил]метилтиазолидин-2,4-диона, 5-[6-(2-фторбензилокси)нафталин-2-илметил]тиазолидин-2,4-диона, 5-[2-(2-нафтил)бензоксазол-5-ил]метилтиазолидин-2,4-диона и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида,включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают метформин. В одном конкретном варианте метформин в указанной комбинации включает одну или несколько его фармацевтически приемлемых солей. В другом конкретном варианте метформин в указанной комбинации представляет собой HCl-соль метформина. В еще одном конкретном варианте метформин в указанной комбинации вводят в суточной дозе, составляющей от 125 до 2550 мг. В еще одном варианте метформин в указанной комбинации вводят в суточной дозе, составляющей от 250 до 2550 мг. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают одно или несколько производных сульфонилмочевины. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают антидиабетическое соединение, выбранное из группы, состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида,толазамида, глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают глимепирид. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают антидиабетическое соединение, выбранное из группы, состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бета-клеток и кратковременно действующих стимуляторов секреции инсулина. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают инсулин. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают один или несколько агонистов GLP-1. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают один или несколько агонистов GLP-2, включая, например, рекомбинантные формы GLP-2 человека. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают одно или несколько антидиабетических производных Dфенилаланина. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают антидиабетическое соединение, выбранное из группы, состоящей из репаглинида и натеглинида, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции,включают гидрат кальциевой соли митиглинида. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают один или несколько ингибиторов альфа-глюкозидазы. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают антидиабетическое соединение, выбранное из группы, состоящей из-5 015169 акарбозы, воглибозы и миглитола, включая их любые фармацевтически приемлемые соли. В одном варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают воглибозу. В другом варианте воглибозу в указанной комбинации вводят в суточной дозе от 0,1 до 1 мг. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают розиглитазон, включая его любые фармацевтически приемлемые соли. В одном варианте розиглитазон в указанной комбинации представляет собой малеатную соль розиглитазона. Одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, также необязательно могут представлять собой тезаглитазар, мураглитазар или навеглитазар,включая их любые фармацевтически приемлемые соли. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают пиоглитазон, включая его любые фармацевтически приемлемые соли. В одном конкретном варианте пиоглитазон в указанной комбинации представляет собой HCl-соль пиоглитазона. В другом конкретном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 7,5 до 60 мг. В еще одном конкретном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 15 до 45 мг. В другом варианте одно или несколько антидиабетических соединений, входящих в состав фармацевтической композиции, включают метформин и пиоглитазон. В одном конкретном варианте пиоглитазон в указанной комбинации представляет собой одну или несколько его фармацевтически приемлемых солей. В другом конкретном варианте пиоглитазон в указанной комбинации представляет собой HClсоль пиоглитазона. В еще одном конкретном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 7,5 до 60 мг. В еще одном конкретном варианте пиоглитазон в указанной комбинации вводят в суточной дозе от 15 до 45 мг. В другом варианте каждого из указанных выше вариантов метформин в указанной комбинации представляет собой одну или несколько его фармацевтически приемлемых солей. В еще одном варианте метформин в указанной комбинации представляет собой HCl-соль метформина. В другом варианте метформин в указанной комбинации вводят в суточной дозе от 125 до 2550 мг. В еще одном варианте метформин в указанной комбинации вводят в суточной дозе от 250 до 2550 мг. Что касается каждого из указанных выше вариантов осуществления и их вариаций, относящихся к фармацевтическим композициям, то соединение I можно вводить в виде свободного основания или в виде его фармацевтически приемлемой соли. В конкретных вариантах соединение I вводят в виде HClсоли, метансульфоната, сукцината, бензоата, толуолсульфоната, R-(-)манделата или бензолсульфонатной соли соединения I. Также в отношении указанных выше вариантов осуществления и их вариаций, касающихся фармацевтических композиций, фармацевтическая композиция необязательно может быть в виде стандартной лекарственной формы, применимой для перорального введения, необязательно в форме твердого препарата, применимого для перорального введения, и необязательно в форме таблетки или капсулы, применимой для перорального введения. Фармацевтический препарат также может представлять собой препарат медленного высвобождения, применимый для перорального введения. Также в отношении каждого из указанных выше вариантов осуществления и их вариаций, касающихся фармацевтических композиций, фармацевтическая композиция может быть использована для предотвращения или лечения состояний, опосредованных DPP-IV, таких как диабет и более конкретно сахарный диабет типа 2; диабетическая дислипидемия; нарушение толерантности к глюкозе (IGT); нарушение уровня глюкозы в плазме натощак (IFG); метаболический ацидоз; кетоз; регуляция аппетита; ожирение; осложнения, связанные с диабетом, включая диабетическую нейропатию, диабетическую ретинопатию и болезнь почек; гиперлипидемия, включая гипертриглицеридемию, гиперхолестеринемию,низкий уровень ЛПВП и постпрандиальную гиперлипидемию; артериосклероз; гипертония; инфаркт миокарда, стенокардия, церебральный инфаркт, апоплексия головного мозга и метаболический синдром. Также в отношении каждого из указанных выше вариантов осуществления и их вариаций, касающихся фармацевтических композиций, фармацевтическая композиция необязательно может быть в виде стандартной лекарственной формы, применимой для парентерального (подкожного, внутривенного, субдермального или внутримышечного) введения, необязательно в форме препарата в виде раствора, применимого для парентерального введения, и необязательно в форме препарата в виде суспензии, применимой для парентерального введения. Фармацевтический препарат также может представлять собой препарат медленного высвобождения, применимый для перорального введения. Также предлагаются наборы, содержащие несколько доз фармацевтической композиции согласно настоящему изобретению. В одном варианте наборы дополнительно содержат инструкции, в которых имеется одна или несколько форм информации, выбранных из группы, состоящей из указания патологического состояния, в случае которого необходимо вводить фармацевтическую композицию, информации о хранении фармацевтической композиции, информации о дозах и инструкций по введению фармацевтической компози-6 015169 ции. Также предлагаются изделия, содержащие несколько доз фармацевтической композиции согласно настоящему изобретению. В одном варианте изделия дополнительно содержат материалы упаковки, такие как контейнер для хранения нескольких доз фармацевтической композиции и/или этикетка, указывающая одну или несколько форм информации из группы, состоящей из указания патологического состояния, в случае которого необходимо вводить соединение, информации о хранении, информации о дозах и/или инструкций по введению композиции. В отношении всех указанных выше вариантов осуществления следует отметить, что варианты необходимо интерпретировать как неокончательные, с возможными поправками в том смысле, что способы могут включать дополнительные действия, кроме указанных, включая введение пациенту других фармацевтически активных веществ. Подобным образом, если не оговорено особо, фармацевтические композиции, наборы и изделия дополнительно могут содержать другие вещества, включая другие фармацевтически активные вещества. Краткое описание фигуры На чертеже показано ингибирование DPP-IV в плазме после однократного перорального введения соединения I обезьяне. Определения Если не оговорено особо, следующие термины, используемые в описании и формуле изобретения, в целях настоящего описания должны иметь следующие значения."Заболевание" в частности включает любое патологическое состояние животного или его части и включает патологическое состояние, которое может быть вызвано или возникает вследствие медицинского или ветеринарного лечения, применяемого по отношению к указанному животному, т.е. "побочные действия" указанной терапии."Фармацевтически приемлемый" означает применимый для получения фармацевтической композиции, которая в общем безопасна, нетоксична и не является биологически или в ином отношении неприемлемой, и включает компоненты, приемлемые для применения в ветеринарии, а также фармацевтического применения на человеке."Фармацевтически приемлемые соли" означает соли, которые являются фармацевтически приемлемыми, как определено выше, и которые обладают требуемой фармакологической активностью. Указанные соли включают, без ограничения, кислотно-аддитивные соли, образованные с неорганическими кислотами, такими как хлористо-водородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и тому подобные; или с органическими кислотами, такими как уксусная кислота, трифторуксусная кислота, пропионовая кислота, капроновая кислота, гептановая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, о-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, п-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, п-толуолсульфоновая кислота, камфорсульфоновая кислота, 4 метилбицикло[2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 4,4'-метиленбис(3 гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота, триметилуксусная кислота, третбутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и тому подобные. Фармацевтически приемлемые соли также включают без ограничения основно-аддитивные соли,которые могут быть образованы, когда имеющиеся протоны кислоты способны взаимодействовать с неорганическими или органическими основаниями. Приемлемые неорганические основания включают без ограничения гидроксид натрия, карбонат натрия, гидроксид калия, гидроксид алюминия и гидроксид кальция. Приемлемые органические основания включают без ограничения этаноламин, диэтаноламин,триэтаноламин, трометамин, N-метилглюкамин и тому подобные."Терапевтически эффективное количество" означает такое количество соединения, которое при введении животному для лечения заболевания является достаточным для осуществления указанного лечения заболевания."Лечение" или "осуществление лечения" означает любое введение терапевтически эффективного количества соединения и включает:(1) предотвращение появления заболевания у животного, которое может быть предрасположено к заболеванию, но еще не испытывает или у которого еще не проявляется патология или симптоматика заболевания,(2) подавление заболевания у животного, которое испытывает или у которого проявляется патология или симптоматика заболевания (т.е. остановку дальнейшего развития патологии и/или симптоматики), или(3) ослабление заболевания у животного, которое испытывает или у которого проявляется патология или симптоматика заболевания (т.е. ремиссии патологии и/или симптоматики).-7 015169 Подробное описание изобретения 1. 2-[6-(3-Аминопиперидин-1-ил)-3-метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1-илметил]-4 фторбензонитрил и его композиции. Изобретение в общем относится к введению 2-[6-(3-аминопиперидин-1-ил)-3-метил-2,4-диоксо-3,4 дигидро-2 Н-пиримидин-1-илметил]-4-фторбензонитрила (называемого в настоящем описании "соединение I"), структура которого представлена ниже. Пример 1 описывает один способ синтеза соединения I. Следует отметить, что могут быть использованы другие способы синтеза соединения I, которые могут быть известны специалисту в данной области. Соединение I можно вводить в форме свободного основания, а также можно вводить в форме солей,гидратов и пролекарств, которые превращаются in vivo в форму свободного основания соединения I. Например, в объем настоящего изобретения включено введение соединения I в виде фармацевтически приемлемой соли, полученной с использованием различных органических и неорганических кислот и оснований способами, хорошо известными в данной области. В используемом в настоящем описании смысле подразумевается, что соединение I охватывает соли, гидраты и пролекарства соединения I, если не оговорено особо. Фармацевтически приемлемая соль соединения I предпочтительно обладает улучшенными фармакокинетическими свойствами по сравнению с формой свободного основания соединения I. Фармацевтически приемлемые соли также исходно могут придавать требуемые фармакокинетические свойства соединению I, которыми оно ранее не обладало, и даже могут положительно влиять на фармакодинамику соединения в отношении терапевтической активности в организме. Конкретные примеры солей, гидратов и пролекарств соединения I включают, без ограничения,формы солей, образованных неорганическими или органическими кислотами, например гидрогалогениды, такие как гидрохлорид, гидробромид, гидройодид; другие неорганические кислоты и соответствующие соли указанных кислот, такие как сульфат, нитрат, фосфат и т.д.; алкил- и моноарилсульфонаты,такие как этансульфонат, толуолсульфонат и бензолсульфонат; и другие органические кислоты и соответствующие соли указанных кислот, такие как ацетат, трифторацетат, тартрат, малеат, сукцинат, цитрат,бензоат, салицилат и аскорбат. Следующие кислотно-аддитивные соли включают без ограничения: адипат, альгинат, аргинат, аспартат, бисульфат, бисульфит, бромид, бутират, камфорат, камфорсульфонат,каприлат, хлорид, хлорбензоат, циклопентанпропионат, диглюконат, дигидрофосфат, динитробензоат,додецилсульфат, фумарат, галактерат (из муциновой кислоты), галактуронат, глюкогептаноат, глюконат,глутамат, глицерофосфат, гемисукцинат, гемисульфат, гептаноат, гексаноат, гиппурат, гидрохлорид,гидробромид, гидройодид, 2-гидроксиэтансульфонат, йодид, изетионат, изобутират, лактат, лактобионат,малат, малонат, манделат, метафосфат, метансульфонат, метилбензоат, моногидрофосфат, 2-нафталинсульфонат, никотинат, нитрат, оксалат, олеат, памоат, пектинат, персульфат, фенилацетат, 3-фенилпропионат, фосфат, фосфонат и фталат. В конкретных вариантах соединение I вводят в виде HCl-соли, метансульфоната, сукцината, бензоата, толуолсульфоната, R-(-)манделата или бензолсульфонатной соли соединения I. В примере 1 описано получение сукцинатной соли соединения I. 2. Введение и применение соединенеия I. Изобретение, в общем, относится к способу, включающему введение соединения I пациенту в суточной дозе от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I (в каждом случае в расчете на основе молекулярной массы формы свободного основания соединения I). Конкретные дозовые количества, которые можно применять, включают без ограничения 2,5, 5, 6,25, 10, 20, 25, 50, 75 и 100 мг соединения I в сутки. Следует отметить, что, если не оговорено особо, соединение I можно вводить в форме свободного основания или в виде фармацевтически приемлемой соли. Однако дозовые количества и диапазоны, приведенные в настоящем описании, всегда основаны на молекулярной массе формы свободного основания соединения I. Изобретение также относится к способу, включающему введение соединения I пациенту один раз в неделю в дозе от 1 до 250 мг/сутки соединения I, необязательно от 10 до 200 мг соединения I, необязательно от 10 до 150 мг соединения I и необязательно от 10 до 100 мг соединения I (в каждом случае в расчете на основе молекулярной массы формы свободного основания соединения I). Конкретные дозовые количества, которые можно применять, включают без ограничения 2,5, 5, 6,25, 10, 20, 25, 50, 75 и 100 мг соединения I в неделю по схеме введения один раз в неделю. Следует отметить, что, если не ого-8 015169 ворено особо, соединение I можно вводить в форме свободного основания или в виде фармацевтически приемлемой соли. Однако дозовые количества и диапазоны, приведенные в настоящем описании, всегда основаны на молекулярной массе формы свободного основания соединения I. Соединение I можно вводить любым способом введения. Однако в конкретных вариантах способ согласно настоящему изобретению осуществляют на практике пероральным введением соединения I. Указанный тип введения имеет преимущества, так как является простым, и пациент может осуществлять введение самостоятельно. Соединение I можно вводить один или несколько раз в сутки. Однако преимущество настоящего изобретения заключается в том, что соединение I можно эффективно вводить при уровнях доз, указанных в настоящем описании, один раз в сутки, а также можно вводить в стандартной лекарственной форме один раз в сутки. Наличие возможности вводить соединение I при соблюдении уровней доз, указанных в настоящем описании, только один раз в сутки и перорально, облегчает пациентам самостоятельное введение соединение I, таким образом улучшая соблюдение режима приема пациентами, которым требуется ингибирование in vivo активности DPP-IV. Преимущество состоит в том, что соединение I подходит для длительного непрерывного применения и его можно вводить пациентам в течение длительного периода времени. Соответственно можно осуществлять способ, при котором соединение I вводят пациенту каждый день (необязательно 1 раз в день) в течение периода времени, составляющего по меньшей мере 1 месяц, необязательно в течение по меньшей мере 3 месяцев и при необходимости необязательно на протяжении всего заболевания пациентов. Вследствие длительного ингибирующего действия соединений I на DPP-IV, предполагается, что может быть использована схема дозирования с менее частым введением, чем один раз в сутки. Преимущество состоит в том, что соединение I можно вводить в любое время суток. Необязательно соединение I вводят ежедневно один раз в сутки, при этом введение осуществляют утром до приема пищи. Так как соединение I может стимулировать секрецию инсулина, когда уровень глюкозы в крови становится выше 100 мг/дл, то может быть полезным наличие соединения I в кровообращении до повышения уровня глюкозы в крови, которое происходит после приема пищи. Соединение I можно вводить любому пациенту, который получает пользу от лечения, приводящего к уменьшению активности DPP-IV in vivo. На фиг. 1 и в примере 3 описано наблюдаемое действие, которое оказывает введение соединения I на активность DPP-IV в плазме обезьян после однократного перорального введения. Как можно видеть по данным, показанным на фиг. 1, посредством введения соединения I один раз в сутки на уровне доз, указанных в настоящем описании, соединение I можно эффективно использовать в отношении патологических состояний, при которых требуется уменьшение активности DPP-IV в плазме. Принимая во внимание представленные данные, полагают, что при введении пациенту по меньшей мере 2,5 мг соединения I, активность DPP-IV в плазме пациента может быть снижена на более, чем 60% по сравнению с исходным уровнем в течение периода времени, составляющего по меньшей мере 6, 12, 18 и даже 24 ч после введения. Примеры конкретных применений способа на основе введения соединения I включают, без ограничения, предотвращение, замедление прогрессирования и/или лечение состояний, опосредованных DPPIV, в частности диабета и более конкретно сахарного диабета типа 2, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), метаболического ацидоза, кетоза, регуляции аппетита, ожирения и осложнений, связанных с диабетом, включая диабетическую нейропатию, диабетическую ретинопатию, воспалительное заболевание кишечника, болезнь Крона, индуцированный химиотерапией энтерит, мукозит слизистой оболочки рта, синдром укороченной кишки и заболевание почек. Состояния, опосредованные DPP-IV, кроме того, включают гиперлипидемию, такую как гипертриглицеридемия, гиперхолестеринемия, низкий уровень ЛПВП и постпрандиальная гиперлипидемия; артериосклероз; гипертонию; инфаркт миокарда, стенокардию, церебральный инфаркт, апоплексию головного мозга и метаболический синдром. Предполагается, что введение соединения I пациентам с диабетом типа I или типа II после минимального лечения по меньшей мере в течение 30 суток будет улучшать один или несколько показателей сердечно-сосудистой системы. Примеры показателей сердечно-сосудистой системы, которые могут быть улучшены, включают, без ограничения, снижение среднего систолического кровяного давления, увеличение уровня холестерина ЛПВП, улучшение соотношения ЛПНП/ЛПВП и уменьшение уровня триглицеридов. Также предполагается, что введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями пациентам с диабетом типа I или типа II после минимального лечения в течение по меньшей мере 30 суток будет улучшать один или несколько показателей сердечно-сосудистой системы. Примеры показателей сердечно-сосудистой системы, которые могут быть улучшены, включают, без ограничения, снижение среднего систолического кровяного давления, увеличение уровня холестерина ЛПВП, улучшение соотношения ЛПНП/ЛПВП и уменьшение уровня триглицеридов. Также предполагается, что введение соединения I в комбинации с одним или несколькими антидиабетическими средствами или инкретинами пациентам с желудочно-кишечными воспалительными забо-9 015169 леваниями (включая, без ограничения, воспалительное заболевание кишечника, болезнь Крона, индуцированный химиотерапией энтерит, мукозит слизистой оболочки ротовой полости и синдром укороченной кишки) после минимального лечения в течение по меньшей мере 30 суток будет улучшать состояние слизистой оболочки, выстилающей желудочно-кишечный тракт. Показателями улучшения состояния слизистой оболочки, выстилающей желудочно-кишечный тракт, могут быть необязательно увеличение площади поверхности кишечника, уменьшение воспаления и/или увеличение всасывания питательных веществ. В одном варианте соединение I вводят пациенту с диабетом типа 2. Пациенты, получающие соединение I, также могут иметь нарушение функции секреции инсулина из островков поджелудочной железы, а не развитую резистентность к инсулину в периферических чувствительных к инсулину тканях/органах. Преимущество заключается в том, что введение соединения I один раз в сутки или один раз в неделю при уровнях доз, указанных в настоящем описании, также можно использовать для лечения пациентов, у которых имеет место преддиабетическое состояние. Предполагается, что введение соединения I пациенту, у которого имеется преддиабетическое состояние, служит для замедления развития диабета типа II у указанного пациента. Длительное увеличение уровня глюкозы в крови десенсибилизирует функцию островков поджелудочной железы и нарушает секрецию инсулина. При повышении уровней циклического АМФ и улучшении динамики кальция в бета-клетках активируются гены, восстанавливающие поврежденные клеточные компоненты, и клетки становятся менее подверженными токсичному действию глюкозы. Предполагается, что введение соединения I один раз в сутки или один раз в неделю при уровнях доз, указанных в настоящем описании, оказывает ряд желательных биологических действий in vivo. Например, введение соединения I один раз в сутки или один раз в неделю при уровнях доз, указанных в настоящем описании, снижает уровень глюкозы в крови пациента по сравнению с контролем в виде плацебо. Указанное снижение постпрандиальных уровней глюкозы в крови помогает пациентам с диабетом поддерживать более низкие уровни глюкозы. Также предполагается, что введение соединения I один раз в сутки или один раз в неделю при уровнях доз, указанных в настоящем описании, оказывает влияние в виде увеличения уровня инсулина у пациента или чувствительности к инсулину. Инсулин способствует поступлению глюкозы в мышечную,жировую и несколько других тканей. Механизм, посредством которого клетки могут поглощать глюкозу,осуществляется посредством облегченной диффузии при стимуляции рецептора инсулина. С-пептид и инсулин представляют собой цепи белка, образуемые при активации и расщеплении проинсулина (неактивного предшественника инсулина). С-пептид и инсулин образуются и хранятся в бета-клетках поджелудочной железы. Когда инсулин высвобождается в кровяное русло, также высвобождаются равные количества С-пептида. Это делает С-пептид применимым в качестве маркера продукции инсулина. Предполагается, что введение соединения I согласно настоящему изобретению увеличивает уровень Спептида у пациента. Также предполагается, что введение соединения I один раз в сутки при уровнях доз, указанных в настоящем описании, оказывает влияние в виде снижения уровня гемоглобина A1c у пациента на более чем 0,5% по сравнению с контролем в виде плацебо после длительного лечения соединением I. Кроме того, также предполагается, что введение соединения I один раз в неделю при уровнях доз, указанных в настоящем описании, оказывает влияние в виде снижения уровня гемоглобина A1c у пациента на более чем 0,2% по сравнению с контролем в виде плацебо после длительного лечения соединением I. Известно,что значения Hb-А 1 с прямо пропорциональны концентрации глюкозы в крови, наблюдаемой на протяжении периода времени, соответствующего продолжительности жизни эритроцитов. Таким образом, HbА 1 с является показателем уровней глюкозы в крови пациента в последние предшествующие 90 дней,особенно в последние 30 дней. Таким образом, наблюдаемое уменьшение уровня гемоглобина A1c у пациента подтверждает устойчивое снижение уровней глюкозы в крови пациента в результате введения соединения I один раз в сутки в случае уровней доз, указанных в настоящем описании. 3. Комбинированная терапия, включающая соединение I. Изобретение также относится к применению соединения I в комбинации с одним или несколькими другими антидиабетическими соединениями и/или инкретинами. Примеры других антидиабетических соединений включают, без ограничения, модуляторы пути передачи сигнала инсулина, подобные ингибиторам протеинтирозинфосфатазы (РТР-азы) и ингибиторам глутаминфруктозо-6-фосфатамидотрансферазы (GFAT); соединения, влияющие на нарушенную регуляцию продукции глюкозы в печени,подобные ингибиторам глюкозо-6-фосфатазы (G6P-азы), ингибиторам фруктозо-1,6-бисфосфатазы (F1,6-ВР-азы), ингибиторам гликогенфосфорилазы (GP), антагонистам рецептора глюкагона и ингибиторам фосфоенолпируваткарбоксикиназы (РЕРСК); ингибиторы киназы пируватдегидрогеназы (PDHK); усилители чувствительности к инсулину (сенсибилизаторы инсулина); усилители секреции инсулина (стимуляторы секреции инсулина); ингибиторы альфа-глюкозидазы; ингибиторы опорожнения желудка; активаторы глюкокиназы, агонисты рецептора GLP-1, агонисты рецептора GLP-2, модуляторы UCP, модуляторы RXR, ингибиторы GSK-3, модуляторы PPAR, метформин, инсулин; и антагонисты 2-адренер- 10015169 гических рецепторов. Соединение I можно вводить по меньшей мере с одним другим антидиабетическим соединением либо одновременно в виде одной дозы, в одно время в виде раздельных доз или последовательно (т.е. когда одно соединение вводят до или после другого соединения). Примеры ингибиторов РТР-азы, которые можно использовать в комбинации с соединением I,включают, без ограничения, ингибиторы, описанные в патентах США 6057316, 6001867 и публикациях РСТWO 99/58518, WO 99/58522, WO 99/46268, WO 99/46267, WO 99/46244, WO 99/46237,WO 99/46236 и WO 99/15529. Примеры ингибиторов GFAT, которые можно использовать в комбинации с соединением I, включают, без ограничения, ингибиторы, описанные в Mol. Cell. Endocrinol. 1997, 135(1), 67-77. Примеры ингибиторов G6P-азы, которые можно использовать в комбинации с соединением I,включают, без ограничения, ингибиторы, описанные в публикациях РСТWO 00/14090, WO 99/40062 и WO 98/40385, публикации европейского патентаЕР 682024 и в Diabetes 1998, 47,16301636. Примеры ингибиторов F-1,6-ВР-азы, которые можно использовать в комбинации с соединением I,включают, без ограничения, ингибиторы, описанные в публикациях РСТWO 00/14095, WO 99/47549, WO 98/39344, WO 98/39343 и WO 98/39342. Примеры ингибиторов GP, которые можно использовать в комбинации с соединением I, включают,без ограничения, ингибиторы, описанные в патенте США 5998463, публикациях РСТWO 99/26659, WO 97/31901, WO 96/39384 и WO 9639385 и публикациях европейских патентовЕР 978279 и ЕР 846464. Примеры антагонистов рецепторов глюкагона, которые можно использовать в комбинации с соединением I, включают, без ограничения, антагонисты, описанные в патентах США 5880139 и 5776954,публикациях РСТWO 99/01423, WO 98/22109, WO 98/22108, WO 98/21957, WO 97/16442 и WO 98/04528, и антагонисты, описанные в Bioorg. Med. Chem. Lett 1992, 2, 915-918, J. Med. Chem. 1998, 41,5150-5157, и J. Biol Chem. 1999, 274, 8694-8697. Примеры ингибиторов РЕРСК, которые можно использовать в комбинации с соединением I, включают, без ограничения, ингибиторы, описанные в патенте США 6030837 и в Mol. Biol. Diabetes 1994,2, 283-99. Примеры ингибиторов PDHK, которые можно использовать в комбинации с соединением I, включают, без ограничения, ингибиторы, описанные в J. Med. Chem. 42 (1999) 2741-2746. Примеры усилителей чувствительности к инсулину,. которые можно использовать в комбинации с соединением I, включают, без ограничения, ингибиторы GSK-3, агонисты ретиноидного рецептора X(RXR), агонисты бета-3 AR, модуляторы UCP, антидиабетические тиазолидиндионы (глитазоны), агонисты PPAR-гамма неглитазонового типа, двойные агонисты PPAR-гамма/PPAR-альфа, антидиабетические ванадийсодержащие соединения и бигуаниды, такие как метформин. Примеры ингибиторов GSK-3 включают, без ограничения, ингибиторы, описанные в публикациях РСТWO 00/21927 и WO 97/41854. Примеры модуляторов RXR включают без ограничения модуляторы, описанные в патентах США 4981784, 5071773, 5298429 и 5506102 и публикациях РСТWO 89/05355, WO 91/06677, WO 92/05447, WO 93/11235, WO 95/18380, WO 94/23068 и WO 93/23431. Примеры агонистов бета-3 AR включают без ограничения CL-316243 (Lederle Laboratories) и агонисты, описанные в патенте США 5705515 и публикациях РСТWO 99/29672, WO 98/32753, WO 98/20005, WO 98/09625, WO 97/46556 и WO 97/37646. Примеры модуляторов UCP включают агонисты UCP-1, UCP-2 и UCP-3. Примеры модуляторовCommun., Vol. 235(1) pp. 79-82 (1997). Примеры антидиабетических модулирующих PPAR тиазолидиндионов (глитазонов) включают, без ограничения, (S)-3,4-дигидро-2-(фенилметил)-2 Н-1-бензопиран-6-ил)метил)тиазолидин-2,4-дион (энглитазон),5-[4-(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метилтиазолидин-2,4-дион(AD-5075),5-[4-(1-фенил-1 циклопропанкарбониламино)бензил]тиазолидин-2,4-дион (DN-108), 5-[4-2-(2,3-дигидроиндол-1-ил) этокси]фенилметилтиазолидин-2,4-дион, 5-[3(4-хлорфенил)-2-пропинил]-5-фенилсульфонилтиазолидин-2,4-дион, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2,4-дион, 5-[4-(2(метил-2-пиридиниламино)этокси)фенил]метилтиазолидин-2,4-дион (розиглитазон), 5-[4-(2-(5-этил-2 пиридил) этокси)фенил]метилтиазолидин-2,4-дион (пиоглитазон; продаваемый под торговой маркой(KRP297). Примеры агонистов PPAR-гамма неглитазонового типа включают, без ограничения, аналоги N-(2 бензоилфенил)-L-тирозина, такие как GI-262570, регликсан (JTT501) и FK-614 и метаглидазен (МВХ 102). Примеры двойных агонистов PPAR-гамма/PPAR-альфа включают, без ограничения, омега[(оксохиназолинилалкокси)фенил]алканоаты и их аналоги, включая такие, которые описаны в публикации РСТWO 99/08501 и Diabetes 2000, 49(5), 759-767; тезаглитазар, мураглитазар и навеглитазар. Примеры антидиабетических ванадийсодержащих соединений включают, без ограничения, соединения, описанные в патенте США 5866563. Метформин (диметилдигуанид) и его гидрохлоридная соль продаются под торговой маркой GLUCOPHAGE. Примеры усилителей секреции инсулина включают, без ограничения, антагонисты рецептора глюкагона (которые описаны выше), производные сульфонилмочевины, инкретиновые гормоны или их миметики, особенно глюкагон-подобный пептид-1 (GLP-1) или агонисты GLP-1, антагонисты рецептора имидазолина бета-клеток и кратковременно действующие стимуляторы секреции инсулина, подобные антидиабетическим производным фенилуксусной кислоты, антидиабетические производные Dфенилаланина и митиглинид и его фармацевтически приемлемые соли. Примеры производных сульфонилмочевины включают, без ограничения, глизоксепид, глибурид,глибенкламид, ацетогексамид, хлорпропамид, глиборнурид, толбутамид, толазамид, глипизид, карбутамид, гликвидон, глигексамид, фенбутамид, толцикламид, глимепирид и гликлазид. Толбутамид, глибенкламид, гликлазид, глиборнурид, гликвидон, глизоксепид и глимепирид можно вводить в форме, в которой они продаются под торговыми марками RASTINON HOECHS, AZUGLUCON,DIAMICRON, GLUBORID, GLURENORM, PRO-DIABAN и AMARYL соответственно. Примеры агонистов GLP-1 включают, без ограничения, агонисты, описанные в патентах США 5120712, 5118666 и 5512549 и публикации РСТWO 91/11457. В частности, агонисты GLP-1 включают соединения, подобные GLP-1 (7-37), в. котором амидная функциональная группа на карбоксильном конце Arg36 заменена Gly в положении 37 молекулы GLP-1 (7-36)NH2, и его варианты и аналоги, включаяGLN9-GLP-1 (7-37), D-GLN9-GLP-1 (7-37), ацетил-LYS9-GLP-1 (7-37), LYS18-GLP-1 (7-37) и, в частности,GLP-1 (7-37) ОН, VAL8-GLP-1 (7-37), GLY8-GLP-1 (7-37), THR8-GLP-1 (7-37), GLP-1 (7-37) и 4 имидазопропионил-GLP-1. Одним конкретным примером агониста GLP-1 является экстендатид, амид 39-аминокислотного пептида, который продается под торговой маркой BYETTA. Эксенатид имеет эмпирическую формулуC184H282N50O60S и молекулярную массу 4186,6 дальтон. Эксенатид имеет следующую аминокислотную последовательность: Н-His-Gly-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-ValArg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-NH2. Примеры глюкагон-подобного пептида-2 (GLP-2) или агонистов GLP-2 включают, без ограничения,соединения, описанные в патенте США 7056886 и публикациях РСТWO 00/53208, WO 01/49314 и WO 03/099854. Одним конкретным примером агониста GLP-2 является TEDUGLUTIDE, амид 39 аминокислотного пептида (NPS Pharmaceuticals, Inc.). Примеры антагонистов рецептора имидазолина бета-клеток включают, без ограничения, антагонисты, описанные в публикации РСТWO 00/78726 и в J. Pharmacol. Exp. Ther. 1996, 278, 82-89. Примером антидиабетического производного фенилуксусной кислоты является репаглинид и его фармацевтически приемлемые соли. Примеры антидиабетических производных D-фенилаланина включают, без ограничения, натеглинид (N-[(транс-4-изопропилциклогексил)карбонил]-D-фенилаланин, ЕР 196222 и ЕР 526171) и репаглинид S)-2-этокси-4-2-3-метил-1-[2-(1-пиперидинил)фенил]бутил]амино]-2-оксоэтилбензойная кислота, ЕР 0147850 А 2 и ЕР 0207331 А 1). Подразумевается, что натеглинид включает конкретные кристаллические формы (полиморфы), описанные в патенте США 5488510 и публикации европейского патентаЕР 0526171 В 1. Репаглинид и натеглинид могут быть введены в форме, в которой они продаются под торговой маркой NOVONORM и STARLIX, соответственно. Примеры ингибиторов альфа-глюкозидазы включают, без ограничения, акарбозу, N-(1,3 дигидрокси-2-пропил)валиоламин (воглибозу) и производное 1-дезоксинойиримицина миглитол. Акарбоза представляет собой 4",6"-дидезокси-4'-[(1S)-(1,4,6/5)-4,5,6-тригидрокси-3-гидроксиметил-2-циклогексениламино)мальтотриозу. Структура акарбозы также может быть описана как O-4,6-дидезокси-41S,4R,5S,6S]-4,5,6-тригидрокси-3-(гидроксиметил)-2-циклогексен-1-ил]амино-альфа-D-глюкопиранозил-(1-4)-О-альфа-D-глюкопиранозил-(1-4)-D-глюкопираноза (патент США 4062950 и публикация европейского патентаЕР 0226121). Акарбозу и миглитол можно вводить в формах, которые продаются под торговыми марками GLUCOBAY и DIASTABOL 50, соответственно. Примеры ингибиторов опорожнения желудка, отличных от GLP-1, включают, без ограничения, ингибиторы, описанные в J. Clin. Endocrinol. Metab. 2000, 85(3), 1043-1048, и Diabetes Care 1998; 21; 897893, в частности амилин и его аналоги, такие как прамлинтид. Амилин описан в Diabetologia 39, 1996,- 12015169 492-499. Примеры 2-адренергических антагонистов включают, без ограничения, мидаглизол, который описан в Diabetes 36, 1987, 216-220. Инсулин, который можно использовать в комбинации с соединением I,включает, без ограничения, препараты инсулина животных, экстрагированного из поджелудочной железы коров и свиней; препараты инсулина человека, генетически синтезированного с использованием Escherichia coli или дрожжей; цинк-инсулин; протамин-цинк-инсулин; фрагмент или производное инсулина(например, INS-1) и пероральный препарат инсулина. В одном конкретном варианте антидиабетическое соединение, вводимое в комбинации с соединением I, выбрано из группы, состоящей из натеглинида, митиглинида, репаглинида, метформина, экстендатида, розиглитазона, тезаглитазара, пиоглитазона, глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида, толазамида, глипизида, карбутамида, гликвидона,глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. Примеры получения и приготовления препаратов ингибиторов РТР-азы, ингибиторов GSK-3, миметиков, не являющихся малыми молекулами, ингибиторов GFAT, ингибиторов G6P-азы, антагонистов рецептора глюкагона, ингибиторов РЕРСК и ингибиторов F-1,6-BP-азы, ингибиторов GP, модуляторовRXR, агонистов бета-3 AR, ингибиторов PDHK, ингибиторов опорожнения желудка и модуляторов UCP описаны в патентах, заявках и публикациях, указанных в настоящем описании. В случае комбинированной терапии с соединением I другое антидиабетическое соединение может быть введено (например, в отношении пути и формы дозирования) таким образом, который известен для указанного соединения. Соединение I и другое антидиабетическое соединение могут быть введены последовательно (т.е. в разных временных точках) или в одно и то же время, либо один после другого по отдельности в виде двух разных форм дозирования, либо в виде одной комбинированной стандартной лекарственной формы. В одном конкретном варианте другое антидиабетическое соединение вводят с соединением I в виде одной комбинированной стандартной лекарственной формы. Доза антидиабетического соединения может быть выбрана из диапазона, известного для клинического применения указанного соединения. Любые терапевтические соединения для лечения диабетических осложнений, антигиперлипидемические соединения, соединения против ожирения или противогипертонические соединения можно использовать в комбинации с соединением I таким же образом, как и указанные выше антидиабетические соединения. Примеры терапевтических соединений для лечения диабетических осложнений включают без ограничения, ингибиторы альдозоредуктазы, такие как толрестат, эпалрестат, зенарестат,зополрестат, миналрестат, фидарестат, СТ-112 и ранирестат; нейротрофические факторы и увеличивающие их уровень соединения, такие как NGF, NT-3, BDNF и активаторы продукции-секреции нейротрофина, описанные в WO 01/14372 (например, 4-(4-хлорфенил)-2-(2-метил-1-имидазолил)-5-[3-(2-метилфенокси)пропил]оксазол); стимуляторы регенерации нервной ткани, такие как Y-128; ингибиторы РКС,такие как мезилат рубоксистаурина; ингибиторы AGE, такие как ALT946, пимагедин, бромид Nфенацилтиазолия (ALT766) , ALT-711, ЕХО-226, пиридорин и пиридоксамин; ловушки активных форм кислорода, такие как тиоктовая кислота; средства, расширяющие сосуды головного мозга, такие как тиаприд и мексилетин; агонисты рецептора соматостатина, такие как BIM23190; и ингибиторы регулирующей сигналы апоптоза киназы-1 (ASK-1). Примеры антигиперлипидемических соединений включают,без ограничения, ингибиторы HMG-CoA-редуктазы, такие как правастатин, симвастатин, ловастатин,аторвастатин, флувастатин, росувастатин и питавастатин; ингибиторы скваленсинтазы, такие как соединения, описанные в WO 97/10224 (например, N-(3R,5S)-1-(3-ацетокси-2,2-диметилпропил)-7-хлор-5(2,3-диметоксифенил)-2-оксо-1,2,3,5-тетрагидро-4,1-бензоксазепин-3-ил]ацетил]пиперидин-4-уксусная кислота); фибратные соединения, такие как безафибрат, клофибрат, симфибрат и клинофибрат; ингибиторы АСАТ, такие как авасимиб и эфлуцимиб; анионообменные смолы, такие как колестирамин; пробукол; основанные на никотиновой кислоте лекарственные средства, такие как никомол и ницеритрол; этиликозапентат; и растительные стерины, такие как соевый стерин и -оризанол. Примеры соединений против ожирения включают, без ограничения, дексфенфлурамин, фенфлурамин, фентермин, сибутрамин,амфепрамон, дексамфетамин, мазиндол, фенилпропаноламин, клобензорекс; антагонисты рецептора МСН, такие как SB-568849 и SNAP-7941; антагонисты нейропептида Y, такие как СР-422935; антагонисты каннабиноидных рецепторов, такие как SR-141716 и SR-147778; антагонисты грелина; ингибиторы 11-гидроксистероиддегидрогеназы, такие как BVT-3498; ингибиторы липазы поджелудочной железы,такие как орлистат и ATL-962; агонисты бета-3 AR, такие как AJ-9677; пептидные средства, снижающие аппетит, такие как лептин и CNTF (цилиарный нейротрофический фактор); агонисты холецистокинина,такие как линтитрипт и FPL-15849; и средство, сдерживающее потребление пищи, такое как Р-57. Примеры противогипертонических соединений включают ингибиторы фермента превращения ангиотензина,такие как каптоприл, эналаприл и делаприл; антагонисты ангиотензина II, такие как кандесартан цилексетил, лозартан, эпросартан, валсартан, телмисартан, ирбесартан, олмесартан медоксомил, тазосартан и 1-2'-(2,5-дигидро-5-оксо-4 Н-1,2,4-оксадиазол-3-ил)бифенил-4-ил]метил]-2-этокси-1 Н-бензимидазол-7 карбоновая кислота; блокаторы кальциевых каналов, такие как манидипин, нифедипин, никардипин, ам- 13015169 лодипин и эфонидипин; открыватели калиевых каналов, такие как левкромакалим, L-27152, AL0671 иNIP-121; и клонидин. Структуру активных средств, указанных в настоящем описании кодовыми номерами, родовыми или коммерческими названиями, можно найти в современной редакции стандартного руководства "ThePublications). Соответствующее содержание указанных источников включено в настоящее описание в виде ссылки. Любой специалист в данной области вполне может идентифицировать активные средства, а также на основе указанных ссылок может создать и тестировать показания к фармацевтическому применению и фармацевтические свойства в стандартных моделях для тестирования, как in vitro, так и in vivo. 4. Композиции, содержащие соединение I. Соединение I может входить в состав фармацевтической композиции, приспособленной для различных путей введения. Например, соединение I может входить в состав фармацевтической композиции,приспособленной для введения путем, выбранным из группы, состоящей из перорального, парентерального, внутрибрюшинного, внутривенного, внутриартериального, трансдермального, подъязычного, внутримышечного, ректального, трансбуккального, интраназального, липосомного, ингаляционного, вагинального, внутриглазного введения, локальной доставки (например, через катетер или стент), подкожного, введения в жировую ткань, внутрисуставного, внутрибрюшинного и интратекального введения. Как таковое соединение I может быть приготовлено в различных фармацевтически приемлемых композициях, включая инъекционные формы (например, для подкожных, внутривенных, внутримышечных и внутрибрюшинных инъекций), капельные инфузии, формы для наружного применения (например, препараты в виде назальных спреев, трансдермальные препараты; мази и т.д.) и суппозитории (например, ректальные и вагинальные суппозитории). Указанные различные фармацевтически приемлемые композиции могут быть приготовлены различными способами, обычно используемыми в фармацевтической промышленности, с фармацевтически приемлемым носителем, обычно используемым в фармацевтической промышленности. В используемом в настоящем описании смысле подразумевается, что композиция, содержащая соединение I, включает форму свободного основания соединения I, соли, гидраты и пролекарства соединения I, а также другие вещества, которые могут быть включены в состав указанной композиции для достижения предполагаемой цели, включая другие активные ингредиенты, если не оговорено особо. Конкретные формы солей соединения I, которые могут быть использованы, включают, без ограничения, HClсоль, метансульфонат, сукцинат, бензоат, толуолсульфонат, R-(-)манделат или бензолсульфонатную соль соединения I. Как указано выше, соединение I предпочтительно можно применять при введении пациенту в суточной дозе от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I (в каждом случае в расчете на молекулярную массу формы свободного основания соединения I) . Конкретные дозовые количества, которые можно использовать, включают, без ограничения, 2,5, 5, 6,25, 10, 20, 25, 50, 75 и 100 мг соединения I в сутки. Как указано выше, желательно вводить соединение I один раз в сутки. Соответственно, фармацевтические композиции согласно настоящему изобретению могут быть в стандартной лекарственной форме, содержащей от 1 до 250 мг/сутки соединения I, необязательно от 2,5 до 200 мг соединения I, необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I. В конкретных вариантах фармацевтическая композиция содержит 2,5, 5, 6,25, 10, 20, 25, 50, 75 или 100 мг соединения I. Как указано выше, соединение I преимущественно можно применять посредством перорального введения. Соответственно, композиции согласно настоящему изобретению необязательно могут быть приспособлены для перорального введения. В одном варианте указанная фармацевтическая композиция представляет собой твердый препарат, предназначенный для перорального введения. В этом отношении композиция, например, может быть в форме таблетки или капсулы. В примере 2 предлагаются примеры твердых препаратов, содержащих соединение I, предназначенных для перорального введения. В другом варианте указанная фармацевтическая композиция представляет собой жидкий препарат, приспособленный для перорального введения. Также, как указано выше, соединение I преимущественно можно применять посредством парентерального введения. Соответственно, композиции согласно настоящему изобретению необязательно могут быть приспособлены для парентерального введения. В одном варианте указанная фармацевтическая композиция представляет собой состав в виде раствора, предназначенный для парентерального введения. В другом варианте указанная фармацевтическая композиция представляет собой суспензионный препарат, приспособленный для парентерального введения. Как указано выше, соединение I преимущественно можно применять в комбинации с одним или несколькими другими антидиабетическими соединениями и/или инкретинами. Соответственно, композиции согласно настоящему изобретению необязательно могут содержать соединение I в комбинации с одним или несколькими другими антидиабетическими соединениями или- 14015169 инкретинами в одной комбинированной стандартной лекарственной форме. Необязательно указанная комбинированная стандартная лекарственная форма, содержащая соединение I в комбинации с одним или несколькими другими антидиабетическими соединениями и/или инкретинами, предназначена для перорального введения и необязательно представляет собой твердую пероральную лекарственную форму. Альтернативно, указанная комбинированная стандартная лекарственная форма, содержащая соединение I в комбинации с одним или несколькими другими антидиабетическими средствами и/или инкретинами, может быть предназначена для парентерального введения и необязательно может иметь форму дозируемого раствора. В одном варианте указанная комбинированная стандартная лекарственная форма, содержащая соединение I в комбинации с одним или несколькими другими антидиабетическими соединениями, содержит от 1 до 250 мг/сутки соединения I, вводимого пациенту, необязательно от 2,5 до 200 мг соединения I,необязательно от 2,5 до 150 мг соединения I и необязательно от 5 до 100 мг соединения I (в каждом случае в расчете на молекулярную массу формы свободного основания соединения I). В конкретных вариантах указанная комбинированная стандартная лекарственная форма, содержащая соединение I в комбинации с одним или несколькими другими антидиабетическими соединениями, содержит 2,5, 5, 6,25, 10, 20,25, 50, 75 и 100 мг соединения I. Любое антидиабетическое соединение или группу антидиабетических соединений можно объединять с соединением I с образованием указанной комбинированной стандартной лекарственной формы. В конкретных вариантах указанная комбинированная стандартная лекарственная форма содержит соединение I и один или несколько представителей группы, состоящей из модуляторов пути передачи сигнала инсулина, подобных ингибиторам протеинтирозинфосфатазы (РТР-азы) и ингибиторам глутаминфруктозо-6-фосфатамидотрансферазы (GFAT), соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, подобных ингибиторам глюкозо-6-фосфатазы (G6P-азы), ингибиторам фруктозо-1,6-бисфосфатазы (F-1,6-ВР-азы), ингибиторам гликогенфосфорилазы (GP), антагонистам рецептора глюкагона и ингибиторам фосфоенолпируваткарбоксикиназы (PEPCK), ингибиторов киназы пируватдегидрогеназы (PDHK), усилителей чувствительности к инсулину (сенсибилизаторов инсулина), усилителей секреции инсулина (стимуляторов секреции инсулина), ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, активаторов глюкокиназы, агонистов рецептора GLP-1, агонистов рецептораGLP-2, модуляторов UCP, модуляторов RXR, ингибиторов GSK-3, модуляторов PPAR, метформина, инсулина и антагонистов 2-адренергических рецепторов. Соединение I можно вводить по меньшей мере с одним другим антидиабетическим соединением либо одновременно в виде одной дозы, в одно время в виде раздельных доз или последовательно (т.е. когда одно соединение вводят до или после другого соединения). В одном варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и антидиабетический тиазолидиндион. Конкретные примеры тиазолидиндионов, которые можно использовать в настоящем варианте, включают, без ограничения, (S)-(3,4-дигидро-2-(фенилметил)-2 Н-1 бензопиран-6-ил)метилтиазолидин-2,4-дион (энглитазон), 5-[4-(3-(5-метил-2-фенил-4-оксазолил)-1 оксопропил)фенил]метилтиазолидин-2,4-дион (дарглитазон), 5-[(4-(1-метилциклогексил)метокси)фенил]метилтиазолидин-2,4-дион (циглитазон), 5-[4-(2-(1-индолил)этокси)фенил]метилтиазолидин-2,4 дион (DRF2189), 5-4-[(2-(5-метил-2-фенил-4-оксазолил)этокси)]бензилтиазолидин-2,4-дион (ВМ 13.1246), 5-(2-нафтилсульфонил)тиазолидин-2,4-дион (AY-31637), бис 4-[(2,4-диоксо-5-тиазолидинил) метил]фенилметан (YM268), 5-4-[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензилтиазолидин-2,4-дион (AD-5075), 5-[4-(1-фенил-1-циклопропанкарбониламино)бензил]тиазолидин-2,4-дион(CS-011) и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамид (KRP2 97). В одном конкретном варианте тиазолидиндионом в указанной комбинированной стандартной лекарственной форме является 5-[4-(2-(5-этил-2-пиридил)этокси)фенил]метилтиазолидин-2,4-дион (пиоглитазон) и его гидрохлоридная соль, которая продается под торговой маркой ACTOS. В другом конкретном варианте тиазолидиндионом является 5-[4-(2-(метил-2-пиридиниламино) этокси)фенил]метилтиазолидин-2,4-дион (розиглитазон) и его малеатная соль. В другом варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и агонист PPAR-гамма неглитазонового типа. В другом варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и бигуанид. Конкретным примером бигуанида, который можно использовать в настоящем варианте, является метформин (диметилдигуанид) и его гидрохлоридная соль, которая продается под торго- 15015169 вой маркой GLUCOPHAGE. В другом варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и производное сульфонилмочевины. Конкретные примеры производных сульфонилмочевины,которые можно использовать в настоящем варианте, включают без ограничения глизоксепид, глибурид,глибенкламид, ацетогексамид, хлорпропамид, глиборнурид, толбутамид, толазамид, глипизид, карбутамид, гликвидон, глигексамид, фенбутамид, толцикламид, глимепирид и гликлазид. Толбутамид, глибенкламид, гликлазид, глиборнурид, гликвидон, глизоксепид и глимепирид можно вводить в форме, в которой они продаются под торговыми марками RASTINON HOECHS, AZUGLUCON,DIAMICRON, GLUBORID, GLURENORM, PRO-DIABAN и AMARYL соответственно. В другом варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и антидиабетическое производное D-фенилаланина. Конкретные примеры антидиабетических производных D-фенилаланина, которые можно использовать в настоящем варианте, включают без ограничения репаглинид и натеглинид, которые можно вводить в форме, в которой они продаются под торговыми марками NOVONORM и STARLIX соответственно. В другом варианте указанная комбинированная стандартная лекарственная форма содержит соединение I и ингибитор альфа-глюкозидазы. Конкретные примеры ингибиторов альфа-глюкозидазы, которые можно использовать в настоящем варианте, включают, без ограничения, акарбозу, миглитол и воглибозу, которые можно вводить в форме, в которой они продаются под торговыми марками GLUCOBAY, DIASTABOL 50 и BASEN соответственно. В одном конкретном варианте антидиабетическое соединение, вводимое в комбинации с соединением I в указанной комбинированной стандартной лекарственной форме, выбрано из группы, состоящей из натеглинида, репаглинида, метформина, экстендатида, розиглитазона, пиоглитазона, глизоксепида,глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида, толбутамида, толазамида,глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. Что касается каждого из указанных выше вариантов осуществления и их вариаций, относящихся к комбинированной стандартной лекарственной форме, содержащей комбинацию соединения I и одного или нескольких других антидиабетических соединений, то фармацевтическая композиция необязательно может быть адаптирована для перорального введения и в связи с этим необязательно может представлять собой твердый препарат, такой как таблетка или капсула, или, альтернативно, может быть в виде жидкого препарата, адаптированного для перорального введения. Доза антидиабетического соединения может быть выбрана из диапазона, известного для клинического применения указанного соединения. Любые терапевтические соединения для лечения диабетических осложнений, антигиперлипидемические соединения, соединения против ожирения или противогипертонические соединения можно использовать в комбинации с соединением I таким же образом, как и указанные выше антидиабетические соединения. Примеры терапевтических соединений для лечения диабетических осложнений включают, без ограничения, ингибиторы альдозоредуктазы, такие как толрестат, эпалрестат, зенарестат, зополрестат, миналрестат, фидарестат, СТ-112 и ранирестат; нейтрофические факторы и увеличивающие их уровень соединения, такие как NGF, NT-3, BDNF и активаторы продукции-секреции нейротрофина, описанные в WO 01/14372 (например, 4-(4-хлорфенил)-2-(2-метил-1-имидазолил)-5-[3-(2-метилфенокси)пропил]оксазол); стимуляторы регенерации нервной ткани, такие как Y-128; ингибиторы РКС, такие как мезилат рубоксистаурина; ингибиторы AGE, такие как ALT946, пимагедин, бромид N-фенацилтиазолия (ALT766), ALT711, ЕХО-226, пиридорин и пиридоксамин; ловушки активных форм кислорода, такие как тиоктовая кислота; средства, расширяющие сосуды головного мозга, такие как тиаприд и мексилетин; агонисты рецептора соматостатина, такие как BIM23190; и ингибиторы регулирующей сигналы апоптоза киназы-1(ASK-1). Примеры антигиперлипидемических соединений включают, без ограничения, ингибиторы(например, N-(3R,5S)-1-(3-ацетокси-2,2-диметилпропил)-7-хлор-5-(2,3-диметоксифенил)-2-оксо-1,2,3,5 тетрагидро-4,1-бензоксазепин-3-ил]ацетил]пиперидин-4-уксусная кислота); фибратные соединения, такие как безафибрат, клофибрат, симфибрат и клинофибрат; ингибиторы АСАТ, такие как авасимиб и эфлуцимиб; анионообменные смолы, такие как колестирамин; пробукол; основанные на никотиновой кислоте лекарственные средства, такие как никомол и ницеритрол; этиликозапентат; и растительные стерины, такие как соевый стерин и -оризанол. Примеры соединений против ожирения включают без ограничения дексфенфлурамин, фенфлурамин, фентермин, сибутрамин, амфепрамон, дексамфетамин, мазиндол, фенилпропаноламин, клобензорекс; антагонисты рецептора МСН, такие как SB-568849 и SNAP7941; антагонисты нейропептида Y, такие как СР-422935; антагонисты каннабиноидных рецепторов, такие как SR-141716 и SR-147778; антагонисты грелина; ингибиторы 11-гидроксистероиддегидрогеназы,такие как BVT-3498; ингибиторы липазы поджелудочной железы, такие как орлистат и ATL-962; агонисты бета-3 AR, такие как AJ-9677; пептидные средства, снижающие аппетит, такие как лептин и CNTF(цилиарный нейротрофический фактор); агонисты холецистокинина, такие как линтитрипт и FPL-15849;- 16015169 и средство, сдерживающее потребление пищи, такое как Р-57. Примеры противогипертонических соединений включают ингибиторы фермента превращения ангиотензина, такие как каптоприл, эналаприл и делаприл; антагонисты ангиотензина II, такие как кандесартан цилексетил, лозартан, эпросартан, валсартан, телмисартан, ирбесартан, олмесартан медоксомил, тазосартан и 1-2'-(2,5-дигидро-5-оксо-4 Н-1,2,4 оксадиазол-3-ил)бифенил-4-ил]метил]-2-этокси-1 Н-бензимидазол-7-карбоновая кислота; блокаторы кальциевых каналов, такие как манидипин, нифедипин, никардипин, амлодипин и эфонидипин; открыватели калиевых каналов, такие как левкромакалим, L-27152, AL0671 и NIP-121; и клонидин. 5. Наборы и изделия, содержащие соединение I. Изобретение также относится к наборам, содержащим фармацевтическую композицию согласно настоящему изобретению, содержащую соединение I (и необязательно одно или несколько других антидиабетических соединений), при этом указанный набор дополнительно содержит инструкции, в которых имеется одна или несколько форм информации, выбранных из группы, состоящей из указания патологического состояния, в случае которого необходимо вводит фармацевтическую композицию, информации о хранении фармацевтической композиции, информации о дозах и инструкций по введению фармацевтической композиции. Набор также может содержать упаковочные материалы. Упаковочный материал также может включать контейнер для хранения фармацевтической композиции. Контейнер необязательно может иметь этикетку, на которой указано патологическое состояние, при котором необходимо вводить фармацевтическую композицию, приведена информация о хранении, информация о дозах и/или инструкции в отношении того, как вводить композицию. Набор также может содержать дополнительные компоненты для хранения или введения композиции. Набор также может содержать композицию в форме однократно вводимой дозы или многократных доз. В одном варианте фармацевтическая композиция в наборе содержит несколько доз фармацевтической композиции согласно настоящему изобретению, при этом указанная фармацевтическая композиция представляет собой стандартную лекарственную форму, которая содержит соединение I в одном из диапазонов доз, указанных в настоящем описании. В другом варианте фармацевтическая композиция в наборе содержит несколько доз фармацевтической композиции согласно настоящему изобретению, при этом указанная фармацевтическая композиция представляет собой стандартную лекарственную форму, которая содержит соединение I и одно или несколько других антидиабетических соединений, указанных в настоящем описании. Настоящее изобретение также относится к изделиям, содержащим фармацевтическую композицию согласно настоящему изобретению, содержащую соединение I (и необязательно одно или несколько других антидиабетических соединений), при этом указанные изделия дополнительно содержат упаковочные материалы. В одном варианте упаковочный материал включает контейнер для хранения композиции. В другом варианте изобретение относится к изделию, в котором контейнер имеет этикетку, на которой указана одна или несколько форм информации из группы, состоящей из патологического состояния, в случае которого необходимо вводить композицию, информации о хранении, информации о дозах и/или инструкций по введению композиции. В одном варианте фармацевтическая композиция в изделии содержит несколько доз фармацевтической композиции согласно настоящему изобретению, при этом указанная фармацевтическая композиция представляет собой стандартную лекарственную форму, которая содержит соединение I в одном из диапазонов доз, указанных в настоящем описании. В другом варианте фармацевтическая композиция в изделии содержит несколько доз фармацевтической композиции согласно настоящему изобретению, при этом указанная фармацевтическая композиция представляет собой стандартную лекарственную форму, которая содержит соединение I и одно или несколько других антидиабетических соединений, указанных в настоящем описании. Следует отметить, что из упаковочного материала, используемого в наборах и изделиях согласно настоящему изобретению, могут состоять несколько отдельных контейнеров, например, отдельных флаконов или отдельных упаковок из фольги. Контейнер может иметь любую обычную конфигурацию или форму, которая известна в данной области и сделана из фармацевтически приемлемого материала, например, бумажная или картонная коробочка, стеклянный или пластиковый флакон или баночка, многократно герметично закрываемый мешочек (например, для хранения "запаса" таблеток для помещения их в разные контейнеры) или блистерная упаковка, содержащая отдельные дозы, выдавливаемые из упаковки согласно терапевтической схеме. Контейнер, который будет использован, зависит от конкретной используемой формы дозирования. Возможно использование более одного контейнера вместе для одной упаковки при продаже стандартной лекарственной формы. Например, таблетки могут находиться во флаконе, который в свою очередь находится в коробочке. Одним конкретным примером набора согласно настоящему изобретению является так называемая блистерная упаковка. Блистерные упаковки хорошо известны в упаковочной промышленности и широко используются для упаковки фармацевтических стандартных лекарственных форм (таблеток, капсул и тому подобного). Блистерные упаковки обычно состоят из листа относительно жесткого материала(предпочтительно листа прозрачной пластмассы), покрытого фольгой. В ходе осуществления процесса упаковки в жестком материале образуют углубления. Углубления имеют размер и форму отдельных таб- 17015169 леток или капсул, которые необходимо упаковать, или могут иметь размер и форму для размещения нескольких таблеток и/или капсул, которые необходимо упаковать. Затем таблетки или капсулы соответственно помещают в углубления и лист относительно жесткого материала запаивают сверху полимерной фольгированной пленкой, при этом лицевую сторону фольги располагают противоположно направлению, в котором создавали углубления. В результате таблетки или капсулы запаивают по отдельности или запаивают вместе, в зависимости от потребности, в углублениях между фольгой и листом. Прочность листа предпочтительно такова, что таблетки или капсулы можно извлечь из блистерной упаковки, надавливая вручную на углубления, при этом в фольге образуется отверстие в месте углубления. Таблетку или капсулу затем можно извлечь через указанное отверстие. Примеры 1. Получение 2-[6-(3-аминопиперидин-1-ил)-3-метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1 илметил]-4-фторбензонитрила и фармацевтически приемлемых солей 4-Фтор-2-метилбензонитрил (3). Смесь 2-бром-5-фтортолуол (2) (3,5 г, 18,5 ммоль) и CuCN (2 г, 22 ммоль) в ДМФА (100 мл) кипятили с обратным холодильником в течение 24 ч. Реакционную смесь разбавляли водой и экстрагировали гексаном. Органический слой сушили над MgSO4 и растворитель удаляли, получая продукт 3 (выход 60%). 1 Н-ЯМР (400 МГц, CDCl3):7,60 (дд, J=5,6, 8,8 Гц, 1 Н), 6,93-7,06 (м, 2 Н), 2,55 (с, 3 Н). 2-Бромметил-4-фторбензонитрил (4). Смесь 4-фтор-2-метилбензонитрила (3) (2 г, 14,8 ммоль), NBS (2,64 г, 15 ммоль) и AIBN (100 мг) вCCl4 кипятили с обратным холодильником в атмосфере азота в течение 2 ч. Реакционную смесь охлаждали до комнатной температуры. Твердое вещество удаляли фильтрованием. Органический раствор концентрировали, получая неочищенный продукт в виде масла, который использовали на следующей стадии без дополнительной очистки. 1 Н-ЯМР (400 МГц, CDCl3):7,68 (дд, J=5,2, 8,4 Гц, 1 Н), 7,28 (дд, J=2,4, 8,8 Гц, 1 Н), 7,12 (м, 1 Н), 4,6 (с, 2 Н). 2-(6-Хлор-3-метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1-илметил)-4-фторбензонитрил (6). Смесь неочищенного 3-метил-6-хлорурацила (5) (0,6 г, 3,8 ммоль), 2-бромметил-4 фторбензонитрила (0,86 г, 4 ммоль) и K2CO3 (0,5 г, 4 ммоль) в ДМСО (10 мл) перемешивали при 60 С в течение 2 ч. Реакционную смесь разбавляли водой и экстрагировали EtOAc. Органический слой сушили над MgSO4 и растворитель удаляли. Остаток очищали хроматографией на колонке. Получали 0,66 г продукта (выход: 60%). 1H-ЯМР (400 МГц, CDCl3):7,73 (дд, J=7,2, 8,4 Гц, 1 Н), 7,26 (д, J=4,0 Гц, 1 Н), 7,117,17 (м, 1 Н), 6,94 (дд, J=2,0, 9,0 Гц, 1 Н) 6,034 (с, 2 Н), 3,39 (с, 3 Н). МС (ES) [m+Н] вычислено для 2-(6-Хлор-3-метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1-илметил)-4-фторбензонитрил (5) (300 мг, 1,0 ммоль), дигидрохлорид (R)-3-аминопиперидина (266 мг, 1,5 ммоль) и бикарбонат натрия (500 мг,5,4 ммоль) перемешивали в герметично закрытой пробирке в EtOH (3 мл) при 100 С в течение 2 ч. После очистки ВЭЖХ получали конечное соединение в виде ТФА-соли. 1H-ЯМР (400 МГц, CD3OD):7,77-7,84 ТФА-соль соединения I суспендировали в ДХМ и затем промывали насыщенным Na2CO3. Органический слой сушили и растворитель удаляли в вакууме. Остаток растворяли в ацетонитриле и добавлялиHCl в диоксане (1,5 эквивалента) при 0 С. После удаления растворителя получали HCl-соль. 1 Н-ЯМР(400 МГц, CD3OD):7,77-7,84 (м, 1 Н), 7,12-7,26 (м, 2 Н), 5,47 (с, 1 Н), 5,21-5,32 (ABq, 2 Н, J=32,0, 16,0 Гц),3,35-3,5 (м, 2 Н), 3,22 (с, 3 Н), 3,01-3,1 (м, 1 Н), 2,69-2,93 (м, 2 Н), 2,07-2,17 (м, 1 Н), 1,83-1,93 (м, 1 Н), 1,551,80 (м, 2 Н). МС (ES) [m+H] вычислено для C18H20FN5O2, 357,38; найдено 357,38. Общий способ получения солей соединения I Продукт бензонитрил при необходимости может быть выделен в виде свободного основания, но предпочтительно продукт может быть далее превращен в соответствующую кислотно-аддитивную соль. В частности, продукт бензонитрил (примерно 10 мг) в растворе МеОН (1 мл) обрабатывали разными кислотами (1,05 эквивалента). Растворы оставляли стоять в течение трех суток на открытом воздухе. Если образовывался осадок, то смесь фильтровали и соль сушили. Если не образовывалось твердого вещества,то смесь концентрировали в вакууме и выделяли остаток. Таким образом получали соли 34, используя следующие кислоты: бензойную, п-толуолсульфоновую, янтарную, R-(-)-миндальную и бензолсульфоновую. Стадии выделения и/или очистки промежуточных соединений в описанном выше способе необязательно можно избежать, если промежуточные продукты из реакционной смеси получают в виде относительно чистых соединений и побочные продукты или примеси в реакционной смеси не мешают следующим стадиям реакции. В том случае, когда это возможно, одна или несколько стадий выделения могут быть исключены, чтобы уменьшить время обработки, и исключение дополнительной обработки также может давать более высокие общие выходы реакции. 2. Типичные препараты, содержащие сукцинатную соль 2-[6-(3-аминопиперидин-1-ил)-3-метил-2,4 диоксо-3,4-дигидро-2 Н-пиримидин-1-илметил]-4-фторбензонитрила. Предлагаются примеры препаратов в форме таблеток, которые можно использовать для введения сукцинатной соли 2-[6-(3-аминопиперидин-1-ил)-3-метил-2,4-диоксо-3,4-дигидро-2 Н-пиримидин-1 илметил]-4-фторбензонитрила (сукцинатная соль соединения I) согласно настоящему изобретению. Следует отметить, что препараты, предлагаемые в настоящем описании, могут варьировать, как известно в данной области. Типичными препаратами в форме таблеток являются следующие препараты: 12,5 мг соединения I (масса формы свободного основания) на таблетку. Состав ядра таблетки(3) Opadry II 85F18422, белое - часть 3 (COLORCON) 6. Влияние введения на активность DPP-IV в плазме. Однократную дозу соединения I вводили перорально обезьяне в дозе 0,3 мг/кг. На фиг. 1 показан наблюдаемый эффект, который оказывает введение соединения I на активность DPP-IV в плазме обезьяны после введения дозы. Как можно видеть, соединение I уменьшало активность DPP-IV в плазме обезьяны на более чем 90% по сравнению с исходным уровнем через 12 ч после введения дозы. Таким образом, как можно видеть на основании данных, показанных на фиг. 1, посредством введения соединения I- 20015169 один раз в сутки при уровнях доз, указанных в настоящем описании, соединение I можно эффективно применять в случае патологических состояний, при которых требуется уменьшение активности DPP-IV в плазме. Принимая во внимание представленные данные, полагают, что при введении пациенту по меньшей мере 25 мг соединения I активность DPP-IV в плазме пациента может быть снижена на более чем 60% по сравнению с исходным уровнем в течение периода времени, составляющего по меньшей мере 6,12, 18 и даже 24 ч после введения. 7. Влияние совместного введения с пиоглитазоном на уровень глкозы в плазме. Влияние введения соединения I в комбинации с пиоглитазоном исследовали посредством измерения уровней глюкозы в плазме у мышей. Самцов мышей db/db (BKS. Cg-+Leprdb/+Leprdb) (6-недельного возраста, CLEA Japan (Tokyo, Japan делили на 4 группы (n=7 в каждой группе), включая группы A-D. Группа А имела свободный доступ к порошковому корму СЕ-2 (CLEA Japan) в течение 21 дня. Группа В имела свободный доступ к порошковому корму СЕ-2 (CLEA Japan), содержащему 0,03% (мас./мас.) сукцинатной соли соединения I, в течение 21 дня. Рассчитана доза соединения I в группе В, составляющая 74,8+2,5 (средняя+SD) мг/кг массы тела/сутки. Группа С имела свободный доступ к порошковому корму СЕ-2 (CLEA Japan), содержащему 0,0075% (мас./мас.) гидрохлорида пиоглитазона в течение 21 дня. Рассчитана доза пиоглитазона в группе С, составляющая 17,7+0,6 (средняяSD) мг/кг массы тела/сутки. Группа D имела свободный доступ к порошковому корму СЕ-2 (CLEA Japan), содержащему 0,03%(мас./мас.) сукцинатной соли соединения I в комбинации с 0,0075% (мас./мас.) гидрохлорида пиоглитазона, в течение 21 дня. Рассчитаны дозы соединения I и пиоглитазона в группе D, составляющие 63,1+1,9(средняяSD) мг/кг массы тела/сутки и 15,80,5 (средняя+SD) мг/кг массы тела/сутки, соответственно. На протяжении 21 дня введения порошкового корма не было значимых различий вводимого количества порошкового корма между указанными выше 4 группами. После 21 дня введения порошкового корма брали образцы крови из глазной вены мышей капиллярной пипеткой в условиях приема пищи, и уровни глюкозы в плазме измеряли ферментативно, используя автоматический анализатор 7080 (Hitachi, Japan). Результаты показаны в табл. 1. Значения в таблице означают среднее (n=7) + стандартное отклонение. Таблица 1 Как показано в табл. 1, комбинация соединения I с пиоглитазоном оказывает превосходное действие, снижая уровни глюкозы в плазме. Специалистам в данной области будет понятно, что могут быть осуществлены различные модификации и варианты, касающиеся соединений, композиций, наборов и способов согласно настоящему изобретению, не отходя от сути и не выходя за рамки объема изобретения. Таким образом, подразумевается,что настоящее изобретение охватывает модификации и варианты настоящего изобретения, которые входят в объем прилагаемых пунктов формулы изобретения и их эквивалентов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типаII, воспалительного заболевания кишечника, болезни Крона, индуцированного химиотерапией энтерита,мукозита слизистой оболочки полости рта, синдрома укороченной кишки, диабетической дислипидемии,нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), метаболического ацидоза, кетоза, регуляции аппетита, ожирения, диабетической нейропатии, диабетической ретинопатии, болезни почек, гиперлипидемии, артериосклероза, гипертонии, инфаркта миокарда, стенокардии, церебрального инфаркта, апоплексии головного мозга и метаболического синдрома, включающий введение пациенту суточной дозы, составляющей от 1 до 250 мг/сутки, соединения I, где соединение I имеет формулу- 21015169 2. Способ по п.1, в котором суточная доза соединения I, вводимая пациенту, составляет от 5 до 100 мг. 3. Способ по п.1, в котором суточная доза соединения I, вводимая пациенту, составляет 6,25 мг. 4. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки. 5. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в виде однократной дозы. 6. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в течение периода времени, составляющего по меньшей мере 30 суток. 7. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки в течение периода времени, составляющего по меньшей мере 60 суток. 8. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки утром. 9. Способ по любому из пп.1-3, в котором введение осуществляют 1 раз в сутки утром перед первым приемом пищи пациентом в этот день. 10. Способ по любому из пп.1-9, в котором введение осуществляют путем, выбранным из группы,состоящей из перорального, парентерального, внутрибрюшинного, внутривенного, внутриартериального,трансдермального, подъязычного, внутримышечного, ректального, трасбуккального, интраназального,липосомного, ингаляционного, вагинального, внутриглазного, введения путем локальной доставки, подкожного, введения в жировую ткань, внутрисуставного, внутрибрюшинного и интратекального введения. 11. Способ по любому из пп.1-9, в котором введение осуществляют перорально. 12. Способ по любому из пп.1-11, в котором введение осуществляют для лечения патологического состояния пациента, представляющего собой диабет типа I или типа II. 13. Способ по любому из пп.1-11, в котором указанный пациент имеет диабет типа II. 14. Способ по любому из пп.1-11, в котором указанный пациент находится в преддиабетическом состоянии. 15. Способ по любому из пп.1-14, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, отличными от соединения I,для лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), диабетической нейропатии, диабетической ретинопатии и метаболического синдрома. 16. Способ лечения заболевания, выбранного из группы, состоящей из диабета типа I, диабета типаII, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), диабетической нейропатии, диабетической ретинопатии и метаболического синдрома, включающий введение суточной дозы, составляющей от 1 до 250 мг/сутки, соединения I пациенту в комбинации с одним или несколькими антидиабетическими соединениями, отличными от соединения I, где соединение I имеет формулу 17. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину и усилителей секреции инсулина. 18. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из ингибиторов протеинтирозинфосфатазы, ингибиторов глутаминфруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо-6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецепторов глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, активаторов глюкокиназы, агонистов рецептора GLP-1, агонистов рецептораGLP-2, модуляторов UCP, модуляторов RXR, ингибиторов GSK-3, модуляторов PPAR, инсулина и 2 адренергических антагонистов. 19. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из ингибиторов GSK-3, агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-альфа, антидиабетических ванадийсодержащих соединений и бигуа- 22015169 нидов. 20. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из (S)-(3,4-дигидро-2-(фенилметил)-2 Н-1-бензопиран-6-ил)метилтиазолидин-2,4-диона, 5-[4(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метилтиазолидин-2, 4-диона, 5-[(4-(1-метил 5-[4-(2-(1-индолил)этокси)фенил]метил циклогексил)метокси)фенил]метилтиазолидин-2,4-диона,тиазолидин-2,4-диона, 5-4-[2-(5-метил-(2-фенил-4-оксазолил)этокси)]бензилтиазолидин-2,4-диона, 5(2-нафтилсульфонил)тиазолидин-2,4-диона, бис 4-[(2,4-диоксо-5-тиазолидинил)метил]фенилметана, 54-[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензилтиазолидин-2,4-диона, 5-[4-(1-фенил-1 циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-[4-(2-(2,3-дигидроиндол-1-ил)этокси) фенилметил]тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-(5-фенилсульфонил)тиазолидин-2,4 диона, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2,4-диона, 5-[4-(2-(метил-2-пиридиниламино)этокси)фенил]метилтиазолидин-2,4-диона, 5-[4-(2-(5-этил-2-пиридил)этокси) фенил]метилтиазолидин-2,4-диона, 5-[2-(2-нафтил)бензоксазол-5-ил]метилтиазолидин-2,4-диона и 5(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида, включая их любые фармацевтически приемлемые соли. 21. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с метформином, включая его любые фармацевтически приемлемые соли. 22. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими производными сульфонилмочевины. 23. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида,толбутамида, толазамида, глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. 24. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бетаклеток и кратковременно действующих стимуляторов секреции инсулина. 25. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с инсулином. 26. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими агонистами GLP-1. 27. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими агонистами GLP-2. 28. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с экстендатидом. 29. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из репаглинида, митиглинида и натеглинида, включая их любые фармацевтически приемлемые соли. 30. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими ингибиторами альфа-глюкозидазы. 31. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с одним или несколькими антидиабетическими соединениями, выбранными из группы,состоящей из акарбозы, воглибозы и миглитола, включая их любые фармацевтически приемлемые соли. 32. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с розиглитазоном, включая его любые фармацевтически приемлемые соли. 33. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с пиоглитазоном, включая его любые фармацевтически приемлемые соли. 34. Способ по любому из пп.15 и 16, в котором введение представляет собой введение соединения I в комбинации с метформином и пиоглитазоном, включая их любые фармацевтически приемлемые соли. 35. Способ по любому из пп.33 и 34, в котором пиоглитазон представляет собой пиоглитазон-HCl. 36. Способ по любому из пп.1-35, в котором соединение I вводят в виде свободного основания. 37. Способ по любому из пп.1-35, в котором соединение I вводят в виде фармацевтически приемлемой соли. 38. Способ по любому из пп.1-35, в котором соединение I вводят в виде сукцинатной соли. 39. Фармацевтическая композиция, приготовленная в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит 2,5, 5, 6,25, 20, 25, 50 или 75 мг соединения I, где соединение I имеет формулу 40. Фармацевтическая композиция по п.39, в которой указанная стандартная лекарственная форма содержит 6,25 мг соединения I. 41. Фармацевтическая композиция по любому из пп.39-40, в которой указанная стандартная лекарственная форма дополнительно содержит одно или несколько антидиабетических соединений, отличных от соединения I. 42. Фармацевтическая композиция, приготовленная в стандартной лекарственной форме, при этом указанная стандартная лекарственная форма содержит от 1 до 250 мг соединения I и одно или несколько антидиабетических соединений, отличных от соединения I, где соединение I имеет формулу 43. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из модуляторов пути передачи сигнала инсулина, соединений, влияющих на нарушенную регуляцию продукции глюкозы в печени, усилителей чувствительности к инсулину и усилителей секреции инсулина. 44. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из ингибиторов протеинтирозинфосфатазы, ингибиторов глутаминфруктозо-6-фосфатамидотрансферазы, ингибиторов глюкозо-6-фосфатазы, ингибиторов фруктозо-1,6-бисфосфатазы, ингибиторов гликогенфосфорилазы, антагонистов рецепторов глюкагона, ингибиторов фосфоенолпируваткарбоксикиназы, ингибиторов киназы пируватдегидрогеназы, ингибиторов альфа-глюкозидазы, ингибиторов опорожнения желудка, инсулина и 2-адренергических антагонистов. 45. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из ингибиторов GSK-3, агонистов ретиноидного рецептора X, агонистов бета-3 AR, модуляторов UCP, антидиабетических тиазолидиндионов, агонистов PPAR-гамма неглитазонового типа, двойных агонистов PPAR-гамма/PPAR-альфа, антидиабетических ванадийсодержащих соединений и бигуанидов. 46. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из (S)-(3,4-дигидро-2-(фенилметил)-2 Н-1-бензопиран-6-ил)метилтиазолидин-2,4-диона, 5-[4(3-(5-метил-2-фенил-4-оксазолил)-1-оксопропил)фенил]метилтиазолидин-2,4-диона, 5-[4-(1-метилциклогексил)метокси)фенил]метилтиазолидин-2,4-диона,5-[4-(2-(1-индолил)этокси)фенил]метилтиазолидин-2,4-диона, 5-4-[2-(5-метил-2-фенил-4-оксазолил)этокси]бензилтиазолидин-2,4-диона, 5-(2 нафтилсульфонил)тиазолидин-2,4-диона, бис 4-[(2,4-диоксо-5-тиазолидинил)метил]фенилметана, 5-4[2-(5-метил-2-фенил-4-оксазолил)-2-гидроксиэтокси]бензилтиазолидин-2,4-диона,5-[4-(1-фенил-1 циклопропанкарбониламино)бензил]тиазолидин-2,4-диона, 5-[4-(2-(2,3-дигидроиндол-1-ил)этокси)фенилметил)тиазолидин-2,4-диона, 5-[3-(4-хлорфенил)-2-пропинил]-(5-фенилсульфонил)тиазолидин-2,4 диона, 5-[3-(4-хлорфенил)-2-пропинил]-5-(4-фторфенилсульфонил)тиазолидин-2, 4-диона, 5-[4-(2(метил-2-пиридиниламино)этокси)фенил]метилтиазолидин-2,4-диона, 5-[2-(2-нафтил)бензоксазол-5 ил]метилтиазолидин-2,4-диона и 5-(2,4-диоксотиазолидин-5-илметил)-2-метокси-N-(4-трифторметилбензил)бензамида, включая их любые фармацевтически приемлемые соли. 47. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит метформин, включая его любые фармацевтически приемлемые соли. 48. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит производное сульфонилмочевины. 49. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из глизоксепида, глибурида, глибенкламида, ацетогексамида, хлорпропамида, глиборнурида,толбутамида, толазамида, глипизида, карбутамида, гликвидона, глигексамида, фенбутамида, толцикламида, глимепирида и гликлазида, включая их любые фармацевтически приемлемые соли. 50. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекар- 24015169 ственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из инкретиновых гормонов или их миметиков, антагонистов рецептора имидазолина бетаклеток и кратковременно действующих стимуляторов секреции инсулина. 51. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит инсулин. 52. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько агонистов GLP-1. 53. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько агонистов GLP-2. 54. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит экстендатид. 55. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из репаглинида, митиглинида и натеглинида, включая их любые фармацевтически приемлемые соли. 56. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит один или несколько ингибиторов альфа-глюкозидазы. 57. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит одно или несколько антидиабетических соединений, выбранных из группы,состоящей из акарбозы, воглибозы и миглитола, включая их любые фармацевтически приемлемые соли. 58. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит розиглитазон, включая его любые фармацевтически приемлемые соли. 59. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит пиоглитазон, включая его любые фармацевтически приемлемые соли. 60. Фармацевтическая композиция по любому из пп.39-42, в которой указанная стандартная лекарственная форма содержит метформин и пиоглитазон, включая их любые фармацевтически приемлемые соли. 61. Фармацевтическая композиция по любому из пп.59 и 60, в которой пиоглитазон представляет собой пиоглитазон-НС 1. 62. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма предназначена для перорального введения. 63. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой твердый препарат, предназначенный для перорального введения. 64. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой таблетку или капсулу, предназначенную для перорального введения. 65. Фармацевтическая композиция по любому из пп.39-61, в которой указанная стандартная лекарственная форма представляет собой препарат длительного высвобождения, предназначенный для перорального введения. 66. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде свободного основания. 67. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде фармацевтически приемлемой соли. 68. Фармацевтическая композиция по любому из пп.39-65, в которой соединение I присутствует в фармацевтической композиции в виде сукцинатной соли. 69. Набор, содержащий несколько доз фармацевтической композиции по любому из пп.39-68 и инструкции, которые содержат одну или несколько форм информации, выбранных из группы, состоящей из указания патологического состояния, в случае которого необходимо вводить фармацевтическую композицию, информации о хранении фармацевтической композиции, информации о дозах и инструкций по введению фармацевтической композиции. 70. Изделие, содержащее несколько доз фармацевтической композиции по любому из пп.39-68 и упаковочные материалы. 71. Изделие по п.70, в котором упаковочный материал включает контейнер для хранения нескольких доз фармацевтической композиции. 72. Изделие по п.71, в котором контейнер имеет этикетку, на которой указана одна или несколько форм информации из группы, состоящей из информации о патологическом состоянии, в случае которого необходимо вводить соединение, информации о хранении, информации о дозах и/или инструкций по введению композиции. 73. Применение фармацевтической композиции по любому из пп.39-68 для лечения диабета типа II. 74. Применение фармацевтической композиции по любому из пп.39-68 для лечения диабета типа I. 75. Применение фармацевтической композиции по любому из пп.39, 40 и 62-68 для лечения лече- 25015169 ния заболевания, выбранного из группы, состоящей из диабета типа I, диабета типа II, воспалительного заболевания кишечника, болезни Крона, индуцированного химиотерапией энтерита, мукозита слизистой оболочки полости рта, синдрома укороченной кишки, диабетической дислипидемии, нарушения толерантности к глюкозе (IGT), нарушения уровня глюкозы в плазме натощак (IFG), метаболического ацидоза, кетоза, регуляции аппетита, ожирения, диабетической нейропатии, диабетической ретинопатии, болезни почек, гиперлипидемии, артериосклероза, гипертонии, инфаркта миокарда, стенокардии, церебрального инфаркта, апоплексии головного мозга и метаболического синдрома.
МПК / Метки
МПК: A61P 3/10, A61K 31/44, A61K 31/513
Метки: применение, дипептидилпептидазы, ингибиторов
Код ссылки
<a href="https://eas.patents.su/27-15169-primenenie-ingibitorov-dipeptidilpeptidazy.html" rel="bookmark" title="База патентов Евразийского Союза">Применение ингибиторов дипептидилпептидазы</a>
Предыдущий патент: Противоопухолевая фармацевтическая композиция и ее применение
Следующий патент: Высоковязкие диутановые камеди и способы их получения
Случайный патент: Аминоалкилзамещенные производные бензопирана












