Полиморфные модификации кристаллического цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина в качестве антагонистов рецепторов нейрокинина 1 (nk1)
Номер патента: 4206
Опубликовано: 26.02.2004
Авторы: Массетт Стивен Сарджент, Уинт Льюин Теофилус, Роуз Питер Роберт, Куоллич Джордж Джозеф
Формула / Реферат
1. Кристаллические формы цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина, имеющего формулу
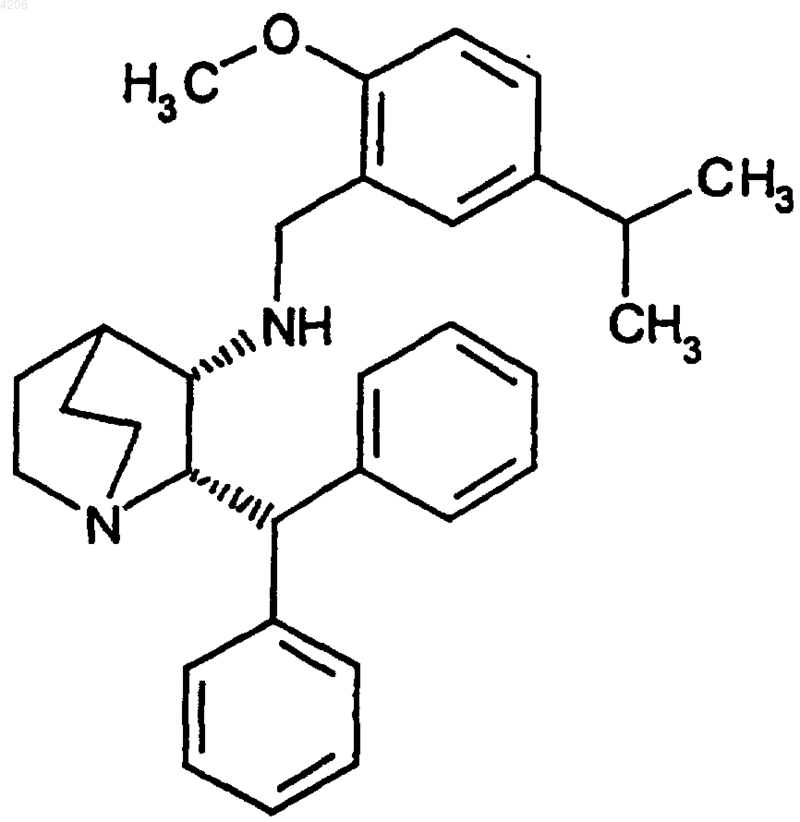
где указанная кристаллическая форма выбрана из группы, состоящей из
(а) стабильной негигроскопичной безводной формы цитрата, имеющей картину дифракции рентгеновских лучей на порошке
| Пик ь | Расстояние D |
| 1 | 17,61 |
| 2 | 10,95 |
| 3 | 8,78 |
| 4 | 7,96 |
| 5 | 7,37 |
| 6 | 6,80 |
| 7 | 6,57 |
| 8 | 5,87 |
| 9 | 5,46 |
(б) моногидрата цитрата, полиморфной модификации формы А, имеющей картину дифракции рентгеновских лучей на порошке
| Пик ь | Расстояние D |
| 1 | 17,74 |
| 2 | 10,93 |
| 3 | 9,65 |
| 4 | 8,25 |
| 5 | 6,71 |
| 6 | 5,98 |
| 7 | 5,67 |
| 8 | 5,45 |
| 9 | 4,83 |
и
(в) моногидрата цитрата, полиморфной модификации формы Б, имеющей картину дифракции рентгеновских лучей на порошке
| Пик ь | Расстояние D |
| 1 | 12,3 |
| 2 | 11,3 |
| 3 | 6,5 |
| 4 | 6,9 |
| 5 | 5,9 |
| 6 | 4,3 |
| 7 | 4,1 |
| 8 | 3,5 |
| 9 | 3,2 |
2. Полиморфная модификация моногидрата по п.1, где габитусы кристалла формы А являются или остроконечными иглами, или пластинками.
3. Полиморфная модификация форма Б моногидрата по п.1, где габитусы кристалла формы Б являются кристаллическими пластинками.
4. Полиморфная модификация форма Б моногидрата по п.1, полученная посредством концентрирования раствора моногидрата цитрата в метаноле.
5. Соль безводный цитрат по п.1, имеющая точку начала плавления примерно при 159,9шC.
6. Безводный цитрат по п.1, где содержание воды составляет 1,11 мас.% при относительной влажности примерно 90%.
7. Безводный цитрат по п.1, где габитусы его кристалла являются микрокристаллическими чешуйками.
8. Полиморфная модификация форма А моногидрата по п.1, которая характеризуется точкой начала плавления примерно при 162,6шC.
9. Полиморфная модификация форма Б моногидрата по п.1, которая характеризуется точкой начала плавления примерно при 149шC с разложением.
10. Фармацевтическая композиция, обладающая антагонистической активностью в отношении вещества Р, содержащая по меньшей мере одну из полиморфных форм А или Б по п.1 в количестве, которое эффективно в лечении рвоты, и фармацевтически приемлемый носитель.
11. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество полиморфной формы А соединения по п.1.
12. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество полиморфной формы Б соединения по п.1.
13. Фармацевтическая композиция, обладающая антагонистической активностью в отношении вещества Р, содержащая безводный цитрат по п.1 в количестве, которое эффективно в лечении рвоты, и фармацевтически приемлемый носитель.
14. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество безводного цитрата соединения по п.1.
15. Способ получения кристаллической полиморфной формы А моногидрата цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина, при котором растворяют безводный цитрат в смеси изопропилового спирта и воды, перемешивают смесь в течение ночи при комнатной температуре, осуществляют кристаллизацию соли моногидрата цитрата, собирают форму А путем фильтрации и сушат в вакууме примерно при 20-80шC.
16. Способ по п.15, где синтез проводят в условиях окружающей среды в течение примерно 1,5-72 ч.
17. Способ по п.15, где большие кристаллы формы А с пластинчатым габитусом выращивают из раствора изопропанол/вода, а большие кристаллы формы А с игольчатым габитусом выращивают из смеси ацетон/диизопропиловый эфир/вода.
18. Способ получения кристаллической полиморфной формы Б моногидрата цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина, при котором концентрируют раствор моногидрата цитрата в метаноле при комнатной температуре в течение примерно 48-72 ч.
Текст
1 Предпосылки изобретения Данное изобретение относится к некоторым полиморфным модификациям и формам кристаллического цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина (далее соли цитрата) и их фармацевтическим композициям. Соль цитрат является активным антагонистом рецепторов NK1 ЦНС (центральной нервной системы), и данное изобретение относится к способам лечения состояний, на которые оказывает влияние снижение нейропередачи, опосредованной веществом Р, или которым оно способствует. Изобретение также относится к антагонисту вещества Р, который определен для избавления от острой и отсроченной рвоты у млекопитающего, включая людей, получающего химиотерапию. Лечение определено здесь как предупреждение и лечение. В патенте США 5393762 и заявке в США с порядковым номером 08/816016, которые включены путем ссылки, описаны фармацевтические композиции и лечение рвоты с использованием антагонистов рецепторов NK1. Кристаллическая безводная соль цитрат негигроскопична и имеет четкую порошковую рентгенограмму и точку начала плавления 159,9 С. Безводный цитрат превратили в воде в моногидрат. Краткое изложение сущности изобретения Данное изобретение относится к безводному цитрату[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил) амина, моногидрату цитрата и двум его полиморфным модификациям. В одном воплощении изобретения безводный цитрат является единственной кристаллической стабильной негигроскопичной формой. Габитусы кристалла в безводном цитрате являются микрокристаллическими чешуйками и характеризуются картиной дифракции рентгеновских лучей на порошке, представленной ниже. Безводный цитрат Пик 1 2 3 4 5 6 7 8 9 Расстояние D 17,61 10,95 8,78 7,96 7,37 6,80 6,57 5,87 5,46 В двух других воплощениях моногидрат цитрата находится в кристаллических формах А или Б. Форма А характеризуется рентгенограммой, представленной ниже. Форма А моногидрата цитрата Пик 1 2 3 4 5 6 7 8 9 Расстояние D 17,74 10,93 9,65 8,25 6,71 5,98 5,67 5,45 4,83 2 Габитусы кристалла формы А являются двоякопреломляющими иглами, которые подвергаются испарению примерно при 84 С, перекристаллизуются с образованием лейстообразного габитуса и плавятся примерно при 162,6 С. Габитусы кристалла формы Б являются двоякопреломляющими пластинками, которые подвергаются испарению при 102 С, перекристаллизуются с образованием кристаллов с менее выраженным двойным лучепреломлением, характеризующихся точкой начала плавления примерно при 120 С и перекристаллизующихся с образованием микрокристаллов с точкой начала плавления примерно при 149 С с разложением. Форма Б характеризуется представленной ниже рентгенограммой. Форма Б моногидрата цитрата Пик 1 2 Расстояние 12,3 11,3 Другой аспект данного изобретения относится к фармацевтической композиции, обладающей фармацевтической активностью, которая содержит по меньшей мере одну из полиморфных форм А и Б моногидрата цитрата и безводный цитрат, для лечения рвоты. Изобретение также относится к способу лечения рвоты,при котором субъекту, нуждающемуся в таком лечении, вводят эффективное противорвотное количество полиморфных форм А или Б либо безводного цитрата. Полиморфную форму А моногидрата цитрата(2-бензгидрил-1-азабицикло[2.2.2]окт-3 ил)-(5-изопропил-2-метоксибензил)амина получают путем растворения безводного цитрата в смеси изопропилового спирта и воды и перемешивания смеси в течение ночи при комнатной температуре. Соль моногидрат цитрата кристаллизуется, и форму А собирают путем фильтрации. Форму А затем сушат примерно при 2080 С в вакууме. Синтез проводят примерно в течение 1,5-72 ч в условиях окружающей среды. Большие кристаллы формы А с пластинчатым габитусом выращивают из раствора эфир/вода, а с игольчатым габитусом из смеси ацетон/диизопропиловый эфир/вода. Способ получения полиморфной формы Б моногидрата цитрата включает в себя концентрирование раствора моногидрата цитрата в метаноле при комнатной температуре примерно в течение 48-72 ч. Подробное описание изобретения Синтез безводного цитрата осуществляли путем добавления 1,1 эквивалента лимонной кислоты к перемешиваемой суспензии свободного основания в изопропаноле (15 объемов) при комнатной температуре. Полученный раствор перемешивали и контролировали с помощью дифференциальной сканирующей калориметрии. После того, как все свободное основание прореагировало (18 ч), получили соль безводный цитрат в виде белого кристаллического 3 твердого вещества путем фильтрации и сушки в нужном вакууме (house vacuum) при 45 С с продувкой азотом (выход 83%). Дифракция рентгеновских лучей на порошке и поляризующая световая микроскопия (ПСМ) показали, что соль является кристаллической. Часто встречающиеся габитусы кристалла являются микрокристаллическими чешуйками. Наиболее интенсивные отражения, расстояния d, наблюдаемые с помощью дифракции рентгеновских лучей на порошке, составили 17,608, 10,953, 8,782, 7,956,7,371, 6,802, 6,571, 5,866, 5,462, 4,907, 4,415,4,188, 3,635 и 3,512 . Кристаллы показали точку начала плавления при 159,8 С с разложением. Измерения гигроскопичности показали, что было абсорбировано 1,11 мас.% воды при относительной влажности 90%. Способ получения кристаллического моногидрата цитрата, полиморфной формы А,включает в себя добавление раствора 13,9 кг лимонной кислоты (безводной, 99,5+%) в ацетоне (125 л) к раствору 50 кг свободного основания в изопропиловом спирте (250 л). Прозрачный раствор фильтровали, перемешивали и ацетон удаляли путем перегонки. Полученную смесь перемешивали при температуре окружающей среды до тех пор, пока не началась кристаллизация, а затем гранулировали в течение дополнительных 16 ч. Полученный белый кристаллический безводный цитрат собирали посредством фильтрации и сушили при 25 С в вакууме (выход 80%). Безводный цитрат (26,4 кг) растворили в изопропиловом спирте (264 л), добавили воду(13,2 л) и смесь перемешивали в течение ночи при комнатной температуре. Соль моногидрат цитрата выкристаллизовалась, и ее собирали посредством фильтрации и сушили при 25 С в вакууме. Получили 24,9 кг продукта (выход 91,8%). Полученную соль моногидрат цитрата,форму А, сравнили с аутентичным образцом и охарактеризовали с помощью ПСМ, дифракции рентгеновских лучей на порошке, протонного магнитного резонанса, анализа по Карлу Фишеру, дифференциальной сканирующей калориметрии и элементарного анализа. Дифракция рентгеновских лучей на порошке и ПСМ показали, что соль является кристаллической. Два габитуса кристалла, имеющие похожие встречающиеся рефрактограммы (refractograms),представляли собой пластинки и иглы. Игольчатый габитус образовался в результате различной скорости роста граней кристалла в воде, тогда как в смеси изопропанол/вода более равномерный рост граней кристалла дал пластинки. Наиболее интенсивные отражения, расстояния ,наблюдаемые с помощью дифракции рентгеновских лучей на порошке, составили 17,736,10,928, 9,651, 8,253, 6,707, 5,981, 5,666, 5,450,4,833, 4,488 и 3,646 . Кристаллы показали испарение при 84 С и точку начала плавления при 4 159,9 С с разложением. Измерения гигроскопичности показали, что было абсорбировано 2,44 мас.% воды при относительной влажности 90%. Анализ по Карлу Фишеру показал присутствие 2,7% воды (теоретически 2,66%), подтвердив, что синтезировали моногидрат. С помощью элементарного анализа подтвердили чистоту синтезированной соли. Получение соли моногидрата цитрата формы Б осуществляли путем суспендирования в метаноле при условиях окружающей среды примерно в течение 1,5-72 ч. Продукт собирали посредством фильтрации. Нагревание с обратным холодильником соли моногидрата цитрата в течение 18 ч дает тот же самый результат. Форма Б является полиморфной модификацией моногидрата цитрата. После выделения индивидуальные кристаллические формы формы Б являются двоякопреломляющими пластинками. Форму Б можно превратить в форму А в этилацетате при комнатной температуре. Форма Б, по данным дифференциальной сканирующей калориметрии, теряет воду при 76 С,подвергается незначительной перекристаллизации при 120 С, начинает плавится при 138,8 С,подвергается перекристаллизации, и точка начала конечного плавления составляет 159,9 С. Растворение формы А в метаноле обратно дало форму Б, которая легко высохла с образованием довольно стабильной полиморфной модификации. "Переброска мостиков" в полиморфных модификациях в этилацетате дало форму А. "Переброска мостиков" представляет собой распространенный термин, используемый в микроскопии химических объектов и кристаллографии для фазовых превращений в растворе,экспериментальный метод, часто используемый для определения (самой стабильной) кристаллической формы с наименьшей энергией. Обычно кристаллические формы загружают вместе в ряд предварительно насыщенных растворителей(насыщенных соединением, которое обеспечило кристаллические формы). После суспендирования в течение подходящего периода времени кристаллы собирают и определяют, какая кристаллическая форма преобладает. Кристаллической формой будет форма с наименьшей энергией по экспериментальным условиям."Переброска мостиков" у формы А с формой Б дала форму А из смеси этилацетата и ацетона и обратно дала исходную смесь форм из следующих растворителей: тетрагидрофуран,этилацетат, циклогексан, гексаны, ацетонитрил и метилэтилкетон. При перемешивании менее стабильной формы, например формы Б, в этилацетате в условиях окружающей среды происходит превращение в форму А. В результате суспендирования безводной формы или смеси форм в воде образуется кристаллический моногидрат, который не теряет 5 воду в условиях сушки, например, при 45 С в вакууме. Формы А и Б моногидрата цитрата обладают чрезвычайно полезными и неочевидными свойствами. Поскольку форма А моногидрата цитрата гигроскопически стабильна, то трудности при приготовлении препаратов, связанные с изменением массы активного ингредиента во время операций таблетирования или приготовления капсул, облегчаются. Форма Б обладает аналогичными преимуществами при относительной влажности примерно ниже 85%. Формы А и Б и безводный цитрат можно также вводить внутривенно. Эффективная дозировка моногидрата цитрата для фармацевтической композиции зависит от предполагаемого пути введения, индикатора,показания для лечения и других факторов, таких как возраст и масса субъекта. В следующих пределах дозировок термин "мг А" относится к миллиграммам моногидрата. Рекомендуемый предел для перорального введения составляет 5300 мг А/сутки, предпочтительно 40-200 мг А/сутки, более предпочтительно 40-80 мг А/сутки, в виде разовых или разделенных доз. Рекомендуемый предел для перорального введения в пероральных формах, таких как пилюли или таблетки, составляет от 2,5 мг А/сутки до 160 мг А/сутки и предпочтительно 5-80 мг А/сутки. Стабильность формы А по отношению ко всем другим формам демонстрируется у нее отсутствием гигроскопичности и "переброской мостиков" при более низкой энергии и термическими превращениями. Следующие примеры иллюстрируют способы и соединения по настоящему изобретению. Понятно, однако, что изобретение не ограничивается этими конкретными примерами. Пример 1. Получение кристаллического моногидрата цитрата, форма А. Раствор 13,9 кг лимонной кислоты (безводной, 99,5+%) в ацетоне (125 л) добавили к раствору 50 кг свободного основания в изопропиловом спирте (250 л). Прозрачный раствор отфильтровали, перемешали и ацетон удалили путем перегонки. Полученную смесь перемешивали при температуре окружающей среды до тех пор, пока не началась кристаллизация, а затем гранулировали в течение дополнительных 16 ч. Полученный белый кристаллический безводный цитрат собирали посредством фильтрации и сушили при 25 С в вакууме (выход 80%). Пример 2. Получение кристаллического моногидрата цитрата, форма Б. Образец моногидрата формы А растворили в метаноле. Раствор перемешали при комнатной температуре и оставили концентрироваться при испарении растворителя. Полученную форму Б собирали посредством фильтрации. По результатам рентгенографического анализа конфигурации, Н 1-ЯМР (протонного магнитного резо 004206 6 нанса) и анализа сжиганием установили, что соединение является формой Б моногидрата. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Кристаллические формы цитрата (2 бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина,имеющего формулу где указанная кристаллическая форма выбрана из группы, состоящей из(а) стабильной негигроскопичной безводной формы цитрата, имеющей картину дифракции рентгеновских лучей на порошке Пик 1 2 3 4 5 6 7 8 9 Расстояние D 17,61 10,95 8,78 7,96 7,37 6,80 6,57 5,87 5,46(б) моногидрата цитрата, полиморфной модификации формы А, имеющей картину дифракции рентгеновских лучей на порошке Пик 1 2 3 4 5 6 7 8 9 Расстояние D 17,74 10,93 9,65 8,25 6,71 5,98 5,67 5,45 4,83(в) моногидрата цитрата, полиморфной модификации формы Б, имеющей картину дифракции рентгеновских лучей на порошке Пик 1 2 Расстояние 12,3 11,3 2. Полиморфная модификация моногидрата по п.1, где габитусы кристалла формы А являются или остроконечными иглами, или пластинками. 3. Полиморфная модификация форма Б моногидрата по п.1, где габитусы кристалла формы Б являются кристаллическими пластинками. 4. Полиморфная модификация форма Б моногидрата по п.1, полученная посредством концентрирования раствора моногидрата цитрата в метаноле. 5. Соль безводный цитрат по п.1, имеющая точку начала плавления примерно при 159,9 С. 6. Безводный цитрат по п.1, где содержание воды составляет 1,11 мас.% при относительной влажности примерно 90%. 7. Безводный цитрат по п.1, где габитусы его кристалла являются микрокристаллическими чешуйками. 8. Полиморфная модификация форма А моногидрата по п.1, которая характеризуется точкой начала плавления примерно при 162,6 С. 9. Полиморфная модификация форма Б моногидрата по п.1, которая характеризуется точкой начала плавления примерно при 149 С с разложением. 10. Фармацевтическая композиция, обладающая антагонистической активностью в отношении вещества Р, содержащая по меньшей мере одну из полиморфных форм А или Б по п.1 в количестве, которое эффективно в лечении рвоты, и фармацевтически приемлемый носитель. 11. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество полиморфной формы А соединения по п.1. 12. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество полиморфной формы Б соединения по п.1. 13. Фармацевтическая композиция, обладающая антагонистической активностью в отношении вещества Р, содержащая безводный цитрат по п.1 в количестве, которое эффективно в лечении рвоты, и фармацевтически приемлемый носитель. 14. Способ лечения рвоты, при котором субъекту, нуждающемуся в лечении, вводят эффективное противорвотное количество безводного цитрата соединения по п.1. 8 15. Способ получения кристаллической полиморфной формы А моногидрата цитрата (2 бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5 изопропил-2-метоксибензил)амина, при котором растворяют безводный цитрат в смеси изопропилового спирта и воды, перемешивают смесь в течение ночи при комнатной температуре, осуществляют кристаллизацию соли моногидрата цитрата, собирают форму А путем фильтрации и сушат в вакууме примерно при 20-80 С. 16. Способ по п.15, где синтез проводят в условиях окружающей среды в течение примерно 1,5-72 ч. 17. Способ по п.15, где большие кристаллы формы А с пластинчатым габитусом выращивают из раствора изопропанол/вода, а большие кристаллы формы А с игольчатым габитусом выращивают из смеси ацетон/диизопропиловый эфир/вода. 18. Способ получения кристаллической полиморфной формы Б моногидрата цитрата (2 бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина, при котором концентрируют раствор моногидрата цитрата в метаноле при комнатной температуре в течение примерно 48-72 ч.
МПК / Метки
МПК: C07D 453/02, A61P 25/28, A61K 31/435
Метки: нейрокинина-2, кристаллического, модификации, антагонистов, рецепторов, цитрата, полиморфные, качестве, nk1, 2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина
Код ссылки
<a href="https://eas.patents.su/5-4206-polimorfnye-modifikacii-kristallicheskogo-citrata-2-benzgidril-1-azabiciklo222okt-3-il-5-izopropil-2-metoksibenzilamina-v-kachestve-antagonistov-receptorov-nejjrokinina-1-nk1.html" rel="bookmark" title="База патентов Евразийского Союза">Полиморфные модификации кристаллического цитрата (2-бензгидрил-1-азабицикло[2.2.2]окт-3-ил)-(5-изопропил-2-метоксибензил)амина в качестве антагонистов рецепторов нейрокинина 1 (nk1)</a>
Предыдущий патент: Ингибиторы герпесвирусов на основе альфа-метилбензилсодержащей тиомочевины, включающие фенилендиаминогруппу
Следующий патент: Производные пиридина, ингибирующие фосфодиэстеразу iv
Случайный патент: Химерные гибридные анальгетики









