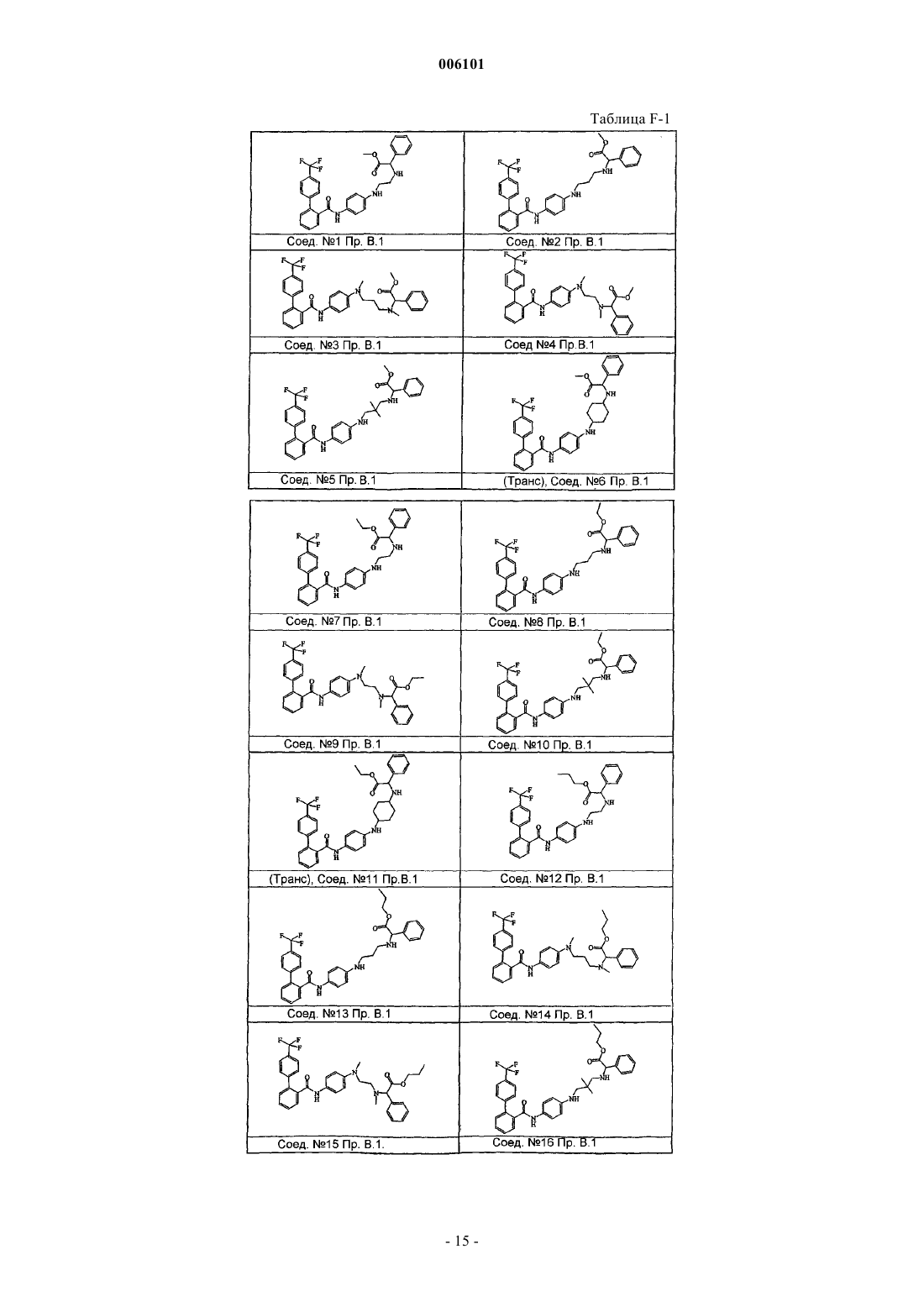
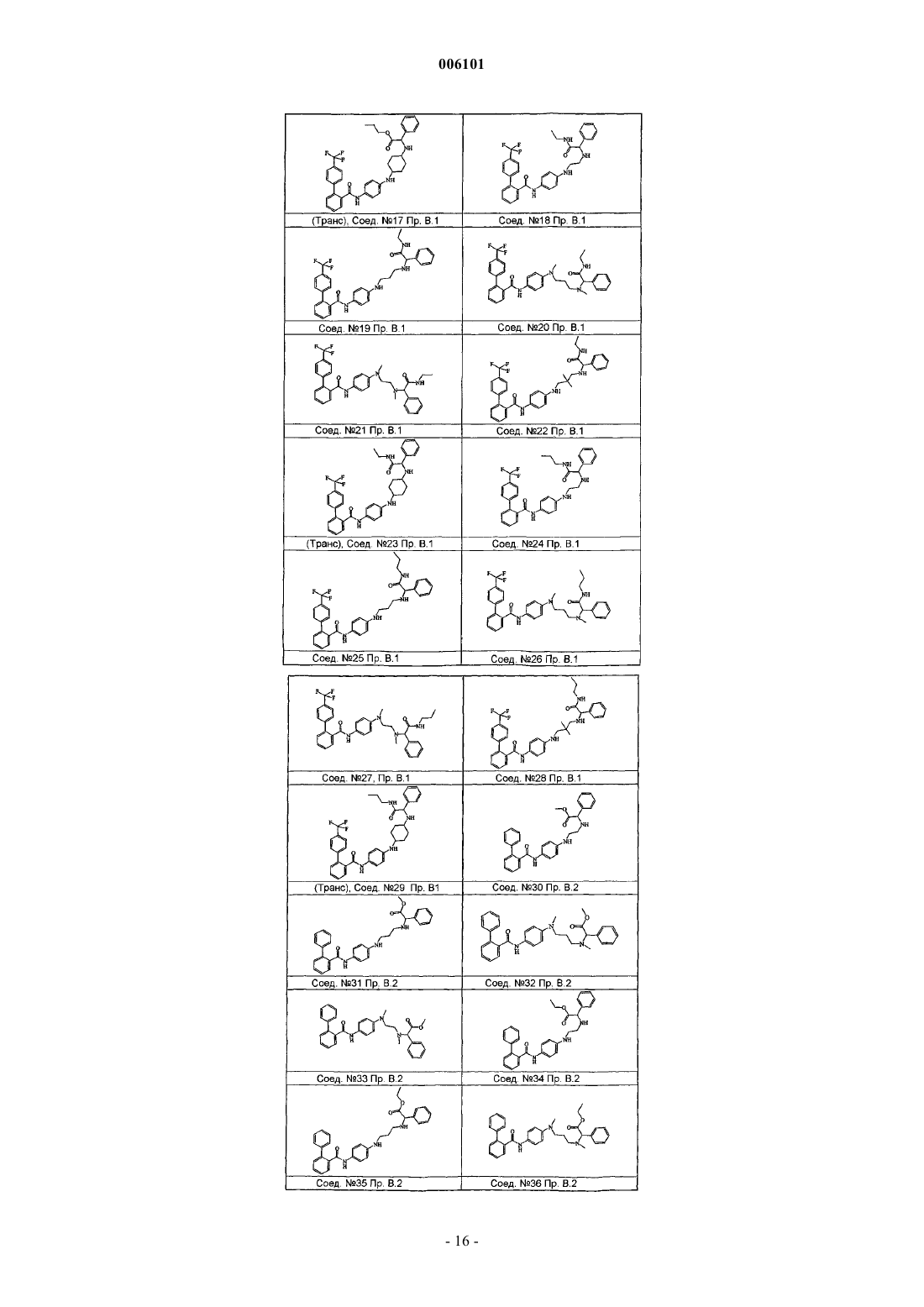
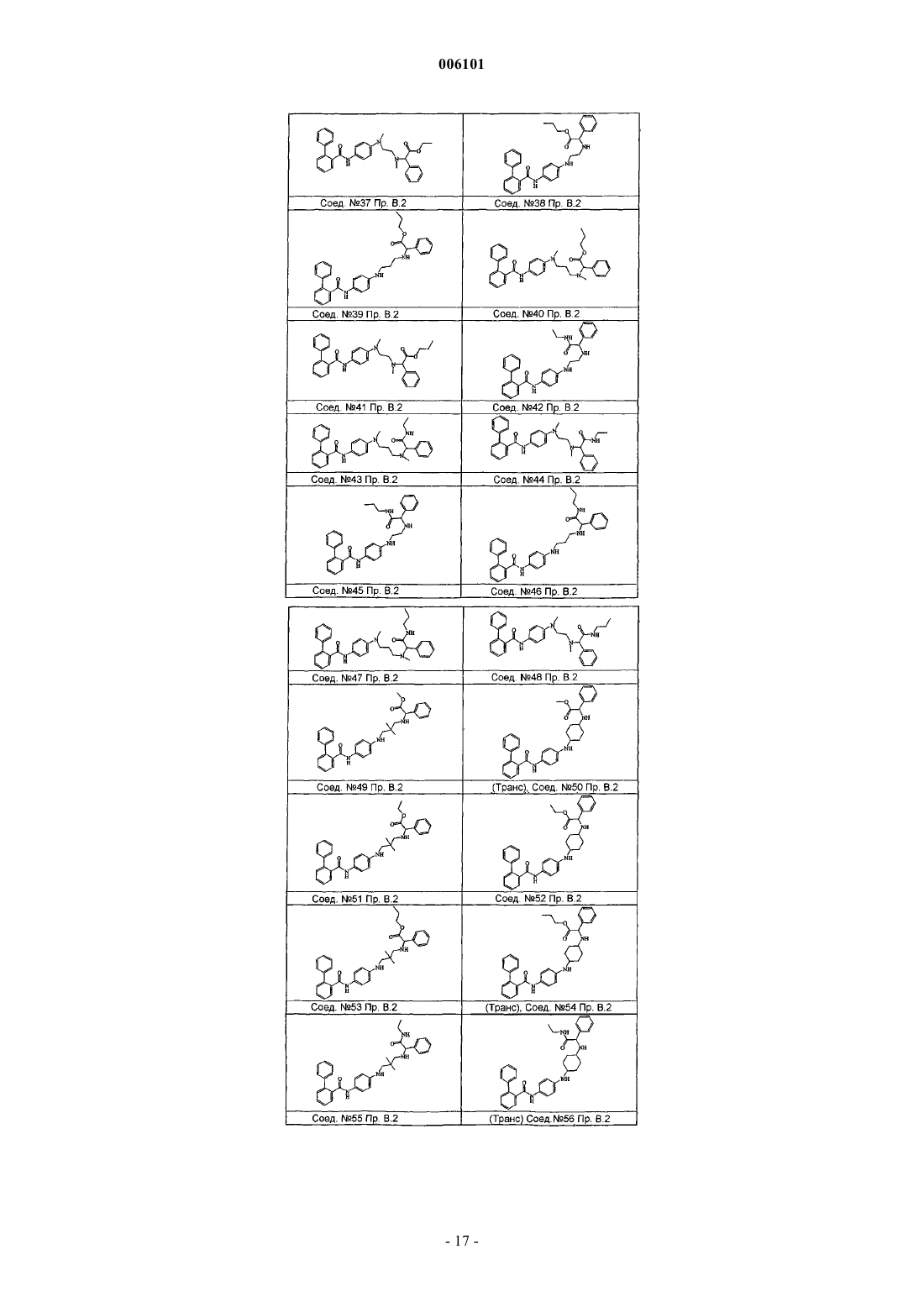
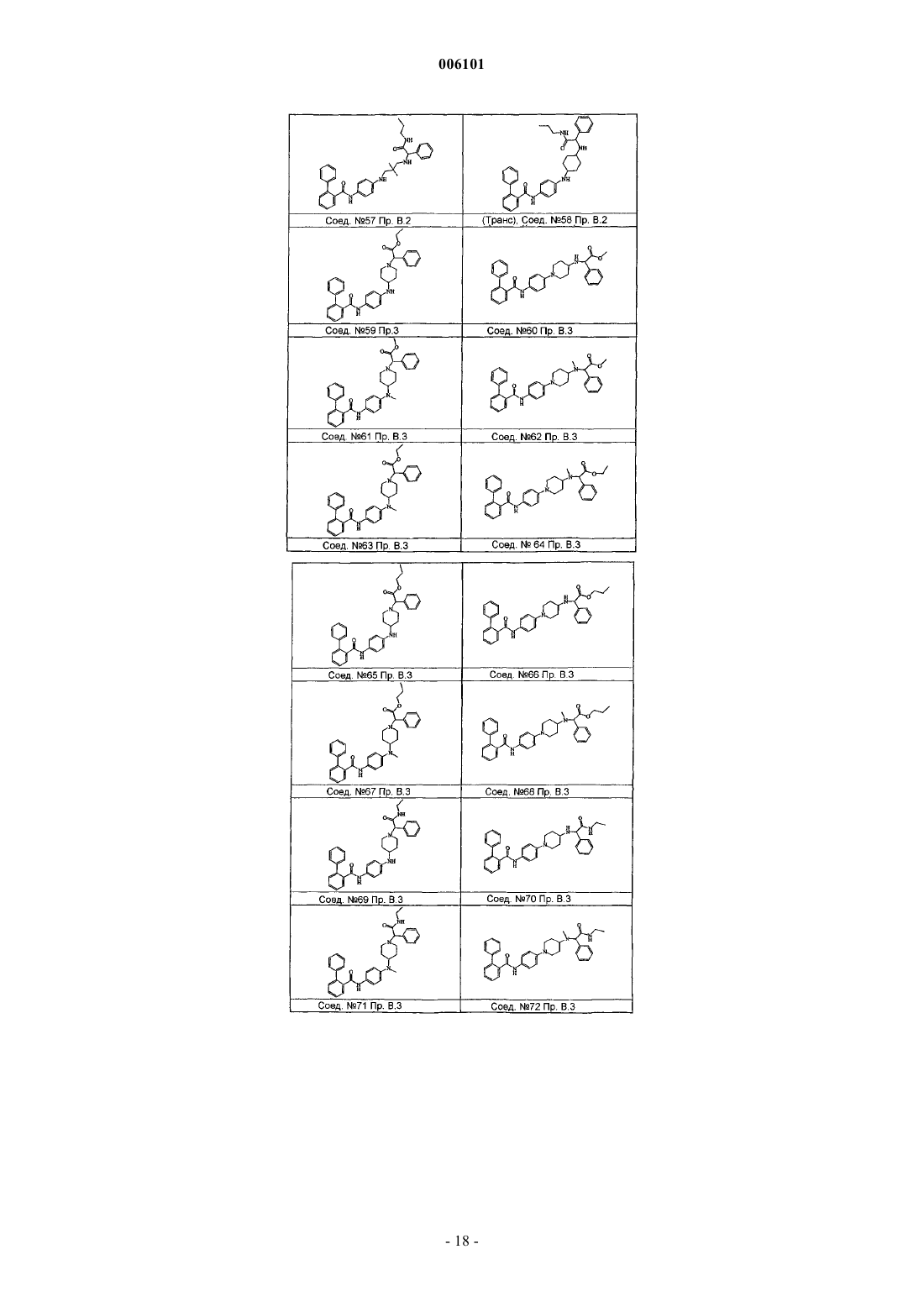
Бифенилкарбоксамиды, полезные в качестве снижающих содержание липидов агентов
Формула / Реферат
1. Соединение формулы (I)
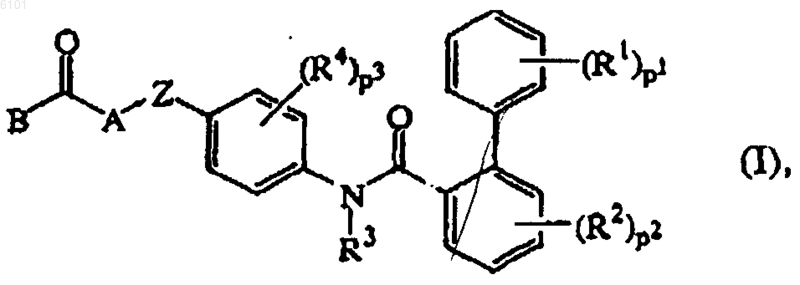
N-оксиды, фармацевтически приемлемые кислотно-аддитивные соли и их стереохимически изомерные формы,
где p1, p2 и p3 означают целые числа, каждое из которых независимо равно 1-3;
каждый из R1 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси, галоген, гидрокси, меркапто, циано, нитро, C1-4-алкилтио или полигалоген-C1-6-алкил, амино, C1-4-алкиламино и ди(C1-4-алкил)амино;
каждый из R2 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкокси, галоген или трифторметил;
R3 означает водород, C1-4-алкил,
каждый из R4 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси, галоген или трифторметил;
Z означает двухвалентный радикал формулы

где n означает целое число от 2 до 4 и -(CH2)n-группа в радикале (a-1) может необязательно быть замещена одной или двумя группами C1-4-алкил;
m и m' означают целые числа от 1 до 3;
каждый из R5 и R6 независимо выбирают из группы, включающей водород, C1-6-алкил или арил;
каждый из X1 и X2 независимо выбирают из группы, включающей CH, N или атом углерода в sp2-гибридизации и в радикале (a-1) по меньшей мере один из X1 или X2 означает N;
A означает C1-6-алкандиил, замещенный одной арильной группой;
B означает водород; C1-10-алкил; арил или гетероарил, каждый из которых необязательно замещен группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил; арил-C1-10-алкил; гетероарил-C1-10-алкил; C3-10-циклоалкил; полигалоген-C1-6-алкил; C3-6-алкенил; C3-6-алкинил; NR7R8 или OR9;
где каждый из R7 и R8 независимо означает водород, C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой, выбранной из группы, включающей галоген, циано, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил; арил-C1-10-алкил, гетероарил-C1-10-алкил; C3-10-циклоалкил; C7-10-полициклоалкил, полигалоген-C1-6-алкил, C3-8-алкенил, C3-8-алкинил, конденсированный бензо-C5-8-циклоалкил, и
где R9 означает C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил; арил-C1-10-алкил; гетероарил-C1-10-алкил; C3-10-циклоалкил; C7-10-полициклоалкил; полигалоген-C1-6-алкил; C3-8-алкенил; C3-8-алкинил или конденсированный бензо-C5-8-циклоалкил, причем
арил представляет собой моно- или полиароматические группы, такие как фенил, необязательно замещенный группами, выбранными из галогена, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил; и
гетероарил представляет собой моно- или полигетероароматические группы, такие как группы, включающие один или более гетероатомов, выбранных из азота, кислорода, серы и фосфора, в частности пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, триазолил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, пирролил, фуранил, тиенил и подобные, включая все возможные их изомерные формы, и необязательно замещенные группой, выбранной из галогена, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил.
2. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (a-1), где каждый из X1 и X2 означает азот, n означает целое число, равное 2, и каждый из R5 и R6 независимо означает водород или метил.
3. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (a-2) или (a-3), где X1 означает азот, m и m' означают целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил.
4. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (a-2) или (a-3), где X1 означает азот, m означает целое число, равное 2, m' означает целое число, равное 1; и каждый из R5 и R6 независимо означает водород или метил.
5. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (a-4), где m означает целое число, равное 2, и m' означает целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил.
6. Соединение по любому из пп.1-5, где A означает C1-6-алкандиил, замещенный фенилом, и B означает C1-4-алкилокси или C1-10-алкиламино.
7. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения по любому из пп.1-6.
8. Способ получения фармацевтической композиции по п.7, где терапевтически эффективное количество соединения по любому из пп.1-6 тщательно смешивают до однородной смеси с фармацевтически приемлемым носителем.
9. Применение соединения по любому из пп.1-6 в качестве лекарственного средства для лечения гиперлипемии, ожирения и диабета II типа.
10. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (II), где B, A, Z, R4 и p3 принимают значения, указанные по п.1,
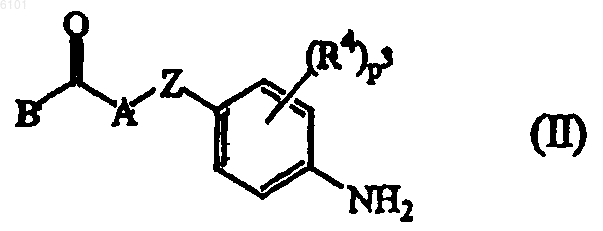
с бифенилкарбоновой кислотой или хлорангидридом формулы (III), где R1, R2, p1 и p2 принимают указанные для формулы (I) значения и Y1 выбирают из гидрокси и галогена, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии подходящего основания
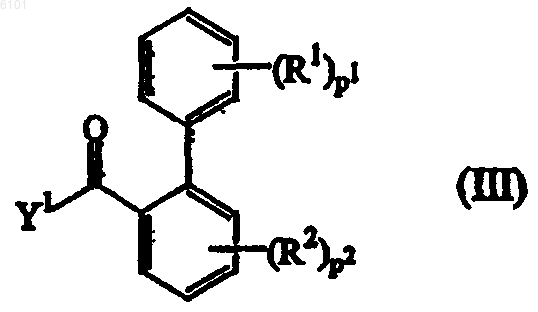
с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредсттюь обработки щелочью и, по желанию, получают их стереохимически изомерные формы.
11. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (IV)
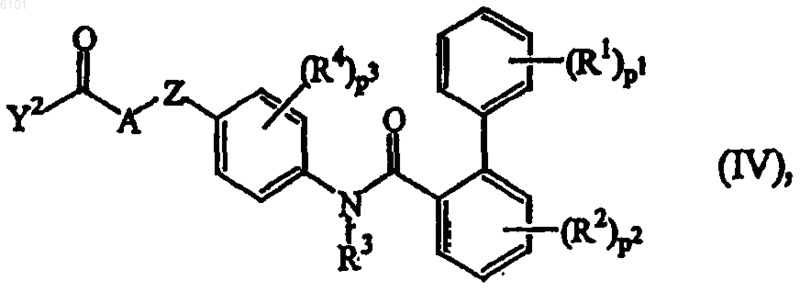
где R1, R2, R3, R4, A, Z, p1, p2 и p3 принимают значения, указанные по п.1, и Y2 выбирают из галогена и гидрокси, с промежуточным соединением (V) формулы B-H, где B означает NR7R8 или OR9 и R7, R8 и R9 принимают значения, указанные по п.1, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии по меньшей мере одного подходящего связующего реагента и/или подходящего основания,
с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредством обработки щелочью и, по желанию, получают их стереохимически изомерные формы.
12. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (VI), где R1, R2, R3, R4, p1, p2 и p3 принимают значения, указанные по п.1, и Y3 выбирают из галогена, B(OH)2, алкилборонатов и их циклических аналогов,
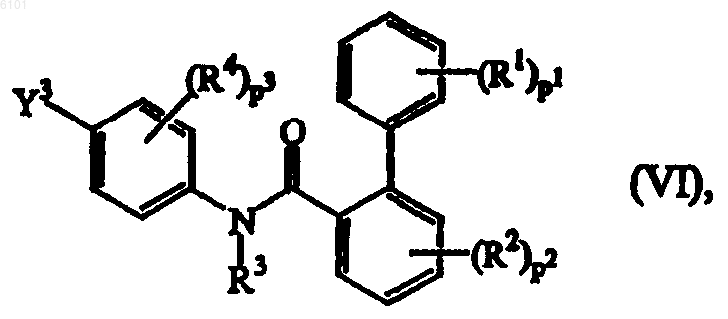
с реагентом формулы (VII), где B, A и Z принимают значения, указанные в п.1, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии по меньшей мере одного связующего реагента на основе переходного металла и/или по меньшей мере одного подходящего лиганда,
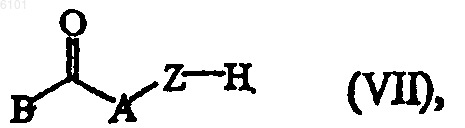
с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредством обработки щелочью и, по желанию, получают их стереохимически изомерные формы.
Текст
006101 Настоящее изобретение относится к новым соединениям бифенилкарбоксамида, обладающим ингибирующей активностью в отношении В аполипопротеида и сопутствующим действием по снижению содержания липидов. Изобретение также относится к способам получения указанных соединений, фармацевтическим композициям, включающим указанные соединения, а также применения указанных соединений для лечения гиперлипемии, ожирения и диабета II типа. Ожирение является причиной большого числа серьезных заболеваний, давая, например, начало диабету взрослых или болезням сердца. Кроме того, снижение веса становится навязчивой идеей для все возрастающей части населения. В настоящее время общепризнанна причинная взаимосвязь между гиперхолестеринемией, в особенности связанной с повышенными концентрациями в плазме липопротеидов низкой плотности (далее обозначенных LDL) и липопротеидов очень низкой плотности (далее обозначенных VLDL), и ранними атеросклерозом и/или сердечно-сосудистым заболеванием. Однако ограниченное число лекарственных препаратов приемлемо в настоящее время для лечения гиперлипемии. Лекарства, используемые главным образом для лечения гиперлипемии, включают смолы на основе веществ, усиливающих секрецию желчной кислоты, такие как холестирамин и колестипол, производные фибриновой кислоты, такие как безафибрат, клофибрат, фенофибрат, ципрофибрат и гемфиброзил, никотиновая кислота и ингибиторы синтеза холестерина, такие как ингибиторы HMG-кофермент-А-редуктазы. Основным недостатком смол на основе веществ, усиливающих секрецию желчной кислоты, является неудобство их введения (гранулированная форма, диспергируемая в воде или апельсиновом соке) и основные побочные действия (желудочно-кишечный дискомфорт и запор). Производные фибриновой кислоты вызывают небольшое снижение (на 5-25%) холестерина LDL (за исключением гипертриглицеридемических пациентов, у которых первоначально низкие уровни имеют тенденцию к возрастанию) и, хотя обычно хорошо переносимы,обладают побочными действиями, включающими потенцирование варфарина, зуд, головную боль, бессонницу, болезненную ревертирующую миопатию и ригидность больших мышечных групп, импотенцию и ослабление почечной функции. Никотиновая кислота является мощным снижающим содержание липидов агентом, приводящим к 15-40% снижению содержания холестерина LDL (и даже 45-60% в комбинации со смолой на основе веществ, усиливающих секрецию желчной кислоты), но с высокой степенью проявления опасных побочных эффектов, связанных с вызванным лекарством сосудорасширяющим действием, таких как головная боль, приливы, сердцебиение, тахикардия и периодические обмороки, а также других побочных действий, таких как желудочно-кишечный дискомфорт, гиперурикемия и ухудшение толерантности к глюкозе. Из семейства ингибиторов HMG-кофермент-А-редуктазы, ловастатин и симвастатин, оба являются неактивными пролекарствами, содержащими лактоновый цикл, который гидролизуется в печени до формы, соответствующей активному гидроксикислотному производному. Вызывая снижение холестерина LDL на 35-45%, указанные вещества обычно хорошо толерантны при низкой частоте незначительных побочных действий. Однако все же сохраняется потребность в новых снижающих содержание липидов агентах с улучшенной эффективностью и/или действующих по иным механизмам,чем вышеуказанные лекарственные средства. Липопротеиды плазмы являются водорастворимыми комплексами высокой молекулярной массы,образованными липидами (холестерином, триглицеридом, фосфолипидами) и аполипопротеидами. Пять основных классов липопротеидов, отличающихся соотношением липидов и типом аполипопротеида, источником которых являются печень и/или кишечник, охарактеризованы по их плотности (измеренной путем ультрацентрифугирования). Указанные классы включают LDL, VLDL, липопротеиды промежуточной плотности (далее обозначенные IDL), липопротеиды высокой плотности (далее обозначенныеHDL) и хиломикроны. Идентифицировано десять основных аполипопротеидов человеческой плазмы.VLDL, секретируемый печенью и содержащий аполипопротеид В (далее обозначенный Аро-В), подвергается разложению до LDL, который переносит 60-70% общего холестерина сыворотки. Аро-В является также основным белковым компонентом LDL. Повышенные уровни LDL-холестерина в сыворотке из-за избыточного синтеза или сниженного обмена каузально связаны с атеросклерозом. Напротив, липопротеиды высокой плотности (далее обозначенные HDL), содержащие аполипопротеид Аl, обладают защитным эффектом и имеют обратную корреляцию с риском ишемической болезни сердца. Таким образом,соотношение HDL/LDL является удобным способом оценки атерогенного потенциала профиля липидов плазмы индивидуума. Две изоформы аполипопротеида (аро) В, аро В-48 и аро В-100 являются важными белками в липопротеидном обмене человека. Аро В-48, названный так потому, что его объем, очевидно, составляет около 48% от аро В-100 на гелях натрийдодецилсульфатполиакриламид, синтезируется кишечником человека. Аро В-48 необходим для сборки хиломикронов и поэтому играет обязательную роль при всасывании кишечником поступающих с пищей жиров. Аро В-100, продуцируемый печенью человека, требуется для синтеза и секреции VLDL. LDL, содержащие порядка 2/3 холестерина в плазме человека, являются продуктами обмена VLDL. Аро В-100 фактически является единственным белковым компонентом LDL. Повышенные концентрации аро В-100 и холестерина LDL в плазме являются общепризнанными факторами риска развития атеросклеротической болезни коронарной артерии сердца.-1 006101 Большое число генетических и приобретенных болезней приводит к гиперлипемии. Вызываемые состояния могут быть классифицированы на первичные и вторичные гиперлипемические состояния. Наиболее общими причинами вторичных гиперлипемий являются сахарный диабет, злоупотребление алкоголем, лекарствами, гипотиреоз, хроническая почечная недостаточность, нефротоксический синдром, холестаз и булимия. Первичные гиперлипемические состояния также подразделяются на общую гиперхолестеринемию,семейную комбинированную гиперлипемию, семейную гиперхолестеринемию, остаточную гиперлипемию, синдром хиломикронемии и семейную гипертриглицеридемию. Известно, что микросомальный белок транспорта триглицерида (обозначенный далее МТР) катализирует транспорт триглицерида и сложного холестерилового эфира путем превращения в фосфолипиды,такие как фосфатидилхолин. D.Sharp'ом и др., Nature (1993) 365:65, продемонстрировано, что дефект,вызывающий абеталипопротеинемию, находится в гене МТР. Это указывает на то, что МТР требуется для синтеза Аро В-содержащих липопротеидов, таких как VLDL, предшественник LDL. Отсюда также следует, что ингибитор МТР должен ингибировать синтез VLDL и LDL, снижая тем самым уровниVLDL, LDL, холестерина и триглицерида в организме человека. Ингибиторы МТР описаны в патентной заявке Канады 2.091.102 и в WO 96/26205. Ингибиторы МТР, принадлежащие к классу полиарилкарбоксамидов, описаны также в патенте США 5.760.246, а также в WO-96/40640 и WO-98/27979. США 5.968.950 описывает гидрохлорид [2-(2-ацетиламиноэтил)-1,2,3,4-тетрагидроизохинолин-6-ил]амида 4'трифторметилбифенил-2-карбоновой кислоты в качестве ингибитора Аро В секреция/МТР. Патент США 5.827.875 описывает пирролидинилзамещенные флуорены в качестве ингибиторов микросомального белка транспорта триглицерида. Патент США 5.965.577 описывает гетероциклические ингибиторы микросомального белка транспорта триглицерида. Одна из задач настоящего изобретения состоит в обеспечении улучшенного лечения пациентов,страдающих ожирением или атеросклерозом, в особенности коронарным атеросклерозом, и в более общем случае, от нарушений, связанных с атеросклерозом, таких как ишемическая болезнь сердца, заболевание периферических сосудов и заболевание сосудов головного мозга. Другая задача настоящего изобретения состоит в том, чтобы вызвать регрессию атеросклероза и подавить его клинические последствия, главным образом, заболеваемость и летальность. Настоящее изобретение основано на неожиданном открытии того, что класс новых соединений бифенилкарбоксамида является активным в качестве селективных ингибиторов МТР, т.е. способен селективно блокировать МТР на уровне кишечной стенки в организме млекопитающих, и является поэтому перспективным в качестве лекарственного препарата, а именно, препарата для лечения гиперлипемии. Кроме того, настоящее изобретение относится к некоторым способам получения таких соединений бифенилкарбоксамида, а также фармацевтическим композициям, включающим указанные соединения. К тому же изобретение относится к ряду новых соединений, полезных в качестве промежуточных соединений для получения терапевтически активных соединений бифенилкарбоксамида, а также способам получения указанных промежуточных соединений. Наконец, изобретение относится к способу лечения состояния, выбранного из группы, включающей: атеросклероз, панкреатит, ожирение, гиперхолестеринемию, гипертриглицеридемию, гиперлипемию, диабет и диабет типа, включающий введение млекопитающему терапевтически активного соединения. Настоящее изобретение относится к семейству новых соединений формулы (I)N-оксидам, фармацевтически приемлемым кислотно-аддитивным солям и их стереохимически изомерным формам,где р 1, р 2 и р 3 означают целые числа, каждое из которых независимо равно 1-3; каждый из R1 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси,галоген, гидрокси, меркапто, циано, нитро, C1-4-алкилтио или полигалоген-С 1-6-алкил, амино, C1-4 алкиламино и ди(C1-4-алкил)амино; каждый из R2 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкокси, галоген или трифторметил;R3 означает водород, C1-4-алкила,каждый из R4 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси,галоген или трифторметил;Z означает двухвалентный радикал формулы где n означает целое число от 2 до 4 и -(СН 2)n-группа в радикале (а-1) может необязательно быть замещена одной или двумя группами C1-4-алкил;m и m' означают целые числа от 1 до 3; каждый из R5 и R6 независимо выбирают из группы, включающей водород, C1-6-алкил или арил; каждый из X1 и X2 независимо выбирают из группы, включающей СН, N или атом углерода в sp2 гибридизации и в радикале (а-1) по меньшей мере один из X1 или X2 означает N; А означает химическую связь, C1-6-алкандиил, необязательно замещенный одной или двумя группами, выбранными из арила, гетероарила и С 3-10-циклоалкила; В означает водород; C1-10-алкил; арил или гетероарил, каждый из которых необязательно замещен группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10 алкиламино,ди(C1-10-алкил)амино,C1-10-ацил,С 1-10-алкилтио,C1-10-алкоксикарбонил,C1-10 алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил; арил-С 1-10-алкил; гетероарил-С 1-10-алкил; С 3-10 циклоалкил; полигалоген-С 1-10-алкил; С 3-6-алкенил; С 3-6-алкинил; NR7R8 или OR9; где каждый из R7 и R8 независимо означает водород, C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой, выбранной из группы, включающей галоген, циано, C1-4 алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил) амино, C1-10-ацил, C1-10-алкилтио, C1-10 алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил; арил-С 1-10-алкил, гетероарил-С 1-10-алкил; С 3-10 циклоалкил; С 7-10-полициклоалкил, полигалоген-С 1-6-алкил, С 3-8-алкенил, С 3-8-алкинил, конденсированный бензо-С 5-8 циклоалкил, и где R7 и R8, взятые вместе с атомом азота, к которому они присоединены,могут образовывать насыщенный гетероциклический радикал с 4-8 атомами углерода; и где R9 означает C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой,выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино,ди(C1-10-алкил)амино,C1-10-ацил,C1-10-алкилтио,C1-10-алкиламинокарбонил и ди(C1-10 алкил)аминокарбонил; арил-C1-10-алкил; гетероарил-С 1-10-алкил; С 3-10-циклоалкил; С 7-10-полициклоалкил; полигалоген-С 1-6-алкил; С 3-8-алкенил; С 3-8-алкинил или конденсированный бензо-С 5-8-циклоалкил, причем арил представляет собой моно- или полиароматические группы, такие как фенил, необязательно замещенный группами, выбранными из галогена, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино,ди(С 1-10-алкил)амино, C1-10-ацила, C1-10-алкилтио, C1-10-алкоксикарбонила, C1-10-алкиламинокарбонила и ди(С 1-10-алкил)аминокарбонила; и гетероарил представляет собой моно- или полигетероароматические группы, такие как группы,включающие один или более гетероатомов, выбранных из азота, кислорода, серы и фосфора, частности пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, триазолил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, пирролил, фуранил, тиенил и подобные, включая все возможные их изомерные формы, и необязательно замещенные группой, выбранной из галогена, циано, нитро, C1-4-алкилокси, амино, С 1-10-алкиламино, ди(С 1-10-алкил)амино, C1-10-ацила, C1-10-алкилтио, C1-10-алкоксикарбонила,C1-10-алкиламинокарбонила и ди(C1-10-алкил)аминокарбонила. Если не оговорено особо, как использовано в приведенных выше определениях и далее в тексте,- галоген является общим названием для фтора, хлора, брома и иода;- C1-4-алкил означает линейные и разветвленные насыщенные углеводородные радикалы с 1-4 атомами углерода, такие как, например, метил, этил, пропил, н-бутил, 1-метилэтил, 2-метилпропил, 1,1 диметилэтил и тому подобное;- подразумевается, что C1-6-алкил включает C1-4-алкил (как определено выше) и его высшие гомологи с 5 или 6 атомами углерода, такие как, например, 2-метилбутил, н-пентил, диметилпропил, н-гексил,2-метилпентил, 3-метилпентил и тому подобное;- подразумевается, что C1-10-алкил включает C1-6-алкил (как определено выше) и его высшие гомологи с 7-10 атомами углерода, такие как, например, гептил, этилгексил, октил, нонил, децил и тому подобное;- С 3-10-циклоалкил является общим названием для группы, включающей: циклопропил, циклобутил,циклопентил, циклогексил, циклогептил, циклооктил, циклононил и циклодецил;- полигалоген-С 1-6-алкил определяется как полигалогензамещенный C1-6-алкил, в частности C1-6 алкил (как определено выше), замещенный 2-13 атомами галогена, такой как дифторметил, трифторметил, трифторэтил, октафторпентил и тому подобное;- арил определяется как моно- и полиароматические группы, такие как фенил, необязательно замещенные группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10 алкиламино,ди(C1-10-алкил)амино,C1-10-ацил,C1-10-алкилтио,C1-10-алкоксикарбонил,C1-10 алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил;-3 006101 гетероарил определяется как моно- и полигетероароматические группы, такие как группы, включающие один или более гетероатомов, выбранных из азота, кислорода, серы и фосфора, в частности пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, триазолил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, пирролил, фуранил, тиенил и тому подобное, включая все возможные изомерические формы, и необязательно замещенные группами, выбранными из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10 алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил;- С 3-6-алкенил означает линейные и разветвленные углеводородные радикалы, содержащие одну двойную связь и имеющие 3-6 атомов углерода, такие как, например, 2-пропенил, 3-бутенил, 2-бутенил,2-пентенил, 3-пентенил, 3-метил-2-бутенил, 3-гексенил, 2-гексенил и тому подобное;- С 3-6-алкинил означает линейные и разветвленные углеводородные радикалы, содержащие одну тройную связь и имеющие 3-6 атомов углерода, такие как, например, 2-пропинил, 3-бутинил, 2-бутинил,2-пентинил, 3-пентинил, 3-метил-2-бутинил, 3-гексинил, 2-гексинил и тому подобное;- С 4-8-циклоалкенил означает циклические углеводородные радикалы, содержащие одну двойную связь и имеющие 4-8 атомов углерода, такие как, например, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил и тому подобное;- C1-6-алкиламино означает первичные аминорадикалы с 1-6 атомами углерода, такие как, например,метиламино, этиламино, пропиламино, изопропиламино, бутиламино, изобутиламино и тому подобное;- ди(C1-6-алкил)амино означает вторичные аминорадикалы с 1-6 атомами углерода, такие как, например, диметиламино, диэтиламино, дипропиламино, диизопропиламино, N-метил-N'-этиламино, Nэтил-N'-пропиламино и тому подобное;- C1-6-ацил означает C1-6-алкильную группу, соединенную с карбонильной группой, такую как, например, ацетил, пропионил, бутирил, изобутирил и тому подобное. Примерами двухвалентного радикала Z, где один из X1 или X2 представляет атом углерода в sp2 гибридизации Подразумевается, что вышеуказанные фармацевтически приемлемые кислотно-аддитивные соли включают терапевтически активные нетоксические формы кислотно-аддитивных солей, которые способны образовывать соединения формулы (I). Фармацевтически приемлемые кислотно-аддитивные соли удобно получать обработкой основной формы такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например, хлористоводородную или бромисто-водородную кислоту, серную, азотную, фосфорную и тому подобные кислоты; или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная, молочная,пиировиноградная, щавелевая (т.е. бутандионовая), малеиновая, фумаровая, яблочная, винная, лимонная,метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и тому подобные кислоты. И наоборот, указанные солевые формы могут быть превращены путем обработки подходящим основанием в форму свободного основания. Термин аддитивная соль, как использован здесь выше, включает сольваты, которые способны образовывать соединения формулы (I), а также их соли. Такими сольватами являются, например, гидраты,алкоголяты и тому подобное. Подразумевается, что N-оксидные формы соединений формулы (I), которые могут быть получены известным из уровня техники способом, включают те соединения формулы (I), в которых атом азота окислен до N-оксида. Термин "стереохимически изомерные формы" как использован здесь выше, означает все возможные изомерные формы, которые могут принимать соединения формулы (I). Если не указано или не оговорено особо, химическое название соединений означает смесь всех возможных стереохимически изомерных форм, указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. Точнее, образующие стереоизомерию центры имеют R- или S-конфигурацию; заместители на двухвалентных циклических (частично) насыщенных радикалах могут иметь либо цис-, либо транс- конфигурацию. Если не указано или не оговорено особо, химическое название соединений означает смесь всех возможных стереоизомерных форм, указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. То же самое применимо к описанным здесь промежуточным соединениям, используемым для получения конечных продуктов формулы (I).-4 006101 Термины цис- и транс- использованы здесь в соответствии с номенклатурой Chemical Abstracts и указывают на положение заместителей в циклической группе. Абсолютная стереохимическая конфигурация соединений бифенилкарбоксамида формулы (I) и используемых для их получения промежуточных соединений, легко может быть определена специалистом в данной области на основании хорошо известных способов, например рентгенографии. Кроме того, некоторые соединения бифенилкарбоксамида формулы (I) и некоторые используемые для их получения промежуточные соединения могут обладать полиморфизмом. Подразумевается, что настоящее соединение охватывает любые полиморфные формы, обладающие свойствами, полезными для лечения вышеперечисленных заболеваний. Группа представляющих интерес соединений состоит из тех соединений формулы (I), где применимы одно или более следующих ограничений:a) R1 означает водород или трифторметил;h) Z означает двухвалентный радикал формулы (а-1), где каждый из X1 и X2 означает азот;i) Z означает двухвалентный радикал формулы (а-2), где X1 означает азот и m и m' означают целое число, равное 1;j) Z означает двухвалентный радикал формулы (а-2), где X1 означает азот, m означает целое число,равное 2, и m' означает целое число, равное 1;k) Z означает двухвалентный радикал формулы (а-3), где Х 1 означает азот и m и m' означают целое число, равное 1; 1) Z означает двухвалентный радикал формулы (а-3), где Х 1 означает азот, m означает целое число,равное 2, и m' означает целое число, равное 1;m) Z означает двухвалентный радикал формулы (а-4), где m означает целое число, равное 2, и m' означает целое число, равное 1;n) каждый из R5 и R6 независимо означает водород или метил; о) двухвалентный радикал А означает C1-6-алкандиил, замещенный одной арильной группой, в частности А означает метиленовую группу, замещенную фенилом; р) В означает C1-4-алкилокси или C1-10-алкиламино. Соединениями, представляющими наибольший интерес, являются те соединения формулы (1), гдеR1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-1), где каждый из X1 и X2 означает азот, n означает целое число, равное 2, и каждый из R5 и R6 независимо означает водород или метил. Другими представляющими больший интерес соединениями являются те соединения формулы (I),где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-2) или (а-3), где X1 означает азот, m и m' означают целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил. Еще другими представляющими больший интерес соединениями являются те соединения формулы(I), где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-2) или (а-3), где Х означает азот, m означает целое число, равное 2, m' означает целое число, равное 1; и каждый из R5 и R6 независимо означает водород или метил. Еще другими представляющими больший интерес соединениями являются те соединения формулы(I), где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-4), m означает целое число, равное 2, и m' означает целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил. Одно из преимуществ настоящего изобретения состоит в легкости, с которой соединения формулы(I) могут быть получены в промышленных масштабах большим числом различных способов. Некоторые из этих способов далее описаны подробно, хотя приведенным перечнем не исчерпываются способы получения указанных соединений. Первым способом получения соединения бифенилкарбоксамида по настоящему изобретению является способ, по которому промежуточный фениленамин формулы где В, А, Z и R4 принимают указанные для формулы (I) значения, подвергают взаимодействию с бифенилкарбоновой кислотой или хлорангидридом формулы (III) где R1 и R2 принимают указанные для формулы (I) значения и Y1 выбирают из гидрокси и галогена по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии подходящего основания, причем указанный способ далее необязательно включает превращение соединения формулы(I) в его аддитивную соль и/или получение его стереохимически изомерных форм. В случае когда Y1 означает гидроксигруппу, может быть удобно активировать бифенилкарбоновую кислоту формулы (III) добавлением эффективного количества промотора реакции. Не ограничивающие примеры таких промоторов реакции включают карбонилдиимидазол, диимиды, такие как N,N'-дициклогексилкарбодиимид или 1-(3-диметиламинопропил)-3-этилкарбодиимид и их функциональные производные. Для такого типа способа ацилирования предпочтительно использовать полярный апротонный растворитель, такой как,например, метиленхлорид. Подходящие основания для осуществления первого способа включают третичные амины, такие как триэтиламин, триизопропиламин и тому подобное. Подходящие температуры для осуществления первого способа по изобретению обычно находятся в пределах приблизительно от 20 до 140 С в зависимости от конкретного используемого растворителя. Вторым способом получения соединения бифенилкарбоксамида по изобретению является способ,включающий взаимодействие промежуточного соединения формулы (IV) где R1, R2, R3, R4, А и Z принимают указанные для формулы (I) значения и Y2 выбирают из галогена и гидрокси с промежуточным соединением (V) формулы В-Н, где В означает NR7R8 или OR9 и R7, R8 и R9 принимают указанные для формулы (I) значения по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии по меньшей мере одного подходящего связующего реагента и/или подходящего основания, причем указанный способ в дальнейшем необязательно включает превращение соединения формулы (I) в его аддитивную соль и/или получение его стереохимически изомерных форм. В случае когда Y2 означает гидроксигруппу, может быть удобно активировать карбоновую кислоту формулы (IV) добавлением эффективного количества промотора реакции. Неограничивающие примеры таких промоторов реакции включают карбонилдиимидазол, диимиды, такие как N,N'дициклогексилкарбодиимид или 1-(3-диметиламинопропил)-3-этилкарбодиимид и их функциональные производные. В случае использования хирально чистого реагента формулы (V), быстрое и не сопровождающееся энантиомеризацией взаимодействие промежуточного соединения формулы (IV) с указанным промежуточным соединением (V) может быть осуществлено в дополнительном присутствии эффективного количества соединения, такого как гидроксибензотриазол, бензотриазолилокситрис(диметиламино) фосфонийгексафторфосфат, тетрапирролидинофосфонийгексафторфосфат, бромтрипирролидинофосфонийгексафторфосфат или его функциональное производное, как описано в D. Hudson, J.Org.Chem.(1988), 53:617. В случае когда Y2 означает гидрокси и В означает OR9, реакцию эстерификации может быть удобно осуществлять в присутствии эффективного количества кислоты, такой как серная кислота и тому подобное. Третьим способом получения соединения бифенилкарбоксамида по настоящему изобретению является способ, по которому промежуточное соединение формулы (VI) где R1, R2, R3 и R4 принимают указанные для формулы (I) значения и Y3 выбирают из галогена, В(ОН)2,алкилборонатов и их циклических аналогов, подвергают взаимодействию с реагентом формулы (VII) где В, А и Z принимают указанные для формулы (I) значения по меньшей мере в одном реакционноинертном растворителе и необязательно в присутствии по меньшей мере одного связующего реагента на основе переходного металла и/или по меньшей мере одного подходящего лиганда, указанный способ-6 006101 далее необязательно включает превращение соединения формулы (I) в его аддитивную соль и/или получение его стереохимически изомерных форм. Указанный тип взаимодействия известен из уровня техники как реакция Buchwaldt'a, ссылки на применимость связующих реагентов на основе металлов и/или подходящих лигандов, например соединений палладия, таких как палладийтетра(трифенилфосфин),трис(дибензилиденацетондипалладий, 2,2'-бис(бифенилфосфино)-1,1'-динафтил и тому подобное, могут быть найдены, например, в Terpahedron Letters (1996) 37(40) 7181-7184 и J.Am.Chem.Soc. (1996) 118:7216. Если Y3 означает В(ОН)2, алкилборонат или его циклический аналог, то, согласно TetpahedronLetters (1998) 39:2933-6, в качестве связующего реагента следует использовать ацетат двухвалентной меди. Соединения формулы (I) удобно получать, используя методы синтеза в твердой фазе, как показано на схеме 1 ниже. В целом, синтез в твердой фазе включает взаимодействие промежуточного для синтеза соединения с полимерной основой. Это промежуточное соединение на полимерной основе может быть затем использовано на протяжении ряда синтетических стадий. После каждой стадии промежуточные продукты удаляют фильтрованием полимерных смол и многократной промывкой различными растворителями. На каждой стадии полимерная смола может быть разделена для проведения взаимодействия с различными промежуточными соединениями на следующей стадии, что таким образом дает возможность синтеза большого числа соединений. После проведения последней стадии способа полимерную смолу обрабатывают реагентом или подвергают обработке, позволяющей удалить указанную смолу из образца. Более подробное объяснение приемов, используемых в химии твердых фаз, приведено, например, вHandbook (Novabiochem AG, Switzerland), оба литературных источника включены здесь в качестве ссылки. Схема 1 Сокращенные обозначения, используемые в схеме 1, объясняются в экспериментальной части. Заместители R1, R2, R3, R4, А, В и Z принимают указанные для соединений формулы (1) значения. PG озна-7 006101 чает защитную группу, такую как, например, трет-бутоксикарбонил, C1-6-алкилоксикарбонил, фенилметилоксикарбонил и тому подобное. Соединения формулы (I), полученные вышеуказанным способом, могут быть синтезированы в форме рацемических смесей энантиомеров, которые могут быть друг от друга следующими известными из уровня техники способами разделения. Рацемические соединения формулы (I) могут быть превращены в соответствующие диастереомерные формы солей путем взаимодействия с подходящей хиральной кислотой. Указанные диастереомерные формы солей впоследствии разделяют, например, селективной или фракционной кристаллизацией и энантиомеры выделяют из них в свободном состоянии, используя щелочь. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с применением хиральной стационарной фазы. Указанные чистые стереохимически изомерные формы могут также быть получены из соответствующих чистых стереохимически изомерных форм подходящих исходных материалов при условии, что взаимодействие протекает стереоспецифически. Если требуется специфический стереоизомер, предпочтительно указанное соединение синтезировать стереоспецифическими способами получения. В этих способах целесообразно использовать энантиомерно чистые стереоспецифические исходные материалы. Соединения бифенилкарбоксамида формулы (I), их N-оксидные формы, фармацевтически приемлемые соли и стереоизомерные формы обладают подходящей ингибирующей активностью в отношении В аполипопротеида и сопутствующим действием по снижению содержания липидов. Кроме того, настоящие соединения пригодны в качестве лекарственного средства, в особенности в способе лечения пациентов, страдающих гиперлипемией, ожирением, атеросклерозом и диабетом типа II. В частности,настоящие соединения могут быть использованы для промышленного получения лекарственного препарата для лечения нарушений, вызванных избытком липопротеидов очень низкой плотности (VLDL) или липопротеидов низкой плотности (LDL) и, в особенности, нарушений, вызванных холестерином, связанным с указанными VLDL и LDL. Хорошо установлена каузальная взаимосвязь между гиперхолестеринемией, в особенности гиперхолестеринемией, вызванной повышенными концентрациями в плазме липопротеидов низкой плотности(LDL) и липопротеидов очень низкой плотности (VLDL), и ранними атеросклерозом и сердечнососудистым заболеванием. VLDL секретируется печенью и содержит аполипопротеид В (Аро-В); эти частицы подвергаются при циркуляции разложению до LDL, который переносит порядка 60-70% общего холестерина сыворотки. Аро-В является также основным белковым компонентом LDL. Повышенные уровни LDL-холестерина в сыворотке из-за избыточного синтеза или сниженного обмена каузально связаны с атеросклерозом. Напротив, липопротеиды высокой плотности (HDL), содержащие аполипопротеид А 1, обладают защитным эффектом и имеют обратную корреляцию с риском ишемической болезни сердца. Таким образом, соотношение HDL/LDL является удобным способом оценки атерогенного потенциала профиля липидов плазмы индивидуума. Принципиальный механизм действия соединений формулы (I) очевидно включает ингибирование активности МТР (микросомального белка транспорта триглицерида) в гепатоцитах и эпителиальных клетках кишечника, что приводит к пониженному продуцированию VLDL и хиломикронов соответственно. Указанный механизм составляет новый и усовершенствованный подход к лечению гиперлипемии и, по всей вероятности, состоит в снижении уровней LDL-холестерина и триглицеридов через пониженное продуцирование в печени VLDL и продуцирования хиломикронов в кишечнике. Большое число генетических и приобретенных болезней приводит к гиперлипемии. Вызываемые состояния могут быть классифицированы на первичные и вторичные гиперлипемические состояния. Наиболее общими причинами вторичных гиперлипемий являются сахарный диабет, злоупотребление алкоголем, лекарствами, гипотиреоз, хроническая почечная недостаточность, нефротоксический синдром, холестаз и булимия. Первичными гиперлипемиями являются общая гиперхолестеринемия, семейная комбинированная гиперлипемия, семейная гиперхолестеринемия, остаточная гиперлипемия, синдром хиломикронемии, семейная гипертриглицеридемия. Настоящие соединения могут также быть полезны для профилактики или лечения пациентов, страдающих ожирением или атеросклерозом, в особенности коронарным атеросклерозом, и в более общем случае от нарушений, связанных с атеросклерозом, таких как ишемическая болезнь сердца, заболевание периферических сосудов, заболевание сосудов головного мозга. Настоящие соединения могут вызвать регрессию атеросклероза и подавлять клинические последствия атеросклероза, главным образом, заболеваемость и летальность. С учетом применимости соединений формулы (I), отсюда следует, что настоящее изобретение также представляет способ лечения теплокровных, включая человека (обычно называемых здесь пациенты),страдающих нарушениями, вызванными избытком липопротеидов очень низкой плотности (VLDL) или липопротеидов низкой плотности (LDL) и в особенности нарушений, вызванных холестерином, связанным с указанными VLDL и LDL. Следовательно, способ лечения предусмотрен для оказания помощи пациентам, страдающим заболеваниями, такими как, например, гиперлипемия, ожирение, атеросклероз и диабет типа II. Аро В-48, синтезируемый в кишечнике, необходим для сборки хиломикронов и поэтому играет обязательную роль при всасывании кишечником поступающих с пищей жиров. Настоящее изобретение от-8 006101 носится к соединениям бифенилкарбоксамида, действующим как селективные ингибиторы МТР на уровне кишечной стенки. Кроме того, настоящее изобретение относится к фармацевтическим композициям, включающим по меньшей мере один фармацевтически приемлемый носитель и терапевтически эффективное количество соединения бифенилкарбоксамида, имеющего формулу (I). С целью получения фармацевтических композиций по настоящему изобретению эффективное количество конкретного соединения, в основной форме или в форме аддитивной соли, в качестве активного ингредиента, объединяют в однородную смесь по меньшей мере с одним фармацевтически приемлемым носителем, указанный носитель может находиться в различных формах в зависимости от требуемой для введения формы препарата. Указанные фармацевтические композиции представлены в дозированной лекарственной форме, подходящей преимущественно для перорального введения, ректального введения,введения через кожу или парентерального введения. Например, при получении композиций в лекарственной форме, предназначенной для перорального введения, могут быть использованы любые обычные жидкие фармацевтические носители, такие как, например, вода, гликоли, масла, спирты и тому подобное, в случае жидких препаратов для перорального введения, таких как суспензии, сиропы, эликсиры и растворы; или твердые фармацевтические носители,такие как крахмалы, сахара, каолин, смазывающие средства, связывающие вещества, дезинтегрирующие средства и тому подобное, в случае порошков, пилюль, капсул и таблеток. Из-за легкости их применения таблетки и капсулы представляют наиболее удобную дозированную лекарственную форму для перорального введения, в этом случае, безусловно, используют твердые фармацевтические носители. При получении композиций для парентерального введения фармацевтический носитель в основном включает стерильную воду, хотя могут быть включены и другие ингредиенты с целью улучшения растворимости активного ингредиента. Растворы для инъекций могут быть получены, например, использованием фармацевтического носителя, включающего солевой раствор, раствор глюкозы или смесь обоих растворов. Суспензии для инъекции могут также быть получены использованием подходящих жидких носителей,суспендирующих средств и тому подобного. В композициях, подходящих для введения через кожу, фармацевтический носитель может необязательно включать усиливающий проникновение агент и/или подходящее смачивающее средство, необязательно объединенное с незначительными количествами подходящих добавок, не оказывающих значительного вредного действия на кожу. Указанные добавки могут быть выбраны так, чтобы они облегчали введение активного ингредиента через кожу и/или способствовали получению требуемых композиций. Такие топические композиции могут быть введены различными путями, например посредством трансдермальных пластырей, нанесением пятна на кожу или в виде мази. Аддитивные соли соединений формулы (I) безусловно более подходят для получения водных композиций. В особенности удобно формулировать фармацевтические композиции в дозированную лекарственную форму для легкости введения и получения стандартных доз. "Дозированная лекарственная форма",как использовано здесь, означает физически дискретные единицы, пригодные в качестве стандартных доз, каждая единица содержит заранее определенное количество активного ингредиента, рассчитанное так, чтобы производить желаемое терапевтическое действие в сочетании с требуемым фармацевтическим носителем. Примерами таких дозированных лекарственных форм являются таблетки (включая штрихованные и покрытые оболочкой таблетки), капсулы, пилюли, пакетики с порошком, облатки, растворы или суспензии для инъекции, составы, отмеряемые чайной ложкой, столовой ложкой и тому подобное, и их сегрегированные множества. Для перорального введения фармацевтические композиции по настоящему изобретению могут быть взяты в форме твердых лекарственных форм, например таблеток (как проглатываемые, так и жевательные формы), капсул или желатиновых капсул, полученных общепринятыми способами с фармацевтически приемлемыми наполнителями и носителями, такими как связывающие агенты (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон, гидроксипропилметилцеллюлоза и тому подобное), наполнителями (например, лактозой, микрокристаллической целлюлозой, фосфатом кальция и тому подобным), смазывающими веществами (например, стеаратом магния, тальком, двуокисью кремния и тому подобным), дезинтегрирующими средствами (например, картофельным крахмалом, натрийкрахмалгликоллятом и тому подобным), смачивающими средствами (например, натрийлаурилсульфатом) и тому подобным. На такие таблетки могут также быть нанесены покрытия путем применения хорошо известных из уровня техники способов. Жидкие препараты для перорального введения могут быть взяты, например, в форме растворов, сиропов или суспензий, либо указанные препараты могут быть формулированы как сухой продукт для смешивания перед употреблением с водой и/или другим подходящим жидким носителем. Такие жидкие препараты могут быть получены общепринятыми способами необязательно с другими фармацевтически приемлемыми добавками, такими как суспендирующие агенты (например, сироп сорбита, метилцеллюлоза, гидроксипропилметилцеллюлоза или гидрогенизированные пищевые жиры), эмульгирующие агенты (например, лецитин или сок акации), неводные носители (например, миндальное масло, масличные-9 006101 эфиры или этиловый спирт), подсластители, корригенты, маскирующие агенты и консерванты (например, метил- или пропил- п-гидроксибензоаты или сорбиновая кислота). Фармацевтически приемлемые подсластители, используемые в фармацевтических композициях по изобретению, включают предпочтительно по меньшей мере один сильный подсластитель, такой как аспартам, ацесульфамкалий, натрийцикламат, алитам, дигидрохалконовый подсластитель, монеллин, стевиозидсукралоза (4,1',6'-трихлор-4,1',6'-тридеоксигалактосахароза) или предпочтительно сахарин, натрий- или кальцийсахарин и необязательно по меньшей мере один объемный подсластитель, такой как сорбит, маннит, фруктоза, сахароза, мальтоза, изомальт, глюкоза, гидрогенизированный сироп глюкозы,ксилит, карамель или мед. Сильные подсластители обычно используют в низких концентрациях. Например, в случае натрийсахарина указанная концентрация может быть в пределах приблизительно от 0,04% до 0,1% (масса/объем) от конечного состава. Объемный подсластитель можно эффективно использовать в большем интервале концентраций, приблизительно от 10 до 35%, предпочтительно от 10 до 15% (масса/объем). Фармацевтически приемлемыми корригентами, маскирующими ингредиенты с горьким вкусом в составах с низкими дозами, являются предпочтительно фруктовые вкусовые добавки, такие как добавки со вкусом вишни, малины, черной смородины или клубники. Комбинация из двух вкусовых добавок может давать очень хорошие результаты. В составах с высокими дозами могут потребоваться более сильные фармацевтически приемлемые вкусовые добавки, такие как Caramel Chocolate, Mint Cool, Fantasy и тому подобные. Каждая вкусовая добавка может быть представлена в конечной композиции в пределах концентраций приблизительно от 0,05 до 1% (масса на объем). Удобно использовать комбинации указанных сильных вкусовых добавок. Предпочтительно используют вкусовую добавку, которая не подвергается никаким изменениям или потере вкуса и/или цвета в среде состава. Соединения бифенилкарбоксамида по настоящему изобретению могут быть формулированы для парентерального введения путем инъекций, обычно путем внутривенной, внутримышечной или подкожной инъекции, например путем инъекции ударной дозы вещества или путем непрерывного внутривенного вливания. Составы для инъекции могут быть представлены в виде дозированной лекарственной формы, например в ампулах или контейнерах с многократными дозами, включающих добавленный консервант. Они могут выпускаться в таких формах как суспензии, растворы или эмульсии в масляном или водном растворителях и могут содержать формулирующие агенты, такие как изотонизирующие, суспендирующие, стабилизирующие и/или диспергирующие средства. Альтернативно, активный ингредиент может быть представлен в форме порошка для смешивания с подходящим растворителем, например стерильной апирогенной водой, перед употреблением. Соединения бифенилкарбоксамида по настоящему изобретению могут также быть формулированы в ректальные композиции, такие как суппозитории или удерживающие клизмы, например, содержащие обычные основы для суппозиториев, такие как масло какао и/или другие глицериды. Соединения бифенилкарбоксамида по настоящему изобретению могут быть использованы в сочетании с другими фармацевтическими агентами, в частности фармацевтические композиции по настоящему изобретению могут дополнительно включать по меньшей мере один дополнительный снижающий содержание липидов агент, что таким образом ведет к так называемой комбинированной снижающий содержание липидов терапии. Указанным дополнительным снижающим содержание липидов агентом может быть, например, известное лекарственное средство, обычно используемое для лечения гиперлипемии, такое как, например, смола на основе веществ, усиливающих секрецию желчной кислоты, производное фибриновой кислоты или никотиновая кислота, как упомянуто выше в разделе обоснование изобретения. Подходящие дополнительные снижающие содержание липидов агенты включают также другие ингибиторы биосинтеза холестерина и ингибиторы всасывания холестерина, в особенности ингибиторы HMG-CoA-редуктазы и ингибиторы HMG-CoA-синтазы, ингибиторы экспрессии гена HMG-CoAредуктазы, ингибиторы СЕТР, ингибиторы АСАТ, ингибиторы сквален-синтетазы и тому подобные. В соответствии с настоящим изобретением любой ингибитор HMG-СоА-редуктазы может быть использован в качестве второго соединения в комбинированной терапии. Термин "ингибитор HMG-CoAредуктазы", как используется здесь, если не оговорено особо, означаетсоединение, ингибирующее биотрансформацию гидроксиметилглутарилкофермента А до мевалоновой кислоты, катализируемую ферментом HMG-CoA-редуктазой. Такое ингибирование может быть легко оценено специалистом в данной области на основе стандартных методик анализа, т.е. Methods of Enzymology (1981) 71:455-509. Характерные примеры соединений описаны, например, в патенте США 4.231.938 (включающем ловастатин), патенте США 4.444.784 (включающем симвастатин), патенте США 4.739.073 (включающем флувастатин), патенте США 4.346.227 (включающем правастатин), ЕР-А-491.226 (включающем ривастатин) и патенте США 4.647.576 (включающем аторвастатин). В соответствии с настоящим изобретением любой ингибитор HMG-СоА-синтазы может быть использован в качестве второго соединения в комбинированной терапии. Термин "ингибитор HMG-CoAсинтазы", как используется здесь, если не оговорено особо, означает соединение, ингибирующее биосинтез гидроксиметилглутарилкофермента А из ацетилкофермента А и ацетоацетилкофермента А, катализируемый ферментом HMG-CoA-синтазой. Такое ингибирование может быть легко оценено специалистом- 10006101 в данной области на основе стандартных методик анализа, т.е. Methods of Enzymology (1985) 110:19-26. Характерные примеры соединений описаны, например, в патенте США 5.120.729, касающемся производных бета-лактама, патенте США 5.064.856, касающемся производных спиролактона, и патенте США 4.847.271, касающемся соединений оксетана. В соответствии с настоящим изобретением любой ингибитор экспресси гена HMG-CoA-редуктазы может быть использован в качестве второго соединения в комбинированной терапии. Такими агентами могут быть ингибиторы транскрипции HMG-CoA-редуктазы, которые блокируют транскрипцию ДНК,или ингибиторы трансляции, предотвращающие трансляцию кодируемой мРНК HMG-CoA-редуктазы в белок. Такие ингибиторы могут влиять на транскрипцию или трансляцию непосредственно либо могут быть биотрансформированы в соединения, обладающие вышеуказанными свойствами, при помощи одного или более ферментов в каскаде биосинтеза холестерина, либо могут вести к аккумуляции метаболита, обладающего вышеуказанными действиями. Такая регуляция может быть легко оценена специалистом в данной области на основе стандартных методик анализа, т.е. Methods of Enzymology (1985) 110: 919. Характерные примеры соединений описаны, например, в патенте США 5.041.432 и E.I.Mercer,Prog.Lip.Res. (1993) 32:357-416. В соответствии с настоящим изобретением любой ингибитор СЕТР может быть использован в качестве второго соединения в комбинированной терапии. Термин "ингибитор СЕТР", как используется здесь, если не оговорено особо, означает соединение, ингибирующее белок транспорта сложного холестерилового эфира (СЕТР), опосредующий транспорт различных сложных холестериловых эфиров и триглицеридов от HDL к LDL и VLDL. Характерные примеры соединений описаны, например, в патенте США 5.512.548, в J.Antibiot. (1996) 49 (8):815-816 и Bioorg.Med.Chem.Lett. (1996) 6:1951-1954. В соответствии с настоящим изобретением любой ингибитор АСАТ может быть использован в качестве второго соединения в комбинированной терапии. Термин "ингибитор АСАТ", как используется здесь, если не оговорено особо, означает соединение, ингибирующее внутриклеточную этерификацию поступающего с пищей холестерина при помощи фермента ацил-СоА:холестеринацилтрансферазы. Такое ингибирование может быть легко оценено специалистом в данной области на основе стандартных методик анализа, т.е. по методу Heider et al., Journal of Lipid. Research (1983) 24:1127. Характерные примеры соединений описаны, например, в патенте США 5.510.379, в WO 96/26948 и WO 96/10559. В соответствии с настоящим изобретением любой ингибитор сквален-синтетазы может быть использован в качестве второго соединения в комбинированной терапии. Термин "ингибитор скваленсинтетазы", как используется здесь, если не оговорено особо, означает соединение, ингибирующее конденсацию двух молекул фарнезилпирофосфата с образованием сквалена, катализируемую ферментом сквален-синтетазой. Такое ингибирование может быть легко оценено специалистом в данной области на основе стандартных методик анализа, т.е. Methods of Enzymology (1985) 110:359-373. Характерные примеры соединений описаны, например, в ЕР-А-567.026, в ЕР-А-645.378 и в ЕР-А-645.377. Специалисту в лечении гиперлипемии легко определить терапевтически эффективное количество соединения бифенилкарбоксамида по настоящему изобретению по представленным ниже результатам тестов. В целом считается, что терапевтически эффективная доза должна составлять приблизительно от 0,001 до 5 мг/кг массы тела, более предпочтительно приблизительно от 0,01 до 0,5 мг/кг массы тела проходящего лечение пациента. Удобно вводить терапевтически эффективную дозу в форме двух или более разделенных доз с соответствующими интервалами в течение дня. Указанные подразделенные дозы могут быть формулированы как дозированные лекарственные формы, например, каждая из которых содержит около 0,1-350 мг, в особенности 1-200 мг активного ингредиента на дозированную лекарственную форму. Как хорошо известно специалистам из уровня техники, точная доза и частота введения зависят от конкретного используемого соединения бифенилкарбоксамида формулы (I), конкретного требующего лечения состояния, тяжести требующего лечения заболевания, возраста, массы и общего физического состояния конкретного пациента, а также другого медицинского средства (включая вышеуказанные дополнительные снижающие содержание липидов агенты), принимаемого пациентом. Кроме того, указанное эффективное суточное количество может быть снижено или увеличено в зависимости от реакции проходящего лечение пациента и/или в зависимости от оценки лечащего врача, прописывающего соединения бифенилкарбоксамида по настоящему изобретению. Вышеуказанные интервалы эффективного суточного количества носят только характер рекомендаций. Экспериментальная часть В описанных ниже методиках приведены следующие сокращенные обозначения: ACN означает ацетонитрил; THF означает терагидрофуран (ТГФ); DCM означает дихлорметан; DIPE означает диизопропиловый эфир; DMF означает N,N-диметилформамид (ДМФ); NMP означает N-мeтил-2-пиppoлидoн;- 11006101 А. Синтез промежуточных соединений В целях реализации комбинаторного подхода ряд промежуточных полимерных смол получают исходя из промышленно выпускаемых смол. Схема 2 Пример А.1. Смесь промышленно выпускаемой полимерной смолы Novabiochem 01-64-0261 (25,1 г), 4 броманилина (24 г) изопропоксида титана (IV) (41 мл) в DCM (400 мл) осторожно перемешивают в течение 1 ч при комнатной температуре. Добавляют натрийтриацетоксиборогидрид (30 г) и реакционную смесь перемешивают в течение ночи при комнатной температуре. Добавляют метанол (50 мл) и смесь перемешивают в течение 1 ч, затем фильтруют, промывают однократно DCM, однократно метанолом,затем однократно смесью DCM (200 мл) + DIPEA (20 мл), промывают трижды, первично DCM, после чего вторично метанолом, затем сушат, получая 29,28 г полимерной смолы, обозначенной как полимерная смола (1) в схеме 2, которую используют на следующей реакционной стадии без дополнительной очистки. Пример А.2. 2-Фенилбензойную кислоту (8,3 г) растворяют в DCM (100 мл). Добавляют тионилхлорид (10 г). Добавляют ДМФ (10 капель) и смесь перемешивают и нагревают до температуры кипения с обратным холодильником в течение 1 ч. Растворитель упаривают. К остатку добавляют DCM (три раза по 50 мл) и растворитель упаривают. Остаток растворяют в DCM (50 мл). Полученный раствор добавляют к смеси полимерной смолы (1) по примеру A.I (14,64 г), DIPEA (24 мл) и 4-диметиламинопиридина (здесь далее обозначен как DMAP) (0,5 г) в DCM (150 мл). Реакционную смесь перемешивают в течение ночи при комнатной температуре, затем фильтруют и остаток на фильтре промывают смесью 100 мл ДМФ + 20 млDIPEA, затем метанолом, водой, DCM, метанолом, DCM и метанолом, после чего сушат, получая 15,73 г полимерной смолы, обозначенной как полимерная смола (2-а) в схеме 2. Пример А.3. 4'-(Трифторметил)-2-бифенилкарбоновую кислоту (14,64 г) растворяют в DCM (100 мл). Добавляют ДМФ (1 мл). Добавляют тионилхлорид (10 г) и смесь перемешивают и нагревают до температуры кипения с обратным холодильником в течение 1 ч. Растворитель упаривают. Добавляют DCM (два раза по 50 мл), затем растворитель упаривают. Остаток растворяют в DCM (50 мл). Полученный раствор добавляют к смеси полимерной смолы (1) по примеру A.I (14,64 г), DIPEA (24 мл) и DMAP (0,5 г) в DCM (150 мл). Реакционную смесь встряхивают 4 ч при комнатной температуре,затем фильтруют и остаток на фильтре промывают смесью 100 мл ДМФ + 20 мл DIPEA, затем промывают трижды сначала DCM, потом дважды метанолом и наконец сушат. Полученный реакционный продукт еще раз подвергают взаимодействию с половиной исходных количеств 4'-(трифторметил)-2 бифенилкарбоновой кислоты, тионил хлорида, DIPEA и DMAP. Реакционную смесь встряхивают в течение ночи при комнатной температуре, затем фильтруют и остаток на фильтре промывают смесью ДМФ + 20 мл DIPEA, затем метанолом, водой, метанолом, DCM, метанолом, смесью DCM + метанол, затем сушат, получая 17,48 г полимерной смолы, обозначенной как полимерная смола (2-b) в схеме 2. Пример А.4.a) Раствор 4'-(трифторметил)-[1,1'-бифенил]-2-карбонилхлорида (0,019 моль) в DCM (50 мл) добавляют медленно при 5 С к смеси 1-амино-4-иодбензол (0,017 моль) и триэтиламин (0,026 моль) в DCM (40 мл). Смесь перемешивают при комнатной температуре в течение 1 ч, затем промывают 1 н НСl, после чего 10% K2CO3. Органический слой отделяют, сушат, фильтруют и растворитель упаривают. Остаток кристаллизуют из DIPE. Остаток фильтруют и сушат, получая 6,1 г N-(4-иодфенил)-[4'-(трифторметил)[1,1'-бифенил]-2-карбоксамида (промежуточный продукт 1; т.пл. 147 С).b) Смесь промежуточного продукта (1) (0,012 моль), N-аллилфталимида (0,012 моль), ацетата палладия(II) (0,001 моль) и триэтиламина (0,024 моль) перемешивают при 100 С в течение 12 ч в сосуде высокого давления, затем растворяют в DCM и промывают 10% K2 СО 3. Органический слой отделяют, сушат, фильтруют и растворитель упаривают. Остаток кристаллизуют из ACN. Остаток фильтруют и сушат, получая 3,2 г N-(4-[(1 Е)-3-(1,3-дигидро-1,3-диоксо-2 Н-изоиндол-2-ил)-1-пропенил]фенил]-4'(трифторметил)-[1,1'-бифенил]-2-карбоксамида (промежуточный продукт 2; т.пл. 190 С). с) Смесь промежуточного продукта (2) (0,005 моль) и водного раствора гидразина (0,005 моль) в этаноле (30 мл) перемешивают и нагревают до температуры кипения с обратным холодильником в течение 2 ч. Осадок фильтруют и промывают этанолом. Добавляют воду. Суспензию подщелачивают NaOH и фильтруют через целит. Целит промывают этилацетатом. Фильтрат экстрагируют этилацетатом и промывают K2 СО 3, затем NaCl. Органический слой отделяют, сушат, фильтруют и упаривают растворитель. Остаток кристаллизуют из ACN. Остаток фильтруют и сушат, получая 2,5 г N-(4-[(1 Е)-3-амино-1 пропенил]фенил]-4'-(трифторметил)-[1,1'-бифенил]-2-карбоксамида (промежуточный продукт 3; т.пл. 190 С). В. Синтез конечных соединений Пример В.1. Суспензию BINAP (0,00014 моль) в NMP (1 мл) добавляют к полимерной смоле (2-b) (0,00014 моль) и трет-бутоксиду натрия (0,00252 моль). Добавляют 1,2-диаминоэтан (0,0021 моль) в NMP (2 мл) смесь перемешивают в атмосфере аргона. Добавляют Рd2(dbа)3 (0,000028 моль) и NMP (1 мл) и реакционную смесь встряхивают 19 ч при 105 С. Смесь охлаждают, фильтруют и остаток на фильтре промывают ДМФ, водой, ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х) и NMP (2 х). Добавляют NMP (3 мл). Добавляют метил-2-бром-2-фенилацетат (0,0007 моль) в NMP (1 мл). ДобавляютDIPEA (0,3 мл) и реакционную смесь встряхивают в течение 18 ч при комнатной температуре. Реакционную смесь фильтруют, промывают ДМФ и водой, затем ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х),DCM (3 х), СН 3 ОН (3 х) и DCM (3 х). Добавляют раствор TFA/TIS/DCM (49:2:49) (4 мл) и смесь встряхивают 1 ч при комнатной температуре. Смесь фильтруют и добавляют еще TFA/TIS/DCM (49:2:49) (1,5 мл). Смесь встряхивают в течение 15 мин, фильтруют, промывают DCM (2 мл), затем фильтраты сушат в токе азота. Остаток очищают ВЭЖХ на Purospher Star RP-18 (20 г, 5 мкм; элюент: 0,5% NH4OAc вH2O)/CH3CN 90/10)/CH3OH/CH3CN (0 мин) 75/25/0, (10,00 мин) 0/50/50, (16,00 мин) 0/0/100, (18,10-20 мин) 75/25/0). Собирают требуемые фракции и органический растворитель упаривают. Водный концентрат обрабатывают водным раствором NB2CO3, затем экстрагируют DCM. Экстракт отделяют на Extrelut и фильтраты сушат в токе азота при 50 С. Остаток дополнительно сушат (вакуум, 50 С), получая 0,006 г соединения 1. Соединения, обозначенные как 2-29 в следующей табл. F-1, получены аналогично, использованием той же экспериментальной методики, но заменой 1,2-диаминоэтана соответствующим реакционноспособным диамином. Пример В.2.NMP (2 мл) добавляют к полимерной смоле (2-а) (0,00014 моль). Добавляют BINAP (0,00014 моль) и трет-бутоксид натрия (0,00252 моль). Добавляют 1,2-диаминоэтан (0,0021 моль) в NMP (1 мл) и смесь встряхивают 1 ч в атмосфере аргона. Добавляют Рd2(dbа)3 (0,000028 моль) в NMP (1 мл) и реакционную смесь встряхивают в течение 18 ч при 105 С. Смесь охлаждают, фильтруют и остаток на фильтре промывают смесью ДМФ - вода 50-50, ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х) и NMP (2 х). Добавляют NMP (3 мл). Добавляют метил-2-бром-2-фенилацетат (0,0007 моль) в NMP (1 мл). Добавляют DIPEA (0,300 мл) и смесь встряхивают еще 18 ч при комнатной температуре. Смесь фильтруют, промывают ДМФ и водой, промывают ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х),DCM (3 х), СН 3 ОН (3 х), DCM (3 х). Добавляют смесь TFA/TIS/DCM (49:2:49) (4 мл) и смесь встряхивают 2 ч при комнатной температуре. Добавляют еще смесь TFA/TIS/DCM (49:2:49) (2 мл) и реакционную смесь встряхивают в течение 15 мин, затем фильтруют. Остаток на фильтре промывают DCM (2 мл), затем фильтраты сушат в токе азота. Остаток очищают ВЭЖХ на Purospher Star RP-18 (20 г, 5 мкм; элюент: 0,5% NH4OAC в Н 2O)/CH3CN 90/10)/CH3OH/CH3CN (0 мин) 75/25/0, (10,00 мин) 0/50/50, (16,00 мин) 0/0/100, (18,10-20 мин) 75/25/0). Требуемые фракции собирают и органический растворитель упаривают. Водный концентрат обрабатывают раствором Na2CO3, затем экстрагируют DCM. Экстракт отделяют и фильтраты сушат в токе азота при 50 С. Остаток дополнительно сушат (вакуум, 50 С), получая 0,007 г соединения 30. Соединения, обозначенные как 31-58 в следующей табл. F-1, получены аналогично, использованием той же экспериментальной методики, но заменой 1,2-диаминоэтана соответствующим реакционноспособным диамином. Пример В.3.(0,00252 моль). Добавляют 4-амино-1-третбутоксикарбонилпиперидин (0,0021 моль) в NMP (1 мл) и смесь встряхивают 1 ч в атмосфере азота. Добавляют Pd2(dba)3 (0,000028 моль) в NMP (1 мл) и реакционную смесь встряхивают в течение 18 ч при- 13006101 105 С. Смесь охлаждают, фильтруют и остаток на фильтре промывают смесью ДМФ-вода 50-50, ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х) и DCM (3 х). Добавляют TMSOTf (1 М) и 2,6-лутидин (1,5 М) в DCM (3 мл) и смесь встряхивают 2 ч при комнатной температуре. Смесь фильтруют, промывают DCM (3 х) и добавляют метанол (4 мл). Смесь встряхивают 1 ч при комнатной температуре, фильтруют и остаток на фильтре промывают DCM (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х),DCM (3 х), СН 3 ОН (3 х) и однократно NMP. Добавляют NMP (3 мл). Добавляют этил-2-бром-2 фенилацетат (0,0007 моль) в NMP (1 мл). Добавляют DIPEA (0,3 мл) и реакционную смесь встряхивают 20 ч при комнатной температуре. Реакционную смесь фильтруют, промывают трижды ДМФ, 3 х водой, 3 х ДМФ, 3 х СН 3 ОН, 3 х DCM, 3 х СН 3 ОН и 3 х DCM. Добавляют смесь TFA/TIS/DCM (49:2:49) (4 мл) и смесь встряхивают 1 ч при комнатной температуре, затем фильтруют. Добавляют еще смесьTFA/TIS/DCM (49:2:49) (2 мл) и смесь встряхивают 30 мин, затем фильтруют и промывают DCM (2 мл). Фильтраты сушат в токе азота при 50 С. Остаток очищают ВЭЖХ на Purospher Star RP-18 (20 г, 5 мкм; элюент: 0,5% NH4OAC в Н 2O)/CH3CN 90/10)/CH3OH/CH3CN (0 мин) 75/25/0, (10,00 мин) 0/50/50, (16,00 мин) 0/0/100, (18,10-20 мин) 75/25/0). Требуемые фракции собирают и органический растворитель упаривают. Водный концентрат обрабатывают раствором Na2CO3, затем экстрагируют DCM. Экстракт отделяют и фильтраты сушат в токе азота при 50 С. Остаток дополнительно сушат (вакуум, 55 С), получая 0,007 г соединения 59. Соединения, обозначенные как 60-96 в следующей табл. F-1, получены аналогично, использованием той же экспериментальной методики, но заменой 4-амино-1-трет-бутоксикарбонилпиперидина соответствующим реакционноспособным амином. Пример В.4. Полимерную смолу (2-b) (0,00014 моль) промывают NMP (2 мл). Добавляют BINAP (0,00014 моль) и трет-бутоксид натрия (0,00252 моль). Добавляют 4-амино-1-трет-бутоксикарбонилпиперидин (0,0021 моль) в NMP (1 мл). Добавляют NMP (3 мл) и смесь встряхивают в течение 1 ч в атмосфере аргона. Добавляют Рd2(dbа)3 (0,000028 моль) в NMP (1 мл) и реакционную смесь встряхивают в течение 18 ч при 105 С. Смесь охлаждают, фильтруют и остаток на фильтре промывают ДМФ, смесью ДМФ-вода 50-50,ДМФ (3 х), водой (3 х), ДМФ (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х) и DCM (3 х). ДобавляютTMSOTf (1 М) и 2,6-лутидин (1,5 М) в DCM (3 мл) и смесь встряхивают 2 ч при комнатной температуре. Смесь фильтруют, промывают DCM (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х), затем NMP (2 х). Добавляют NMP (3 мл). Добавляют метил-2-бром-2-фенилацетат (0,160 г) в NMP (1 мл). Добавляют DIPEA (0,3 мл). Реакционную смесь встряхивают 20 ч при комнатной температуре,фильтруют, промывают ДМФ, затем смесью ДМФ-вода 50-50, затем ДМФ (3 х), водой (3 х), ДМФ (3 х),СН 3 ОН (3 х), DCM (3 х), СН 3 ОН (3 х) и DCM (3 х). Добавляют смесь TFA/TIS/DCM (49:2:49) (4 мл) и смесь встряхивают 1 ч при комнатной температуре, затем фильтруют. Добавляют еще смесьTFA/TIS/DCM (49:2:49) (2 мл) и реакционную смесь встряхивают 30 мин, затем фильтруют. Фильтраты сушат в токе азота при 50 С. Остаток очищают ВЭЖХ на Purospher Star RP-18 (20 г, 5 мкм; элюент: 0,5% NH4OAC в H2O)/CH3CN 90/10)/СН 3 ОН/СН 3 СN (0 мин) 75/25/0, (10,00 мин) 0/50/50, (16,00 мин) 0/0/100, (18,10-20 мин) 75/25/0). Требуемые фракции собирают и органический растворитель упаривают. Водный концентрат обрабатывают раствором NB2CO3, затем экстрагируют DCM. Экстракт отделяют и фильтраты сушат в токе азота при 50 С. Остаток дополнительно сушат (вакуум, 50 С), получая 0,031 г соединения 97. Соединения, обозначенные как 98-l36 в следующей таблице F-1, получены аналогично, использованием той же экспериментальной методики, но заменой 4-амино-1-трет-бутоксикарбонилпиперидина соответствующим реакционноспособным амином. Пример В.5. Смесь промежуточного соединения (3) (0,006 моль), метил-2-бром-2-фенилацетата (0,011 моль),триэтиламина (1,6 мл) и тетрабутиламмонийиодида (0,001 моль) в ТГФ (20 мл) перемешивают при комнатной температуре в течение 8 ч. Добавляют воду. Смесь экстрагируют этилацетатом. Органический слой отделяют, сушат, фильтруют и растворитель упаривают. Остаток очищают хроматографией на колонке с силикагелем (элюент: СН 2 Сl2/СН 3 ОН 98,5/1,5) и кристаллизуют из диэтилового эфира, получая соединение (137), т.пл. 142 С. В табл. F-1 перечислены соединения, полученные по одному из вышеуказанных примеров. В таблице используются следующие условные обозначения: .С 2 НF3O2 означает трифторуксусную кислоту.C.1. Количественная оценка секреции АроВ. Клетками HepG2 засевают 24-луночные планшеты, используя MEM Rega 3 среду, содержащую 10% фетальную сыворотку теленка. При 70% слиянии среду заменяют и добавляют испытуемое соединение или носитель (ДМСО, конечная концентрация 0,4%). После инкубации в течение 24 ч среду переносят в пробирки Eppendorf'a и очищают центрифугированием. К надосадочной жидкости добавляют овечье антитело к обоим ароВ и смесь выдерживают при 8 С в течение 24 ч. Затем добавляют кроличье антиовечье антитело и дают осаждаться иммунному комплексу в течение 24 ч при 8 С. Иммунопреципитат получают в виде осадка в пробирке путем центрифугирования в течение 25 мин при 1320 г и дважды промывают буферным раствором, содержащим 40 мМ Mops, 40 мМ NaH2PO4, 100 мМ NaF, 0,2 мМ DTT,5 мМ EDTA, 5 мМ EGTA, 1% Triton-X-100, 0,5% натрийдеоксихолат (DOC), 0,1% SDS, 0,2 мкМ лейпептин и 0,2 мкМ PMSF. Радиоактивность осадка количественно измеряют, используя жидкостной сцинтилляционный счет. Полученные значения IC50 приведены в табл. C.1. Таблица C.1. pIC50 значения (= -log IC50 значение) С.2. Анализ на МТР Активность МТР измеряют, используя методику анализа, аналогичную описанной в J.R. Wetterauand D.B. Zilversmit in Chemistry and Physics of Lipids, 38, 205-222 (1985). Для получения донорных и акцепторных везикул соответствующие липиды в хлороформе помещают в стеклянные аналитические пробирки и сушат в токе N2. К высушенному липиду добавляют буферный раствор, содержащий 15 мМ TrisHCl pH 7,5, 1 мМ EDTA, 40 мМ NaCl, 0,02% NaN3 (буфер для анализа). Смесь несколько раз взбалтывают и затем дают возможность липидам гидролизоваться в течение 20 мин на льду. Затем получают везикулы обработкой на ультразвуковой бане (Branson 2200) при комнатной температуре в пределах 15 мин. Бутилированный гидрокситолуол включают во все везикулярные препараты при концентрации 0,1%. Смесь для анализа на транспорт липидов содержит донорные везикулы (40 нмоль фосфатидилхолина, 7,5 мольн.% кардиолипина и 0,25 мольн.% глицеролтри-[1-14C]-олеата), акцепторные везикулы (240 нмоль фосфатидилхолина) и 5 мг BSA в общем объеме 675 мкл в пробирке для микроцентрифугирования на 1,5 мл. Добавляют испытуемые соединения, растворенные в ДМСО (0,13% конечная концентрация). После 5 мин преинкубации при 37 С реакцию начинают добавлением МТР в 100 мкл диализного буфера. Реакцию останавливают добавлением 400 мкл DEAE-52 целлюлозы, предварительно уравновешенной в 15 мМ Tris-HCl pH 7,5, смесью 1 мМ EDTA, 0,02% NaN3 (1:1, об/об). Смесь перемешивают в течение 4 мин и центрифугируют 2 мин при максимальной скорости на Eppendorf центрифуге (4 С) до получения осадка DEAE-52-связанных донорных везикул. Определяют счет аликвотной пробы надосадочной жидкости,содержащей акцепторные липосомы, и значения [14 С]-счета используют для расчета процента переноса триглицерида от донорных к акцепторным везикулам. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I)N-оксиды, фармацевтически приемлемые кислотно-аддитивные соли и их стереохимически изомерные формы,где р 1, р 2 и р 3 означают целые числа, каждое из которых независимо равно 1-3; каждый из R1 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси,галоген, гидрокси, меркапто, циано, нитро, C1-4-алкилтио или полигалоген-С 1-6-алкил, амино, C1-4 алкиламино и ди(C1-4-алкил)амино; каждый из R2 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкокси, галоген или трифторметил;R3 означает водород, C1-4-алкил,каждый из R4 независимо выбирают из группы, включающей водород, C1-4-алкил, C1-4-алкилокси,галоген или трифторметил;Z означает двухвалентный радикал формулы- 23006101 где n означает целое число от 2 до 4 и -(СН 2)n-группа в радикале (а-1) может необязательно быть замещена одной или двумя группами C1-4-алкил;m и m' означают целые числа от 1 до 3; каждый из R5 и R6 независимо выбирают из группы, включающей водород, C1-6-алкил или арил; каждый из Х 1 и X2 независимо выбирают из группы, включающей СН, N или атом углерода в sp2 гибридизации и в радикале (а-1) по меньшей мере один из Х 1 или X2 означает N; А означает C1-6-алкандиил, замещенный одной арильной группой; В означает водород; C1-10-алкил; арил или гетероарил, каждый из которых необязательно замещен группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10 алкиламино,ди(C1-10-алкил)амино,C1-10-ацил,C1-10-алкилтио,C1-10-алкоксикарбонил,C1-10 алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил; арил-С 1-10-алкил; гетероарил-С 1-10-алкил; С 3-10 циклоалкил; полигалоген-С 1-6-алкил; С 3-6-алкенил; С 3-6-алкинил; NR7R8 или OR9; где каждый из R7 и R8 независимо означает водород, C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой, выбранной из группы, включающей галоген, циано, C1-4 алкилокси, амино, C1-10-алкиламино, ди(C1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10 алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил; арил-С 1-10-алкил, гетероарил-С 1-10-алкил; С 3-10 циклоалкил; С 7-10-полициклоалкил, полигалоген-С 1-6-алкил, С 3-8-алкенил, С 3-8-алкинил, конденсированный бензо-С 5-8-циклоалкил, и где R9 означает C1-10-алкил, арил или гетероарил, каждый из которых независимо замещен группой, выбранной из группы, включающей галоген, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино, ди(C1-10 алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил; арилC1-10-алкил; гетероарил-С 1-10-алкил; С 3-10-циклоалкил; С 7-10-полициклоалкил; полигалоген-С 1-6-алкил; С 3-8 алкенил; С 3-8-алкинил или конденсированный бензо-С 5-8-циклоалкил, причем арил представляет собой моно- или полиароматические группы, такие как фенил, необязательно замещенный группами, выбранными из галогена, циано, нитро, C1-4-алкилокси, амино, C1-10-алкиламино,ди(С 1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(С 1-10-алкил)аминокарбонил; и гетероарил представляет собой моно- или полигетероароматические группы, такие как группы,включающие один или более гетероатомов, выбранных из азота, кислорода, серы и фосфора, в частности пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, триазолил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, пирролил, фуранил, тиенил и подобные, включая все возможные их изомерные формы, и необязательно замещенные группой, выбранной из галогена, циано, нитро, C1-4 алкилокси, амино, C1-10-алкиламино, ди(С 1-10-алкил)амино, C1-10-ацил, C1-10-алкилтио, C1-10-алкоксикарбонил, C1-10-алкиламинокарбонил и ди(C1-10-алкил)аминокарбонил. 2. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-1), где каждый из X1 и X2 означает азот, n означает целое число, равное 2, и каждый из R5 и R6 независимо означает водород или метил. 3. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-2) или (а-3), где X1 означает азот, m и m' означают целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил. 4. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-2) или (а-3), где X1 означает азот, m означает целое число,равное 2, m' означает целое число, равное 1; и каждый из R5 и R6 независимо означает водород или метил. 5. Соединение по п.1, где R1 означает водород или трифторметил; R2, R3 и R4 означают водород и Z означает двухвалентный радикал формулы (а-4), где m означает целое число, равное 2, и m' означает целое число, равное 1, и каждый из R5 и R6 независимо означает водород или метил. 6. Соединение по любому из пп.1-5, где А означает C1-6-алкандиил, замещенный фенилом, и В означает C1-4-алкилокси или C1-10-алкиламино. 7. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения по любому из пп.1-6. 8. Способ получения фармацевтической композиции по п.7, где терапевтически эффективное количество соединения по любому из пп.1-6 тщательно смешивают до однородной смеси с фармацевтически приемлемым носителем. 9. Применение соединения по любому из пп.1-6 в качестве лекарственного средства для лечения гиперлипемии, ожирения и диабета II типа. 10. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (II), где В, A, Z, R4 и р 3 принимают значения, указанные по п.1,с бифенилкарбоновой кислотой или хлорангидридом формулы (III), где R1, R2, р 1 и р 2 принимают указанные для формулы (I) значения и Y1 выбирают из гидрокси и галогена, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии подходящего основания с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредством обработки щелочью и, по желанию, получают их стереохимически изомерные формы. 11. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (IV) где R1, R2, R3, R4, A, Z, p1, р 2 и р 3 принимают значения, указанные по п.1, и Y2 выбирают из галогена и гидрокси, с промежуточным соединением (V) формулы В-Н, где В означает NR7R8 или OR9 и R7, R8 и R9 принимают значения, указанные по п.1, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии по меньшей мере одного подходящего связующего реагента и/или подходящего основания,с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредством обработки щелочью и, по желанию,получают их стереохимически изомерные формы. 12. Способ получения соединения формулы (I), включающий взаимодействие промежуточного соединения формулы (VI), где R1, R2, R3, R4, р 1, р 2 и р 3 принимают значения, указанные по п.1, и Y3 выбирают из галогена, В(ОН)2, алкилборонатов и их циклических аналогов, с реагентом формулы (VII), где В, А и Z принимают значения, указанные в п.1, по меньшей мере в одном реакционно-инертном растворителе и необязательно в присутствии по меньшей мере одного связующего реагента на основе переходного металла и/или по меньшей мере одного подходящего лиганда,с последующим, если необходимо, превращением соединения формулы (I) одно в другое, следуя известным из уровня техники реакциям превращения; или, по желанию, соединение формулы (I) превращают в его кислотно-аддитивную соль либо, наоборот, кислотно-аддитивную соль соединения формулы (I) превращают в форму свободного основания посредством обработки щелочью и, по желанию, получают их стереохимически изомерные формы.
МПК / Метки
МПК: A61P 3/06, C07C 233/80, A61K 31/40, C07D 211/58
Метки: содержание, полезные, качестве, липидов, агентов, бифенилкарбоксамиды, снижающих
Код ссылки
<a href="https://eas.patents.su/26-6101-bifenilkarboksamidy-poleznye-v-kachestve-snizhayushhih-soderzhanie-lipidov-agentov.html" rel="bookmark" title="База патентов Евразийского Союза">Бифенилкарбоксамиды, полезные в качестве снижающих содержание липидов агентов</a>
Предыдущий патент: Способ получения растительных клеток, аккумулирующих каротиноиды, и выделенная днк, используемая для осуществления способа
Следующий патент: Замещенные дипептиды в качестве средств, усиливающих секрецию гормона роста
Случайный патент: Жидкая антимикробная очищающая композиция для твердых поверхностей