1,3-двузамещенные-4-фенил-1н-пиридин-2-оны
Номер патента: 16969
Опубликовано: 30.08.2012
Авторы: Макдональд Грегор Джеймс, Лютьенс Роберт Иоганнес, Трабанко-Суарес Андрес Авелино, Сид-Нуньес Хосе Мария, Финн Терри Патрик, Дювей Гийом Альбер Жак
Формула / Реферат
1. Соединение, имеющее формулу (I)
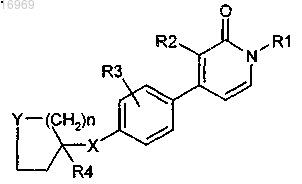
или его стереохимически изомерная форма, где
R1 представляет собой С1-6алкил или С1-3алкил, замещенный С3-7циклоалкилом, фенил или фенил, замещенный галогено, трифторметилом или трифторметокси;
R2 представляет собой галогено, трифторметил, C1-3алкил или циклопропил;
R3 представляет собой водород, галогено или трифторметил;
R4 представляет собой водород, C1-3алкил, С1-3алкилокси, гидроксиС1-3алкил или тетрагидрофуран-2-илоксиС1-3алкил;
n равно 1 или 2;
X представляет собой ковалентную связь, О или NR5;
R5 представляет собой водород, С1-3алкил или гидроксиС2-3алкил;
Y представляет собой О или CR6(OH);
R6 представляет собой водород или C1-3алкил или
R4 и R6 образуют радикал -СН2-СН2-;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где
R1 представляет собой 1-бутил, 2-метил-1-пропил, 3-метил-1-бутил, (циклопропил)метил или 2-(циклопропил)-1-этил;
R2 представляет собой галогено;
R3 представляет собой водород, хлоро или трифторметил;
R4 представляет собой водород или гидроксиметил;
n равно 2;
X представляет собой ковалентную связь, О или NR5;
R5 представляет собой водород;
Y представляет собой О или CR6(OH);
R6 представляет собой водород или метил;
или его фармацевтически приемлемая соль.
3. Соединение по п.1, где
R1 представляет собой 1-бутил, 3-метил-1-бутил, (циклопропил)метил или 2-(циклопропил)-1-этил;
R2 представляет собой хлоро;
R3 представляет собой водород или хлоро;
R4 представляет собой водород или гидроксиметил;
n равно 2;
X представляет собой ковалентную связь, О или NR5;
R5 представляет собой водород;
Y представляет собой О или CR6(OH);
R6 представляет собой водород или метил;
или его фармацевтически приемлемая соль.
4. Соединение, представляющее собой 1-бутил-3-хлор-2-оксо-1,2-дигидропиридин-4-иловый эфир трифторметансульфоновой кислоты.
5. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по любому из пп.1-4 и фармацевтически приемлемый носитель или эксципиент.
6. Применение соединения по любому из пп.1-4 в качестве лекарственного средства.
7. Применение соединения по любому из пп.1-4 для изготовления лекарственного средства для лечения или предупреждения состояния у млекопитающего, включая человека, лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом положительных аллостерических модуляторов mGluR2.
8. Применение соединения по любому из пп.1-4 для изготовления лекарственного средства для лечения или предупреждения расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства, связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия.
9. Применение по п.8, где расстройство центральной нервной системы представляет собой тревожное расстройство, выбранное из группы: агорафобия, генерализованное тревожное расстройство (GAD), обсессивно-компульсивное расстройство (OCD), паническое расстройство, посттравматическое стрессовое расстройство (PTSD), социальная фобия и другие фобии.
10. Применение по п.8, где расстройство центральной нервной системы представляет собой психотическое расстройство, выбранное из группы: шизофрения, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство и психотическое расстройство, вызванное веществом.
11. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство личности, выбранное из группы: обсессивно-компульсивное личностное расстройство и шизоидное, шизотипическое расстройство.
12. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство, связанное с веществом, выбранное из группы: злоупотребление алкоголем, алкогольная зависимость, алкогольная абстиненция, делирий при алкогольной абстиненции, психотическое расстройство, вызванное алкоголем, амфетаминовая зависимость, амфетаминовая абстиненция, кокаиновая зависимость, кокаиновая абстиненция, никотиновая зависимость, никотиновая абстиненция, опиоидная зависимость и опиоидная абстиненция.
13. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство питания, выбранное из группы: нервная анорексия и нейрогенная булимия.
14. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство настроения, выбранное из группы: биполярные расстройства (I и II), циклотимическое расстройство, депрессия, дистимическое расстройство, большое депрессивное расстройство и расстройство настроения, вызванное веществом.
15. Применение по п.8, где расстройство центральной нервной системы представляет собой мигрень.
16. Применение по п.8, где расстройство центральной нервной системы представляет собой эпилепсию или конвульсивное расстройство, выбранное из группы: генерализованная неконвульсивная эпилепсия, генерализованная конвульсивная эпилепсия, малый эпилептический припадок, большой эпилептический припадок, парциальная эпилепсия с нарушением сознания или без нарушения сознания, младенческие судороги, непрерывная парциальная эпилепсия и другие формы эпилепсии.
17. Применение по п.8, где детское расстройство представляет собой синдром дефицита внимания/гиперактивности.
18. Применение по п.8, где расстройство центральной нервной системы представляет собой когнитивное расстройство, выбранное из группы: делирий, персистирующий делирий, вызванный веществом, деменция, деменция вследствие ВИЧ-заболевания, деменция вследствие болезни Гентингтона, деменция вследствие болезни Паркинсона, деменция альцгеймеровского типа, персистирующая деменция, вызванная веществом, и легкое когнитивное нарушение.
19. Применение по п.8, где расстройство центральной нервной системы выбрано из группы: тревога, шизофрения, мигрень, депрессия и эпилепсия.
20. Применение соединения по любому из пп.1-4 в комбинации с ортостерическим агонистом mGluR2 для изготовления лекарственного средства для лечения или предупреждения состояния, указанного в любом из пп.7-19.
21. Применение соединения по любому из пп.1-4 в лечении или предупреждении расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства, связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия.
22. Способ лечения или предупреждения расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства, связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия, включающий введение субъекту соединения по любому из пп.1-4.
Текст
Настоящее изобретение относится к новым соединениям, в частности новым производным пиридинона формулы (I), где все радикалы такие, как определено в заявке и в формуле изобретения. Соединения по изобретению представляют собой положительные аллостерические модуляторы метаботропных рецепторов - подтип 2 ("mGluR2"), которые полезны для лечения или предупреждения неврологических и психиатрических расстройств, связанных с глутаматной дисфункцией, и заболеваний, в которые вовлечен подтип mGluR2 метаботропных рецепторов. В частности, такие заболевания представляют собой расстройства центральной нервной системы,выбранные из группы тревоги, шизофрении, мигрени, депрессии и эпилепсии. Изобретение также направлено на фармацевтические композиции и способы получения таких соединений и композиций, а также на применение таких соединений для предупреждения и лечения таких заболеваний, в которые вовлечен mGluR2. Сид-Нуньес Хосе Мария, ТрабанкоСуарес Андрес Авелино (ES),Макдональд Грегор Джеймс (BE),Дювей Гийом Альбер Жак, Лютьенс Роберт Иоганнес, Финн Терри Патрик 016969 Область изобретения Настоящее изобретение относится к новым производным пиридинона, которые являются положительными аллостерическими модуляторами метаботропных глутаматных рецепторов подтипа 2("mGluR2") и которые полезны для лечения или предупреждения неврологических и психиатрических расстройств, связанных с глутаматной дисфункцией, и заболеваний, в которые вовлечен подтип mGluR2 метаботропных рецепторов. Кроме того, изобретение направлено на фармацевтические композиции, содержащие такие соединения, на способы получения таких соединений и композиций и на применение таких соединений для предупреждения или лечения неврологических и психиатрических расстройств и заболеваний, в которые вовлечен mGluR2. Предшествующий уровень техники Глутамат является важным аминокислотным нейромедиатором в центральной нервной системе млекопитающих. Глутамат играет важную роль в многочисленных физиологических функциях, таких как обучение и память, а также сенсорное восприятие, развитие синаптической пластичности, регуляция моторики, дыхание и регуляция сердечно-сосудистой функции. Кроме того, глутамат находится в центре нескольких разных неврологических и психиатрических заболеваний, в которых имеется нарушение баланса глутаматергической нейротрансмиссии. Глутамат опосредует синаптическую нейротрансмиссию через активацию каналов ионотропных глутаматных рецепторов (iGluRs) и рецепторов NMDA (N-метил-D-аспартат), АМРА (2-альфа-амино-3 гидрокси-5-метил-4-изоксазольпропионовая кислота) и каинатных рецепторов, которые являются ответственными за быструю возбудительную трансмиссию. Кроме того, глутамат активирует метаботропные глутаматные рецепторы (mGluR), играющие дополнительную модуляторную роль, способствующую тонкой корректировке синаптической эффективности. Глутамат активирует mGluR посредством связывания с большим внеклеточным аминоконцевым доменом рецептора, называемым в данном описании изобретения ортостерическим центром связывания. Это связывание вызывает конформационное изменение в рецепторе, что приводит к активации G-белка и внутриклеточных сигнальных путей. Подтип mGluR2 негативно связан с аденилатциклазой через активацию Gi-белка, и его активация приводит к ингибированию высвобождения глутамата в синапсе. В центральной нервной системе (CNS) рецепторы mGluR2 распространены главным образом в коре головного мозга, таламических участках,придаточной обонятельной луковице, гиппокампе, миндалевидном теле, хвостатом ядре-путамене и прилежащем ядре. Активирование mGluR2, как показали клинические исследования, является эффективным в лечении тревожных расстройств. Кроме того, активирование mGluR2 в различных животных моделях показало их эффективность, таким образом предоставляя возможный новый терапевтический подход к лечению шизофрении, эпилепсии, аддикции/наркотической зависимости, болезни Паркинсона, боли, расстройств сна и болезни Гентингтона. В настоящее время большинство доступных фармакологических средств, нацеленных на mGluR,представляют собой ортостерические лиганды, которые активируют некоторые члены семейства, так как они являются структурными аналогами глутамата. Новым направлением для развития селективных соединений, действующих на mGluR, является идентификация соединений, которые действуют посредством аллостерических механизмов, модулируя рецептор путем связывания с сайтом, отличным от высококонсервативного ортостерического центра связывания. Недавно положительные аллостерические модуляторы mGluR выступили в качестве новых фармакологических объектов, предлагающих эту привлекательную альтернативу. В качестве положительных аллостерических модуляторов mGluR2 были описаны различные соединения. В WO 2004/092135 (NPSWO 2006/030032 (AddexJanssen Pharmaceutica) описаны соответственно фенилсульфонамид, ацетофенон, инданон, пиридилметилсульфонамид и производные пиридинона в качестве положительных аллостерических модуляторов mGluR2. Ни одно из конкретно раскрытых в них соединений не является структурно родственным соединениям по настоящему изобретению. Показано, что такие соединения не активируют рецептор сами по себе. Быстрее они обеспечивают возможность для рецептора продуцировать максимальный ответ на концентрацию глутамата, которая самостоятельно индуцирует минимальный ответ. Мутационный анализ однозначно продемонстрировал,что связывание положительных аллостерических модуляторов mGluR2 происходит не в ортостерическом центре, но вместо этого на аллостерическом сайте, расположенном внутри семитрансмембранного участка рецептора. Данные на животных позволяют предположить, что положительные аллостерические модуляторыmGluR2 оказывают эффекты в моделях тревоги и психоза, аналогичные полученным с ортостерическими агонистами. Аллостерические модуляторы mGluR2, как было показано, активны в страхе, усиленном испугом, и стресс-индуцированных гипертермических моделях тревоги. Кроме того, такие соединения,-1 016969 как показано, активны в реверсировании кетамин- или амфетамин-индуцированной гиперлокомоции и в реверсировании амфетамин-индуцированного нарушения преимпульсного ингибирования акустической реакции испуга в модели шизофрении (J. Pharmacol. Exp. Ther. 2006, 318, 173-185; Psychopharmacology 2005, 179, 271-283). Современные исследования на животных также выявили, что селективный положительный аллостерический модулятор подтипа 2 метаботропных глутаматных рецепторов, бифенилинданон (BINA),блокирует модель психоза на основе галлюциногенных лекарственных средств, подтверждая стратегию нацеливания рецепторов mGluR2 на лечение глутаматергической дисфункции при шизофрении (Mol.Pharmacol. 2007, 72, 477-484). Положительные аллостерические модуляторы обеспечивают возможность потенциирования глутаматного ответа, но, кроме того, было доказано, что они потенциируют ответ на ортостерические агонисты mGluR2, такие как LY379268 или DCG-IV. Такие данные обеспечивают доказательство в отношении еще одного нового терапевтического подхода к лечению указанных выше неврологических и психиатрических заболеваний, в которые вовлечен mGluR2, с использованием комбинации положительного аллостерического модулятора mGluR2 вместе с ортостерическим агонистом mGluR2. Подробное описание изобретения Настоящее изобретение относится к соединениям, имеющим активность модуляторов метаботропных глутаматных рецепторов 2, где указанные соединения имеют формулу (I) и их стериохимически изомерным формам, гдеR4 представляет собой водород, С 1-3 алкил, С 1-3 алкилокси, гидроксиС 1-3 алкил или тетрагидрофуран 2-илоксиС 1-3 алкил; n равно 1 или 2;X представляет собой ковалентную связь, О или NR5;R5 представляет собой водород, С 1-3 алкил или гидроксиС 2-3 алкил;R6 представляет собой водород или С 1-3 алкил илиR4 и R6 образуют радикал -СН 2-СН 2-; и их фармацевтически приемлемым солям и сольватам. В одном воплощении данное изобретение относится к соединению формулы (I) или его стереохимически изомерной форме, гдеR4 представляет собой водород или гидроксиметил;X представляет собой ковалентную связь, О или NR5;R6 представляет собой водород или метил; или его фармацевтически приемлемой соли или сольвату. В одном воплощении изобретение относится к соединению формулы (I) или его стереохимически изомерной форме, гдеR3 представляет собой водород или хлоро;R4 представляет собой водород или гидроксиметил;X представляет собой ковалентную связь, О или NR5;R6 представляет собой водород или метил; или его фармацевтически приемлемой соли или сольвату. Обозначение C1-3 алкил в виде группы или части группы означает насыщенный, прямой или раз-2 016969 ветвленный углеводородный радикал, имеющий от 1 до 3 атомов углерода, такой как метил, этил, 1 пропил и 1-метилэтил. Обозначение C1-6 алкил в виде группы или части группы означает насыщенный, прямой или разветвленный углеводородный радикал, имеющий от 1 до 6 атомов углерода, такой как метил, этил, 1 пропил, 1-метилэтил, 1-бутил, 2-метил-1-пропил, 3-метил-1-бутил, 1-пентил, 1-гексил и тому подобное. Обозначение -(СН 2)n в формуле сокращено как Cn. Обозначение С 3-7 циклоалкил означает насыщенный, циклический углеводородный радикал, имеющий от 3 до 7 атомов углерода, такой как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Обозначение галогено или галоген в качестве группы или части группы является общим для фтора,хлора, брома и йода. Для терапевтического использования соли соединений формулы (I) представляют собой соли, где противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут найти применение, например, в получении или очистке фармацевтически приемлемого соединения. Все соли, как фармацевтически приемлемые, так и фармацевтически неприемлемые, включены в рамки настоящего изобретения. Фармацевтически приемлемые соли, как определено, включают терапевтически активные нетоксичные солевые формы присоединения кислоты, которые способны образовывать соединения формулы(I). Указанные соли могут быть получены с помощью обработки основной формы соединений формулы(I) соответствующими кислотами, например неорганическими кислотами, например гидрогалогеновой кислотой, в частности соляной кислотой, бромисто-водородной кислотой, серной кислотой, азотной кислотой и фосфорной кислотой; органическими кислотами, например уксусной кислотой, гидроксиуксусной кислотой, пропионовой кислотой, молочной кислотой, пировиноградной кислотой, щавелевой кислотой, малоновой кислотой, янтарной кислотой, малеиновой кислотой, фумаровой кислотой, яблочной кислотой, винно-каменной кислотой, лимонной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, бензолсульфоновой кислотой, пара-толуолсульфоновой кислотой, цикламиновой кислоты,салициловой кислотой, пара-аминосалициловой кислотой и памовой кислотой. С другой стороны, указанные солевые формы можно превращать в форму нейтрального основания посредством обработки соответствующим основанием. Соединения формулы (I), содержащие кислые протоны, также могут быть превращены в их терапевтически активные нетоксичные формы основных солей посредством обработки соответствующими органическими и неорганическими основаниями. Подходящие формы основных солей включают, например, соли аммония, соли щелочных и щелочно-земельных металлов, в частности соли лития, натрия,калия, магния и кальция, соли органических оснований, например бензатина, N-метил-D-глюкамина,гибрамина, и соли аминокислот, например аргинина и лизина. С другой стороны, указанные солевые формы могут быть превращены в формы свободных кислот посредством обработки соответствующей кислотой. Термин "сольват" включает формы присоединения растворителя, а также их соли, которые способны образовывать соединения формулы (I). Примерами таких форм присоединения растворителя являются, например, гидраты, алкоголяты и тому подобное. Термин "стереохимически изомерные формы" при использовании в данном описании изобретения определяют все возможные изомерные формы, которые могут иметь соединения формулы (I). Если не установлено и не указано иное, химическое название соединений означает смесь всех возможных стереохимически изомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. Изобретение также включает каждую из отдельных изомерных форм соединений формулы (I) и их соли и сольваты, по существу, не содержащие, то есть вместе менее чем с 10%, предпочтительно менее 5%, в частности менее 2% и наиболее предпочтительно менее 1% других изомеров. Таким образом, если соединение формулы (I) обозначено, например, как (R), это означает, что это соединение, по существу, не содержит изомера (S). Стереогенные центры могут иметь R- или Sконфигурацию; заместители на бивалентных циклических (частично) насыщенных радикалах могут иметь или цис-, или транс-конфигурацию. Следуя условным обозначениям номенклатуры CAS, когда в соединении присутствуют два стереогенных центра с известной абсолютной конфигурацией, дескриптор R или S присваивают (на основе правила последовательного старшинства Кана-Ингольда-Прелога) хиральному центру с самым низким порядковым номером, центру отсчета. Конфигурацию второго стереогенного центра обозначают, используя относительные дескрипторы [R,R] или [R,S], где R всегда указывают в качестве центра отсчета и [R,R] указывает центры с одинаковой хиральностью, и [R,S] указывает центры с разной хиральностью. Например, если хиральный центр самым низким порядковым номером в соединении имеет S-конфигурацию и второй центр имеет R-конфигурацию, стереодескриптор следует указать как S[R,S]. Если используют и , положение заместителя с высшим приоритетом на асимметрическом атоме углерода в кольцевой системе, имеющей самый низкий номер кольца, всегда произвольно является-3 016969 положением средней плоскости, определяемой кольцевой системой. Положение заместителя с высшим приоритетом на другом асимметрическом атоме углерода в кольцевой системе (атом водорода в соединениях формулы (I относительно положения заместителя с высшим приоритетом на атоме отсчета обозначают , если он находится на той же стороне средней плоскости, определяемой кольцевой системой, или , если он находится на другой стороне средней плоскости, определяемой кольцевой системой. В рамках данной заявки элемент, в частности, при упоминании в отношении соединения формулы(I) содержит все изотопы и изотопные смеси данного элемента, или имеющиеся в природе, или полученные синтетически, или с распространнностью элементов в природе или в изотопно обогащенной форме. Меченные радиоактивным изотопом соединения формулы (I) могут содержать радиоактивный изотоп,выбранный из группы 3 Н, 11 С, 18F, 122I, 123I, 125I, 131I, 75Br, 76Br, 77Br и 82Br. Предпочтительно радиоактивный изотоп выбран из группы 3 Н, 11C и 18F. Получение. Соединения по изобретению в основном могут быть получены при помощи последовательности стадий, каждая из которых известна специалисту. В частности, соединения могут быть получены согласно следующим методам синтеза. Соединения формулы (I) можно синтезировать в форме рацемических смесей энантиомеров, которые могут быть отделены один от другого, следуя известным в данной области технике методикам разделения. Рацемические соединения формулы (I) могут быть превращены в соответствующие диастереоизомерные солевые формы путем взаимодействия с подходящей хиральной кислотой. Указанные диастереоизомерные солевые формы затем разделяют, например, селективной или фракционной кристаллизацией, и энантиомеры выделяют из них щелочами. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы также могут быть произведены из соответствующих чистых стереохимически изомерных форм соответствующих исходных веществ при условии, что взаимодействие происходит стереоспецифически. А. Получение конечных соединений. Экспериментальная методика 1. Соединения формулы (I) могут быть получены посредством взаимодействия промежуточного соединения формулы (II) с соединением формулы (III) согласно схеме взаимодействия 1, взаимодействия,которое выполняют в подходящем реакционно-инертном растворителе, таком как, например, 1,4 диоксан, или в смеси инертных растворителей, такой как, например, 1,4-диоксан/DMF (диметилформамид), в присутствии подходящего основания, такого как, например, водный NaHCO3 или Na2CO3, комплексного Pd-катализатора, такого как, например, тетракис(трифенилфосфин)палладий(0), нагревания в течение подходящего периода времени, которое обеспечивает завершение взаимодействия или при обычном нагревании, или под действием микроволнового излучения. W представляет собой группу, пригодную для опосредованного Pd сочетания с бороновыми кислотами или бороновыми эфирами, такими как, например, галоген или трифлат, и R5 и R6 могут представлять собой водород или алкил, или могут быть взяты вместе для образования, например, бивалентного радикала формул -СН 2 СН 2-, -СН 2 СН 2 СН 2 или -С(СН 3)2 С(СН 3)2-. В схеме взаимодействия 1 все другие переменные определены, как в формуле (I). Схема взаимодействия 1 Экспериментальная методика 2. Альтернативно, соединения формулы (I), в случае, когда R2 является галогеном, можно получать взаимодействием промежуточного соединения формулы (IV) с N-галосукцинимидным реагентом, таким как, например, N-хлорсукцинимид, N-бромсукцинимид или N-йодосукцинимид, в соответствии со схемой взаимодействия 2. Данное взаимодействие выполняют в подходящем реакционно-инертном и апротонном растворителе, таком как, например, дихлорметан или диметилформамид, перемешивая реакционную смесь при соответствующей температуре и в течение требуемого времени до достижения завершения взаимодействия. В схеме взаимодействия 2 все другие переменные определены, как в формуле (I). Схема взаимодействия 2-4 016969 Такие промежуточные соединения (II)-(IV) могут быть получены согласно схемам взаимодействия 3-21 (см. ниже). Превращения разных функциональных групп, присутствующих в итоговых соединениях или в промежуточных соединениях, в другие функциональные группы согласно формуле (I) могут быть выполнены методами синтеза, хорошо известными специалистам в данной области техники. В. Получение промежуточных соединений Экспериментальная методика 3. Промежуточные соединения формулы (II-а) могут быть получены взаимодействием промежуточного соединения формулы (V) с подходящим галогенирующим агентом, таким как, например, фосфорилбромид, взаимодействием, которое выполняют в подходящем реакционно-инертном растворителе, таком как, например, DMF при умеренно повышенной температуре, такой как, например, 110 С. В схеме взаимодействия 3 все переменные определены, как в формуле (I). Схема взаимодействия 3 Экспериментальная методика 4. Промежуточные соединения формулы (II-b) могут быть получены посредством взаимодействия промежуточного соединения формулы (V) с трифликовым ангидридом (также называемым трифторметансульфоновым ангидридом), взаимодействия, которое осуществляют в подходящем реакционноинертном растворителе, таком как, например, дихлорметан, в присутствии основания, такого как, например, пиридин, при низкой температуре, такой как, например, -78 С. В схеме взаимодействия 4 все переменные определены, как в формуле (I). Схема взаимодействия 4 Экспериментальная методика 5. Промежуточные соединения формулы (V-a), где R2 представляет собой галогено, могут быть получены посредством взаимодействия промежуточного соединения формулы (VI) с N-галосукцинимидным реагентом, таким как N-хлорсукцинимид, N-бромсукцинимид или N-йодосукцинимид, согласно схеме взаимодействия 5. Данное взаимодействие выполняют в подходящем реакционно-инертном и апротонном растворителе, таком как, например, дихлорметан или 1,2-дихлорэтан, перемешивание реакционной смеси при подходящей температуре, обычно при комнатной температуре, в течение времени, необходимого для достижения завершения взаимодействия. В схеме взаимодействия 5 переменная R1 определена,как в формуле (I). Схема взаимодействия 5 Экспериментальная методика 6. Промежуточные соединения формулы (V-b) (где R2=трифторметил, C1-3 алкил или циклопропил) могут быть получены посредством гидрирования промежуточных соединений формулы (VII) в подходящем реакционно-инертном растворителе, таком как, например, этанол, в присутствии катализатора, такого как, например, 10% палладий на активированном угле, в течение периода времени, который обеспечивает завершение взаимодействия, обычно при комнатной температуре и давлении водорода 1 атмосфера Экспериментальная методика 7. Промежуточные соединения формулы (VI) могут быть получены гидрогенолизом промежуточных соединений формулы (VIII) в подходящем реакционно-инертном растворителе, таком как, например,этанол, в присутствии катализатора, такого как, например, 10% палладий на активированном угле, в течение периода времени, который обеспечивает завершение взаимодействия, обычно при комнатной тем-5 016969 пературе и давлении водорода 1 атм (0,1 МПа) в течение 2 ч. В схеме взаимодействия 7 переменная R1 определена, как в формуле (I). Схема взаимодействия 7 Экспериментальная методика 8. Промежуточные соединения формулы (VIII) могут быть получены известными в данной области техники способами взаимодействия имеющегося в продаже 4-бензилокси-1H-пиридин-2-она с имеющимся в продаже алкилирующим агентом формулы (IX), где Z представляет собой подходящую уходящую группу, используя основание, такое как, например, K2CO3, и, возможно, соль йода, например KI, в инертном растворителе, таком как, например, ацетонитрил или DMF, при умеренно высокой температуре, такой как, например, 80-120 С, в течение подходящего периода времени, которое обеспечивает завершение взаимодействия, например 16 ч. В схеме взаимодействия 8 переменная R1 определена, как в формуле (I), и Z представляет собой подходящую уходящую группу, такую как, например, галоген. Схема взаимодействия 8 Экспериментальная методика 9. Промежуточные соединения формулы (VII-a) могут быть получены взаимодействием промежуточного соединения формулы (X) с имеющимся в продаже N-галогеносукцинимидом, таким как N-хлор(NCS), N-бром-(NBS) или N-йодосукцинимид (NIS), в подходящем реакционно-инертном растворителе,таком как, например, DMF, дихлорметан или уксусная кислота, обычно при комнатной температуре в течение 1-24 ч. В схеме взаимодействия 9 переменная R1 определена, как в формуле (I). Схема взаимодействия 9 Экспериментальная методика 10. Промежуточные соединения формулы (VII-b) могут быть получены взаимодействием промежуточного соединения формулы (VII-a), где галогено представляет собой йод, с имеющимся в продаже метил 2,2-дифтор-2-(фторсульфонил)ацетатом в подходящем реакционно-инертном растворителе, таком как,например, DMF, в присутствии подходящей соли меди, такой как иодид меди(I), при нагревании в течение подходящего периода времени, который обеспечивает завершение взаимодействия, например, при 100 С в течение 5 ч. В схеме взаимодействия 10 переменная R1 определена, как в формуле (I). Схема взаимодействия 10 Экспериментальная методика 11. Промежуточные соединения формулы (VII-c) могут быть получены взаимодействием промежуточного соединения формулы (VII-a) с производным C1-3 алкил- или циклопропилбороновой кислоты, такой как, например, циклопропилбороновая кислота или метилбороновая кислота, в подходящем реакционноинертном растворителе, таком как, например, 1,4-диоксан, в присутствии подходящего комплекса палладиевого катализатора, такого как, например, [1,1'-бис-(дифенилфосфино)ферроцен]дихлорпалладий(II)комплекс DCM, и в присутствии подходящего основания, такого как NaHCO3, при нагревании в течение подходящего периода времени, который обеспечивает завершение взаимодействия, например, при 175 С в течение 20 мин под действием микроволнового излучения. В схеме взаимодействия 11 переменная R1 определена, как в формуле (I). Схема взаимодействия 11-6 016969 Экспериментальная методика 12. Промежуточные соединения формулы (III) могут быть получены известными в данной области техники способами посредством взаимодействия промежуточного соединения формулы (XI) с подходящим источником бора, таким как, например, бис-(пинаколато)дибор, в присутствии палладиевого катализатора, такого как, например, 1,1'-бис-(дифенилфосфино)ферроценпалладий(II)дихлорид, в инертном растворителе, таком как, например, дихлорметан, в присутствии подходящей соли, такой как, например, ацетат калия, при умеренно высокой температуре, такой как, например, 110 С, в течение, например, 16 ч. Кроме того, промежуточные соединения формулы (III) могут быть получены известными в данной области техники методами замены металл-галоген и последующего взаимодействия с подходящим источником бора из промежуточных соединений формулы (XI). Таким образом, например, взаимодействие промежуточного соединения формулы (XI) с литийорганическим соединением, таким как, например, нбутиллитий, при умеренно низкой температуре, такой как, например, -40 С, в инертном растворителе,таком как, например, THF, с последующим взаимодействием с подходящим источником бора, таким как,например, триметоксиборан. В схеме взаимодействия 12 все переменные определены, как в формуле (I),и R5 и R6 могут представлять собой водород или алкил, или могут быть взяты вместе с образованием,например, бивалентного радикала формул -СН 2 СН 2-, -СН 2 СН 2 СН 2- или -С(СН 3)2 С(СН 3)2-. Схема взаимодействия 12 Экспериментальная методика 13. Кроме того, промежуточные соединения формулы (III-а) могут быть получены взаимодействием имеющегося в продаже промежуточного соединения формулы (XII) с производным циклического кетона формулы (XIII) в условиях восстановительного аминирования, которые известны специалистам в данной области техники, например в присутствии триацетоксиборгидрида в подходящем реакционно-инертном растворителе, таком как, например, 1,2-дихлорэтан, при подходящей температуре, обычно комнатной температуре, в течение подходящего периода времени, который обеспечивает завершение взаимодействия. Схема взаимодействия 13 Экспериментальная методика 14. Промежуточные соединения формулы (IV) могут быть получены взаимодействием промежуточного соединения формулы (II-а), где R2=Н, с промежуточным соединением формулы (III) в соответствии со схемой взаимодействия 14. Данное взаимодействие может быть выполнено в подходящем реакционноинертном растворителе, таком как, например, 1,4-диоксан, или в смеси инертных растворителей, такой как, например, 1,4-диоксан/DMF. Взаимодействие может быть выполнено в присутствии подходящего основания, такого как, например, водный NaHCO3 или Na2CO3, комплексного Pd-катализатора, такого как, например, тетракис(трифенилфосфин)палладий(0), при нагревании в течение подходящего периода времени, который обеспечивает завершение взаимодействия либо при обычном нагревании, либо под действием микроволнового излучения. В схеме взаимодействия 14 все переменные определены, как в формуле (I). W представляет собой группу, подходящую для Pd-опосредованного сочетания с бороновыми кислотами или бороновыми эфирами, такими как, например, галоген или трифлат, и R5 и R6 могут представлять собой водород или алкил или могут быть взяты вместе с образованием, например, бивалентного радикала формул -СН 2 СН 2-, -СН 2 СН 2 СН 2- или -С(СН 3)2 С(СН 3)2-. Схема взаимодействия 14 Экспериментальная методика 15. Промежуточные соединения формулы (XI-a) могут быть получены известными в данной области техники методами посредством взаимодействия анилинового промежуточного соединения формулы(XIV-а) с циклическим кетонным производным формулы (XIII) в условиях восстановительного аминирования, известных специалистам в данной области техники, например в присутствии триацетоксиборгидрида в подходящем реакционно-инертном растворителе, таком как, например, 1,2-дихлорэтан, при подходящей температуре, обычно при комнатной температуре, в течение подходящего периода времени,который обеспечивает завершение взаимодействия. В схеме взаимодействия 15 все переменные опреде-7 016969 лены, как в формуле (I), и галогено- может представлять собой хлор-, бром- или йод-. Схема взаимодействия 15 Экспериментальная методика 16. Промежуточные соединения формулы (XI-b) могут быть получены известными в данной области техники методами посредством взаимодействия фенольного промежуточного соединения формулы(XIV-b) с циклическим спиртом формулы (XV) в присутствии фосфина, такого как, например, трифенилфосфин, и подходящего агента сочетания для сочетаний типа Мицунобу, такого как, например, дитрет-бутилазадикарбоксилат, в инертном растворителе, таком как, например, дихлорметан, при умеренно низкой температуре, такой как, например, 25 С, в течение, например, 2 ч. В схеме взаимодействия 16 все переменные определены, как в формуле (I), и галогено- может представлять собой хлор-, бром- или йод-. Схема взаимодействия 16 Экспериментальная методика 17. Кроме того, промежуточные соединения формулы (XI-c) могут быть получены известными в данной области техники методами посредством замены металл-галоген из промежуточных соединений формулы (XIV-c) и последующего взаимодействия с циклическим кетоном формулы (XIII). Таким образом,например, взаимодействие промежуточного соединения формулы (XI-c) с органолитиевым соединением,таким как, например, н-бутиллитий, при умеренно низкой температуре, такой как, например, -40 С, в инертном растворителе, таком как, например, THF, с последующим взаимодействием с тетрагидро-4 Нпиран-4-оном. В схеме взаимодействия 17 все переменные определены, как в формуле (I), и галогеноможет представлять собой хлор-, бром- или йод-. Схема взаимодействия 17 Экспериментальная методика 18. Кроме того, промежуточные соединения формулы (XI-d) могут быть получены известными в данной области техники методами в двухстадийной последовательности, состоящей из реакции дегиратации с последующей реакцией гидрирования, из промежуточных соединений формулы (XI-c). Таким образом,например, взаимодействие промежуточного соединения формулы (XI-с) с кислотой, такой как, например,моногидрат пара-толуолсульфоновой кислоты, при умеренно высокой температуре, такой как, например,100 С, в инертном растворителе, таком как, например, толуол, в течение, например, 2 ч, с получением промежуточного соединения формулы (XI-e). Затем данное промежуточное соединение можно гидрировать в присутствии каталитического количества подходящего катализатора, такого как, например, оксид платины, в растворителе, таком как, например, этанол, с получением промежуточного соединения (XI-d). В схеме взаимодействия 18 галогено- может представлять собой хлор-, бром- или йод-. Все другие переменные определены, как в формуле (I). Схема взаимодействия 18 Экспериментальная методика 19. Кроме того, промежуточные соединения формулы (XI-f) могут быть получены известными в данной области техники методами из имеющихся в продаже или синтетически доступных алкилэфирных производных (4-галогенофенил)уксусной кислоты в двухстадийной последовательности, состоящей из реакции алкилирования с соответствующим дигалогенпроизводным с последующим восстановлением эфирной функциональной группы до спирта. Таким образом, например, в результате взаимодействия с 2 хлорэтиловым эфиром в присутствии основания, такого как гидрид натрия, в инертном растворителе,таком как DMF, при подходящей температуре и в течение периода времени, необходимого для обеспечения завершения взаимодействия, обычно при комнатной температуре в течение 10-16 ч, получают промежуточное соединение формулы (XI-g). Затем данное промежуточное соединение можно привести во взаимодействие с металлическим восстановителем, таким как, например, алюмогидрид лития, в инертном растворителе, таком как тетрагидрофуран, при подходящей температуре и в течение периода време-8 016969 ни, необходимого для обеспечения завершения взаимодействия, обычно от -10 С до комнатной температуры в течение 2 ч, с получением промежуточного соединения формулы (XI-f). В схеме взаимодействия 19 все переменные определены, как в формуле (I), и галогено- может представлять собой хлор-, бромили йод-. Схема взаимодействия 19 Экспериментальная методика 20. Кроме того, промежуточные соединения формулы (XI) могут быть получены известными в данной области техники методами из анилин-подобных промежуточных соединений формулы (XVI) посредством реакции типа Зандмейера. В схеме взаимодействия 20 все переменные определены, как в формуле(I), и галогено- может представлять собой хлор-, бром- или йод-. Схема взаимодействия 20 Экспериментальная методика 21. Промежуточные соединения формулы (XVI) могут быть получены известными в данной области техники методами из промежуточных соединений формулы (XVII) путем восстановления нитрогруппы до аминогруппы известными в данной области техники способами, такими как каталитическое гидрирование или использование двуводного хлорида олова(II) в качестве восстановителя. В схеме взаимодействия 21 все переменные определены, как в формуле (I). Схема взаимодействия 21 Экспериментальная методика 22. Промежуточные соединения формулы (XVII) могут быть получены известными в данной области техники методами взаимодействия промежуточного соединения формулы (XVIII) с подходящим промежуточным соединением формулы (XIX) в присутствии подходящего основания, такого как, например,карбонат цезия, в инертном растворителе, таком как, например, диметилформамид или ацетонитрил, при подходящей температуре и в течение подходящего периода времени для обеспечения завершения взаимодействия. В схеме взаимодействия 22 все переменные определены, как в формуле (I). Схема взаимодействия 22 Исходные вещества формул (IX), (XIII), (XIV-а, -b и -с), (XV), (XVIII) и (XIX) представляют собой промежуточные соединения, которые или имеются в продаже или могут быть получены в соответствии с обычно используемыми методиками взаимодействия, хорошо известными любому специалисту в данной области техники. Фармакология. Соединения, предложенные в данном изобретении, представляют собой положительные аллостерические модуляторы метаботропных глутаматных рецепторов, в частности они представляют собой положительные аллостерические модуляторы mGluR2. Соединения по настоящему изобретению, как оказалось, не связываются с сайтом узнавания глутамата, сайтом ортостерического лиганда, но вместо этого связываются с аллостерическим сайтом в рамках семитрансмембранной области рецептора. В присутствии глутамата или агониста mGluR2 соединения по данному изобретению усиливают ответ mGluR2. Предполагается, что соединения, предложенные в данном изобретении, оказывают эффект на mGluR2 благодаря своей способности повышать ответ таких рецепторов на глутамат или агонисты mGluR2, усиливая ответ рецептора. Таким образом, настоящее изобретение относится к соединениям по настоящему изобретению для применения в качестве лекарственного средства, а также к применению соединения по изобретению или фармацевтической композиции по изобретению для изготовления лекарственного средства для лечения или предупреждения, в частности лечения, состояния млекопитающего, включая человека, лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом аллостерических модуляторов mGluR2, в частности его положительных аллостерических модуляторов. Настоящее изобретение также относится к соединению по настоящему изобретению-9 016969 или к фармацевтической композиции по изобретению для применения в изготовлении лекарственного средства для лечения или предупреждения, в частности лечения, состояния млекопитающего, включая человека, лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом аллостерических модуляторов mGluR2, в частности его положительных аллостерических модуляторов. Настоящее изобретение также относится к соединению по настоящему изобретению или к фармацевтической композиции по изобретению для лечения или предупреждения, в частности лечения, состояния млекопитающего, включая человека, лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом аллостерических модуляторов mGluR2, в частности его положительных аллостерических модуляторов. Кроме того, настоящее изобретение относится к применению соединения по изобретению или фармацевтической композиции по изобретению для изготовления лекарственного средства для лечения,предупреждения, улучшения, управления или снижения риска различных неврологических и психиатрических расстройств, связанных с глутаматной дисфункцией у млекопитающего, включая человека, лечение или предупреждение которых находится под влиянием или облегчается нейромодуляторным эффектом положительных аллостерических модуляторов mGluR2. Если говорится, что изобретение относится к применению соединения или композиции по изобретению для изготовления лекарственного средства, например для лечения млекопитающего, следует понимать, что такое применение следует интерпретировать в некоторых сферах как способ, например, лечения млекопитающего, включающий введение млекопитающему, нуждающемуся в таком, например,лечении, эффективного количества соединения или композиции по изобретению. В частности, неврологические и психиатрические расстройства, связанные с глутаматной дисфункцией, включают одно или более из следующих состояний или заболеваний: острые неврологические и психиатрические расстройства, такие как, например, церебральные недостаточности после операции коронарного шунтирования и имплантации, инсульт, церебральная ишемия, травма спинного мозга, травма головы, перинатальная гипоксия, остановка сердца, гипогликемическое нейронное повреждение, деменция (включая деменцию, вызванную СПИД), болезнь Альцгеймера, хорея Гентингтона, боковой амилотрофический склероз, повреждение зрения, ретинопатия, когнитивные расстройства, идиопатическая и вызванная лекарственным средством болезнь Паркинсона, мышечные судороги и расстройства, связанные с мышечной спастичностью, включая треморы, эпилепсию, судороги, мигрень (включая головную боль, связанную с мигренью), недержание мочи, толерантность к веществам, синдром отмены веществ(включая вещества, такие как, например, опиаты, никотин, табачные продукты, алкоголь, бензодиазепины, кокаин, седативные вещества, снотворные средства и так далее), психоз, шизофрения, тревога (включая генерализованное тревожное расстройство, паническое расстройство и обсессивно-компульсивное расстройство), расстройства настроения (включая депрессию, мании, биполярные расстройства), невралгия тройничного нерва, потеря слуха, шум в ушах, дистрофия желтого ядра глаза, рвота, отек мозга, боль(включая острые и хронические состояния, сильную боль, неустранимую боль, невропатическую боль и посттравматическую боль), поздняя дискинезия, расстройства сна (включая нарколепсию), синдром дефицита внимания и гиперактивности, расстройство поведения. В частности, состояние или заболевание представляет собой расстройство центральной нервной системы, выбранное из группы тревожных расстройств, психотических расстройств, личностных расстройств, расстройств, связанных с веществами, расстройств питания, расстройств настроения, мигрени,эпилепсии или конвульсивных расстройств, детских расстройств, когнитивных расстройств, нейродегенерации, нейротоксичности и ишемии. Предпочтительно расстройство центральной нервной системы представляет собой тревожное расстройство, выбранное из группы: агорафобия, генерализованное тревожное расстройство (GAD), обсессивно-компульсивное расстройство (OCD), паническое расстройство, посттравматическое стрессовое расстройство (PTSD), социальная фобия и другие фобии. Предпочтительно расстройство центральной нервной системы представляет собой психотическое расстройство, выбранное из группы: шизофрения, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство и психотическое расстройство, вызванное веществом. Предпочтительно расстройство центральной нервной системы представляет собой личностное расстройство, выбранное из группы: обсессивно-компульсивное личностное расстройство и шизоидное, шизотипическое расстройство. Предпочтительно расстройство центральной нервной системы представляет собой расстройство,связанное с веществом, выбранное из группы: злоупотребление алкоголем, алкогольная зависимость,алкогольная абстиненция, алкогольный абстинентный делирий, психотическое расстройство, вызванное алкоголем, амфетаминовая зависимость, амфетаминовая абстиненция, кокаиновая зависимость, кокаиновая абстиненция, никотиновая зависимость, никотиновая абстиненция, опиоидная зависимость и опиоидная абстиненция. Предпочтительно расстройство центральной нервной системы представляет собой расстройство питания, выбранное из группы нейрогенной анорексии и нейрогенной булимии. Предпочтительно расстройство центральной нервной системы представляет собой расстройство на- 10016969 строения, выбранное из группы: биполярные расстройства (I и II), циклотимическое расстройство, депрессия, дистимическое расстройство, большое депрессивное расстройство и расстройство настроения,вызванное веществом. Предпочтительно расстройство центральной нервной системы представляет собой мигрень. Предпочтительно расстройство центральной нервной системы представляет собой эпилепсию или конвульсивное расстройство, выбранное из группы: генерализованная неконвульсивная эпилепсия, генерализованная конвульсивная эпилепсия, малый эпилептический припадок, большой эпилептический припадок, парциальная эпилепсия с нарушением сознания или без нарушения сознания, младенческие судороги, непрерывная парциальная эпилепсия и другие формы эпилепсии. Предпочтительно расстройство центральной нервной системы представляет собой синдром дефицита внимания/гиперактивности. Предпочтительно расстройство центральной нервной системы представляет собой когнитивное расстройство, выбранное из группы: делирий, персистирующий делирий, вызванный веществом, деменция, деменция вследствие ВИЧ-заболевания, деменция вследствие болезни Гентингтона, деменция вследствие болезни Паркинсона, деменция альцгеймеровского типа, персистирующая деменция, вызванная веществом, и легкое когнитивное нарушение. Из расстройств, перечисленных выше, лечение тревоги, шизофрении, мигрени, депрессии и эпилепсии является особенно важным. В настоящее время в четвертом издании DiagnosticStatistical Manual of Mental Disorders (DSMIV) Американской Психиатрической Ассоциации предложено диагностическое средство для идентификации расстройств, описанных в данном описании изобретения. Специалистам в данной области техники понятно, что существуют альтернативные варианты номенклатуры, нозологии и системы классификации неврологических и психиатрических расстройств, описанных в данном описании изобретения, и что они развиваются вместе с медицинским и научным прогрессом. Так как такие положительные аллостерические модуляторы mGluR2, включающие соединения формулы (I), усиливают ответ mGluR2 на глутамат, преимущество состоит в том, что настоящие способы используют эндогенный глутамат. Так как положительные аллостерические модуляторы mGluR2, включающие соединения формулы(I), усиливают ответ mGluR2 на агонисты, понятно, что настоящее изобретение распространяется на лечение неврологических и психиатрических расстройств, связанных с глутаматной дисфункцией, путем введения эффективного количества положительного аллостерического модулятора mGluR2, включающего соединения формулы (I), в комбинации с агонистом mGluR2. Соединения по настоящему изобретению можно использовать в комбинации с одним или более другими лекарственными средствами в лечении, предупреждении, управлении, смягчении или снижении риска заболеваний или состояний, для которых соединения формулы (I) или другие лекарственные средства могут быть полезны, когда комбинация лекарственных средств, взятых вместе, является более безопасной или более эффективной, чем любое из этих лекарственных средств поодиночке. Фармацевтические композиции. Изобретение также относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель или разбавитель и в качестве активного ингредиента терапевтически эффективное количество соединения по изобретению, в частности соединения формулы (I), его фармацевтически приемлемой соли, его сольвата или его стереохимически изомерной формы. Соединения по изобретению, в частности соединения формулы (I), их фармацевтически приемлемые соли, их сольваты и стереохимически изомерные формы, или любая их подгруппа или комбинация могут быть приготовлены в виде препарата в различных фармацевтических формах с целью введения. В качестве подходящих композиций здесь можно упомянуть все композиции, обычно используемые для системно вводимых лекарственных средств. Для получения фармацевтических композиций по данному изобретению эффективное количество конкретного соединения, возможно в форме соли, в качестве активного ингредиента объединяют в однородную смесь с фармацевтически приемлемым носителем или разбавителем, причем носитель или разбавитель может принимать большое разнообразие форм в зависимости от формы препарата, требующегося для введения. Эти фармацевтические композиции желательно находятся в единичной лекарственной форме, пригодной, в частности, для введения перорально, ректально, чрескожно, посредством парентеральной инъекции или ингаляции. Например, при получении композиций в пероральной лекарственной форме можно использовать любую из обычных фармацевтических сред, таких как, например, вода, гликоли, масла, спирты и тому подобное в случае пероральных жидких препаратов, таких как, например,суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как, например, крахмалы, сахара, каолин, разбавители, смазывающие вещества, связывающие вещества, разрыхлители и тому подобное в случае порошков, драже, капсул и таблеток. Из-за легкости введения предпочтительным является пероральное введение, и таблетки и капсулы представляют собой наиболее полезные пероральные стандартные лекарственные формы, в этом случае, очевидно, используют твердые фармацевтические носители. Для парентеральных композиций носитель обычно содержит стерильную воду, по меньшей- 11016969 мере, в значительной части, однако могут быть включены другие ингредиенты, например, способствующие растворимости. Например, могут быть получены инъецируемые растворы, в которых носитель содержит солевой раствор, раствор глюкозы или смесь солевого и глюкозного растворов. Также могут быть получены инъецируемые суспензии, при этом могут быть использованы подходящие жидкие носители,суспендирующие агенты и тому подобное. Кроме того, включены препараты в твердой форме, которые предназначены для превращения, незадолго до использования, в препараты в жидкой форме. В композициях, подходящих для чрескожного введения, носитель возможно содержит усиливающий проникновение агент и/или подходящий смачивающий агент, возможно объединенный с подходящими вспомогательными веществами любой природы в минимальных соотношениях, которые не оказывают выраженного вредного воздействия на кожу. Указанные вспомогательные вещества могут облегчать введение на кожу и/или могут быть полезны для приготовления желательных композиций. Данные композиции можно вводить различными путями, например в виде трансдермального пластыря, в виде препарата для нанесения на кожу, в виде мази. Особенно полезно приготовление вышеуказанных фармацевтических композиций в стандартной лекарственной форме для легкого введения и равномерности дозирования. Стандартная лекарственная форма при использовании в данном описании изобретения относится к физически дискретным единицам,пригодным в качестве единичных дозировок, где каждая единица содержит заранее определенное количество активного ингредиента, рассчитанное для получения нужного терапевтического эффекта, в сочетании с требующимся фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с риской или покрытые оболочкой таблетки), капсулы, драже, пакетики с порошком, облатки, суппозитории, инъецируемые растворы или суспензии и тому подобное и их отдельные составные части. Точная дозировка и частота введения зависят от конкретного используемого соединения формулы(I), конкретного состояния, подлежащего лечению, тяжести состояния, подлежащего лечению, возраста,массы, пола, степени расстройства и общего физического состояния конкретного пациента, а также другого лечения, которое может принимать индивидуум, как хорошо известно специалистам в данной области техники. Кроме того, очевидно, что указанное эффективное суточное количество может быть уменьшено или увеличено в зависимости от ответа получающего лечение субъекта, и/или в зависимости от заключения терапевта, прописывающего соединения по настоящему изобретению. В зависимости от способа введения фармацевтическая композиция содержит от 0,05 до 99 мас.%,предпочтительно от 0,1 до 70 мас.%, более предпочтительно от 0,1 до 50 мас.% активного ингредиента и от 1 до 99,95 мас.%, предпочтительно от 30 до 99,9 мас.%, более предпочтительно от 50 до 99,9 мас.% фармацевтически приемлемого носителя, все процентные содержания основаны на общей массе композиции. Как уже отмечалось, данное изобретение также относится к фармацевтической композиции, содержащей соединения по изобретению и одно или более чем одно другое лекарственное средство, в лечении, предупреждении, контроле, смягчении или снижении риска заболеваний или состояний, для которых могут быть полезны соединения формулы (I) или другие лекарственные средства, а также к использованию такой композиции для изготовления лекарственного средства. Настоящее изобретение также относится к комбинации соединения по настоящему изобретению и ортостерического агониста mGluR2. Настоящее изобретение также относится к такой комбинации для использования в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение по настоящему изобретению, его фармацевтически приемлемую соль или его сольват, и (б) ортостерический агонист mGluR2 в виде комбинированного препарата для одновременного, раздельного или последовательного применения в лечении или предупреждении состояния млекопитающего, включая человека,лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом аллостерических модуляторов mGluR2, в частности положительных аллостерических модуляторов mGluR2. Разные лекарственные средства такой комбинации или продукта могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями или разбавителями, или каждый из них может присутствовать в отдельном препарате вместе с фармацевтически приемлемыми носителями или разбавителями. Следующие примеры предназначают для иллюстрации, но не для ограничения объема настоящего изобретения. Химия. Некоторые способы получения соединений по данному изобретению проиллюстрированы в следующих примерах. Если не указано иное, все исходные вещества были получены от торговых поставщиков и использовались без дополнительной очистки. Ниже в данном описании изобретения "THF" означает тетрагидрофуран; "DMF" означает N,Nдиметилформамид; "EtOAc" означает этилацетат; "DCM" означает дихлорметан; "DME" означает 1,2 диметоксиэтан; "DCE" означает 1,2-дихлорэтан; "DIPE" означает диизопропиловый эфир; "DMSO" означает диметилсульфоксид; "DBU" означает 1,8-диаза-7-бицикло[5.4.0]ундецен. Реакции под действием микроволн выполняли в однорежимном реакторе: микроволновом реакторе К раствору 4-бензилокси-7H-пиридин-2-она (5,0 г, 24,84 ммоль) в ацетонитриле (200 мл) добавляли 1-бромбутан (3,75 г, 27,33 ммоль) и карбонат калия (10,3 г, 74,52 ммоль) и смесь нагревали при температуре дефлегмации в течение 16 ч. Реакционную смесь фильтровали через диатомитовую землю и концентрировали в вакууме. Неочищенный остаток затем растирали с диэтиловым эфиром с получением чистого D1 (6,26 г, 98%) в виде белого твердого вещества. Описание 2. 1-Бутил-4-гидрокси-1H-пиридин-2-он (D2) Смесь промежуточного соединения D1 (2,01 г, 7,83 ммоль) и каталитического количества 10%-ного палладия на активированном угле в этаноле (300 мл) перемешивали в атмосфере водорода в течение 2 ч. Смесь фильтровали через диатомитовую землю и растворитель выпаривали в вакууме с получением промежуточного соединения D2 (1,3 г, 100%), которое использовали без дополнительной очистки. Описание 3. 4-Бром-1-бутил-1H-пиридин-2-он (D3) К раствору промежуточного соединения D2 (1,44 г, 8,6 ммоль) в DMF (140 мл) добавляли бромокись фосфора (5,4 г, 18,9 ммоль) и смесь нагревали при 110 С в течение 1 ч. После охлаждения на ледяной бане раствор распределяли между водой и EtOAc. После трех экстракций EtOAc объединенные органические фракции сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный продукт очищали колоночной хроматографией (силикагель; DCM в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением промежуточного соединения D3 (1,82 г, 93%). Описание 4. 4-Бром-1-(3-метилбутил)-1H-пиридин-2-он (D4)D3, используя 4-гидрокси-1-(3-метилбутил)-1 Н-пиридин-2-он в качестве исходного вещества, которое получали способом, аналогичным использованному для синтеза промежуточного соединения D2, посредством взаимодействия 4-бензилокси-1H-пиридин-2-она с 1-бром-3-метилбутаном. Описание 5. 1-Бутил-3-хлор-4-гидрокси-1H-пиридин-2-он (D5) К раствору промежуточного соединения D2 (2,0 г, 11,96 ммоль) в DMF (30 мл) добавляли Nхлорсукцинимид (1,6 г, 11,96 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи и затем концентрировали в вакууме. Неочищенный продукт очищали колоночной хроматографией (силикагель; 0-5% метанол/DCM в качестве элюента) с получением промежуточного соединенияD5 (2,0 г, 83%). Описание 6. 1-Бутил-3-хлор-2-оксо-1,2-дигидропиридин-4-иловый эфир трифторметансульфоновой кислоты (D6) К раствору промежуточного соединения D5 (2,0 г, 9,92 ммоль) в DCM (80 мл), охлажденному при-78 С, добавляли пиридин (1,60 мл, 19,8 ммоль). Полученный раствор перемешивали в течение 10 мин,- 13016969 после чего добавляли ангидрид трифторметансульфоновой кислоты (1,90 мл, 10,9 ммоль) и полученный раствор перемешивали при -78 С в течение 3 ч. Затем смесь нагревали до комнатной температуры и гасили ее добавлением водного насыщенного хлорида аммония, разбавляли ее водой и экстрагировалиDCM, сушили (Na2SO4) и растворитель выпаривали в вакууме, получая промежуточное соединение D6(3,31 г, 100%) в виде неочищенного продукта, который использовали без дополнительной очистки. Описание 7. (Тетрагидрофуран-4-ил)-[4-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)фенил]амин Смесь 4-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)фениламина (0,5 г, 2,28 ммоль), тетрагидрофуран-4-она (0,25 мл, 2,73 ммоль) и триацетоксиборгидрида натрия (0,71 г, 3,42 ммоль) в DCE (50 мл) перемешивали при комнатной температуре в течение 16 ч. Неочищенный продукт фильтровали через диатомитовую землю, промывали DCM и фильтрат упаривали в вакууме с получением D7 (0,69 г), который использовали без дополнительной очистки. Описание 8. 1-(3-Метилбутил)-4-[4-(тетрагидрофуран-4-иламино)фенил]-1H-пиридин-2-он (D8) Суспензию промежуточного соединения D4 (0,46 г, 1,9 ммоль), промежуточного соединения D7(0,69 г, 2,28 ммоль) и тетракис(трифенилфосфин)палладия(0) (0,21 г, 0,19 ммоль) в смеси диоксана (4 мл) и насыщенного водного карбоната натрия (4 мл) нагревали при 150 С в течение 10 мин под действием микроволнового излучения. Неочищенный продукт фильтровали через диатомитовую землю и промывали EtOAc. Органический слой отделяли и промывали рассолом, сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный продукт очищали колоночной хроматографией (силикагель;DCM/EtOAc 8:2 и в заключение EtOAc в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением D8 (0,64 г, 95%) в виде желтого твердого вещества. Описание 9. Метиловый эфир 4-(4-бромфенил)тетрагидрофуран-4-карбоновой кислоты (D9) К перемешиваемому раствору метилового эфира (4-бромфенил)уксусной кислоты (12,52 г, 54,6 ммоль) и 15-краун-5 (1,2 г, 5,46 ммоль) в DMF (100 мл) при комнатной температуре порциями добавлялиNaH (60%) (4,74 г, 119 ммоль). После перемешивания при комнатной температуре в течение 40 мин добавляли NaI (8,14 г, 54,6 ммоль) и 2-хлорэтиловый эфир (13,76 г, 96,2 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 10 ч, после чего растворитель выпаривали в вакууме. Остаток обрабатывали смесью EtOAc и толуола (1:1) и промывали раствором 0,5 н. HCl. Водный слой затем экстрагировали дополнительным EtOAc/толуол (1:1) и объединенные органические экстракты промывали водой, затем водным насыщенным раствором NaHCO3 и в заключение рассолом. Объединенные органические экстракты сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный остаток растирали с н-гептаном и растворимую фракцию выпаривали досуха при пониженном давлении с получением D9 (3,96 г, 24%) в виде желтой жидкости. Описание 10. [4-(4-Бромфенил)тетрагидрофуран-4-ил]метанол (D10) К раствору промежуточного соединения D9 (1,07 г, 3,58 ммоль) в THF (20 мл), перемешиваемому при -10 С в атмосфере N2, добавляли по каплям 1,0 М раствор алюмогидрида лития в THF (3,58 мл, 3,58 ммоль). Полученный раствор постепенно нагревали до комнатной температуры и дополнительно перемешивали в течение 2 ч. После охлаждения до 0 С осторожно добавляли 10% водный раствор NaOH и полученную смесь оставляли достигать комнатной температуры. Затем ее экстрагировали DCM, сушили(Na2SO4) и растворитель выпаривали в вакууме с получением промежуточного соединения D10 (0,96 г,99%) в виде белого твердого вещества, которое использовали без дополнительной очистки. 4-[4-(4,4,5,5-Тетраметил-[1,3,2]диоксаборолан-2-ил)фенил]тетрагидрофуран-4 К раствору промежуточного соединения D10 (0,96 г, 3,53 ммоль) в диоксане (12 мл) и DMF (3 мл) добавляли бис-(пинаколато)дибор (1,43 г, 5,65 ммоль) и ацетат калия (1,04 г, 10,59 ммоль). Смесь дегазировали и затем добавляли [1,1'-бис-(дифенилфосфино)ферроцен]дихлорпалладий(II) комплекс с DCM(1:1) (0,09 г, 0,106 ммоль). Реакционную смесь нагревали при 150 С в течение 40 мин под действием микроволнового излучения. После охлаждения до комнатной температуры добавляли воду и смесь экстрагировали EtOAc. Органическую фракцию сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный остаток очищали колоночной хроматографией (силикагель; DCM в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением маслянистого остатка, который растирали с н-гептаном с получением D11 (0,65 г, 58%) в виде белого твердого вещества. Описание 12. 4-(Тетрагидрофуран-2-илоксиметил)-4-[4-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2 ил)фенил]тетрагидрофуран (D12) Смесь промежуточного соединения D11 (0,58 г, 1,8 ммоль), 3,4-дигидро-2 Н-пирана (0,2 мл, 2,18 ммоль) и пара-толуолсульфоновой кислоты (каталитическое количество) в сухом DCM (20 мл) перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь затем промывали водным насыщенным раствором NaHCO3, объединенные органические экстракты сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный остаток очищали колоночной хроматографией (силикагель; DCM в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением D12 (0,73 г, 100%),который использовали без дополнительной очистки. Пример 1. 3-Хлор-1-(3-метилбутил)-4-[4-(тетрагидрофуран-4-иламино)фенил]-1H-пиридин-2-он Раствор промежуточного соединения D8 (0,65 г, 1,91 ммоль) и N-хлорсукцинимида (0,25 г, 1,91 ммоль) в DMF (10 мл) перемешивали при 45 С в течение 16 ч. После охлаждения до комнатной температуры добавляли воду и раствор экстрагировали EtOAc, органический слой отделяли и промывали рассолом, сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный продукт очищали колоночной хроматографией (силикагель; DCM/EtOAc 8:2 в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением Е 1 (0,20 г, 28%) в виде светло-розового твердого вещества. Точка плавления:300 С. Пример 2. 1-Бутил-3-хлор-4-4-[4-(тетрагидропиран-2-илоксиметил)тетрагидропиран-4-ил]фенил 1H-пиридин-2-он (Е 2) Смесь промежуточного соединения D6 (0,17 г, 0,5 ммоль), промежуточного соединения D12 (0,2 г,0,5 ммоль), катализатора тетракис(трифенилфосфин)палладия(0) (0,03 г, 0,025 ммоль) и NaHCO3 (3 г,избыток) в диоксане (6 мл) нагревали при 150 С в течение 10 мин под действием микроволнового излучения. После охлаждения до комнатной температуры реакционную смесь фильтровали через диатомитовую землю, обрабатывали EtOAc и органический слой промывали водой и затем рассолом. Органическую фракцию сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный остаток очищали- 15016969 колоночной хроматографией (силикагель; 0-10% EtOAc/DCM в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением Е 2 (0,10 г, 45%) в виде бесцветного масла. Пример 3. 1-Бутил-3-хлор-4-[4-(4-гидроксиметилтетрагидрофуран-4-ил)фенил]-1H-пиридин-2-он Смесь соединения Е 2 (0,10 г, 0,22 ммоль) и каталитического количества пара-толуолсульфоновой кислоты в метаноле (10 мл) перемешивали при комнатной температуре в течение 1 ч. Растворитель выпаривали в вакууме и полученный остаток переносили в DCM, промывали водным насыщенным раствором NaHCO3, объединенные органические экстракты сушили (Na2SO4) и растворитель выпаривали в вакууме. Неочищенный остаток очищали колоночной хроматографией (силикагель; 0-30% EtOAc/DCM в качестве элюента). Нужные фракции собирали и упаривали в вакууме с получением Е 3 (0,05 г, 61%) в виде бесцветного масла. Соединения Е 4-Е 9 (табл. 1) получали аналогично. Физико-химические данные.LCMS (жидкостная хроматомасс-спектрометрия) - общая методика. Измерение посредством ВЭЖХ выполняли, используя HP 1100 от Agilent Technologies, содержащий насос (для четырех- или двухкомпонентной смеси) с дегазатором, автоматический дозатор, термостат для колонок, детектор на диодной матрице (DAD) и колонку, указанную в соответствующих методах ниже. Поток из колонки разделяли для масс-спектрометра (MS). MS-Детектор был оснащен источником ионизации электрораспылением. Азот использовали в качестве газа для распылителя. Источник температуры поддерживали при 140 С. Сбор данных осуществляли с помощью программного обеспечения MassLynxOpenlynx. В дополнение к общей методике: обращенно-фазовую ВЭЖХ проводили на картридже XDB-C18(1,8 мкм, 2,130 мм) от Agilent, со скоростью потока 1 мл/мин при 60 С. Используемые градиентные условия представляют собой: 90% А (0,5 г/л раствор ацетата аммония), 5% В (ацетонитрил), от 5% С (метанол) до 50% В и 50% С за 6,5 мин, до 100% В за 7 мин и уравновешивали к начальным условиям за 7,59,0 мин. Объем введенной пробы - 2 мкл. Масс-спектры с высоким разрешением (время пролета, TOF) получали только в режиме положительной ионизации, сканируя от 100 до 750 в течение 0,5 с, используя время задержки 0,1 с. Напряжение на капиллярной игле составляло 2,5 кВ и напряжение на конусе составляло 20 В. Лейцин-энкефалин представлял собой стандартное вещество, используемое для калибровки по фиксированной массе. Точки плавления. Для ряда соединений точки плавления определяли в открытых капиллярных пробирках на аппаратеMettler FP62. Точки плавления измеряли с температурным градиентом 3 или 10 С/минута. Максимальная температура составляла 300 С. Точку плавления считывали с цифрового дисплея и получали с погрешностями эксперимента, которые обычно связаны с данным аналитическим способом. В табл. 1 перечислены соединения формулы (I), которые получали согласно одному из указанных выше примеров (Пр. ). Таблица 1D. Фармакологические примеры. Соединения, предложенные в настоящем изобретении, являются положительными аллостерическими модуляторами mGluR2. Оказалось, что данные соединения усиливают глутаматные ответы посредством связывания с аллостерическим участком, отличным от участка связывания глутамата. Ответ mGluR2 на концентрацию глутамата усиливается, если присутствуют соединения формулы (I). Ожидается, что соединения формулы (I) будут осуществлять эффект, по существу, в отношении к mGluR2 благодаря их способности усиливать функцию этого рецептора. Поведение положительных аллостерических модуляторов, протестированных на mGluR2, с использованием метода анализа связывания [35S]GTPS, описанного ниже, который является пригодным для идентификации таких соединений, и, более конкретно, соединений формулы (I), показано в табл. 4. Анализ связывания [35S]GTPS. Анализ связывания [35S]GTPS представляет собой анализ на основе функциональных мембран, используемый для изучения функции рецептора, сопряженного с G-белком (GPCR), при помощи которого измеряют включение негидролизуемой формы GTP, [35S]GTPS (гуанозин-5'-трифосфат, меченный гамма-излучающим 35S). -Субъединица G-белка катализирует обмен гуанозин-5'-дифосфата (GDP) на гуанозин-трифосфат (GTP) и при активации GPCR агонистом, [35S]GTPS включается и не может быть отщеплен для продолжения цикла обмена (Harper (1998) Current Protocols in Pharmacology 2.6.1-10, JohnWileySons, Inc.). Величина включения радиоактивного [35S]GTPS является непосредственным измерением активности G-белка, и, таким образом, может быть определена активность агониста. Показано,что рецепторы mGluR2 преимущественно сочетаются с Gi-белком преимущественным сочетанием для данного способа, и, следовательно, их широко используют для изучения рецепторной активацииMolecular Pharmacology 53, с. 228-33). В данном описании изобретения авторы изобретения описано применение анализа связывания [35S]GTPS с использованием мембран из клеток, трансфицированных человеческим рецептором mGluR2 и адаптированных по Schaffhauser et al. (2003) Molecular Pharmacology 4, с. 798-810 для обнаружения свойств положительного аллостерического модулирования (РАМ) соединений по данному изобретению. Приготовление мембран. СНО-клетки культивировали до начала слияния и стимулировали 5 мМ бутиратом в течение 24 ч,затем промывали в PBS и затем собирали соскабливанием в буфер для гомогенизации (50 мМ буфер трис-HCl, рН 7,4, 4 С). Клеточные лизаты быстро гомогенизировали (15 с), используя гомогенизаторULTRA-TURRAX. Гомогенат центрифуговали при 23500g в течение 10 мин и надосадочную жидкость отбрасывали. Осадок ресуспендировали в 5 мМ трис-HCl, рН 7,4 и еще раз центрифугировали (30000g,20 мин, 4 С). Конечный пеллет ресуспендировали в 50 мМ HEPES, рН 7,4 и хранили при -80 С в подхо- 17016969 дящих аликвотах перед использованием. Концентрацию белка определяли методом Брэдфорда (Bio-Rad,USA) с бычьим сывороточным альбумином в качестве стандарта. Анализ связывания [35S]GTPS. Измерение положительной аллостерической модуляторной активности mGluR2 исследуемыми соединениями в мембранах, содержащих mGluR2 человека, осуществляли, используя замороженные мембраны, которые размораживали и быстро гомогенизировали перед преинкубированием в 96-луночных микропланшетах (15 мкг/аналитическая лунка, 30 мин, 30 С) в буфере для анализа (50 мМ HEPES рН 7,4,100 мМ NaCl, 3 мМ MgCl2, 50 мкМ GDP, 10 мкг/мл сапонина) с возрастающими концентрациями положительного аллостерического модулятора (от 0,3 нМ до 50 мкМ) и либо с минимальной предварительно определенной концентрацией глутамата (анализ РАМ), либо без добавления глутамата. Для РАМанализа мембраны предварительно инкубировали с глутаматом в концентрации ЕС 25, то есть концентрации, которая обеспечивает 25% максимального ответа глутамата и соответствует опубликованным данным (Pin et al. (1999) Eur. J. Pharmacol. 375, с. 277-294). После добавления [35S]GTPS (0,1 нМ, f.c.) для достижения общего реакционного объема 200 мкл, микропланшеты быстро встряхивали и дополнительно инкубировали, чтобы обеспечить включение [35S]GTPS при активации (30 мин, 30 С). Взаимодействие останавливали быстрой вакуум-фильтрацией микропланшета через планшеты из стекловолоконного фильтра (Unifilter 96-well GF/B filter plates, Perkin-Elmer, Downers Grove, USA), используя сборщик клеток для 96-луночного планшета (Filtermate, Perkin-Elmer, USA), и затем промыванием три раза 300 мкл ледяного промывочного буфера (Na2PO42H2O 10 мМ, NaH2PO4H2O 10 мМ, рН 7,4). Затем фильтры сушили на воздухе, добавляли в каждую лунку 40 мкл жидкой сцинтилляционной смеси (Microscint-O) и измеряли связанный с мембраной [35S]GTPS в 96-луночном сцинтилляционном планшетном ридере(Top-Count, Perkin-Elmer, USA). Неспецифическое связывание [35S]GTPS определяют в присутствие холодного 10 мкМ GTP. Каждую кривую выполняли по меньшей мере один раз, используя двойную выборку на точку на графике и при 11 концентрациях. Анализ данных. Кривые концентрация-ответ типичных соединений по настоящему изобретению в присутствие добавленной ЕС 25 mGluR2 агониста глутамата для определения положительного аллостерического модулирования (РАМ) получали, используя программное обеспечение Prism GraphPad (Graph Pad Inc., SanDiego, USA). Кривые соответствовали четырехпараметрическому логистическому уравнению (Y=Нижнее+(Верхнее-Нижнее)/(1+10LogEC50-Х)Наклон), позволяющему определить значения EC50. EC50 представляет собой концентрацию соединения, которая вызывает полумаксимальное потенциирование глутаматного ответа. Ее рассчитывают путем вычитания максимальных ответов глутамата в присутствии полностью насыщающей концентрации положительного аллостерического модулятора из ответа глутамата в отсутствие положительного аллостерического модулятора. Концентрацию, вызывающую полумаксимальный эффект, рассчитывали затем как ЕС 50. Таблица 2. Фармакологические данные для соединений по изобретению. Все соединения испытывали в присутствие агониста mGluR2, глутамата в предварительно определенной концентрации ЕС 25, для определения положительного аллостерического модулирования (GTPSPAM). Показанные значения являются средними из парных значений 11 концентраций на кривых ответа,по меньшей мере из одного эксперимента. Все исследованные соединения показали значение рЕС 50(-logEC50) больше 5,0, от 6,09 до 7,40. Погрешность определения значения рЕС 50 для единичного эксперимента устанавливают равной примерно 0,3 log единиц."Активный ингредиент" при использовании во всех этих примерах относится к конечному соединению формулы (I), его фармацевтически приемлемым солям, сольватам и стереохимически изомерным формам.- 18016969 Типичными примерами прописей композиции по изобретению являются следующие. 1. Таблетки. В данном примере активный ингредиент может быть заменен таким же количеством любого из соединений по настоящему изобретению, в частности таким же количеством любого из соединений, приведенных в качестве примера. 2. Суспензия. Водную суспензию готовят для перорального введения так, что каждый 1 мл содержит от 1 до 5 мг одного из активных соединений, 50 мг натрий карбоксиметилцеллюлозы, 1 мг бензоата натрия, 500 мг сорбитола и воду до 1 мл. 3. Инъекционная. Парентеральную композицию получают перемешиванием 1,5 мас.% активного ингредиента по изобретению в 10 об.% пропиленгликоля в воде. 4. Мазь. В данном примере активный ингредиент может быть заменен таким же количеством любого из соединений по настоящему изобретению, в частности таким же количеством любого из соединений, приведенных в качестве примера. Приемлемые варианты не следует рассматривать в качестве отклонения от объема изобретения. Очевидно, что таким образом описанное изобретение специалисты в данной области техники могут варьировать разным образом. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение, имеющее формулу (I) или его стереохимически изомерная форма, гдеR4 представляет собой водород, C1-3 алкил, С 1-3 алкилокси, гидроксиС 1-3 алкил или тетрагидрофуран 2-илоксиС 1-3 алкил;X представляет собой ковалентную связь, О или NR5;R5 представляет собой водород, С 1-3 алкил или гидроксиС 2-3 алкил;R6 представляет собой водород или C1-3 алкил илиR4 и R6 образуют радикал -СН 2-СН 2-; или его фармацевтически приемлемая соль. 2. Соединение по п.1, гдеR4 представляет собой водород или гидроксиметил;X представляет собой ковалентную связь, О или NR5;R6 представляет собой водород или метил; или его фармацевтически приемлемая соль. 3. Соединение по п.1, гдеR3 представляет собой водород или хлоро;R4 представляет собой водород или гидроксиметил;X представляет собой ковалентную связь, О или NR5;R6 представляет собой водород или метил; или его фармацевтически приемлемая соль. 4. Соединение, представляющее собой 1-бутил-3-хлор-2-оксо-1,2-дигидропиридин-4-иловый эфир трифторметансульфоновой кислоты. 5. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по любому из пп.1-4 и фармацевтически приемлемый носитель или эксципиент. 6. Применение соединения по любому из пп.1-4 в качестве лекарственного средства. 7. Применение соединения по любому из пп.1-4 для изготовления лекарственного средства для лечения или предупреждения состояния у млекопитающего, включая человека, лечение или предупреждение которого находится под влиянием или облегчается нейромодуляторным эффектом положительных аллостерических модуляторов mGluR2. 8. Применение соединения по любому из пп.1-4 для изготовления лекарственного средства для лечения или предупреждения расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства, связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия. 9. Применение по п.8, где расстройство центральной нервной системы представляет собой тревожное расстройство, выбранное из группы: агорафобия, генерализованное тревожное расстройство (GAD),обсессивно-компульсивное расстройство (OCD), паническое расстройство, посттравматическое стрессовое расстройство (PTSD), социальная фобия и другие фобии. 10. Применение по п.8, где расстройство центральной нервной системы представляет собой психотическое расстройство, выбранное из группы: шизофрения, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство и психотическое расстройство, вызванное веществом. 11. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство личности, выбранное из группы: обсессивно-компульсивное личностное расстройство и шизоидное, шизотипическое расстройство. 12. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство, связанное с веществом, выбранное из группы: злоупотребление алкоголем, алкогольная зависимость, алкогольная абстиненция, делирий при алкогольной абстиненции, психотическое расстройство,вызванное алкоголем, амфетаминовая зависимость, амфетаминовая абстиненция, кокаиновая зависимость, кокаиновая абстиненция, никотиновая зависимость, никотиновая абстиненция, опиоидная зависимость и опиоидная абстиненция. 13. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство питания, выбранное из группы: нервная анорексия и нейрогенная булимия. 14. Применение по п.8, где расстройство центральной нервной системы представляет собой расстройство настроения, выбранное из группы: биполярные расстройства (I и II), циклотимическое расстройство, депрессия, дистимическое расстройство, большое депрессивное расстройство и расстройство настроения, вызванное веществом. 15. Применение по п.8, где расстройство центральной нервной системы представляет собой мигрень. 16. Применение по п.8, где расстройство центральной нервной системы представляет собой эпилепсию или конвульсивное расстройство, выбранное из группы: генерализованная неконвульсивная эпилепсия, генерализованная конвульсивная эпилепсия, малый эпилептический припадок, большой эпилептический припадок, парциальная эпилепсия с нарушением сознания или без нарушения сознания, младенческие судороги, непрерывная парциальная эпилепсия и другие формы эпилепсии. 17. Применение по п.8, где детское расстройство представляет собой синдром дефицита внимания/гиперактивности.- 20016969 18. Применение по п.8, где расстройство центральной нервной системы представляет собой когнитивное расстройство, выбранное из группы: делирий, персистирующий делирий, вызванный веществом,деменция, деменция вследствие ВИЧ-заболевания, деменция вследствие болезни Гентингтона, деменция вследствие болезни Паркинсона, деменция альцгеймеровского типа, персистирующая деменция, вызванная веществом, и легкое когнитивное нарушение. 19. Применение по п.8, где расстройство центральной нервной системы выбрано из группы: тревога, шизофрения, мигрень, депрессия и эпилепсия. 20. Применение соединения по любому из пп.1-4 в комбинации с ортостерическим агонистомmGluR2 для изготовления лекарственного средства для лечения или предупреждения состояния, указанного в любом из пп.7-19. 21. Применение соединения по любому из пп.1-4 в лечении или предупреждении расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства, связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия. 22. Способ лечения или предупреждения расстройства центральной нервной системы, выбранного из группы: тревожные расстройства, психотические расстройства, расстройства личности, расстройства,связанные с веществами, расстройства питания, расстройства настроения, мигрень, эпилепсия или конвульсивные расстройства, детские расстройства, когнитивные расстройства, нейродегенерация, нейротоксичность и ишемия, включающий введение субъекту соединения по любому из пп.1-4.
МПК / Метки
МПК: C07D 405/14, C07D 405/12, C07D 213/64, A61K 31/47
Метки: 1,3-двузамещенные-4-фенил-1н-пиридин-2-оны
Код ссылки
<a href="https://eas.patents.su/22-16969-13-dvuzameshhennye-4-fenil-1n-piridin-2-ony.html" rel="bookmark" title="База патентов Евразийского Союза">1,3-двузамещенные-4-фенил-1н-пиридин-2-оны</a>












