Новые дигидрофуро[3, 4-b]хинолин-1-оны, способ их получения и содержащие их фармацевтические композиции
Номер патента: 3996
Опубликовано: 25.12.2003
Авторы: Пьер Алан, Юссон Анри-Филипп, Жиоржи-Рено Сильвиан, Тратра Кристоф, Ренар Пьер, Атасси Ганем, Пфейффер Брюно
Формула / Реферат
1. Соединение формулы (I)
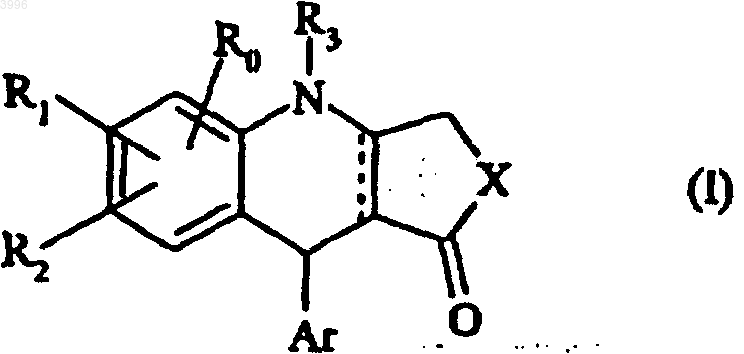
где
----- представляет собой одинарную или двойную связь,
R0 представляет собой атом водорода, гидроксильную группу или линейную или разветвленную (C1-C6)алкоксигруппу,
каждый из R1 и R2, которые могут быть одинаковыми или различными, представляет собой
- атом водорода,
- линейную или разветвленную(C1-C6)алкильную группу,
- линейную или разветвленную(C1-C6)алкоксигруппу,
- гидроксильную группу,
- или вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, содержащую в кольце от 5 до 12 членов, необязательно содержащую 1 или 2 гетероатома, выбираемых из кислорода, серы или азота,
R3 представляет собой атом водорода или группу формулы R4, где R4 представляет собой
- арильную группу,
- линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную арильной группой, гетероарильной группой, гидроксильной группой или группой формулы NR5R6, где каждый из заместителей R5 и R6, которые одинаковы или различны, представляет собой линейную или разветвленную (C1-C6)алкильную группу или линейную или разветвленную (C1-C6)гидроксиалкильную группу,
- или группу формулы COR7, где заместитель R7 представляет собой линейный или разветвленный (C1-C6)алкил, необязательно замещенный группой формулы NR8R9, где каждый из заместителей R8 и R9, которые одинаковы или различны, представляет собой линейную или разветвленную (C1-C6)алкильную группу или линейную или разветвленную (C1-C6)гидроксиалкильную группу,
X представляет собой атом кислорода или атом серы или группу -CH2-или -CH2-CH2-,
Ar представляет собой арил, гетероарил или арил-(C1-C6)алкильную группу, в которой алкил является линейным или разветвленным, при том, что по меньшей мере один из R0, R1 или R2 отличен от водорода; их оптические изомеры, их гидраты, сольваты, а также их аддитивные соли с фармацевтически приемлемой кислотой,
где арил следует понимать как фенил, необязательно замещенный одной или более одинаковыми или разными атомами или группами, выбираемыми из атомов галогена и линейного или разветвленного (C1-C6)алкила, гидроксигруппы, линейной или разветвленной (C1-C6)алкоксигруппы, линейного или разветвленного (C1-C6)полигалогеналкила, аминогруппы (необязательно замещенной одной или более линейными или разветвленными (C1-C6)алкильными группами), нитрогруппы, линейной или разветвленной (C1-C6)ацильной или (C1-C2)алкилендиоксигруппы;
гетероарил следует понимать как ароматическую моноциклическую группу, содержащую в кольце от 5 до 6 членов и содержащую один гетероатом, выбираемый из кислорода, азота и серы, где гетероарильная группа может быть необязательно замещена одной или более одинаковыми или разными атомами или группами, выбираемыми из атомов галогена и групп линейного или разветвленного (C1-C6)алкила, гидроксигруппы, линейной или разветвленной (C1-C6)алкоксигруппы, линейного или разветвленного (C1-C6)полигалогеналкила и аминогруппы (необязательно замещенной одной или более линейными или разветвленными (C1-C6)алкильными группами).
2. Соединение формулы (I) по п.1, где ----- представляет собой двойную связь.
3. Соединение формулы (I) по любому из пп.1 или 2, где R0 представляет собой атом водорода.
4. Соединение формулы (I) по любому из пп.1-3, где каждый из заместителей R1 и R2, которые одинаковы или различны, представляет собой
- атом водорода,
- линейную или разветвленную (C1-C6)алкильную группу,
- линейную или разветвленную (C1-C6)алкоксигруппу,
- гидроксильную группу.
5. Соединение формулы (I) по любому из пп.1-3, где заместители R1 и R2 вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, имеющую в кольце от 5 до 12 членов и содержащую 1 или 2 гетероатома, выбираемых из кислорода, серы и азота.
6. Соединение формулы (I) по п.5, где заместители R1 и R2 вместе с несущими их атомами углерода образуют группу формул G3 или G4
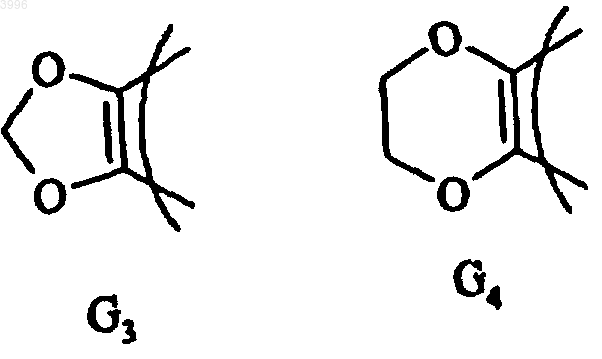
7. Соединение формулы (I) по п.5, где заместители R1 и R2 вместе с несущими из атомами углерода образуют группу фенилена.
8. Соединение формулы (I) по любому из пп.1-7, где X представляет собой атом кислорода.
9. Соединение формулы (I) по любому из пп.1-7, где X представляет собой атом серы.
10. Соединение формулы (I) по любому из пп.1-7, где X представляет собой группу -CH2- или -CH2-CH2-.
11. Соединение формулы (I) по любому из пп.1-10, где Ar представляет собой арильную группу.
12. Соединение формулы (I) по любому из пп.1-10, где Ar представляет собой гетероарильную группу.
13. Соединение формулы (I) по п.11, где Ar представляет собой фенильную группу.
14. Соединение формулы (I) по п.1, которое представляет собой (+)-4-метил-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин-1(3H)-он, а также его оптические изомеры и его гидраты и сольваты.
15. Соединение формулы (I) по п.1, которое представляет собой (+)-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
16. Соединение формулы (I) по п.1, которое представляет собой (+)-6-метокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро-[3,4-b]хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
17. Соединение формулы (I) по п.1, которое представляет собой (+)-7-(3,4,5-триметоксифенил)-7,11-дигидробензо[h]фуро-[3,4-b]хинолин-8(10H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
18. Соединение формулы (I) по п.1, которое представляет собой (+)-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-2,3,4,9-тетрагидроциклопента[b]хинолин-1-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
19. Соединение формулы (I) по п.1, которое представляет собой (+)-6,7-этилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
20. Соединение формулы (I) по п.1, которое представляет собой (+)-7-(3,4,5-триметоксифенил)-7,9,10,11-тетрагидро-8H-бензо[h]циклопента[b]хинолин-8-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой.
21. Способ получения соединений формулы (I) по п.1, отличающийся тем, что соединение формулы (II)
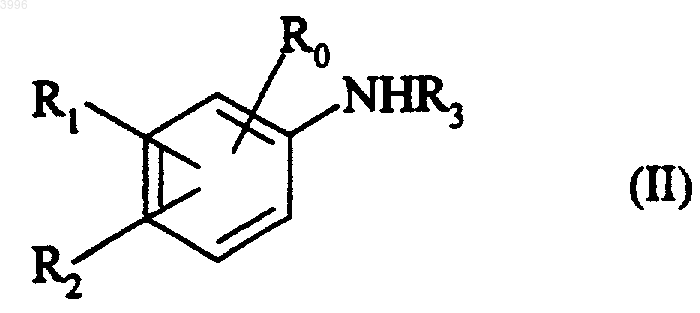
где заместители R0, R1, R2 и R3 имеют те же значения, что определены для формулы (I),
реагирует с соединением формулы (III)
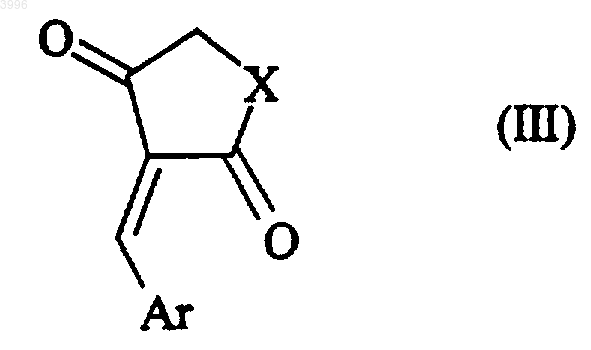
где X и Ar имеют те же самые значения, что определхэы для формулы (I),
с образованием соединения формулы (Ia), представляющего собой частный случай соединений формулы (I)
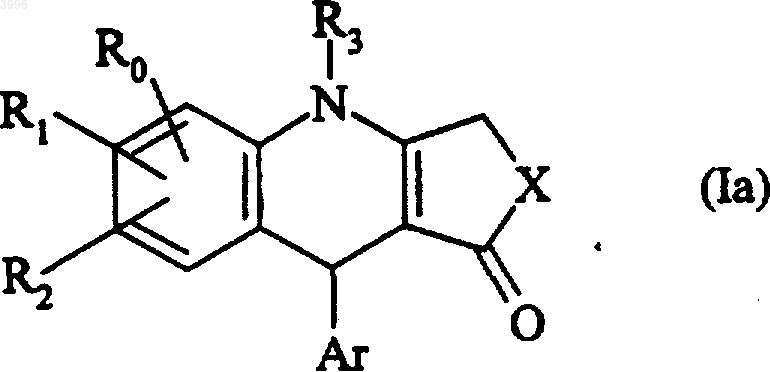
где R0, R1, R2, R3, X и Ar имеют определенные выше значения,
которое затем восстанавливают, если необходимо, до соединения (Ib), представляющего собой частный случай соединений формулы (I)
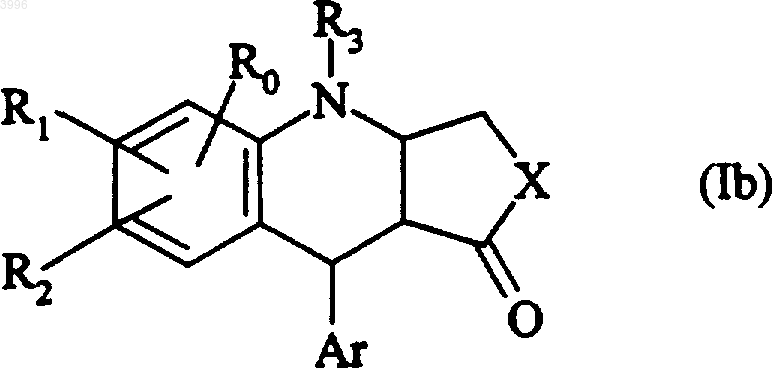
где R0, R1, R2, R3, X и Ar имеют определенные выше значения,
и причем соединения формул (Ia) и (Ib), которые составляют все соединения формулы (I), очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют, если это желательно, на их оптические изомеры в соответствии с обычными методиками разделения и превращают, если это желательно, в их аддитивные соли с фармацевтически приемлемой кислотой.
22. Способ получения соединений формулы (I) по п.1, отличающийся тем, что в одном сосуде взаимодействуют соединение формулы (II)
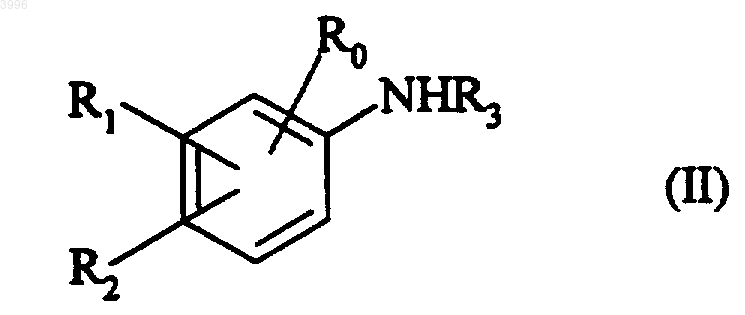
где R0, R1, R2 и R3 имеют те же значения, что определены для формулы (I), соединение формулы (VIII)
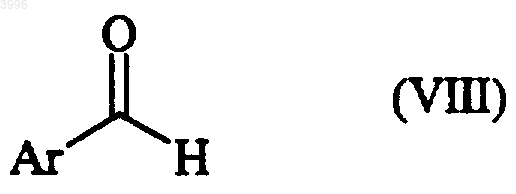
где Ar принимает те же значения, что и в формуле (I), и соединение формулы (IX)
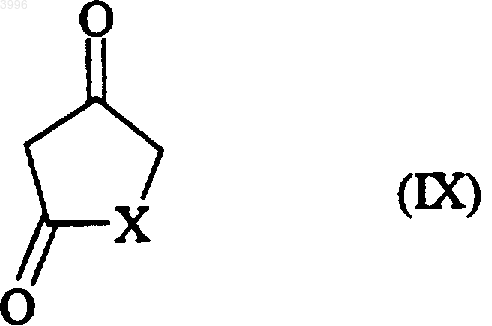
где X принимает те же значения, что и в формуле (I), с образованием соединения формулы (Ia), представляющего собой частный случай соединений формулы (I)
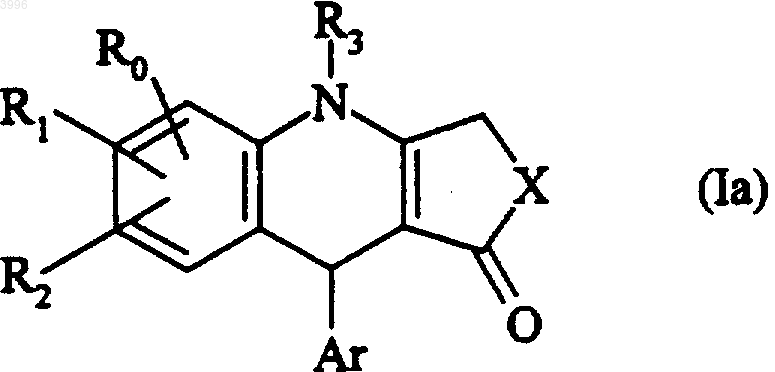
где R0, R1, R2, R3, X и Ar имеют определенные выше значения,
которое затем восстанавливают, если это необходимо, до соединения (Ib), представляющего собой частный случай соединений формулы (I)
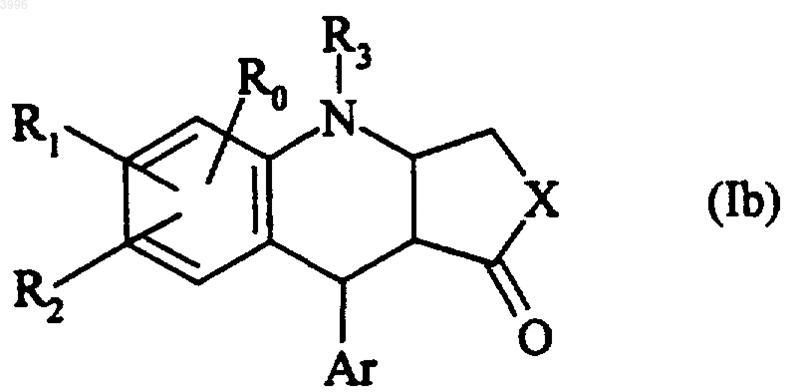
где R0, R1, R2, R3, X и Ar имеют определенные выше значения,
причем соединения формул (Ia) и (Ib), которые составляют все соединения формулы (I), очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют, если это желательно, на их оптические изомеры в соответствии с обычными методиками разделения и превращают, если это желательно, в их аддитивные соли с фармацевтически приемлемой кислотой.
23. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по любому из пп.1-20 само по себе или в сочетании с одним или более фармацевтически приемлемыми инертными, нетоксичными носителями.
24. Применения фармацевтической композиции по п.23 для получения противораковых лекарственных средств.
Текст
1 Настоящее изобретение относится к новым дигидрофуро[3,4-b]хинолин-1-онам, способу их получения, содержащим их фармацевтическим композициям и к их применению в качестве противораковых агентов. Требования противораковой терапии предусматривают постоянную разработку новых противоопухолевых агентов с целью получения лекарственных средств, которые являются как более активными, так и лучше переносимыми. Соединения настоящего изобретения являются не только новыми, но и обладают весьма ценными противоопухолевыми свойствами. Соединения аналогичной структуры уже описаны в литературе, особенно фуро[3,4-b] хинолин-1-оны, как средства против остеопороза (патент ЕР 0634169). С другой стороны, никогда не описывалась цитотоксическая активность этих соединений. Настоящее изобретение более конкретно относится к соединениям формулы (I) гдепредставляет собой одинарную или двойную связь,R0 представляет собой атом водорода, гидроксильную группу или линейную или разветвленную (C1-C6)алкоксигруппу,каждый из R1 и R2, которые могут быть одинаковы или различны, представляет собой:- атом водорода,- атом галогена,- линейную или разветвленную (C1-C6)алкильную группу,- линейную или разветвленную (C1-C6)алкоксигруппу,- гидроксильную группу,- линейную или разветвленную (C1-C6)полигалогеналкильную группу,- нитрогруппу,- аминогруппу, необязательно замещенную одной или двумя линейными или разветвленными (C1-C6)алкильными группами,- группу формулы, где m представляет собой целое число, причем 1m4,- или вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, содержащую в кольце от 5 до 12 членов, необязательно содержащую 1 или 2 гетероатома, выбираемых их О, S или N,= R3 представляет собой атом водорода или группу формулы R4,где R4 представляет собой:- линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную арильной группой, гетероарильной группой,гидроксильной группой, линейной или разветвленной (C1-C6)алкоксигруппой или группой формулы NR5R6, где каждый из заместителей R5 и R6, которые одинаковы или различны, представляет собой линейную или разветвленную(C1-C6)алкильную группу или линейную или разветвленную(C1-C6)гидроксиалькильную группу, или вместе с несущим их атомом азота образуют азотсодержащий гетероцикл,- или группу формулы COR7, где заместитель R7 представляет собой одну из следующих групп:- арил,- линейный или разветвленный (C1-C6)алкил (необязательно замещенный группой формулы NR8R9, где каждый из заместителей R8 иR9, которые одинаковы или различны, представляет собой линейную или разветвленную (C1C6)алкильную группу или линейную или разветвленную (C1-C6)гидроксиалкильную группу,или вместе с несущим их атомом азота образуют азотный гетероцикл), аминогруппу, необязательно замещенную одной или более группами из числа арила, гетероарила или линейного или разветвленного (C1-C6)алкила, необязательно замещенного группой формулы NR8R9, где каждый из заместителей R8 и R9, которые являются одинаковыми или разными, представляет собой линейную или разветвленную (C1-C6)алкильную группу или линейную или разветвленную(C1-C6)гидроксиалкильную группу, или вместе с несущим их атомом азота образуют азотный гетероцикл, или OR10, где заместитель R10 представляет собой атом водорода или арильную группу, или линейный или разветвленный (C1C6)алкил, необязательно замещенный группой формулы NR8R9, где каждый из заместителей R8 и R9, которые одинаковы или различны, представляет собой линейную или разветвленную(C1-C6)алкильную группу или линейную или разветвленную (C1-C6)гидроксиалкильную группу, или вместе с несущим их атомом азота образуют азотсодержащий гетероцикл),X представляет собой атом кислорода или атом серы, или группу -СН 2- или -СН 2-СН 2-,Ar представляет собой арил, гетероарил или арил-(C1-C6)-алкильную группу, в которой алкил является линейным или разветвленным,их оптические изомеры, их аддитивные соли с фармацевтически приемлемой кислотой и их гидраты и сольваты. К фармацевтически приемлемым кислотам относятся, но не ограничиваясь ими, соляная,бромистоводородная, серная, фосфорная, уксусная, фторуксусная, молочная, пировиноградная, малоновая, янтарная, глутаровая, фумаровая, винная, малеиновая, лимонная, аскорбиновая, щавелевая, метансульфоновая, бензолсульфоновая и камфорная кислота. 3 Под арильной группой следует понимать фенильную, бифенильную, нафтильную или тетрагидронафтильную, причем каждая из этих групп необязательно замещена одним или более одинаковыми или разными атомами или одной или более одинаковыми или разными группами,выбираемыми из атомов галогена или линейного или разветвленного (C1-C6)алкила, гидроксигруппы, линейной или разветвленной (C1-C6) алкоксигруппы, линейного или разветвленного(C1-C6)полигалогеналкила, аминогруппы (необязательно замещенной одной или более линейными или разветвленными (C1-C6)алкильными группами), нитрогруппы, линейной или разветвленной (C1-C6)ацильной или (C1-C2)алкилендиоксигруппы. Гетероарильную группу следует понимать как ароматическую, моно- или бициклическую группу, содержащую в кольце от 5 до 12 членов и содержащую один, два или три гетероатома,выбираемых из атома кислорода, азота и серы,где гетероарильная группа может быть необязательно замещена одним или более одинаковыми или разными атомами или одной или более одинаковыми или разными группами, выбираемыми из: атомов галогена и линейного или разветвленного (C1-C6)алкила, гидроксигруппы,линейной или разветвленной (C1-C6)алкоксигруппы, линейного или разветвленного (C1-C6) полигалогеналкила и аминогруппы (необязательно замещенной одной или более линейными или разветвленными (C1-C6 )алкильными группами). Среди гетероарильных групп могут быть названы, но без всякого ограничения, такие группы, как тиенил, пиридил, фурил, пирролил,имидазолил, оксазолил, изоксазолил, тиазолил,изотиазолил, хинолил, изохинолил и пиримидинил. Под азотным (азотосодержащим) гетероциклом следует понимать насыщенную моноциклическую группу, содержащую в кольце от 5 до 7 членов и содержащую один, два или три гетероатома, один из которых представляет собой азот, тогда как необязательно присутствующий(е) дополнительный(е) гетероатом(ы) выбирае(ю)тся из атомов кислорода, азота и серы. Предпочтительными азотными гетероциклами являются такие группы, как пирролидинил, пиперидил, морфолинил и пиперазинил. Среди ароматических или неароматических, моно- или бициклических групп, содержащих в кольце от 5 до 12 членов и необязательно содержащих 1 или 2 гетероатома, выбираемых из О, S и N, следует назвать, но без всякого ограничения, фенилен, нафтилен, циклопентенилен и группы формул G1-G5 4 Предпочтительными соединениями формулы (I) являются соединения, где представляет собой двойную связь. Предпочтительными соединениями формулы (I) являются соединения, где заместительR0 представляет собой атом водорода. Предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы (I), где каждый из заместителейR1 и R2, которые одинаковы или различны,представляет собой:- атом водорода,- атом галогена,- линейную или разветвленную (C1-C6)алкильную группу,- линейную или разветвленную (C1-C6)алкоксигруппу, гидроксильную группу,- линейную или разветвленную (C1-C6)полигалогеналкильную группу,- нитрогруппу,- аминогруппу, необязательно замещенную одной или двумя линейными или разветвленными (C1-C6)алкильными группами, или, где m пред- группу формулы ставляет собой целое число, причем 1m4. Другой предпочтительный вариант осуществления изобретения относится к соединениям формулы (I), где заместители R1 и R2 вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, содержащую в кольце от 5 до 12 членов и необязательно содержащую 1 или 2 гетероатома, выбираемых из О, S и N. Среди них наиболее предпочтительными являются соединения, в которых заместители R1 и R2 вместе с несущими их атомами углерода образуют фениленовую группу или группу формул G3 или G4, которые определены выше. Другой предпочтительный вариант осуществления изобретения составляют соединения формулы (I), где X представляет собой атом кислорода или серы. Другой предпочтительный вариант осуществления изобретения относится к соединениям формулы (I), где X представляет собой -СН 2 или -СН 2-СН 2-группу. Еще один предпочтительный вариант осуществления изобретения относится к соединениям формулы (I), где Ar представляет собой арильную группу, более предпочтительно необязательно замещенную фенильную группу. Еще один предпочтительный вариант осуществления изобретения относится к соединениям формулы (I), где Ar представляет собой гетероарильную группу. Среди предпочтительных соединений настоящего изобретения можно назвать-4-метил-6,7-метилендиокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он, а также его оптические изомеры и его гидраты и сольваты, 5-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин 1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой,-6-метокси-9-(3,4,5-триметоксифенил)4,9-дигидрофуро[3,4-b]-хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой,-7-(3,4,5-триметоксифенил)-7,11-дигидробензо[h]фуро[3,4-b]-хинолин-8(10 Н)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой,-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-2,3,4,9-тетрагидроциклопента[b]хинолин-1-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой,-6,7-этилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин-1(3H)он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой,-7-(3,4,5-триметоксифенил)-7,9,10,11 тетрагидро-8 Н-бензо-[h]циклопента[b]-хинолин-8-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. Настоящее изобретение также относится к способу получения соединений формулы (I),который отличается тем, что соединение формулы (II) где заместители R0, R1, R2 и R3 имеют те же самые значения, что определены для формулы где X и Ar имеют те же самые значения,что определены для формулы (I),с образованием соединения формулы (Iа),представляющего собой часть класса соединений формулы (I) где заместители R0, R1, R2, R3, X и Ar имеют определенные выше значения, которое затем восстанавливают, если это необходимо, до соединения (Ib), представляющего собой частный случай классу соединений формулы (I) 6 где R0, R1, R2, R3, X и Ar имеют определенные выше значения,и соединения формул (Iа) и (Ib), которые составляют все соединения формулы (I), очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют, если это желательно, на их оптические изомеры, в соответствии с обычными методиками разделения, и превращают, если это желательно, в их аддитивные соли с фармацевтически приемлемой кислотой. Когда заместитель R3 не представляет собой атом водорода, соединение формулы (II) может быть получено реакцией соединения формулы (IV) где заместители R0, R1 и R2 имеют определенные выше значения,с соединением формулы (V)(V) где заместитель R4 имеет те же самые значения, что и в формуле (I), a Y представляет собой уходящую группу, такую как, например,атом галогена или мезилатная, тозилатная или трифторметансульфонатная группа. Когда заместитель R3 представляет собой группу формулы -CH2R'3, где заместитель R'3 представляет собой арильную группу, гетероарильную группу или линейную или разветвленную (C1-C5)алкильную группу, необязательно замещенную арильной группой, гетероарильной группой, гидроксильной группой, необязательно замещенной линейной или разветвленной (C1C6)алкоксигруппой или группой формулыNR5R6, где R5 и R6, которые одинаковы или различны и каждый из которых представляет собой линейную или разветвленную (C1-C6)алкильную группу или линейную или разветвленную (C1C6)гидроксиалкильную группу, или вместе с несущим их атомом азота образуют азотный гетероцикл, соединение формулы (II) может быть также получено реакцией в присутствии восстанавливающего агента соединения формулы (IV) с соединением формулы (VI) где заместитель R'3 имеет определенные выше значения. Когда заместитель R3 представляет собой группу формулы -COR'7, где заместитель R'7 представляет собой арильную группу, соединение формулы (II) может быть также получено реакцией соединения формулы (VII) где заместители R0, R1, R2 и R'7 имеют определенные выше значения, с окисляющим агентом. 7 Когда заместитель R3 представляет собой СН 3-группу, соединение формулы (II) может быть также получено реакцией соединения формулы (IV) с муравьиной кислотой в присутствии восстанавливающего агента. Соединение формулы (III) получают реакцией соединения формулы (VIII)J.Org.Chem. 1978, 43, 1541. Изобретение также охватывает второй способ получения соединений формулы (I), который отличается тем, что в одном сосуде подвергают взаимодействию соединение формулы(II), соединение формулы (VII) и соединение формулы (VIII), с образованием соединения формулы (Iа), которое затем, если желательно,восстанавливают до соединения формулы (Ib), и соединения формул (Iа) и (Ib), которые составляют все соединения формулы (I) очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют, если это желательно, на их оптические изомеры, в соответствии с обычными методиками разделения, и превращают, если это желательно, в их аддитивные соли с фармацевтически приемлемой кислотой. Соединения настоящего изобретения являются не только новыми, но также обладают ценными фармакологическими свойствами. Эти соединения обладают цитотоксическими свойствами, делающими их полезными при лечении рака. Изобретение также охватывает фармацевтические композиции, содержащие в качестве активного ингредиента, по меньшей мере, одно соединение формулы (I) с одним или более подходящими, инертными, нетоксичными наполнителями. Среди фармацевтических композиций в соответствии с настоящим изобретением в особенности следует назвать композиции, которые приемлемы для перорального, парентерального(внутривенного, внутримышечного или подкожного) или назального введения, таблетки или драже, подъязычные таблетки, желатиновые капсулы, лепешки, свечи, кремы, мази, кожные гели, препараты для инъекций, смеси для питья и т.д. Необходимая дозировка может быть подобрана в соответствии с природой и серьезностью заболевания и с учетом способа введения,возраста и веса пациента, возможности сопутст 003996 8 вующего лечения. Дозировка лекарственного средства меняется от 0,5 мг до 2 г в сутки при одном или более введениях. Следующие примеры иллюстрируют изобретение, но ни коим образом не ограничивают его. Используемые исходные вещества являются известными продуктами или продуктами,получаемыми в соответствии с известными методиками. Синтезы A-S приводят к промежуточным соединениям, которые используются в способах получения соединений настоящего изобретения. Структуры описанных в примерах соединений определяют в соответствии с обычными спектрометрическими методиками (ИК, ЯМР,масс-спектрометрия). СинтезA. 3-(3,4,5-Триметоксибензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3,4,5-триметоксибензальдегида и тетроновой кислоты. Синтез В. 3-(4-Гидрокси-3,5-диметоксибензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4-гидрокси-3,5 диметоксибензальдегида и тетроновой кислоты. Синтез С. 3-(3-Пиридилметилен)-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из никотинового альдегида и тетроновой кислоты. Синтез D. 3-(3-Метокси-4,5-метилендиоксибензилиден)-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3-метокси-4,5 метилендиоксибензальдегида и тетроновой кислоты. Синтез Е. 3-(2,3,4-Триметоксибензилиден)2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 2,3,4-триметоксибензальдегида и тетроновой кислоты. Синтез F. 3-(3,4-Диметоксибензилиден)2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978,43,1541,исходя из 3,4-диметоксибензальдегида и тетроновой кислоты. Синтез G. 3-(3-Гидрокси-4-метоксибензилиден)-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3-гидрокси-4 метоксибензальдегида и тетроновой кислоты. Синтез Н. 3-(4-Метоксибензилиден)-2,4(3H,5 Н)фурандион. 9 Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4-метоксибензальдегида и тетроновой кислоты. Синтез I. 3-(3-Метоксибензилиден)-2,4(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3-метоксибензальдегида и тетроновой кислоты. Синтез J. 3-Бензилиден-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из бензальдегида и тетроновой кислоты. Синтез К. 3-(2-Фурилметилен)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 2-фурилальдегида и тетроновой кислоты. Синтез L. 3-(3,4,5-Триметоксибензилиден)1,3-циклопентандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3,4,5-триметоксибензальдегида и 1,3-циклопентандиона. Синтез М. 3-(4,5-Метилендиоксибензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4,5-метилендиоксибензальдегида и тетроновой кислоты. Синтез N. 3-(4-Хлорбензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4-хлор-бензальдегида и тетроновой кислоты. Синтез О. 3-(4-Нитробензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4-нитробензальдегида и тетроновой кислоты. Синтез Р. 3-(3-Нитробензилиден)-2,4-(3 Н,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 3-нитробензальдегида и тетроновой кислоты. Синтез Q. 3-(4-Диметиламинобензилиден)2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 4-диметиламинобензальдегида и тетроновой кислоты. Синтез R. 3-(4-Пиридилметилен)-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 10 1978, 43, 1541, исходя из изоникотинового альдегида и тетроновой кислоты. Синтез S. 3-(2-Пиридилметилен)-2,4-(3H,5 Н)фурандион. Ожидаемый продукт получают в соответствии с методикой, описанной в J. Org. Chem. 1978, 43, 1541, исходя из 2-пиридинкарбоксальдегида и тетроновой кислоты. Пример 1. -4-Метил-6,7-метилендиокси 9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Стадия А. N-метил-3,4-метилендиоксианилин. Раствор 3,4-метилендиоксианилина (10 ммолей) в муравьиной кислоте (36 мл) кипятят обратным холодильником в течение 1 ч. После удаления избытка муравьиной кислоты полученный остаток разбавляют водой и экстрагируют дихлорметаном. Объединенные органические фазы упаривают. Полученный остаток растворяют в эфире, затем маленькими порциями при температуре 10 С добавляют алюмогидрид лития (42 ммоля). После перемешивания смеси при комнатной температуре в течение 3 ч добавляют воду и 10%-ный раствор гидроксида натрия, и смесь фильтруют через целит. Фильтрат сушат и упаривают, и полученный остаток очищают хроматографированием на силикагеле,используя в качестве элюента дихлорметан, получают ожидаемый продукт в виде масла. Стадия В. -4-Метил-6,7-метилендиокси 9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-и]хинолин-1(3H)-он. К соединению, полученному на предыдущей стадии (10 ммолей) , суспендированному в этаноле, добавляют 10 ммолей соединения, описанного в синтезе А, и затем смесь кипятят с обратным холодильником в течение 30 мин. После охлаждения до комнатной температуры полученный осадок фильтруют и промывают, а затем перекристаллизовывают, получают названный продукт. Температура плавления: 226 С. Элементный анализ. Вычислено, %: С 64,23, Н 5,14, N 3,40. Найдено, %: С 64,11, Н 5,09, N 3,26. Пример 2. -4-Метил-6,7-мелилендиокси-9-(3,4,5-триметоксифенил)-3 а,4,9,9 а-тетрагидрофуро[3,4-b]хинолин-1(3H)-он. Суспензию соединения, описанного в примере 1 (10 ммолей), в этаноле помещают в атмосферу водорода при давлении 50 фунтов/кв.дюйм (3,515 кг/см 3) при комнатной температуре в присутствии палладия на угле. После удаления катализатора путем фильтрования растворитель упаривают, и полученный остаток очищают хроматографированием на силикагеле,используя в качестве элюента дихлорметан. Пример 3. -6,7-Метилендиокси-4-(4 нитробензил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. 11 Стадия A. N-(4-Нитробензил)-3,4-метилендиоксианилин. Раствор 3,4-метилендиоксианилина (10 ммолей) и 4-нитробензальдегида (10 ммолей) в метаноле перемешивают при комнатной температуре в течение 18 ч. Полученный осадок отфильтровывают, промывают, затем растворяют в тетрагидрофуране. После добавления уксусной кислоты и боргидрида натрия (25 ммолей) реакционную смесь перемешивают при комнатной температуре в течение 1 ч, растворители упаривают, и сырой продукт очищают хроматографированием на силикагеле, используя в качестве элюента дихлорметан. Температура плавления: 114 С. Стадия В: -6,7-Метилендиокси-4-(4 нитробензил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, полученного на предыдущей стадии и соединения, описанного в синтезе А. Температура плавления: 240 С. Элементный анализ. Вычислено, %: С 62,11, Н 4,80, N 5,17 (полугидрат). Найдено, %: С 62,43, Н 4,49, N 5,13. Пример 4.-4-(4-Хлорбензил)-6,7 метилендиокси-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 4-хлорбензальдегида и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 63,34, Н 4,74, N 2,64. (полугидрат). Найдено, %: С 63,51, Н 4,73, N 2,59. Пример 5. -4-(3-Гидроксибензил)-6,7 метилендиокси-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3-гидроксибензальдегида и соединения, описанного в синтезе А. Температура плавления: 245 С. Элементный анализ. Вычислено, %: С 64,49, Н 5,22, N 2,68. (гидрат). Найдено, %: С 64,71, Н 4,99, N 2,58. Пример 6: -6,7-Метилендиокси-4-(3,4 метилендиоксибензил)-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,4-метилендиоксибензальдегида и соединения, описанного в синтезе А. Температура плавления: 260 С. 12 Элементный анализ. Вычислено, %: С 63,38, Н 4,95, N 2,55 (гидрат). Найдено, %: С 63,72, Н 4,73, N 2,51 Пример 7. -6,7-Метилендиокси-4-(3,4,5 триметоксибензил)-9-(3,4,5-триметоксифенил)4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,4,5 триметоксибензальдегида и соединения, описанного в синтезе А. Температура плавления: 190 С. Элементный анализ. Вычислено, %: С 63,47, Н 5,50, N 2,39. (полугидрат). Найдено, %: С 63,58, Н 5,59, N 2,65. Пример 8. -4-(3,5-Диметокси-4-гидроксибензил)-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин 1(3 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,5-диметокси-4-гидроксибензальдегида и соединения,описанного в синтезе А. Температура плавления: 242 С. Элементный анализ. Вычислено, %: С 63,94, Н 5,19, N 2,49. Найдено, %: С 63,72, Н 5,21, N 2,46. Пример 9. -4-(2-Гидроксиэтил)-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Стадия A. N-(3,4-метилендиоксифенил)-2 аминоэтанол. К 10 ммолям 3,4-метилендиоксианилина,растворенного в этаноле, добавляют 27 ммолей ацетата натрия и 15 ммолей 2-бромэтанола. Через 24 ч кипячения с обратным холодильником реакционную смесь охлаждают до комнатной температуры, добавляют воду и затем водную фазу экстрагируют дихлорметаном. Органические фазы объединяют, растворитель упаривают, и сырой остаток очищают колоночной хроматографией на силикагеле, используя в качестве элюента смесь дихлорметан/этилацетат(10:90), получают ожидаемый продукт в виде масла. Стадия В. -4-(2-Гидроксиэтил)-6,7 метилендиокси-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, полученного на предыдущей стадии, и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 61,33, Н 5,37, N 3,11. (полугидрат). Найдено, %: С 61,54, Н 5,28, N 2,94. Пример 10. -6,7-Метилендиокси-4(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4b]хинолин-1(3H)-он. 13 Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиокси-анилина и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 63,47, Н 4,82, N 3,52. Найдено, %: С 63,32, Н 4,86, N 3,45. Пример 11. -6,7-Метилендиокси-4-пропил-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 9, исходя из 3,4-метилендиоксианилина, пропилбромида и соединения, описанного в синтезе А. Температура плавления: 230 С. Пример 12. -4-(N,N-Диметиламинопропил)-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 9, исходя из 3,4-метилендиоксианилина, 3-хлор-1 диметиламинопропана и соединения, описанного в синтезе А. Температура плавления: 182 С. Пример 13. -4,9-Бис-(3,4,5-триметоксифенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Стадия A. N-(3,4-метилендиоксифенил)3,4,5-триметоксианилин. К растворенным в толуоле 10 ммолям 3,4 метилендиоксианилина добавляют 10 ммолей 3,4,5-триметоксийодбензола, 0,4 ммоля ацетата палладия, 0,4 ммоля 2,2'-бис(дифенилфосфино)1,1'-бинафтила и 14 ммолей трет.-бутилата калия. После нагревания в течение 15 мин при температуре 100 С реакционную смесь доводят до комнатной температуры и затем добавляют дихлорметан и воду. Органическую фазу отделяют и перегоняют при пониженном давлении. Остаток очищают хроматографией на силикагеле, используя в качестве элюента дихлорметан,получают названное соединение в виде масла. ИК-спектр (пленка): 3361, 2934, 1602, 1503,1488, 1232, 1204, 1128, 1037, 930 и 813 см-1. Стадия В. -4,9-Бис-(3,4,5-триметоксифенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b] хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, полученного на предыдущей стадии, и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 62,93, Н 5,28, N 2,44. (полугидрат). Найдено, %: С 62,73, Н 5,11, N 2,21. Пример 14. -6,7-Диметокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3 Н)-он. 14 Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-диметоксианилина и соединения, описанного в синтезе А. Температура плавления: 218 С. Пример 15: -9-(3,5-Диметокси-4-гидроксифенил)-4-метил-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, описанного на стадии А примера 1, и соединения, описанного в синтезе В. Температура плавления: 250 С. Элементный анализ. Вычислено, %: С 60,72, Н 4,85, N 3,37. (гидрат). Найдено, %: С 60,78, Н 4,99, N 3,14. Пример 16. -9-(3,5-Диметокси-4-гидроксифенил)-6,7-метилендиокси-4-(4-нитробензил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, описанного на стадии А примера 3, и соединения, описанного в синтезе В. Температура плавления: 193 С. Элементный анализ. Вычислено, %: С 61,48, Н 4,30, N 5,31. (полугидрат). Найдено, %: С 61,61, Н 4,36, N 5,11. Пример 17: -4-(4-Хлорбензил)-9-(3,5 диметокси-4-гидроксифенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 4-хлорбензальдегида и соединения, описанного в синтезе В. Температура плавления: 252 С. Пример 18. -9-(3,5-Диметокси-4-гидроксифенил)-4-(3-гидроксибензил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3-гидроксибензальдегида и соединения, описанного в синтезе В. Температура плавления: 220 С. Элементный анализ. Вычислено, %: С 62,79, Н 5,07, N 2,71. (С 27 Н 23NO81,5 Н 2O). Найдено, %: С 62,44, Н 4,89, N 2,75. Пример 19. -9-(3,5-Диметокси-4-гидроксифенил)-6,7-метилендиокси-4-(3,4-метилендиоксибензил)-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,4-метилендиоксибензальдегида и соединения, описанного в синтезе В. Температура плавления: 260 С. 15 Элементный анализ. Вычислено, %: С 63,88, Н 4,59, N 2,66: (полугидрат). Найдено, %: С 63,89, Н 4,51, N 2,69. Пример 20. -9-(3,5-Диметокси-4-гидроксифенил)-6,7-метилендиокси-4-(3,4,5-триметоксибензил)-4,9-дигидрофуро[3,4-b]хинолин 1(3 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,4,5-триметоксибензальдегида и соединения, описанного в синтезе В. Температура плавления: 165 С. Элементный анализ. Вычислено, %: С 59,21, Н 5,63, N 2,30. (C30H29NO102,5H2O). Найдено, %: С 59,22, Н 5,51, N 2,34. Пример 21. -4-(3,5-Диметокси-4-гидроксибензил)-9-(3,5-диметокси-4-гидроксифенил)6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 3,5-диметокси-4-гидроксибензальдегида и соединения,описанного в синтезе В. Температура плавления: 235 С. Элементный анализ. Вычислено, %: С 62,36, Н 5,05, N 2,51 (полугидрат). Найдено, %: С 62,16, Н 4,96, N 2,34. Пример 22. -9-(3,5-Диметокси-4-гидроксифенил)-4-(2-гидроксиэтил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, описанного на стадии А примера 9, и соединения, описанного в синтезе В. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 60,55, Н 5,08, N 3,21 (полугидрат). Найдено, %: С 60,84, Н 5,05, N 3,11. Пример 23. -9-(3,5-Диметокси-4-гидроксифенил)-6-метил-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из м-толуидина и соединения,описанного в синтезе В. Пример 24. -6,7-Метилендиокси-9-(3 пиридил)-4,9-дигидрофуро-[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе С. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 64,35, Н 4,13, N 8,83 (полугидрат). Найдено, %: С 64,14, Н 4,15, N 8,61. Пример 25. -6,7-Этилендиокси-9-(3-метокси-4,5-метилендиоксифенил)-4-[(2-тиенил) 16 метил]-4,9-дигидрофуро[3,4-b]хинолин-1(3H)он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-этилендиоксианилина, тиофен-2 карбоксальдегида и соединения, описанного в синтезе D. Пример 26. -4-(Диметиламиноэтилкарбонил)-9-(3-метокси-4,5-метилендиоксифенил)6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 9, исходя из 3,4-метилендиоксианилина, 3-(диметиламино)пропионилхлорида и соединения, описанного в синтезе D. Пример 27. -6-Метокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3-метоксианилина, и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 65,79, Н 5,52, N 3,65. Найдено, %: С 65,80, Н 5,60, N 3,50. Пример 28. -6,7,8-Триметокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4,5-триметоксианилина, и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 61,05, Н 5,79, N 3,09. Найдено, %: С 61,19, Н 6,02, N 3,00. Пример 29. -6-Гидрокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3-аминофенола и соединения,описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 64,25, Н 5,26, N 3,74. (0,25 Н 2O). Найдено, %: С 64,41, Н 5,24, N 3,62. Пример 30. -6,8-Диметокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,5-диметоксианилина и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 63,91, Н 5,61, N 3,39. Найдено, %: С 63,85, Н 5,77, N 3,24. 17 Пример 31. -6,7-Метилендиокси-9-(2,3,4-триметоксифенил)-4,9-дигидрофуро[3,4-b] хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе Е. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 63,47, Н 4,82, N 3,52. Найдено, %: С 63,57, Н 4,91, N 3,34. Пример 32. -9-(3,4-Диметоксифенил)6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе F. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 65,39, Н 4,66, N 3,81. Найдено, %: С 64,87, Н 4,73, N 3,52. Пример 33. -9-(3-Гидрокси-4-метоксифенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе G. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 64,59, Н 4,28, N 3,96. Найдено, %: С 64,75, Н 4,25, N 3,76. Пример 34. -9-(4-Метоксифенил)-6,7 метилендиокси-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе Н. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 67,65, Н 4,48, N 4,15. Найдено, %: С 67,98, Н 4,43, N 3,95. Пример 35. -9-(3-Метоксифенил)-6,7 метилендиокси-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина, и соединения, описанного в синтезе I. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 67,65, Н 4,48, N 4,15. Найдено, %: С 67,48, Н 4,49, N 3,97. Пример 36. -6,7-Метилендиокси-9-фенил-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе J. Температура плавления: 260 С. 18 Элементный анализ. Вычислено, %: С 70,35, Н 4,26, N 4,56. Найдено, %: С 70,28, Н 4,18, N 4,38. Пример 37. -9-(2-Фурил)-6,7-метилендиокси-4,9-дигидрофуро-[3,4-b]хинолин-1(3H)он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе К. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 64,65, Н 3,73, N 4,71. Найдено, %: С 62,25, Н 3,87, N 4,31. Пример 38. -7-(3,4,5-Триметоксифенил)7,11-дигидробензо[h]-фуро[3,4-b]хинолин-8(10 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 1-нафтиламина и соединения,описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 69,89, Н 5,34, N 3,39. (полугидрат). Найдено, %: С 70,28, Н 5,40, N 3,31. Пример 39. -11-(3,4,5-Триметоксифенил)-7,11-дигидробензо[f]-фуро[3,4-b]хинолин 10(8 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 2-нафтиламина и соединения,описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 71,45, Н 5,25, N 3,47. Найдено, %: С 69,90, Н 5,44, N 3,44. Пример 40. -6,7-Метилендиокси-9-(3,4,5-триметоксифенил)-2,3,4,9-тетрагидроциклопента[b]хинолин-1-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе L. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 66,07, Н 5,42, N 3,50. (0,25 Н 2O). Найдено, %: С 66,09, Н 5,34, N 3,36. Пример 41: -6,7-Метилендиокси-9-(3,4 метилендиоксифенил)-4,9-диридрофуро[3,4-b] хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе М. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 64,96, Н 3,73, N 3,99. Найдено, %: С 65,12, Н 4,19, N 3,75. Пример 42. -10-(3,4,5-Триметоксифенил)-1,6,7,10-тетрагидро-9 Н-фуро[3,4-b]пирроло[2,3-f]хинолин-9-он. 19 Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 1 Н-индол-6-амина и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 65,10, Н 5,34, N 6,90. (0,75 Н 2O). Найдено, %: С 65,25, Н 5,23, N 6,50. Пример 43. -4-Бензил-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, бензальдегида и соединения, описанного в синтезе А. Температура плавления: 236 С. Элементный анализ. Вычислено, %: С 68,98, Н 5,17, N 2,87. Найдено, %: С 68,95, Н 5,27, N 2,83. Пример 44. -9-(4-Хлорфенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе N. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 62,24, Н 3,77, N 4,03. (полугидрат). Найдено, %: С 62,33, Н 3,90, N 3,90. Пример 45. -6,7-Метилендиокси-9-(4 нитрофенил)-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе О. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 60,59, Н 3,53, N 7,85. (0,25 Н 2O). Найдено, %: С 60,86, Н 3,57, N 7,62. Пример 46. -6,7-Метилендиокси-9-(3 нитрофенил)-4,9-дигидрофуро[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе Р. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 60,59, Н 3,53, N 7,85. Найдено, %: С 60,30, Н 3,65, N 7,69. Пример 47. -9-(3,5-Диметокси-4-гидроксифенил)-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе В. Температура плавления: 260 С. 20 Элементный анализ. Вычислено, %: С 61,93, Н 4,55, N 3,61. (0,25 Н 2O). Найдено, %: С 61,93, Н 4,59, N 3,34. Пример 48. -9-(4-Диметиламинофенил)6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе Q. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 67,69, Н 5,25, N 7,89. (0,25 Н 2O). Найдено, %: С 67,52, Н 5,29, N 7,69. Пример 49. -6,7-Этилендиокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-этилендиоксианилина и соединения, описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 63,53, Н 5,21, N 3,37. (0,25 Н 2O). Найдено, %: С 63,56, Н 5,18, N 3,39. Пример 50. -4-Метил-6,7-метилендиокси-9-(4-пиридил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из соединения, описанного на стадии А примера 1, и соединения, описанного в синтезе R. Температура плавления: 255 С. Элементный анализ. Вычислено, %: С 66,15, Н 4,47, N 8,57. (моногидрат). Найдено, %: С 65,88, Н 4,48, N 8,42. Пример 51. -6,7-Метилендиокси-9-(2 пиридил)-4,9-дигидрофуро-[3,4-b]хинолин 1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3,4-метилендиоксианилина и соединения, описанного в синтезе S. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 66,34, Н 3,92, N 9,08. Найдено, %: С 66,68, Н 4,12, N 8,91. Пример 52. -13-(3,5-Диметокси-4-гидроксифенил)-4,13-дигидронафто[2,3-f]фуро[3,4-b] хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 2-антриламина и соединения,описанного в синтезе В. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 71,32, Н 5,35, N 2,91. (СН 3 ОН). Найдено, %: С 71,10, Н 5,72, N 2,72. Пример 53. -13-(3,4,5-Триметоксифенил)-4,13-дигидронафто-[2,3-f]фуро[3,4-b]хинолин-1(3H)-он. 21 Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 2-антриламина и соединения,описанного в синтезе А. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 72,72, Н 5,23, N 3,03. (полугидрат). Найдено, %: С 73,05, Н 5,73, N 2,71. Пример 54. -6,7-Метилендиокси-4-(4 пиридилметил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, изоникотинового альдегида и соединения, описанного в синтезе А. Температура плавления: 240 С. Элементный анализ. Вычислено, %: С 66,38, Н 4,95, N 5,73. Найдено, %: С 66,24, Н 4,97, N 5,71. Пример 55. -6,7-Метилендиокси-4-(2 пиридилметил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, 2-пиридинкарбоксальдегида и соединения, описанного в синтезе А. Температура плавления: 258 С. Элементный анализ. Вычислено, %: С 66,38, Н 4,95, N 5,73. Найдено, %: С 66,25, Н 5,01, N 5,72. Пример 56. -7-(3,4,5-Триметоксифенил)7,9,10,11-тетрагидро-8 Н-бензо[h]циклопента[b]хинолин-8-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 1-нафтиламина и соединения,описанного в синтезе L. Температура плавления: 250 С. Элементный анализ. Вычислено, %: С 74,79, Н 5,77, N 3,49. Найдено, %: С 74,46, Н 6,37, N 3,09. Пример 57. -6-Метокси-9-(3,4,5-триметоксифенил)-2,3,4,9-тетрагидро-1 Н-циклопента[b]хинолин-1-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 3-метоксианилина и соединения, описанного в синтезе L. Температура плавления: 254 С. Элементный анализ. Вычислено, %: С 68,47, Н 6,14, N 3,63. (0,25 Н 2O). Найдено, %: С 68,41, Н 6,30, N 3,43. Пример 58. -6,7-Метилендиокси-4-(2 тиенилметил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, тиофен-2 карбоксальдегида и соединения, описанного в синтезе А. 22 Температура плавления: 230 С. Элементный анализ. Вычислено, %: С 62,70, Н 4,75, N 2,81. (0,25 Н 2O). Найдено, %: С 62,83, Н 4,58, N 2,77. Пример 59. -6,7-Метилендиокси-4-(3 тиенилметил)-9-(3,4,5-триметоксифенил)-4,9 дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 3, исходя из 3,4-метилендиоксианилина, тиофен-3 карбоксальдегида и соединения, описанного в синтезе А. Температура плавления: 238 С. Элементный анализ. Вычислено, %: С 63,27, Н 4,70, N 2,84. Найдено, %: С 63,12, Н 4,70, N 2,71. Пример 60. (+)-4-Метил-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают разделением рацемической смеси Примера 1 методом ВЭЖХ на хиральной колонке. Пример 61. (-)-4-Метил-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. Ожидаемый продукт получают разделением рацемической смеси примера 1 методом ВЭЖХ на хиральной колонке. Пример 62. -6-(3,4,5-Триметоксифенил)2,3,4,6,9,10-гексагидро-7 Н-фуро[3,4-b]пирано[3,2-g]хинолин-7-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 7-хроманамина и соединения,описанного в синтезе А. Пример 63. -9-(3,4,5-Триметоксифенил)2,3,6,9-тетрагидродифуро[3,4-b:2,3-g]хинолин 8(5 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной на стадии В примера 1, исходя из 2,3-дигидро-1-бензофуран-5 амина и соединения, описанного в синтезе А. Пример 64. -9-Бензил-6,7-метилендиокси-4,9-дигидрофуро[3,4-b]хинолин-1(3H)-он. К растворенным в этаноле 10 ммолям 3,4 метилендиоксианилина добавляют 10 ммолей фенилацетальдегида и 10 ммолей тетроновой кислоты, затем реакционную смесь кипятят с обратным холодильником в течение ночи. После доведения до комнатной температуры полученный остаток фильтруют и промывают этанолом, получают ожидаемый продукт. Пример 65. -6,7-Метилендиокси-9(3,4,5-триметоксифенил)-3,4,9,10-тетрагидро 1(2 Н)акридинов. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 64,исходя из 3,4-метилендиоксианилина, 3,4,5 триметоксибензальдегида и 1,3-циклогександиона. Пример 66. -6,7-Метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидротиено[3,4-b] хинолин-1(3H)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 64,исходя из 3,4-метилендиоксианилина, 3,4,5 триметоксибензальдегида и тиотетроновой кислоты. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 61,00, Н 4,63, N 3,39. Найдено, %: С 60,84, Н 4,66, N 3,55. Пример 67. -7-(3,4,5-Триметоксифенил)7,11-дигидробензо[h]-тиено[3,4-b]хинолин-8(10 Н)-он. Ожидаемый продукт получают в соответствии с методикой, описанной в примере 64,исходя из 1-нафтиламина, 3,4,5-триметоксибензальдегида и тиотетроновой кислоты. Температура плавления: 260 С. Элементный анализ. Вычислено, %: С 68,13, Н 5,19, N 3,27. Найдено, %: С 68,48, Н 5,60, N 3,02. Фармакологическое изучение соединений настоящего изобретения Пример 68. Цитотоксичность in vitro. Изучены три линии клеток:- 1 линия клеток мышиной лейкемии,L1210,- 1 линия клеток немелкоклеточного рака легких человека, А 549,- 1 линия клеток рака толстой кишки человека, НТ 29. Клетки культивируют в полной культуральной среде RPMI 1640, содержащей 10% сыворотки плода крупного рогатого скота, 1 мМ глутамина, 50 ед./мл пенициллина, 50 мкг/мл стрептомицина и 10 мМ Hepes (N-2 гидроксиэтилпиперазин-N'-2-этансульфоновая кислота), рН = 7,4. Клетки распределяют в микропланшеты и подвергают воздействию цитотоксических соединений. Клетки затем инкубируют в течение 2 дней (L1210) или в течение 4 дней (А 549, НТ 129). Затем количество жизнеспособных клеток определяют с помощью калориметрического анализа с тетразолием - Microculture Tetrazolium Assay (Cancer Res. 1987,47, 939-942). Полученные результаты представлены в виде IС 50 - концентрации цитотоксического агента, которая ингибирует пролиферацию обработанных клеток на 50%. Например, соединения примеров 1, 8 и 10 имеют значения IC50,которые представлены в таблице: Испытуемое соединение Пример 1 Пример 8 Пример 10 Пример 69. Активность in vivo. Противоопухолевая активность соединений в отношении Р 388 лейкемии. 24 Линия клеток Р 388 (клетки мышиной лейкемии) поставляется Национальным Институтом Рака (Frederick, США). Опухолевые клетки(106 клеток) инокулируют на нулевой день в брюшинную полость самки мыши BDF1 (IffaCredo, Франция) весом от 18 до 20 г (группа из 6 животных). Исследуемые продукты вводят внутрибрюшинно на 1-ый день (Д 1). Противоопухолевую активность выражают в виде % О/К: Среднее время жизни обработанных животных%O/К=х 100 Среднее время жизни контрольных животных Например, соединение примера 1 активно в дозе от 50 мг/кг и делает возможным увеличение в 2 раза количества выживающих обработанных животных (О/К 200 %). Пример 70. Фармацевтическая композиция. Рецептура (состав) для получения 1000 таблеток, каждая из которых содержит: Активный ингредиент, соединение примера 1 Гидроксипропилцеллюлозу Пшеничный крахмал Лактозу Стеарат магния Тальк гдепредставляет собой одинарную или двойную связь,R0 представляет собой атом водорода, гидроксильную группу или линейную или разветвленную (С 1-C6)алкоксигруппу,каждый из R1 и R2, которые могут быть одинаковыми или различными, представляет собой- атом водорода,- линейную или разветвленную(С 1-C6)алкильную группу,- линейную или разветвленную(С 1-C6)алкоксигруппу,- гидроксильную группу,- или вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, содержащую в кольце от 5 до 12 членов, необязательно содержащую 1 или 2 гетероатома, выбираемых из кислорода, серы или азота,R3 представляет собой атом водорода или группу формулы R4, где R4 представляет собой- арильную группу,- линейную или разветвленную (С 1-C6)алкильную группу, необязательно замещенную арильной группой, гетероарильной группой,гидроксильной группой или группой формулыNR5R6, где каждый из заместителей R5 и R6, ко 25 торые одинаковы или различны, представляет собой линейную или разветвленную (С 1-С 6) алкильную группу или линейную или разветвленную (С 1-С 6)гидроксиалкильную группу,- или группу формулы COR7, где заместитель R7 представляет собой линейный или разветвленный (С 1-C6)алкил, необязательно замещенный группой формулы NR8R9, где каждый из заместителей R8 и R9, которые одинаковы или различны, представляет собой линейную или разветвленную (С 1-C6)алкильную группу или линейную или разветвленную (С 1-C6)гидроксиалкильную группу,X представляет собой атом кислорода или атом серы или группу -СН 2-или -СН 2-СН 2-,Ar представляет собой арил, гетероарил или арил-(С 1-С 6)алкильную группу, в которой алкил является линейным или разветвленным,при том, что по меньшей мере один из R0, R1 или R2 отличен от водорода; их оптические изомеры, их гидраты, сольваты, а также их аддитивные соли с фармацевтически приемлемой кислотой,где арил следует понимать как фенил, необязательно замещенный одной или более одинаковыми или разными атомами или группами,выбираемыми из атомов галогена и линейного или разветвленного (С 1-C6)алкила, гидроксигруппы, линейной или разветвленной (С 1-C6) алкоксигруппы, линейного или разветвленного(С 1-C6)полигалогеналкила, аминогруппы (необязательно замещенной одной или более линейными или разветвленными (С 1-С 6)алкильными группами), нитрогруппы, линейной или разветвленной (С 1-C6)ацильной или (С 1-C2)алкилендиоксигруппы; гетероарил следует понимать как ароматическую моноциклическую группу, содержащую в кольце от 5 до 6 членов и содержащую один гетероатом, выбираемый из кислорода, азота и серы, где гетероарильная группа может быть необязательно замещена одной или более одинаковыми или разными атомами или группами,выбираемыми из атомов галогена и групп линейного или разветвленного (С 1-C6)алкила, гидроксигруппы, линейной или разветвленной (С 1 С 6)алкоксигруппы, линейного или разветвленного (С 1-C6)полигалогеналкила и аминогруппы(необязательно замещенной одной или более линейными или разветвленными (С 1-C6)алкильными группами). 2. Соединение формулы (I) по п.1, где представляет собой двойную связь. 3. Соединение формулы (I) по любому из пп.1 или 2, где R0 представляет собой атом водорода. 4. Соединение формулы (I) по любому из пп.1-3, где каждый из заместителей R1 и R2, которые одинаковы или различны, представляет собой- линейную или разветвленную (С 1-C6)алкильную группу,- линейную или разветвленную (С 1-C6)алкоксигруппу,- гидроксильную группу. 5. Соединение формулы (I) по любому из пп.1-3, где заместители R1 и R2 вместе с несущими их атомами углерода образуют ароматическую или неароматическую, моно- или бициклическую группу, имеющую в кольце от 5 до 12 членов и содержащую 1 или 2 гетероатома, выбираемых из кислорода, серы и азота. 6. Соединение формулы (I) по п.5, где заместители R1 и R2 вместе с несущими их атомами углерода образуют группу формул G3 или G4 7. Соединение формулы (I) по п.5, где заместители R1 и R2 вместе с несущими из атомами углерода образуют группу фенилена. 8. Соединение формулы (I) по любому из пп.1-7, где X представляет собой атом кислорода. 9. Соединение формулы (I) по любому из пп.1-7, где X представляет собой атом серы. 10. Соединение формулы (I) по любому из пп.1-7, где X представляет собой группу -СН 2 или -СН 2-СН 2-. 11. Соединение формулы (I) по любому из пп.1-10, где Ar представляет собой арильную группу. 12. Соединение формулы (I) по любому из пп.1-10, где Ar представляет собой гетероарильную группу. 13. Соединение формулы (I) по п.11, где Ar представляет собой фенильную группу. 14. Соединение формулы (I) по п.1, которое представляет собой -4-метил-6,7-метилендиокси-9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин-1(3H)-он, а также его оптические изомеры и его гидраты и сольваты. 15. Соединение формулы (I) по п.1, которое представляет собой -6,7-метилендиокси 9-(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4-b]-хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 16. Соединение формулы (I) по п.1, которое представляет собой -6-метокси-9-(3,4,5 триметоксифенил)-4,9-дигидрофуро-[3,4-b]хинолин-1(3H)-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 17. Соединение формулы (I) по п.1, которое представляет собой -7-(3,4,5-триметоксифенил)-7,11-дигидробензо[h]фуро-[3,4-b] хинолин-8(10 Н)-он, его оптические изомеры,его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 18. Соединение формулы (I) по п.1, которое представляет собой -6,7-метилендиокси 9-(3,4,5-триметоксифенил)-2,3,4,9-тетрагидроциклопента[b]хинолин-1-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 19. Соединение формулы (I) по п.1, которое представляет собой -6,7-этилендиокси-9(3,4,5-триметоксифенил)-4,9-дигидрофуро[3,4b]хинолин-1(3H)-он, его оптические изомеры,его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 20. Соединение формулы (I) по п.1, которое представляет собой -7-(3,4,5-триметоксифенил)-7,9,10,11-тетрагидро-8 Н-бензо[h] циклопента[b]хинолин-8-он, его оптические изомеры, его гидраты и сольваты, а также его аддитивные соли с фармацевтически приемлемой кислотой. 21. Способ получения соединений формулы (I) по п.1, отличающийся тем, что соединение формулы (II) где заместители R0, R1, R2 и R3 имеют те же значения, что определены для формулы (I),реагирует с соединением формулы (III) где X и Ar имеют те же самые значения,что определены для формулы (I),с образованием соединения формулы (Iа),представляющего собой частный случай соединений формулы (I) где R0, R1, R2, R3, X и Ar имеют определенные выше значения,которое затем восстанавливают, если необходимо, до соединения (Ib), представляющего собой частный случай соединений формулы (I) где R0, R1, R2, R3, X и Ar имеют определенные выше значения,и причем соединения формул (Iа) и (Ib),которые составляют все соединения формулы(I), очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют, если это желательно, на их оптические изомеры в соответствии с обычными методиками разделения и превращают, если это желательно, 28 в их аддитивные соли с фармацевтически приемлемой кислотой. 22. Способ получения соединений формулы (I) по п.1, отличающийся тем, что в одном сосуде взаимодействуют соединение формулы где R0, R1, R2 и R3 имеют те же значения,что определены для формулы (I), соединение формулы (VIII) где Ar принимает те же значения, что и в формуле (I), и соединение формулы (IX) где X принимает те же значения, что и в формуле (I), с образованием соединения формулы (Iа), представляющего собой частный случай соединений формулы (I) где R0, R1, R2, R3, X и Ar имеют определенные выше значения,которое затем восстанавливают, если это необходимо, до соединения (Ib), представляющего собой частный случай соединений формулы (I): где R0, R1, R2, R3, X и Ar имеют определенные выше значения,причем соединения формул (Iа) и (Ib), которые составляют все соединения формулы (I),очищают, если это необходимо, в соответствии с обычными методиками очистки, разделяют,если это желательно, на их оптические изомеры в соответствии с обычными методиками разделения и превращают, если это желательно, в их аддитивные соли с фармацевтически приемлемой кислотой. 23. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по любому из пп.1-20 само по себе или в сочетании с одним или более фармацевтически приемлемыми инертными, нетоксичными носителями. 24. Применения фармацевтической композиции по п.23 для получения противораковых лекарственных средств.
МПК / Метки
МПК: A61P 35/00, A61K 31/4741, C07D 491/056
Метки: содержащие, способ, композиции, получения, фармацевтические, 4-b]хинолин-1-оны, новые, дигидрофуро[3
Код ссылки
<a href="https://eas.patents.su/15-3996-novye-digidrofuro3-4-bhinolin-1-ony-sposob-ih-polucheniya-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Новые дигидрофуро[3, 4-b]хинолин-1-оны, способ их получения и содержащие их фармацевтические композиции</a>
Предыдущий патент: Производные 1-арил- и пиридилпиразола с пестицидными свойствами
Следующий патент: Способ синтеза производных (1h)-бензо[c]хинолизин-3-онов
Случайный патент: Малатная соль n-(4-{[6,7-бис-(метилокси)хинолин-4-ил]окси}фенил)-n'-(4-фторфенил)циклопропан-1,1-дикарбоксамида и ее кристаллические формы для лечения рака












