Конъюгаты белок-полимер и способ лечения инфекции вируса гепатита c или гепатита b
Формула / Реферат
1. Конъюгат белок-полимер формулы I
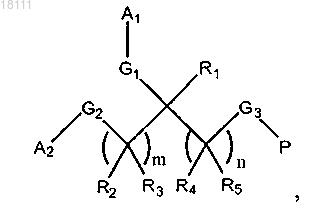
в которой каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5алкил, С2-5алкенил, C2-5алкинил, арил, гетероарил, C3-8циклоалкил или C3-8гетероциклоалкил;
каждый из А1 и А2 независимо представляет собой полиэтиленгликоль;
каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу;
Р представляет собой белковый фрагмент;
m равно 0 или целому числу 1-10 и
n равно целому числу 1-10.
2. Конъюгат по п.1, в котором G3 представляет собой связь, а Р представляет собой белковый фрагмент, в котором аминогруппа N-конца связана с G3.
3. Конъюгат по п.2, в котором каждый из A1 и А2 представляет собой фрагмент mPEG с молекулярной массой 10-30 кДа.
4. Конъюгат по п.3, в котором каждый из G1 и G2 представляет собой
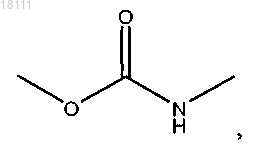
где О связан с A1 или А2, a NH связан с атомом углерода, как показано в формуле I.
5. Конъюгат по п.4, в котором Р представляет собой фрагмент модифицированного интерферона, содержащий 1-4 дополнительных аминокислотных остатка на N-конце.
6. Конъюгат по п.5, в котором n равно 2.
7. Конъюгат по п.6, который представляет собой

где молекулярная масса mPEG составляет 20 кДа, a IFN представляет собой фрагмент интерферона-α2b.
8. Способ лечения инфекции вируса гепатита С или инфекции вируса гепатита В, включающий введение нуждающемуся в этом субъекту эффективного количества конъюгата белок-полимер формулы I
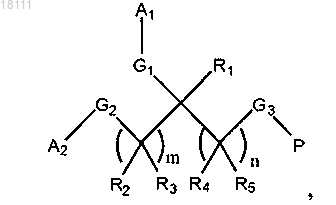
в которой каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5алкил, C2-5алкенил, С2-5 алкинил, арил, гетероарил, С3-8циклоалкил или C3-8гетероциклоалкил;
каждый из А1 и А2 независимо представляет собой полиэтиленгликоль;
каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу;
Р представляет собой фрагмент интерферона;
m равно 0 или целому числу 1-10 и
n равно целому числу 1-10.
Текст
КОНЪЮГАТЫ БЕЛОК-ПОЛИМЕР И СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИИ ВИРУСА ГЕПАТИТА C ИЛИ ГЕПАТИТА B Данное изобретение относится к конъюгатам белок-полимер формулы I в которой каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5 алкил,C2-5 алкенил, С 2-5 алкинил, арил, гетероарил, C3-8 циклоалкил или C3-8 гетероциклоалкил; каждый изA1 и А 2 независимо представляет собой полиэтиленгликоль; каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу; Р представляет собой белковый фрагмент; m равно 0 или целому числу 1-10 и n равно целому числу 1-10. Кроме того, описан способ получения конъюгата белок-полимер и способ лечения инфекции вируса гепатита С или гепатита В. Уровень техники Прогресс в клеточной биологии и технологиях рекомбинатных белков привел к развитию белковой терапии. Тем не менее, все еще существуют большие трудности. Большинство белков чувствительны к протеолитическому расщеплению и, следовательно, имеют короткое время полужизни в циркуляционной системе. Другие недостатки включают низкую растворимость в воде и стимулирование нейтрализующих антител. Связывание полимера, например полиэтиленгликоля (PEG), с белком затрудняет доступ протеолитических ферментов к остову белка, приводя к повышенной стабильности белка. Кроме того, это может также повысить растворимость в воде и свести к минимуму иммуногенность. Таким образом, существует потребность в эффективных способах связывания полимера с белками. Краткое описание Один из аспектов настоящего изобретения относится, по существу, к чистому (80% чистоты) конъюгату, содержащему один или более полимерных фрагментов, белковый фрагмент и линкер. В конъюгате полимерный фрагмент или фрагменты связаны с линкером; атом азота N-конца белкового фрагмента связан с линкером; линкер представляет собой ковалентную связь, C1-10 алкилен, C2-10 алкенилен или C2-10 алкинилен; и белковый фрагмент представляет собой фрагмент интерферона-, фрагмент человеческого гормона роста или фрагмент эритропоэтина. Предпочтительно чистота конъюгата составляет 90% или выше. Данный конъюгат имеет неожиданно продолжительное время полужизни in vivo. Другой аспект настоящего изобретения относится к конъюгатам белок-полимер формулы I в которой каждый из R1; R2, R3, R4 и R5 независимо представляет собой H, C1-5 алкил, С 2-5 алкенил, С 2-5 алкинил, арил, гетероарил, C3-8 циклоалкил или C3-8 гетероциклоалкил; каждый из A1 и A2 независимо представляет собой полиэтиленгликоль; каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу; P представляет собой белковый фрагмент; m равно 0 или целому числу 1-10 и n равно целому числу 1-10. Ссылаясь на приведенную выше формулу, конъюгат белок-полимер может иметь один или более следующих признаков: G3 представляет собой связь, а Р представляет собой белковый фрагмент, в котором аминогруппа на N-конце связана с G3; A1 и А 2 представляют собой полиалкиленоксидные группы с молекулярной массой 2-100 кДа (предпочтительно 10-30 кДа), каждый из G1 и G2 представляет собой(где О связан с A1 или A2, a NH связан с атомом углерода, как показано в формуле I) или каждый из G1 и G2 представляет собой мочевину, сульфонамид или амид (в котором N связан с атомом углерода, как показано в формуле I), m равно 4, n равно 2, каждый из R1, R2, R3, R4 и R5 представляет собой Н; и Р представляет собой фрагмент интерферона или фрагмент модифицированного интерферона, содержащий 1-4 дополнительных аминокислотных остатка. Термин "алкил" относится к одновалентному линейному или разветвленному углеводородному радикалу. Примеры алкильных групп включают метил, этил, н-пропил, изопропил, трет-бутил и н-пентил. Аналогичным образом, термин "алкенил" или "алкинил" относится к одновалентному линейному или разветвленному углеводородному радикалу, содержащему одну или более C=C двойных связей или одну или более CC тройных связей. Термин "алкилен" относится к двухвалентному линейному или разветвленному углеводородному радикалу. Аналогичным образом, термин "алкенилен" или "алкинилен" относится к двухвалентному линейному или разветвленному углеводородному радикалу, содержащему одну или более C=C двойных связей или одну или более CC тройных связей. Термин "арил" относится к углеводородной кольцевой системе (моноциклической или бициклической), содержащей по меньшей мере одно ароматическое кольцо. Примеры арильных групп включают,но не ограничиваются ими, фенил, нафтил и пиренил. Термин "гетероарил" относится к углеводородной кольцевой системе (моноциклической или бициклической), имеющей по меньшей мере одно ароматическое кольцо, которое содержит по меньшей мере один гетероатом, такой как О, N или S, как часть кольцевой системы, а остальные атомы являются атомами углерода. Примеры гетероарильных групп включают, но не ограничиваются ими, фурил, пирролил, тиенил, оксазолил, имидазолил, тиазолил, пиридинил, пиримидинил, хиназолинил и индолил. Термин "циклоалкил" относится к частично или полностью насыщенной моноциклической или би-1 018111 циклической кольцевой системе, содержащей в кольце только атомы углерода. Примеры включают, но не ограничиваются ими, циклопропанил, циклопентанил и циклогексанил. Термин "гетероциклоалкил" относится к частично или полностью насыщенной моноциклической или бициклической кольцевой системе, содержащей помимо атомов углерода один или более гетероатомов (например, О, N или S) в качестве атомов кольца. Примеры включают, но не ограничиваются ими,пиперидин, пиперазин, морфолин, тиоморфолин и 1,4-оксазепан. Упомянутые в настоящем описании алкил, алкенил, алкинил, арил, гетероарил, циклоалкил и гетероциклоалкил включают как замещенные, так и незамещенные группы. Примеры заместителей включают С 1-С 10 алкил, С 2-С 10 алкенил, С 2-С 10 алкинил, С 3-С 8 циклоалкил, С 5-С 8 циклоалкенил, С 1-С 10 алкокси,арил, арилокси, гетероарил, гетероарилокси, амино, С 1-С 10 алкиламино, С 1-С 20 диалкиламино, ариламино,диариламино, гидроксиамино, алкоксиамино, С 1-С 10 алкилсульфонамид, арилсульфонамид, гидрокси,галоген, тио, С 1-С 10 алкилтио, арилтио, циано, нитро, ацил, ацилокси, карбоксил и эфир карбоновой кислоты. Термин "полиалкиленоксидная группа" относится к одновалентному радикалу, полученному из линейного, разветвленного или звездообразного полиалкиленоксида. Молекулярная масса полиалкиленоксидной группы может составлять 2-100 кДа. Полиалкиленоксидная группа является либо насыщенной, либо ненасыщенной. Примеры полиалкиленоксидной группы включают, но не ограничиваются ими, полиэтиленоксид, полиэтиленгликоль, полиизопропиленоксид,полибутиленоксид и их сополимеры. Для замены полиалкиленоксидной группы можно также использовать другие полимеры, такие как декстран, поливиниловые спирты, полиакриламиды или полимеры на основе углеводов, если они не являются антигенными, токсичными или вызывающими иммунную реакцию. Полиалкиленоксидная группа является либо насыщенной, либо ненасыщенной. Например, она может представлять собой полиэтиленгликоль с концевой метоксигруппой (mPEG). Термин "белковая группа" относится к одновалентному радикалу, полученному либо из природного белка, либо из модифицированного белка. Природный белок может представлять собой интерферон-,интерферон-, человеческий гормон роста, эритропоэтин и гранулоцитарный колоннестимулирующий фактор или антитело. Модифицированный белок может представлять собой, например, белок, содержащий интерферон- и 1-4 дополнительных аминокислотных остатков на N-конце интерферона. Примером при этом IFN представляет собой группу интакого модифицированного интерферона является терферона-2b, аминогруппа на N-конце которого связана с карбонильной группой. Термин "интерферон-" относится к семейству высокогомологичных видоспецифических белков,которые ингибируют вирусную репликацию и клеточную пролиферацию и модулируют иммунную реакцию. См. Bonnem et al., J. Biol. Response Mod., 1984, 3(6):580-598 и Finter, J. Hepatol., 1986, 3 Suppl 2:S157-160. Многие виды белков интерферона- являются коммерчески доступными, включая интерферон Intron-A, предоставляемый Schering Corporation, Kenilworth, N.J., интерферон Roferon, предоставляемыйHoffmann-La Roche, Nutley, N.J., интерферон Berofor 2, предоставляемый Boehringer Ingelheim Pharmaceutical, Inc., Ridgefield, Conn., Sumiferon, предоставляемый Sumimoto, Japan, и интерферон Wellferon n1 (INS), предоставляемый Glaxo-Wellcome Ltd., London, Great Britain. Ниже перечислены аминокислотные последовательности пяти приведенных в качестве примера белков интерферона- человека либо в форме предшественника, либо в зрелой форме:(см. Lund et al., J. Interferon Res. 5 (2), 229-238, 1985). В одном из примеров белок интерферон-, используемый для получения конъюгата по настоящему изобретению, имеет аминокислотную последовательность, по меньшей мере на 80% (например, 85, 90,-2 018111 95 или 99%) идентичную одной из перечисленных выше аминокислотных последовательностей или ее фрагменту, соответствующему зрелому интерферону-. Термин "человеческий гормон роста" относится к природному человеческому гормону роста либо в форме предшественника, либо в зрелой форме и его функциональным вариантам, т.е. имеющему аминокислотную последовательность, по меньшей мере на 80% (например, 85, 90, 95 или 99%) идентичную природному человеческому гормону роста и обладающему такой же физиологической активностью этого человеческого гормона роста. Аминокислотные последовательности природного человеческого гормона роста (в форме предшественника и в зрелой форме) приведены ниже:lvygasdsnv ydllkdleeg iqtlmgrled gsprtgqifk qtyskfdtns hnddallkny gllycfrkdm dkvetflriv qcrsvegscg f (зрелая форма). Эритропоэтин (ЕРО), вырабатываемый либо печенью, либо почками, представляет собой гликопротеиновый гормон, который регулирует эритропоэз или выработку эритроцитов. См. патент США 5621080. Аминокислотные последовательности ЕРО человека (в форме предшественника и в зрелой форме) приведены ниже:lvkssqpwep lqlhvdkavs glrslttllr algaqkeais ppdaasaapl rtitadtfrk lfrvysnflr gklklytgea crtgdr (зрелая форма). Эритропоэтиновый белок, используемый для получения конъюгата по настоящему изобретению,может представлять собой любой ЕРО белок либо в форме предшественника, либо в зрелой форме, вырабатываемый подходящими видами, например человеческий, мышиный, свиной и бычий. В одном из примеров эритропоэтиновый белок имеет аминокислотную последовательность, по меньшей мере на 80% (например, 85, 90, 95 или 99%) идентичную одной из приведенных выше аминокислотных последовательностей."Процентную идентичность" двух аминокислотных последовательностей определяют, используя алгоритм Karlin and Altschul Proc. Natl. Acad. Sci. USA 87:2264-68, 1990, модифицированный, как в публикации Karlin and Altschul Proc. Natl. Acad. Sci. USA 90:5873-77, 1993. Такой алгоритм включен в программы NBLAST и XBLAST (версия 2.0) Altschul, et al. J. Mol. Biol. 215:403-10, 1990. Исследование белка BLAST можно осуществить с использованием программы XBLAST, шкала=50, длина слова=3, для получения аминокислотных последовательностей, гомологичных молекулам белка по настоящему изобретению. При наличии промежутков между двумя последовательностями можно использовать GappedBLAST, как описано в публикации Altschul, et al., Nucleic Acids Res. 25(17):3389-3402, 1997. Применяя программы BLAST и Gapped BLAST, можно использовать значения параметров по умолчанию для соответствующих программ (например, XBLAST и NBLAST). Термин "линкерная функциональная группа" относится к двухвалентной функциональной группе,один из концов которой связан с полимерным фрагментом, а другой конец связан с белковым фрагментом. Примеры включают, но не ограничиваются ими, -O-, -S-, карбоксиэфирную, карбонильную, карбонатную, амидную, карбаматную, мочевинную, сульфонильную, сульфинильную, амино, имино, гидроксиамино, фосфонатную или фосфатную группу. Описанный выше конъюгат белок-полимер может находиться в свободной форме или в форме соли,если это применимо. Например, соль может быть образована анионом и положительно заряженной группой (например, амино) в конъюгате белок-полимер по настоящему изобретению. Подходящие анионы включают хлорид, бромид, йодид, сульфат, нитрат, фосфат, цитрат, метансульфонат, трифторацетат и ацетат. Аналогичным образом, соль может быть также образована катионом и отрицательно заряженной группой (например, карбоксилатной) в конъюгате белок-полимер по настоящему изобретению. Подходящие анионы включают ион натрия, ион калия, ион магния, ион кальция и катион аммония, такой как ион тетраметиламмония. Кроме того, конъюгат белок-полимер может содержать одну или более двойных связей или один или более асимметрических центров. Такой конъюгат может существовать в виде рацематов, рацемических смесей, индивидуальных энантиомеров, индивидуальных диастереомеров, диастереомерных смесей и изомерных форм с цис- или транс- или Е- или Z-двойной связью. Пример конъюгата белок-полимер по настоящему изобретению приведен ниже где молекулярная масса mPEG составляет 20 кДа, a IFN представляет собой фрагмент интерферона-2b. Еще один из аспектов данного изобретения относится к соединениям, которые пригодны для получения конъюгатов белок-полимер. Данные соединения имеют формулу II в которой X является реакционноспособной группой; каждый из A1 и А 2 независимо представляет собой полимерный фрагмент; или один из A1 и А 2 представляет собой полимерный фрагмент, а другой является реакционноспособной группой; каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу; каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5 алкил,C2-5 алкенил, C2-5 алкинил, арил, гетероарил, C3-8 циклоалкил, C3-8 гетероциклоалкил или -G4-X', при этомG4 представляет собой связь или линкерную функциональную группу, а X' является реакционноспособной группой; каждый m и n независимо равен 0 или целому числу 1-10; при условии, что если -G3-X представляет собой -CO(O)-N-сукцинимидил, то n равно целому числу 1-10. В одном из вариантов осуществления X, X', A1, A2, G1, G2, G3, G4, R1, R2, R3, R4, R5 и m определены выше, а n равно целому числу 1-10. Некоторые соединения формулы II имеют один или более следующих признаков: полимерный фрагмент может содержать одну или более реакционноспособных групп; G3 представляет собой связь, а Р представляет собой белковый фрагмент, в котором аминогруппа на N-конце связана с G3; A1 и А 2 представляют собой полиалкиленоксидные группы с молекулярной массой 2-100 кДа (предпочтительно 12-30 кДа), каждый из G1 и G2 представляет собой где О связан с A1 или А 2, a NH связан с атомом углерода, как показано в формуле I; m равно 4; n равно 1; каждый из R1, R2, R3, R4 и R5 представляет собой Н; и X представляет собой СН(=О) или X представляет собой уходящую группу (например, сукцинимидил или п-нитрофенокси). Термин "реакционноспособная группа" относится к функциональной группе, которая может взаимодействовать с другой функциональной группой таким образом, что она либо заменяется другой функциональной группой, либо связывается с другой функциональной группой. Реакционноспособная группа может быть уходящей группой, нуклеофильной группой, альдегидом или рецептором Михаэля. Термин "уходящая группа" относится к функциональной группе, которая способна отщепляться при непосредственном замещении или ионизации с парой электронов от одной из своих ковалентных связей (см., например, F.A. Carey and R.J. Sunberg, Advanced Organic Chemistry, 3rd Ed. Plenum Press,1990). Примеры уходящей группы включают, но не ограничиваются ими, метансульфонат, трифлат, птолуолсульфонат, йодид, бромид, хлорид, трифорацетат, сукцинимидил (Su), п-нитрофенокси и пиридин 2-илокси. Термин "нуклеофильная группа" относится к богатой электронами функциональной группе, которая взаимодействует с принимающей электроны группой, такой как электрофил, за счет передачи электронной пары. Термин "электрофильная группа" относится к обедненной электронами функциональной группе,которая взаимодействует с группой, являющейся донором электронов, такой как нуклеофил, за счет акцептирования электронной пары. Рецепторы Михаэля представляют собой подкласс электрофильных групп. При контакте с нуклеофилом они подвергаются реакции Михаэля. Типичный рецептор Михаэля содержит ,-ненасыщенную кетонную группу. Примеры соединений формулы II приведены ниже: В еще одном аспекте данное изобретение относится к способу получения конъюгатов белокполимер формулы I, где аминогруппа на N-конце белкового фрагмента Р связана с линкерной функциональной группой G3. Этот способ включает конденсацию свободного N-конца белка Н-Р с разветвленной молекулой диполимера, имеющей формулу, которая аналогична приведенной выше формуле II, за исключением того, что X является уходящей группой. Свободный N-конец белка Н-Р относится к белку, в котором атом азота терминальной аминогруппы белкового фрагмента Р связан с атомом водорода Н. Иными словами, Н-Р содержит терминальную первичную или вторичную аминогруппу. Альтернативно, данный способ включает (1) конденсацию только что упомянутого свободного Nконца белка Н-Р с разветвленной молекулой диполимера, имеющей формулу, которая аналогична приведенной выше формуле II, за исключением того, что G3 представляет собой связь, n равно 0 или целому числу 1-9, а X представляет собой СНО; и (2) восстановление продукта конденсации с образованием конъюгата белок-полимер. Интерферон представляет собой иммуномодулирующее средство для лечения инфекции вируса гепатита В (HBV) или инфекции вируса гепатита С (HCV). Кроме того, интерферон (например, интерферон-) можно использовать для лечения неходжкинской лимфомы, волосатоклеточного лейкоза, хронической миелогенной лейкемии, СПИД-ассоциированной саркомы Капоши, фолликулярной лимфомы,злокачественной меланомы и остроконечной кондиломы. Таким образом, следующий аспект данного изобретения относится к способу лечения любого из упомянутых выше нарушений с помощью описанного в данном документе конъюгата интерферон-полимер. Кроме того, в объем данного изобретения входит композиция, содержащая конъюгат интерферонполимер для применения при любом из упомянутых выше нарушений, а также данное терапевтическое применение и использование данного конъюгата для получения лекарственного средства для лечения одного из этих нарушений. Подробности одного или более вариантов осуществления изобретения представлены в приведенном ниже описании. Другие признаки, объекты и преимущества изобретения будут ясны из описания и формулы изобретения. Подробное описание Конъюгаты белок-полимер по настоящему изобретению можно получить методами синтеза, хорошо известными в области химии. Например, линкерную молекулу можно связать, одновременно или последовательно, с двумя полимерными молекулами, а затем связать молекулу белка с линкерной молекулой с образованием конъюгата белок-полимер по настоящему изобретению. В объем данного изобретения входят также соединения формулы (II). Данные соединения применимы для получения только что описанных конъюгатов белок-полимер. Их можно получить методами синтеза, хорошо известными в области химии. Иллюстративная схема синтеза и реальный пример приведены ниже. На схеме 1 показан пример получения конъюгатов белок-полимер по настоящему изобретению. Соединение диамина 1, которое содержит ацетальную группу, подвергают взаимодействию с Nгидроксисукцинимидилкарбонатом mPEG (т.е. соединением 2), получая дипегилированное соединение 3,которое затем преобразуют в альдегид 4. Данное альдегидное соединение подвергают взаимодействию с белком, содержащим свободную аминогруппу, путем восстановительного алкилирования, получая Синтезированный таким образом конъюгат белок-полимер можно дополнительно очистить таким способом, как ионообменная хроматография, гель-фильтрационная хроматография, электрофорез, диализ, ультрафильтрация или ультрацентрифугирование. Описанные выше химические реакции включают использование растворителей, реагентов, катализаторов, реагентов для введения защитной группы и снятия защитной группы и определенные условия реакций. Они могут дополнительно включать стадии или до, или после конкретно описанных здесь стадий, для введения или удаления подходящих защитных групп, чтобы, в конечном счете, обеспечить возможность синтеза конъюгата белок-полимер. Кроме того, для получения желательных конъюгатов белок-полимер различные стадии синтеза можно осуществить в другой последовательности или другом порядке. Синтетические химические преобразования и методики для защитных групп (введение и снятие защиты), пригодные для синтеза применимых конъюгатов белок-полимер, известны в данной области и включают, например, преобразования и методики, описанные в публикациях R. Larock, ComprehensiveSynthesis, 2d. Ed., John Wiley and Sons (1991); L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); and L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) и их последующие издания. Конъюгат по изобретению имеет очень высокую чистоту. А именно, в 80% или более молекул конъюгата полимерный фрагмент связан с одним и тем же атомом азота на N-конце одного и того же белкового фрагмента. Другими словами, по меньшей мере в 80% молекул конъюгата белковый фрагмент идентичен во всех аспектах, включая его последовательность и его положение связывания с полимерным фрагментом. Конъюгат по изобретению может быть фармацевтически активным в форме конъюгата. Альтернативно, он может высвобождать фармацевтически активный белок in vivo (например, при гидролизе) за счет ферментативного расщепления связи между белковым фрагментом и полимерным фрагментом. Примеры ферментов, участвующих в расщеплении связей in vivo, включают окислительные ферменты(например, пероксидазы, аминоксидазы или дегидрогеназы), восстановительные ферменты (например,кеторедуктазы) и гидролитические ферменты (например, протеазы, эстеразы, сульфатазы или фосфатазы). Таким образом, один из аспектов данного изобретения относится к способу введения эффективного количества одного или более описанных выше конъюгатов белок-полимер для лечения заболевания (например, инфекций HBV или HCV). Конкретно, заболевание можно лечить введением субъекту одного или более конъюгатов белок-полимер в эффективном количестве. Такой субъект может быть выявлен специалистом в области здравоохранения на основании результатов любого подходящего диагностического метода. Как используется в настоящем описании, термин "лечить" или "лечение" определяют как применение или введение композиции, содержащей конъюгат белок-полимер, субъекту (человеку или животному), имеющему нарушение, симптом заболевания, заболевание или нарушение, вторичное по отношению к заболеванию, или предрасположение к заболеванию с целью лечения, облегчения, ослабления или устранения нарушения, симптома заболевания, заболевания или нарушения, вторичного по отношению к заболеванию, или предрасположения к заболеванию. "Эффективное количество" относится к количеству конъюгата белок-полимер, которое оказывает терапевтический эффект на подлежащего лечению субъекта. Терапевтический эффект может быть объективным (т.е. определяемым при помощи некоторых тестов или маркеров) или субъективным (т.е. субъект обнаруживает признак или ощущает эффект). В объем данного изобретения также входит фармацевтическая композиция, содержащая эффективное количество по меньшей мере одного из описанных выше конъюгатов белок-полимер и фармацевтически приемлемый носитель. Кроме того, данное изобретение включает способ введения эффективного количества одного или более конъюгатов белок-полимер пациенту с одним или более заболеваниями. Эффективные дозы будут изменяться, как признают специалисты в данной области, например, в зависимости от скорости гидролиза конъюгата белок-полимер, типов заболеваний, подлежащих лечению, пути введения, использования эксципиента и возможности совместного использования с другим терапевтическим лечением. Для осуществления на практике способа по настоящему изобретению композицию, содержащую одно или более из упомянутых выше соединений, можно вводить парентерально, перорально, назально,ректально, местно или буккально. Используемый в описании термин "парентерально" относится к подкожной, внутрикожной, внутривенной, внутримышечной, внутрисуставной, внутриартериальной, интрасиновиальной, внутригрудинной, интратекальной, внутрирубцовой, внутрибрюшинной, интратрахеальной или внутричерепной инъекции, а также к любому подходящему инфузионному способу. Стерильная композиция для инъекций может представлять собой раствор или суспензию в нетоксичном, парентерально применимом разбавителе или растворителе, например раствор в 1,3-бутаноле. В число приемлемых носителей и растворителей, которые можно использовать, входят маннит, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды удобно использовать жирные масла (например, синтетические моно- или диглицериды). Для получения инъекционных препаратов пригодна жирная кислота, такая как олеиновая кислота и ее глицеридные производные, как природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных вариантах. Данные растворы или суспензии в масле могут также содержать разбавитель или диспергатор на основе длинноцепочечного спирта или карбоксиметилцеллюлозу, или аналогичное диспергирующее вещество. Для цели препарата можно использовать другие обычно используемые поверхностно-активные вещества, такие как Tween или Span, или другие аналогичные эмульгаторы, или усилители биодоступности, которые обычно используют при производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм. Композиция для перорального введения может представлять собой любую перорально приемлемую лекарственную форму, включая капсулы, таблетки, эмульсии и водные суспензии, дисперсии и растворы. В случае таблеток обычно используемые носители включают лактозу и кукурузный крахмал. Также обычно добавляют смазывающее вещество, такое как стеарат магния. Для перорального введения в форме капсулы пригодные разбавители включают лактозу и сухой кукурузный крахмал. Если водные суспензии или эмульсии вводят перорально, то активный ингредиент может быть суспендирован или растворен в масляной фазе в сочетании с эмульгирующими или суспендирующими агентами. При желании можно добавить подслащивающие, вкусовые или окрашивающие агенты. Назальная аэрозольная или ингаляционная композиция может быть получена в соответствии с методикой, которая хорошо известна в области фармацевтических составов. Например, такую композицию можно приготовить в виде раствора в солевом растворе, используя бензиловый спирт или другие подходящие консерванты, усилители абсорбции для повышения биодоступности, фторуглероды и/или другие солюбилизирующие или диспергирующие агенты, известные в данной области. Композицию, содержащую один или более из описанных выше соединений, можно также вводить в виде суппозиториев для ректального введения. По стандартной методике фармацевтически приемлемый носитель используют с одним или более активными соединениями, упомянутыми выше. Носитель в фармацевтической композиции должен быть"приемлемым" в смысле его совместимости с активным ингредиентом композиции (и предпочтительно способности стабилизировать активный ингредиент) и не быть опасным для подлежащего лечению субъекта. В качестве фармацевтических эксципиентов для доставки упомянутого выше соединения можно использовать один или более солюбилизирующих агентов. Примеры других носителей включают коллоидный оксид кремния, стеарат магния, целлюлозу, лаурилсульфат натрия и DC Yellow10. Для предварительной оценки эффективности описанных выше конъюгатов для ингибирования вируса гепатита В или вируса гепатита С можно использовать подходящие анализы in vitro. Конъюгаты можно дополнительно исследовать на предмет их эффективности для лечения инфекции вируса гепатита В или вируса гепатита С при помощи анализов in vivo. Например, их можно вводить животному (например, на мышиной модели) или человеку с инфекцией вируса гепатита В или вируса гепатита С, а затем оценить их терапевтические эффекты. Исходя из этих результатов, можно также определить диапазоны доз и пути введения. Приведенный ниже пример следует истолковывать лишь как иллюстративный, а не ограничиваю-7 018111 щий каким бы то ни было образом оставшуюся часть описания. Без дополнительной доработки предполагается, что на основании приведенного описания специалист в данной области использует настоящее изобретение в его наиболее полной степени. Все цитированные в настоящем описании публикации включены путем ссылки во всей своей полноте. Получение ди-PEG альдегида.PEGO(C=O)OSu 20 кДа получали из mPEGOH 20 кДа, приобретенного у (SunBio Inc., CA, США),по методике, описанной в Bioconjugate Chera. 1993, 4, 568-569. Раствор 6-(1,3-диоксолан-2-ил)гексан-1,5-диамина в дихлорметане (11,97 г раствора, содержащего 9,03 мг диамина, 47,8 мкмоль) добавляли в колбу, содержащую PEGO(C=O)OSu 20 кДа (1,72 г, 86,0 мкмоль). После полного растворения PEGO(C=O)OSu добавляли N,N-диизопропилэтиламин (79 мкл, 478 мкмоль). Реакционную смесь перемешивали при комнатной температуре в течение 24 ч, а затем добавляли по каплям при перемешивании метил-трет-бутиловый эфир (200 мл). Полученный осадок собирали и сушили в вакууме, получая ди-PEG ацеталь (1,69 г, 98%) в виде твердого вещества белого цвета. 1 Н ЯМР (400 МГц, d6-ДМСО)7,16 (т, J=5,2 Гц, 1 Н), 7,06 (д, J=8,8 Гц, 1 Н), 4,76 (т, J=4,8 Гц, 1 Н),4,10-3,95 (м, 4 Н), 1,80-1,65 (м, 1 Н), 1,65-1,50 (м, 1 Н), 1,48-1,10 (м, 6 Н). Ди-PEG ацеталь (4,0 г, 0,2 ммоль) суспендировали в буфере с рН 2,0 (лимонная кислота, 40 мл). Реакционную смесь перемешивали при 35C в течение 24 ч, а затем экстрагировали дихлорметаном (350 мл). Объединенные органические слои сушили над сульфатом магния, концентрировали, а затем повторно растворяли в дихлорметане (20 мл). Данный раствор добавляли по каплям при перемешивании к метил-трет-бутиловому эфиру (400 мл). Полученный осадок собирали и сушили при пониженном давлении,получая ди-PEG альдегид (3,8 г, 95%) в виде твердого вещества белого цвета. 1 Модифицированный рекомбинантный человеческий интерферон-2b клонировали методом ПЦР с использованием геномной ДНК человека в качестве матрицы. Олигонуклеотиды синтезировали, исходя из фланкирующих последовательностей человеческого интерферона-2b ( доступа в GenBank J00207, 8 января 2008 г.). Полученные продукты ПЦР субклонировали в вектор pGEM-T (Promega). Вариант IFN вновь амплифицировали ПЦР при помощи клонов pGEM-T, а затем субклонировали в вектор экспрессии белка рЕТ-24 а (Novagen), вектор, управляемый промотором Т 7 РНК полимеразы, с использованиемBL21-CodonPlus (DE 3)-RIL (Stratagene). Клоны с высокой экспрессией отбирали, поддерживая трансформированный Е. coli BL21-CodonPlus (DE 3)-RIL в присутствии карамицина (50 мкг/мл) и хлорамфеникала (50 мкг/мл). Для размножения Е. coli BL21-CodonPlus (DE 3)-RIL с Pro-IFN геном использовали бульонную среду Terrific (BD, 200 мл) в колбе на 1000 мл. Колбу встряхивали при 37C и при 230 об/мин в течение 16 ч. Ферментацию в периодическом режиме и в периодическом режиме с подпиткой проводили в 5-литровом вибрационном ферментере (Bioflo 3000; New Brunswick Scientific Co., Edison, NJ). При ферментации в периодическом режиме использовали 150 мл прекультуры для посева, стоявшей в течение ночи, и 3 л бульонной среды Terrific с карамицином (50 мкг/мл), хлорамфеникалом (50 мкг/мл), 0,4% глицерина и 0,5% (об./об.) следовых элементов (10 г/л FeSO47H2O, 2,25 г/л ZnSO47H2O, 1 г/л CuSO45H2O, 0,5 г/лMnSO4H2O, 0,3 г/л Н 3 ВО 3, 2 г/л CaCl22 Н 2 О, 0,1 г/л (NH4)6Mo7O24, 0,84 г/л EDTA, 50 мл HCl). Концентрацию растворенного кислорода регулировали на уровне 35%, а pH поддерживали при 7,2 добавлением 5 н. водного раствора NaOH. Готовили питательный раствор, содержащий 600 г/л глюкозы и 20 г/лMgSO47H2O. Если значение pH превышало контрольную величину, то добавляли соответствующее количество питательного раствора для увеличения концентрации глюкозы в культуральном бульоне. Экспрессию гена Pro-IFN индуцировали, добавляя IPTG до конечной концентрации 1 мМ, и собирали клетки из культурального бульона после инкубирования в течение 3 ч. Собранные клеточные гранулы повторно суспендировали в TEN буфере (50 мМ Tris-HCl (рН 8,0), 1 мМ EDTA, 100 мМ NaCl) в соответствующем соотношении 1:10 (масса во влажном состоянии г/мл) и дробили с помощью микрофлюидизатора, а затем центрифугировали при 10000 об/мин в течение 20 мин. Гранулы, содержащие тельце включения (IB), дважды промывали TEN буфером и центрифугировали,как описано выше. Затем гранулы, содержащие IB, суспендировали в 150 мл 4 М водного раствора гуанидинияHCl (GuHCl) и центрифугировали при 20000 об/мин в течение 15 мин. После этого IB солюбилизировали в 50 мл 6 М раствора GuHCl. Солюбилизированный в GuHCl продукт центрифугировали при 20000 об/мин в течение 20 мин. Рефолдинг инициировали растворением денатурированного IB в 1,5 л свежеприготовленного рефолдингового буфера (100 мМ Tris-HCl (рН 8,0), 0,5 М L-аргинина, 2 мМEDTA), который перемешивали только во время добавления. Рефолдинговую реакционную смесь оставляли для инкубирования в течение 48 ч без перемешивания. Подвергшийся рефолдингу рекомбинантный человеческий интерферон-2b (т.е. Pro-IFN) диализировали против 20 мМ Tris буфера (с 2 мМ EDTA и 0,1 М мочевины, pH 7,0) для дополнительной очистки методом колоночной хроматографии на QSepharose. Подвергшийся рефолдингу рекомбинантный человеческий белок Pro-IFN загружали в колонку с QSepharose (GE Amersham Pharmacia, Pittsburg, PA). Колонку предварительно уравновешивали и промывали 20 мМ Tris-HCl буфером (рН 7,0). Продукт элюировали смесью 20 мМ Tris-HCl буфера (рН 7,0) и 200 мМ NaCl. Фракции, содержащие Pro-IFN, собирали, исходя из их поглощения при 280 нм. КонцентрациюPro-IFN определяли с помощью набора для анализа белков с использованием метода Бредфорда (Pierce,Rockford, IL). Получение конъюгата белок-полимер. К раствору полученного выше ди-PEG альдегида (1,2 г, 0,03 ммоль) в воде (72 мл) добавляли буфер 2 М фосфата натрия (pH 4,0, 5 мл) и Pro-IFN (200 мг в 22,2 мл буфера с pH 7,0, содержащего 20 мМ TrisHCl и 0,2 М NaCl, 0,01 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 10 мин, затем добавляли водный раствор цианоборгидрида натрия (400 мМ, 1,25 мл, 0,5 ммоль). Реакционную смесь перемешивали в темноте в течение 16 ч и очищали методом хроматографии SP XL наSepharose. Фракции, содержащие требуемый конъюгат полимер-белок, собирали, исходя из их времени удерживания и поглощения при 280 нм. Концентрацию конъюгата определяли с помощью набора для анализа белков с использованием метода Бредфорда (Pierce, Rockford, IL). Выход выделенного конъюгата составлял приблизительно 40% или более. Другие варианты осуществления. Все признаки, приведенные в данном описании, могут быть объединены в любой комбинации. Каждый признак, приведенный в данном описании, может быть заменен на альтернативный признак, служащий той же, эквивалентной или похожей цели. Таким образом, если специально не указано иное, каждый описанный признак является лишь примером общего ряда эквивалентных или похожих признаков. Из приведенного выше описания специалист в данной области легко сможет установить основные характеристики настоящего изобретения и, не выходя за пределы его сущности и объема, сможет произвести различные изменения и модификации данного изобретения, чтобы приспособить его к различным областям применения и условиям. Таким образом, другие варианты осуществления также входят в объем следующей формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Конъюгат белок-полимер формулы I в которой каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5 алкил, С 2-5 алкенил, C2-5 алкинил, арил, гетероарил, C3-8 циклоалкил или C3-8 гетероциклоалкил; каждый из А 1 и А 2 независимо представляет собой полиэтиленгликоль; каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу; Р представляет собой белковый фрагмент;m равно 0 или целому числу 1-10 иn равно целому числу 1-10. 2. Конъюгат по п.1, в котором G3 представляет собой связь, а Р представляет собой белковый фрагмент, в котором аминогруппа N-конца связана с G3. 3. Конъюгат по п.2, в котором каждый из A1 и А 2 представляет собой фрагмент mPEG с молекулярной массой 10-30 кДа. 4. Конъюгат по п.3, в котором каждый из G1 и G2 представляет собой где О связан с A1 или А 2, a NH связан с атомом углерода, как показано в формуле I. 5. Конъюгат по п.4, в котором Р представляет собой фрагмент модифицированного интерферона,содержащий 1-4 дополнительных аминокислотных остатка на N-конце. 6. Конъюгат по п.5, в котором n равно 2. 7. Конъюгат по п.6, который представляет собой где молекулярная масса mPEG составляет 20 кДа, a IFN представляет собой фрагмент интерферона-2b. 8. Способ лечения инфекции вируса гепатита С или инфекции вируса гепатита В, включающий введение нуждающемуся в этом субъекту эффективного количества конъюгата белок-полимер формулы I в которой каждый из R1, R2, R3, R4 и R5 независимо представляет собой H, C1-5 алкил, C2-5 алкенил, С 2-5 алкинил, арил, гетероарил, С 3-8 циклоалкил или C3-8 гетероциклоалкил; каждый из А 1 и А 2 независимо представляет собой полиэтиленгликоль; каждый из G1, G2 и G3 независимо представляет собой связь или линкерную функциональную группу; Р представляет собой фрагмент интерферона;m равно 0 или целому числу 1-10 иn равно целому числу 1-10.
МПК / Метки
МПК: A61K 47/48
Метки: конъюгаты, вируса, гепатита, способ, лечения, белок-полимер, инфекции
Код ссылки
<a href="https://eas.patents.su/11-18111-konyugaty-belok-polimer-i-sposob-lecheniya-infekcii-virusa-gepatita-c-ili-gepatita-b.html" rel="bookmark" title="База патентов Евразийского Союза">Конъюгаты белок-полимер и способ лечения инфекции вируса гепатита c или гепатита b</a>
Предыдущий патент: Пептиды с пониженным уровнем образования димеров
Следующий патент: Вагинальная система доставки
Случайный патент: Многослойный стеклопакет и способ его получения















