Фармацевтическая композиция блокатора натриевых каналов и селективного ингибитора обратного захвата серотонина
Номер патента: 13812
Опубликовано: 30.08.2010
Авторы: Немет Дьёрдь, Тарнава Иштван, Кочиш Паль, Тан Марта, Тиханьи Карой
Формула / Реферат
1. Фармацевтическая композиция, которая включает блокатор натриевых каналов, выбранный из группы, состоящей из ламотригина и кробенетина вместе с селективным ингибитором обратного захвата серотонина, выбранным из группы, состоящей из флуоксетина и сертралина.
2. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является ламотригином.
3. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является кробенетином.
4. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является ламотригином.
5. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является кробенетином.
6. Применение блокатора натриевых каналов, выбранного из группы, состоящей из ламотридина и кробенетина, и селективного ингибитора обратного захвата серотонина, выбранного из группы, состоящей из флуоксетина и сертралина, в способе получения фармацевтической композиции, пригодной для лечения и/или предупреждения заболеваний млекопитающих, которые вызваны хронической болью или эпилепсией, или симптомами или заболеваниями, вызванными расстройствами и/или поражением двигательной системы.
7. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является ламотригином.
8. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является кробенетином.
9. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является ламотригином.
10. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является кробенетином.
Текст
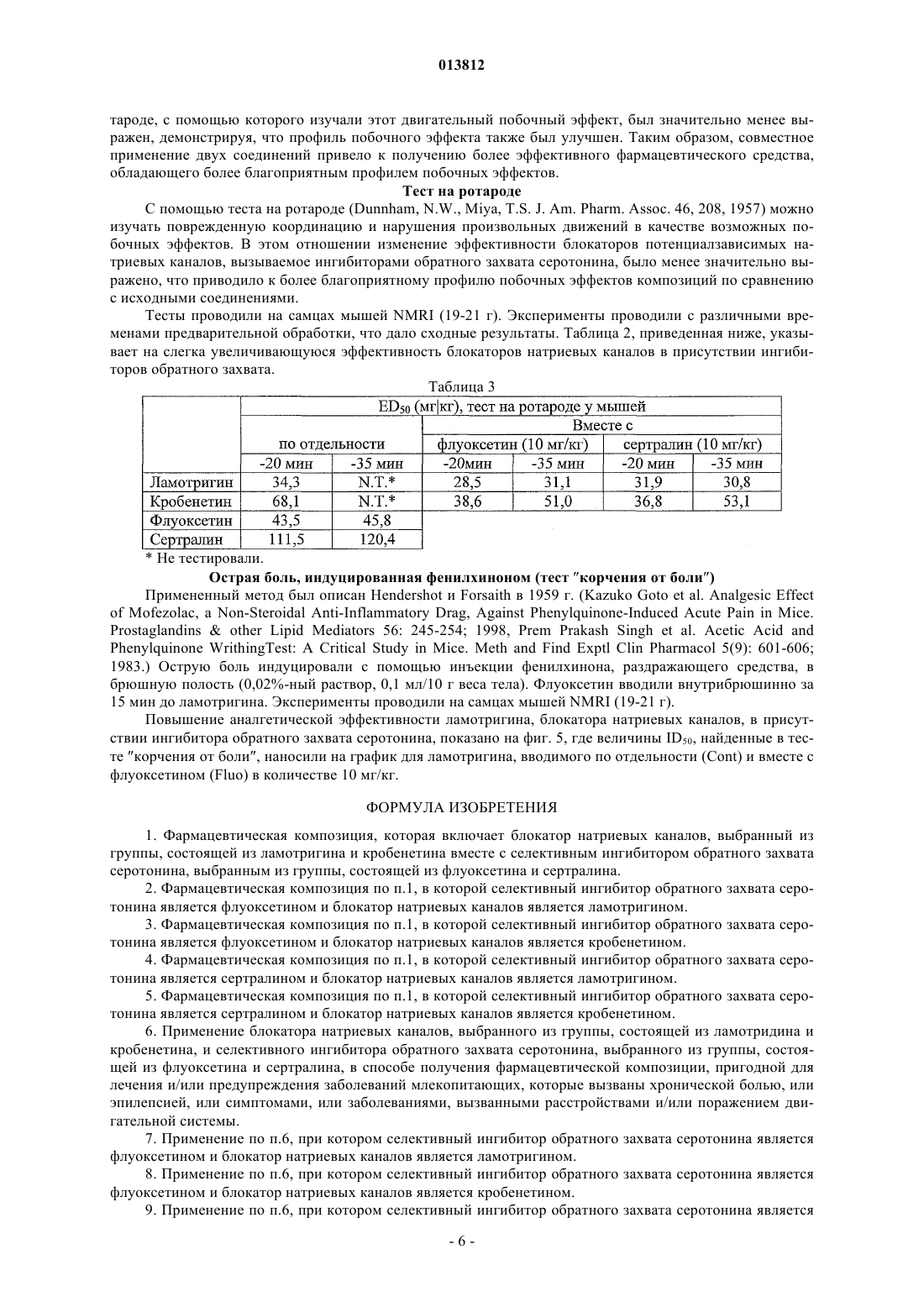
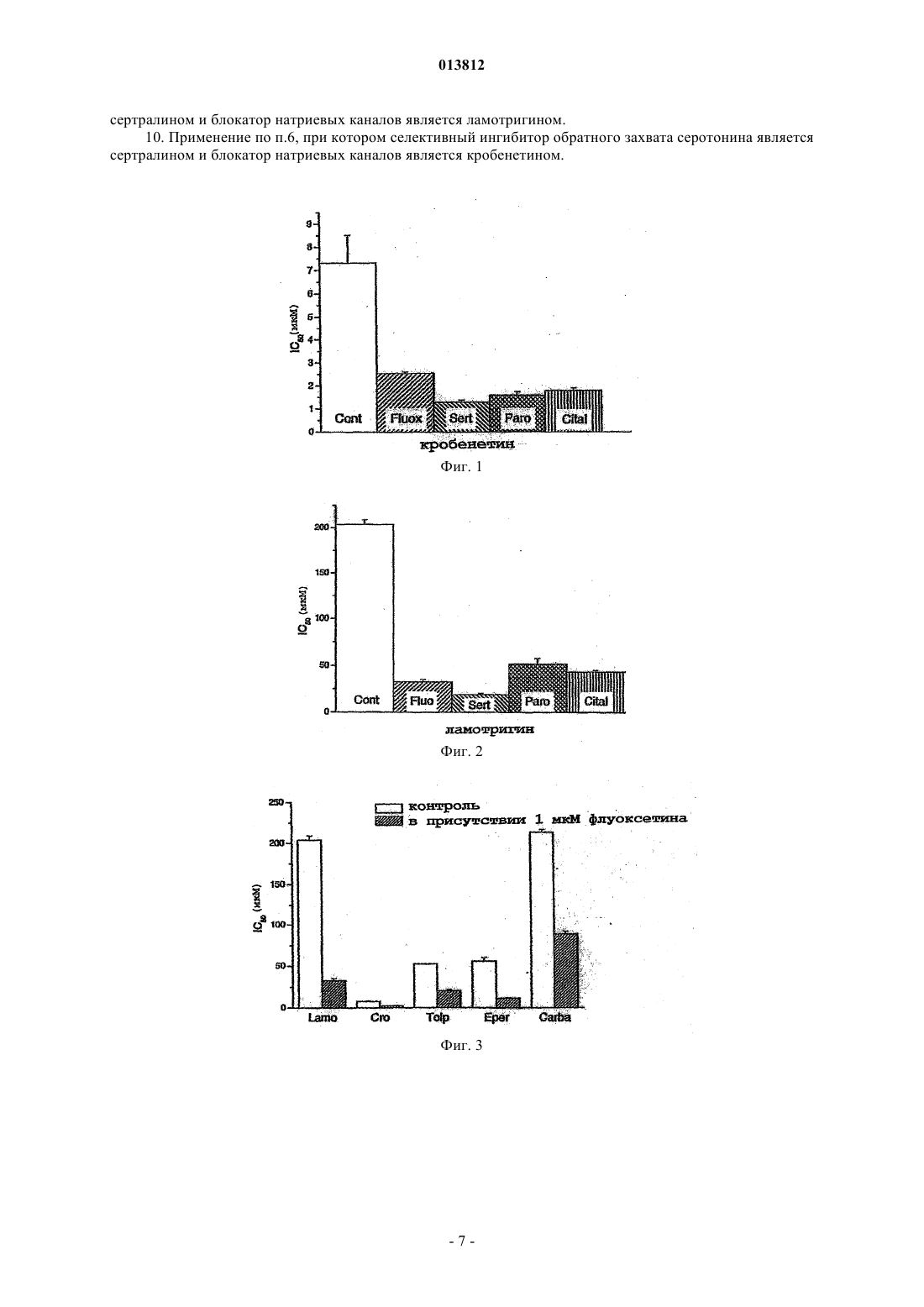
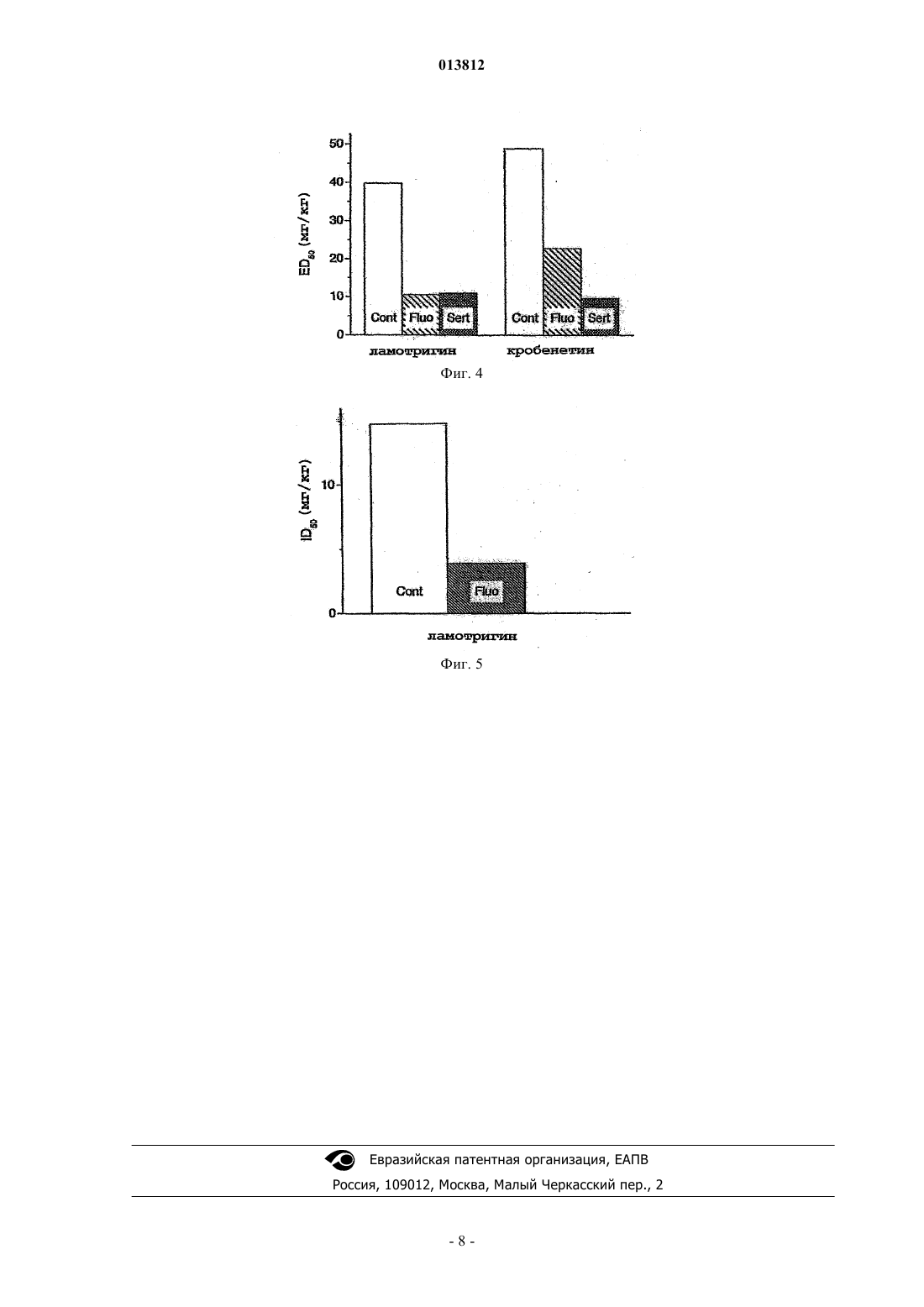
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ БЛОКАТОРА НАТРИЕВЫХ КАНАЛОВ И СЕЛЕКТИВНОГО ИНГИБИТОРА ОБРАТНОГО ЗАХВАТА СЕРОТОНИНА Настоящее изобретение имеет отношение к новым фармацевтическим композициям с улучшенным блокирующим эффектом в отношении натриевых каналов, содержащим блокатор натриевых каналов, выбранный из ламотридина или кробенетина, и селективный ингибитор обратного захвата серотонина, выбранный из флуоксетина или сертралина. Кроме этого, настоящее изобретение имеет отношение к применению указанных композиций при хронической боли, при нарушениях в двигательной системе, при эпилепсии, а также в других терапевтических областях, в которых принято применение блокаторов натриевых каналов.(71)(73) Заявитель и патентовладелец: РИХТЕР ГЕДЕОН ВЕДЬЕСЕТИ ДЬЯР РТ. 013812 Область техники, к которой относится изобретение Настоящее изобретение имеет отношение к новым фармацевтическим композициям с повышенным блокирующим эффектом на натриевые каналы. Кроме того, изобретение имеет отношение к применению фармацевтических композиций при хронической боли, при нарушениях в двигательной системе, при эпилепсии, а также в других терапевтических областях, в которых применяют блокаторы натриевых каналов. Уровень техники Известно, что потенциалзависимые натриевые каналы играют исключительно важную роль в генерации и проводимости потенциалов действия и, таким образом, в регулировании возбудимости нервных клеток. Натриевые каналы образуют поры в мембране нервных клеток, в ответ на деполяризацию мембраны каналы на короткое время открываются и позволяют ионам натрия входить в клетку, вызывая тем самым электрические преобразования. При некоторых заболеваниях нервной системы можно наблюдать изменение канальной функции, приводящее в основном к аномальному увеличению возбудимости нервных клеток. В продаже или на стадии разработки существуют лекарственные средства, которые обладают полезным эффектом при таких заболеваниях, направленным на блокирование потенциалзависимых натриевых каналов. Блокаторы натриевых каналов, например лидокаин, традиционно применяют как локальные анестетики. Некоторые структурно похожие вещества (например, мексилетин) применяют как антиаритмические средства. В настоящее время на стадии разработки находятся некоторые другие соединения, в том числе и кробенетин, для которого показано, что он эффективен даже при очень низких дозах (Carter, A.J.Natl. Acad. Sci. USA 97: 4944-4949; 2000). Оказалось, что последнее соединение также полезно против невропатической боли (Laird, J.M.A. et al. Analgesic activity of a novel use-dependent sodium channelblocker, crobenetine, in mono-arthritic rats. Br. J. Pharmacol. 134: 1742-1748; 2001). Некоторые другие блокаторы натриевых каналов эффективны против хронической боли (Hunter, J.С., Loughhead, D. Voltagegated sodium channel blockers for the treatment of chronic pain. Curr. Opin. CPNS Invest. Drags 1: 72-81; 1999). Рилузол, применяемый для лечения нейродегенеративных заболеваний, обладает тем же самым механизмом действия (Hurko, О., Walsh, F.S. Novel drag development for amyotrophic lateral sclerosis. J.Neurol. Sci. 180: 21-28; 2000). Недавно было обнаружено, что блокаторы натриевых каналов могут быть полезными при лечении заболеваний, сопровождающихся болезненными мышечными спазмами, затрудняющими нормальное движение пациентов (Kocsis, P. et al. Mydeton: a centrally acting muscle relaxant drugof Gedeon Richter Ltd. Acta Pharm Hung 72: 49-61; 2002). Другой возможной областью применения является церебральная ишемия, наследственные заболевания каналов, звон в ушах, мигрень и токсикомания(Clare, J.J., et al. Voltage-gated sodium channels as therapeutic targets. Drug Discov. Today 5: 506-520; 2000). Долгое время применяли некоторые антиэпилептики (фенитоин, карбамазепин). Активность, направленная на ингибирование натриевых каналов, признавалась главным компонентом механизма их действияvoltage-sensitive sodium channels in neuroblastoma cells. Molecular Pharmacology 27: 549-558, 1985). На основе этого механизма действия был разработан препарат ламотригин (Leach, M.J., et al. PharmacologicalDiscov. Today 5: 506-520; 2000). Исследования Leander показали, что флуоксетин усиливает противоконвульсионный эффект карбамазепина, фенитоина и амелтолида в тесте судорог при максимальном электрошоке (MES) у мышей(Leander, J.D. Fluoxetine, a selective serotonin-uptake inhibitor enhances the anticonvulsant effects of phenytoin, carbamazepine, and ameltolide (LY201116). Epilepsia 33: 573-576, 1992). Автор приходит к выводу,что флуоксетин может быть полезен при лечении пациентов с депрессией, у которых есть эпилептические проблемы, так как флуоксетин может усиливать эффект антиэпилептических средств, принимаемых одновременно с ним. Однако он не упоминает возможный механизм действия. Также, Raju et al. (Raju,S.S. et al. Effect of fluoxetine on maximal electroshock seizures in mice: acute vs. chronic administration. Pharmacological Research 39: 451-454, 1999) обнаружили, что кратковременно примененный флуоксетин вызывал уменьшение значения ED50 противосудорожного препарата фенитоина. С другой стороны, Dailey и соавт. в своих экспериментах обнаружили, что флуоксетин, применяемый сам по себе, демонстрировал противосудорожную активность (Dailey, J.W. et al. Neurochemical correlates of antiepileptic drugs in thegenetically epilepsy-prone rat (GEPR). Life Sciences 58: 259-266, 1996). Их последующие данные показали,что истощение по серотонину уменьшало эффективность некоторых антиэпилептических препаратов(карбамазепин, антиэпилепсирин), однако не оказывало влияния на эффективность фенитоина. С другой стороны, другие исследователи подчеркивали, что с точки зрения противосудорожного эффекта норадренергическая система является наиболее важной частью моноаминергической системы (Fisher, W., Muller, M. Pharmacological modulation of central monoaminergic systems and influence on the anticonvulsant effectiveness of standard antiepileptics in maximal electroshock seizure. Biomedica Biochimica Acta 47: 631-645,1988). В то время как симпатомиметики вызывали значительное повышение эффективности некоторых-1 013812 антиэпилептиков (фенитоин, карбамазепин), ослабление функции норадренергической системы приводило к уменьшению эффективности исследованных антиэпилептиков. В соответствии с этими результатами модуляция серотонергической системы не влияла существенным образом на эффективность антиэпилептиков. Время открытия натриевых каналов очень короткое (1-2 мс), так как после открытия они будут быстро инактивироваться. С помощью модификации процесса инактивации возбудимости можно более эффективно влиять на нервные клетки. Последние результаты показывают, что некоторые нейротрансмиттеры (например, ацетилхолин, серотонин, норадреналин) могут модулировать канальную функцию через рецепторы, сопряженные с G-белками (Carr, D.B. et al. Transmitter modulation of slow, activitydependent alterations in sodium channel availability endows neurons with a novel form of cellular plasticity.synaptic transmission in spinal lumbar dorsal horn of rat. Brain Res. Bull. 54: 639-647; 2001). Несмотря на то,что некоторые авторы сообщали о том, что агонисты серотониновых рецепторов могут непрямым образом ингибировать функцию натриевых каналов с помощью активации серотониновых рецепторов (Carr,D.B. et al. Serotonin receptor activation inhibits sodium current and dendritic excitability in prefrontal cortex viaa protein kinase C-dependent mechanism. J. Neurosci. 22: 6846-6855; 2002), они не исследовали возможный синергизм между блокаторами натриевых каналов и серотонергических агентов. С другой стороны,Rapeport сообщил о том, что синергизма между ингибиторами обратного захвата серотонина и блокаторами натриевых каналов обнаружено не было (Rapeport, W.G. et al. Absence of a sertraline-mediated effecton the pharmacokinetics and pharmacodynamics of carbamazepine. Journal of Clinical Psychiatry 57 (Suppl. 1): 20-23; 1996). Опубликованная патентная заявка US No 2002/0147196 A1 раскрывает благоприятный эффект комбинаций ингибиторов обратного захвата серотонина и блокаторов натриевых каналов при лечении невропатической боли. В кратком изложении, опубликованные экспериментальные данные, касающиеся возможного усиливающего эффекта ингибиторов обратного захвата серотонина на блокаторы натриевых каналов, противоречивы. В то время как в результате некоторых случайных комбинаций был обнаружен усиливающий эффект, другие результаты наводят на мысль о противоположной тенденции. Блокаторы натриевых каналов, однако, обладают некоторыми побочными эффектами, частью которых, как следствие, является собственно блокирование натриевых каналов, к ним относятся, например,побочные эффекты в сердечно-сосудистой системе (например, брадикардия, гипотония) или ЦНС (например, атаксия, успокоение). Другие побочные эффекты не имеют отношение к натриевым каналам и ассоциированы с их химической структурой, например высокие дозы ламотригина могут вызывать желудочно-кишечные заболевания, повреждение печени или заболевания кожи и т. д. Риск таких побочных эффектов можно уменьшить, если каким-либо образом снизить эффективную дозу лекарственного препарата. Очевидно, что для этой цели подходит комбинация с агентом, который усиливает действие блокаторов натриевых каналов. Раскрытие изобретения В наших экспериментах мы с удивлением обнаружили значительное увеличение активности, блокирующей натриевые каналы, если одновременно вводилось соединение, блокирующее поглощение серотонина; однако оказалось, что в отношении побочных эффектов эта усиливающая серотонергическая активность была менее значительной. В результате, фармацевтические композиции в соответствии с настоящим изобретением обладают более выгодными терапевтическими индексами по сравнению с блокаторами натриевых каналов, применяемых так, как они есть. Как показано в тесте на вращающемся стержне (ротарод), усиливающий эффект ингибиторов обратного захвата серотонина значительно менее выражен или может даже отсутствовать, и, таким образом, терапевтические индексы композиций значительно выше, чем в случае введения только блокаторов натриевых каналов. Например, терапевтический индекс ламотригина (ротарод ED50/MES ID50) составляет 7,6, тогда как в присутствии флуоксетина в количестве 10 мг/кг этот индекс возрастает примерно в три раза. Применение композиций в соответствии с настоящим изобретением может привести к успеху в терапии эпилепсии, а также в отношении побочных эффектов. Таким образом, объектом настоящего изобретения является новая фармацевтическая композиция,демонстрирующая повышенную активность в терапии заболеваний, которые являются терапевтическими мишенями для блокаторов натриевых каналов (например, хроническая боль, некоторые нарушения двигательной системы, эпилепсия, наркомания или хронический алкоголизм, недержание кала или мочи,воспаление, зуд, внутричерепной отек, ишемия и/или последующие повреждения, вызываемые реперфузией или ретинопатией, являющихся осложнением глаукомы), и обладающая более полезным профилем побочных эффектов по сравнению с профилем при применении только блокаторов натриевых каналов. В фармацевтических композициях в соответствии с настоящим изобретением эффективные терапевтические дозировки блокаторов натриевых каналов могут быть снижены и, соответственно, их клиническая эффективность может быть увеличена. Указанные фармацевтические композиции включают в качестве активного ингредиента блокатор натриевых каналов вместе с ингибитором обратного захвата серотонина.-2 013812 Блокаторы натриевых каналов для применения в фармацевтической композиции в соответствии с настоящим изобретением представляют собой соединения, для которых известен такой механизм действия. Примерами таких соединений являются ламотригин, кробенетин, карбамазепин, фенитоин, толперизон, эперизон, окскарбамазепин, фосфенитоин, предпочтительно ламотригин, окскарбамазепин, фосфенитоин или кробенетин. Дополнительно, смеси таких соединений, применяемые при осуществлении изобретения, также входят в объем притязаний настоящего изобретения. Ингибиторы обратного захвата серотонина, которые могут применяться, являются соединениями,для которых известен такой механизм действия. Предпочтительно применяют селективные ингибиторы обратного захвата серотонина, такие как флуоксетин, пароксетин, дулоксетин, сертралин, циталопрам,эсциталопрам, наиболее предпочтительно флуоксетин, сертралин или циталопрам. Дополнительно, смеси таких соединений, применяемые при осуществлении изобретения, также входят в объем притязаний настоящего изобретения. Применение солей, сольватов, кристаллических модификаций или стереоизомеров указанных блокаторов натриевых каналов или ингибиторов обратного захвата серотонина, а также их смесей также входят в объем притязаний настоящего изобретения. Фармацевтические композиции в соответствии с настоящим изобретением могут быть эффективными при лечении и/или предупреждении хронической боли (например, невропатической боли воспалительного или ревматического происхождения, невралгии тройничного нерва, головной боли, фибромиалгии) и синдрома воспаленного кишечника (IBS), при лечении и предупреждении заболеваний двигательной системы (например, при спастических заболеваниях, эссенциальном треморе, дистонии, звоне в ушах, экстрапирамидальных заболеваниях, тиках) и нейродегенеративных заболеваниях (например, приALS, ВИЧ-индуцированной деменции, синдроме Паркинсона, болезни Альцгеймера, хорее Хантингтона,множественном склерозе, прионовых болезнях, инсульте, повреждениях головного и спинного мозга,ишемии головного мозга), а также при лечении и предупреждении наркомании и хронического алкоголизма, недержании кала и мочи, воспалении, зуда, отека мозга, ишемии и/или последующего повреждения, вызванного реперфузией или ретинопатией, являющихся осложнением глаукомы, кроме того, при лечении и предупреждении различных форм эпилепсии, таких как парциальных приступы, например простые парциальные приступы (двигательные, соматосенсорные-сенсорные, автономные, психические симптомы), сложные парциальные приступы (парциальный приступ и/или потеря сознания) или парциальные приступы с вторичной генерализацией (генерализованные тонические или хронические приступы), генерализованные приступы, такие как абсанс (типичный или атипичный), миоклонус, клонические,тонико-клонические (grand mal, судорожные припадки) приступы, потеря тонуса (астатический приступ),а также последующие формы приступов, которые не поддаются классификации (International classification of epileptic seizures, Epilepsia, 22, 489-501, 1981). Указанные выше заболевания можно успешно лечить не только с помощью одновременного введения блокаторов натриевых каналов и ингибиторов обратного захвата серотонина (в этом случае указанные вещества могут входить в состав двух различных композиций или присутствовать в одной единственной композиции, то есть в комбинации), но также с помощью их последовательного введения, когда любой из активных ингредиентов может быть введен первым. Активные соединения или их фармацевтически приемлемые производные можно применять без составления композиции или предпочтительно в форме, пригодной для медицинского применения, в частности для лечения человека. В дополнение к активным соединениям, разработанным в подходящей форме, композиции могут содержать один или несколько фармацевтически приемлемых вспомогательных материалов. Композиции могут применяться в пероральной форме, парентеральной форме, включая внутривенную, подкожную, внутримышечную, ректальную формы, форму для местного нанесения, буккальную,кожную или сублингвальную формы, а также в формах, пригодных для ингаляции. Композиции, пригодные для перорального введения, могут быть в виде единичной дозированной формы, такой как капсулы, таблетки (например, жевательные таблетки для применения в педиатрии),могут быть в форме порошка или в гранулированной форме, в форме водного или неводного раствора или суспензии или в форме водно-масляной или масляно-водной эмульсии. Таблетки могут быть приготовлены в спрессованной или формованной форме, с необязательным использованием одного или нескольких вспомогательных материалов. Спрессованные таблетки получают с помощью подходящей таблетировочной машины, в которой порошкообразные или гранулированные активные ингредиенты необязательно смешивают с известными вспомогательными материалами,такими как связующие вещества, наполнители, смазывающие вещества, дезинтегрирующие вещества,увлажняющие агенты и ароматизаторы. Примерами связывающих веществ являются сироп, гуммиарабик, желатин, сорбит и поливинилпирролидон. Примерами наполнителей являются различные гидроксиметилцеллюлозные наполнители, лактоза, сахар, микрокристаллическая целлюлоза, кукурузный крахмал,фосфат кальция или гидроксиметилцеллюлоза. Примерами смазывающих веществ являются стеарат магния, стеариновая кислота, тальк, полиэтиленгликоль или силикагель. Примерами дезинтегрирующих веществ являются картофельный крахмал или гликолят натрия. Формованные таблетки могут быть полу-3 013812 чены из смеси порошкообразных активных соединений и инертного жидкого растворителя в подходящей формовочной машине. Таблетки необязательно могут быть покрыты оболочкой с помощью методов, известных в фармацевтической промышленности. Также можно получить таблетки с медленным или контролируемым высвобождением. Композиции для перорального введения могут также быть в жидкой форме, такой как водная или масляная суспензии, эмульсии, сиропы или эликсиры. Такие композиции можно получить также в сухой форме, которую можно перевести в жидкую форму с помощью подходящих способов непосредственно перед лечением. Указанные жидкие композиции могут содержать известные добавки, такие как суспендирующие вещества (сорбит, сироп, метилцеллюлоза, сироп глюкозы, желатин, гидроксиэтилцеллюлоза, карбоксиметилцеллюлоза, гель стеарата алюминия или пищевые гидрогенизированные жиры), эмульгирующие вещества (лецитин, моноолеат сорбита, гуммиарабик), неводные материалы (масло сладкого миндаля,фракционированное кокосовое масло, сложные эфиры, пропиленгликоль, этиловый спирт), консерванты(метил- или пропил-n-гидроксибензоат, сорбит) или ароматизирующие добавки. Композиции в форме суппозитория могут содержать традиционные связующие вещества, такие как масло какао, твердые жиры, полиэтиленгликоль или этиленгликоль или глицерин и их производные. Композиции для парентерального применения представляют собой водные или неводные растворы для инъекции и могут содержать антиоксиданты, буферы, бактерицидные вещества и соединения, растворенные в изотоническом растворе. Композицию затем помещают, например, в ампулы (в виде единичной дозировки или в виде нескольких дозировок) или могут хранить в лиофилизированной форме. Примерами композиций, пригодных для местного применения, являются крем, гель, мазь или трансдермальный пластырь. Примерами интраназальных композиций являются аэрозоли, порошки или капли. Композиция, пригодная для применения при лечении, может быть аэрозолем, содержащим в дополнение к активному ингредиенту газ-вытеснитель, такой как двуокись углерода, 1,1,1-трифторэтан,1,1,1,2,3,3,3-гептафторпропан и т.п. Осуществление изобретения Биологические данные Ингибирование спинального рефлекса Эксперименты проводились в соответствии с методами, описанными Otsuka и Konishi (Otsuka, M.,Konishi, S. Electrophysiology of mammalian spinal cord in vitro. Nature 252, 733-734; 1974), с небольшими модификациями (Kocsis, P. et al. Participation of AMPA-and NMDA-type excitatory amino acid receptors inthe spinal reflex transmission, in rat. Brain Research Bulletin 60: 81-91; 2003). L5 дорсальный корешок изолированного препарата надрезанного спинного мозга стимулировали с помощью супрамаксимального электрического импульса и записывали рефлекторный потенциал L5 вентрального корешка. Полученные различные компоненты рефлекторного потенциала хорошо различаются на базе их послестимульньгх латенций и продолжительности. Блокаторы натриевых каналов, в том числе и толперизон и эперизон, которые имеют много общего как в структуре, так и в активности, в основном демонстрируют значительный ингибиторный эффект на спинальный рефлекс в препарате надрезанного спинного мозга in vitro. Этот препарат идеален для исследования фармакодинамических взаимодействий между двумя веществами, так как метаболические факторы не участвуют в нем. Результаты приведены на фиг. 1, 2 и 3. А именно, на фиг. 1 показано усиливающее действие различных ингибиторов обратного захвата серотонина на рефлекторную ингибирующую активность кробенетина, показан блокатор натриевого канала. Cont (контроль) = собственно влияние кробенетина; а также его влияние в присутствии флуоксетина (Fluo; 1 мкМ), сертралина (Serf; 0,5 мкМ), пароксетина (Faro; 10 нМ) и циталопрама (Cital; 5 нМ). На фиг. 2 показано усиливающее действие различных ингибиторов обратного захвата серотонина на рефлекторную ингибирующую активность ламотригина, показан блокатор натриевого канала. Cont(контроль) = собственно влияние ламотригина; а также его влияние в присутствии флуоксетина (Fluo; 1 мкМ), сертралина (Serf; 0,5 мкМ), пароксетина (Faro; 10 нМ) и циталопрама (Cital; 5 нМ). На фиг. 3 показано усиливающее действие ингибитора обратного захвата серотонина (1 мкМ флуоксетин) на рефлекторную ингибирующую активность различных блокаторов натриевых каналов, где можно видеть рефлекторное ингибирующее действие ламотригина (Lamo), кробенетина (Cro), толперизона (Tolp), эперизона (Eper) и карбамазепина (Carba) в отсутствие и в присутствии 1 мкМ флуоксетина. Добавление ингибитора обратного захвата серотонина в каждом случае вызывало значительное повышение блокирующей активности, направленной на натриевые каналы. Также измеряли in vivo различия в эффективности блокаторов натриевых каналов при повышенном серотониновом тонусе, а именно их треморную ингибирующую активность анализировали в тесте на тремор, вызванный GYKI 20039.-4 013812 Тест на тремор Ингибирующее влияние на тремор, вызванный лекарственными средствами, у мышей является хорошим указанием эффективности соединений в качестве мышечных релаксантов у человека. Тремор может быть вызван введением GYKI 20039 (3-(2,6-дихлорфенил)-2-иминотиазолидина). Метод был опубликован Kocsis P., Tarnawa I., Kovacs Gy., Szombathelyi Zs., Farkas S., 2002; Acta Pharmaceut. Hung., 72:4961; US 5340823, 1994, US 5198446, JP 1992270293, EP 0468825, 1990 HU 4647. Наши эксперименты обнаружили, что GYKI 20039 индуцирует интенсивный тремор в дозе 10 мг/кг веса при внутрибрюшинном введении мышам, который длится 30-60 мин и достигает максимума между 4-8-й мин. Механизм его действия окончательно не выяснен, но его структурная схожесть с LON-954,тремогенным соединением, позволяет предположить вовлеченность в нисходящие допаминергические и серотонинергические системы (Mohanakumar, K.P., Ganguly, D.K., 1989; Brain Res. Bull. 22: 191-5). Тремор, вызванный с помощью GYKI 20039, можно ингибировать дозозависимым способом мышечно-релаксантными лекарственными препаратами с различными способами действия, таким образом,это подходящий метод сравнения мышечно-релаксантной эффективности лекарственных препаратов. Модель была подтверждена с помощью нескольких различных мышечно-релаксантных лекарственных препаратов, применяемых в клинической практике. Все они вызывали дозозависимый ингибирующий эффект, который коррелировал с клинической антиспастической эффективностью мышечнорелаксантных лекарственных препаратов. В нашем исследовании было доказано, что блокаторы натриевых каналов обладают ингибирующей противотреморной активностью, и также было определено изменение их эффективности в присутствии повышенного уровня серотонина. Тесты проводили на самцах мышей NMRI (19-21 г), активные соединения совместно вводили внутрибрюшинно. На фиг. 4 показано влияние блокаторов натриевых каналов ламотригина и кробенетина, а также увеличение их эффективности в случае, если присутствует ингибитор обратного захвата серотонина в дозировке, которая сама по себе не оказывает существенного влияния. А именно, на график наносили величины ID50, полученные в тесте на тремор для ламотригина и кробенетина, применяемых по отдельности (Copt) и совместно с флуоксетином в количестве 10 мг/кг (Fluo) или совместно с сертралином в количестве 10 мг/кг (Serf); все соединения вводили внутрибрюшинно. Также проводили эксперименты с композициями, содержавшими активные соединения при фиксированном соотношении. В этом случае также обнаружили повышение эффективности. В табл. 1, приведенной ниже, показано повышение эффективности блокатора натриевых каналов (ламотригин), достигнутого с помощью добавления фиксированных соотношений ингибитора обратного захвата серотонина Ингибирование судорог при максимальном электрошоке Ингибирование судорог при максимальном электрошоке (MES; Swinyard, E.A., Brown, W.C., Goodman L.S. Comparative assay of antiepileptic drugs in mice and rats. Journal of Pharmacology and ExperimentalTherapeutics 106, 319-330; 1952) демонстрирует антиэпилептическую эффективность соединения. Эксперименты в этом направлении проводили на самцах мышей NMRI (19-21 г). Предварительная обработка животных соединениями SSRI вызывала значительное повышение эффективности блокаторов натриевых каналов, тогда как соединения SSRI, вводимые сами по себе в этой дозировке, были в этом тесте практически неэффективными. Табл. 2, приведенная ниже, демонстрирует увеличенную эффективность блокаторов натриевых каналов в присутствии ингибиторов обратного захвата серотонина, которые сами по себе не оказывали значительного влияния. Ингибиторы обратного захвата серотонина вводили внутрибрюшинно за 45 мин,тогда как блокаторы натриевых каналов вводили за 30 мин до электрошока. Таблица 2 Эти результаты показывают, что ингибиторы обратного захвата серотонина усиливают эффект антиэпилептиков с механизмом действия, блокирующим натриевые каналы. С другой стороны, тест на ро-5 013812 тароде, с помощью которого изучали этот двигательный побочный эффект, был значительно менее выражен, демонстрируя, что профиль побочного эффекта также был улучшен. Таким образом, совместное применение двух соединений привело к получению более эффективного фармацевтического средства,обладающего более благоприятным профилем побочных эффектов. Тест на ротароде С помощью теста на ротароде (Dunnham, N.W., Miya, T.S. J. Am. Pharm. Assoc. 46, 208, 1957) можно изучать поврежденную координацию и нарушения произвольных движений в качестве возможных побочных эффектов. В этом отношении изменение эффективности блокаторов потенциалзависимых натриевых каналов, вызываемое ингибиторами обратного захвата серотонина, было менее значительно выражено, что приводило к более благоприятному профилю побочных эффектов композиций по сравнению с исходными соединениями. Тесты проводили на самцах мышей NMRI (19-21 г). Эксперименты проводили с различными временами предварительной обработки, что дало сходные результаты. Таблица 2, приведенная ниже, указывает на слегка увеличивающуюся эффективность блокаторов натриевых каналов в присутствии ингибиторов обратного захвата. Таблица 3 Не тестировали. Острая боль, индуцированная фенилхиноном (тест корчения от боли) Примененный метод был описан Hendershot и Forsaith в 1959 г. (Kazuko Goto et al. Analgesic EffectPhenylquinone WrithingTest: A Critical Study in Mice. Meth and Find Exptl Clin Pharmacol 5(9): 601-606; 1983.) Острую боль индуцировали с помощью инъекции фенилхинона, раздражающего средства, в брюшную полость (0,02%-ный раствор, 0,1 мл/10 г веса тела). Флуоксетин вводили внутрибрюшинно за 15 мин до ламотригина. Эксперименты проводили на самцах мышей NMRI (19-21 г). Повышение аналгетической эффективности ламотригина, блокатора натриевых каналов, в присутствии ингибитора обратного захвата серотонина, показано на фиг. 5, где величины ID50, найденные в тесте корчения от боли, наносили на график для ламотригина, вводимого по отдельности (Cont) и вместе с флуоксетином (Fluo) в количестве 10 мг/кг. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, которая включает блокатор натриевых каналов, выбранный из группы, состоящей из ламотригина и кробенетина вместе с селективным ингибитором обратного захвата серотонина, выбранным из группы, состоящей из флуоксетина и сертралина. 2. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является ламотригином. 3. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является кробенетином. 4. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является ламотригином. 5. Фармацевтическая композиция по п.1, в которой селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является кробенетином. 6. Применение блокатора натриевых каналов, выбранного из группы, состоящей из ламотридина и кробенетина, и селективного ингибитора обратного захвата серотонина, выбранного из группы, состоящей из флуоксетина и сертралина, в способе получения фармацевтической композиции, пригодной для лечения и/или предупреждения заболеваний млекопитающих, которые вызваны хронической болью, или эпилепсией, или симптомами, или заболеваниями, вызванными расстройствами и/или поражением двигательной системы. 7. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является ламотригином. 8. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является флуоксетином и блокатор натриевых каналов является кробенетином. 9. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является-6 013812 сертралином и блокатор натриевых каналов является ламотригином. 10. Применение по п.6, при котором селективный ингибитор обратного захвата серотонина является сертралином и блокатор натриевых каналов является кробенетином.
МПК / Метки
МПК: A61P 25/08, A61K 31/53, A61P 25/00, A61K 45/06, A61K 31/4525, A61K 31/55, A61K 31/135, A61K 31/675, A61K 31/381, A61K 31/343, A61K 31/485
Метки: ингибитора, каналов, обратного, серотонина, селективного, композиция, захвата, фармацевтическая, блокатора, натриевых
Код ссылки
<a href="https://eas.patents.su/9-13812-farmacevticheskaya-kompoziciya-blokatora-natrievyh-kanalov-i-selektivnogo-ingibitora-obratnogo-zahvata-serotonina.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция блокатора натриевых каналов и селективного ингибитора обратного захвата серотонина</a>
Предыдущий патент: 2,4,6-тризамещённые пиримидины, являющиеся ингибиторами фосфотидилинозитол (рi)-3-киназы, и их применение при лечении рака
Следующий патент: Применение иматиниба для лечения гепатита с
Случайный патент: Способ приведения старых захоронений твердых радиоактивных отходов в безопасное состояние