Способ синтеза (2s)-индолин-2-карбоновой кислоты и его использование в синтезе периндоприла
Формула / Реферат
1. Способ синтеза (2S)-индолин-2-карбоновой кислоты формулы (I)
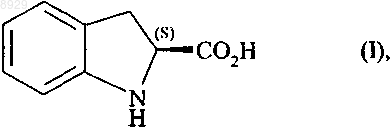
характеризующийся тем, что рацемическую индолин-2-карбоновую кислоту формулы (III)
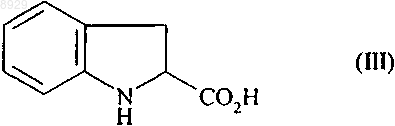
подвергают взаимодействию с хиральным амином, получая соль формулы (IV)
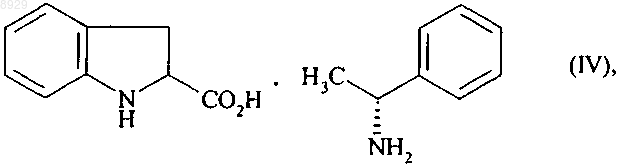
которую отфильтровывают и таким образом выделяют, с одной стороны, (2S) изомер формулы (IVа)
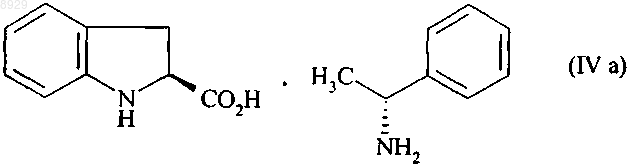
в виде кристаллов,
затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),
и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер
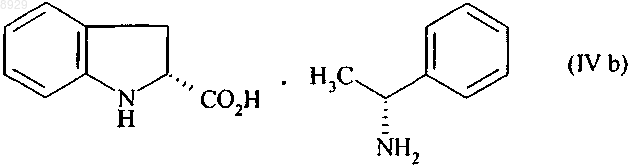
путем упаривания фильтрата,
и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2-карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота,
которую рацемизируют путем взаимодействия с раствором гидроксида натрия при температуре от 140 до 200шС и давлении от 5 до 15 бар,
получая после выделения соединение формулы (III), и в котором вышеописанные последовательности операций повторяют,
затем, после осуществления от 2 до 6 циклов, объединяют все порции, составляющие соединение формулы (I).
2. Способ синтеза (2S)-индолин-2-карбоновой кислоты формулы (I)
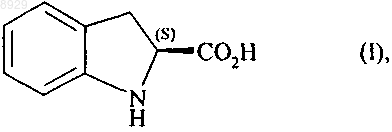
характеризующийся тем, что подвергают взаимодействию (2R)-индолин-2-карбоновую кислоту формулы (V)
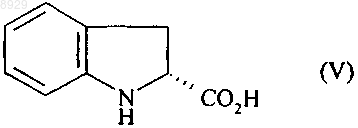
которую рацемизируют путем взаимодействия с раствором гидроксида натрия при температуре от 140 до 200шС и давлении от 5 до 15 бар,
получая после выделения соединение формулы (III)

которое подвергают взаимодействию с хиральным амином, получая соль формулы (IV)
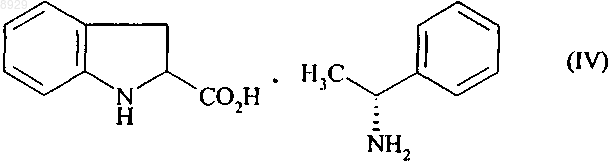
которую отфильтровывают и таким образом выделяют, с одной стороны, (2S) изомер формулы (IVа)
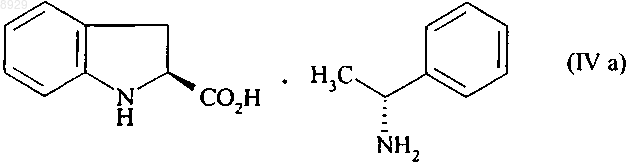
в виде кристаллов, затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),
и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер
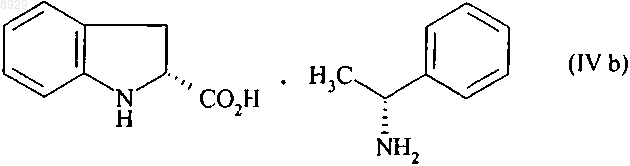
путем упаривания фильтрата,
и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2-карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота,
и, если это является желательным, то вышеописанные последовательности операций повторяют,
затем после осуществления от 1 до 6 циклов объединяют все порции, составляющие соединение формулы (I).
3. Способ синтеза в соответствии с п.1 или 2, отличающийся тем, что хиральный амин представляет собой (R)-a-метилбензиламин.
4. Способ синтеза периндоприла или его фармацевтически приемлемых солей, в котором соединение формулы (III) превращают в промежуточное соединение формулы (I) в соответствии со способом по п.1, и затем промежуточное соединение формулы (I) превращают в периндоприл или его фармацевтически приемлемые соли.
5. Способ синтеза периндоприла или его фармацевтически приемлемых солей, в котором соединение формулы (V) превращают в промежуточное соединение формулы (I) в соответствии со способом по п.2 и затем промежуточное соединение формулы (I) превращают в периндоприл или его фармацевтически приемлемые соли.
Текст
008929 Настоящее изобретение относится к способу синтеза (2S)-индолин-2-карбоновой кислоты, и к ее применению в синтезе периндоприла и его фармацевтически приемлемых солей. Более конкретно, настоящее изобретение относится к новому способу промышленного синтеза (2S)индолин-2-карбоновой кислоты формулы (I) Соединение формулы (I), полученное в соответствии со способом по изобретению, пригодно для синтеза периндоприла формулы (II) и для синтеза его фармацевтически пригодных солей. Периндоприл и его соли обладают ценными фармакологическими свойствами. Его главное свойство состоит в ингибировании фермента, превращающего ангиотензин I (или кининазы II), что, с одной стороны, позволяет предотвратить превращение декапептида ангиотензина I в октапептид ангиотензин II (сосудосуживающий фактор) и, с другой стороны, предотвратить расщепление брадикинина (сосудорасширяющий фактор) до неактивного пептида. Эти два действия обусловливают положительное влияние периндоприла на сердечно-сосудистые заболевания, в особенности на артериальную гипертонию и сердечную недостаточность. Периндоприл, его получение и его применение для лечения описано в заявке на европейский патент ЕР 0049658. Принимая во внимание фармацевтическую ценность этого соединения, важной является возможность получить промежуточный продукт формулы (I) при помощи эффективного способа синтеза, который позволяет селективно получить (S) энантиомер с очень хорошим выходом и с отличной чистотой. Некоторые способы получения соединения формулы (I) уже известны. Например, в заявках на европейский патент ЕР 0308339 и ЕР 0308341 описано получение (2S)индолин-2-карбоновой кислоты путем разделения рацемической индолин-2-карбоновой кислоты при помощи (R)метилбензиламина, (R)метилбензиламиновую соль (2S)-индолин-2-карбоновой кислоты выделяют путем фракционированной кристаллизации, затем подкисляют, получая соединение формулы (I). Преимуществом этого способа является использование недорогих и легко доступных реагентов и исходного вещества. С другой стороны, выход соединения формулы (I) при применении этого способа составляет только 35%. Сейчас заявителем был разработан способ синтеза соединения формулы (I), при котором (2R) изомер, образующийся при реакции разделения, возвращают на повторную переработку. При этом разработанный способ предоставляет возможность получить соединение формулы (I), исходя из рацемической индолин-2-карбоновой кислоты, с выходом в диапазоне от 50 до 70%, в соответствии с количеством осуществленных процессов повторной переработки. Более конкретно, настоящее изобретение относится к способу синтеза соединения формулы (I), который характеризуется тем, что рацемическую индолин-2-карбоновую кислоту формулы (III) подвергают взаимодействию с хиральным амином, получая соль формулы (IV) которую отфильтровывают, и таким образом выделяют с одной стороны, (2S) изомер формулы (IVа) в виде кристаллов,затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер путем упаривания фильтрата,и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2 карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота,после этого рацемизируют путем взаимодействия с раствором гидроксида натрия,при температуре от 140 до 200 С и давлении от 5 до 15 бар,получая, после выделения, соединение формулы (III), и в котором вышеописанные последовательности операций повторяют,затем, после осуществления от 2 до 6 циклов, объединяют все порции, составляющие соединение формулы (I). Таким образом получают соединение формулы (I) с выходом в диапазоне от 50 до 70% в соответствии с количеством осуществленных циклов. Его химическая и энантиомерная чистота является очень хорошей, что делает его чрезвычайно пригодным для синтеза периндоприла формулы (II). Например, каталитическая гидрогенизация соединения формулы (I), полученного в соответствии со способом по изобретению, с последующим сочетанием таким образом полученной (2S,3 аS,7 аS)пергидроиндол-2-карбоновой кислоты с соединением формулы (VI) позволяет получить периндоприл формулы (II) с очень хорошей чистотой и выходом. Настоящее изобретение также относится к варианту вышеописанного способа, в котором подвергают реакции (2R)-индолин-2-карбоновую кислоту формулы (V) которую рацемизируют путем взаимодействия с раствором гидроксида натрия,при температуре от 140 до 200 С и давлении от 5 до 15 бар,получая, после выделения, соединение формулы (III) которое подвергают взаимодействию с хиральным амином, получая соль формулы (IV) которую отфильтровывают, и таким образом выделяют с одной стороны, (2S) изомер формулы (IVа) в виде кристаллов,-2 008929 затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер путем упаривания фильтрата,и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2 карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота, и, если это является желательным, то вышеописанные последовательности операций повторяют,затем, после осуществления от 1 до 6 циклов, объединяют все порции, составляющие соединение формулы (I). Среди хиральных аминов, которые могут применяться в способе в соответствии с изобретением или его варианте, могут быть упомянуты, но не ограничиваясь только ими, (R)метилбензиламин, 1-(1 нафтил)этиламин, эфедрин, -химотрипсин, втор-бутиламин, 1-амино-2-метилбутан, N,N-диметил-1 фенилэтиламин, 1-циклогексилэтиламин, циклосерин, 2-(метоксиметил)пирролидин, -диметиламино-капролактам, изоборниламин, 1-(4-нитрофенил)этиламин, -аминокапролактам, 2-амино-1-бутанол, 1 амино-2-пропанол, цинхонидин, цинхонин, N-метилэфедрин, фенилаланинол, хинидин, валинол, фенилглицинол, лейцинол. Предпочтительным хиральным амином является (R)метилбензиламин. Под "смесью, в которой преобладает (2R) изомер" подразумевают смесь (2R) и (2S) изомеров, в которой большую часть смеси составляет (2R) изомер. Последующий пример иллюстрирует изобретение. Пример. (2S)-Индолин-2-карбоновая кислота. Стадия А. Разделение рацемической индолин-2-карбоновой кислоты. 3,7 кг (R)метилбензиламина добавляли к раствору 5 кг индолин-2-карбоновой кислоты в этаноле и затем смесь перемешивали в течение 2 ч и фильтровали. Стадия А 1. (2S)-Индолин-2-карбоновая кислота. Белый осадок, собранный на стадии А, перекристаллизовывали из изопропанола и затем растворяли в 13 л воды и добавляли 12 л 1 н. раствора соляной кислоты. После перемешивания в течение 2 ч осадок отфильтровывали и затем промывали и высушивали, получая (2S)-индолин-2-карбоновую кислоту (1-ая часть) в виде кристаллов (1,80 кг) с химической чистотой 98% и энантиомерной чистотой, превышающей 99,5%. Стадия А 2. Идолин-2-карбоновая кислота (смесь, в которой преобладает (2R. Фильтрат, собранный на стадии А, упаривали и полученный остаток растворяли в 13 л воды и затем добавляли 12 л 1 н. раствора соляной кислоты. После перемешивания в течение 2 ч осадок отфильтровывали и затем промывали и высушивали, получая индолин-2-карбоновую кислоту в виде смеси (2R) и (2S) энантиомеров (2,6 кг), в которой преобладает (2R) энантиомер. Стадия В. Рацемизация. В автоклав вносили осадок, полученный на стадии А 2 (2,6 кг), и затем 12 л воды и 3,1 л 8,65 н. раствора гидроксида натрия, после этого нагревали при 170 С в течение 3 ч под давлением 7 бар. Затем реакционную смесь доводили до температуры окружающей среды и после этого переносили в реактор, и потом добавляли концентрированную соляную кислоту до установления значения рН 3,4, при этом температуру поддерживали в диапазоне от 20 до 25 С. Затем смесь перемешивали в течение 1 ч и после этого осадок отфильтровывали, промывали и высушивали, получая рацемическую индолин-2-карбоновую кислоту при выходе 90% (2,34 кг). Стадия С. Повторная переработка индолин-2-карбоновой кислоты. Рацемическую индолин-2-карбоновую кислоту, полученную на стадии В (2,34 кг), разделяли в соответствии с методикой со стадии А. Выделяли (R)метилбензиламиновую соль (2S)-индолин-2-карбоновой кислоты, которая при этом образуется, и затем подвергали взаимодействию с соляной кислотой в соответствии с методикой со стадии А 1, получая (2S)-индолин-2-карбоновую кислоту (2-ая часть) в виде кристаллов (0,84 кг), которая имеет химическую чистоту 98% и энантиомерную чистоту, превышающую 99,5%. После этого объединяли 1-ую часть, полученную на стадии А 1, и 2-ую часть, полученную на стадии С. Таким образом получали (2S)-индолин-2-карбоновую кислоту при суммарном выходе 52,8%, с химической чистотой 98% и энантиомерной чистотой, превышающей 99,5%. подвергают взаимодействию с хиральным амином, получая соль формулы (IV) в виде кристаллов,затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер путем упаривания фильтрата,и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2 карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота,которую рацемизируют путем взаимодействия с раствором гидроксида натрия при температуре от 140 до 200 С и давлении от 5 до 15 бар,получая после выделения соединение формулы (III), и в котором вышеописанные последовательности операций повторяют,затем, после осуществления от 2 до 6 циклов, объединяют все порции, составляющие соединение формулы (I). 2. Способ синтеза (2S)-индолин-2-карбоновой кислоты формулы (I) характеризующийся тем, что подвергают взаимодействию (2R)-индолин-2-карбоновую кислоту формулы которую рацемизируют путем взаимодействия с раствором гидроксида натрия при температуре от 140 до 200 С и давлении от 5 до 15 бар,получая после выделения соединение формулы (III) которое подвергают взаимодействию с хиральным амином, получая соль формулы (IV) в виде кристаллов, затем соединение формулы (IVа) подвергают реакции с соляной кислотой, получая соединение формулы (I),и, с другой стороны, смесь (2S) изомера формулы (IVа) и (2R) изомера формулы (IVb), в которой преобладает (2R) изомер путем упаривания фильтрата,и после этого смесь подвергают реакции с соляной кислотой, получая смесь (2R)-индолин-2 карбоновой кислоты и (2S)-индолин-2-карбоновой кислоты, в которой преобладает (2R) кислота,и, если это является желательным, то вышеописанные последовательности операций повторяют,затем после осуществления от 1 до 6 циклов объединяют все порции, составляющие соединение формулы (I). 3. Способ синтеза в соответствии с п.1 или 2, отличающийся тем, что хиральный амин представляет собой (R)метилбензиламин. 4. Способ синтеза периндоприла или его фармацевтически приемлемых солей, в котором соединение формулы (III) превращают в промежуточное соединение формулы (I) в соответствии со способом по п.1, и затем промежуточное соединение формулы (I) превращают в периндоприл или его фармацевтически приемлемые соли. 5. Способ синтеза периндоприла или его фармацевтически приемлемых солей, в котором соединение формулы (V) превращают в промежуточное соединение формулы (I) в соответствии со способом по п.2 и затем промежуточное соединение формулы (I) превращают в периндоприл или его фармацевтически приемлемые соли.
МПК / Метки
МПК: C07D 209/42, C07B 57/00
Метки: синтезе, кислоты, 2s)-индолин-2-карбоновой, использование, синтеза, способ, периндоприла
Код ссылки
<a href="https://eas.patents.su/6-8929-sposob-sinteza-2s-indolin-2-karbonovojj-kisloty-i-ego-ispolzovanie-v-sinteze-perindoprila.html" rel="bookmark" title="База патентов Евразийского Союза">Способ синтеза (2s)-индолин-2-карбоновой кислоты и его использование в синтезе периндоприла</a>
Предыдущий патент: Активаторы рецепторов, активируемых пролифератором пероксисом (ppar )
Следующий патент: Непэгилированные, длительно циркулирующие липосомы
Случайный патент: Способ непрерывного получения поликристаллического кремния с использованием реактора с псевдоожиженным слоем










