Новый способ синтеза периндоприла и его фармацевтически приемлемых солей
Формула / Реферат
1. Способ синтеза соединений формулы (I)
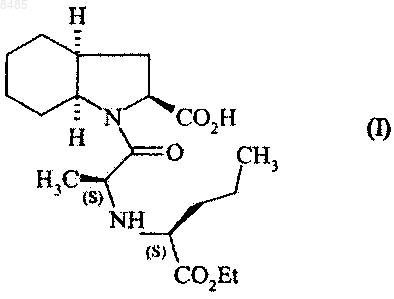
и их фармацевтически приемлемых солей, характеризующийся тем, что соединение формулы (II)
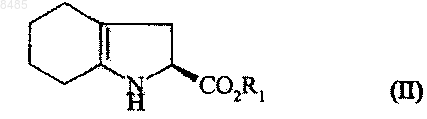
в которой R1 представляет собой атом водорода или бензил или линейную или разветвленную С1-С6-алкильную группу,
подвергают реакции с соединением формулы (III), имеющим S-конфигурацию
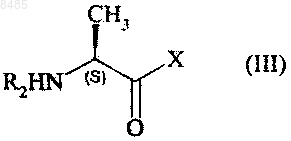
в которой X представляет собой атом галогена и
R2 представляет собой защитную группу для функциональной аминогруппы, в присутствии основания, получая после снятия защиты с функциональной аминогруппы соединение формулы (IV)
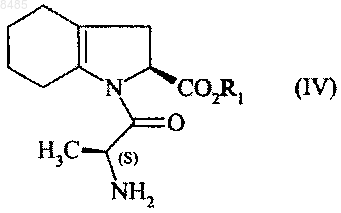
в которой R1 имеет значения, указанные выше,
которое подвергают реакции с соединением формулы (V)
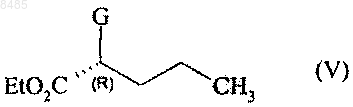
в которой G представляет собой атом хлора, брома или йода или n-толуолсульфонилокси, метансульфонилокси или трифторметансульфонилоксигруппу,
в присутствии основания, получая соединение формулы (VI)
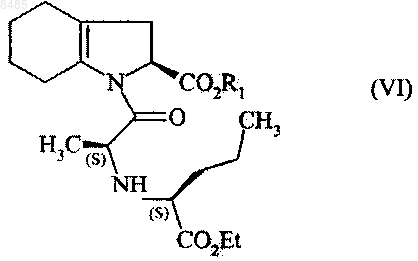
в которой R1 имеет значения, указанные выше,
которое гидрируют в присутствии катализатора, такого как палладий, платина, родий или никель,
получая, при необходимости, после снятия защиты соединение формулы (I).
2. Способ синтеза в соответствии с п.1, характеризующийся тем, что защитная аминогруппа для функциональной аминогруппы представляет собой трет-бутоксикарбонильную или бензильную группу.
3. Способ синтеза в соответствии с п.2, характеризующийся тем, что R1 представляет собой бензильную группу, а защитная аминогруппа для функциональной аминогруппы представляет собой трет-бутоксикарбонильную группу.
4. Способ синтеза в соответствии с любым из пп.1-3, характеризующийся тем, что основание, используемое для взаимодействия между соединениями формул (II) и (III), представляет собой органический амин, выбранный из триэтиламина, пиридина, N-метилморфолина и диизопропилэтиламина, или неорганическое основание, такое как NaOH, KОН, Na2CO3, K2CO3, NaHCO3 или KНСО3.
5. Способ синтеза в соответствии с любым из пп.1-4, характеризующийся тем, что основание, используемое для взаимодействия между соединениями формул (IV) и (V), представляет собой органический амин, выбранный из триэтиламина, пиридина, N-метилморфолина и диизопропилэтиламина, или неорганическое основание, такое как NaOH, KОН, Na2CO3, K2CO3, NaHCO3 или KНСО3.
6. Способ в соответствии с любым из пп.1-5 для синтеза периндоприла в виде его трет-бутиламиновой соли.
Текст
008485 Настоящее изобретение относится к способу синтеза периндоприла формулы (I) и его фармацевтически приемлемых солей. Периндоприл и его фармацевтически приемлемые соли, в особенности его трет-бутиламиновая соль, обладают ценными фармакологическими свойствами. Их главное свойство состоит в ингибировании фермента, превращающего ангиотензин I (или кининазы II), что, с одной стороны, позволяет предотвратить превращение декапептида ангиотензина I в октапептид ангиотензин II (сосудосуживающий фактор), а, с другой стороны, предотвратить расщепление брадикинина (сосудорасширяющий фактор) до неактивного пептида. Эти два действия обуславливают положительное влияние периндоприла на сердечно-сосудистые заболевания, в особенности на артериальную гипертонию и сердечную недостаточность. Периндоприл, его получение и его применение для лечения описано в заявке на Европейский патент ЕР 0049658. Принимая во внимание фармацевтическую ценность этого соединения, важной является возможность его получения при помощи эффективного способа синтеза, который легко можно осуществить в промышленном масштабе, что приводит к получению периндоприла с хорошим выходом и с отличной чистотой при использовании исходных веществ с приемлемой стоимостью. В патентной заявке ЕР 0308341 описан промышленный синтез периндоприла путем сочетания бензилового эфира (2S,3 аS,7 аS)октагидроиндол-2-карбоновой кислоты с этиловым эфиром N-[(S)-1-карбоксибутил]-(S)-аланина с последующим снятием защиты с карбоксильной группы гетероцикла посредством каталитической гидрогенизации. Сейчас заявителем был открыт новый способ синтеза периндоприла. Более конкретно, настоящее изобретение относится к способу синтеза периндоприла и его фармацевтически приемлемых солей, который характеризуется тем, что соединение формулы (II) в которой R1 представляет собой атом водорода или бензил или линейную или разветвленную C1 С 6-алкильную группу,подвергают реакции с соединением формулы (III), имеющим S-конфигурацию в которой X представляет собой атом галогена и R2 представляет собой защитную группу для функциональной аминогруппы,в присутствии основания,получая после снятия защиты с функциональной аминогруппы соединение формулы (IV)-1 008485 в которой G представляет собой атом хлора, брома или йода или n-толуолсульфонилокси, метансульфонилокси или трифторметансульфонилоксигруппу,в присутствии основания, получая соединение формулы (VI) в которой R1 имеет значения, указанные выше,которое гидрируют в присутствии катализатора, такого как палладий, платина, родий или никель,получая, при необходимости, после снятия защиты соединение формулы (I). Защитными группами для функциональной аминогруппы, которые могут применяться в способе согласно настоящему изобретению, являются, но не ограничиваясь только ими, трет-бутоксикарбонильная и бензильная группы.R1 предпочтительно представляет собой бензильную группу. В этом случае защитная группа для функциональной аминогруппы предпочтительно представляет собой трет-бутоксикарбонильную группу. Для взаимодействия между соединениями формул (II) и (III) или между соединениями формул (IV) и (V) могут применяться следующие основания, но не ограничиваясь только ими: органические амины,такие как триэтиламин, пиридин, N-метилморфолин или диизопропилэтиламин, а также неорганические основания, такие как NaOH, KОН, Na2CO3, K2CO3, NaHCO3 или KНСО 3. Пример 1. трет-Бутиламиновая соль (2S,3aS,7aS)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионилоктагидро-1H-индол-2-карбоновой кислоты Стадия А: Бензил (2S)-1-(2S)-2-[(трет-бутоксикарбонил)амино]пропионил-2,3,4,5,6,7-гексагидро 1H-индол-2-карбоксилат В реактор вносили 200 г бензил (2S)-2,3,4,5,6,7-гексагидро-1 Н-индол-2-карбоксилата и 1,5 л дихлорметана, после этого температуру реакционной смеси доводили до 0 С и добавляли 107 мл триэтиламина и затем 162 г (2S)-2-трет-бутоксикарбонил)амино]пропионилхлорида. После этого температуру смеси доводили до температуры окружающей среды. После перемешивания в течение 1 ч при этой температуре смесь промывали водой и затем разведенным раствором уксусной кислоты. Полученный таким образом раствор бензил (2S)-1-(2S)-2-[(трет-бутоксикарбонил)амино]пропионил-2,3,4,5,6,7-гексагидро 1H-индол-2-карбоксилат использовали на следующей стадии без дополнительной обработки. Стадия Б: Бензил (2S)-1-(2S)-2-aминопропионил-2,3,4,5,6,7-гексагидро-1 Н-индол-2-карбоксилат В реактор вносили раствор, полученный на вышеописанной стадии, и затем добавляли 133 г трифторуксусной кислоты. После перемешивания в течение 1 ч 30 мин при температуре окружающей среды смесь промывали водой, затем насыщенным раствором гидрокарбоната натрия и растворители выпаривали, получая бензил (2S)-1-(2S)-2-аминопропионил-2,3,4,5,6,7-гексагидро-1H-индол-2-карбоксилат. Стадия В: Бензил (2S)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионил-2,3,4,5,6,7 гексагидро-1 Н-индол-2-карбоксилат В реактор вносили 200 г соединения, полученного на вышеописанной стадии, 106 мл диизопропилэтиламина и 1,5 л тетрагидрофурана, и затем 183 г этил (2R)-2-n-толуолсульфонилоксипентаноата, и после этого нагревали при 70 С в течение 2 ч. После возвращения температуры до температуры окружающей среды смесь промывали водой и затем концентрировали насухо. Остаток ресуспендировали в дихлорметане. Добавляли 2 М раствор соляной кислоты до установления значения рН, приблизительно равного 7,5. После декантирования растворители испаряли, получая бензил (2S)-1-(2S)-2-[(1S)-1(этоксикарбонил)бутиламино]пропионил-2,3,4,5,6,7-гексагидро-1 Н-индол-2-карбоксилат. Стадия Г: (2S,3aS,7aS)-1-(2S)-2-[(1S)-1-(Этоксикарбонил)бутиламино]пропионилоктагидро-1Hиндол-2-карбоновая кислота В сосуд для гидрирования вносили 200 г соединения, полученного на вышеописанной стадии, в растворе в уксусной кислоте, и затем 5 г 10 % Pt/C. Гидрировали под давлением 5 бар при температуре от 15 до 30 С до абсорбирования теоретического количества водорода. Катализатор удаляли путем фильтрации, затем охлаждали до температуры от 0 до 5 С и полученное твердое вещество собирали путем фильтрации. Осадок промывали и высушивали до постоянного веса. Таким образом получали(2S,3aS,7aS)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионил-октагидро-1H-индол-2-карбоновой кислоты Осадок, полученный на вышеописанной стадии (200 г), растворяли в 2,8 л ацетонитрила и затем до-2 008485 бавляли 40 г трет-бутиламина и 0,4 л этилацетата. Затем полученную суспензию нагревали в колбе с обратным холодильником до полного растворения и после этого полученный раствор фильтровали в горячем состоянии и охлаждали при перемешивании до температуры от 15 до 20 С. После этого полученный осадок отфильтровывали, снова превращали в пасту с ацетонитрилом, высушивали и затем перекристаллизовывали из этилацетата, получая ожидаемый продукт с выходом 95% и энантиомерной чистотой 99%. Пример 2. трет-Бутиламиновая соль (2S,3aS,7aS)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионилоктагидро-1H-индол-2-карбоновой кислоты Стадии А и Б: аналогично стадиям Аи Б примера 1. Стадия В: Бензил (2S)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионил-2,3,4,5,6,7 гексагидро-1H-индол-2-карбоксилат В реактор вносили 200 г соединения, полученного на вышеописанной стадии, 106 мл диизопропилэтиламина и 1,5 л этилацетата, затем 165 г этил (2R)-2-хлорпентаноата и после этого нагревали при 50 С в течение 3 ч. После возвращения температуры до температуры окружающей среды смесь промывали водой и затем концентрировали насухо. Остаток ресуспендировали в дихлорметане. Добавляли 2 М раствор соляной кислоты до установления значения рН, приблизительно равного 7,5. После декантирования растворители упаривали,получая бензил(2S)-1-(2S)-2-[(1S)-1-(этоксикарбонил)бутиламино]пропионил-2,3,4,5,6,7-гексагидро-1 Н-индол-2-карбоксилат. Стадии Г и Д: аналогично стадиям Г и Д примера 1. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ синтеза соединений формулы (I) и их фармацевтически приемлемых солей, характеризующийся тем, что соединение формулы (II) в которой R1 представляет собой атом водорода или бензил или линейную или разветвленную С 1 С 6-алкильную группу,подвергают реакции с соединением формулы (III), имеющим S-конфигурацию в которой X представляет собой атом галогена иR2 представляет собой защитную группу для функциональной аминогруппы, в присутствии основания, получая после снятия защиты с функциональной аминогруппы соединение формулы (IV) в которой G представляет собой атом хлора, брома или йода или n-толуолсульфонилокси, метансульфонилокси или трифторметансульфонилоксигруппу,-3 008485 в присутствии основания, получая соединение формулы (VI) в которой R1 имеет значения, указанные выше,которое гидрируют в присутствии катализатора, такого как палладий, платина, родий или никель,получая, при необходимости, после снятия защиты соединение формулы (I). 2. Способ синтеза в соответствии с п.1, характеризующийся тем, что защитная аминогруппа для функциональной аминогруппы представляет собой трет-бутоксикарбонильную или бензильную группу. 3. Способ синтеза в соответствии с п.2, характеризующийся тем, что R1 представляет собой бензильную группу, а защитная аминогруппа для функциональной аминогруппы представляет собой третбутоксикарбонильную группу. 4. Способ синтеза в соответствии с любым из пп.1-3, характеризующийся тем, что основание, используемое для взаимодействия между соединениями формул (II) и (III), представляет собой органический амин, выбранный из триэтиламина, пиридина, N-метилморфолина и диизопропилэтиламина, или неорганическое основание, такое как NaOH, KОН, Na2CO3, K2CO3, NaHCO3 или KНСО 3. 5. Способ синтеза в соответствии с любым из пп.1-4, характеризующийся тем, что основание, используемое для взаимодействия между соединениями формул (IV) и (V), представляет собой органический амин, выбранный из триэтиламина, пиридина, N-метилморфолина и диизопропилэтиламина, или неорганическое основание, такое как NaOH, KОН, Na2CO3, K2CO3, NaHCO3 или KНСО 3. 6. Способ в соответствии с любым из пп.1-5 для синтеза периндоприла в виде его третбутиламиновой соли.
МПК / Метки
МПК: C07K 5/02, C07K 5/06, C07D 209/42
Метки: солей, способ, новый, фармацевтически, приемлемых, синтеза, периндоприла
Код ссылки
<a href="https://eas.patents.su/5-8485-novyjj-sposob-sinteza-perindoprila-i-ego-farmacevticheski-priemlemyh-solejj.html" rel="bookmark" title="База патентов Евразийского Союза">Новый способ синтеза периндоприла и его фармацевтически приемлемых солей</a>
Предыдущий патент: Фунгицидные смеси
Следующий патент: Пластинчатый элемент для соединения паркетных щитов
Случайный патент: Инсектицидные соединения оксадиазина









