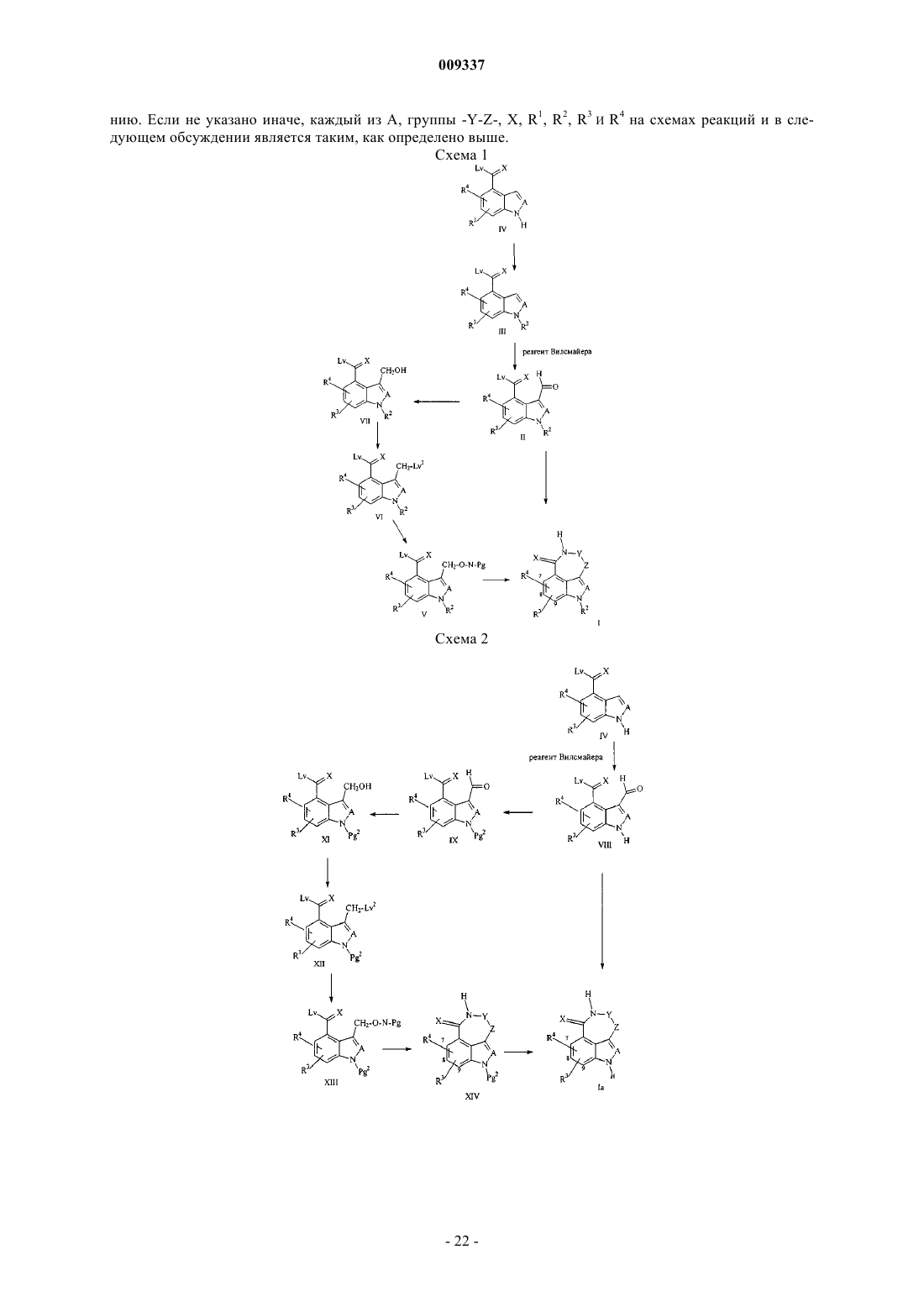
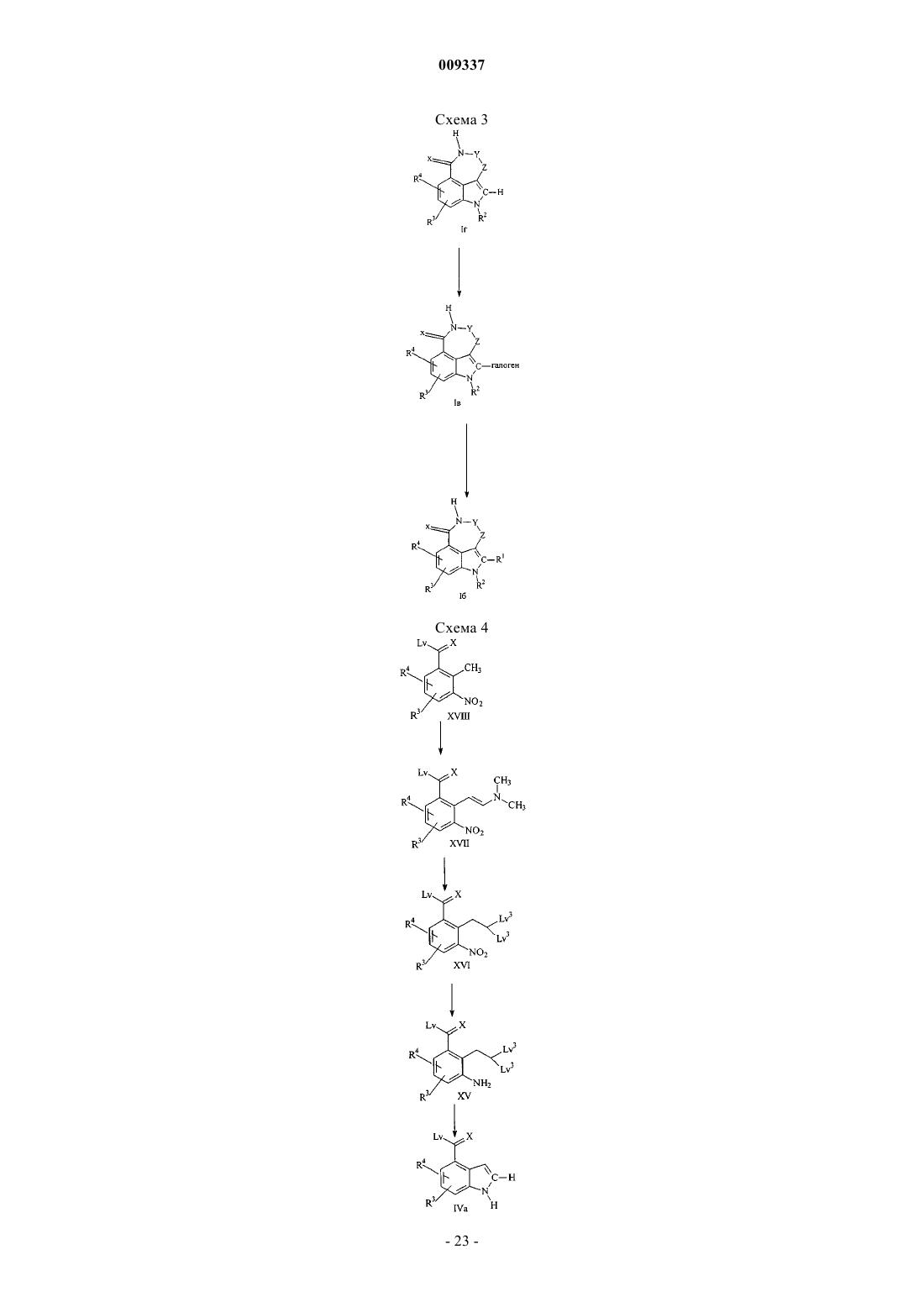
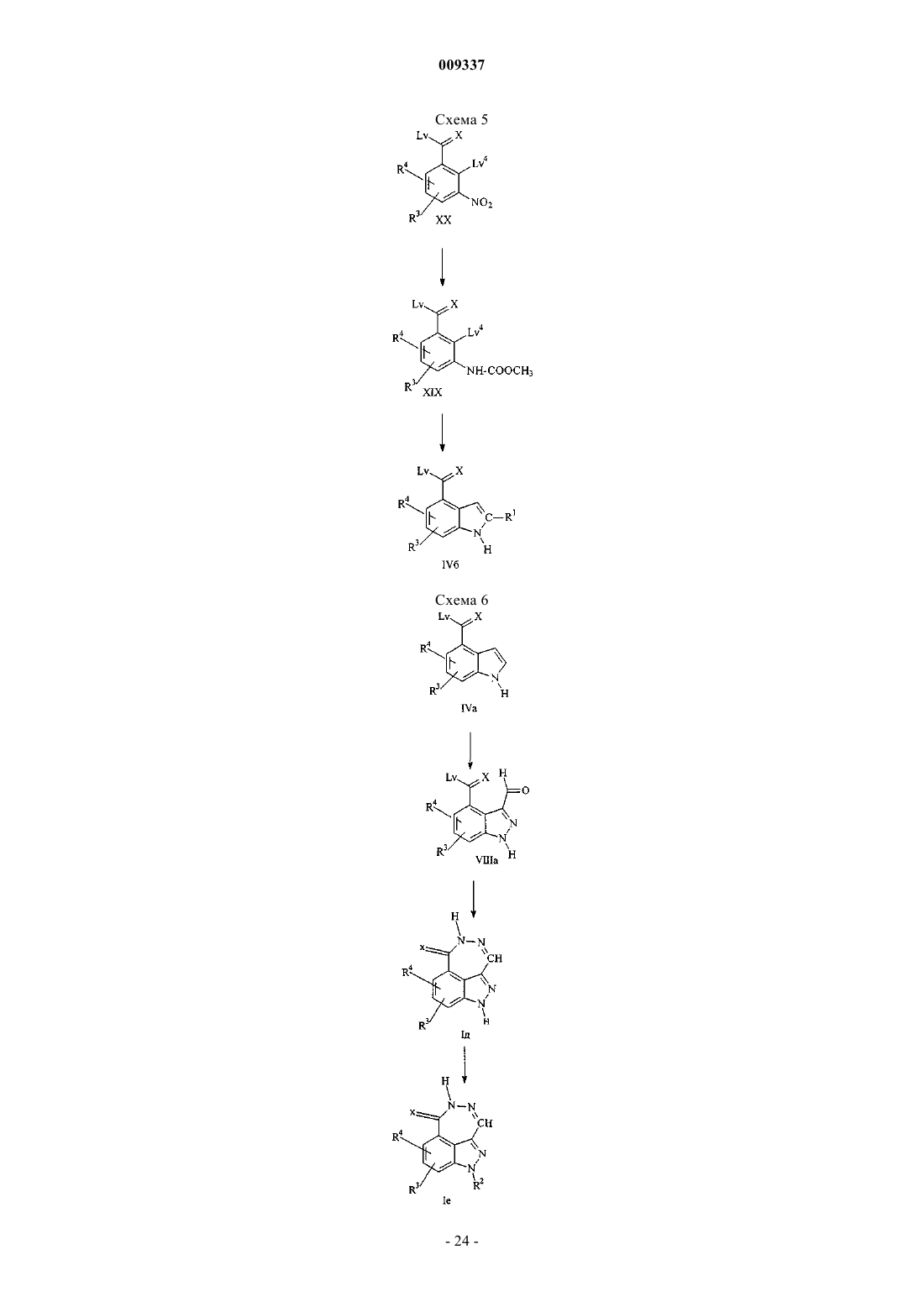
Трициклические соединения, представляющие собой ингибиторы протеинкиназ, для увеличения эффективности противоопухолевых агентов и лучевой терапии
Номер патента: 9337
Опубликовано: 28.12.2007
Авторы: Беннетт Майкл Джон, Руй Юджин Йюэнджин, Жу Джинджианг, Уэнг Фен, Нинковиц Саша, Тенг Мин, Бенедикт Сюзанн Притчетт, Уэнг Йонг
Формула / Реферат
1. Соединение формулы
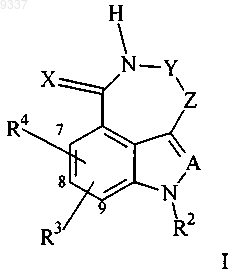
где X представляет собой =O;
А представляет собой =CR1-;
группа -Y-Z- имеет формулу-О-CH2- или -N=CH-;
R1 представляет собой:
(а) (C1-C8)алкил;
(б) -C(=O)-R5;
(в) -C(=O)-NR6R7; или
(г) R35 или R36, (С2-С8)алкенил или (С2-С8)алкинил {где каждый из указанных (С2-С8)алкенила или (С2-С8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из F, Cl, ОН, -NH2, R40 и R42};
R2 представляет собой
(а) Н, ОН или (C1-C8)алкил; или
(б) R39;
R3 представляет собой
(а) -C(=O)-R12;
(б) -C(=O)-NR13R14;
(в) -NRl5-C(=O)-R16;
(г) -NR17-SO2R18;
(д) -NR19-SOn-NR20R21 {где n представляет собой 1 или 2};
(е) -NR22-(C=S)-R23 или -NR22-(C=S)-NR23R24;
(ж) R36, (C2-С8)алкенил или (С2-С8)алкинил {где каждый из указанных R3 (C2-С8)алкенила или (C2-С8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из -(С=O)-O-(C1-C8)алкил, -O-(С=O)-(С1-С8)алкил, -(С=O)-(C1-C8)алкил, R40, R41 и R42};
(з) R37, -NH2, -NH((С2-С8)алкенил), -NH((С2-С8)алкинил), -N((С1-С8)алкил)((С2-С8)алкенил) или
-N((C1-C8)алкил)((С2-С8)алкинил) {где каждый из указанных R26 (С2-С8)алкенила или (С2-С8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R40, R41 и R42}; или
(и) R38;
R4 выбран из группы, состоящей из Н, F, Br, Cl и (C1-C8)алкила;
R5 выбран из группы, состоящей из Н, (C1-C8)алкила, (C1-C8)алкил-O- и R36;
каждый R6 и R7 независимо выбран из группы, состоящей из Н, (C1-C8)алкила и R36;
R12 выбран из группы, состоящей из Н, ОН, (C1-C8)алкила, (C1-C8)алкил-O- и R36;
R13 представляет собой Н или (C1-C8)алкил;
R14 выбран из группы, состоящей из Н, (C1-C8)алкила, -CH2-(C=O)-O-(C1-С8)алкила и R36;
R15 представляет собой Н или (C1-C8)алкил;
R16 выбран из группы, состоящей из Н, (C1-C8)алкила, (С2-С8)алкенила, (С2-С8)алкинила, -NH2, R36 и R37;
где каждый из указанных R15 и R16 (С2-С8)алкенила или (С2-С8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R40, R41 и R42;
R17 выбран из группы, состоящей из Н, (C1-C8)алкила и R36;
R18 представляет собой (C1-C8)алкил или R36;
R19, R20 и R21 независимо выбраны из группы, состоящей из Н, (C1-C8)алкила и R36;
R22, R23 и R24 независимо выбраны из группы, состоящей из Н, (C1-C8)алкила и R36;
R25 представляет собой Н или (C1-C8)алкил;
R26 выбран из группы, состоящей из -С(=O)-O-С(CH3)3, (C1-C8)алкила, (C3-C10)циклоалкила, (С2-C10) гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
или R25 и R26 возможно могут быть взяты вместе с атомом азота, к которому они присоединены, с образованием 5-8-членного гетероарильного или гетероциклильного кольца;
R27 выбран из группы, состоящей из (C1-C8)алкила, (C3-C10)циклоалкила, (C2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
R28 выбран из группы, состоящей из (C1-C8)алкила, (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
R29 представляет собой Н или (C1-C8)алкил;
R30 представляет собой (C1-C8)алкил, (C3-C10)циклоалкил, (С2-C10)гетероциклил, (С6-C10)арил или (C1-C10)гетероарил;
или R29 и R30 возможно могут быть взяты вместе с атомом азота, к которому они присоединены, с образованием 5-8-членного гетероарильного или гетероциклильного кольца;
R31 представляет собой Н или (C1-C8)алкил;
R32 независимо выбран из группы, состоящей из (C1-C8)алкила, (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
или R31 и R32 возможно могут быть взяты вместе с атомом азота, к которому они присоединены, с образованием 5-8-членного гетероарильного или гетероциклильного кольца;
R33 представляет собой (C1-C8)алкил, (C3-C10)циклоалкил, (С2-C10)гетероциклил, (С6-C10)арил или (C1-C10)гетероарил;
R34 представляет собой (C1-C8)алкил, (C3-C10)циклоалкил, (С2-C10)гетероциклил, (С6-C10)арил или (С1-C10)гетероарил;
каждый R35 независимо выбран из группы, состоящей из Н, F, Cl, Br, I, CN, ОН, NO2, -NH2, -NH-C(=O)-O-C(CH3)3 и CF3;
каждый R36 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
каждый R37 независимо выбран из группы, состоящей из
(в) -NR25R26; и
(г) R27-O-;
R38 представляет собой R28 -SOn-; где n представляет собой 0, 1 или 2, когда -SOn- связан с R28 через атом углерода R28, или где n представляет собой 1 или 2, когда -SOn- связан с R28 через кольцевой атом азота R28;
R39 представляет собой R29R30N-SOn-; где n представляет собой 1 или 2;
где каждый из указанного (C1-C8)алкила, где бы он не находился в любом из указанных R1(a)-(г), R2(a)-(с), R3(a)-(и), R4, R37, R38 или R39, не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (С2-С8)алкенила, R40, R41 и R42;
где каждый из указанных (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила или (C1-C10)гетероарила, где бы он не находился в указанных R36, R37, R38 или R39, независимо не замещен или замещен 1-4 заместителями, независимо выбранными из R40;
R40 выбран из группы, состоящей из (C1-C8)алкила, R41, R42 и R43;
каждый R41 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -NH2, -NH-C(=O)-O-C(CH3)3, СООН, -С(=O)(С1-С8)алкил, -С(=O)-O-(C1-C8)алкил, -NH-SO2-(C1-C8)алкил, -NH-SO2-(C6-C10)арил и CF3;
каждый R42 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10) арила и (C1-C10)гетероарила;
каждый R43 независимо выбран из группы, состоящей из
(б) -NR31R32;
(г) R33-O-; и
(в) R34-SOn-; где n представляет собой 0, 1 или 2, когда -SOn- связан с R34 через атом углерода R34, или где n представляет собой 1 или 2, когда -SOn- связан с R34 через кольцевой атом азота R34;
где каждый из указанного (C1-C8)алкила, где бы он не находился в любом из R40, независимо не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R44 и R45;
где каждый из указанных (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила или (C1-C10) гетероарила, где бы он не находился в любом из указанных R42 или R43, независимо не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R47, выбранного из группы, состоящей из (C1-С8)алкила, R44 и R45;
каждый R44 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -NH2, -CF3,
-C(=NH)-NH2, -C(=NH)-NH-OH, -С(=NH)-NH-O-(C1-C8)алкил, -(C=O)-O-(C1-C8)алкил, -O-(С=O)-(C1-C8)алкил, -(С=O)-(C1-C8)алкил, -(C=O)-NH2, -(C=O)-NH(C1-C8)алкил, -(С=O)-N<[(C1-C8)алкил]2, -NH-(С=O)-(C1-C8)алкил, R37 и R38;
каждый R45 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
где каждый из указанного (C1-C8)алкила, где бы он не находился в любом из указанных R44 или R45, независимо не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R46 и R47;
где каждый из указанных (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила или (C1-C10)гетероарила, где бы он не находился в любом из указанных R43 или R44, независимо не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (C1-C8)алкила, R46 и R47;
каждый R46 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -C(=NH)-NH2,
-C(=NH)-NH-OH, -С(=NH)-NH-O-(C1-C8)алкил, -(C=O)-O-(C1-С8)алкил, -O-(С=O)-(C1-C8)алкил, -(С=O)-(C1-C8)алкил, -(C=O)-NH2, -(C=O)-NH(C1-С8)алкил, -(С=O)-N<[(C1-C8)алкил]2, -NH-(С=O)-(C1-C8)алкил,
-C(=NH)-NH2, -C(=NH)-NH-OH, -С(=NH)-NH-O-(C1-C8)алкил, -(С=O)-O-(C1-C8)алкил, -O-(C=O)-(C1-C8)алкил, -(С=O)-(C1-C8)алкил, -(C=O)-NH2, -(С=O)-NH(C1-C8)алкил, -(С=O)-N>[(C1-C8)алкил]2, -NH-(С=O)-(C1-C8)алкил, R37 и R38; и
каждый R47 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила;
где каждый (С1-C10)гетероарил и каждый (С2-C10)гетероциклил содержит 1-5 кольцевых гетероатомов, выбранных из азота, кислорода и серы,
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R3 представляет собой -NR15-C(=O)-R16, где R16 представляет собой (C3-C10)циклоалкил, незамещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, состоящей из (C1-C8)алкила, F, Cl, CN, ОН, NH2, CF3, (С2-C10)гетероциклила, (С6-C10)арила и (C1-C10)гетероарила, где указанный (С6-C10)арильный заместитель не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (C1-C8)алкила, F, Cl, Br, CN, ОН и CF3, и где указанный (С2-C10)гетероциклильный заместитель не замещен или замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из (С1-С8)алкила, -(С=O)-(C1-C8)алкил,
-(С=O)-O-(C1-C8)алкил, -S-(C1-С8)алкил, F, Br, ОН и CF3.
3. Соединение по п.1, где R2 представляет собой Н или (C1-C8)алкил, незамещенный или замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из ОН, -NH2, (C1-C8)алкил-NH-, [(C1-C8)алкил]2>N-, (С2-C10)гетероциклила и (C1-C10)гетероарила.
4. Соединение по п.1, где X представляет собой =O.
5. Соединение по п.1, где группа -Y-Z- имеет формулу -N=CH-.
6. Соединение по п.1, выбранное из группы, состоящей из
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилацетамида,
2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-фенилбутирамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-фенилпропионамида,
3-фтор-2-метил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)бензамида,
2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-трифторметилбензамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
2-(3-хлорфенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-тиен-2-илбутанамида,
1-ацетил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пиперидин-4-карбоксамида,
3-(2-метилфенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пропанамида,
соединения (2S)-2-амино-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-фенилбутирамида с трифторуксусной кислотой,
трифторацетата (2R)-2-амино-2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил)этанамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
2-этилсульфанил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)никотинамида,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
N-[2-(3-диметиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]-2-фтор-3-трифторметилбензамида,
6-оксо-2-фенил-N-(2-фенилциклопропил)-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-карбоксамида,
N-[1-(4-фторфенил)этил]-6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-карбоксамида,
[2-(3-диметиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепио[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-диметиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты (соли гидрохлорида),
3-{6-оксо-8-[((1R,2R)-2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-ил}бензилового эфира уксусной кислоты,
[2-(3-гидроксиметилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2R)-2-амино-2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида (соли гидрохлорида),
N-[1-(4-гидроксифенил)этил]-6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-карбоксамида,
2,3-дифтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)бензамида,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
N-(4-фторбензил)-6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-карбоксамида,
[2-(3-циклобутиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил] амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты (соли гидрохлорида),
[6-оксо-2-(3-пирролидин-1-илметилфенил)-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]]индол-8-ил] амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты (соли гидрохлорида),
трифторацетата N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-(1,2-транс)-2-[6-(трифторметил)пиридин-3-ил]циклопропанкарбоксамида,
(2R)-2-амино-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилацетамида (соли гидрохлорида),
(2R)-2-амино-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил)-3-фенилпропионамида (соли гидрохлорида),
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (3E)-4-фенил-бут-3-еновой кислоты,
2-индан-2-ил-N-(6-оксо-2-фенил-5,6-дигидро-1H- [1,2]диазепино [4,5,6-cd]индол-8-ил)ацетамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(4-фтор-фенил)циклопропанкарбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-пиридин-3-ил-циклопропанкарбоновой кислоты (соли гидрохлорида),
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(3-метоксифенил)циклопропанкарбоновой кислоты,
2-индан-2-ил-(6-оксо-5,6-дигидро-1-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида,
(2R)-2-гидрокси-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилэтанамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида уксусной кислоты (1,2-транс)-2-пиридин-2-илциклопропанкарбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида уксусной кислоты (1,2-транс)-2-(1H-имидазол-4-ил)циклопропанкарбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида(2R)-пиперидин-2-карбоновой кислоты (соли гидрохлорида),
(2S)-2-амино-3-циано-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пропионамида уксусной кислоты,
(2R)-2-амино-3-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пропанамида(соли гидрохлорида),
метилового эфира (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)-амино]-5,6-дигидро-1H-[1,2] диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2R)-3-(4-гидроксифенил)-2-(метиламино)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пропанамида (соли гидрохлорида),
(2R)-2-амино-3-(4-фторфенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)пропанамида (соли гидрохлорида),
метиламида (1R,2R)-6-оксо-8-[(2-фенил-циклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2-гидроксиэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2-диметиламиноэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-2-карбоновой кислоты,
(2R)-2-амино-2-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)этанамида (соли гидрохлорида),
(6-оксо-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(4-гидроксифенил)циклопропанкарбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(4-гидроксифенил)циклопропанкарбоновой кислоты,
(2-этил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2-хлор-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(3-бромфенил)циклопропанкарбоновой кислоты,
(6-оксо-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(3-гидроксифенил) циклопропанкарбоновой кислоты,
2-(3,4-дигидроизохинолин-2(1H)-ил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd] индол-8-ил)ацетамида,
(2-бром-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[6-оксо-2-(1,2,3,6-тетрагидропиридин-4-ил)-5,6-дигидро-1Н-[1,2]диазепино[4,5,6-cd]индол-8-ил]-амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты (соли гидрохлорида),
(1R,2R)-N-(6-оксо-2-пиридин-4-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилциклопропанкарбоксамида,
N-(6-оксо-2-пиридин-4-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-(1,2-транс)-2-пиридин-3-илциклопропанкарбоксамида,
N-(6-оксо-2-пиридин-3-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-(1,2-транс)-2-пиридин-3-илциклопропанкарбоксамида,
(1R,2R)-N-(6-оксо-2-пиридин-3-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилциклопропанкарбоксамида,
[2-(3-диметиламинопроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-диметиламинопропил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-диметиламинопропенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-метиламинопроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты (соли гидрохлорида),
[2-(3-метиламинопроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1,2-транс)-2-пиридин-3-илциклопропанкарбоновой кислоты (соли дигидрохлорида),
(2R)-2-амино-2-циклогексил-N-[2-(3-метиламино-проп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]ацетамида (соли дигидрохлорида),
(1,2-транс)-N-[1-(2-гидроксиэтил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]-2-фенилциклопропанкарбоксамида,
(2-диметиламинометил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенил-циклопропанкарбоновой кислоты,
[1-(2-аминоэтил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-морфолин-4-илпроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида(1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[6-оксо-2-(3-пирролидин-1-ил-проп-1-инил)-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил] амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты и
[1-(2-аминоэтил)-2-хлор-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(1H-имидазол-2-ил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2-циано-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты и
[2-(1H-имидазол-2-ил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты или
их фармацевтически приемлемой соли или сольвата.
7. Соединение по п.1, выбранное из группы, состоящей из
3-фтор-2-метил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)бензамида,
2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-тиен-2-илбутанамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-диметиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
3-{6-оксо-8-[((1R,2R)-2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]]индол-2-ил}бензилового эфира уксусной кислоты,
[2-(3-гидроксиметилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2R)-2-амино-2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-циклобутиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[6-оксо-2-(3-пирролидин-1-илметилфенил)-5,6-дигидро-1Н-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
2-индан-2-ил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(4-фторфенил)циклопропанкарбоновой кислоты,
(2R)-2-амино-3-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd] индол-8-ил)пропанамида,
метилового эфира (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2] диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
метиламида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2] диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2-гидроксиэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2-гидроксиэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(2R)-2-амино-2-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)этанамида,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(4-гидроксифенил) циклопропанкарбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(4-гидроксифенил)циклопропанкарбоновой кислоты,
(2-этил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2-этил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
2-(3,4-дигидроизохинолин-2(1H)-ил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd] индол-8-ил)ацетамида,
2-(3,4-дигидроизохинолин-2(1H)-ил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd] индол-8-ил)ацетамида,
[6-оксо-2-(1,2,3,6-тетрагидропиридин-4-ил)-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил] амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(1R,2R)-N-(6-оксо-2-пиридин-4-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилциклопропанкарбоксамида,
(1R,2R)-N-(6-оксо-2-пиридин-3-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилциклопропанкарбоксамида,
[2-(3-диметиламинопроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-диметиламинопропенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(3-метиламинопроп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2R)-2-амино-2-циклогексил-N-[2-(3-метиламино-проп-1-инил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]ацетамида,
(2-гидроксиметил-6-оксо-5,6-дигидро-1H-[1,2-cd]диазепино[4,5,6]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[6-оксо-2-(3-пирролидин-1-ил-проп-1-инил)-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил] амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
[2-(1H-имидазол-2-ил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2-циано-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты и
гидрохлорида (2R)-2-амино-2-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил)этанамида или
их фармацевтически приемлемой соли или сольвата.
8. Соединение по п.1, выбранное из группы, состоящей из
2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-тиен-2-илбутанамида,
[2-(3-гидроксиметилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2R)-2-амино-2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида (гидрохлорида),
6-оксо-2-фенил-N-[(1R)-1-фенилэтил]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-карбоксамида,
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2R)-2-гидрокси-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилэтанамида,
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-пиридин-2-илциклопропанкарбоновой кислоты (соли уксусной кислоты),
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1,2-транс)-2-(1H-имидазол-4-ил)циклопропанкарбоновой кислоты (соли уксусной кислоты),
(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (2R)-пиперидин-2-карбоновой кислоты (соли гидрохлорида),
гидрохлорида (2R)-2-амино-3-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил)пропанамида,
(2-диметиламиноэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
(6-оксо-2-фенил-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(4-гидрокси-фенил)циклопропанкарбоновой кислоты,
(2-этил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(1R,2R)-N-(6-оксо-2-пиридин-3-ил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-фенилциклопропанкарбоксамида и
[1-(2-аминоэтил)-2-хлор-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты или
их фармацевтически приемлемой соли или сольвата.
9. Соединение по п.1, выбранное из группы, состоящей из
2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-2-трифторметилбензамида,
N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-4-тиен-2-илбутанамида,
N-[2-(3-диметиламинометилфенил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]-2-фтор-3-трифторметилбензамида,
(2R)-2-амино-2-циклогексил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)ацетамида (гидрохлорида),
(6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты,
(2-диметиламиноэтил)амида (1R,2R)-6-оксо-8-[(2-фенилциклопропанкарбонил)амино]-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-2-карбоновой кислоты,
гидрохлорида (2R)-2-амино-2-(4-гидроксифенил)-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино [4,5,6-cd]индол-8-ил)этанамида,
(6-оксо-2-фенил-5,6-дигидро-1-[1,2]диазепино[4,5,6]индол-8-ил)амида (1,2-транс)-2-(4-гидроксифенил)циклопропанкарбоновой кислоты и
(2-этил-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)амида (1R,2R)-2-фенилциклопропанкарбоновой кислоты или
их фармацевтически приемлемой соли или сольвата.
10. Фармацевтическая композиция, содержащая соединение по п.1 или его фармацевтически приемлемую соль, для лечения новообразования.
11. Фармацевтическая композиция по п.10, где новообразование представляет собой рак.
12. Соединение по п.1, выбранное из группы, состоящей из
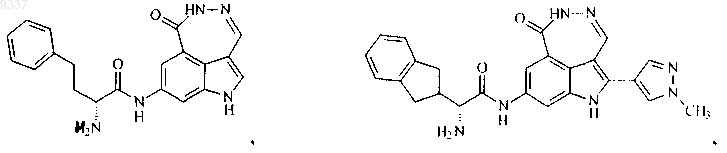
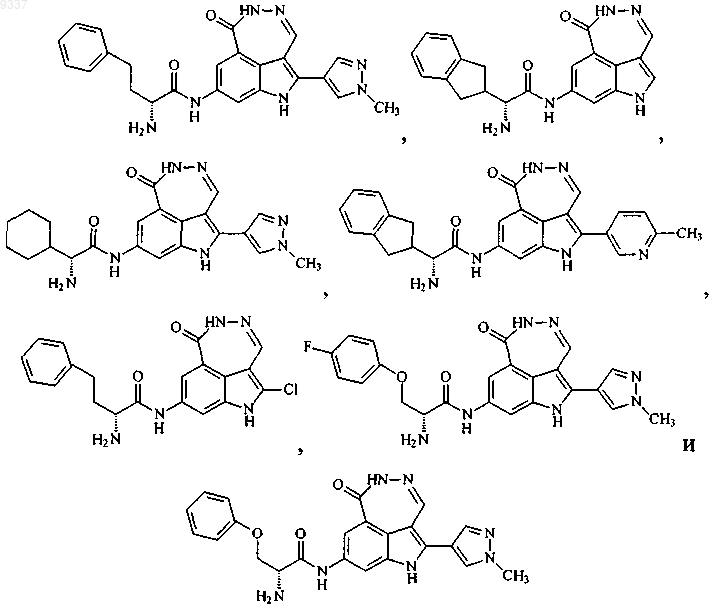
или его фармацевтически приемлемая соль.
13. Соединение по п.1, выбранное из группы, состоящей из
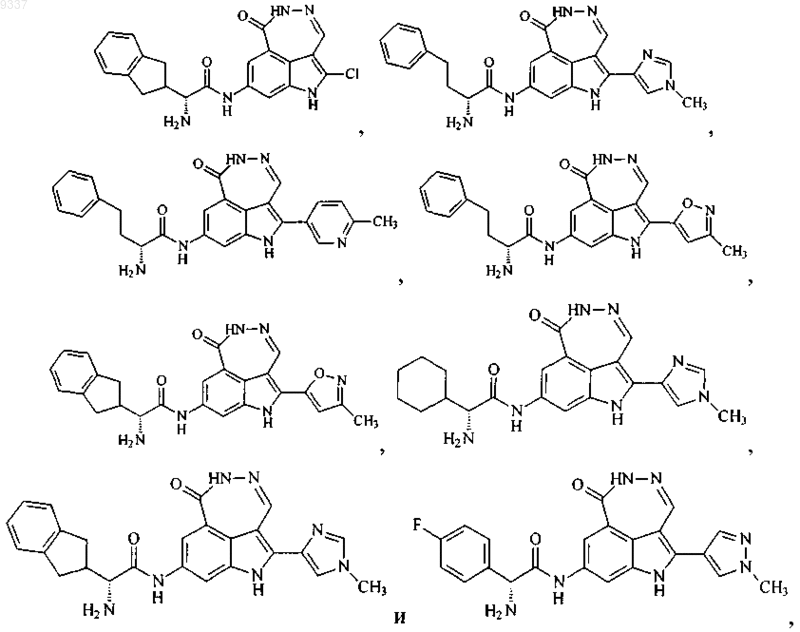
или его фармацевтически приемлемая соль.
14. Соединение по 1 формулы I(a)
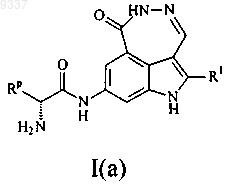
Где R1 выбран из группы, состоящей из Н, Cl,
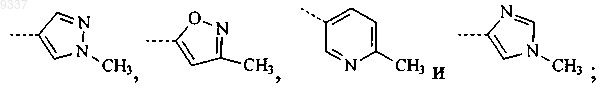
Rp выбран из группы, состоящей из
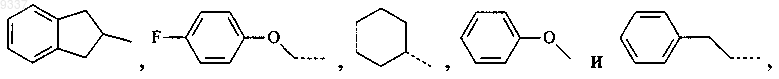
где "-----" указывет точки присоединения;
или его фармацевтически приемлемая соль.
Текст
009337 Область изобретения Данное изобретение относится к новым трициклическим соединениям формулы I, которые ингибируют протеинкиназы, предпочтительно чекпойнт протеинкиназу 1 (CHK-1). Кроме того, данное изобретение относится к фармацевтическим композициям, содержащим такие соединения, и к способам лечения состояния у млекопитающего, которое можно лечить путем ингибирования протеинкиназ, предпочтительно CHK-1, путем введения эффективных количеств таких соединений в комбинации с противоопухолевым агентом, лучевой терапией или в виде одиночного агента. Предшествующий уровень техники Клеточный цикл эукариотической клетки имеет тщательно отрегулированную последовательность фаз: пресинтетическая фаза (d), синтез ДНК (S), постсинтетическая фаза (G2) и митоз (М). G1, S и G2 известны как интерфаза. В фазе G1 клетка, биосинтетические пути которой были замедлены во время митоза, возобновляет высокую скорость биосинтеза РНК и белка. Фаза S начинается, когда начинается синтез ДНК, и заканчивается, когда содержимое ДНК ядра реплицировано. Тогда клетка входит в G2, где вновь происходит биосинтез РНК и белка. После G2 клетка вступает в фазу М, которая начинается с деления ядра и заканчивается полным делением цитоплазмы на две дочерние клетки. Это указывает на начало интерфазы для новых клеток. Неделящиеся клетки существуют в фазе покоя (G0), представляющей собой период после митоза, но перед синтезом ДНК. Чекпойнт-ферменты, такие как сериновая/треониновая протеинкиназа, названная чекпойнт киназой 1 (CHK-1 или р 56CHK-1), ответственны за поддержание последовательности и точности событий клеточного цикла. CHK-1 передает сигналы с комплекса, чувствительного к повреждению ДНК, для ингибирования активации комплекса Cdc2-циклин В, который способствует входу в митоз (Science, 277,1501-1505 (1997); Science, 277, 1497-1501 1997. У эукариот Cdc2 известен как Cdk1 (циклинзависимая киназа 1). CHK-1 регулирует Cdc25, представляющий собой фосфатазу двойной специфичности, которая активирует Cdc2. Таким образом, CHK-1 служит в качестве прямой связи между чекпойнтом G2 и отрицательным регулированием Cdc2. У здоровых клеток имеются оба чекпойнта G1 и G2 и ассоциирующиеся с ними процессы восстановления для обеспечения жизнеспособности после лечения повреждения ДНК (химиотерапией и/или облучением). Тем не менее, раковые клетки полагаются исключительно на чекпойнт G2 и ассоциирующиеся с ним процессы восстановления для того, чтобы оставаться жизнеспособными и продолжать репликацию. Отмена чекпойнта G2 может оставить раковые клетки без способов задерживать вхождение в митоз после повреждения ДНК. Было продемонстрировано, что инактивация CHK-1 отменяет задержкуG2, индуцированную повреждением ДНК, вызванным противоопухолевыми агентами или эндогенным повреждением ДНК. В дополнение, инактивация СНК-1 приводит в результате к предпочтительной гибели образующихся в результате клеток с повреждением ДНК, имеющих дефект чекпойнта (Cell, 91, 865867 (1997); Science, 277,1450-1451 (1997); Nature, 363, 368-371 (1993); Molec. Biol. Cell, 5, 147-160(1994. Таким образом, существует необходимость в небольших молекулярных ингибиторах CHK-1 для предпочтительной отмены чекпойнта G2 по равнению с G1 и для эффективного удаления только того чекпойнт-контроля, который обнаружен при многих типах раков. При введении в процессе повреждения ДНК, таком как химиотерапия с использованием противоопухолевых агентов, лучевая терапия, способы иммунотерапии и антиангиогенной терапии, ингибитор CHK-1 может сенсибилизировать раковые клетки, инициируя тем самым апоптоз, опосредованный повреждением. Таким образом, существует необходимость в комбинированном лечении, включающем ингибитор CHK-1 в процессе повреждения ДНК. Поскольку протеинкиназы распространены повсеместно и взаимосвязаны, избирательное модулирование одной киназы, такой как CHK-1, или семейства киназ может в результате не привести к эффективному терапевтическому лечению. Таким образом, существует необходимость в небольших молекулярных ингибиторах для влияния на одну или более чем одну целевую протеинкиназу, ингибирование которой в целом может привести к желаемому терапевтическому лечению. Хотя избирательность киназ и их связь с генерализованной токсичностью являются важными, терапевтическая эффективность может основываться на ингибировании более чем одной протеинкиназы. Химические основные структуры, которые могут быть подходящим образом прикреплены для избирательного и сильного взаимодействия с целевыми протеинкиназами, представляют собой ценное средство для разработки лекарств и научного исследования. Таким образом, существует необходимость в такой основной структуре в качестве ингибитора одной или более чем одной протеинкиназы. При введении в виде одиночного агента или в качестве вспомогательной терапии, ингибиторы протеинкиназы, такие как ингибиторы CHK-1 по настоящему изобретению, могут оказаться благоприятными при лечении ряда заболеваний человека, таких как рак. Для лечения рака были предложены некоторые ингибиторы CHK-1 (см. Sanchez, Y. et. al. (1997)Science 277: 1497-1501 и Flaggs, G. et. al. (1997) Current Biology 7: 977-986; патенты США 6,413,755,6,383,744 и 6,211,164; и международные публикацииWO 01/16306, WO 01/21771, WO 00/16781 и WO 02/070494). Краткое изложение сущности изобретения Задача данного изобретения заключается в том, чтобы предложить соединения, которые ингибируют активность одной или более чем одной протеинкиназы, такой как CHK-1.-1 009337 В общем аспекте данное изобретение относится к ингибитору протеинкиназы, предпочтительно ингибитору CHK-1, представляющему собой трициклические соединения формулы I(г) R35 или R36, (С 2-С 8)алкенил или (C2-C8)алкинил где каждый из указанных (С 2-С 8)алкенила или(C2-C8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из F, Cl, ОН, -NH2, R40 и R42;(з) R36, (С 2-С 8)алкенил или (С 2-С 8)алкинил где каждый из указанных R3(С 2-С 8)алкенила или (С 2-С 8) алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из-NС 1-С 8)алкил)С 2-С 8)алкинил) где каждый из указанных R26(C2-С 8)алкенила или (C2-C8)алкинила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из R40, R41 иR5 выбран из группы, состоящей из Н, (С 1-С 8)алкиа, (С 1-С 8)алкил-O- и R36; каждый R6 и R7 независимо выбран из группы, состоящей из Н, (С 1-С 3)алкила и R36;R ; каждый из R9, R10 и R11 независимо выбран из группы, состоящей из Н, (C1-С 8)алкила и R36;R ; где каждый из указанных R15 и R16 (С 2-С 8)алкенила или (C2-С 8)алкинила не замещен или замещен 14 заместителями, независимо выбранными из группы, состоящей из R40, R41 и R42;R19, R20 и R21 независимо выбраны из группы, состоящей из Н, (С 1-С 8)алкила и R36;R22, R23 и R24 независимо выбраны из группы, состоящей из Н, (С 1-С 8)алкила и R36;R26 выбран из группы, состоящей из -С(=O)-O-С(CH3)3, (С 1-С 8)алкила, (C3-С 10)циклоалкила, (С 2-C10) гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; или R25 и R26 могут быть взяты вместе с атомом азота, к которому они присоединены, с образовани-2 009337 ем 5-8-членного гетероарильного или гетероциклильного кольца;(С 1-C10)гетероарил; или R29 и R30 могут быть взяты вместе с атомом азота, к которому они присоединены, с образованием 5-8-членного гетероарильного или гетероциклильного кольца;R32 независимо выбран из группы, состоящей из (С 1-С 8)алкила, (C3-C10)циклоалкила, (C2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; или R31 и R32 могут быть взяты вместе с атомом азота, к которому они присоединены, с образованием 5-8-членного гетероарильного или гетероциклильного кольца;(С 1-C10)гетероарил; каждый R35 независимо выбран из группы, состоящей из Н, F, Cl, Br, I, CN, ОН, NO2, -NH2, -NHC(=O)-O-C(CH3)3 и CF3; каждый R36 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; каждый R37 независимо выбран из группы, состоящей изR38 представляет собой R28 -SOn-; где n представляет собой 0, 1 или 2, когда -SOn- связан с R28 через атом углерода R28, или где n представляет собой 1 или 2, когда -SOn-связан с R28 через кольцевой атом азота R28;R39 представляет собой R29R30N-SOn-; где n представляет собой 1 или 2; где каждый из указанного (С 1-С 8)алкила, где бы он не находился в любом из указанных R1(a)-(г),2R (a)-(г), R3(a)-(к), R4, R37, R38 или R39, является незамещенным или замещенным 1-4 заместителями, независимо выбранными из группы, состоящей из (С 2-С 8)алкенила, R40, R41 и R42; где каждый из указанных (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила или (С 1-C10) гетероарила, где бы он не находился в указанных R36, R37, R38 или R39, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из R40;R40 выбран из группы, состоящей из (С 1-С 8)алкила, R41, R42 и R43; каждый R41 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -NH2, -NHC(=O)-O-C(CH3)3, СООН, -С(=O)(С 1-С 8)алкила, -C(=O)-O-(C1-С 8)алкила, -NH-SO2-(C1-C8)алкила, -NHSO2-(С 6-C10)арила и CF3; каждый R42 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10) арила и (С 1-С 10)гетероарила; каждый R43 независимо выбран из группы, состоящей из:(в) R34-SOn-; где n представляет собой 0, 1 или 2, когда -SOn- связан с R34 через атом углерода R34,или где n представляет собой 1 или 2, когда -SOn- связан с R34 через кольцевой атом азота R34; где каждый из указанного (С 1-С 8)алкила, где бы он не находился в любом из R40, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из группы, состоящей из R44 и R45; где каждый из указанных (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила или (С 1-C10)гетероарила, где бы он не находился в любом из указанных R42 или R43, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из группы, состоящей из R47, выбранного из группы, состоящей из (С 1-С 8)алкила, R44 и R45; каждый R44 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -NH2, -CF3,-C(=NH)-NH2, -C(=NH)-NH-OH, -C(=NH)-NH-O-(С 1-С 8)алкила, -(С=O)-O-(С 1-С 8)алкила, -O-(С=O)-(С 1-С 8) алкила, -(С=O)-(С 1-С 8)алкила, -(C=O)-NH2, -(C=O)-NH(С 1-С 8)алкила, -(C=O)-N[(С 1-С 8)алкил]2, -NH(C=O)-(С 1-С 8)алкила, R37 и R38; каждый R45 независимо выбран из группы, состоящей из (С 3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10) арила и (С 1-C10)гетероарила; где каждый из указанного (С 1-С 8)алкила, где бы он не находился в любом из указанных R44 или R45,независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из-3 009337 группы, состоящей из R46 и R47; где каждый из указанных (С 3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила или (С 1-C10) гетероарила, где бы он не находился в любом из указанных R43 или R44, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, R46 и R47; каждый R46 независимо выбран из группы, состоящей из F, Cl, Br, I, CN, ОН, NO2, -C(=NH)-NH2,-C(=NH)-NH-OH, -С(=NH)-NH-O-(С 1-С 8)алкила, -(C=O)-O-(C1-С 8)алкила, -O-(С=O)-(С 1-С 8)алкила,-(С=O)-(С 1-С 8)алкила, -(C=O)-NH2, -(C=O)-NH(C1-C8)алкила, -(C=O)-N[(С 1-С 8)алкил]2, -NH-(C=O)-(С 1 С 8)алкила, -C(=NH)-NH2, -C(=NH)-NH-OH, -C(=NH)-NH-O-(C1-C8)алкила, -(С=O)-O-(С 1-С 8)алкила, -O(C=O)-(C1-C8)алкила, -(С=O)-(С 1-С 8)алкила, -(C=O)-NH2, -(С=O)-NH(С 1-С 8)алкила, -(C=O)-N[(C1-С 8) алкил]2, -NH-(С=O)-(C1-C8)алкила, R37 и R38; и каждый R47 независимо выбран из группы, состоящей из (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; или их фармацевтически приемлемую соль. Данное изобретение также относится к фармацевтически приемлемым пролекарствам, фармацевтически активным метаболитам и фармацевтически приемлемым солям соединений формулы I. Также предложены фармацевтически приемлемые соли таких активных метаболитов. Также описаны благоприятные способы получения соединений формулы I. Соединения по данному изобретению включают все стереоизомеры (например, цис и транс изомеры) и все оптические изомеры соединений формулы I (например, R и S энантиомеры), а также рацемические, диастереоизомерные и другие смеси таких изомеров. Соединения по данному изобретению могут также существовать в различных таутомерных формах. Данное изобретение относится ко всем таутомерам формулы I. Соединения по данному изобретению могут содержать олефиноподобные двойные связи. Когда такие связи присутствуют, соединения по данному изобретению существуют в цис и транс конфигурациях и в виде их смесей. В первом воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой (С 1-С 8)алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из F, ОН, -NH2, (С 1-С 8)алкил-NH-, (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 6-C10) гетероарила. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R3 выбран из группы, состоящей из (С 2-С 8)алкенила, (С 2-С 8)алкинила, (C3-С 6)циклоалкила, (С 2-C10)гетероциклила,фенила и (С 1-C10)гетероарила; где каждый из указанных (С 2-С 8)алкенила или (С 2-С 8)алкинила не замещен или замещен 1-3 заместителями, независимо выбранными из группы, состоящей из F, ОН, -NH2, (C1-С 8) алкил-NH-, [(С 1-С 8)алкил]2N-, (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1C10)гетероарила; и где каждый из указанных (C3-С 6)циклоалкила, (C2-C10)гетероциклила, фенила или (С 1C10)гетероарила не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкила]2N-, (C3-C10)циклоалкила, (С 2C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила. В предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -C(=O)-NR13R14 где R13 представляет собой Н или (С 1-С 8)алкил, где указанный R13(С 1-С 4)алкил не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из F, ОН, -NH2, R41 и R42; где каждый из указанного R36 не замещен или замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из (С 6-C10)арила, (C1-C10)гетероарила, (С 2-C10) гетероциклила, (С 1-С 8)алкил-NH- и [(С 1-С 8)алкил]2N-; и где каждый из указанного (С 6-C10)арильного заместителя не замещен или замещен 1-3 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, Cl, -CF3, и ОН. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R15 представляет собой (С 1-С 8)алкил, не замещенный или замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из ОН, CN, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N-, [(С 1-С 8)алкил][(С 3C10)циклоалкил]N-, (С 3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; где указанный (С 6-C10)арильный заместитель не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, Cl, Br, CN, ОН и CF3; и где указанный (С 2-C10) гетероциклильный заместитель не замещен или замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из (C1-С 8)алкила, -(С=O)-(С 1-С 8)алкила, -(С=O)-O-(С 1-С 8)алкила, -S(С 1-С 8)алкила, F, Br, ОН и CF3. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -NR15-C(=O)-R16; где R16 представляет собой (С 2-С 8)алкенил, незамещенный или замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из (С 3-C10)циклоалкила, (С 2C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; где указанный (С 6-C10)арильный заместитель не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)ал-4 009337 кила, F, Cl, Br, CN, ОН и CF3; и где указанный (C2-C10)гетероциклильный заместитель не замещен или замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, -(С=O)-(С 1-С 8)алкила, -(C=O)-O-(С 1-С 8)алкила, -S-(С 1-С 8)алкила, F, Br, ОН и CF3. В предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -NR15-C(=O)-R16; где R16 представляет собой (C1-C10)гетероарил, незамещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, состоящей из (С 1-С 8) алкила, -(С=O)-(С 1-С 8)алкила, -S-(С 1-С 8)алкила, F, Cl, CN, ОН и CF3. Более предпочтительно, R16 (С 1-C10) гетероарил представляет собой пиридинил. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -NR15-C(=O)-R16; где R16 представляет собой (C3-C10)циклоалкил, не замещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, Cl, CN, ОН, NH2, CF3, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; где указанный (С 6-C10)арильный заместитель не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, Cl, Br, CN, ОН и CF3; и где указанный(С 2-C10)гетероциклильный заместитель не замещен или замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, -(С=O)-(С 1-С 8)алкила, -(С=O)-O-(С 1-С 8)алкила, -S-(C1-С 8)алкила, F, Br, ОН и CF3. Более предпочтительно, указанный R16 (C3-C10)циклоалкил выбран из группы, состоящей из циклопропила и циклогексила. Более предпочтительно, указанные (С 6C10)арильные заместители не замещены. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -NRl5-C(=O)-R16; где R16 представляет собой (С 2-C10)гетероциклил, незамещенный или замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из (С 1 С 8)алкила, -(С=O)-(С 1-С 8)алкила, -(С=O)-O-(С 1-С 8)алкила, F, Cl, CN, ОН и CF3. Более предпочтительно,указанный R16 (С 2-C10)гетероциклил выбран из группы, состоящей из пиперазинила, пиперидинила, пирролидинила, пирролидинонила, тиадиазолила, тетрагидроизохинолинила, тетрагидронафталинила и инданила. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R3 представляет собой -NR15-C(=O)-R16; где R16 представляет собой фенил, незамещенный или замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, (С 1-С 8) алкил-O-, F, Cl, Br, CN, ОН и CF3. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R1 представляет собой (С 1-С 8)алкил, замещенный 1-2 заместителями, независимо выбранными из группы, состоящей из F, Cl, -ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (С 1-С 8)алкил-О-; где каждый из указанного (С 1-С 8)алкильного заместителя, где бы он не находился, независимо является незамещенным или замещенным 1-3 заместителями, независимо выбранными из группы, состоящей из -NH2, (С 1-С 8)алкилNH-, [(С 1-С 8)алкил]2N-, -O-(С=O)-(С 1-С 8)алкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1C10)гетероарила. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R1 представляет собой незамещенный (С 1-С 8)алкил, такой как метил или этил. В еще одном воплощении данное изобретение относится к соединениям формулы I где R1 представляет собой (C2-C8)алкенил или (C2-C8)алкинил; где каждый из указанного (C2-C8)алкенила или (С 2 С 8)алкинила не замещен или замещен 1-2 заместителями, независимо выбранными из группы, состоящей из -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N-, (С 2-C10)гетероциклила и (С 1-C10)гетероарила; где каждый из указанного (С 1-С 8)алкильного заместителя, где бы он не находился, независимо является незамещенным или замещенным 1 -3 заместителями, независимо выбранными из группы, состоящей из -NH2, (С 1 С 8)алкил-NH-, [(С 1-С 8)алкил]2N-, -O-(С=O)-(С 1-С 8)алкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1C10)гетероарила. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R1 представляет собой R36, выбранный из группы, состоящей из Н, Cl и Br. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R1 выбран из группы, состоящей из (C3-С 6)циклоалкила, (С 2-C10)гетероциклила, фенила и (С 1-C10)гетероарила; где каждый из указанных (С 2-C10)гетероциклила, фенила или (С 1-C10)гетероарила не замещен или замещен 13 заместителями, независимо выбранными из группы, состоящей из (С 1-С 8)алкила, F, Cl, -NH2, -ОН, (С 1 С 8)алкил-NH- и [(С 1-С 8)алкил]2-N-; где каждый из указанного (C1-С 8)алкильного заместителя, где бы он не находился, не замещен или замещен 1-3 заместителями, выбранными из -NH2, (С 1-С 8)алкила-NH-,[(С 1-С 8)алкил]2N-, -O-(С=O)-(С 1-С 8)алкила, (С 2-С 10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила. В данном воплощении предпочтительно R1 представляет собой фенил, тетрагидропиридинил, пиперидинил или пиридинил. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R1 представляет собой -C(=O)-R5, и R5 представляет собой (С 1-С 8)алкил-O- или (С 2-C10)гетероциклил, такой как морфолинил; где указанный R5 (С 2-C10)гетероциклил не замещен или замещен (С 1-С 8)алкилом, таким как метил или этил.-5 009337 В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где R1 представляет собой -C(=O)-NR6R7; где каждый из указанных R6 и R7 независимо представляет собой Н или (С 1-С 8)алкил; и где каждый из указанных R6 и R7 (С 1-С 8)алкила не замещен или замещен 1-3 заместителями, независимо выбранными из группы, состоящей из ОН, -NH2, (С 1-С 8)алкил-NH-, [(C1 С 8)алкил]2N-, (С 2-C10)гетероциклила и (С 1-C10)гетероарила. В еще одном предпочтительном воплощении данное изобретение относится к соединениям Формулы I, где R2 представляет собой Н или (С 1-С 8)алкил, не замещенный или замещенный 1-4 заместителями,независимо выбранными из группы, состоящей из ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N-, (С 2C10)гетероциклила и (С 1-C10)гетероарила. В еще одном воплощении данное изобретение относится к соединениям формулы I, где А представляет собой =N-. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R2 представляет собой -C(=O)-R8, где R8 выбран из группы, состоящей из (С 1-С 8)алкила, (С 2-С 8)алкенила, (С 2 С 8)алкинила, -NH2, и R37 выбран из группы, состоящей из (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (С 1 С 8)алкил-O-; где каждый из указанных R8 и R37 (С 1-С 8)алкила, где бы он не находился, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из R40, выбранного из группы, состоящей из F, ОН, -NH2, (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила, (С 1-C10) гетероарила, (С 1-С 8)алкил-NH- и [(С 1-С 8)алкил]2N-; где каждый из указанного R40 (С 1-С 8)алкила, где бы он не находился, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из R44, независимо выбранного из группы, состоящей из ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (C3-C10)циклоалкил-NH-; где каждый из указанных R40 (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила или (С 1C10)гетероарила, где бы он не находился, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из R47, выбранного из группы, состоящей из (С 1-С 8)алкила, ОН,-NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (C3-C10)циклоалкил-NH-; и где каждый из указанного R47 (С 1-С 8)алкила, где бы он не находился, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из группы, состоящей из ОН,-NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (C3-С 10)циклоалкил-NH. В еще одном воплощении данное изобретение относится к соединениям формулы I, где R2 представляет собой -C(=O)-R8, где R8 выбран из группы, состоящей из (C3-С 6)циклоалкила, (С 2-C10) гетероциклила, фенила или (С 1-C10)гетероарила; где каждый из указанных R8(C3-С 6)циклоалкила, (С 2-C10)гетероциклила, фенила или (C1-C10)гетероарила не замещен или замещен 1-4 заместителями, независимо выбранными из R40, выбранного из группы, состоящей из (С 1-С 8)алкила, F, ОН, -NH2, (С 1-С 8)алкил-NH-,[(С 1-С 8)алкил]2N-, (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила и (С 1-C10)гетероарила; где каждый из указанного R40 (С 1-С 8)алкила, где бы он не находился, независимо является незамещенным или замещенным 1-4 заместителями, независимо выбранными из R44, независимо выбранного из группы,состоящей из ОН, -NH2, (С 1-С 8)алкил]-NH-, [(С 1-С 8)алкил]2N-, и (C3-C10)циклоалкил-NH-; где каждый из указанных R40 (C3-C10)циклоалкила, (С 2-C10)гетероциклила, (С 6-C10)арила или (C1-C10)гетероарила не замещен или замещен 1-4 заместителями, независимо выбранными из R47, выбранного из группы, состоящей из (С 1-С 8)алкила, ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (C3-C10)циклоалкил-NH-; где каждый из указанного R47 (С 1-С 8)алкила, где бы он не находился, не замещен или замещен 1-4 заместителями, независимо выбранными из группы, состоящей из ОН, -NH2, (С 1-С 8)алкил-NH-, [(С 1-С 8)алкил]2N- и (C3-C10)циклоалкил-NH. В еще одном воплощении данное изобретение относится к соединениям формулы I, где указанныйR3 находится в любом из положений 7, 8 или 9 указанного соединения формулы I. Предпочтительно,данное изобретение относится к соединениям формулы I, где указанный R3 находится в положении 8 указанного соединения формулы I. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где указанный R4 находится в положении 7 указанного соединения формулы I. Более предпочтительно, указанный R3 находится в положении 8 указанного соединения формулы I, и указанный R4 находится в положении 7 указанного соединения формулы I. В еще одном воплощении данное изобретение относится к соединениям формулы I, где указанныйR4 представляет собой Cl или Br в положении 7 указанного соединения формулы I. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где указанный R4 представляет собой Н в положении 7 указанного соединения формулы I. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где X представляет собой О. В еще одном предпочтительном воплощении данное изобретение относится к соединениям формулы I, где группа -Y-Z- имеет формулу -N=CH-. Предпочтительно, данное изобретение относится к соединениям формулы I, выбранными из группы[2-(1H-имидазол-2-ил)-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида(1R,2R)-2 фенилциклопропанкарбоновой кислоты; или их фармацевтически приемлемых солей или сольватов. Другие предпочтительные соединения выбраны из группы, состоящей из 3-фтор-2-метил-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)бензамида; 2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида;[4,5,6-cd]индол-8-ил)этанамида; или их фармацевтически приемлемых солей или сольватов. Другие предпочтительные соединения формулы I выбраны из группы, состоящей из 2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3 трифторметилбензамида;[1-(2-аминоэтил)-2-хлор-6-оксо-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил]амида (1R,2R)2-фенилциклопропанкарбоновой кислоты; или их фармацевтически приемлемых солей или сольватов. В еще одном воплощении данное изобретение также относится к соединениям формулы I, которые являются избирательными в отношении CHK-1 по сравнению с CHK-2, причем отношение избирательности составляет от приблизительно 5 раз до приблизительно 5000 раз; предпочтительно от приблизительно 50 раз до приблизительно 1000 раз; и более предпочтительно от приблизительно 70 раз до приблизительно 830 раз. В этом воплощении более предпочтительные соединения выбраны из группы, состоящей из 2-фтор-N-(6-оксо-2-фенил-5,6-дигидро-1H-[1,2]диазепино[4,5,6-cd]индол-8-ил)-3-трифторметилбензамида;(1R,2R)-2-фенилциклопропанкарбоновой кислоты; или их фармацевтически приемлемых солей или сольватов. В задачу данного изобретения также входит предложение композиции для лечения новообразований и для усиления противоопухолевых действий противоопухолевых агентов и терапевтического облучения. В одном воплощении данное изобретение относится к композиции, содержащей соединение формулы I, его фармацевтически приемлемую соль, сольват или пролекарство и противоопухолевый агент в виде комбинированного препарата для одновременного, раздельного или последовательного применения при лечении новообразования. В еще одном воплощении данное изобретение относится к композиции, содержащей соединение формулы I, его фармацевтически приемлемую соль, сольват или пролекарство и противоопухолевый агент в виде комбинированного препарата для одновременного, раздельного или последовательного применения при лечении новообразования, где противоопухолевый агент выбран из группы, состоящей из алкилирующих агентов, антибиотиков и растительных алкалоидов, гормонов и стероидов, синтетических агентов, обладающих противоопухолевой активностью, антиметаболитов и биологических молекул,обладающих противоопухолевой активностью. В еще одном воплощении данное изобретение относится к композиции, содержащей соединение формулы I, его фармацевтически приемлемую соль, сольват или пролекарство и противоопухолевый агент в виде комбинированного препарата для одновременного, раздельного или последовательного применения при лечении новообразования, где противоопухолевый агент выбран из группы, состоящей из цитарабина (Ara-с), этопозида (VP-16), цис-платина, адриамицина, 2-хлор-2-дезоксиаденозина, 9-(3-Dарабинозил)-2-фтораденина, карбоплатина, гемцитабина, камптотецина, паклитаксела, кармустина(BCNU), 5-фторурацила, иринотекана и доксорубицина. Задача данного изобретения также заключается в предложении способа лечения новообразований. В одном воплощении данное изобретение относится к способу лечения новообразования, при котором осуществляют введение млекопитающему, нуждающемуся в таком лечении, противоопухолевого агента в комбинации с соединением формулы I, его фармацевтически приемлемой солью, сольватом или пролекарством. В еще одном воплощении данное изобретение относится к способу лечения новообразования, при котором осуществляют введение млекопитающему, нуждающемуся в таком лечении, противоопухолевого агента в комбинации с соединением формулы I, его фармацевтически приемлемой солью, сольватом или пролекарством, где противоопухолевый агент выбран из группы, состоящей из Аra-c, VP-16, цис- 11009337 платина, адриамицина, 2-хлор-2-дезоксиаденозина, 9D-арабинозил-2-фтораденина, карбоплатина,гемцитабина, камптотецина, паклитакселя, BCNU, 5-фторурацила, иринотекана и доксорубицина. В еще одном воплощении может быть применено более чем один противоопухолевый агент в комбинации соединением формулы I, его фармацевтически приемлемыми солями, сольватами или пролекарствами. Задача данного изобретения также заключается в предложении способов усиления противоопухолевого действия терапевтического облучения. В одном воплощении данное изобретение относится к способу лечения новообразования, при котором применяют в отношении млекопитающего, нуждающегося в таком лечении, терапевтическое облучение, оказывающее противоопухолевое действие, в комбинации с соединением формулы I, его фармацевтически приемлемой солью, сольватом и пролекарством. Задача данного изобретения также заключается в предложении способов усиления противоопухолевого действия противоопухолевого агента. В одном воплощении данное изобретение относится к способу усиления противоопухолевого действия противоопухолевого агента у млекопитающего, при котором осуществляют введение млекопитающему, нуждающемуся в таком лечении, соединения формулы I, его фармацевтически приемлемой соли, сольвата или пролекарства в комбинации с противоопухолевым агентом. Противоопухолевые агенты включают алкилирующие агенты, антибиотики и растительные алкалоиды, гормоны и стероиды, синтетические агенты, обладающие противоопухолевой активностью, антиметаболиты и биологические молекулы, обладающие противоопухолевой активностью. Конкретные противоопухолевые агенты включают Ara-c, VP-16, цис-платин, адриамицин, 2-хлор-2-дезоксиаденозин, 9D-арабинозил-2-фтораденин,карбоплатин, гемцитабин, камптотецин, паклитаксел, BCNU, 5-фторурацил, иринотекан и доксорубицин. В еще одном воплощении данное изобретение относится к способу усиления противоопухолевого действия терапевтического облучения у млекопитающего, при котором осуществляют введение млекопитающему, нуждающемуся в таком лечении, соединения формулы I, его фармацевтически приемлемой соли, сольвата или пролекарства в комбинации с терапевтическим облучением, оказывающим противоопухолевое действие. Задача данного изобретения также заключается в предложении способа лечения состояния, которое можно лечить путем ингибирования протеинкиназ. В первом воплощении данного изобретения протеинкиназы выбраны из группы, состоящей из чекпойнт киназы 1 (CHK-1), чекпойнт киназы 2 (CHK-2), циклинзависимой киназы 1 (CDK1), сывороточной и регулируемой глюкокортикоидами киназы (SGK), аденозин-5'-монофосфат (АМФ)-активируемой протеинкиназы (AMPK), тирозинкиназы лимфоидных Тклеток (LCK), митогенактивируемой протеинкиназы 2 (MAPK-2), митоген- и стрессактивируемой протеинкиназы 1 (MSK1), Rho-киназы (ROCK-II), P70 S6 киназы (p70S6K), цАМФ (циклический аденозин 3',5'-монофосфат)-зависимой протеинкиназы (PKA), митогенактивируемой протеинкиназы (MAPK), митогенактивируемой протеинкиназы 1 (MAPK-1), киназы 2, родственной протеинкиназе-С (PRK2), 3'фосфоинозитидзависимой киназы-1 (PDK1), Fyn-киназы (FYN), протеинкиназы-С (PKC), протеинкиназы-С бета 2 (PKCII), протеинкиназы-С гамма (PKC), рецептора 2 фактора роста эндотелия сосудов(VEGFR-2), рецептора фактора роста фибробластов (FGFR), киназы фосфорилазы (РНК), Wee1 киназы(Wee1) и протеинкиназы В (PKB). Предпочтительно, протеинкиназы выбраны из группы, состоящей из чекпойнт киназы 1 (CHK-1), чекпойнт киназы 2 (CHK-2), митогенактивируемой протеинкиназы (MAPK),митогенактивируемой протеинкиназы 1 (MAPK-1), митогенактивируемой протеинкиназы 2 (MAPK-2),рецептора 2 фактора роста эндотелия сосудов (VEGFR-2), рецептора фактора роста фибробластов(FGFR), киназы фосфорилазы (PHK), протеинкиназы В альфа (PKBa) и Wee1 киназы (Wee1). В одном воплощении данное изобретение относится к способу лечения состояния, которое можно лечить путем ингибирования протеинкиназ, у млекопитающего, включающего человека, при котором млекопитающему, нуждающемуся в таком лечении, вводят соединение формулы I, его фармацевтически приемлемую соль, сольват или пролекарство. В еще одном воплощении указанное состояние, которое можно лечить путем ингибирования протеинкиназ, выбрано из группы, состоящей из расстройств соединительной ткани, воспалительных расстройств, иммунологических/аллергических расстройств, инфекционных заболеваний, респираторных заболеваний, сердечно-сосудистых заболеваний, заболеваний глаз, метаболических заболеваний, расстройств центральной нервной системы (ЦНС), заболевания печени/почек, расстройств репродуктивного здоровья, желудочных расстройств, кожных расстройств и рака. Другие преимущества и предпочтительные особенности данного изобретения будут понятны из приведенного ниже подробного описания.- 12009337 Подробное описание и предпочтительные воплощения данного изобретения Для задач настоящего изобретения, как здесь описано и заявлено, термины и сокращения определены следующим образом. Если не указано иначе, термин "где бы он не находился" относится к любому появлению любой из функциональных групп (таких как R1, R2 или любых их заместителей), включая любое появление любого компонента любых функциональных групп, упомянутых здесь (например, (C1-С 8)алкильный компонент(С 1-С 8)алкил-O-). Если не указано иначе, "(C1-С 8)алкил", так же как и (C1-С 8)алкильный компонент других терминов,упомянутых здесь (например, (C1-С 8)алкильный компонент (С 1-С 8)алкил-O-), может быть линейным или разветвленным (таким как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил). Если не указано иначе, термин "(С 2-С 8)алкенил" обозначает прямоцепочечный или разветвленный углеводородный радикал, заместитель, группировку или субгруппировку, упомянутую здесь, имеющую 2-8 атомов углерода, по меньшей мере одну двойную связь, включающие этенил, 1-пропенил, 2 пропенил (аллил), изопропенил, 2-метил-1-пропенил, 1-бутенил или 2-бутенил, но не ограничивающиеся ими. Если не указано иначе, термин "(С 2-С 8)алкинил" используется здесь для обозначения прямоцепочечного или разветвленного углеводородного радикала, заместителя, группировки или субгруппировки,упомянутой здесь, имеющей 2-8 атомов углерода, имеющей одну тройную связь, включающей этинил-СС-СН 2CH3), но не ограничивающейся ими. Если не указано иначе, термин "(C3-C10)циклоалкил" относится к неароматическому, насыщенному или частично насыщенному, моноциклическому или конденсированному, спиро- или неконденсированному бициклическому или трициклическому углеводородному радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, содержащим в общем от 3 до 10 атомов углерода, предпочтительно 5-8 кольцевых атомов углерода. Примеры (C3-C10)циклоалкилов включают моноциклические кольца,имеющие 3-7, предпочтительно 3-6 атомов углерода, такие как циклопропил, циклобутил, циклопентил,циклогексил, циклогептил и т. п. Иллюстративные примеры (C3-C10)циклоалкила получают из следующих: но не ограничиваются ими. Если не указано иначе, термин "(С 2-C10)гетероциклил" относится к неароматическому, насыщенному или частично насыщенному, моновалентному, моноциклическому или конденсированному, спироили неконденсированному бициклическому или трициклическому радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, содержащим в общем от 2 до 10 кольцевых атомов углерода и от 1 до 5 кольцевых гетероатомов, выбранных из азота, кислорода и серы. Иллюстративные примеры (С 2C10)гетероциклила включают азетидинил, пирролидил, пиперидил, пиперазинил, морфолинил, хроменил,тетрагидро-2H-1,4-тиазинил, тетрагидрофурил, дигидрофурил, тетрагидропиранил, дигидропиранил, 1,3 диоксоланил, 1,3-диоксанил, 1,4-диоксанил, 1,3-оксатиоланил, 1,3-оксатианил, 1,3-дитианил, азабицикло[3.2.1]октил, азабицикло[3.3.1]нонил, азабицикло[4.3.0]нонил, оксабицикло[2.2.1]гептил, 1,5,9-триазациклододецил и так далее. Дополнительные иллюстративные примеры (С 2-C10)гетероциклила получают из следующих: но не ограничиваются ими. Если не указано иначе, вышеупомянутый (С 2-C10)гетероциклил может быть присоединен по атому С или N, когда это возможно. Например, пиперидил может представлять собой пиперид-1-ил (присоединен по N) или пиперид-2-ил (присоединен по С). Если не указано иначе, термин "(С 6-C10)арил" относится к ароматическому моновалентному, моноциклическому или конденсированному или неконденсированному бициклическому или трициклическому радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, содержащим в общем от 6 до 10 кольцевых атомов углерода. Иллюстративные примеры (С 6-C10)арила получают из следующих: и но не ограничиваются ими. Если не указано иначе, термин "(C1-C10)гетероарил" относится к ароматическому, моновалентному,моноциклическому, конденсированному или неконденсированному бициклическому или трициклическому радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, содержащим в общем от 1 до 10 кольцевых атомов углерода и от 1 до 5 кольцевых гетероатомов, выбранных из азота, кислорода и серы. Иллюстративные примеры (С 1-C10)гетероарила включают в себя тиенил, пирролил, имидазолил, пиразолил, фурил, изотиазолил, фуразанил, изоксазолил, тиазолил, пиридил, пиразинил, пиримидинил, пиридазинил, триазинил, бензо[b]тиенил, нафто[2,3-b]тиантренил, изобензофуранил, хроменил, ксантенил, феноксантиенил, индолизинил, изоиндолил, индолил, индазолил, пуринил, изохинолинил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хинзолинил, бензотиазолил, бензимидазолил,тетрагидрохинолинил, циннолинил, птеридинил, карбазолил, бета-карболинил, фенантридинил, акридинил, перимидинил, фенантролинил, феназинил, изотиазолил, фенотиазинил и феноксазинил, но не ограничиваются ими. Дополнительные примеры (C1-C10)гетероарила получают из следующих: но не ограничиваются ими. Если не указано иначе, вышеупомянутый (C1-C10)гетероарил может быть присоединен по атому С или N, когда это возможно. Например, пиридил может представлять собой пирид-1-ил (присоединен поN) или пирид-3-ил (присоединен по С). Если не указано иначе, термин C3-C10)циклоалкил)C1-C8)алкил)N-" относится к радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, имеющей формулу: где термины "(C3-C10)циклоалкил" и "(C1-C8)алкил" являются такими, как определено выше. Если не указано иначе, термин "С 6-C10)арил)C1-C8)алкил)N-" относится к радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, имеющей формулу: где термины "(С 6-C10)арил" и "(C1-C8)алкил" являются такими, как определено выше. Если не указано иначе, термин "(C1-C10)гетероарил-NH-" относится к радикалу, заместителю, группировке или субгруппировке, упомянутой здесь, имеющей формулу: где термин "(C1-C10)гетероарил" является таким, как определено выше, и где указанный (C1-C10)гетероарил связан с -NH- через кольцевой атом углерода (C1-C10)гетероарила. Если не указано иначе, термин "(C2-C10)гетероциклил-NH-" относится к радикалу, заместителю,группировке или субгруппировке, упомянутой здесь, имеющей формулу: где термин "(С 2-C10)гетероциклил" является таким, как определено выше, и где указанный (С 2-C10) гетероциклил связан с -NH- через кольцевой атом углерода (C2-C10)гетероциклила. Термин "фармацевтически приемлемая соль" относится к соли, которая сохраняет биологическую эффективность свободных кислот и оснований конкретного соединения и не является нежелательной биологически или каким-либо иным образом. Соединение по данному изобретению может обладать достаточно кислыми или достаточно основными, или обеими функциональными группами, и, соответственно, вступать в реакцию с любым из ряда неорганических или органических оснований и неорганических и органических кислот с образованием фармацевтически приемлемой соли. Примеры фармацевтически приемлемых солей включают соли, которые получают путем реакции соединений по настоящему изобретению с неорганической или органической кислотой или неорганическим основанием, такие как соли,включающие сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, иодиды, ацетаты, пропионаты,- 15009337 деканоаты, каприлаты, акрилаты, формиаты, изобутираты, капроаты, гептаноаты, пропиолаты, оксалаты,малонаты, сукцинаты, субераты, себацаты, фумараты, малеаты, бутин-1,4-диоаты, гексин-1,6-диоаты,бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, сульфонаты, ксилолсульфонаты, фенилацетаты, фенилпропионаты, фенилбутираты, цитраты, лактаты, -гидроксибутираты, гликоляты, тартраты, метансульфонаты, пропанульфонаты, нафталин-1 сульфонаты, нафталин-2-сульфонаты и манделаты. Используемый здесь термин "пролекарство" относится к метаболическому предшественнику соединения формулы I (или его соли), который является фармацевтически приемлемым. Пролекарство может быть неактивным при его введении субъекту, но превращаться in vivo в активное соединение формулы I. Используемый здесь термин "активный метаболит" относится к продукту метаболизма соединения формулы I, который является фармацевтически приемлемым и эффективным. Пролекарства и активные метаболиты соединений формулы I могут быть определены с использованием способов, известных в данной области техники. Пролекарства и активные метаболиты соединения могут быть идентифицированы с использованием стандартных способов, известных в данной области техники. См., например, Bertolini et al., J. Med.Chem., 40, 2011-2016 (1997); Shan, et al., J. Pharm.Sci., 86 (7), 765-767; Bagshawe, Drug(Krogsgaard-Larsen et al., eds., Harwood Academic Publishers, 1991). Ингибитор CHK-1 по настоящему изобретению может быть введен в комбинации с другими способами противоопухолевой терапии, включающими противоопухолевые агенты и лучевую терапию. Термин "в комбинации с" означает, что соединение формулы I может быть введено непосредственно перед, непосредственно после, одновременно или в виде любой комбинации перед, после или одновременно с такими другими способами противоопухолевой терапии. Таким образом, соединение и противоопухолевый агент могут быть введены одновременно в виде одной композиции или двух отдельных композиций, или последовательно в виде двух отдельных композиций. Аналогично, соединение и лучевая терапия могут быть введены одновременно, раздельно или последовательно. Соединение может быть введено в комбинации с более чем одним способом противоопухолевой терапии. В предпочтительном воплощении соединение можно вводить в течение от 2 недель до 1 суток перед какой-либо химиотерапией, или от 2 недель до 1 суток перед какой-либо лучевой терапией. В еще одном предпочтительном воплощении ингибитор CHK-1 может быть введен в течение противоопухолевой химиотерапии и лучевой терапии. Если ингибитор CHK-1 вводят после такой химиотерапии или лучевой терапии, его можно вводить в течение от 1 до 14 суток после первичного лечения. Ингибитор CHK-1 также можно вводить постоянно или полупостоянно в течение промежутка времени от приблизительно 2 недель до приблизительно 5 лет. Специалисту в данной области техники будет понятно, что количество ингибитора CHK-1,которое вводят в соответствии с настоящим изобретением в комбинации с другими противоопухолевыми агентами или способами терапии, представляет собой такое количество, которое достаточно для усиления противоопухолевых действий противоопухолевых агентов или лучевой терапии, или такое количество, которое достаточно для индукции апоптоза, или клеточной смерти, вместе с противоопухолевой или лучевой терапии и/или для поддержания антиангиогенного действия. Такое количество может варьировать наряду с другими факторами в зависимости от размера и типа новообразования, концентрации соединения в терапевтическом препарате, конкретных используемых противоопухолевых агентов, времени введения ингибиторов CHK-1 относительно других способов терапии и возраста, размера и состояния пациента. Используемый здесь термин "протеинкиназы" относится к ферментам, которые катализируют фосфорилирование гидроксильных групп тирозиновых, сериновых и треониновых остатков белков. Следствия этого, по-видимому, простого действия представляют собой расположение; клеточный рост, дифференцировка и пролиферация, то есть, в сущности, все аспекты клеточной жизни тем: или иным образом зависят от протеинкиназной активности. Кроме того, аномальная протеинкиназная активность имеет отношение к расстройствам у хозяина, от сравнительно не опасных для жизни заболеваний, таких как псориаз, до весьма опасных заболеваний, таких как глиобластома (рак головного мозга). Протеинкиназы для удобства могут быть разделены на два основные класса, протеинтирозинкиназы (РТК) и серинтреонинкиназы (STK). Кроме того, известен третий класс киназ, обладающих двойной специфичностью,которые могут фосфорилировать как остатки тирозина, так и серина-треонина. Примеры протеинкиназ и их изоформ, рассматриваемых в данном изобретении, включают в себя чекпойнт киназу 1 (CHK-1), чекпойнт киназу 2 (CHK-2), циклинзависимую киназу 1 (CDK1), сывороточную и регулируемую глюкокортикоидами киназу (SGK), аденозин-5'-монофосфат (АМФ)-активируемую протеинкиназу (AMPK), тирозинкиназу лимфоидных Т-клеток (LCK), митогенактивируемую протеинкиназу 2 (MAPK-2), митоген- и стрессактивируемую протеинкиназу 1 (MSK1), протеинкиназу В (PKB), протеинкиназу В альфа (PKB),Rho-киназу (ROCK-II), P70 S6 киназу (p70S6K), цАМФ (циклический аденозин-3',5'-монофосфат)зависимую протеинкиназу (PKA), митогенактивируемую протеинкиназу (MAPK), митогенактивируемую протеинкиназу 1 (MAPK-1), киназу 2, родственную протеинкиназе-С (PRK2), 3'-фосфоинозити- 16009337 дзависимую киназу 1 (PDK1), Fyn-киназу (FYN), протеинкиназу-С (PKC), протеинкиназу-С бета 2(PKCII), протеинкиназу-С гамма (PKC), рецептор 2 фактора роста эндотелия сосудов (VEGFR-2), рецептор фактора роста фибробластов (FGFR), киназу фосфорилазы (PHK), Wee-1 киназу (Wee1) и протеинкиназу В (PKB). Чекпойнт киназа 2 (CHK-2) действует в качестве чекпойнт-контролера клеточного цикла в ответ на повреждение ДНК. CHK-2 представляет собой нисходящий эффектор ATM, который фосфорилирует белок р 53 и влияет на переход клеточного цикла из фазы G1 в фазу S. Активация CHK-2 также оказывает влияние на протекание фазы S. Кроме того, вместе с CHK-1, CHK-2 оказывает влияние на переход G2/M и играет роль в апоптозе, если повреждение не может быть восстановлено. CHK-2 может играть роль при сенсибилизации раковых клеток в отношении способов терапии, повреждающих ДНК. CHK-2 может также играть роль в качестве средства, подавляющего опухоль. Bartek, J. et. al. (2001) Nature Reviews,Molecular Cell biology 2: 877-886. Циклинзависимая киназа 1 (CDK1), также известная как Cdc2 в дрожжевых клетках. Клеточный цикл направляет специфические события, которые контролируют рост и пролиферацию клеток. Комплекс циклин B/Cdk1 способствует вхождению в митоз. Сверхэкспрессия циклина В 1 была обнаружена в 90% случаев рака толстой и прямой кишки. Поскольку регулировка клеточного цикла при раках у человека нарушается, модуляция активности CDK представляет собой возможный способ лечения. Было показано, что оломуцин, представляющий собой ингибитор CDK, ингибирует пролиферацию человеческих раковых клеток. В клетках лимфомы оломуцин останавливает клеточный цикл как в фазе G1, так и G2 путем ингибирования комплексов циклин E/CDK2 и циклин B/CDK1. Buolamwini, J.K. (2000) CurrentPharmaceutical Design 6: 379-392; Fan, S. et. al. (1999) Chemotherapy 45: 437-445. Сывороточная и регулируемая глюкокортикоидами киназа (SGK) быстро и сильно регулируется кортикостероидами в клетках А 6 на уровне мPHK и белком уровне. SGK также индуцируется альдостероном в почках крыс, перенесших адренэктомию. SGK активируется 3'-фосфоинозитидзависимой киназой 1 (PDK.1). SGK может играть важную роль в клетках, являющихся мишенью для альдостерона, и может быть физиологически важной при ранней реакции на альдостерон. Недавно было показано, что антагонисты рецептора альдостерона являются перспективными в клинических испытаниях на пациентах, страдающих от сердечной недостаточности. Способность опосредовать физиологические реакции на альдостерон может также оказаться полезной. См. Leslie, N. R. et. al. (2001) Chemical Reviews 101 (8): 2365-2380; Funder, J. W. (1999) Molecular and Cellular Endocrinology 151 (1-2): 1-3; Verrey, F. et al. (2000)Kidney International 57 (4): 1277-1282. Аденозин-5'-монофосфат (АМФ)-активируемая протеинкиназа (AMPK) изоформа 2 (AMPK 2) представлена в высоких концентрациях в скелетных мышцах, сердце и печени, тогда как изоформа 1 распространена широко. AMPK, возможно изоформа 2, фосфорилирует изоформуацетилкоэнзим А(КоА)-карбоксилазы (АСС) и инактивирует ее в условиях электрической стимуляции или физической нагрузки. В скелетных мышцах крыс малонил-КоА регулируется АСС и вовлечен в регуляторный механизм переноса длинноцепочечных жирных кислот в митохондрии, где они окисляются. Таким образом,AMPK связана с ожирением и/или резистентностью к инсулину, и модуляция AMPK может быть потенциально полезна при лечении этих заболеваний. AMPK ингибирует ферменты, вовлеченные в синтез гликогена и холестерина. Именно она представляет собой возможный регулирующий фермент, который в ответ на уменьшение концентрации аденозин-5'-трифосфата (АТФ) уменьшает дальнейшее потребление АТФ путем инициирования клеточных механизмов, направленных на поддержание уровней АТФ. Кроме того, AMPK связана с транскрипцией, регулированием креатининкиназы, апоптозом и транспортом глюкозы. См. Kemp, В. Е. et al. (1999) Trends in Biochemical Sciences 24(1): 22-25; Friedman, J. (2002)Nature 415 (6869): 268-269; Ruderman, N. B. et al. (1999) American Journal of Physiology 276 (1, Pt. 1): E1E18. Тирозинкиназа лимфоидных Т-клеток (LCK) представляет собой цитозольную тирозинкиназу, не являющуюся рецептором, и Т-лимфоцитарный член семейства Src. LCK вовлечена в раннюю фазу активации Т-клеточного рецептора антигенами и играет важную роль в опосредованных Т-клетками иммунных ответах. После активации путем аутофосфорилирования LCK фосфорилирует -цепи Т-клеточного рецептора, которые могут затем вовлекать вторую цитоплазматическую протеинтирозинкиназу ZAP-70,способствующую активации Т-клеток. Ингибиторы могут быть использованы для лечения ревматоидного артрита, заболеваний, связанных с иммунным ответом и лейкемий и лимфом, связанных с Т-клетками. См. Garcia-Echeverria, С. (2001) Current Medicinal Chemistry 8 (13): 1589-1604; Majolini, M. В. et al. (1999)LeukemiaLymphoma 35(3/4): 245-254. Митоген- и стрессактивируемая протеининаза 1 (MSK1) активируется при стимуляции пути Rasмитогенактивируемой протеинкиназы (MAPK) и также пути р 38 стресскиназы. Оба пути вовлечены в онкогенез. Стимуляция пути передачи сигнала Ras-MAPK факторами роста или форболовыми эфирами приводит в результате к фосфорилированию гистона H3. Было показано, что MSK1 опосредует вызванное эпидермальным фактором роста (EGF) или ТРА (12-О-тетрадеканоилфорбол-13-ацетат, форболовый эфир) фосфорилирование H3. Существует доказательство того, что постоянная активация пути Ras- 17009337MAPK и MSK1, приводящая в результате к увеличению уровней фофорилированного H3, может вносить вклад в отклонения генной экспрессии, наблюдаемые в клетках, трансформированных онкогенами. Ингибирование MSK1 подавляло индукцию генов c-fos (протоонкоген) и uPА в парентеральных клетках и клетках, трансформированных онкогенами. Как c-fos, так и uPA вовлечены в начало развития опухоли и метастаз. Смотри Strelkov, I. et. al. (2002) Cancer Research 62(1): 75-78; Zhong, S. et al. (2001) Journal ofRho-киназа (ROCK-II) также известная как ROK. Путем ингибирования ROCK-II, потенциально можно влиять на Rho гуанозинтрифосфатазы ГТФазы, которые действуют в качестве молекулярных контролей, которые регулируют многие важные клеточные процессы, включающие динамику актина, протекание клеточного цикла и клеточную адгезию. Биологические эффекты in vitro и in vivo Y-27632, представляющей собой специфический ингибитор ROCK, были описаны в литературе и включают уменьшение кровяного давления у крыс, страдающих от гипертензии, ингибирование образования стрессорных волокон, индуцированного Rho, и очаговые адгезии, и ингибирование роста опухоли. См. Narumiya, S. etP70S6 киназа (Р 70S6K) обнаружена в виде двух изоформ, одна из которых цитоплазматическая, а другая находится в ядре. Они похожи, за исключением N-конца, и обе называются р 70S6K или S6K1. Также был идентифицирован второй функциональный гомолог S6K2. Р 70S6K представляет собой нисходящую мишень липидной киназы фосфоинозитид 3-ОН киназы (PI(3)K). P70S6K вовлечена в контроль клеточного цикла и дифференциации нейронов. p70S6K может также действовать при регулировании клеточной подвижности, которая может влиять на опухолевые метастазы, иммунный ответ и восстановлении ткани. Вместе с PKB/Akt p70S6K представляет собой важный эффектор сигнального пути онкогенной протеин-тирозинкиназы (PTK). p70S6K может представлять собой более сильную киназу в отношении BAD,нежели чем PKB/Akt (см. выше) в ответ на стимуляцию инсулиноподобным фактором роста 1 (IGF-1). Таким образом, p70S6K может играть важную антиапоптозную роль. Смотри See Blume-Jensen, P. et al.Hidalgo, M. et al. (2000) Oncogene 19 (56): 6680-6686; Berven, L. et al. (2000) Immunology and Cell Biology 78 (4): 447-451. цАМФ (циклический аденозин-3',5'-монофосфат)зависимая протеинкиназа (PKA) вовлечена в широкий диапазон физиологических реакций после взаимодействия с цАМФ. цАМФ представляет собой вторичный мессенджер, который регулирует множество различных клеточных активностей, таких как транскрипцию генов, клеточный рост и дифференциация, проводимость ионных каналов и высвобождение нейромедиаторов. Взаимодействие цАМФ/PKA действует в качестве основного регуляторного механизма у млекопитающих, и было показано, что PKA фосфорилирует огромное количество физиологических субстратов. PKA имеет две основные изоформы PKAI и PKAII. Показано, что ингибиторы PKAI усиливают эффекты, когда их применяют в комбинации с некоторыми цитотоксическими способами лечения рака. Антисмысловые олигонуклеотиды, нацеленные на субъединицу RI PKAI, проявляли усиленные противоопухолевые действия в комбинации с таксолом. Глюкагон активирует PKA, и PKA может влиять на инсулиновый ответ вместе с кальмодулинзависимой протеинкиназой С. PKA вовлечена в регулирование сердечных кальциевых каналов L-типа, и модуляция вовлеченных регуляторных путей может оказаться полезной при лечении болезней сердца. Кроме того, дисфункциональные Т-клетки, выделенные у пациентов, страдающих от вируса иммунодефицита человека (ВИЧ), восстанавливались при добавлении антагонистов PKAI. Смотри Skalhegg, В. S. et al. (2000) Frontiers in Bioscience [электронная публикация]5: D678-D693; Brandon, E. P. et. al. (1997) Current Opinion in Neurobiology 7 (3): 397-403; Nesher, R. et al. (2002) Diabetes 51 (Suppl. 1): S68-S73; Shabb, J. B. (2001) Chemical Reviews 101 (8): 23812411; Kamp, T. J. et al. (2000) Circulation Research 87 (12); 1095-1102; Tortora, G. et al. (2002) Clinical Cancer Research 8: 303-304; Tortora, G. et al. (2000) Clinical Cancer Research 6: 2506-2512. Митогенактивируемая протеинкиназа (MAPK) также известная как ERK. При онкогенезе ras онкогены передают внеклеточные сигналы роста. MAPK путь представляет собой важный сигнальный путь между связанным с мембраной ras и ядром. Вовлечен каскад фосфорилирования, охватывающий три ключевые киназы. Они представляют собой Raf, MEK (киназа киназы MAP) и MAPK/ERK. ИзоформыRaf фосфорилируют и активируют изоформы MEK1 и MEK2. MEK1 и 2 представляют собой киназы двойной специфичности, которые, в свою очередь, фосфорилируют и активируют изоформы MAPKMAPK1/ERK1 и MAPK2/ERK2. В фибробластах обе MAPK1/ERK1 и MAPK2/ERK2 значительно активируются факторами роста и канцерогенными форболовыми эфирами. MAPK1/ERK1 и MAPK2/ERK2 также вовлечены в регулирование глюкозы, регулирование нейромедиаторов и регулирование веществ, усиливающих секрецию (в эндокринных тканях). MAPK путь также связан с индукцией мPHK циклина D1 и, таким образом, связан с фазой G1 клеточного цикла. См. Webb, С. P. et al. (2000) Cancer Research 60 (2),342-349; Roovers, K. et al. (2000) BioEssays 22 (9): 818-826; Chen, Z. et al. (2001) Chemical Reviews 101 (8): 2449-2476; Lee, J. C. et al. (2000) Immunopharmacology 47 (2-3): 185-201, Sebolt-Leopold J. S. (2000) Onco- 18009337cSrc (также известная как p60 c-src) представляет собой цитозольную тирозинкиназу, не являющуюся рецептором. c-Src вовлечена в передачу митогенных сигналов от ряда полипептидных факторов роста, таких как эпидермальный фактор роста (EGF) и тромбоцитарный фактор роста (PDGF). c-Src сверхэкспрессируется при раках молочной железы, раках поджелудочной железы, нейробластомах и так далее. Мутантная c-Src была идентифицирована при раке толстой кишки у людей. c-Src фосфорилирует ряд белков, которые вовлечены в регулирование поперечных связей между внеклеточным матриксом и цитоплазматическим актиновым цитоскелетом. Модуляция активности cSrc может иметь применение при заболеваниях, связанных с клеточной пролиферацией, дифференциацией и гибелью. Смотри Bjorge,J. D. et al. (2000) Oncogene 19 (49): 5620-5635; Halpern, M. S. et al. (1996) Proc. Natl. Acad. Sci. U.S.A. 93(2), 824-7; Belches, A. P. et al. (1997) Frontiers in Bioscience [электронная публикация] 2: D501-D518; Zhan,X. et al (2001) Chemical Reviews 101: 2477-2496; Haskell, M. D. et al. (2001) Chemical Reviews 101: 24252440. Киназа 2, родственная протеинкиназе-С (PRK2), регулируется G-белком Rho. PRK2 найдена в областях с высоким оборотом актина. Эндогенная активность киназы PRK2 увеличивается при дифференциации кератиноцитов и ассоциируется с межклеточной адгезией кератиноцитов и активацией Fynкиназы. См. Gross, С, et al. (2001) FEBS Letters 496 (2,3): 101-104; Calautti, E. et al. (2002) Journal of CellBiology 156(1): 137-148. 3'-Фосфоинозитидзависимая киназа 1 (PDK1) фосфорилирует и активирует члены семейства киназAGC (цАМФ-зависимые, цГМФ-зависимые и протеинкиназа С), которые претерпевают нисходящую активацию фосфоинозитид-3-киназой (PI3K). PI3K становится активной посредством стимуляции инсулином. PDK1 активирует ряд протеинкиназ и, таким образом, может быть связана с регулированием ряда инсулиноспецифических процессов. Фосфорилирование PDK1 и активация PKC необходима для инсулинозависимого переноса GLUT4. Индуцируемый инсулином перенос GLUT4 физиологически связан с актиновым цитоскелетом. Нарушения актиновых филаментов связаны с утратой влияния инсулина на транспорт глюкозы и уменьшением переноса GLUT4. См. Wick, K.L. et al. (2001) Current Drug Targets:Fyn-киназа (FYN) представляет собой член семейства Src тирозинкиназ. Fyn вовлечена в положительный контроль межклеточной адгезии кератиноцитов. Адгезия играет важную роль при образовании и поддержании организованных тканей. Нокаут Fyn у трансгенных мышей доказал, что Fyn участвует в передаче сигнала с Т-клеточного рецептора (TCR). Сверхэкспрессия трансгена fyn (T) приводит к образованию Т-клеток с увеличенной чувствительностью к сигналам TCR. В противоположность, экспрессия неактивной формы киназы приводит к ингибированию. Fyn может представлять собой подходящую мишень при лечении аутоиммунных заболеваний. Мыши Fyn-/- гиперчувствительны к спирту, что свидетельствует о том, что Fyn может представлять собой мишень для лечения алкоголизма. Изменение уровней Fyn может также способствовать лечению кожных расстройств. Fyn вовлечена в регулирование запрограммированной клеточной гибели, и мыши Fyn-/-демонстрируют уменьшенный апоптоз. См. такжеBiochemistryCell Biology 30 (11): 1159-1162. Рецептор 2 фактора роста эндотелия сосудов (VEGFR-2) также известен как FLK-1 и KDR (рецептор домена встраивания киназы). Другие тирозинкиназы, представляющие собой рецептор VEGF, включают VEGFR-1 (Fit-1) и VEGFR-3 (Fit-4). Ангиогенез или развитие новой сосудистой сети является центральным моментом для процессов, при помощи которых растут солидные опухоли. Степень васкуляризации связана с увеличением возможности метастаза. VEGFR-2, экспрессируемый только на эндотелиальных клетках, связывается с сильным ангиогенным фактором роста VEGF и опосредует последующую передачу сиигнала. Ингибирование активности VEGF-R2 приводит в результате к уменьшению ангиогенеза и роста опухоли в моделях in vivo, и ингибиторы VEGFR-1 в настоящее время проходят клинические испытания для лечения рака. См. Strawn et al., (1996) Cancer Research 56: 3540-3545; Millauer etal.,(1996) Cancer Research 56: 1615-1620; Sakamoto, K. M.(2001) IDrugs 4 (9): 1061-1067; Ellis, L. M. et al.(2000) Oncologist 5 (Suppl. 1): 11-15; Mendel, D. B. et. al (2000) Anti-Cancer Drug Design 15:29-41; Kumar,С.С. et al. (2001) Expert Opin. Emerging Drugs 6 (2): 303-315; Vajkoczy, P. et al (1999) Neoplasia 1(1): 31-41. Рецептор фактора роста фибробластов (FGFR) связывается с ангиогенными факторами роста aFGF и bFGF и опосредует последующую передачу сигнала. Факторы роста, такие как bFGF, могут играть важную роль при индукции ангиогенеза в солидных опухолях, которые достигли определенного размера.FGFR экспрессируется в ряде различных типов клеток в организме и может играть важную роль при нормальных физиологических процессах у взрослых людей. Сообщалось, что системное введение небольшого молекулярного ингибитора FGFR блокирует индуцированный bFGF ангиогенез у мышей. См.- 19009337 Киназа фосфорилазы (PHK) активирует гликогенфосфорилазу. Первичное следствие этой активации заключается в высвобождении глюкозо-1-фосфата из гликогена. Превращение в гликоген представляет собой основное средство, при помощи которого глюкоза сохраняется у млекопитающих. Внутриклеточные запасы гликогена используются для поддержания гомеостаза глюкозы в крови во время голодания и представляют собой источник энергии для мышечного сокращения. In vivo PHK фосфорилируется цАМФ-зависимой протеинкиназой (PKA), которая увеличивает специфическую активность PHK. У диабетиков 1 и 2 типа показано уменьшение уровней гликогена в печени и мышечных клетках. Уровни гликогена жестко регулируются гормонами и метаболическими сигнальными путями. Ингибиторы киназы, которые могут увеличивать внутриклеточные уровни гликогена, могут оказаться полезными при лечении диабета. См. Brushia, R. J. et al. (1999) Frontiers in Bioscience [электронная публикация]4: D618D641; Newgard, С. В. et al. (2000) Diabetes 49: 1967-1977; Venien-Bryan, С et al. (2002) Structure 10: 33-41;Wee1-киназа (Wee1) вместе с Mikl-киназой, как было показано, фосфорилирует Cdc2. Было показано, что фосфорилирование Cdc2 предотвращает вход в митоз. Wee1 может играть важную роль в нормальном цикле роста клеток и может быть вовлечена в чекпойнт-контроль клеточного цикла. Rhind, N.et. al. (2001) Molecular and Cellular Biology 21 (5): 1499-1508. Протеинкиназа В (PKB) также известная как Akt. Существуют три очень похожие изоформы, известные как PKB ,и(или Akt 1,2, и 3). Ультрафиолетовое излучение в диапазоне 290-320 нм ассоциируется с вредными эффектами солнечного света. Это излучение вызывает активацию PKB/Akt и может быть вовлечено в онкогенез. Сверхэкспрессия PKB/Akt была продемонстрирована при раке яичников, предстательной железы, молочной железы и поджелудочной железы. PKB/Akt также вовлечена в протекание клеточного цикла. PKB/Akt способствует выживанию клеток множеством путей. Она фосфорилирует проапоптотический белок BAD, таким образом, что он не способен связываться и инактивировать антиапоптотический белок Bcl-xI. PKB/Akt также служит для ингибирования апоптоза путем ингибирования каспазы 9 и разветвленного транскрипционного фактора и путем активации киназы IkB. См.Leslie, N. R. (2001) Chem Rev 101: 2365-2380. Классические изоформы протеинкиназы С (PKC) обозначаются , 1, 2 ии все являются Са 2+ зависимыми. Изоформы PKC вовлечены в пути передачи сигнала, связанные с рядом физиологических реакций, включающих мембранный транспорт, клеточную дифференциацию и пролиферацию, организацию белков цитоскелета и генную экспрессию. Канцерогенные форболовые эфиры активируют классические изоформы PKC, и антисмысловые нуклеотиды могут блокировать эту активацию. Изоформы PKC часто сверхэкспрессируются при различных раках. Было показано, что ингибиторы PKC обращают опосредованную р-гликопротеином устойчивость к лекарственным средствам и могут увеличивать внутриклеточные концентрации других противоопухолевых агентов. В миоцитах изоформы PKC вовлечены в некоторые сердечные патологии. PKC- имеет высокую степень экспрессии в головном мозге и спинном мозге и преимущественно локализован в дендритах и телах нейронов. PKC-2 вовлечен в клеточную пролиферацию и сверхэкспрессия увеличивает чувствительность к раку. Ингибиторы PKC представляют собой потенциально новый способ лечения диабетической ретинопатии в проводимых в настоящее время клинических испытаниях. См. Magnelli, L. et al. (1997) Journal of Cancer Research and Clinical Oncology 123 (7): 365-369; Clerk, A. et al (2001) Circulation Research 89 (10): 847-849; Carter, С. (2000) CurrentJournal 19 (4): 496-503; Newton, A. C. (2001) Chem. Rev. 101: 2353-2364. Используемый здесь термин "лечение" или "который лечат" относится к обращению, ослаблению,подавлению развития или предотвращению расстройства или состояния, в отношении которых применяется такой термин, или одного или более чем одного симптома такого расстройства или состояния. Используемый здесь термин "лечение" относится к процессу лечения в соответствии с тем, как "лечение" определено непосредственно выше. Используемый здесь термин "расстройства соединительной ткани" относится к расстройствам, таким как утрата хряща после травматического повреждения сустава, остеоартрит, остеопороз, болезнь Педжета, ослабление искусственных суставных имплантатов, периодонтальное заболевание и воспаление десен. Используемый здесь термин "разрушение суставного хряща" относится к расстройствам соединительной ткани, приводящим в результате к разрушению суставного хряща, преимущественно повреждению сустава, реактивному артриту, острому пирофосфатному артриту (псевдоподагра), псориатическому- 20009337 артриту или болезни Стилла, преимущественно остеоартриту. Используемый здесь термин "воспалительные расстройства" относится к расстройствам, таким как ревматоидный артрит, анкилозирующий спондилоартрит, псориатический артрит, псориаз, отложение солей кальция в хрящевых и синовиальных тканях, подагра, воспалительное заболевание кишечника,неспецифический язвенный колит, болезнь Крона, фибромиалгия и кахексия. Используемый здесь термин "иммунологические/аллергические расстройства" относится к расстройствам, таким как токсичность при трансплантации органов, аллергические реакции, аллергическая контактная гиперчувствительность, аутоиммунные расстройства, такие как расстройства, ассоциированные с продуктивным воспалением/реконструкцией ткани (таким как астма), иммуносупрессия и саркоид. Используемый здесь термин "инфекционные заболевания", включающий заболевания, опосредованные вирусами, бактериями, грибками или микобактериальную инфекцию, относится к расстройствам,таким как септический артрит, СПИД, лихорадка; прионовые инфекции, астенический бульбарный паралич, малярия, сепсис, гемодинамический шок и септический шок. Используемый здесь термин "респираторные заболевания" относится к расстройствам, таким как хроническое обструктивное заболевание легких (включающее эмфизему), острый респираторный дистресс-синдром, астма, гипероксическое повреждение альвеол и идиопатический легочный фиброз и другие легочные фиброзы. Используемый здесь термин "сердечно-сосудистые заболевания" относится к расстройствам, таким как атеросклероз, включающий прорыв атеросклеротических бляшек; аневризма аорты, включающая аневризму брюшной аорты и аневризму мозговой аорты; застойная сердечная недостаточность; инфаркт миокарда и головного мозга; удар; ишемия головного мозга; коагуляция и ответ острой фазы; дилатация левого желудочка; повреждение при постишемической реперфузии; ангиофибромы; гемангиомы и рестеноз. Используемый здесь термин "заболевания глаз" относится к расстройствам, таким как аберрантный ангиогенез, глазной ангиогенез, глазное воспаление, кератоконус, ксеродерматоз, миопия, глазные опухоли, отторжение трансплантата роговицы, повреждение роговицы, реваскулярная глаукома, изъязвление роговицы, рубцевание роговицы, дегенерация желтого пятна (включающая в себя "возрастную дегенерацию желтого пятна" (ВДЖП), включающую в себя влажную и сухую формы), пролиферативная витреоретинопатия и ретинопатия при недоношенности. Используемый здесь термин "метаболические заболевания" относится к расстройствам, таким как диабет (включающий в себя инсулиннезависимый сахарный диабет, диабетическую ретинопатию, резистентность к инсулину, диабетическую язву). Используемый здесь термин "расстройства центральной нервной системы (ЦНС)" относится к расстройствам, таким как травма головы, повреждение спинного мозга, воспалительные заболевания центральной нервной системы, нейродегенеративные расстройства (острые и хронические), болезнь Альцгеймера, демиелинизирующие заболевания нервной системы, болезнь Гентингтона, болезнь Паркинсона,периферическая невропатия, боль, церебральная амилоидная ангиопатия, ноотропное усиление познавательной способности, боковой амиотрофический склероз, рассеянный склероз, мигрень, депрессия и анорексия. Используемый здесь термин "заболевания печени/почек" относится к расстройствам, таким как нефротические синдромы, такие как гломерулонефрит и клубочковое заболевание почек, протеинурия,цирроз печени и интерстициальный нефрит. Используемый здесь термин "расстройства репродуктивного здоровья" относится к расстройствам,таким как эндометриоз, контрацепция (мужская/женская), дисменорея, дисфункциональное маточное кровотечение, преждевременный разрыв плодных оболочек и аборт. Используемый здесь термин "желудочные расстройства" относится к расстройствам, таким как анастомоз толстой кишки и язвы желудка. Используемый здесь термин "кожные расстройства" относится к расстройствам, таким как старение кожи, пролежни, псориаз, экзема, дерматит, радиационное поражение, изъязвление ткани, пролежни,врожденный буллезный эпидермолиз, аномальное заживление раны (препараты для местного и перорального введения), ожоги и склерит. Используемый здесь термин "рак" относится к расстройствам, таким как солидная опухоль, рак,включающий в себя рак толстой кишки, рак молочной железы, рак легкого и рак предстательной железы,прорастание опухолью, злокачественный рост, опухолевый метастаз, рак ротовой полости и глотки (губ,языка, ротового отверстия, глотки), пищевода, желудка, тонкой кишки, толстой кишки, прямой кишки,печени и желчных протоков, поджелудочной железы, гортани, легкого, кости, соединительной ткани,кожи, шейки матки, тела матки, яичников, яичка, мочевого пузыря, почки и других тканей мочеполовой системы, глаза, головного мозга и центральной нервной системы, щитовидной железы и других эндокринных желез, болезнь Ходжкина, неходжкинские лимфомы, множественная миелома и злокачественные болезни кроветворной ткани, включающие в себя лейкозы и лимфомы, включающие в себя лимфоцитарный, гранулоцитарный и моноцитарный лейкоз. На следующих схемах реакций иллюстрируется получение соединений по настоящему изобрете- 21009337 нию. Если не указано иначе, каждый из А, группы -Y-Z-, X, R1, R2, R3 И R4 на схемах реакций и в следующем обсуждении является таким, как определено выше. Схема 1- 24009337 Схема 1 относится к получению соединений формулы I. В соответствии со схемой 1 путем реакции соединения формулы II, где R2 отличается от водорода и где Lv представляет собой уходящую группу, с гидразином в растворителе может быть получено соединение формулы I, где группа -Y-Z- имеет формулу -N=CH- и R2 отличается от водорода. Подходящие уходящие группы Lv включают в себя метокси,этокси или бензилокси, предпочтительно, метокси. Подходящие растворители включают в себя спирты(такие как этанол), предпочтительно метанол. Вышеупомянутую реакцию можно проводить при температуре от приблизительно 25 С до приблизительно 90 С, предпочтительно приблизительно 65 С. Вышеупомянутая реакция может быть осуществлена в течение времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 0,5 ч. Соединения формулы II, где R2 отличается от водорода и где Lv является такой, как описано выше,может быть получено путем реакции соединения формулы III, где R2 отличается от водорода и где Lv является такой, как описано выше, с формилирующим реагентом Вилсмайера в растворителе. Подходящие формилирующие реагенты Вилсмайера включают в себя POCl3 и диметилформамид (ДМФ) или(CF3SO2)2O и ДМФ; предпочтительно POCl3 и ДМФ. Подходящие растворители включают в себя хлороформ, диоксан, тетрагидрофуран, диметилформамид или метиленхлорид; предпочтительно метиленхлорид. Вышеупомянутую реакцию можно проводить при температуре от приблизительно 0 С до приблизительно 25 С, предпочтительно приблизительно 0 С, во время добавления реагента, затем давая возможность реакционной смеси нагреваться до 23 С в течение приблизительно 0,5 ч. Вышеупомянутая реакция может быть осуществлена в течение периода времени от приблизительно 5 мин до приблизительно 24 ч,предпочтительно приблизительно 0,5 ч. Соединения формулы III, где R2 отличается от водорода и где Lv является такой, как описано выше,может быть получено путем реакции соединения формулы IV, где Lv является такой, как описано выше,с соединением формулыR2-Lv1,1 где Lv представляет собой уходящую группу, такую как галогено, предпочтительно бромо или хлоро, в присутствии подходящего основания в полярном растворителе. Подходящие основания включают в себя алкоксидные основания (такие как метоксид натрия, этоксид натрия или трет-бутоксид калия); гидридные основания (такие как гидрид натрия) или карбонатные основания (такие как карбонат калия или карбонат цезия); предпочтительно карбонат калия. Подходящие полярные растворители включают в себя тетрагидрофуран, диметилформамид, диметилсульфоксид или спирты (такие как этанол),предпочтительно диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 100 С, предпочтительно приблизительно 80 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 0,5 часа до приблизительно 72 ч, предпочтительно приблизительно 24 ч. Соединение формулы I, где группа -Y-Z- представляет собой -О-CH2- и где R2 отличается от водорода, может быть получено путем реакции соединения формулы V, где R2 отличается от водорода, где Pg представляет собой защитную группу и Lv является такой, как описано выше, с агентом, удаляющим защиту Pg. Подходящий Pg включает в себя фталоил, трет-бутоксикарбонил, бензилоксикарбонил или этоксикарбонил; предпочтительно фталоил. Подходящие агенты, удаляющие защиту Pg, включают в себя гидразин, трифторуксусную кислоту, соляную кислоту, гидрохлорид, гидробромид в уксусной кислоте или газообразный водород и Pd катализатор; предпочтительно гидразин. Кислые реакционные смеси могут быть нейтрализованы после удаления защиты подходящим основанием, включающим в себя третичные амины (такие как триэтиламин или диизопропилэтиламин) или карбонатные основания (такие как карбонат калия); предочтительно триэтиламин. Подходящие растворители включают в себя диметилформамид, метиленхлорид, хлороформ или спирт (такой как метанол); предпочтительно метанол. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 20 С до приблизительно 130 С, предпочтительно приблизительно 65 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 0,5 ч до приблизительно 48 ч, предпочтительно приблизительно 2 ч. Соединение формулы V, где R2 отличается от водорода, где Pg представляет собой защитную группу и Lv является такой, как описано выше, может быть получено путем реакции соединения формулы VI,где R2 отличается от водорода, Lv2 представляет собой уходящую группу и Lv является такой, как описано выше, с соединением формулыPg-N-OH в присутствии основания в растворителе. Подходящие уходящие группы Lv2 включают в себя галогено, толуолсульфонил, метансульфонил, трифторметансульфонил или реакционные аддукты типа Мицунобу. Подходящие соединения формулы Pg-N-OH включают в себя N-гидроксифталимид, трет-бутилN-гидроксикарбамат, N-гидроксиуретан или бензил-N-гидроксикарбамат. Подходящие основания включают в себя гидрид натрия, 1,8-диазабицикло[5.4.0]ундец-7-ен, пиридин, третичные амины (такие как диизопропилэтиламин или триэтиламин) или карбонатные основания (такие как карбонат натрия); предпочтительно карбонат натрия. Подходящие растворители включают в себя диметилформамид, диметил- 25009337 сульфоксид, тетрагидрофуран, метиленхлорид, хлороформ или спирт (такой как метанол); предпочтительно диметилсульфоксид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно -25 С до приблизительно 80 С, предпочтительно приблизительно 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 ч до приблизительно 48 ч, предпочтительно приблизительно 20 ч. Соединение формулы VI, где R2 отличается от водорода и Lv2 и Lv являются такими, как описано выше, может быть получено путем реакции соединения формулы VII, где R2 отличается от водорода и Lv является такой, как описано выше, с агентом, продуцирующим Lv2, в растворителе. Подходящие агенты,продуцирующие Lv2, включают в себя (С 6 Н 5)3 Р и CCl4; (С 6 Н 5)3 Р и PBr3; пара-CH3C6H4SO2Cl; CH3SO2Cl;(CF3SO2)2O; или реагенты типа Мицунобу (такие как диэтилазодикарбоксилат и (С 6 Н 5)3 Р); предпочтительно (С 6 Н 5)3 Р и CCl4. Подходящие растворители включают в себя метиленхлорид, хлороформ, тетрагидрофуран, тетрахлорид углерода, бензол или толуол; предпочтительно метиленхлорид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно -25 С до приблизительно 80 С, предпочтительно приблизительно 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 20 ч. Соединение формулы VII, где R2 отличается от водорода и Lv является такой, как описано выше,может быть получено путем реакции соединения формулы II, где R2 отличается от водорода и Lv является такой, как описано выше, с восстановителем в растворителе. Подходящие восстановители включают в себя борогидрид натрия, борогидрид лития, борогидрид цинка, диборан, борановые комплексы, триацетоксиборогидрид, цианоборогидрид натрия или цианоборогидрид лития; предпочтительно борогидрид натрия. Подходящие растворители включают в себя спирт (такой как метанол), тетрагидрофуран, смесь метанола и безводного HCl, или смесь метанола и уксусной кислоты; предпочтительно метанол. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 50 С, предпочтительно приблизительно 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 15 мин. Схема 2 относится к получению соединений формулы Ia, которые представляют собой соединение формулы I где R2 представляет собой водород. В соответствии со схемой 2, соединение формулы Ia, где группа -Y-Z- имеет формулу -N=CH-, может быть получено путем реакции соединения формулы VIII,где Lv представляет собой уходящую группу, как описано выше, с гидразином в растворителе. Условия реакции являются такими, как определено выше в описании к схеме 1 для получения соединения формулы I из соединения формулы II. Соединения формулы VIII, где Lv является такой, как опиано выше, может быть получено путем реакции соединения формулы IV, где Lv является такой, как описано выше, с реагентом Вилсмайера в растворителе. Условия реакции являются такими, как определено выше в описании к схеме 1 для получения соединения формулы II из соединения формулы III. Соединение формулы Ia, где группа -Y-Z- представляет собой -О-CH2-, может быть получено путем реакции соединения формулы XIV, где Pg2 представляет собой защитную группу, с агентом, удаляющим защиту Pg2, в растворителе. Подходящие защитные группы Pg2 включают в себя трет-бутоксикарбонил,бензилоксикарбонил, или 2-(триметилсилил)этоксиметил; предпочтительно трет-бутоксикарбонил. Подходящие агенты, удаляющие защиту Pg2, включают в себя трифторуксусную кислоту, соляную кислоту,гидрохлорид, гидробромид в уксусной кислоте, газообразный водород и Pd катализатор, или фторид тетрабутиламмония; предпочтительно трифторуксусную кислоту. Подходящие растворители включают в себя метиленхлорид, хлороформ, диоксан, диметилформамид или спирт (такой как метанол); предпочтительно метиленхлорид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 20 С до приблизительно 80 С, предпочтительно приблизительно 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 15 мин до приблизительно 48 ч, предпочтительно приблизительно 2 ч. Соединение формулы XIV, где Pg2 является таким, как описано выше, может быть получено путем реакции соединения формулы XIII, где Pg представляет собой защитную группу, как описано для соединения формулы V схемы 1, и Pg2 и Lv являются такими, как описано выше, с агентом, удаляющим защиту Pg. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединения формулы I из соединения формулы V. Соединение формулы XIII, где Pg2, Lv и Lv2 являются такими, как описано выше, может быть получено путем реакции соединения формулы XII, где Pg, Lv и Lv2 являются такими, как опиано выше, с соединением формулыPg-N-OH,где Pg является таким, как описано выше, в присутствии основания в растворителе. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединения формулыV из соединения формулы VI.- 26009337 Соединение формулы XII, где Pg, Lv2 и Lv являются такими, как описано выше, может быть получено путем реакции соединения формулы XI, где Pg2 и Lv являются такими, как описано выше, с агентом, продуцирующим Lv2, в растворителе. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединения формулы VI из соединения формулы VII. Соединение формулы XI, где Pg2 и Lv являются такими, как описано выше, может быть получено путем реакции соединения формулы IX, где Pg2 и Lv являются такими, как опсано выше, с восстановителем в растворителе. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединения формулы VII из соединения формулы II. Соединение формулы IX, где Pg2 и Lv являются такими, как описано выше, может быть получено путем реакции соединения формулы VIII, где Lv является такой, как описано выше, с агентом, защищающим Pg2, в присутствии подходящего основания в растворителе. Подходящие агенты, защищающиеPg2, включают в себя ди-трет-бутилдикарбонат, бензилхлорформиат или 2-(триметилсилил)этоксиметилхлорид; предпочтительно ди-трет-бутилдикарбонат. Подходящие основания включают в себя гидридные основания (такие как гидрид натрия, гидрид лития или гидрид калия); предпочтительно гидрид натрия. Подходящие растворители включают в себя тетрагидрофуран или диметилформамид; предпочтительно тетрагидрофуран. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 60 С, предпочтительно приблизительно 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 15 мин до приблизительно 24 ч, предпочтительно приблизительно 1 ч. Схема 3 относится к получению соединения формулы 1 б, которое представляет собой соединение формулы I, где А представляет собой =CR1-. В соответствии со схемой 3, соединение формулы Iб может быть получено путем реакции соединения формулы Iв, где галоген выбран из бромо или иодо, с реагентом сочетания формулыR1-M,где М представляет собой Н или металл, в присутствии палладиевого и медного катализаторов в растворителе. Подходящие металлы включают в себя бор и олово, предпочтительно бор. Подходящие реагенты сочетания включают в себя реагент сочетания Стилла (см. Chamoin, S., Houldsworth, S.,Snieckus, V. Tetrahedron Lett. 1998, 39, 4175-4178, включенную здесь путем ссылки), реагент сочетания Сузуки (смотри Littke, A. F., Chaoyang, D., Fu, G. С. J. Am. Chem. Soc. 2000, 122, 4020-4028, включенную здесь путем ссылки) или реагент сочетания Соногашира (см. Sonogashira, K., Tohda, Y., Hagihara, N. Tetrahedron Lett. 1975, 16, 44467-4470, включенную здесь путем ссылки); предпочтительно реагент сочетания Сузуки или реагент сочетания Стилла. Подходящие палладиевый и медный катализаторы включают в себя Pd(C6H5)3P)4, Pd(dba)2, Pd(P(C6H5)3)Cl2 и CuI. Подходящие растворители включают в себя диметилформамид или тетрагидрофуран; предпочтительно диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 22 С до приблизительно 110 С, предпочтительно приблизительно 90 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 48 ч, предпочтительно приблизительно 2 ч. Некоторым соединениям формулы 16, таким как соединения где R1 представляет собой замещенный алкин (например, метиламинопропинил) могут потребоваться дополнительные стадии, для которых необходимо применение защитной группы (например, трет-бутоксикарбонила). Эти защитные группы и способы их удаления хорошо известны в данной области техники и могут быть найдены в Greene andWuts, "Protecting Groups in Organic Synthesis," (John WileySons, 2nd Ed). Кроме того, соединения 1 б,такие как соединения где R1, R2 или R3 представляет собой замещенный алкил, алкинил, ароматическую группу или винил, подвергают дополнительным стандартным химическим превращениям (например,каталитическому гидрированию, OsO4/NMMO/NaIO4 окислительному отщеплению, мезилированию/замещению, восстановлениям и восстановительному аминированию). Эти способы также хорошо известны в данной области техники и могут быть найдены в Larock, R.С., "Comprehensive Organic Transformations" (Wiley-VCH, 2nd Ed.). Соединение формулы Iб, где А представляет собой =CR- и R1 представляет собой -(С=O)-O-(C1 С 6)алкил, может быть получено путем реакции соединения формулы Iв, где галоген выбран из бромо или иодо, с монооксидом углерода в присутствии палладиевого катализатора, основания и соединения формулы Н-O-(С 1-С 6)алкил (в зависимости от -(С 1-С 6)алкильной части желаемого R1) в растворителе. Подходящие палладиевые катализаторы включают в себя Pd(dppf)Cl2. Подходящие основания включают в себя третичные аминные основания, такие как триэтиламин. Подходящие соединения формулы Н-O-(С 1 С 6)алкил включают в себя метанол, этанол или пропанол. Подходящие растворители включают в себя диметилформамид или тетрагидрофуран; предпочтительно диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 22 С до приблизительно 110 С, предпочтительно приблизительно 85 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 30 мин до приблизительно 48 ч, предпочтительно приблизительно 16 часов. Соединение формулы 1 б, где А представляет собой =CR1- и R1 представляет собой -(C=O)-NH-(C1- 27009337C6)алкил или -(C=O)-NH-(C1-C6)алкил-OH, или -(C=O)-NH-(C1-С 6)алкил-N(CH3)2, или -(С=O)-1-(4-Nметилпиперазин), может быть получено путем реакции соединения формулы Iв, где галоген выбран из бромо или иодо, с монооксидом углерода в присутствии палладиевого катализатора, основания и соединения формулы Н 2N-(C1-C6)алкил или Н 2N-(C1-C6)алкил-ОН, или H2N-(C1-С 6)алкил-N(CH3)2, или Nметилпиперазина (в зависимости от -(C1-C6)алкильной части желаемого R1) в растворителе. Подходящие палладиевые катализаторы включают в себя Pd(dppf)Cl2. Подходящие основания включают в себя третичные аминные основания, такие как триэтиламин. Подходящие соединения формул Н 2N-(C1-C6)алкил или Н 2N-(C1-C6)алкил-ОН, или Н 2N-(C1-C6)алкил-N(CH3)2, или N-метилпиперазин включают в себя 2 аминоэтанол, N,N-диметилэтилендиамин, метиламин N-метилпиперазин. Подходящие растворители включают в себя диметилформамид или толуол; предпочтительно, диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 22 С до приблизительно 110 С,предпочтительно приблизительно 85 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 30 мин до приблизительно 48 ч, предпочтительно приблизительно 16 ч. Соединение формулы Iв, где галоген представляет собой бромо или иодо, может быть получено путем реакции соединения формулы Iг с подходящим галогенирующим агентом в растворителе. Подходящие галогенирующие агенты включают в себя N-бромсукцинимид или N-иодосукцинимид; предпочтительно N-бромсукцинимид. Подходящие растворители включают в себя тетрагидрофуран или диметилформамид, предпочтительно диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 75 С, предпочтительно приблизительно 22 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 1 ч. Соединение формулы Iв, где галоген представляет собой хлоро, может быть получено путем реакции соединения формулы Iг с подходящим хлорирующим агентом в растворителе. Подходящие хлорирующие агенты включают в себя N-хлорсукцинимид. Подходящие растворители включают в себя тетрагидрофуран или диметилформамид; предпочтительно диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 75 С, предпочтительно приблизительно 45 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 1 ч. Схема 4 относится к получению соединения формулы IVa, которое представляет собой соединение формулы IV схемы 1, где А представляет собой =СН-. В соответствии со схемой 4 соединение формулыIVa, где Lv является такой, как описано выше, может быть получено путем реакции соединения формулыXV, где Lv является такой, как описано выше и каждый Lv3 представляет собой уходящую группу, с подходящей кислотой в полярном протонном растворителе (см. Сое, J. W., Vetelino, M. G., Bradlee, M. J.Tetrahedron Lett. 1996, 37, 6045-6047, включенную здесь путем ссылки). Подходящие уходящие группыLv3 включают в себя метокси или этокси, предпочтительно метокси. Подходящие кислоты включают в себя HCl, H2SO4, пара-толуолсульфоновую кислоту, камфорсульфоновую кислоту или кислоты Льюиса; предпочтительно HCl. Подходящие полярные протонные растворители включают в себя спирты (такие как метанол или этанол), предпочтительно метанол. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 100 С, предпочтительно приблизительно 65 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 1 ч. Соединение формулы XV, где Lv и Lv3 являются такими, как описано выше, может быть получено путем реакции соединения формулы XVI, где Lv и Lv3 являются такими, как описано выше, с восстановителем в полярном растворителе. Подходящие восстановители включают в себя реагенты каталитического переноса, такие как гидрат гидразина, формиат аммония, хлорид аммония, циклогексен или газообразный водород, в присутствии катализаторов [таких как Pd на углероде (см. Сое, J. W., Vetelino, M.G., Bradlee, M. J. Tetrahedron Lett. 1996, 37, 6045-6047, включенную здесь путем ссылки), Ru, Rh, ренеевский никель или Pt]; HCl или уксусная кислота в присутствии In, Fe, Sn или Zn; HCl/SnCl2;SnCl22H2O;Bu3SnH/AlBN или Fe3(CO)12; предпочтительно SnCl22H2O или газообразный водород в присутствии Pd на углероде или никеля Ренея. Подходящие полярные растворители включают в себя спирты(такие как метанол или этанол), предпочтительно метанол. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 100 С, предпочтительно приблизительно 23 С. Когда используют газообразный водород, реакционное давление может составлять от 1 до 4 атм (от 1,01325 х 105 Па до 4,053 х 105 Па), предпочтительно 1 атм (1,01325 х 105 Па). Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 2 ч до приблизительно 48 ч, предпочтительно приблизительно 24 ч. Соединение формулы XVI, где Lv и Lv3 являются такими, как описано выше, может быть получено путем реакции соединения формулы XVII, где Lv является такой, как описано выше, с подходящей кислотой в безводном полярном протонном растворителе формулы Lv3-H. Подходящие кислоты включают- 28009337 в себя HCl, H2SO4 или паратолуолсульфоновую кислоту, предпочтительно HCl. Альтернативно, HCl может быть образован in situ путем использования агента, продуцирующего HCl, такого как тетраметилсилан-Cl (ТМС-Cl) или ацетилхлорид, предпочтительно ТМС-Cl, в безводном полярном протонном растворителе, таком как метанол. Подходящие безводные полярные протонные растворители формулы Lv3-H включают в себя безводные спирты (такие как метанол или этанол), предпочтительно безводный метанол. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 23 С до приблизительно 78 С, предпочтительно приблизительно 65 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 30 мин до приблизительно 48 ч, предпочтительно приблизительно 24 ч. Соединение формулы XVII, где Lv является такой, как описано выше, может быть получено путем реакции соединения формулы XVIII, где Lv является такой, как описано выше, с соединением формулы где каждый из Lv3 является таким, как описано выше, в полярном растворителе. Подходящие соединения формулы (CH3)2-N-CH-(Lv3)2 включают в себя диметилформамид-диметилацеталь. Подходящие полярные растворители включают в себя диметилформамид, толуол или спирт (такой как этанол),предпочтительно, диметилформамид. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 22 С до приблизительно 150 С, предпочтительно приблизительно 110 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 15 мин до приблизительно 24 ч, предпочтительно приблизительно 6 ч. Соединения формулы (CH3)2-N-CH-(Lv3)2 имеются в продаже. Соединения формулы XVII, где Lv является такой, как описано выше, имеются в продаже или, альтернативно, могут быть получены с использованием способов, хорошо известных специалисту в данной области техники. Схема 5 относится к получению соединения формулы IVб, которое представляет собой соединение формулы IV схемы 1, где А представляет собой =CR1-. В соответствии со схемой 5 соединение формулыIVб может быть получено путем реакции соединения формулы XIX, где Lv является такой, как описано выше и Lv4 представляет собой уходящую группу, с подходящим замещенным алкином формулыM1-CC-R1,1 где М представляет собой Н или металл (такой как Sn или В), предпочтительно Н или Sn, в присутствии металлического катализатора в полярном растворителе. Подходящие уходящие группы Lv4 включают в себя галогено, предпочтительно бромо или иодо. Подходящие металлические катализаторы включают в себя паладиевый или медный катализаторы (см. Fagnola, M. С. et al. Tetrahedron Lett. 1997, 38,2307-2310, включенную здесь путем ссылки). Подходящие полярные растворители включают в себя диметилформамид, диоксан, диметилсульфоксид или их смеси, предпочтительно смесь диметилформамида и диоксана. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 22 С до приблизительно 150 С, предпочтительно приблизительно 90 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч,предпочтительно приблизительно 8 ч. Соединения формулы M1-CC-R1 имеются в продаже или могут быть получены с использованием способов, хорошо известных специалисту в данной области техники. Соединение формулы XIX, где Lv и Lv4 являются такими, как описано выше, может быть получено путем реакции соединения формулы XX, где Lv и Lv4 являются такими, как описано выше, с восстановителем в присутствии (СН 3 СО)2 О в полярном растворителе. Подходящие восстановители включают в себя газообразный водород в присутствии катализаторов, таких как Pd/C (см. Сое, J. W., Vetelino, M. G., Bradlee, М. J. Tetrahedron Lett. 1996, 37, 6045-6047, включенную здесь путем ссылки), Rd, ренеевский никель или Pt; уксусную кислоту в присутствии In, Fe или Zn; SnCl2 или Fe3(CO)12; предпочтительно газообразный водород в присутствии Pd/C; или уксусная кислота в присутствии Fe. Подходящие полярные растворители включают в себя диметилформамид, метанол, этанол или уксусную кислоту; предпочтительно метанол или уксусную кислоту. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 20 С до приблизительно 100 С, предпочтительно приблизительно 22 С. Когда используют газообразный водород реакционное давление может составлять от 1 до 4 атм (от 1,01325 х 105 Па до 4,053 х 105 Па), предпочтительно 1 атм (1,01325 х 105 Па). Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 2 ч до приблизительно 48 ч, предпочтительно приблизительно 24 ч. Соединения формулы XX имеются в продаже или могут быть получены с использованием способов, хорошо известных специалистам в данной области техники. Схема 6 относится к получению соединения формулы Ie, которое представляет собой соединение формулы I схемы 1, где группа -Y-Z- имеет формулу -N=CH-, A представляет собой =N- и R2 отличается- 29009337 от водорода. В соответствии со схемой 6 соединение формулы Iд может быть получено путем реакции соединения формулы Iд, которое представляет собой соединение формулы I схемы 1, где группа -Y-Zимеет формулу -N=CH-, А представляет собой =N- и R представляет собой водород, с соединением формулыR2-Lv1,1 где Lv представляет собой уходящую группу, такую как галогено, предпочтительно бромо или хлоро, в присутствии подходящего основания в полярном растворителе. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединений формулы III из соединения формулы IV. Соединения формулы Iд могут быть получены путем реакции соединения формулы VIIIa, которое представляет собой соединение формулы VIII схемы 2, где А представляет собой =N- и Lv является такой, как описано выше, с гидазином в растворителе. Условия реакции являются такими, как определено выше в описании для схемы 1 для получения соединения формулы I из соединения формулы II. Соединения формулы VIIIa могут быть получены путем взаимодействия соединения формулы IVa,которое представляет собой продукт схемы 4, с агентом, продуцирующим азотистую кислоту, в присутствии кислоты в растворителе. Подходящие агенты, продуцирующие азотистую кислоту, включают в себя NaNO2, KNO2, изоамиловый нитрит или трет-бутилнитрит, предпочтительно NaNO2. Подходящие кислоты включают в себя уксусную кислоту или водную HCl; предпочтительно уксусную кислоту. Подходящие растворители включают в себя уксусную кислоту, бензол, диметилформамид, толуол или спирты (такие как метанол), предпочтительно уксусную кислоту. Вышеупомянутая реакция может быть осуществлена при температуре от приблизительно 0 С до приблизительно 30 С, предпочтительно приблизительно 0 С с нагреванием до 23 С. Вышеупомянутая реакция может быть осуществлена в течение промежутка времени от приблизительно 5 мин до приблизительно 24 ч, предпочтительно приблизительно 1 ч. В данном изобретении понятно, что соединение формулы I может демонстрировать явление таутомерии и что изображения формул в данном описании представляют только одну из возможных таутомерных форм. Понятно, что данное изобретение охватывает любую таутомерную форму, которая модулирует и/или ингибирует киназную активность, а не ограничивается исключительно какой-либо одной таутомерной формой, используемой в изображениях формул. Некоторые из заявленных соединений могут существовать в виде одиночных стереоизомеров (т.е.,по существу без других стереоизомеров), рацематов и/или смесей энантиомеров и/или диастереоизомеров. Предполагается, что все такие одиночные стереоизомеры, рацематы и их смеси находятся в объеме настоящего изобретения. Предпочтительно заявленные соединения, которые являются оптически активными, используют в оптически чистой форме. Как в общем понятно специалисту в данной области техники, оптически чистое соединение, имеющее один хиральный центр (т.е., один асимметрический атом углерода), представляет собой соединение,которое состоит по существу из одного из двух возможных энантиомеров (т.е., является энантиомерно чистым), и оптически чистое соединение, имеющее более чем один хиральный центр, представляет собой соединение, которое является диастереоизомерно чистым и энантиомерно чистым. Предпочтительно соединения по настоящему изобретению применяют в форме, которая по меньшей мере на 90% является оптически чистой, то есть форме, которая содержит по меньшей мере 90% одного изомера (80% энантиомерный избыток ("э. и.") или диастереоизмерный избыток ("д. и. ", более предпочтительно по меньшей мере 95% (90% э. и. или д. и.), еще более предпочтительно по меньшей мере 97,5% (95% э. и. или д. и.), и наиболее предпочтительно по меньшей мере 99% (98% э. и. или д. и.). Кроме того, предполагается, что формула I охватывает сольватированные а также несольватированные формы идентифицированных структур. Например, формула I включает в себя соединения указанной структуры в гидратированной и негидратированной формах. Другие примеры сольватов включают в себя структуры в комбинации с изопропанолом, этанолом, метанолом, диметилсульфоксидом(ДМСО), этилацетатом, уксусной кислотой или этаноламином. Если заявленное соединение представляет собой основание, желаемая фармацевтически приемлемая соль может быть получена с использованием любого подходящего способа, доступного в данной области техники, например, обработки свободного основания неорганической кислотой, такой как соляная кислота, бромоводородная кислота, серная кислота, азотная кислота, ортофосфорная кислота и т.п.,или органической кислотой, такой как уксусная кислота, малеиновая кислота, янтарная кислота, миндальная кислота, фумаровая кислота, малоновая кислота, виноградная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота, пиранозидиловая кислота, такая как глюкуроновая кислота или галактуроновая кислота, альфа-гидроксикислота, такая как лимонная кислота или винная кислота, аминокислота, такая как аспарагиновая кислота или глютаминовая кислота, ароматическая кислота, такая как бензойная кислота или коричная кислота, сульфоновая кислота, такая как паратолуолсульфоновая кислота или этансульфоновая кислота или т. п. Если заявленное соединение представляет собой кислоту, желаемая фармацевтически приемлемая
МПК / Метки
МПК: A61K 31/55, A61P 35/00, C07D 487/06
Метки: ингибиторы, протеинкиназ, трициклические, увеличения, эффективности, агентов, собой, противоопухолевых, соединения, представляющие, терапии, лучевой
Код ссылки
<a href="https://eas.patents.su/30-9337-triciklicheskie-soedineniya-predstavlyayushhie-sobojj-ingibitory-proteinkinaz-dlya-uvelicheniya-effektivnosti-protivoopuholevyh-agentov-i-luchevojj-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Трициклические соединения, представляющие собой ингибиторы протеинкиназ, для увеличения эффективности противоопухолевых агентов и лучевой терапии</a>
Следующий патент: 4-(3-гетероциклил-1-бензоил)пиразолы
Случайный патент: Регистрация гамма-излучения в буровой скважине