Новые спиротрициклические производные и их применение в качестве ингибиторов фосфодиэстеразы-7
Номер патента: 6815
Опубликовано: 28.04.2006
Авторы: Бернарделли Патрик, Лортиуа Эдвиг, Вернье Фабрис, Дюкро Пьер
Формула / Реферат
1. Соединение, имеющее следующую формулу (I)
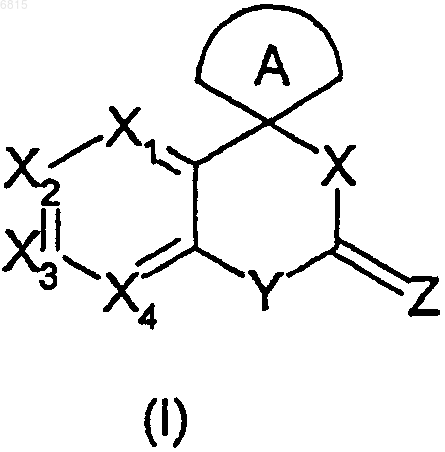
где a) X1, Х2, Х3 и Х4 одинаковые или различные и выбраны из
C-R1, где R1 выбран из
Q1 или
низшего алкила, низшего алкенила или низшего алкинила, причем эти группы не замещены или замещены одной или несколькими группами Q2;
группы Х5-R5,
где X5 выбран из
одинарной связи;
низшего алкилена, низшего алкенилена или низшего алкинилена, возможно прерванных 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, причем атомы углерода этих групп не замещены или замещены одной или несколькими группами, одинаковыми или различными, выбранными из SR6, OR6, NR6R7, =O, =S или =N-R6, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, и
R5 выбран из арила, гетероарила, циклоалкила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, циклоалкенила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или бициклической группы, причем эти группы не замещены или замещены одной или несколькими группами, выбранными из Q3, гетероарила или низшего алкила, возможно замещенного Q3;
где Q1, Q2, Q3 одинаковые или различные и выбраны из
водорода, галогена, CN, NO2, SО3Н, Р(=O)(ОН)2;
OR2, OC(=O)R2, C(=O)OR2, SR2, S(=O)R2, С(=O)-NН-SO2-СН3, NR3R4, Q-R2, Q-NR3R4, NR2-Q-NR3R4 или NR3-Q-R2, где Q выбран из C(=NR), C(=O), C(=S) или SO2, R выбран из водорода, CN, SO2NH2 или низшего алкила, и R2, R3 и R4 одинаковые или различные и выбраны из
водорода,
низшего алкила, возможно прерванного С(=O), Q4-арила, Q4-гетероарила, Q4-циклоалкила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или Q4-циклоалкенила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, где
Q4 выбран из (СН2)n, низшего алкила, прерванного одним гетероатомом, выбранным из О, S или N, низшего алкенила или низшего алкинила, причем эти группы возможно замещены низшим алкилом, OR' или NR'R", где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила;
n является целым числом, выбранным из 0, 1, 2, 3 или 4;
причем эти группы не замещены или замещены одной или несколькими группами, выбранными из низшего алкила, галогена, CN, СН3, SO3Н, SO2СН3, С(=O)-NН-SO2-СН3, СF3, OR6, COOR6, C(=O)R6, NR6R7, NR6C(=O)R7, C(=O)NR6R7 или SO2NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, возможно замещенного одной или двумя группами, выбранными из OR, COOR или NRR8, где R и R8 являются водородом или низшим алкилом, и
R6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено
(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, или
низшим алкилом, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из
водорода или
низшего алкила, возможно замещенного OR или COOR,
где R является водородом или низшим алкилом, и
R' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N; или когда X1 и Х2 оба представляют собой C-R1, 2 заместителя R1 могут образовывать вместе с атомами углерода, к которым они присоединены, 5-членное гетероциклическое кольцо, содержащее атом азота и возможно второй гетероатом, выбранный из О, S или N;
б) Х представляет собой NR9, где R9 представляет собой водород;
в) Y представляет собой N-R12, где R12 представляет собой водород;
г) Z выбран из О, S или NR13, где R13 представляет собой CN;
д) А является циклом, выбранным из
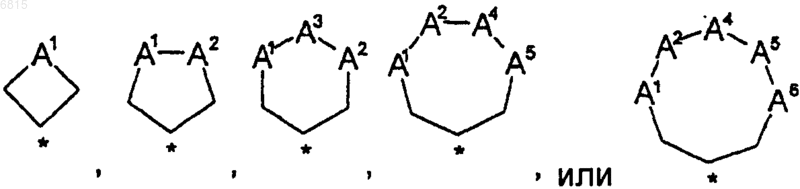
где А1, А2, А4, А5 и А6 представляют собой атом углерода;
* представляет собой атом углерода, который является общим для цикла А и основного цикла, содержащего Х и/или Y;
каждый атом углерода в цикле А не замещен или замещен 1 или 2 группами, одинаковыми или различными, выбранными из низшего алкила;
2 атома цикла А, которые не являются соседними, могут быть соединены посредством цепи из 2, 3 или 4 атомов углерода;
или их таутомерные формы, их рацемические формы или их изомеры и их фармацевтически приемлемые производные;
при этом подразумевается, что
низший алкил и низший алкилен означают прямые и разветвленные углеродные цепи, имеющие от 1 до 6 атомов углерода;
низший алкенил и низший алкенилен означают прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 атомов углерода и по меньшей мере одну двойную связь;
низший алкинил и низший алкинилен означают прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 атомов углерода и по меньшей мере одну тройную связь;
низший галогеноалкил означает низший алкил, как он определен выше, замещенный одним или несколькими атомами галогена;
циклоалкил означает насыщенный карбоцикл, содержащий от 3 до 8 атомов углерода;
циклоалкенил означает карбоцикл, содержащий от 3 до 10 атомов углерода и по меньшей мере одну двойную связь;
арил означает ароматический карбоцикл, содержащий от 6 до 10 атомов углерода;
гетероарил означает ароматический цикл, который имеет от 5 до 10 кольцевых атомов, от 1 до 4 из которых независимо выбраны из группы, состоящей из О, S и N;
гетероциклическое кольцо включает гетероарил, как он определен выше, и циклоалкил или циклоалкенил, как они определены выше, прерванный 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N;
бициклическая группа означает два цикла, которые являются одинаковыми или различными и выбраны из арила, как он определен выше, гетероциклического кольца, как оно определено выше, циклоалкила, как он определен выше, или циклоалкенила, как он определен выше, конденсированных вместе с образованием указанной бициклической группы.
2. Соединение формулы (I) по п.1, где
a) X1, X2 и Х3 одинаковые или различные и представляют собой C-R1, где R1 выбран из
водорода, галогена, CN, SО3Н, NO2, СF3, OR2, SR2, NR2R3, COR2, COOR2, CONR2R3, SО2СН3, SO2NR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, возможно замещенного галогеном, CN, OR6, COOR6, NR6R7, SO2NR6R7 или C(=O)NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, и
R6 и R7 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, как оно определено в п.1;
низшего алкила, как он определен в п.1, низшего алкенила, как он определен в п.1, или низшего алкинила, как он определен в п.1, причем эти группы не замещены или замещены 1, 2 или 3 группами, выбранными из галогена, CN, SO3H, OR2, COOR2, NR3R4, SO2NR3R4 или С(=O)NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, и
R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо;
группы X5-R5,
где X5 выбран из низшего алкилена, как он определен в п.1, или одинарной связи, и
R5 выбран из фенила, пиридила или индолила,
причем эти группы не замещены или замещены 1, 2 или 3 группами, выбранными из Q3, гетероарила, как он определен в п.1, или низшего алкила, как он определен в п.1, возможно замещенного Q3, где Q3 выбран из
галогена, CN, SО3Н, NO2, СF3, OR2, OC(=O)R2, C(=O)R2, C(=O)OR2, NH-C(=O)R2, NR3R4, SО2NR3R4 или С(=O)NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из
водорода, низшего алкила, как он определен в п.1, незамещенного или замещенного одной или несколькими группами, выбранными из галогена, OR6, COOR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, и
R6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать одинили два гетероатома, выбранные из О, S или N, и которое может быть замещено
4-8-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен в п.1, или
низшим алкилом, как он определен в п.1, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из
Н или
низшего алкила, как он определен в п.1, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен в п.1, и R' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N;
б) Х4 представляет собой C-R1, где R1 выбран из водорода, галогена, CN, NO2, SО2СН3, SO3Н, СН3, СF3, OR2, SR2, NR2R3, COOR2, CONR2R3 или SO2NR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1;
в) Х представляет собой NH;
г) Y представляет собой NH;
д) Z выбран из О, S или NR13, где R13 представляет собой CN;
е) А является циклом, выбранным из
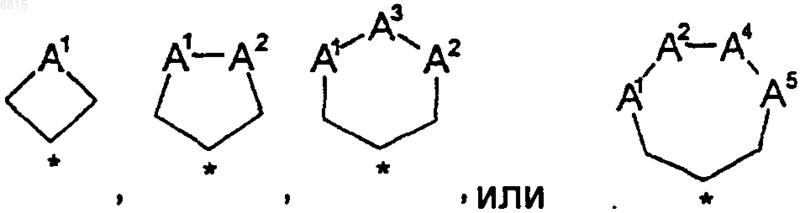
где А1, А2, А3, А4 и А5 одинаковые или различные и выбраны из
атома углерода, незамещенного или замещенного 1 или 2 группами, одинаковыми или различными, выбранными из низшего алкила, как он определен в п.1;
* представляет собой атом углерода, который является общим для цикла А и основного цикла, содержащего Х и/или Y;
2 атома цикла А, которые не являются соседними, могут быть соединены посредством цепи из 2, 3 или 4 атомов углерода.
3. Соединение формулы (I) по п.1, где Х1, Х2, Х3 и Х4 одинаковые или различные и представляют собой C-R1, где R1 выбран из
Q1 или
низшего алкила, низшего алкенила или низшего алкинила, как они определены в п.1, причем эти группы не замещены или замещены 1, 2 или 3 группами Q2;
группы Х5-R5,
где X5 выбран из
одинарной связи;
низшего алкилена, как он определен в п.1, возможно прерванного 1 гетероатомом, выбранным из О, S и N;
R5 выбран из арила, как он определен в п.1, гетероарила, как он определен в п.1, циклоалкила, как он определен в п.1, возможно прерванного С(=O) или 1, 2 либо 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, циклоалкенила, как он определен в п.1, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или бициклической группы, причем эти группы не замещены или замещены 1, 2 или 3 группами, выбранными из Q3, гетероарила, как он определен в п.1, или низшего алкила, как он определен в п.1, возможно замещенного Q3;
где Q1, Q2, Q3 одинаковые или различные и выбраны из
водорода, галогена, CN, NO2, SО3Н,
OR2, OC(=O)R2, C(=O)OR2, SR2, S(=O)R2, С(=O)-NН-SO2-СН3, NR3R4, Q-R2, Q-NR3R4, NR2-Q-NR3R4 или NR3-Q-R2, где Q выбран из C(=NR), C(=O), C(=S) или SO2, R выбран из водорода или низшего алкила, и R2, R3 и R4 одинаковые или различные и выбраны из
водорода,
низшего алкила, как он определен в п.1, возможно прерванного С(=O), Q4-арила, как он определен в п.1, Q4-гетероарила, как он определен в п.1, Q4-циклоалкила, как он определен в п.1, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или Q4-циклоалкенила, как он определен в п. 1, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N,
где Q4 выбран из (СH2)n, низшего алкила, как он определен в п.1, прерванного одним гетероатомом, выбранным из О, S или N, низшего алкенила, как он определен в п.1, или низшего алкинила, как он определен в п.1, причем эти группы возможно замещены низшим алкилом, как он определен в п.1, OR' или NR'R", где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1;
n является целым числом, выбранным из 0, 1, 2, 3 или 4;
причем эти группы не замещены или замещены 1 или 2 группами, выбранными из низшего алкила, как он определен в п.1, галогена, CN, СН3, SО3Н, SO2СН3, СF3, С(=O)NН-SO2СН3, OR6, COOR6, C(=O)R6, NR6R7, C(=O)NR6R7 или SO2NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, возможно замещенного одной или двумя группами, выбранными из OR, COOR или NRR8, где R и R8 являются водородом или низшим алкилом, как он определен в п.1, и
R6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один шыш два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено
(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен в п.1, или
низшим алкилом, как он определен в п.1, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из
Н или
низшего алкила, как он определен в п.1, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен в п.1, и
R' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N.
4. Соединение формулы (I) по п.3, где X1, X2, Х3 и Х4 одинаковые или различные и представляют собой C-R1, где R1 выбран из
Q1 или
низшего алкила или низшего алкинила, причем эти группы такие, как определено в п.1, и не замещены или замещены 1, 2 или 3 атомами фтора, OR3, COOR3 или NR3R4, где R3 и R4 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1;
R3 и R4 вместе с атомом азота, к которому они присоединены, могут также образовывать 6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N;
группы X5-R5, где X5 представляет собой одинарную связь, и R5 выбран из арила, гетероарила или бициклической группы, причем эти группы такие, как определено в п.1, и не замещены или замещены 1, 2 или 3 группами, выбранными из Q3,
где Q1 и Q3 одинаковые или различные и выбраны из
водорода, галогена, CN, низшего алкила, как он определен в п.1,
OR2, C(=O)OR2, NR3R4, С(=O)NR3R4 или SO2NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из
водорода,
низшего алкила, как он определен в п.1, Q4-гетероарила, где Q4 выбран из низшего алкила, прерванного одним гетероатомом, выбранным из О, S или N, и (CH2)n, где n является целым числом, выбранным из 0, 1, 2 или 3, и где гетероарил такой, как определено в п.1;
причем эти группы не замещены или замещены 1 или 2 группами, выбранными из низшего алкила, CN, SО3Н, С(=O)-NН-SO2-СН3, OR6, COOR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, возможно замещенного одной или двумя группами, выбранными из OR, COOR или NRR8, где R и R8 являются водородом или низшим алкилом, как он определен в п.1, и
R6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено
6-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено низшим алкилом, или
низшим алкилом, как он определен в п.1, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из
Н или
низшего алкила, как он определен в п.1, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен в п.1, и
R' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N.
5. Соединение формулы (I) по п.3, где Х1 представляет собой C-R1, где R1 выбран из
водорода, галогена, OR2, COR2, COOR2, CONR2R3, где R2 и R3 одинаковые или различные и выбраны из
водорода,
низшего алкила, как он определен в п.1, Q4-арила, Q4-гетероарила, Q4-циклоалкила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S или N, или Q4-циклоалкенила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S или N,
где Q4 выбран из (CH2)n, низшего алкила, как он определен в п.1, прерванного одним гетероатомом, выбранным из О, S или N, низшего алкенила, как он определен в п.1, или низшего алкинила, как он определен в п.1;
арил, гетероарил, циклоалкил и циклоалкенил такие, как определено в п.1;
n является целым числом, выбранным из 0, 1, 2 или 3;
причем эти группы не замещены или замещены низшим алкилом, CN, OR6, SO3Н, C(=O)-NH-SO2-CH3, CONR6R7, COOR6, COR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, возможно замещенного NН3, СООН, ОН;
R6 и R7 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено
(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен в п.1, или
COR' или низшим алкилом, как он определен в п.1, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1;
низшего алкила, как он определен в п.1, возможно замещенного CN, SО3Н, OR3, NR3R4, COOR3 или CONR3R4, где R3 и R4 одинаковые или различные и выбраны из
водорода и
низшего алкила, как он определен в п.1, возможно замещенного ОН, СООН или NH2,
группы X5-R5, где X5 является низшим алкиленом, как он определен в п. 1, возможно прерванным гетероатомом, выбранным из О и N, и R5 выбран из арила, как он определен в п.1, гетероарила, как он определен в п.1, циклоалкила, как он определен в п.1, возможно прерванного С(=O) либо 1, 2 или 3 гетероатомами, выбранными из О, S или N, и циклоалкенила, как он определен в п.1, возможно прерванного С(=O), либо 1, 2 или 3 гетероатомами, выбранными из О, S или N, причем эти группы не замещены или замещены OR3 или COOR3, где R3 выбран из водорода и низшего алкила, как он определен в п.1;
R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено
(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен в п.1, или
C(=O)-R' или низшим алкилом, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1.
6. Соединение формулы (I) по п.3, где Х1 представляет собой C-R1, где R1 выбран шч водорода, галогена или OR2, где R2 выбран из
водорода,
низшего алкила, как он определен в п.1, незамещенного или замещенного CN, С(=O)-NН-SO2-СН3, OR6, SO3Н, COOR6 или NR6R7,
Q4-оксадиазола, Q4-тетразола, Q4-морфолина, Q4-фурана, Q4-изоксазола, где Q4 выбран из низшего алкила, как он определен в п.1, прерванного одним гетероатомом, выбранным из О, S или N, и (СН2)n, где n является целым числом, выбранным из 1 и 2;
причем эти группы не замещены или замещены СН3, OR6 или COOR6, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1, возможно замещенного NH2 или СООН.
7. Соединение формулы (I) по любому из пп.3, 5 и 6, где Х2 представляет собой C-R1, где R1 представляет собой X5-R5,
где X5 представляет собой одинарную связь,
R5 представляет собой фенил или пиридил,
возможно замещенный низшим алкилом, как он определен в п.1, и
замещенный C(=O)NR3R4, где R3 и R4 вместе с атомом азота, к которому они присоединены, образуют 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено
4-8-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен в п.1, или
низшим алкилом, как он определен в п.1, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из
Н или
низшего алкила, как он определен в п.1, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен в п.1, и
R' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N.
8. Соединение формулы (I) по любому из пп.3-7, где один из X1, X2, Х3 и Х4 представляет собой C-R1, где R1 является водородом, а остальные являются одинаковыми или различными и представляют собой C-R1, где R1 отличен от водорода.
9. Соединение формулы (I) по п.8, где Х3 представляет собой C-R1, где R1 является водородом.
10. Соединение формулы (I) по любому из пп.3-8, где Х3 представляет собой C-R1, где R1 выбран из
водорода или галогена или
X5-R5, где X5 представляет собой одинарную связь и R5 является арилом, как он определен в п.1, или гетероарилом, как он определен в п.1, возможно замещенными одной, двумя или тремя группами, которые являются одинаковыми или различными и выбраны из галогена, CN, СF3, SO2Me, OR2, COOR2, NR2R3, SO2NR2R3 и CONR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1.
11. Соединение формулы (I) по п.10, где Х3 представляет собой C-R1, где R1 выбран из водорода или галогена.
12. Соединение формулы (I) по любому из пп.3-11, где Х4 представляет собой C-R1, где R1 выбран из
водорода, галогена, CF3, O-низшего алкила (причем низший алкил такой, как определено в п.1), COOR2 или
низшего алкила, как он определен в п.1, возможно замещенного OR2, COOR2 или SO2NR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен в п.1.
13. Соединение формулы (I) по любому из пп.1-12, где Z представляет собой О.
14. Соединение формулы (I) по любому из пп.1-13, где А выбран из циклогексила или циклогептила, незамещенных или замещенных СН3.
15. Соединение формулы (I) по любому из пп.1-13, где А выбран из незамещенных циклогексила или циклогептила.
16. Соединение, выбранное из группы, состоящей из
спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
спиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
7'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-фенилспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
7'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-бромоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-фтороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5',8'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6',7'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5',6'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-фенилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-иодоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-бромоспиро[циклобутан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-бромоспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-бромо-4-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-бромоспиро[бицикло[3,2,1]октан-2-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6',8'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-иодоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-фенилспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-фенилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(3-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(4-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-(4-карбоксифенил)-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1 'Н)-она,
6'-(3-кapбoкcифeнил)-8'-xлopocпиpo[циклoгeкcaн-1-4'-(3',4'-дигидpo)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(1Н-индол-5-ил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(2-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(3-диметиламино-проп-1-инил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(3-метиламино-проп-1-инил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(3-N-диметиламинопропилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(2-N-диметиламиноэтилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[3-(3-N-диметиламинопропилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[3-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[3-(2-N-диметиламиноэтилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-тиона,
8'-хлоро-2'-цианоиминоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолина],
8'-хлоро-6'-[4-(4-пиримидин-2-ил-пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(4-(2-морфолин-4-ил-этил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(4-(2-морфолин-4-ил-2-оксоэтил)-пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(4-(2-гидроксиэтоксиэтил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
спиро[циклогексан-1-9'-(8',9'-дигидро)пиразоло[4',3'-f]хиназолин]-7'(6'Н)-она,
8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5',8'-дифтороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-(морфолин-4-ил)метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-гидроксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-гидрокси-6'-иодо-спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-иодо-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-циано-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(4-морфолино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-диметиламиноэтокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(2-аминоэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(метиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(2-аминоэтокси)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[3-диметиламинопропокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-этоксикарбонилметоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5'-карбоксиметокси-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
5'-карбоксипропокси-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(3-сульфопропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(тетрагидропиран-2-илокси)-этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназо-лин]-2'(1'Н)-она,
8'-хлоро-5'-(2-гидроксиэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(5-этоксикарбонилфуран-2-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(5-карбоксифуран-2-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-цианометоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(1Н-тетразол-5-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(5-гидрокси-[1,2,4]оксадиазол-3-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-иодо-5'-[2-диметиламиноэтокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-(4-карбоксифенил)-8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
6'-(3-карбоксифенил)-8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[2-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[2-метил-4-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-(пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-карбамоилфенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-[4-((1-метилпиперидин-4-ил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-метокси-6'-[4-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-трифторметилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-6'-цианометилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(3-диметиламино-2-гидроксипропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(3-метиламино-2-гидроксипропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(этоксикарбонилметиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-[2-(карбоксиметиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она гидрохлорида,
8'-хлоро-5'-(2-метансульфониламино-2-оксоэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,
8'-хлоро-5'-(2-[(5-метилизоксазол-3-илметил)амино]этокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она.
17. Применение соединения по любому из пп.1-16 для применения в качестве лекарства.
18. Фармацевтическая композиция, содержащая соединение по любому из пп.1-16 в комбинации с подходящим носителем.
19. Применение соединения по любому из пп.1-16 для приготовления лекарства для предупреждения или лечения расстройств, для которых показана терапия ингибитором PDE7.
20. Применение по п.19, где указанное расстройство выбрано из связанных с Т-клетками заболеваний, аутоиммунных заболеваний, остеоартрита, рассеянного склероза, остеопороза, хронической обструктивной болезни легких, астмы, рака, синдрома приобретенного иммунодефицита, аллергии или воспалительного заболевания кишечника.
21. Способ предупреждения или лечения расстройства, для которого показана терапия ингибитором PDE7, при котором млекопитающему, нуждающемуся в такой терапии, вводят эффективное количество соединения по любому из пп.1-16.
22. Способ по п.21, где указанное расстройство выбрано из связанных с Т-клетками заболеваний, аутоиммунных заболеваний, остеоартрита, рассеянного склероза, остеопороза, хронической обструктивной болезни легких, астмы, рака, синдрома приобретенного иммунодефицита, аллергии или воспалительного заболевания кишечника.
23. Способ получения соединения формулы (I) по п.1, где X1, Х2, Х3, Х4, А и R9 такие, как определено в п.1, и Y представляет собой NH, при котором
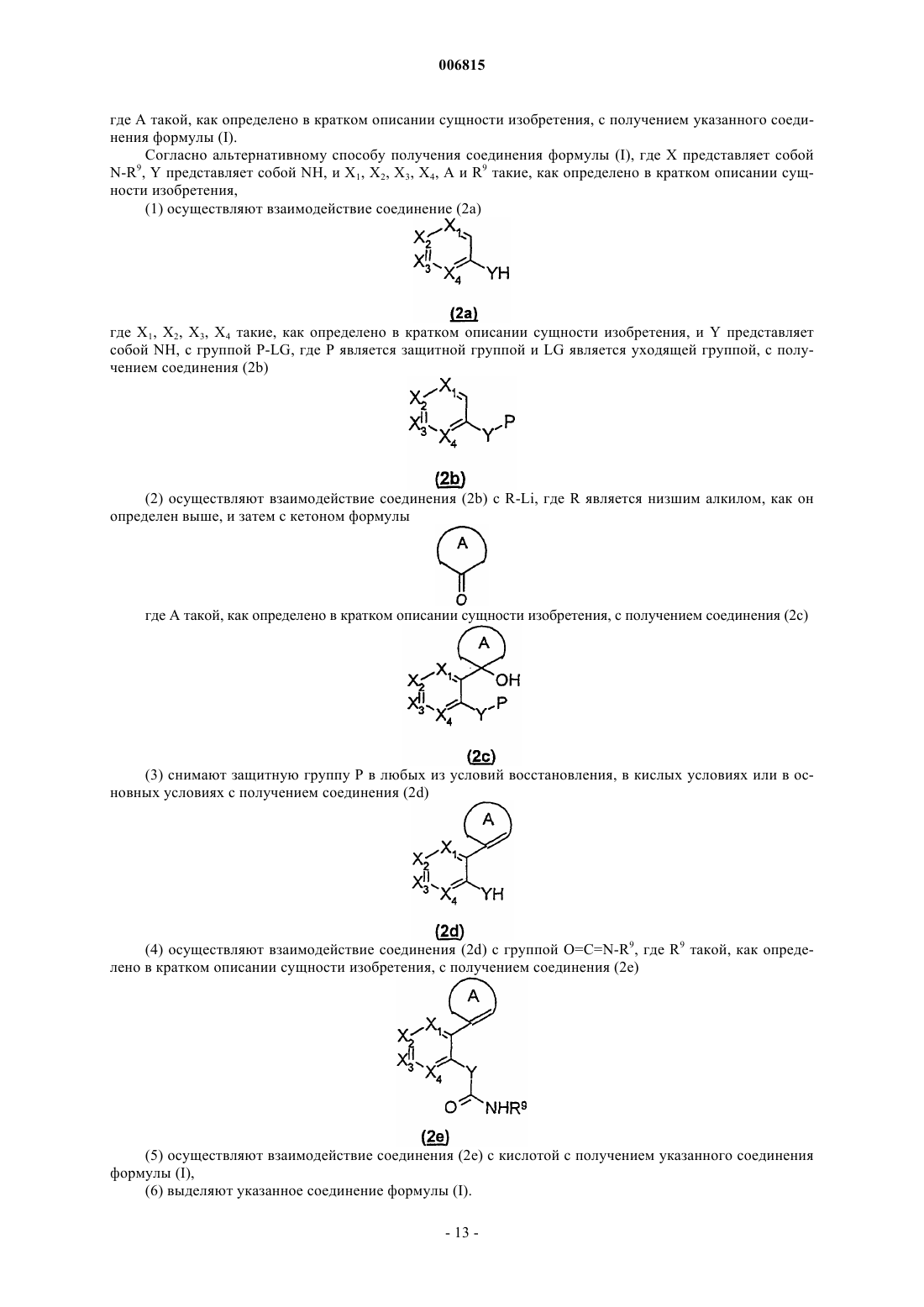
(1) осуществляют взаимодействие соединения (2а),
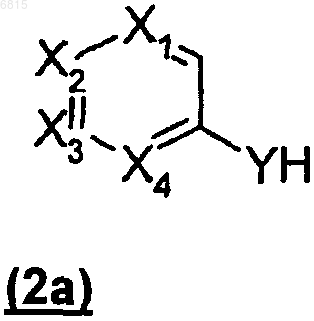
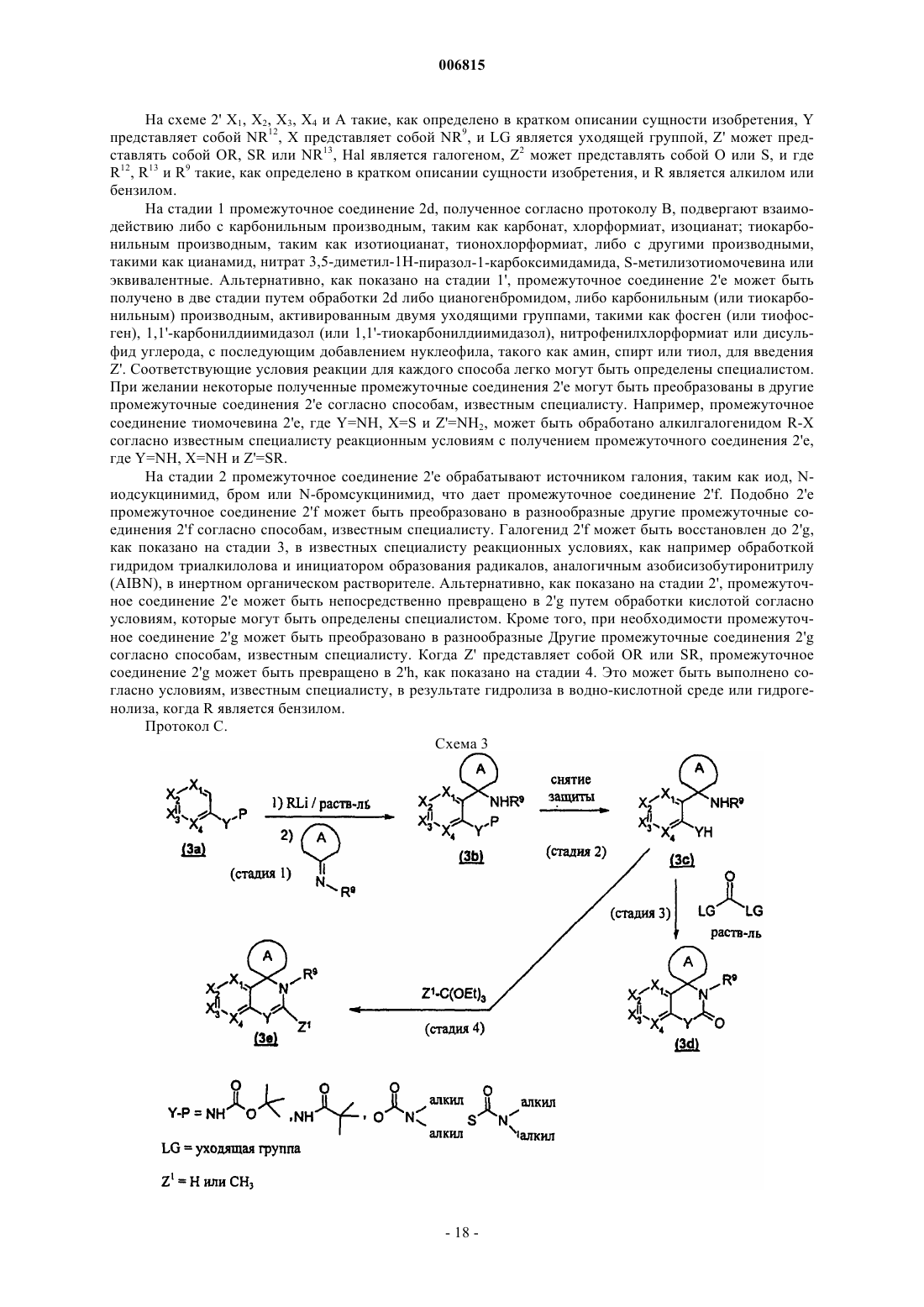
где X1, X2, Х3, Х4 такие, как определено в п.1, и Y представляет собой NH, с группой P-LG, где Р является защитной группой и LG является уходящей группой, с получением соединения (2b)
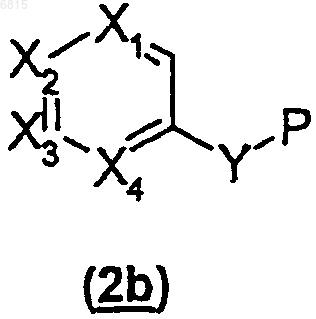
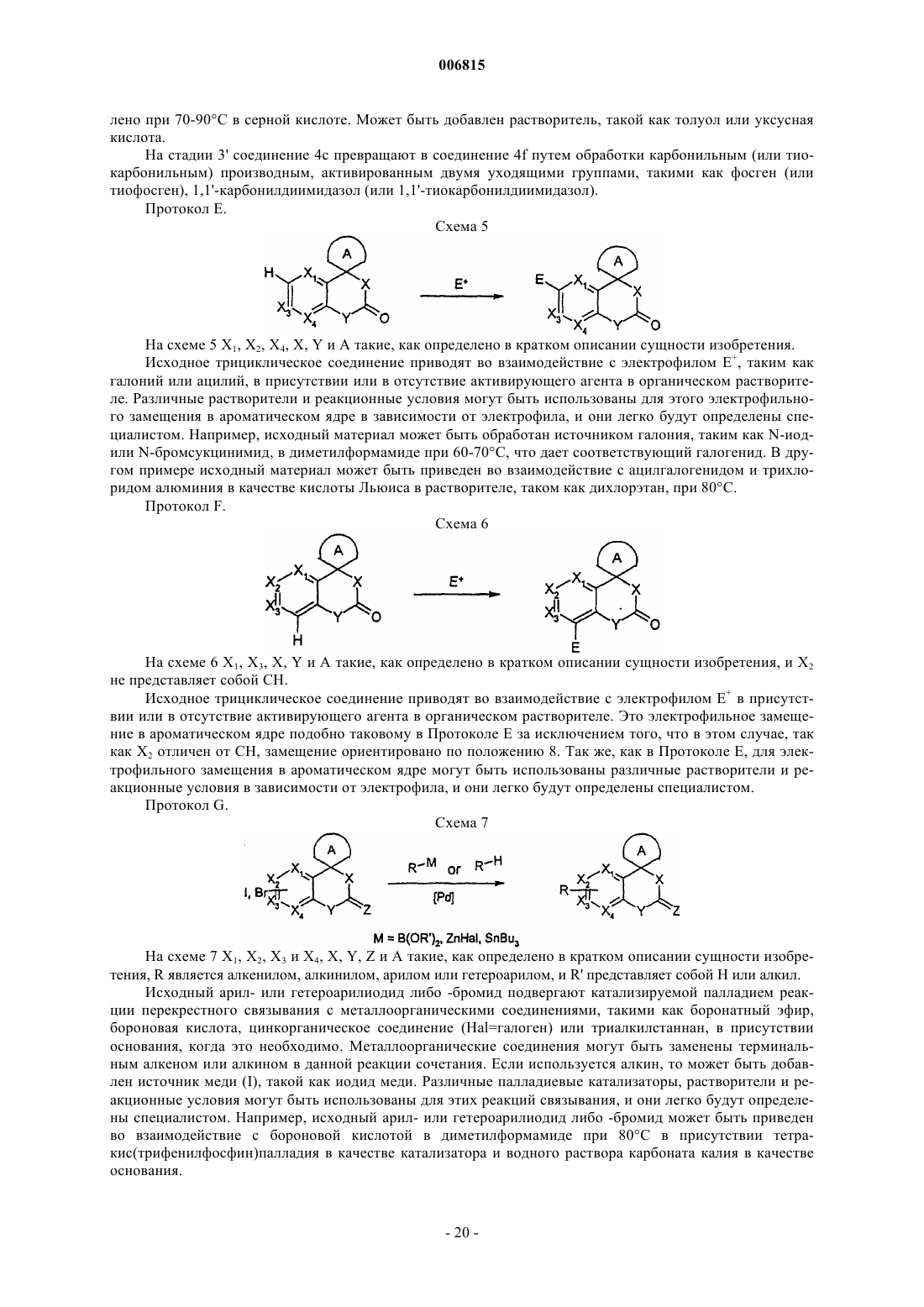
(2) осуществляют взаимодействие соединения (2b) с R-Li, где R является низшим алкилом, как он определен в п.1, и затем с кетоном формулы

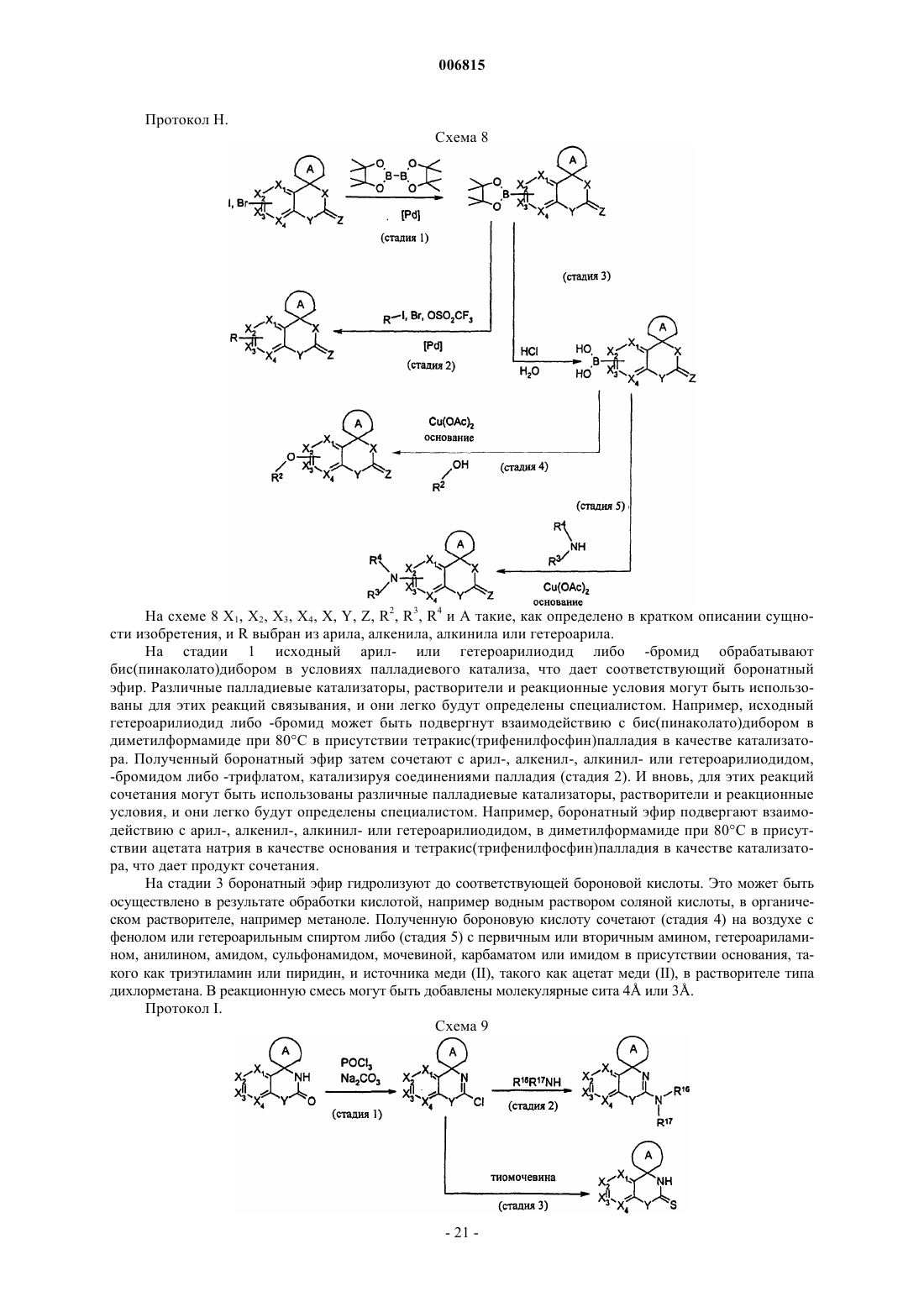
где А такой, как определено в п.1, с получением соединения (2с)
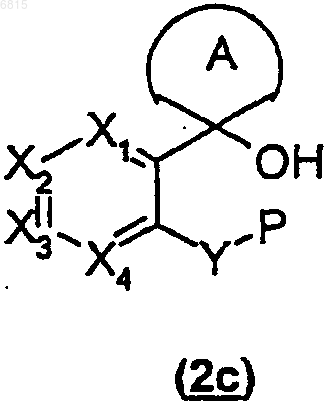
(3) снимают защитную группу Р в любых из условий восстановления, в кислых условиях или в основных условиях с получением соединения (2d)
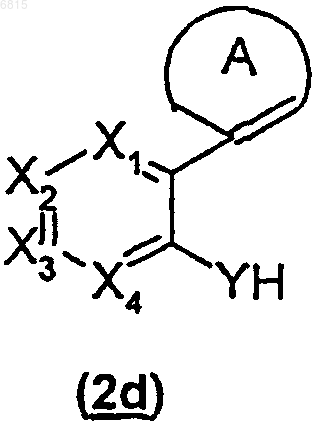
(4) осуществляют взаимодействие соединения (2d) с группой O=C=N-R9, где R9 такой, как определено в п.1, с получением соединения (2е)

(5) осуществляют взаимодействие соединения (2е) с кислотой с получением указанного соединения формулы (I),
(6) выделяют указанное соединение формулы (I).
Текст
006815 Область изобретения Данное изобретение относится к спиротрициклическим производным, способам их получения и их применению в качестве ингибиторов фосфодиэстеразы-7 (PDE7). Предпосылки изобретения Фосфодиэстеразы (PDE) играют важную роль в различных биологических процессах, гидролизуя ключевые вторичные мессенджеры аденозин- и гуанозин-3',5'-циклические монофосфаты (цАМФ и цГМФ, соответственно) до их соответствующих нуклеотид-5'-монофосфатов. Таким образом, ингибирование активности PDE приводит к увеличению внутриклеточных уровней цАМФ и цГМФ, что активирует пути фосфорилирования специфических белков, вовлеченных в ряд функциональных ответов. По меньшей мере одиннадцать изоферментов циклонуклеотид-фосфодиэстераз млекопитающих,пронумерованных от PDE 1 до PDE 11, были охарактеризованы на основе первичной структуры, субстратной специфичности или чувствительности к кофакторам либо к лекарствам на основе ингибиторов. Среди этих фосфодиэстераз PDE7 является цАМФ-специфичной PDE. Определение биохимических и фармакологических характеристик позволило выявить высокоаффинную цАМФ-специфичную PDE(Km=0,2 мкМ), на которую не оказывают никакого действия ингибиторы изофермента PDE с высокой цГМФ-селективностью.PDE7 по активности или содержанию белка детектируется в Т-клеточных линиях, В-клеточных линиях, линиях эпителиальных клеток воздушных путей (АЕ) и некоторых эмбриональных тканях. По-видимому, увеличение уровней цАМФ путем селективного ингибирования PDE7 является возможным многообещающим подходом для специфического блокирования опосредованных Т-клетками иммунных ответов. Дальнейшими исследованиями продемонстрировано, что повышение уровней внутриклеточного цАМФ может модулировать воспалительные и иммунологические процессы. Этот селективный подход предположительно мог бы не иметь побочных эффектов, ассоциированных с известными селективными ингибиторами PDE (например PDE3- или РDЕ 4-селективными ингибиторами), которые ограничивают их применение. Кроме того, раскрыта функциональная роль PDE7 в Т-клеточной активации; поэтому селективные ингибиторы PDE7 следует рассматривать в качестве кандидатов для лечения связанных с Т-клетками заболеваний. АЕ-клетки принимают деятельное участие в воспалительных заболеваниях дыхательных путей путем высвобождения таких медиаторов, как арахидонатные метаболиты и цитокины. Селективное ингибирование PDE7 может быть полезным противовоспалительным подходом для лечения связанных с АЕклетками заболеваний. Таким образом, существует необходимость в селективных ингибиторах PDE7, которые активны в очень низких концентрациях, то есть предпочтительно в наномолярных ингибиторах. В WO 88/01508 описаны соединения формулыR1, R2, R3 и R5 являются водородом или алкилом;R4 и R6 являются водородом, алкилом или аралкилом; а и b равны 0, 1 или 2 и а+b=0, 1 или 2; группы R4 и R5 на соседних углеродных атомах вместе могут образовывать углерод-углеродную двойную связь; и расположенные парами группы R4 и R5 вместе могут образовывать спиро-заместитель,-(CH2)d-, где d равен от 2 до 5; или их фармацевтически приемлемая соль. Эти соединения описаны как кардиотонические средства. В WO 00/66560 описаны соединения формулы Эти соединения описаны как модуляторы рецептора прогестерона. Краткое описание сущности изобретения Согласно данному изобретению предложены спиротрициклические производные, которые являются ингибиторами PDE и, более конкретно, ингибиторами PDE7, имеющие следующую формулу (I): где a) X1, X2, Х 3 и Х 4 одинаковые или различные и выбраны из:Q1 или низшего алкила, низшего алкенила или низшего алкинила, причем эти группы не замещены или замещены одной или несколькими группами Q2; группы X5-R5,где X5 выбран из одинарной связи; низшего алкилена, низшего алкенилена или низшего алкинилена, возможно прерванных 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, причем атомы углерода этих групп не замещены или замещены одной или несколькими группами, одинаковыми или различными, выбранными из SR6,OR6, NR6R7, =O, =S или =N-R6, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила иR5 выбран из арила, гетероарила, циклоалкила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, циклоалкенила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или бициклической группы, причем эти группы не замещены или замещены одной или несколькими группами, выбранными из Q3, гетероарила или низшего алкила, возможно замещенного Q3; где Q1, Q2, Q3 одинаковые или различные и выбраны из водорода, галогена, CN, NO2, SО 3 Н, Р(=O)(ОН)2;OR2, OC(=O)R2, C(=O)OR2, SR2, S(=O)R2, С(=O)-NН-SO2-СН 3, NR3R4, Q-R2, Q-NR3R4, NR2-Q-NR3R4 или NR3-Q-R2, где Q выбран из C(=NR), C(=O), C(=S) или SO2, R выбран из водорода, CN, SO2NH2 или низшего алкила, и R2, R3 и R4 одинаковые или различные и выбраны из водорода,низшего алкила, возможно прерванного С(=O), Q4-арила, Q4-гетероарила, Q4-циклоалкила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или Q4 циклоалкенила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O),SO2 или N,где Q4 выбран из (СН 2)n, низшего алкила, прерванного одним гетероатомом, выбранным из О, S илиN, низшего алкенила или низшего алкинила, причем эти группы возможно замещены низшим алкилом,OR' или NR'R", где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила;n является целым числом, выбранным из 0, 1, 2, 3 или 4; причем эти группы не замещены или замещены одной или несколькими группами, выбранными из низшего алкила, галогена, CN, СН 3, SО 3 Н, SО 2 СН 3, C(=O)-NH-SO2-CH3, СF3, OR6, COOR6, C(=O)R6,NR6R7, NR6C(=O)R7, C(=O)NR6R7 или SO2NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, возможно замещенного одной или двумя группами, выбранными из OR,COOR или NRR8, где R и R8 являются водородом или низшим алкилом, иR6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 48-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8 членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, или низшим алкилом, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, иR' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N; или когда X1 и Х 2 оба представляют собой C-R1, 2 заместителя R1 могут образовывать вместе с атомами углерода, к которым они присоединены, 5-членное гетероциклическое кольцо, содержащее атом азота и возможно второй гетероатом, выбранный из О, S или N; б) Х представляет собой NR9, где R9 представляет собой водород; в) Y представляет собой N-R12, где R12 представляет собой водород; где А 1, А 2, А 4, А 5 и А 6 представляют собой атом углерода;представляет собой атом углерода, который является общим для цикла А и основного цикла, содержащего Х и/или Y; каждый атом углерода в цикле А не замещен или замещен 1 или 2 группами, одинаковыми или различными, выбранными из низшего алкила; 2 атома цикла А, которые не являются соседними, могут быть соединены посредством цепи из 2, 3 или 4 атомов углерода; или их таутомерные формы, их рацемические формы или их изомеры и их фармацевтически приемлемые производные; при этом подразумевается, что низший алкил и низший алкилен означают прямые и разветвленные углеродные цепи, имеющие от 1 до 6 атомов углерода; низший алкенил и низший алкенилен означают прямые и разветвленные углеводородные радикалы,имеющие от 2 до 6 атомов углерода и по меньшей мере одну двойную связь; низший алкинил и низший алкинилен означают прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 атомов углерода и по меньшей мере одну тройную связь; низший галогеноалкил означает низший алкил, как он определен выше, замещенный одним или несколькими атомами галогена; циклоалкил означает насыщенный карбоцикл, содержащий от 3 до 8 атомов углерода; циклоалкенил означает карбоцикл, содержащий от 3 до 10 атомов углерода и по меньшей мере одну двойную связь; арил означает ароматический карбоцикл, содержащий от 6 до 10 атомов углерода; гетероарил означает ароматический цикл, который имеет от 5 до 10 кольцевых атомов, от 1 до 4 из которых независимо выбраны из группы, состоящей из О, S и N; гетероциклическое кольцо включает гетероарил, как он определен выше, и циклоалкил или циклоалкенил, как они определены выше, прерванный 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O),SO2 или N; бициклическая группа означает два цикла, которые являются одинаковыми или различными и выбраны из арила, как он определен выше, гетероциклического кольца, как оно определено выше, циклоалкила, как он определен выше, или циклоалкенила, как он определен выше, конденсированных вместе с образованием указанной бициклической группы. Эти соединения являются селективными ингибиторами PDE7. Их можно применять в качестве лекарств в лечении различных заболеваний, таких как связанные с Т-клетками заболевания, аутоиммунные заболевания, остеоартрит, ревматоидный артрит, рассеянный склероз, остеопороз, хроническая обструктивная болезнь легких (ХОБЛ), астма, рак, синдром приобретенного иммунодефицита (СПИД), аллергия или воспалительное заболевание кишечника (ВЗК). Данное изобретение также относится к способу получения соединений формулы (I), при котором(1) осуществляют взаимодействие соединения (2 а)(2) осуществляют взаимодействие соединения (2b) с R-Li, где R является низшим алкилом, как он определен выше, и затем с кетоном формулы(3) снимают защитную группу Р в любых из условий восстановления, в кислых условиях или в основных условиях с получением соединения (2d)(4) осуществляют взаимодействие соединения (2d) с группой O=C=N-R9, где R9 такой, как определено в п.1, с получением соединения (2 е)(5) осуществляют взаимодействие соединения (2 е) с кислотой с получением соединения формулы (I),(6) выделяют указанное соединение формулы (I). Согласно данному изобретению предложено также применение соединения формулы (I) для приготовления лекарства для предупреждения или лечения расстройств, для которых показана терапия ингибитором PDE7. Согласно данному изобретению предложен также способ лечения расстройства, для которого показана терапия ингибитором PDE7, при котором млекопитающему, нуждающемуся в такой терапии, вводят эффективное количество соединения формулы (I). В предпочтительном воплощении расстройство, для которого показана терапия ингибитором PDE7,выбрано из связанных с Т-клетками заболеваний, аутоиммунных заболеваний, остеоартрита, рассеянного склероза, остеопороза, хронической обструктивной болезни легких, астмы, рака, синдрома приобретенного иммунодефицита, аллергии или воспалительного заболевания кишечника. Согласно данному изобретению предложена также фармацевтическая композиция, содержащая соединение формулы (I) в комбинации с подходящим носителем. Подробное описание изобретения Согласно настоящему изобретению предложены соединения, которые являются ингибиторами где a) X1, Х 2, Х 3 и Х 4 одинаковые или различные и выбраны из-4 006815 низшего алкила, низшего алкенила или низшего алкинила, причем эти группы не замещены или замещены одной или несколькими группами Q2; группы X5-R5, где X5 выбран из одинарной связи; низшего алкилена, низшего алкенилена или низшего алкинилена, возможно прерванных 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, причем атомы углерода этих групп не замещены или замещены одной или несколькими группами, одинаковыми или различными, выбранными из SR6,OR6, NR6R7, =O, =S или =N-R6, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила иR5 выбран из арила, гетероарила, циклоалкила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, циклоалкенила, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или бициклической группы, причем эти группы не замещены или замещены одной или несколькими группами, выбранными из Q3, гетероарила или низшего алкила, возможно замещенного Q3; где Q1, Q2, Q3 одинаковые или различные и выбраны из водорода, галогена, CN, NO2, SО 3 Н, Р(=O)(ОН)2;OR2, OC(=O)R2, C(=O)OR2, SR2, S(=O)R2, С(=O)-NН-SO2-СН 3, NR3R4, Q-R2, Q-NR3R4, NR2-Q-NR3R4 или NR3-Q-R2, где Q выбран из C(=NR), C(=O), C(=S) или SO2, R выбран из водорода, CN, SO2NH2 или низшего алкила, и R2, R3 и R4 одинаковые или различные и выбраны из водорода,низшего алкила, возможно прерванного С(=O), Q4-арила, Q4-гетероарила, Q4-циклоалкила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или Q4 циклоалкенила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O),SO2 или N, гдеQ4 выбран из (СH2)n, низшего алкила, прерванного одним гетероатомом, выбранным из О, S или N,низшего алкенила или низшего алкинила, причем эти группы возможно замещены низшим алкилом, OR' или NR'R", где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила;n является целым числом, выбранным из 0, 1, 2, 3 или 4; причем эти группы не замещены или замещены одной или несколькими группами, выбранными из низшего алкила, галогена, CN, СН 3, SО 3 Н, SO2 СН 3, С(=O)-NН-SO2-СН 3, СF3, OR6, COOR6, C(=O)R6,NR6R7, NR6C(=O)R7, С(=O)NR6R7 или SO2NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, возможно замещенного одной или двумя группами, выбранными из OR,COOR или NRR8, где R и R8 являются водородом или низшим алкилом, иR6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 48-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8 членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, или низшим алкилом, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, иR' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N; или когда X1 и Х 2 оба представляют собой C-R1, 2 заместителя R1 могут образовывать вместе с атомами углерода, к которым они присоединены, 5-членное гетероциклическое кольцо, содержащее атом азота и возможно второй гетероатом, выбранный из О, S или N; б) Х представляет собой NR9, где R9 представляет собой водород; в) Y представляет собой N-R12, где R12 представляет собой водород; г) Z выбран из О, S или NR13, где R13 представляет собой CN; д) А является циклом, выбранным из где А 1, А 2, А 4, А 5 и А 6 представляют собой атом углерода;представляет собой атом углерода, который является общим для цикла А и основного цикла, содержащего Х и/или Y;-5 006815 каждый атом углерода в цикле А не замещен или замещен 1 или 2 группами, одинаковыми или различными, выбранными из низшего алкила; 2 атома цикла А, которые не являются соседними, могут быть соединены посредством цепи из 2, 3 или 4 атомов углерода; или их таутомерные формы, их рацемические формы или их изомеры и их фармацевтически приемлемые производные; при этом подразумевается, что низший алкил и низший алкилен означают прямые и разветвленные углеродные цепи, имеющие от 1 до 6 атомов углерода; низший алкенил и низший алкенилен означают прямые и разветвленные углеводородные радикалы,имеющие от 2 до 6 атомов углерода и по меньшей мере одну двойную связь; низший алкинил и низший алкинилен означают прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 атомов углерода и по меньшей мере одну тройную связь; низший галогеноалкил означает низший алкил, как он определен выше, замещенный одним или несколькими атомами галогена; циклоалкил означает насыщенный карбоцикл, содержащий от 3 до 8 атомов углерода; циклоалкенил означает карбоцикл, содержащий от 3 до 10 атомов углерода и по меньшей мере одну двойную связь; арил означает ароматический карбоцикл, содержащий от 6 до 10 атомов углерода; гетероарил означает ароматический цикл, который имеет от 5 до 10 кольцевых атомов, от 1 до 4 из которых независимо выбраны из группы, состоящей из О, S и N; гетероциклическое кольцо включает гетероарил, как он определен выше, и циклоалкил или циклоалкенил, как они определены выше, прерванный 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O),SO2 или N; бициклическая группа означает два цикла, которые являются одинаковыми или различными и выбраны из арила, как он определен выше, гетероциклического кольца, как оно определено выше, циклоалкила, как он определен выше, или циклоалкенила, как он определен выше, конденсированных вместе с образованием указанной бициклической группы. Предпочтительную группу составляют соединения формулы (I), где a) X1, Х 2 и Х 3 одинаковые или различные и представляют собой C-R1, где R1 выбран из водорода, галогена, CN, SО 3 Н, NO2, CF3, OR2, SR2, NR2R3, COR2, COOR2, CONR2R3, SO2 СН 3,SO2NR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, возможно замещенного галогеном, CN, OR6, COOR6, NR6R7, SO2NR6R7 илиC(=O)NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, и R6 и R7 вместе с атомом азота, к которому они присоединены, могут образовывать 48-членное гетероциклическое кольцо, как оно определено выше; низшего алкила, как он определен выше, низшего алкенила, как он определен выше, или низшего алкинила, как он определен выше, причем эти группы не замещены или замещены 1, 2 или 3 группами,выбранными из галогена, CN, SО 3 Н, OR2, COOR2, NR3R4, SO2NR3R4 или C(=O)NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, иX5 выбран из низшего алкилена, как он определен выше, или одинарной связи иR5 выбран из фенила, пиридила или индолила,причем эти группы не замещены или замещены 1, 2 или 3 группами, выбранными из Q3, гетероарила, как он определен выше, или низшего алкила, как он определен выше, возможно замещенного Q3, гдеQ3 выбран из галогена, CN, SO3 Н, NO2, CF3, OR2, OC(=O)R2, C(=O)R2, C(=O)OR2, NH-C(=O)R2, NR3R4, SO2NR3R4 или C(=O)NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из водорода, низшего алкила, как он определен выше, незамещенного или замещенного одной или несколькими группами, выбранными из галогена, OR6, COOR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, иR6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 48-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено 4-8-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен выше, или низшим алкилом, как он определен выше, возможно замещенным OR', NR'R", C(=O)NR'R" илиCOOR', где R' и R" одинаковые или различные и выбраны из Н или низшего алкила, как он определен выше, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен выше, и R' и R" вместе с атомом азота, к которому они-6 006815 присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N; б) Х 4 представляет собой C-R1, где R1 выбран из водорода, галогена, CN, NO2, SO2 СН 3, SО 3 Н, СН 3,CF3, OR2, SR2, NR2R3, COOR2, CONR2R3 или SO2NR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше; в) Х представляет собой NH; г) Y представляет собой NH; д) Z выбран из О, S или NR13, где R13 представляет собой CN; е) А является циклом, выбранным из где А 1, А 2, А 3, А 4 и А 5 одинаковые или различные и выбраны из атома углерода, незамещенного или замещенного 1 или 2 группами, одинаковыми или различными,выбранными из низшего алкила, как он определен выше;представляет собой атом углерода, который является общим для цикла А и основного цикла, содержащего Х и/или Y; 2 атома цикла А, которые не являются соседними, могут быть соединены посредством цепи из 2, 3 или 4 атомов углерода. Еще одну предпочтительную группу составляют соединения формулы (I), гдеX1, X2, Х 3 и Х 4 одинаковые или различные и представляют собой C-R1, где R1 выбран изQ1 или низшего алкила, низшего алкенила или низшего алкинила, как они определены выше, причем эти группы не замещены или замещены 1, 2 или 3 группами Q2; группы Х 5-R5, гдеX5 выбран из одинарной связи; низшего алкилена, как он определен выше, возможно прерванного 1 гетероатомом, выбранным из О, S и N;R5 выбран из арила, как он определен выше, гетероарила, как он определен выше, циклоалкила, как он определен выше, возможно прерванного С(=O) или 1, 2 либо 3 гетероатомами, выбранными из О, S,S(=O), SO2 или N, циклоалкенила, как он определен выше, возможно прерванного С(=O) или 1, 2 или 3 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или бициклической группы,причем эти группы не замещены или замещены 1, 2 или 3 группами, выбранными из Q3, гетероарила, как он определен выше, или низшего алкила, как он определен выше, возможно замещенного Q3; где Q1, Q2, Q3 одинаковые или различные и выбраны из водорода, галогена, CN, NO2, SО 3 Н,OR2, OC(=O)R2, C(=O)OR2, SR2, S(=O)R2, C(=O)-NH-SO2-CH3, NR3R4, Q-R2, Q-NR3R4, NR2-Q-NR3R4 или NR3-Q-R2, где Q выбран из C(=NR), C(=O), C(=S) или SO2, R выбран из водорода или низшего алкила, и R2, R3 и R4 одинаковые или различные и выбраны из водорода,низшего алкила, как он определен выше, возможно прерванного С(=O), Q4-арила, как он определен выше, Q4-гетероарила, как он определен выше, Q4-циклоалкила, как он определен выше, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, или Q4 циклоалкенила, как он определен выше, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S, S(=O), SO2 или N, гдеQ4 выбран из (СН 2)n, низшего алкила, как он определен выше, прерванного одним гетероатомом,выбранным из О, S или N, низшего алкенила, как он определен выше, или низшего алкинила, как он определен выше, причем эти группы возможно замещены низшим алкилом, как он определен выше, OR' или NR'R", где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше;n является целым числом, выбранным из 0, 1, 2, 3 или 4; причем эти группы не замещены или замещены 1 или 2 группами, выбранными из низшего алкила,как он определен выше, галогена, CN, СН 3, SО 3 Н, SO2 СН 3, СF3, С(=O)NН-SO2 СН 3, OR6, COOR6, C(=O)R6,NR6R7, C(=O)NR6R7 или SO2NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, возможно замещенного одной или двумя группами, выбранными из OR, COOR или NRR8, где R и R8 являются водородом или низшим алкилом, как он определен выше, иR6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 48-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SО 2 или N, и которое может быть замещено(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8 членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен выше, или низшим алкилом, как он определен выше, возможно замещенным OR', NR'R", C(=O)NR'R" илиCOOR', где R' и R" одинаковые или различные и выбраны из Н или низшего алкила, как он определен выше, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен выше, иR' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N. В более предпочтительном воплощении X1, X2, Х 3 и Х 4 одинаковые или различные и представляют собой C-R1, где R1 выбран изQ1 или низшего алкила или низшего алкинила, причем эти группы такие, как определено выше, и не замещены или замещены 1, 2 или 3 атомами фтора, OR3, COOR3 или NR3R4, где R3 и R4 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше;R3 и R4 вместе с атомом азота, к которому они присоединены, могут также образовывать 6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N; группы X5-R5, где X5 представляет собой одинарную связь, и R5 выбран из арила, гетероарила или бициклической группы, причем эти группы такие, как определено ввыше, и не замещены или замещены 1, 2 или 3 группами, выбранными из Q3, где Q1 и Q3 одинаковые или различные и выбраны из водорода, галогена, CN, низшего алкила, как он определен выше,OR2, C(=O)OR2, NR3R4, C(=O)NR3R4 или SO2NR3R4, где R2, R3 и R4 одинаковые или различные и выбраны из водорода,низшего алкила, как он определен выше, Q4-гетероарила, где Q4 выбран из низшего алкила, прерванного одним гетероатомом, выбранным из О, S или N, и (СН 2)n, где n является целым числом, выбранным из 0, 1, 2 или 3, и где гетероарил такой, как определено выше; причем эти группы не замещены или замещены 1 или 2 группами, выбранными из низшего алкила,CN, SО 3 Н, С(=O)-NН-SO2-СН 3, OR6, COOR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, возможно замещенного одной или двумя группами, выбранными из OR, COOR или NRR8, где R и R8 являются водородом или низшим алкилом,как он определен выше, иR6 и R7 и/или R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 46-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено 6-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено низшим алкилом, или низшим алкилом, как он определен выше, возможно замещенным OR', NR'R", C(=O)NR'R" илиCOOR', где R' и R" одинаковые или различные и выбраны из Н или низшего алкила, как он определен выше, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен выше, иR' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N. В другом более предпочтительном воплощении X1 представляет собой С-R1, где R1 выбран из: водорода, галогена, OR2, COR2, COOR2, CONR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода,низшего алкила, как он определен выше, Q4-арила, Q4-гетероарила, Q4-циклоалкила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S или N, или Q4-циклоалкенила, возможно прерванного С(=O) либо 1 или 2 гетероатомами, выбранными из О, S или N,где Q4 выбран из (СН 2)n, низшего алкила, как он определен выше, прерванного одним гетероатомом, выбранным из О, S или N, низшего алкенила, как он определен выше, или низшего алкинила, как он определен выше; арил, гетероарил, циклоалкил и циклоалкенил такие, как определено выше;-8 006815 причем эти группы не замещены или замещены низшим алкилом, CN, OR6, SО 3 Н, С(=O)-NН-SO2 СН 3, CONR6R7, COOR6, COR6 или NR6R7, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, возможно замещенного NH2, СООН, ОН;R6 и R7 вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N,и которое может быть замещено(CH2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8 членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен выше, илиCOR' или низшим алкилом, как он определен выше, возможно замещенным OR', NR'R",C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше; низшего алкила, как он определен выше, возможно замещенного CN, SО 3 Н, OR3, NR3R4, COOR3 или CONR3R4, где R3 и R4 одинаковые или различные и выбраны из водорода и низшего алкила, как он определен выше, возможно замещенного ОН, СООН или NH2,группы X5-R5, где X5 является низшим алкиленом, как он определен выше, возможно прерванным гетероатомом, выбранным из О и N, и R5 выбран из арила, как он определен выше, гетероарила, как он определен выше, циклоалкила, как он определен выше, возможно прерванного С(=O) либо 1, 2 или 3 гетероатомами, выбранными из О, S или N, и циклоалкенила, как он определен выше, возможно прерванного С(=O), либо 1, 2 или 3 гетероатомами, выбранными из О, S или N,причем эти группы не замещены или замещены OR3 или COOR3, где R3 выбран из водорода и низшего алкила, как он определен выше;R3 и R4 вместе с атомом азота, к которому они присоединены, могут образовывать 4-6-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О или N, и которое может быть замещено(СН 2)n-Q5, где n является целым числом, выбранным из 0, 1, 2 и 3, и Q5 представляет собой 4-8 членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен выше, илиC(=O)-R' или низшим алкилом, возможно замещенным OR', NR'R", C(=O)NR'R" или COOR', где R' и R" одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше. Еще в одном более предпочтительном воплощении X1 представляет собой C-R1, где R1 выбран из водорода, галогена или OR2, где R2 выбран из водорода,низшего алкила, как он определен выше, незамещенного или замещенного CN, С(=O)-NН-SO2-СН 3,OR6, SO3 Н, COOR6 или NR6R7,Q4-оксадиазола, Q4-тетразола, Q4-морфолина, Q4-фурана, Q4-изоксазола, где Q4 выбран из низшего алкила, как он определен выше, прерванного одним гетероатомом, выбранным из О, S или N, и (СН 2)n,где n является целым числом, выбранным из 1 и 2; причем эти группы не замещены или замещены СН 3, OR6 или COOR6, где R6 и R7 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше, возможно замещенногоNH2 или СООН. Еще в одном более предпочтительном воплощении Х 2 представляет собой C-R1, где R1 представляет собой X5-R5,где X5 представляет собой одинарную связь,R5 представляет собой фенил или пиридил,возможно замещенный низшим алкилом, как он определен выше, и замещенный C(=O)NR3R4, где R3 и R4 вместе с атомом азота, к которому они присоединены, образуют 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S, S(=O), SO2 или N, и которое может быть замещено 4-8-членным гетероциклическим кольцом, которое может содержать один или два гетероатома, выбранные из О, S или N, и которое может быть замещено низшим алкилом, как он определен выше, или низшим алкилом, как он определен выше, возможно замещенным OR', NR'R", C(=O)NR'R" илиCOOR', где R' и R" одинаковые или различные и выбраны из Н или низшего алкила, как он определен выше, возможно замещенного OR или COOR, где R является водородом или низшим алкилом, как он определен выше, иR' и R" вместе с атомом азота, к которому они присоединены, могут образовывать 4-8-членное гетероциклическое кольцо, которое может содержать один или два гетероатома, выбранные из О, S или N. Предпочтительно, один из X1, Х 2, Х 3 и Х 4 представляет собой C-R1, где R1 является водородом, а остальные являются одинаковыми или различными и представляют собой C-R1, где R1 отличен от водорода. Предпочтительно, Х 3 представляет собой C-R1, где R1 является водородом.-9 006815 В другом предпочтительном воплощении Х 3 представляет собой C-R1, где R1 выбран из водорода или галогена илиX5-R5, где X5 представляет собой одинарную связь, и R5 является арилом, как он определен выше,или гетероарилом, как он определен выше, возможно замещенными одной, двумя или тремя группами,которые являются одинаковыми или различными и выбраны из галогена, CN, СF3, SO2Me, OR2, COOR2,NR2R3, SO2NR2R3 и CONR2R3, где R2 и R3 одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше. Предпочтительно, Х 3 представляет собой C-R1, где R1 выбран из водорода или галогена. Еще в одном предпочтительном воплощении Х 4 представляет собой С-R1, где R1 выбран из водорода, галогена, СF3, O-низшего алкила (причем низший алкил такой, как определено выше),COOR2 или низшего алкила, как он определен выше, возможно замещенного OR2, COOR2 или SO2NR2R3, где R2 3 и R одинаковые или различные и выбраны из водорода или низшего алкила, как он определен выше. Предпочтительно, Z представляет собой О. Предпочтительно, А выбран из циклогексила или циклогептила, незамещенных или замещенных СН 3. Более предпочтительно, А выбран из незамещенных циклогексила или циклогептила. В следующем далее и приведенном выше тексте: галоген включает в себя фторо, хлоро, бромо и иодо. Предпочтительными галогенами являются F и Сl; низший алкил включает в себя прямые и разветвленные углеродные цепи, имеющие от 1 до 6 углеродных атомов. Примеры таких алкильных групп включают в себя метил, этил, изопропил, трет-бутил и им подобные; низший алкенил включает в себя прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 углеродных атомов и по меньшей мере одну двойную связь. Примеры таких алкенильных групп включают в себя этенил, 3-бутен-1-ил, 2-этенилбутил, 3-гексенил и им подобные; низший алкинил включает в себя прямые и разветвленные углеводородные радикалы, имеющие от 2 до 6 углеродных атомов и по меньшей мере одну тройную связь. Примеры таких алкинильных групп включают в себя этинил, 3-бутин-1-ил, пропинил, 2-бутин-1-ил, 3-пентил-1-ил и им подобные; низший галогеноалкил включает в себя низший алкил, как он определен выше, замещенный одним или несколькими атомами галогена. Предпочтительным галогеноалкилом является трифторметил. Очевидно, что арил относится к ароматическому карбоциклу, содержащему от 6 до 10, предпочтительно 6, атомов углерода. Предпочтительной арильной группой является фенил. Гетероарил включает в себя ароматические циклы, которые имеют от 5 до 10 кольцевых атомов, от 1 до 4 из которых независимо выбраны из группы, состоящей из О, S и N. Предпочтительные гетероарильные группы имеют 1, 2, 3 или 4 гетероатома в 5- или 6-членном ароматическом кольце. Примерами таких групп являются тетразол, пиридил, тиенил и им подобные. Предпочтительный циклоалкил содержит от 3 до 8 атомов углерода. Примерами таких групп являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Термин прерванный означает, что в основной цепи атом углерода заменен гетероатомом или группой, как они здесь определены. Например, во фразе циклоалкил или циклоалкенил, возможно прерванный С(=O) или 1 гетероатомом, выбранным из О, S, S(=O), SO2 или N, термин прерванный означает, что С(=O) или гетероатом может заменять кольцевой атом углерода. Примерами таких групп являются морфолин или пиперазин. Циклоалкенил включает в себя 3-10-членный циклоалкил, содержащий по меньшей мере одну двойную связь. Гетероциклическое кольцо включает в себя гетероарил, как он определен выше, и циклоалкил или циклоалкенил, как они определены выше, прерванные 1, 2 или 3 гетероатомами, выбранными из О, S,S(=O), SО 2 или N. Бициклические заместители относятся к двум циклам, одинаковым или различным и выбранным из арила, гетероциклического кольца, циклоалкила или циклоалкенила, сконденсированных вместе с образованием указанных бициклических заместителей. Предпочтительным бициклическим заместителем является индолил. Конкретными предпочтительными соединениями являются: спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,спиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,7'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-фенилспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-xлopocпиpo[циклoгeкcaн-1-4'-(3',4'-дигидpo)xинaзoлин]-2'(1'H)-oн,7'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,- 10006815 6'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-бромоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-фтороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5',8'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6',7'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5',6'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-фенилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-иодоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-бромоспиро[циклобутан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-бромоспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-бромо-4-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-бpoмocпиpo[бициклo[3,2,1]oктaн-2-4'-(3',4'-дигидpo)xинaзoлин]-2'(1'H)-он,6',8'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-иодоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-фенилспиро[циклогептан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-фенилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-xлopo-6'-мeтилcпиpo[циклoгeкcaн-1-4'-(3',4'-дигидpo)xинaзoлин]-2'(1'H)-он,8'-хлоро-6'-(3-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-(4-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-(4-карбоксифенил)-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1 'Н)-он,6'-(3-карбоксифенил)-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-(1 Н-индол-5-ил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-(2-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'H)-oн,8'-хлоро-6'-(3-диметиламино-проп-1-инил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-(3-метиламино-проп-1-инил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(4-метил-пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(3-N-диметиламино-пропилкарбоксамид)фенил]спиро-[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(2-N-диметиламиноэтилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[3-(3-N-диметиламинопропилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[3-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[3-(2-N-диметиламиноэтилкарбоксамид)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-тион,8'-хлоро-2'-цианоиминоспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин],8'-хлоро-6'-[4-(4-пиримидин-2-ил-пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(4-(2-морфолин-4-ил-этил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(4-(2-морфолин-4-ил-2-оксоэтил)пиперазин-1-карбонил)фенил]спиро[циклогексан-14'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(4-(2-гидроксиэтоксиэтил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'дигидро)хиназолин]-2'(1'Н)-он,спиро[циклогексан-1-9'-(8',9'-дигидро)пиразоло[4',3'-f]хиназолин]-7'(6'Н)-он,8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5',8'-дифтороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-она,8'-хлоро-5'-метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-(морфолин-4-ил)метилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-гидроксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-гидрокси-6'-иодоспиро[цикпогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-иодо-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-циано-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[2-(4-морфолино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[2-диметиламиноэтокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(2-аминоэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[2-(метиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,- 11006815 8'-хлоро-5'-[2-(2-аминоэтокси)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[3-диметиламинопропокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-этоксикарбонилметоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5'-карбоксиметокси-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,5'-карбоксипропокси-8'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(3-сульфопропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[2-(тетрагидропиран-2-илокси)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-он,8'-хлоро-5'-(2-гидроксиэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(5-этоксикарбонилфуран-2-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(5-карбоксифуран-2-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-он,8'-хлоро-5'-цианометоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(1 Н-тетразол-5-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(5-гидрокси-[1,2,4]оксадиазол-3-илметокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'H)-он,8'-хлоро-6'-иодо-5'-[2-диметиламиноэтокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-он,6'-(4-карбоксифенил)-8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,6'-(3-карбоксифенил)-8'-хлоро-5'-метоксиспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[2-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[2-метил-4-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-(пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-он,8'-хлоро-6'-[4-карбамоилфенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-[4-1-метилпиперидин-4-ил)пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-метокси-6'-[4-(4-метил-пиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-трифторметилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-6'-цианометилспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(3-диметиламино-2-гидроксипропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(3-метиламино-2-гидроксипропокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-он,8'-хлоро-5'-[2-(этоксикарбонилметиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-[2-(карбоксиметиламино)этокси]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]2'(1'Н)-она гидрохлорид,8'-хлоро-5'-(2-метансульфониламино-2-оксоэтокси)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он,8'-хлоро-5'-(2-[(5-метил-изоксазол-3-илметил)амино]этокси)спиро[циклогексан-1-4'-(3',4'-дигидро) хиназолин]-2'(1'Н)-он. Общий способ получения соединений по изобретению Согласно одному способу получения соединения формулы (I), определенного выше, где Y представляет собой N-R12, Х представляет собой NR9, и Z представляет собой О, осуществляют взаимодействие замещенной мочевины формулы где Х 1, Х 2, Х 3, Х 4, R9 и R12 такие, как определено в кратком описании сущности изобретения, с циклическим кетоном формулы- 12006815 где А такой, как определено в кратком описании сущности изобретения, с получением указанного соединения формулы (I). Согласно альтернативному способу получения соединения формулы (I), где Х представляет собойN-R9, Y представляет собой NH, и Х 1, Х 2, Х 3, Х 4, А и R9 такие, как определено в кратком описании сущности изобретения,(1) осуществляют взаимодействие соединение (2 а) где X1, X2, Х 3, Х 4 такие, как определено в кратком описании сущности изобретения, и Y представляет собой NH, с группой P-LG, где Р является защитной группой и LG является уходящей группой, с получением соединения (2b)(2) осуществляют взаимодействие соединения (2b) с R-Li, где R является низшим алкилом, как он определен выше, и затем с кетоном формулы где А такой, как определено в кратком описании сущности изобретения, с получением соединения (2 с)(3) снимают защитную группу Р в любых из условий восстановления, в кислых условиях или в основных условиях с получением соединения (2d)(4) осуществляют взаимодействие соединения (2d) с группой O=C=N-R9, где R9 такой, как определено в кратком описании сущности изобретения, с получением соединения (2 е)(5) осуществляют взаимодействие соединения (2 е) с кислотой с получением указанного соединения формулы (I),(6) выделяют указанное соединение формулы (I).- 13006815 Согласно альтернативному способу получения соединения формулы (I), где Х представляет собойN-R9, Y представляет собой N-R12, Z представляет собой О, S или N-R13, X1, Х 2, Х 3, Х 4, А, R9, R12 и R13 такие, как определено в кратком описании сущности изобретения,(1) осуществляют взаимодействие соединение (2d) где Х 1, X2, Х 3, Х 4 и А такие, как определено выше, с группой LG-C(=X)Z' или X=C=Z', где LG является уходящей группой, Х представляет собой N-R9, Z' представляет собой OR, SR или NR13, где R является низшим алкилом или бензилом, и R9 и R13 такие, как определено в кратком описании сущности изобретения, с получением соединения (2'е)(2) осуществляют взаимодействие соединения (2'е) с источником галония с получением соединения (2'f)(3) восстанавливают соединение (2'f) с получением указанного соединения формулы (I),(4) возможно, когда Z' представляет собой OR или SR, осуществляют гидролиз или гидрогенолиз соединения (2'f) с получением указанного соединения формулы (I), где Z представляет собой О или S, и(5) выделяют указанное соединение формулы (I). Соединения по изобретению включают фармацевтически приемлемые производные соединений формулы (I), такие как сольваты, гидраты, фармацевтически приемлемые соли и полиморфы (дескрипторы различных форм кристаллической решетки). Фармацевтически приемлемые соли соединения формулы (I) включают соли, имеющие основную часть, и соли, имеющие кислотную часть. Следует понимать, что выражение фармацевтически приемлемая соль соединения формулы (I),имеющая основную часть, относится к солям соединений формулы (I), которые могут быть образованы присоединением нетоксичных неорганических или органических кислот, таким как, например, соли бромисто-водородной, соляной, серной, фосфорной, азотной, уксусной, янтарной, винной, лимонной, малеиновой, гидроксималеиновой, бензойной, фумаровой и толуолсульфоновой кислот и им подобные. Различные четвертичные аммониевые соли соединений формулы (I) также включены в эту категорию соединений по изобретению. Выражение фармацевтически приемлемая соль соединения формулы (I), имеющая кислотную часть, относится к обычным солям соединений формулы (I), которые могут быть образованы с нетоксичными неорганическими или органическими основаниями, такими как, например, гидроксиды щелочных металлов и щелочно-земельных металлов (натрия, калия, магния и кальция), амины (дибензилэтилендиамин, триметиламин, пиперидин, пирролидин, бензиламин и им подобные) или, альтернативно, гидроксиды четвертичного аммония, такие как тетраметиламмонийгидроксид (см. также Pharmaceutical saltsBerge S.M. et al. (1997) J. Pharm. Sci. 66: 1-19, которая введена сюда посредством ссылки). Кроме того, предусмотрено применение пролекарства соединения по изобретению, которое может быть осуществлено специалистом в данной области техники (смотри Bundgaard, et al., Acta. Pharm. Suec.,1987; 24: 233-246). Фармацевтические композиции Продукты по изобретению вводят в форме композиций, соответствующих природе и серьезности заболевания, которое лечат. Как правило, суточная доза для людей находится в пределах от 1 мг до 1 г продукта, которая может быть принята в виде одной или более чем одной индивидуальной дозы. Компо- 14006815 зиции готовят в формах, совместимых с предполагаемым путем введения, таких как, например таблетки,таблетки с покрытием, капсулы, жидкости для полоскания рта, аэрозоли, порошки для ингаляции, суппозитории, клизмы, губки (например ректальные губки), гели или суспензии. Эти композиции готовят способами, известными специалистам в данной области техники, и они включают в себя от 0,5 до 60 мас.% активного начала (соединения по изобретению) и от 40 до 99,5 мас.% фармацевтического наполнителя или носителя, который является подходящим и совместим с активным началом и физической формой предполагаемой композиции. Препараты в твердой форме включают порошки, таблетки, диспергируемые гранулы, капсулы, облатки и суппозитории. Твердым носителем может быть одно или более чем одно вещество, которое также может действовать как разбавитель, корригент, солюбилизатор, смазывающее вещество, суспендирующий агент, связующее вещество или разрыхлитель таблеток; им также может быть инкапсулирующий материал. В порошках носитель является тонко измельченным твердым веществом, которое находится в смеси с тонко измельченным активным компонентом. В таблетках активный компонент смешан с носителем, имеющим необходимые связывающие свойства, в подходящих пропорциях и спрессован до желаемой формы и размера. Порошки, таблетки, облатки или инкапсулированные формы для капсул предпочтительно содержат от 5 до 70% активного компонента. Подходящими носителями являются карбонат магния, стеарат магния, тальк, лактоза, сахар, пектин, декстрин, крахмал, трагакант, метилцеллюлоза, натрий карбоксиметилцеллюлоза, легкоплавкий воск, масло какао и им подобные. Таблетки, порошки, облатки и капсулы могут быть использованы в виде твердых лекарственных форм, подходящих для перорального введения. Лекарство может доставляться в виде спрея (либо в находящемся под давлением контейнере, оснащенном соответствующим клапаном, либо в не находящемся под давлением контейнере, оборудованном дозирующим клапаном). Препараты в жидкой форме включают в себя растворы, суспензии и эмульсии. В качестве примера препаратов в жидкой форме, подходящих для парентерального введения, могут быть упомянуты стерильные водные и водно-пропиленгликолиевые растворы активных соединений. Кроме того, препараты в жидкой форме могут быть изготовлены в виде раствора в воднопропиленгликолиевом растворе. Водные растворы для перорального введения могут быть приготовлены путем растворения активного компонента в воде и добавления подходящих красителей, корригентов, стабилизаторов и загущающих агентов, как будет желательно. Водные суспензии для перорального применения могут быть изготовлены путем диспергирования тонко измельченного активного компонента в воде вместе с вязким материалом, таким как натуральные синтетические камеди, смолы, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и другие суспендирующие агенты, известные в технологии изготовления фармацевтических препаратов. Для получения препаратов в виде суппозиториев сначала расплавляют легкоплавкий воск, такой как смесь глицеридов жирных кислот и масла какао, и в нем диспергируют активный ингредиент, например путем перемешивания. Затем расплавленную гомогенную смесь выливают в формы удобного размера и оставляют охладиться и отвердеть. Клизмы готовят согласно известным методикам приготовления растворов, адаптированных для ректального введения. Губки готовят согласно известным способам (эти губки могут быть подобны губкам, используемым для введения лекарства, такого как 5-ASA для лечения ректоколита). Фармацевтический препарат предпочтительно находится в стандартной лекарственной форме. Препарат в такой форме разделен на стандартные дозы, содержащие соответствующие количества лекарственного средства. Стандартная лекарственная форма может представлять собой упакованный препарат,при этом упаковка содержит дискретные количества препарата, например упакованные таблетки, капсулы и порошки во флаконах или ампулах. Кроме того, стандартная лекарственная форма может представлять собой капсулу, облатку или саму таблетку либо она может представлять собой соответствующее количество любых из этих упакованных форм. Способы лечения Соединения по изобретению являются ингибиторами PDE и, в частности, ингибиторами PDE7. Эти соединения имеют низкие значения IC50, обычно самое большее 5 мкМ, предпочтительно ниже 1 мкМ и даже ниже 100 нМ. Согласно изобретению показано, что соединения по изобретению являются селективными ингибиторами PDE7. Фраза селективные ингибиторы PDE7 относится к соединению, которое имеет IC50 дляPDE7 по меньшей мере в 5 раз ниже, чем IC50 для PDE, отличной от PDE7, и предпочтительно по меньшей мере в 10 раз, 15 раз, 20 раз, 30 раз, 40 раз, 50 раз или 100 раз ниже, чем IC50 для PDE, отличной от PDE7.PDE, отличная от PDE7, предпочтительно относится к PDE, выбранной из PDE1, PDE3, PDE4 или PDE5. В частности, согласно изобретению показано, что соединения по изобретению и, более конкретно,семейство соединений, представленных в качестве примеров в настоящем описании, имеют значение IC50 для фермента PDE7, которое часто в 100 раз ниже, чем значение своих IC50 для PDE, отличной от PDE7,в частности PDE1, PDE3, PDE4 или PDE5.- 15006815 Соединения по изобретению могут быть использованы для лечения различных заболеваний, поскольку они могут модулировать воспалительные и иммунологические процессы посредством увеличения уровней внутриклеточного цАМФ. Заболеваниями, которые могут быть подвергнуты лечению, являются связанные с Т-клетками заболевания, связанные с АЕ-клетками заболевания и иммунные нарушения, такие как аутоиммунные заболевания, остеоартрит, ревматоидный артрит, рассеянный склероз, остеопороз, астма, ХОБЛ, рак, СПИД,воспаление, аллергия и различные воспалительные расстройства, такие как, например воспалительное заболевание кишечника (ВЗК). И наконец, данное изобретение относится к способу лечения вышеупомянутых заболеваний, при котором млекопитающему, в частности человеку, нуждающемуся в таком лечении, вводят эффективное количество соединения по изобретению. Методики синтеза соединений общей формулы (I) Соединения по настоящему изобретению могут быть получены путем осуществления нескольких методик синтеза. Некоторые из этих методик синтеза (протоколы A-L) описаны ниже. Растворитель, продолжительность реакции, температура, катализатор, если он имеется, могут варьироваться на всех описанных ниже стадиях для всех способов, что очевидно специалисту. Протокол А. Схема 1 На схеме 1 Х 1, Х 2, Х 3, Х 4, A, R9 и R12 такие, как определено в кратком описании сущности изобретения. Исходные материалы либо имеются в продаже, либо могут быть получены способами, известными специалисту. Если исходной мочевины стадии 3 нет в продаже, то она может быть получена путем обработки соответствующего изоцианата первичным амином в растворителе, таком как тетрагидрофуран(стадия 1), или обработки соответствующего анилина замещенным изоцианатом в органическом растворителе, таком как дихлорметан или ацетонитрил (стадия 2). На стадии 3 мочевину превращают в желаемый хиназолинон путем взаимодействия с циклическим кетоном в полифосфорной кислоте при 80-130 С. Протокол В. Схема 2- 16006815 На схеме 2 X1, Х 2, Х 3, Х 4, А и R9 такие, как определено в кратком описании сущности изобретения,Y представляет собой NH, LG является уходящей группой, и R является низшим алкилом. Исходные материалы либо имеются в продаже, либо могут быть получены способами, известными специалисту. На стадии 1 соединение (2 а) подвергают взаимодействию с диалкил-карбамоилхлоридом с образованием желаемого N,N-диалкилкарбамата или тиокарбамата способами, известными специалисту. Смотри Poirier, M.; Simard, М.; Wuest, J.D.; Organometallics, 1996, 15 (4), 1296-1300. Могут быть использованы и другие защитные группы, например группы прямого металлирования на основе кислорода, такие как ОМе, ОМОМ, ОР(ОR2), OPO(NMe)2 (см. Snieckus, Chem. Rev., 1990, 90,879-933). Анилиновое производное защищают как трет-бутилкарбамат или пивалоиламид согласно способам,известным специалисту (см. Tet. Lett., 1994, 35(48), 9003-9006). На стадии 2 соединение (2b) превращают в его литиевую соль (когда Y представляет собой О или S) или в его дилитиевую соль в результате взаимодействия с избытком образующего литиевое соединение агента, такого как mpem-бутиллитий, в комбинированном растворе безводного эфира (например диэтилового эфира и тетрагидрофурана) и алкана (например, пентана) и приводят во взаимодействие с соответствующим кетоном. Взаимодействие осуществляют при низкой температуре (между -78 и 0 С), что дает ожидаемый третичный спирт. Литийорганическое промежуточное соединение также может быть образовано в результате обмена галоген-металл. Кроме того, литийорганическое соединение может быть трансметаллировано в другой металлоорганический реагент, такой как церат (например с использованием безводного трихлорида церия) перед обработкой кетоном. На стадии 3 защитную группу удаляют согласно методикам, известным специалисту, в любых из условий восстановления (когда Y=O-Р или S-P), в кислых условиях или в основных условиях с получением соединения (2d). На стадии 4 соединение (2d) приводят во взаимодействие с соответствующим замещенным изоцианатом с целью получения соединения (2 е). На стадии 5 обработка соединения (2 е) кислотой (минеральной кислотой или кислотой Льюиса) инициирует циклизацию, что дает соединение (2f). Протокол В'. Схема 2'- 17006815 На схеме 2' Х 1, Х 2, Х 3, Х 4 и А такие, как определено в кратком описании сущности изобретения, Y представляет собой NR12, Х представляет собой NR9, и LG является уходящей группой, Z' может представлять собой OR, SR или NR13, Hal является галогеном, Z2 может представлять собой О или S, и гдеR12, R13 и R9 такие, как определено в кратком описании сущности изобретения, и R является алкилом или бензилом. На стадии 1 промежуточное соединение 2d, полученное согласно протоколу В, подвергают взаимодействию либо с карбонильным производным, таким как карбонат, хлорформиат, изоцианат; тиокарбонильным производным, таким как изотиоцианат, тионохлорформиат, либо с другими производными,такими как цианамид, нитрат 3,5-диметил-1 Н-пиразол-1-карбоксимидамида, S-метилизотиомочевина или эквивалентные. Альтернативно, как показано на стадии 1', промежуточное соединение 2'е может быть получено в две стадии путем обработки 2d либо цианогенбромидом, либо карбонильным (или тиокарбонильным) производным, активированным двумя уходящими группами, такими как фосген (или тиофосген), 1,1'-карбонилдиимидазол (или 1,1'-тиокарбонилдиимидазол), нитрофенилхлорформиат или дисульфид углерода, с последующим добавлением нуклеофила, такого как амин, спирт или тиол, для введенияZ'. Соответствующие условия реакции для каждого способа легко могут быть определены специалистом. При желании некоторые полученные промежуточные соединения 2'е могут быть преобразованы в другие промежуточные соединения 2'е согласно способам, известным специалисту. Например, промежуточное соединение тиомочевина 2'е, где Y=NH, Х=S и Z'=NH2, может быть обработано алкилгалогенидом R-X согласно известным специалисту реакционным условиям с получением промежуточного соединения 2'e,где Y=NH, Х=NH и Z'=SR. На стадии 2 промежуточное соединение 2'е обрабатывают источником галония, таким как иод, Nиодсукцинимид, бром или N-бромсукцинимид, что дает промежуточное соединение 2'f. Подобно 2'е промежуточное соединение 2'f может быть преобразовано в разнообразные другие промежуточные соединения 2'f согласно способам, известным специалисту. Галогенид 2'f может быть восстановлен до 2'g,как показано на стадии 3, в известных специалисту реакционных условиях, как например обработкой гидридом триалкилолова и инициатором образования радикалов, аналогичным азобисизобутиронитрилу(AIBN), в инертном органическом растворителе. Альтернативно, как показано на стадии 2', промежуточное соединение 2'е может быть непосредственно превращено в 2'g путем обработки кислотой согласно условиям, которые могут быть определены специалистом. Кроме того, при необходимости промежуточное соединение 2'g может быть преобразовано в разнообразные Другие промежуточные соединения 2'g согласно способам, известным специалисту. Когда Z' представляет собой OR или SR, промежуточное соединение 2'g может быть превращено в 2'h, как показано на стадии 4. Это может быть выполнено согласно условиям, известным специалисту, в результате гидролиза в водно-кислотной среде или гидрогенолиза, когда R является бензилом. Протокол С. Схема 3- 18006815 На схеме 3 X1, Х 2, Х 3, Х 4 и А такие, как определено в кратком описании сущности изобретения, R9 является алкилом, арилом, алкилсульфонилом или арилсульфонилом, R является низшим алкилом и Y может представлять собой О, S или NH. Альтернативный способ получения соединения по изобретению показан ниже, и он осуществляется посредством взаимодействия литийорганического промежуточного соединения с имином. На стадии 1 соединение (3 а) превращают в его дилитиевую соль (когда Y представляет собой NH) в результате взаимодействия с избытком образующего литиевое соединение агента, такого как тpeтбутиллитий, в комбинированном растворе безводного эфира (например, диэтилового эфира и тетрагидрофурана) и алкана (например, пентана). Полученное литийорганическое соединение подвергают взаимодействию с соответствующим имином при низкой температуре, что дает ожидаемый третичный амин(3b). Кроме того, литийорганическое соединение может быть трансметаллировано в другой металлоорганический реагент, такой как церат (например с использованием безводного трихлорида церия), перед обработкой кетоном. На стадии 2 защитную группу удаляют согласно методикам, известным специалисту, в любых из условий восстановления, в кислых условиях или в основных условиях, с получением соединения (3 с). Когда R9 является алкилом или арилсульфонилом, защита этой группы может быть снята с образованиемNН-производного восстановительными способами или гидролизом согласно способам, известным специалисту. На стадии 3 соединение (3 с) подвергают взаимодействию с соединением, выбранным из галогенангидрида угольной кислоты, такого как диэфир фосгена и угольной кислоты, 1,1'-карбонилдиимидазола и так далее, с целью получения соединения (3d). На стадии 4 соединение (3 с) подвергают взаимодействию с ортоэфиром в присутствии кислоты с целью получения соединения (3 е) или его таутомерных форм. Протокол D. Схема 4 На схеме 4 Х 1, Х 2, Х 3, Х 4, A, R9 и R12 такие, как определено в кратком описании сущности изобретения, Z представляет собой О или S. Исходные материалы либо имеются в продаже, либо могут быть получены согласно способам, известным специалисту. На стадии 1 исходную антраниловую кислоту обрабатывают фосгеном или эквивалентным источником карбонила, таким как трифосген или карбонилдиимидазол. Могут быть использованы различные растворители и реакционные условия, и они легко будут определены специалистом. Полученный изатоевый ангидрид обрабатывают реагентом Гриньяра, полученным из дигалогенида и магния в растворителе, таком как тетрагидрофуран или эфир (стадия 2). На стадии 3 анилин превращают в мочевину обработкой замещенным изоцианатом. Могут быть использованы различные растворители и реакционные условия, и они легко будут определены специалистом. Например, взаимодействие может быть осуществлено при комнатной температуре или температуре дефлегмации в инертном растворителе,таком как дихлорметан, ацетонитрил или тетрагидрофуран, в присутствии или в отсутствие основания,такого как триэтиламин или пиридин. На стадии 4 полученную гидроксимочевину подвергают действию кислоты с органическим растворителем или без него. Например, взаимодействие может быть осуществ- 19006815 лено при 70-90 С в серной кислоте. Может быть добавлен растворитель, такой как толуол или уксусная кислота. На стадии 3' соединение 4 с превращают в соединение 4f путем обработки карбонильным (или тиокарбонильным) производным, активированным двумя уходящими группами, такими как фосген (или тиофосген), 1,1'-карбонилдиимидазол (или 1,1'-тиокарбонилдиимидазол). Протокол Е. Схема 5 На схеме 5 X1, Х 2, Х 4, X, Y и А такие, как определено в кратком описании сущности изобретения. Исходное трициклическое соединение приводят во взаимодействие с электрофилом Е+, таким как галоний или ацилий, в присутствии или в отсутствие активирующего агента в органическом растворителе. Различные растворители и реакционные условия могут быть использованы для этого электрофильного замещения в ароматическом ядре в зависимости от электрофила, и они легко будут определены специалистом. Например, исходный материал может быть обработан источником галония, таким как N-иодили N-бромсукцинимид, в диметилформамиде при 60-70 С, что дает соответствующий галогенид. В другом примере исходный материал может быть приведен во взаимодействие с ацилгалогенидом и трихлоридом алюминия в качестве кислоты Льюиса в растворителе, таком как дихлорэтан, при 80 С. Протокол F. Схема 6 На схеме 6 X1, Х 3, X, Y и А такие, как определено в кратком описании сущности изобретения, и Х 2 не представляет собой СН. Исходное трициклическое соединение приводят во взаимодействие с электрофилом Е+ в присутствии или в отсутствие активирующего агента в органическом растворителе. Это электрофильное замещение в ароматическом ядре подобно таковому в Протоколе Е за исключением того, что в этом случае, так как X2 отличен от СН, замещение ориентировано по положению 8. Так же, как в Протоколе Е, для электрофильного замещения в ароматическом ядре могут быть использованы различные растворители и реакционные условия в зависимости от электрофила, и они легко будут определены специалистом. Протокол G. Схема 7 На схеме 7 X1, X2, Х 3 и Х 4, X, Y, Z и А такие, как определено в кратком описании сущности изобретения, R является алкенилом, алкинилом, арилом или гетероарилом, и R' представляет собой Н или алкил. Исходный арил- или гетероарилиодид либо -бромид подвергают катализируемой палладием реакции перекрестного связывания с металлоорганическими соединениями, такими как боронатный эфир,бороновая кислота, цинкорганическое соединение (Hal=галоген) или триалкилстаннан, в присутствии основания, когда это необходимо. Металлоорганические соединения могут быть заменены терминальным алкеном или алкином в данной реакции сочетания. Если используется алкин, то может быть добавлен источник меди (I), такой как иодид меди. Различные палладиевые катализаторы, растворители и реакционные условия могут быть использованы для этих реакций связывания, и они легко будут определены специалистом. Например, исходный арил- или гетероарилиодид либо -бромид может быть приведен во взаимодействие с бороновой кислотой в диметилформамиде при 80 С в присутствии тетракис(трифенилфосфин)палладия в качестве катализатора и водного раствора карбоната калия в качестве основания. На схеме 8 X1, Х 2, Х 3, Х 4, X, Y, Z, R2, R3, R4 и А такие, как определено в кратком описании сущности изобретения, и R выбран из арила, алкенила, алкинила или гетероарила. На стадии 1 исходный арил- или гетероарилиодид либо -бромид обрабатывают бис(пинаколато)дибором в условиях палладиевого катализа, что дает соответствующий боронатный эфир. Различные палладиевые катализаторы, растворители и реакционные условия могут быть использованы для этих реакций связывания, и они легко будут определены специалистом. Например, исходный гетероарилиодид либо -бромид может быть подвергнут взаимодействию с бис(пинаколато)дибором в диметилформамиде при 80 С в присутствии тетракис(трифенилфосфин)палладия в качестве катализатора. Полученный боронатный эфир затем сочетают с арил-, алкенил-, алкинил- или гетероарилиодидом,-бромидом либо -трифлатом, катализируя соединениями палладия (стадия 2). И вновь, для этих реакций сочетания могут быть использованы различные палладиевые катализаторы, растворители и реакционные условия, и они легко будут определены специалистом. Например, боронатный эфир подвергают взаимодействию с арил-, алкенил-, алкинил- или гетероарилиодидом, в диметилформамиде при 80 С в присутствии ацетата натрия в качестве основания и тетракис(трифенилфосфин)палладия в качестве катализатора, что дает продукт сочетания. На стадии 3 боронатный эфир гидролизуют до соответствующей бороновой кислоты. Это может быть осуществлено в результате обработки кислотой, например водным раствором соляной кислоты, в органическом растворителе, например метаноле. Полученную бороновую кислоту сочетают (стадия 4) на воздухе с фенолом или гетероарильным спиртом либо (стадия 5) с первичным или вторичным амином, гетероариламином, анилином, амидом, сульфонамидом, мочевиной, карбаматом или имидом в присутствии основания, такого как триэтиламин или пиридин, и источника меди (II), такого как ацетат меди (II), в растворителе типа дихлорметана. В реакционную смесь могут быть добавлены молекулярные сита 4 или 3. Протокол I. Схема 9- 21006815 На схеме 9 X1, X2, Х 3 и Х 4, Y и А такие, как определено в кратком описании сущности изобретения. На стадии 1 мочевину, карбамат или тиокарбамат сначала превращают в галогеноимин с использованием хлорирующего агента, такого как РОСl3, который затем дополнительно подвергают взаимодействию (стадия 2) с подходящим амином с получением конечного соединения. Взаимодействие может быть осуществлено без растворителя или в растворителе, например спирте, таком как этанол, при температуре между 40 и 80 С или под давлением в случае например летучего амина. На стадии 3 галогеноимин превращают в тиопроизводное с использованием тиомочевины. Указанный выше на схеме 9 способ также может быть применен к соединениям формулы (I), где Y представляет собой NH, и Х представляет собой N-R9. Протокол J. Схема 10 На схеме 10 X1, Х 2, Х 3, Х 4, R9, R12 и А такие, как определено в кратком описании сущности изобретения, и LG является уходящей группой, такой как трифторметансульфонат, мезилат или галоген. На стадии 1 хиназолинон подвергают взаимодействию с R12-LG с получением N-замещенного хиназолинона. На стадии 2 N-замещенный хиназолинон приводят во взаимодействие с R9-LG. Могут быть использованы различные растворители, рабочие условия и основания, и они легко будут определены специалистом. Например, и без какого-либо ограничения, для взаимодействия можно использовать гидрид натрия или карбонат цезия в качестве основания в диметилформамиде в качестве растворителя. Протокол K. Схема 11 На схеме 11 X1, X2, Х 3, Х 4, R9 и А такие, как определено в кратком описании сущности изобретения,и LG является уходящей группой, такой как трифторметансульфонат, мезилат или галоген. На стадии 1 хиназолинон подвергают взаимодействию с параметоксибензилхлоридом (РМВ). Может быть использована другая защитная группа. Могут быть использованы различные растворители, рабочие условия и основания, и они легко будут определены специалистом. Например, и без какого-либо ограничения, для взаимодействия можно использовать карбонат цезия в качестве основания в диметилформамиде в качестве растворителя. На стадии 2 защищенный хиназолинон приводят во взаимодействие с R9-LG. Могут быть использованы различные растворители, рабочие условия и основания, и они легко будут определены специалистом. Например, и без любого ограничения, для взаимодействия можно использовать гидрид натрия в качестве основания в диметилформамиде в качестве растворителя. На стадии 3 обработка N1-PMB-защищенного хиназолинона с помощью TFA удаляет защитную группу. Могут быть использованы другие защитные группы и условия снятия защиты. Протокол L. Схема 12- 22006815 На схеме 12 Х 2, Х 3, Х 4, А и Y такие, как определено в кратком описании сущности изобретения, R является алкилом или С(=O)-алкилом, и LG является уходящей группой. На стадии 1 исходное метоксипроизводное деметилируют трибромидом бора в растворителе, таком как дихлорметан. Полученное фенольное промежуточное соединение обрабатывают на стадии 2 электрофилом, таким как алкилгалогенид, ацилгалогенид или им подобные, в присутствии основания, такого как карбонат калия, карбонат цезия или гидрид натрия, в растворителе типа диметилформамида. Примеры синтеза Примеры 1-100 иллюстрируют без ограничения синтез наиболее активных соединений формулы (I) по изобретению. В следующих далее протоколах экспериментов данные протонного ЯМР, если не оговорено особо,получены на приборе ЯМР с частотой 400 МГц. Пример 1. Спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он.X1=CH, X2=CH, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А. Фенилмочевину (13,6 г; 0,1 моль) порциями добавляют к раствору полифосфорной кислоты (100 г), перемешиваемому при 100 С. После полного растворения мочевины к горячей смеси по каплям добавляют циклогексанон (10,3 мл; 0,1 моль). Смесь перемешивают при 100-120 С до завершения добавления и выливают в холодную воду. Осадок отфильтровывают, промывают холодной водой, переносят в горячий этанол и нейтрализуют раствором NH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в этаноле. Указанное в заголовке соединение получают в виде белого порошка. Температура плавления (т.пл.)=224226 С. 1X1=CH, Х 2=С-O-СН 3, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 4 метоксифенилмочевину (30 г; 0,18 моль) и циклогексанон (18,6 мл; 0,18 моль) в полифосфорной кислоте(200 мл). Осадок отфильтровывают, промывают холодной водой, переносят в горячий этанол и нейтрализуют раствором NH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в этаноле. Указанное в заголовке соединение получают в виде белого порошка (8,2 г; 18%-ный выход); т.пл.=233-235 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=СН, А=циклогептил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя фенилмочевинуNH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в этаноле. Указанное в заголовке соединение получают в виде белого порошка (14,7 г; 32%-ный выход); т.пл.=198-200 С. 1X1=CH, Х 2=СН, Х 3=С-O-СН 3, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 3 метоксифенилмочевину (33,2 г; 0,2 моль) и циклогексанон (20,7 мл; 0,2 моль) в полифосфорной кислоте(200 мл). Осадок отфильтровывают, промывают холодной водой, переносят в горячий этанол и нейтрализуют раствором NH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в этаноле. Указанное в заголовке соединение получают в виде белого порошка (9,8 г; 20%-ный выход); т.пл.=228-230 С. 1X1=CH, Х 2=С-фенил, Х 3=СН, Х 4=СН, А=циклогептил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 4-фенилфенилмочевину (42,4 г; 0,2 моль) и циклогептанон (23,5 мл; 0,2 моль) в полифосфорной кислоте (400 г). Осадок отфильтровывают, промывают холодной водой, переносят в горячий этанол и нейтрализуют рас- 23006815 твором NH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в этаноле. Указанное в заголовке соединение получают в виде белого порошка (23,3 г; 38%-ный выход); т.пл.=180182 С. 1X1=CH, X2=СН, Х 3=СН, Х 4=С-O-СН 3, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 метоксифенилмочевину (49,8 г; 0,3 моль) и циклогексанон (31 мл; 0,3 моль) в полифосфорной кислоте(600 г). Осадок отфильтровывают, промывают холодной водой, переносят в горячий этанол и нейтрализуют раствором NH4OH. Для приготовления раствора 50% этанол/вода добавляют воду и осадок отфильтровывают, промывают водой и высушивают. Неочищенный материал очищают кристаллизацией в изопропаноле. Указанное в заголовке соединение получают в виде белого порошка (48,1 г; 65%-ный выход); т.пл.=209-211 С. 1X1=CH, X2=CH, Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 хлорфенилмочевину (51,15 г; 0,3 моль) и циклогексанон (29,4 г; 0,3 моль) в полифосфорной кислоте (600 г). Осадок отфильтровывают, промывают холодной водой и перекристаллизовывают из этилацетата. Указанное в заголовке соединение получают в виде твердого вещества оранжевого цвета (21%-ный выход); т.пл.=209-211 С. 1X1=C-Cl, Х 2=СН, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанные в заголовке соединения получают согласно протоколу А, используя 3 хлорфенилмочевину (0,51 г; 3 ммоль) и циклогексанон (0,5 мл; 4,8 ммоль; 1,6 экв.) в полифосфорной кислоте (11 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над МgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэшхроматографией на силикагеле (СН 2 Сl2/СН 3 СN: от 90/10 до 60/40) с последующей перекристаллизацией в толуоле, что дает 7'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он в виде твердого вещества белого цвета (110 мг; 15%-ный выход); т.пл.=254 С. 1H ЯМР [(СD3)2SO]9,28 (br s, 1H, NH), 7,27 (d, J=8,0 Гц, 1 Н), 6,91-6,89 (m, 2H), 6,82 (s, 1H, NH),1,83-1,61 (m, 7H), 1,49 (m, 2H), 1,24 (m, 1H). И 5'-хлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он в виде твердого вещества белого цвета (101 мг; 14%-ный выход); т.пл.=229 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=С-СН 3, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя о-толилмочевину(551 мг; 3,66 ммоль) и циклогексанон (430 мкл; 4,15 ммоль; 1,1 экв.) в полифосфорной кислоте (5 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над МgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизацией в толуоле, что дает 290 мг (34%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=204 С. 1X1=CH, X2=C-Cl, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 4 хлорфенилмочевину (0,85 г; 5 ммоль) и циклогексанон (0,55 мл; 5,5 ммоль; 1,1 экв.) в полифосфорной кислоте (29 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллиза- 24006815 цией в толуоле с получением 79 мг (6%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=241 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=С-Вr, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 бромфенилмочевину (1,075 г; 5 ммоль) и циклогексанон (0,6 мл; 5,8 ммоль; 1,2 экв.) в полифосфорной кислоте (39 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизацией в толуоле с получением 415 мг (28%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=213 С. 1X1=CH, X2=CH, Х 3=СН, X4=C-F, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 фторфенилмочевину (0,77 г; 5 ммоль) и циклогексанон (0,55 мл; 5,5 ммоль; 1,1 экв.) в полифосфорной кислоте (20 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 95/5) с последующей перекристаллизацией в толуоле, что дает 272 мг (23%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=221 С. 1X1=CH, Х 2=С-СН 3, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 4 метилфенилмочевину (1,5 г; 10 ммоль) и циклогексанон (1,1 мл; 11 ммоль; 1,1 экв.) в полифосфорной кислоте (38 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизацией в толуоле, что дает 405 мг (18%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=229 С. 1X1=C-Cl, X2=CH, Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2,5-дихлорфенилмочевину (0,615 г; 3 ммоль) и циклогексанон (0,50 мл; 5 ммоль; 1,6 экв.) в полифосфорной кислоте (15 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают надMgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 92/8) с последующей перекристаллизацией в толуоле, что дает 56 мг (7%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=243 С. 1X1=C-Cl, X2=C-Cl, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанные в заголовке соединения получают согласно протоколу А, используя 3,4 дихлорфенилмочевину (0,61 г; 3 ммоль) и циклогексанон (0,50 мл; 5 ммоль; 1,6 экв.) в полифосфорной кислоте (16 г). Водный слой экстрагируют СH2 Сl2/МеОН (2/1). Объединенные органические экстракты высушивают над МgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на силикагеле (СН 2 Сl2/СН 3 СN: от 90/10 до 60/40) с последующей перекристаллизацией в толуоле, что дает 6',7'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он в виде твердого вещества белого цвета (55 мг; 6%-ный выход); т.пл.=269 С. 1- 25006815 И 5',6'-дихлороспиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он в виде твердого вещества белого цвета (26 мг; 3%-ный выход); т.пл.=240 С. 1X1=CH, Х 2=С-фенил, Х 3=СН, Х 4=СН, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 4-фенилфенилмочевину (0,67 г; 3,15 ммоль) и циклогексанон (0,50 мл; 5 ммоль; 1,6 экв.) в полифосфорной кислоте (16 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизацией в толуоле, что дает 410 мг (13%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=213 С. 1X1=CH, X2=CH, Х 3=СН, X4=C-I, А=циклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 иодфенилмочевину (2 г; 7,6 ммоль) и циклогексанон (1 мл; 9,6 ммоль; 1,25 экв.) в полифосфорной кислоте (25 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Объединенные органические экстракты высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизацией в толуоле, что дает 80 мг (3%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=256 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=С-Вr, А=циклобутил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2-бромфенилмочевину (0,6 г; 2,8 ммоль) и циклобутанон (0,25 мл; 3,35 ммоль; 1,2 экв.) в полифосфорной кислоте (22 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Органические экстракты высушивают над MgSO4,фильтруют и концентрируют. Неочищенный материал очищают флэш-хроматографией на силикагеле(CH2Cl2/MeOH: от 99/1 до 90/10) и полученный порошок промывают диизопропиловым эфиром. Указанное в заголовке соединение получают в виде белого порошка (0,03 г; 4%-ный выход); т.пл.=203-205 С. 1X1=CH, Х 2=СН, Х 3=СН, Х 4=С-Вr, А=циклогептил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2-бромфенилмочевину (0,6 г; 2,8 ммоль) и циклогептанон (0,5 мл; 4,2 ммоль; 1,5 экв.) в полифосфорной кислоте (22 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Органические экстракты высушивают над MgSO4,фильтруют и концентрируют. Неочищенный материал очищают флэш-хроматографией на силикагеле(CH2Cl2/MeOH: от 99/1 до 90/10) и полученный порошок промывают диизопропиловым эфиром. Указанное в заголовке соединение получают в виде белого порошка (0,12 г; 14%-ный выход); т.пл.=215-217 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=С-Вr, А=4-метилциклогексил, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2-бромфенилмочевину (0,6 г; 2,8 ммоль) и 4-метилциклогексанон (0,41 мл; 3,35 ммоль; 1,2 экв.) в полифосфорной кислоте(22 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Органические экстракты высушивают над MgSO4,фильтруют и концентрируют. Неочищенный материал очищают флэш-хроматографией на силикагеле(CH2Cl2/MeOH: от 99/1 до 90/10) и полученный порошок промывают диизопропиловым эфиром. Указанное в заголовке соединение получают в виде белого порошка (0,11 г; 11%-ный выход); т.пл.=187-189 С. 1X1=CH, X2=CH, Х 3=СН, Х 4=С-Вr, А=бицикло[3,2,1]октан, X=NH, Z=O, Y=NH Указанное в заголовке соединение получают согласно протоколу А, используя 2 бромфенилмочевину (0,6 г; 2,8 ммоль) и бицикло[3,2,1]октан-2-он (0,55 г; 4,47 ммоль; 1,6 экв.) в поли- 26006815 фосфорной кислоте (22 г). Водный слой экстрагируют CH2Cl2/MeOH (2/1). Органические экстракты высушивают над MgSO4, фильтруют и концентрируют. Неочищенный материал очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) и полученный порошок промывают диизопропиловым эфиром. Указанное в заголовке соединение получают в виде белого порошка (0,003 г; 1%ный выход); т.пл.=276-278 С. 1X1=CH, X2=C-Cl, Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH Раствор соединения из примера 7 (100,2 мг; 0,4 ммоль) в диметилформамиде (2 мл) обрабатываютN-хлорсукцинимидом (80 мг; 0,6 ммоль; 1,5 экв.) при 60 С в течение ночи. Реакционную смесь концентрируют, затем очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 100/0 до 90/10) и обращенно-фазовой ВЭЖХ (колонка С 18, градиент ацетонитрила в воде: от 50/50 до 95/5), что дает указанное в заголовке соединение в виде твердого вещества белого цвета (48%-ный выход); т.пл.=245 С. 1X1=CH, X2=C-I, Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH К раствору соединения из примера 7 (5 г; 20 ммоль) в трифторуксусной кислоте (25 мл) последовательно добавляют N-иодсукцинимид (6 г; 22 ммоль; 1,1 экв.) и серную кислоту (4 мл). Полученный раствор нагревают до 55 С в течение ночи, концентрируют при пониженном давлении, переносят в дихлорметан и дважды промывают водой. Реакционную смесь концентрируют и очищают флэшхроматографией на силикагеле (CH2Cl2/MeOH: 97/3), что дает 4,5 г (73%-ный выход) указанного в заголовке соединения в виде твердого вещества желтоватой окраски; т.пл.=261 С. 1X1=CH, Х 2=С-фенил, Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH Раствор соединения из примера 18 (232 мг; 0,79 ммоль) в диметилформамиде (4 мл) обрабатываютN-хлорсукцинимидом (80 мг; 0,6 ммоль; 1,5 экв.) при 60 С в течение ночи. Реакционную смесь концентрируют, затем очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10), что дает указанное в заголовке соединение в виде твердого вещества белого цвета (41%-ный выход); т.пл.=226 С. 1X1=CH, Х 2=С-O-СН 3, Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH Раствор соединения из примера 2 (500 мг; 2,03 ммоль) в диметилформамиде (10 мл) обрабатываютN-хлорсукцинимидом (300 мг; 2,24 ммоль; 1,1 экв.) при 60 С в течение ночи. Реакционную смесь концентрируют и очищают флэш-хроматографией на силикагеле (CH2Cl2/MeOH: от 99/1 до 90/10) с последующей перекристаллизации в толуоле, что дает 76 мг (13%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=226 С. 1X1=CH, Х 2=С-фенил, Х 3=СН, X4=C-Cl, А=циклогептил, X=NH, Z=O, Y=NH Раствор соединения из примера 5 (150 мг; 0,49 ммоль) в диметилформамиде (2 мл) обрабатываютN-хлорсукцинимидом (75 мг; 0,56 ммоль; 1,1 экв.) при 60 С в течение ночи. Реакционную смесь концентрируют, затем очищают флэш-хроматографией на силикагеле (СН 2 Сl2/МеОН: от 99/1 до 90/10), что дает 158 мг (95%-ный выход) указанного в заголовке соединения в виде твердого вещества желтоватой окраски; т.пл.=201 С. 1X1=CH, Х 2=С-СН 3, Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH Раствор соединения из примера 14 (350 мг; 1,51 ммоль) в диметилформамиде (7 мл) обрабатываютN-хлорсукцинимидом (305 мг; 2,3 ммоль; 1,5 экв.) при 60 С в течение ночи. Реакционную смесь концентрируют и очищают флэш-хроматографией на силикагеле (СН 2 Сl2/МеОН: от 99/1 до 90/10). Полученное твердое вещество растирают с метанолом, что дает указанное в заголовке соединение в виде твердого вещества белого цвета (28%-ный выход); т.пл.=266 С. 1X1=CH, Х 2=С-(3-пиридил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (0,5 г; 1,4 ммоль) в диметилформамиде (5 мл) последовательно добавляют 3-пиридилбороновую кислоту (0,22 г; 1,7 ммоль; 1,2 экв.) и 2 М водный раствор карбоната калия (1,5 мл). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракистрифенилфосфинпалладий (60 мг; 0,05 ммоль; 0,04 экв.). После нагревания до 90 С в течение ночи смесь концентрируют при пониженном давлении, растирают с водой и фильтруют. Полученное твердое вещество растирают с этилацетатом, отфильтровывают и очищают флэш-хроматографией на силикагеле(CH2Cl2/EtOAc: от 80/20 до 50/50), что дает 140 мг (30%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=246 С. 1H ЯМР [(СD3)2SO]8,93 (br s, 1H, NH), 8,55 (m, 2H), 8,10 (m, 1H), 7,71 (d, J=1,5 Гц,1H), 7,65 (d,J=1,5 Гц, 1H), 7,45 (dd, J=8,0, 5,0 Гц, 1H), 7,19 (brs, 1H, NH), 1,91-1,77 (m, 6H), 1,63 (m, 1H), 1,54 (m, 2H),1,32 (m, 1H). Пример 31. 8'-Хлоро-6'-(4-пиридил)спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он. Х 1=СН, Х 2=С-(4-пиридил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (0,5 г; 1,4 ммоль) в диметилформамиде (5 мл) последовательно добавляют 4-пиридилбороновую кислоту (0,22 г; 1,7 ммоль; 1,2 экв.) и 2 М водный раствор карбоната калия (1,5 мл). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракистрифенилфосфинпалладий (60 мг; 0,05 ммоль; 0,04 экв.). После нагревания до 90 С в течение ночи смесь концентрируют при пониженном давлении, промывают водой и этилацетатом, затем очищают флэш-хроматографией на силикагеле (от CH2Cl2/EtOAc: 80/20 до CH2Cl2/MeOH: 97/3), что дает 40 мг(10%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=320321 С. 1X1=CH, Х 2=С-(4-карбоксифенил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (1 г; 2,8 ммоль) в диметилформамиде (10 мл) последовательно добавляют 4-карбоксифенилбороновую кислоту (0,55 г; 3,35 ммоль; 1,2 экв.) и 2 М водный раствор карбоната калия (3 мл). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракистрифенилфосфинпалладий (120 мг; 0,1 ммоль; 0,04 экв.). После нагревания до 90 С в течение 4 ч смесь концентрируют при пониженном давлении, переносят в этилацетат и промывают водой. Водный слой подкисляют до рН 2 и экстрагируют этилацетатом. Органический слой концентрируют при пониженном давлении до трети своего объема и фильтруют. Полученное твердое вещество очищают флэш-хроматографией на силикагеле (СН 2 Сl2/МеОН: от 97/3 до 95/5), что дает 250 мг (40%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=309 С. 1X1=CH, Х 2=С-(3-карбоксифенил), Х 3=СН, X4=C-Cl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (1 г; 2,8 ммоль) в диметилформамиде (10 мл) последовательно добавляют 3-карбоксифенилбороновую кислоту (0,55 г; 3,35 ммоль; 1,2 экв.) и 2 М водный раствор карбоната калия (3 мл). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракистрифенилфосфинпалладий (120 мг; 0,1 ммоль; 0,04 экв.). После нагревания до температуры дефлегмации в течение ночи смесь концентрируют при пониженном давлении, переносят в дихлорметан и промывают водой. Водный слой подкисляют до рН 1 и фильтруют, что дает 330 мг (58%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=300 С. 1X1=CH, Х 2=С-индол-5-ил, Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (0,5 г; 1,4 ммоль) в диметилформамиде (5 мл) последовательно добавляют 5-индолилбороновую кислоту (0,26 г; 1,6 ммоль; 1,2 экв.) и 2 М водный раствор карбоната калия (1,5 мл). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракистрифенилфосфинпалладий (60 мг; 0,05 ммоль; 0,04 экв.). После нагревания до 80 С в течение ночи смесь концентрируют при пониженном давлении, переносят в этилацетат и трижды промывают водой. Затем остаток очищают флэш-хроматографией на силикагеле (CH2Cl2/EtOAc: 80/20), что дает 210 мг(44%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=257 С.X1=CH, Х 2=С-(2-пиридил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К раствору соединения из примера 25 (0,5 г; 1,3 ммоль) в тетрагидрофуране (5 мл) добавляют 0,5 М раствор бромида 2-пиридилцинка в тетрагидрофуране (60 мкл; 30 ммоль; 23 экв.). Смесь дегазируют путем барботирования азота в течение 30 мин и добавляют тетракис(трифенилфосфин)палладий (60 мг; 0,05 ммоль; 0,04 экв.). После кипячения с обратным холодильником в течение 4 ч добавляют дополнительное количество тетракис(трифенилфосфин)палладия (100 мг) и толуол (5 мл). После нагревания до 90 С в течение ночи смесь разбавляют дихлорметаном и трижды промывают водой. Органический слой концентрируют при пониженном давлении и очищают флэш-хроматографией на силикагелеX1=CH, Х 2=С-(3-диметиламинопроп-1-инил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К суспензии соединения из примера 25 (0,5 г; 1,4 ммоль) в пирролидине (10 мл) последовательно добавляют 1-диметиламино-2-пропин (0,170 мл; 1,6 ммоль; 1,2 экв.), толуол (10 мл) и тетракис(трифенилфосфин)палладий (80 мг; 0,07 ммоль; 0,05 экв.). После нагревания до 45 С в течение ночи смесь фильтруют, разбавляют этилацетатом и дважды промывают 1 М водным раствором соляной кислоты. Водный слой подщелачивают до рН 9 и дважды экстрагируют этилацетатом. Объединенные экстракты высушивают над сульфатом натрия, концентрируют при пониженном давлении, что дает 60 мг (13%ный выход) указанного в заголовке соединения в виде твердого вещества желтоватой окраски; т.пл.=208 С. 1X1=CH, Х 2=С-(3-метиламинопроп-1-инил), Х 3=СН, Х 4=С-Сl, А=циклогексил, X=NH, Z=O, Y=NH К раствору соединения из примера 25 (0,2 г; 0,5 ммоль) в диметилформамиде (3 мл) последовательно добавляют N-метилпропаргил-амин (0,1 мл; 1 ммоль; 2 экв.) и триэтиламин (1 мл; 7 ммоль; 14 экв.). Смесь дегазируют путем барботирования азота в течение 30 мин, затем добавляют тетракис(трифенилфосфин)палладий (20 мг; 0,025 ммоль; 0,05 экв.) и иодид меди (I) (20 мг; 0,1 ммоль; 0,02 экв.). После нагревания до 80 С в течение ночи смесь разбавляют дихлорметаном и трижды промывают водой. Органический слой высушивают над сульфатом натрия, фильтруют, концентрируют при пониженном давлении и очищают флэш-хроматографией на силикагеле (от CH2Cl2/MeOH: 98/2 доX1=CH, Х 2=С-(4-(4-метилпиперазин-1-карбонил)фенил), Х 3=СН, X4=C-Cl, А=циклогексил, X=NH,Z=O, Y=NH К суспензии соединения из примера 32 (100 мг; 0,27 ммоль) в толуоле (3 мл) добавляют тионилхлорид(0,03 мл; 0,4 ммоль; 1,5 экв.). Полученную смесь нагревают до температуры дефлегмации в течение 2 ч,затем дважды концентрируют при пониженном давлении и переносят в толуол. К полученному твердому веществу в толуоле (2 мл) добавляют триэтиламин (0,1 мл; 0,54 ммоль; 2 экв.) и 1-метилпиперазин (0,04 мл; 0,32 ммоль; 1,2 экв.). После перемешивания в течение ночи смесь разбавляют дихлорметаном и дважды промывают водой. Органический слой концентрируют при пониженном давлении и очищают флэшхроматографией на силикагеле (СH2Cl2/МеОН: 97/3), что дает 20 мг (16%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=277 С. 1X1=CH, Х 2=С-[4-(3-N-диметиламино-пропилкарбоксамид)фенил], Х 3=СН, Х 4=С-Cl, А=циклогексил,X=NH, Z=O, Y=NH К суспензии соединения из примера 32 (122 мг; 0,33 ммоль) в толуоле (3 мл) добавляют тионилхлорид (0,04 мл; 0,5 ммоль; 1,5 экв.). Полученную смесь нагревают до температуры дефлегмации в течение ночи, затем концентрируют при пониженном давлении. К полученному твердому веществу в толуоле (2 мл) добавляют триэтиламин (0,1 мл; 0,54 ммоль; 1,6 экв.) и 3-диметиламинопропиламин (0,037 мл; 0,26 ммоль; 0,8 экв.). После перемешивания в течение 4 ч смесь разбавляют дихлорметаном и дважды промывают водой и 1 н водным раствором соляной кислоты. Водный слой подщелачивают до рН 9 и дважды экстрагируют дихлорметаном. Объединенные органические экстракты концентрируют при пониженном давлении, что дает 40 мг (34%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=232 С. 1H ЯМР [(СD3)2SO]8,59-8,55 (m, 2 Н), 7,90 (d, J=8,5 Гц, 2 Н), 7,79 (d, J= 8,5 Гц, 2 Н), 7,68 (d, J=1,5 Гц, 1H), 7,63 (s, 1H), 7,18 (br s, 1H, NH), 3,29 (m, 2H), 2,26 (t, J=7,0 Гц, 2H), 2,14 (s, 6H), 1,92-1,77 (m, 6H),1,67 (m, 3H), 1,54 (m, 2H), 1,32 (m, 1H). Пример 40. 8'-Хлоро-6'-[4-(2-N-диметиламиноэтилкарбоксамид)фенил]спиро[циклогексан-1-4'(3',4'-дигидро)хиназолин]-2'(1'Н)-он. Х 1=СН, Х 2=С-[4-(2-N-диметиламиноэтилкарбоксамид)фенил], Х 3=СН, Х 4=С-Сl, А=циклогексил,X=NH, Z=O, Y=NH К суспензии соединения из примера 32 (150 мг; 0,4 ммоль) в толуоле (3 мл) добавляют тионилхлорид (0,03 мл; 0,41 ммоль; 1,0 экв.). Полученную смесь нагревают до температуры дефлегмации в течение 3 ч, затем концентрируют при пониженном давлении. К полученному твердому веществу в толуоле (3 мл) добавляют триэтиламин (0,14 мл; 0,8 ммоль; 2 экв.) и 2-диметиламиноэтиламин (0,04 мл; 0,32 ммоль; 0,8 экв.). После перемешивания в течение ночи смесь концентрируют, разбавляют дихлорметаном и дважды промывают водой и 1 н водным раствором соляной кислоты. Водный слой подщелачивают до рН 9 и дважды экстрагируют дихлорметаном. Объединенные органические экстракты концентрируют при пониженном давлении, что дает 100 мг (56%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=234 С. 1X1=CH, Х 2=С-[3-(3-N-диметиламинопропилкарбоксамид)фенил], Х 3=СН, Х 4=С-Cl, А=циклогексил,X=NH, Z=O, Y=NH К суспензии соединения из примера 33 (100 мг; 0,27 ммоль) в толуоле (10 мл) добавляют тионилхлорид (0,1 мл; 1,3 ммоль; 5 экв.). Полученную смесь нагревают до температуры дефлегмации в течение 2 ч, затем концентрируют при пониженном давлении. К полученному твердому веществу в толуоле (10 мл) добавляют триэтиламин (0,1 мл; 0,54 ммоль; 2 экв.) и 3-диметиламинопропиламин (0,03 мл; 0,21 ммоль; 0,8 экв.). После перемешивания в течение 3 ч смесь концентрируют, разбавляют дихлорметаном и дважды промывают водой и 1 н водным раствором соляной кислоты. Водный слой промывают этилацетатом,подщелачивают до рН 9 и дважды экстрагируют дихлорметаном. Объединенные органические экстракты концентрируют при пониженном давлении, что дает 30 мг (30%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=208 С. 1(d, J=8,0 Гц, 1H), 7,69 (d, J=1,5 Гц, 1H), 7,60 (s, 1H), 7,52 (t, J=7,5 Гц, 1H), 7,15 (br s, 1H, NH), 3,29 (m, 2H),2,27 (t, J=7,0 Гц, 2 Н), 2,14 (s, 6H), 1,85-1,78 (m, 6H), 1,67 (m, 3 Н), 1,55 (m, 2H), 1,30 (m, 1H). Пример 42. 8'-Хлоро-6'-[3-(4-метилпиперазин-1-карбонил)фенил]спиро[циклогексан-1-4'-(3',4'-дигидро)хиназолин]-2'(1'Н)-он. Х 1=СН, Х 2=С-[3-(4-метилпиперазин-1-карбонил)фенил], Х 3=СН, X4=C-Cl, А=циклогексил, X=NH,Z=O, Y=NH К суспензии соединения из примера 33 (100 мг; 0,27 ммоль) в толуоле (5 мл) добавляют тионилхлорид(0,03 мл; 0,4 ммоль; 1,5 экв.). Полученную смесь нагревают до температуры дефлегмации в течение 3 ч,затем дважды концентрируют при пониженном давлении и переносят в толуол. К полученному твердому веществу в толуоле (5 мл) добавляют триэтиламин (0,1 мл; 0,54 ммоль; 2 экв.) и 1-метилпиперазин (0,024 мл; 0,21 ммоль; 0,8 экв.). После перемешивания в течение ночи смесь разбавляют дихлорметаном и дважды промывают водой. Органический слой концентрируют при пониженном давлении, переносят в этилацетат и промывают 1 н водным раствором соляной кислоты. Водный слой промывают этилацетатом, подщелачивают до рН 9 и дважды экстрагируют дихлорметаном. Объединенные органические экстракты концентрируют при пониженном давлении, что дает 60 мг (61%-ный выход) указанного в заголовке соединения в виде твердого вещества белого цвета; т.пл.=207 С.
МПК / Метки
МПК: C07D 405/12, C07D 413/12, A61K 31/527, C07D 403/04, C07D 239/70, A61P 29/00, C07D 401/04, C07D 401/12
Метки: новые, фосфодиэстеразы-7, производные, применение, качестве, спиротрициклические, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-6815-novye-spirotriciklicheskie-proizvodnye-i-ih-primenenie-v-kachestve-ingibitorov-fosfodiesterazy-7.html" rel="bookmark" title="База патентов Евразийского Союза">Новые спиротрициклические производные и их применение в качестве ингибиторов фосфодиэстеразы-7</a>
Предыдущий патент: Система и способ использования множества приложений
Следующий патент: Смеси гербицидов, содержащие специальные сульфонилмочевины
Случайный патент: Способ лечения острой мании