Замещенные производные бензимидазола и их применение для лечения злокачественной опухоли
Номер патента: 6802
Опубликовано: 28.04.2006
Авторы: Карре Шанталь, Реснер Манфред, Клерк Франсуа, Ами Франсуа, Депре Стефани, Ангуйан-Бонифас Одиль, Депати Изабелль
Формула / Реферат
1. Соединения формулы (I)
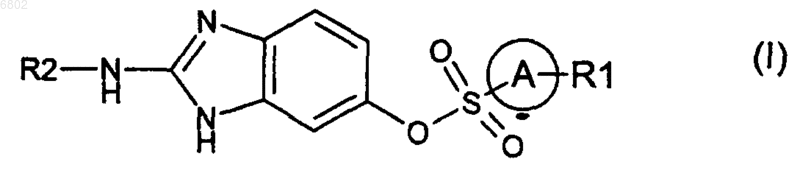
где А представляет собой фенил,
где R1 выбран из одной или нескольких аналогичных групп, выбранных из
алкила, возможно, замещенного алкокси, гетероалкилом, арилом, ацилом, группой ацильного производного, галогеном;
алкокси, возможно, замещенного алкилом, гетероалкилом, арилом, гетероарилом, алкоксиалкилом, гидроксиалкиламидом или перфторалкоксигруппой или алкилтио, возможно, замещенного амидом или перфторалкилтио;
арила или гетероарила, возможно, замещенных одной или более алкильной группой, алкоксигруппой, нитрогруппой, цианогруппой, группой ацильного производного, перфторалкоксигруппой, перфторалкильной группой, гетероарильной группой, арилоксигруппой;
галогена;
4-NH2;
4-NH алкила или циклоалкила, возможно, замещенных ацилом, группой ацильного производного, гидрокси, амино, алкокси, гетероциклической или арильной группой;
4-N-имидазолила;
3-SO2Me;
где R2 выбран из группы, включающей
СО-алкила, возможно, замещенного амино, кислотной группой, группой производного кислоты, алкокси, арил или ОН-группами;
СО-аралкила, возможно, замещенного алкокси, галогеном, амино, кислотной группой или группой производного кислоты;
СО-арила, возможно, замещенного;
СО-алкокси, возможно, замещенного арилом;
СО-амино, CO-NHR3, СО-NR3R4, где R3 и R4 независимо выбраны из водорода, алкила, гидроксиалкила, алкоксиалкила, фторалкила, алкинила, гетероалкила, алкилгетероалкила, арила, аралкила, или вместе они образуют алкиленовую цепь, включающую в себя, возможно, от 1 до 4 гетероатомов;
арила или аралкила, возможно, замещенных гетероциклоалкилом, алкилом, арилом, алкокси, амино, фторалкилом, группами ацильных производных, галогеном;
или фармацевтически приемлемая соль или пролекарство,
при условии, что R1 не может являться галогеном, алкилом или алкокси, когда R2 представляет собой -СО-алкокси,
где вышеуказанные алкильные заместители содержат от 1 до 10 атомов углерода, алкокси заместители содержат от 1 до 4 атомов углерода, гетероарильные заместители содержат от 1 до 4 гетероатомов, гетероциклоалкильные заместители содержат от 1 до 4 гетероатомов, и
где группы производных кислот включают в себя группы сложных алкиловых эфиров и сложных карбамоиловых эфиров.
2. Соединения по п.1, где арильные, аралкильные, гетероарильные или гетероарилалкильные группы, возможно, замещены одной или несколькими аналогичными или различными группами, выбранными из галогена, алкокси, алкила, гидроксиалкила, алкилтио, амино, моно- или диалкиламино, гетероциклиламино, ариламино, гетероариламино, гетероарила, нитро, гетероциклоалкила, перфторалкила, перфторалкокси, перфторалкилтио, групп ацильных производных.
3. Соединения по п.1, где алкильные или алкиленовые заместители замещены одним или несколькими амино, аминоалкильными, аминоалкиламино, гидрокси, алкокси, гидроксиалкокси, ацильными группами, группами ацильных производных, алкильными, гетероалкильными, арилалкильными, ариламино, арилокси или арильными группами.
4. Соединения по п.1, где алкокси или алкилтио заместители замещены одним или несколькими амино, ацильными группами, группами ацильных производных, алкильными, арилалкильными или арильными группами.
5. Соединения по п.1, где ацильные группы или группы ацильных производных включают в себя группы карбоновых кислот и группы сульфоновых кислот или их производные.
6. Применение соединений формулы (I) при получении лекарственного средства для лечения злокачественных заболеваний.
Текст
006802 Область техники Настоящее изобретение относится к соединениям, пригодным для лечения патологических состояний, возникающих или обостряющихся в результате пролиферации клеток, к фармацевтическим композициям, включающим данные соединения, и к способам подавления пролиферации клеток у млекопитающих. Предпосылки изобретения Неопластические заболевания, характеризующиеся пролиферацией клеток, не подчиняющихся нормальным механизмам контроля пролиферации клеток, представляют собой основную причину смерти человека и других млекопитающих. Химиотерапия злокачественных опухолей предоставляет новые и более эффективные лекарственные средства для лечения данных заболеваний, а также демонстрирует то,что лекарственные средства, представляющие собой ингибиторы циклинзависимых киназ, являются эффективными для подавления пролиферации неопластических клеток. Регуляторы контрольных точек клеточного цикла определяют выбор клетки, продолжать ли прохождение по клеточному циклу. Прохождение клеточного цикла регулируют циклинзависимые киназы(CDK), активацию которых осуществляют различные представители семейства циклинов, что приводит к фосфорилированию субстрата и, в конечном счете, к делению клетки. Кроме того, активность CDK негативно регулируют эндогенные ингибиторы CDK (семейство INK4 и семейство KIP/CIP). Нормальный рост клеток представляет собой результат баланса между активаторами CDK (циклинами) и эндогенными ингибиторами CDK. Для отдельных типов злокачественных опухолей описана отклоняющаяся от нормы экспрессия или активность отдельных компонентов клеточного цикла.Cdk4 функционирует в фазе клеточного цикла G1 и ее активируют циклины типа D, что приводит к фосфорилированию субстрата и переходу в S-фазу. Единственным известным субстратом для cdk4 является продукт гена ретинобластомы (pRb), основной продукт гена-супрессора опухоли, действующего как основной регулятор контрольной точки при регуляции перехода фаз G1/S. Избыточное фосфорилирование pRb посредством CDK приводит к высвобождению E2F (семейство факторов транскрипции), связанных с pRb, которые затем активируют гены, необходимые для дальнейшего прохождения клеточного цикла, например гены тимидинкиназы, тимидилатсинтазы, циклина Е и циклина А. Циклин D1 амплифицирован или сверхэкспрессирован во многих типах злокачественных опухолей (молочной железы,яичников, мочевого пузыря, пищевода, легких, лимфоме), в то время как ген, кодирующий р 16, эндогенный ингибитор cdk4, во многих типах опухолей делегирован, мутирован или аберрантно метилирован. При меланоме описана точечная мутация cdk4, приводящая к отсутствию способности фермента связывать р 16, что приводит к постоянной активности фермента. Все описанные выше состояния приводят к активации cdk4, прохождению клеточного цикла и росту опухолевых клеток. Аргументы для определения CDK2 как противоракового средства можно найти в литературе: "Циклин Е активирует Cdk2, которая действует, фосфорилируя pRb, приводя к необратимому коммитированию клетки в направлении деления и входа в S-фазу" (PL Toogood, Medicinal Research Reviews (2001),21(6); 487-498. и "CDK2 (и, возможно, CDK3) необходима для прохождения G1 и входа в S-фазу. В комплексе с циклином Е она обеспечивает гиперфосфорилирование pRb, поддерживая прохождение черезG1 и в S-фазу. Кроме того, для CDK-циклина Е идентифицировали много других клеточных мишенейВ комплексе с циклином А CDK2 играет роль в инактивации E2F и необходима для завершения S-фазы."TD. Davies et. al. (2001) Structure 9, 389-397. Существует дополнительный уровень регуляции активности CDK. Активирующая киназу циклинзависимая киназа (САK) представляет собой положительный регулятор CDK. САK фосфорилирует каталитические CDK по консервативному остатку треонина, что делает фермент-мишень полностью активным. Поскольку дефекты молекул клеточного цикла приводят к активации CDK с последующим прохождением клеточного цикла, логично, что ингибирование ферментативной активности CDK должно блокировать прохождение клеточного цикла и рост опухолевых клеток. Первым ингибитором CDK, проходящим клинические испытания, является соединение, известное как флавопиридол. Данное соединение в настоящее время находится в фазе II клинических испытаний и в настоящее время является единственной молекулой в данном классе в клинике. Цель настоящего изобретения представляет собой получение молекул, более активных, чем флавопиридол. Из публикации WO 00/41669 известно, что производные бензимидазолкарбамата представляют собой повреждающие сосуды средства, которые можно применять для лечения злокачественных опухолей; заявленные в данной заявке на выдачу патента производные сульфонового сложного эфира не полностью проиллюстрированы примерами, и их механизм противоракового действия не описан. Данное изобретение конкретно относится к производным сульфоновых сложных эфиров данных карбаматов.-1 006802 Сущность изобретения В одном из осуществлений данного изобретения описаны соединения формулы (I) где А представляет собой фенил,R1 выбран из одной или нескольких аналогичных групп, выбранных из- алкокси, возможно, замещенного алкилом, гетероалкилом, арилом, гетероарилом, алкоксиалкилом, гидроксиалкиламидом или перфторалкоксигруппой или алкилтио, возможно, замещенного амидом или перфторалкилтио;- арила или гетероарила, возможно, замещенных одной или более алкильной группой, алкоксигруппой, нитрогруппой, цианогруппой, группой ацильного производного, перфторалкоксигруппой, перфторалкильной группой, гетероарильной группой, арилоксигруппой;- 4-NH2; 4-NH алкила или циклоалкила, возможно, замещенных ацилом, группой ацильного производного,гидрокси, амино, алкокси, гетероциклической или арильной группой;- СО-аралкила, возможно, замещенного алкокси, галогеном, амино, кислотной группой или группой производного кислоты;- СО-алкокси, возможно, замещенного арилом; СО-амино, CO-NHR3, СО-NR3R4, где R3 и R4 независимо выбраны из водорода, алкила, гидроксиалкила, алкоксиалкила, фторалкила, алкинила, гетероалкила, алкилгетероалкила, арила, аралкила, или вместе они образуют алкиленовую цепь, включающую в себя, возможно, от одного до 4 гетероатомов; арила или аралкила, возможно, замещенных гетероциклоалкилом, алкилом, арилом, алкокси, амино,фторалкилом, группами ацильных производных, галогеном; или фармацевтически приемлемая соль или пролекарство,при условии, что R1 не может являться галогеном, алкилом или алкокси, когда R2 представляет собой -СО-алкокси. Из соединений формулы (I) предпочтительными являются такие, где арильные, аралкильные, гетероарильные или гетероарилалкильные группы, возможно, замещены одной или несколькими аналогичными или различными группами, выбранными из галогена, алкокси, алкила, гидроксиалкила, алкилтио,амино, моно- или диалкиламино, гетероциклиламино, ариламино, гетероариламино, гетероарила, нитро,гетероциклоалкила, перфторалкила, перфторалкокси, перфторалкилтио, групп ацильных производных. В число замещенных алкильных или алкиленовых заместителей, включены такие, которые замещены одной или несколькими амино, аминоалкильной, аминоалкиламино, гидрокси, алкокси, гидроксиалкокси, ацильной группами, ацильными производными, алкильной, гетероалкильной, арилалкильной,ариламино, арилокси или арильной группами. В число алкокси или алкилтиозаместителей включены алкокси или алкилтиогруппы, замещенные одной или более амино, ацильными группами, ацильными производными, алкильными, арилалкильными или арильными группами. В число ацильных групп или групп ацильных производных включены карбоновые кислоты или сульфокислоты, производные которых являются в основном сложными эфирами или карбамоиловыми сложными эфирами. Алкильная цепь по настоящему изобретению включает в себя линейную, разветвленную или циклическую цепь, содержащую от 1 до 10 атомов углерода. Алкокси-цепь по настоящему изобретению включает в себя линейную, разветвленную или циклическую цепь, содержащую от 1 до 4 атомов углерода. Арильные группы включают в себя фенильные или нафтильные группы, гетероарильные группы, содержащие от одного до четырех гетероатомов, выбранных из S, N или О, такие как фурил, тиофен, изоксазол, оксазол, пиразол, фуран, пиридин. Гетероциклическая группа содержит от одного до четырех гетероатомов, выбранных из N, О, S и от 2 до 6 атомов углерода. Из данных соединений предпочтительными являются такие, которые содержат в алкильной цепи от 1 до 10 атомов углерода и которые содержат в циклоалкильной цепи от 3 до 5 атомов углерода. Когда-2 006802 алкильная цепь замещена алкоксигруппой, предпочтительно, чтобы данная последняя группа содержала один атом углерода. Из соединений формулы (I) наиболее предпочтительными являются следующие соединения: метил-5-(4-[2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4- [4-гидроксибутил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-метоксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[1-имидазолил]фенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-пиридилметил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-этиламинофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[N-глицинил]фенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[1-метил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-метил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-изопропиламинофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[1-этил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-бутиламинофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[3-метоксипропил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-метиламинофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-сульфонилэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-диэтиламиноэтил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[1-тетрагидрофурилметил]аминофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамат метил-5-(4-[2-фенилэтил]аминофенилсульфонилокси)бензимидазол-2-карбаматN-[5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2-ил]диметилмочевина 2-бензоиламино-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-фенилацетиламино-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(2-трет-бутоксикарбониламиноацетиламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1 илбензолсульфоновой кислоты метиловый эфир N-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-ил]сукцинамовой кислоты метиловый эфир 4-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-илкарбамоил]масляной кислоты метиловый эфир 4-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-илкарбамоил]масляной кислоты 2-(циклогексанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[(пиридин-2-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[(пиридин-3-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[(пиридин-4-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-пентаноиламино-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-гексаноиламино-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(2-циклопропилацетиламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(2-циклогексилацетиламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(2-метоксиацетиламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(2-диметиламиноацетиламино)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-бензоиламино-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-фенилацетиламино-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(2-трет-бyтoкcикapбoнилaминoaцeтилaминo)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты метиловый эфир-5 006802 2-[3-(2-гидроксиэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(4-фторфенил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(4-фторфенил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-хлорбензил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-хлорбензил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-фторбензил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-фторбензил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[(азетидин-1-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[(азетидин-1-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(3-пиридин-3-илметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(3-пиридин-3-илметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-3-[3-(4-метилпиперазин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1 илбензолсульфоновой кислоты 2-3-[3-(4-метилпиперазин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4 циклопентиламинобензолсульфоновой кислоты 2-(3-бензилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-(3-бензилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты метиловый эфир 4-3-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 ил]уреидомасляной кислоты этиловый эфир 4-3-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 ил]уреидомасляной кислоты метиловый эфир 4-3-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 ил]уреидоуксусной кислоты 2-[3-(3-имидазол-1-илпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 1-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2S-илкарбамоил]пирролидин-2 карбоновая кислота метиловый эфир 1-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2Sилкарбамоил]пирролидин-2-карбоновой кислоты 2-(3-карбамоилметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты этиловый эфир 1-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 илкарбамоил]пиперидин-4-карбоновой кислоты 2-(3-пиперидин-4-илметилуреидо)-1H-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-амино-2-метилпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(4-гидроксициклогексил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(3-гидроксипропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(1,1-диметилпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-3-[2-(2-гидроксиэтиламино)этил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(4-гидроксибутил)уреидо]-1H-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты-6 006802 2-3-[3-(2-оксопирролидин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-карбамоилэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[(2S-карбамоилпирролидин-1-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-3-[2-(2-гидроксиэтокси)этил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(3-пирролидин-1-илпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(1-этилпирролидин-2-илметил)уреидо]-1H-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-пирролидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-гидрокси-1-метилэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-изопропиламиноэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3-(2-диэтиламиноэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты метиловый эфир 2-3-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 ил]уреидо-3S-гидроксипропионовой кислоты метиловый эфир 4-3-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-ил]уреидомасляной кислоты этиловый эфир 4-3-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-ил]уреидомасляной кислоты метиловый эфир 3-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-ил]уреидоуксусной кислоты 2-[3-(3-имидазол-1-илпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 1-[5-(4-имидазол-1-илбензолсульфонилокси)-1H-бензимидазол-2-илкарбамоил]пирролидин-2-карбоновая кислота метиловый эфир 1-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2 илкарбамоил]пирролидин-2-карбоновой кислоты 2-(3-карбамоилметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты этиловый эфир 1-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-илкарбамоил]пиперидин-4-карбоновой кислоты 2-(3-пиперидин-4-илметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-амино-2-метилпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(4-гидроксициклогексил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(3-гидроксипропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(1,1-диметилпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-3-[2-(2-гидроксиэтиламино)этил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1 илбензолсульфоновой кислоты 2-[3-(4-гидроксибутил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-3-[3-(2-оксопирролидин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1 илбензолсульфоновой кислоты 2-[3-(2-карбамоилэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(1,1-диметилпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты-7 006802 2-[(2-карбамоилпирролидин-1-карбонил)амино]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1 илбензолсульфоновой кислоты 2-3-[2-(2-гидроксиэтокси)этил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(3-пирролидин-1-илпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(1-этилпирролидин-2-илметил)уреидо]-1H-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-пирролидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-гидрокси-1-метилэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-изопропиламиноэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты 2-[3-(2-диэтиламиноэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-имидазол-1-илбензолсульфоновой кислоты метиловый эфир 2-3-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Н-бензимидазол-2-ил]уреидо-3 гидроксипропионовой кислоты 2-(3-карбамоилметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-гидроксиэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(3-гидроксипропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(4-гидроксибутил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-метокси-1-метилэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-[3-(1-этилпирролидин-2-илметил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран 2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-пирролидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-[3-(3-пирролидин-1-илпропил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-(3-этилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-(3-метилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-1 Нбензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-(3-пиридин-3-илметилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-3-[3-(4-метилпиперазин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-сульфоэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-(3-циклобутилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-3-[3-(2-оксопирролидин-1-ил)пропил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2-илметил)амино]бензолсульфоновой кислоты 2-3-[2-(2-гидроксиэтиламино)этил]уреидо-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран 2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-бензиламинобензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-метиламинобензолсульфоновой кислоты 4-[3-(2-гидроксиэтилами 006802 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2 илметил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2Rилметил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(тетрагидрофуран-2S-илметил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-бутиламиноэтиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-метиламинопропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(1S,2-дикарбамоилэтиламино)бензолсульфоновой кислоты метиловый эфир 2-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламино-3R-гидроксипропионовой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-карбамоилэтиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-метоксипропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3,4,5-триметоксибензиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(карбамоилметиламино)бензолсульфоновой кислоты этиловый эфир 1-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилпиперидин-4-карбоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-амино-2-метилпропиламино)бензолсульфоновой кислоты метиловый эфир 3-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламинопропионовой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-морфолин-4-илпропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(5-гидроксипентиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-[(5S-амино-2,2,4S-триметилциклопентилметил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-гидроксиметилфениламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-этоксифениламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-этиламинобензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-сульфоэтиламино)бензолсульфоновой кислоты этиловый эфир 4-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламинопиперидин-1-карбоновой кислоты 4-(4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламинометил)бензойная кислота 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(1-карбамидоил-пиперидин-4 илметил)амино]бензолсульфоновой кислоты трет-бутиловый эфир 4-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилпиперазин-1-карбоновой кислоты 3-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламино-3-фенилпропионовая кислота 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-пиперидин-1-илбензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(1-метил-4-оксоимидазолидин 2-илиденамино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-метилпиперазин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-гидроксипирролидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(циклопропилметиламино)бензолсульфоновой кислоты 4-[(1-карбамоилпиперидин-44-(2-пиррол-1-илэтилами эфир 4-(4-циклопентилпиперазин-1 эфир 4-(2-пропоксиэтиламино)бензолэфир 4-(3-циклогексиламинопропилэфир 4-(1 Н-индол-5-иламино)бензолэфир 4-(4-аминобензиламино)бензолэфир 4-(2S-метоксиметилпирролидинэфир 4-[4-(2-гидроксиэтил)пиперидинэфир 4-[2-(2-гидроксиэтил)пиперидинэфир 4-(2-изопропиламиноэтилами 006802 3-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламинопропионовая кислота 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[метил-(2-метиламиноэтил)амино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(3-ацетиламинопирролидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(карбамоилметиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-диметиламинобензиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-имидазол-1-илпропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(хиноксалин-5-иламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[4-(2-гидроксиэтил)пиперазин 1-ил]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(2-гидрокси-1,1-диметилэтиламино)бензолсульфоновой кислоты 1-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилпиперидин-4 карбоновая кислота метиловый эфир 6-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фениламиногексановой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-[4-(4-метоксифенил)пиперазин 1-ил]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[4-(2-метоксиэтил)пиперазин-1 ил]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(2-гидроксиэтил)фениламино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[(фуран-2-илметил)амино]бензолсульфоновой кислоты метиловый эфир 1-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилазиридин-2-карбоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-карбамоилпиперидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-метилпиперазин-1-ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2,6-диметилморфолин-4 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-фенилпиперазин-1-ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-пиридин-2-илпиперазин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-диэтиламино-1-метилбутиламино)бензолсульфоновой кислоты этиловый эфир 4-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилпиперазин-1-карбоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(5-гидроксинафталин-1-иламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[2-(4-гидрокси-3-метоксифенил)этиламино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(9 Н-пурин-6-иламино)бензолсульфоновой кислоты 1-4-[2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илоксисульфонил]фенилпиперидин-3 карбоновая кислота 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(3,3-диметилпиперидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(4-метилпиперидин-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(2-пиридин-2-илэтиламино)бензолсульфоновой кислоты- 13006802 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(3-гидроксиметилфениламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2-оксо-2,3-дигидро-1 Нпиримидин-4-илиденамино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-пиперидин-1-илпропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[2-(1H-индол-3-ил)этиламино]бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(5-карбамоил-1 Н-имидазол-4 иламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(1-гидроксиметилбутиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1H-бензимидазол-5-иловый эфир 4-(1-бензилпиперидин-4 иламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-4-[2-(2-гидроксиэтокси)этил]пиперазин-1-илбензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(4-метил-[1,4]диазепан-1 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(3-азепан-1-илпропиламино)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2,6-цисдиметилморфолин-4 ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-(2S-гидроксиметилпирролидин-1-ил)бензолсульфоновой кислоты 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-иловый эфир 4-[4-(3-пирролидин-1-илпропил)[1,4]диазепан-1-ил]бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-трифторметоксибензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 3,5-диметилизоксазол-4-сульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир тиофен-2-сульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 5-изоксазол-3-илтиофен-2-сульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 2-фторбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 5-(1-метил-5-трифторметил-1 Нпиразол-3-ил)тиофен-2-сульфоновой кислоты 2-метоксикарбониламино-1 Н-бензоимидазол-5-иловый эфир 3-трифторметоксибензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензоимидазол-5-иловый эфир 2-трифторметоксибензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 2,6-дифторбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 3-метоксибензолсульфоновой кислоты метиловый эфир 3-(2-метоксикарбониламино-1 Н-бензимидазол-5-илоксисульфонил)тиофен-2 карбоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 3,4-диметоксибензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 3-нитробензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензоимидазол-5-иловый эфир 3-трифторметилбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 2-цианобензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензоимидазол-5-иловый эфир 2-трифторметилбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 2,4-дифторбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензоимидазол-5-иловый эфир 5-фтор-2-метилбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 3-фторбензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-цианобензолсульфоновой кислоты метиловый эфир 2-метокси-5-(2-метоксикарбониламино-3 Н-бензимидазол-5-илоксисульфонил)тиофен-3-карбоновой кислоты 2-метоксикарбониламино-3H-бензимидазол-5-иловый эфир 1,3,5-триметил-1 Н-пиразол-4 сульфоновой кислоты[4-(2-метоксикарбониламино-3H-бензимидазол-5-илоксисульфонил)фенокси]уксусная кислота 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(2-оксо-2-пирролидин-1 илэтокси)бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-[2-(4-метилпиперазин-1-ил)-2 оксоэтокси]бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-[(3-диэтиламинопропилкарбамоил)метокси]бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-[(фуран-2-илметил)карбамоил]метоксибензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(циклопропилметиламино)бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(2-метоксиэтиламино)бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(2-гидрокси-1-метилэтиламино)бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(бензиламино)бензолсульфоновой кислоты 2-метоксикарбониламино-1 Н-бензимидазол-5-иловый эфир 4-(2-морфолин-4-илэтиламино)бензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-пиперидин-4 илэтиламино)бензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-[(1-этилпирролидин-2 илметил)амино]бензолсульфоновой кислоты 2-(3,4-диметоксифениламино)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-фениламино-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(4-морфолин-4-илфениламино)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(3,5-диметилфениламино)-1H-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(4-метоксифениламино)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(4-диметиламинофениламино)-1H-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсулфоновой кислоты 2-(3-метокси-5-трифторметилфениламино)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты этиловый эфир 3-[5-(4-циклопентиламинобензолсульфонилокси)-1 Н-бензимидазол-2 иламино]бензойной кислоты 2-[4-(4-метилпиперазин-1-ил)фениламино]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-(3-фенилпропиониламино)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[2-(2-метоксиэтокси)ацетиламино]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 2-[3(хлор-4-метоксибензил)амино]-3H-бензимидазол-5-иловый эфир 4-фторбензолсульфоновой кислоты 2-[(3-фенил-[1,2,4]оксадиазол-5-илметил)амино]-3H-бензимидазол-5-иловый эфир 4-фторбензолсульфоновой кислоты 2-(3-хлорбензиламино)-3H-бензимидазол-5-иловый эфир 4-фторбензолсульфоновой кислоты- 16006802 2-[(4-гидроксипиперидин-1-карбонил)амино]-1H-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1-ил)бензолсульфоновой кислоты 2-[(4-метилпиперазин-1-карбонил)амино]-3H-бензимидазол-5-иловый эфир 4-(4-метилпиперазин-1 ил)бензолсульфоновой кислоты 2-[3-(тетрагидропиран-4-илметил)уреидо]-3H-бензимидазол-5-иловый эфир 4-[(тетрагидропиран-4 илметил)амино]бензолсульфоновой кислоты 2-[3-(2-фторэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-фторэтиламино)бензолсульфоновой кислоты 2-[3-(2-пиперидин-1-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-пиперидин-1 илэтиламино)бензолсульфоновой кислоты 2-(3-фенэтилуреидо)-3H-бензимидазол-5-иловый эфир 4-фенэтиламинобензолсульфоновой кислоты 2-3-[3-(2-оксопирролидин-1-ил)пропил]уреидо-3H-бензимидазол-5-иловый эфир 4-[3-(2-оксопирролидин-1-ил)пропиламино]бензолсульфоновой кислоты 2-[3-(4-фторбензил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-фторбензиламино)бензолсульфоновой кислоты 2-[3-(2-гидрокси-3-метилпропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-гидрокси-2 метилпропиламино)бензолсульфоновой кислоты 2-[3-(3-гидроксипропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(3-гидроксипропиламино)бензолсульфоновой кислоты 2-[3-(2,2,6,6-тетраметилпиперидин-4-ил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2,2,6,6 тетраметилпиперидин-4-иламино)бензолсульфоновой кислоты 2-[3-(2-диметиламиноэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-диметиламиноэтиламино)бензолсульфоновой кислоты 2-[(морфолин-4-карбонил)амино]-3H-бензимидазол-5-иловый эфир 4-морфолин-4-илбензолсульфоновой кислоты 2-[3-(2-гидрокси-3-метоксипропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-гидрокси-3 метоксипропиламино)бензолсульфоновой кислоты 2-(3-пиридин-2-илэтилуреидо)-3H-бензимидазол-5-иловый эфир 4-[(пиридин-2-илметил)амино]бензолсульфоновой кислоты 2-[3-(2-гидроксипропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-гидроксипропиламино)бензолсульфоновой кислоты 2-[3-(4-метоксибензил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-[3-(2-пирролидин-1-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-пирролидин-1 илэтиламино)бензолсульфоновой кислоты 2-[3-(1-фенилэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(1-фенилэтиламино)бензолсульфоновой кислоты 2-[3-(2-диэтиламиноэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-диэтиламиноэтиламино)бензолсульфоновой кислоты 2-[3-(1-гидроксиметилциклопентил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(1-гидроксиметилциклопентиламино)бензолсульфоновой кислоты метиловый эфир 3-(4-2-[3-(3-метоксикарбонилэтил)уреидо]-1 Н-бензимидазол-5-илоксисульфонилфениламино)пропионовой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1 ил)бензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метилпиперазин-1 ил)бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 4-(4-метилпиперазин-1-ил)бензолсульфоновой кислоты 2-[3-(2-метоксиэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метилпиперазин-1-ил)бензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1 ил)бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1 ил)бензолсульфоновой кислоты 2-[3-(2-метоксиэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1-ил)бензолсульфоновой кислоты 2-(3-этилуреидо)-3H-бензимидазол-5-иловый эфир 4-(4-гидроксипиперидин-1-ил)бензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-[(пиридин-2-илметил)амино]бензолсульфоновой кислоты- 18006802 2-[3-(3-гидроксипропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-фенэтиламинобензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-гидроксипропиламино)бензолсульфоновой кислоты 2-(3-этилуреидо)-3H-бензимидазол-5-иловый эфир 4-(2-гидроксипропиламино)бензолсульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-(3-этилуреидо)-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-[3-(3-гидроксипропил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-[3-(2-метоксиэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(4-метоксибензиламино)бензолсульфоновой кислоты 2-(3-этилуреидо)-3H-бензимидазол-5-иловый эфир 4-(2-пирролидин-1-илэтиламино)бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 4-(2-пирролидин-1-илэтиламино)бензолсульфоновой кислоты 2-[3-(2-метоксиэтил)уреидо]-3H-бензимидазол-5-иловый эфир 4-(2-пирролидин-1-илэтиламино)бензолсульфоновой кислоты 2-(3-этилуреидо)-3H-бензимидазол-5-иловый эфир 4-(1-фенилэтиламино)бензолсульфоновой кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 4-(2-диэтиламиноэтиламино)бензолсульфоновой кислоты 2-[3-(2-этил)уреидо]-1 Н-бензимидазол-5-иловый эфир тиофен-2-сульфоновой кислоты 2-[3-(2-метоксиэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир тиофен-2-сульфоновой кислоты 2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-иловый эфир тиофен-2-сульфоновой кислоты 2-(3-пиридин-2-илметил)уреидо]-1 Н-бензимидазол-5-иловый эфир тиофен-2-сульфоновой кислоты 4-2-[3-(2-метоксиэтил)уреидо]-1 Н-бензимидазол-5-илоксисульфонилфениловый эфир 4-2-[3-(2-морфолин-4-илэтил)уреидо]-1 Н-бензимидазол-5-илоксисульфонилфениловый эфир бензойной кислоты 4-[2-([3-пиридин-2-илметил]уреидо)-1 Н-бензимидазол-5-илоксисульфонил]фениловый эфир бензойной кислоты 2-(3-пиридин-2-илметилуреидо)-3H-бензимидазол-5-иловый эфир 2,6-дифторбензолсульфоновой кислоты 3-(2-метоксиэтил)-3H-бензимидазол-5-иловый эфир 2,6-дифторбензолсульфоновой кислоты. Еще в одном осуществлении описано применение соединений формулы (I) при получении лекарственного средства для лечения злокачественных заболеваний. Термин "фармацевтически допустимая соль", как применяют здесь, относится к солям, подходящим для применения в контакте с тканями людей и низших животных. Фармацевтически допустимые соли подробно описаны в J. Pharmaceutical sciences, 1977, 66:1 и, следовательно, включенному сюда посредством ссылки. Характерные кислотные аддитивные соли включают в себя ацетат, цитрат, аспартат, бензолсульфонат, гидрохлорид, лактат, малеат, метансульфонат, оксалат и фосфат. Способы синтеза Соединения по настоящему изобретению можно легко получить, исходя из 2-амино-5-(-4 фторфенилсульфонилокси)нитробензола, способ получения которого описан в US 3996368. На первой стадии данное исходное вещество взаимодействует с амином, несущим радикал R1, в подходящем для проведения реакции растворителе. Среди растворителей, подходящих для растворения 2-амино-5-(-4-фторфенилсульфонилокси)нитробензола и амина, можно указать гликоли, такие как этилгликоль, апротонные растворители, такие как диоксан, диметилформамид, N-метилпирролидинон. Предпочтительная температура для данной реакции представляет собой температуру от комнатной температуры до температуры образования флегмы. Для получения промежуточного продукта предпочтительно осаждать промежуточное соединение соляной кислотой. На второй стадии соединение, полученное на стадии 1, гидрируют водородом, предпочтительно в присутствии никеля Ренея (способ А восстановления нитрогрупп) или палладия на углероде (способ В восстановления нитрогрупп) в подходящем растворителе, выбранном среди такого же списка, как и для стадии 1, в смеси со спиртом, таким как метанол. После реакции катализатор удаляют фильтрованием. На третьей стадии бензимидазольное кольцо закрывают посредством воздействия 1,3 бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины на промежуточное соединение, полученное на- 19006802 стадии 2 без промежуточного выделения. Реакционную смесь кипятят с обратным холодильником при перемешивании. Конечный продукт (метилбензимидазол-2-карбамат) выделяют после выпаривания растворителя при пониженном давлении и растворения в этилацетате дальнейшей кристаллизацией. Окончательную очистку проводят в метаноле с кристаллизацией в том же самом растворителе. Метилбензимидазол-2-карбамат можно преобразовать в бензимидазол-2-мочевины посредством обработки амином в подходящем растворителе, таком как диметилформамид, тетрагидрофуран или Nметилпирролидинон в присутствии основания, такого как 1,8-диазабицикло[5.4.0]ундец-7-ен в автоклаве. Предпочтительная температура для данной реакции представляет собой температуру от комнатной температуры до 120 С. трет-Бутилбензимидазол-2-карбамат можно получить посредством проведения третьей стадии, описанной выше, с применением вместо 1,3-бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины 1,3 бис(трет-бутоксикарбонил)-2-метил-2-тиопсевдомочевины. Данные производные можно преобразовывать в соответствующее производное 2-Аминобензимидазола с применением способов снятия защиты трет-бутилкарбамата, известных специалистам в данной области. 2-Аминобензимидазолы можно преобразовывать в соответствующие амиды посредством взаимодействия с производными карбоновой кислоты с применением производных, известных специалистам в данной области. Способы лечения Настоящее изобретение также относится к фармацевтическим композициям, включающим соединения по настоящему изобретению, составленных совместно с одним или несколькими нетоксичным фармацевтически допустимыми носителями. Фармацевтические композиции можно составлять конкретно для орального введения в твердой или жидкой форме или для парентеральной инъекции. Как используется здесь, термин "парентеральный" относится к способам введения, включающим внутривенный, внутримышечный, интраперитонеальный, подкожный и инфузию. Твердые стандартные лекарственные формы для орального введения включают в себя капсулы,таблетки, пилюли, порошки и гранулы. В данных твердых дозированных формах активное соединение смешивают, по меньшей мере, с одним инертным, фармацевтически допустимым наполнителем или носителем. Твердые композиции подобного типа можно также применять в качестве наполнителя в мягких и наполненных твердым наполнителем желатиновых капсулах. Соединения по настоящему изобретению можно вводить отдельно или смешивать с другими противораковыми средствами. Среди возможных комбинаций можно упомянуть следующие: алкилирующие средства, в частности, циклофосфамид, мелфалан, изосфамид, хлорамбуцил, бусульфан, тиотепа, преднимустин, кармустин, ломустин, семустин, стрептозотоцин, декарбазин, темозоломид, прокарбазин и гексаметилмеламин- производные платины, такие как, например, цисплатин, карбоплатин или оксалиплатин,- антибиотики, такие как, например, блеомицин, митомицин, дактиномицин,- средства, направленные против микротрубочек, такие как, например, винбластин, винкристин,виндезин, винорельбин, таксоиды (паклитаксел и доцетаксел),антрациклины, такие как, например, доксорубицин, даунорубицин, идарубицин, эпирубицин, митоксантрон, лозоксантрон,топоизомеразы I и II групп, такие как этопозид, тенипозид, амсакрин, иринотекан, топотекан и томудекс,фторпиримидины, такие как 5-фторурацил, UFT, фтороксиуридин,аналоги цитидина, такие как 5-азацитидин, цитарабин, гемцитабин, 6-меркаптопурин, 6-тиогуанин,аналоги аденозина, такие как пентостатин, фосфаты цитарабина или флударабина,- метотрексат и формилтетрагидрофолиевая кислота,различные ферменты и соединения, такие как L-аспарагиназа, гидроксимочевина, трансретиноловая кислота, сурамин, дексразоксан, амифостин, герцептин, а также эстрогенные и андрогенные гормоны. Также с соединениями по настоящему изобретению возможно комбинировать радиационную терапию. Данное лечение можно проводить одновременно, раздельно или последовательно. Лечащий врач может адаптировать лечение для подвергающегося лечению пациента. Данное изобретение более подробно описано в примерах, следующих ниже, которые не следует рассматривать как ограничение изобретения. Способ аналитического определения Жидкостная хроматография, совмещенная с масс-спектрометрическим анализом (ЖХ/МС) Анализы ЖХ/МС проводили на устройстве Micromass модели LCT, соединенном с устройством модели HP 1100. Относительное содержание соединения определяли с применением фотодиодного матричного детектора HP G1315A (модель) в диапазоне длин волн 200-600 нм и испарительного детектора светового рассеяния Sedex 65 (модель). Спектр массы получали в диапазоне от 160 до 2000 а.е.м. Данные анализировали с применением программного обеспечения Micromass MassLynx. Разделение проводили на колонке (50 х 4,6 мм) с Hypersil Highpurity С 18, с частицами размером 5 мкм, элюируя линейным гра- 20006802 диентом от 10 до 90% ацетонитрила, содержащего 0,05% (об./об.) трифторуксусной кислоты (TFA) в воде, содержащей 0,05% (об./об.) TFA в течение 6,5 мин при скорости потока 1 мл/мин. Способ очистки Очистка переключаемой ЖХ/МС Соединения очищали посредством ЖХ/МС с применением системы Waters FractionLynx, составленной из градиентного насоса Waters модели 600, регенерирующего насоса Waters модели 515, подпиточного насоса Waters Reagent Manager, устройства управления автоматическим вводом образцов Waters 2700, двух переключателей Rheodyne модели LabPro, фотодиодного матричного детектора Waters модели 996, масс-спектрометра Waters модели ZMD и коллектора фракций Gilson модели 204. Прибор управлялся программным обеспечением Waters FractionLynx. Разделение проводили альтернативно на двух колонках Waters Symmetry (C18, 5 мкм, 19 х 50 мм, каталожный номер 186000210); одну колонку регенерировали посредством смеси вода/ацетонитрил 95/5 (об./об.), содержащей 0,07% TFA (об./об.), в то время как на другой проводили разделение. Колонки элюировали линейным градиентом от 5 до 95% (об./об.) ацетонитрила, содержащего 0,07% (об./об.) TFA, в воде, содержащей 0,07% (об./об.) TFA, в течение 8 мин и 2 мин в 95% ацетонитриле, содержащем 0,07% (об./об.) TFA, при скорости потока 10 мл/мин. На выходе из разделяющей колонки поток разделяли в соотношении 1/1000 с применением делителя LCPacking AccuRate; 1/1000 потока смешивали с метанолом (скорость потока 0,5 мл/мин) и посылали на детекторы, данный поток опять разделяли, посылая 3/4 потока на фотодиодный матричный детектор, и 1/4 на масс-спектрометр; остальной продукт с колонки (999/1000) подавали на коллектор фракций, где поток обычно направляли в отходы, пока программное обеспечение FractionLynx не детектировало сигнал, соответствующий ожидаемой массе. Программное обеспечение FractionLynx снабжали молекулярными формулами ожидаемых соединений, и оно запускало сбор компонентов, когда определяло сигнал, соответствующий[М+Н]+ и [М+Na]+. В определенных случаях (в зависимости от аналитических результатов ЖХ/МС, когда определяли [М+2 Н] как сильный ион), программное обеспечение FractionLynx дополнительно снабжали расчетной величиной половины молекулярной массы (MW/2), в данных условиях сбор запускали также, когда определяли сигнал, соответствующий массе [М+2 Н] и [M+Na+H]. Соединение собирали в просмоленные стеклянные пробирки. После сбора растворитель выпаривали в центрифужном испарителе Jouan модели RC 10.10 или в центрифужном испарителе Genevac модели НТ 8 и определяли количество соединения взвешиванием пробирок после выпаривания растворителя. Способ получения соединений по данному изобретению Исходное вещество, 2-амино-5-(4-фторфенилсульфонилокси)нитробензол (точка плавления 161 С),можно получить в соответствии с патентом США 3996368. Пример 1. Получение метил-5-(4-[2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2 карбамата Стадия 1: 15,6 г 2-Амино-5-(4-фторфенилсульфонилокси)нитробензола смешивали с 25 мл этаноламина в 100 мл этиленгликоля в круглодонной колбе. Реакционную смесь в течение 90 мин кипятили с обратным холодильником и затем охлаждали на льду. Затем реакционную смесь разбавляли 250 мл 2 н. водной НСl, соединение осаждали и отфильтровывали с отсасыванием. Осадок промывали водой и сушили с получением 15,5 г 2-амино-5-(4-[2-гидроксиэтил]аминофенилсульфонилокси)нитробензола (точка плавления 180 С). Стадия 2: 15,5 г 2-Амино-5-(4-[2-гидроксиэтил]аминофенилсульфонилокси)нитробензола в 75 мл метанола и 75 мл диметилформамида гидрировали при атмосферном давлении в присутствии каталитического количества никеля Ренея (способ А). После окончания поглощения водорода, катализатор отфильтровывали с отсасыванием, промывали метанолом и концентрировали фильтрат при пониженном давлении. Стадия 3: концентрированный фильтрат со стадии 2 помещали в 150 мл метанола и 30 мл ледяной уксусной кислоты, добавляли 10,3 г 1,3-бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины и реакционную смесь в течение 3 ч кипятили с обратным холодильником при перемешивании. Потом растворители выпаривали при пониженном давлении, затем концентрат растворяли в горячем этилацетате, кристаллизовали охлаждением и промывали этилацетатом. Далее компоненты растворяли в 250 мл кипящего с обратным холодильником метанола, кристаллизовали охлаждением, промывали метанолом и высушивали с получением 7,4 г указанного в заголовке соединения. (Точка плавления 170 С, анализ ЖХ/МС: время удержания = 2,8 мин, масс спектр: 407,24, [М+Н]+). Стадия 1: 19,7 г 2-Амино-5-(4-фторфенилсульфонилокси)нитробензола смешивали с 20 г бутаноламина в 200 мл N-метипирролидинона в круглодонной колбе. Реакционную смесь в течение 120 мин кипятили с обратным холодильником и затем выпаривали растворитель при пониженном давлении. Затем концентрат растворяли в этилацетате и экстрагировали 2 н. водной НСl и водой, и затем обезвоживали над сульфатом натрия и высушивали при пониженном давлении. Концентрат перекристаллизовывали в изопропаноле, фильтровали с отсасыванием, промывали изопропанолом и высушивали с получением 13,1 г 2-амино-5- (4-[4-гидроксибутил]аминофенилсульфонилокси)нитробензола (точка плавления 105 С). Стадия 2: 13,1 г 2-Амино-5- (4- [4-гидроксибутил]аминофенилсульфонилокси)нитробензола в 75 мл метанола и 75 мл диметилформамида гидрировали при атмосферном давлении в присутствии каталитического количества никеля Ренея (способ А). После окончания поглощения водорода катализатор отфильтровывали с отсасыванием, промывали метанолом и фильтрат концентрировали при пониженном давлении. Стадия 3: концентрированный фильтрат со стадии 2 помещали в 100 мл метанола и 20 мл ледяной уксусной кислоты, добавляли 8,2 г 1,3-бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины и реакционную смесь в течение 3 ч кипятили с обратным холодильником при перемешивании. Затем растворители выпаривали при пониженном давлении, концентрат промывали 2 н. водным аммиаком, водой и высушивали. Затем концентрат растворяли в горячем этилацетате, кристаллизовали охлаждением и промывали этилацетатом. Затем соединение растворяли в кипящем с обратном холодильником метаноле, кристаллизовали охлаждением, промывали метанолом и высушивали с получением 6,3 г указанного в заголовке соединения. (Точка плавления 180 С, анализ ЖХ/МС: время удержания =2,9 мин, масс спектр: 435,29, [М+Н]+). Пример 3. Получение метил-5-(4-[2-метоксиэтил]аминофенилсульфонилокси)бензимидазол-2 карбамата Стадия 1: 15,6 г 2-амино-5-(4-фторфенилсульфонилокси)нитробензола смешивали с 30 мл метоксиэтиленамина в 100 мл диоксана в круглодонной колбе. Реакционную смесь в течение 8 ч кипятили с обратным холодильником и затем охлаждали до 40 С и дважды экстрагировали 250 мл воды. Концентрат растворяли в этилацетате и экстрагировали 2 н водной НСl и водой, затем органическую фазу высушивали при пониженном давлении с получением 19,2 г 2-амино-5-(4-[2-метоксиэтил]аминофенилсульфонилокси)нитробензола (точка плавления 105 С). Стадия 2: 18,2 г 2-Амино-5-(4-[2-метоксиэтил]аминофенилсульфонилокси)нитробензола в 75 мл метанола и 75 мл диметилформамида гидрировали при атмосферном давлении в присутствии каталитического количества никеля Ренея (способ А). После окончания поглощения водорода катализатор отфильтровывали отсасыванием, промывали метанолом и фильтрат концентрировали при пониженном давлении. Стадия 3: концентрированный фильтрат со стадии 2 помещали в 150 мл метанола и 25 мл ледяной уксусной кислоты, добавляли 12,3 г 1,3-бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины и реакционную смесь в течение 3 ч кипятили с обратным холодильником при перемешивании. Затем растворители выпаривали при пониженном давлении, концентрат кристаллизовали в метаноле, насыщенном аммиаком, промывали водой, метанолом и высушивали с получением указанного в заголовке соединения 12 г. Стадия 1: 15,6 г 2-Амино-5-(4-фторфенилсульфонилокси)нитробензол смешивали с 20,7 г имидазола в 100 мл диметилформамида в круглодонной колбе. Реакционную смесь в течение 3 ч кипятили с об- 22006802 ратным холодильником и затем охлаждали до комнатной температуры. Затем реакционную смесь осаждали добавлением воды, фильтровали и промывали осадок водой и высушивали. Осадок перерастворяли в горячем метилгликоле, кристаллизовали охлаждением, промывали кристаллы метанолом и высушивали с получением 10,4 г 2-амино-5-(4-[1-имидазолил]фенилсульфонилокси)нитробензола (точка плавления 209 С). Стадия 2: 10,4 г 2-Амино-5-(4-[1-имидазолил]фенилсульфонилокси)нитробензола в 75 мл метанола и 75 мл диметилформамида гидрировали при атмосферном давлении в присутствии каталитического количества никеля Ренея. После окончания поглощения водорода катализатор отфильтровывали отсасыванием, промывали метанолом и концентрировали фильтрат при пониженном давлении (способ А). Альтернативно 5 г 2-амино-5- (4-[1-имидазолил]фенилсульфонилокси)нитробензола в 475 мл метанола и 25 мл диметилформамида гидрировали в течение 6 ч в присутствии 10% (мас./мас.) палладия на углероде при давлении 5 бар при 30 С (способ В) с получением 4,18 г (91%) ожидаемого продукта. Стадия 3: Концентрированный фильтрат со стадии 2 помещали в 150 мл метанола и 25 мл ледяной уксусной кислоты, добавляли 10,3 г 1,3-бис(метоксикарбонил)-2-метил-2-тиопсевдомочевины и реакционную смесь в течение 3 ч кипятили с обратным холодильником при перемешивании. После охлаждения до комнатной температуры реакционную смесь осаждали добавлением этилацетата, фильтровали отсасыванием и промывали этилацетатом. Затем фильтрат перерастворяли в 50 мл диметилформамида и добавляли 250 мл метанола. Смесь кристаллизовали охлаждением, промывали кристаллы метанолом и высушивали при пониженном давлении с получением 9,4 г указанного в заголовке соединения. (Точка плавления 258 С, анализ ЖХ/МС: время удержания = 2,5 мин, масс спектр: 414,23, [М+Н]+; 382,19,фрагментация карбамата: потеря метанола, NMR, IR). Пример 5. Получение метил-5-(4-[2-пиридилметил]аминофенилсульфонилокси)бензимидазол-2 карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 2-аминометилпиридина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания =2,6 мин, масс спектр: 454,28, [М+Н]+; 907,53, [2 М+Н]+; 422,24, фрагментация карбамата: потеря метанола). Пример 6. Получение метил-5-(4-этиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия этиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,2 мин, масс спектр: 390,98, [М+Н]+). Пример 7. Получение метил-5-(4-[N-глицинил]фенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия глицина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,8 мин, масс спектр: 421,21, [М+Н]+). Пример 8. Получение метил-5-(4-[1-метил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2 карбамата- 23006802 Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 2-аминопропанола с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,9 мин, масс спектр: 421,27, [М+Н]+). Пример 9. Получение метил-5-(4-[2-метил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2 карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 1-метил,2-аминоэтанола с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,9 мин, масс спектр: 421,27, [М+Н]+). Пример 10. Получение метил-5-(4-изопропиламинофенилсульфонилокси)бензимидазол-2 карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия изопропиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,4 мин, масс спектр: 405,27, [М+Н]+). Пример 11. Получение метил-5-(4-[1-этил,2-гидроксиэтил]аминофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 2-аминобутанола с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,0 мин, масс спектр: 435,30, [М+Н]+). Пример 12. Получение метил-5-(4-бутиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия бутиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,6 мин, масс спектр: 419,25, [М+Н]+). Пример 13: Получение метил-5-(4-[3-метоксипропил]аминофенилсульфонилокси)бензимидазол-2 карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 3-метоксипропаноламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания =3,2 мин, масс спектр: 435,27, [М+Н]+). Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия метиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,0 мин, масс спектр: 377,22, [М+Н]+). Пример 15. Получение метил-5-(4-[2-сульфонилэтил]аминофенилсульфонилокси)бензимидазол-2 карбамат Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 2-аминоэтансульфоновой кислоты с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,6 мин, масс спектр: 471,19, [М+Н]+; 941,41,[2 М+Н]+). Пример 16. Получение метил-5-(4-аминофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия аммиака с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,9 мин, масс спектр: 363,19, [M+Н]+). Пример 17. Получение метил-5-(4-[2-диэтиламиноэтил]аминофенилсульфонилокси)бензимидазол 2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия 2-диэтиламиноэтиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 2,6 мин, масс спектр: 462,34, [М+Н]+; 923,65, [2 М+Н]+; 430,30, фрагментация карбамата: потеря метанола). Пример 18. Получение метил-5-(4-[1-тетрагидрофурилметил]аминофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия тетрагидрофурфуриламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,2 мин, масс спектр: 447,24, [М+Н]+). Пример 19. Получение метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2 карбамата- 25006802 Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия циклопентиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,6 мин, масс спектр: 431,29, [М+Н]+). Пример 20. Получение метил-5-(4-[2-фенилэтил]аминофенилсульфонилокси)бензимидазол-2 карбамата Способом, подобным способу в примерах с 1 по 4, указанное в заголовке соединение получали посредством взаимодействия фенэтиламина с 2-амино-5-(4-фторфенилсульфонилокси)нитробензолом на стадии 1 описанного выше способа и применяя способ восстановления нитрогруппы А. (Анализ ЖХ/МС: время удержания = 3,6 мин, масс спектр: 467,26, [М+Н]+). Пример 21. Получение N-5-(4-[1-имидазолил]фенилсульфонилокси)-1 Н-бензимидазол-2-ила, представляющего собой промежуточное соединение для синтеза амидных продуктов На стадиях 1 и 2 промежуточный продукт указанного в заголовке соединения получали способом,подобным стадиям 1 и 2 примера 4. Стадия 3: 8 г соединения стадии 2 помещали в 128 мл метанола и 21,6 мл уксусной кислоты в круглодонной колбе объемом 250 мл. Смесь кипятили с обратным холодильником и добавляли 9,13 г 1,3 бис(трет-бутоксикарбонил)-2-метил-2-тиопсевдомочевины. Реакционную смесь в течение 4 ч кипятили с обратным холодильником при помешивании. Твердое вещество получали посредством охлаждения в течение одного часа при 0 С и промывали этилацетатом, растирали и высушивали на стеклянной фритте с получением 7,55 г соединения. Стадия 4: Соединение стадии 3 помещали в 80 мл дихлорметана и 40 мл трифторуксусной кислоты. Реакционную смесь перемешивали в течение 4 ч при комнатной температуре. Растворители выпаривали при пониженном давлении. Концентрированный фильтрат обрабатывали в 75 мл воды и 50 мл водного раствора карбоната натрия (10% мас./мас.). Полученный осадок промывали дихлорметаном и сушили на стеклянной фритте с получением 5,3 г указанного в заголовке соединения. Пример 22. Получение N-5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2-ила,представляющего собой промежуточное соединение для синтеза амидных продуктов На стадиях 1 и 2 промежуточный продукт указанного в заголовке соединения получали способом,подобным стадиям 1 и 2 примера 19. На стадиях 3 и 4 указанное в заголовке соединение получали способом, подобным способу в примере 21. Пример 23. Получение метилового эфира N-[5-(4-имидазол-1-илбензолсульфонилокси)-1 Нбензимидазол-2-ил]сукцинамовой кислоты Стадия 1: 8,9 мг метилового эфира сукцинамовой кислоты, 25 мг 2-(1 Н-бензотриазол-1-ил)-1,1,3,3 тетраметилуронийгексафторфосфата (HBTU) и 12 мкл диизопропилэтиламина помещали в 0,4 мл диметилформамида. Реакционную смесь в течение одного часа перемешивали при комнатной температуре и добавляли N-5-(4-[1-имидазолил]фенилсульфонилокси)-1 Н-бензимидазол-2-ил в 0,2 мл диметилформамида. Затем реакционную смесь перемешивали в течение 24 ч при комнатной температуре. Растворитель выпаривали в модели RC 10.10 центрифужного испарителя Jouan и соединение, указанное в заголовке растворяли в 0,5 мл диметилсульфоксида для очистки посредством переключаемых ЖХ/МС с получением 3,9 мг метилового эфира N-[5-(4-[1-имидазолил]фенилсульфонилокси)-1 Н-бензимидазол-2 ил]сукцинамовой кислоты. (Анализ ЖХ/МС: время удержания = 2,70 мин, масс спектр: 470,34, [М+Н]+). Стадия 1: 11,3 мг N-(трет-бутоксикарбонил)глицина, 25 мг HBTU и 12 мкл диизопропилэтиламина помещали в 0,4 мл диметилформамида. Реакционную смесь в течение одного часа перемешивали при комнатной температуре и добавляли N-5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол 2-ил в 0,2 мл диметилформамида. Затем реакционную смесь перемешивали в течение 24 ч при комнатной температуре. Растворитель выпаривали в модели RC 10.10 центрифужного испарителя Jouan и указанное в заголовке соединение растворяли в 0,5 мл диметилсульфоксида для очистки посредством переключаемых ЖХ/МС с получением 2,4 мг N-[5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2 ил]-трет-бутоксикарбонилглицинамида. (Анализ ЖХ/МС: время удержания = 3,87 мин, масс спектр: 530,38, [М+Н]+). Пример 25. Получение метилового эфира N-[5-(4-циклопентиламинобензолсульфонилокси)-1 Нбензимидазол-2-ил]сукцинамовой кислоты Способом, подобным способу в примере 24, указанное в заголовке соединение получали посредством взаимодействия метилового эфира сукцинамовой кислоты сN-5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2-илом. (Анализ ЖХ/МС: время удержания = 3,72 мин, масс спектр: 487,34, [М+Н]+). Пример 26. Получение метилового эфира 4-[5-(4-циклопентиламинобензолсульфонилокси)-1 Нбензимидазол-2-илкарбамоил]масляной кислоты Способом, подобным способу в примере 24, указанное в заголовке соединение получали посредством взаимодействия метилового эфира масляной кислоты с N-5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2-илом. (Анализ ЖХ/МС: время удержания = 3,75 мин, масс спектр: 501,36, [М+Н]+). Пример 27. Получение 2-(циклопропанкарбониламино)-1 Н-бензимидазол-5-илового эфира 4 циклопентиламинобензолсульфоновой кислоты Способом, подобным способу в примере 24, указанное в заголовке соединение получали посредством взаимодействия циклопропанкарбоновой кислоты с Способом, подобным способу в примере 24, указанное в заголовке соединение получали посредством взаимодействия метоксиуксусной кислоты с N-5-(4-циклопентиламинофенилсульфонилокси)-1 Нбензимидазол-2-илом. (Анализ ЖХ/МС: время удержания = 3,66 мин, масс спектр: 445,34, [М+Н]+). Способом, подобным способу в примере 24, указанное в заголовке соединение получали посредством взаимодействия N,N-диметилглицина с N-5-(4-циклопентиламинофенилсульфонилокси)-1 Нбензимидазол-2-илом. (Анализ ЖХ/МС: время удержания = 3,36 мин, масс спектр: 458,36, [М+Н]+). Пример 30. N-[5-(4-[имидазолил]фенилсульфонилокси)-1 Н-бензимидазол-2-ил]метилмочевины 10 мг метил-5-(4-[имидазолил]фенилсульфокси)бензимидазол-2-карбамата (пример 4) смешивали с 50 мкл метиламина (2,0 М в тетрагидрофуране) и 5 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена в 2 мл Nметилпирролидинона/тетрагидрофурана (1/1) в 24-луночных устойчивых к окислению планшетах для реакций под высоким давлением. Реакционную смесь помещали в аргон под давлением 10 бар и затем в течение 4 ч нагревали при 80 С, а затем охлаждали до комнатной температуры. Соединения помещали в пробирку для анализа и выпаривали тетрагидрофуран при пониженном давлении, а соединение в Nметилпирролидиноне непосредственно очищали препаративным ЖХ/МС в указанных выше условиях. После очистки раствор концентрировали сушкой в испарителе Jouan RC10.10. (Анализ ЖХ/МС: время удержания = 2,23 мин, масс спектр: 413,23, [М+Н]+). Пример 31. N-[5-(4-циклопентиламинофенилсульфонилокси)-1 Н-бензимидазол-2-ил]метилмочевины Способом, подобным способу в примере 30, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Указанное в заголовке соединение получали посредством взаимодействия 10 мг метил-5-(4 циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата (пример 19) с 50 мкл диметиламина(2,0 М в тетрагидрофуране) и 5 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена в 2 мл диметилформамида. В 24 луночных устойчивых к окислению планшетах для реакций под высоким давлением. Реакционную смесь помещали в аргон под давлением 10 бар и затем в течение 4 ч нагревали при 80 С, а затем охлаждали до комнатной температуры. Соединения помещали в пробирку для анализа и концентрировали путем упаривания диметилформамида досуха в испарителе Jouan RC10.10. Соединение разводили в 0,5 мл диметилсульфоксида для очистки посредством переключаемых ЖХ/МС с ожидаемым выходом 9 мг (Анализ ЖХ/МС: время удержания = 3,35 мин, масс спектр: 444,29, [М+Н]+). Пример 33. 2-(3-циклопропилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты 10 мг метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата (пример 19) смешивали с 25 мкл циклопропиламина и 10 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена в 2 мл Nметилпирролидинона/тетрагидрофурана (0,8/1,2). В 24-луночных планшетах для inox для реакций под высоким давлением. Реакционную смесь помещали в аргон под давлением 10 бар и затем в течение 40 ч- 28006802 нагревали при 60 С, а затем охлаждали до комнатной температуры. Соединения помещали в пробирку для анализа, выпаривали тетрагидрофуран при пониженном давлении, а соединение в Nметилпирролидиноне непосредственно очищали посредством очистки переключаемыми ЖХ/МС с получением 8,7 мг указанного в заголовке соединения. (Анализ ЖХ/МС: время удержания = 3,66 мин, масс спектр: 456,36, [М+Н]+). Пример 34. 2-(3-изопропилуреидо)-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 30, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-[имидазолил]фенилсульфокси)бензимидазол-2-карбамата (пример 4) с 2 фторанилином. (Анализ ЖХ/МС: время удержания = 3,03 мин, масс спектр: 493,28, [М+Н]+). Пример 37. 2-[3-(2-фторфенил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата 4-циклопентил Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамат (пример 19) с р-анизидином (Анализ ЖХ/МС: время удержания = 3,97 мин, масс спектр: 522,34, [М+Н]+). Пример 40. 2-[3-(4-хлорфенил)уреидо]-1 Н-бензимидазол-5-иловый эфир 4-циклопентиламинобензолсульфоновой кислоты Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата Способом, подобным способу в примере 33, указанное в заголовке соединение получали посредством взаимодействия метил-5-(4-циклопентиламинофенилсульфонилокси)бензимидазол-2-карбамата
МПК / Метки
МПК: C07D 401/14, C07D 409/12, C07D 403/12, A61K 31/4184, C07D 235/32, C07D 235/30, C07D 401/12, A61P 35/00, C07D 405/12
Метки: замещенные, опухоли, злокачественной, производные, применение, бензимидазола, лечения
Код ссылки
<a href="https://eas.patents.su/30-6802-zameshhennye-proizvodnye-benzimidazola-i-ih-primenenie-dlya-lecheniya-zlokachestvennojj-opuholi.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные производные бензимидазола и их применение для лечения злокачественной опухоли</a>
Предыдущий патент: Смеси гербицидов, содержащие специальные сульфонилмочевины
Следующий патент: 1,3-диарилпроп-2-ен-1-оны, композиция на их основе и применение
Случайный патент: Микробицидные композиции


































