Новые производные 6-триазолпиридинсульфанил-бензотиазола или -бензимидазола, способ их получения, применение их в качестве лекарственных средств, фармацевтические композиции и новое применение в качестве ингибиторов мет
Номер патента: 23465
Опубликовано: 30.06.2016
Авторы: Венслер Сильви, Бак Эрик, Юголини Антонио, Альбер Эва, Немесек Консепсьон
Формула / Реферат
1. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I)
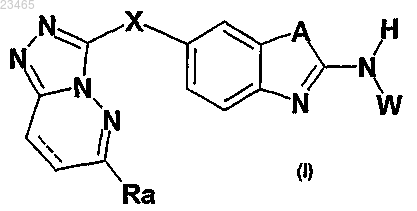
в которой ---- означает простую или двойную связь;
Ra означает атом водорода; радикал С1-5алкокси, необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом; ОС3-10циклоалкильный радикал; гетероарильный радикал, необязательно замещенный С1-6алкилом; фенильный радикал, необязательно замещенный атомом галогена; радикал NHCOC1-6алкил или радикал NR1R2, описанный ниже;
X означает S;
А означает NH или S;
W означает атом водорода; С1-6алкильный радикал, необязательно замещенный С1-4алкоксигруппой или NR3R4; или радикал COR, в котором R означает
C3-10циклоалкильный радикал или С1-6алкильный радикал, необязательно замещенный С1-4алкоксигруппой;
радикал С1-4алкокси, необязательно замещенный NR3R4, С1-4алкокси или гетероциклоалкилом; или О-фенил;
или радикал NR1R2,
в котором R1 означает атом водорода и R2 означает атом водорода, C3-10циклоалкильный радикал или C1-6алкильный радикал, необязательно замещенный С1-4алкокси или группой NR3R4,
или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами;
R3 и R4, одинаковые или различные, означают С1-6алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими C1-6алкильными группами;
где гетероциклоалкильный радикал обозначает моноциклический или бициклический карбоциклический радикал, содержащий 3-10 звеньев, прерываемые одним или несколькими гетероатомами, выбранными из атомов О, N или S;
гетероариловый радикал обозначает ненасыщенный или частично ненасыщенный, моноциклический или бициклический, карбоциклический радикал, содержащий 3-12 звеньев, который может необязательно содержать один или несколько гетероатомов, одинаковых или различных, выбранных из О, N или S.
2. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по п.1, в которой
----, X и А имеют значения, указанные в п.1;
Ra означает радикал С1-5алкокси, необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом; О-циклоалкильный радикал; радикал NHCOC1-6алкил или радикал NR1R2, причем R1 означает атом водорода и R2 означает атом водорода, С3-10циклоалкильный радикал или C1-6алкильный радикал, необязательно замещенный С1-4алкокси или NR3R4;
W означает атом водорода; С1-6алкильный радикал, необязательно замещенный С1-4алкокси или группой NR3R4; или радикал COR, в котором R означает
C3-10циклоалкильный радикал или С1-6алкильный радикал, необязательно замещенный радикалом С1-4алкокси;
радикал С1-4алкокси, необязательно замещенный NR3R4, С1-4алкокси или гетероциклоалкилом; или О-фенильный радикал;
или радикал NR1R2, в котором R1 означает атом водорода и R2 означает атом водорода, С3-10циклоалкильный радикал или C1-6алкильный радикал, необязательно замещенный NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими C1-6алкильными группами;
R3 и R4, одинаковые или различные, означают С1-6алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими C1-6алкильными группами.
3. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по п.1 или 2, в которой
----, Ra и X имеют значения, указанные в п.1 или 2;
А означает NH или S;
W означает атом водорода; С1-6алкильный радикал, необязательно замещенный С1-4алкокси; или радикал COR, в котором R означает
C3-10циклоалкильный радикал или С1-6алкильный радикал, необязательно замещенный С1-4алкоксигруппой;
радикал С1-4алкокси, необязательно замещенный NR3R4, С1-4алкокси или гетероциклоалкилом; или О-фенильный радикал;
или радикал NR1R2, в котором R1 означает атом водорода и R2 означает атом водорода, С3-10циклоалкильный радикал или C1-6алкильный радикал, необязательно замещенный NR3R4 или алкокси, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами;
NR3R4 такой, что R3 и R4, одинаковые или различные, означают С1-4алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами.
4. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-3, в которой
---- означает простую или двойную связь;
Ra означает атом водорода или фенильный радикал, необязательно замещенный атомом галогена;
X означает S;
А означает NH или S;
W означает атом водорода или радикал COR, в котором R означает
C3-10циклоалкильный радикал;
радикал С1-4алкокси, необязательно замещенный NR3R4, или О-фенильный радикал;
или радикал NR1R2, в котором R1 означает атом водорода и R2 означает С3-10циклоалкильный радикал или С1-6алкильный радикал, необязательно замещенный С1-4алкокси и группой NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами;
R3 и R4, одинаковые или различные, означают C1-6алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами.
5. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-4, в которой
----, Ra и X имеют значения, указанные в любом из пп.1-4;
А означает NH или S;
W означает атом водорода или C1-6алкильный радикал или радикал COR, в котором R означает
С1-6алкильный радикал, необязательно замещенный ОСН3;
C3-10циклоалкильный радикал;
радикал С1-4алкокси, необязательно замещенный ОСН3 или NR3R4, или О-фенильный радикал;
или радикал NR1R2, в котором R1 означает атом водорода и R2 означает С1-6алкильный радикал, необязательно замещенный NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами;
NR3R4 такой, что R3 и R4, одинаковые или различные, означают C1-6алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами.
6. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-5, в которой
----, Ra и X имеют значения, указанных в любом из пп.1-5;
А означает NH или S;
W означает атом водорода или радикал COR, в котором R означает
C1-4алкокси радикал, необязательно замещенный NR3R4, или O-фенильный радикал;
или радикал NR1R2, в котором R1 означает атом водорода и R2 означает C1-6алкильный радикал, необязательно замещенный NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами;
NR3R4 такой, что R3 и R4, одинаковые или различные, означают C1-6алкильный радикал или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С1-6алкильными группами.
7. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-6, в которой
----, X, А и W имеют значения, указанные в любом из пп.1-6;
Ra означает атом водорода или радикал
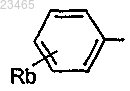
где Rb означает атом галогена.
8. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-7, в которой А означает NH, заместители ----, Ra, X и W выбраны из всех значений, указанных для этих радикалов в любом из пп.1-7.
9. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-8, в которой А означает S, заместители ----, Ra, X и W выбраны из всех значений, указанных для этих радикалов в любом из пп.1-8.
10. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-9, соответствующее формуле (Ia) или (Ib)
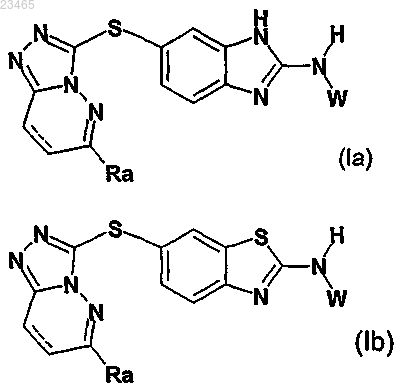
в которых ----, Ra и W выбраны из всех значений, указанных в любом из пп.1-9.
11. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-10, в которой ---- обозначает простую связь, соответствующее формуле (I')
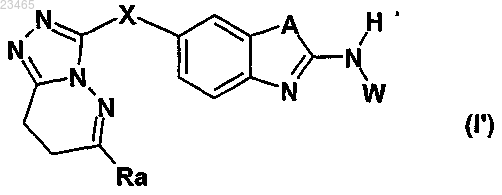
в которой заместители Ra, X, А и W выбраны из значений, указанных в любом из пп.1-10.
12. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-11, в которой ---- обозначает двойную связь, соответствующее формуле (I'')
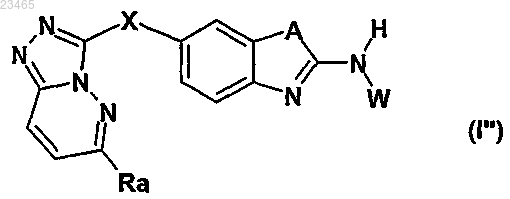
в которой заместители Ra, X, А и W имеют значения, указанные в любом из пп.1-11.
13. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (Ia) по любому из пп.1-12, в которой ---- обозначает простую связь, соответствующее формуле (I'а)
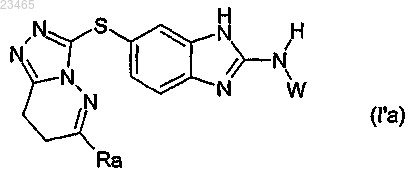
в которой заместители Ra и W выбраны из значений, указанных в любом из пп.1-12.
14. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (Ia) по любому из пп.1-13, в которой ---- обозначает двойную связь, соответствующее формуле (I''а)
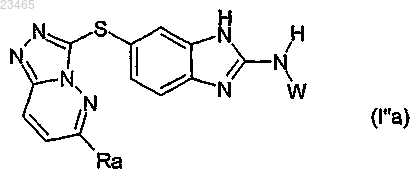
в которой заместители Ra и W выбраны из значений, указанных в любом из пп.1-13.
15. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (Ib) по любому из пп.1-14, в которой ---- обозначает простую связь, соответствующее формуле (I'b)
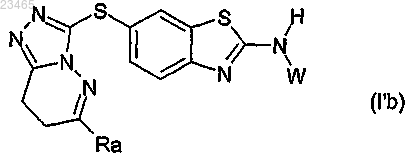
в которой заместители Ra и W выбраны из значений, указанных в любом из пп.1-14.
16. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (Ib) по любому из пп.1-15, в которой ---- обозначает двойную связь, соответствующее формуле (I''b)
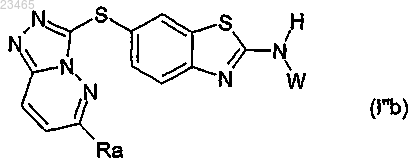
в которой заместители Ra и W выбраны из значений, указанных в любом из пп.1-15.
17. Производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-16, выбранное из группы, включающей
метил-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
метил-6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1Н-бензимидазол-2-ил)карбамат;
1-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1Н-бензимидазол-2-ил)-3-(2-морфолин-4-илэтил)карбамид;
6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1Н-бензимидазол-2-амин;
1-(2-морфолин-4-илэтил)-3-[6-([1,2,4]триазоло[4,3-b]пиридазин-3-илсульфанил}-1,3-бензотиазол-2-ил]карбамид;
1-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-(2-морфолин-4-илэтил)карбамид;
1-{2-[(2R,6S)-2,6-диметилморфолин-4-ил]этил}-3-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамид;
2-морфолин-4-илэтил-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
1-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-[2-(4-метилпиперазин-1-ил)этил]карбамид;
N-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-4-морфолин-4-илбутанамид;
1-[2-(диэтиламино)этил]-3-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамид;
1-{6-[(6-метокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-[2-(морфолин-4-ил)этил]карбамид;
N-[6-({6-[(2-метоксиэтил)амино][1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]ацетамид;
6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-N-[2-(морфолин-4-ил)этил]-1,3-бензотиазол-2-амин;
фенил-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
1-{6-[(6-этокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-[2-(морфолин-4-ил)этил]карбамид;
1-{6-[(6-этокси-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-[2-(морфолин-4-ил)этил]карбамид;
N-[6-({6-[(2-метоксиэтил)амино][1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]циклопропанкарбоксамид;
6-{[6-(1-метил-1Н-пиразол-4-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
1-(6-{[6-(4-фторфенил)-7,8-дигидро-[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-[2-(морфолин-4-ил)этил]карбамид;
оксетан-2-илметил-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
N-{6-[(6-метокси)][1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}циклопропанкарбоксамид;
N-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)ацетамид;
1-{6-[(6-метокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-[2-(пирролидин-1-ил)этил]карбамид;
6-[(6-этокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-амин;
6-{[6-(3-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
1-циклопропил-3-{6-[(6-этокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}карбамид;
N-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)циклопропанкарбоксамид;
N-(6-{[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)циклопропанкарбоксамид;
1-(6-{[6-(3-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-[2-(морфолин-4-ил)этил]карбамид;
1,1-диметилэтил-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
метил-(6-{[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1Н-бензимидазол-2-ил)карбамат;
6-[(4-{3-[(2-амино-1,3-бензотиазол-6-ил)]сульфанил]-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-ил}фенил)сульфанил]-1,3-бензотиазол-2-амин;
1-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-[2-(4-метилпиперазин-1-ил)этил]карбамид;
1,1-диметилэтил-(6-{[6-(морфолин-4-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
N-(6-{[6-(морфолин-4-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)ацетамид;
гидрохлорид 1,1-диметилэтил-(6-{[6-(4-метилпиперазин-1-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамата;
1-(6-{[6-(1Н-имидазол-1-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-3-[2-(морфолин-4-ил)этил]карбамид;
1,1-диметилэтил-{6-[(6-метокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}карбамат;
1,1-диметилэтил-(6-{[6-(1Н-имидазол-1-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
1,1-диметилэтил-[6-({6-(2-метоксиэтил)амино[1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]карбамат;
N-(6-{[6-(4-метилпиперазин-1-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)ацетамид;
6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-N-(2-метоксиэтил)-1,3-бензотиазол-2-амин;
1-[2-(морфолин-4-ил)этил]-3-(6-{[6-(морфолин-4-ил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамид;
1-{6-[(6-амино[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-[2-(морфолин-4-ил)этил]карбамид;
N-(3-{[2-({[2-(морфолин-4-ил)этил]карбамоил}амино)-1,3-бензотиазол-6-ил]сульфанил}[1,2,4]триазоло[4,3-b]пиридазин-6-ил)ацетамид;
2,2-диметил-N-(3-{[2-({[2-(морфолин-4-ил)этил]карбамоил}амино)-1,3-бензотиазол-6-ил]сульфанил}[1,2,4]триазоло[4,3-b]пиридазин-6-ил)пропанамид;
1-[2-(морфолин-4-ил)этил]-3-(6-{[6-(оксетан-2-илметокси)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамид;
N-[6-({6-[(2-метоксиэтил)амино][1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]-4-(морфолин-4-ил)бутанамид;
этил-{6-[(6-метокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}карбамат;
3-метоксипропил-{6-[(6-метокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}карбамат;
3-метоксипропил-[6-({6-[(2-метоксиэтил)амино][1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]карбамат;
1-[6-[{6-(2-метоксиэтил)амино[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил]-3-[2-(пирролидин-1-ил)этил]карбамид;
2-метилпропан-2-ил-(6-{[6-(4-хлор-2-гидроксибутокси)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)карбамат;
2-метилпропан-2-ил-[6-({6-[3-хлор-2-(гидроксиметил)-2-метилпропокси][1,2,4]триазоло[4,3-b]пиридазин-3-ил}сульфанил)-1,3-бензотиазол-2-ил]карбамат;
6-{[6-(3-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
N-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)морфолин-4-карбоксамид;
6-{[6-(2-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
N-(2-метоксиэтил)-3-({2-[(2-метилбутил)амино]-1,3-бензотиазол-6-ил}сульфанил)[1,2,4]триазоло[4,3-b]пиридазин-6-амин;
N-{6-[(6-этокси[1,2,4]триазоло[4,3-b]пиридазин-3-ил)сульфанил]-1,3-бензотиазол-2-ил}-3-метоксипропанамид;
3-[(2-амино-1,3-бензотиазол-6-ил)сульфанил]-N-циклогексил[1,2,4]триазоло[4,3-b]пиридазин-6-амин;
6-{[6-(циклогексилокси)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-амин;
N-(6-{[6-(3-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)ацетамид;
N-(6-{[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)-2-метилпропанамид;
N-(6-{[6-(3-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-1,3-бензотиазол-2-ил)циклопропанкарбоксамид;
6-{[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил}-N-(2-метилбутил)-1,3-бензотиазол-2-амин.
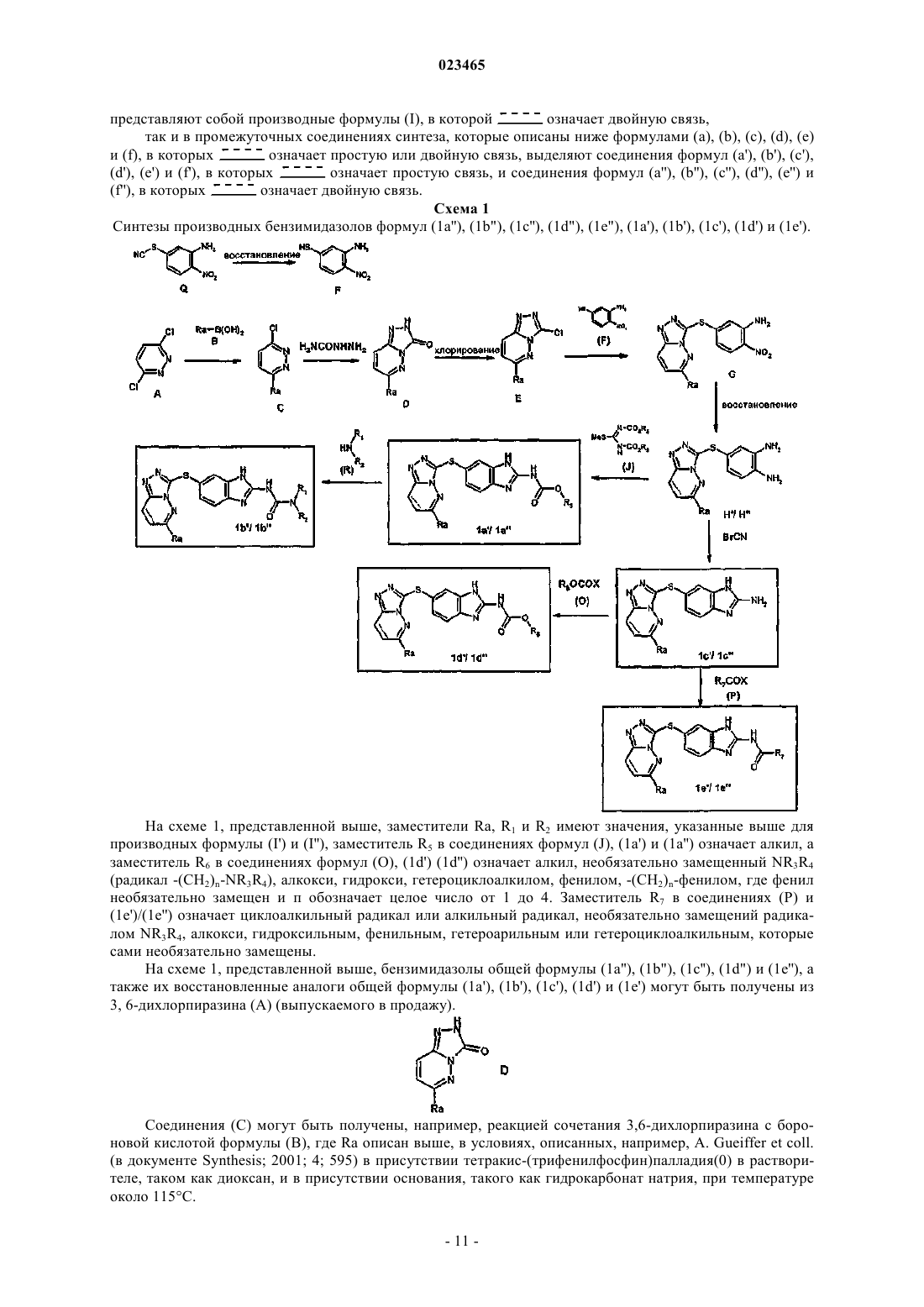
18. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, в которой А означает NH, X означает S и W означает атом водорода или радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
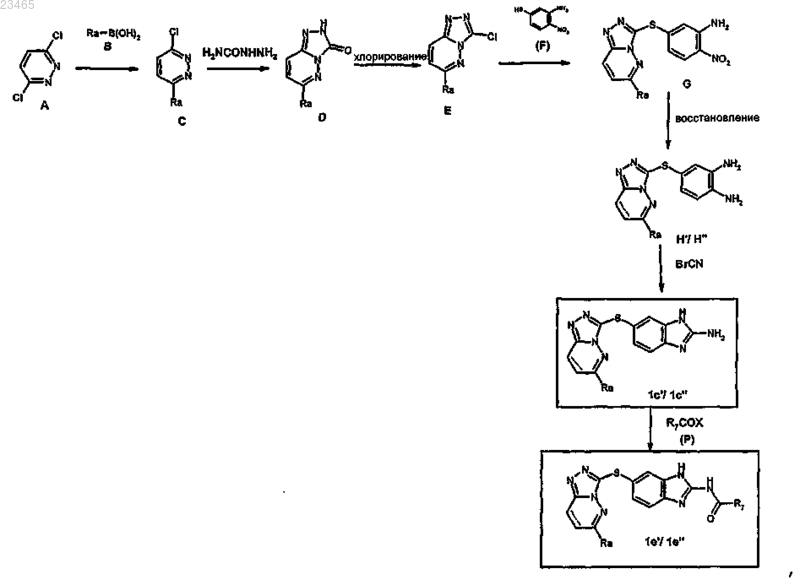
где заместитель Ra имеет значения, указанные в п.1;
заместитель R7 представляет собой С3-10циклоалкильный радикал или C1-6алкильный радикал, С1-4алкокси радикал, необязательно замещенный NR3R4; или О-фенил, где R3 и R4 имеют значения, указанные в п.1;
в соединениях формул Н', 1с' и 1е' ---- означает простую связь;
в соединениях формул Н", 1с" и 1е" ---- означает двойную связь;
соединения (Е) получают взаимодействием трихлорида фосфора (оксихлорид фосфора) с соединением формулы (D);
соединение (Н''), в котором ---- означает двойную связь, получают восстановлением с помощью железа(0) соединений формулы (G);
соединение (Н'), в котором ---- означает простую связь, получают восстановлением с помощью цинка(0) соединений формулы (G).
19. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, в которой А означает NH, X означает S и W означает радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
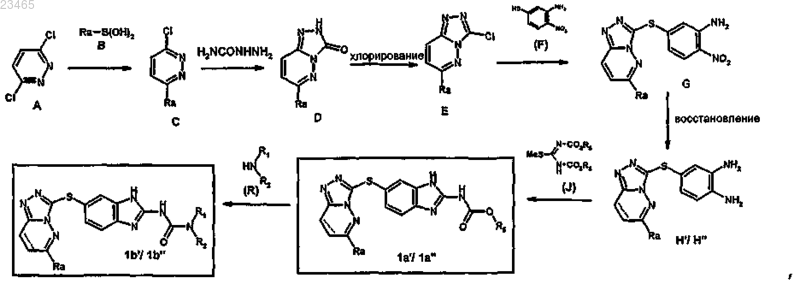
где заместители Ra, R1 и R2 имеют значения, указанные в п.1;
заместитель R5 представляет собой С1-4алкил;
в соединениях формул Н', 1а' и 1b' ---- означает простую связь;
в соединениях формул Н", 1а" и 1b" ---- означает двойную связь;
соединения (Е) получают взаимодействием трихлорида фосфора (оксихлорид фосфора) с соединением формулы (D);
соединение (Н''), в котором ---- означает двойную связь, получают восстановлением с помощью железа(0) соединений формулы (G);
соединение (Н'), в котором ---- означает простую связь, получают восстановлением с помощью цинка(0) соединений формулы (G).
20. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, в которой А означает NH, X означает S и W означает атом водорода или радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
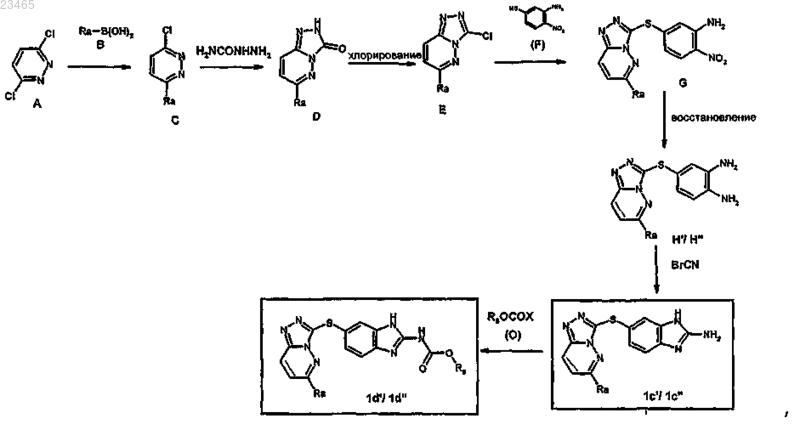
где заместитель Ra имеет значения, указанные в п.1;
заместитель R6 представляет собой С1-4алкил, необязательно замещенный NR3R4, С1-4алкокси, гетероциклоалкилом; или фенил, где R3 и R4 имеют значения, указанные в п.1;
n обозначает целое число от 1 до 4;
в соединениях формул Н', 1с' и 1d' ---- означает простую связь;
в соединениях формул Н", 1с" и 1d" ---- означает двойную связь;
соединения (Е) получают взаимодействием трихлорида фосфора (оксихлорид фосфора) с соединением формулы (D);
соединение (Н''), в котором ---- означает двойную связь, получают восстановлением с помощью железа(0) соединений формулы (G);
соединение (Н'), в котором ---- означает простую связь, получают восстановлением с помощью цинка(0) соединений формулы (G).
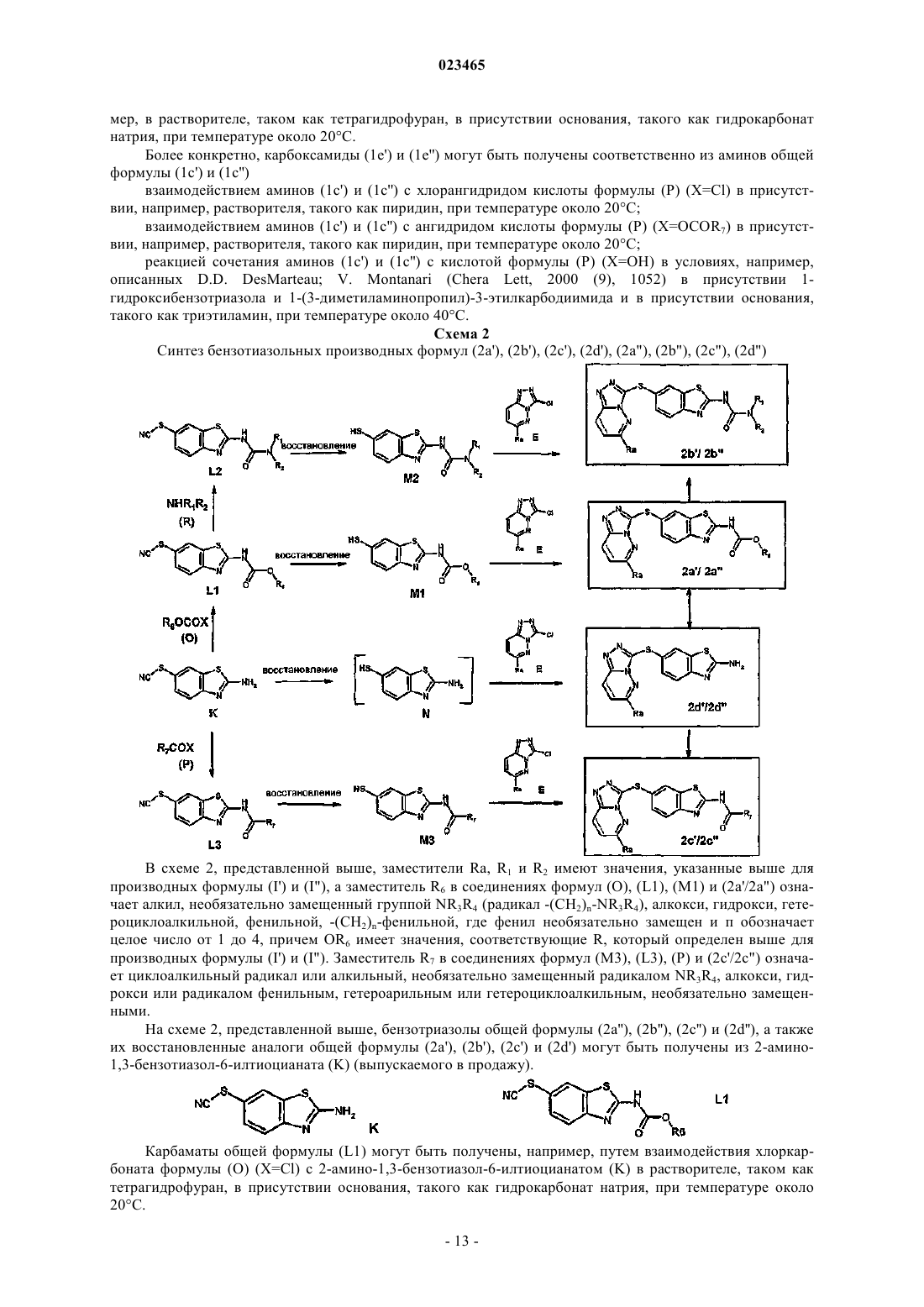
21. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, где А означает S, X означает S и W означает радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
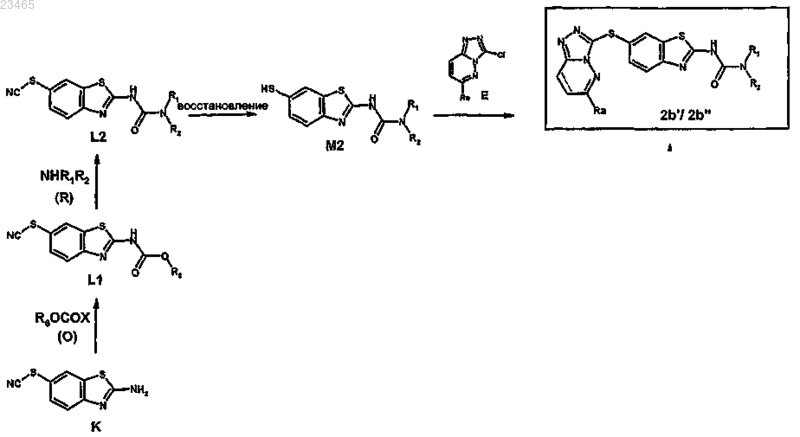
где заместители Ra, R1 и R2 имеют значения, указанные в п.1;
заместитель R6 представляет собой С1-6алкил, необязательно замещенный группой NR3R4 (радикал -(СН2)n-NR3R4), С1-4алкокси, гидрокси, гетероциклоалкильной, фенильной, -(СН2)n-фенильной, где фенил необязательно замещен; где R3 и R4 имеют значения, указанные в п.1;
n обозначает целое число от 1 до 4;
в соединении формулы 2b' ---- означает простую связь;
в соединении формулы 2b'' ---- означает двойную связь;
соединения формулы (М2) получают восстановлением соединений (L2) с помощью DL-дитиотреитола в присутствии дигидрокарбоната натрия в растворителе.
22. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, где А означает S, X означает S и W означает радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
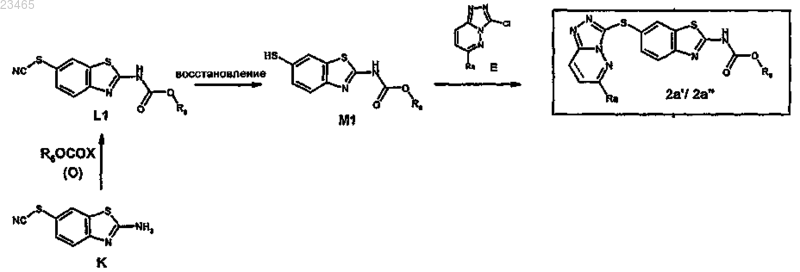
где заместитель Ra имеет значения, указанные в п.1;
заместитель R6 представляет собой С1-4алкил, необязательно замещенный группой NR3R4, алкокси, гетероциклоалкилом; или фенил, где R3 и R4 имеют значения, указанные в п.1;
в соединении формулы 2а' ---- означает простую связь;
в соединении формулы 2а'' ---- означает двойную связь;
соединения формулы (M1) получают восстановлением соединений (L1) с помощью DL-дитиотреитола в присутствии дигидрокарбоната натрия в растворителе.
23. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, где А означает S, X означает S и W означает атом водорода, характеризующийся следующей схемой:
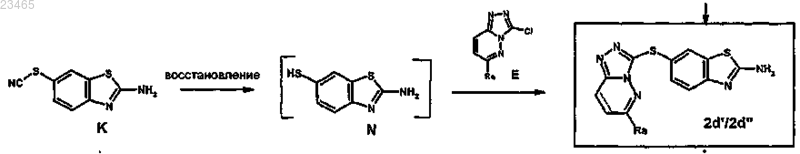
где заместитель Ra имеет значения, указанные в п.1;
в соединении формулы 2d' ---- означает простую связь;
в соединении формулы 2d'' ---- означает двойную связь;
соединение формулы (N) получают путем восстановления соединения (K) с помощью боргидирида натрия в растворителе, таком как N,N-диметилформамид, в присутствии основания.
24. Способ получения производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17, где А означает S, X означает S и W означает радикал COR, где R имеет значение, указанные в п.1, характеризующийся следующей схемой:
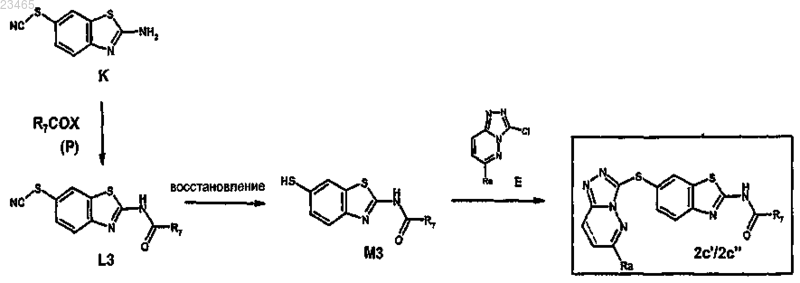
где заместитель Ra имеет значения, указанные в п.1;
заместитель R7 представляет собой C3-10циклоалкильный радикал или С1-6алкильный радикал; С1-4алкокси, необязательно замещенный радикалом NR3R4; или О-фенил, где R3 и R4 имеют значения, указанные в п.1;
в соединении формулы 2с' ---- означает простую связь;
в соединении формулы 2с'' ---- означает двойную связь;
соединения формулы (M3) получают восстановлением соединений (L3) с помощью DL-дитиотреитола в присутствии дигидрокарбоната натрия в растворителе.
25. Лекарственное средство для ингибирования активности протеинкиназы МЕТ или для лечения или предупреждения заболевания, выбранного из следующей группы: нарушения пролиферации кровеносных сосудов, нарушения фибротических процессов, нарушения пролиферации "мезангиальных" клеток, метаболические расстройства, аллергии, астмы, тромбозы, болезни нервной системы, ретинопатия, псориаз, ревматоидный артрит, диабет, мышечная дегенерация и рак, представляющее собой производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по одному из пп.1-17.
26. Лекарственное средство для ингибирования активности протеинкиназы МЕТ или для лечения или предупреждения заболевания, выбранного из следующей группы: нарушения пролиферации кровеносных сосудов, нарушения фибротических процессов, нарушения пролиферации "мезангиальных" клеток, метаболические расстройства, аллергии, астмы, тромбозы, болезни нервной системы, ретинопатия, псориаз, ревматоидный артрит, диабет, мышечная дегенерация и рак, представляющее собой производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по п.17.
27. Фармацевтическая композиция для ингибирования активности протеинкиназы МЕТ или для лечения или предупреждения заболевания, выбранного из следующей группы: нарушения пролиферации кровеносных сосудов, нарушения фибротических процессов, нарушения пролиферации "мезангиальных" клеток, метаболические расстройства, аллергии, астмы, тромбозы, болезни нервной системы, ретинопатия, псориаз, ревматоидный артрит, диабет, мышечная дегенерация и рак, содержащая в качестве активного начала по меньшей мере одно производное 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по одному из пп.1-17, и фармацевтически приемлемый носитель.
28. Применение производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17 для получения лекарственного средства, предназначенного для ингибирования активности протеинкиназы МЕТ.
29. Применение по п.28, в котором протеинкиназа находится в клеточной культуре.
30. Применение по п.28 или 29, в котором протеинкиназа находится в организме млекопитающего.
31. Применение производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по любому из пп.1-17 для получения лекарственного средства, предназначенного для лечения или предупреждения заболевания, выбранного из следующей группы: нарушения пролиферации кровеносных сосудов, нарушения фибротических процессов, нарушения пролиферации "мезангиальных" клеток, метаболические расстройства, аллергии, астмы, тромбозы, болезни нервной системы, ретинопатия, псориаз, ревматоидный артрит, диабет, мышечная дегенерация и рак.
32. Применение производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по одному из пп.1-17 для получения лекарственного средства, предназначенного для лечения рака.
33. Применение по п.32, предназначенное для лечения солидных опухолей или опухолей мягких тканей.
34. Применение по п.32 или 33, предназначенное для лечения раков, резистентных к цитотоксическим агентам.
35. Применение по одному или нескольким пп.32-34, предназначенное для лечения первичных опухолей и/или метастаз, в частности, при раке желудка, печени, мочевых путей, яичников, ободочной кишки, предстательной железы, легких (NSCLC и SCLC), глиобластом, при раке щитовидной железы, мочевого пузыря, молочной железы, при меланоме, гематопоэтических лимфоидных или миелоидных опухолях, при саркомах, при раке мозга, гортани, лимфатической системы, рака костей и поджелудочной железы.
36. Применение производного 6-триазолпиридазинсульфанил-бензотиазола или -бензимидазола формулы (I) по пп.1-17 для получения лекарственного средства, предназначенного для химиотерапевтического лечения рака.
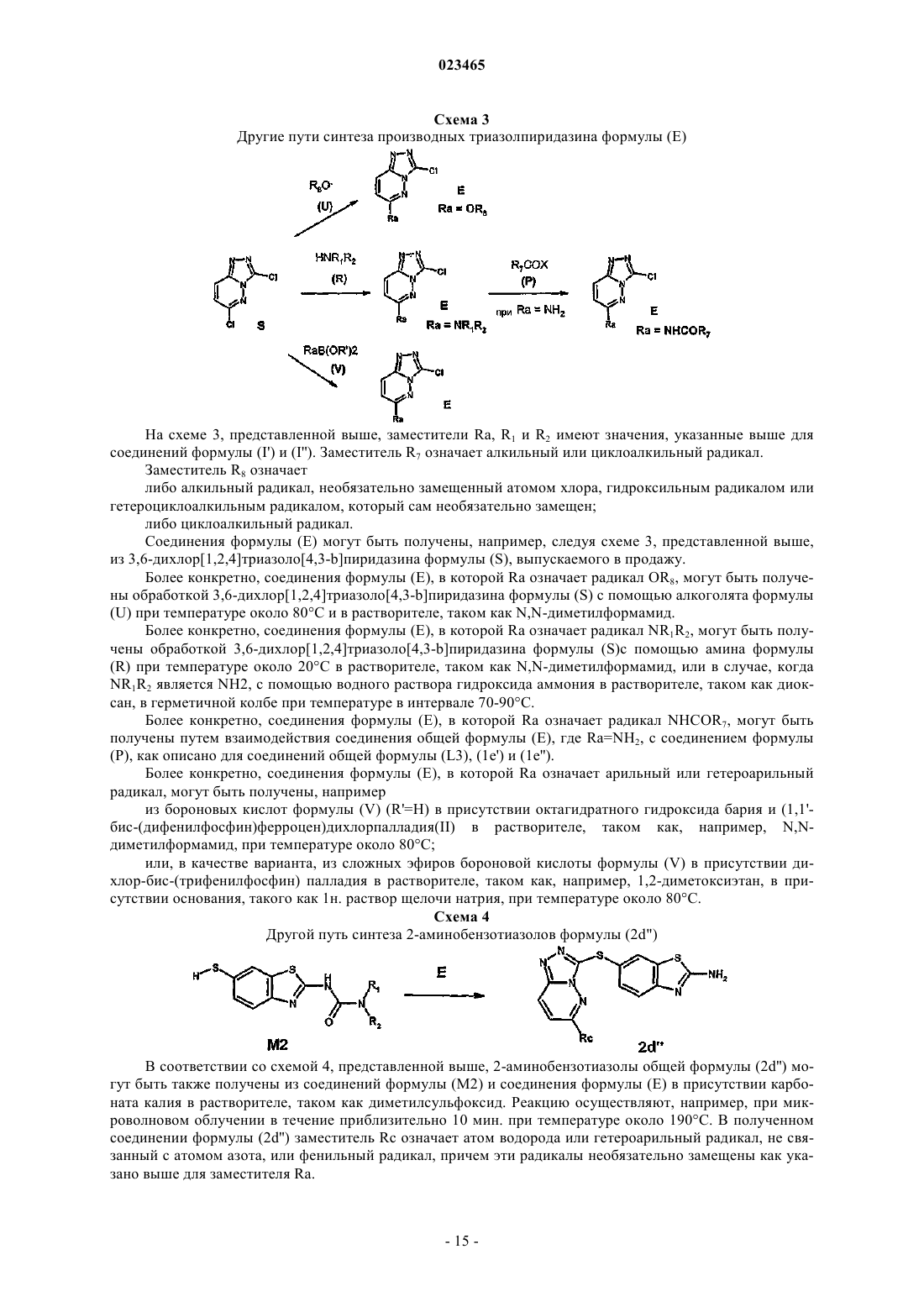
37. Производное триазолопиридазина, представляющее собой промежуточный продукт синтеза формулы Е'
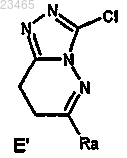
где Ra имеет указанные в п.1 значения.
38. Производное бензотиазола, представляющее собой промежуточный продукт синтеза формул M1, M2 и M3:
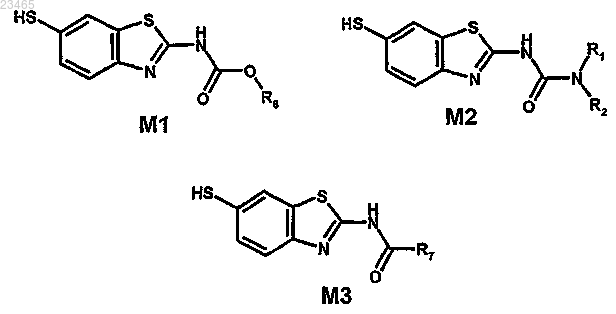
в которых R6 означает радикал С1-4алкил, необязательно замещенный группой NR3R4, С1-4алкокси или гетероциклоалкилом, или фенил, причем OR6 имеет значения, соответствующие радикалу R, описанному в п.1;
R7 означает С3-10циклоалкильный или С1-6алкильный радикал, необязательно замещенный С1-4алкоксигруппой;
R1, R2, R3 и R4 имеют указанные в п.1 значения.
Текст
в которой означает простую или двойную связь; Ra означает атом водорода; радикал С 1-5 алкокси,необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом; ОС 3-10 циклоалкильный радикал; гетероарильный радикал, необязательно замещенный С 1-6 алкилом; фенильный радикал, необязательно замещенный атомом галогена; радикал NHCOC1-6 алкил или радикал NR1R2, описанный ниже; X означает S; А означает NH или S; W означает атом водорода; С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкоксигруппой или NR3R4; или радикал COR, в котором R означает С 3-10 циклоалкильный радикал или C1-6 алкильный радикал, необязательно замещенный С 1-4 алкоксигруппой; радикал С 1-4 алкокси, необязательно замещенный NR3R4, С 1-4 алкокси или гетероциклоалкилом; или О-фенил; или радикал NR1R2, в котором R1 означает атом водорода, R2 означает атом водорода, С 3-10 циклоалкильный радикал, или С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкокси или группой NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены,морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами; R3 и R4, одинаковые или различные, означают С 1-6 алкильный радикал, или R3 иR4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами; где гетероциклоалкильный радикал обозначает моноциклический или бициклический карбоциклический радикал, содержащий 3-10 звеньев, прерываемые одним или несколькими гетероатомами, выбранными из атомов О, N или S; гетероариловый радикал обозначает ненасыщенный или частично ненасыщенный,моноциклический или бициклический, карбоциклический радикал, содержащий 3-12 звеньев, который может необязательно содержать один или несколько гетероатомов, одинаковых или различных, выбранных из О, N или S с N, используемым в качестве лекарственных средств, в частности в качестве ингибиторов МЕТ. Настоящее изобретение относится к новым производным 6-триазолпиридазинсульфанилбензотиазола и -бензимидазола, к способу их получения, к новым полученным промежуточным продуктам, к применению их в качестве лекарственных средств, к фармацевтическим композициям на их основе и к новому применению указанных производных 6-триазолпиридазинсульфанил-бензотиазола и-бензимидазола. Более конкретно,настоящее изобретение относится к новым производным 6 триазолпиридазинсульфанил-бензотиазола и -бензимидазола, обладающим противораковой активностью посредством модуляции активности белков, в частности, киназ. В настоящее время большинство соединений, выпускаемых в продажу и используемых в химиотерапии, являются цитотоксичными и создают серьезные проблемы побочных эффектов и переносимости их пациентами. Эти эффекты могут быть ограничены в случае, когда используемые лекарственные средства действуют селективно на раковые клетки, исключая здоровые клетки. Одно из решений, ограничивающих нежелательные эффекты химиотерапии, может заключаться в использовании лекарственных средств, действующих на метаболические пути или на конститутивные элементы этих путей, которые экспрессировались бы главным образом в раковых клетках и не экспрессировались или незначительно экспрессировались в здоровых клетках. Протеинкиназы относятся к семейству ферментов, которые катализируют фосфорилирование гидроксигрупп специфических остатков протеинов, таких как остатки тирозина, серина и треонина. Такое фосфорилирование может широко модифицировать функцию протеинов: так, протеинкиназы играют важную роль в регуляции большого числа разнообразных клеточных процессов, включая, в частности, метаболизм, клеточную пролиферацию, адгезию и подвижность клеток,дифференцировку клеток или их выживаемость, причем некоторые протеинкиназы играют решающую роль в инициации, развитии и завершении клеточных циклов. Среди различных клеточных функций, в которых задействована активность протеинкиназ, некоторые процессы представляют собой привлекательную мишень для лечения определенных заболеваний. Например, можно назвать, в частности, ангиогенез и контроль клеточного цикла, а также контроль за пролиферацией клеток, в которых протеинкиназы могут играть главную роль. Эти процессы являются существенными, в частности, при росте солидных опухолей, а также при других заболеваниях, в частности ингибирующие молекулы таких киназ способны ограничивать нежелательные клеточные пролиферации, такие как пролиферации, наблюдаемые при раковых заболеваниях, и могут участвовать в предупреждении, регуляции или лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера или нейрональный апоптоз. Настоящее изобретение относится к новым производным, обладающим ингибирующим эффектом в отношении протеинкиназ. Производные согласно изобретению могут быть использованы, в частности,для предупреждения или лечения заболеваний, которые можно модулировать путем ингибирования протеинкиназ. Производные согласно изобретению обладают, в частности, противораковой активностью посредством модуляции активности киназ. Среди киназ, в отношении которых желательно модулирование активности, предпочтительны МЕТ и мутанты МЕТ-белка. Настоящее изобретение относится также к применению указанных производных для получения лекарственного средства, предназначенного для лечения людей. Таким образом, одной из целей настоящего изобретения является создание композиций, имеющих противораковую активность, и воздействующих, в частности, на киназы. Среди киназ, в отношении которых желательно модулировать активность, предпочтителен МЕТ. В фармакологической части, изложенной ниже, показано с помощью биохимических тестов на клеточных линиях, что производные согласно настоящему изобретению ингибируют, в частности, аутофосфорилирование МЕТ и пролиферацию клеток, рост которых зависит от МЕТ или его мутантных форм. МЕТ или Hepatocyte Growth Factor Receptor (рецептор гепацитарного фактора роста) является рецептором с тирозинкиназной активностью, экспрессирующимся, в частности, в эпителиальных и эндотелиальных клетках. HGF, Hepatocyte Growth Factor (гепацитарный фактор роста) описан в качестве специфического лиганда MET. HGF секретируется мезенхиальными клетками и активирует рецептор МЕТ,который гомодимеризуется. Следовательно, рецептор аутофосфорилируется на тирозинах каталитического домена Y1230, Y1234 и Y1235. Стимуляция МЕТ с помощью HGF инициирует пролиферацию, рассеивание (или дисперсию), подвижность клеток, резистентность к апоптозу, инвазию и ангиогенез. Обнаружено, что МЕТ, также как и HGF, гиперэкспрессируются в многочисленных человеческих опухолях и в большинстве различных злокачественных опухолях. Обнаружено также, что МЕТ амплифицируется в опухолях желудка и в глиобластомах. Описано в литературе множество точечных мутаций гена МЕТ вопухолях, в частности в киназном домене, а также в околомембранном домене и домене SEMA. Гиперэкспрессия, амплификация или мутации вызывают конститутивную активацию рецептора и дерегуляцию его функций. Таким образом, настоящее изобретение относится, в частности, к новым ингибиторам протеинкиназы МЕТ и ее мутантов, которые могут быть использованы для антипролиферативного и антиметастати-1 023465 ческого лечения, в частности, в области онкологии. Настоящее изобретение относится также к новым ингибиторам протеинкиназы МЕТ и ее мутантов,которые могут быть использованы для антиангиогенного лечения, в частности, в области онкологии. Настоящее изобретение относится к производным 6-триазолпиридазинсульфанил-бензотиазола и в которой означает простую или двойную связь;Ra означает атом водорода; радикал С 1-5 алкокси, необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом; OC1-10 циклоалкильный радикал; гетероарильный радикал, необязательно замещенный C1-6 алкилом; фенильный радикал, необязательно замещенный атомом галогена; радикал NHCOC1-6 алкил или радикал NR1R2, описанный ниже;W означает атом водорода; С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкоксигруппой или NR3R4; или радикал COR, в котором R означает С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкоксигруппой; радикал С 1-4 алкокси, необязательно замещенный NR3R4, С 1-4 алкокси или гетероциклоалкилом; или О-фенила; или радикал NR1R2,в котором R1 означает атом водорода и R2 означает атом водорода, С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкокси или группой NR3R4,или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами;R3 и R4, одинаковые или различные, означают С 1-6 алкильный радикал, или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами; где гетероциклоалкильный радикал обозначает моноциклический или бициклический карбоциклический радикал, содержащий 3-10 звеньев, прерываемые одним или несколькими гетероатомами, выбранными из атомов О, N или S; гетероариловый радикал обозначает ненасыщенный или частично ненасыщенный, моноциклический или бициклический, карбоциклический радикал, содержащий 3-12 звеньев, который может необязательно содержать один или несколько гетероатомов, одинаковых или различных, выбранных из О, N илиS с N; причем указанные производные формулы (I) находятся во всех возможных изомерных рацемических, энантиомерных и диастереоизомерных формах, а также к аддитивным солям указанных производных формулы (I) с минеральными или органическими кислотами или с минеральными или органическими основаниями. Настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой, X и А имеют значения, указанные выше или ниже;Ra означает радикал С 1-5 алкокси, необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом; О-циклоалкильный радикал; радикал NHCOC1-6 алкил; или радикал NR1R2, причем R1 означает атом водорода и R2 означает атом водорода, С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкокси или NR3R4;W означает атом водорода; С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкокси или группой NR3R4; или радикал COR, в котором R означает С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный радикалом С 1-4 алкокси; радикал С 1-4 алкокси, необязательно замещенный NR3R4, С 1-4 алкокси или гетероциклоалкилом; или О-фенильный радикал; или радикал NR1R2, в котором R1 означает атом водорода и R2 означает атом водорода,С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены,морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами; с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами. Настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой, Ra и X имеют значения, указанные выше или ниже; А означает NH или S;C3-10 циклоалкильный радикал или C1-6 алкильный радикал, необязательно замещенный С 1-4 алкоксигруппой; радикал С 1-4 алкокси, необязательно замещенный NR3R4, C1-4 алкокси или гетероциклоалкилом; или О-фенильный радикал; или радикал NR1R2, в котором R1 означает атом водорода и R2 означает атом водорода,С 3-10 циклоалкильный радикал или C1-6 алкильный радикал, необязательно замещенный NR3R4 или алкокси, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами;NR3R4 такой, что R3 и R4, одинаковые или различные, означают С 1-4 алкильный радикал, или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами. Настоящее изобретение относится к производным формулы (I), описанным выше, в которой означает простую или двойную связь;Ra означает атом водорода или фенильный радикал, необязательно замещенный атомом галогена;W означает атом водорода или радикал COR, в котором R означаетC3-10 циклоалкильный радикал; радикал С 1-4 алкокси, необязательно замещенный NR3R4, или О-фенильный радикал; или радикал NR1R2, в котором R1 означает атом водорода и R2 означает С 3-10 циклоалкильный радикал или С 1-6 алкильный радикал, необязательно замещенный С 1-4 алкокси и группой NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены, морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами;R3 и R4, одинаковые или различные, означают С 1-6 алкильный радикал, или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими С 1-6 алкильными группами. Таким образом, настоящее изобретение, которое относится к производным формулы (I), описанным выше, в которой означает простую или двойную связь, относится, более конкретно, к производным формулы (I'), которые представляют собой производные формулы (I), в которой означает простую связь, и к производным формулы (I), которые представляют собой производные формулы (I), в которой означает двойную связь. Таким образом, производные формулы (I), описанные выше или ниже, представляют собой, более конкретно, производные формулы (I'), в которой означает простую связь. Производные формулы (I), описанные выше или ниже, представляют собой также производные формулы (I), в которой означает двойную связь. Настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой, Ra и X имеют значения, указанные выше или ниже; А означает NH или S;W означает атом водорода или С 1-6 алкильный радикал или радикал COR, в котором R означает С 1-6 алкильный радикал, необязательно замещенный ОСН 3;C3-10 циклоалкильный радикал; радикал С 1-4 алкокси, необязательно замещенный ОСН 3 или NR3R4, или О-фенильный радикал; или радикал NR1R2, в котором R1 означает атом водорода и R2 означает С 1-6 алкильный радикал, необязательно замещенный NR3R4, или R1 и R2 образуют вместе с атомом азота, с которым они соединены,морфолинильную или пиперазинильную группу, необязательно замещенную одной или несколькимиNR3R4 такой, что R3 и R4, одинаковые или различные, означают С 1-6 алкильный радикал, или R3 и R4 образуют вместе с атомом азота, с которым они соединены, морфолинильную, пиперазинильную или пирролидинильную группу, необязательно замещенную одной или несколькими C1-6 алкильными группами. Настоящее изобретение относится к производным формулы (I), описанным выше, в которой, X, А и W имеют значения, указанные выше или ниже;Ra означает атом водорода или радикал: где Rb означает атом галогена; все остальные заместители имеют указанные выше значения. В производных формулы (I) и в последующем тексте: термин "алкильный радикал (или алк)" обозначает радикалы, линейные и, в случае необходимости,разветвленные: метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, вторбутильный, трет-бутильный, пентильный, изопентильный, гексильный, изогексильный, а также гептильный, октильный, нонильный и децильный, а также их изомеры положения, линейные или разветвленные: предпочтительны алкильные радикалы, содержащие 1-6 атомов углерода, более конкретно, алкильные радикалы, содержащие 1-4 атома углерода, указанного выше списка; термин "радикал алкокси" обозначает радикалы, линейные или, при необходимости, разветвленные,метокси, этокси, пропокси, изопропокси, линейный, вторичный или третичный бутокси, пентокси или гексокси, а также их изомеры положения, линейные или разветвленные: предпочтительны радикалы алкокси, содержащие 1-4 атома углерода, указанного выше списка; термин "атом галогена" обозначает атомы хлора, брома, йода или фтора, предпочтительно атом хлора, брома или фтора; термин "циклоалкильный радикал" обозначает насыщенный карбоциклический радикал, содержащий 3-10 атомов углерода, таким образом, обозначает, в частности, радикалы циклопропильный, циклобутильный, циклопентильный и циклогексильный, более конкретно циклопропильный, циклопентильный и циклогексильный радикалы; термин "гетероциклоалкильный радикал" обозначает, следовательно, моноциклический или бициклический карбоциклический радикал, содержащий 3-10 звеньев, прерываемые одним или несколькими гетероатомами, одинаковыми или различными, выбранными из атомов кислорода, азота или серы: в качестве примера могут быть названы радикалы морфолиниловый, тиоморфолиниловый, азиридиловый,азетидиловый, пиперазиниловый, пиперидиловый, гомопиперазиниловый, пирролидиниловый, имидазолидиниловый, пиразолидиниловый, тетрагидрофуриловый, тетрагидротиениловый, гексагидропирановый, оксодигидропиридазиниловый или оксетаниловый, причем все эти радикалы необязательно замещены; термины "ариловый" или "гетероариловый" обозначают ненасыщенные или частично ненасыщенные радикалы, соответственно карбоциклические и гетероциклические, моноциклические или бициклические, содержащие не более 12 звеньев, которые могут необязательно содержать звено -С(О), причем гетероциклические радикалы, содержащие один или несколько гетероатомов, одинаковых или различных, выбранных из О, N или S, где N, при необходимости, замещены; термин "ариловый радикал" обозначает, таким образом, моноциклические или бициклические радикалы, содержащие 6-12 звеньев, такие как, например, радикалы фенильный, нафтильный, бифенильный, инденильный, флуоренильный и антраценильный, более конкретно, радикалы фенильный и нафтильный, еще более конкретно, фенильный радикал. Следует указать, что карбоциклический радикал,содержащий звено -С(О), представляет собой, например, радикал тетралон; термин "гетероарильный радикал" обозначает, таким образом, моноциклические или бициклические радикалы, содержащие 5-12 звеньев: моноциклические гетероарильные радикалы, такие как, например, радикалы тиениловый, такой как 2-тиенил и 3-тиенил, фуриловый, такой как 2-фурил, 3-фурил, пираниловый, пирролиловый, пирролиниловый, пиразолиниловый, имидазолиловый, пиразолиловый, пиридиловый, такой как 2-пиридил, 3-пиридил и 4-пиридил, пиразиниловый, пиримидиниловый, пиридазиниловый, оксазолиловый, тиазолиловый, изотиазолиловый, диазолиловый, тиадиазолиловый, тиатриазолиловый, оксадиазолиловый, изоксазолиловый, такой как 3- или 4-изоксазолил, фуразаниловый, тетразолиловый свободный или в форме соли, причем все эти радикалы необязательно замещены заместителями, среди которых, более конкретно, радикалы тиениловый, такой как 2-тиенил и 3-тиенил, фуриловый,такой как 2-фурил, пирролиловый, пирролиниловый, пиразолиниловый, имидазолиловый, пиразолиловый, оксазолиловый, изоксазолиловый, пиридиловый, пиридазиниловый, причем эти радикалы необязательно замещены; бициклические гетероарильные радикалы, такие как, например, радикалы бензотиениловый, такой как 3-бензотиенил, бензотиазолиловый, хинолиловый, изохинолиловый, дигидрохинолиловый, хинолоновый, тетралоновый, адаментиловый, бензофуриловый, изобензофуриловый, дигидробензофурановый, этилендиоксифениловый, тиантрениловый, бензопирролиловый, бензимидазолиловый,бензоксазолиловый, тионафтиловый, индолиловый, азаиндолиловый, индазолиловый, пуриниловый, тиенопиразолиловый, тетрагидроиндазолиловый, тетрагидроциклопентапиразолиловый, дигидрофуропиразолиловый, тетрагидропирролопиразолиловый, оксотетрагидропирролопиразолиловый, тетрагидропиранопиразолиловый, тетрагидропиридинопиразолиловый или оксодигидропиридинопиразолиловый, причем все эти радикалы необязательно замещены. В качестве примеров гетероарильных или бициклических радикалов могут быть названы, более конкретно, радикалы пиримидиниловый, пиридиловый, пирролиловый, азаиндолиловый, индазолиловый или пиразолиловый, необязательно замещенные одним или несколькими заместителями, одинаковыми или различными, такими как указано выше. Радикал или радикалы карбокси производных формулы (I) могут быть превращены в соли или этерифицированы с помощью различных групп, известных специалисту, в числе которых можно назвать,например среди солеобразующих соединений минеральные основания, такие как, например, эквивалент натрия, калия, лития, кальция, магния или аммония, или органические основания, такие как, например, метиламин, пропиламин, триметиламин, диэтиламин, триэтиламин, N,N-диметилэтаноламин, трис(гидроксиметил)аминометан, этаноламин, пиридин, пиколин, дициклогексиламин, морфолин, бензиламин, прокаин, лизин, аргинин, гистидин, N-метилгюкамин; из этерифицирующих соединений, алкильные радикалы, образующие алкоксикарбонильные группы, такие как, например, метоксикарбонильная, этоксикарбонильная, трет-бутоксикарбонильная или бензилоксикарбонильная, причем эти алкильные радикалы могут быть замещены радикалами, выбранными, например, из атомов галогена, радикалов гидроксильный, алкокси, ацильный, ацилокси, алкилтио,амино или арильный, как, например, в хлорметильной, гидроксипропильной, метоксиметильной, пропионилметильной, метилтиометильной, диметиламиноэтильной, бензильной или фенетильной группах. Аддитивными солями производных формулы (I) с минеральными или органическими кислотами могут быть, например, соли, образованные с хлористо-водородной, бромисто-водородной, иодистоводородной, азотной, серной, фосфорной, пропионовой, уксусной, трифторуксусной, муравьиной, бензойной, малеиновой, фумаровой, янтарной, винной, лимонной, оксалиновой, глиоксиловой, аспарагиновой, аскорбиновой кислотой, с алкилмоносульфоновыми кислотами, такими как, например, метансульфоновая кислота, этансульфоновая кислота, пропансульфоновая кислота, с алкилдисульфоновыми кислотами, таким как, например, метандисульфоновая кислота, альфа, бета-этандисульфоновая кислота, с арилмоносульфоновыми кислотами, такими как бензолсульфоновая кислота, и с арилдисульфоновыми кислотами. Можно напомнить, что стереоизомерия может пониматься в широком смысле, как изомерия соединений, имеющих одинаковые структурные формулы, но различные группы которых расположены в пространстве по разному, такие как, в частности, в монозамещенных циклогексанах, заместитель которых может занимать аксиальное или экваториальное положение, и возможные различные ротационные конформации производных этана. Однако существует другой тип стереоизомерии, обусловленный различными пространственными перегруппировками заместителей, связанных либо с двойными связями, либо с циклами, которую называют часто геометрической изомерией или изомерией цис-транс. Термин стереоизомеры используется в настоящем описании в наиболее широком смысле и относится к совокупности соединений, указанных выше. Циклические радикалы, которые могут образовывать, с одной стороны, R1 и R2 с атомом азота, с которым они соединены, и, с другой стороны, R3 и R4 с атомом азота, с которым они соединены, необязательно замещены одним или несколькими радикалами, выбранными из радикалов, указанных выше для возможных заместителей гетероциклоалкильных радикалов, т.е. одним или несколькими радикалами,выбранными из атомов галогена, радикалов гидроксильный, оксо, алкокси, NH2; NH-алк, N(алк)2, и радикалов алкильный, гетероциклоалкильный, СН 2-гетероциклоалкильный, фенильный, СН 2-фенильный, гетероарильный и СО-фенильный, причем в этих последних радикалах радикалы алкильный, гетероциклоалкильный и фенильный сами необязательно замещены одним или несколькими радикалами, выбранными из атомов галогена и радикалов гидроксильный, оксо, алкильный и алкокси, содержащих 1-4 атома углерода, NH2; NH-алк и N(алк)2. Циклические радикалы, которые могут образовывать, с одной стороны, R1 и R2 с атомом азота, с которым они соединены, и, с другой стороны, R3 и R4 с атомом азота, с которым они соединены, необязательно замещены, в частности, одним или несколькими радикалами, одинаковыми или различными, выбранными из атомов галогена и радикалов алкильный, гидроксильный, алкокси, СН 2 пирролидиниловый, СН 2-фенильный, гетероарильный и фенильный, в которых радикалы алкильный,пирролидиниловый и фенильный сами необязательно замещены одним или несколькими радикалами,одинаковыми или различными, выбранными из атомов галогена и радикалов алкильный, гидроксильный,оксо и алкокси. Гетероциклоалкильные радикалы, которые описаны выше, обозначают, в частности, радикалы азепаниловый, морфолиниловый и пирролидиниловый, пиперидиловый и пиперазиниловый, которые сами необязательно замещены, так как описано выше или ниже. Когда NR1R2 или NR3R4 образуют цикл, такой как описан выше, то этот аминоцикл может быть выбран, в частности, из радикалов пирролидиниловый, пиразолидиниловый, пиразолиниловый, пиперидиловый, азепиниловый, морфолиновый или пиперазиниловый, причем эти радикалы сами необязательно замещены как указано выше или ниже: например, одним или несколькими радикалами, одинаковыми или различными, выбранными из атомов галогена и радикалов алкильный, гидроксильный, алкокси, фенильный и СН 2-фенильный, причем алкильный или фенильный радикалы сами необязательно замещены од-5 023465 ним или несколькими радикалами, одинаковыми или различными, выбранными из атомов галогена и алкильного, гидроксильного и алкокси радикалов. Более конкретно, цикл NR1R2 или NR3R4 может быть выбран из радикалов пирролидиниловый,морфолиновый, необязательно замещенный одним или двумя радикалами алкильным или пиперазиниловым, необязательно замещенным на втором атоме азота алкильным, фенильным или СН 2-фенильным радикалами, которые сами необязательно замещены одним или несколькими радикалами, одинаковыми или различными, выбранными из атомов галогена и алкильного, гидроксильного и алкокси радикалов. Настоящее изобретение относится, в частности, к производным формулы (I), в которой А означаетNH, а заместители Ra, X и W выбраны из всех значений, указанных для этих радикалов выше или ниже,причем указанные производные формулы (I) находятся во всех возможных изомерных, рацемических,энантиомерных и диастереоизомерных формах, а также к аддитивным солям производных формулы (I) с минеральными и органическими кислотами или с минеральными или органическими основаниями. Настоящее изобретение относится, в частности, к производным формулы (I), в которой А означаетS, а заместители Ra, X и W выбраны из всех значений, указанных для этих радикалов выше или ниже,причем указанные производные формулы (I) находятся во всех возможных изомерных, рацемических,энантиомерных и диастереоизомерных формах, а также к аддитивным солям производных формулы (I) с минеральными и органическими кислотами или с минеральными или органическими основаниями. В частности, настоящее изобретение относится к производным формулы (I), отвечающим формуле, Ra и W выбирают из всех значений, указанных выше или ниже,причем указанные производные формулы (Ia) и (Ib) находятся во всех возможных изомерных рацемических, энантиомерных и диастереоизомерных формах, а также к аддитивным солям производных формулы (Ia) и (Ib) с минеральными и органическими кислотами или с минеральными или органическими основаниями. Более конкретно, настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой означает простую связь, отвечающую производным формулы (I') в которой радикалы Ra, X, А и W выбирают из всех значений, указанных выше или ниже. Более конкретно, настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой означает двойную связь, отвечающую производным формулы (I) в которой радикалы Ra, X, А и W выбирают из всех значений, указанных выше или ниже. Более конкретно, настоящее изобретение относится к производным формулы (I), описанным выше или ниже, в которой означает простую связь, отвечающую производным формулы (Ia') в которой радикалы Ra и W выбирают из всех значений, указанных выше или ниже,причем указанные производные формулы (Ia') находятся во всех возможных изомерных рацемиче-6 023465 ских, энантиомерных и диастереоизомерных формах, а также к аддитивным солям производных формулы (Ia') с минеральными и органическими кислотами или с минеральными или органическими основаниями. Более конкретно, настоящее изобретение относится к производным формулы (Ia), описанным выше или ниже, в которой означает двойную связь, отвечающую производным формулы (I"а) в которой радикалы Ra и W выбирают из всех значений, указанных выше или ниже,причем указанные производные формулы (Iа) находятся во всех возможных изомерных рацемических, энантиомерных и диастереоизомерных формах, а также к аддитивным солям производных формулы (Iа) с минеральными и органическими кислотами или с минеральными или органическими основаниями. Более конкретно, настоящее изобретение относится к производным формулы (Ib), описанным выше или ниже, в которой означает простую связь, отвечающую производным формулы (I'b) в которой радикалы Ra и W выбирают из всех значений, указанных выше или ниже. Более конкретно, настоящее изобретение относится к производным формулы (Ib), описанным выше означает двойную связь, отвечающую производным формулы (I"b): или ниже, в которой в которой радикалы Ra и W выбирают из всех значений, указанных выше или ниже. Когда в продуктах формулы (I) Ra означает радикал то Rb находится, в частности, в пара-положении. Еще более конкретно, настоящее изобретение относится к производным формулы (I), которые описаны ниже, отвечающим следующим формулам: а также к аддитивным солям указанных производных формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями. Настоящее изобретение относится также к любому способу получения производных формулы (I),описанных выше. Таким образом, настоящее изобретение относится к любому способу получения производных формулы (I), описанных выше, в которых А означает NH. Таким образом, настоящее изобретение относится к любому способу получения производных формулы (I), описанных выше, в которых А означает S. Продукты согласно изобретению могут быть получены с использованием традиционных методов органической химии. Схемы 1-7, представленные ниже, приведены в качестве иллюстрации способов,используемых для получения производных формулы (I). Это означает, что не следует вводить ограничения в объем изобретения в отношении способов получения заявленных соединений. Таким образом, производные формулы (I), описанные выше, согласно настоящему изобретению могут быть получены, в частности, в соответствии со способами, описанными на ниже представленных схемах 1-7. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 1, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 2, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 3, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 4, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 5, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 6, представленной ниже. Так, настоящее изобретение относится также к способу получения производных формулы (I) согласно схеме 7, представленной ниже. Точно так же, как среди производных формулы (I), описанных выше, в которых означает простую или двойную связь, выделяют производные формулы (I'), которые представляют собой производные формулы (I), в которой означает простую связь, и производные формулы (I), которые представляют собой производные формулы (I), в которой означает двойную связь,так и в промежуточных соединениях синтеза, которые описаны ниже формулами (а), (b), (с), (d), (е) и (f), в которых означает простую или двойную связь, выделяют соединения формул (а'), (b'), (c'),(d'), (e') и (f'), в которых означает простую связь, и соединения формул (а), (b), (c), (d), (е) и(f), в которых означает двойную связь. Схема 1 Синтезы производных бензимидазолов формул (1 а), (1b"), (1c), (1d"), (1e"), (1a'), (1b'), (1c'), (1d') и (1 е'). На схеме 1, представленной выше, заместители Ra, R1 и R2 имеют значения, указанные выше для производных формулы (I') и (I), заместитель R5 в соединениях формул (J), (1a') и (1 а) означает алкил, а заместитель R6 в соединениях формул (О), (1d') (1d) означает алкил, необязательно замещенный NR3R4(радикал -(СН 2)n-NR3R4), алкокси, гидрокси, гетероциклоалкилом, фенилом, -(СН 2)n-фенилом, где фенил необязательно замещен и п обозначает целое число от 1 до 4. Заместитель R7 в соединениях (Р) и(1 е')/(1 е) означает циклоалкильный радикал или алкильный радикал, необязательно замещений радикалом NR3R4, алкокси, гидроксильным, фенильным, гетероарильным или гетероциклоалкильным, которые сами необязательно замещены. На схеме 1, представленной выше, бензимидазолы общей формулы (1a), (1b"), (1c), (1d") и (1 е), а также их восстановленные аналоги общей формулы (1a'), (1b'), (1 с'), (1d') и (1 е') могут быть получены из 3, 6-дихлорпиразина (А) (выпускаемого в продажу). Соединения (С) могут быть получены, например, реакцией сочетания 3,6-дихлорпиразина с бороновой кислотой формулы (В), где Ra описан выше, в условиях, описанных, например, A. Gueiffer et coll.(в документе Synthesis; 2001; 4; 595) в присутствии тетракис-(трифенилфосфин)палладия(0) в растворителе, таком как диоксан, и в присутствии основания, такого как гидрокарбонат натрия, при температуре около 115 С. Соединения (D) такие, в которых Ra отличается от Н, могут быть получены, например, реакцией между гидрохлоридом гидразинкарбоксамида и соединением формулы (С) в растворителе, таком как бутанол, и в присутствии основания, такого как триэтиламин, при температуре около 140 С. Соединения (D), в которых Ra=H, могут быть получены согласно способу, описанному P. Francavilla et F. Lairia (Journal of Heterocyclic Chemistry; 1971; 415) путем гидрогенолиза соединения (D), в котором Ra=Cl (выпускаемое в продажу), например, в присутствии формиатаммония и палладия на угле в растворителе, таком как метанол, при температуре около 70 С. Соединения (Е) могут быть получены, например, взаимодействием трихлорида фосфора (оксихлорид фосфора) с соединениями формулы (D). Реакцию осуществляют, например, при температуре около 150 С в герметично закрытой колбе при микроволновом облучении. Соединения (G) могут быть получены, например, взаимодействием 3-амино-4-нитробензолтиола формулы (F) с соединениями формулы (Е). Соединения формулы (F) получают путем восстановления insitu 3-амино-4-нитрофенилтиоцианата (Q) (выпускаемое в продажу), например, в присутствии боргидрида натрия в растворителе, таком как N,N-диметилформамид, при температуре около 20 С. Соединения (Н), в которых означает двойную связь, могут быть получены, например, путем восстановления с помощью железа(0) соединений формулы (G) в растворителе, таком как метанол, в присутствии уксусной кислоты при температуре около 70 С. Соединения (Н'), в которых означает простую связь, могут быть получены, например, путем восстановления с помощью цинка(0) соединений формулы (G) в присутствии уксусной кислоты при температуре около 20 С. Более конкретно, карбаматы общей формулы (1a') и (1 а) могут быть получены, в частности, в соответствии с тем, как описано в патенте WO 03028721A2, но исходя соответственно из 3,4 диаминофенилсульфида формулы (Н') и (Н) и псевдо-тиокарбамида формулы (J) в присутствии уксусной кислоты и в протонном растворителе, таком как метанол, при температуре около 80 С. Более конкретно, бензимидазолы общей формулы (1b') и (1b) могут быть получены, соответственно взаимодействием амина NHR1R2 формулы (R) (где R1 и R2 имеют значения, указанные выше) с карбаматом формулы (1a') и (1 а), например, в присутствии апротонного растворителя, такого как 1-метил-2 пирролидинон. Реакцию осуществляют, например, при температуре около 120 С в герметично закрытой колбе при микроволновом облучении. Более конкретно, 2-аминобензимидазолы общей формулы (1 с') и (1 с) могут быть получены, например, взаимодействием цианбромида с соединением формулы соответственно (Н') и (Н) в присутствии протонного растворителя, такого как этанол. Реакцию осуществляют при температуре около 80 С. Более конкретно, карбаматы общей формулы (1d') и (1d) могут быть получены взаимодействием хлоркарбоната формулы (О) (Х=Cl) с соединением общей формулы, соответственно, (1 с') и (1 с), напри- 12023465 мер, в растворителе, таком как тетрагидрофуран, в присутствии основания, такого как гидрокарбонат натрия, при температуре около 20 С. Более конкретно, карбоксамиды (1 е') и (1 е) могут быть получены соответственно из аминов общей формулы (1 с') и (1 с) взаимодействием аминов (1 с') и (1 с) с хлорангидридом кислоты формулы (Р) (Х=Cl) в присутствии, например, растворителя, такого как пиридин, при температуре около 20 С; взаимодействием аминов (1 с') и (1 с) с ангидридом кислоты формулы (Р) (X=OCOR7) в присутствии, например, растворителя, такого как пиридин, при температуре около 20 С; реакцией сочетания аминов (1 с') и (1 с) с кислотой формулы (Р) (Х=ОН) в условиях, например,описанных D.D. DesMarteau; V. Montanari (Chera Lett, 2000 (9), 1052) в присутствии 1 гидроксибензотриазола и 1-(3-диметиламинопропил)-3-этилкарбодиимида и в присутствии основания,такого как триэтиламин, при температуре около 40 С. Схема 2 Синтез бензотиазольных производных формул (2 а'), (2b'), (2c'), (2d'), (2 а"), (2b"), (2 с"), (2d") В схеме 2, представленной выше, заместители Ra, R1 и R2 имеют значения, указанные выше для производных формулы (I') и (I"), а заместитель R6 в соединениях формул (О), (L1), (M1) и (2 а'/2 а") означает алкил, необязательно замещенный группой NR3R4 (радикал -(СН 2)n-NR3R4), алкокси, гидрокси, гетероциклоалкильной, фенильной, -(СН 2)n-фенильной, где фенил необязательно замещен и п обозначает целое число от 1 до 4, причем OR6 имеет значения, соответствующие R, который определен выше для производных формулы (I') и (I"). Заместитель R7 в соединениях формул (M3), (L3), (Р) и (2 с'/2 с") означает циклоалкильный радикал или алкильный, необязательно замещенный радикалом NR3R4, алкокси, гидрокси или радикалом фенильным, гетероарильным или гетероциклоалкильным, необязательно замещенными. На схеме 2, представленной выше, бензотриазолы общей формулы (2 а), (2b), (2 с) и (2d), а также их восстановленные аналоги общей формулы (2 а'), (2b'), (2 с') и (2d') могут быть получены из 2-амино 1,3-бензотиазол-6-илтиоцианата (K) (выпускаемого в продажу). Карбаматы общей формулы (L1) могут быть получены, например, путем взаимодействия хлоркарбоната формулы (О) (Х=Cl) с 2-амино-1,3-бензотиазол-6-илтиоцианатом (K) в растворителе, таком как тетрагидрофуран, в присутствии основания, такого как гидрокарбонат натрия, при температуре около 20 С. Соединения общей формулы (L2) могут быть получены, например, взаимодействием карбаматов формулы (L1), где R6=фенил, с аминами NHR3R4 формулы (R) (где R1 и R2 имеют указанные выше значения) в присутствии апротонного растворителя, такого как тетрагидрофуран, при температуре около 20 С. Карбамиды (2b') и (2b) могут быть получены, например, соответственно, из карбаматов (2 а') и(2 а), где R6=фенил, таким же образом, как и карбамиды (L2) получены взаимодействием аминов с карбаматами типа (L1). Соединения общей формулы (L3) могут быть получены, например реакцией хлорангидрида кислоты формулы (Р) (Х=Cl) с 2-амино-1,3-бензотиазол-6-илтиоцианатом(K) в присутствии, например, растворителя, такого как пиридин, при температуре около 20 С; реакцией ангидрида кислоты формулы (Р) (X=OCOR7) с 2-амино-1,3-бензотиазол-6-илтиоцианатом(K) в присутствии, например, растворителя, такого как пиридин, при температуре около 20 С; реакцией сочетания 2-амино-1,3-бензотиазол-6-илтиоцианатом (K) с кислотой формулы (Р) (Х=ОН) в условиях, например, описанных D.D. DesMarteau; V. Montanari (Chem Lett, 2000 (9), 1052) в присутствии 1-гидроксибензотриазола и 1-(3-диметиламинопропил)-3-этилкарбодиимида и в присутствии основания, такого как триэтиламин, при температуре около 40 С. Таким же способом как карбамиды (L3) могут быть получены путем ацилирования амина (K), карбоксиамиды (2 с') и (2 с) могут быть получены соответственно из аминов (2d') и (2d). Соединения общей формулы (M1), (M2) и (M3) могут быть получены, например, восстановлением соединений общей формулы (L1), (L2), (L3) с помощью DL-дитиотреитола в присутствии дигидрокарбоната натрия в растворителе, таком как этанол, при температуре около 80 С. Соединение общей формулы (N) может быть получено in situ путем восстановления соединения формулы (K) с непосредственным получением аминопроизводных формулы (2d') и (2d), например, с помощью боргидирида натрия в растворителе, таком как N,N-диметилформамид, в присутствии основания, такого как триэтиламин, при температуре около 95 С или в интервале от 20 до 95 С. Более конкретно, бензотиазолы общей формулы (2d') и (2d) могут быть также получены, соответственно, из карбаматов формулы (2 а') и (2 а), где R6 = трет-бутил, путем реакции, например, с трифторуксусной кислотой в растворителе, таком как дихлорметан, при температуре около 20 С. И наоборот, бензотиазолы общей формулы (2 а') и (2 а) могут быть также получены, соответственно, из бензотиазолов формулы, соответственно, (2d') и (2d), например, путем взаимодействия с хлоркарбонатом формулы (О) (Х=Cl) в растворителе, таком как тетрагидрофуран, в присутствии основания, такого как гидрокарбонат натрия, при температуре около 20 С. Более конкретно, бензотиазолы общей формулы (2 а), (2b), (2 с) и (2d), а также их восстановленные аналоги общей формулы (2 а'), (2b'), (2 с') и (2d') могут быть получены, например: 1) либо реакцией сочетания соединения формулы (Е) с производными (M1), (М 2), (M3) и (N), осуществляемой in situ восстановлением производных (L1), (L2), (L3) и (K) с помощью боргидрида натрия в растворителе, таком как N,N-диметилформамид, в присутствии основания, такого как триэтиламин, при температуре около 95 С или в интервале от 50 до 95 С; 2) либо реакцией сочетания выделенных производных (M1), (М 2) и (M3) с соединением формулы(Е) в присутствии боргидрида натрия в растворителе, таком как N,N-диметилформамид, и в присутствии основания, такого как триэтиламин, при температуре около 95 С; 3) либо реакцией сочетания выделенных производных (M1), (М 2) и (M3) с соединением формулы(Е) в условиях, например, описанных U. Schopfer et coll (Tetrahedron, 2001, 57, 3069) в присутствии нтрибутилфосфина, трет-бутилата калия, трис-(дибензилиденацетон)дипалладия(0) и бис-(2 дифенилфосфинфенилового)эфира в растворителе, таком как толуол, при температуре около 110 С. 4) либо реакцией сочетания соединения формулы (Е) с производными (M1), (M2) и (M3) и (N),осуществляемой in situ восстановлением производных (L1), (L2), (L3) и (K) в присутствии DLдитиотреитола и дигидрокарбоната натрия в растворителе, таком как этанол, при температуре около 80 С. В восстановительных условиях 1) и 2) можно получить производные формулы (2 а), (2b), (2 с) и (2d),в которых означает простую или двойную связь, а в условиях 3) и 4) получают производные формулы (2 а), (2b), (2 с) и (2d), в которых означает двойную связь. Схема 3 Другие пути синтеза производных триазолпиридазина формулы (Е) На схеме 3, представленной выше, заместители Ra, R1 и R2 имеют значения, указанные выше для соединений формулы (I') и (I). Заместитель R7 означает алкильный или циклоалкильный радикал. Заместитель R8 означает либо алкильный радикал, необязательно замещенный атомом хлора, гидроксильным радикалом или гетероциклоалкильным радикалом, который сам необязательно замещен; либо циклоалкильный радикал. Соединения формулы (Е) могут быть получены, например, следуя схеме 3, представленной выше,из 3,6-дихлор[1,2,4]триазоло[4,3-b]пиридазина формулы (S), выпускаемого в продажу. Более конкретно, соединения формулы (Е), в которой Ra означает радикал OR8, могут быть получены обработкой 3,6-дихлор[1,2,4]триазоло[4,3-b]пиридазина формулы (S) с помощью алкоголята формулы(U) при температуре около 80 С и в растворителе, таком как N,N-диметилформамид. Более конкретно, соединения формулы (Е), в которой Ra означает радикал NR1R2, могут быть получены обработкой 3,6-дихлор[1,2,4]триазоло[4,3-b]пиридазина формулы (S)c помощью амина формулы(R) при температуре около 20 С в растворителе, таком как N,N-диметилформамид, или в случае, когдаNR1R2 является NH2, с помощью водного раствора гидроксида аммония в растворителе, таком как диоксан, в герметичной колбе при температуре в интервале 70-90 С. Более конкретно, соединения формулы (Е), в которой Ra означает радикал NHCOR7, могут быть получены путем взаимодействия соединения общей формулы (Е), где Ra=NH2, с соединением формулы(Р), как описано для соединений общей формулы (L3), (1 е') и (1 е). Более конкретно, соединения формулы (Е), в которой Ra означает арильный или гетероарильный радикал, могут быть получены, например из бороновых кислот формулы (V) (R'=H) в присутствии октагидратного гидроксида бария и (1,1'бис-(дифенилфосфин)ферроцен)дихлорпалладия(II) в растворителе, таком как, например, N,Nдиметилформамид, при температуре около 80 С; или, в качестве варианта, из сложных эфиров бороновой кислоты формулы (V) в присутствии дихлор-бис-(трифенилфосфин) палладия в растворителе, таком как, например, 1,2-диметоксиэтан, в присутствии основания, такого как 1 н. раствор щелочи натрия, при температуре около 80 С. Схема 4 Другой путь синтеза 2-аминобензотиазолов формулы (2d") В соответствии со схемой 4, представленной выше, 2-аминобензотиазолы общей формулы (2d) могут быть также получены из соединений формулы (М 2) и соединения формулы (Е) в присутствии карбоната калия в растворителе, таком как диметилсульфоксид. Реакцию осуществляют, например, при микроволновом облучении в течение приблизительно 10 мин. при температуре около 190 С. В полученном соединении формулы (2d) заместитель Rc означает атом водорода или гетероарильный радикал, не связанный с атомом азота, или фенильный радикал, причем эти радикалы необязательно замещены как указано выше для заместителя Ra. Схема 5 Синтез производных бензотиазолов формулы (2 е') и (2 е") В соответствии со схемой 5, представленной выше, бензотиазолы общей формулы (2 е') и (2 е) могут быть также получены из соединений, соответственно, формулы (2 а') и (2 а). На схеме 5, представленной выше, заместитель OR6 означает, предпочтительно, О-трет-бутил. Заместитель R9 означает радикал алкильный или циклоалкильный радикал, необязательно замещенный радикалом алкокси, гетероциклоалкильным или NR3R4 (R3 и R4 имеют значения, описанные выше). Карбаматы общей формулы (Т') и (Т) могут быть получены путем взаимодействия карбаматов, соответственно, общей формулы (2 а') и (2 а), гед, предпочтительно, R6=трет-бутил, например, с алкилгалогенидами формулы (W) в растворителе, таком как N,N-диметилформамид, в присутствии гидрида натрия при температуре 20-90 С. Бензотиазолы общей формулы (2 е') и (2 е) могут быть также получены из соединений формулы(L1), где, предпочтительно, R6=трет-бутил, с использованием соединений формулы (Т') и (Т"). Более конкретно, соединения общей формулы (2 е') и (2 е) могут быть получены обработкой, соответственно, выделенных соединений (Т') и (Т"), например, с помощью трифторуксусной кислоты в растворителе, таком как дихлорметан, при температуре около 20 С. В качестве варианта, соединения общей формулы (2 е) могут быть получены сразу в результате реакции соединений формулы (L4) и (Е) с использованием соединения (Т"), образующегося in situ, например, в присутствии DL-дитиотреитола и дигидрокарбоната натрия, в растворителе, таком как этанол, при температуре около 80 С с последующей необязательной обработкой in situ трифторуксусной кислотой при температуре 20 С, если необходимо. Карбаматы общей формулы (L4) могут быть получены путем взаимодействия карбаматов общей формулы (L1), например, с алкилгалогенидами формулы (W) в растворителе, таком как N,Nдиметилформамид, в присутствии гидрида натрия при температуре в интервале 20-90 С. Схема 5-бис Синтез производных бензотиазолов формулы (2 е') и (2 е") В качестве варианта, в соответствии со схемой 5-бис, представленной выше, бензотиазолы общей формулы (2 е) могут быть получены из соединений формул (L6) и (Е), например, в присутствии DLдитиотреитола и дигидрокарбоната натрия, в растворителе, таком как этанол, при температуре около 80 С. Бензотиазолы общей формулы (2 е') могут быть получены из соединений формулы (2 е) согласно способам, описанным ниже для получения соединений (I'), исходя из соединений (I). Соединения формулы (L6) могут быть получены из 2-бромбензотиазольного производного (L5) путем обработки производным NH2R9, например, в растворителе, таком как тетрагидрофуран, при температуре около 20 С. Заместитель R9 означает алкильный или циклоалкильный радикал, необязательно замещенный радикалом алкокси, гетероциклоалкильным или NR3R4 (R3 и R4 имеют описанные выше значения). Соединения формулы (L5) могут быть получены из 2-амино-1,3-бензотиазол-6-илтиоцианата (K)(выпускаемое в продажу), например, обработкой алкилнитритом и бромидом меди(I) в растворителе,таком как ацетонитрил, при температуре около 0-20 С, в соответствии со способом, описанным Jagabandhu Das et al. J. Med. Chem. 2006, 49, 6819-6832. Схема 6 Другие синтезы восстановленных производных формулы (I') В соответствии со схемой 6, представленной выше, бензотиазолы общей формулы (I') могут быть получены также из соединений формулы (I) путем восстановления, например, боргидридом натрия в растворителе, таком как этанол, при температуре около 80 С, или цинком(0) в присутствии уксусной кислоты при температуре около 20 С. В качестве варианта соединения (I') могут быть получены также из соединений формулы (Е') путем сочетания с соединениями типа M1, M2, M3 или N, полученными в качестве промежуточных соединений восстановлением соединений L1, L2, L3 или K in situ, как описано выше на схеме 2. Соединения типаM1, M2 или M3 могут быть также выделены и использованы для реакции сочетания с (Е'). Соединения(Е') могут быть получены из соединений формулы (Е) путем восстановления, например, восстановлением с использованием цинка(0) в присутствии уксусной кислоты при температуре около 20 С. В качестве варианта соединения (I') могут быть получены также из других соединений формулы (I') путем превращения группы W в группу W' таким же образом, как описано выше для W и согласно типу реакций, описанному на схеме 2: превращения 2d'/2d" в 2 а'/2 а и в 2 с'/2 с", превращения 2 а'/2 а" в 2d'/2d и в 2b'/2b. Схема 7 Синтез N-оксидных производных бензотиазолов формул (2f') и (2f") В соответствии со схемой 7, представленной выше, бензотиазолы общей формулы (2f') и (2f) могут быть получены, соответственно, из соединений формулы (2 а') и (2 а), у которых заместитель W содержит функциональную группу основного характера типа NR3R4 (R3 и R4 имеют определенные выше значения,причем R3 и R4 отличаются от Н), путем окисления, например, периодатом натрия, в присутствии уксусной кислоты при температуре около 20 С. В соединениях общей формулы (I), описанных выше, можно окислить серу S до сульфоксида SO или сульфона SO2 в соответствии со способами, известными специалисту, одновременно защищая, при необходимости, возможные реакционноспособные группы с помощью соответствующих защитных групп. Среди исходных производных формулы А, В, J, K, О, Р, Q, R, S, U, V, W некоторые продукты известны и могут быть приобретены либо на рынке, либо получены известными специалисту способами,например, из продуктов, имеющихся в продаже. Специалисту должно быть известно, что для осуществления способов согласно изобретению, описанных выше, следует, при необходимости, вводить защитные группы для аминной, карбоксильной и спиртовой функциональной группы, чтобы избежать побочных реакций. Ниже представлен неограничивающийся перечень примеров защиты функциональных реакционоспособных групп: гидроксильные группы могут быть защищены, например, алкильными радикалами, такими как трет-бутильный, триметилсилильный, трет-бутилдиметилсилильный, метоксиметильный, тетрагидропиранильный, бензильный или ацетильный; аминогруппы могут быть защищены, например, радикалами ацетильным, тритильным, бензильным,трет-бутоксикарбонильным, ВОС, бензилоксикарбонильным, фталимидо или другими радикалами, известными в химии пептидов. Кислотные функции могут быть защищены, например, в форме сложных эфиров, образующихся с легко отщепляемыми сложными эфирами, такими как бензиловые или трет-бутиловые сложные эфиры или сложные эфиры, известные в химии пептидов. Перечень различных используемых защитных групп можно найти в известных специалисту учебниках и, например, в патенте BF 2499995. Следует отметить, что, при желании или необходимости, промежуточные продукты или производные формулы (I), полученные указанными выше способами, можно подвергнуть, для получения других промежуточных соединений или других производных формулы (I), одной или нескольким реакциям превращения, известным специалисту, таким как, например:a) реакции этерификации кислотной группы;b) реакции омыления сложноэфирной группы в кислотную группу;c) реакции восстановления свободной или этерифицированной карбоксигруппы до спиртовой группы;d) реакции превращения алкоксигруппы в гидроксильную группу или же гидроксильной группы в алкоксигруппу;e) реакции удаления защитных групп, которые могут нести защищенные функциональные группы;f) реакции солеобразования с помощью минеральной или органической кислоты или основания с получением соответствующей соли;g) реакции разделения рацемических форм с получением разделенных продуктов,причем полученные таким образом указанные производные формулы (I) находятся во всех возможных изомерных формах, рацемической, энантиомерной и диастереоизомерной. Реакции а)-g) могут быть осуществлены в известных условиях, используемых специалистом, таких как, например, условия, указанные ниже.a) Продукты, описанные выше, при желании подвергают реакциям этерификации по возможным карбоксильным группам, которые можно осуществить в соответствии с известными способами, используемыми специалистом.b) Возможные превращения сложноэфирных групп в кислотные группы описанных выше продуктов могут быть, при желании, осуществлены в известных условиях, используемых специалистом, в частности, путем кислотного или щелочного гидролиза, например, гидроксидом натрия или калия, в спирто- 18023465 вой среде, такой как, например, в среде метанола, или же хлористо-водородной или серной кислотой. Реакция омыления может быть осуществлена в соответствии с известными методами, используемыми специалистом, такими как, например, в растворителе, таком как метанол или этанол, диоксан или диметоксиэтан, в присутствии гидроксида натрия или калия.c) Возможные карбоксильные группы, свободные или этерифицированные, продуктов, описанных выше, могут быть, при желании, восстановлены до спиртовых групп известными специалисту способами: возможные этерифицированные карбоксигруппы, при желании, могут быть восстановлены до спиртовой группы известными специалисту способами, в частности, литийалюминиевым гидридом в растворителе, таком как, например, тетрагидрофуран или диоксан или этиловый эфир. Возможные свободные карбоксигруппы продуктов, описанных выше, при желании, могут быть восстановлены до спиртовой группы, в частности, с помощью гидрида бора.d) Возможные алкоксигруппы, такие как, например, метоксигруппы продуктов, описанных выше,при желании, могут быть превращены в гидроксильные группы в известных условиях, используемых специалистом, например, с помощью трибромида бора, в растворителе, таком как, например, метиленхлорид, с помощью гидробромида или гидрохлорида пиридина, или же с помощью бромисто-водородной или хлористо-водородной кислоты в воде или трифторуксусной кислоты при температуре кипения с обратным холодильником.e) Удаление защитных групп, таких как, например, группы, указанные выше, может быть осуществлено в известных условиях, используемых специалистом, в частности, путем кислотного гидролиза,осуществляемого кислотой, такой как хлористо-водородная, бензолсульфоновая или паратолуолсульфоновая, муравьиная или трифторуксусная кислота, или же путем каталитического гидрирования. Удаление фталимидной группы может быть осуществлено с помощью гидразина,f) Продукты, описанные выше, при желании, могут быть подвергнуты реакции солеобразования,например, с помощью минеральной или органической кислоты, или минерального или органического основания в соответствии с известными способами, используемыми специалистом: такая реакция солеобразования может быть осуществлена, например, в присутствии хлористо-водородной кислоты, например, или же винной, лимонной или метансульфоновой кислоты, в спирте, таком как, например, этанол или метанол.g) Возможные оптически активные формы продуктов, описанных выше, могут быть получены разделением рацемической смеси в соответствии с используемыми методами, известными специалисту. Производные формулы (I), описанные выше, а также их аддитивные соли с кислотами имеют интересные фармакологические свойства, а именно, обусловленные их киназ-ингибирующими свойствами,изложенными выше. Продукты согласно изобретению полезны, в частности, для терапии опухолей. Продукты согласно изобретению могут также увеличивать терапевтические эффекты широко используемых противораковых агентов. Свойства этих продуктов оправдывают их применение в терапии, поэтому, более конкретно, изобретение относится к производным формулы (I), описанным выше, в качестве лекарственных средств,причем указанные производные формулы (I) находятся во всех возможных изомерных рацемических,энантиомерных и диастереомерных формах, а также к аддитивным солям производных формулы (I) с фармацевтически приемлемыми минеральными или органическими кислотами или с минеральными или органическими основаниями. Еще более конкретно, изобретение относится к лекарственным средствам, представляющим продукты, имеющие следующие формулы: а также к аддитивным солям производных формулы (I) с фармацевтически приемлемыми минеральными или органическими кислотами или минеральными или органическими основаниями. Изобретение относится также к фармацевтическим композициям, содержащим в качестве активного начала по меньшей мере один из производных формулы (I), описанных выше, или одну фармацевтически приемлемую соль этого продукта или одно пролекарство этого продукта и, при необходимости, фармацевтически приемлемый носитель. Изобретение относится также к фармацевтическим композициям, содержащим в качестве активного начала по меньшей мере одно из лекарственных средств, описанных выше. Упомянутые фармацевтические композиции согласно настоящему изобретению могут, при необходимости, содержать также активные начала других антимитотических лекарственных средств, в частности, средства на основе таксола, цис-платины, ДНК-интеркалирующие агенты и другие. Эти фармацевтические композиции согласно настоящему изобретению могут вводиться буккальным путем, парентеральным путем или локально путем топического нанесения на кожу или слизистые,или путем внутривенных или внутримышечных инъекций. Эти композиции могут быть жидкими или твердыми и находиться во всех фармацевтических формах, широко используемых в медицине человека, как, например, таблетки, простые или дражированные,пилюли, лепешки, желатиновые капсулы, капли, гранулы, препараты для инъекций, мази, кремы и гели; композиции получают в соответствии с известными способами. Активное начало может быть введено в них вместе со вспомогательными добавками, используемыми обычно в фармацевтических композициях,такими как тальк, гуммиарабик, лактоза, крахмал, стеарат магния, масло какао, водные или неводные носители, жировые вещества животного или растительного происхождения, парафиновые производные,гликоли, различные смачивающие агенты, диспергаторы или эмульгаторы, консерванты. Используемую дозировку вирьируют в зависимости от используемого продукта, от лечимого больного и его заболевания, она может составлять, например, 0,05-5 г в день для взрослого, предпочтительно,0,1-2 г в день. Настоящее изобретение относится также к применению производных формулы (I), описанных выше, или фармацевтически приемлемых солей этих продуктов для получения лекарственного средства,предназначенного для ингибирования активности протеинкиназы. Настоящее изобретение относится также к применению производных формулы (I), описанных выше, для получения лекарственного средства, предназначенного для лечения или предупреждения заболевания, характеризующегося дерегуляцией активности протеинкиназы. Такое лекарственное средство может быть предназначено, в частности, для лечения или предупреждения заболевания у млекопитающих. Настоящее изобретение относится также к применению, описанному выше, при котором протеинкиназа является протеинтирозинкиназой. Настоящее изобретение относится также к применению, описанному выше, при котором протеинтирозинкиназа является МЕТ или ее мутантными формами. Настоящее изобретение относится также к применению, описанному выше, при котором протеинкиназа находится в клеточной культуре. Настоящее изобретение относится также к применению, описанному выше, при котором протеинкиназа находится в организме млекопитающего. Настоящее изобретение относится, в частности, к применению продукта формулы (I), описанного выше, для получения лекарственного средства, предназначенного для предупреждения или лечения заболеваний, связанных с неконтролируемой пролиферацией. Настоящее изобретение относится, в частности, к применению продукта формулы (I), описанного выше, для получения лекарственного средства, предназначенного для лечения или предупреждения заболевания, выбранного из следующей группы: нарушения пролиферации кровеносных сосудов, наруше- 22023465 ния фибротических процессов, нарушения пролиферации "мезангиальных" клеток, метаболические расстройства, аллергии, астмы, тромбозы, болезни нервной системы, ретинопатия, псориаз, ревматоидный артрит, диабет, мышечная дегенерация и раки. Еще более конкретно, настоящее изобретение относится к применению продукта формулы (I), описанного выше, для получения лекарственного средства, предназначенного для лечения или предупреждения онкологических заболеваний, в частности, предназначенного для лечения раков. Среди раковых заболеваний привлекает внимание лечение солидных опухолей и опухолей мягких тканей, лечение злокачественных опухолей, резистентных к цитотоксическим агентам. Продукты согласно изобретению могут быть использованы, в частности, для лечения первичных опухолей и/или метастаз, в частности, при раке желудка, печени, мочевых путей, яичников, ободочной кишки, предстательной железы, легких (NSCLC и SCLC), глиобластом, при раках щитовидной железы,мочевого пузыря, молочной железы, при меланоме, гематопоэтических лимфоидных или миелоидных опухолей, саркомах, при раках мозга, гортани, лимфатической системы, рака костей и поджелудочной железы. Настоящее изобретение относится также к применению производных формулы (I), описанных выше, для получения лекарственных средств, предназначенных для химиотерапии раков. Указанные лекарственные средства, предназначенные для химиотерапевтического лечения раков,могут быть использованы индивидуально или в комплексной терапии. Продукты согласно изобретению могут вводиться, в частности, индивидуально или могут быть применены в комплексе с химиотерапевтическим или радиотерапевтическим лечением или в комплексе с другими терапевтическими средствами. Такими терапевтическими средствами могут быть широко используемые противоопухолевые агенты. В качестве ингибиторов киназ можно назвать бутиролактоны, флавопиридол и 2-(2 гидроксиэтиламино)-6-бензиламино-9-метилпурин, называемый оломуцином. Настоящее изобретение относится также к новым промежуточным производным триазолопиридазина формулы Е' и производным бензотиазола, соответствующим формулам Е', M1, M2, M3 и N, описанным выше, и представленным ниже: в которых Ra имеет указанные выше значения;R6 означает радикал С 1-4 алкил, необязательно замещенный группой NR3R4, C1-4 алкокси, гетероциклоалкильной или фенильной, причем OR6 имеет значения, соответствующие радикалу R, описанному выше;R1, R2, R3 и R4 имеют указанные выше значения, в качестве новых промышленных продуктов. Следующие примеры, относящиеся к производным формулы (I), иллюстрируют изобретение, не ограничивая его объема. Экспериментальная часть Номенклатура соединений согласно настоящему изобретению устанавливалась с помощью программного обеспечения ACDLABS, версия 10.0. Используемая микроволновая печь: Biotage, Initiator EXP-EU, максимальная мощность 300 W, частота 2450 МГц. Спектры ЯМР 1 Н при 400 МГц и 1 Н при 300 МГц регистрировались на спектрометре BRUKERDAD проводится при длине волны =210-400 нм.ELSD: Sedere SEDEX 85; температура распыления = 35 С; давление распыления = 3,7 бар. Пример 1. Метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2 ил)карбамат. а) Метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2 ил)карбамат может быть получен следующим образом. К суспензии 242 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазина и 100 мг метил-(6 сульфанил-1,3-бензотиазол-2-ил) карбамата в 3 см 3 N,N-диметилформамида при 20 С прибавляют 0,14 см 3 триэтиламина и 31 мг боргидрида натрия. Частично растворенную суспензию фиолетовокоричневого цвета перемешивают при 95 С в течение 2 ч. Раствор охлаждают до 20 С, затем обрабатывают смесью 50/50 воды и этилацетата. Полученную суспензию центрифугируют и получают 155 мг нерастворенного продукта бело-кремого цвета, который содержит целевой продукт с 70% метил-(6 сульфанил-1,3-бензотиазол-2-ил)карбамата. После экстракции маточных растворов этилацетатом с последующей сушкой органических фаз над сульфатом магния, фильтрацией и упариванием досуха в ротационном испарителе образуется полукристаллизованное масло, которое затем фильтруют. Получают 48 мг белого порошка, содержащего 80% метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3 ил]сульфанил-1,3-бензотиазол-2-ил)карбамата. 155 мг продукта, содержащего 70% метил-(6-сульфанил-1,3-бензотиазол-2-ил)карбамата, снова вводят в реакцию с 50 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазина в N,Nдиметилформамиде, содержащем 0,07 см 3 триэтиламина и 15 мг боргидрида натрия. Частично растворенную суспензию фиолетово-коричневого цвета перемешивают при 95 С в течение 2 ч. Раствор охлаждают до 20 С, затем обрабатывают смесью 50/50 воды и этилацетата. Полученную суспензию фильтруют и получают 112 мг нерастворенного продукта бело-кремового цвета, содержащего метил-(6-[6-(4 фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2-ил)карбамат. Объединяют партии массой 48 мг и 112 мг и очищают путем хроматографии на колонке Biotage Si 12M+, элюируя с градиентом 95/5, затем 90/10 дихлорметана и раствора 38/17/2 дихлорметан/метанол/водный раствор гидроксида аммония. Получают 56 мг метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3 бензотиазол-2-ил)карбамата в виде белого порошка, который имеет следующие характеристики: Температура плавления 270 С (по Кофлеру). Спектр 1 Н ЯМР (400 МГц,м.д.) (ДМСО-d6): 3,78 (с, 3 Н); 7,40 (т, J=9,0 Гц, 2 Н); 7,54 (дд, J=2,0 и 8,0 Гц, 1 Н); 7,65 (д, J=8,0 Гц, 1 Н); 8,03 (д, J=9,5 Гц, 1 Н); 8,10 (дд, J=5,0 и 9,0 Гц, 2 Н); 8,21 (д, J=2,0 Гц, 1 Н); 8,51 (д, J=9,5 Гц, 1 Н); 12,15 (уш.м, 1 Н). Масс-спектр: LC-MS-DAD-ELSD: 451(-)=(М-Н)(-); 453(+)=(М+Н)(+).b) Метил-(6-сульфанил-1,3-бензотиазол-2-ил)карбамат может быть получен следующим образом. К суспензии белого цвета, содержащей 280 мг метил(6-тиоцианат-1,3-бензотиазол-2-ил)карбамата в 11 см 3 этанола, при 20 С прибавляют раствор 5 мг дигидрофосфата калия в 1,1 см 3 воды, затем вводят 480 мг DL-дитиотреитола. Суспензию белого цвета перемешивают 18 ч при температуре кипения с обратным холодильником. Реакционную смесь охлаждают до 20 С, затем добавляют 10 см 3 воды и перемешивают в течение 15 мин. Выпавший осадок центрифугируют, затем промывают большим количеством воды. Получают 231 мг метил-(6-сульфанил-1,3-бензотиазол-2-ил)карбамата в виде порошка кремового цвета, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 239(-)=(М-Н)(-); 241(+)=(М+Н)(+).c) Метил(6-тиоцианат-1,3-бензотиазол-2-ил)карбамат может быть получен следующим образом. К раствору зеленого цвета 1 г 2-амино-1,3-бензотиазол-6-илтиоцианата (выпускаемого в продажу) в 12 см 3 пиридина при 0 С, вводят с помощью шприца 0,467 см 3 метилхлоркарбоната, поддерживая температуру на уровне 0 С. Суспензию перемешивают 2 ч при 20 С, а затем добавляют 6 см 3 смеси 50/50 воды и этилацетата. Полученный белый порошок отфильтровывают на фриттированном стекле, затем промывают последовательно водой и этилацетатом. Получают 816 мг метил(6-тиоцианат-1,3-бензотиазол-2-ил)карбамата в виде белого порошка, имеющего следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 264(-)=(М-Н)(-); 266(+)=(М+Н)(+).d) 3-Хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазин может быть получен следующим образом. В колбу для микроволнового облучения, снабженную магнитной мешалкой, вводят при 20 С 700 мг 6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазин-3-ола и 3,5 см 3 оксихлорида фосфора. Реакционную смесь нагревают в микроволновой печи в течение 1 ч при 150 С, затем добавляют 100 см 3 насыщенного водного раствора гидрокарбоната натрия, затем дополнительно вводят гидрокарбонат натрия для нейтрализации среды. Полученную смесь экстрагируют 3100 см 3 этилацетата. Органические фазы объединяют, затем сушат над сульфатом магния и упаривают досуха с получением 696 мг твердого вещества оранжевого цвета, которое хроматографируют на картридже Analogix, наполнитель 40 г диоксида кремния, размер частиц 50 мкм (элюирование чистым дихлорметаном, затем смесью 80/20 дихлорметан/этилацетат). Получают 597 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазина в виде твердого продукта бежевого цвета, который имеет следующие характеристики: Спектр 1 Н ЯМР (400 МГц,м.д.) (ДМСО-d6): 7,47 (т, J=9,0 Гц, 2 Н); 8,07 (д, J=9,5 Гц, 1 Н); 8,21 (дд,J=5,0 и 9,0 Гц, 2 Н); 8,51 (д, J=9,5 Гц, 1 Н). Масс-спектр: LC-MS-DAD-ELSD: 249 (+)/=(М+Н)(+)/; (1 Cl присутствует).e) 6-(4-Фторфенил)-1,2,4-триазоло[4,3-b]пиридазин-3-ол может быть получен следующим образом. К смеси 4,3 г 3-хлор-6-(4-фторфенил)пиридазина в 70 см 3 бутанола при 20 С добавляют 4,6 г гидрохлорида гидразинкарбоксамида и 5,7 см 3 триэтиламина. Полученную смесь нагревают при 140 С в течение 65 ч, затем охлаждают до 20 С и добавляют 300 см 3 дихлорметана. Реакционную смесь затем промывают 150 см 3 деминерализованной воды. Органические фазы объединяют, затем сушат над сульфатом магния и упаривают досуха с получением 4,93 г твердого вещества оранжевого цвета. Это твердое вещество обрабатывают диэтилоксидом, центрифугируют и получают 2,5 г 6-(4-фторфенил)-1,2,4 триазоло[4,3-b]пиридазин-3-ола в виде твердого продукта желтого цвета, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 231 (+)/=(М+Н)(+) /; (1 Cl присутствует).f) 3-Хлор-6-(4-фторфенил)пиридазин может быть получен следующим образом. К раствору 300 мг 3,6-дихлорпиразина, выпускаемого в продажу, в 12 см 3 диоксана прибавляют 140 мг 4-фторбензолбороновой кислоты и 231 мг гидрокарбоната натрия в 7 см 3 деминерализованной воды. Среду дегазируют путем барботирования аргона в течение 5 мин, затем добавляют 115 мг тетракис(трифенилфосфин)палладия(0). Полученную смесь нагревают при 115 С в течение 1 ч 30 мин, затем охлаждают до 20 С и потом добавляют 20 см 3 деминерализованной воды. Образующийся осадок центрифугируют и промывают деминерализованной водой. После сушки получают 213 мг твердого вещества розового цвета. Экстрагируют водные фазы 40 см 3 дихлорметана, затем сушат над сульфатом магния,упаривают досуха органическую фазу и получают 213 мг бежевого порошка. Две партии твердого вещества объединяют и хроматографируют на картридже Analogix, 12 г диоксида кремния, 50 мкм - (элюент: дихлорметан). Так получают 285 мг целевого продукта, который снова хроматографируют в тех же условиях с получением 175 мг 3-хлор-6-(4-фторфенил)пиридазина в виде твердого белого продукта, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 209 (+)/= (М+Н)(+)/; (1 Cl присутствует). Пример 2. 1,1-Диметилэтил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3 бензотиазол-2-ил)карбамат. а) 1,1-Диметилэтил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3 бензотиазол-2-ил)карбамат может быть получен как в пример 1 а, но исходя из 56 мг 1,1-диметилэтил-(6 сульфанил-1,3-бензотиазол-2-ил)карбамата и 50 мг 3-хлор-6-(4-фторфенил)-1, 2,4-триазоло[4,3b]пиридазина. Хроматографируют на колонке Biotage Quad 12/25 (KP-SIL, 60A; 32-63 мкМ), элюируя смесью дихлорметан/раствор В 95/5 (раствор В = дихлорметан/метанол/гидроксид аммония 38/17/2). Получают 27 мг 1,1-диметилэтил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил 1,3-бензотиазол-2-ил)карбамата в виде желтого порошка, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 495 (+)=(М+Н)(+). Спектр 1 Н ЯМР (400 МГц, ДМСО-d6),м.д.: 1,50 (с, 9 Н); 7,40 (т, J=9,0 Гц, 2 Н); 7,54 (дд, J=2,0 и 8,3 Гц, 1 Н); 7,65 (д, J=8,3 Гц, 1 Н); 8,02 (д, J=9,8 Гц, 1 Н); 8,10 (дд, J=5,6 и 9,0 Гц, 2 Н); 8,19 (д, J=2,0 Гц, 1 Н); 8,51 (д, J=9,8 Гц, 1 Н); 11,82 (уш.с, 1 Н).b) 1,1-Диметилэтил-(6-сульфанил-1,3-бензотиазол-2-ил)карбамат может быть получен, как в примере 1b, но исходя из 615 мг 1,1-диметилэтил-(6-тиоцианатбензотиазол-2-ил)карбамата, 10 мг дигидрофосфата калия и 926 мг DL-дитиотреитола. Так получают 659 мг 1,1-диметилэтил-(6-сульфанил-1,3 бензотиазол-2-ил)карбамата в виде белого порошка, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 281(-)=(М-Н)(-); 227(+)=(М+Н)(-)-трет-бутил.c) 1,1-Диметилэтил-(6-тиоцианатбензотиазол-2-ил)карбамат может быть получен следующим образом. К смеси 1 г 6-тиоцианатбензотиазол-2-иламина, выпускаемого в продажу, и 2 см 3 триэтиламина в 20 см 3 дихлорметана при 0 С в атмосфере аргона прибавляют 2,1 г ди-трет-бутилдикарбоната и перемешивают полученную смесь 1 ч при 0 С. Добавляют 147 мг N,N-диметилпиридин-4-амина и полученную смесь постепенно доводят до 20 С в течение 2 ч при перемешивании. Зеленый прозрачный раствор выливают в воду и экстрагируют этилацетатом. Получают 1,765 г порошкообразного вещества желтого цвета, которое очищают путем хроматографии на колонке Biotage Quad 12/25 (KP-SIL, 60A; 32-63 мкм),элюируя градиентом циклогексан/этилацетат 95/5, 90/10, 85/15, 80/20, 70/30, 60/40. Получают 1,058 г 1,1 диметилэтил(6-тиоцианатбензотиазол-2-ил)карбамата в виде порошка желтого цвета, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 308(+)=(М+Н)(+). Пример 3. 6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2-амин. 6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2-амин может быть получен следующим образом. К смеси 127 мг 1,1-диметилэтил-6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3 ил]сульфанил-1,3-бензотиазол-2-ил)карбамата в 5 см 3 дихлорметана, которую перемешивают при 20 С,прибавляют 40,1 см 3 трифторуксусной кислоты (с 10% анизола) в течение 7 ч до исчезновения исходного продукта. Упаривают реакционную смесь при пониженном давлении с получением 186,5 мг желтого порошкообразного вещества, которое очищают путем хроматографии на колонке Biotage Quad 12/25(KP-SIL, 60A; 32-63 мкм), элюируя градиентом дихлорметана, затем дихлорметан/метанол: 99,5/0,5, 99/1,98,5/1,5, 98/2, 97,5/2,5, 97/3. Получают 36,6 мг 6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3 ил]сульфанил-1,3-бензотиазол-2-амина в виде беловатого порошка, который имеет следующие характеристики: Т. плавления 260 С (по Кофлеру). Спектр ЯМР 66292V 1H ЯМР (400 МГц, ДМСО-d6)м.д. 7,31 (д, J=8,3 Гц, 1 Н); 7,35-7,48 (м, 3 Н); 7,66 (с, 2 Н); 7,98 (д, J=2,0 Гц, 1 Н); 8,01 (д, J=9,8 Гц, 1 Н); 8,12 (дд, J=8,8 и 5,4 Гц, 2 Н); 8,49 (д, J=9,8 Гц,1 Н). Масс-спектр: LC-MS-DAD-ELSD: 393(-)=(М-Н)(-); 395(+)=(М+Н)(+). Пример 4. Метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2 ил)карбамат. а) Метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол 2-ил)карбамат может быть получен следующим образом. К смеси 110 мг 4-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанилбензол-1,2 диамина в 4 см 3 метанола добавляют 0,02 см 3 ледяной уксусной кислоты и 65 мг диметил-[(Z)(метилтио)метилиден]бискарбамата. Нагревают полученную смесь при температуре около 80 С в течение 2 ч 30 мин, затем оставляют при перемешивании в течение двух суток при 20 С. Затем реакционную смесь доводят до щелочного значения рН с помощью 28%-го водного раствора гидроксида аммония. Выпавший осадок отфильтровывают, затем промывают водой и этилацетатом и сушат под вакуумом. Получают 53 мг метил-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Нбензимидазол-2-ил)карбамата в виде твердого вещества бежевого цвета, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 434(-)=(М-Н)(-); 436(+)=(М+Н)(+). Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 3,74 (с, 3 Н); 7,33 (дд, J=8,5 и 2,0 Гц, 1 Н); 7,35-7,48 (м,маскирован, 1 Н); 7,42 (т, J=9,0 Гц, 2 Н); 7,67 (шир.с, 1 Н); 8,01 (д, J=10,0 Гц, 1 Н); 8,11 (дд, J=9,0 и 5,5 Гц,2 Н); 8,49 (д, J=10,0 Гц, 1 Н); 10,92-12,44 (уш.м, 2 Н).b) 4-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанилбензол-1,2-диамин может быть получен следующим образом. К смеси 146 мг 5-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-2 нитроанилина в 7 см 3 метанола прибавляют 0,6 см 3 уксусной кислоты и 145 мг железа(0). Реакционную смесь перемешивают при температуре кипения с обратным холодильником в течение 5 ч 15 мин, затем в течение ночи при 20 С, а затем добавляют 10 см 3 5 н водного раствора гидроксида натрия и 10 см 3 деминерализованной воды. Полученную смесь экстрагируют 230 см 3 этилацетата. Объединенные органические фазы промывают 20 см 3 воды, затем сушат над сульфатом магния и упаривают досуха. Полученное твердое вещество бежевого цвета обрабатывают диэтилоксидом, центрифугируют, затем сушат под вакуумом. Получают 71 мг 4-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанилбензол 1,2-диамина, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 353(+)=(М+Н)(+).c) 5-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-2-нитроанилин может быть получен следующим образом. К смеси 1,76 г 3-амино-4-нитрофенилтиоцианата, выпускаемого в продажу, в 15 см 3 N,Nдиметилформамида прибавляют 342 мг боргидрида натрия. Реакционную среду перемешивают 2 ч при комнатной температуре, затем прибавляют 746 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3b]пиридазина и 1,25 см 3 триэтиламина. Полученную смесь затем нагревают при 95 С, затем перемеши- 26023465 вают 1 ч при 20 С. После добавления деминерализованной воды полученную смесь экстрагируют 3100 см 3 этилацетата (добавляя небольшое количество метанола для улучшения растворимости). Органические фазы объединяют, затем сушат над сульфатом магния и упаривают досуха для получения твердого вещества каштанового цвета, который хроматографируют на картридже Мерка, 25 г диоксида кремния,15-40 мкм (элюирование этилацетатом). Получают 360 мг 5-[6-(4-фторфенил)[1,2,4]триазоло[4,3b]пиридазин-3-ил]сульфанил-2-нитроанилина в виде твердого вещества зеленого цвета, которое имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 383(+)=(М+Н)(+). Пример 5. Метил-(6-[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Нбензимидазол-2-ил)карбамат. а) Метил-(6-[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Нбензимидазол-2-ил)карбамат может быть получен следующим образом. К раствору 223 мг 4-[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3 ил]сульфанилбензол-1,2-диамина в 9 см 3 метанола и 0,038 см 3 ледяной уксусной кислоты прибавляют 130 мг диметил-[(Z)-(метилтио)метилиден]бискарбамата, выпускаемого в продажу. Нагревают полученную смесь при 80 С в течение 5,5 ч. Затем снова прибавляют 0,038 см 3 ледяной уксусной кислоты и 130 мг диметил-[(Z)-(метилтио)метилиден]бискарбамата и нагревают при 80 С в течение 8 ч. После выдерживания в течение ночи при 20 С в полученную смесь вводят 28%-ый водный раствор гидроксида аммония для доведения рН до щелочного значения. Выпавший осадок отфильтровывают, затем последовательно промывают водой и этилацетатом. Полученный твердый продукт сушат в вакууме, затем хроматографируют на картридже Мерка (25 г диоксида кремния, 15-40 мкм), элюируя этилацетатом. Получают 105 мг метил-(6-[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Нбензимидазол-2-ил)карбамата в виде твердого продукта каштанового цвета, которое имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 438(+)=(М+Н)(+). Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 3,16 (с, 4 Н); 3,76 (с, 3 Н); 7,29 (дд, J=8,3 и 2,0 Гц, ОН); 7,35 (т, J=8,8 Гц, 2 Н); 7,41 (д, J=8,3 Гц, 1 Н); 7,64 (с, 1 Н); 7,95 (дд, J=8,8 и 5,4 Гц, 2 Н); 11,33 (уш.с, 1 Н); 11,94 (уш.с, 1 Н).b) 4-[6-(4-Фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанилбензол-1,2 диамин может быть получен следующим образом. К раствору 240 мг 5-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-2 нитроанилина в 13 см 3 уксусной кислоты добавляют 422 мг цинка(0) и перемешивают полученную смесь 1 ч при 20 С. Затем приливают в реакционную смесь 30 см 3 воды и создают щелочную среду добавлением 16 см 3 28%-го водного раствора гидроксида аммония. Экстрагируют полученную смесь этилацетатом. Образовавшийся органический слой последовательно промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, затем сушат над сульфатом магния, фильтруют и упаривают досуха. Остаток затирают эфиром, фильтруют, затем сушат в вакууме при 20 С. Получают 479 мг 4-[6-(4-фторфенил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-3 ил]сульфанилбензол-1,2-диамина, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 355(+)=(М+Н)(+). Пример 6. 1-(6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-ил)-3(2-морфолин-4-илэтил)карбамид. 1-(6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-ил)-3(2-морфолин-4-илэтил)карбамид может быть получен следующим образом. В колбу для микроволнового облучения помещают 200 мг метил-(6-[6-(4 фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-ил)карбамата, 60 мг N(2-аминоэтил)морфолина и 2 см 3 1-метил-2-пирролидинона. Полученную смесь нагревают при 125 С в течение 25 мин. Упаривают растворитель при пониженном давлении (7 мбар/80 С) для получения 292,6 мг порошка каштанового цвета. Этот твердый продукт смешивают с другой порцией в количестве 50,4 мг, полученных аналогичным способом в параллельном эксперименте. Общую массу сырого продукта 343 мг очищают хроматографией на колонке Biotage Quad 12/25(KP-SIL, 60A; 32-63 мкм), элюируя градиентом дихлорметана, затем дихлорметан/элюент В: 99/1, 98/2, 95/5, 90/10, 85/15, 82,5/17,5 (элюент В=дихлорметан/метанол/гидроксид аммония 38/17/2). Получают 190 мг 1-(6-[6-(4 фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-ил)-3-(2-морфолин-4 илэтил)карбамида в виде порошка бежевого цвета, который имеет следующие характеристики: Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 2,35-2,45 (м, 6 Н); 3,21-3,29 (м, 2 Н); 3,50-3,58 (м, 4 Н); 7,29 (д, J=6,8 Гц, 2 Н); 7,35 (д, J=6,8 Гц, 1 Н); 7,42 (т, J=8,8 Гц, 2 Н); 7,61 (уш.с, 1 Н); 8,00 (д, J=9,8 Гц, 1 Н); 8,12 (дд, J=8,8 и 5,4 Гц, 2 Н); 8,48 (д, J=9,8 Гц, 1 Н); 10,05 (уш.с, 1 Н); 11,70 (уш.с, 1 Н); Масс-спектр: LC-MS-DAD-ELSD: 532(-)=(М-Н)(-); 534(+)=(М+Н)(+). Пример 7. 6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-амин. 6-[6-(4-Фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-амин может быть получен следующим образом. Смесь 4-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанилбензол-1,2-диамина и 42 мг цианидбромида в 10 см 3 этанола кипятят с обратным олодильником в течение 3 ч. Полученную реакционную смесь хвыливают в 2,5 н водный раствор гидроксида натрия и полученную смесь экстрагируют смесью этилацетата и метанола 90/10. Органические фазы объединяют, затем сушат над сульфатом магния и выпаривают. Получают желтый порошок, который хроматографируют на колонке Biotage Quad 12/25 (KP-SIL, 60A; 32-63 мкм), элюируя градиентом дихлорметана, затем дихлорметан/элюент В: 95/5,92,5/7,5, 90/10, 87,5/12,5, 85/15 (элюент В=дихлорметан/метанол/гидроксид аммония 38/17/2). Получают 43,2 мг 6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1 Н-бензимидазол-2-амина в виде беловатого порошка, который имеет следующие характеристики: Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 6,33 (уш.с, 2 Н); 7,07-7,12 (м, 1 Н); 7,19 (уш.с, 2 Н); 7,38(уш.с, 1 Н); 7,43 (т, J=8,8 Гц, 2 Н); 7,99 (д, J=9,8 Гц, 1 Н); 8,13 (дд, J=8,8 и 5,4 Гц, 2 Н); 8,46 (д, J=9,8 Гц, 1 Н); 10,85 (уш.с, 1 Н); Масс-спектр: LC-MS-DAD-ELSD: 376(-)=(М-Н)(-); 378(+)=(М+Н)(+). Пример 8. 6-[(4-3-[(2-Амино-1,3-бензотиазол-6-ил)]сульфанил]-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин 6-илфенил)сульфанил]-1,3-бензотиазол-2-амин. 6-[(4-3-[(2-Амино-1,3-бензотиазол-6-ил)]сульфанил]-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин 6-илфенил)сульфанил]-1,3-бензотиазол-2-амин может быть получен следующим образом. К раствору 500 мг 2-амино-1,3-бензотиазол-6-илтиоцианата в 6 см 3 N,N-диметилформамида прибавляют 92 мг боргидрида натрия. Полученную смесь перемешивают при 20 С в течение 2 ч. К суспензии ржавого цвета добавляют 200 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазина и 0,34 см 3 триэтиламина. Образующуюся смесь перемешивают при 90-110 С в течение 1 ч, затем охлаждают до 20 С. Реакционную смесь обрабатывают смесью воды и этилацетата. После разделения органическую фазу сушат над сульфатом магния, затем упаривают досуха в вакууме. Остаток хроматографируют на колонке Biotage Si 12M+, элюируя дихлорметаном, затем смесью дихлорметан/элюент В: 95/5 (элюент В=дихлорметан/метанол/гидроксид аммония 38/17/2). Получают 41 мг 6-[(4-3-[(2-амино-1,3 бензотиазол-6-ил)]сульфанил]-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-илфенил)сульфанил]-1,3 бензотиазол-2-амина в виде желтого порошка, который имеет следующие характеристики: Т. плавления: 182 С (по Кофлеру). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 3,12 (дд, J=6,6 и 4,6 Гц, 4 Н); 7,19 (д, J=8,5 Гц, 2 Н); 7,30 (д,J=8,3 Гц, 1 Н); 7,34-7,46 (м, 3 Н); 7,62 (с, 2 Н); 7,69 (с, 2 Н); 7,80 (д, J=8,5 Гц, 2 Н); 7,90 (д, J=2,0 Гц, 1 Н); 7,92a) 1-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин-3-ил]сульфанил-1,3-бензотиазол-2-ил)-3(2-морфолин-4-илэтил)карбамид получают в соответствии со способом, описанным в примере 1 а, но исходя из 240 мг 3-хлор-6-(4-фторфенил)-1,2,4-триазоло[4,3-b]пиридазина, 338 мг 1-(2-морфолин-4 илэтил)-3-(6-сульфанил-1,3-бензотиазол-2-ил)карбамида, 0,14 см 3 триэтиамина и 38 мг боргидрида натрия. Полученный сырой продукт хроматографируют на картридже Мерка (30 г диоксида кремния, 15-40 мкм), элюируя дихлорметаном. Получают 117 мг 1-(6-[6-(4-фторфенил)[1,2,4]триазоло[4,3-b]пиридазин 3-ил]сульфанил-1,3-бензотиазол-2-ил)-3-(2-морфолин-4-илэтил)карбамида в виде твердого бежевого вещества, который имеет следующие характеристики: Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 2,34-2,46 (м, 6 Н); 3,23-3,29 (м, 2 Н); 3,59 (т, J=3,9 Гц,4 Н); 6,77 (уш.с, 1 Н); 7,41 (т, J=8,8 Гц, 2 Н); 7,52 (дд, J=8,3 и 2,0 Гц, 1 Н); 7,59 (д, J=8,3 Гц, 1 Н); 8,03 (д,J=9,8 Гц, 1 Н); 8,11 (дд, J=8,8 и 5,4 Гц, 2 Н); 8,17 (д, J=2,0 Гц, 1 Н); 8,51 (д, J=9,8 Гц, 1 Н); 10,90 (уш.с, 1 Н); Масс-спектр: LC-MS-DAD-ELSD: 549(-)=(М-Н)(-); 551(+)=(М+Н)(+).b) 1-(2-Морфолин-4-илэтил)-3-(6-сульфанил-1,3-бензотиазол-2-ил) карбамид получают согласно способу, описанному в примере 1b, но исходя из 900 мг 2-[(2-морфолин-4-илэтил)карбамоил]амино 1,3-бензотиазол-6-илтиоцианата, 11 мг дигидрофосфата калия и 1,1 г DL-дитиотреитола. Получают 633 мг 1-(2-морфолин-4-илэтил)-3-(6-сульфанил-1,3-бензотиазол-2-ил)карбамида в виде твердого белого вещества, который имеет следующие характеристики:c) 2-[(2-Морфолин-4-илэтил)карбамоил]амино-1,3-бензотиазол-6-илтиоцианат получают следующим образом. К раствору 1 г фенил-(6-тиоцианат-1,3-бензотиазол-2-ил)карбамата в 30 см 3 тетрагидрофурана добавляют 0,44 см 3 2-морфолин-4-илэтанамина при 20 С. Спустя 24 ч реакционную смесь упаривают досуха и полученный остаток хроматографируют на картридже Мерка 70 г (твердый слой; элюирование градиентом дихлорметана, затем дихлорметан/метанол 90/10). Получают 902 мг 2-[(2-морфолин-4 илэтил)карбамоил]амино-1,3-бензотиазол-6-илтиоцианата в виде бесцветного пенообразного вещества,который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 364(+)=(М+Н)(+).d) Фенил-(6-тиоцианат-1,3-бензотиазол-2-ил)карбамат получают следующим образом. К раствору 2,5 г 2-амино-1,3-бензотиазол-6-илтиоцианата, выпускаемого в продажу, в 94 см 3 тетрагидрофурана добавляют при 20 С 7,5 г фенилхлоркарбоната, затем 4,05 г гидрокарбоната натрия и 9,4 см 3 воды. Полученную смесь перемешивают при 20 С в течение 20 ч, затем экстрагируют 2150 см 3 этилацетата. Органические фазы объединяют и промывают 350 см 3 водного насыщенного раствора гидрокарбоната натрия. Образующуюся органическую фазу сушат над сульфатом магния, затем упаривают досуха при пониженном давлении. Остаток обрабатывают 50 см 3 воды, затем центрифугируют и сушат в вакууме при 20 С. Получают 3,45 г фенил-(6-тиоцианат-1,3-бензотиазол-2-ил)карбамата в виде твердого вещества бледно-желтого цвета, который имеет следующие характеристики: Масс-спектр: LC-MS-DAD-ELSD: 326(-)=(М-Н)(-); 328(+)=(М+Н)(+). Пример 10. 1-(2-Морфолин-4-илэтил)-3-[6-([1,2,4]триазоло[4,3-b]пиридазин-3-илсульфанил)-1,3-бензотиазол-2 ил]карбамид. а) 1-(2-Морфолин-4-илэтил)-3-[6-([1,2,4]триазоло[4,3-b]пиридазин-3-илсульфанил)-1,3-бензотиазол 2-ил]карбамид может быть получен следующим образом. К раствору 462 мг 1-(2-морфолин-4-илэтил)-3-(6-сульфанил-1,3-бензотиазол-2-ил)карбамида в 5,5 см 3 тетрагидрофурана добавляют 277 мг н-трибутилфосфина. Эту смесь перемешивают 1 ч при 20 С при барботировании аргоном, а затем добавляют 176 мг 3-хлор-1,2,4-триазоло[4,3-b]пиридазина, 166 мг третбутилата калия, 12 мг тетрафенилдифосфоксана и 11 см 3 толуола и перемешивают 30 мин при 20 С при барботировании аргоном. Затем в полученную смесь вводят 10 мг трис-(1,5-дифенилпента-1,4-диен-3 он)дипалладия(0) и кипятят с обратным холодильником в течение 17 ч. Растворитель упаривают при пониженном давлении, затем обрабатывают остаток водой и 0,1 н раствором соляной кислотой. Полученную смесь экстрагируют смесью этилацетат/метанол 90/10. Получают 632 мг желтого масла, которое хроматографируют на колонке Biotage Quad 12/25(KP-SIL, 60 А; 32-63 мкм), элюируя градиентом дихлорметана, затем дихлорметан/элюент В: 99/1, 98/2, 97/3, 96/4, 95/6, 92/8, 90/10, 80/20. Получают 75 мг 1-(2-морфолин-4-илэтил)-3-[6-([1,2,4]триазоло[4,3-b]пиридазин-3-илсульфанил)-1,3-бензотиазол-2 ил]карбамида в виде бежевого порошка, который имеет следующие характеристики: Т. плавления: 252 С (по Кофлеру); Спектр 1 Н ЯМР (400 МГц, ДМСО-d6)м.д.: 2,36-2,45 (м, 6 Н); 3,24-3,36 (м, 2 Н), 3,55-3,63 (м, 1 Н); 6,78 (уш.с, ОН); 7,38-7,48 (м, ОН); 7,57 (д, J=8,5 Гц, ОН); 8,04 (д, J=1,5 Гц, ОН); 8,46 (дд, J=9,5 и 1,5 Гц,ОН); 8,70 (дд, J=4,5 и 1,5 Гц, ОН); 10,85-10,95 (м, ОН); Масс-спектр: UPLC-MS-DAD-ELSD: 457(+)=(М+Н)(+).b) 3-Хлор-1,2,4-триазоло[4,3-b]пиридазин может быть получен следующим образом. Смесь 436 мг [1,2,4]триазоло[4,3-b]пиридазин-3-ола в 6 см 3 трихлорида фосфорной кислоты перемешивают при температуре кипения с обратным холодильником в течение 3 ч 30 мин. Реакционную смесь выливают в 4 н водный раствор гидроксида натрия и полученную смесь экстрагируют смесью этилацетат/метанол 90/10. Водную кислую фазу (рН 1) доводят до pH 11 добавлением концентрированной щелочи натрия, затем снова экстрагируют смесью этилацетат/метанол 90/10. Органические фазы объединяют и сушат над сульфатом магния, фильтруют, затем упаривают в вакууме. Получают 808 мг беловатой смолы. Обрабатывают 640 мг этой смолы этилацетатом и промывают полученный раствор водой. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают в вакууме с получением 281 мг 3-хлор-1,2,4-триазоло[4,3-b]пиридазина в виде белого порошка, который имеет следующие характеристики: Масс-спектр: UPLC-MS-DAD-ELSD: 155 (+)/= (М+Н)(+)/ (1 Cl присутствует) с) [1,2,4]триазоло[4,3-b]пиридазин-3-ол может быть получен следующим образом. Смесь 1,71 г 6-хлор[1,2,4]триазоло[4,3-b]пиридазин-3-ола, выпускаемого в продажу, 1,90 г формиата аммония и 2,13 г 5%-го Pd/C в 50 см 3 метанола перемешивают при кипении с обратным холодильником в течение 3 ч. Реакционную смесь фильтруют для удаления катализатора и полученный фильтрат упаривают при пониженном давлении с получением 2,74 г зеленоватого порошка, который хроматогра- 29
МПК / Метки
МПК: C07D 487/04, A61P 35/00, A61K 31/5025
Метки: применение, получения, качестве, фармацевтические, композиции, лекарственных, новое, ингибиторов, 6-триазолпиридинсульфанил-бензотиазола, производные, бензимидазола, способ, новые, средств, мет
Код ссылки
<a href="https://eas.patents.su/30-23465-novye-proizvodnye-6-triazolpiridinsulfanil-benzotiazola-ili-benzimidazola-sposob-ih-polucheniya-primenenie-ih-v-kachestve-lekarstvennyh-sredstv-farmacevticheskie-kompozicii-i-novoe.html" rel="bookmark" title="База патентов Евразийского Союза">Новые производные 6-триазолпиридинсульфанил-бензотиазола или -бензимидазола, способ их получения, применение их в качестве лекарственных средств, фармацевтические композиции и новое применение в качестве ингибиторов мет</a>
Предыдущий патент: Тяжелая вращающаяся технологическая машина
Следующий патент: Способ определения стволовых клеток рака молочной железы и применение антагонистов cxcr1 для лечения рака
Случайный патент: Остекление, покрытое тонкими слоями