Арилсульфонамиды для лечения заболеваний цнс
Номер патента: 22776
Опубликовано: 29.02.2016
Авторы: Ковальский Петр, Весоловская Анна, Буцкий Адам, Колачковский Марцин, Митка Катажина, Павловский Мацей, Яськовская Йолянта, Марцинковская Моника
Формула / Реферат
1. Соединение общей формулы (I)
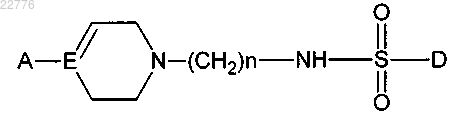
и его фармацевтически приемлемые соли,
в которой E обозначает С;
n означает целое число от 2 до 6 включительно;
A обозначает 9- или 10-членную бициклическую группу, состоящую из бензольного кольца, конденсированного с 5- или 6-членным гетероциклическим кольцом, связанную с Е через один из ее атомов углерода и имеющую следующую формулу (А):
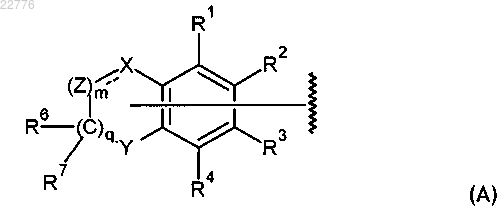
в которой X обозначает CR5, C(R5)2, NH или О;
Z обозначает CR5, C(R5)2 или N;
R5 обозначает атом водорода, атом галогена или С1-С4-алкил;
Y обозначает NH, О или S;
каждый из R1, R2, R3 и R4 независимо обозначает атом водорода или атом галогена;
каждый из R6 и R7 независимо обозначает атом водорода, атом галогена или С1-С4-алкил;
или R6 и R7 вместе образуют =O;
обозначает простую связь или двойную связь;
m=0 или 1;
q=0 или 1;
причем по меньшей мере один из q и m=1;
D выбран из
незамещенного фенила или фенила, замещенного одним или более заместителями, независимо выбранными из группы, состоящей из разветвленного С1-С4-алкила, прямого C1-C4-алкила в орто- или мета-положении относительно сульфонамидной группы, C1-C3-алкилокси, галоген-С1-С3-алкила, галоген-С1-С3-алкилокси, атома галогена, -CN, -ОН и фенила;
незамещенного нафтила или нафтила, замещенного одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила, C1-C3-алкилокси, галоген-C1-C3-алкила, атома галогена, -CN, -ОН и фенила;
5-членной ароматической гетероциклической группы, имеющей от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S, которая является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила, C1-C3-алкилокси, галоген-C1-C3-алкила, атома галогена, -CN, -ОН и фенила;
бициклической группы, состоящей из кольца, выбранного из бензола и пиридина, конденсированного с 5-членным ароматическим или неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О, S, причем указанная бициклическая группа является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила, C1-С3-алкилокси, галоген-С1-С3-алкила, атома галогена, =O, -CN, -ОН и фенила;
бициклической группы, состоящей из кольца, выбранного из бензола и пиридина, конденсированного с 6-членным неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S, причем указанная бициклическая группа является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила, C1-С3-алкилокси, галоген-C1-C3-алкила, атома галогена, =O, -CN, -ОН и фенила.
2. Соединение по п.1, в котором А представлен общей формулой (А1)
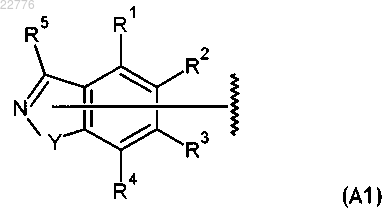
в которой Y, R1, R2, R3, R4 и R5 имеют значения, определенные в п.1.
3. Соединение по п.1, в котором А представлен общей формулой (А2)
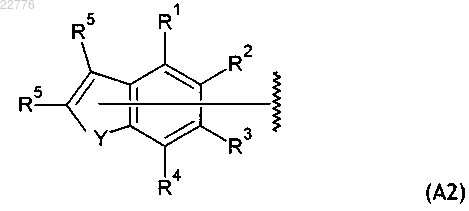
в которой Y, R1, R2, R3, R4 и R5 имеют значения, определенные в п.1.
4. Соединение по п.1, в котором А представлен общей формулой (A3)
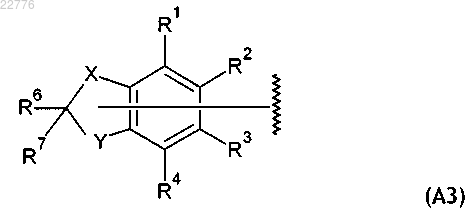
в которой X, Y, R1, R2, R3, R4, R6 и R7 имеют значения, определенные в п.1.
5. Соединение по п.1, в котором А представлен общей формулой (А4)
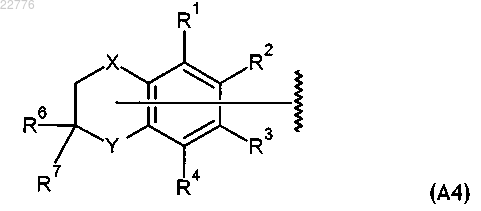
в которой X, Y, R1, R2, R3, R4, R6 и R7 имеют значения, определенные в п.1.
6. Соединение по любому из пп.1-5, в котором D обозначает незамещенный фенил или фенил, замещенный одним или более заместителями, независимо выбранными из группы, состоящей из разветвленного С1-С4-алкила; прямого С1-С4-алкила в орто- или мета-положении относительно сульфонамидной группы; C1-C3-алкилокси; галоген-С1-С3-алкила; галоген-С1-С3-алкилокси; атома галогена; -CN; -ОН и фенила.
7. Соединение по любому из пп.1-5, в котором D обозначает незамещенный нафтил или нафтил, замещенный одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила; C1-C3-алкилокси; галоген-C1-C3-алкила; атома галогена; -CN; -ОН и фенила.
8. Соединение по любому из пп.1-5, в котором D обозначает 5-членную ароматическую гетероциклическую группу, имеющую от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S, в которых D незамещен или замещен одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила; C1-C3-алкилокси; галоген-C1-C3-алкила; атома галогена; -CN; -ОН и фенила.
9. Соединение по п.8, в котором D обозначает тиенил.
10. Соединение по любому из пп.1-5, в котором D обозначает бензольное кольцо, конденсированное с 5-членным ароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О, S, в которых D незамещен или замещен одним или более заместителями, независимо выбранными из группы, состоящей из C1-C4-алкила; C1-С3-алкилокси; галоген-C1-C3-алкила; атома галогена, -CN; -ОН и фенила.
11. Соединение по п.10, в котором D выбран из группы, состоящей из 1-бензотиофен-3-ила, 1-бензотиофен-2-ила, 1-бензофуран-2-ила, 1-бензофуран-3-ила, 1H-бензимидазол-2-ила, 1H-индол-2-ила, 1H-индол-5-ила, 1H-индол-6-ила, 1H-индазол-7-ила, 1H-индазол-6-ила, 1,2-бензоксазол-5-ила, 1,3-бензоксазол-4-ила, 1,3-бензотиазол-4-ила и 1,3-бензотиазол-5-ила.
12. Соединение по любому из пп.1-5, в котором D обозначает бициклическую группу, состоящую из бензольного кольца, конденсированного с 5-членным неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О, S, и в которых D незамещен или замещен одним или более заместителями, независимо выбранными из группы, состоящей из С1-С4-алкила; C1-C3-алкилокси; галоген-C1-C3-алкила; атома галогена; =O; -CN; -ОН и фенила.
13. Соединение по п.12, в котором D выбран из группы, состоящей из 2,3-дигидро-1-бензофуран-5-ила, 2-оксо-2,3-дигидро-1,3-бензоксазол-6-ила, 2-оксо-1,3-дигидро-2Н-индол-5-ила и 1,3-бензодиоксол-5-ила.
14. Соединение по любому из пп.1-5, в котором D обозначает бициклическую группу, состоящую из кольца пиридина, конденсированного с 5-членным ароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, O, S, в которых D незамещен или замещен одним или более заместителями, независимо выбранными из группы, состоящей из C1-C4-алкила; C1-C3-алкилокси; галоген-С1-С3-алкила; атома галогена; -CN; -ОН и фенила.
15. Соединение по п.14, в котором D выбран из группы, состоящей из имидазо[1,2-а]пиридин-3-ила и 1H-пирроло[2,3-b]пиридин-3-ила.
16. Соединение по любому из пп.1-15, в котором n=2.
17. Соединение по любому из пп.1-15, в котором n=3.
18. Соединение по любому из пп.1-15, в котором n=4.
19. Соединение по любому из пп.1-18, в котором А связан с Е через атом углерода бензольного кольца.
20. Соединение по любому из пп.1-18, в котором А связан с Е через атом углерода гетероциклического кольца.
21. Соединение по п.1, выбранное из группы, состоящей из следующих соединений:
N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}нафталин-1-сульфонамид,
N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}нафталин-2-сульфонамид,
4-фтор-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
3-фтор-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
4-хлор-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
3-хлор-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
3-метил-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
3-гидрокси-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
4-метокси-N-{4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}нафталин-1-сульфонамид,
N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}нафталин-2-сульфонамид,
4-фтор-N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}бензолсульфонамид,
3-фтор-N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}бензолсульфонамид,
4-хлор-N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}бензолсульфонамид,
3-хлор-N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}бензолсульфонамид,
3-гидрокси-N-{3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]пропил}бензолсульфонамид,
N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}нафталин-1-сульфонамид,
N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}нафталин-2-сульфонамид,
N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}-4-фторбензолсульфонамид,
3-фтор-N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}бензолсульфонамид,
4-хлор-N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}бензолсульфонамид,
3-хлор-N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}бензолсульфонамид,
3-метил-N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}бензолсульфонамид,
3-гидрокси-N-{2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]этил}бензолсульфонамид,
4-хлор-N-{4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2Н)-ил]бутил}бензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-хлорбензолсульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-3-хлорбензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-фторбензолсульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-3-фторбензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-4-трет-бутилбензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]нафталин-1-сульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]нафталин-2-сульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-4-фторбензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-гидроксибензолсульфонамид,
N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-метилбензолсульфонамид,
N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]нафталин-2-сульфонамид,
3-фтор-N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]бензолсульфонамид,
N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-сульфонамид оксибензола,
N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]бутил]-3-метилбензолсульфонамид,
3-фтор-N-[3-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]бензолсульфонамид,
N-[3-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-3-сульфонамид оксибензола,
N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]нафталин-2-сульфонамид,
3-фтор-N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]бензолсульфонамид,
N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]-3-метилбензолсульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]нафталин-1-сульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]нафталин-2-сульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-4-фторбензолсульфонамид,
4-хлор-N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]бензолсульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-3-гидроксибензолсульфонамид,
N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропил]-3-метилбензолсульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]нафталин-1-сульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]нафталин-2-сульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]-4-фторбензолсульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]-3-фторбензолсульфонамид,
4-хлор-N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]бензолсульфонамид,
3-хлор-N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]бензолсульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]-3-гидроксибензолсульфонамид,
N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2Н-пиридин-1-ил]этил]-3-метилбензолсульфонамид,
и его фармацевтически приемлемые соли.
22. Применение соединения формулы (I), определенного в любом из пп.1-21, в качестве лекарственного средства для лечения и/или профилактики нарушений центральной нервной системы, связанных с допаминергической, и/или серотонинергической, и/или норадренергической трансмиссией.
23. Фармацевтическая композиция, включающая соединение формулы (I), определенное в любом из пп.1-21, в качестве активного ингредиента в комбинации с фармацевтически приемлемым(и) носителем(ями) и/или эксципиентом(ами) для лечения и/или профилактики нарушений центральной нервной системы, связанных с допаминергической, и/или серотонинергической, и/или норадренергической трансмиссией.
24. Применение соединений формулы (I), как определено в любом из пп.1-21, для лечения и/или профилактики нарушений центральной нервной системы, связанных с допаминергической, и/или серотонинергической, и/или норадренергической трансмиссией.
25. Применение по п.24, в котором нарушение центральной нервной системы выбрано из шизофрении; шизоаффективных расстройств; шизофрениформных расстройств; бредовых синдромов; аффективного расстройства; биполярного расстройства; мании; депрессии; тревожных нарушений различной этиологии; стрессовых реакций напряжения; расстройств сознания; комы; делирия; агрессии; психомоторного возбуждения; нарушений сна различной этиологии; синдромов отмены различной этиологии; зависимости; болевых синдромов различной этиологии; интоксикации психотропными веществами; нарушений мозгового кровообращения различной этиологии; психосоматических нарушений различной этиологии; конверсионных нарушений; диссоциирующих нарушений; нарушений мочеиспускания; аутизма, ноктурии, заикания, тиков; когнитивных нарушений различных типов, включая болезнь Альцгеймера.
Текст
АРИЛСУЛЬФОНАМИДЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦНС Производные арилсульфонамида формулы (I) и их фармацевтически приемлемые соли. Эти соединения могут быть использованы для лечения и/или профилактики нарушений центральной нервной системы. Область изобретения Настоящее изобретение относится к новым арилсульфонамидам, имеющим сродство к допаминергическим, серотонинергическим, адренергическим рецепторам, сигма и рецепторам транспортера серотонина, к содержащим их фармацевтическим композициям и к их применению. Эти соединения могут быть использованы для лечения заболеваний центральной нервной системы, таких как шизофрения, биполярное аффективное расстройство, депрессия, тревожные расстройства, нарушения сна или болезнь Альцгеймера. Уровень техники Нарушения ЦНС считаются глобальной медицинской проблемой. Число людей, страдающих этими заболеваниями, постоянно растет, особенно в высокоразвитых и интенсивно развивающихся странах. Приблизительно 20% популяции в высокоразвитых обществах страдают нарушениями ЦНС. Кроме того, стоимость лечения таких нарушений представляет почти 35% всех расходов, затраченных на лечение всех заболеваний в семи странах, которые рассматриваются как самые крупные фармацевтические рынки. Среди всех психиатрических заболеваний наиболее важными являются шизофрения, биполярное расстройство, депрессия, тревожность, нарушения сна и зависимость. Важнейшими неврологическими нарушениями являются болезнь Альцгеймера, болезнь Паркинсона, эпилепсия и различные болевые нарушения. Нейролептические лекарственные средства, которые являются основными средствами лечения шизофрении, делятся на два главных класса на основе их склонности вызывать неврологические побочные эффекты после долговременного лечения. Типичные нейролептические препараты, такие как хлорпромазин и галоперидол, вызывают после повторных введений различные экстрапирамидальные побочные эффекты (EPS), включая паркинсоноподобные симптомы и позднюю дискинезию. Повторное лечение так называемыми атипичными нейролептическими лекарственными средствами, таким как клозапин,рисперидон, оланзапин, кветиапин, зипрасидон и арипипразол, связано с более низкой частотой неврологических побочных эффектов. Типичные нейролептики уменьшают позитивные симптомы, но не уменьшают негативные симптомы и когнитивные дисфункции. У человека повышаются плазменные уровни пролактина и наблюдается увеличение массы тела, потенциально приводящее к развитию метаболического синдрома. Атипичные нейролептические лекарственные средства эффективно уменьшают позитивные симптомы и также до некоторой степени негативные симптомы и когнитивные нарушения, приводя к менее серьезным EPS. Атипичные нейролептические лекарственные средства отличаются по их склонности повышать плазменные уровни пролактина у человека. Типичные нейролептические лекарственные средства блокируют допаминовые рецепторы D2 в мезолимбической и нигростриатальной системах. Этот механизм ответственен за нейролептический эффект (сокращение положительных симптомов), а также индукцию EPS. Клиническое подтверждение допаминовой гипотезы нейролептического действия лекарственного средства обеспечивается сделанными при помощи PET открытиями высокой заполненности рецепторами допамина D2 в стриатуме пациентов, отвечающих на различные нейролептические фармакотерапии. Пациенты с хорошим ответом демонстрируют заполненность рецепторами допамина D2 более 65% (Nord and Farde, 2010). Проявление EPS представляется связанным с более высокой заполненностью рецепторами допамина D2 (выше 80%). Атипичные нейролептики, также называемые нейролептиками второго поколения, имеют клиническую апробацию для лечения психозов и маний. Каждое лекарственное средство имеет уникальный фармакодинамический и фармакокинетический профиль. Некоторые из атипичных нейролептических лекарственных средств имеют дополнительный антидепрессантный, транквилизирующий или снотворный профиль (Schwartz and Stahl 2011). Атипичные нейролептические лекарственные средства показывают в целом мощное антагонистическое действие в отношении рецептора серотонина 5-НТ 2 А по сравнению с более слабым антагонизмом в отношении рецептора допамина D2. Это фармакодинамическое свойство является основанием "атипичности" (Meltzer 1989). Антагонизм в отношении рецепторов 5-НТ 2 А вероятно обеспечивает большую допаминовую активность и нейротрансмиссию в нигростриатальной системе, что позволяет избежать EPS. Тот же самый механизмможет позволить небольшое облегчение негативных симптомов, и 5-НТ 2 антагонизм в тубероинфундибулярном пути может помочь избежать гиперпролактинемии (Schwartz and Stahl, 2011). Атипичные нейролептики не ответили на первоначальные ожидания по облегчению негативных симптомов и когнитивных дисфункций при шизофрении. Поэтому в настоящее время исследуется большее число молекулярных мишеней для разработки новых лекарственных средств для лечения шизофрении (Gray and Roth, 2007; Schizophrenia Research Forum, 2007). Допаминергические рецепторы D3 локализованы в лимбической коре, и, таким образом, предпочтительная блокада этих рецепторов обеспечивает локально селективную антидопаминергическую активность. Это приводит к повышенной эффективности в отношении уменьшения положительных симптомов шизофрении, уменьшает блокаду экстрапирамидальной системы и поэтому снижает риск главного побочного эффекта, такого как псевдопаркинсонический синдром. Кроме того, несколько доклинических данных позволяют предположить, что антагонизм в отношении рецептора допамина D3 более эффективен в уменьшении негативных симптомов шизофрении и улучшает рабочую память. Агонизм или частичный агонизм в отношении рецепторов 5-НТ 1 А считается возможным механизмом, связанным с активностью некоторых атипичных нейролептиков, таких как арипипразол и зипрасидон. Предполагается, что возбуждение рецепторов 5-НТ 1 А принимает участие в нейролептическом эффекте в комбинации с блокадой рецептора D2, особенно в профиле безопасности лекарственного средства, а также является полезным при агрессивном настрое и когнитивных симптомах при шизофренииof Schizophrenia, Neurotherapeutics, 6(1), 78-85, 2009). Серотонинергические рецепторы типа 5-НТ 6 локализованы исключительно в центральной нервной системе (ЦНС). Как локализация рецепторов 5-НТ 6 в лимбической и корковой областях мозга, так и относительно мощное сродство и антагонистическая активность некоторых нейролептиков (клозапин,оланзапин, сертиндол) и антидепрессантов (миансерин, амитриптилин) к рецепторам 5-НТ 6 приводят к предположению о потенциальной роли в патофизиологии и лечении нарушений ЦНС. Недавние литературные данные показывают, что блокада рецепторов 5-НТ 6 может участвовать в прокогнитивном эффекте вследствие увеличения холинергической трансмиссии, антидепрессантной активности вследствие увеличения норадренергического и допаминергического, а также транквилизирующего эффекта. Очевидно,что рецептор 5-НТ 6 представляется очень интересной молекулярной мишенью, и антагонисты этого рецептора могут служить потенциальными лекарственными средствами для лечения нарушений, характеризующихся когнитивными расстройствами, таких как болезнь Альцгеймера, шизофрения, депрессия,тревожность (Liu K. i Robichaud А., 5-НТ 6 Antagonists as Potential Treatment for Cognitive Dysfunction,2009; Wesolowska A. i Nikiforuk A., Effects of the brain-penetrant and selective 5-НТ 6 receptor antagonist SB399885 in animal models of anxiety and depression, 2007). Кроме того, было продемонстрировано, что антагонисты рецептора 5-НТ 6 являются активными в снижении потребления пищи и массы тела через клинически апробированный механизм, что сочетается с увеличением чувства насыщения. Таким образом,некоторые соединения с антагонистической активностью в отношении рецептора 5-НТ 6 в настоящее время проходят клиническую оценку в лечении ожирения (Heal D. et al., Selective 5-НТ 6 receptor ligands:progress in the development of a novel pharmacological approach to the treatment of obesity and related metabolic disorders, 2008). Интенсивное исследование, проводимое с 1993 г., показывает, что серотонинергические рецепторы 5-НТ 7 могут играть некоторую роль в контроле циркадных ритмов, сна, регуляции температуры, когнитивных процессах, боли и мигрени, а также в нейронной возбудимости. Мощное сродство и антагонистическая активность нескольких нейролептиков и антидепрессантов в отношении рецепторов 5-НТ 7 позволяют предположить потенциальную роль этих рецепторов в патофизиологии многих психоневрологических нарушений. Принимая во внимание поведенческие данные, представленные в литературе, было установлено, что селективные антагонисты рецептора 5-НТ 7 показывают антидепрессантную и транквилизирующую активность у крыс и мышей (Wesolowska A. et al., Effect of the selective 5-HT7 receptor antagonist SB-269970 in animal models of anxiety and depression, 2006). Используя мышиные модели нейролептической активности, Galici et al. показали, что селективный антагонист рецептора 5-НТ 7 SB-269970 может также вызывать подобные нейролептику эффекты (Galici R. et al., Effects of SB-269970, a 5-HT7receptor antagonist, in mouse models predictive of antipsychotic-like activity, 2008). Серотонинергические 5-НТ 2 С и гистаминергические H1 рецепторы, локализованные в гипоталамусе, играют важную роль в регулировании потребления пищи. Блокада обоих типов этих рецепторов, проведенная с использованием нейролептических лекарственных средств, наиболее близко коррелирует с увеличенным риском увеличения массы тела и диабета. С другой стороны, блокада рецепторов 5-НТ 2 С,главным образом локализованных в корковых областях и в гиппокампе, стриатуме, септальных ядрах,таламических ядрах и ядрах среднего мозга, может оказать выгодные антидепрессантные и прокогнитивные эффекты. В черной субстанции рецепторы 5-НТ 2 С солокализованы с ГАМК, что показывает, что они приводят к косвенному контролю допаминергической трансмиссии. Следовательно, блокада рецепторов 5-НТ 2 С вместе с одним рецептором 5-НТ 2 А, по всей видимости, потенцирует опосредуемый рецептором D2 тонический ингибирующий контроль допаминергической проекции с защитным эффектом против экстрапирамидальных симптомов (Kim D., Building a Better Antipsychotic: Receptor Targets for theTreatment of Multiple Symptom Dimensions of Schizophrenia, 2009). Блокада гистаминергического рецептора H1, произведенная нейролептическими препаратами, может участвовать в седативном эффекте, который является клинически выгодным в контроле активаций, сопровождающих острую фазу психоза. По-видимому, одновременное уменьшение сродства новой молекулы к обоим типам этих рецепторов может быть элементом, который защищает против избытка массы тела. Однако полное устранение сродства к этим рецепторам, возможно, не является необходимым из-за определенных выгод блокады рецепторов 5-НТ 2 С и H1. Блокада 1 адренергических рецепторов, несмотря на потенциальные периферические неблагоприятные эффекты, включающие гипотензию, может повлечь некоторую выгоду для центральной нервной системы, включающую уменьшение риска экстрапирамидальных побочных эффектов, вызываемых нейролептиками. Это может быть связано со взаимодействием между норадренергическими и серотонинергическими нейронами (Horacek J. et al., Mechanism of Action of Atypical Antipsychotic Drugs and the Neu-2 022776robiology of Schizophrenia, CNS Drugs, 20(5), 389-409, 2006). Блокада 2 адренергических рецепторов потенцирует вызываемое антидепрессантами увеличение внеклеточных моноаминов. Это может означать, что вещества, ингибирующие транспортеры моноаминов и одновременно блокирующие 2 адренергические рецепторы, могут быть мощными и быстродействующими новыми антидепрессантами. Кроме того, 2 антагонисты потенцируют секрецию ацетилхолина во фронтальной коре и могут улучшать когнитивные функции, что может обеспечить дополнительные преимущества как в антидепрессантной терапии, так и в нейролептической терапии (особенно уменьшение негативных симптомов). Блокада 2 адренергических рецепторов может также противодействовать половым дисфункциям, вызванным ингибиторами обратного захвата серотонина (Millan M., Dual- andDrugs, 2009). Антагонисты 2 могут также быть полезными в ослаблении экстрапирамидальных симптомов, вызванных блокадой рецепторов D2 в стриатуме. Сигма-рецепторы представляют собой отдельную группу рецепторов ЦНС; однако их физиологическая роль все еще неизвестна. Показано, что некоторые психотомиметические вещества, такие как фенциклидин, метамфетамин, героин или декстрометорфан, являются мощными агонистами сигмарецептора. С другой стороны, классическое нейролептическое лекарственное средство, галоперидол, является мощным антагонистом сигма-рецепторов, что может быть важным для его нейролептического потенциала. Было установлено, что селективные агонисты сигма-рецептора могут оказывать антидепрессантный эффект (Cobos E. et al., Pharmacology and Therapeutic Potential of Sigma Receptor Ligands, 2008). Вышеупомянутые открытия обеспечивают доказательство того, что сродство к сигма-рецепторам может вносить свой вклад в полный полезный фармакологический профиль нового психотропного лекарственного средства. Благодаря важной роли холинергической системы в познавательных процессах, текущее исследование сосредоточено на веществах, которые могут прямо или косвенно потенцировать активности холинергической системы. Они включают вещества, которые являются агонистами выбранных подтипов никотиновых или мускариновых рецепторов и антагонистами рецепторов 5-НТ 6. С другой стороны, потенциальные прокогнитивные эффекты, вызванные взаимодействием с вышеупомянутыми рецепторами,могут быть замаскированы холинолитической активностью. Таким образом, интерес представляют вещества, не имеющие антагонистических свойств в отношении холинергических рецепторов. Кроме того, эта стратегия позволяет устранить многие нежелательные периферические автономные эффекты, такие как запоры, ксеростомия или тахикардия (Miamoto S., Treatments for schizophrenia: a critical review of pharmacology and mechanisms of action of antipsychotic drugs, 2005). Кроме того, было обнаружено, что M3 мускариновые рецепторы задействованы в контроле секреции инсулина, и их активация стимулирует секрецию инсулина поджелудочной железой. Следовательно, можно ожидать, что блокада рецепторов M3 может быть неблагоприятной в отношении риска развития диабета типа II у пациентов, получающих лечение нейролептиками второго поколения (например, оланзапином, клозапином, кветиапином). Недавнее исследование сосредоточено на веществах, не оказывающих этого нежелательного эффекта (Silvestre J. iantipsychotics to induce type 2 diabetes, 2005). Другими серьезными побочными эффектами, вызываемыми нейролептическими лекарственными средствами, например сертиндолом, зипрасидоном, являются аритмии сердца, связанные с отсроченной реполяризацией кардиомиоцитов. Это состояние появляется на электрокардиограммах (ЭКГ) как пролонгированный скорректированный интервал QT (QTc), что чаще всего вызывается веществами, которые блокируют hERG калиевые каналы. Чтобы предотвратить придание разрабатываемым лекарственным средствам проаритмического потенциала, на очень ранней стадии исследования новые вещества скринируют in vitro на их потенциал в отношении блокировки hERG калиевых каналов, используя электрофизиологические способы (Recanatni M., QT Prolongation Through hERG K+ Channel Blockade: CurrentKnowledge and Strategies for the Early Prediction During Drug Development, 2005). Несмотря на подвижки, которые были сделаны в развитии антидепрессантов, все еще не выполняются клинические потребности как в отношении эффективности, так и в отношении побочных эффектов. Эти потребности простираются от эффективности в лечении резистентных пациентов (приблизительно 30%) с улучшенным началом действия до сокращения побочных эффектов, таких как половая дисфункция, желудочно-кишечные расстройства, седативный эффект, увеличение массы тела. Существует множество подходов к улучшению имеющихся в настоящее время фармакологических средств коррекции нейротрансмиссии биогенных аминов либо комбинированием механизмов, либо, альтернативно, селективной стимуляцией/блокировкой подтипов рецептора, которые могут вызвать улучшенную эффективность или меньшее число побочных эффектов. Одними из них являются комбинированные терапии, которые сохраняют выгоды, связанные с селективными ингибиторами обратного захвата серотонина(SSRIs) (блокаторы транспортера серотонина), но при этом либо улучшают эффективность, либо уменьшают побочные эффекты, добавляя дополнительный механизм, включающий блокаду рецепторов 5 НТ 2 А или 5-НТ 2 С (Millan M., Dual- and Triple-Acting Agents for Treating Core and Co-morbid Symptoms ofMajor Depression: Novel Concepts, New Drugs, Neurotherapeutics, 6(1), 53-77, 2009). Антагонисты рецептора 5-НТ 2 А при индивидуальном введении могут демонстрировать антидепрессантную активность, а также при совместном введении с SSRIs улучшают их антидепрессантные эффекты. Механизм этого взаимодействия может состоять в дополнительном увеличении внеклеточных уровней продуцируемого серотонина, когда SSRIs дают с 5-НТ 2 А антагонистами. Кроме того, блокада рецепторов 5-НТ 2 А является частью фармакологического профиля антидепрессантных лекарственных средств, таких как миансерин и миртазапин. Пресинаптические рецепторы 5-НТ 1 А связаны с риском депрессивного поведения, и их блокада усиливает эффекты SSRIs. Постсинаптические рецепторы 5-НТ 1 А являются существенными для оказания антидепрессивных эффектов агонистов рецептора 5-НТ 1 А и возможно SSRIs. Таким образом,частичный агонизм в отношении рецепторов 5-НТ 1 А является предпочтительной характеристикой новых молекул, тем более что этот механизм наблюдается у апробированного транквилизатора буспирона и антидепрессанта/транквилизатора тандоспирона. Хотя введение новых психотропных лекарственных средств (среди других нарколептических средств, антидепрессантов, бензодиазепинов, ингибиторов ацетилхолинэстеразы) с 50-х годов XX века было неоспоримым крупным достижением, терапия психоневрологических нарушений все еще является не совсем удовлетворительной как из-за ограниченной эффективности, так и широкого спектра побочных эффектов, вызываемых доступными лекарственными средствами. Эти недостатки являются вызовом для современного медикаментозного лечения и прилагаются непрерывные усилия в поиске новых, более эффективных психотропных лекарственных средств. Производные арилсульфонамида, потенциально пригодные для лечения сердечно-сосудистых заболеваний, таких как стенокардия, нарушение мозгового кровообращения и тромбоз, были описаны в публикации европейской заявки на патент EP 0330065 A. Раскрытые соединения имели ароматическое кольцо, например фенил, нафтил или пиридил, связанный с кольцом пиперазина. В публикации международной заявки на патент WO 98/43956 раскрыты 1,4-двузамещенные циклические амины следующей формулы, в которой циклический амин может быть связан с бициклической системой. Упомянутые выше производные были описаны как имеющие антагонистическую активность по отношению к серотонинергическим рецепторам и показывающие отсутствие сродства или очень низкое сродство к -адренергическим рецепторам. В публикации международной заявки на патент WO 2004/069794 арилсульфонамидные производные следующей формулы были описаны как агонисты рецептора 5-НТ 1 А, имеющие очень высокую активность и селективность и низкую или отсутствующую перекрестную реактивность с другими рецепторами. В публикации европейской заявки на патент EP 190472 A раскрыты имеющие нейролептическую активность соединения общей формулы, представленной ниже. Это соединение было предложено как структурная модификация другого соединения, N-[4-[4-(1,2 бензоксазол-3-ил)-1-пиперазинил]бутил]-1,2-цис-циклогександикарбоксимида (пероспирон, SM-9018),показывающая высокое сродство к рецепторам 5-НТ 2 и D2. По сообщениям, замена сукцинимида 4 метилбензолсульфонамидной группой заканчивалась однако уменьшением сродства к упомянутым выше рецепторам, в особенности к рецептору D2. Аналогично упомянутой выше публикации, статья Navas F. et al., Bioorg. Med. Chem. 6 (1998), 811823, также относилась к исследованию зависимости структура-активность. Было раскрыто соединение следующей формулы: Было обнаружено, что замена амидной группы сульфонамидной группой, как в раскрытом соединении, привела к значительному уменьшению сродства к серотонинергическим 5-НТ 1 А и допаминергическим D2 рецепторам. В публикации Forbes I.T. et al., Bioorg. Med. Chem. Lett. 10(2000) 1803-1806 раскрыты производные индолопиперидина, имеющие антагонистическую активность по отношению к рецептору хемокинаCCR2B, потенциально полезные для лечения заболеваний воспалительного происхождения, таких как атеросклероз и ревматоидный артрит. Среди протестированных производных был раскрыт 3,4-дихлор-N[4-(1H-индол-3-ил)пиперидин-1-ил]пентилбензолсульфонамид следующей формулы: Однако из вышеупомянутой публикации не следовало, что это соединение могло обладать активностью по отношению к терапевтическим мишеням, связанным с лечением заболеваний центральной нервной системы. Расширенное сродство N-4-[4-(1,2-бензоксазол-3-ил)пиперазин-1-ил]бутилбензолсульфонамида к 5-HT1A, 5-НТ 2 А, 5-НТ 6, 5-НТ 7, 1 и допаминергическим рецепторам D2 было раскрыто R. Bugno et al. в постере "Examination of 5-HT6 receptor affinity in the group of arylsulfonamide derivatives", опубликованном 10 мая 2010 г. в течение седьмой мультидисциплинарной Конференции по исследованию лекарственных средств, 9-12 мая 2010 г., Закопане, Польша. Цель изобретения Цель настоящего изобретения состоит в том, чтобы получить новые соединения, потенциально пригодные для лечения заболеваний центральной нервной системы. Следующая цель изобретения состоит в том, чтобы получить новые соединения, пригодные для лечения заболеваний центральной нервной системы, имеющие более высокую эффективность по сравнению с используемыми в настоящее время лекарственными средствами. Следующая цель настоящего изобретения состоит в том, чтобы получить новые соединения, пригодные для лечения заболеваний центральной нервной системы, которые могли бы позволить устранить или минимизировать неблагоприятные эффекты, связанные с используемыми в настоящее время терапиями. Раскрытие изобретения Настоящее изобретение относится к новым соединениям арилсульфонамида, имеющим структуру,представленную общей формулой (I) и к их фармацевтически приемлемым солям,в которойn означает целое число от 2 до 6 включительно;A обозначает 9- или 10-членную бициклическую группу, состоящую из бензольного кольца, конденсированного с 5- или 6-членным гетероциклическим кольцом, связанную с Е через один из ее атомов углерода и имеющую следующую формулу (А):R5 обозначает атом водорода, атом галогена или С 1-С 4-алкил;Y обозначает NH, О или S; каждый из R1, R2, R3 и R4 независимо обозначает атом водорода или атом галогена; каждый из R6 и R7 независимо обозначает атом водорода, атом галогена или C1-C4-алкил; или R6 и R7 вместе образуют карбонильную группу =O; обозначает простую связь или двойную связь;q=0 или 1; причем по меньшей мере один из q и m=1;D выбран из незамещенного фенила или фенила, замещенного одним или более заместителями, независимо выбранными из группы, состоящей из разветвленного С 1-С 4-алкила, прямого C1-C4-алкила в орто- или метаположении относительно сульфонамидной группы, C1-C3-алкилокси, галоген-С 1-С 3-алкила, галоген-C1C3-алкилокси, атома галогена, -CN, -ОН и фенила; незамещенного нафтила или нафтила, замещенного одним или более заместителями, независимо выбранными из группы, состоящей из С 1-С 4-алкила, C1-C3-алкилокси, галоген-С 1-С 3-алкила, атома галогена, -CN, -ОН и фенила; 5-членной ароматической гетероциклической группы, имеющей от 1 до 3 гетероатомов, независимо выбраных из группы, состоящей из N, О и S, которая является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы, состоящей из С 1-С 4-алкила, C1-C3-алкилокси,галоген-C1-C3-алкила, атома галогена, -CN, -ОН и фенила; бициклической группы, состоящей из кольца, выбранного из бензола и пиридина, конденсированного с 5-членным ароматическим или неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О, S, причем указанная бициклическая группа является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы, состоящей из C1-C4-алкила, C1-С 3-алкилокси, галоген-C1-C3-алкила, атома галогена, =O,-CN, -ОН и фенила; бициклической группы, состоящей из кольца, выбранного из бензола и пиридина, конденсированного с 6-членным неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S, причем указанная бициклическая группа является незамещенной или замещенной одним или более заместителями, независимо выбранными из группы,состоящей из С 1-С 4-алкила, C1-С 3-алкилокси, галоген-С 1-С 3-алкила, атома галогена, =O, -CN, -ОН и фенила. В одном варианте соединений согласно настоящему изобретению группа А связана с Е через атом углерода бензольного кольца. В альтернативном варианте соединений согласно настоящему изобретению группа А связана с Е через атом углерода гетероциклического кольца. Специалисту будет понятно, что соответствующий заместитель R1, R2, R3, R4, R5, R6 или R7 на атоме углерода, через который группа А связана с Е, отсутствует и заменен связью. Согласно одному из вариантов соединения согласно настоящему изобретению имеют формулу (I), в которой в группе А обозначает двойную связь, q=0, X обозначает C(R5) и Z обозначает N. В этих соединениях А соответствует следующей общей формуле (А 1), в которой Y, R1, R2, R3, R4 и R5 имеют те же самые значения, как определено выше, и которая является частным вариантом формулы (А) Группа формулы (А 1) может быть связана с Е через атом углерода фенильного кольца или через атом углерода 5-членного гетероциклического кольца. Предпочтительно в указанном варианте (А 1) обозначает 1,2-бензотиазол-3-ил или 1,2-бензоксазол 3-ил, который может быть замещен атомом галогена. Следующим вариантом соединений согласно настоящему изобретению являются соединения формулы (I), в которой в группе А обозначает двойную связь, q=0, X обозначает C(R5) и Z обозначает 5C(R ). В этих соединениях А соответствует следующей общей формуле (А 2), в которой Y, R1, R2, R3, R4 иR5 имеют значения, как определено выше, и которая является частным вариантом формулы (А) Группа формулы (А 2) может быть связана с Е через атом углерода фенильного кольца или через атом углерода 5-членного гетероароматического кольца. Предпочтительно в указанном варианте (А 2) обозначает 1H-индол-3-ил, 2-(С 1-С 4-алкил)-lH-индол 3-ил или 1H-индол-4-ил, который может быть замещен атомом галогена. Другим вариантом соединений согласно настоящему изобретению являются соединения формулы(I), в которой в группе А обозначает простую связь, и m=0. В этих соединениях А соответствует следующей общей формуле (A3), в которой X, Y, R1, R2, R3, R4, R6 и R7 имеют значения, как определено выше, и которая является частным вариантом формулы (А) Группа формулы (A3) может быть связана с Е через атом углерода фенильного кольца или через атом углерода гетероциклического кольца. Предпочтительно в указанном варианте (A3) обозначает 2-оксо-2,3-дигидро-1H-бензимидазол-4-ил,2-оксо-2,3-дигидро-1,3-бензоксазол-4-ил, 2-оксо-2,3-дигидро-1,3-бензоксазол-7-ил, 2-оксо-2,3-дигидро 1H-индол-4-ил, 2,2-диметил-2,3-дигидро-1H-индол-4-ил, 2,2-диметил-1,3-бензодиоксол-4-ил или 2,2 дифтор-1,3-бензодиоксол-4-ил. Еще один вариант соединений согласно настоящему изобретению представляет собой соединения формулы (I), в которой в группе А обозначает простую связь, m=1, q=1 и Z обозначает СН 2. В этих соединениях А соответствует следующей общей формуле (А 4), в которой X, Y, R1, R2, R3, R4, R6 и R7 имеют значения, как определено выше, и которая является частным вариантом формулы (А) Группа формулы (А 4) может быть связана с Е через атом углерода фенильного кольца или через атом углерода 6-членного гетероциклического кольца. Предпочтительно в указанном варианте (А 4) обозначает 1,4-бензодиоксан-5-ил или 3-оксо-3,4 дигидро-2 Н-1,4-бензоксазин-8-ил. Другой подгруппой соединений по изобретению являются соединения формулы (I), в которой D обозначает фенил. Фенил может быть незамещенным или замещенным, как определено для заместителяD выше, например, одним или более заместителями, независимо выбранными из группы, состоящей из прямого C1-C4-алкила в положении орто или мета относительно сульфонамидной группы, атома галогена, -CN, -ОН и фенила. Еще одна подгруппа соединений по изобретению представлена соединениями формулы (I), в которой D обозначает нафтил. Нафтил может быть связан с атомом серы сульфонамидной группой в положении 1 или 2 нафтильного кольца. Нафтил может быть незамещенным или замещенным, как определено для заместителя D выше, например, атомом галогена. Еще одна группа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой D обозначает 5-членную ароматическую гетероциклическую группу, имеющую от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S. Предпочтительной ароматической гетероциклической группой является тиенил, т.е. гетероатом представляет собой атом серы. 5 Членная ароматическая гетероциклическая группа может быть незамещенной или замещенной, как определено для заместителя D выше. Другая подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой D обозначает бициклическую группу, состоящую из бензольного кольца, конденсированного с 5-членным ароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов,независимо выбранных из группы, состоящей из N, О и S. Эта бициклическая группа может быть незамещенной или замещенной, как определено выше для заместителя D, например, атомом галогена и/илиC1-C4-алкилом. Предпочтительно бициклическая группа выбрана из группы, состоящей из 1 бензотиофен-3-ила, 1-бензотиофен-2-ила, 1-бензофуран-2-ила, 1-бензофуран-3-ила, 1H-бензимидазол-2 ила, 1H-индол-2-ила, 1H-индол-5-ила, 1H-индол-6-ила, 1H-индазол-7-ила, 1H-индазол-6-ила, 1,2 бензоксазол-5-ила, 1,3-бензоксазол-4-ила, 1,3-бензотиазол-4-ила и 1,3-бензотиазол-5-ила. Следующая подгруппа изобретений согласно настоящему изобретению представлена соединениями формулы (I), в которой D обозначает бициклическую группу, состоящую из кольца пиридина, конденсированного с 5-членным гетероциклическим ароматическим кольцом, имеющим от 1 до 3 гетероатомов,независимо выбранных из группы, состоящей из N, О и S. Эта бициклическая группа может быть незамещенной или замещенной, как определено выше для заместителя D, например, атомом галогена и/или С 1-С 4-алкилом. Предпочтительно бициклическая группа выбрана из группы, состоящей из имидазо[1,2 а]пиридин-3-ила и 1H-пирроло[2,3-b]пиридин-3-ила. Еще одна подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой D обозначает бициклическую группу, состоящую из бензольного кольца, конденсированного с 5-членным неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S. Эта бициклическая группа может быть незамещенной или замещенной, как определено выше для заместителя D. Предпочтительная бициклическая группа выбрана из группы, состоящей из 2,3-дигидро-1-бензофуран-5-ила, 2-оксо-2,3-дигидро-1,3 бензоксазол-6-ила, 2-оксо-1,3-дигидро-2 Н-индол-5-ила и 1,3-бензодиоксол-5-ила. Еще одна подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой D обозначает бициклическую группу, состоящую из бензольного кольца, конденсированного с 6-членным неароматическим гетероциклическим кольцом, имеющим от 1 до 3 гетероатомов, независимо выбранных из группы, состоящей из N, О и S. Эта бициклическая группа может быть незамещенной или замещенной, как определено выше для заместителя D. Предпочтительной бициклической группой является 2,3-дигидро-1,4-бензодиоксин-6-ил. Другая подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой n=2. Другая подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой n=3. Другая подгруппа соединений согласно настоящему изобретению представлена соединениями формулы (I), в которой n=4. Могут быть названы следующие конкретные соединения формулы (I) по изобретению: и их фармацевтически приемлемые соли. Производные арилсульфонамида приведенной выше формулы (I) демонстрируют сродство с рецеп- 12022776 торами, признанными в качестве терапевтических мишеней для лечения нарушений ЦНС, такими как допаминергические, в частности D2 и D3, серотонинергические, в частности 5-НТ 1 А, 5-НТ 2 А, 5-НТ 6, 5 НТ 7, адренергические, в частности 1 и 2 С, сигма-рецепторы и рецепторы транспортера серотонина, и не демонстрируют сродства или имеют низкое сродство с биологическими мишенями, связанными с неблагоприятными эффектами, такими как hERG калиевых каналов, мускариновые рецепторы, гистаминергические рецепторы и серотонинергические 5-НТ 2 С рецепторы. Вследствие такого широкого фармакологического профиля, соединения по изобретению могут быть использованы в медицине в качестве лекарственных средств для лечения и/или профилактики нарушений центральной нервной системы, таких как шизофрения, шизоаффективные нарушения, шизофрениформные нарушения, бредовые синдромы и другие психотические состояния, связанные и не связанные с приемом психотропных веществ, аффективное расстройство, биполярное расстройство, мания, депрессия, тревожные нарушения различной этиологии, стрессовые реакции, расстройства сознания, кома, алкогольный делирий или делирий другой этиологии, агрессия, психомоторное возбуждение и другие поведенческие расстройства, нарушения сна различной этиологии, абстиненция различной этиологии, зависимость, болевые синдромы различной этиологии, интоксикация психотропными веществами, нарушения мозгового кровообращения различной этиологии, психосоматические нарушения различной этиологии, конверсионные нарушения, диссоциирующие нарушения, нарушения мочеиспускания, аутизм и другие нарушения развития, включая ноктурию, заикание, тики, когнитивные нарушения различных типов, такие как болезнь Альцгеймера, психопатологические симптомы и неврологические нарушения в рамках других заболеваний центральной и периферической нервной системы. Таким образом, объектом настоящего изобретения являются соединения формулы (I), определенной выше, для применения в качестве лекарственного средства для лечения и/или профилактики нарушений центральной нервной системы, связанных с допаминергической, и/или серотонинергической, и/или норадренергической трансмиссией. При лечении нарушений центральной нервной системы соединение формулы (I) может вводиться в форме фармацевтической композиции или препарата, ее содержащего. Таким образом, объектом настоящего изобретения также является фармацевтическая композиция для лечения и/или профилактики нарушений центральной нервной системы, связанных с допаминергической, и/или серотонинергической, и/или норадренергической трансмиссией, содержащая соединение или соединения формулы (I), определенной выше, в качестве активного вещества, в комбинации с фармацевтически приемлемым носителем(ями) и/или эксципиентом(ами). Объектом изобретения также является применение производных арилсульфонамида приведенной выше формулы (I) для лечения нарушений центральной нервной системы. Изобретение относится также к способу лечения нарушений центральной нервной системы у млекопитающих, включая человека, включающему введение терапевтически эффективного количества соединения приведенной выше формулы (I) или фармацевтической композиции, содержащей в качестве активного вещества соединение формулы (I), определенной выше. Термины, используемые в описании настоящего изобретения, имеют следующие значения. Если не указано иное, термин "С 1-С 4-алкил" относится к насыщенной, прямой или разветвленной углеводородной группе, имеющей указанное число атомов углерода. Частными примерами групп, охваченных этим термином, являются метил, этил, н-пропил, изопропил, н-бутил, трет-бутил и втор-бутил. Термин "С 1-С 3-алкилокси" относится к -O-C1-C3-алкильной группе, в которой C1-C3-алкил обозначает насыщенную углеводородную группу, имеющую указанное число атомов углерода, которая имеет прямую или разветвленную цепь. Частными примерами групп, охваченных этим термином, являются метокси, этокси, н-пропокси и изопропокси. Термин "атом галогена" относится к заместителю, выбранному из F, Cl, Br и I. Термин "галоген-С 1-С 3-алкил" относится к насыщенной прямой или разветвленной углеводородной группе, имеющей указанное число атомов углерода, в которой один атом углерода может быть замещен 1-3 атомами галогена, в зависимости от числа атомов углерода, связанных с ним. Атом галогена имеет значение, как определено выше. Особенно предпочтительным примером группы, охваченной этим термином, является трифторметильная группа CF3. Термин "галоген-С 1-С 3-алкилокси" относится к -О-С 1-С 3-галогеналкильной группе, в которой C1-C3 галогеналкил представляет собой насыщенную прямую или разветвленную углеводородную группу,имеющую указанное число атомов углерода, в которой один атом углерода может быть замещен 1-3 атомами галогена, в зависимости от числа атомов углерода, связанных с ним. Атом галогена имеет значение,как определено выше. Особенно предпочтительным примером группы, охваченной этим термином, является трифторметоксигруппа -O-CF3. Соединения формулы (I) могут быть получены способом, представленным в следующей схеме: На первой стадии соединение (IVa), например, в форме гидрохлорида вводят в реакцию с подходящим 2-(бромалкил)-1H-изоиндолин-1,3(2 Н)-дионом (IVb) в растворителе, таком как N,Nдиметилформамид или ацетонитрил, в присутствии основания при комнатной температуре или в повышенной температуре с получением соединения формулы (III). Затем имид (III) гидролизуют, используя 40%-ный водный раствор метиламина при комнатной температуре, с получением производного амина(IIa). Соединение (IIa) вводят в реакцию с подходящим арилсульфонилхлоридом (IIb), например, в метиленхлориде в присутствии триэтиламина при комнатной температуре с получением арилсульфонамидного производного (I) по изобретению. Исходные соединения формул (IVa) и (IVb) либо являются известными или коммерчески доступными, либо могут быть получены из коммерчески доступных исходных материалов путем адаптации и использования известных способов, таких как описанный в публикации Hallett D.J. et al., J. Org. Chem. 2000, 65, 4984-4993. Получение некоторых исходных соединений формулы (III) описано подробно в экспериментальной части. Так как соединения формулы (I) имеют щелочной характер (содержат по меньшей мере одну группу третичного амина), они могут образовывать соли присоединения с кислотой. Соли с кислотами могут быть фармацевтически приемлемыми, особенно когда они предназначены для использования в качестве активного ингредиента в фармацевтической композиции. Настоящее изобретение относится также к солям соединений формулы (I) с кислотами, отличными от фармацевтически приемлемых, которые могут быть использованы, например, в качестве промежуточных соединений, подходящих для очистки соединений по изобретению. Практически часто желательно выделить сначала соединение из реакционной смеси в форме соли, которая не является фармацевтически приемлемой, для очистки соединения и затем преобразовать эту соль в свободное основание путем обработки щелочным веществом и выделить и в случае необходимости снова преобразовать в соль. Соли присоединения с кислотой можно образовать с неорганическими (минеральными) или органическими кислотами. В частности, как примеры кислот могут быть названы хлористо-водородная, бромисто-водородная, йодисто-водородная, фосфорная, серная, азотная, угольная, янтарная, малеиновая,муравьиная, уксусная, пропионовая, фумаровая, лимонная, винная, молочная, бензойная, салициловая,глутаминовая, аспарагиновая, п-толуолсульфоновая, бензолсульфоновая, метансульфоновая, этансульфоновая, нафталинсульфоновая, такая как 2-нафталинсульфоновая, памовая, ксинафоевая или гексановая кислоты. Соль присоединения с кислотой может быть получена простым образом путем реакции соединения формулы (I) с подходящей неорганической или органической кислотой, в случае необходимости в подходящем растворителе, таком как органический растворитель, с образованием соли, которую обычно выделяют, например, кристаллизацией и фильтрацией. Например, соединения в форме свободного основания могут быть преобразованы в соответствующие гидрохлоридные соли реакцией соединения в растворе, например в метаноле, со стехиометрическим количеством соляной кислоты или с раствором соляной кислоты в метаноле, этаноле или простом диэтиловом эфире с последующим выпариванием растворителя(ей). Термин "нарушения центральной нервной системы" должен быть понят как включающий нарушения, выбранные из шизофрении, шизоаффективных расстройств, шизофрениформных расстройств, бредовых синдромов и других психотических состояний, связанных и не связанных с приемом психотропных веществ, аффективного расстройства, биполярного расстройства, мании, депрессии, тревожных нарушений различной этиологии, стрессовых реакций напряжения, расстройств сознания, комы, алкогольного делирия или делирия другой этиологии, агрессии, психомоторного возбуждения и других поведенческих расстройств, нарушений сна различной этиологии, синдромов отмены различной этиологии, зависимости, болевых синдромов различной этиологии, интоксикации психотропными веществами, нарушений мозгового кровообращения различной этиологии, психосоматических нарушений различной этиоло- 14022776 гии, конверсионных нарушений, диссоциирующих нарушений, нарушений мочеиспускания, аутизма и других нарушений развития, включая ноктурию, заикание, тики, когнитивных нарушений различных типов, таких как болезнь Альцгеймера, психопатологических симптомов и неврологических нарушений в рамках других заболеваний центральной и периферической нервной системы. При лечении упомянутых выше нарушений соединения формулы (I) согласно настоящему изобретению могут вводиться как химическое соединение, но обычно вводятся в форме фармацевтических композиций, содержащих соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, определенную выше, в качестве активного ингредиента в комбинации с фармацевтически приемлемым носителем(ями) и/или эксципиентом(ами). При лечении вышеуказанных нарушений фармацевтические композиции по изобретению могут быть доставлены любым путем введения, предпочтительно пероральным или парентеральным, и имеют форму препарата для использования в медицине в зависимости от намеченного пути введения. Композиции для перорального введения могут иметь форму твердых или жидких препаратов. Твердые препараты могут быть в форме, например, таблеток или капсул, полученных обычным образом с использованием фармацевтически приемлемых неактивных ингредиентов, таких как связующие вещества (например, предварительно желатинированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза, сахароза, карбоксиметилцеллюлоза,микрокристаллическая целлюлоза или гидрофосфат кальция), лубриканты (например, стеарат магния,тальк или диоксид кремния); дезинтеграторы (например, кросповидон, кукурузный крахмал или гликолят крахмала натрия); смачивающие вещества (например, лаурилсульфат натрия). Таблетки могут быть покрыты с использованием способов, известных в данный области техники, обычными покрытиями, покрытиями для отсроченного/контролируемого высвобождения или энтеросолюбильными покрытиями. Жидкие препараты для перорального введения могут иметь форму, например, растворов, сиропов или суспензий или могут быть получены из сухого продукта, подходящего для восстановления с водой или другим подходящим носителем ex tempore. Такие жидкие препараты могут быть получены обычными способами с фармацевтически приемлемыми неактивными ингредиентами, такими как суспендирующие агенты (например, сорбитовый сироп, производные целлюлозы или гидрированные пищевые жиры),эмульгаторы (например, лецитин или гуммиарабик), неводные матричные компоненты (например, миндальное масло, сложные эфиры масел, этиловый спирт или фракционированные растительные масла) и консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота). Препараты могут также содержать подходящие буферизующие системы, вкусовые и ароматизирующие агенты, красители и подсластители. Препараты для перорального введения могут быть составлены согласно способам, известным специалисту, так, чтобы обеспечить контролируемое высвобождение активного соединения. Парентеральный путь введения включает введение внутримышечными и внутривенными инъекциями и внутривенными непрерывными инфузиями. Композиции для парентерального введения могут быть в стандартной лекарственной форме, например в ампулах или в мультидозных емкостях с добавлением консерванта. Композиции могут быть в форме суспензий, растворов или эмульсий в масляных или водных средах и могут содержать фармацевтически приемлемые эксципиенты, такие как суспендирующие агенты, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в форме порошка для восстановления ex tempore в подходящем носителе, например, стерильной апирогенной воде. Способ лечения с использованием соединения по изобретению основан на введении пациенту терапевтически эффективного количества соединения по изобретению, предпочтительно в форме фармацевтической композиции. Предлагаемая доза соединений по изобретению находится в диапазоне от 1 до приблизительно 1000 мг в сутки в единственной дозе или в раздельных дозах. Для специалиста будет очевидно, что выбор дозы, необходимой для достижения желаемого биологического действия, будет зависеть от нескольких факторов, таких как тип конкретного соединения, показание, путь введения, возраст и состояние пациента, и точная доза в конечном итоге определяется на усмотрение лечащего врача. Пример 1. Получение исходных материалов общей формулы (III).b1) Общая процедура для исходных соединений (IVa), легко растворимых в N,Nдиметилформамиде. Смесь 5,6 ммоль соединения (IVa) и 5,6 ммоль соединения (IVb), 12 ммоль N,Nдиизопропилэтиламина и 20 мл N,N-диметилформамида перемешивали при комнатной температуре до исчезновения исходных материалов (TLC контроль). Обычно реакцию проводили в течение 2,5 дней. Затем к смеси добавляли 100 мл воды и оставляли на 1 ч. Затем к полученной смеси добавляли 20 мл метанола и после нагревания нагревали с обратным холодильником в течение 20 мин. Осажденный продукт выделяли фильтрацией и высушивали до постоянного веса. Структура продукта была подтверждена масс-спектрометрией. Следующие соединения были получены согласно вышеописанной процедуре: 2-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутил-1H-изоиндол-1,3(2 Н)-дионb2) Общая процедура для исходных соединений (IVa), плохо растворимых в ацетонитриле. Смесь 13 ммоль соединения (IVa) и 13 ммоль соединения (IVb), 13 ммоль N,Nдиизопропилэтиламина, каталитического количества йодида калия и 300 мл смеси N,Nдиметилформамида и ацетонитрила 1:1 перемешивали при 70C в течение 3 дней. Затем реакционную смесь концентрировали при пониженном давлении и остаток очищали, используя хроматографию на колонках на силикагеле, используя метиленхлорид:метанол = 9:1 в качестве элюента. Структура продукта была подтверждена масс-спектрометрией. Согласно вышеописанной процедуре были получены следующие соединения: 2-4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутил-1H-изоиндол 1,3(2 Н)-дион (III-12), MS: 448 [М+Н+]. Выход: 36%; 2-3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропил-1H-изоиндол 1,3(2 Н)-дион (III-22), MS: 404 [М+Н+]. Выход: 40%; 2-2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этил-1H-изоиндол-1,3(2 Н)дион (III-23), MS: 390 [М+Н+]. Выход: 47%. Пример 2. Общая процедура для получения исходных материалов общей формулы (IIa) гидролизом имида (III). 1,7 ммоль соединения (III) суспендировали в 40 мл 40%-го водного раствора метиламина и перемешивали при комнатной температуре в течение 16 ч. Затем метиламин выпаривали и полученный осадок фильтровали. Осадок промывали водой и высушивали до постоянного веса. Структура продукта была подтверждена масс-спектрометрией. Согласно вышеописанной процедуре были получены следующие соединения: 4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутан-1-амин (IIa-9) из соединения (III9), MS: 304 [М+Н+]. Выход: 85%; 3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропан-1-амин (IIa-10) из соединения 2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этил-1-амин (IIa-23) из соединения (III-23), MS: 290 [М+Н+]. Выход: 60%. Пример 3. Общая процедура для получения соединений (I) по изобретению. Соединения по изобретению были получены согласно следующей схеме. 0,2 ммоль амина (IIa) растворяли в 5 мл безводного N,N-диметилформамида и затем добавляли 4 ммоль N,N-диизопропилэтиламина. Смесь продували аргоном и затем добавляли 0,24 ммоль подходящего арилсульфонил хлорида (IIb). После 30 мин перемешивания при комнатной температуре смесь вливали в приблизительно 20 мл воды со льдом. Смесь экстрагировали этилацетатом или метиленхлоридом. Органический слой промывали солевым раствором, высушивали над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Сырые сульфонамиды обычно очищали посредством кристаллизации (из метанола), и некоторые из них, используя хроматографию на колонках на силикагеле с использованием смеси метиленхлорид/метанол 20:1 в качестве элюента. Структура полученных соединений была подтверждена данными MS, а чистота - анализом ВЭЖХ. Для выбранных соединений идентификация структуры была дополнительно подтверждена анализом 1H-ЯМР. Следуя общей процедуре, описанной выше, и исходя из соответствующего амина соединений (IIa) и арилсульфонилхлорида (IIb), получали следующие соединения. Соединение 34.N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н) -ил]бутилнафталин-1-сульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и нафталин-1-сульфонилхлорида. Выход: 42%. MS: 494 [М+Н+]. Соединение 35.N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилнафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и нафталин-2-сульфонилхлорида. Выход: 40%. MS: 494 [М+Н+]. Соединение 36. 4-Фтор-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 4-фторбензолсульфонилхлорида. Выход: 42%. MS: 462 [М+Н+]. Соединение 37. 3-Фтор-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 3-фторбензолсульфонилхлорида. Выход: 60%. MS: 462 [М+Н+]. Соединение 38. 4-Хлор-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 4-хлорбензолсульфонилхлорида. Выход: 55%. MS: 478 [М+Н+]. Соединение 39. 3-Хлор-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 3-хлорбензолсульфонилхлорида. Выход: 30%. MS: 478 [М+Н+]. Соединение 40. 3-Метил-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 3-метилбензолсульфонил хлорида. Выход: 55%. MS: 458 [М+Н+]. Соединение 41. 3-Гидрокси-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 3-гидроксибензолсульфонилхлорида. Выход: 20%. MS: 460 [М+Н+]. Соединение 42. 4-Метокси-N-4-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-9) и 4-метоксибензолсульфонилхлорида. Выход: 52%. MS: 474 [М+Н+]. Соединение 43. Целевое соединение получали, исходя из амина (IIa-10) и нафталин-1-сульфонилхлорида. Выход: 99%. MS: 480 [М+Н+]. Соединение 44.N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилнафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и нафталин-2-сульфонилхлорида. Выход: 76%. MS: 480 [М+Н+]. Соединение 45. 4-Фтор-N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и 4-фторбензолсульфонилхлорида. Выход: 99%. MS: 448 [М+Н+]. Соединение 46. 3-Фтор-N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и 3-фторбензолсульфонилхлорида. Выход: 98%. MS: 448 [М+Н+]. Соединение 47. 4-Хлор-N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и 4-хлорбензолсульфонилхлорида. Выход: 72%. Соединение 48. 3-Хлор-N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и 3-хлорбензолсульфонилхлорида. Выход: 98%. MS: 464 [М+Н+]. Соединение 49. 3-Гидрокси-N-3-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]пропилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-10) и 3-гидроксибензолсульфонилхлорида. Выход: 29%. MS: 446 [М+Н+]. Соединение 50.N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилнафталин-1-сульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и нафталин-1-сульфонилхлорида. Выход: 99%. MS: 466 [М+Н+]. Соединение 51.N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилнафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и нафталин-2-сульфонилхлорида. Выход: 99%. MS: 466 [М+Н+]. Соединение 52.N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этил-4-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 4-фторбензолсульфонилхлорида. Выход: 98%. MS: 434 [М+Н+]. Соединение 53. 3-Фтор-N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 3-фторбензолсульфонилхлорида. Выход: 52%. MS: 434 [М+Н+]. Соединение 54. 4-Хлор-N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 4-хлорбензолсульфонилхлорида. Выход: 98%. MS: 450 [М+Н+]. Соединение 55. 3-Хлор-N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 3-хлорбензолсульфонилхлорид. Выход: 89%. MS: 450 [М+Н+]. Соединение 56. 3-Метил-N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 3-метилбензолсульфонилхлорида. Выход: 48%. MS: 430 [М+Н+]. Соединение 57. 3-Гидрокси-N-2-[4-(5-хлор-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]этилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-11) и 3-гидроксибензолсульфонилхлорида. Выход: 12%. MS: 432 [М+Н+]. Соединение 58. 4-Хлор-N-4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидропиридин-1(2 Н)-ил]бутилбензолсуль- 18022776 фонамид. Целевое соединение получали, исходя из амина (IIa-12) и 4-хлорбензолсульфонилхлорида. Выход: 10%. MS: 492 [М+Н+]. Соединение 137.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-хлорбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 3-хлорбензолсульфонилхлорида. Выход: 95%. MS: 4 92 [М+Н+]. Соединение 138.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-3-хлорбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 3-хлорбензолсульфонилхлорида. Выход: 89%. MS: 478 [М+Н+]. Соединение 139.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 3-фторбензолсульфонилхлорида. Выход: 86%. MS: 476 [М+Н+]. Соединение 140.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-3-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 3-фторбензолсульфонилхлорида. Выход: 85%. MS: 462 [М+Н+]. Соединение 141.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-4-трет-бутилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 4-трет-бутилбензолсульфонилхлорида. Выход: 67%. MS: 514 [М+Н+]. Соединение 366.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]нафталин-1-сульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и нафталин-1-сульфонилхлорида. Выход: 60%. MS: 508 [М+Н+]. Соединение 367.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]нафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и нафталин-2-сульфонилхлорида. Выход: 82%. MS: 508 [М+Н+]. Соединение 368.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-4-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 4-фторбензолсульфонилхлорида. Выход: 93%. MS: 376 [М+Н+]. Соединение 369.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-гидроксибензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 3-гидроксибензолсульфонилхлорида. Выход: 43%. MS: 474 [М+Н+]. Соединение 370.N-[4-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-метилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-12) и 3-метилбензолсульфонилхлорида. Выход: 84%. MS: 472 [М+Н+]. Соединение 432.N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]нафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-19) и нафталин-2-сульфонилхлорида. Выход: 65%. 1H-ЯМР (300 МГц, CDCl3): 8,40 (с, 1H), 8,20 (с, 1H), 6,98 (т, 1H, J=3,4 Гц), 6,02 (с, 1H), 3,15-3,10 (м,2 Н), 2,98-2,90 (м, 2 Н), 2,80-2,72 (м, 4 Н), 2,56-2,52 (м, 2 Н), 1,65-1,48 (м, 4 Н). MS: 478 [М+Н+]. Соединение 433. 3-Фтор-N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-19) и 3-фторбензолсульфонилхлорида. Выход:N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-гидроксибензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-19) и 3-гидроксибензолсульфонилхлорида. Выход: 67%. MS: 444 [М+Н+]. Соединение 435.N-[4-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]бутил]-3-метилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-19) и 3-метилбензолсульфонилхлорида. Выход: 76%. 1 Н-ЯМР (300 МГц, CD3OD): 7,54-7,46 (м, 3H), 7,30-7,18 (м, 4 Н), 6,90 (дт, 1H, J=8,9 и 2,5 Гц), 6,045,98 (м, 1H), 3,38-3,30 (м, 2 Н), 2,87 (т, 2 Н, J=5,9 Гц), 2,80-2,60 (м, 4 Н), 2,48 (т, 2 Н, J=6,6 Гц), 1,58-1,52 (м,4 Н). MS: 442 [М+Н+]. Соединение 436. 3-Фтор-N-[3-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-20) и 3-фторбензолсульфонилхлорида. Выход: 70%. 1 Н-ЯМР (300 МГц, CD3OD): 7,54-7,46 (м, 3H), 7,30-7,18 (м, 4 Н), 6,90 (дт, 1H, J=8,9 и 2,5 Гц), 6,045,98 (м, 1H), 3,38-3,30 (м, 2 Н), 2,87 (т, 2 Н, J=5,9 Гц), 2,80-2,60 (м, 4 Н), 2,48 (т, 2 Н, J=6,6 Гц), 1,58-1,52 (м,4 Н). MS: 432 [М+Н+]. Соединение 437.N-[3-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-3-гидроксибензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-20) и 3-гидроксибензолсульфонилхлорида. Выход: 62%. MS: 430 [М+Н+]. Соединение 438.N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]нафталин-2-сульфонамид. Целевое соединение получали, исходя из амина (IIa-21) и нафталин-2-сульфонилхлорида. Выход: 54%. MS: 450 [М+Н+]. Соединение 439. 3-Фтор-N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-21) и 3-фторбензолсульфонилхлорида. Выход: 70%. 1 Н-ЯМР (300 МГц, CDCl3): 8,17 (с, 1H), 7,70-7,46 (м, 4 Н), 7,32-7,20 (м, 3H), 7,00-6,94 (м, 1H), 6,025,98 (м, 1H), 3,12 (т, 2 Н, J=5,3 Гц), 3,06-3,02 (м, 2 Н), 2,62-2,48 (м, 4 Н), 1,76-1,62 (м, 2 Н). MS: 418 [М+Н+]. Соединение 440.N-[2-[4-(5-фтор-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]-3-метилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-21) и 3-метилбензолсульфонилхлорида. Выход: 83%. 1N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]нафталин-1 сульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и нафталин-1-сульфонилхлорида. Выход: 74%. MS: 494 [М+Н+]. Соединение 442.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]нафталин-2 сульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и нафталин-2-сульфонилхлорида. Выход: 67%. MS: 494 [М+Н+]. Соединение 443.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-4-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 4-фторбензолсульфонилхлорида. Выход: 50%. MS: 462 [М+Н+]. Соединение 444. 4-Хлор-N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 4-хлорбензолсульфонилхлорида. Выход: 69%. MS: 478 [М+Н+]. Соединение 445.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-3-гидроксибензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 3-гидроксибензолсульфонилхлорида. Выход: 40%. MS: 460 [М+Н+]. Соединение 446.N-[3-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]пропил]-3-метилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-22) и 3-метилбензолсульфонилхлорида. Выход: 82%. MS: 458 [М+Н+]. Соединение 447.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]нафталин-1-сульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и нафталин-1-сульфонилхлорида. Выход: 89%. MS: 480 [М+Н+]. Соединение 448.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]нафталин-2 сульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и нафталин-2-сульфонилхлорида. Выход: 61%. MS: 480 [М+Н+]. Соединение 449.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]-4-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 4-фторбензолсульфонилхлорида. Выход: 45%. MS: 448 [М+Н+]. Соединение 450.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]-3-фторбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 3-фторбензолсульфонилхлорида. Выход: 56%. MS: 448 [М+Н+]. Соединение 451. 4-Хлор-N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 4-хлорбензолсульфонилхлорида. Выход: 88%. MS: 464 [М+Н+]. Соединение 452. 3-Хлор-N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]бензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 3-хлорбензолсульфонилхлорида. Выход: 63%. MS: 464 [М+Н+]. Соединение 453.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]-3-гидроксибензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 3-гидроксибензолсульфонилхлорида. Выход: 46%. MS: 446 [М+Н+]. Соединение 454.N-[2-[4-(5-хлор-2-метил-1H-индол-3-ил)-3,6-дигидро-2 Н-пиридин-1-ил]этил]-3-метилбензолсульфонамид. Целевое соединение получали, исходя из амина (IIa-23) и 3-метилбензолсульфонилхлорида. Выход: 51%. MS: 444 [М+Н+]. Тесты in vitro. Пример 4. Фармакология in vitro: тесты связывания. Сродство соединений согласно настоящему изобретению к допаминергическим, серотонинергическим, адренергическим, мускариновым M3, гистаминергическим H1, сигма-рецепторам и рецепторам транспортера серотонина проверяли, используя способы, описанные ниже, состоящие в измерении их связывания с этими рецепторами, используя способы радиорецепторов. Специфическое связывание лиганда с рецепторами определяют как различие между общим связыванием и неспецифическим связыванием, определенным в присутствии избытка немеченного лиганда. Результаты выражают как процент контрольного специфического связывания измеренное специфическое связывание/контрольное специфическое связывание)100) и как процент ингибирования кон- 21022776 трольного специфического связывания (100-измеренное специфическое связывание/контрольное специфическое связывание)100, полученный в присутствии тестируемых соединений. Специфическое связывание лиганда с рецептором определяют как различие между общим и неспецифическим связыванием, определенным в присутствии избытка немеченного лиганда. Соединения проверяли в концентрации 110-6 М, и подсчет сцинтилляции осуществляли способом детекции связывания лиганда. Условия и методология (со ссылкой на литературу) тестов in vitro приведены в табл. 1, результаты тестов для репрезентативных соединений приведены в табл. 2 (допаминергический рецептор D2), в табл. 3 (допаминергический рецептор D3), в табл. 4 (серотонинергические рецепторы 5-НТ 1 А и 5-НТ 2 А), в табл. 5 (серотонинергические рецепторы 5-НТ 6 и 5-НТ 7), в табл. 6 (рецептор транспортера серотонина (SERT, в табл. 7 (сигма-рецептор ), в табл. 8 (адренергический 1 рецептор), в табл. 9 (адренергический 2 С рецептор), в табл. 10 (гистаминергический H1 рецептор), в табл. 11 (мускариновый M3 рецептор) и в табл. 12 (серотонинергический 5-НТ 2 С рецептор). Таблица 1 Условия и методология тестов in vitro проверки на связывание Таблица 2 Результаты теста на сродство репрезентативных соединений к допаминергическому рецептору D2 Таблица 3 Результаты теста на сродство репрезентативных соединений к допаминергическому рецептору D3 Таблица 4 Результаты теста на сродство репрезентативных соединений к серотонинергическим рецепторам 5-НТ 1 А и 5-НТ 2 А Таблица 5 Результаты теста на сродство репрезентативных соединений к серотонинергическим рецепторам 5-НТ 6 и 5-НТ 7 Таблица 6 Результаты теста на сродство репрезентативных соединений к рецептору транспортера серотонина (SERT) Таблица 7 Результаты теста на сродство репрезентативных соединений к сигма-рецептору Таблица 8 Результаты теста на сродство репрезентативных соединений к адренергическому 1 рецептору Таблица 9 Результаты теста на сродство репрезентативных соединений к адренергическому 2 С рецептору Таблица 10 Результаты теста на сродство репрезентативных соединений к гистаминергическому H1 рецептору Таблица 11 Результаты теста на сродство репрезентативных соединений к мускариновому M3 рецептору Таблица 12 Результаты теста на сродство репрезентативных соединений к серотонинергическому 5-НТ 2 С рецептору
МПК / Метки
МПК: A61P 25/00, C07D 209/40, C07D 413/12, C07D 319/20, A61K 31/496, C07D 275/04, C07D 235/30
Метки: цнс, лечения, арилсульфонамиды, заболеваний
Код ссылки
<a href="https://eas.patents.su/30-22776-arilsulfonamidy-dlya-lecheniya-zabolevanijj-cns.html" rel="bookmark" title="База патентов Евразийского Союза">Арилсульфонамиды для лечения заболеваний цнс</a>
Предыдущий патент: Устойчивый к смещению микроэлектрод, пучок микроэлектродов и массив микроэлектродов для имплантации в мягкую ткань человека или животного
Следующий патент: Аэрированная шоколадная композиция и ее получение
Случайный патент: Анкер для крепления облицовочной стены к блокам из ячеистого бетона