Циклические аналоги 4-амино-4-оксобутаноил пептидов, ингибиторы репликации вирусов
Номер патента: 21794
Опубликовано: 30.09.2015
Авторы: Ванг Ксиангчжу, Чэн Давэй, Дешпенде Майлинд, Ли Шоуминг, Агарвал Атул, Фадке Авинаш, Гадхачанда Венкат, Пейс Гудвин, Лиу Куиксиан, Хасимото Акихиро, Чжанг Суоминг
Формула / Реферат
1. Соединение формулы
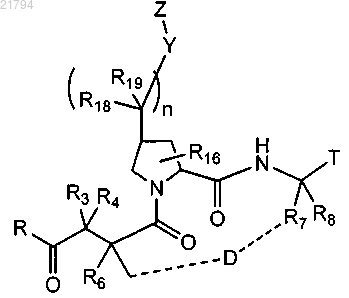
или его фармацевтически приемлемая соль,
где R представляет собой -COOH или C1-C6-алкилэфир либо -NR1R2;
R1 представляет собой C1-C6-алкил или C3-C7-циклоалкил;
R2 представляет собой водород; или
R1 и R2 объединяются с образованием 4-7-членного гетероциклоалкильного кольца, содержащего 0-2 дополнительных гетероатома, независимо выбранных из N, О и S, причем кольцо является необязательно конденсированным с 5- или 6-членным гетероциклическим кольцом, содержащим 1 или 2 гетероатома, независимо выбранных из N, О и S, или 5- или 6-членным карбоциклическим кольцом с образованием бициклической кольцевой системы, каждый из которых (5-7-членное гетероциклоалкильное кольцо или бициклическая кольцевая система) является необязательно замещенным;
R1 и R2, взятые вместе, образуют необязательно замещенное 5-9-членное мостиковое гетероциклическое кольцо, содержащее 0, 1 или 2 дополнительных атома N, S или О, или необязательно замещенное 5-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-7-членным карбоциклическим или гетероциклическим кольцом с образованием бициклической кольцевой системы, которая является мостиковой; или
R1 и R2, взятые вместе, образуют необязательно замещенное 4-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-9-членным мостиковым карбоциклическим или гетероциклическим кольцом; или
R3, R4 и R8 представляют собой независимо:
(a) водород, галоген или аминогруппу, или
(b) C1-C6-алкил, C2-C6-алкенил, (C3-C7-циклоалкил)C0-C4-алкил, (арил)C0-C4-алкил, (гетероарил)C0-C4-алкил, (C3-C7-циклоалкенил)C0-C4-алкил, (гетероциклоалкил)C0-C4-алкил, C2-C6-алканоил или моно- или ди-C1-C6-алкиламиногруппу, каждый из которых является необязательно замещенным; или
R6 представляет собой водород, C1-C6-алкил или (C3-C7-циклоалкил)C0-C2-алкил;
D представляет собой C7-C11 насыщенную или ненасыщенную углеводородную цепь, которая является (i) ковалентно связанной с R7, где R7 представляет собой метиленовую или метановую группу, или D представляет собой C7-C11 насыщенную или ненасыщенную углеводородную цепь, которая является (ii) ковалентно связанной с необязательно замещенным циклоалкильным кольцом, образованным R7 и R8, когда они объединяются с образованием 3-7-членного необязательно замещенного циклоалкильного кольца;
Т представляет собой группу формулы 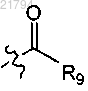
R9 представляет собой гидроксил, аминогруппу, -COOH, -NR10R11, -OR12, -SR12, -NR10(S=O)R11, -NR10SO2R11, -NR10SONR11R12, -NR10SO2NR11R12, -(C=O)OR10, -NR10(C=O)OR11 или -CONR10R11 или
R9 представляет собой C1-C6-алкил, C2-C6-алкенил, C2-C6-алканоил, (C3-C7-циклоалкил)С0-С4-алкил, (C3-C7-циклоалкенил)C0-C4-алкил, (C3-C7-циклоалкил)CH2SO2-, (С3-C7-циклоалкил)CH2SO2NR10-, (гетероциклоалкил)C0-C4-алкил, (арил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2-алкил, каждый из которых необязательно является замещенным; или
R10, R11 и R12 представляют собой в каждом случае водород или трифторметил либо C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, (арил)C0-C2-алкил, (C3-C7-циклоалкил)C0-C2-алкил, (C3-C7-циклоалкенил)C0-C2-алкил, (гетероциклоалкил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2-алкил, каждый из которых необязательно является замещенным;
n представляет собой 0, 1 или 2;
Y представляет собой О, -О(С=О)- или -(NR20)(C=O)-;
R16 представляет 0-4 заместителя, которые являются независимо выбранными из галогена, C1-C2-алкила и C1-C2-алкоксигруппы;
R18 и R19 представляют собой независимо водород, гидроксил, галоген, C1-C2-алкил, C1-С2-алкоксигруппу, C1-C2-галоалкил или C1-C2-галоалкоксигруппу;
R20 представляет собой водород, C1-C2-алкил, C1-C2-галоалкил или C1-С2-галоалкоксигруппу;
Z представляет собой хинолин формулы
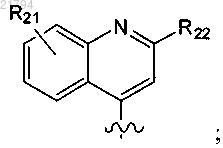
R21 представляет собой заместитель в положении 7 хинолина и 0-2 дополнительных заместителя, независимо выбранных из галогена, гидроксила, аминогруппы, цианогруппы, -CONH2, -COOH, C1-C4-алкила, C2-C4-алканоила, C1-C4-алкоксигруппы, моно- и ди-C1-C4-алкиламиногруппы, C1-C2-галоалкила и C1-C2-галоалкоксигруппы;
R22 представляет собой тиазолил, который является замещенным 0, 1 или 2 заместителями, независимо выбранными из галогена, гидроксила, аминогруппы, цианогруппы, -COOH, -CONH2, C1-C4-алкила, C1-C4-алкоксигруппы, моно- и ди-C1-C4-алкиламиногруппы, трифторметила и трифторметоксигруппы, где термин "замещенный" означает, что любой один или более водородов на обозначенном атоме или группе замещается с использованием выбора из указанной группы при условии, что нормальная валентность обозначенного атома не превышается, указанная группа включает галоген; цианогруппу; гидроксил; нитрогруппу; азидогруппу; алканоил; карбоксамидогруппу; алкильную или циклоалкильную группы, имеющие примерно 1-8 атомов углерода; алкенильную и алкинильную группы, имеющие одну или более ненасыщенных связей и примерно 2-8 атомов углерода; алкоксигруппу, имеющую одну или более кислородных связей и примерно 1-8 атомов углерода; арилоксигруппу; алкилтиогруппу, имеющую одну или более тиоэфирных связей и примерно 1-8 атомов углерода; алкилсульфинильную группу, имеющую одну или более сульфинильных связей и примерно 1-8 атомов углерода; алкилсульфонильную группу, имеющую одну или более сульфонильных связей и примерно 1-8 атомов углерода; аминоалкильную группу, имеющую один или более атомов N и примерно 1-8 атомов углерода; арил, имеющий 6 или более углеродов и одно или более колец; арилалкил, имеющий 1-3 отдельных или конденсированных колец и примерно 6-18 атомов углерода в кольце; арилалкоксигруппу, имеющую 1-3 отдельных или конденсированных колец и примерно 6-18 атомов углерода в кольце; или насыщенную, ненасыщенную или ароматическую гетероциклическую группу, имеющую 1-3 отдельных или конденсированных колец примерно с 3-8 членами на кольцо и одним или более атомами N, О или S, где гетероциклическая группа может быть дополнительно замещенной гидроксигруппой, алкилом, алкоксигруппой, галогеном и аминогруппой.
2. Соединение или его соль по п.1, где R1 и R2 объединяются с образованием пирролидинового, морфолинового, пиперидинового или пиперазинового кольца, каждое из которых является замещенным 0-2 заместителями, независимо выбранными из фтора, аминогруппы, гидроксила, метила и трифторметила.
3. Соединение или его соль по п.1, где R1 и R2, взятые вместе, образуют группы формул:
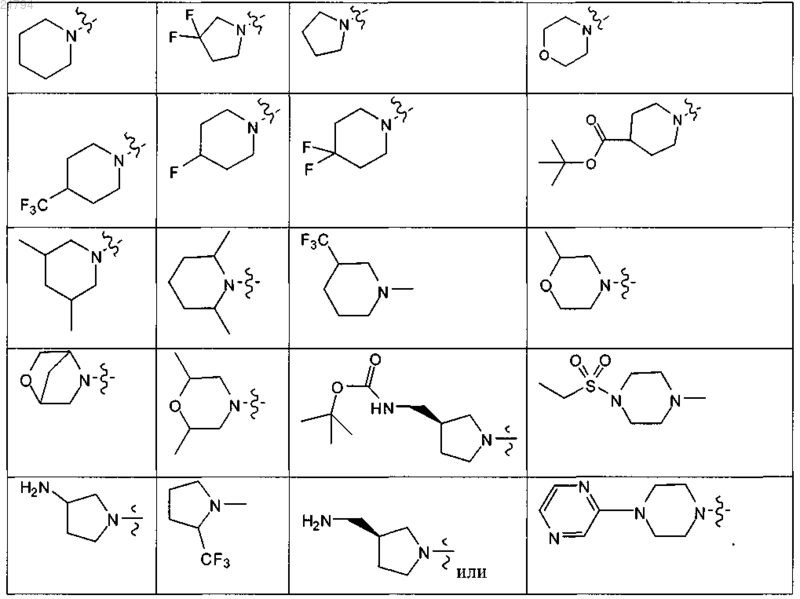
4. Соединение или его соль по п.2, где R3 представляет собой водород или метил и R4 представляет собой водород или C1-C4-алкил.
5. Соединение или его соль по п.4, где R3 и R4 представляют собой независимо водород или метил.
6. Соединение или его соль по п.5 формулы
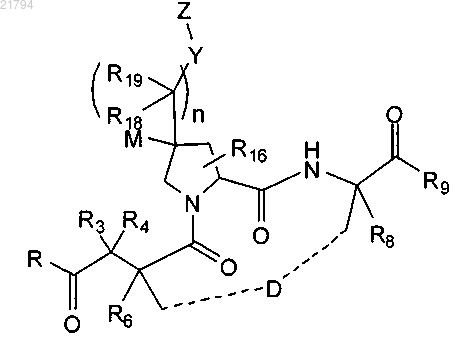
где D представляет собой алкильную или алкенильную группу, имеющую 6-10 атомов углерода; и
R3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил.
7. Соединение или его соль по п.6 формулы
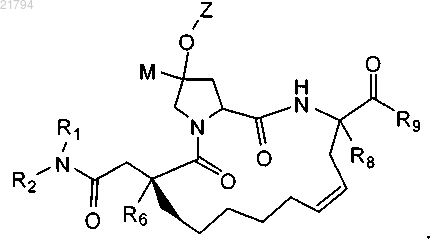
8. Соединение или его соль по п.5 формулы
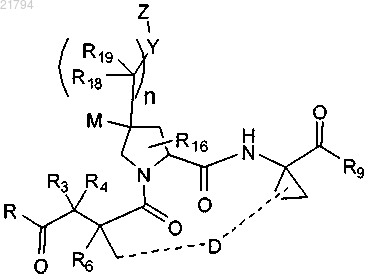
где D представляет собой алкильную или алкенильную группу, имеющую 6-10 атомов углерода; и
R3, R4 и R6 представляют собой независимо водород или C1-C4-алкил.
9. Соединение или его соль по п.8 формулы
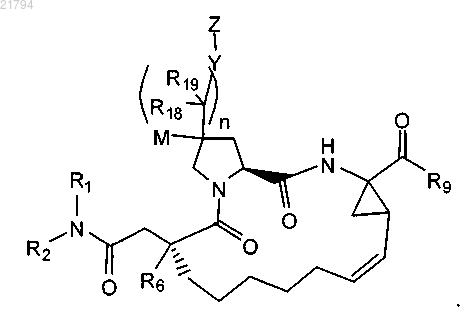
10. Соединение или его соль по п.2, в котором
Т представляет собой группу формулы 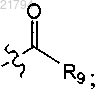
R9 представляет собой гидроксил, -OR12 или -NR10SO2R11;
R11 представляет собой C1-C4-алкил, C3-C6-циклоалкил, фенил или бензил, каждый из которых является замещенным 0-2 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы, C2-C4-алкенила и (фенил)C0-C2-алкила;
R12 представляет собой C1-C4-алкил.
11. Соединение или его соль по п.10, в котором
R10 представляет собой водород или метил;
R11 представляет собой C1-C4-алкил или циклопропил;
R12 представляет собой C1-C4-алкил.
12. Соединение или его соль по п.2, в котором
n представляет собой 0;
Y представляет собой О, -О(С=О)- или
Y представляет собой -(NR20)(C=O)-;
R20 представляет собой водород или метил.
13. Соединение или его соль по п.2, в котором Z представляет собой
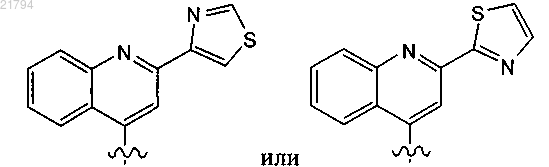
каждый из которых является замещенным 0, 1, 2 или 3 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы и моно- и ди-C1-C4-алкиламиногруппы.
14. Соединение или его соль по п.1, где
R21 представляет собой метокси- или этоксигруппу в положении 7 хинолина и необязательно дополнительный галоген в положении 8 хинолина;
R22 представляет собой тиазолил, который является замещенным 0, 1 или 2 заместителями, независимо выбранными из метила, метоксигруппы, хлора, C1-C4-алкила, C1-C4-моно- и диалкиламиногруппы.
15. Соединение или его соль по п.1 формулы
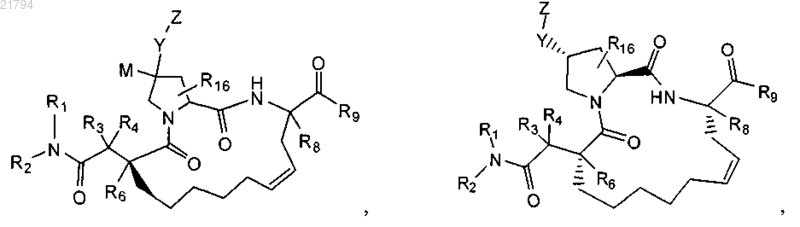
или
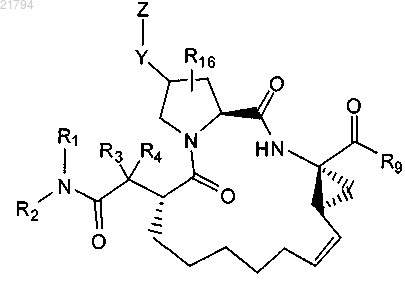
где R1 и R2 объединяются с образованием азетидинового, пирролидинового, морфолинового, пиперидинового или пиперазинового кольца, каждое из которых является замещенным 0-3 заместителями, независимо выбранными из фтора, аминогруппы, гидроксила, C1-С2-алкила и трифторметила, а также замещенным 0 или 1 заместителем, выбранным из метоксииминогруппы, аминоС1-С4-алкила, C1-C2-алкилсульфонила и пиразинила;
R3 представляет собой водород;
R4 представляет собой водород, C1-C4-алкил или (C3-C7-циклоалкил)C0-C2-алкил;
R6 и R8 представляют собой независимо водород или метил;
Т представляет собой группу формулы
R9 представляет собой гидроксил, -OR12 или -NR10SO2R11;
R10 представляет собой водород или метил;
R11 представляет собой C1-C4-алкил или C3-C7-циклоалкил;
R12 представляет собой C1-C4-алкил;
R16 представляет собой 0-2 заместителя, независимо выбранных из галогена, C1-C2-алкила и C1-C2-алкоксигруппы;
М представляет собой водород или метил;
Y представляет собой О, -О(С=О)- или -(NH)(C=O)-;
Z представляет собой группу формулы
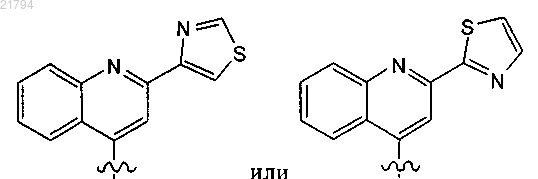
каждая из которых является замещенной 0, 1, 2 или 3 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы и моно- и ди-C1-C4-алкиламиногруппы.
16. Фармацевтическая композиция, содержащая терапевтически эффективное количество одного или более соединений или его солей по п.15 и по меньшей мере один фармацевтически приемлемый носитель.
17. Способ лечения инфекции гепатита C у пациента, включающий предоставление терапевтически эффективного количества одного или более соединений по п.15 пациенту.
18. Соединение или его соль по п.15, где Z представляет собой группу формулы
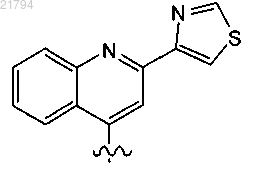
которая является замещенной 0, 1, 2 или 3 заместителями, независимо выбранными из галогена,
C1-C4-алкила, C1-C4-алкоксигруппы и моно- и ди-C1-C4-алкиламиногруппы.
19. Соединение или его соль по п.1, где соединение представляет собой
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-2-(2-(4-изопропилтиазол-2-ил)-7-метоксихинолин-4-илокси)-5,16-диоксо-6-(2-оксо-2-(пиперидин-1-ил)этил)-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4] диазациклопентадецин-14а-карбоксамид;
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-2-(2-(4-изопропилтиазол-2-ил)-7-метоксихинолин-4-илокси)-5,16-диоксо-6-(2-оксо-2-(4-(трифторметил)пиперидин-1-ил)этил)-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
(2R,6R,13aS,16aS,Z)-N-(циклопропилсульфонил)-2-(2-(2-(изопропиламино)тиазол-4-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-6-(2-оксо-2-(4-(трифторметил)пиперидин-1-ил)этил)-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-2-(2-(4-изопропилтиазол-2-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-6-(2-оксо-2-(4-(трифторметил)пиперидин-1-ил)этил)-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
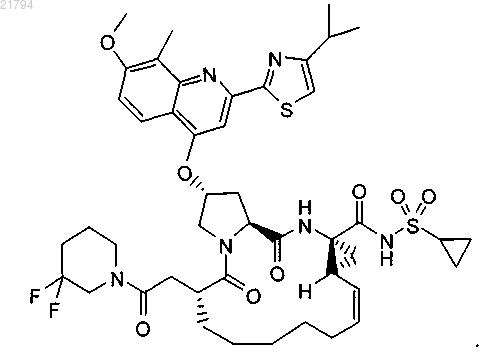
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-6-(2-(3,3-дифторпиперидин-1-ил)-2-оксоэтил)-2-(2-(4-изопропилтиазол-2-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-6-(2-(3,3-дифторпиперидин-1-ил)-2-оксоэтил)-2-(2-(2-изопропилтиазол-4-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-6-(2-(3,3-дифторциклогексил)-2-оксоэтил)-2-(2-(2-(изопропиламино)тиазол-4-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид;
(2R,6R,14aR,16aS,Z)-N-(циклопропилсульфонил)-2-(2-(4-изопропилтиазол-2-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-6-(2-оксо-2-(пиперидин-1-ил)этил)-1,2,3,5,6,7,8,9,10,11,13а, 14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид или
(2R,6R,13aS,16aS,Z)-N-(циклопропилсульфонил)-6-(2-(3-фторпиперидин-1-ил)-2-оксоэтил)-2-(2-(4-изопропилтиазол-2-ил)-7-метокси-8-метилхинолин-4-илокси)-5,16-диоксо-1,2,3,5,6,7,8,9,10,11,13а,14,14а,15,16,16а-гексадекагидроциклопропа[е]пирроло[1,2-а][1,4]диазациклопентадецин-14а-карбоксамид.
20. Соединение или его соль по п.1 формулы
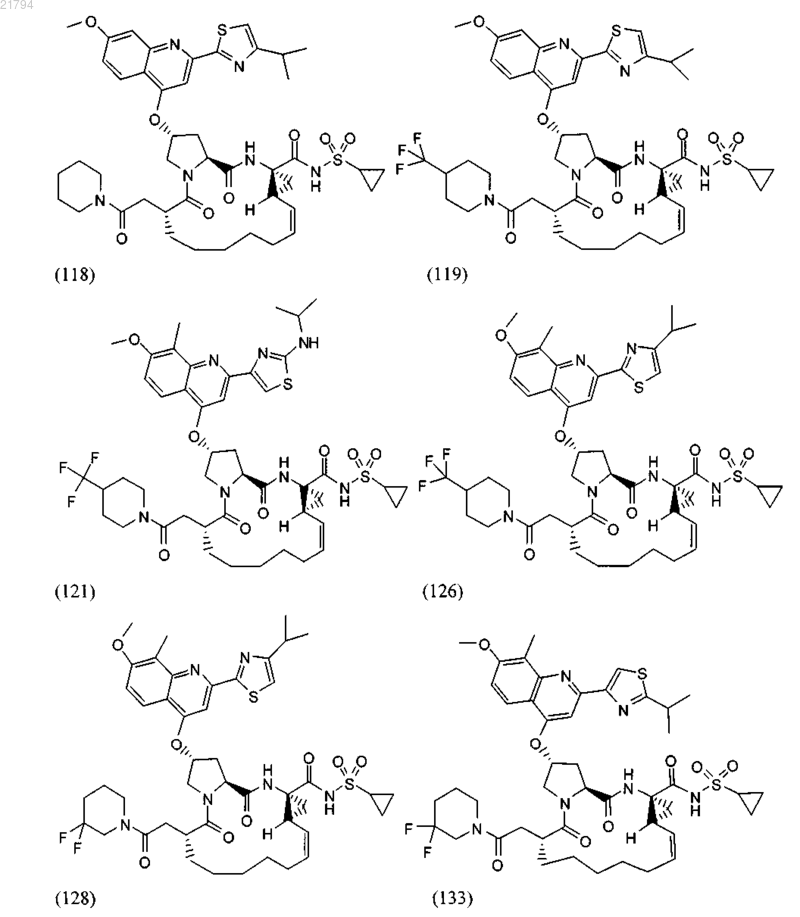
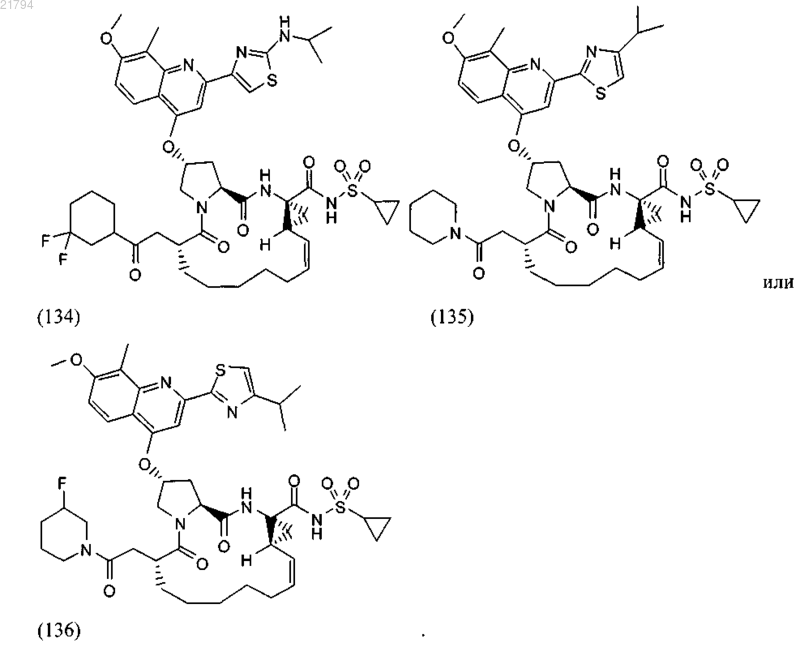
21. Соединение или его соль по п.1, где соединение представляет собой
Текст
ЦИКЛИЧЕСКИЕ АНАЛОГИ 4-АМИНО-4-ОКСОБУТАНОИЛ ПЕПТИДОВ,ИНГИБИТОРЫ РЕПЛИКАЦИИ ВИРУСОВ Гадхачанда Венкат, Чэн Давэй,Агарвал Атул, Чжанг Суоминг, Лиу Куиксиан, Ли Шоуминг, Дешпенде Майлинд (US) Изобретение предоставляет 4-амино-4-оксобутаноил пептиды и их циклические аналоги формулы I Фадке Авинаш, Ванг Ксиангчжу,Пейс Гудвин, Хасимото Акихиро, и их фармацевтически приемлемые соли. Переменные определяются в описании. Некоторые соединения формулы I являются пригодными в качестве противовирусных средств. Такие циклические аналоги 4-амино-4-оксобутаноил пептидов, как раскрытые в описании, являются эффективными и/или селективными ингибиторами репликации вирусов, в частности репликации вируса гепатита С. Изобретение также предоставляет фармацевтические композиции, содержащие один или более циклических аналогов 4-амино-4-оксобутаноил пептидов и один или более фармацевтически приемлемых носителей. Такие фармацевтические композиции могут содержать циклический аналог 4-амино-4-оксобутаноил пептидов как единственное активное вещество или могут содержать комбинацию циклического аналога 4-амино-4-оксобутаноил пептидов и одного или более других фармацевтически активных веществ. Изобретение также предоставляет способы лечения вирусных инфекций у пациентов, включая инфекции вирусом гепатита С. Перекрестные ссылки на родственные заявки Заявка на данное изобретение утверждает приоритет предварительной патентной заявки США 61/121378, зарегистрированной 10 декабря 2008 г., и 61/226317, зарегистрированной 17 июля 2009 г.,обе полностью включены в описание путем отсылки. Область техники, к которой относится изобретение Настоящее изобретение предоставляет циклические аналоги 4-амино-4-оксобутаноил пептидов, пригодные в качестве противовирусных средств. Некоторые циклические аналоги 4-амино-4-оксобутаноил пептидов, раскрытые в описании, являются эффективными и/или селективными ингибиторами репликации вирусов, в частности репликации вируса гепатита C. Изобретение также предоставляет фармацевтические композиции, содержащие один или более циклических аналогов 4-амино-4-оксобутаноил пептидов и один или более фармацевтически приемлемых носителей. Такие фармацевтические композиции могут содержать циклический аналог 4-амино-4-оксобутаноил пептида как единственное активное вещество или могут содержать комбинацию циклического аналога 4-амино-4-оксобутаноил пептида и одного или более других фармацевтически активных веществ. Изобретение также предоставляет способы лечения вирусных инфекций, включая инфекции вируса гепатита C. Предшествующий уровень техники По оценкам, 3% населения в мире инфицировано вирусом гепатита C. Из тех кто подвергался воздействию HCV, 80-85% становятся хронически инфицированными, по меньшей мере у 30% развивается цирроз печени и у 1-4% развивается гепатоциллюлярная карцинома. Вирус гепатита C (HCV) является одной из наиболее распространенных причин хронической болезни печени в Соединенных Штатах Америки, которые, по имеющимся данным, обусловливают примерно 15% острых вирусных гепатитов,60-70% хронического гепатита и до 50% цирроза, конечной стадии болезни печени и рака печени. Хроническая инфекция HCV является наиболее частой причиной трансплантации печени в США, Австралии и большей части Европы. В Соединенных Штатах Америки гепатит C вызывает приблизительно от 10000 до 12000 смертей ежегодно. Наряду с тем, что острая фаза HCV инфекции обычно связана со слабовыраженными симптомами, опыт показывает, что примерно только 15-20% инфицированных людей спонтанно освобождаются от HCV.HCV представляет собой вирус в оболочке с одноцепочечной РНК, который содержит позитивную цепь генома около 9,6 килобаз. HCV является членом рода Hepacivirus семейства Flaviviridae. Были охарактеризованы по меньшей мере 4 штамма HCV (GT-1-GT-4). Жизненный цикл HCV включает вхождение в клетки хозяина; трансляцию HCV генома, процессинг полипротеинов и сборку комплекса репликазы; репликацию РНК, сборку вирионов и высвобождение. Трансляция РНК-генома HCV дает полипротеин длиной больше чем 3000 аминокислот, который расщепляется по меньшей мере двумя клеточными и двумя вирусными протеазами. Полипротеин HCV представляет собой NH2-C-E1-E2-p7-NS2-NS3-NS4A-NS4B-NS5A-NS5B-COOH. Как сообщалось, клеточная сигнальная пептидаза и сигнальная пептидпептидаза являются ответственными за отщепление N-концевой трети полипротеина (С-Е 1-Е 2-р 7) от неструктурных протеиновNS2-NS3. Затем протеаза NS3-NS4A опосредует второе цис-расщепление в месте соединения NS3-NS4A. Затем комплекс NS3-NS4A расщепляется в трех нижележащих сайтах для отделения оставшихся неструктурных протеинов. Утверждается, что правильный процессинг полипротеина необходим для формирования активного комплекса репликазы HCV. Как только полипротеин расщепился, собирается комплекс репликазы, содержащий, по меньшей мере, NS3-NS5B неструктурные протеины. Комплекс репликазы является цитоплазматическим и мембраносвязанным. Основные виды ферментативной активности комплекса репликазы включают серинпротеазную активность и геликазную активность НТФазы (нуклеозидтрифосфатазы) в NS3 и РНК-зависимую РНК-полимеразную активность NS5B. В процессе репликации РНК производится комплементарная негативная копия геномной РНК. Копия негативной нити используется как матрица для синтеза дополнительных позитивных нитей геномных РНК, которые могут участвовать в трансляции,репликации, упаковке или любой их комбинации для получения вирусного потомства. Сборка функционального комплекса репликазы была описана как составная часть механизма репликации HCV. Предварительная заявка 60/669,872 "Pharmaceutical Compositions and Methods of Inhibiting HCV Replication", зарегистрированная 11 апреля 2005 г., полностью включается путем отсылки в отношении раскрытия, связанного со сборкой комплекса репликазы. Современное лечение инфекции вирусом гепатита C обычно включает введение интерферона, такого как пегилированный интерферон (IFN), в комбинации с рибавирином. Успех современных методов лечения, который определяется устойчивым вирусологическим ответом (SVR), зависит от штамма HCV,которым инфицирован пациент, и строгого соблюдения пациентом лечебного режима. Только 50% пациентов, зараженных штаммом GT-1 вируса HCV, демонстрируют устойчивый вирусологический ответ. Противовирусные препараты прямого действия для лечения хронического HCV, такие как ACH-806,VX-950 и NM 283 (пролекарство NM 107), проходят клинические испытания. Из-за отсутствия эффективных способов лечения определенных штаммов HCV и высокой скорости мутации HCV необходимы новые способы лечения. Настоящее изобретение удовлетворяет эту потребность и предоставляет дополнительные преимущества, которые здесь описываются. Сущность изобретения Изобретение предоставляет соединения формулы I (показанной ниже) и включает 4-амино-4-оксобутаноил пептиды и их циклические аналоги. 4-Амино-4-оксобутаноил пептиды и их циклические аналоги формулы I, раскрытые в описании, обладают противовирусной активностью. Изобретение предоставляет соединения формулы I, которые являются эффективными и/или селективными ингибиторами репликации вируса гепатита C. Изобретение также предоставляет фармацевтические композиции, содержащие одно или более соединений формулы I или соль, сольват или ацилированное пролекарство таких соединений и один или более фармацевтически приемлемых носителей. Изобретение дополнительно включает способы лечения пациентов, страдающих от некоторых инфекционных болезней, путем предоставления таким пациентам эффективного количества соединения формулы I для уменьшения признаков или симптомов болезни или расстройства. Эти инфекционные болезни включают вирусные инфекции, в частности инфекции вирусом HCV. В частности, изобретение включает способы лечения людей, страдающих от инфекционной болезни, а также включает способы лечения других животных, в том числе сельскохозяйственных животных и домашних животных, страдающих от инфекционной болезни. Способы лечения включают предоставление соединения формулы I как единственного активного вещества или предоставление соединения формулы I в комбинации с одним или более другими терапевтическими средствами. Таким образом, в первом аспекте изобретение включает соединения формулы I и его фармацевтически приемлемые соли:R1 и R2 объединяются с образованием 4-7-членного гетероциклоалкильного кольца, содержащего от 0 до 2 дополнительных гетероатомов, независимо выбранных из N, О и S, причем кольцо является необязательно конденсированным с 5- или 6-членным гетероциклическим кольцом, содержащим 1 или 2 гетероатома, независимо выбранных из N, О и S, или 5- или 6-членным карбоциклическим кольцом с образованием бициклической кольцевой системы, каждый из которых (5-7-членное гетероциклоалкильное кольцо или бициклическая кольцевая система) является необязательно замещенным;R1 и R2, взятые вместе, образуют необязательно замещенное 5-9-членное мостиковое гетероциклическое кольцо, содержащее 0, 1 или 2 дополнительных атома N, S или О, или необязательно замещенное 5-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-7-членным карбоциклическим или гетероциклическим кольцом с образованием бициклической кольцевой системы, которая является мостиковой; илиR1 и R2, взятые вместе, образуют необязательно замещенное 4-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-9-членным мостиковым карбоциклическим или гетероциклическим кольцом;(a) водород, галоген или аминогруппу илиC1-C6-алкил,C2-C6-алкенил,(C3-C7-циклоалкил)C0-C4-алкил,(арил)C0-C4-алкил,(гетероарил)C0-C4-алкил,(C3-C7-циклоалкенил)C0-C4-алкил,(гетероциклоалкил)C0-C4-алкил,C2-C6-алканоил или моно- или ди-C1-C6-алкиламиногруппу, каждый из которых является необязательно замещенным;D представляет собой C7-C11 насыщенную или ненасыщенную углеводородную цепь, которая является (i) ковалентно связанной с R7, где R7 представляет собой метиленовую или метиновую группу, или(ii) ковалентно связанной с необязательно замещенным циклоалкильным кольцом, образованным R7 и R8,когда они объединяются с образованием 3-7-членного необязательно замещенного циклоалкильного кольца; Т представляет собой группу формулыR9 представляет собой C1-C6-алкил, C2-C6-алкенил, C2-C6-алканоил, (C3-C7-циклоалкил)C0-C4-алкил,(C3-C7-циклоалкенил)C0-C4-алкил, (C3-C7-циклоалкил)CH2SO2-, (C3-C7-циклоалкил)CH2SO2NR10-, (гетероциклоалкил)C0-C4-алкил, (арил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2-алкил, каждый из которых необязательно является замещенным;R10, R11 и R12 представляют собой в каждом случае водород или трифторметил илиC1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, (арил)C0-C2-алкил, (C3-C7-циклоалкил)C0-C2-алкил,(C3-C7-циклоалкенил)C0-C2-алкил, (гетероциклоалкил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2 алкил, каждый из которых необязательно является замещенным;R16 представляет от 0 до 4 заместителей, которые являются независимо выбранными из галогена,C1-C2-алкила и C1-C2-алкоксигруппы;R18 и R19 представляют собой независимо водород, гидроксил, галоген, C1-C2-алкил,C1-C2-алкоксигруппу, C1-C2-галоалкил или C1-C2-галоалкоксигруппу;Z представляет собой хинолин формулыR22 представляет собой тиазолил, который является замещенным 0, 1 или 2 заместителями, независимо выбранными из галогена, гидроксила, аминогруппы, цианогруппы, -COOH, -CONH2, C1-C4-алкила,C1-C4-алкоксигруппы, моно- и ди-C1-C4-алкиламиногруппы, трифторметила и трифторметоксигруппы,где термин "замещенный" означает, что любой один или более водородов на обозначенном атоме или группе замещается с использованием выбора из указанной группы при условии, что нормальная валентность обозначенного атома не превышается, и указанная группа включает галоген; цианогруппу; гидроксил; нитрогруппу; азидогруппу; алканоил; карбоксамидогруппу; алкильную или циклоалкильную группы, имеющие примерно 1-8 атомов углерода; алкенильную и алкинильную группы, имеющие одну или более ненасыщенных связей и примерно 2-8 атомов углерода; алкоксигруппу, имеющую одну или более кислородных связей и примерно 1-8 атомов углерода; арилоксигруппу; алкилтиогруппу, имеющую одну или более тиоэфирных связей и примерно 1-8 атомов углерода; алкилсульфинильную группу, имеющую одну или более сульфинильных связей и примерно 1-8 атомов углерода; алкилсульфонильную группу,имеющую одну или более сульфонильных связей и примерно 1-8 атомов углерода; аминоалкильную группу, имеющую один или более атомов N и примерно 1-8 атомов углерода; арил, имеющий 6 или более углеродов и одно или более колец; арилалкил, имеющий 1-3 отдельных или конденсированных кольца и примерно 6-18 атомов углерода в кольце; арилалкоксигруппу, имеющую 1-3 отдельных или конденсированных кольца и примерно 6-18 атомов углерода в кольце; или насыщенную, ненасыщенную или ароматическую гетероциклическую группу, имеющую 1-3 отдельных или конденсированных кольца примерно с 3-8 членами на кольцо и одним или более атомами N, О или S, где гетероциклическая группа может быть дополнительно замещенной гидроксигруппой, алкилом, алкоксигруппой, галогеном и аминогруппой. Некоторые соединения формулы I, раскрытые в описании, проявляют хорошую активность при анализе репликации HCV, таком как анализ репликона HCV, изложенный в примере 6. Предпочтительные соединения формулы I показывают ЕС 50 около 40 мкмоль или менее, или более предпочтительно ЕС 50 около 10 мкмоль или менее, или еще более предпочтительно ЕС 50 около 5 нмоль или менее при анализе репликации HCV-репликона. Осуществление изобретения Химическое описание и терминология. Перед началом подробного изложения изобретения может быть полезным предоставление определений некоторых терминов, использованных в описании. Соединения настоящего изобретения описываются с использованием стандартной номенклатуры. Если не определено иначе, все технические и научные термины, использованные в описании, имеют то же самое значение, которое обычно понятно специалисту в области техники, к которой относится данное изобретение. Если только явно не противопоказано контекстом, каждое название соединения включает форму свободной кислоты или свободного основания соединения, а также гидраты соединения и все фармацевтически приемлемые соли соединения. Термин "циклические аналоги 4-амино-4-оксобутаноил пептидов" включает все соединения, которые удовлетворяют формуле I, включая любые энантиомеры, рацематы и стереоизомеры, а также все фармацевтически приемлемые соли таких соединений. Фраза "соединение формулы I" включает все подгруппы формулы I, включая формулу IA, и формулII-VII, а также все формы таких соединений, включая соли и гидраты, только если это явно не противоречит контексту, в котором используется эта фраза. Термин "или" означает "и/или". Термины "содержащий", "имеющий", "включая" и "включающий" должны истолковываться как неограниченные термины (т.е. означающие "включая, но не ограничиваясь этим"). Перечисление пределов значений служит только как стенографический способ упоминания в отдельности каждого отдельного значения, попадающего в предел, если в описании не указано иначе, и каждое отдельное значение включается в подробное описание, как если бы значения были перечислены в описании по отдельности. Конечные точки всех пределов включаются в предел и независимо комбинируются. Все способы, описанные здесь, могут быть выполнены в подходящем порядке, если в описании не указано иначе или если только явно не противопоказано контекстом. Использование всех без исключения примеров или типичных выражений (например, "такой как") предназначается только для того, чтобы лучше иллюстрировать изобретение и не ставит ограничения на рамки изобретения, если не утверждается иначе. Никакая формулировка в подробном описании не должна истолковываться как указывающая на какой-либо незаявленный элемент, использованный здесь, как существенный для осуществления на практике изобретения. Если не определено иначе, технические и научные термины, использованные в описании, имеют то же самое значение, которое обычно понятно специалисту в области техники, к которой относится данное изобретение."Активное вещество" означает соединение (включая соединение изобретения), элемент или смесь,которые при введении пациенту, отдельно или в комбинации с другим соединением, элементом или смесью, оказывают, прямо или непрямо, физиологическое действие на пациента. Непрямое физиологическое действие может совершаться через метаболит или другой непрямой механизм. Когда активное вещество представляет собой соединение, тогда включаются соли, сольваты (включая гидраты) свободного соединения, кристаллические формы, некристаллические формы и любые полиморфы данного соединения. Соединения могут содержать один или более асимметричных элементов, таких как стереогенные центры,стереогенные оси и т.п., например асимметричные атомы углерода, так что соединения могут находиться в разных стереоизомерных формах. Эти соединения могут быть, например, рацематами или оптически активными формами. Что касается соединений с двумя или более асимметричными элементами, эти соединения дополнительно могут быть смесями диастереомеров. В отношении соединений, имеющих асимметричные центры, включаются все оптические изомеры в чистой форме и их смеси. Кроме того,соединения с углерод-углеродными двойными связями могут существовать в Z- и Е-формах при всех изомерных формах соединений. В этих ситуациях отдельные энантиомеры, т.е. оптически активные формы, могут быть получены с помощью асимметричного синтеза, синтеза из оптически чистых предшественников или путем разделения рацематов. Разделение рацематов также можно осуществить, например, при помощи обычных методов, таких как кристаллизация в присутствии разделяющего агента или хроматография с использованием, например, хиральной ВЭЖХ-колонки. В описании рассматриваются все формы, не принимая во внимание методы, использованные для их получения. Тире ("-"), располагающееся не между двумя буквами или символами, используется, чтобы показать точку прикрепления заместителя. Например, -(CH2)C3-C8-циклоалкил присоединяется через углерод метиленовой (CH2) группы."Алканоил" означает алкильную группу, как определено в описании, прикрепленную через кето(-(С=О)-)мостик. Алканоильные группы имеют указанное число атомов углерода, при этом углерод кетогруппы включается в пронумерованные атомы углерода. Например, С 2-алканоильная группа представляет собой ацетильную группу, имеющую формулу CH3(C=O)-. Связь, показанная комбинацией сплошной и пунктирной линий, т.е. может быть одинарной или двойной связью."Алкил" представляет собой насыщенную алифатическую углеводородную группу с разветвлнной или прямой цепью, которая имеет определенное число атомов углерода, в основном примерно от 1 до 12 атомов углерода. Термин "C1-C6-алкил" при использовании в описании означает алкильную группу,-4 021794 имеющую 1, 2, 3, 4, 5 или 6 атомов углерода. Другие варианты осуществления включают алкильные группы, имеющие от 1 до 8 атомов углерода, от 1 до 4 атомов углерода или 1 или 2 атома углерода, например C1-C8-алкил, C1-C4-алкил и C1-C2-алкил. Когда в описании C0-Cn-алкил используется совместно с другой группой, например (арил)C0-C4-алкилом, указанная группа, в этом случае арил, является или прямо связанной с помощью одинарной ковалентной связи (С 0) или прикрепляется с помощью алкильной цепи, имеющей указанное число атомов углерода, в этом случае 1, 2, 3 или 4 атома углерода.(5-10-членным гетероарил)C0-C2-алкилом,(арил)C0-C2-алкилом,(фенил)C0-C2-алкилом, (C3-C7-циклоалкил)C0-C4-алкилом и (гетероциклоалкил)C0-C4-алкилом. Примеры алкила включают, но не ограничиваются этим, метил, этил, н-пропил, изопропил, н-бутил, 3-метилбутил,т-бутил, н-пентил и втор-пентил."Алкенил" означает прямую или разветвленную углеводородную цепь, содержащую одну или более ненасыщенных углерод-углеродных двойных связей, которые могут находиться в любой устойчивой точке вдоль цепи. Алкенильные группы, описанные здесь, имеют указанное число атомов углерода. Например, C2-C6-алкенил означает алкенильную группу из 2, 3, 4, 5 или 6 атомов углерода. Когда число атомов углерода не указано, алкенильные группы, описанные в документе, обычно имеют примерно от 2 до 12 атомов углерода, хотя предпочтительными являются низшие алкенильные группы, имеющие 8 или меньше атомов углерода. Примеры алкенильных групп включают этенильные, пропенильные и бутенильные группы."Алкоксигруппа" означает алкильную группу, как определено выше, с указанным числом атомов углерода, присоединенных через кислородный мостик (-О-). Примеры алкоксигруппы включают, но не ограничиваются этим, метокси, этокси, н-пропокси, и-пропокси, н-бутокси, 2-бутокси, т-бутокси,н-пентокси, 2-пентокси, 3-пентокси, изопентокси, неопентокси, н-гексокси, 2-гексокси, 3-гексокси и 3-метилпентокси группы. Когда "C0-Cn-алкоксигруппа" используется с другой группой, например (гетероарил)C0-C4-алкоксигруппой, указанная группа, в этом случае гетероарильная, прикрепляется или через ковалентно связанный кислородный мостик (С 0-алкоксигруппа), или с помощью алкоксигруппы, имеющей определенное число атомов углерода, в этом случае примерно от 1 до 4 атомов углерода, т.е. ковалентно связывается с группой, в которой она становится заместителем, через атом кислорода алкоксигруппы."Моно- и/или диалкилкарбамат" означает группы формулы (алкил 1)-O(C=O)NH- и(алкил 1)-О(С=О)N(алкил 2)-, в которых группы алкил 1 и алкил 2 являются независимо выбранными алкильными группами, как определяется выше, имеющими указанное число атомов углерода. Термин "алкилэфир" означает алкильную группу, как определено здесь, присоединенную через сложную эфирную связь. Сложная эфирная связь может находиться в любой ориентации, например,группа формулы -O(C=O)алкил или группа формулы -(C=O)O-алкил."Алкилоксим" представляет собой группу формулы -C=N-O-алкил, где алкильная группа представляет собой алкильную группу, как определено в описании, имеющую указанное число атомов углерода."Алкилсульфонил" представляет собой алкил-SO2-, и "алкилтио" представляет собой алкил-S-, где алкильная группа представляет собой алкильную группу, как определено в описании, имеющую указанное число атомов углерода. Точка прикрепления алкилсульфонильного или алкилтиозаместителя находится на атоме серы."Арил" означает ароматическую группу, содержащую только углерод в ароматическом кольце или кольцах. Такие ароматические группы могут быть дополнительно замещенными углеродом или неуглеродными атомами или группами. Типичные арильные группы содержат 1 или 2 отдельных, соединенных или пендантных колец и примерно от 6 до 12 кольцевых атомов, не считая гетероатомы в качестве членов кольца. Причем указанные арильные группы могут быть замещенными. Такое замещение может включать объединение с 5-7-членной насыщенной циклической группой, которая необязательно содержит 1 или 2 гетероатома, независимо выбранных из N, О и S, с образованием, например,3,4-метилендиоксифенильной группы. Арильные группы включают, например, фенил, нафтил, включая 1-нафтил и 2-нафтил, и бифенил. В термине "(арил)алкил" арил и алкил представляют собой, как определено выше, а точка прикрепления находится на алкильной группе. "(Арил)C0-C4-алкил" означает арильную группу, которая прямо присоединяется через одинарную ковалентную связь (арил)С 0-алкил или присоединяется через алкильную группу, имеющую примерно от 1 до 4 атомов углерода. Примеры (арил)алкильных групп включают пиперонильные и (фенил)алкильные группы, такие как бензил и фенилэтил. Подобным образом, термин"(арил)C0-C4-алкокси" означает арильную группу, которая прямо присоединяется к молекуле, в которой она становится заместителем, через кислородный мостик, например (арил)С 0-алкокси, или ковалентно связывается с алкоксигруппой, имеющей от 1 до 4 атомов углерода."Мостиковая" группа представляет собой кольцевую группу, обычно насыщенную, в которой два несмежных кольцевых атома являются ковалентно связанными той же самой связывающей группой. Связывающая группа представляет собой метилен, этилен или атом кислорода. Примеры мостиковых групп включают бицикло[2.2.1]гептан, 7-оксабицикло[2/2/1]гептан, бицикло[2.2.2]октан."Карбоциклическое кольцо" представляет собой насыщенную, ненасыщенную или ароматическую кольцевую группу, имеющую указанное число атомов углерода в кольце и имеющую только атомы углерода в кольце."Циклоалкил" представляет собой насыщенную углеводородную кольцевую группу, имеющую определенное число атомов углерода. Моноциклические циклоалкильные группы обычно имеют примерно от 3 до 8 кольцевых углеродных атомов или от 3 до 7 (3, 4, 5, 6 или 7) кольцевых углеродных атомов. Циклоалкильные заместители могут присоединяться через замещенный атом азота или углерода, или замещенный атом углерода, который может иметь два заместителя, может иметь циклоалкильную группу, которая присоединяется как спирогруппа. Примеры циклоалкильных групп включают циклопропильную, циклобутильную, циклопентильную или циклогексильную, а также мостиковые или каркасные(caged) насыщенные кольцевые группы, такие как норборнан или адамантан. Аналогично "циклоалкенил" представляет собой углеводородную кольцевую группу, имеющую указанное число атомов углерода и, по меньшей мере, углерод-углерод двойную связь между кольцевыми атомами углерода. Термин "(циклоалкил)C0-Cn-алкил" означает заместитель, в котором циклоалкил и алкил представляют собой, как определено в описании, а точка присоединения (циклоалкил)алкильной группы к молекуле, в которой она становится заместителем, является или одинарной ковалентной связью, (С 0-алкил) или находится на алкильной группе. (Циклоалкил)алкил включает, но не ограничивается этим, циклопропилметил, циклогексилметил и циклогексилметил."Галоалкил" означает алкильные группы с разветвленной и прямой цепью, имеющие определенное число атомов углерода, замещенных 1 или более атомами галогена, до предельно допустимого числа атомов галогена. Примеры галоалкила включают, но не ограничиваются этим, трифторметил, дифторметил, 2-фторэтил и пентафторэтил."Галоалкокси" указывает на галоалкильную группу, как определено в описании, присоединенную через кислородный мостик (кислород радикала спирта)."Гало" или "галоген" означает любой из числа фтора, хлора, брома и йода."Гетероарил" означает устойчивое моноциклическое ароматическое кольцо, имеющее указанное число кольцевых атомов, которое содержит от 1 до 3 или в некоторых вариантах осуществления от 1 до 2 гетероатомов, выбранных из N, О и S, при этом остальные атомы кольца являются углеродом, или устойчивую бициклическую или трициклическую систему, содержащую по меньшей мере одно 5-7-членное ароматическое кольцо, которое содержит от 1 до 3 или в некоторых вариантах осуществления от 1 до 2 гетероатомов, выбранных из N, О и S, при этом остальные атомы кольца являются углеродом. Моноциклические гетероарильные группы типично имеют от 5 до 7 атомов в кольце. В некоторых вариантах осуществления бициклические гетероарильные группы представляют собой 9-10-членные гетероарильные группы, т.е. группы, содержащие 9 или 10 кольцевых атомов, в которых одно 5-7-членное ароматическое кольцо объединяется со вторым ароматическим или неароматическим кольцом. Когда общее число атомов S и О в гетероарильной группе превышает 1, эти гетероатомы не располагаются рядом друг с другом. Предпочтительно, что общее число атомов S и О в гетероарильной группе составляет не более чем 2. Особенно предпочтительно, что общее число атомов S и О в ароматическом гетероцикле составляет не более чем 1. Примеры гетероарильных групп включают, но не ограничиваются этим, оксазолил, пиранил,пиразинил, пиразолопиримидинил, пиразолил, пиридизинил, пиридил, пиримидинил, пирролил, хинолинил, тетразолил, тиазолил, тиенилпиразолил, тиофенил, триазолил, бензо[d]оксазолил, бензофуранил,бензотиазолил, бензотиофенил, бензоксадиазолил, дигидробензодиоксинил, фуранил, имидазолил, индолил и изоксазолил."Гетероциклическое кольцо" представляет собой насыщенную, ненасыщенную или ароматическую кольцевую группу, имеющую по меньшей мере одно кольцо, содержащее гетероатом, выбранный из N, О и S, причем остальные атомы в кольце являются углеродом. Примеры гетероциклических колец включают пиридил, дигидропиридил, тетрагидропиридил (пиперидил), тиазолил, тетрагидротиофенил, окисленный по атому серы тетрагидротиофенил, пиримидинил, фуранил, тиенил, пирролил, пиразолил, имидазолил, тетразолил, бензофуранил, тианафталинил,индолил, индоленил, хинолинил, изохинолинил, бензимидазолил, пиперидинил, 4-пиперидонил, пирролидинил, 2-пирролидонил, пирролинил, тетрагидрофуранил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, октагидроизохинолинил, азоцинил, триазанил, 6 Н-1,2,5-тиадиазинил,2 Н,6 Н-1,5,2-дитиазинил, тиенил, тиантренил, пиранил, изобензофуранил, хроменил, ксантенил, феноксантинил, 2 Н-пирролил, изотиазолил, изоксазолил, пиразинил, пиридазинил, индолизинил, изоиндолил,3 Н-индолил, 1H-индазолил, пуринил, 4 Н-хинолизинил, фталазинил, нафтиридинил, квиноскалинил, квиназолинил, циннолинил, птеридинил, 4 аН-карбазолил, карбазолил, -карболинил, фенантридинил, акри-6 021794 динил, пиримидинил, фенантролинил, феназинил, фенотиазинил, фуразанил, феноксазинил, изохроманил, хроманил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперазинил, индолинил,изоиндолинил, квинуклидинил, морфолинил, оксазолидинил, бензатриазолил бензизоксазолил, оксиндолил, бензоксазолинил, изатиноил и бис-тетрагидрофуранил. Как пример и без ограничения этим, связанные с помощью углерода гетероциклические кольца присоединяются в положении 2, 3, 4, 5 или 6 пиридина, положении 3, 4, 5 или 6 пиридазина, положении 2, 4, 5 или 6 пиримидина, положении 2, 3, 5 или 6 пиразина, положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положении 2, 4 или 5 оксазола, имидазола или тиазола, положении 3, 4 или 5 изоксазола, пиразола или изотиазола, положении 2 или 3 азиридина,положении 2, 3 или 4 азетидина, положении 2, 3, 4, 5, 6, 7 или 8 хинолина или положении 1, 3, 4, 5, 6, 7 или 8 изохинолина. Гетероциклические кольца, соединенные углеродом, включают 2-пиридил,3-пиридил, 4-пиридил, 5-пиридил, 6-пиридил, 3-пиридазинил, 4-пиридазинил, 5-пиридазинил,6-пиридазанил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 6-пиримидинил, 2-пиразинил,3-пиразинил, 5-пиразинил, 6-пиразинил, 2-тиазолил, 4-тиазолил или 5-тиазолил. Как пример и без ограничения этим, связанные с помощью азота гетероциклические кольца присоединяются в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролин,имидазол, имидазолидин, 2-имидазолин, 3-имидазолин, пиразол, пиразолин, 2-пиразолин, 3-пиразолин,пиперидин, пиперазин, индол, индолин, 1 Н-индазол, положении 2 изоиндола, или изоиндолина, положении 4 морфолина и положении 9 карбазола или -карболина. Связанные с помощью азота гетероциклы включают 1-азиридил, 1-азетедил, 1-пирролил, 1-имидазолил, 1-пиразолил и 1-пиперидинил. Термин "гетероциклоалкил" означает насыщенную моноциклическую группу, имеющую указанное число кольцевых атомов и содержащую примерно от 1 до 3 гетероатомов, выбранных из N, О и S, при этом остальные атомы в кольце являются углеродом, или насыщенную бициклическую кольцевую систему, имеющую по меньшей мере один N, О или S атом в кольце, при этом остальные атомы в кольце являются углеродом. Моноциклические гетероциклоалкильные группы обычно имеют примерно от 4 до 8 атомов в кольце. В некоторых вариантах осуществления моноциклические гетероциклоалкильные группы имеют от 5 до 7 атомов в кольце. Бициклические гетероциклоалкильные группы обычно имеют примерно от 5 до 12 атомов в кольце. Примеры гетероциклоалкильных групп включают морфолинильные, пиперазинильные, пиперидинильные и пирролидинильные группы. Термин "(гетероциклоалкил)алкил" указывает на насыщенный заместитель, в котором гетероциклоалкил и алкил представляют собой, как определено в описании, а точка прикрепления (гетероциклоалкил)алкильной группы к молекуле, в которой она становится заместителем, находится на алкильной группе. Этот термин включает, но не ограничивается этим, пиперидилметил, пиперазинилметил и пирролидинилметил. Термин "моно- и/или диалкиламино" означает вторичные или третичные алкиламиногруппы, в которых алкильные группы являются независимо выбранными алкильными группами, как определено здесь, имеющими указанное число атомов углерода. Точка присоединения алкиламиногруппы находится на азоте. Примеры моно- и диалкиламиногруппвключают этиламиногруппу, диметиламиногруппу и метилпропиламиногруппу."Моно- и/или диалкилкарбоксамид" означает моноалкилкарбоксамидную группу формулы (алкил 1)NH-(C=O)- или диалкилкарбоксамидную группу формулы (алкил 1)(алкил 2)-N-(С=О)-, в которой точка присоединения моно- или диалкилкарбоксамидного заместителя к молекуле, в которой она становится заместителем, находится на углероде карбонильной группы. Термин "моно- и/или диалкилкарбоксамид" также включает группы формулы (алкил 1)(C=O)NH- и (алкил 1)(С=О)(алкил 2)N-, в которых точкой присоединения является атом азота. Группы алкил 1 и алкил 2 являются независимо выбранными алкильными группами, имеющими указанное число атомов углерода."Оксо" означает кетогруппу (С=О). Оксогруппа, которая является заместителем неароматического атома углерода, приводит к превращению -CH2- в -C(=O)-. Оксогруппа, которая является заместителем ароматического атома углерода, приводит к превращению -CH- в -C(=O)- и утрате ароматичности. Термин "замещенный", при использовании здесь, означает, что любой один или более водородов на обозначенном атоме или группе замещается с использованием выбора из указанной группы при условии,что нормальная валентность обозначенного атома не превышается. Когда заместитель представляет собой оксо (т.е. =O), тогда замещаются 2 водорода при данном атоме. Когда оксогруппа замещает ароматические фрагменты, соответствующее частично ненасыщенное кольцо замещает ароматическое кольцо. Например, пиридильная группа, замещенная оксогруппой, представляет собой пиридон. Комбинации заместителей и/или переменных допускаются, только если такие комбинации приводят к устойчивым соединениям или полезным синтетическим промежуточным соединениям. Устойчивое соединение или устойчивая структура означает соединение, которое является достаточно сильным, чтобы перенести выделение из реакционной смеси и последующее приготовление эффективного терапевтического средства. Если не указано иначе, заместители называются как находящиеся в основной структуре. Например,должно быть понятно, что, когда (циклоалкил)алкил числится в списке как возможный заместитель, точка присоединения этого заместителя к основной структуре находится на алкильном участке. Подходящие группы, которые могут быть в "замещенном" положении, включают, но не ограничиваются этим, например, галоген; цианогруппу; гидроксил; нитрогруппу; азидогруппу; алканоил (такой как, C2-C6-алканоильная группа, например ацил или т.п.); карбоксамидогруппу; алкильные группы(включая циклоалкильные группы), имеющие примерно от 1 до 8 атомов углерода или примерно от 1 до 6 атомов углерода; алкенильные и алкинильные группы, включая группы, имеющие одну или более ненасыщенных связей, и примерно от 2 до 8, или примерно от 2 до 6 атомов углерода; алкоксигруппы,имеющие одну или более кислородных связей и примерно от 1 до 8 или примерно от 1 до 6 атомов углерода; арилоксигруппу, такую как феноксигруппа; алкилтиогруппы, включая группы, имеющие одну или более тиоэфирных связей, и примерно от 1 до 8 атомов углерода или примерно от 1 до 6 атомов углерода; алкилсульфинильные группы, включая группы, имеющие одну или более сульфинильных связей, и от 1 до 8 атомов углерода или от 1 до 6 атомов углерода; алкилсульфонильные группы, включая группы,имеющие одну или более сульфонильных связей, и от 1 до 8 атомов углерода или от 1 до 6 атомов углерода; аминоалкильные группы, включая группы, имеющие один или более атомов N и примерно от 1 до 8 или примерно от 1 до 6 атомов углерода; арил, имеющий 6 или более углеродов и одно или более колец, (например, фенил, бифенил, нафтил или т.п., каждое кольцо или замещенное, или незамещенное ароматическое); арилалкил, имеющий от 1 до 3 отдельных или конденсированных колец и примерно от 6 до 18 атомов углерода в кольце, при этом бензил является примером арилалкильной группы; арилалкоксигруппу, имеющую от 1 до 3 отдельных или конденсированных колец и примерно от 6 до 18 атомов углерода в кольце, при этом бензилоксигруппа является примером арилалкоксигруппы; или насыщенную, ненасыщенную или ароматическую гетероциклическую группу, имеющую от 1 до 3 отдельных или конденсированных колец примерно с 3-8 членами на кольцо и одним или более атомами N, О или S, например кумаринил, хинолинил, изохинолинил, хиназолинил, пиридил, пиразинил, пиримидинил, фуранил, пирролил, тиенил, тиазолил, триазинил, оксазолил, изоксазолил, имидазолил, индолил,бензофуранил, бензотиазолил, тетрагидрофуранил, тетрагидропиранил, пиперидинил, морфолинил, пиперазинил и пирролидинил. Такие гетероциклические группы могут быть дополнительно замещенными,например, гидроксигруппой, алкилом, алкоксигруппой, галогеном и аминогруппой."Лекарственная форма" означает единицу введения активного вещества. Примеры лекарственных форм включают таблетки, капсулы, препараты для инъекций, суспензии, жидкости, эмульсии, кремы,мази, суппозитории, формы для ингаляции, чрескожные формы и т.п."Фармацевтические композиции" представляют собой композиции, содержащие по меньшей мере одно активное вещество, такое как соединение или его соль формулы I, и по меньшей мере одну иную субстанцию, такую как носитель. Фармацевтические композиции соответствуют стандартам GMP (надлежащая производственная практика) FDA США для лекарственных средств для человека и лекарственных средств, не имеющих отношения к человеку."Фармацевтически приемлемые соли" включают производные раскрытых соединений, в которых исходное соединение модифицировано путем создания их неорганических и органических, нетоксичных солей присоединения кислоты или основания. Соли настоящих соединений могут быть синтезированы из исходного соединения, которое содержит основной или кислый остаток, при помощи обычных химических методов. Как правило, такие соли можно получить при реагировании свободных кислых форм этих соединений со стехиометрическим количеством подходящего основания (такого как гидроксид, карбонат, бикарбонат Na, Ca, Mg или K или т.п.) или при реагировании свободных основных форм этих соединений со стехиометрическим количеством подходящей кислоты. Обычно такие реакции проводят в воде или в органическом растворителе либо в их смеси. Как правило, на практике предпочтительной является неводная среда, такая как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Соли настоящего соединения дополнительно включают сольваты соединений и соли соединений. Примеры фармацевтически приемлемых солей включают, но не ограничиваются этим, минеральные или органические кислые соли основных остатков, таких как амины; щелочные или органические соли кислотных остатков, например карбоксильных кислот; и т.п. Фармацевтически приемлемые соли включают обыкновенные нетоксичные соли и соли четвертичного аммония исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Например, обыкновенные нетоксичные кислые соли включают соли, полученные из неорганических кислот, таких как соляная,бромисто-водородная, серная, сульфаминовая, фосфорная, азотная и т.п.; и соли, полученные из органических кислот, таких как уксусная, пропионовая, янтарная, гликолевая, стеариновая, молочная, яблочная,винная, лимонная, аскорбиновая, памовая, малеиновая, гидроксималеиновая, фенилуксусная, глутаминовая, бензойная, салициловая, метансульфоновая, этансульфоновая, бензолсульфоновая, сульфаниловая,2-ацетоксибензойная, фумаровая, толуолсульфоновая, метансульфоновая, этандисульфоновая, щавелевая, изэтионовая, HOOC-(CH2)n-COOH, где n составляет 0-4, и т.п. Списки дополнительных подходящих солей можно найти, например, в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company,Easton, Pa., p. 1418 (1985). Термин "носитель" применительно к фармацевтическим композициям изобретения относится к разбавителю, эксципиенту (вспомогательному веществу) или наполнителю, вместе с которым предоставляется активное соединение. Эксципиент представляет собой любое инертное вещество, добавляемое к лекарственному средству, с целью приготовления фармацевтической композиции, которое является, как правило, безопасным, нетоксичным и не является биологически или другим образом нежелательным. Предпочтительными являются эксципиенты, которые являются приемлемыми для применения в ветеринарии, а также для фармацевтического применения человеком."Пациент" является человеком или животным, не являющимся человеком, нуждающимся в медицинском лечении. Медицинское лечение может включать лечение существующего состояния, такого как болезнь или расстройство, профилактическое или предупредительное лечение или диагностическое лечение. В некоторых вариантах осуществления пациент является человеком."Предоставление" означает назначение для приема, введение, продажу, распространение, транспортировку (с целью извлечения прибыли или нет), производство, приготовление или распределение."Предоставление соединения формулы I по меньшей мере с одним дополнительным активным веществом" означает, что соединение формулы I и дополнительное активное вещество(а) предоставляются одновременно в единой лекарственной форме, предоставляются одновременно в отдельных лекарственных формах или предоставляются в отдельных лекарственных формах для введения, отделенного некоторым количеством времени, т.е. в пределах времени, когда и соединение формулы I и по меньшей мере одно дополнительное активное вещество находятся в кровотоке пациента. Соединение формулы I и дополнительное активное вещество необязательно должно быть назначено пациенту тем же самым работником здравоохранения. Для дополнительного активного вещества или веществ не требуется предписания (рецепта). Введение соединения формулы I или по меньшей мере одного дополнительного активного вещества может осуществляться любым подходящим способом, например при помощи таблеток для перорального приема, капсул и жидкостей для перорального приема, путем ингаляции, инъекции, суппозиториев или местного контакта."Лечение" при использовании в описании включает предоставление соединения формулы I или как единственного активного вещества или вместе по меньшей мере с одним дополнительным активным веществом, достаточным для (а) предотвращения болезни или симптома болезни от возникновения у пациента, который может быть предрасположен к болезни, но у которого болезнь еще не была диагностирована (например, включая болезни, которые могут быть связаны с или вызваны первичной болезнью (как при фиброзе печени, который может произойти в результате хронической инфекции HCV); (b) подавления болезни, т.е. задержки ее развития; и (с) ослабления болезни, т.е. может вызвать регрессию болезни."Лечение" также означает предоставление терапевтически эффективного количества соединения формулы I как единственного активного вещества или вместе по меньшей мере с одним дополнительным активным веществом пациенту, имеющему инфекцию или чувствительного к инфекции гепатита C."Терапевтически эффективное количество" фармацевтической комбинации данного изобретения означает количество, эффективное при введении пациенту, для обеспечения терапевтической пользы,такой как уменьшение интенсивности симптомов, например, количество, эффективное для уменьшения симптомов инфекции гепатитом С. Например, пациент, зараженный вирусом гепатита C, может показывать повышенные уровни некоторых ферментов печени, включая AST и ALT. Нормальные уровни AST составляют от 5 до 40 единиц на литр сыворотки (жидкая часть крови), а нормальные уровни ALT составляют от 7 до 56 единиц на литр сыворотки. Таким образом, терапевтически эффективное количество представляет собой количество, достаточное для обеспечения значительного уменьшения повышенных уровней AST и ALT, или количество, достаточное для того, чтобы обеспечить возврат уровней AST и ALT к нормальному пределу. Также терапевтически эффективное количество представляет собой количество, достаточное для предотвращения значительного повышения или значительного снижения обнаруживаемого уровня вируса или вирусных антител в крови, сыворотке или тканях пациента. Один способ определения эффективности лечения включает измерение уровней РНК HCV с помощью обычного способа определения уровней вирусной РНК, такого как тест Roch TaqMan. В некоторых предпочтительных вариантах осуществления лечение снижает уровни РНК HCV ниже предела количественного определения (30 IU/мл, как измерено с помощью теста Roche TaqMan(R или более предпочтительно ниже предела обнаружения(10 IU/мл, Roche TaqMan). Значительное повышение или снижение обнаруживаемого уровня вируса или вирусных антител представляет собой любое обнаруживаемое изменение, которое является статистически значимым в стандартном параметрическом тесте статистической значимости, таком как Т-тест Стьюдента, где р 0,05. Химическое описание. Формула I включает все ее подформулы. В некоторых ситуациях соединения формулы I могут содержать один или более асимметричных элементов, таких как стереогенные центры, стереогенные оси и т.п., например, асимметричные атомы углерода, так что соединения могут находиться в разных стереоизомерных формах. Эти соединения могут быть, например, рацематами или оптически активными формами. Что касается соединений с двумя или более асимметричными элементами, эти соединения дополнительно могут быть смесями диастереомеров. В отношении соединений, имеющих асимметричные центры, должно быть понятно, что включаются все оптические изомеры и их смеси. Кроме того, соединения с углерод-углеродными двойными связями могут существовать в Z- и Е-формах, при этом все изомерные формы соединений включаются в настоящее изобретение. В этих ситуациях отдельные энантиомеры, т.е. оптически активные формы, могут быть получены с помощью асимметричного синтеза, синтеза из оптически чистых предшественников или путем разделения рацематов. Разделение рацематов также может быть выполнено, например, при помощи обычных методов, таких как кристаллизация в присутствии разделяющего агента или хроматография с использованием, например, хиральной ВЭЖХ-колонки. Когда соединение существует в различных таутомерных формах, изобретение не ограничивается каким-либо одним из характерных таутомеров, а скорее включает все таутомерные формы. Настоящее изобретение имеет целью включать все изотопы атомов, встречающихся в настоящих соединениях. Изотопы включают атомы, имеющие то же самое атомное число, но разные массовые числа. В качестве общего примера и без ограничения, изотопы водорода включают тритий и дейтерий, а изотопы углерода включают 11 С, 13 С и 14 С. Некоторые соединения описываются здесь с использованием общей формулы, которая включает переменные, например R, R1-R8, R16, R18, R19, M, n, T, Y и Z. Если не указано иначе, каждая переменная в такой формуле определяется независимо от других переменных. Таким образом, если группа, как сказано, является замещенной, например, 0-2 R, тогда группа может быть замещена до двух групп R, и R при каждом появлении независимо выбирается из определения R. Также комбинации заместителей и/или переменных являются допустимыми, только если такие комбинации приводят к устойчивым соединениям. В дополнение к соединениям формулы I, как описано выше, изобретение также включает соединения формул II-IV, которые несут любую комбинацию определений переменных, изложенных ниже, которые приводят к устойчивому соединению. В формуле II D представляет собой алкильную или алкенильную группу, имеющую от 6 до 10 атомов углерода. В формуле IV D представляет собой алкильную или алкенильную группу, имеющую от 6 до 10 атомов углерода. Например, изобретение включает варианты осуществления, в которых выполняется любое одно или более из следующих условий, поскольку получается устойчивое соединение.R1 и R2 заместители. Изобретение включает варианты осуществления, в которых R1 и R2 имеют любое из следующих определений.(a) R1 и R2 объединяются с образованием пирролидинового, морфолинового, пиперидинового или пиперазинового кольца, каждое из которых является необязательно замещенным 0-2 заместителями, независимо выбранными из фтора, аминогруппы, гидроксила, метила и трифторметила.(a) R3 представляет собой водород или метил, R4 представляет собой водород или C1-C4-алкил.(b) R3 и R4 представляют собой независимо водород или метил.(c) Соединение или его соль формулы II, где R3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил.(d) Соединение или его соль формулы III, где R3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил.(e) Соединение или его соль формулы IV, где R3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил.(f) Соединение или его соль формулы V, где R3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил. Т и R9 заместители. Изобретение включает соединения и соли формулы I, в которых Т представляет собой группу формулыR9 имеет любое из определений, следующих ниже.C1-C4-алкил, C3-C6-циклоалкил, фенил или бензил, каждый из которых является замещенным от 0 до 2 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы,C2-C4-алкенила и (фенил)C0-C2-алкила; и R12 представляет собой C1-C4-алкил.(c) В некоторых вариантах осуществления R10 представляет собой водород или метил; R11 представляет собой циклопропил. Переменные Y, n, J и L и М-заместитель. Изобретение включает соединения и соли формулы I, в которых удовлетворяется любое из следующих условий для Y.(а) В некоторых вариантах осуществления n представляет собой 0; Y отсутствует или представляет собой О, -О(С=О)- или Y представляет собой -(NR20)(C=O)-, где R20 представляет собой водород или метил.Z-заместитель может иметь любое из следующих определений.(a) Z представляет собой группу формулы каждая из которых является замещенной 0, 1, 2 или 3 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы и моно- и ди-C1-C4-алкиламиногруппы.(b) Z представляет собой хинолин формулы(с) В других вариантах осуществления R21 представляет собой метокси- или этоксигруппу в 7-положении хинолина, R22 представляет собой фенил, пиридил или тиазолил, каждый из которых является замещенным 0, 1 или 2 заместителями, независимо выбранными из метила, метоксигруппы, хлора,C1-C4-алкила, моно- и ди-C1-C4-алкиламиногруппы. Изобретение включает соединения формул VI-VIII (которые являются подгруппами формулы I):R1 и R2 объединяются с образованием азетидинового, пирролидинового, морфолинильного, пиперидинового или пиперазинового кольца, каждое из которых является замещенным 0-3 заместителями,независимо выбранными из фтора, аминогруппы, гидроксила, C1-C2-алкила и трифторметила, и каждый из которых является замещенным 0 или 1 заместителем, выбранным из метоксииминогруппы,амино-C1-C4-алкила, C1-C2-алкилсульфонила и пиразинила;R6 и R8 представляют собой независимо водород или метил; Т представляет собой группу формулыR9 представляет собой гидроксил, -OR12 или -NR10SO2R11, где R10 представляет собой водород или метил, R11 представляет собой C1-C6-алкил или C3-C7-циклоалкил и R12 представляет собой C1-C4-алкил;R16 представляет собой 0-2 заместителя, независимо выбранных из галогена, C1-C2-алкила иM представляет собой водород или метил;Z представляет собой группу формулы каждая из которых является замещенной 0, 1, 2 или 3 заместителями, независимо выбранными из галогена, C1-C4-алкила, C1-C4-алкоксигруппы и моно- и ди-C1-C4-алкиламиногруппы. Следующие соединения удалены по условию: Фармацевтические препараты. Соединения изобретения могут быть введены как чистый химический препарат, но предпочтительно их вводят как фармацевтическую композицию. Соответственно, изобретение предоставляет фармацевтические композиции, содержащие соединение или его фармацевтически приемлемую соль формулыI по меньшей мере вместе с одним фармацевтически приемлемым носителем. Фармацевтическая композиция может содержать соединение или соль формулы I как единственное активное вещество или она может содержать одно или более дополнительных активных веществ. Соединения изобретения могут быть введены орально, местно, парентерально, с помощью ингаляции или опрыскивания, подъязычно, чрескожно, посредством щечного введения, ректально, как офтальмологический раствор или с помощью других способов в стандартных лекарственных формах, содержащих обычные фармацевтически приемлемые носители. Фармацевтическая композиция может быть создана в виде любой фармацевтически пригодной формы, например как аэрозоль, крем, гель, пилюля, капсула, таблетка, сироп, чрескожный пластырь или офтальмологический раствор. Некоторые лекарственные формы, такие как таблетки и капсулы, подразделяются на подходящие по величине стандартные дозы, содержащие соответствующие количества активных компонентов, например эффективное количество для достижения желательной цели. Носители включают эксципиенты и разбавители, которые должны быть достаточно высокой чистоты и достаточно низкой токсичности, чтобы делать их пригодными для введения пациенту, которого лечат. Носитель должен быть инертным или он может обладать собственными фармацевтическими преимуществами. Количество носителя, используемого вместе с соединением, является достаточным для того, чтобы обеспечить количество материала, удобное для введения, на стандартную дозу соединения. Классы носителей включают, но не ограничиваются этим, связывающие вещества, буферные вещества, красящие вещества, разбавители, разрыхлители, эмульгаторы, ароматизаторы, способствующие скольжению вещества, смазывающие вещества, консервирующие вещества, стабилизирующие вещества,поверхностно-активные вещества, таблетирующие средства и увлажняющие вещества. Некоторые носители могут перечисляться в нескольких классах, например растительное масло может использоваться как смазывающее вещество в некоторых композициях и как разбавитель в других. Примеры фармацевтически приемлемых носителей включают сахара, крахмалы, целлюлозу, порошкообразную трагакантовую камедь, солод, желатин, тальк и растительные масла. В фармацевтическую композицию могут быть включены необязательные активные вещества, которые существенно не затрагивают активность соединения настоящего изобретения. Фармацевтические композиции, созданные для перорального введения, часто являются предпочтительными. Эти композиции содержат от 0,1 до 99 мас.% соединения по изобретению и обычно по меньшей мере около 5 мас.% соединения по изобретению. Некоторые варианты осуществления содержат примерно от 25 до 50 мас.% или примерно от 5 до 75 мас.% соединения по изобретению. Способы лечения. Изобретение включает способы предотвращения и лечения инфекций вируса гепатита C путем предоставления эффективного количества соединения изобретения пациенту, у которого есть риск заражения гепатитом С или который инфицирован вирусом гепатита C. Соединение изобретения может быть предоставлено как единственное активное вещество или может быть предоставлено вместе с одним или более дополнительными активными веществами. Фармацевтические композиции, раскрытые в описании, пригодны для предотвращения и лечения инфекций гепатита C у пациентов. Эффективное количество фармацевтической композиции изобретения может быть количеством, достаточным для того, чтобы (а) предотвратить возникновение гепатита C или симптома гепатита C у пациента, который может быть предрасположен к развитию гепатита C, но у которого гепатит еще не был диагностирован, или предотвратить болезни, которые могут быть связаны с или вызваны первичной инфекцией вирусом гепатита C (например, фиброза печени, который может появиться в результате хронической инфекции HCV); (b) препятствовать развитию гепатита C и (с) вызвать регрессию инфекции гепатитом С. Количество фармацевтической композиции, эффективное для того, чтобы ингибировать прогрессирование или вызвать регрессию гепатита C, включает количество, эффективное для остановки ухудшения симптомов гепатита C или уменьшения симптомов, испытываемых пациентом, зараженным вирусом гепатита C. Альтернативно, остановка прогрессирования или регрессия гепатита C может быть установлена с помощью какого-либо из нескольких маркеров болезни. Например, прекращение увеличения или уменьшение вирусной нагрузки гепатита C или прекращение увеличения или уменьшение числа циркулирующих HCV-антител в крови пациента представляют собой маркеры остановки прогрессирования или регрессии инфекции гепатита C. Другие маркеры болезни гепатита C включают уровни аминотрансферазы, в частности уровни ферментов печени AST и ALT. Нормальные уровни AST составляют от 5 до 40 единиц на 1 л сыворотки (жидкая часть крови), а нормальные уровни ALT составляют от 7 до 56 единиц на 1 л сыворотки. Обычно эти уровни являются повышенными у пациентов, инфицированныхHCV. При регрессии болезни обычно отмечается возвращение уровней AST и ALT к нормальному пределу. Симптомы гепатита C, которые могут подвергаться воздействию эффективного количества фармацевтической композиции изобретения, включают ослабленную функцию печени, утомляемость, гриппоподобные симптомы: жар, озноб, мышечную боль, боль в суставах и головную боль, тошноту, отвращение к некоторой пище, потерю веса, неизвестной этиологии, физиологические расстройства, включая депрессию, болезненность в животе и желтуху."Функция печени" относится к нормальной функции печени, включая, но не ограничиваясь этим,синтетическую функцию, включая синтез белков, таких как сывороточные белки (например, альбумин,факторы свертывания крови, щелочная фосфатаза, аминотрансферазы (например, аланин трансаминаза,аспартат трансаминаза), 5'-нуклеозидаза, гамма-глутамилтранспептидаза и т.д.), синтез билирубина, синтез холестерина и синтез желчных кислот; метаболическую функцию печени, включая метаболизм углеводородов, метаболизм аминокислот и аммиака, метаболизм гормонов и метаболизм липидов; детоксификацию экзогенных лекарственных препаратов; и гемодинамическую функцию, включая висцеральную и портальную гемодинамику. Эффективное количество композиции, описанной здесь, также будет обеспечивать достаточную концентрацию активных веществ в концентрации при введении пациенту. Достаточная концентрация активного вещества представляет собой концентрацию вещества в организме пациента, необходимую для предотвращения или борьбы с инфекцией. Такое количество может быть определено экспериментально, например путем оценки концентрации вещества в крови, или теоретически, путем вычисления биодоступности. Количество активного вещества, достаточного для того, чтобы ингибировать вирусную инфекцию in vitro, можно определить с помощью обычных методов исследования инфекционности вируса, таких как анализ на основе репликона, который описан в литературе. Также изобретение включает применение фармацевтических композиций, содержащих соединение изобретения, в профилактическом лечении. В контексте профилактического или предупредительного лечения эффективное количество соединения изобретения представляет собой количество, достаточное для значительного снижения риска приобретения пациентом инфекции гепатита C. Изобретение включает способ ингибирования репликации HCV in vivo, включающий предоставление соединения или соли изобретения пациенту, зараженному HCV, причем концентрация соединения или соли является достаточной для того, чтобы ингибировать репликацию HCV-репликона in vitro. В этом случае концентрация включает концентрацию in vivo, например концентрацию в крови или плазме. Концентрация соединения, достаточная для того, чтобы ингибировать репликацию HCV-репликона invitro, может быть определена из метода анализа репликации репликона, такого как анализ, предоставленный в примере 6 описания. Способы лечения включают предоставление пациенту дозировки соединения изобретения определенных размеров. При лечении вышеуказанных состояний являются пригодными уровни дозировки каждого активного вещества примерно от 0,1 до 140 мг на 1 кг массы тела в день (примерно от 0,5 мг до 7 г на пациента в день). Количество активного ингредиента, которое может быть объединено с материалами носителя для получения единой лекарственной формы, будет изменяться в зависимости от пациента, которого лечат, и конкретного способа введения единицы дозировки соединения изобретения. В некоторых вариантах осуществления пациенту предоставляется ежедневно от 25 до 500 мг или от 25 до 200 мг соединения изобретения. Частота дозирования может также изменяться в зависимости от используемого соединения и конкретной болезни, которую лечат. Однако для лечения большинства инфекционных расстройств предпочтительным является режим дозирования 4 раза в день или менее, а режим дозирования 1 или 2 раза в день является особенно предпочтительным. Однако понятно, что конкретный уровень дозирования для любого отдельного пациента будет зависеть от ряда факторов, включая активность конкретного используемого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время введения, способ введения и скорость выведения из организма, комбинацию лекарственных препаратов и тяжесть конкретной болезни у пациента, подвергаемого лечению. Составы в упаковке. Изобретение включает предоставление соединения или соли формулы I в контейнере вместе с инструкциями по использованию композиции для лечения пациента, страдающего от инфекции гепатита C. Изобретение включает упакованные фармацевтические композиции. Такие упакованные композиции включают соединение формулы I в контейнере. Контейнер может дополнительно включать инструкции для применения композиции для лечения или предотвращения у пациента вирусной инфекции, такой как инфекция вирусом гепатита C. Упакованная фармацевтическая композиция может включать одно или более дополнительных активных веществ. Способы комбинации. Изобретение включает фармацевтические композиции и способы лечения, в которых соединение или соль изобретения предоставляется вместе с одним или более дополнительными активными веществами. В определенных вариантах осуществления активное вещество (или вещества) представляет собой ингибитор HCV-протеазы или ингибитор HCV-полимеразы. Например, ингибитор протеазы может быть телапревиром (VX-950), а ингибитор полимеразы может быть валопицитабином, или NM 107, активное вещество, в которое превращается валопицитабин in vivo. В определенных вариантах осуществления второе активное вещество представляет собой рибавирин, интерферон или коньюгат пегилированный интерферон альфа. Согласно способам изобретения соединение изобретения и дополнительное активное вещество могут (1) совместно заключаться в состав и вводиться или доставляться одновременно в объединенной композиции; (2) доставляться периодически или параллельно как отдельные композиции или (3) доставляться с помощью любой другой комбинации режимов лечения, известной в данной области техники. При доставке в периодическом лечении способы изобретения могут включать введение или доставку соединения изобретения и дополнительного активного вещества последовательно, например в отдельных растворах, эмульсиях, суспензиях, таблетках, пилюлях или капсулах, или с помощью разных инъекций в отдельных шприцах. В общем, во время периодической терапии эффективная дозировка каждого активного ингредиента вводится последовательно, т.е. серийно, тогда как при одновременном лечении эффективные дозировки двух или более активных ингредиентов вводятся вместе. Также могут использоваться разные последовательности прерывистой комбинированной терапии. В определенных вариантах осуществления способ лечения включает предоставление пациенту соединения формулы I и интерферона, такого как пегилированный интерферон или интерферон гамма. Интерферон может быть единственным соединением, предоставленным вместе с соединением изобретения,или может предоставляться вместе с дополнительным активным веществом, которое не является интерфероном. Изобретение включает способы лечения и фармацевтические композиции, содержащие соединения изобретения, любое одно или комбинацию следующих соединений и веществ в качестве дополнительного активного средства: ингибиторы каспаз: IDN 6556 (Idun Pharmaceuticals); ингибиторы циклофилина: NIM811 (Novartis) и DEBIO-025 (Debiopharm); ингибиторы цитохром-Р 450-монооксигеназы: ритонавир (WO 94/14436), кетоконазол, тролеандомицин, 4-метилпиразол, циклоспорин, клометиазол, циметидин, итраконазол, флуконазол, миконазол,флувоксамин, флуоксетин, нефазодон, сертралин, индинавир, нелфинавир, ампренавир, фосампренавир,- 16021794 саквинавир, лопинавир, делавирдин, эритромицин, VX-944 и VX-497. Предпочтительные CYP-ингибиторы включают ритонавир, кетоконазол, тролеандромицин,4-метилпиразол, циклоспорин и клометиазол. Глюкокортикоиды: гидрокортизон, кортизон, преднизон, преднизолон, метилпреднизолон, триамцинолон, параметазон, бетаметазон и дексаметазон. Гематопоэтины: гематопоэтин-1 и гематопоэтин-2. Другие члены суперсемейства гематопоэтинов,такие как различные колониестимулирующие факторы (например, G-CSF, GM-CSF, M-CSF), Еро и SCF(фактор стволовых клеток). Гомеопатическая терапия: расторопша, силимарин, женьшень, глицирризин, лакричный корень,шизандра, витамин С, витамин Е, бета-каротин и селен. Иммуномодулирующие соединения: талидомид, IL-2, гематопоэтины, ингибиторы IMPDH (инозинмонофосфатдегидрогеназы), например меримеподиб (Vertex Pharmaceuticals Inc.), интерферон, включая природный интерферон (такой как, омниферон, Viragen, и сумиферон, Sumitomo, смесь природных интерферонов), природный интерферон альфа (алферон, Hemispherx Biopharma, Inc.), интерферон альфаnl из лимфобластоидных клеток (веллеферон, Glaxo Wellcome), альфа интерферон для перорального приема, пегилированный интерферон, пегилированный интерферон альфа 2 а (пегасис, Roche), рекомбинантный интерферон альфа 2 а (роферон, Roche), интерферон альфа 2b для вдыхания (AERX, Aradigm), пегилированный интерферон альфа 2b (албуферон, Human Genome Sciences/ Novartis, пегинтрон, Schering),рекомбинантный интерферон альфа 2b (интрон А, Schering), пегилированный интерферон альфа 2b (пегилированный интрон, Schering, вираферонпег, Schering), интерферон бета-1 а (ребиф, Serono, Inc. иPfizer), согласованный интерферон альфа (инферген, Valeant Pharmaceutical), интерферон гамма-1b (актиммун, Intermune, Inc.), непегилированный интерферон альфа, альфа интерферон и его аналоги и синтетический тимозин альфа 1 (задаксин, SciClone Pharmaceuticals Inc.). Иммунодепрессанты: сиролимус (Рапамун, Wyeth). Интерлейкины: (IL-1, IL-3, IL-4, IL-5, IL-6, IL-10, IL-11, IL-12), LIF, TGF-бета, TNF-альфа) и другие низкомолекулярные факторы (например, AcSDKP, pEEDCK, тимические гормоны и миницитокины). Усилители (энхансеры) интерферона: EMZ702 (Transition Therapeutics).IRES-ингибиторы: VGX-410C (VGX Pharma). Моноклональные и поликлональные антитела: XTL-6865 (XTL), HuMax-HepC (Genmab), иммуноглобулин против гепатита C (человека) (CIVACIR, Nabi Biopharmceuticals). Аналоги нуклеозидов: ламивудин (эпивир, ЗТС, GlaxoSmithKline), MK-0608 (Merck), залцитабинPharmaceuticals и виразол (ICN Pharmaceuticals) и вирамидин (Valeant Pharmaceuticals), амидиновое пролекарство рибавирина. Также могут быть использованы комбинации нуклеозидных аналогов. Ненуклеозидные ингибиторы: PSI-6130 (Roche/Pharmasset), делавиридин (рескриптор, Pfizer) иHCV-796 (Viropharm). Ингибитор белка Р 7: амантадин (симметрел, Endo Pharmaceuticals, Inc.). Ингибиторы полимеразы: NM283 (валопицитабин) (Idenix) и NM 107 (Idenix). Ингибиторы протеазы: BILN-2061 (Boehringer Ingelheim), GW-433908 (пролекарство ампренавира,Glaxo/ Vertex), индинавир (криксиван, Merck), ITMN-191 (Intermune/Array Biopharma), VX950 (Vertex) и комбинации, содержащие один или более из вышеупомянутых ингибиторов протеазы. РНК-интерференция: SIPHK-034 iPHK (SiPHK Therapeutics). Терапевтические вакцины: IC41 (Intercell), IMN-0101 (Imnogenetics), GI 5005 (Globeimmune),Chronvac-C (Tripep/ Inovio), ED-002 (Imnogenetics), Hepavaxx С (ViRex Medical). Агонисты TNF: адалимумаб (хумира, Abbott), энтанерцепт (энбрел, Amgen и Wyeth), инфликсимабTLR-агонисты: ANA-975 (Anadys Pharmaceuticals), TLR7-агонист (Anadys Pharmaceuticals),CPG10101(Coley) и TLR9-агонисты, включая CPG 7909 (Coley). Ингибиторы циклофилина: NIM811 (Novartis) и DEBIO-025 (Debiopharm). Пациентам, получающим медикаментозное лечение гепатита C, обычно назначают интерферон вместе с другим активным веществом. Таким образом, способы лечения и фармацевтические комбинации, в которых соединение изобретения предоставляется вместе с интерфероном, таким как пегилированный интерферон альфа 2 а, в качестве дополнительных активных веществ являются включенными как варианты осуществления. Подобным образом, в описании предоставляются способы и фармацевтические комбинации, в которых рибавирин является дополнительным активным веществом. Примеры Это изобретение дополнительно иллюстрируется с помощью следующих примеров, которые не следует истолковывать как ограничивающие. Соединения, предоставленные в описании, в большинстве случаев могут быть получены с использованием стандартных методов синтеза. Исходные материалы, как правило, являются легкодоступными от коммерческих источников, таких как Sigma-Aldrich Corp. (St. Louis, МО). Например, может быть использован способ синтеза, который показан в примере 1 или 2. Очевидно, что конечный продукт и любое промежуточное соединение(я), показанное на следующих схемах, может быть выделено, высушено, отфильтровано и/или концентрировано и может быть дополнительно очищено (например, с помощью хроматографии). Каждая переменная (например, "R") в следующих схемах относится к любой группе в соответствии с описанием соединения, предоставленным здесь. Специалист в данной области техники может найти модификации одного или нескольких шагов синтеза, описанных здесь, без значительного отклонения от общей схемы синтеза. Дополнительные экспериментальные подробности, касающиеся синтеза репрезентативного соединения с помощью этих схем, предоставляются в примерах 1-5. Сокращения. Следующие химические сокращения используются в примере 1. Дополнительные сокращения в этих примерах будут привычны для специалистов в области органического химического синтеза:(J. Org. Chem. 70:5869-79 (2005, добавляют к смеси CDI/этилацетат и перемешивают при комнатной температуре (RT) до тех пор, пока не израсходуется исходный материал. К этой смеси добавляют циклопропилсульфонамид (2,2 г; 18,4 ммоль; 1,1 экв.), а затем DBU (2,1 мл; 20,5 ммоль: 1,23 экв.), смесь перемешивают при RT в течение 2 ч. Обработка и очистка с помощью хроматографии с силикагелем дает 2 г соединения 2.WO 02/060926, в DMF перемешивают вместе с О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфатом (4,1 г; 10,5 ммоль; 1,3 экв.) в течение 30 мин, а затем добавляют циклопропиламин 2(1,92 г; 8,3 ммоль; 1,0 экв.) и N-метилморфолин (2,52 г; 25,0 ммоль; 3,0 экв.). Смесь перемешивают в течение ночи и удаляют растворитель при пониженном давлении. Полученный осадок растворяют в этилацетате и промывают насыщенным водным NaHCO3. Органический растворитель высушивают надMgSO4 и концентрируют при пониженном давлении с получением сырого продукта 3, который используется для следующей стадии без дополнительной очистки. Соединение 3 в 10 мл обезвоженного CH2Cl2 обрабатывают 5 мл TFA и перемешивают в течение ночи. Растворитель удаляют, а осадок подвергают рекристаллизации из этилацетата с получением 4,12 г соединения 4 (выход двух стадий 61%). Пример 2. Синтез макроциклических соединений. Метод 1. Снятие защитных групп (превращение N-Boc в N-амин или т-бутилового эфира в карбоновую кислоту).TFA (3-4 мл) добавляют к раствору Вос-защищенного исходного материала (1 ммоль) или т-бутилэфира в безводном DCM (7 мл) при комнатной температуре. Реакцию контролируют с помощью ЖХ/МС и ТСХ. Примерно через 1-3 ч реакционную смесь выпаривают при пониженном давлении до сухости. Сырой продукт используют для следующего этапа реакции без дополнительной очистки. Метод 2. Образование амида.N-метилморфолин (2 ммоль) и HBTU (1,2 ммоль) добавляют в одной части при комнатной температуре к раствору кислоты (1 ммоль) в безводном DMF (10 мл). После перемешивания при комнатной температуре в течение ночи амин (1 ммоль) добавляют в одну часть и затем перемешивают в течение ночи. Реакционную смесь выливают в ледяную воду и экстрагируют с этилацетатом (100 мл). Органический слой промывают Н 2 О, рассолом и высушивают над безводным MgSO4. Осадок фильтруют и выпаривают в вакууме до сухости. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (гексанэтилацетат от 100:0 до 50:50) для получения искомого продукта. Метод 3. RCM катализировали катализатором Граббса 2 (CAS Reg. No. 246047-72-3) или катализатором Hoveyda-Grubbs 2 (CAS Reg. No. 301224-40-8) Смесь исходного материала (диолефин, 1 ммоль), катализатора (примерно 5-30 мол.%) в 1,2-дихлорэтане дегазируют и нагревают до 110 С в течение примерно 12-24 ч в атмосфере аргона. Реакцию контролируют с помощью ЖХ/МС и ТСХ. Реакционную смесь выпаривают до сухости при пониженном давлении. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (гексанэтилацетат от 100:0 до 50:50) для получения искомого продукта. Метод 4. Гидролиз сложных эфиров. Гидрат LiOH (6 экв.) при комнатной температуре добавляют к одной части раствора эфира(1 ммоль) в THF (5 мл), метанола (2,5 мл) и воды (2,5 мл) и затем реакционную смесь перемешивают в течение ночи. После того как реакция завершилась (показано с помощью ЖХ/МС), смесь охлаждают до 0 С и подкисляют примерно до рН 2 и экстрагируют с помощью DCM (220 мл). Реакционную смесь высушивают над MgSO4, фильтруют и выпаривают до сухости под пониженным давлением. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (гексан-этилацетат 100:0 до 20:80) для получения искомого продукта. Схема 1 Соединение 21 получают методами 1 и 2 из исходного соединения 14 и аминокислоты 20.MS (M1) 754. Соединение 22 получают с помощью метода этапа 3. Соединение 29 получают методом 4 из исходного соединения 28. Соединение 30 получают методом, указанным в этапе 2, из исходного соединения 29. Соединение 31 получают методом, указанным в этапах 1 и 2, из исходного соединения 30. Соединение 33 получают методом, указанным в этапе 4, из исходного соединения 28 и 32. Соединения 34 и 35 получают с помощью метода, указанного в этапе 3. После RCM реакционную смесь отделяют с помощью препаративной тонкослойной хроматографии Пример 4. Получение промежуточных продуктов. Получение промежуточных продуктов 20 и 32 Этап 1. 8-Ноненовую кислоту (1,56 г; 10 ммоль) помещают в 100-мл колбу, добавляют обезвоженный эфир (35 мл) в атмосфере N2, охлаждают до 0 С, добавляют TEA (1,6 г; 16 ммоль), а затем по каплям пивалоил хлорид (1,26 г; 10,5 ммоль). Ледяную баню убирают, а реакционную смесь перемешивают при комнатной температуре в течение 1 ч. Полученную суспензию охлаждают до 0 С и фильтруют в колбу 250 мл под N2 (промывая дважды обезвоженным эфиром 210 мл). Фильтрат охлаждают до -78 С и разбавляют обезвоженным THF (25 мл). Немного кристаллов 1,10-фенантролина добавляют к раствору (S)(-)-4-бензил-2-оксазолидинона вTHF (25 мл). Раствор охлаждают до -78 С и добавляют по каплям раствор n-BuLi (н-бутиллитий) (1,6 М в гексане, 6,5 мл, 10,4 ммоль) до тех пор, пока красный цвет сохраняется в течение 10 мин. Этот раствор добавляют к вышеупомянутому охлажденному перемешанному раствору ангидрида при -78 С в течение 20 мин через канюлю. Полученную смесь перемешивают при -78 С в течение дополнительных 30 мин,затем выливают в насыщенный раствор NH4Cl, органический слой отделяют, водный слой экстрагируют с эфиром (50 мл, 3 Х). Объединенные органические слои промывают рассолом и высушивают над MgSO4,фильтруют, концентрируют при пониженном давлении до сухости. Сырой продукт очищают с помощью флэш-хроматографии (гексан-этилацетат 100:0-100:20) с получением 3,01 г соединения 26 (95%). Этап 2. Раствор соединения 26 (3,01 г; 9,6 ммоль) в обезвоженном THF охлаждают до -78 С, затем добавляют по каплям 2,0 М раствор NaN(TMS)2 в гексане (5,76 мл) в течение 10 мин. Через 30 мин добавили по каплям т-бутилбромацетат при -78 С. Реакционную смесь перемешивали при -78 С в течение 2 ч. Реакцию контролировали ЖХ/МС и ТСХ. Реакцию потушили с помощью 10% KHSO4 до значения рН примерно 4-6, экстрагировали с этилацетатом, органический слой промыли Н 2 О, рассолом, высушили над MgSO4, профильтровали, выпарили при пониженном давлении до сухости. Сырой продукт очистили с помощью хроматографии на силикагеле (гексан-этилацетат 100:0-100:20) с получением соединения 14. Этап 3. Добавляют по каплям Н 2 О 2 (50%, 0,9 мл) в течение 5 мин при 0 С, а затем раствор LiOH(0,2 г в 2 мл Н 2 О). Реакционную смесь добавляют к раствору соединения 27 (1,05 г; 2,44 ммоль) вTHF/H2O (5:1, 24 мл). Смесь перемешивают при 0 С в течение 1 ч и затем тушат, добавляя по каплям обезвоженный раствор тиосульфата натрия (10 мл) и сохраняя температуру ниже 20 С. Смесь экстрагируют этилацетатом, а водную фазу подкислили до рН примерно 2 твердой лимонной кислотой и экстрагировали этилацетатом. Объединенную органическую фазу промывают рассолом, высушивают над обезвоженным сульфатом натрия и удаляют растворитель при пониженном давлении. Осадок очищают с по- 22021794 мощью колоночной хроматографии на силикагеле, элюируя с системой градиента гексан:этилацетат(100:0) до 50:50 с выходом искомого соединения 20 (503 мг). Этап 4. Соединение 36 получают методом 1. Этап 5. Соединение 37 получают методом 2. Этап 6. Соединение 32 получают из 37 с помощью метода, представленного в этапе 3, для получения соединения 20. Пример 5. Дополнительные соединения. Соединения, раскрытые в таблице, получают способами, представленными в примерах 1-4. Пример 6. Исследование с целью выявления соединений, которые ингибируют репликацию HCV. Соединения, заявленные в описании, исследуют на способность ингибировать репликацию репликона вируса гепатита C в культивируемых клетках, в которые был встроен конструкт HCV-репликона. Система HCV-репликона была описана Bartenschlager, et. al (Science, 285, p. 110-113 (1999. Система репликона является прогностической по отношению к анти-HCV активности: соединения, которые являются активными на людях, постоянно показывают активность при проверке на репликоне. В этом исследовании клетки, содержащие HCV-репликон, обрабатывают разными концентрациями испытываемого соединения с целью выявления способности испытываемого соединения подавлять репликацию HCV-репликона. В качестве положительного контроля клетки, содержащие HCV-репликон,обрабатывали разными концентрациями интерферона альфа, известного ингибитора репликации HCV. Система анализа репликона включает неомицин фосфотрансферазу (NPT) как компонент самого репликона для того, чтобы обнаружить транскрипцию генных продуктов репликона в клетке-хозяине. Клетки,в которых HCV-репликон активно реплицируется, имеют высокие уровни NPT; уровень NPT является пропорциональным репликации HCV. Клетки, в которых HCV репликон не реплицируется, имеют низкие уровни NPT и, таким образом, не выживают при обработке неомицином. Уровень NPT каждого образца измеряют с помощью метода ELISA с захватом. Протокол способности испытываемых соединений ингибировать вирусную репликацию репликона гепатита C в культивируемых клетках, в которые был введен конструкт репликона, следует далее. Этап 6 А. HCV-репликон и экспрессия репликона. Геном HCV состоит из одной ORF (открытой рамки считывания), которая кодирует полипротеин,состоящий из 3000 аминокислот. По бокам ORF со стороны 5' располагается нетранслируемая область,которая служит как участок внутренней посадки рибосомы (IRES) и со стороны 3' - высококонсервативная последовательность, необходимая для репликации вируса (3'-NTR). Структурные белки, необходимые для вирусной инфекции, располагаются около 5'-конца ORF. Неструктурные белки, обозначенные сHCV-репликон содержит 5'-3', HCV-IRES, ген (нео)неомицин-фосфотрансферазы, IRES вируса энцефаломиокардита, который управляет трансляцией последовательностей HCV с NS3 по NS5B, и 3'-NTR. Последовательность HCV-репликона сдана на хранение в GenBank (инвентарныйAJ242652). Репликон трансфицируют в клетки Huh-7 с помощью стандартных методов, таких как электропорация. Этап 6 В. Поддержание клеток. Оборудование и материалы включают, но не ограничиваются этим, клетки Huh-7, содержащиеHCV-репликон, среду для поддержания (DMEM (среда Игла, модифицированная Дульбекко) с добавлением 10% FBS, L-глутамина, неосновных аминокислот, пенициллина (100 единиц/мл), стрептомицина(100 мкг/мл) и 500 мкг/мл генетицина (G418), среду для скрининга (DMEM, дополненная 10% FBS,L-глутамином, неосновными аминокислотами, пенициллином (100 единиц/мл) и стрептомицином(100 мкг/мл, 96-луночные планшеты для тканевой культуры (с плоским дном), 96-луночные планшеты(с U-образным дном для разведения лекарственных препаратов), интерферон альфа для позитивного контроля, реактив для фиксации (такой как метанол, ацетон), первичные антитела (кроличьи анти-NPTII),вторичные антитела: Eu-N11 и усиливающий раствор. Клетки, содержащие HCV-репликон, поддерживают высокие уровни репликации вирусного РНКрепликона, когда их плотность является подходящей. Сверхзаселенность вызывает пониженную репликацию вирусной РНК. Следовательно, клетки необходимо поддерживать в логарифмической фазе роста в присутствии 500 мкг/мл G418. Как правило, клетки необходимо пассировать дважды в неделю при разведении 1: 4-6. Поддержание клеток проводится, как указано далее. Клетки, содержащие HCV-репликон, проверяют под микроскопом, чтобы удостовериться, что клетки хорошо растут. Клетки один раз промывают PBS и добавляют 2 мл трипсина. Смесь клетки/трипсин инкубируют при 37 С в СО 2-инкубаторе в течение 3-5 мин. После инкубации добавляют 10 мл полной среды для того, чтобы остановить реакцию трипсинизации. Клетки осторожно отсасывают, помещают в 15 мл пробирку и откручивают при 1200 об/мин в течение 4 мин. Раствор трипсин/среда удаляют. Добавляют среду (5 мл) и осторожно перемешивают клетки. Клетки подсчитывают. Затем клетки рассевают в 96-луночные планшеты при плотности 6000-7500 клеток/100 мкл/лунку(6-7,5105 клеток/10 мл/планшет). Затем планшеты инкубируют при 37 С в инкубаторе с содержанием 5% СО 2. Клетки проверяют под микроскопом приблизительно через 24 ч после высева и перед добавлением лекарственных препаратов. Если подсчет и разведение были выполнены правильно, клетки являются слившимися на 60-70%, и почти все клетки должны прикрепиться и равномерно распространиться в лунке. Этап 6 С. Обработка клеток, содержащих HCV-репликон, испытываемым соединением. Клетки, содержащие HCV-репликон, один раз промывают PBS, затем добавляют 2 мл трипсина. Клетки инкубируют при 37 С в 5% СО 2-инкубаторе в течение 3-5 мин. Для прекращения реакции добавляют 10 мл полной среды. Клетки осторожно отсасывают, помещают в 15-мл пробирку и откручивают при 1200 об/мин в течение 4 мин. Раствор трипсин/среда удаляют и добавляют 5 мл среды (500 млDMEM (с высоким содержанием глюкозы от BRL каталожный номер 12430-054; 50 мл 10% FBS, 5% генетицин G418 (50 мг/мл, BRL каталожный номер 10131-035), 5 мл MEM неосновных аминокислот(100 BRL 11140-050) и 5 мл пенициллина-стрептомицина (BRL 15140-148). Клетки и среду осторожно перемешивают. Клетки высевают со средой для скрининга (500 мл DMEM (BRL 21063-029), 50 мл FBS(BRL 10082-147) и 5 мл MEM неосновных аминокислот (BRL 11140-050) при 6000-7500 клеток/100 мкл/лунку 96-луночного планшета (6-7,5105 клеток/10 мл/планшет). Планшеты помещают на ночь в инкубатор при 37 С и 5% СО 2. Этап 6D. Анализ. На следующее утро лекарственные препараты (испытываемые соединения или интерферон альфа) разводят средой или раствором DMSO/среда в 96-луночных планшетах с U-образным дном, в зависимости от окончательной концентрации, выбранной для скрининга. Как правило, использовали 6 концентраций каждого из испытываемых соединений в пределах от 10 до 0,03 мкМ. 100 мкл разведения испытываемого соединения помещают в лунки 96-луночного планшета, содержащие клетки с HCV-репликоном. Среду без лекарственного средства добавляют в некоторые лунки в качестве отрицательных контролей. Известно, что DMSO влияет на рост клеток. Следовательно, если используются лекарственные средства,разведенные в DMSO, все лунки, включая отрицательный контроль (только среда) и положительный контроль (интерферон альфа), должны содержать ту же самую концентрацию DMSO с целью скрининга однократной дозы. Планшеты инкубируют при 37 С во влажной среде с содержанием 5% СО 2 в течение 3 дней. На четвертый день проводится количественный анализ NTPII. Среду выливают из планшетов и промывают планшеты один раз в 200 мкл PBS. Затем PBS отделяют, а планшеты осушают с помощью бумажного полотенца, чтобы удалить оставшийся PBS. Клетки фиксируют in situ с помощью предварительно охлажденного раствора (-20 С) метанол:ацетон (1:1) 100 мкл/лунку и помещают планшеты на-20 С на 30 мин. Раствор для фиксации сливают из планшетов и дают возможность планшетам полностью высохнуть на воздухе (приблизительно 1 ч). Регистрируют появление слоя высушенных клеток, и плотность клеток в лунках с токсичным веществом отмечают невооруженным глазом. Альтернативно, жизнеспособность клеток можно оценить с помощью MTS-теста, описанного ниже. Лунки блокируют с помощью 200 мкл "блокирующего" раствора (blocking solution) (10% FBS; 3%NGS в PBS) в течение 30 мин при комнатной температуре. "Блокирующий" раствор удаляют и в каждую лунку добавляют 100 мкл кроличьего анти-NPTII в разведении 1:1000 в "блокирующем" растворе. Затем планшеты инкубируют 45-60 мин при комнатной температуре. После инкубации лунки промывают шесть раз раствором PBS-0,05% Твин-20. К каждой лунке добавляют 100 мкл разведенного в "блокирующем" буфере 1:15000 европия (EU), коньюгированного с козьими антикроличьими антителами, и инкубируют при комнатной температуре в течение 30-45 мин. Планшеты вновь промывают и добавляют в каждую лунку 100 мкл усиливающего раствора (Perkin Elmer 4001-0010). Каждый планшет встряхивают (приблизительно 30 об/мин) в шейкере для планшетов в течение 3 мин. 95 мкл переносят из каждой лунки в black plate; сигнал EU количественно определяют с помощью планшетного ридера VICTOR Perkin-Elmer (EU-Lance). При проверке в этом испытании соединения 11, 16, 25, 33, 38, 39 и 40 продемонстрировали значения ЕС 50 около 10 мкМ или менее. Пример 7. Исследование цитотоксичности. Чтобы гарантировать, что уменьшение репликации репликона наблюдается вследствие активности соединения против HCV-репликона, а не вследствие неспецифической токсичности, проводят исследования с целью количественного определения цитотоксичности соединений. Этап 7 А. Исследование цитотоксичности на клеточном белке альбумине. Измерение клеточного белка альбумина предоставляет один маркер цитотоксичности. Уровни белка, полученные из анализа клеточного альбумина, также могут быть использованы, чтобы обеспечить эталон нормирования для противовирусной активности соединений. При исследовании белка альбумина клетки, содержащие HCV-репликон, обрабатывают в течение трех дней разными концентрациями гелиоксантина; соединение, которое, как известно, является цитотоксическим в высоких концентрациях. Клетки лизируют, а клеточный лизат используют, чтобы связать планшет-связанные козлиные антиальбумин антитела при комнатной температуре (от 25 до 28 С) в течение 3 ч. Затем планшеты промывают 6 раз 1 PBS. После отмывки несвязанных протеинов используют мышиные моноклональные антитела античеловек сывороточный альбумин, чтобы связать альбумин на планшете. Затем комплекс обнаруживают с помощью меченного фосфатазой антимышиного IgG в качестве вторичного антитела. Этап 7 В. MTS анализ на цитотоксичностъ. Жизнеспособность клеток также можно определить с помощью метода CELLTITER 96 AQUEOUSONE Solution Cell Proliferation Assay (Promega, Madison WI), колориметрического метода для определения числа жизнеспособных клеток. В этом методе до фиксирования клеток 10-20 мкл MTS-реактива добавляют к каждой лунке согласно инструкциям производителя, планшеты инкубируют при 37 С и считывают данные OD при 490 нм. Во время периода инкубации живые клетки превращают MTS-реактив в формазан, который поглощает при 490 нм. Таким образом, оптическая плотность 490 нм является прямо пропорциональной числу живых клеток в культуре. Прямое сравнение клеточного альбумина и методов MTS для определения цитотоксичности может быть получено, как указано далее. Клетки обрабатываются разными концентрациями исследуемого соединения или гелиоксантина в течение трехдневного периода. Перед лизисом для определения альбумина, как описано выше, к каждой лунке добавляют MTS-реактив согласно инструкции производителя, инкубируют при 37 С и снимают показания OD при 490 нм. Затем осуществляют количественный анализ клеточного альбумина, как описано выше. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы или его фармацевтически приемлемая соль,где R представляет собой -COOH или C1-C6-алкилэфир либо -NR1R2;R1 и R2 объединяются с образованием 4-7-членного гетероциклоалкильного кольца, содержащего 02 дополнительных гетероатома, независимо выбранных из N, О и S, причем кольцо является необязательно конденсированным с 5- или 6-членным гетероциклическим кольцом, содержащим 1 или 2 гетероатома, независимо выбранных из N, О и S, или 5- или 6-членным карбоциклическим кольцом с образованием бициклической кольцевой системы, каждый из которых (5-7-членное гетероциклоалкильное кольцо или бициклическая кольцевая система) является необязательно замещенным;R1 и R2, взятые вместе, образуют необязательно замещенное 5-9-членное мостиковое гетероциклическое кольцо, содержащее 0, 1 или 2 дополнительных атома N, S или О, или необязательно замещенное 5-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-7-членным карбоциклическим или гетероциклическим кольцом с образованием бициклической кольцевой системы, которая является мостиковой; илиR1 и R2, взятые вместе, образуют необязательно замещенное 4-7-членное гетероциклическое кольцо, содержащее 0 или 1 дополнительный атом N, S или О, конденсированное с необязательно замещенным 5-9-членным мостиковым карбоциклическим или гетероциклическим кольцом; или(b) C1-C6-алкил, C2-C6-алкенил, (C3-C7-циклоалкил)C0-C4-алкил, (арил)C0-C4-алкил, (гетероарил)C0C4-алкил, (C3-C7-циклоалкенил)C0-C4-алкил, (гетероциклоалкил)C0-C4-алкил, C2-C6-алканоил или моноили ди-C1-C6-алкиламиногруппу, каждый из которых является необязательно замещенным; илиD представляет собой C7-C11 насыщенную или ненасыщенную углеводородную цепь, которая является (i) ковалентно связанной с R7, где R7 представляет собой метиленовую или метановую группу, илиD представляет собой C7-C11 насыщенную или ненасыщенную углеводородную цепь, которая является(ii) ковалентно связанной с необязательно замещенным циклоалкильным кольцом, образованным R7 и R8,когда они объединяются с образованием 3-7-членного необязательно замещенного циклоалкильного кольца; Т представляет собой группу формулы(C3-C7-циклоалкенил)C0-C4-алкил, (C3-C7-циклоалкил)CH2SO2-, (С 3-C7-циклоалкил)CH2SO2NR10-, (гетероциклоалкил)C0-C4-алкил, (арил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2-алкил, каждый из которых необязательно является замещенным; илиR10, R11 и R12 представляют собой в каждом случае водород или трифторметил либо C1-C6-алкил,C2-C6-алкенил,C2-C6-алкинил,(арил)C0-C2-алкил,(C3-C7-циклоалкил)C0-C2-алкил,(C3-C7 циклоалкенил)C0-C2-алкил, (гетероциклоалкил)C0-C2-алкил или (5-10-членный гетероарил)C0-C2-алкил,каждый из которых необязательно является замещенным;R16 представляет 0-4 заместителя, которые являются независимо выбранными из галогена, C1-C2 алкила и C1-C2-алкоксигруппы;R18 и R19 представляют собой независимо водород, гидроксил, галоген, C1-C2-алкил, C1-С 2 алкоксигруппу, C1-C2-галоалкил или C1-C2-галоалкоксигруппу;Z представляет собой хинолин формулыR21 представляет собой заместитель в положении 7 хинолина и 0-2 дополнительных заместителя,независимо выбранных из галогена, гидроксила, аминогруппы, цианогруппы, -CONH2, -COOH, C1-C4 алкила, C2-C4-алканоила, C1-C4-алкоксигруппы, моно- и ди-C1-C4-алкиламиногруппы, C1-C2-галоалкила иR22 представляет собой тиазолил, который является замещенным 0, 1 или 2 заместителями, независимо выбранными из галогена, гидроксила, аминогруппы, цианогруппы, -COOH, -CONH2, C1-C4-алкила,C1-C4-алкоксигруппы, моно- и ди-C1-C4-алкиламиногруппы, трифторметила и трифторметоксигруппы,где термин "замещенный" означает, что любой один или более водородов на обозначенном атоме или группе замещается с использованием выбора из указанной группы при условии, что нормальная валентность обозначенного атома не превышается, указанная группа включает галоген; цианогруппу; гидроксил; нитрогруппу; азидогруппу; алканоил; карбоксамидогруппу; алкильную или циклоалкильную группы, имеющие примерно 1-8 атомов углерода; алкенильную и алкинильную группы, имеющие одну или более ненасыщенных связей и примерно 2-8 атомов углерода; алкоксигруппу, имеющую одну или более кислородных связей и примерно 1-8 атомов углерода; арилоксигруппу; алкилтиогруппу, имеющую одну или более тиоэфирных связей и примерно 1-8 атомов углерода; алкилсульфинильную группу, имеющую одну или более сульфинильных связей и примерно 1-8 атомов углерода; алкилсульфонильную группу,имеющую одну или более сульфонильных связей и примерно 1-8 атомов углерода; аминоалкильную группу, имеющую один или более атомов N и примерно 1-8 атомов углерода; арил, имеющий 6 или более углеродов и одно или более колец; арилалкил, имеющий 1-3 отдельных или конденсированных колец и примерно 6-18 атомов углерода в кольце; арилалкоксигруппу, имеющую 1-3 отдельных или конденсированных колец и примерно 6-18 атомов углерода в кольце; или насыщенную, ненасыщенную или ароматическую гетероциклическую группу, имеющую 1-3 отдельных или конденсированных колец примерно с 3-8 членами на кольцо и одним или более атомами N, О или S, где гетероциклическая группа может быть дополнительно замещенной гидроксигруппой, алкилом, алкоксигруппой, галогеном и аминогруппой. 2. Соединение или его соль по п.1, где R1 и R2 объединяются с образованием пирролидинового,морфолинового, пиперидинового или пиперазинового кольца, каждое из которых является замещенным 0-2 заместителями, независимо выбранными из фтора, аминогруппы, гидроксила, метила и трифторметила. 3. Соединение или его соль по п.1, где R1 и R2, взятые вместе, образуют группы формул: 4. Соединение или его соль по п.2, где R3 представляет собой водород или метил и R4 представляет собой водород или C1-C4-алкил. 5. Соединение или его соль по п.4, где R3 и R4 представляют собой независимо водород или метил. 6. Соединение или его соль по п.5 формулы где D представляет собой алкильную или алкенильную группу, имеющую 6-10 атомов углерода; иR3, R4, R6 и R8 представляют собой независимо водород или C1-C4-алкил. 7. Соединение или его соль по п.6 формулы 8. Соединение или его соль по п.5 формулы где D представляет собой алкильную или алкенильную группу, имеющую 6-10 атомов углерода; иR3, R4 и R6 представляют собой независимо водород или C1-C4-алкил. 9. Соединение или его соль по п.8 формулы
МПК / Метки
МПК: C07D 417/14, C07D 403/14, C07D 403/12
Метки: вирусов, циклические, аналоги, ингибиторы, пептидов, репликации, 4-амино-4-оксобутаноил
Код ссылки
<a href="https://eas.patents.su/30-21794-ciklicheskie-analogi-4-amino-4-oksobutanoil-peptidov-ingibitory-replikacii-virusov.html" rel="bookmark" title="База патентов Евразийского Союза">Циклические аналоги 4-амино-4-оксобутаноил пептидов, ингибиторы репликации вирусов</a>
Предыдущий патент: Способ контроля тормозной системы транспортной системы
Следующий патент: Колосник и колосниковая решетка
Случайный патент: Контейнер с корпусом и выдвижным элементом с двумя отделениями












