Аналоги гетероариламидов
Номер патента: 20332
Опубликовано: 30.10.2014
Авторы: Юань Цзюнь, Вустро Дэвид Дж., Капитости Скотт М., Бактхаватчалам Раджагопал, Айл Дэвид К.
Формула / Реферат
1. Соединение или его фармацевтически приемлемая соль формулы Ia или Ib
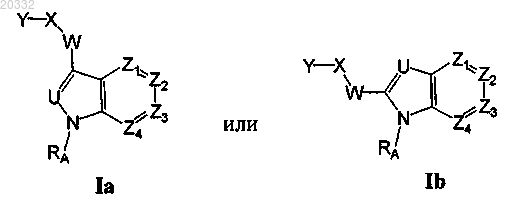
где U является СН или N;
W является -C(=O)NR4- или -NR4C(=O);
R4 означает водород;
X отсутствует или означает С1-С6алкилен, который необязательно замещен от 1 до 4 заместителями, выбранными из RB, RC, RD и RE;
RB, RC, RD и RE, каждая группа независимо, означают гидрокси, С1-С8алкил, (С3-С8циклоалкил)С0-С4алкил, (4-7-членный гетероциклоалкил)С0-С4алкил и фенилС0-С2алкил; или любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они связаны, образуют 3-7-членный циклоалкил или 4-7-членный гетероциклоалкил;
Y означает циклопропил, циклобутил, циклопентил, циклогексил, морфолинил, циклогептил, циклооктил, адамантил, миртанил, фенил или пиридил, каждый из которых необязательно замещен гидрокси, галогеном, С1-С6алкилом или С1-С6алкокси;
Z1, Z2, Z3 и Z4 независимо означают CR1 или N;
каждая группа R1 независимо означает водород, галоген, циано или аминокарбонил и
RA является группой формулы -L-A-M, где
L отсутствует;
А отсутствует и
M означает 5- или 6-членный гетероарил, содержащий по меньшей мере один атом азота, необязательно замещенный C1-С6алкилом, -СООН, СООС1-С6алкилом, CN или галогеном;
и ²гетероциклоалкил² означает 4-7-членный гетероциклоалкил, содержащий 1, 2, 3 или 4 атома в кольце, независимо выбранные из С, О, N и S.
2. Соединение или его фармацевтически приемлемая соль по п.1 формулы Ia.
3. Соединение или его фармацевтически приемлемая соль по п.1 формулы Ib.
4. Соединение или его фармацевтически приемлемая соль по любому из пп.1-3, где гетероарил в М содержит по меньшей мере один атом азота в кольце.
5. Соединение или его фармацевтически приемлемая соль по любому из пп.1-4, где гетероарил в M содержит по меньшей мере два атома азота в кольце.
6. Соединение или его фармацевтически приемлемая соль по любому из пп.1-5, где гетероарил в М означает пиримидинил.
7. Соединение или его фармацевтически приемлемая соль по п.1, где X означает С1-С2алкилен, замещенный С1-С4алкилом.
8. Соединение или его фармацевтически приемлемая соль по п.1, где группа X замещена по меньшей мере 2 заместителями, выбранными из RB, RC, RD и RE, где любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они соединены, образуют 3-7-членный циклоалкил.
9. Соединение или его фармацевтически приемлемая соль по п.3, где группа X замещена по меньшей мере 2 заместителями, выбранными из RB, RC, RD и RE, где любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они соединены, образуют 5-6-членный циклоалкил.
10. Соединение или его фармацевтически приемлемая соль по п.5, где Y означает адамантил, фенил, пиридил или морфолинил, каждый необязательно замещен гидрокси, галогеном, С1-С6алкилом или С1-С6алкокси.
11. Соединение или его фармацевтически приемлемая соль, где соединением является
N-(адамантан-1-илметил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{4-метил-2-[4-(трифторметил)фенил]пентил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)пентил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
1-пиримидин-2-ил-N-({1-[4-(трифторметил)фенил]циклогексил}метил)-1Н-индол-3-карбоксамид;
N-{[1-(4-хлорфенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(4-метоксифенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[(1-морфолин-4-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[4-метил-2-(4-метилфенил)пентил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-(4-метил-2-пиридин-3-илпентил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-(4-метил-2-фенилпентил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(6-метилпиридин-3-ил)циклогексил]метил}-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-{[1-(4-фторфенил)циклогексил]метил}-1-пиримидин-2-ил-1-Н-индол-3-карбоксамид;
1-(5-фторпиримидин-2-ил)-N-[(1-пиридин-3-илциклогексил)метил]-1Н-индол-3-карбоксамид;
1-(3-этилпиразин-2-ил)-N-[(1-пиридин-3-илциклогексил)метил]-1Н-индол-3-карбоксамид;
4-хлор-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-{[1-(4-метоксифенил)циклопентил]метил}-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-{[1-(4-метилфенил)циклогексил]метил}-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-{[1-(4-хлор-3-фторфенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
метил 2-(3-{[(1-пиридин-3-илциклогексил)метил]карбамоил}-1Н-индол-1-ил)никотинат;
N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
4-бром-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-циано-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(4-метоксифенил)циклогексил]метил}-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
N-{[1-(4-фторфенил)циклогексил]метил}-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
N-{[1-(6-метилпиридин-3-ил)циклогексил]метил}-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
7-хлор-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-фтор-N-(4-метил-2-пиридин-3-илпентил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-4-метилпентил]-4-фтор-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-фтор-N-[4-метил-2-(4-метилфенил)пентил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-фтор-N-{4-метил-2-[4-(трифторметил)фенил]пентил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(4-хлор-3-фторфенил)циклогексил]метил}-4-фтор-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-фтор-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-фтор-N-{[1-(4-метилфенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-фтор-N-{[1-(4-метоксифенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-фтор-N-{[1-(4-фторфенил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(4-хлорфенил)циклогексил]метил}-4-фтор-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
1-пиримидин-2-ил-1H-индол-3,4-дикарбоновой кислоты 4-амид 3-[(1-пиридин-3-илциклогексилметил)амид];
1-[(1-метил-1Н-имидазол-2-ил)метил]-N-[(1-пиридин-3-илциклогексил)метил]-1Н-индол-2-карбоксамид;
4-метил-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-метил-N-(4-метил-2-пиридин-3-илпентил)-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-{[1-(4-метоксифенил)циклогексил]метил}-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-4-метилпентил]-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-{[1-(4-хлорфенил)циклогексил]метил}-4-метил-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
N-[2-(4-хлорметил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-4-(трифторметил)-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-4-фтор-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-4-фтор-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-фтор-N-[2-(6-метоксипиридин-3-ил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
N-[2-(6-метоксипиридин-3-ил)-2-пиперидин-1-илэтил]-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-(адамантан-1-илметил)-4-метил-1-пиримидин-2-ил-1Н-индол-3 -карбоксамид;
4-хлор-N-[2-(4-хлорфенил)-2-пиперазин-1-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-(2-морфолин-4-ил-2-фенилэтил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-{2-пиперидин-1-ил-2-[4-(трифторметил)фенил]этил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[2-(4-хлор-3-фторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-[2-(6-метоксипиридин-3-ил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[2-(3,4-дифторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
3-хлор-1-[(1-метил-1Н-имидазол-2-ил)метил]-N-(4-метил-2-пиридин-3-илпентил)-1Н-индол-2-карбоксамид;
4-хлор-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-(4-метил-2-пиридин-3-илпентил)-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
2-адамантан-1-ил-N-(4-хлор-1-пиримидин-2-ил-1Н-индол-3-ил)ацетамид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (адамантан-1-илметил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (2-адамантан-1-илэтил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты ((R)-6,6-диметилбицикло[3.1.1]гепт-2-илметил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (4-метил-2-р-толилпентил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [2-(4-хлорфенил)-4-метилпентил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [1-(4-хлорфенил)циклогексилметил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [1-(4-трифторметилфенил)циклогексилметил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [4-(4-хлорфенил)тетрагидропиран-4-илметил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [1-(4-метоксифенил)циклогексилметил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [4-метил-2-(4-трифторметилфенил)пентил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [2-(4-хлорфенил)пентил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (4-метил-2-пиридин-3-илпентил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [1-(4-хлорфенил)циклобутилметил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (2-адамантан-1-ил-2-гидроксиэтил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (3-метилбутил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (2-фенилпентил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (4-метил-2-фенилпентил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (3-циклопентил-2-фенилпропил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (2-циклогексил-2-фенилэтил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (2,3-дифенилпропил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (3-фенилбутил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (4-фенилбутил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [2-(4-бромфенил)этил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (3,3,5-триметилциклогексил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты адамантан-2-иламид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты циклогептилметиламид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты [2-(2-бромфенил)этил]амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты ((1S,2R)-2-гидроксициклогексилметил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (1-гидроксициклогексилметил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (1-гидроксициклопентилметил)амид;
4-хлор-1-пиримидин-2-ил-1Н-индол-3-карбоновой кислоты (4-гидрокситетрагидротиопиран-4-илметил)амид;
N-[2-(4-фторфенил)-2-пиперидин-1-илэтил]-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(3,4-дифторфенил)-2-пиперидин-1-илэтил]-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-метил-N-(2-морфолин-4-ил-2-фенилэтил)-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-4-метил-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
3-хлор-N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-1-[(1-метил-1Н-имидазол-2-ил)метил]-1Н-индол-2-карбоксамид;
N-{[4-(4-хлорфенил)тетрагидро-2Н-пиран-4-ил]метил}-4-метил-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
3-хлор-N-{[4-(4-хлорфенил)тетрагидро-2Н-пиран-4-ил]метил}-1-[(1-метил-1Н-имидазол-2-ил)метил]-1Н-индол-2-карбоксамид;
N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-4-метил-1-пиразин-2-ил-1H-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-4-метил-1-пиразин-2-ил-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-1-(3-цианопиридин-2-ил)-4-метил-1Н-индол-3-карбоксамид;
1-(3-цианопиридин-2-ил)-4-метил-N-(2-морфолин-4-ил-2-фенилэтил)-1Н-индол-3-карбоксамид;
N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-1-(3-цианопиридин-2-ил)-4-метил-1Н-индол-3-карбоксамид;
4-метил-N-(4-метил-2-морфолин-4-илпентил)-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-{2-пиперидин-1-ил-2-[6-(трифторметил)пиридин-3-ил]этил}-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-[2-(4-фторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[(1-гидроксициклогептил)метил]-1-пиримидин-2-ил-1H-индол-3-карбоксамид;
4-хлор-N-[2-(3,4-дифторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[2-(2,4-дифторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-индол-3-карбоксамид;
4-хлор-N-[2-(4-хлорфенил)-2-морфолин-4-илэтил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-[2-(4-хлорфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-{[4-(4-хлорфенил)тетрагидро-2Н-пиран-4-ил]метил}-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-[(1-гидроксициклогептил)метил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-[(1-гидроксициклогексил)метил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-[2-(3,4-дифторфенил)-2-пиперидин-1-илэтил]-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид;
4-хлор-N-(2-морфолин-4-ил-2-фенилэтил)-1-пиримидин-2-ил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид или
4-хлор-N-{[1-(4-метилпиперазин-1-ил)циклогексил]метил}-1-пиримидин-2-ил-1Н-индол-3-карбоксамид.
12. Фармацевтическая композиция, содержащая по меньшей мере одно соединение или его фармацевтически приемлемую соль по любому одному из пп.1-11 в комбинации с физиологически приемлемым носителем или наполнителем, для лечения у больного состояния, отвечающего на модуляцию рецептора Р2Х7.
Текст
Соединения и фармацевтические композиции описаны относительно аналогов гетероариламидов формулы Ia и/или Ib Указанные аналоги гетероариламидов являются агонистами и/или лигандами допаминовых рецепторов и могут быть пригодными, наряду с прочими, для лечения состояния, отвечающего на модуляцию рецептора Р 2 Х 7. Область техники, к которой относится изобретение Настоящее изобретение относится в целом к аналогам гетероариламидов, проявляющим полезные фармакологические свойства. Изобретение дополнительно относится к применению таких соединений для лечения состояний, связанных с активацией рецептора Р 2 Х 7. Уровень техники Восприятие боли, или ноцицепция, опосредуется периферическими окончаниями группы специализированных сенсорных нейронов, названных "болевыми рецепторами" (ноцицепторами). Широкий ряд физических и химических стимулов индуцируют активацию таких нейронов у млекопитающих, приводящую к распознаванию потенциально неблагоприятного стимула. Несоответствующая или избыточная активация болевых рецепторов, однако, может приводить к ослаблению острой или хронической боли. Неврологическая боль, которая обычно возникает в результате повреждения нервной системы, вовлекает передачу болевого сигнала в отсутствие раздражителя, боль от обычно нейтрального раздражителя (аллодиния) и повышенную боль от обычно болезненного раздражителя (гипералгезия). В большинстве случаев, как полагают, неврологическая боль возникает вследствие сенсибилизации в периферической и центральной нервной системе после первоначального повреждения периферической системы (например, посредством прямого повреждения или системного заболевания). Неврологическая боль обычно бывает жгучей, внезапной и неослабевающей по интенсивности и иногда может быть более изнуряющей,чем первоначальное повреждение или патологический процесс, вызывающий боль. Существующие терапии неврологической боли обычно являются субоптимальными. Опиаты, такие как морфин, являются сильными аналгетиками, но их пригодность ограничена из-за неблагоприятных побочных эффектов, таких как привыкание (зависимость) и синдром отмены, а также угнетение дыхания,изменения настроения и снижение перистальтики кишечника с сопровождающимися явлениями - запором, тошнотой, рвотой, и изменения в эндокринной и вегетативной нервной системе. Кроме того, неврологическая боль часто является невосприимчивой или только частично восприимчивой к обычным схемам лечения опиодными аналгезирующими средствами, или к лечению другими лекарственными средствами, такими как габапентин. Лечения с использованием антагониста N-метил-D-аспартатного рецептора, кетамина, или (2)-адренергического агониста, клонидина, могут привести к снижению острой или хронической боли и уменьшению потребления опиоида, но указанные средства часто плохо переносятся из-за побочных эффектов. Другим общим состоянием, для которого существующие терапии представляются недостаточными или проблематичными, является воспаление. Преходящее воспаление является благоприятным механизмом (положительным эффектом), который защищает организм млекопитающих от проникающих в него патогенных микроорганизмов. Неконтролируемое воспаление, однако, вызывает повреждение ткани и боль и является основной причиной многих заболеваний, включающих астму, а также другие аллергические, инфекционные, аутоиммунные, дегенеративные и идиопатические заболевания. Существующие терапии часто проявляют низкую, замедленную или только временную эффективность, нежелательные побочные эффекты и/или отсутствие избирательности. До сих пор сохраняется необходимость в новых лекарственных средствах, которые смогут преодолеть один или более из недостатков лекарственных средств, постоянно используемых для иммуносупрессии или в лечении или предотвращении воспалительных нарушений, включающих аллергические расстройства, аутоиммунные расстройства, фиброгенные нарушения и нейродегенеративные заболевания, такие как боковой амиотрофический склероз, болезнь Альцгеймера и болезнь Гентингтона. Рецептор Р 2 Х 7 является лиганд-зависимым ионным каналом, который активируется АТР и присутствует на ряде типов клеток, включающих микроглию в центральной нервной системе и клетки, вовлеченные в воспаление и функцию иммунной системы, такие как иммунокомпетентные клетки. В частности, рецептор Р 2 Х 7 вовлекается в активацию лимфоцитов и моноцитов/макрофагов, приводящую к увеличению степени высвобождения провоспалительных цитокинов (например, TNF и IL-1) из указанных клеток. Недавние исследования показали, что ингибирование активации рецептора Р 2 Х 7 в случаях воспаления (например, ревматоидный артрит и другие аутоиммунные заболевания, остеоартрит, увеит, астма, хроническое обструктивное легочное заболевание и воспалительное заболевание кишечника) или интерстициального фиброза приводит к терапевтическому эффекту. Указанные выше исследования и другие исследования свидетельствуют о том, что антагонисты рецептора Р 2 Х 7 могут найти применение в лечении и профилактике боли, включающей острую, хроническую и неврологическую боль, а также при ряде других состояний, включающих остеоартрит, ревматоидный артрит, атеросклероз, воспалительное заболевание кишечника, болезнь Альцгеймера, травматическое повреждение головного мозга, астму,хроническое обструктивное легочное заболевание и фиброз внутренних органов (например, интерстициальный фиброз). Низкомолекулярные антагонисты рецептора Р 2 Х 7 являются желательными для таких терапий. Настоящее изобретение удовлетворяет данному требованию и предоставляет также связанные с этим преимущества. Сущность изобретения Настоящее изобретение относится к аналогам гетероариламидов формулы Ia или Ib где U является СН или N;X отсутствует или означает С 1-С 6 алкилен, который необязательно замещен от 1 до 4 заместителями,выбранными из RB, RC, RD и RE;RB, RC, RD и RE каждая группа независимо означает гидрокси, С 1-С 8 алкил, (С 3-С 8 циклоалкил)С 0 С 4 алкил, (4-7-членный гетероциклоалкил)С 0-С 4 алкил и фенилС 0-С 2 алкил; или любые две группы из RB,RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они связаны, образуют 3-7-членный циклоалкил или 4-7-членный гетероциклоалкил;Y означает циклопропил, циклобутил, циклопентил, циклогексил, морфолинил, циклогептил, циклооктил, адамантил, миртанил, фенил или пиридил, каждый из которых необязательно замещен гидрокси, галогеном, С 1-С 6 алкилом или С 1-С 6 алкокси;Z1, Z2, Z3 и Z4 независимо означают CR1 или N; каждая группа R1 независимо означает водород, галоген, циано или аминокарбонил; и RA является группой формулы -L-A-M, гдеL отсутствует; А отсутствует; и М означает 5- или 6-членный гетероарил, содержащий по меньшей мере один атом азота, необязательно замещенный C1-С 6 алкилом, -СООН, COOC1-С 6 алкилом, CN или галогеном. В некоторых аспектах аналоги гетероариламидов формулы Ia и/или Ib являются антагонистами рецептора Р 2 Х 7 с величиной IC50, составляющей не выше чем 20 мкм/л (micromolar), 10 мкм/л, 5 мкм/л, 1 мкм/л, 500 нм/л или 100 нм/л в in vitro исследовании при определении антагонистической активности соединений относительно рецептора Р 2 Х 7. В некоторых вариантах осуществления изобретения такие антагонисты рецептора Р 2 Х 7 проявляют не детектируемую агонистическую активность в in vitro анализе активности рецептора Р 2 Х 7 (например, в анализе, приведенном в примере 7 описания) при концентрации, равной IC50, в 10 раз выше IC50 или в 100 раз выше IC50 и/или при концентрации 2500 нМ. Настоящее изобретение также относится, в других аспектах, к фармацевтическим композициям, содержащим по меньшей мере один аналог гетероариламида, приведенный в описании, в комбинации с физиологически приемлемым носителем или наполнителем. Указанные выше и другие аспекты изобретения будут очевидны при обращении к следующему подробному описанию. Подробное описание иллюстративных вариантов осуществления изобретения Терминология Соединения описаны, как правило, с использованием стандартной номенклатуры. Относительно соединений, имеющих асимметричные центры, следует понимать (если не указано иное), что все оптические изомеры и их смеси включены в описание. Кроме того, соединения с углерод-углеродными двойными связями могут быть в Z- и Е-формах, все изомерные формы соединений включены в настоящее изобретение, если не указано иное. Фраза "аналог гетероариламида", используемый в описании, охватывает все соединения формулы Ia или Ib, а также соединения других формул, представленных в описании (включая любые энантиомеры,рацематы и стереоизомеры, и включая различные кристаллические формы и полиморфы), и фармацевтически приемлемые соли, сольваты (например, гидраты, включающие гидраты солей), амиды и сложные эфиры таких соединений."Фармацевтически приемлемая соль" соединения, представленного в описании, представляет собой соль кислоты или соль основания, которая является подходящей для ее использования в контакте с тканями людей или животных без повышенной токсичности и канцерогенности и предпочтительно без раздражения, аллергической реакции или другой проблемы или осложнения. Такие соли включают соли,образованные из минеральных и органических кислот и основных остатков, таких как амины, а также соли щелочных металлов и органические соли, образованные из кислотных остатков, таких как карбоновые кислоты. Отдельные фармацевтически приемлемые анионы, участвующие в образовании соли,включают, но не ограничиваются ими, такие ионы, как ацетат, 2-ацетоксибензоат, аскорбат, бензоат, бикарбонат, бромид, кальция эдетат, карбонат, хлорид, цитрат, дигидроксихлорид, дифосфат, дитартрат,-2 020332(трифторметансульфонат) и тозилат (р-толуолсульфонат), таннат, тартрат, теоклат и триэтиодид. Аналогично, фармацевтически приемлемые катионы, участвующие в образовании солей, включают, но не ограничиваются ими, такие ионы, как аммоний, бензатин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин, прокаин, и ионы металлов, таких как алюминий, кальций, литий, магний, калий, натрий и цинк. Специалисты в данной области также смогут определить фармацевтически приемлемые соли для соединений, представленных в описании. В целом, фармацевтически приемлемая соль кислоты или основания может быть синтезирована из родительского соединения, которое содержит основный или кислотный фрагмент, любым обычным химическим методом. Кратко, такие соли могут быть получены путем взаимодействия указанных соединений в виде свободных кислот или оснований со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе или в смеси из двух растворителей; обычно, использование неводных сред, таких как эфир, этилацетат,этанол, метанол, изопропанол или ацетонитрил, является предпочтительным. Очевидно, что каждое соединение, представленное в описании, может быть, но не обязательно, получено в виде сольвата (например, гидрата) или нековалентного комплекса. Кроме того, различные кристаллические формы или полиморфы включены в объем настоящего изобретения. Также включенными являются пролекарства соединений перечисленных формул."Пролекарство" является соединением, которое может не полностью удовлетворять структурным требованиям соединений, представленных в описании, но которые модифицируются in vivo после введения больному с образованием соединения формулы, представленной в описании. Например, пролекарство может быть ацилированным производным такого соединения. Пролекарства включают соединения,где гидроксигруппа, аминогруппа и сульфгидрильная группа связаны с любой группой так, что при введении млекопитающему субъекту связь расщепляется с образованием свободной гидроксигруппы, аминогруппы или сульфгидрильной группы, соответственно. Примеры пролекарств включают, но не ограничиваются ими, ацетатные, формиатные, бензоатные и пептидные производные спиртовых или аминных функциональных групп у соединения, представленного в описании. В большинстве случаев, пролекарства могут быть получены модификацией функциональных групп, представленных в соединениях,так, что модификации расщепляются in vivo с получением родительских соединений. Используемый в описании термин "алкил" относится к насыщенному алифатическому углеводороду с прямой или разветвленной цепью. Алкильные группы включают группы, содержащие от 1 до 8 атомов углерода (С 1-С 8 алкил), от 1 до 6 атомов углерода (С 1-С 6 алкил) и от 1 до 4 атомов углерода (C1 С 4 алкил), такие как метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил, 2-пентил,изопентил, неопентил, гексил, 2-гексил, 3-гексил и 3-метилпентил. "C0-Cnалкил" относится к простой ковалентной связи (С 0) или алкильной группе, содержащей от 1 до n атомов углерода; например, "С 0 С 4 алкил" относится к простой ковалентной связи или C1-С 4 алкильной группе. В некоторых примерах заместитель алкильной группы указан особо. Например, "С 1-С 6 гидроксиалкил" означает C1-С 6 алкильную группу, замещенную по меньшей мере одной группой -ОН; "C1-С 6 аминоалкил" означает C1-С 6 алкильную группу, замещенную по меньшей мере одной группой -NH2; C1-С 6 цианоалкил означает C1-С 6 алкильную группу, замещенную по меньшей мере одной группой -CN."Алкенил" относится к алкенам с прямой или разветвленной цепью, которые содержат по меньшей мере одну ненасыщенную углерод-углеродную связь. Алкенильные группы включают С 2 С 8 алкенильные, С 2-С 6 алкенильные и С 2-С 4 алкенильные группы, которые содержат от 2 до 8, от 2 до 6 и от 2 до 4 атомов углерода, соответственно, такие как этенил, аллил или изопропенил. "С 2 С 6 цианоалкенил" означает С 2-С 6 алкенильную группу, замещенную по меньшей мере одной группой -CN."Алкинил" относится к алкинам с прямой или разветвленной цепью, содержащим одну или более насыщенные углерод-углеродные связи, по меньшей мере одна из которых представляет собой тройную связь. Алкинильные группы включают С 2-С 8 алкинильные, С 2-С 6 алкинильные и С 2-С 4 алкинильные группы, содержащие от 2 до 8, от 2 до 6 и от 2 до 4 атомов углерода, соответственно."Алкилен" относится к двухвалентной алкильной группе, как определено выше. С 1-С 2 алкилен означает метилен или этилен; С 0-С 4 алкилен означает простую ковалентную связь или алкиленовую группу,содержащую 1, 2, 3 или 4 атома углерода; С 0-С 2 алкилен означает простую ковалентную связь, метилен или этилен, "C1-С 6 алкилен, который необязательно модифицирован заменой углерод-углеродной простой связи двойной или тройной углерод-углеродной связью" означает С 1-С 6 алкиленовую группу, как описано выше, или двухвалентный С 2-С 6 алкен или С 2-С 6 алкин."Циклоалкил" означает группу, содержащую одно или более насыщенные и/или частично насыщенные кольца, в которых все члены кольца являются углеродами, такие как циклопропил, циклобутил,-3 020332 циклопентил, циклогексил, циклогептил, циклооктил, адамантил, миртанил и частично насыщенные варианты указанных выше соединений, такие как циклогексенил. Циклоалкильные группы не содержат ароматическое кольцо или гетероциклическое кольцо. Некоторые циклоалкильные группы означают С 3 С 7 циклоалкил, у которого циклоалкильная группа включает одно кольцо, содержащее от 3 до 7 членов кольца, все из которых являются атомами углерода. "(С 3-С 7 циклоалкил)С 0-С 4 алкил" означает С 3 С 7 циклоалкильную группу, связанную через простую ковалентную связь, или С 1-С 4 алкиленовую группу."(С 4-С 7 циклоалкил)С 0-С 4 алкилен" означает двухвалентную (С 3-С 7 циклоалкил)С 0-С 4 алкильную группу, связанную через две простые ковалентные связи с двумя указанными фрагментами. Обычно,одна простая ковалентная связь расположена на циклической части, и другая расположена на алкиленовой части, если присутствует; альтернативно, если алкиленовая группа не присутствует, обе простые ковалентные связи находятся у разных членов кольца. Например, относительно группы RA, если А означает Под "алкокси", как используют в описании, подразумевают алкильную группу, как описано выше,присоединенную через кислородный мостик. Алкоксигруппы включают C1-С 6 алкоксигруппы и С 1 С 4 алкоксигруппы, содержащие от 1 до 6 или от 1 до 4 атомы углерода, соответственно. Метокси, этокси,пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, н-пентокси, 2-пентокси, 3-пентокси, изопентокси, неопентокси, гексокси, 2-гексокси, 3-гексокси и 3-метилпентокси являются характерными примерами алкоксигрупп. Термин "оксо", употребляемый в описании, относится к кислородному заместителю атома углерода, который приводит к образованию карбонильной группы (С=O). Оксогруппа, являющаяся заместителем неароматического атома углерода, приводит к превращению -СН 2- в -C(=O)-. Оксогруппа, являющаяся заместителем ароматического атома углерода, приводит к превращению -СН в -С(=O)- и может приводить к потере ароматичности. Термин "алканоил" относится к ацильной группе (например, -(С=O)-алкил), у которой атомы углерода располагаются линейно или разветвлено, и где присоединение происходит через углерод кетогруппы. Алканоильные группы имеют указанное число атомов углерода, с углеродом кетогруппы, включенным в занумерованные атомы углерода. Например, С 2 алканоильная группа означает (С=О)СН 3. Алканоильные группы включают, например, С 2-С 8 алканоильные, С 2-С 6 алканоильные и С 2-С 4 алканоильные группы, содержащие от 2 до 8, от 2 до 6 или от 2 до 4 атома углерода, соответственно. "С 1 алканоил" относится к -(С=О)Н, который (наряду с С 2-С 8 алканоилом) охватывается термином "C1-С 8 алканоил"."Алкиловый простой эфир" относится к линейному или разветвленному эфирному заместителю(т.е. алкильной группе, которая замещается алкоксигруппой). Алкильные эфирные группы включают С 2 С 8 алкильные эфирные группы, С 2-С 6 алкильные эфирные группы и С 2-С 4 алкильные эфирные группы,содержащие от 2 до 8, 6 или 4 атома углерода, соответственно. С 2 алкильным эфирным заместителем является -СН 2-О-СН 3. Термин "алкоксикарбонил" относится к алкоксигруппе, присоединенной через кетомостик (-(С=O)-)(т.е. группа, имеющая общую структуру -С(=O)-O-алкил). Алкоксикарбонильные группы включают C1C8, C1-С 6 и С 1-С 4 алкоксикарбонильные группы, содержащие от 1 до 8, 6 или 4 атома углерода, соответственно, в алкильной части группы (т.е. углерод кетомостика не включен в указанное число атомов углерода). "С 1 алкоксикарбонил" относится к -С(=O)-О-СН 3; С 3 алкоксикарбонил означает -С(=O)-О(СН 2)2 СН 3 или -С(=O)-O- (CH)(СН 3)2."Алканоилокси", употребляемый в описании, относится к алканоильной группе, связанной через кислородный мостик (т.е. группа, имеющая общую структуру -O-C(=O)-алкил). Алконоилоксигруппы включают C1-C8, C1-C6 и C1-С 4 алканоилоксигруппы, содержащие от 1 до 8, 6 или 4 атома углерода, соответственно, в алкильной части группы. Например, "С 1 алканоилокси" относится к -O-C(=O)-СН 3. Аналогично, "алканоиламино", употребляемый в описании, относится к алканоильной группе, связанной через азотный мостик (т.е. группа, имеющая общую структуру -N(R)-С(=O)-алкил), у которой R означает водород или C1-С 6 алкил. Алканоиламиногруппы включают C1-С 8, C1-С 6 и С 1 С 4 алканоиламиногруппы, содержащие от 1 до 8, 6 или 4 атома углерода в алканоильной группе, соответственно, в алкильной части группы."Алкилсульфонил" относится к группам формулы -(SO2)-алкил, у которых атом серы является точкой присоединения. Алкилсульфонильные группы включают C1-С 6 алкилсульфонильные и С 1 С 4 алкилсульфонильные группы, содержащие от 1 до 6 или от 1 до 4 атома углерода, соответственно. Метилсульфонил является одним характерным примером алкилсульфонильной группы. "C1 С 4 галогеналкилсульфонил" означает алкилсульфонильную группу, содержащую от 1 до 4 атома углерода и замещенную по меньшей мере одним галогеном (например, трифторметилсульфонил)."Аминосульфонил" относится к группам формулы -(SO2)-NH2, у которых атом серы является точ-4 020332 кой присоединения. Термин "моно- или ди-(C1-С 6 алкил)аминосульфонил" относится к группам, удовлетворяющим формуле -(SO2)-NR2, в которой атом серы является точкой присоединения и в которой одна группа R означает C1-С 6 алкил, и другая группа R означает водород или независимо выбранный C1 С 6 алкил."Алкиламиноалкил" относится к алкиламиногруппе, связанной через алкиленовую группу (т.е. группа, имеющая общую структуру -алкилен-NH-алкил или -алкилен-N(алкил)(алкил, у которой каждый алкил выбран независимо из алкильных, циклоалкильных и (циклоалкил)алкильных групп. Алкиламиноалкильные группы включают, например, моно- и ди-(С 1-С 8 алкил)аминоС 1-С 8 алкил, моно- и ди-(C1 С 6 алкил)аминоС 1-С 6 алкил и моно- и ди-(C1-С 6 алкил)аминоС 1-С 4 алкил. "Моно- или ди-(C1-С 6 алкил) аминоС 0-С 6 алкил" относится к моно- или ди-(C1-С 6 алкил)аминогруппе, связанной посредством простой ковалентной связи или C1-С 6 алкиленовой группы. Следующие формулы представляют собой характерные примеры алкиламиноалкильных групп Очевидно, что определение "алкил", употребляемое в терминах "алкиламино" и "алкиламиноалкил", отличается от определения "алкил", используемого для всех других алкилсодержащих групп, с включением циклоалкильных и (циклоалкил)алкильных групп (например, (С 3-С 7 циклоалкил)С 0 С 6 алкил). Термин "аминокарбонил" относится к амидной группе (т.е. -(C=O)NH2). "Моно- или ди-(С 1 С 6 алкил)аминокарбонил" относится к группам формулы -(С=O)-N(R)2, в которой карбонил является точкой присоединения, одна группа R означает C1-С 6 алкил, и другая группа R означает водород или независимо выбранный C1-С 6 алкил."Моно- или ди-(C1-С 6 алкил) аминокарбонилС 0-С 4 алкил" означает аминокарбонильную группу, у которой один или оба атома водорода заменены C1-С 6 алкилом и которая связана посредством простой ковалентной связи (т.е. моно- или ди-(C1-С 6 алкил)аминокарбонил) или С 1-С 4 алкиленовой группы (т.е. (С 0-С 4 алкил)-(С=O)N(C1-С 6 алкил)2). Если оба атома водорода заменены таким образом, C1-С 6 алкильные группы могут быть одинаковыми или разными. Термин "аминосульфонил" относится к сульфонамидной группе (т.е. -(SO2)NH2). "Моно- или ди(С 1-С 8 алкил)аминосульфонил" относится к группам формулы - (SO2)-N(R)2, в которой атом серы является точкой присоединения, одна группа R означает C1-С 8 алкил, и другая группа R означает водород или независимо выбранный С 1-С 8 алкил."Моно- или ди-(C1-С 6 алкил)аминосульфонилС 0-С 4 алкил" означает аминосульфонильную группу, у которой один или оба атома водорода заменены C1-С 6 алкилом, и которая связана посредством простой ковалентной связи (т.е. моно- или ди-(C1-С 6 алкил)аминосульфонил) или С 1-С 4 алкиленовой группы (т.е.(C1-С 4 алкил)-(SO2)N(С 1-С 6 алкил)2). Если оба атома водорода заменены таким образом, С 1-С 6 алкильные группы могут быть одинаковыми или разными. Термин "галоген" относится к фтору, хлору, брому или йоду."Галогеналкил" является алкильной группой, которая замещена 1 или более независимо выбранными галогенами (например, "C1-С 6 галогеналкильные" группы содержат от 1 до 6 атомов углерода). Примеры галогеналкильных групп включают, но не ограничиваются ими, моно-, ди- или трифторметил; моно-, ди- или трихлорметил; моно-, ди-, три-, тетра- или пентафторэтил; моно-, ди-, три-, тетра- или пентахлорэтил и 1,2,2,2-тетрафтор-1-трифторметилэтил. Типичными галогеналкильными группами являются трифторметил и дифторметил. Термин "галогеналкокси" относится к галогеналкильной группе, как определено выше, которая связана посредством кислородного мостика. Черточка ("-"), которая находится между двумя буквами или символами, используется для обозначения точки присоединения заместителя. Например, -CONH2 присоединяется через атом углерода."Карбоцикл" или "карбоциклическая группа" включает по меньшей мере одно кольцо, образованное только углерод-углеродными связями (названное в описании как карбоциклическое кольцо), и не содержит гетероцикл. Если не указано иное, каждое кольцо в карбоцикле может быть независимо насыщенным, частично насыщенным или ароматическим, и необязательно замещенным, как указано. Обычно карбоцикл содержит от 1 до 3 конденсированных, подвешенных или спироколец и необязательно также содержит один или более алкиленовых мостиков; карбоциклы в некоторых вариантах осуществления изобретения имеют одно кольцо или два конденсированных кольца. Обычно, каждое кольцо содержит от 3 до 8 членов кольца (т.е. С 3-С 8); С 5-С 7 кольца перечислены в некоторых вариантах осуществления изобретения. Карбоциклы, содержащие конденсированные, подвешенные или спирокольца, обычно включают от 9 до 16 членов кольца. Некоторыми характерными примерами карбоциклов являются циклоалки-5 020332 ют от 9 до 16 членов кольца. Некоторыми характерными примерами карбоциклов являются циклоалкилы, как описано выше (например, циклогексил, циклогептил или адамантил). Другими карбоциклами являются арилы (т.е. содержат по меньшей мере одно ароматическое карбоциклическое кольцо с или без одного или более дополнительных ароматических и/или циклоалкильных колец). Такие арильные карбоциклы включают, например, фенил, нафтил (например, 1-нафтил и 2-нафтил), фторенил, инданил и 1,2,3,4-тетрагидронафтил. Термин "галогенарил" относится к арильной группе, которая замещена по меньшей мере одним галогеном. Некоторые карбоциклы, перечисленные в описании, представляют собой С 6-С 10 арилС 0 С 8 алкильные группы (т.е. группы, у которых 6-10-членная карбоциклическая группа, включающая по меньшей мере одно ароматическое кольцо, связана посредством простой ковалентной связи или С 1 С 8 алкиленовой группы). Фенильные группы, связанные посредством простой ковалентной связи или C1 С 2 алкиленовой группы, обозначают фенилС 0-С 2 алкил (например, бензил, 1-фенилэтил и 2-фенилэтил)."Гетероцикл" или "гетероциклическая группа" содержит от 1 до 3 конденсированных, подвешенных или спироколец, по меньшей мере одно из которых является гетероциклическим кольцом (т.е. один или более атом в кольце представляет собой гетероатом, независимо выбранный из О, S и N, с остальными атомами в кольце, представленными углеродом). Дополнительными кольцами, если присутствуют, могут быть гетероциклические или карбоциклические кольца. Обычно, гетероциклическое кольцо содержит 1,2, 3 или 4 гетероатома; в некоторых вариантах осуществления изобретения каждое гетероциклическое кольцо содержит 1 или 2 гетероатома на кольцо. Каждое гетероциклическое кольцо обычно содержит от 3 до 8 членов в кольце (кольца, имеющие от 4 или 5 до 7 членов в кольце, перечислены в описании в некоторых вариантах осуществления изобретения), и гетероциклы, включающие конденсированные, подвешенные или спирокольца, обычно содержат от 9 до 14 членов в кольце. Некоторые гетероциклы содержат атом серы в качестве члена кольца; в некоторых вариантах осуществления изобретения атом серы окислен до SO или SO2. Если не указано иное, гетероциклом может быть гетероциклоалкильная группа(т.е. каждое кольцо насыщено или частично насыщено), такая как 4-7-членный гетероциклоалкил, который обычно содержит 1, 2, 3 или 4 атома в кольце, независимо выбранные из С, О, N и S; или гетероарильная группа (т.е. по меньшей мере одно кольцо в группе является ароматическим), такая как 5-10 членный гетероарил (который может быть моноциклическим или бициклическим), или 6-членный гетероарил (например, пиридил или пиримидил). N-связанные гетероциклические группы соединены через компонент атом азота. Как используют в описании, "аралкил" относится к фрагменту, состоящему из алкильного радикала,несущего арильный заместитель, где аралкильный фрагмент содержит приблизительно от 7 до 50 атомов углерода (и все комбинации и субкомбинации наборов и определенное число атомов углерода) и где арил и алкил имеют, как ранее определено, приблизительно от 7 до 11 атомов углерода, будучи предпочтительными. Неограниченные примеры включают, например, бензил, дифенилметил, трифенилметил, или -фенилэтил и дифенилэтил. Как используют в описании, "гетероаралкил" относится к кольцевой системе, состоящей из гетероарилом замещенного алкильного радикала, где гетероарил и алкил являются такими, как определено ранее, и где гетероаралкильная группа содержит приблизительно от 7 до 50 атомов углерода (и все комбинации и субкомбинации диапазонов и определенные числа атомов углерода). Неограниченные примеры включают, например, 2-(1 Н-пиррол-3-ил)этил, 3-пиридилметил, 5-(2 Н-тетразолил)метил и 3(пиримидин-2-ил)-2-метилциклопентанил."ГетероциклС 0-С 4 алкил" означает гетероциклическую группу, связанную посредством простой ковалентной связи или C1-С 4 алкиленовой группы. "(4-7-Членный гетероциклоалкил)С 1-С 4 алкил" означает гетероциклоалкильное кольцо, содержащее от 4 до 7 членов в кольце, которое связано через С 1 С 4 алкиленовую группу."(4-7-Членный гетероциклоалкил)С 0-С 4 алкилен" означает двухвалентную (4-7-членный гетероциклоалкил)С 0-С 4 алкильную группу, которая связана посредством двух простых ковалентных связей с двумя определенными фрагментами. Вообще, одна такая простая ковалентная связь расположена на циклической части, и другая расположена на алкиленовой части, если присутствует; альтернативно, если алкиленовая группа отсутствует, обе такие простые ковалентные связи расположены у разных членов кольца. Например, относительно группы RA, если А означает (пиперидинил) С 2 алкилен, и М означает СООН,один фрагмент RA, образованный таким образом, представляет собой"Заместитель", как используют в описании, относится к молекулярному фрагменту, который ковалентно связан с атомом в интересующей молекуле. Например, кольцевым заместителем может быть фрагмент, такой как галоген, алкильная группа, галогеналкильная группа или другая группа, которая ковалентно связана с атомом (предпочтительно атом углерода или азота), который является членом кольца. Заместители ароматических групп обычно ковалентно связаны с атомом углерода кольца. Термин "за-6 020332 мещение" относится к замене атома водорода в структуре молекулы заместителем, так что валентность означенного атома не становится больше и так что химически устойчивое соединение (т.е. соединение,которое может быть выделено, охарактеризовано и исследовано на биологическую активность) образуется в результате замещения. Группы, которые являются "необязательно замещенными", не замещены или замещены отличной от водорода группой у одного или более доступных положений, обычно 1, 2, 3, 4 или 5 положений, одной или более подходящими группами (которые могут быть одинаковыми или разными). Необязательное замещение также указано фразой "группа, замещенная от 0 до X заместителями", где X означает максимальное число возможных заместителей. Некоторые необязательно замещенные группы замещены от 0 до 2, 3 или 4 независимо выбранными заместителями (т.е. не замещены или замещены вплоть до описанного максимального числа заместителей). Другие необязательно замещенные группы замещены по меньшей мере одним заместителем (например, замещены от 1 до 2, 3 или 4 независимо выбранными заместителями). Термин "рецептор Р 2 Х 7" относится к любому рецептору Р 2 Х 7, предпочтительно рецептору млекопитающего, такому как рецептор Р 2 Х 7 человека или крысы, описанный в патенте США 6133434, а также к их гомологам, обнаруженным в других видах."Модулятор рецептора Р 2 Х 7", также названный в описании как "модулятор", представляет собой соединение, которое повышает или уменьшает степень активации рецептора Р 2 Х 7 и/или опосредованной рецептором Р 2 Х 7 активности (например, передача сигнала). Модуляторами рецептора Р 2 Х 7, особо представленными в описании, являются соединения формулы I и их фармацевтически приемлемые соли, гидраты и сложные эфиры. Модулятор может быть агонистом или антагонистом рецептора Р 2 Х 7. Модулятор рассматривается как "антагонист", если он заметно ингибирует опосредованную рецептором Р 2 Х 7 сигнальную трансдукцию (с использованием, например, типичного анализа, описанного в примере 7); в целом, такой антагонист ингибирует активацию рецептора Р 2 Х 7 с величиной IC50 менее чем 20 мкм/л (micromolar), предпочтительно менее чем 1 мкм/л, более предпочтительно менее чем 500 нм/л и наиболее предпочтительно менее чем 100 нм/л, как показано анализом, описанным в примере 7. Антагонисты рецептора Р 2 Х 7 включают нейтральные антагонисты и обратные агонисты."Обратный агонист" рецептора Р 2 Х 7 представляет собой соединение, которое снижает активность рецептора Р 2 Х 7 ниже его базисного уровня активности в отсутствие добавленного лиганда. Обратные агонисты рецептора также могут ингибировать активность лиганда у рецептора Р 2 Х 7 и/или связывание лиганда с рецептором Р 2 Х 7. Базисная активность рецептора Р 2 Х 7, а также снижение активности рецептора Р 2 Х 7 вследствие присутствия антагониста рецептора Р 2 Х 7 может быть определена анализом мобилизации кальция (например, анализ примера 7)."Нейтральный антагонист" рецептора Р 2 Х 7 представляет собой соединение, которое ингибирует активность лиганда у рецептора Р 2 Х 7, но не изменяет в значительной степени базисную активность рецептора (т.е. в анализе мобилизации кальция, описанном в примере 7, выполненном в отсутствие лиганда,активность рецептора Р 2 Х 7 снижается не более чем на 10%, предпочтительно не более чем на 5% и наиболее предпочтительно не более чем на 2%, наиболее предпочтительное, когда не наблюдается определяемого снижения активности). Нейтральные антагонисты рецептора Р 2 Х 7 могут ингибировать связывание лиганда с рецептором Р 2 Х 7. Как используют в описании, "агонист рецептора Р 2 Х 2" представляет собой соединение, которое повышает активность рецептора Р 2 Х 7 выше базисного уровня активности рецептора (т.е. усиливает активацию рецептора Р 2 Х 7 и/или опосредуемую рецептором Р 2 Х 7 активность, такую как сигнальная трансдукция). Активность агониста рецептора Р 2 Х 7 можно определить с помощью типичного анализа, описанного в примере 7. Агонисты рецептора Р 2 Х 7 включают АТР и 2'(3')-О-(4-бензоилбензоил)аденозин-5'трифосфат (BzATP)."Терапевтически эффективное количество" (или доза) означает количество, которое, при введении больному, приносит ощутимую пользу больному (например, способствует определяемому облегчению,по меньшей мере одного состояния, которое подвергается лечению). Такое облегчение может быть определено с помощью любого соответствующего критерия, включающего частичное снятие одного или более симптомов, таких как боль. Терапевтически эффективное количество или доза обеспечивает концентрацию соединения в жидкости организма (такой как кровь, плазма, сыворотка, CSF, синовиальная жидкость, лимфа, клеточная интерстициальная жидкость, слезы или моча), которая является достаточной для изменения опосредуемой рецептором Р 2 Х 2 сигнальной трансдукции (посредством анализа, описанного в примере 7). Очевидно, ощутимую пользу больному можно наблюдать после введения однократной дозы,или она может быть выраженной после повторного введения терапевтически эффективной дозы в соответствии с преопределенной схемой лечения, в зависимости от показания, в связи с которым соединение вводят. Под термином "статистически значимые", как употребляют в описании, подразумевают результаты,отличающиеся от контроля при уровне значимости р 0,1, как измерено стандартным параметрическим анализом статистической значимости, таким как t-критерий Стьюдента. тением. Больные включают людей, а также других животных, таких как домашних животных (например,собаки и кошки) и скот. Больные могут испытывать один или более симптомы состояния, отвечающего на модуляцию рецептора Р 2 Х 7, или могут не иметь такого симптома(ов) (т.е. лечение может быть профилактическим у больного, у которого предполагается риск развития таких симптомов). Аналоги гетероариламидов Как отмечено выше, настоящее изобретение предоставляет аналоги гетероариламидов. В некоторых вариантах осуществления изобретения настоящее изобретение предоставляет аналоги гетероариламидов формулы Ia и/или Ib и где U является СН или N;X отсутствует или означает С 1-С 6 алкилен, который необязательно замещен от 1 до 4 заместителями,выбранными из RB, RC, RD и RE;RB, RC, RD и RE каждая группа независимо означает гидрокси, С 1-С 8 алкил, (С 3-С 8 циклоалкил)С 0 С 4 алкил, (4-7-членный гетероциклоалкил)С 0-С 4 алкил и фенилС 0-С 2 алкил; или любые две группы из RB,RC, RD И RE, взятые вместе с атомом или атомами углерода, посредством которого они связаны, образуют 3-7-членный циклоалкил или 4-7-членный гетероциклоалкил;Y означает циклопропил, циклобутил, циклопентил, циклогексил, морфолинил, циклогептил, циклооктил, адамантил, миртанил, фенил или пиридил, каждый из которых необязательно замещен гидрокси, галогеном, С 1-С 6 алкилом или С 1-С 6 алкокси;Z1, Z2, Z3 и Z4 независимо означают CR1 или N; каждая группа R1 независимо означает водород, галоген, циано или аминокарбонил; и RA является группой формулы -L-A-M, гдеM означает 5- или 6-членный гетероарил, содержащий по меньшей мере один атом азота, необязательно замещенный C1-С 6 алкилом, -СООН, COOC1-С 6 алкилом, CN или галогеном. В некоторых аспектах такие соединения могут быть использованы in vitro или in vivo в качестве модуляторов рецепторов Р 2 Х 7, которые могут быть использованы в ряде контекстов, включая лечение состояний, отвечающих на модуляцию рецептора Р 2 Х 7. В некоторых вариантах осуществления изобретения соединения согласно настоящему изобретению или их соли являются соединениями формулы Ia. В других вариантах осуществления изобретения соединения согласно настоящему изобретению или их соли являются соединениями формулы Ib. В некоторых вариантах осуществления настоящего изобретения соединения формулы Ia и/или Ib предоставлены в виде их соли. В формуле Ia и/или Ib гетероарильное ядро включает по меньшей мере один атом азота, как указано, и необязательно включает дополнительный атом(ы) азота у одной или более групп U, V, Z1, Z2, Z3 и/или Z4. В некоторых вариантах осуществления изобретения U является СН. В других вариантах осуществления изобретения Z1, Z2 и Z3 каждая группа означает CR1. В некоторых других модификациях соединений формулы Ia и/или Ib X является замещенной группой от 1 до 4 заместителями, выбранными из RB, RC, RD и RE. В некоторых других модификациях соединений формулы Ia и/или Ib группы RB, RC, RD и RE каждая независимо означает гидрокси, С 1-С 8 алкил, (С 3-С 8 циклоалкил) С 0-С 4 алкил, (4-7-членный гетероциклоалкил)С 0-С 4 алкил и фенилС 0-С 2 алкил; или любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они связаны, образуют 3-7-членный циклоалкил или 4-7 членный гетероциклоалкил. В некоторых других модификациях соединений формулы Ia и/или Ib группы RB, RC, RD и RE каждая независимо означает C1-С 4 алкил, (С 3-С 8 циклоалкил)С 0-С 2 алкил или фенилС 0-С 2 алкил. В других аспектах соединений формулы Ia и/или Ib любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они соединены, образуют 3-7-членный циклоалкил или 4-7-членный гетероциклоалкил. В некоторых аспектах соединений формулы Ia и/или Ib любая одна группа из RB, RC, RD и RE, взятая вместе с R4 и атомом или атомами, посредством которого они соединены, образуют 4-7-членный гетероциклоалкил. В некоторых модификациях соединений формулы Ia и/или Ib U является СН. В других модификациях соединений формулы Ia и/или Ib U является N. В некоторых модификациях соединений формулы Ia и/или Ib Y означает циклопропил, циклобутил,циклопентил, циклогексил, морфолинил, циклогептил, циклооктил, адамантил, миртанил, фенил или пиридил, каждый из которых необязательно замещен гидрокси, галогеном, C1-С 6 алкилом или С 1-С 6 алкокси. В еще других модификациях соединений формулы Ia и/или Ib группы Z1, Z2, Z3 и Z4 независимо означают СН. В других аспектах Z4 является N. В других аспектах по меньшей мере одна из групп Z1, Z2,Z3 и Z4 является CR1. В некоторых других аспектах Z1 или Z4 является CR1; или Z1 является CR1. В некоторых модификациях формулы Ia и/или Ib R1 означает водород, галоген, циано или аминокарбонил. В некоторых аспектах, где R1 является галогеном, указанный галоген представляет собой фтор, хлор или бром; указанным выше галогеном является фтор. Альтернативно, каждая группа R1 означает Н. В некоторых модификациях соединений формулы Ia и/или Ib W является -NR4C(=O)-. В других модификациях осуществления изобретения R4 является Н. В некоторых модификациях соединений формулы Ia и/или Ib M означает 5- или 6-членный гетероарил, содержащий по меньшей мере один атом азота, необязательно замещенный С 1-С 6 алкилом, -СООН,СООС 1-С 6 алкилом, CN или галогеном. В некоторых таких соединениях M является замещенной группой; в других - незамещенной. В некоторых модификациях соединений формулы Ia и/или Ib W является -C(=O)N(H)-. В некоторых модификациях соединений формулы Ia и/или Ib группа M означает 5- или 6-членный гетероарил, содержащий по меньшей мере один атом азота, необязательно замещенный C1-С 6 алкилом,-СООН, СООС 1-С 6 алкилом, CN или галогеном. В некоторых вариантах М является необязательно замещенным пиримидинилом. В некоторых модификациях соединений формулы Ia и/или Ib X означает С 1-С 2 алкилен, необязательно замещенный, предпочтительно замещенный С 1-С 4 алкилом. В других модификациях группа X замещена по меньшей мере 2 заместителями, выбранными из RB, RC, RD и RE, где любые две группы из RB,Rc, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они соединены, образуют 3-7-членный циклоалкил. Альтернативно, в некоторых модификациях группа X замещена по меньшей мере 2 заместителями, выбранными из RB, RC, RD и RE, где любые две группы из RB, RC, RD и RE, взятые вместе с атомом или атомами углерода, посредством которого они соединены, образуют 3-7 членный циклоалкил, предпочтительно 5-6-членный циклоалкил. В некоторых модификациях соединений формулы Ia и/или Ib Y означает циклопропил, циклобутил,циклопентил, циклогексил, морфолинил, циклогептил, циклооктил, адамантил, миртанил, фенил или пиридил, каждый из которых необязательно замещен гидрокси, галогеном, С 1-С 6 алкилом или С 1-С 6 алкокси. В некоторых других модификациях соединений формулы Ia и/или Ib соединение является соединением, представленным в таблице в описании, или его солью. Характерные примеры гетероариламидных аналогов, представленных в описании, включают, но не ограничиваются ими, соединения, особо описанные в примерах 1-6 и в сопровождающей таблице. Понятно, что отдельные соединения, перечисленные в описании, являются только характерными примерами и не предназначены ограничить объем настоящего изобретения. Кроме того, как упомянуто выше, все соединения согласно настоящему изобретению могут быть представлены в виде свободной кислоты или основания или в виде фармацевтически приемлемой соли. Кроме того, другие виды, такие как гидраты и пролекарства таких соединений, особо рассматриваются настоящим изобретением. В некоторых аспектах настоящего изобретения аналоги гетероариламидов, представленные в описании, заметно изменяют (модулируют) активность рецептора Р 2 Х 7, как определено в исследовании, таком как анализ, описанный в примере 7. Дополнительные исследования, которые могут быть использованы для этой цели, включают анализы, позволяющие количественно определить высвобождение IL-1; анализы, позволяющие количественно определить накопление неспособного к проникновению через мембрану флуоресцентного красителя, такого как YO-PRO1; анализы, позволяющие количественно определить накопление красителя люцифера желтого; анализы, позволяющие количественно определить поглощение бромида этидия; и анализы, в которых используют визуализацию кальция для определения активности Р 2 Х 7, все из которых анализов хорошо известны в данной области. Некоторые модуляторы,представленные в описании, заметно модулируют активность рецептора Р 2 Х 7 при микромолярных концентрациях, при наномолярных концентрациях или при субнаномолярных концентрациях. Как отмечено выше, соединения, которые представляют собой антагонисты рецептора Р 2 Х 7, являются предпочтительными соединениями в некоторых вариантах осуществления изобретения. ВеличиныIC50 для таких соединений могут быть определены стандартным анализом in vitro, позволяющим измерить мобилизацию кальция, опосредованную рецептором Р 2 Х 7, как описано в примере 7. Кратко, клетки,экспрессирующие рецептор Р 2 Х 7, контактируют с представляющим интерес соединением и с индикатором внутриклеточной концентрации кальция (например, проникающий через мембрану, чувствительный к кальцию краситель Fluo-3, Fluo-4 или Fura-2 (Invitrogen, Carlsbad, CA), каждый из указанных красителей производит флуоресцентный сигнал, когда связывается с Са). Такой контакт предпочтительно осуществляют путем одной или более инкубации клеток в буфере или культуральной среде, содержащей любой компонент или оба из соединения и индикатора в растворе. Контакт поддерживается в течение времени, достаточного для прохождения красителя в клетки (например, 1-2 ч). Клетки промывают или фильтруют для удаления избытка красителя, и затем их подвергают контакту с агонистом рецептора Р 2 Х 7 (например, АТР или 2'(3')-О-(4-бензоилбензоил)аденозин-5'-трифосфат при концентрации, например, равной концентрации ЕС 50), и измеряют флуоресцентный ответ. Когда клетки, находящиеся в контакте с агонистом, подвергают взаимодействию с соединением, которое является антагонистом рецептора Р 2 Х 7, флуоресцентный ответ обычно снижается по меньшей мере на 20%, предпочтительно по меньшей мере на 50% и более предпочтительно по меньшей мере на 80% по сравнению с клетками, которые вступали в контакт с агонистом в отсутствие испытуемого соединения. В некоторых вариантах осуществления изобретения антагонисты рецептора Р 3 Х 7, представленные в описании, не проявляют определяемой активности агонистов в анализе in vitro агонизма рецептора Р 2 Х 7 при концентрации соединения,равной IC50. Некоторые такие антагонисты не проявляют обнаруживаемой агонистической активности в анализе in vitro агонизма рецептора Р 2 Х 7 при концентрации соединения, которая в 100 раз выше, чем величина IC50. Модулирующая рецептор Р 2 Х 2 активность может также, или альтернативно, быть оценена с помощью in vitro анализа облегчения боли, как описано в примере 8. Модуляторы, представленные в описании, предпочтительно проявляют статистически значимое определенное действие на активность рецептора Р 2 Х 7 в таком функциональном исследовании. В некоторых вариантах осуществления изобретения предпочтительные модуляторы не проявляют сомногенный эффект. Другими словами, доза модулятора, которая превышает в два раза минимальную дозу, достаточную для обезболивания, изучаемого на модели животного для определения степени облегчения боли (такой как модель, описанная в примере 7), оказывает только преходящее действие (т.е. продолжительность не более чем 1/2 времени, в течение которого облегчение боли сохраняется) или предпочтительно не оказывает статистически значимого седативного эффекта, изучаемого на модели животного с помощью анализа седативного эффекта (используя метод, описанный Fitzgerald et al. (1988) Toxicology 49 (2-3):433-9). Предпочтительно доза, которая превышает минимальную дозу в пять раз, достаточную для достижения обезболивания, не производит статистически значимого седативного эффекта. Более предпочтительно модулятор, представленный в описании, не производит седативного эффекта при внутривенных дозах менее чем 25 мг/кг (предпочтительно менее чем 10 мг/кг) или при пероральных дозах менее чем 140 мг/кг (предпочтительно менее чем 50 мг/кг, более предпочтительно менее чем 30 мг/кг). Если желательно, соединения, представленные в описании, могут быть оценены с точки зрения фармакологических свойств, включающих, но не ограничивающихся ими, биодоступность при пероральном введении (предпочтительные соединения являются биодоступными при пероральном введении до степени, позволяющей достичь терапевтически эффективных концентраций при пероральных дозах,составляющих менее чем 140 мг/кг, предпочтительно менее чем 50 мг/кг, более предпочтительно менее чем 30 мг/кг, даже более предпочтительно менее чем 10 мг/кг, еще более предпочтительно менее чем 1 мг/кг и наиболее предпочтительно менее чем 0,1 мг/кг), токсичность (предпочтительное соединение является нетоксичным, когда субъекту вводят терапевтически эффективное количество соединения), связывание белка сыворотки и in vitro и in vivo период полу-жизни (предпочтительное соединение имеет период полу-жизни in vivo, допускающий дозировку Q.I.D, предпочтительно дозировку T.I.D., более предпочтительно дозировку B.I.D. и наиболее предпочтительно дозировку один раз в день). Кроме того,дифференциальное проникновение через гематоэнцефалический барьер может быть желательным для модуляторов, используемых для лечения боли или нейродегенеративного заболевания путем модуляции активности рецептора CNS P2X7, так что общие суточные пероральные дозы, описанные выше, достигают такой модуляции до терапевтически эффективной степени, в то время как низкие уровни модуляторов в головном мозге, используемых для лечения боли, опосредуемой периферическим нервом, или некоторых воспалительных заболеваний (например, ревматоидный артрит), могут быть предпочтительными(т.е. такие дозы не приводят к уровням соединения в мозге (например, CSF), достаточным для значительной модуляции активности рецептора Р 2 Х 7). Обычные исследования, которые хорошо известны в данной области, могут быть использованы для определения указанных выше свойств и идентификации наилучших соединений для отдельного использования. Например, исследования по прогнозированию биодоступности включают транспорт через монослои интерстициальных клеток, включающие монослои линии клеток Сасо-2. Проникновение соединения через гематоэнцефалический барьер у людей можно прогнозировать, исходя из уровней соединения в мозге лабораторных животных, которым вводят соединение (например, внутривенно). Связывание белка сыворотки можно прогнозировать, исходя из анализов связывания альбумина. Период полу-жизни соединения обратно пропорционален частоте дозировки соединения. Периоды полу-жизни соединений можно вычислить in vitro, исходя из исследований периодов полу-жизни с использованием микросом печени, как описано, например, в примере 7 в публикации патентной заявки США 2005/0070547. Как отмечено выше, предпочтительные соединения, представленные в описании, являются нетоксичными. Вообще, термин "нетоксичные" следует понимать в относительном значении, и он предназначен ссылаться на любое вещество, которое одобрено Департаментом по контролю качества пищевых продуктов, медикаментов и косметических средств Соединенных Штатов Америки ("FDA") для введения млекопитающим (предпочтительно людям) или, согласно установленным критериям, подвержено испытанию FDA для введения млекопитающим (предпочтительно людям). Кроме того, наиболее предпочтительное нетоксичное соединение обычно удовлетворяет одному или более следующим критериям: (1) существенно не ингибирует продукцию АТР в клетках; (2) существенно не удлиняет QT-интервалы; (3) не вызывает значительного увеличения печени, или (4) не вызывает значительного высвобождения ферментов печени. Как используют в описании, соединение, которое существенно не ингибирует продукцию АТР в клетках, является соединением, удовлетворяющим критериям, указанным в примере 8 публикации патентной заявки США 2005/0070547. Другими словами, клетки, обработанные, как представлено в описании, 100 мкМ такого соединения, имеют уровни АТР, составляющие по меньшей мере 50% уровней АТР, определяемых в необработанных клетках. Соединение, которое существенно не удлиняет QT-интервалы, представляет собой соединение, которое не приводит к статистически значимому удлинению QT-интервалов (как установлено электрокардиографией) у морских свинок, минипигов или собак при введении дозы, достигающей концентрации в сыворотке, равной EC50 или IC50 для соединения. В некоторых предпочтительных вариантах осуществления изобретения доза 0,01, 0,05, 0,1, 0,5, 1, 5, 10, 40 или 50 мг/кг, введенная парентерально или перорально, не приводит к статистически значимому удлинению QT-интервалов. Соединение не вызывает значительного увеличения печени, если суточная обработка лабораторных грызунов (например, мыши или крысы) в течение 5-10 дней дозой, достигающей концентрации в сыворотке, равной EC50 или IC50 для соединения, приводит к увеличению отношения массы печени к массе тела, которое составляет не более 100% над равноценными контролями. В более предпочтительных вариантах осуществления изобретения такие дозы не вызывают увеличения печени более чем на 75% или 50% над равноценными контролями. Если в исследованиях используют млекопитающих, отличных от грызунов (например, собаки), такие дозы не должны приводить к повышению отношения массы печени к массе тела более чем на 50%, предпочтительно более чем на 25% и более предпочтительно более чем на 10% над равноценными необработанными контролями. Предпочтительные дозы в таких анализах включают 0,01, 0,05, 0,1, 0,5, 1, 5, 10, 40 или 50 мг/кг соединения, введенного парентерально или перорально. Аналогично, соединение не способствует значительному высвобождению ферментов печени, если введение удвоенной минимальной дозы, которая приводит к концентрации в сыворотке, равной ЕС 50 илиIC50 у рецептора Р 2 Х 7 для соединения, не повышает уровни ALT, LDH или AST в сыворотке лабораторных животных (например, грызуны) более чем на 100% над равноценными контролями ложнообработанных животных. В наиболее предпочтительных вариантах осуществления изобретения, такие дозы не повышают уровни в сыворотке более чем на 75 или 50% над равноценными контролями. Альтернативно, соединение не способствует значительному высвобождению ферментов печени, если в invitro анализе гепатоцитов концентрации (в культуральных средах или других таких растворах, которые контактируют или инкубируют с гепатоцитами in vitro), равные ЕС 50 или IC50 для соединения, не вызывают заметного высвобождения любого из таких ферментов печени в культуральную среду выше исходных уровней, наблюдаемых в средах с равноценными контрольными ложно-обработанными клетками. В наиболее предпочтительных вариантах осуществления изобретения не наблюдается заметное высвобождение любого из таких ферментов печени в культуральную среду выше исходных уровней, когда концентрации такого соединения в пять раз и более предпочтительно в 10 раз выше ЕС 50 или IC50 для соединения. В других вариантах осуществления изобретения некоторые предпочтительные соединения не ингибируют или не индуцируют ферментативные активности микросомальных цитохромов Р 450, таких как активность CYP1A2, активность CYP2A6, активность CYP2C9, активность CYP2C19, активностьCYP2D6, активность CYP2E1 или активность CYP3A4, при концентрации, равной ЕС 50 или IC50 у рецептора Р 2 Х 7 для соединения. Некоторые предпочтительные соединения не являются кластогенными (например, как определено микроядерным тестом на клетках-предшественниках эритроцитов мыши, микроядерным тестом Эймса,микроядерным тестом с применением спиральной компьютерной томографии или тому подобное) при концентрации, равной ЕС 50 или IC50 для соединения. В других вариантах осуществления изобретения некоторые предпочтительные соединения не индуцируют сестринский хроматидный обмен (например, в клетках яичника женской особи китайского хомячка) при таких концентрациях. С целью обнаружения, как описано подробно ниже, модуляторы, представленные в описании, могут быть изотопно-мечеными или меченными радиоактивным изотопом. Например, соединения могут иметь один или более атомы, замененные атомом такого же элемента, имеющего атомную массу или массовое число, отличные от атомной массы или массового числа, обычно существующие в природе. Примеры изотопов, которые могут присутствовать в соединениях, представленных в описании, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2 Н, 3 Н, 11 С, 13 С,14 С, 15N, 18O, 17O, 31 Р, Р, 35S, 18F и 36Cl. Кроме того, замещение тяжелыми изотопами, такими как дейтерий (т.е. 2 Н), может дать некоторые положительные терапевтические результаты вследствие большей метаболической стабильности, например, увеличения in vivo периода полу-жизни или снижения требований дозирования, и поэтому может быть предпочтительным в некоторых ситуациях. Получение гетероариламидных аналогов Герероариламидные аналоги обычно можно получать стандартными способами синтеза. Исходные материалы являются коммерчески доступными от компаний-поставщиков, таких как Sigma-Aldrich Corp.(St. Louis, МО), или могут быть синтезированы из коммерчески доступных предшественников с использованием общепринятых протоколов. В качестве примера, способ синтеза, подобный способу, представленному на любой из следующих схем, может быть использован, вместе со способами синтеза, известными в области синтетической органической химии. В некоторых случаях, в процессе получения могут потребоваться защитные группы. Такие защитные группы могут быть удалены способами, хорошо известными специалистам в данной области, такими как способы, описанные в публикации Greene andWuts, "Protective Groups in Organic Synthesis" (2nd Edition, John WileySons, 1991) or Philip J. Kocienski,"Protecting Groups'", 2nd ed., John WileySons, Inc., New York (2005). В некоторых случаях, дальнейшие органические превращения могут быть осуществлены способами, хорошо известными специалистам в данной области, такими как способы, описанные в публикации Richard С. Larock, "Comprehensive OrganicTransformation," (VCH Publisher, Inc. 1989). Каждый переменный параметр на следующих схемах относится к любой группе в соответствии с описанием соединений, представленных в описании. Типичные условия реакций для использования на следующих схемах представлены в примерах. Некоторые сокращения, используемые на следующих схемах и в других местах описания, включают ВОР - бензотриазол-1-илокситрис(диметиламино)фосфония гексафторфосфатхимический сдвигh - час(ы) 1 Н NMR - протонный ядерный магнитный резонанс (1 Н ЯМР)(CF3CO)2O - ангидрид трифторуксусной кислоты. Схемы 1-8 иллюстрируют некоторые варианты осуществления настоящего изобретения и предназначены быть только примерами и неограничивающими примерами. Например, понятно, что любая реакция, описанная на схеме, может быть осуществлена без комбинации, в комбинации с некоторыми или со всеми другими реакциями, представленными в описании. Кроме того, различные модификации условий реакции будут очевидны, включая использование различных растворителей и кислот/оснований и изменения времени реакции и температур. Все способы, описанные в связи с настоящим изобретением,предполагается использовать на практике в любом масштабе, включая миллиграмм, грамм, мультиграмм,килограмм, мультикилограмм или коммерческий промышленный масштаб. Также очевидно, что исходные материалы для каждой стадии и каждый продукт реакции могут быть указанным соединением или могут быть его солью (например, фармацевтически приемлемая соль) или сольватом (например, гидрат). Если не указано иное, каждое значение является таким, как определено выше. Схема 6 иллюстрирует общий способ получения некоторых промежуточных соединений NH2-CH2CHR5-Y формулы X, где R5 означает замещенный фенил или гетероарил, и Y = N-R5bR5b, где R5b независимо означает водород, C1-С 6 алкил или С 3-С 7 циклоалкил; или обе группы R5b, взятые вместе, с образованием гетероцикла. Конденсация Штреккера арилкарбоксальдегида и амина либо с TMSCN в растворителе, таком как ацетонитрил, либо с NaCN или KCN в растворителе, таком как смесь МеОН-вода или вода при рН 3-4 (доведено хлористым водородом), приводит к аминонитрилу, который восстанавливают LAH в растворителе, таком как ТГФ, или гидрированием с никелем Ренея в качестве катализатора в растворителе,таком как 7 N раствор аммиака в метаноле, с образованием промежуточного амина NH2-CH2-CHR5-Y. Схема 7 Схема 7 иллюстрирует общий способ получения некоторых промежуточных соединений NH2-CH2CHR5-Y или NH2-CH2-CR5R5-Y формулы X, где Y означает замещенный фенил или гетероарил. Алкилирование исходного ацетонитрила одним эквивалентом X-R5 (Х=Br или I) с основанием, таким как гидрид натрия, в растворителе, таком как смесь ТГФ-ДМСО, приводит к промежуточному соединению Y-X(R5)-CN. Алкилирование исходного ацетонитрила двумя эквивалентами X-R5 (X=Br или I) или одним эквивалентом диброма или дийода (когда группы R5 и R5, взятые вместе, образуют кольцо) с основанием,таким как гидрид натрия, в растворителе, таком как смесь ТГФ-ДМСО, приводит к промежуточному соединению Y-X(R5) (R5)-CN. Восстановление любого продукта LAH в растворителе, таком как ТГФ, или гидрированием с никелем Ренея в качестве катализатора в растворителе, таком как 7 N раствор аммиака в метаноле, приводит к NH2-CH2-CHR5-Y или NH2-CH2-CR5R5-Y. Схема 8 Схема 8 иллюстрирует общий способ получения некоторых промежуточных соединений NH2-CH2- 14020332CR5R5-Y формулы X, где R5 независимо означает водород, С 1-С 6 алкил, С 3-С 7 циклоалкил или фенил; или обе группы R5, взятые вместе, образуют C3-С 8 циклоалкил или гетероцикл, и Y=N-R5bR5b, где R5b означаетC1-С 6 алкил, необязательно замещенный галогеном, гидроксилом, C1-С 4 алкилом, С 1-С 4 алкокси или СО 2 Н,или обе группы R5b, взятые вместе, образуют 5-7-членный гетероцикл. Конденсация Штреккера кетона и амина либо с TMSCN в растворителе, таком как метанол, с катализатором, таким как ZnI2, либо с NaCN или KCN в растворителе, таком как смесь МеОН-вода или вода при рН 3-4 (доведено хлористым водородом), приводит к аминонитрилу. Восстановление аминонитрила LAH в растворителе, таком как ТГФ,или гидрированием с никелем Ренея в качестве катализатора в растворителе, таком как 7N раствор аммиака в метаноле, приводит к NH2-CH2-CR5R5-Y. Фармацевтические композиции Настоящее изобретение также относится к фармацевтическим композициям, содержащим одно или более соединения, представленные в описании, вместе по меньшей мере с одним фармацевтически приемлемым носителем или наполнителем. Фармацевтические композиции могут содержать, например,один или более наполнители или носители, такие как вода, буферы (например, бикарбонат натрия, нейтральный забуференный раствор или забуференный фосфатом физиологический раствор), этанол, минеральное масло, растительное масло, диметилсульфоксид, углеводы (например, глюкоза, манноза, сахароза, крахмал, манит или декстраны), белки, адъюванты, полипептиды или аминокислоты, такие как глицин, антиоксиданты, хелатирующие агенты, такие как ЭДТА или глутатион, и/или консерванты. Кроме того, другие активные ингредиенты могут (но необязательно) быть включены в фармацевтические композиции, представленные в описании. Фармацевтические композиции могут быть приготовлены для любого соответствующего способа введения, включающего, например, местное, пероральное, назальное, ректальное или парентеральное введение. Термин парентеральный, как используют в описании, включает подкожную, внутрикожную,внутрисосудистую (например, внутривенную), внутримышечную, спинальную, внутричерепную, интратекальную и внутрибрюшинную инъекцию или инфузию. В некоторых вариантах осуществления изобретения композиции, подходящие для перорального использования, являются предпочтительными. Такие композиции включают, например, таблетки, лепешки, пастилки, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсии, твердые или мягкие капсулы или сиропы или эликсиры. В других вариантах осуществления изобретения фармацевтические композиции могут быть приготовлены в виде лиофилизата. Композиция для местного введения может быть предпочтительной для некоторых состояний (например, в лечении кожных болезней, таких как ожоги и зуд). Композиция для прямого введения в пузырь (интравезикулярное введение) может быть предпочтительной для лечения недержания мочи или гиперактивного мочевого пузыря. Композиции, предназначенные для перорального использования, также могут содержать один или более компоненты, такие как подсластители, вкусовую добавку, красители и/или консерванты для получения привлекательных и приятных на вкус препаратов. Таблетки содержат активный ингредиент в смеси с физиологически приемлемыми наполнителями, которые являются подходящими для производства таблеток. Такие наполнители включают, например, инертные разбавители (например, карбонат кальция,карбонат натрия, лактоза, фосфат кальция или фосфат натрия), гранулирующие или дезинтегрирующие средства (например, кукурузный крахмал или альгиновая кислота), связывающие средства (например,крахмал, желатин или камедь) и смазывающие средства (например, стеарат магния, стеариновая кислота или тальк). Таблетки получают стандартными способами, включающими сухое гранулирование, прямую компрессию и влажное гранулирование. Таблетки могут быть не покрыты оболочками, или они могут быть покрыты оболочками известными способами. Препараты для перорального использования могут быть приготовлены в виде твердых желатиновых капсул, где активный ингредиент смешан с инертным твердым разбавителем (например, карбонат кальция,фосфат кальция или каолин), или в виде мягких желатиновых капсул, где активный ингредиент смешан с водой или масляной средой (например, арахисовое масло, жидкий вазелин или оливковое масло). Водные суспензии содержат активный материал(ы) в смеси с подходящими наполнителями, такими как суспендирующие средства (например, карбоксиметилцеллюлоза натрия, метицеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакант и аравийская камедь); и диспергирующие или смачивающие средства (например, природные фосфатиды, такие как лецитин, продукты конденсации алкиленоксида с жирными кислотами, такими как полиоксиэтиленстеарат, продукты конденсации этиленоксида с длинноцепочечными алифатическими спиртами, такими как гептадекаэтиленоксицетанол, продукты конденсации этиленоксида с частичными сложными эфирами, произведенными из жирных кислот и гексита, такие как полиоксиэтиленсорбитмоноолеат, или продукты конденсации этиленоксида с частичными сложными эфирами, произведенными из жирных кислот и ангидридов гексита, такие как полиэтиленсорбитанмоноолеат). Водные суспензии также могут включать один или более консерванты, такие как этил или п-пропил р-гидроксибензоат, один или более красители, одну или более вкусовые добавки и/или один или более подсластители, такие как сахароза или сахарин. Масляные суспензии могут быть приготовлены путем суспендирования активного ингредиента(ов) в растительном масле (например, арахисовое масло, оливковое масло, кунжутное масло или кокосовое масло) или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, такой как воск, твердый парафин или цетиловый спирт. Подсластители, такие как те, перечисленные выше, и/или вкусовые добавки могут быть добавлены для получения привлекательных и приятных на вкус препаратов. Такие суспензии могут быть защищены путем добавления антиоксиданта, такого как аскорбиновая кислота. Диспергируемые порошки и гранулы, подходящие для приготовления водной суспензии путем добавления воды, содержат активный ингредиент в смеси с диспергирующим или увлажняющим средством, суспендирующим средством и одним или более консервантами. Подходящие диспергирующие или увлажняющие средства и суспендирующие средства представлены средствами, упомянутыми выше. Дополнительные наполнители, такие как подсластители, вкусовые добавки и красители также могут присутствовать. Фармацевтические композиции могут быть приготовлены в виде эмульсий масло-в-воде. Масляной фазой может быть растительное масло (например, оливковое масло или арахисовое масло), минеральное масло (например, жидкий парафин) или их смесь. Подходящие эмульгирующие средства включают природные камеди (например, аравийская камедь или трагакант), природные фосфатиды (например, соевый лецитин и сложные эфиры или частичные эфиры, произведенные из жирных кислот и гексита), ангидриды (например, сорбитанмоноолеат) и продукты конденсации частичных эфиров, произведенных из жирных кислот и гексита, с этиленоксидом (например, полиоксиэтиленсорбитанмоноолеат). Эмульсия также может содержать один или более подсластители и/или вкусовые добавки. Сиропы и эликсиры могут быть приготовлены с добавлением подсластителей, таких как глицерин,пропиленгликоль, сорбит или сахароза. Такие препараты могут также содержать одно или более успокоительные средства, консерванты, вкусовые добавки и/или красители. Препараты для местного введения обычно включают носитель местного использования, комбинированный с активным средством(ами), с или без дополнительных необязательных компонентов. Подходящие носители для местного использования и дополнительные компоненты хорошо известны в данной области, и очевидно, что выбор носителя будет зависеть от отдельной физической формы и способа доставки. Носители для местного применения включают воду; органические растворители, такие как спирты(например, этанол или изопропиловый спирт) или глицерин; гликоли (например, бутилен, изопрен или пропиленгликоль); алифатические спирты (например, ланолин); смеси воды и органических растворителей и смеси органических растворителей, такие как спирт и глицерин; основанные на липидах материалы, такие как жирные кислоты, ацетилглицерины (включающие масла, такие как минеральное масло, и жиры природного или синтетического происхождения), фосфоглицериды, сфинголипиды и воски; материалы на основе белков, таких как коллаген и желатин; материалы на основе силикона (как не летучие,так и летучие); и материалы на основе углеводородов, таких как микропористые материалы и полимерные матриксы. Композиция также может включать один или более компоненты, приспособленные для улучшения стабильности или эффективности применяемого препарата, такие как стабилизирующие средства, суспендирующие средства, эмульгирующие средства, средства, регулирующие вязкость, гелеобразующие средства, консерванты, антиоксиданты, вещество, способствующее проникновению через кожу, увлажняющие средства и материалы замедленного высвобождения. Примеры таких компонентов описаны в публикации Martindale-The Extra Pharmacopoeia (Pharmaceutical Press, London 1993) and Remington: The Science and Practice of Pharmacy, 21st ed., Lippincott WilliamsWilkins, Philadelphia, PA(2005). Препараты могут включать микрокапсулы, такие как гидроксиметилцеллюлоза или желатинмикрокапсулы, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы или нанокапсулы. Препарат местного значения может быть приготовлен в любом виде, включая, например, твердые частицы, пасты, кремы, пены, лосьоны, гели, порошки, водные жидкости и эмульсии. Физическое состояние и вязкость таких фармацевтически приемлемых форм могут быть обусловлены присутствием и количеством эмульгатора (ов) и регулирующего вязкость средства(средств), присутствующих в препарате. Твердые частицы обычно являются прочными и не текучими и обычно приготовлены в виде брусков или карандашей или в отдельной форме; твердые частицы могут быть непрозрачными или прозрачными и необязательно могут содержать растворители, эмульгирующие средства, увлажняющие средства, смягчающие вещества, ароматизирующие вещества, красители/красящие вещества, консерванты и другие активные ингредиенты, которые повышают или усиливают эффективность конечного продукта. Кремы и лосьоны часто подобны один другому, отличаясь, главным образом, по их вязкости; как лосьоны, так и кремы могут быть непрозрачными, полупрозрачными или прозрачными и часто содержат эмульгирующие средства, растворители и регулирующие вязкость средства, а также увлажняющие средства, увлажняющие средства, смягчающие вещества, ароматизирующие вещества, красители/красящие вещества,консерванты и другие активные ингредиенты, которые повышают или усиливают эффективность конечного продукта. Гели могут быть приготовлены с диапазоном вязкости от густых гелей или с высокой вязкостью до разжиженных или с низкой вязкостью. Указанные препараты, подобные лосьонам и кремам, также могут содержать растворители, эмульгирующие средства, увлажняющие средства, смягчающие вещества, ароматизирующие вещества, красители/красящие вещества, консерванты и другие активные ингредиенты, которые повышают или усиливают эффективность конечного продукта. Жидкости являются более текучими, чем кремы, лосьоны или гели и часто не содержат эмульгирующие средства. Жидкие местнодействующие продукты часто содержат растворители, эмульгирующие средства, увлажняющие средства, смягчающие вещества, ароматизирующие вещества, красители/красящие вещества,консерванты и другие активные ингредиенты, которые повышают или усиливают эффективность конечного продукта. Подходящие эмульгирующие средства для использования в препаратах местного действия включают, но не ограничиваются ими, ионные эмульгирующие средства, цетиариловый спирт, неионные эмульгирующие средства, подобные полиоксиэтиленолеиловому эфиру, стеарат ПЭГ-40, цетеарет-12, цетеарет-20, цетеарет-30, цетеаретовый спирт, стеарат ПЭГ-100 и глицерилстеарат. Подходящие регулирующие вязкость средства включают, но неограничиваются ими, защитные коллоиды или неионные камеди,такие как гидроксиэтилцеллюлоза, ксантановая камедь, силикат магнияалюминия, двуокись кремния,микрокристаллический воск, пчелиный воск, парафин и цетилпальмитат. Гелевая композиция может быть приготовлена путем добавления гелеобразующего средства, такого как хитозан, метилцеллюлоза,этилцеллюлоза, поливиниловый спирт, поликватерниумы, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбомер или аммонизированный глицирризинат. Подходящие поверхностно-активные вещества включают, но не ограничиваются ими, неионные, амфотерные, ионные и анионные поверхностно-активные вещества. Например, один или более средства из диметиконкополиола, полисорбата 20, полисорбата 40, полисорбата 60, полисорбата 80, лаурамида DEA, кокамидаDEA и кокамида МЕА, олеилбетаина, кокамидопропилфосфатидил PG-димониум хлорида и аммония лауретсульфата могут быть использованы в препаратах местного действия. Подходящие консерванты включают, но не ограничиваются ими, противомикробные средства, такие как метилпарабен, пропилпарабен, сорбиновая кислота, бензойная кислота и формальдегид, а также физические стабилизаторы и антиоксиданты, такие как витамин Е, аскорбат натрия/аскорбиновая кислота и пропилгаллат. Подходящие увлажняющие средства включают, но не ограничиваются ими, молочную кислоту и другие гидроксикислоты и их соли, глицерин, пропиленгликоль и бутиленгликоль. Подходящие смягчающие средства включают ланолиновый спирт, ланолин, производные ланолина, холестерин, вазелин, изостеарилнеопентаноат и минеральные масла. Подходящие ароматизирующие средства и красители включают, но не ограничиваются ими, FDC Red No. 40 FDC Yellow No. 5. Другие подходящие дополнительные ингредиенты,которые могут быть включены в препарат местного действия, включают, но не ограничиваются ими, абразивные средства, абсорбенты, средства, предотвращающие слипание, противовспенивающие средства,антистатические средства, вяжущие средства (например, гамамелис, спирт и травяные экстракты, такие как экстракт ромашки), связывающие вещества/наполнители, буферные компоненты, хелатирующие средства, пленкообразующие средства, кондиционирующие компоненты, пропелланты, замутняющие компоненты, регулирующие рН средства и защитные средства. Примером подходящего носителя для местного препарата в виде геля является: гидроксипропилцеллюлоза (2,1%); смесь 70/30 изопропиловый спирт/вода (90,9%); пропиленгликоль (5,1%) и полисорбат 80 (1,9%). Примером подходящего носителя для местного препарата в виде пены является: цетиловый спирт (1,1%); стеариловый спирт (0,5%); кватерниум 52 (1,0%); пропиленгликоль (2,0%); этанол 95 PGF3(61,05%); деионизированная вода (30,05%); Р 75 углеводородный пропеллант (4,30%). Все проценты даны в расчете на массу. Обычные способы доставки местных композиций включают нанесение с помощью пальцев; нанесение посредством физического аппликатора, такого как салфетка, ткань, тампон, шпатель или щеточка; разбрызгивание (включающее распылитель, аэрозоль или пенораспылитель); нанесение с помощью капельницы (пипетки); насыпание; намачивание и промывание. Фармацевтическая композиция может быть приготовлена в виде стерилизованной инъецируемой водной или масляной суспензии. Соединение(я), представленные в описании, в зависимости от носителя и используемой концентрации, могут либо быть суспендированы, либо растворены в носителе. Такая композиция может быть приготовлена согласно известным способам в данной области с использованием подходящих диспергирующих, увлажняющих средств и/или суспендирующих средств, таких как средства, перечисленные выше. Среди приемлемых носителей и растворителей, которые могут быть использованы, имеются вода, 1,3-бутандиол, раствор Рингера и изотоничный раствор хлорида натрия. Кроме того,стерилизованные нелетучие масла могут быть использованы в виде растворителя или суспендирующей среды. Для этих целей любое безвкусное нелетучее масло может быть использовано, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, нашли применение в приготовлении инъецируемых композиций, и адъюванты, такие как местные анестетики, консерванты и/или буферные вещества, могут быть растворены в носителе. Фармацевтические композиции могут быть приготовлены в виде суппозиториев (например, для ректального введения). Такие композиции могут быть приготовлены путем смешивания лекарственного средства с подходящим нераздражающим наполнителем, который является твердым веществом при обычных температурах, но жидким при ректальной температуре, и, следовательно, будет расплавляться в прямой кишке с высвобождением лекарственного средства. Подходящие наполнители включают, например, масло какао и полиэтиленгликоли. Композиции для ингаляции обычно получают в виде раствора, суспензии или эмульсии, которые можно вводить в виде сухого порошка или в виде аэрозоля с использованием обычного пропелланта (например, дихлордифторметан или трихлорфторметан). Фармацевтические композиции могут быть получены для высвобождения при предопределенной скорости. Немедленное высвобождение может быть достигнуто, например, путем сублингвального введения (например, перорально таким способом, что активный ингредиент(ы) быстро всасывается через кровеносные сосуды под языком скорее, чем через пищеварительный тракт). Препараты с контролируемым высвобождением (например, препараты, такие как капсула, таблетка или покрытая оболочкой таблетка, которые замедляют или задерживают высвобождение активного ингредиента (ов) после введения) могут быть введены, например, посредством пероральной, ректальной или подкожной имплантации или путем имплантации у участка-мишени. Обычно, препарат с контролируемым высвобождением содержит матрикс и/или покрытие, которое задерживает дезинтеграцию и всасывание в желудочно-кишечном тракте (или участке имплантации) и, тем самым, способствует отсроченному действию или замедленному действию в течение более длительного периода. Один тип препарата с контролируемым высвобождением является препаратом с замедленным высвобождением, у которого по меньшей мере один активный ингредиент постоянно высвобождается в течение периода времени при постоянной скорости. Предпочтительно терапевтическое средство высвобождается при такой скорости, что концентрации в крови (например, плазме) сохраняются в терапевтическом диапазоне, но ниже токсического уровня, в течение периода времени, который составляет по меньшей мере 4 ч, предпочтительно по меньшей мере 8 ч и более предпочтительно по меньшей мере 12 ч. Такие препараты обычно получают с использованием хорошо известного способа и вводят, например, посредством пероральной, ректальной или подкожной имплантации или путем имплантации у желаемого участка-мишени. Носителями для использования в таких препаратах являются биосовместимые носители, и также могут быть биодеградируемые носители; предпочтительно, когда препарат сохраняет относительно постоянный уровень высвобождения модулятора. Количество модулятора, содержащегося в препарате с замедленным высвобождением, зависит от, например, участка имплантации, скорости и желаемой продолжительности высвобождения и природы состояния, которое подвергается лечению или профилактике. Контролируемое высвобождение может быть достигнуто путем комбинирования активного ингредиента(ов) с матриксным материалом, который сам по себе изменяет скорость высвобождения, и/или посредством использования покрытия с контролируемым высвобождением. Скорость высвобождения можно изменять с помощью способов, хорошо известных в данной области, включающих (а) изменение толщины или состава покрытия, (b) изменение количества пластификатора и способа его добавления в покрытие, (с) включение дополнительных ингредиентов, таких как средства, модифицирующие высвобождение, (d) изменение состава, размера частиц или формы частиц матрикса и (е) предоставление одного или более путей прохождения через покрытие. Количество модулятора, содержащегося в препарате с замедленным высвобождением, зависит от, например, способа введения (например, участок имплантации), скорости и желаемой продолжительности высвобождения и природы состояния, которое подвергается лечению или профилактике. Матриксным материалом, который сам по себе может или не может выполнять функцию контролируемого высвобождения, обычно является любой материал, который поддерживает активный ингредиент(ы). Например, материал замедленного действия, такой как глицерилмоностеарат или глицерилдистеарат, может быть использован. Активный ингредиент(ы) может быть комбинирован с матриксным материалом до образования дозированной формы (например, таблетки). Альтернативно, или в добавление, активный ингредиент(ы) может быть нанесен на поверхности частицы, гранулы, сферы, микросферы, шарика или катышка, который содержит матриксный материал. Такое покрытие может быть получено обычными способами, такими как растворение активного ингредиента(ов) в воде или другом подходящем растворителе и разбрызгивание. Необязательно, дополнительные ингредиенты добавляют до нанесения покрытия (например, чтобы способствовать связыванию активного ингредиента(ов) с матриксным материалом или окрашивать раствор). Затем, матрикс можно покрывать защитным средством до нанесения покрытия с контролируемым высвобождением. Единицы матрикса с многослойным покрытием, если желательно, можно инкапсулировать с получением конечной дозированной лекарственной формы. В некоторых вариантах осуществления изобретения контролируемое высвобождение достигается посредством использования покрытия с контролируемым высвобождением (например, покрытие, которое допускает высвобождение активного ингредиента(ов) при контролируемой скорости в водной среде). Покрытие с контролируемым высвобождением должно быть прочным, в виде непрерывной пленки, которая является гладкой, способной поддержать пигменты и другие добавки, нетоксичной, инертной и нелипнущей. Покрытия, которые регулируют высвобождение модулятора, включают рН-независимые покрытия, рН-зависимые покрытия (которые могут быть использованы для высвобождения модулятора в желудке) и энтеросолюбильные покрытия (которые позволяют препарату проходить интактным через желудок и в тонкую кишку, где покрытие растворяется, и содержимое всасывается организмом). Очевидно, что многослойные покрытия могут быть использованы (например, чтобы допустить высвобождение части дозы в желудке и далее части дозы по всему желудочно-кишечному тракту). Например, часть активного ингредиента(ов) может быть нанесена на энтеросолюбильное покрытие, и, тем самым, указанная часть высвобождается в желудке, в то время как остальная часть активного ингредиента(ов) в матриксной сердцевине защищена энтеросолюбильным покрытием и высвобождается далее в сторону GI тракта. рН-Зависимые покрытия включают, например, шеллак, целлюлозаацетатфталат, поливинилацетатфталат, гидроксипропилметилцеллюлозафталат, сополимеры метакриловой кислоты и зеина. В некоторых вариантах осуществления изобретения покрытие представлено гидрофобным материалом, предпочтительно используемым в количестве, эффективном для замедления гидратации гелеобразующего средства после введения. Подходящие гидрофобные материалы включают алкилцеллюлозы(например, этилцеллюлоза или карбоксиметилцеллюлоза), простые эфиры целлюлозы, сложные эфиры целлюлозы, акриловые полимеры (например, поли(акриловая кислота), поли(метакриловая кислота), сополимеры акриловой кислоты и метакриловой кислоты, сополимеры метилметакрилата, этоксиэтилметакрилаты, цианоэтилметакрилат, сополимер алкамида метакриловой кислоты, поли(метилметакрилат),полиакриламид, сополимеры аммония метакрилата, сополимер аминоалкилметакрилата, сополимеры поли(ангидрида метакриловой кислоты) и глицидилметакрилата) и смеси упомянутых выше соединений. Характерные примеры водных дисперсий этилцеллюлозы включают, например, AQUACOAT (FMCCorp., Philadelphia, PA) и SURELEASE (Colorcon, Inc., West Point, PA), оба примера из которых могут быть применены к субстрату согласно инструкциям производителя. Типичные акриловые полимеры включают, например, различные полимеры EUDRAGIT (Rohm America, Piscataway, NJ) , которые могут быть использованы самостоятельно или в комбинации в зависимости от желаемого профиля высвобождения, согласно инструкциям производителя. Физические свойства покрытий, которые включают водную дисперсию гидрофобного материала,могут быть улучшены добавлением одного или более пластификаторов. Подходящие пластификаторы для алкилцеллюлоз включают, например, дибутилсебацат, диэтилфталат, триэтилцитрат, трибутилцитрат и триацетин. Подходящие пластификаторы для акриловых полимеров включают, например, сложные эфиры лимонной кислоты, такие как триэтилцитрат и трибутилцитрат, дибутилфталат, полиэтиленгликоли, пропиленгликоль, диэтилфталат, касторовое масло и триацетин. Покрытия с контролируемым высвобождением обычно наносят обычными способами, такими как разбрызгивание в виде водной дисперсии. Если желательно, покрытие может иметь поры или каналы для облегчения высвобождения активного ингредиента. Поры и каналы могут быть образованы хорошо известными способами, включающими добавление органического или неорганического материала, который растворяется, экстрагируется или выносится из покрытия в среду, где используется активный ингредиент. Некоторые такие порообразующие материалы включают гидрофильные полимера, такие как гидроксиалкилцеллюлозы (например, гидроксипропилметилцеллюлоза), простые эфиры целлюлозы, синтетические водорастворимые полимеры (например, поливинилпирролидон, поперечносвязанный поливинилпирролидон и полиэтиленоксид), водорастворимую полидекстрозу, сахариды и полисахариды и соли щелочных металлов. Альтернативно, или в добавление, покрытие с контролируемым высвобождением может включать одно или более отверстия, образованные способами, такими как описаны в патентах США 3845770; 4034758; 4077407; 4088864; 4783337 и 5071607. Контролируемое высвобождение может быть достигнуто с помощью трансдерамальных пластырей при использовании обычного способа(см., например, патент США 4668232). Другие примеры препаратов с контролируемым высвобождением и их компоненты можно найти,например, в патентах США 4572833; 4587117; 4606909; 4610870; 4684516; 4777049; 4994276; 4996058; 5128143; 5202128; 5376384; 5384133; 5445829; 5510119; 5618560; 5643604; 5891474; 5958456; 6039980; 6143353; 6126969; 6156342; 6197347; 6387394; 6399096; 6437000; 6447796; 6475493; 6491950; 6524615; 6838094; 6905709; 6923984; 6923988; и 6911217; каждый из которых включен в описание посредством ссылки для получения рекомендаций по приготовлению дозированных лекарственных форм с контролируемым высвобождением. В добавление к или вместе с указанными выше способами введения, представленное в описании соединение может быть добавлено обычным образом к пище или питьевой воде (например, для введения животным, отличным от человека, включающим домашние животные (например, собаки и кошки) и скот). Пищевые композиции и водные композиции, содержащие питьевую воду, для животных могут быть приготовлены таким образом, что животное принимает в соответствующем количестве композицию наряду с его едой. Также, может быть целесообразным подавать композицию в виде примикса для добавления к пище или питьевой воде. Соединения обычно вводят в терапевтически эффективном количестве. Предпочтительные системные дозы составляют не выше 50 мг на килограмм массы тела в день (например, изменяющиеся дозы приблизительно от 0,001 до 50 мг на килограмм массы тела в день), с пероральными дозами, обычно составляющими приблизительно в 5-20 раз выше внутривенных доз (например, изменяющиеся дозы от 0,01 до 40 мг на килограмм массы тела в день). Количество активного ингредиента, который может быть объединен с материалами-носителями для получения стандартной лекарственной формы, будет изменяться в зависимости, например, от больного,- 19020332 подвергаемого лечению, отдельного способа введения и любых других вводимых совместно лекарственных средств. Дозированные единицы обычно содержат приблизительно от 10 мкг до 500 мг активного ингредиента. Оптимальные дозировки могут быть установлены посредством стандартного испытания и процедур, которые хорошо известны в данной области. Фармацевтические композиции могут быть упакованными для лечения состояний, отвечающих на модуляцию рецептора Р 2 Х 7 (например, боль, воспаление, нейродегенеративное нарушение или другое состояние, представленное в описании). Упакованные фармацевтические композиции обычно включают(i) контейнер с заключенной в нем фармацевтической композицией, содержащей по меньшей мере один модулятор, представленный в описании, и (ii) инструкции (например, ярлык или листок-вкладыш в упаковке), указывающие, что содержащаяся композиция должна использоваться для лечения состояния, отвечающего на модуляцию рецептора Р 2 Х 7 у больного. Способы использования Модуляторы рецептора Р 2 Х 7, представленные в описании, могут быть использованы для изменения активности и/или активации рецепторов Р 2 Х 7 в ряде контекстов, как in vitro, так и in vivo. В некоторых аспектах антагонисты рецептора Р 2 Х 7 могут быть использованы для ингибирования связывания лигандаагониста с рецептором Р 2 Х 7 in vitro или in vivo. Вообще, такие способы включают стадию контакта рецептора Р 2 Х 7 с одним или более модуляторами рецептора Р 2 Х 7, представленными в описании, в присутствии лиганда в водном растворе и в условиях, противоположных подходящим для связывания лиганда с рецептором Р 2 Х 7. Обычно, модулятор(ы) присутствует в концентрации, достаточной для изменения сигнальной трансдукции, опосредованной рецептором Р 2 Х 7 (при использовании анализа, описанного в примере 7). Рецептор Р 2 Х 7 может находиться в растворе или суспензии (например, в изолированной мембране или клеточном препарате) или в культивированной или изолированной клетке. В некоторых вариантах осуществления изобретения рецептор Р 2 Х 7 экспрессируется клеткой, которая имеется у больного, и водным раствором является жидкость организма. Предпочтительно один или более модуляторы вводят животному в таком количестве, что модулятор присутствует по меньшей мере в одной жидкости тела животного при терапевтически эффективной концентрации, составляющей 20 мкм/л или меньше, 10 мкм/л или меньше, 5 мкм/л или меньше или 1 мкм/л или меньше. Например, такие соединения можно вводить при терапевтически эффективной дозе, составляющей менее чем 20 мг/кг массы тела, предпочтительно менее чем 5 мг/кг и, в некоторых случаях, менее чем 1 мг/кг. Следующие примеры предложены для иллюстрации, а не для ограничения изобретения. Если не указано иное, все реагенты и растворители имеют стандартное торговое качество и используются без дальнейшей очистки. Посредством обычных модификаций, исходные материалы могут быть изменены, и дополнительные стадии могут использоваться для получения других соединений, представленных в описании. Данные масс-спектроскопии получены с помощью МС с электрораспылением, в режиме определения положительных ионов. Если не указано иное, такие данные получали с помощью прибора MicromassGlobal Server, с обработкой данных OpenLynx и AutoLynx использовали для сбора данных и анализа. Условия МС были следующие: напряжение на входе в капилляр = 3,5 кВ; напряжение на конусе=30 В,температура десольватации и источника=350 и 120 С соответственно; диапазон массовых чисел = 181750 со временем считывания 0,22 с и задержкой между сканами 0,05 с. Относительно данных, обозначенных символом "," данные масс-спектроскопии получали с помощью масс-спектрометра Waters ZMD II Mass Spectrometer (Waters Corp.), снабженного насосом Waters 600 (Waters Corp.), детектором с фотодиодным устройством Waters 996 (Waters Corp.) и автоматическим дозатором Gilson 215 (Gilson, Inc.; Middleton, WI). Программное обеспечение MassLynx (Waters Corp.) версия 4.0 с OpenLynx Global Server, с обработкой данных OpenLynx и AutoLynx использовали для сбора данных и анализа. Условия МС были следующие: напряжение на входе в капилляр = 3,5 кВ; напряжение на конусе = 30 В, температура десольватации и источника= 250 и 100 С, соответственно; диапазон массовых чисел = 100-800 со временем считывания 0,5 с и задержкой между сканами 0,1 с. Для любого метода, объем образца 1 мкл впрыскивали в колонку 504,6 мм Chromolith SpeedRODRP-18e (Merck KGaA, Darmstadt, Germany) и элюировали, используя 2-фазный линейный градиент при скорости потока 6 мл/мин. Образец детектировали, используя общий счет поглощения в диапазоне 220340 нм в УФ-области. Условия элюции были следующие: подвижная фаза А - 95% вода, 5% МеОН с 0,05% ТФУ; подвижная фаза В - 5% вода, 95% МеОН с 0,025% ТФУ. Следующий градиент использовали: 0-0,5 мин 10-100% В, удержание при 100% В до 1,2 мин, возвращение к 10% В при 1,21 мин. Цикл от впрыскивания до впрыскивания составлял 2,15 мин. Где указано, время удерживания (RT) при ЖХ дано в мин. Калий t-бутилат (2,52 г, 0,022 моль) добавляли к смеси метил 1 Н-индол-3-карбоксилата (3,5 г, 0,02 моль) и 2-хлорпиримидина (2,28 г, 0,02 моль) в 50 мл диоксана. Реакционную смесь нагревали до 110 С и перемешивали в течение 20 ч. Диоксан удаляли в вакууме и остаток разбавляли водой (100 мл). Твердое вещество фильтровали и очищали колоночной хроматографией на силикагеле (15% EtOAc/ДХМ) с получением указанного в заголовке соединения в виде белого твердого вещества. Стадия 2. 1-(Пиримидин-2-ил)-1 Н-индол-3-карбоновая кислота 1,0 N Водный раствор NaOH (10 мл) добавляли к смеси метил 1-(пиримидин-2-ил)-1 Н-индол-3 карбоксилата (1,4 г, 0,0055 моль) в 50 мл EtOH и нагревали при 70 С в течение 4 ч. Реакционную смесь концентрировали в вакууме, разбавляли водой (50 мл), подкисляли концентрированной HCl до рН 2,0. Отделенное белое твердое вещество фильтровали, промывали водой (225 мл) и сушили с получением указанного в заголовке соединения. Стадия 3. N-(Адамантан-1-илметил)-1-пиримидин-2-ил-1 Н-индол-3-карбоксамид К смеси 1-(пиримидин-2-ил)-1 Н-индол-3-карбоновой кислоты (72 мг, 0,3 ммоль) в 2,0 мл ДМФ добавляли последовательно диизопропилэтиламин (0,2 мл), 1-адамантанметиламин (49,5 мг, 0,3 ммоль) и ВОР (150 мг). Образовавшуюся смесь перемешивали при кт в течение 20 ч. Воду (3 мл) добавляли, и твердое вещество фильтровали и очищали колоночной хроматографией на силикагеле (25% смесьEtOAc/гексан) с получением указанного в заголовке соединения в виде белого твердого вещества. 1 Круглодонную колбу с 50 мл ДМФ охлаждали до 0 С и хлорокись фосфора (8,1 мл, 88 ммоль) добавляли по каплям. После перемешивания в течение приблизительно 5 мин раствор 4-броминдола (5,0 мл, 40 ммоль) в 50 мл ДМФ добавляли по каплям. Баню со льдом удаляли и реакционную смесь перемешивали в течение 1 ч при кт. Реакционная смесь превращалась в густую суспензию. Смесь вновь охлаждали до 0 С и реакцию осторожно гасили 22 г KOH в 80 мл воды. Образовавшуюся смесь распределяли между EtOAc (200 мл) и насыщенным раствором NaHCO3 (100 мл). Слой EtOAc промывали насыщен- 21020332 ным раствором соли (100 мл) и водой (100 мл), сушили (Na2SO4), фильтровали и упаривали в вакууме с получением коричневого твердого вещества, которое растирали в эфире с получением указанного в заголовке соединения в виде не совсем белого твердого вещества. Стадия 2. 4-(Трифторметил)-1 Н-индол-3-карбальдегид Метил 2-(фторсульфонил)дифторацетат (3,5 мл, 27,6 ммоль) и йодид меди (I) (5,3 г, 27,6 ммоль) добавляли к раствору 4-бром-1 Н-индол-3-карбальдегида (3,1 г, 13,8 ммоль) в 65 мл ДМФ. Реакционную смесь нагревали до 85 С в течение 18 ч. После охлаждения до кт смесь разбавляли EtOAc и фильтровали через целит. Целит тщательно промывали EtOAc. Фильтрат промывали водой (3 раза) и насыщенным раствором соли, сушили (Na2SO4), фильтровали и упаривали с получением коричневого масла. Очисткой колоночной хроматографией на силикагеле (градиент от смеси 10% EtOAc/гексан до смеси 40%EtOAc/гексан) получили указанное в заголовке соединение в виде коричневого твердого вещества. Стадия 3. 1-Пиримидин-2-ил-4-(трифторметил)-1 Н-индол-3-карбальдегид Калия t-бутилат (753 мг, 6,71 ммоль) добавляли к смеси 4-(трифторметил)-1 Н-индол-3 карбальдегида (1,3 г, 6,10 ммоль) и 2-хлорпиримидина (699 мг, 6,10 ммоль) в 20 мл диоксана. Реакционную смесь нагревали до 100 С и перемешивали в течение 15 ч. Диоксан удаляли в вакууме, и остаток распределяли между EtOAc и водой (30 мл каждого раствора). Водную фазу экстрагировали еще два разаEtOAc (20 мл каждый раз) и объединенные EtOAc-экстракты сушили (Na2SO4), фильтровали и упаривали в вакууме с получением коричневого твердого вещества. Очисткой колоночной хроматографией на силикагеле (смесь 2% EtOAc/ДХМ) получали указанное в заголовке соединение в виде светло-коричневого твердого вещества. Стадия 4. 1-Пиримидин-2-ил-4-(трифторметил)-1 Н-индол-3-карбоновая кислота К раствору 1-пиримидин-2-ил-4-(трифторметил)-1 Н-индол-3-карбальдегида (450 мг, 1,55 ммоль) в 15 мл диоксана и 5 мл воды добавляли хлорид натрия (183 мг, 2,02 ммоль) и сульфаминовую кислоту(858 мг, 8,84 ммоль). После перемешивания при кт в течение 10 мин реакцию осторожно гасили насыщенным водным раствором NaHCO3 и концентрировали в вакууме. Остаток брали в смеси 10% МеОН/ДХМ и промывали 10% HCl и водой. Объединенные водные фазы вновь экстрагировали 10% смесью МеОН/ДХМ (4 раза) и объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали в вакууме с получением бледно-желтого твердого вещества. Растиранием в эфире получали указанное в заголовке соединение в виде белого твердого вещества. Стадия 5. (1-Пиридин-3-илциклогексил)метиламин(450 мл) добавляли NaH (60% в минеральном масле, 10,42 г) порциями при 0 С в течение 1 ч. Смесь оставляли нагревать до кт и перемешивали в течение ночи. Реакционную смесь выливали в воду и экстрагировали EtOAc. Экстракт концентрировали и остаток очищали хроматографией на силикагеле с получением 1-пиридин-3-илциклогексанкарбонитрила. К раствору полученного выше продукта (18,5 г) в 140 мл 7,0 N NH3 в MeOH осторожно добавляли суспензию никеля Ренея (16 г). Смесь подвергали гидрированию при давлении 50 фунтов/кв. дюйм в течение ночи. Смесь фильтровали через целит и концентрировали в вакууме с получением указанного в заголовке соединения. Стадия 6. N-[(1-Пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-4-(трифторметил)-1 Н-индол 3-карбоксамид К смеси 1-1-метил-1 Н-имидазол-2-ил)метил)-1 Н-индол-2-карбоновой кислоты (21 мг, 0,05 ммоль) в 1,0 мл ДМФ добавляли последовательно диизопропилэтиламин (0,02 мл, 0,10 ммоль), 1-(1-пиридин-3 илциклогексил)метанамин (9,5 мг, 0,05 ммоль) и ВОР (27 мг, 0,06 ммоль). Образовавшуюся смесь перемешивали при кт в течение 20 ч. Воду (3 мл) добавляли и смесь экстрагировали EtOAc (5 мл). СлойEtOAc сушили (Na2SO4), фильтровали и упаривали в вакууме. Остаток очищали препаративной хроматографией (4% смесь МеОН/ДХМ) с получением указанного в заголовке соединения в виде светлокоричневого твердого вещества. 1 Стадия 1. 1-(4-Хлор-1 Н-индол-3-ил)-2,2,2-трифторэтанон Трифторуксусный ангидрид (27,5 мл, 200 ммоль) добавляли к раствору 4-хлориндола (25,0 г, 165 ммоль) и ДМФ (170 мл) в атмосфере N2 в течение 30 мин. Реакционный сосуд герметично закрывали. Через 20 ч раствор выливали в воду (700 мл) и экстрагировали EtOAc (300 мл). Органические слои сушили над Na2SO4, фильтровали и концентрировали. Очисткой колоночной флэш-хроматографией на силикагеле (смесь от 4:1 гексан/EtOAc до 1:1 гексан/EtOAc) получали указанное в заголовке соединение в виде красно-бурого твердого вещества. Стадия 2. 1-(4-Хлор-1-пиримидин-2-ил-1 Н-индол-3-ил)-2,2,2-трифторэтанон Смесь 1-(4-хлор-1 Н-индол-3-ил)-2,2,2-трифторэтанона (10,1 г, 40,8 ммоль), 2-хлорпиримидина (9,3 г, 81 ммоль), карбоната цезия (26,6 г, 81,6 ммоль) и 1,4-диоксана (80 мл) в атмосфере N2 нагревали до 100 С в течение 3 ч. После охлаждения до кт добавляли воду (200 мл). Осадок собирали фильтрованием с получением указанного в заголовке соединения в виде порошка рыжеватого цвета. Стадия 3. 4-Хлор-1-пиримидин-2-ил-1 Н-индол-3-карбоновая кислота водного раствора NaOH (60 мл), воды (20 мл) и этанола (20 мл) в атмосфере воздуха нагревали до 65 С в течение 20 ч. После охлаждения до кт летучие компоненты удаляли при пониженном давлении. Водную смесь охлаждали до 0 С и затем подкисляли 5 М водным раствором HCl (110 мл). Смесь фильтровали. Фильтрат промывали Н 2 О (50 мл) и затем Et2O (100 мл) с получением указанного в заголовке соединения в виде порошка рыжеватого цвета. Стадия 4. 4-Хлор-N-[(1-пиридин-3-илциклогексил)метил]-1-пиримидин-2-ил-1 Н-индол-3-карбоксамид ВОР (58 мг, 130 ммоль) добавляли к суспензии 4-хлор-1-пиримидин-2-ил-1 Н-индол-3-карбоновой кислоты (27 мг, 98 ммоль), (1-пиридин-3-илциклогексил)метиламина (21 мг, 110 ммоль), iPr2NEt (50 мкл,290 ммоль) и ДМФ (0,5 мл) в атмосфере N2. Реакционный сосуд герметично закрывали и раствор оставляли перемешивать в течение 64 ч. Раствор выливали в 50% насыщенный водный раствор NaHCO3 (10 мл) и затем экстрагировали EtOAc (210 мл). Объединенные органические слои сушили над Na2SO4,фильтровали и концентрировали. Очисткой PTLC (смесь 95:5 ДХМ/МеОН) получали указанное в заголовке соединение в виде белого порошка. 1 ЯМР (400 МГц, CDCl3)8,61-8,77 (м, 4 Н), 8,55 (с, 1 Н), 8,41 (с, 1 Н), 7,75 (д, 1 Н), 7,08-7,31 (м, 4 Н),6,14 (с, 1 Н), 3,68 (д, 2 Н), 2,11-2,22 (м, 2 Н), 1,28-1,86 (м, 8 Н). ЖХ-МС m/z (M+H+): 446,18. Пример 4. 60% NaH (527 мг, 0,0132 моль) добавляли к смеси этил 1 Н-индол-2-карбоксилата (1,13 г, 0,0059 моль) в ДМФ (20 мл) при кт и перемешивали в течение 20 ч. Смесь разбавляли ледяной водой (100 мл) и белое твердое вещество фильтровали с получением указанного в заголовке соединения. Стадия 2. 1-1-Метил-1 Н-имидазол-2-ил)метил)-1 Н-индол-2-карбоновая кислота 1,0 N Водный раствор NaOH (10 мл) добавляли к смеси этил 1-1-метил-1 Н-имидазол-2-ил)метил)1 Н-индол-2-карбоксилата (1,5 г, 0,0053 ммоль) в 25 мл EtOH и перемешивали при 25 С в течение 16 ч. Реакционную смесь концентрировали в вакууме, разбавляли водой (50 мл) и подкисляли концентрированной HCl до рН 2,0. Отделенное белое твердое вещество фильтровали, промывали водой (225 мл) и сушили с получением указанного в заголовке соединения. Стадия 3. N 1-1-метил-1 Н-имидазол-2-ил)метил)-N-1-(пиридин-3-ил)циклогексил)метил)-1 Ниндол-2-карбоксамид К смеси 1-1-метил-1 Н-имидазол-2-ил)метил)-1 Н-индол-2-карбоновой кислоты (51 мг, 0,2 ммоль) в мл ДМФ добавляли последовательно диизопропилэтиламин (0,2 мл), 1-(1-пиридин-3- 24020332 илциклогексил)метанамин (38 мг, 0,25 ммоль) и реагент ВОР (100 мг, 0,22 ммоль). Образовавшуюся смесь перемешивали при кт в течение 20 ч. Воду (3 мл) добавляли и смесь экстрагировали EtOAc (5 мл). Слой EtOAc сушили (Na2SO4), фильтровали и упаривали в вакууме. Остаток очищали колоночной хроматографией на силикагеле (смесь 4% МеОН/ДХМ) с получением указанного в заголовке соединения в виде белого твердого вещества. 1 Этиловый эфир хлоругольной кислоты (230 мкл, 2,4 ммоль) добавляли по каплям в течение 5 мин к суспензии 4-хлор-1-пиримидин-2-ил-1 Н-индол-3-карбоновой кислоты (629 мг, 2,30 ммоль) в iPr2NEt (420 мкл, 2,4 ммоль) и ацетона (7,0 мл) в атмосфере N2 при -10 С. Через 1 ч азид натрия (450 мг, 6,9 ммоль) в воде (4 мл) добавляли одной порцией и смесь оставляли перемешивать в атмосфере воздуха в течение 15 ч. Летучие компоненты удаляли при пониженном давлении. Образовавшуюся водную смесь разбавляли водой (10 мл) и затем фильтровали. Твердые вещества собирали и сушили при пониженном давлении с получением указанного в заголовке соединения в виде порошка рыжеватого цвета. Стадия 2. 4-Хлор-1-пиримидин-2-ил-1 Н-индол-3-иламин Суспензию 4-хлор-1-пиримидин-2-ил-1 Н-индол-3-карбонилазида (442 мг, 1,48 ммоль) в толуоле (5 мл) в атмосфере воздуха нагревали до 100 С в течение 1 ч. Концентрированную HCl (1 мл) добавляли по каплям. Смесь нагревали до 110 С в течение 2 ч. Летучие компоненты удаляли при пониженном давлении. ТЭА (1 мл) и воду (10 мл) добавляли. Смесь экстрагировали CH2Cl2 (430 мл) и объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали. Очисткой колоночной флэшхроматографией (смесь от 5:1 гексаны:EtOAc до 3:1 гексаны:EtOAc) получали указанное в заголовке соединение в виде твердого вещества рыжеватого цвета. ЖХ-МС m/z (M+H+): 244,99. Стадия 3. 2-Адамантан-1-ил-N-(4-хлор-1-пиримидин-2-ил-1 Н-индол-3-ил)ацетамид(50 мг, 200 мкмоль), 1-адамантануксусной кислоты (52 мг, 270 мкмоль), iPr2NEt (70 мкл, 400 мкмоль) и ДМФ (1,0 мл) в атмосфере N2. Реакционный сосуд герметично закрывали и раствор оставляли перемешивать в течение 4,5 дней. Воду (5 мл) добавляли и неочищенный продукт собирали фильтрованием. Твердое вещество растворяли в EtOAc (40 мл) и затем промывали смесью 1:1 воды и насыщенного раствора соли (20 мл). Органические слои сушили над Na2SO4, фильтровали и концентрировали. Очисткой препаративной тонкослойной хроматографией (смесь 7,5:1 гексаны:EtOAc) получали указанное в заголовке соединение в виде порошка цвета слоновой кости. 1 Смесь 4-хлор-1 Н-пирроло[2,3-b]пиридина (1,2 г, 7,6 ммоль), полученную, в основном, как описано в публикации Wang et al., J. Org. Chem. 2006, 77, 4021-4023, и гексаметилентетрамина (1,6 г, 11,4 ммоль) в 10 мл 33% водной уксусной кислоте нагревали с обратным холодильником и перемешивали в течение 14 ч. Прозрачный раствор охлаждали до кт и разбавляли водой. Смесь становилась мутной, и твердое вещество начинало выпадать в осадок из раствора. Смесь охлаждали на бане со льдом и перемешивали в течение 30 мин. Осажденное твердое вещество затем собирали вакуум-фильтрацией и сушили в вакууме с получением указанного в заголовке соединения в виде светло-коричневого твердого вещества. Массспектр. (180,92, М+Н). Стадия 2. 4-Хлор-1-пиримидин-2-ил-1 Н-пирроло[2,3-b]пиридин-3-карбальдегид(210 мг, 1,83 ммоль) и карбоната цезия (476 мг, 1,46 ммоль) в 5-10 мл диоксана нагревали до 100 С. После перемешивания в течение 15 ч реакционную смесь охлаждали и диоксан удаляли в вакууме. Остаток суспендировали в воде и фильтровали. Собранное твердое вещество промывали еще водой и сушили в вакууме с получением указанного в заголовке соединения в виде светло-коричневого твердого вещества. Масс-спектр. (258,95, M+H). Стадия 3. 4-Хлор-1-пиримидин-2-ил-1 Н-пирроло[2,3-b]пиридин-3-карбоновая кислота К смеси 4-хлор-1-пиримидин-2-ил-1 Н-пирроло[2,3-b]пиридин-3-карбальдегида (88 мг, 0,34 ммоль) в 3 мл диоксана и 1 мл воды добавляли хлорид натрия (40 мг, 0,44 ммоль) и сульфаминовую кислоту (188 мг, 1,94 ммоль). После перемешивания при кт в течение 20 мин растворители удаляли в вакууме. Остаток брали в 10% смеси MeOH/CH2Cl2 и образовавшуюся смесь фильтровали. Фильтрат концентрировали и получали указанное в заголовке соединение в виде коричневого твердого вещества. Масс-спектр. (274,95,М+Н). К смеси 4-хлор-1-пиримидин-2-ил-1 Н-пирроло[2,3-b]пиридин-3-карбоновой кислоты (45 мг, 0,16 ммоль) в 1,0 мл ДМФ добавляли последовательно диизопропилэтиламин (0,06 мл, 0,32 ммоль), 1-(1 пиридин-3-илциклогексил)метанамин (30 мг, 0,16 ммоль) и ВОР (84 мг, 0,19 ммоль). Образовавшуюся смесь перемешивали при кт в течение 20 ч. Воду (3 мл) добавляли и выпавшее в осадок твердое вещество собирали вакуум-фильтрацией и сушили в вакууме с получением указанного в заголовке соединения в виде коричневого твердого вещества. 1(8 Н, м). Масс-спектр. (447,15, М+Н). Дополнительные аналоги гетероариламидов, полученные посредством общей методологии, представленной в описании, перечислены в таблице. Обозначение "IC50", указывает, что величина IC50,определенная, как описано в примере 7 А, составляет 2 мкм/л или меньше (т.е. концентрация таких соединений, которая требуется для снижения на 50% флуоресцентного ответа клеток, подвергающихся действию 80 мкМ (2'(3')-О-(4-бензоилбензоил)аденозин 5'-трифосфата, составляет 2 мкм/л или меньше). Данные масс-спектроскопии представлены в таблице как (М+1) в колонке, под заглавием "М+Н". Время удерживания при ЖХ, в мин, представлено в колонке под заглавием RT.
МПК / Метки
МПК: C07D 487/04
Метки: аналоги, гетероариламидов
Код ссылки
<a href="https://eas.patents.su/30-20332-analogi-geteroarilamidov.html" rel="bookmark" title="База патентов Евразийского Союза">Аналоги гетероариламидов</a>
Предыдущий патент: Способ производства фармацевтического препарата, содержащего алискирен
Следующий патент: Фармацевтическая композиция, включающая солифенацин или его фармацевтически приемлемую соль
Случайный патент: Новая порошковая ингаляционная система для чрезлегочного введения












