Акриламидопроизводные, применимые как ингибиторы перехода митохондриальной проницаемости
Номер патента: 20320
Опубликовано: 30.10.2014
Авторы: Минуччи Саверио, Варази Марио, Вилла Мануэла, Каппа Анна, Плит Симон, Паин Джиллес, Балларини Марко, Фанчелли Даниеле, Каренци Джакомо
Формула / Реферат
1. Соединение общей формулы (I)
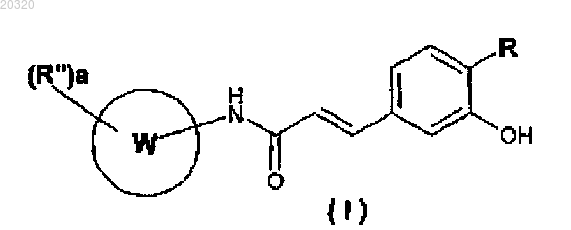
где W является арилом или гетероарилом;
а равно 0, 1 или 2;
R выбран из водорода; галогена; (С1-С3)алкокси; (С1-С2)галоалкокси; (С1-С2)галоалкила; NR1R2; CN; SO2NH2 или необязательно замещенного (С1-С6)алкила, арила или гетероарила;
R" является независимо выбранным из галогена; (С1-С3)алкила; (С1-С3)алкокси; (С1-С3)алкоксиалкила; (С1-С2)галоалкокси; (С1-С2)галоалкила; NR3R4 или (CH2)n-X-(CH2)m-Q, где
n, m независимо равны 0, 1 или 2;
X является прямой связью; O; NH; N(C1-С3)алкилом;
Q является арилом, гетероарилом, гетероциклоалкилом или (С3-С7)циклоалкилом, где
гетероциклоалкил представляет собой 6-членное гетероциклоалкильное кольцо, содержащее 1-3 гетероатома, независимо выбранных из азота или кислорода;
и любой из указанных выше алкила, арила, гетероарила, гетероциклоалкила или (С3-С7)циклоалкила может быть необязательно замещен 1-2 группами, выбранными из галогена, (С1-С6)алкила, (С1-С6)полифторированного алкила, (С3-С7)циклоалкила, 6-12-членного арила, 5-9-членного гетероарила, (С1-С6)алкил-(5-9-членного)гетероарила, (5-9-членного)гетероарил-(С1-С6)алкила, амино-(С1-С6)алкила, аминогрупп (С1-С6)алкиламино, (С1-С6)диалкиламино, ариламино; гидроксигруппы и ее производных (С1-С3)алкокси, (С1-С6)полифторированный алкокси, арилокси, 5-9-членный гетероарилокси, (С3-С7)циклоалкилокси, 5-9-членный гетероциклоалкилокси, арил-(С1-С3)алкокси, 5-9-членный гетероарил-(С1-С3)алкокси; (С1-С6)алкилкарбонил, арилкарбонил;
любой из указанных выше заместителей Q может быть необязательно замещен (С1-С6)алкильной группой;
R1, R2, R3 и R4 являются одинаковыми или разными и независимо друг от друга являются атомом водорода; (С1-С3)алкилом или, когда взяты вместе с атомом азота, к которому они присоединены, R1-N-R2 и R3-N-R4 могут образовывать гетероциклическое кольцо формулы

где R5 является атомом водорода или (С1-С3)алкильной группой;
при условии, что (E)-3-(3-гидроксифенил)-N-[4-[[4-[[(E)-3-(3-гидроксифенил)проп-2-эноил]амино]фенил]метил]фенил]акриламид исключен, и
когда W является фенилом, a не равно 0;
когда W является фенилом и R является водородом, R" не является хлором, метилом, изопропилом, CF3 или NH2;
когда W является индазол-5-илом или пирид-2-илом, R не является водородом, (С1-С3)алкокси;
где арил представляет собой фенил, нафтил или инданил;
где гетероарил представляет собой моноциклическое или бициклическое 5-9-членное ароматическое кольцо, содержащее атомы углерода и 1-4 гетероатома, независимо выбранных из азота, кислорода и серы,
гидроксильная группа может быть в форме ее фосфатного сложного эфира или его соли,
а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры и их смеси и фармацевтически приемлемые соли.
2. Соединение по п.1, где заместители Q могут быть необязательно замещены метильной группой.
3. Соединение по п.1 или 2, где
W является фенильным кольцом, замещенным 1 или 2 группами R";
R является галогеном; (C1-С3)алкокси; (С1-С3)алкилом;
R" является независимо выбранным из галогена; (С1-С3)алкоксиалкила; (С1-С2)галоалкила или (CH2)n-X-(CH2)m-Q,
где n равно 0 или 1;
m равно 0 или 1;
X является O; NH; N(С1-С3)алкилом;
Q является арилом или гетероарилом;
а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, их смеси и фармацевтически приемлемые соли.
4. Соединение по одному из пп.1-3, где
R является фтором; метокси; метилом;
R" является галогеном или (CH2)n-X-(CH2)m-Q, где
n и m выбраны таким образом, что их сумма (n+m) равна 1;
X является О;
Q является арилом или гетероарилом;
а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, их смеси и фармацевтически приемлемые соли.
5. Соединение по п.1, где
W является бициклическим арильным или бициклическим гетероарильным кольцом, необязательно замещенным 1 или 2 группами R";
R является галогеном; (С1-С3)алкокси; (С1-С3)алкилом;
R" является независимо выбранным из галогена; (С1-С2)галоалкила; 4-(С1-С3)алкилпиперазин-1-ила или (CH2)n-X-(CH2)m-Q, где
n равно 0 или 1;
m равно 0 или 1;
X является О; NH; N(С1-С3)алкил;
Q является арилом или гетероарилом;
а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, их смеси и фармацевтически приемлемые соли.
6. Соединение по п.1 или 5, где
W является бициклическим арильным или бициклическим гетероарильным кольцом, незамещенным или замещенным одной группой (CH2)n-X-(CH2)m-Q, где
n и m выбраны таким образом, что их сумма (n+m) равна 1;
X является O;
Q является арилом или гетероарилом;
и необязательно замещенным второй группой R", выбранной из хлора; брома; (С1-С2)галоалкила; 4-(С1-С3)алкилпиперазин-1-ила;
R является фтором; метокси; метилом;
а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, их смеси и фармацевтически приемлемые соли.
7. Соединение формулы (I) по одному из пп.1-6, необязательно в форме своей фармацевтически приемлемой соли, выбранное из группы, включающей
(E)-3-(3-гидрокси-4-метоксифенил)-N-нафталин-1-ил-акриламид;
(E)-N-(2-бензилоксифенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(4-метилпиперазин-1-ил)фенил]акриламид;
(E)-N-(2-хлорпиридин-4-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлор-2-метоксифенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3,4-дихлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлор-4-метоксифенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(2,3-дихлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-бензиламинофенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-[3-(бензилметиламино)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-[2-хлор-3-(пиридин-4-илметокси)фенил]-3-(3-гидрокси-4-метоксифенил)акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{3-[(пиридин-4-илметил)амино]фенил}акриламид;
(E)-N-(3-бензилокси-2-хлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(2-бензилокси-3-хлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(1-бензил-1H-индол-4-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-[3-хлор-2-(пиридин-4-илметокси)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-[4-хлор-3-(пиридин-4-илметокси)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1H-индол-4-ил)акриламид;
(E)-N-(1-бензил-1H-индол-7-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(3-метил-3H-имидазол-4-илметокси)фенил]акриламид;
(E)-3-(4-фтор-3-гидроксифенил)-N-(2-феноксиметилфенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(1H-имидазол-4-илметокси)фенил]акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-4-илоксиметил)фенил]акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-оксазол-5-ил-фенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-индан-1-ил-акриламид;
(E)-N-(2-бензилсульфанилфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1Н-бензимидазол-2-ил)акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(2-феноксиметилфенил)акриламид;
(E)-N-бензоксазол-4-ил-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(1-бензил-1Н-бензимидазол-4-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1Н-бензимидазол-4-ил)акриламида гидрохлорид;
(E)-N-(1-бензил-1Н-индазол-7-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1Н-бензотриазол-4-ил)акриламид;
(E)-N-(1-бензил-1H-индазол-4-ил)-3-(3-гидрокси-4-метоксифенил)акриламида гидрохлорид;
(E)-N-(2-бензил-2Н-индазол-7-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(2-метил-2Н-индазол-7-ил)акриламид;
(E)-N-[3-(2,5-диметил-2Н-пиразол-3-илметокси)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(1-метил-1H-имидазол-2-илметокси)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(3-метоксифеноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(2-метоксифеноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-метоксифеноксиметил)фенил]акриламид;
(E)-N-(2-циклобутоксиметилфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(пиридин-4-илоксиметил)фенил]акриламида гидрохлорид;
(E)-N-[2-(4-фторфеноксиметил)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-имидазол-1-ил-феноксиметил)фенил]акриламид;
(E)-N-[2-(2-фторфеноксиметил)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(2-метоксиметилфенил)акриламид;
(E)-N-[2-(3-фторфеноксиметил)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-бромфенил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-N-(2-бензилоксифенил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-N-(2,3-дихлорфенил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-N-(1-бензил-1H-индол-7-ил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-N-(3-фторфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлорфенил)-3-(3-гидроксифенил)акриламид;
(E)-N-(3-хлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(2-хлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(4-хлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-йодфенил)акриламид;
(E)-N-(3-бромфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-изопропоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-феноксифенил)акриламид;
(E)-N-(3-бензилоксифенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-трифторметилфенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-4-илметокси)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(1-метилпиперидин-3-илметокси)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-4-илокси)фенил]акриламид;
(E)-N-(3,5-дихлорфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(1-метилпиперидин-4-илокси)фенил]акриламид;
(E)-N-(4-бензилоксифенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлорфенил)-3-(3-гидрокси-4-метилфенил)акриламид;
(E)-3-(4-фтор-3-гидроксифенил)-N-нафталин-1-ил-акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(4-метоксипиримидин-2-ил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(1H-тетразол-5-илметокси)фенил]акриламид;
(E)-N-(3-хлорфенил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(2-фенэтилоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(пиридин-4-илметокси)фенил]акриламида гидрохлорид;
(E)-3-(4-фтор-3-гидроксифенил)-N-[3-(пиридин-4-илметокси)фенил]акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-4-илметилсульфанил)фенил]акриламида гидрохлорид;
(E)-N-1,3-бензодиоксол-5-ил-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1H-индазол-7-ил)акриламид;
(E)-N-(4-этокси-1-метил-1H-индазол-7-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(1-метил-1H-индазол-4-ил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(5-метилфуран-2-илметокси)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-3-илметокси)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-(3-фенэтилоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[3-(пиридин-2-илметокси)фенил]акриламид;
(E)-N-(5-хлор-2-феноксиметилфенил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[4-(4-метилпиперазин-1-ил)-2-феноксиметилфенил]акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(3-трифторметилфеноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(3-хлорфеноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-морфолин-4-илметилфеноксиметил)фенил]акриламида гидрохлорид;
(E)-3-(4-фтор-3-гидроксифенил)-N-{2-[4-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламида трифторацетат;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(2-трифторметилфеноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[3-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(пиперидин-4-илокси)феноксиметил]фенил}акриламида гидрохлорид;
(E)-3-(4-хлор-3-гидроксифенил)-N-{2-[3-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(1-метилпиперидин-4-ил)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[2-(4-метилпиперазин-1-ил)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[3-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламида гидрохлорид;
(E)-3-(4-хлор-3-гидроксифенил)-N-(3-хлорфенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[3-(4-метилимидазол-1-ил)феноксиметил]фенил}акриламид;
(E)-3-(2-хлор-3-гидрокси-4-метоксифенил)-N-(3-хлорфенил)акриламид;
(E)-3-(4-фтор-3-гидроксифенил)-N-[3-(пиридин-4-илметилсульфанил)фенил]акриламид;
(E)-N-(1-бензил-1H-индазол-7-ил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламида гидрохлорид;
(E)-N-(3-бензил-3H-бензоимидазол-4-ил)-3-(4-фтор-3-гидроксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-трифторметилфеноксиметил)фенил]акриламид;
(E)-N-[2-(2-хлорфеноксиметил)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[1-(4-имидазол-1-ил-бензил)-1H-индол-7-ил]акриламид;
(E)-3-(4-фтор-3-гидроксифенил)-N-[1-(4-имидазол-1-ил-бензил)-1H-индол-7-ил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(1-метилпиперидин-4-илметил)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[3-(4-метилпиперазин-1-ил)феноксиметил]фенил}акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(4-метилимидазол-1-ил)феноксиметил]фенил}акриламида гидрохлорид;
(E)-N-(1-бензил-2-оксо-2,3-дигидро-1H-индол-7-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлорнафталин-1-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(2-метил-2H-пиразол-3-илоксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(3-пиперазин-1-ил-феноксиметил)фенил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[1-(1-метил-1H-имидазол-4-илметил)-1H-индол-7-ил]акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[1-(1-метил-1H-пиразол-3-илметил)-1H-индол-7-ил]акриламид;
(E)-3-(3-гидроксифенил)-N-(2-феноксиметилфенил)акриламид;
(E)-N-(3-хлорфенил)-3-(2,4-дифтор-3-гидроксифенил)акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-пирролидин-1-илметилфеноксиметил)фенил]акриламида гидрохлорид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(4-метилпиперазин-1-илметил)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[2-(4-пиперидин-1-илметилфеноксиметил)фенил]акриламидатрифторацетат;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{1-[3-(1-метилпиперидин-4-илокси)бензил]-1H-индол-7-ил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[2-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[3-(1-метилпиперидин-4-ил)феноксиметил]фенил}акриламид;
(E)-3-(3-гидрокси-4-метоксифенил)-N-{2-[4-(4-метилпиперазин-1-ил)феноксиметил]фенил}акриламида трифторацетат;
(E)-3-(4-фтор-3-гидроксифенил)-N-[2-(4-имидазол-1-ил-феноксиметил)фенил]акриламид;
(E)-3-(2,4-дифтор-3-гидроксифенил)-N-{2-[3-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(2-хлор-3-гидрокси-4-метоксифенил)-N-{2-[3-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-N-(3-хлорфенил)-3-(4-циано-3-гидроксифенил)акриламид;
(E)-3-(4-циано-3-гидроксифенил)-N-{2-[3-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(2,4-дифтор-3-гидроксифенил)-N-{2-[3-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(2,4-дифтор-3-гидроксифенил)-N-{2-[4-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(2,4-дифтор-3-гидроксифенил)-N-{2-[4-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(2-хлор-3-гидрокси-4-метоксифенил)-N-{2-[3-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(4-циано-3-гидроксифенил)-N-{2-[3-(пиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-3-(4-циано-3-гидроксифенил)-N-{2-[4-(1-метилпиперидин-4-илокси)феноксиметил]фенил}акриламид;
(E)-N-(3-бензил-3H-бензоимидазол-4-ил)-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-[2-(4-хлорфеноксиметил)фенил]-3-(3-гидрокси-4-метоксифенил)акриламид;
(E)-N-(3-хлорфенил)-3-(3-гидрокси-4-сульфамоилфенил)акриламид;
натрия (E)-5-(3-(3-хлорфениламино)-3-оксопроп-1-енил)-2-метоксифенил фосфат;
(E)-3-(3-гидрокси-4-метоксифенил)-N-[1-(3-метил-3H-имидазол-4-илметил)-1H-индол-7-ил]акриламид;
(E)-N-(3-хлорфенил)-3-(4-амино-3-гидроксифенил)акриламид;
а также их изомеры, рацемические формы, энантиомеры, диастереомеры и их смеси.
8. Способ получения соединения общей формулы (I) по любому одному из предыдущих пунктов, при котором
(а) приводят в реакцию гидроксикоричную кислоту формулы (II), где R является таким, как определено в п.1, с защитным средством гидроксила для получения соответствующего защищенного соединения формулы (III)
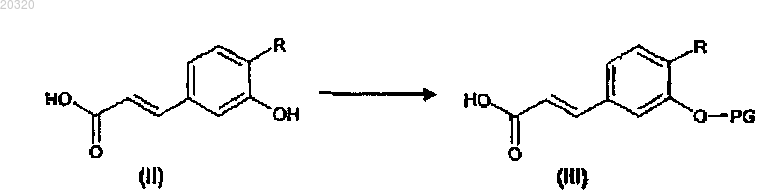
где PG является указанной защитной группой;
(b) активируют карбоксильную часть соединения формулы (III), как определено выше, для амидирования, чтобы получить соединение формулы (V)
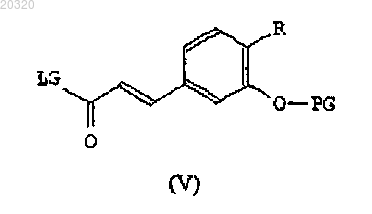
где R и PG являются такими, как определено выше, и LG является любой подходящей активационной группой карбоксильной части;
(с) ацилируют аминосоединение формулы (IV), где W, R" и а являются такими, как определено в п.1, с соединением формулы (V), как определено выше, для получения соединения формулы (VI), где R, R", W, а и PG являются такими, как определено выше
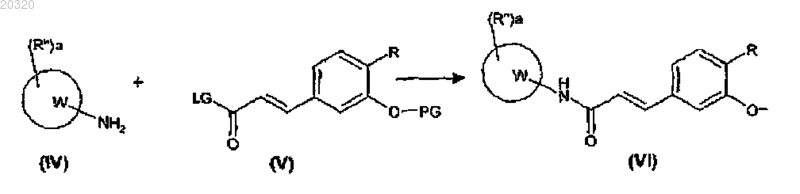
(d) удаляют защитную группу PG из соединения формулы (VI), как определено выше, для получения соединения формулы (I) и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (I).
9. Способ получения соединения общей формулы (I) по любому одному из пп.1-7, при котором
(а) активируют карбоксильную часть соединения формулы (III), как определено в п.8, для амидирования, чтобы получить соединение формулы (Va)
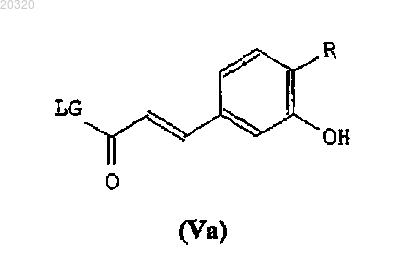
где R является таким, как определено в п.1, и LG является такой, как определено в п.8;
(b) ацилируют аминосоединение формулы (IV), как определено в п.8, с соединением формулы (Va), как определено выше, для получения соединения формулы (I), где R, R", W и а являются такими, как определено в п.1
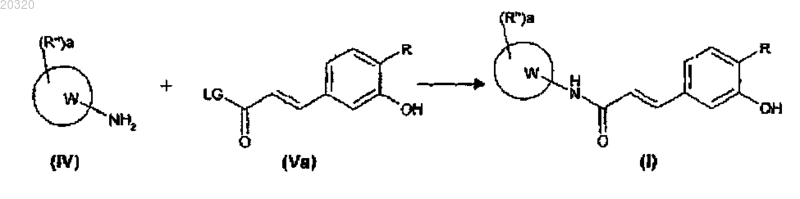
и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (I).
10. Способ получения соединения общей формулы (I) по любому одному из пп.1-7, при котором
(а) ацилируют аминосоединение формулы (VII), где W, R" являются такими, как определено в п.1, a равно 0, 1 или 2 и X является О, с соединением формулы (V), как определено в п.8, для получения соединения формулы (VIII), где R, R", W, a, X и PG являются такими, как определено выше
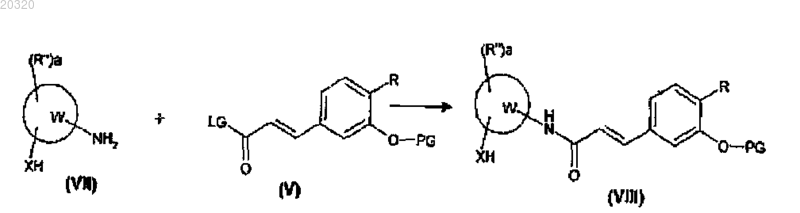
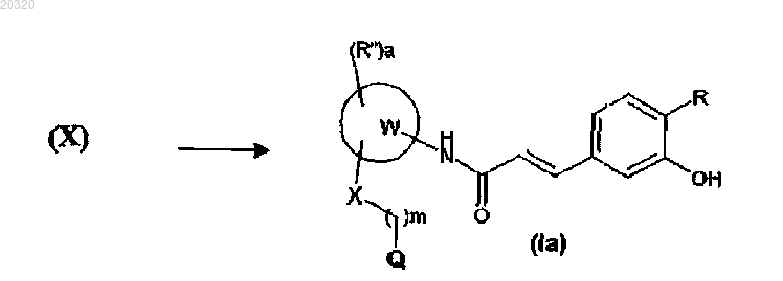
(b) алкилируют соединение формулы (VIII), как определено выше, с соединением формулы (IX), где Y является любой подходящей уходящей группой или гидроксигруппой, m и Q являются такими, как определено в п.1, для получения соединения формулы (X), где R, R", W, a, m, X, Q и PG являются такими, как определено выше
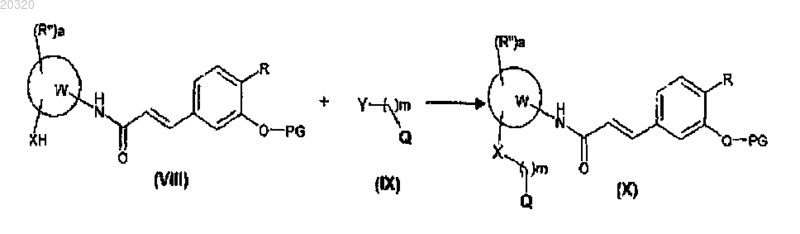
(с) удаляют защитную группу из соединения формулы (X), как определено выше, для получения соединения формулы (Ia), где R, R", W, a, m, X и Q являются такими, как определено выше, и, при необходимости, преобразуют соединение формулы (Ia) в другое соединение формулы (Ia), или преобразуют соединение формулы (Ia) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (Ia)
11. Применение соединения общей формулы (I) по любому одному из пп.1-7, а также его изомеров, рацемических форм, энантиомеров, диастереомеров, эпимеров, их смесей и фармацевтически приемлемых солей для получения лекарственного препарата для предупреждения и/или лечения болезней и состояний, связанных с активностью поры перехода митохондриальной проницаемости (МРТР).
12. Применение по п.11, где лекарственный препарат представляет собой препарат для предупреждения и/или лечения болезней, развивающихся вследствие повреждения ишемией/реперфузией или окислительного повреждения, болезней, связанных с возрастом, дегенеративных и нейродегенеративных болезней.
13. Применение по п.11, где лекарственный препарат представляет собой препарат для предупреждения и/или лечения острого инфаркта миокарда, сердечной недостаточности, ишемии органа, ишемического и травматического повреждения мозга, мышечной дистрофии Дюшенна, врожденной мышечной дистрофии Ульриха, миопатии Бентама, бокового амиотрофического склероза, болезни Хантингтона, болезни Альцгеймера, болезни Паркинсона, диабетов I типа и II типа, осложнений диабета, гипергликемического повреждения ткани, гипогликемического повреждения ткани, холестаза, повреждения, вызванного алкоголем.
14. Фармацевтическая композиция, содержащая одно или более соединений общей формулы (I) по любому одному из пп.1-7 и/или их фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый наполнитель.
Текст
АКРИЛАМИДОПРОИЗВОДНЫЕ, ПРИМЕНИМЫЕ КАК ИНГИБИТОРЫ ПЕРЕХОДА МИТОХОНДРИАЛЬНОЙ ПРОНИЦАЕМОСТИ В данном изобретении описаны акриламидопроизводные, применимые в качестве терапевтических средств,в особенности для предупреждения и/или лечения болезней и состояний, связанных с активностью поры перехода митохондриальной проницаемости (МРТР), таких как болезни, характеризующиеся ишемией/реперфузией, окислительным или дегенеративным повреждением ткани. Эти соединения относятся к структурной формуле (I), где R, R", W и а являются такими, как определено в описании. Данное изобретение также касается получения этих соединений, а также фармацевтических композиций,содержащих их. Область изобретения Данное изобретение относится к акриламидопроизводным и к их применению как терапевтических средств, в частности, для предупреждения и/или лечения болезней и состояний, связанных с активностью поры перехода митохондриальной проницаемости (МРТР), таких как болезни, характеризующиеся ишемией/реперфузией, окислительным или дегенеративным повреждением ткани. Данное изобретение также касается получения этих соединений, а также фармацевтических композиций, содержащих их. Предпосылки изобретения Переход митохондриальной проницаемости (МРТ) относится к переходу в состояние проницаемости внутренней митохондриальной мембраны для растворов с молекулярной массой ниже приблизительно 1500 Да. Полагали, что МРТ является опосредованным обратимым открытием потенциал- и Ca2+зависимого с высокой проводимостью белкового канала во внутренней митохондриальной мембране,МРТ поры (МРТР). Последствия открытия МРТР являются двойственными: во-первых, разобщение окислительного фосфорилирования и, как следствие, обращение F1F0-АТФазы для испытания и поддержания митохондриального мембранного потенциала (m), что приводит к снижению клеточных уровней АТФ и потере метаболического гомеостаза. Во-вторых, МРТР позволяет растворам свободно входить в матрикс митохондрии, что приводит к набуханию и возможному разрыву внешней митохондриальной мембраны с последующим высвобождением накопленного кальция и проапоптотических факторов. Высвобождение накопленного кальция может вызывать перегрузку кальцием, образование активных форм кислорода (ROS) и МРТ в соседней митохондрии, приводя к "цепной реакции" во всей клетке. В зависимости от энергетического состояния клетки позднее возникает апоптоз или некроз, приводя к необратимому повреждению ткани и органа (Grimm S., Brdiczka D. The permeability transition pore in celldeath Apoptosis, 2007, 12, 841-847). Точный молекулярный состав МРТР все еще не известен. Циклофилин D был представлен как фармакологически (применяя ингибитор, циклоспорин А), так и генетически в качестве основного регулятора МРТР. Провели много исследований, демонстрирующих роль МРТР при болезни, применяя циклофилин D-нулевых мышей (Ppif-/-) или циклоспорин А. МРТР можно регулировать с помощью нескольких факторов, включая высокую концентрацию [Ca2+], окислительное повреждение (ROS), химические поперечно-сшивающие средства, передача стрессового сигнала и PI3-киназный путь передачи сигнала, состояния, которые часто присутствуют в клетках из подверженных болезни тканей (Rasola, A., Bernardi,P., The mitochondrial permeability transition pore and its involvement in cell death and in disease pathogenesis.Apoptosis, 2007, 12, 815-833). Хорошо установлена роль опосредованного митохондрией апоптоза и некроза в этиологии многих болезней, и повышенная степень апоптоза/некроза, типичная для условий патологического стресса, таких как наблюдаемые во время инфаркта миокарда, почечной ишемии или нейродегенеративных расстройств, коррелирует с МРТ и потерей митохондриальной целостности. Следовательно, МРТР была вовлечена в этиологию и развитие нескольких болезней, включая острый инфаркт миокарда (летальное реперфузионное повреждение); приступ и неврологические болезни; наследственные дистрофии; гепатит; диабет и диабетическая ретинопатия. Острый инфаркт миокарда (летальное реперфузионное повреждение). При ишемической болезни сердца возникают последовательные события ишемии-реперфузии, приводящие к гибели клеток миокарда путем некроза и/или апоптоза. Летальное реперфузионное повреждение (гибель кардиомиоцитов как прямой результат реперфузии ткани), как полагают, составляет до 50% конечного размера инфаркта миокарда и, как показали, зависит от пути RISK (киназа сохранения при реперфузионном повреждении) и открытия МРТР (Yellon, D.M., Hausenloy, D.J., Myocardial ReperfusionInjury. N. Engl. J. Med., 2008, 357, 1121-1135). При ишемии присутствует истощение АТФ (аденозинтрифосфат), уменьшение клеточного pH и внутриклеточная загрузка Ca2+. При реперфузии повышенная концентрация внутриклеточного [Ca2+] приводит к перегрузке Ca2+ в митохондрии, что вместе с большим взрывом ROS и возвратом к физиологическому pH вызывает, парадоксально, открытие МРТ и гибель клеток кардиомиоцитов из-за некроза и/или апоптоза. Таким образом, ожидается, что ингибирование МРТР уменьшает гибель кардиомиоцитов и снижает размер инфаркта после повреждения ишемией/реперфузией. Действительно, Debio-025, аналог циклоспорина А, имеющий МРТ-ингибиторную активность, снижал размер инфаркта и улучшал функциональное восстановление и смертность в мышиной модели инфаркта миокарда и реперфузионного повреждения (Gomez, L., Thibault. H., Gharib, A., Dumont,J-M., Vuagniaux, G., Scalfaro, P., Derumeaux, G., Ovize, M. Inhibition of mitochondrial permeability transitionimproves functional recovery and reduces mortality following acute myocardial infarction in mice. Am. J. Physiol. Heart Circ. Physiol., 2007, 293, 1654-1661). Приступ и неврологические болезни. Церебральная ишемия с последующей реперфузией активирует несколько путей, включая путь, который вызывает высвобождение больших количеств возбуждающей аминокислоты глутамата в синапсы. Активация рецепторов N-метил-D-аспартата вызывает увеличение поглощения кальция и образованияROS, приводя к открытию МРТР и митохондриальной дисфункции. Следовательно, открытие МРТР вовлечено в гибель клеток нейронов и клинические симптомы, связанные с приступом. Кроме того,NIM811, аналог циклоспорина А, ингибитор МРТ, обеспечивающий 40% защиту в крысиной модели транзиторной фокальной церебральной ишемии, характеризуется снижением высвобождения цитохрома С и образования ROS (Korde, A.S., Pettigrew, L.C., Craddock, S.D., Pocernich, С.В., Waldmeier, P.C., Margolis., W.F. Protective effects of NIM81 1 in transient focal cerebral ischemia suggests involvement of the mitochondrial permability transition. J. Neurotrauma, 2007, 24 (5), 895-908). Острая вызванная инсулином гипогликемия вызывает повреждение нейронов определенных областей мозга, включая внешние слои коры головного мозга и зубчатую извилину. В крысиной модели вызванной инсулином гипогликемической комы циклоспорин А, иммунодепрессивное лекарственное средство с МРТР-ингибиторной активностью, но не FK506 (иммунодепрессивное средство, подобное CSA, но без МРТР-активности) показало сильное снижение ультраструктурного повреждения мозга при введении за 30 мин до гипогликемического инсульта (Friberg, H., Ferrand-Drake, M., Bengtsson, F., Halestrap, A.P.,Wieloch, Т. Cyclosporin A, но не FK 506, protects mitochondria and neurons against hypoglycaemic damageand implicates the mitochondrial permeability transition in cell death. J. Neurosci., 1998, 18, 5151, 5159). Митохондриальная дисфункция, нарушенная передача сигналов Са 2+ и окислительный стресс являются характеристиками бокового амиотрофического склероза, болезней Альцгеймера, Паркинсона и Хантингтона, и открытие МРТР было причинно связано со всеми четырьмя болезнями избирательным применением циклоспорина A (Norenberg, M.D., Rama Rao, K.V. The mitochondrial permeability transition in neurologic disease. Neurochem. Int., 2007, 50, 983-997). МРТР и митохондриальное набухание были также вовлечены в повреждение мозга, происходящее в результате гипергликемического инсульта, экспериментальной травмы и эпилепсии (Li, P.A., Uchino, H.,Elmer, E., Siesjo, B.K. Amelioration by cyclosporin A of brain damage following 5 or 10 min of ischemia in ratsThe mechanism of neuroprotection by topiramate in an animal model of epilepsy. Epilepsia, 2004, 45, 14781487). Наследственные дистрофии. Многие из патологических признаков, приводящих к открытию МРТР (перегрузка Са 2+ и накопление ROS), присутствуют при мышечных дистрофиях, и митохондрии, выделенные из скелетной мышцы у Scgd-/мышей (модель с тяжелой дистрофией), набухали последовательно с открытием МРТР. Scgd-/,Ppif-/мыши (без циклофилина D) не имели набухших митохондрий и не проявляли тяжелой мышечной дегенерации в возрасте 8 недель. Кроме того, лечение mdx- (модель мышечной дистрофии Дюшенна) иScgd-/мышей Debio-025 снижает митохондриальное набухание и некротическую болезнь (Millay, D.P.,Sargent, M.A., Osinska, H., Baines, С.Р., Barton, E.R., Vuagniaux, G., Sweeney, H.L. Robbins, J., Molkentin,J.D. genetic and pharmacologic inhibition of mitochondrial-dependent necrosis attenuates muscular dystrophy.Nature Medicine, 2008, 14, 442-447). Врожденная мышечная дистрофия Ульриха и миопатия Бетлема являются двумя наследственными дистрофиями, которые характеризуются мутациями в гене коллагена VI. Мышиные модели болезней выдвинули на первый план скрытую митохондриальную дисфункцию, которая характеризуется повышенной чувствительностью к открытию МРТР и дегенерации мышечных волокон. Миобласты у пациентов с врожденной мышечной дистрофией Ульриха показали митохондриальную дисфункцию и раннее открытие МРТР, приводящее к повышенному апоптозу. Пациенты с коллаген-VI миопатиями, которых лечили МРТР-ингибитором циклоспорином А на протяжении одного месяца, показали улучшение митохондриальной функции и имели признаки мышечной регенерации (Merlini, L., Angelin, A., Tiepolo, Т.,Braghetta, P., Sabatelli, P., Zamparelli, A., Ferlini, A., Maraldi, M, Bonaldo, P., Bernardi, P. Cyclosporin A corrects mitochondrial dysfunction and muscle apoptosis in patients with collagen VI myopathies. P.N.A.S., 2008,105 (13), 5225-5229). Гепатит. Печень может быть повреждена различными средствами, такими как химические яды, воспалительные факторы или вирусы. Во всех случаях гепатоциты подвергаются массовому апоптозу, к которому приводит МРТР. Кроме того, сообщили, что ингибирование открытия МРТР лечением циклоспорином А сильно снижает поражение печени в крысиной модели TNFзависимого острого воспалительного гепатита (Soriano, M.E., Nicolosi, L. Desensitization of the permeability transition pore by cyclosporine A preventsChem., 2004, 279, 36803-36808). Диабет. Диабет вызывает повреждение и отмирание клеток посредством нескольких механизмов. Диабетическая ретинопатия (DR) является одним из периферических микрососудистых осложнений, сильно увеличивающих процент смертности от диабетических сосудистых болезней. DR начинается на раннем пре-2 020320 пролиферативном этапе (фоновая ретинопатия), который характеризуется потерей капиллярных перицитов, развивающимся закрытием капилляров, микроаневризмами и отеком сетчатки. Последующая ретинальная ишемия (или гипоксия) из-за непроходимости сосудов вызывает патологический рост сосудов,рост сетчатки. Нео-сосуды простираются вдоль внутренней поверхности сетчатки и/или в полость стекловидного тела и могут привести к отслоению сетчатки и кровоизлиянию. Этот этап известен как пролиферативная диабетическая ретинопатия (PDR). Гипергликемический стресс рассматривают как ключевой фактор в PDR, поскольку он индуцирует повышенное образование фактора роста эндотелия сосудов(VEGF) клетками сетчатки, приводя к неоваскуляризации, и вызывает окислительное повреждение клеток, оказывающее влияние на митохондрии. ROS, которые образуются в более высоких количествах при диабете, могут инициировать большинство патологических внутриклеточных путей, включенных в PDR,и показано, что ROS образуются в сетчатке при реперфузии после ишемии, вызванной диабетом. К тому же окислительный стресс также сопоставляли с уровнем и развитием ретролентальной фиброплазии(ROP). Незрелая сетчатка содержит относительно низкие уровни антиоксидантов, таких как гемоксигеназа-1 и каталаза. Во время гипероксигенации образуются ROS и, помимо этого, она способствует образованию биологически активных изопростанов, содействующих ишемии и, следовательно, патогенезуROP. MPTP инициируется ROS, и ее открытие может привести к дополнительному образованию ROS, и поэтому митохондриальная дисфункция может быть основной для осложнений диабета. До настоящего времени ингибирование МРТР, главным образом, было ограничено фармакологической модуляцией компонента циклофилина D МРТР с использованием сильного иммунодепрессивного лекарственного средства циклоспорина А или его аналогов NIM811 и Debio-025 (которые лишены иммунодепрессивной активности). Это большие сложные молекулы на основе пептидной структуры циклоспорина А. К тому же ингибиторная эффективность этих молекул ограничена пределами регулирующей роли циклофилина D в функционировании МРТР и его уровнем экспрессии. Другие известные соединения, которые часто показывают ряд биологических активностей и фармакологических профилей, как сообщили, также имеют несколько дополнительных не специфических взаимодействий с МРТР. В качестве примера было показано, что средство N-[(3,5-ди-трет-бутил-4 гидрокси-1-тиофенил)]-3-пропил-N'-(2,3,4-триметоксибензил)пиперазин (S-15176) взаимодействует с несколькими мишенями на митохондриальных мембранах печени крыс и проявляет некоторые антиишемические свойства, когда дозируется in vitro при низкой концентрации. Наоборот, при более высоких дозах оно вызывает деполяризацию митохондриальной мембраны и разобщение дыхания, что типично связано с сильной цитотоксичностью (Morin D. et al. Effect of the mitochondrial transition pore inhibitor, S15176, on rat liver mitochondria: ATP synthase modulation and mitochondrial uncoupling induction. Biochemical Pharmacology, Pergamon, Oxford, GB, 72, 7, 911-91). Следовательно, существует потребность идентифицировать более сильные и эффективные малые молекулы ингибиторов МРТР, имеющие другую и более эффективную мишень в МРТР, которые применимы для предупреждения или лечения болезней и состояний, связанных с активностью МРТР. Акриламидосоединения данного изобретения являются небольшими молекулами, имеющими сильную МРТингибиторную активность, которые применимы при лечении ряда болезней, таких как те, что возникают в результате повреждения ишемией/реперфузией или окислительного повреждения, болезней, связанных с возрастом, дегенеративных и нейродегенеративных болезней. Определенные акриламидосоединения известны в данном уровне техники как терапевтические средства. В качестве примера, арильные и гетероарильные пропенамиды раскрыты как антипролиферативные, радиозащитные и цитозащитные средства в патентной заявке WO 04/037751. Лиганд акриламидосоединений ваниллоидного рецептора раскрыт в патентной заявке WO 03/049702 как анальгетик для лечения боли различного происхождения и этиологии. N-гетероциклиламидные соединения, серотонинергические антагонисты, раскрыты в патентной заявке WO 01/068585 для лечения или предупреждения нарушений центральной нервной системы. К тому же определенные анилиды кофейной кислоты также известны в данном уровне техники как средства против агрегации тромобоцитов и антиокислительные средства, как сообщили в BioorganicMedicinal Chemistry 2005, 13(5), 1791-7. Краткое описание данного изобретения Данное изобретение направлено на соединения, которые обладают МРТ-ингибирующей активностью и применяются в терапии как средства от МРТР-связанных заболеваний у пациента. Обнаружили, что акриламидосоединения общей формулы (I) и их производные обладают МРТингибирующей активностью. Данное изобретение обеспечивает соединение формулы (I) где W является арилом или гетероарилом;SO2NH2 или необязательно замещенного (С 1-С 6)алкила, арила или гетероарила;R" является независимо выбранными из галогена; (С 1-С 3)алкила; (С 1-С 3)алкокси; (С 1 С 3)алкоксиалкила; (С 1-С 2)галоалкокси; (С 1-С 2)галоалкила; NR3R4 или (CH2)n-X-(CH2)m-Q, гдеQ является арилом, гетероарилом, гетероциклоалкилом или (С 3-С 7)циклоалкилом; где гетероциклоалкил представляет собой 6-членное гетероциклоалкильное кольцо, содержащее 1-3 гетероатома, независимо выбранных из азота или кислорода; и любой из указанных выше алкила, арила, гетероарила, гетероциклоалкила или (С 3-С 7)циклоалкила может быть необязательно замещен 1-2 группами, выбранными из галогена, (С 1-С 6)алкила, (С 1 С 6)полифторированного алкила, (С 3-С 7)циклоалкила, 6-12-членного арила, 5-9-членного гетероарила,(С 1-С 6)алкил-(5-9-членного)гетероарила, (5-9-членного)гетероарил-(С 1-С 6)алкила, амино-(С 1-С 6)алкила,аминогрупп (С 1-С 6)алкиламино, (С 1-С 6)диалкиламино, ариламино; гидроксигруппы и е производных(С 1-С 3)алкокси, (С 1-С 6)полифторированный алкокси, арилокси, 5-9-членный гетероарилокси, (С 3 С 7)циклоалкилокси, 5-9-членный гетероциклоалкилокси, арил-(С 1-C3)алкокси, 5-9-членный гетероарил(С 1-C3)алкокси; (С 1-С 6)алкилкарбонил, арилкарбонил; любой из указанных выше заместителей Q может быть необязательно замещен (С 1-С 6)алкильной группой;R1, R2, R3 и R4 являются одинаковыми или разными и независимо друг от друга являются атомом водорода; (C1-C3)алкилом или, когда взяты вместе с атомом азота, к которому они присоединены, R1-NR2 и R3-N-R4 могут образовывать гетероциклическое кольцо формулы где R5 является атомом водорода или (С 1-С 3)алкильной группой; при условии, что (E)-3-(3-гидроксифенил)-N-[4-4-(E)-3-(3-гидроксифенил)проп-2-эноил]амино] фенил]метил]фенил]акриламид исключен, и когда W является фенилом, а не равно 0; когда W является фенилом и R является водородом, R" не является хлором, метилом, изопропилом,CF3 или NH2; когда W является индазол-5-илом или пирид-2-илом, R не является водородом, (С 1-С 3)алкокси; где арил представляет собой фенил, нафтил или инданил; где гетероарил представляет собой моноциклическое или бициклическое 5-9-членное ароматическое кольцо, содержащее атомы углерода и 1-4 гетероатома, независимо выбранных из азота, кислорода и серы, и гидроксильная группа может быть в форме ее фосфатного сложного эфира или его соли, а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры и их смеси, и их фармацевтически приемлемые соли. Данное изобретение также относится к способам синтеза акриламидосоединений общей формулы(I) и фармацевтически приемлемых солей. Данное изобретение обеспечивает способ получения соединения общей формулы (I), при котором(а) приводят в реакцию гидроксикоричную кислоту формулы (II), где R является таким, как определено выше, с защитным средством гидроксила для получения соответствующего защищенного соединения формулы (III) где PG является указанной защитной группой;(b) активируют карбоксильную часть соединения формулы (III), как определено выше, для амидирования, чтобы получить соединение формулы (V) где R и PG являются такими, как определено выше и LG является любой подходящей активационной группой карбоксильной части;(с) ацилируют аминосоединение формулы (IV), где W, R" и а являются такими, как определено выше, с соединением формулы (V), как определено выше, для получения соединения формулы (VI), где R,R", W, а и PG являются такими, как определено выше(d) удаляют защитную группу PG из соединения формулы (VI), как определено выше, для получения соединения формулы (I) и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль,или преобразуют его соль в свободное соединение формулы (I). В другом варианте осуществления данное изобретение обеспечивает способ получения соединения общей формулы (I), при котором(а) активируют карбоксильную часть соединения формулы (III), как определено выше, для амидирования, чтобы получить соединение формулы (Va)(b) ацилируют аминосоединение формулы (IV), как определено выше, с соединением формулы(Va), как определено выше, для получения соединения формулы (I), где R, R", W и а являются такими,как определено выше и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (I). В другом варианте осуществления данное изобретение обеспечивает способ получения соединения(а) ацилируют аминосоединение формулы (VII), где W, R" являются такими, как определено выше,а равно 0, 1 или 2, X является О, с соединением формулы (V), как определено выше, для получения соединения формулы (VIII), где R, R", W, а, X и PG являются такими, как определено выше(b) алкилируют соединение формулы (VIII), как определено выше, с соединением формулы (IX),где Y является любой подходящей уходящей группой или гидроксигруппой, m и Q являются такими, как определено выше, для получения соединения формулы (X), где R, R", W, a, m, X, Q и PG являются такими, как определено выше(с) удаляют защитную группу из соединения формулы (X), как определено выше, для получения соединения формулы (Ia), где R, R", W, a, m, X и Q являются такими, как определено выше, и, при необходимости, преобразуют соединение формулы (Ia) в другое соединение формулы (Ia), или преобразуют соединение формулы (Ia) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (Ia) В другом варианте осуществления данное изобретение обеспечивает соединения общей формулы(I), как определено выше, а также их изомеры, рацемические формы, таутомеры, энантиомеры, диастереомеры, эпимеры, полиморфы, их смеси, пролекарства и их фармацевтически приемлемые соли для применения в терапии. Данное изобретение также относится к применению соединений общей формулы (I), как определено выше, а также их изомеров, рацемических форм, таутомеров, энантиомеров, диастереомеров, эпимеров, полиморфов, их смесей, пролекарств и их фармацевтически приемлемых солей для получения лекарственного препарата для предупреждения и/или лечения болезней и состояний, связанных с активностью МРТР. Данное изобретение также относится к фармацевтическим композициям, содержащим одно или более соединений общей формулы (I), как определено выше, и/или пролекарства, и/или их фармацевтически приемлемую соль, и, по меньшей мере, один фармацевтически приемлемый наполнитель. Подробное описание изобретения Все выражения, как используется в данной заявке, если не указано иное, следует понимать в их обычном значении, как известно в данном уровне техники. Другие более конкретные определения для определенных выражений, как использовано в данной заявке, изложены ниже и предназначены для применения единообразно во всем описании и формуле изобретения, если специально указанное иное определение не обеспечивает более широкое определение. Выражение "арил" относится к любой ароматической карбоциклической кольцевой системе из 1 или 2 кольцевых частей, или слитых, или связанных друг с другом через одинарную связь. Подходящие арильные группы включают, но без ограничения, фенил, - или -нафтил, бифенил, инданил, инденил и подобное. Выражение "гетероарил" относится к моноциклическим или полициклическим ароматическим кольцам, содержащим атомы углерода и один или более гетероатом, предпочтительно 1-3 гетероатома,-6 020320 независимо выбранных из азота, кислорода и серы. Как хорошо известно специалистам в данной области техники, гетероарильные кольца обладают меньшими ароматическими свойствами, чем их аналоги, состоящие полностью из углерода. Таким образом, для целей данного изобретения гетероарильная группа должна иметь ароматические свойства только в некоторой степени. Иллюстративные примеры гетероарильных групп включают, но без ограничения, фурил, бензофуранил, бензодиоксолил, тиенил, пиридил,пиридил-N-оксид, пиримидил, пиримидинил, пиридазинил, пиразил, пиразинил, пиразолил, оксазолил,тиазолил, изоксазолил, хинолил, (1,2,3,)- и (1,2,4)-триазолил, тетразолил, триазинил, пиридазинил, пирролил, имидазолил, имидазо[1,2-а]пиридин-3-ил, индазолил, изотиазолил, индолил, бензоимидазолил,бензотриазолил, бензоксазолил, оксадиазолил и подобное. Выражение "гетероциклоалкил" относится к неароматическому моноциклическому или полициклическому кольцу, содержащему атомы углерода и водорода и по меньшей мере один гетероатом, предпочтительно 1-4 гетероатома, выбранных из азота, кислорода и серы. Гетероциклоалкильная группа может иметь одну или более двойных связей углерод-углерод или двойных связей углерод-гетероатомы в кольце при условии, что их присутствие не превращает кольцо в ароматическое. Примеры гетероциклоалкильных групп включают, но без ограничения, азиридинил, морфолинил, тиоморфолинил, пиперидинил,пиперазинил, тиазолидинил, оксазолидинил, тетрагидротиенил, дигидрофуранил, тетрагидрофуранил,тетрагидротиофуранил, тетрагидропиранил, пиразолидинил, 1,3-диоксоланил, пирролидинил, пиранил,дигидропиранил, изоксазолидинил, имидазолидинил и подобное. Гетероциклоалкильная группа может быть незамещенной или замещенной одним или двумя заместителями. Выражение "циклоалкил" относится к любой неароматической карбоциклической кольцевой системе 1 или 2 кольцевых частей. Циклоалкильная группа может иметь одну или более двойные связи углерод-углерод в кольце, при условии, что их присутствие не превращает кольцо в ароматическое. Примеры циклоалкильных групп включают, но без ограничения, (С 3-С 7)циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил, и насыщенные циклические и бициклические терпены, и (С 3-С 7)циклоалкенильные группы, такие как циклопропенил, циклобутенил, циклопентенил, циклогексенил и циклогептенил, и ненасыщенные циклические и бициклические терпены. Выражения "(С 1-С 3)алкил" или "(С 1-С 3)алкокси" относятся к любой группе, такой как метил, этил,n-пропил, изопропил, метокси, этокси, n-пропокси и изопропокси. Выражение "(С 1-С 2)галоалкокси" относится к (С 1-С 2)алкоксигруппе, замещенной на углеродных атомах одним или более атомом галогена. Такие группы включают, но без ограничения, трифторметокси,дифторметокси, 2,2-дифторэтокси, 2,2,2-трифторэтокси, 2-хлорэтокси, 1-фтор-2,2-дихлорэтокси и подобное. Выражение "(С 1-С 2)галоалкил" относится к С 1-С 2 галоалкильной группе, в частности CF3. Выражение "галоген" относится к атому фтора, хлора, брома или йода. Выражения "алкил", "(С 1-С 6)алкил" или "алкокси" относятся, если не обеспечено другое, к любой прямой или разветвленной C1-C6 алкильной или алкоксигруппе, следовательно, охватывает вышеупомянутые "(С 1-С 3)алкильные" или "(С 1-С 3)алкокси" группы и также включает n-бутил, изо-бутил, sec-бутил,трет-бутил, п-пентил, n-гексил, n-бутокси, изо-бутокси, sec-бутокси, трет-бутокси, п-пентилокси, nгексилокси и подобное. Любая из вышеописанных (С 1-С 6)алкильных, арильных, гетероарильных, гетероциклоалкильных или циклоалкильных групп может быть факультативно дополнительно замещена в любом из их свободных положений одной или более группой, например 1-6 группами, выбранными из галогена, карбокси,циано, алкила, полифторированного алкила, алкенила, алкинила, циклоалкила, арила, гетероарила, алкил-гетероарила, гетероарил-алкила, аминоалкила, аминогрупп и их производных, таких как, например,алкиламино, диалкиламино, ариламино, диариламино, уреидо, алкилуреидо или арилуреидо; карбониламиногрупп, и их производных, таких как, например, формиламино, алкилкарбониламино, алкенилкарбониламино, арилкарбониламино, алкоксикарбониламино; гидроксигрупп и их производных, таких как,например, алкокси, полифторированный алкокси, арилокси, гетероарилокси, алкилкарбонилокси, арилкарбонилокси или циклоалкилокси, гетероциклоалкилокси, арилалкокси, гетероарилалкокси; карбонильных групп и их производных, таких как, например, алкилкарбонил, арилкарбонил, алкоксикарбонил,арилоксикарбонил, циклоалкилоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил; серосодержащих производных, таких как, например, алкилтио, арилтио, алкилсульфонил, арилсульфонил, алкилсульфинил, арилсульфинил, арилсульфонилокси, аминосульфонил, алкиламиносульфонил или диалкиламиносульфонил. В свою очередь, во всех подходящих случаях каждый из вышеописанных заместителей может дополнительно замещаться одной или более из вышеупомянутых групп. Выражения "алкенил" или "алкинил" относятся, если не указано иное, к любой ненасыщенной прямой или разветвленной С 2-С 6 алкенильной или алкинильной группе, такой как, например, винил, аллил,1-пропенил, изопропенил, 1-, 2- или 3-бутенил, пентенил, гексенил, этинил, 1- или 2-пропинил, бутинил,пентинил, гексинил и подобное. Выражения "полифторированный алкил" или "полифторированный алкокси" относится к любой прямой или разветвленной С 1-С 6 алкильной или алкоксигруппе, как определено выше, где более чем один атом водорода замещен атомами фтора, такой как, например, трифторметил, трифторметокси, 2,2,2 трифторэтил, 2,2,2-трифторэтокси, 1,2-дифторэтил, 1,1,1,3,3,3-гексафторпропил-2-ил и подобное. Из всего вышеописанного специалистам данной области понятно, что любая группа, название которой определили как составное название, такое как, например, циклоалкилалкил, арилалкил, гетероарилалкил, алкилгетероарил, (С 1-С 3)алкоксиалкил, алкилтио, арилтио, аминоалкил, алкиламино, диалкиламино, ариламино, диариламино, алкилуреидо, арилуреидо, алкилкарбониламино, алкенилкарбониламино, арилкарбониламино, арилокси, арилалкилокси, алкилкарбонилокси, алкоксикарбониламино; гетероарилокси, арилкарбонилокси, алкилиденаминокси; алкилкарбонил, арилкарбонил, алкоксикарбонил, арилоксикарбонил, циклоалкилоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилсульфонил, арилсульфонил, алкилсульфинил, арилсульфинил, арилсульфонилокси, аминосульфонил, алкиламиносульфонил или диалкиламиносульфонил и подобное, предполагается как условно составленная из частей, от которых они происходят. До настоящего времени в качестве примера выражение "циклоалкилалкил" означает прямую или разветвленную алкильную группу, замещенную циклоалкильной группой, где алкил и циклоалкил являются такими, как определено выше. Аналогично, выражение "алкоксикарбонил" означает радикал, содержащий алкоксирадикал, как определено выше, присоединенный через атом кислорода к карбонильному радикалу. Выражение "приблизительно" охватывает диапазон экспериментальной ошибки, которая может типично встречаться при измерении. Выражение "уходящая группа", как используется в данном документе, имеет то же значение для специалиста данной области (Advanced Organic Chemistry: reactions, mechanisms and structure - Third Edition by Jerry March, John Wiley and Sons Ed.; 1985, page 179) и представляет группу, которая является частью и присоединена к субстратной молекуле; в реакции, где субстратная молекула подвергается реакции замещения (например, нуклеофилом), уходящая группа затем замещается. Предпочтительными уходящими группами являются галоген, сульфоновые сложные эфиры, такие как р-толуолсульфонат, pбромбензолсульфонат, p-нитробензолсульфонат, метансульфонат, трифторметансульфонат,Выражение "фармацевтически приемлемые соли" относится к относительно нетоксичным минеральным и органическим кислотно-аддитивным солям и основно-аддитивным солям соединений данного изобретения. Эти соли можно получить in situ во время конечного выделения и очистки соединений. В частности, кислотно-аддитивные соли можно получить отдельной реакцией очищенного соединения в его очищенной форме с органической или минеральной кислотой и выделением образованной таким образом соли. Полученными солями являются, например, гидрохлориды, гидробромиды, сульфаты, гидросульфаты, дигидрофосфаты, цитраты, малеаты, фумараты, трифторацетаты, 2 нафталинсульфонаты, паратолуолсульфонаты. Данное изобретение также касается фармацевтически приемлемых солей с органическими или неорганическими основаниями. В частности, основно-аддитивные соли можно получить отдельной реакцией очищенного соединения в его очищенной форме с органическим или неорганическим основанием и выделением образованной таким образом соли. Полученными солями являются, например, соли металла,в частности, соли щелочного металла, соли щелочно-земельного металла и соли переходного металла(такого как натрий, калий, кальций, магний, алюминий), или соли, полученные с основаниями, такими как аммиак или вторичные или третичные амины (такие как диэтиламин, триэтиламин, пиперидин, пиперазин, морфолин), или с основными аминокислотами, или с озаминами (такими как меглумин), или с аминоспиртами (такими как 3-аминобутанол и 2-аминоэтанол). Данное изобретение также относится ко всем изомерам и их примесям, таутомерным формам, рацемическим формам, энантиомерам, диастереоизомерам, эпимерам, а также их кристаллическим формам, включая их полиморфные формы, и их смесям. В случаях, когда соединения могут существовать в таутомерных формах, каждая форма рассматривается как включенная в данное изобретение либо существующая в равновесии, либо преимущественно в одной форме. Данное изобретение направлено не только на рацемические смеси этих соединений, но также на отдельные их стереоизомеры и/или диастереоизомеры, также как и на их смеси во всех соотношениях. Аналогично, метаболиты и фармацевтически приемлемые биопредшественники (иначе названные как пролекарства) соединений формулы (I) включены в объем и подходят для применения в данном изобретении. Так называемые "пролекарства" соединений формулы (I) также находятся в объеме данного изобретения. "Пролекарство" является соединением, которое является метаболически преобразуемым в терапевтически активное соединение после введения. Выражение "пролекарство" должно истолковываться в данном документе так широко, как обычно понимается в данном уровне техники. Без намерений ограничить объем данного изобретения, преобразование может происходить посредством гидролиза биологически лабильных групп in vivo. Например, соединение, содержащее гидроксигруппу, можно вводить в виде сложного эфира, который преобразуется гидролизом in vivo в гидроксисоединение. Таким образом, определенные производные соединений формулы (I), которые сами могут иметь небольшую или не иметь фармакологической активности, при введении в организм могут преобразовываться в соединения фор-8 020320 мулы (I), имеющие желаемую активность, например, посредством гидролитического расщепления. Пролекарства в соответствии с данным изобретением могут, например, быть получены замещением соответствующих функциональных групп, присутствующих в соединениях формулы (I) определенными частями, известными специалистам данной области техники как прокомпоненты, как описано, например,в Design of Prodrags by H. Bundgaard (Elsevier, 1985) или в Prodrugs: design and clinical applications byJarkko Rautio et al. (Nature reviews drug discovery, volume 7, March 2008, 255-270). Неограничивающие примеры пролекарств включают:i) сложный эфир карбоновой кислоты фенольной части соединений формулы (I);ii) сложный эфир фосфата фенольной части соединений формулы (I);iii) фосфонооксиметиловый эфир фенольной части соединений формулы (I);iv) карбаматное производное фенольной части соединений формулы (I). Предпочтительными пролекарствами являются сложный эфир карбоновой кислоты или фосфата фенольной части соединений формулы (I). Не предназначаясь для ограничения, сложным эфиром может быть алкильный сложный эфир, арильный сложный эфир, гетероарильный сложный эфир или неорганический сложный эфир. Акриламидопроизводные по данному изобретению имеют следующую формулу (I): где R, R", а и W являются такими, как определено выше. В предпочтительном варианте осуществления данное изобретение обеспечивает акриламидопроизводные формулы (I), гдеR" является независимо выбранным из галогена; (С 1-С 3)алкоксиалкила; (С 1-С 2)галоалкила илиQ является арилом или гетероарилом. Даже более предпочтительноR" является галогеном или (CH2)n-X-(CH2)m-Q, гдеn и m выбраны таким образом, что их сумма (n+m) равна 1;Q является арилом или гетероарилом; а также его изомеры, таутомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, полиморфы, их смеси, пролекарства и их фармацевтически приемлемые соли. В другом предпочтительном варианте осуществления данное изобретение обеспечивает акриламидопроизводные формулы (I), гдеW является бициклическим арильным или бициклическим гетероарильным кольцом, факультативно замещенным 1 или 2 группами R";R" является независимо выбранным из галогена; (С 1-С 2)галоалкила; 4-(С 1-C3)алкилпиперазин-1-ила или (СН 2)n-X-(CH2)m-Q, гдеQ является арилом или гетероарилом. Даже более предпочтительноW является бициклическим арильным или бициклическим гетероарильным кольцом, незамещенным или замещенным одной группой (CH2)n-X-(CH2)m-Q, гдеn и m выбраны таким образом, что их сумма (n+m) равна 1;Q является арилом или гетероарилом; и необязательно замещен второй группой R", выбранной из хлора; брома; (С 1-С 2)галоалкила; 4-(С 1C3)алкилпиперазин-1-ила; а также его изомеры, рацемические формы, энантиомеры, диастереомеры, эпимеры, их смеси и их фармацевтически приемлемые соли. Для ссылки на любые специфические соединения формулы (I) данного изобретения, факультативно, в форме фармацевтически приемлемой соли, см. следующий экспериментальный раздел. Специфические, неограничивающие примеры соединений формулы (I) показаны в следующем списке:(E)-N-(3-хлорфенил)-3-(4-амино-3-гидроксифенил)акриламид; а также изомеры, таутомеры, рацемические формы, энантиомеры, диастереомеры, полиморфы, смеси, пролекарства и их фармацевтически приемлемые соли. Данное изобретение также относится к способам получения соединений общей формулы (I), как определено выше, следующими способами (способ A и способ B), которые можно осуществить согласно способам, хорошо известным специалисту в данной области техники. Следующие способы представлены для иллюстративных целей. В зависимости от природы соединений формулы (I), которые будут получать, представленная методика может быть адаптирована специалистом в данной области техники путем выбора подходящих исходных материалов, в которых природа заместителей R, R', R" и W может быть модифицирована. Дополнительная цель данного изобретения представлена способом получения соединений формулы(I), пролекарств и их фармацевтически приемлемых солей (способ А), при котором(а) приводят в реакцию гидроксикоричную кислоту формулы (II), где R и R' являются такими, как определено выше в формуле (I), с защитным средством гидроксила для получения соответствующего защищенного соединения формулы (III) где PG является указанной защитной группой;(b) активируют карбоксильную часть соединения формулы (III) для амидирования, чтобы получить соединения формулы (V) где R и PG являются такими, как определено выше, и LG является любой подходящей активационной группой карбоксильной части,(с) ацилируют аминосоединение формулы (IV), где W, R" и а являются такими, как определено выше в формуле (I), с соединением формулы (V) для получения соединения формулы (VI), где R, R', R", W,а и PG являются такими, как определено выше(d) удаляют защитную группу PG из соединения формулы (VI) для получения соединения формулы(I) и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (I). Согласно этапу (а) способа защиты фенольного гидроксила соединения формулы (II) можно выполнить различными способами, хорошо известными специалисту в данной области техники (Theodora W.Greene, Peter G.M. Wuts, Protective Groups in Organic Synthesis, Wiley-Interscience). В качестве примера соединение формулы (II) можно обработать ацилхлоридом или ангидридом карбоновой кислоты в присутствии основания для получения соответствующего фенольного сложного эфира. Реакцию проводят в подходящем растворителе, таком как полярные апротонные растворители, например дихлорметан, тетрагидрофуран, 1,4-диоксан, N,N'-диметилформамид, в присутствии основания, такого как гидрид натрия или калия или трет-бутилат калия, при температуре в диапазоне от комнатной температуры до температуры дефлегмации растворителя в течение времени от приблизительно 30 мин до 18 ч. Предпочтительно этап (а) осуществляют путем реакции соединения формулы (II) с уксусным ангидридом в присутствии металлического гидрида, такого как гидрид натрия или калия, в тетрагидрофуране или 1,4-диоксане при температуре в диапазоне от комнатной температуры до температуры дефлегмации. Согласно этапу (b) способа полученное таким образом фенолзащищенное производное карбоновой кислоты формулы (III) приводят во взаимодействие с анилином формулы (IV) с помощью действий соглас- 13020320 но способам, хорошо известным специалисту в данной области техники, для получения карбоксамидопроизводных. Например, карбоновая кислота (III) промежуточно преобразуется в подходящее ацилирующее средство (V), такое как ацилхлорид, которое затем применяют в реакции амидирования. Типично, в соединениях формулы (V), R" представляет атом галогена и даже более предпочтительно атом хлора. Реакцию соединения проводят в подходящем растворителе, таком как полярные апротонные растворители, например тетрагидрофуран, 1,4-диоксан, диметилформамид, дихлорметан или их смеси, при температуре в диапазоне от приблизительно 0C до дефлегмации и за время от приблизительно 30 мин до 96 ч, если нужно, в присутствии подходящего поглотителя протонов, такого как триэтиламин, N,Nдиизопропилэтиламин или пиридин. Согласно этапу (d) способа фенольную защитную группу соединения формулы (VI) избирательно удаляют для получения соответствующего фенола формулы (I). В зависимости от природы защитной группы ее удаление можно проводить при различных условиях, таких как, например, кислотный или щелочной гидролиз, гидрогенолиз или обработка фторидными солями. Предпочтительно в соединениях формулы (VI) PG представляет фенольный сложный эфир, который подходящим образом гидролизуется либо при кислотных, либо при основных условиях. Типично, кислотный гидролиз можно провести обработкой соляной, метансульфоновой, трифторуксусной кислотой и подобным в подходящем растворителе, таком как полярные апротонные растворители, например дихлорметан, или полярные протонные растворители, например метанол или этанол, при температуре в диапазоне от приблизительно 0C до комнатной температуры за время от приблизительно 15 мин до 24 ч. Альтернативно, с соединения формулы (VI) снимают защиту при основных условиях, и действуя согласно традиционным методикам, например, обработкой водным гидроксидом натрия или калия в присутствии подходящего сорастворителя, такого как полярные протонные растворители, например метанол, этанол, или полярные апротонные растворители, например диметилформамид, 1,4-диоксан, или обработкой третичным амином, таким как триэтиламин или N,N-диизопропилэтиламин, и применяя спирт,такой как метанол или этанол, в качестве растворителя. Снятие защиты может проходить при температуре в диапазоне от приблизительно 0C до температуры дефлегмации растворителя за время от приблизительно 30 мин до 72 ч. Как указано выше, специалисту данной области понятно, что в зависимости от химической реакционной способности производных формул (II) и (IV) вышеуказанных этапов защиты/снятия защиты, этап(а) и этап (d), фенольной части в некоторых случаях можно удобно избежать, таким образом позволяя прямое соединение карбоновой кислоты (II) с анилином (IV) при условиях, описанных выше для этапа(b), для непосредственного образования соответствующего производного формулы (I). Так, согласно дополнительному варианту осуществления данного изобретения способ получения соединений формулы (I), пролекарств и их фармацевтически приемлемых солей содержит этапы, на которых(а) активируют карбоксильную часть соединения формулы (II), как определено выше, для амидирования, чтобы получить соединения формулы (Va)(b) ацилируют аминосоединения формулы (IV), как определено выше, с соединением формулы (Va) для получения соединения формулы (I), как определено выше, и, при необходимости, преобразуют соединение формулы (I) в другое соединение формулы (I), или преобразуют соединение формулы (I) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (I). Согласно дополнительному варианту осуществления данного изобретения обеспечивают альтернативный способ получения соединения формулы (I), пролекарств и их фармацевтически приемлемых солей (способ В), содержащий этапы, на которых(а) ацилируют аминосоединения формулы (VII), где W, R" являются такими, как определено выше в формуле (I), a равно 0, 1 или 2, и X является О или S, с соединением формулы (V), как определено выше,для получения соединения формулы (VIII), где R, R', R", W, a, X и PG являются такими, как определено выше(b) алкилируют соединение формулы (VIII) с соединением формулы (IX), где Y является любой подходящей уходящей группой или гидроксигруппой, m и Q являются такими, как определено выше в формуле (I), для получения соединения формулы (X), где R, R", W, a, m, X, Q и PG являются такими, как определено выше(с) удаляют защитную группу из соединения формулы (X) для получения соединения формулы (Ia),где R, R", W, a, m, X и Q являются такими, как определено выше, и, при необходимости, преобразуют соединение формулы (Ia) в другое соединение формулы (Ia), или преобразуют соединение формулы (Ia) в фармацевтически приемлемую соль, или преобразуют его соль в свободное соединение формулы (Ia) Согласно этапу (а) способа соединение карбоновой кислоты формулы (V) с анилином формулы(VII) можно осуществить, как описано выше для способа А, этап (с). Согласно этапу (b) способа алкилирование фенольной или тиофенольной части соединения формулы (VIII) можно осуществить, например,с помощью реакции с подходящим производным галогенида (IX) в присутствии основания, или, альтернативно, реакцией с подходящим гидроксипроизводным (IX) при условиях Мицунобу, как описано в(2004); Vol. 79, p. 186 (2002). Типично, соединения формулы (VIII) обрабатывают подходящим галогенидным производным (IX) в присутствии основания, такого как, например, гидриды лития, натрия или калия, гидроксиды или карбонаты, в подходящем растворителе, таком как полярные апротонные растворители, например N,N'-диметилформамид, тетрагидрофуран или 1,4-диоксан, при температуре в диапазоне от приблизительно 0C до температуры дефлегмации растворителя за время от приблизительно 30 мин до 48 ч. Альтернативно, этап (b) можно завершить соединением фенольного или тиофенольного соединения формулы (VIII) с подходящим активированным спиртом (IX) при стандартных условиях реакции Мицунобу, например с помощью реакции с трифенилфосфином и диэтилазодикарбоксилатом при температуре в диапазоне от приблизительно 0 до 80C в подходящем растворителе, таком как полярные апротонные или неполярные растворители, например тетрагидрофуран или толуол, за время от приблизительно 30 мин до 48 ч. Согласно этапу (с) способа фенольную защитную группу соединения формулы (X) можно избирательно удалить для получения соответствующего фенола формулы (Ia), как описано выше для способа А,этапа (d). При необходимости образование соли соединения формулы (I) или преобразование его соответствующей соли в свободное соединение (I) согласно этапу (d) способа можно легко осуществлять согласно хорошо известным способам специалисту в данной области техники. Специалисту в данном уровне техники понятно, что если соединение формулы (I), полученное согласно вышеописанным способам (способ А или способ В), получено в виде смеси изомеров, их разделе- 15020320 ние на отдельные изомеры формулы (I), осуществляемое помощью традиционных методик, остается в пределах объема данного изобретения. Как будет оценено специалистом в данном уровне техники, когда во время синтеза соединений формулы (I) определенные функциональные группы могут вызывать нежелательные побочные реакции,эти группы должны быть надлежащим образом защищены согласно общепринятым методикам. Аналогично, преобразование этих соединений в соответствующие незащищенные соединения можно проводить согласно процедурам, хорошо известным специалисту в данном уровне техники. Все из соединений формулы (II), (III), (IV), (VII), (IX) известны, или коммерчески доступны, или могут быть получены из известных соединений согласно стандартным процедурам. В качестве примера исходные материалы формулы (IV), где W является фенилом, можно легко получить, как изложено в схеме 1 (A-D) ниже, начиная с подходящих коммерчески доступных структурных элементов. Схема 1 Пример синтеза исходных материалов формулы (IV), где W является фенилом При необходимости промежуточные производные в схеме 1 могут дополнительно обрабатываться,применяя стандартные процедуры синтеза. Как дополнительный пример, когда (гетеро)арилом-OH в схеме 1 является резорцин, соответствующие промежуточные соединения можно дополнительно обработать спиртом Rx-OH, где Rx является алкильной, циклоалкильной, гетероциклоалкильной, арилалкильной или гетероарилалкильной группой при стандартных условиях Мицунобу, для получения исходных материалов формулы (IV), приведенных в схеме 2. Схема 2 Пример синтеза исходных материалов формулы (IV), где W является фенилом,замещенным производным резорцина В качестве дополнительного примера исходные материалы формулы (II) можно легко получить, как изложено в схеме 3 ниже, путем соединения коммерчески доступных или известных бензальдегидов с малоновой кислотой при основных условиях. Схема 3 Пример синтеза исходных материалов формулы (II) В качестве дополнительного примера фосфатные сложные эфиры пролекарств соединений формулы (I) можно получить, следуя известной процедуре синтеза (J. MedChem. 2000, 43, 2731-2737), представленной в схеме 4. Схема 4 Пример синтеза фосфатного сложного эфира соединений формулы (I) Соединения формулы (I), как определено выше, применяются в терапии как средства против МРТРсвязанных болезней у пациента. Более конкретно, соединения согласно данному изобретению применимы для получения лекарственного препарата для лечения разнообразных болезней, таких как те, которые возникают в результате ишемии и реперфузионного повреждения или окислительного повреждения, болезней, связанных с возрастом, дегенеративных и нейродегенеративных болезней, включая, но без ограничения: болезнь сердца(острый инфаркт миокарда, сердечная недостаточность), трансплантационную хирургию (ишемия органа), ишемическое (приступ) и травматическое повреждение мозга, мышечную дистрофию Дюшенна,врожденную мышечную дистрофию Ульриха, миопатию Бентама, боковой амиотрофический склероз,болезнь Хантингтона, болезнь Альцгеймера, болезнь Паркинсона, диабеты I типа и II типа, осложнения диабета (диабетическая ретинопатия, нефропатия), гипергликемическое повреждение ткани, гипогликемическое повреждение ткани, холестаз, повреждение, вызванное алкоголем. Данное изобретение также относится к способам ингибирования МРТР и обеспечивает способ для лечения болезней и состояний, связанных с активностью пор перехода митохондриальной проницаемости (МРТР). Такой способ включает введение млекопитающему при необходимости эффективного количества соединения формулы (I). Вышеописанный способ позволяет лечение расстройств, характеризующихся ишемией/реперфузией, окислительным или дегенеративным повреждением ткани, болезней, связанных с возрастом, дегенеративных и нейродегенеративных болезней. В предпочтительном варианте осуществления способа, описанного выше, расстройствами являются острый инфаркт миокарда и диабетическая ретинопатия. Ингибирующая активность и эффективность выбранных соединений определены путем in vitro анализа, который оценивает способность соединений данного изобретения препятствовать МРТ в выделенной митохондрии. Митохондриальный in vitro анализ: способ и результаты. Митохондриальный in vitro анализ основан на изучении физиологических процессов в выделенных и функциональных митохондриальных органеллах. Возможно исследовать многие митохондриальные процессы, включая удержание кальция и дыхание, в суспензиях выделенных митохондрий, полученных из разных тканей. Способность выделенной митохондрии поглощать кальций извне является прямой мерой митохондриальной целостности и функции. Перегрузка кальцием вызывает МРТ, который затем нарушает митохондриальную целостность, ухудшает способность митохондрии закачивать кальций и вызывает высвобождение накопленного кальция из митохондриального матрикса. Анализ использует этот феномен поглощения кальция, перегрузки и высвобождения в выделенной митохондрии для оценки способности соединений данного изобретения ингибировать МРТР и предупреждать МРТ. Получение митохондрий мышиной печени. Митохондрии получали из печеней самцов 129 или С 57/В 6 мышей весом 20-25 г. Животных умерщвляли вывихом шеи. Выделяли печень и помещали на ледяную среду выделения (0,25 М сахарозы, 10 мМ Tris-HCl, 0,1 мМ этилен-bis(оксоэтиленнитрило)тетрауксусной кислоты (EGTA), pH 7,4). Печени промывали три-четыре раза ледяной средой, резали ножницами и пропускали через ручной гомогенизатор Поттера, выдерживаемый в ледяной бане. Гомогенат разбавили до 50 мл на печень, а неразрушенные клетки и ядра осадили центрифугированием при 900g в охлажденной центрифуге Beckman AvantiTM J25, поддерживаемой при 4C, в течение 10 мин. Супернатант осторожно декантировали и центрифугировали при 7000g в той же центрифуге в течение 10 мин. Супернатант удалили и осадок митохондрий осторожно ресуспендировали в ледяной среде выделения и центрифугировали, как указано выше. Полученный осадок митохондрий ресуспендировали в небольшом количестве ледяной среды выделения и хранили на льду. Содержание белка митохондрии определяли при помощи биуретового анализа. Способность удерживать кальций (CRC). Способность удерживать кальций (CRC) митохондрий является мерой чувствительности предрасположенности митохондрий к открытию МРТР после поглощения кальция. В присутствии внемитохондриального кальция выделенные митохондрии поглощают кальций в матрикс посредством унипортера кальция. Продолжительное добавление внемитохондриального кальция и последующее поглощение приводит к вызванному кальцием открытию МРТР, потере митохондриальной целостности и высвобождению накопленного кальция. Концентрация кальция, который может удерживаться до вызванного кальцием открытия МРТР, выражается в способности удерживать кальций и выражена в нмоль кальция на 1 мг митохондрий.CRC митохондриальных препаратов (200 мкл суспензии 0,5 мг/мл) измеряли флуориметрически в присутствии флуоресцентного индикатора Са 2+ (0,3 мкМ Calcium Green-5N), применяя планшетный считыватель Tecan Infinite F200 (возбуждение: 505 нм; эмиссия: 535 нм) (Ichas, F.; Jouaville, L.S.; Mazat, J.P.Mitochondria are excitable organelles capable of generating and conveying electrical and calcium signal. Cell. 1997, 89, 1145-1153). Calcium Green-5N является флуорометрическим зондом, который не проникает через мембраны и при добавлении к митохондриальной суспензии способен определять присутствие Са 2+ в среде вне митохондрии. Митохондрии нагружали последовательными 10 мкМ импульсами кальция (1 мкл 2 мМ CaCl2 в 200 мкл митохондриальной суспензии) при интервалах 1 мин, смешивали и сигнал внемитохондриального кальция измеряли приблизительно через 1 мин после каждого добавления для облегчения митохондриального поглощения (выполняли на автоматизированной рабочей станции TecanFreedom Evo 200). При этих условиях митохондрии активно поглощали и удерживали Са 2+ до точки, в которой митохондрии подвергались быстрому процессу высвобождения Са 2+, обусловленного открытием МРТР. Конечной концентрацией кальция, необходимого для открытия МРТР и высвобождения накопленного кальция, является митохондриальная CRC. Этот протокол загрузки Са 2+, таким образом, обеспечивает пригодный и чувствительный анализ для измерения открытия МРТР и применяется для оценки способности соединений данного изобретения ингибировать открытие МРТР. Соединения (конечная концентрация 1 мкМ) добавляли непосредственно в митохондриальный раствор за 1 мин перед началом импульсов кальция и определяли количество импульсов кальция, необходимых для открытия РТР. Соотношение между количеством кальция, необходимого для начала МРТ в присутствии соединения (CRCi),по отношению к необходимому для того, чтобы вызвать МРТ в отсутствие соединения (CRCo), является мерой ингибиторного эффекта соединения на МРТР. Это значение назвали эффективностью CRC, и результаты, полученные от нескольких соединений данного изобретения, сообщили в биологическом примере 1. Эффективности соединения оценили путем сравнения ингибиторной активности при 1 мкМ. Дополнительный объект данного изобретения представлен применением соединения общей формулы (I), как определено выше, а также его изомеров, рацемических форм, таутомеров, энантиомеров, диастереомеров, эпимеров, полиморфов, их смесей, пролекарств и их фармацевтически приемлемых солей для получения лекарственного препарата для предупреждения и/или лечения болезней и состояний, связанных с активностью МРТ-поры. Обеспечен способ применения соединения согласно данному изобретению для изготовления лекарственного препарата для применения при лечении болезненного состояния, которое, как известно, опосредовано МРТР или которое, как известно, лечится ингибиторами МРТР. Дополнительным объектом данного изобретения является фармацевтическая композиция, содержащая в качестве активного ингредиента одно или более соединений формулы (I), как определено выше,и/или пролекарства, и/или их фармацевтически приемлемую соль в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями. Специалисту в данной области техники известно все разнообразие таких наполнителей, подходящих для составления фармацевтической композиции. Подходящие фармацевтически приемлемые наполнители хорошо известны специалистам данной области техники. Наполнители включают в качестве иллюстрации и не ограничиваясь разбавители, заполнители, агглютинирующие вещества, средства, улучшающие распадаемость, ингибиторы распада,ускорители абсорбции,вспомогательное вещество,связующие,носители,суспендирующие/диспергирующие средства, пленкообразователи/покрытия, адгезивы, антиадгезивы, увлажняющие средства, смазочные средства, глиданты, консерванты, сорбенты, поверхностно-активные средства, вещества, добавленные для маскировки или нейтрализации неприятного вкуса или запаха, ароматизаторы,красители, отдушки, ароматизирующие средства, подсластители и вещества, добавленные для улучшения внешнего вида композиции. Выбор наполнителя будет в большой степени зависеть от факторов, таких как конкретный способ введения, влияние наполнителя на растворимость и стабильность и природы лекарственной формы. Фармацевтические композиции данного изобретения можно вводить разнообразными путями,включая пероральный, парентеральный, внутривенный, подкожный, внутримышечный, трансмукозальный (включая буккальный, сублингвальный, трансуретральный и ректальный), местный, трансдермальный, ингаляционный, через слизистую или чрескожный, или применяя любой другой путь введения. Таким образом, они будут присутствовать в форме растворов или суспензий для инъекции или многодозовых флаконов, в форме простых или покрытых таблеток, таблеток, покрытых сахаром или пленкой, облаточных капсул, гелевых капсул, пилюль, крахмальных капсул, саше, порошков, гранул, болюса,- 19020320 электуария, пасты, суппозиториев или ректальных капсул, сиропов, эмульсий, растворов или суспензий,для чрескожного применения в полярном растворителе, или для применения через слизистую. Например, твердые пероральные формы могут содержать вместе с активным соединением разбавители, например карбонаты щелочно-земельного металла, магний фосфат, лактозу, декстрозу, тростниковый сахар, сахарозу, целлюлозу, производные микрокристаллической целлюлозы, крахмалы, кукурузный крахмал или картофельный крахмал, модифицированные крахмалы и подобное; смазочные средства, например диоксид кремния, тальк, стеариновая кислота, магния или кальция стеарат и/или полиэтиленгликоли; связывающие средства, например крахмалы, аравийская камедь, желатиновая метилцеллюлоза,карбоксиметилцеллюлоза или поливинилпирролидон; средства, улучшающие распадаемость, например крахмал, альгиновая кислота, альгинаты или гликолят натриевого крахмала; пенящиеся смеси; красители; подсластители; увлажняющие средства, такие как лецитин, полисорбаты, лаурилсульфаты; и, в основном,нетоксичные и фармакологически неактивные вещества, применяемые в фармацевтических составах. Эти фармацевтические препараты можно изготовить известным способом, например при помощи процессов смешивания, гранулирования, таблетирования, покрытия сахаром или покрытия пленкой. Жидкими дисперсиями для перорального введения могут быть, например, сиропы, эмульсии и суспензии. В качестве примера сиропы могут содержать как носитель сахарозу или сахарозу с глицерином и/или маннитом и сорбит. Суспензии и эмульсии могут содержать в качестве примеров носителей натуральную камедь, агар,альгинат натрия, пектин, метилцеллюлозу, карбоксиметилцеллюлозу или поливиниловый спирт. Суспензия или растворы для внутримышечных инъекций могут содержать вместе с активным соединением фармацевтически приемлемый носитель, например стерильную воду, оливковое масло, этилолеат, гликоли, например пропиленгликоль и, при необходимости, подходящее количество лидокаина гидрохлорида. Растворы для внутривенных инъекций или инфузий могут содержать в качестве носителя стерильную воду, или предпочтительно они могут быть в форме стерильных водных изотонических солевых растворов, или они могут содержать пропиленгликоль в качестве носителя. Суппозитории могут содержать вместе с активным соединением фармацевтически приемлемый носитель, например какао-масло, полиэтиленгликоль, поверхностно-активное вещество полиоксиэтиленового сложного эфира сорбитана и жирной кислоты или лецитин. Вышеописанные компоненты для вводимой фармацевтической композиции являются только типичными представителями. Дополнительные материалы, а также методики обработки и подобное изложены частично в 5 части Remington's Pharmaceutical Sciences, 20th Edition, 2000, Merck Publishing Company, Easton, Pennsylvania, которая включена в данный документ посредством ссылки. Соединение этого изобретения формулы (I) может также вводиться в формах длительного высвобождения или из систем доставки лекарственного средства длительного высвобождения. Описание типичных материалов длительного высвобождения можно также обнаружить во включенных материалах в Remington's Pharmaceutical Sciences. Фармацевтические композиции, содержащие соединения данного изобретения, обычно получают,следуя общепринятым способам, и вводят в подходящей фармацевтической форме. Твердые композиции для перорального введения можно получить обычным смешиванием, заполнением или прессованием. Можно повторить операции смешивания, чтобы диспергировать активное средство в композициях, содержащих высокие количества заполнителей. Эти соотношения являются общепринятыми. Жидкие пероральные препараты можно составить, например, как водные или масляные суспензии или растворы, эмульсии, сиропы или эликсир, или можно представить как лиофилизированный продукт,который восстанавливают добавлением воды или подходящего носителя перед применением. Указанные жидкие препараты могут содержать стандартные добавки, такие как суспендирующие средства, например сорбит, сироп, метилцеллюлозу, желатин, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гель стеарата алюминия или гидрогенизированные пищевые жиры, эмульгирующие средства, например лецитин, сорбитан моноолеат или гуммиарабик; неводные носители (которые могут включать пищевые масла), например миндальное масло, фракционированное кокосовое масло, масляные сложные эфиры, такие как глицериновые сложные эфиры, пропиленгликоль или этиловый спирт; консерванты, например метил- или пропил-p-гидроксибензоат или сорбиновая кислота, и, при необходимости, общепринятые вещества для придания вкуса и красители. Для парентерального введения можно получить жидкие единицы дозировки, содержащие соединение и стерильный носитель. Соединение в зависимости от выбранного носителя и концентрации можно суспендировать или растворить. Парентеральные растворы обычно готовят путем растворения соединения в носителе, стерилизации фильтрацией, заполнения в подходящие сосуды и запаивания. Преимущественно, также можно растворить в носителе подходящие вспомогательные вещества, такие как местные анестетики, консерванты и буферные средства. Для повышения стабильности композицию можно заморозить после заполнения сосуда и удалить воду под вакуумом. Парентеральные суспензии готовят, в основном, тем же способом, с той разницей, что соединение можно скорее суспендировать, чем растворить в носителе, и их можно стерилизовать обработкой этиленоксидом перед суспендированием в стерильном носителе. Преимущественно, в композицию можно включить поверхностно-активное вещество или увлажняющее средство с целью облегчения равномерного распределения соединения данного изобретения. Соединения данного изобретения также можно вводить местно. Местные составы могут содержать,например, мазь, крем, гель, лосьон, раствор, пасту или подобное и/или могут быть получены так, чтобы содержать липосомы, мицеллы и/или микросферы. Мази, как хорошо известно в области техники фармацевтических составов, являются полужидкими препаратами, которые типично основаны на вазелине или других нефтяных производных. Примеры мазей включают маслянистые основы мазей, например растительные масла, жиры, полученные из животных, и полужидкие углеводороды, полученные из нефти,эмульгируемые основы мазей, например гидроксистеарина сульфат, безводный ланолин и гидрофильный вазелин, эмульсионные основы мазей, например цетиловый спирт, глицерилмоностеарат, ланолин и стеариновая кислота, и водорастворимые основы мазей, полученные из полиэтиленгликолей различного молекулярного веса. Кремы, как также хорошо известно специалистам данной области техники, являются вязкими жидкостями или полужидкими эмульсиями и содержат масляную фазу, эмульгатор и водную фазу. Масляная фаза обычно содержит вазелин и жирный спирт, такой как цетиловый или стеариновый спирт. Водная фаза обычно содержит увлажнитель. Эмульгатор в кремовом составе выбран из неионных,анионных, катионных или амфотерных поверхностно-активных веществ. Однофазные гели содержат органические макромолекулы, распределенные, в основном, однородно по всему жидкому носителю,который типично является водным, но также, предпочтительно, содержит спирт и, факультативно, масло. Предпочтительными гелеобразующими средствами являются поперечно-сшитые полимеры акриловой кислоты (такие как полимеры "карбомер", например карбоксиполиалкилены, которые могут быть получены коммерчески под торговым названием Carbopol). Также предпочтительными являются гидрофильные полимеры, такие как полиэтиленоксиды, сополимеры полиоксиэтилена и полиоксипропилена и поливиниловый спирт; целлюлозные полимеры, такие как гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилметилцеллюлозы фталат и метилцеллюлоза; камеди, такие как трагакантовая и ксантановая камедь; альгинат натрия и желатин. Для получения однородных гелей можно добавить диспергирующие средства, такие как спирт или глицерин, или гелеобразующее средство можно диспергировать перетиранием в порошок, механическим смешиванием и/или перемешиванием. Соединения данного изобретения можно также вводить путем трансдермального высвобождения. Типичные трансдермальные составы включают традиционные водные и неводные переносчики, такие как кремы, масла, лосьоны или пасты, или могут быть обеспечены в виде мембран или медикаментозных пластырей. В варианте осуществления соединение данного изобретения диспергировано в чувствительном к давлению пластыре, прилепленном на кожу. Этот состав позволяет соединению проникать с пластыря через кожу пациенту. Для получения лекарственного средства длительного высвобождения через кожу может использоваться натуральный каучук и силикон как клейкие вещества, чувствительные к давлению. Соединения формулы (I) данного изобретения, подходящие для введения млекопитающему, например людям, можно вводить обычными путями, и уровень дозировки зависит от разнообразных факторов,включая активность конкретного применяемого соединения; возраст, вес тела, общее состояние здоровья, пол и питание пациента, получающего лечение; время и путь введения; скорость экскреции; другие лекарственные средства, которые ранее были введены; и тяжести конкретного заболевания, подвергаемого терапии, как хорошо понятно специалистам в данном уровне техники. Например, подходящая дозировка, утвержденная для перорального введения соединения формулы(I), может быть в диапазоне от приблизительно 30 до 500 мг на дозу от 1 до 5 раз ежедневно. В основном будут вводиться более низкие дозы, когда применяют парентеральный путь. Таким образом, например,для внутривенного введения будет обычно применяться доза в диапазоне, например, от 0,5 до 30 мг на 1 кг веса тела. Соединения данного изобретения можно вводить в разнообразных лекарственных формах, например перорально в форме таблеток, таблеток, покрытых сахаром или пленкой, капсул, крахмальных капсул, как порошок или гранулы; как сиропы, эмульсии, раствор или суспензия в водной или неводной жидкости, как эмульсия масло-в-воде или эмульсия вода-в-масле, как болюс, электуарий или паста; ректально в форме суппозиториев; парентерально, например внутримышечно, путем внутривенной инъекции или инфузии. С целью лучшей иллюстрации данного изобретения без какого-либо его ограничения представлены следующие примеры. Примеры Способы. Если не указано иное, было установлено, что все исходные реагенты являются коммерчески доступными или легко получаются следующими стандартными описанными методиками и применяются без любой предварительной очистки. Спектр 1H-NMR (ядерно-магнитный резонанс) получали с Bruker 400 МГц. Химические сдвиги выражали в частях на миллион (ppm,единицы). Константы соединения выражены в герцах (Гц), и паттер- 21020320 ны расщепления описаны как s (синглет), bs (широкий синглет), d (дуплет), t (триплет), q (квартет), квинтLC-MS (жидкостная хроматография-масс-спектрометрия) эксперименты выполнили согласно следующим способам. Способ A-220: Waters Acquity UPLC, Waters SQD Single quadrupole. Колонка Acquity UPLC-BEH(А: 0%, В: 100%), 5-6 мин (А: 0%, В: 100%). Длина волны УФ-определения: 254 нм. Объем введения: 2 мкл. Следующие аббревиатуры относятся соответственно к определениям ниже.SCX (сильный катионообменник); TEA (триэтиламин); ТГФ (тетрагидрофуран). Пример 1. Получение замещенных (E)-3-(3-гидроксифенил)акриловых анилидов из соответствующих (E)-3-(3-ацетоксифенил)производных щелочным гидролизом смеси MeOH (4,5 мл) и 50% вес./вес. водного NaOH (74 мкл) нагревали при перемешивании в течение 40 мин при температуре дефлегмации. Смесь затем концентрировали при сниженном давлении для получения светло-желтого масла, которое поглотили и перетерли в порошок с 4 мл водной 0,5 н HCl. После фильтрации и сушки 213 мг названого (E)-3-(3-гидрокси-4-метоксифенил)-N-нафталин-1-ил-акриламида получили в виде белого порошка. 1 Н NMR (DMSO-d6)(ppm): 10,04 (s, 1H), 9,24 (s, 1H), 8,16 (d, J=8,4 Гц, 1H), 7,96-7,94 (m, 1H), 7,90LC-MS: способ A-220, rt=1,68 (ES+) [2M+Na]+: 661. Аналогично гидролизуя подходящие (E)-3-(3-ацетоксифенил)акриловые анилиды, получили следующие соединения:(очистка колоночной хроматографией на силикагеле, элюант n-гексан/AcOEt 65:35)LC-MS: способ A-220, rt=2,07 (ES+) [M+H]+: 389. Пример 2. Получение замещенных (E)-3-(3-гидроксифенил)акриловых анилидов из соответствующих (E)-3-(3-ацетоксифенил)производных кислотным гидролизом 3 н. метанольный раствор соляной кислоты (10 мл, 30 ммоль) добавили в раствор (E)-N-[2-хлор-3- 24020320(пиридин-4-илметокси)фенил]-3-(3-ацетокси-4-метоксифенил)акриламида гидрохлорида (240 мг, 0,53 ммоль) в ТГФ (5 мл). Полученную в результате смесь перемешивали при RT в течение 16 ч, концентрировали при пониженном давлении, растворили и повторно выпарили (3 раза с MeOH и раз с ацетоном) для получения светло-желтого остатка, который перетерли в порошок с этиловым эфиром. После фильтрации и сушки получили 232 мг названного вещества (E)-N-[2-хлор-3-(пиридин-4-илметокси)фенил]-3(3-гидрокси-4-метоксифенил)акриламида гидрохлорида в виде светло-желтого порошка. 1LC-MS: способ A-220, rt=1,17 (ES+)[M+H]+:411. Аналогично гидролизуя подходящие (E)-3-(3-ацетоксифенил)акриловые анилиды, получили следующие соединения:(очистка колоночной хроматографией на силикагеле, элюант n-гексан/AcOEt 70:30)(очистка колоночной хроматографией на силикагеле, элюант DCM/MeOH/водный гидроксид аммония 98:2:0,2) 1(очистка колоночной хроматографией на силикагеле, элюант DCM/MeOH 100:1)(очистка колоночной хроматографией на силикагеле, элюант DCM/MeOH 100:1)(очистка колоночной хроматографией на силикагеле, элюант DCM/MeOH/водный гидроксид аммония 90:10:1) 1(очистка колоночной хроматографией на силикагеле, элюант DCM/MeOH/AcOEt 97:3)
МПК / Метки
МПК: C07C 235/36, C07D 213/38, C07D 213/30, C07D 213/68, C07D 211/22, C07D 233/60, C07D 231/12, C07D 213/32, C07D 211/46, C07D 295/135, C07C 235/38, C07D 231/56, C07D 209/08, C07C 323/41, C07D 213/75
Метки: перехода, акриламидопроизводные, применимые, митохондриальной, ингибиторы, проницаемости
Код ссылки
<a href="https://eas.patents.su/30-20320-akrilamidoproizvodnye-primenimye-kak-ingibitory-perehoda-mitohondrialnojj-pronicaemosti.html" rel="bookmark" title="База патентов Евразийского Союза">Акриламидопроизводные, применимые как ингибиторы перехода митохондриальной проницаемости</a>
Предыдущий патент: Способ тренировки спортсмена
Следующий патент: Чувствительный элемент датчика
Случайный патент: Устройство для впрыскивания лекарства












