Аминотетрагидропираны в качестве ингибиторов дипептидилпептидазы-iv для лечения или предупреждения диабета
Номер патента: 18613
Опубликовано: 30.09.2013
Авторы: Бифту Тесфайе, Чэнь Пин, Кокс Джейсон М., Вебер Энн Э.
Формула / Реферат
1. Соединение структурной формулы (I)
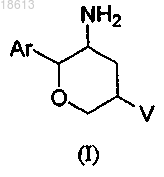
или его фармацевтически приемлемая соль,
где V означает группу
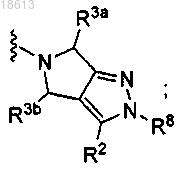
Ar является фенилом, необязательно замещенным одним-пятью заместителями R1;
каждый R1 означает галоген;
каждый R2 означает водород;
R3a и R3b, каждый независимо, являются водородом или C1-4алкилом, необязательно замещенным 1-5 атомами фтора;
R8 выбирают из группы, включающей -SO2C1-6алкил, -SO2C3-6циклоалкил, -SO2-арил, -SO2-гетероарил, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора; арил содержит 6-10 кольцевых атомов; гетероарил и гетероциклил содержат 3-15 кольцевых атомов, включая по крайней мере один гетероатом, выбранный из О, S и N; и арил и гетероарил необязательно замещены одним-пятью заместителями, независимо выбранными из группы, включающей гидрокси, галоген, циано, нитро, СО2Н, С1-6алкилоксикарбонил, C1-6алкил и С1-6алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора.
2. Соединение по п.1, где Ar необязательно замещен одним-тремя заместителями, независимо выбранными из группы, включающей фтор, хлор и бром.
3. Соединение по п.2, где Ar является 2,5-дифторфенилом или 2,4,5-трифторфенилом.
4. Соединение по п.1, где R3a и R3b, оба, являются водородом.
5. Соединение по п.1, где V представляет собой
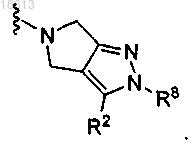
6. Соединение по п.5, где R2 является водородом.
7. Соединение по п.6, где R8 является -SO2C1-6алкилом или -SO2C3-6циклоалкилом, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора.
8. Соединение по п.1 структурной формулы (Ia) или (Ib), имеющее указанную стереохимическую конфигурацию на двух стереогенных атомах углерода, отмеченных *
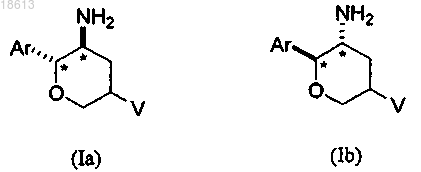
9. Соединение по п.8 структурной формулы (Ia), имеющее указанную абсолютную стереохимическую конфигурацию на двух стереогенных атомах углерода, отмеченных *
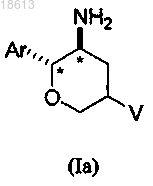
10. Соединение по п.8 структурных формул (Ic) и (Id), имеющее указанную стереохимическую конфигурацию на трех стереогенных атомах углерода, отмеченных *
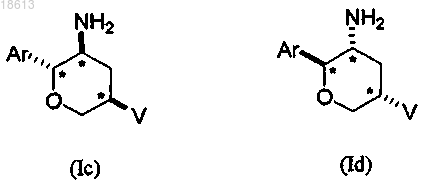
11. Соединение по п.10 структурной формулы (Ic), имеющее указанную абсолютную стереохимическую конфигурацию на трех стереогенных атомах углерода, отмеченных *
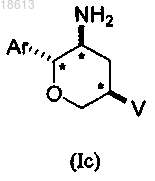
12. Соединение по п.11, где V выбирают из группы, включающей
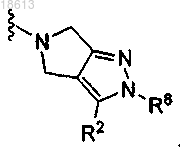
13. Соединение по п.12, где R2 является водородом и R8 является -SO2C1-6алкилом или -SO2C3-6циклоалкилом, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора.
14. Соединение, которое выбирают из группы, состоящей из
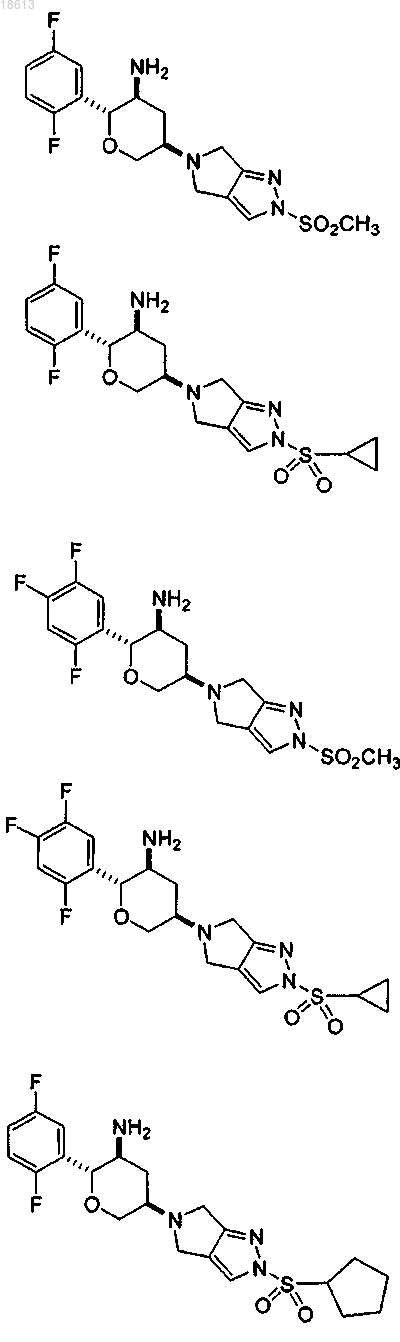
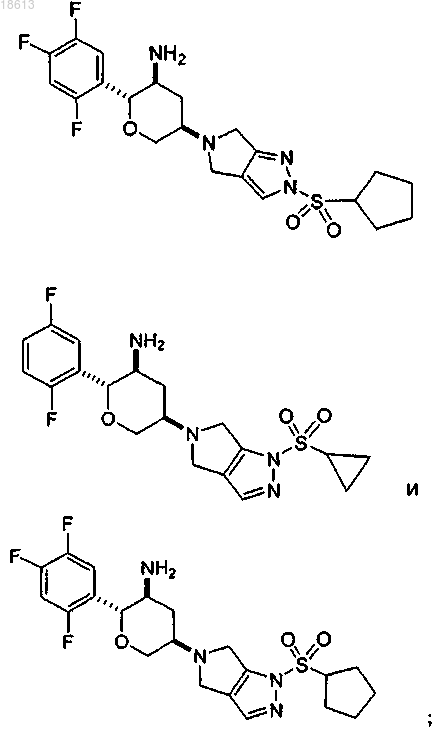
или его фармацевтически приемлемая соль.
15. Соединение, представляющее собой
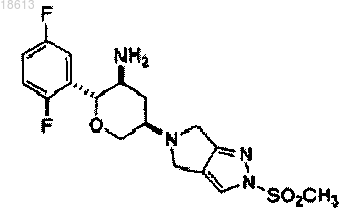
16. Фармацевтическая композиция, содержащая соединение по п.1 и фармацевтически приемлемый носитель.
17. Применение соединения по п.1 для приготовления лекарственного средства, предназначенного для лечения состояния, выбранного из группы, включающей резистентность к инсулину, гипергликемию, диабет II типа у млекопитающих, нуждающихся в таком лечении.
Текст
АМИНОТЕТРАГИДРОПИРАНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ДИПЕПТИДИЛПЕПТИДАЗЫ-IV ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ДИАБЕТА Изобретение относится к новым замещенным аминотетрагидропиранам структурной формулы (I),которые являются ингибиторами фермента дипептидилпептидаза-IV и которые применяют для лечения или предупреждения заболеваний, в которые вовлечен фермент дипептидилпептидазаIV, таких как диабет и особенно - диабет 2 типа. Изобретение также связано с фармацевтическими композициями, содержащими эти соединения, и применением этих соединений и композиций для предупреждения и лечения таких заболеваний, в которые вовлечен фермент дипептидилпептидаза-IV.(71)(73) Заявитель и патентовладелец: МЕРК ШАРП ЭНД ДОМЭ КОРП. Область техники Данное изобретение относится к новым замещенным аминотетрагидропиранам, которые являются ингибиторами фермента дипептидилпептидазы-IV ("ингибиторами ДПП-4") и которые применяют для лечения или предупреждения заболеваний, в которые вовлечен фермент дипептидилпептидаза-IV, таких как диабет, особенно диабет II типа. Данное изобретение также относится к фармацевтическим композициям, содержащим такие соединения, и применению этих соединений и композиций для предупреждения или лечения таких заболеваний, в которые вовлечен фермент дипептидилпептидаза-IV. Уровень техники Диабет относится к болезненным процессам, возникающим из множества причинных факторов и характеризующимся повышенными уровнями глюкозы в плазме или гипергликемией в состоянии натощак или после введения глюкозы во время перорального тестирования толерантности к глюкозе. Постоянная или неконтролируемая гипергликемия связана с повышенной и преждевременной заболеваемостью или смертностью. Часто аномальный гомеостаз глюкозы связан прямо и косвенно с изменениями в метаболизме жиров, липопротеина и аполипопротеина и другими метаболическими и гемодинамическими заболеваниями. Поэтому пациенты с сахарным диабетом II типа особенно подвержены риску макрососудистых и микрососудистых осложнений, включая коронарную болезнь сердца, гипертонию, нефропатию, невропатию и ретинопатию. Поэтому терапевтический контроль гомеостаза глюкозы, метаболизма жиров и гипертонии являются критически важными в клиническом ведении и лечении сахарного диабета. Существуют две распознаваемые формы диабета. При диабете 1 типа, или инсулинозависимом сахарном диабете (ИЗСД), пациент вырабатывает немного или вообще не вырабатывает инсулин, который регулирует переработку глюкозы. При диабете II типа, или инсулинонезависимом сахарном диабете(НИЗСД), пациенты часто имеют уровни инсулина в плазме, которые такие же или повышены, по сравнению с пациентами без диабета; однако у этих пациентов развита резистентность к стимулирующему эффекту инсулина на глюкозу и метаболизм жиров в основных чувствительных к инсулину тканях, которые включают мышцы, печень и жировые ткани, и уровни инсулина в плазме, хотя и повышенные, недостаточны для преодоления явно выраженной резистентности к инсулину. Резистентность к инсулину возникает, в первую очередь, не из-за уменьшенного количества рецепторов инсулина, а из-за дефекта после связывания рецепторов инсулина, который еще не изучен. Такая резистентность к реагированию на инсулин вызывает недостаточную инсулиновую активацию поглощения глюкозы, окисление и хранение в мышцах, неадекватное инсулиновое подавление липолиза в жировой ткани и производства глюкозы и секреции в печени. Доступное лечение диабета II типа, которое существенно не менялось в течение многих лет, имеет известные ограничения. Хотя физические упражнения и снижение калорийности пищи значительно улучшают диабетическое состояние, тем не менее соблюдение такого режима явно недостаточно из-за прочно укоренившегося малоподвижного образа жизни и избыточного питания, особенно пищей, содержащей высокое количество насыщенных жиров. Повышение уровня инсулина в плазме при введении сульфонилмочевин (например, толбутамида и глипизида) или меглитинида, которые стимулируют-клетки поджелудочной железы выделять большее количество инсулина, и/или при введении инсулина,если сульфонилмочевины или меглитинид становятся неэффективными, может давать концентрации инсулина, достаточно высокие для стимулирования очень резистентных к инсулину тканей. Однако очень низкие уровни глюкозы в плазме могут возникать при введении инсулина или секретагогов инсулина(сульфонилмочевин или меглитинида), что приводит к возникновению повышенной резистентности к инсулину даже из-за более высоких уровней инсулина в плазме. Бигуаниды повышают чувствительность к инсулину, что вызывает некоторую коррекцию гипергликемии. Однако два бигуанида, фенформин и метформин, могут вызывать молочный ацидоз и тошноту/диарею. Метформин обладает меньшим количеством побочных эффектов, чем фенформин, и часто назначается для лечения диабета II типа. Глитазоны (т.е. 5-бензилтиазолидин-2,4-дионы) составляют дополнительный класс соединений, потенциально облегчающих многие симптомы диабета II типа. Эти средства значительно повышают чувствительность к инсулину в мышцах, печени и жировой ткани в нескольких животных моделях диабета II типа, что дает частичную или полную коррекцию повышенных уровней глюкозы в плазме без возникновения гипогликемии. Глитазоны, которые в настоящее время доступны на рынке, являются агонистами рецептора, активируемого пролифератором пероксисом (РАПП), преимущественно подтипа РАППгамма. Обычно полагают, что агонизм к РАПП-гамма отвечает за улучшенную сенсибилизацию к инсулину, которая наблюдается с глитазонами. Новые агонисты РАПП, которые тестируют на лечение диабета II типа, являются агонистами альфа, гамма или дельта подтипа или их сочетания и во многих случаях химически отличаются от глитазонов (т.е. они не имеют тиазолидиндионов в структуре). Серьезные побочные эффекты (например, токсичность к печени) возникают при приеме некоторых глитазонов, таких как троглитазон. Дополнительные способы лечения заболевания до сих пор исследуются. Новые биохимические подходы, которые были недавно представлены или до сих пор разрабатываются, включают ингибиторы альфа-глюкозидазы (например, акарбоза), ГПП-1 миметики (например, экзенатид и лираглутид), антаго-1 018613 нисты рецептора глюкагона, активаторы глюкокиназы и агонисты GPR-119. Соединения, которые являются ингибиторами фермента дипептидилпептидазы-IV ("ДПП-4"), также оказались полезными для лечения диабета, особенно диабета II типа [см. WO 97/40832; WO 98/19998; патент США 5939560; патент США 6303661; патент США 6699871; патент США 6166063;(2005); H.-U. Demuth in Biochim. Biophys. Acta. 1751:33-44 (2005) и R. Mentlein, Exp. Opin. Invest. Drugs,14:57-64 (2005). Дополнительные патентные публикации, в которых описаны ингибиторы ДПП-4, применяемые в лечении диабета, включают WO 2006/009886 (26 января 2006 г.); WO 2006/039325 (13 апреля 2006 г.);(22 мая 2008 г.). Полезность ингибиторов ДПП-4 для лечения диабета II типа основана на факте, что ДПП-4 in vivo легко инактивирует глюкагоноподобный пептид-1 (ГПП-1) и желудочный ингибиторный пептид (ЖИП). ГПП-1 и ЖИП являются инкретинами и вырабатываются при потреблении пищи. Инкретины стимулируют производство инсулина. Ингибирование ДПП-4 ведет к пониженной инактивации инкретинов, что,в свою очередь, повышает эффективность инкретинов в стимулировании производства инсулина поджелудочной железой. Поэтому ингибирование ДПП-4 дает повышенный уровень инсулина в сыворотке. Преимущественно, так как инкретины производятся телом только при поглощении пищи, не ожидается,что ингибирование ДПП-4 повысит уровень инсулина в подходящее время, например, между приемами пищи, что может вызвать сильное понижение сахара в крови (гипогликемию). Поэтому ожидается, что ингибирование ДПП-4 повышает инсулин без риска гипогликемии, что является опасным побочным эффектом, связанным с применением секретагогов инсулина. Ингибиторы ДПП-4 также имеют другое терапевтическое применение, описанное здесь. Необходимы новые соединения, чтобы можно было найти улучшенные ингибиторы ДПП-4 для лечения диабета и,потенциально, других заболеваний и состояний. В частности, существует необходимость в ингибиторах ДПП-4, которые являются селективными к другим членам семейства серинпептидаз, которые включают пролиндипептидазу покоящихся клеток (ППП), ДПП 8 и ДПП 9 [см. G. Lankas, et al., "Dipeptidylstudy for selectivity of DPP4, DPP8, and DPP9 inhibitors", Bioorg. Med. Chem. Lett., 17:3716-3721 (2007)]. Терапевтический потенциал ингибиторов ДПП-4 для лечения диабета II типа обсуждается в (i) D.J. Drucker, Exp. Opin. Invest. Drugs, 12:87-100 (2003); (ii) K. Augustyns, et al., Exp. Opin. Ther.(xiii) J.J. Holst, et al., "Glucagon-like peptide-1, glucose homeostasis, and diabetes, Trends in Molecular Medicine, 14:161-168 (2008). Определенные ингибиторы ДПП-4, которые либо уже одобрены, либо находятся в стадии клинических исследований лечения диабета II типа, включают ситаглиптин, вилдаглиптин, саксаглиптин, алоглиптин, кармеглиптин, мелоглиптин и дитоглиптин. Сущность изобретения Данное изобретение относится к новым замещенным 3-аминотетрагидропиранам, которые являются ингибиторами фермента дипептидилпептидазы-IV ("ингибиторы ДПП-4") и которые используют для лечения или предупреждения заболеваний, в которые вовлечен фермент дипептидилпептидаза-IV, таких как диабет и особенно диабет II типа. Данное изобретение также относится к фармацевтическим композициям, содержащим эти соединения, и к применению этих соединений и композиций для предупреждения или лечения таких заболеваний, в которые вовлечен фермент дипептидилпептидаза-IV. Подробное описание изобретения Данное изобретение относится к новым замещенным 3-аминотетрагидропиранам, которые применяют в качестве ингибиторов дипептидилпептидазы-IV. Соединения и их фармацевтически приемлемые соли в соответствии с данным изобретением описаны структурной формулой (I)Ar является фенилом, необязательно замещенным одним-пятью заместителями R1; каждый R1 независимо выбирают из группы, включающей галоген,циано,гидрокси,C1-6 алкил, необязательно замещенный 1-5 атомами фтора, иC1-6 алкокси, необязательно замещенный 1-5 атомами фтора; каждый R2 независимо выбирают из группы, включающей водород,галоген,циано,C1-10 алкокси, где алкокси необязательно замещен одним-пятью заместителями, независимо выбранными из фтора и гидрокси,C1-10 алкил, где алкил необязательно замещен одним-пятью заместителями, независимо выбранными из фтора и гидрокси,С 2-10 алкенил, где алкенил необязательно замещен одним-пятью заместителями, независимо выбранными из фтора и гидрокси,(CH2)n-арил, где арил необязательно замещен одним-пятью заместителями, независимо выбранными из гидрокси, галогена, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонила, С 1-6 алкила и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора,(CH2)n-гетероарил, где гетероарил необязательно замещен одним-тремя заместителями, независимо выбранными из гидрокси, галогена, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонила, C1-6 алкила иC1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора,(CH2)n-гетероциклил, где гетероциклил необязательно замещен одним-тремя заместителями, независимо выбранными из оксо, гидрокси, галогена, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонила,C1-6 алкила и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора,(CH2)n-С 3-6 циклоалкил, где циклоалкил необязательно замещен одним-тремя заместителями, независимо выбранными из галогена, гидрокси, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонила, C1-6 алкила иC1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора,(CH2)n-COOH,(CH2)n-COOC1-6 алкил,(CH2)n-NR4R5,(CH2)n-CONR4R5,(CH2)n-OCONR4R5,(CH2)n-SO2NR4R5,(CH2)n-SO2R6,(CH2)n-NR7SO2R6,(CH2)n-NR7CONR4R5,(CH2)n-NR7COR7 и(CH2)n-NR7CO2R6; где любой отдельный метилен (CH2), атом углерода в (CH2)n, необязательно замещенный однимдвумя заместителями, независимо выбранными из фтора, гидрокси, C1-4 алкила и C1-4 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора;R3a и R3b, каждый независимо, являются водородом или C1-4 алкилом, необязательно замещенным 15 атомами фтора;C1-6 алкил, где алкил необязательно замещен одним-пятью заместителями, независимо выбранными из фтора и гидрокси, и где фенил и циклоалкил необязательно замещены одним-пятью заместителями,независимо выбранными из галогена, гидрокси, C1-6 алкила и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора; илиR4 и R5 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо,выбранное из азетидина, пирролидина, пиперидина, пиперазина и морфолина, где указанное гетероциклическое кольцо необязательно замещено одним-тремя заместителями, независимо выбранными из галогена, гидрокси, C1-6 алкила и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора; каждый R6 независимо является C1-6 алкилом, где алкил необязательно замещен одним-пятью заместителями, независимо выбранными из фтора и гидроксила;R7 является водородом или R6;-С(О)NH-гетероарил; где алкил и циклоалкил необязательно замещены 1-5 атомами фтора и где арил и гетероарил необязательно замещены одним-пятью заместителями, независимо выбранными из группы, включающей гидрокси, галоген, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонил, C1-6 алкил и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора; каждый n независимо равен 0, 1, 2 или 3 и каждый m независимо равен 0, 1 или 2. В одном варианте соединений в соответствии с данным изобретением Ar необязательно замещен одним-тремя заместителями, независимо выбранными из группы, включающей фтор, хлор, бром, метил,трифторметил и трифторметокси. В классе этого варианта Ar является 2,5-дифторфенилом или 2,4,5-трифторфенилом. Во втором варианте соединений в соответствии с данным изобретением R3a и R3b, оба, являются водородом. В третьем варианте соединений в соответствии с данным изобретением V выбирают из группы,включающей где R2 и R8 такие, как описаны выше. В классе этого варианта R2 является водородом. В другом классе этого третьего варианта V является В подклассе этого класса R2 является водородом.-4 018613 В четвертом варианте соединений в соответствии с данным изобретением R8 выбирают из группы,включающей-SO2-гетероарил; где алкил и циклоалкил необязательно замещены 1-5 атомами фтора и где арил и гетероарил необязательно замещены одним-пятью заместителями, независимо выбранными из группы, включающей гидрокси, галоген, циано, нитро, СО 2 Н, C1-6 алкилоксикарбонил, C1-6 алкил и C1-6 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора. В классе этого четвертого варианта R8 является -SO2C1-6 алкилом или -SO2C3-6 циклоалкилом, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора. В пятом варианте соединений в соответствии с данным изобретением представлены соединения структурных формул (Ia) и (Ib) указанной стереохимической конфигурации, имеющих транс-ориентациюAr и NH2 заместителей на двух стереогенных атомах углерода тетрагиропирана, отмеченных : где Ar и V такие, как описаны выше. В классе этого пятого варианта представлены соединения структурной формулы (Ia) указанной абсолютной стереохимической конфигурации, имеющие транс-ориентацию Ar и NH2 заместителей на двух стереогенных атомах углерода тетрагиропирана, отмеченных : Во втором классе этого пятого варианта представлены соединения структурных формул (Ic) и (Id) указанной стереохимической конфигурации, имеющих транс-ориентацию Ar и NH2 заместителей, трансориентацию Ar и V заместителей и цис-ориентацию NH2 и V заместителей на трех стереогенных атомах углерода тетрагидропирана, отмеченных : В подклассе этого класса представлены соединения структурной формулы (Ic) указанной абсолютной стереохимической конфигурации, имеющие транс-ориентацию Ar и NH2 заместителей, трансориентацию Ar и V заместителей и цис-ориентацию NH2 и V заместителей на трех стереогенных атомах углерода тетрагидропирана, отмеченных : В подклассе этого подкласса V выбирают из группы, включающей где R2 и R8 такие, как определены выше. В подклассе этого подкласса R2 является водородом и R8 является -SO2C1-6 алкилом или -SO2C36 циклоалкилом, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора.-5 018613 В третьем классе этого пятого варианта представлены соединения структурных формул (Ie) и (If) указанной стереохимической конфигурации, имеющие транс-ориентацию Ar и NH2 заместителей,цис-ориентацию Ar и V заместителей и транс-ориентацию NH2 и V заместителей на трех стереогенных атомах углерода тетрагидропирана, отмеченных : В подклассе этого класса представлены соединения структурной формулы (Ie) указанной абсолютной стереохимической конфигурации, имеющие транс-ориентацию Ar и NH2 заместителей,цис-ориентацию Ar и V заместителей и транс-ориентацию NH2 и V заместителей на трех стереогенных атомах углерода тетрагидропирана, отмеченных : В подклассе этого подкласса V выбирают из группы, включающей где R2 и R8 такие, как описаны выше. В подклассе этого подкласса R2 является водородом и R8 является -SO2C1-6 алкилом или-SO2C3-6 циклоалкилом, где алкил и циклоалкил необязательно замещены 1-5 атомами фтора. В шестом варианте соединений в соответствии с данным изобретением каждый R2 независимо выбирают из группы, включающей водород;C1-6 алкил, где алкил необязательно замещен 1-5 атомами фтора; и С 3-6 циклоалкил, где циклоалкил необязательно замещен одним-тремя заместителями, независимо выбранными из галогена, гидрокси, C1-4 алкила и C1-4 алкокси, где алкил и алкокси необязательно замещены 1-5 атомами фтора. В классе этого шестого варианта соединений в соответствии с данным изобретением каждый R2 независимо выбирают из группы, включающей водород, C1-3 алкил, трифторметил, 2,2,2-трифторэтил и циклопропил. В подклассе этого класса каждый R2 является водородом. Неограничивающие примеры соединений и их фармацевтически приемлемые соли в соответствии с данным изобретением, которые применяют в качестве ингибиторов дипептидилпептидазы-IV, имеют следующие структуры, имеющие указанные абсолютные стереохимические конфигурации на трех стереогенных атомах углерода тетрагидропирана. В данном описании применяются следующие определения."Алкил", а также другие группы, имеющие префикс "алк", такие как алкокси и алканоил, означают углеродные цепи, которые могут быть линейными или разветвленными, и их сочетания, если углеродная цепь не определена иначе. Примеры алкильных групп включают метил, этил, пропил, изопропил, бутил,-7 018613 втор- и трет-бутил, пентил, гексил, гептил, октил, нонил и подобные. Если дано определенное количество атомов углерода, например от С 3-10, термин "алкил" также включает циклоалкильные группы и сочетания линейных или разветвленных алкильных цепей, объединенных с циклоалкильными структурами. Если не указано количество атомов углерода, подразумевается, что "C1-6 циклоалкил" представляет собой подтип алкила и означает насыщенное карбоциклическое кольцо, имеющее определенное количество атомов углерода. Примеры циклоалкила включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и подобные. Циклоалкильная группа обычно является моноциклической,если не указано иначе. Циклоалкильные группы являются насыщенными, если не указано иначе. Термин "алкокси" относится к прямым или разветвленным алкоксидам с указанным количеством атомов углерода (например, C1-10 алкокси) или любым количеством в пределах этого интервала [например, метокси (МеО-), этокси, изопропокси и т.д.]. Термин "алкилтио" относится к прямым или разветвленным алкилсульфидам с указанным количеством атомов углерода (например, C1-10 алкилтио) или любым количеством в пределах этого интервала[например, метилтио (MeS-), этилтио, изопропилтио и т.д.]. Термин "алкиламино" относится к прямым или разветвленным алкиламинам с указанным количеством атомов углерода (например, C1-6 алкиламино) или любым количеством в пределах этого интервала[например, метиламино, этиламино, изопропиламино, трет-бутиламино и т.д.]. Термин "алкилсульфонил" относится к прямым или разветвленным алкилсульфонам с указанным количеством атомов углерода (например, C1-6 алкилсульфонил) или любым количеством в пределах этого интервала [например, метилсульфонил (MeSO2-), этилсульфонил, изопропилсульфонил и т.д.]. Термин "алкилоксикарбонил" относится к прямым или разветвленным сложным эфирам производного карбоновой кислоты в соответствии с данным изобретением с указанным количеством атомов углерода (например, C1-6 алкилоксикарбонил) или любым количеством в пределах этого интервала [например,метилоксикарбонил (МеОСО-), этилоксикарбонил или бутилоксикарбонил]."Арил" означает моно- или полициклическую ароматическую систему колец, содержащую атомы углерода в кольцах. Предпочтительные арилы являются моноциклическими или бициклическими 6-10-членными ароматическими системами колец. Фенил и нафтил являются предпочтительными арилами. Наиболее предпочтительным арилом является фенил. Термин "гетероциклил" относится к насыщенным или ненасыщенным неароматическим кольцам или системам колец, содержащим по крайней мере один гетероатом, выбранный из О, S и N, также включающим окисленные формы серы, а именно SO и SO2. Примеры гетероциклов включают тетрагидрофуран (ТГФ), дигидрофуран, 1,4-диоксан, морфолин, 1,4-дитиан, пиперазин, пиперидин,1,3-диоксолан, имидазолидин, имидазолин, пирролин, пирролидин, тетрагидропиран, дигидропиран, оксатиолан, дитиолан, 1,3-диоксан, 1,3-дитиан, оксатиан, тиоморфолин, пирролидинон, оксазолидин-2-он,имидазолидин-2-он, пиридон и подобные."Гетероарил" означает ароматический или частично ароматический гетероцикл, который содержит по крайней мере один гетероатом в кольце, выбранный из О, S и N. Гетероарилы также включают гетероарилы, конденсированные с другими видами циклов, такими как арилы, циклоалкилы и гетероциклы,которые не являются ароматическими. Примеры гетероарильных групп включают пирролил, изоксазолил, изотиазолил, пиразолил, пиридинил, 2-оксо-(1 Н)-пиридинил(2-гидроксипиридинил), оксазолил,1,2,4-оксадиазолил, 1,3,4-оксадиазолил, тиадиазолил, тиазолил, имидазолил, триазолил, тетразолил, фурил, триазинил, тиенил, пиримидинил, пиразинил, бензизоксазолил, бензоксазолил, бензотиазолил, бензотиадиазолил, дигидробензофуранил, индолинил, пиридазинил, индазолил, изоиндолил, дигидробензотиенил, индолизинил, циннолинил, фталазинил, хиназолинил, нафтиридинил, карбазолил, бензодиоксолил, хиноксалинил, пуринил, фуразанил, изобензилфуранил, бензимидазолил, бензофуранил, бензотиенил, хинолил, индолил, изохинолил, дибензофуранил, имидазо[1,2-а]пиридинил, [1,2,4-триазоло][4,3 а]пиридинил, пиразоло[1,5-а]пиридинил, [1,2,4-триазоло][1,5-а]пиридинил, 2-оксо-1,3-бензоксазолил,4-оксо-3H-хиназолинил, 3-оксо[1,2,4]триазоло[4,3-а]-2H-пиридинил, 5-оксо[1,2,4]-4H-оксадиазолил,2-оксо[1,3,4]-3H-оксадиазолил,2-оксо-1,3-дигидро-2H-имидазолил,3-оксо-2,4-дигидро-3H-1,2,4 триазолил и подобные. В качестве гетероциклильных и гетероарильных групп также указаны кольца и системы колец, содержащие 3-15 атомов, образующие 1-3 кольца."Галоген" относится к фтору, хлору, брому и йоду. Хлор и фтор обычно предпочтительны. Фтор наиболее предпочтителен, если галогены замещены алкильной или алкоксигруппой (например, CF3O иCF3CH2O). Соединения в соответствии с данным изобретением содержат один или более асимметрических центров и могут существовать как рацематы, рацемические смеси, отдельные энантиомеры, диастереомерные смеси и отдельные диастереомеры. В частности, соединения в соответствии с данным изобретением имеют асимметричный центр на стереогенных атомах углерода, обозначенныхв формулах (Ia)(If). Дополнительные асимметричные центры могут присутствовать в зависимости от природы различных заместителей в молекуле. Каждый такой асимметрический центр независимо образует два оптических изомера, и подразумевают, что все возможные оптические изомеры и диастереомеры в смесях и в виде чистых или частично очищенных соединений включены в объем данного изобретения. Данное изо-8 018613 бретение охватывает все такие изомерные формы этих соединений. Некоторые из соединений, описанных здесь, содержат олефиновые двойные связи и, если не указано иначе, включают Е и Z геометрические изомеры. Некоторые из соединений, описанных здесь, могут существовать в виде таутомеров, которые имеют различные точки присоединения водорода, сопровождаемые одним или более смещениями двойной связи. Например, кетон и его енольная форма являются кетоенольными таутомерами. Отдельные таутомеры,а также их смеси включены в соединения в соответствии с данным изобретением. Примеры таутомеров,которые включены в соединения в соответствии с данным изобретением, показаны ниже: Формула (I) показывает структуру класса соединений без предпочтительной стереохимии. Формулы (Ia) и (Ib) показывают предпочтительную стереохимию на стереогенном атоме углерода, к которому присоединены NH2 и Ar группы на тетрагидропирановом кольце. Формулы (Ic) и (Id) показывают предпочтительную стереохимию на стереогенных атомах углерода,к которым присоединены NH2, Ar и V группы на тетрагидропирановом кольце. Независимый синтез этих диастереомеров или их хроматографическое разделение могут быть проведены, как известно в данной области техники, с применением подходящих модификаций описанной здесь методологии. Их абсолютная стереохимия может быть определена рентгеновской кристаллографией кристаллических продуктов или кристаллических промежуточных соединений, которые получены,при необходимости, с реагентом, содержащим асимметрический центр известной абсолютной конфигурации. При желании, рацемические смеси соединений могут быть разделены так, чтобы выделить отдельные энантиомеры. Отделение может проводиться методами, хорошо известными в данной области техники, такими как сочетание рацемической смеси соединений с энантиомерно чистым соединением с получением диастереомерной смеси, с последующим отделением отдельных диастереомеров стандартными методами, такими как фракционная кристаллизация или хроматография. Реакция сочетания часто представляет собой получение солей с применением энантиомерно чистой кислоты или основания. Диастереомерные производные затем могут быть превращены в чистые энантиомеры отщеплением добавленного хирального остатка. Рацемическая смесь соединений также может быть разделена непосредственно методами хроматографии с применением хиральных неподвижных фаз, данные методы хорошо известны в данной области техники. Альтернативно, любой энантиомер соединения может быть получен стереоселективным синтезом с применением оптически чистых исходных материалов или реагентов известной конфигурации методами,известными в данной области техники. В соединениях общей формулы (I) атомы могут демонстрировать их природные изотопные избытки или один или более атомов могут быть искусственно обогащены в конкретный изотоп, имеющий то же атомное число, но атомную массу или массовое число, отличающиеся от атомной массы или массового числа, преимущественно существующих в природе. Данное изобретение включает все подходящие изотопные варианты соединений общей формулы (I). Например, различные изотопные формы водорода (Н) включают протий (1 Н) и дейтерий (2 Н). Протий является преобладающим изотопом водорода в природе. Обогащение до дейтерия может дать определенные терапевтические преимущества, такие как увеличение периода полураспада in vivo или снижение дозирования, или может давать соединения, применяемые в качестве стандарта для идентификации биологических образцов. Обогащенные изотопами соединения общей формулы (I) могут быть получены без ненужного экспериментирования обычными методами, известными специалистам в данной области техники, или методами, аналогичными описанным на схемах и в примерах, представленных здесь, с применением подходящих обогащенных изотопами реагентов и/или промежуточных соединений. Понятно, что в данном описании ссылки на соединения структурной формулы (I) также включают их фармацевтически приемлемые соли, а также соли, которые не являются фармацевтически приемлемыми, когда они применяются в качестве предшественников свободных соединений или их фармацевтически приемлемых солей или в других манипуляциях синтеза. Соединения в соответствии с данным изобретением могут вводиться в форме фармацевтически приемлемой соли. Термин "фармацевтически приемлемая соль" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, включающих неорганические или органические основания и неорганические или органические кислоты. Соли щелочных соединений, попадающих в термин "фармацевтически приемлемая соль", относятся к нетоксичным солям соединений в соответствии с данным изобретением, которые обычно получают взаимодействием свободного основания с подходящей органической или неорганической кислотой. Типовые соли включают, но не ограни-9 018613 чены ими, следующие: ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, камзилат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат,фумарат, глуцептат, глюконат, глутамат, гликоллиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, миндалят, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, аммониевая сольN-метилглюкамина, олеат, оксалат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат. Далее, если соединения в соответствии с данным изобретением имеют кислотную группу,подходящие фармацевтически приемлемые соли включают, но не ограничены ими, соли, полученные из неорганических оснований, включающих алюминий, аммоний, кальций, медь, железо, двухвалентное железо, литий, магний, трехвалентный марганец, двухвалентный марганец, калий, натрий, цинк и подобные. Особенно предпочтительными являются соли аммония, кальция, магния, калия и натрия. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, циклических аминов и щелочных ионообменных смол, таких как аргинин, бетаин, кофеин, холин, N,N-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол,2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин,трометамин и подобные. Также, в случае присутствия группы карбоновой кислоты (-СООН) или спирта в соединениях в соответствии с данным изобретением, могут применяться фармацевтически приемлемые сложные эфиры производных карбоновой кислоты, такие как метил, этил или пивалоилоксиметил, или ацильные производные спиртов, такие как О-ацетил, О-пивалоил, О-бензоил и О-аминоацил. Включены сложные эфиры и ацильные группы, известные в данной области техники для модификации характеристик растворимости или гидролиза, для применения в качестве композиций с замедленным выделением или пролекарств. Сольваты и, в частности, гидраты соединений структурной формулы (I) также включены в данное изобретение. Иллюстрацией изобретения является применение соединений, описанных в примерах и здесь. Обсуждаемые соединения применяют в способе ингибирования фермента дипептидилпептидазы-IV у пациента, такого как млекопитающее, при необходимости такого ингибирования, включающем введение эффективного количества соединения. Данное изобретение относится к применению соединений,описанных здесь, в качестве ингибиторов активности фермента дипептидилпептидазы-IV. В дополнение к приматам, таким как человек, множество других млекопитающих могут быть лечены согласно способу в соответствии с данным изобретением. Например, могут быть лечены млекопитающие, включающие, но не ограниченные ими, коров, овец, коз, лошадей, собак, кошек, морских свинок, крыс или других видов жвачных животных, овечьих, лошадиных, собачьих, кошачьих, грызунов или мышиных. Однако способ также может применяться на практике для других видов, таких как птицы (например, куры). Данное изобретение также относится к способу получения лекарственного средства для ингибирования активности фермента дипептидилпептидазы-IV у человека и животных, включающему объединение соединения в соответствии с данным изобретением с фармацевтически приемлемым носителем или разбавителем. Более конкретно, данное изобретение относится к применению соединения структурной формулы (I) для производства лекарственного средства для применения в лечении состояния, выбранного из группы, включающей гипергликемию, диабет II типа, ожирение и расстройство жировых клеток у млекопитающего, выбранное из группы, включающей дислипидемию, гиперлипидемию, гипертриглицеридемию, гиперхолестеринемию, низкие ЛПВП и высокие ЛПНП. Пациент, подвергающийся лечению способами в соответствии с данным изобретением, представляет собой млекопитающее, предпочтительно человека, мужчину или женщину, у которых желательно ингибирование активности фермента дипептидилпептидазы-IV. Термин "терапевтически эффективное количество" означает количество соединения, которое вызовет биологическую или медицинскую реакцию ткани, системы, животного или человека, которая ожидается исследователем, ветеринаром, врачом или другим клиницистом. Термин "композиция" в данном описании охватывает продукт, содержащий определенные ингредиенты в определенных количествах, а также любой другой продукт, который получается, прямо или косвенно, при сочетании определенных ингредиентов в определенных количествах. Этот термин в отношении фармацевтической композиции охватывает продукт, содержащий активный ингредиент(ы) и инертный ингредиент(ы), которые составляют носитель, а также любой продукт, который получается, прямо или косвенно, при сочетании, комплексообразовании или агрегации любых двух или более ингредиентов, или при отделении одного или более ингредиентов, или при других реакциях или взаимодействиях одного или более ингредиентов. Следовательно, фармацевтические композиции в соответствии с данным изобретением охватывают любые композиции, получаемые смешиванием соединения в соответствии с данным изобретением и фармацевтически приемлемого носителя. Под "фармацевтически приемлемым"- 10018613 подразумевается, что носитель, разбавитель или наполнитель должен быть совместим с другими ингредиентами композиции и не быть вредным для его получателя. Термины "введение" и "вводить" соединение должны пониматься как получение соединения в соответствии с данным изобретением или пролекарства соединения в соответствии с данным изобретением пациентом при необходимости лечения. Применение соединений в соответствии с данным изобретением в качестве ингибиторов активности фермента дипептидилпептидазы-IV может быть продемонстрировано в методиках, определенных ниже. Константы ингибирования определяют следующим образом. Непрерывный флуорометрический анализ проводят на субстрате Gly-Pro-АМС, который расщепляется ДПП-4 с выделением флуоресцентной уходящей группы АМС. Кинетические параметры, которые описывают эту реакцию, следующие:Km=50 мкМ; kcat=75 с-1; kcat/Km=1,5106 М-1 с-1. Типовая реакция содержит приблизительно 50 пМ фермента, 50 мкМ Gly-Pro-AMC и буфер (100 мМ HEPES, рН 7,5, 0,1 мг/мл АБС) в общем реакционном объеме 100 мкл. Высвобождение АМС отслеживается непрерывно во флуорометре с 96-луночным планшетом с применением длины волны возбуждения 360 нм и длиной волны эмиссии 460 нм. В этих условиях приблизительно 0,8 мкМ АМС получают за 30 мин при 25C. Фермент, применяемый в этих исследованиях,является растворимым (трансмембранный домен и цитоплазматическое удлинение исключено) человеческим белком, полученным в системе экспрессии бакуловируса (Вас-То-Вас, Gibco BRL). Было обнаружено, что кинетические константы для гидролиза Gly-Pro-AMC и ГПП-1 соответствуют значениям в литературе для природного фермента. Для измерения константы диссоциации для соединений растворы ингибитора в ДМСО добавляют в реакционные смеси, содержащие фермент и субстрат (конечная концентрация ДМСО составляет 1%). Все эксперименты проводят при комнатной температуре с применением стандартных условий реакции, описанных выше. Для определения констант диссоциации (K1) скорости реакции подгоняют нелинейной регрессией до уравнения Микаэлиса-Ментона для конкурентного ингибирования. Ошибки в воспроизведении констант диссоциации обычно меньше чем двукратные. Соединения структурной формулы (I), особенно соединения из примеров 1-17, показанных ниже,обладают активностью в ингибировании фермента дипептидилпептидазы-IV в указанных выше анализах,обычно с IC50 менее около 1 мкМ и более часто менее 0,1 мкМ. Такие результаты являются показателями свойственной активности соединений в соответствии с данным изобретением при применении в качестве ингибиторов активности фермента дипептидилпептидазы-IV. Фермент дипептидилпептидаза-IV (ДПП-4) является белком поверхности клетки, который вовлечен в широкий спектр биологических функций. Он широко распространен в ткани (кишечник, почки, печень,поджелудочная железа, плацента, вилочковая железа, селезенка, эпителиальные клетки, сосудистый эндотелий, лимфоидные и миелоидные клетки, сыворотка) и имеет отчетливые уровни экспрессии в тканях и клетках. ДПП-4 идентичен маркеру активации T-клеток CD26, и он может расщеплять множество иммунорегулирующих, эндокринных и неврологических пептидов in vitro. Это предполагает потенциальную роль этой пептидазы во множестве болезненных процессов у человека или других видов. Следовательно, целевые соединения применяют в способе предупреждения или лечения следующих заболеваний, расстройств и состояний. Диабет II типа и родственные заболевания. Установлено, что инкретины ГПП-1 и ЖИП быстро инактивируются in vivo ДПП-4. Исследования ДПП-4(-/-)-дефицитных мышей и предварительные клинические испытания показали, что ингибирование ДПП-4 повышает плато концентрации ГПП-1 и ЖИП, что дает улучшенную толерантность к глюкозе. Аналогично ГПП-1 и ЖИП, похоже, что другие пептиды семейства глюкагонов, вовлеченные в регулирование глюкозы, также инактивируются ДПП-4 (например, РАСАР). Инактивация этих пептидов ДПП 4 также может играть роль в гомеостазе глюкозы. Ингибиторы ДПП-4 в соответствии с данным изобретением поэтому применяются в лечении диабета II типа и при лечении и предупреждении множества состояний, которые часто сопровождают диабет II типа, включая синдром X (также известный как метаболический синдром), реактивную гипогликемию и диабетическую дислипидемию. Ожирение, описанное ниже, является другим состоянием, которые часто находят при диабете II типа, которое может реагировать на лечение соединениями в соответствии с данным изобретением. Следующие заболевания, расстройства и состояния связаны с диабетом II типа и поэтому могут лечиться, контролироваться или в некоторых случаях предотвращаться лечением соединениями в соответствии с данным изобретением: (1) гипергликемия, (2) низкая переносимость глюкозы, (3) резистентность к инсулину, (4) ожирение, (5) липидные расстройства, (6) дислипидемия, (7) гиперлипидемия,(8) гипертриглицеридемия, (9) гиперхолестеринемия, (10) низкие уровни ЛПВП, (11) высокие уровни ЛПНП, (12) атеросклероз и его последствия, (13) сосудистый рестеноз, (14) синдром раздраженного кишечника, (15) воспалительное заболевание кишечника, включая болезнь Крона и язвенный колит,(16) другие воспалительные состояния, (17) панкреатит, (18) абдоминальное ожирение, (19) нейродегенеративное заболевание, (20) ретинопатию, (21) нефропатию, (22) невропатию, (23) синдром X,(24) гиперандрогения яичников (синдром поликистозных яичников) и другие расстройства, в которых резистентность к инсулину является компонентом. При синдроме X, также известном как метаболиче- 11018613 ский синдром, считается, что ожирение способствует резистентности к инсулину, диабету, дислипидемии, гипертонии и повышенному риску сердечно-сосудистых заболеваний. Поэтому ингибиторы ДПП-4 также могут применяться для лечения гипертонии, связанной с этим состоянием. Ожирение. Ингибиторы ДПП-4 могут применяться для лечения ожирения. Это основано на наблюдаемом ингибирующем действии ГПП-1 и ГПП-2 на поглощение пищи и опорожнение желудка. Экзогенное введение ГПП-1 у человека значительно снижает поглощение пищи и замедляет опорожнение желудка (Am. J.Physiol., 277:R910-R916 (1999. ICV (интрацеребровентрикулярное) введение ГПП-1 у крыс и мышей также оказывало сильное действие на поглощение пищи (Nature Medicine, 2:1254-1258 (1996. Такое ингибирование питания не наблюдалось у ГПП-1R(-/-)-мышей, что указывает на опосредование этого эффекта через рецепторы ГПП-1 в мозге. По аналогии с ГПП-1, похоже, что ГПП-2 также регулируется ДПП-4. ИЦ введение ГПП-2 также ингибирует поглощение пищи, аналогично действию, наблюдаемому у ГПП-1 (Nature Medicine, 6:802-807 (2000. Кроме того, исследования на мышах с дефицитом ДПП-4 позволяет предположить, что эти животные устойчивы к вызванному питанием ожирению и связанной с ним патологией (например, гиперинсулинемией). Сердечно-сосудистое заболевание. Было показано, что ГПП-1 является благоприятным при введении пациентам после острого инфаркта миокарда, что приводит к улучшению функции левого желудочка и снижению смертности после первичной ангиопластики (Circulation, 109:962-965 (2004. Введение ГПП-1 всегда полезно для лечения дисфункции систолы левого желудочка у собак с дилатационной кардиомиопатией и вызванной ишемией дисфункцией левого желудочка и, таким образом, может оказаться полезным для лечения пациентов с сердечной недостаточностью (US 2004/0097411). Ожидается, что ингибиторы ДПП-4 показывают подобное действие через их способность стабилизировать эндогенную ГПП-1. Дефицит гормона роста. Ингибирование ДПП-4 может быть полезным для лечения дефицита гормона роста, это утверждение основано на гипотезе, что фактор, высвобождающий гормон роста (ФВГР), пептид, который стимулирует выделение гормона роста из передней доли гипофиза, расщепляется ферментом ДПП-4 in vivo(WO 00/56297). Следующие данные являются доказательством того, что ФВГР является эндогенным субстратом: (1) ФВГР эффективно расщепляется in vitro с образованием неактивного продукта ФВГР[3-44](ВВА 1122:147-153 (1992; (2) ФВГР быстро разлагается в плазме до ФВГР[3-44]; это предотвращается ингибитором ДПП-4 дипролином А; и (3) ФВГР[3-44] найден в плазме человеческого ФВГР трансгенных свиней (J. Clin. Invest., 83:1533-1540 (1989. Таким образом, ингибиторы ДПП-4 могут быть полезны для того же спектра показаний, который относят к секретагогам гормона роста. Повреждение кишечника. Потенциальное применение ингибиторов ДПП-4 для лечения повреждения кишечника предполагается на основе результатов исследований, которые показали, что глюкагоноподобный пептид-2 (ГПП-2),подходящий эндогенный субстрат для ДПП-4, может оказывать трофическое действие на эпителий кишечника (Regulatory Peptides, 90:27-32 (2000. Введение ГПП-2 вызывает увеличение массы тонкого кишечника у грызунов, и облегчает повреждение кишечника на моделях колита и энтерита у крыс. Иммунодепрессия. Ингибирование ДПП-4 может быть полезным для модулирования иммунной реакции на основании исследований, в которых фермент ДПП-4 вовлекали в активацию T-клеток и обработку хемокинов, и эффективности ингибиторов ДПП-4 в in vivo моделях заболевания. Было показано, что ДПП-4 идентиченCD26, маркеру поверхности клеток для активированных иммунных клеток. Экспрессия CD26 регулируется статусом дифференциации и активации иммунных клеток. Обычно считают, что CD26 действует в качестве костимулирующей молекулы в in vitro моделях активации T-клеток. Множество хемокинов содержат пролин в предпоследнем положении, предположительно для защиты их от расщепления неспецифическими аминопептидазами. Было показано, что многие из них обрабатываются in vitro ДПП-4. В некоторых случаях (RANTES, LD78-beta, MDC, эотаксин, SDF-1 alpha), расщепление вызывает изменение активности в анализах хемотаксиса и сигнализации. Селективность рецептора также, очевидно, модифицируется в некоторых случаях (RANTES). Множество усеченных на N-конце форм множества хемокинов были идентифицированы в in vitro системах клеточных культур, включая ожидаемые продукты гидролиза ДПП-4. Было показано, что ингибиторы ДПП-4 являются эффективными иммунодепрессантами в животных моделях трансплантации и артрита. Было показано, что продипин (Pro-Pro-дифенилфосфонат), необратимый ингибитор ДПП-4, вдвое увеличивает выживаемость сердечного аллографта у крыс с 7 дня до 14 дня (Transplantation, 63:1495-1500 (1997. Ингибиторы ДПП-4 были тестированы на вызванном коллагеном и алкилдиамином артрите у крыс и показали статистически значимое затухание опухания задней лапы в этой модели [Int. J, Immunopharmacology, 19:15-24 (1997) и Immunopharmacology, 40:21-26(1998)]. ДПП-4 активируется во множестве аутоиммунных заболеваний, включая ревматоидный артрит,рассеянный склероз, болезнь Грейвса и тироидит Хашимото (Immunology Today, 20:367-375 (1999.- 12018613 Инфекция ВИЧ. Ингибирование ДПП-4 может быть полезным для лечения или предупреждения инфекции ВИЧ или СПИД, так как множество хемокинов, которые ингибируют вход клетки ВИЧ, являются потенциальными субстратами для ДПП-4 (Immunology Today, 20:367-375 (1999. В случае SDF-1 альфа расщепление снижает противовирусное действие (PNAS, 95:6331-6 (1998. Таким образом, стабилизация SDF-1 альфа через ингибирование ДПП-4 предположительно снижает инфекционность ВИЧ. Гематопоэз. Ингибирование ДПП-4 может быть полезным для лечения или предупреждения гематопоэза, так как ДПП-4 может быть вовлечен в гематопоэз. Ингибитор ДПП-4, Val-Boro-Pro, стимулирует гематопоэз в мышиной модели нейтропении, вызванной циклофосфамидом (WO 99/56753). Нервные расстройства. Ингибирование ДПП-4 может быть полезным для лечения или предупреждения различных нервных или психиатрических расстройств, так как множество пептидов, вовлеченных в множество нервных процессов, расщепляются in vitro ДПП-4. Таким образом, ингибитор ДПП-4 может обладать терапевтическим действием при лечении нервных расстройств. Было показано, что эндоморфин-2, бета-казоморфин и вещество Р являются in vitro субстратами для ДПП-4. Во всех случаях in vitro расщепление является высокоэффективным при kcat/Km около 106 М-1 с-1 или более. В модели тестирования аналгезии при прыжке вследствие электрического шока у крыс ингибитор ДПП-4 показал значительное действие, которое не зависит от присутствия экзогенного эндоморфина-2 (Brain Research, 815:278-286 (1999. Нейрозащитное и нейрорегенеративное действие ингибиторов ДПП-4 также подтверждается способностью ингибиторов защищать двигательные нейроны от эксайтотоксичной смерти клеток, защищать стриарное возбуждение допаминергических нейронов при введении одновременно с МРТР и способствовать восстановлению плотности стриарного возбуждения при введении в терапевтической манере после лечения МРТР [см.Conf. On Dipeptidyl Aminopeptidases: Basic Science and Clinical Applications, September 26-29, 2002 (Berlin,Germany)]. Тревога. Крысы, от природы имеющие дефицит ДПП-4, имеют анксиолитический фенотип (WO 02/34243;Karl et al., Physiol. Behav. 2003). Мыши с дефицитом ДПП-4 также имеют анксиолитический фенотип с применением порсолта и моделей свет/темнота. Таким образом, ингибиторы ДПП-4 могут быть полезными для лечения тревоги и связанных с ней расстройств. Память и познавательная способность. Агонисты ГПП-1 являются активными в моделях обучения (пассивное избегание, тест водного лабиринта Морриса) и нервного повреждения (вызванный каинатом нервный апоптоз), что продемонстрировано у During et al. (Nature Med. 9:1173-1179 (2003. Результаты позволяют предположить физиологическую роль для ГПП-1 в обучении и нейропротекции. Ожидается, что стабилизация ГПП-1 ингибиторами покажет подобное действие. Инфаркт миокарда. Было показано, что ГПП-1 является полезным при введении пациентам после острого инфаркта миокарда (Circulation, 109:962-965 (2004. Ожидается, что ингибиторы ДПП-4 покажут похожее действие через их способность стабилизировать эндогенную ГПП-1. Инвазия опухоли и метастазы. Ингибирование ДПП-4 может быть полезным при лечении или предупреждении инвазии опухоли и метастазов благодаря повышению или снижению экспрессии некоторых эктопептидаз, включая ДПП-4,которое было замечено при превращении нормальных клеток в злокачественный фенотип (J. Ехр. Med.,190:301-305 (1999. Повышающая или понижающая регуляция этих белков оказалась специфической к типу тканей и клеток. Например, повышенная экспрессия CD26/ДПП-4 наблюдается при лимфоме Tклеток, острой лимфобластной лейкемии T-клеток, вызванной клетками карциноме щитовидной железы,карциномах базальных клеток и карциномах молочной железы. Таким образом, ингибиторы ДПП-4 могут применяться при лечении таких карцином. Доброкачественная гипертрофия простаты. Ингибирование ДПП-4 может быть полезным для лечения доброкачественной гипертрофии простаты, так как повышенная активность ДПП-4 была отмечена в ткани простаты у пациентов с ДГП (Eur. J.Clin. Chem. Clin. Biochem., 30:333-338 (1992. Подвижность спермы/мужская контрацепция. Ингибирование ДПП-4 может быть полезным для изменения подвижности спермы и мужской контрацепции, так как в семенной жидкости, простатосомы, полученной из простаты органеллы, важные для подвижности спермы, имеет очень высокие уровни активности ДПП-4 (Eur. J. Clin. Chem. Clin. Biochem.,30:333-338 (1992.- 13018613 Гингивит. Ингибирование ДПП-4 может быть полезным для лечения гингивита, так как активность ДПП-4 была обнаружена в десневой жидкости, и в некоторых исследованиях коррелируется с тяжестью пародонтита (Arch. Oral Biol. 37:167-173 (1992. Остеопороз. Ингибирование ДПП-4 может быть полезным для лечения или предупреждения остеопороза из-за того, что рецепторы ЖИП присутствуют в остеобластах. Трансплантация стволовых клеток. Было показано, что ингибирование ДПП-4 на донорных стволовых клетках приводит к улучшению стремления к родному микроокружению и приживаемости их в костном мозге и повышению выживаемости у мышей (Christopherson, et al., Science, 305:1000-1003 (2004. Таким образом, ингибиторы ДПП-4 могут быть полезны при трансплантации костного мозга. Соединения в соответствии с данным изобретением применяются при лечении или предупреждении одного или более из следующих состояний или заболеваний: (1) гипергликемия, (2) низкая толерантность к глюкозе, (3) резистентность к инсулину, (4) ожирение, (5) липидные расстройства, (6) дислипидемия, (7) гиперлипидемия, (8) гипертриглицеридемия, (9)гиперхолестеринемия, (10) низкие уровни ЛПВП, (11) высокие уровни ЛПНП, (12) атеросклероз и его последствия, (13) сосудистый рестеноз,(14) синдром раздраженного кишечника, (15) воспалительная болезнь кишечника, включая болезнь Крона и язвенный колит, (16) другие воспалительные состояния, (17) панкреатит, (18) абдоминальное ожирение, (19) нейродегенеративное заболевание, (20) ретинопатия, (21) нефропатия, (22) невропатия,(23) синдром X, (24) гиперандрогенизм яичников (синдром поликистозных яичников), (25) диабет II типа, (26) дефицит гормона роста, (27) нейтропения, (28) нервные расстройства, (29) опухолевые метастазы, (30) доброкачественная гипертрофия простаты, (32) гингивит, (33) гипертония, (34) остеопороз,(35) тревога, (36) дефицит памяти, (37) дефицит познавательной способности, (38) удар, (39) болезнь Альцгеймера и другие состояния, которые могут быть лечены или предотвращены ингибированием ДПП-4. Соединения в соответствии с данным изобретением также применяются в способах предупреждения или лечения указанных выше болезней, расстройств и состояний в сочетании с другими терапевтическими агентами. Соединения в соответствии с данным изобретением могут применяться в сочетании с одним или более другими лекарственными средствами для лечения, предупреждения, подавления или облегчения заболеваний или состояний, для которых могут применяться соединение формулы (I) или другие лекарственные средства, где сочетание лекарственных средств является более безопасным или более эффективным, чем любое лекарственное средство по отдельности. Такие другие лекарственные средства могут вводиться путем и в количествах, обычных для них, одновременно или последовательно с соединением формулы (I). Если соединение формулы (I) используют одновременно с одним или более лекарственными средствами, фармацевтическая композиция в стандартной лекарственной форме, содержащая такие другие лекарственные средства и соединение формулы (I), является предпочтительной, особенно в сочетании с фармацевтически приемлемым носителем. Однако комбинированная терапия также может включать терапии, в которых соединение формулы (I) и одно или более лекарственных средств вводят по различным, пересекающимся, режимам. Также необходимо принять во внимание, что при применении в сочетании с одним или более активными ингредиентами соединения в соответствии с данным изобретением и другие активные ингредиенты могут применяться в более низких дозах, чем каждое из них по отдельности. Следовательно, фармацевтические композиции в соответствии с данным изобретением включают такие, которые содержат один или более активных ингредиентов в дополнение к соединению формулы (I). Если соединение в соответствии с данным изобретением применяют одновременно с одним или более другими лекарственными средствами, фармацевтическая композиция, содержащая такие другие лекарственные средства в дополнение к соединению в соответствии с данным изобретением, предпочтительна. Следовательно, фармацевтические композиции в соответствии с данным изобретением включают такие, которые также содержат один или более активных ингредиентов, в дополнение к соединению в соответствии с данным изобретением. Массовое отношение соединения в соответствии с данным изобретением ко второму активному ингредиенту может варьироваться и зависит от эффективной дозы каждого ингредиента. Обычно применяется эффективная доза каждого ингредиента. Таким образом, если соединение в соответствии с данным изобретением объединяют с другим агентом, массовое отношение соединения в соответствии с данным изобретением к другому агенту обычно составляет от около 1000:1 до около 1:1000, предпочтительно от около 200:1 до около 1:200. Сочетания соединения в соответствии с данным изобретением и других активных соединений обычно попадают в указанные выше интервалы, но в каждом случае необходимо использовать эффективную дозу каждого активного ингредиента. В таких сочетаниях соединение в соответствии с данным изобретением и другие активные агенты могут вводиться отдельно или вместе, кроме того, введение одного элемента может быть до, одновре- 14018613 менно или после введения другого агента. Примеры других активных ингредиентов, которые могут вводиться в сочетании с соединением формулы (I), отдельно или в одной фармацевтической композиции, включают, но не ограничены ими:(1) сенсибилизаторы инсулина, включая (i) агонисты РАПП, такие как глитазоны (например,пиоглитазон, розиглитазон, нетоглитазон, ривоглитазон и балаглитазон) и другие лиганды РАПП, включая (1) двойные агонисты РАПП/, такие как мураглитазар, алеглитазар, соделглитазар и навеглитазар,(2) агонисты РАПП, такие как производные фенофибриновой кислоты (гемфиброзил, клофибрат, ципрофибрат, фенофибрат и безафибрат), (3) селективные модуляторы РАПП (ММРАПП), такие как описаны в WO 02/060388, WO 02/08188, WO 2004/019869, WO 2004/020409, WO 2004/020408 иWO 2004/066963, и (4) частичные агонисты РАПП; (ii) бигуаниды, такие как метформин и его фармацевтически приемлемые соли, в частности гидрохлорид метформина, и композиции с замедленным выделением, такие как Glumetza, Fortamet и GlucophageXR; (iii) ингибиторы протеинтирозинфосфатазы-1 В (ПТФ-1 В);(2) инсулин и аналоги инсулина или производные, такие как инсулин лиспро, инсулин детемир, инсулин гларгин, инсулин глулизин и ингалируемые композиции каждого из них;(5) сульфонилмочевина и не сульфонилмочевинные секретагоги инсулина, такие как толбутамид,глибурид, глипизид, глимепирид, митиглинид и меглитиниды, такие как натеглинид и репаглинид;(7) антагонисты рецептора глюкагона, такие как описаны в WO 98/04528, WO 99/01423,WO 00/39088 и WO 00/69810;(8) миметики инкретина, такие как ГПП-1, аналоги, производные и миметики ГПП-1 (см., например, WO 2008/011446, US 5545618, US 6191102 и US 56583111); и агонисты рецептора ГПП-1, такие как оксинтомодулин и его аналоги и производные (см., например, WO 2003/022304, WO 2006/134340,WO 2007/100535), глюкагон и его аналоги и производные (см., например, WO 2008/101017), экзенатид,лираглутид, таспоглутид, албиглутид, AVE0010, CJC-1134-PC, NN9535, LY2189265, LY2428757 и(9) агенты, понижающие ЛПНП холестерин, такие как (i) ингибиторы HMG-CoA редуктазы (ловастатин, симвастатин, правастатин, церивастатин, флувастатин, аторвастатин, питавастатин и розувастатин), (ii) секвестранты желчной кислоты (такие как холестирамин, колестимид, гидрохлорид колесевелама, колестипол и диалкиламиноалкильные производные поперечно сшитого декстрана,(iii) ингибиторы абсорбции холестерина, такие как эзетимиб, и (iv) ингибиторы ацил CoA:холестерин ацилтрансферазы, такие как авасимиб;(10) лекарственные средства, повышающие ЛПВП, такие как ниацин или его соль и его варианты с замедленным выделением; MK-524 А, которое является сочетанием ниацина с замедленным выделением и антагониста DP-1 МК-524; и агонисты рецептора никотиновой кислоты;(12) агенты, предполагаемые для применения при воспалительных состояниях, такие как аспирин,нестероидные противовоспалительные лекарственные средства (НСПВЛС), глюкокортикоиды и селективные ингибиторы циклооксигеназы-2 (ЦОГ-2);(13) антигипертензивные агенты, такие как ингибиторы АСЕ (такие как эналаприл, лизиноприл, рамиприл, каптоприл, квинаприл и тандолаприл), блокаторы рецептора A-II (такие как лосартан, кандесартан, ирбесартан, олмесартан медоксомил, валсартан, телмисартан и эпросартан), ингибиторы ренина (такие как алискирен), бета-блокаторы (такие как и блокаторы кальциевого канала);(15) ингибиторы 11-гидроксистероидной дегидрогеназы типа 1, такие как описаны в патенте США 6730690; WO 03/104207 и WO 04/058741;(16) ингибиторы транспортного белка холестеринового эфира (ТБХЭ), такие как торцетрапиб и(17) ингибиторы фруктозы 1,6-бисфосфатазы, такие как описаны в патентах США 6054587; 6110903; 6284748; 6399782 и 6489476;(21) антагонисты SSTR3, такие как описаны в WO 2009/011836;(22) агонисты рецептора 1 нейромедина U (NMUR1) и/или рецептора 2 нейромедина U (NMUR2),такие как описаны в WO 2007/109135 и WO 2009/042053, включая, но не ограничиваясь ими, нейромедин(24) антагонисты GPR-105 (P2YR14), такие как описаны в WO 2009/000087;(25) ингибиторы поглощения глюкозы, такие как ингибиторы транспортера натрия-глюкозы(ИТНГ) и его различные изоформы, такие как SGLT-1; SGLT-2, такие как дапаглифлозин и ремоглифлозин; и SGLT-3;(27) ингибиторы синтазы жирной кислоты;(31) агонисты рецептора гистамина Н 3 и(32) агонисты 2-адренергического или 3-адренергического рецептора. Соединения против ожирения, которые могут быть объединены с соединениями формулы (I), включают топирамат; зонисамид; налтрексон; фентермин; бупропион; сочетание бупропиона и налтрексона; сочетание бупропиона и зонисамида; сочетание топирамата и фентермина; фенфлурамин; дексфенфлурамин; сибутрамин; ингибиторы липазы, такие как орлистат и цетилистат; агонисты рецептора меланокортина, в частности агонисты рецептора меланокортина-4; агонисты CCK-1; антагонисты рецептора меланин-концентрирующего гормона (МКГ); антагонисты нейропептида Y1 или Y5 (такие как MK-0557); обратные агонисты и антагонисты рецептора СВ 1 (такие как римонабант и таранабант); агонисты адренергического рецептора 3; антагонисты грелина; агонисты рецептора бомбезина (такие как агонисты подтипа-3 рецептора бомбезина); обратные агонисты рецептора гистамина Н 3; агонисты 5-гидрокситриптамина-2 с (5-ГТ 2 с), такие как лорказерин; и ингибиторы синтазы жирной кислоты(СЖК). Обзор соединений против ожирения, которые могут быть объединены с соединениями в соответствии с данным изобретением, см. в S. Chaki et al., "Recent advances in feeding suppressing agents: potential(2002) и K.М. Gadde, et al., "Combination pharmaceutical therapies for obesity", Exp. Opin. Pharmacother.,10:921-925 (2009). Антагонисты рецептора глюкагона, которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими:N-(4-(1S)-1-[(4-хлорфенил)-(6-хлор-8-метилхинолин-4-ил)метил]бутилбензоил)аланин и их фармацевтически приемлемые соли. Ингибиторы стеароилкоэнзима А дельта-9 десатуразы (SCD), которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими:(5-2-[4-(5-бром-2-хлорфенокси)пиперидин-1-ил]пиримидин-5-ил-2H-тетразол-2-ил)уксусная кислота и их фармацевтически приемлемые соли. Активаторы глюкокиназы, которые могут применяться в сочетании с соединениями формулы (I),включают, но не ограничены ими: 3-(6-этансульфонилпиридин-3-илокси)-5-(2-гидрокси-1-метилэтокси)-N-(1-метил-1 Н-пиразол-3 ил)бензамид; 5-(2-гидрокси-1-метилэтокси)-3-(6-метансульфонилпиридин-3-илокси)-N-(1-метил-1 Н-пиразол-3 ил)бензамид; 5-(1-гидроксиметилпропокси)-3-(6-метансульфонилпиридин-3-илокси)-N-(1-метил-1 Н-пиразол-3- 16018613 ил)бензамид; 3-(6-метансульфонилпиридин-3-илокси)-5-(1-метоксиметилпропокси)-N-(1-метил-1 Н-пиразол-3 ил)бензамид; 5-изопропокси-3-(6-метансульфонилпиридин-3-илокси)-N-(1-метил-1 Н-пиразол-3-ил)бензамид; 5-(2-фтор-1-фторметилэтокси)-3-(6-метансульфонилпиридин-3-илокси)-N-(1-метил-1 Н-пиразол-3 ил)бензамид; 3-(4-[2-(диметиламино)этокси]фенилтио)-N-(3-метил-1,2,4-тиадиазол-5-ил)-6-[(4-метил-4 Н-1,2,4 триазол-3-ил)тио]пиридин-2-карбоксамид; 3-(4-[(1-метилазетидин-3-ил)окси]фенилтио)-N-(3-метил-1,2,4-тиадиазол-5-ил)-6-[(4-метил-4 Н 1,2,4-триазол-3-ил)тио]пиридин-2-карбоксамид;N-(3-метил-1,2,4-тиадиазол-5-ил)-6-[(4-метил-4 Н-1,2,4-триазол-3-ил)тио]-3-[4-(2-пирролидин-1 илэтокси)фенил]тиопиридин-2-карбоксамид; 3-(4-2-[(2R)-2-метилпирролидин-1-ил]этоксифенил)тио-N-(3-метил-1,2,4-тиадиазол-5-ил)-6-[(4 метил-4 Н-1,2,4-триазол-3-ил)тио]пиридин-2-карбоксамид и их фармацевтически приемлемые соли. Агонисты рецептора GPR-119, которые могут применяться в сочетании с соединениями формулы(I), включают, но не ограничены ими: рац-цис-5-хлор-2-4-[2-(2-[5-(метилсульфонил)пиридин-2-ил]оксиэтил)циклопропил]пиперидин 1-илпиримидин; 5-хлор-2-4-[(1R,2S)-2-(2-[5-(метилсульфонил)пиридин-2-ил]оксиэтил)циклопропил]пиперидин 1-илпиримидин; рац-цис-5-хлор-2-[4-(2-2-[4-(метилсульфонил)фенокси]этилциклопропил)пиперидин-1 ил]пиримидин; 5-хлор-2-[4-1S,2R)-2-2-[4-(метилсульфонил)фенокси]этилциклопропил)пиперидин-1 ил]пиримидин; 5-хлор-2-[4-1R,2S)-2-2-[4-(метилсульфонил)фенокси]этилциклопропил)пиперидин-1 ил]пиримидин; рац-цис-5-хлор-2-[4-(2-2-[3-(метилсульфонил)фенокси]этилциклопропил)пиперидин-1 ил]пиримидин; рац-цис-5-хлор-2-[4-(2-2-[3-(5-метил-1,3,4-оксадиазол-2 ил)фенокси]этилциклопропил)пиперидин-1-ил]пиримидин и их фармацевтически приемлемые соли. Селективные модуляторы РАПП (СМРАПП), которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими:(2R)-2-3-[3-(4-хлор)бензоил-2-метил-6-(трифторметокси)-1H-индол-1-ил]феноксипропановая кислота и их фармацевтически приемлемые соли. Ингибиторы 11-гидроксистероидной дегидрогеназы типа 1, которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими: 3-[1-(4-хлорфенил)-транс-3-фторциклобутил]-4,5-дициклопропил-r-4H-1,2,4-триазол; 3-[1-(4-хлорфенил)-транс-3-фторциклобутил]-4-циклопропил-5-(1-метилциклопропил)-r-4H-1,2,4 триазол; 3-[1-(4-хлорфенил)-транс-3-фторциклобутил]-4-метил-5-[2-(трифторметокси)фенил]-r-4H-1,2,4 триазол; 3-[1-(4-хлорфенил)циклобутил]-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол; 3-4-[3-(этилсульфонил)пропил]бицикло[2.2.2]окт-1-ил-4-метил-5-[2-(трифторметил)фенил]-4H1,2,4-триазол;- 17018613 4-метил-3-4-[4-(метилсульфонил)фенил]бицикло[2.2.2]окт-1-ил-5-[2-(трифторметил)фенил]-4H1,2,4-триазол; 3-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3-илбицикло[2.2.2]окт-1-ил)-5-(3,3,3 трифторпропил)-1,2,4-оксадиазол; 3-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3-илбицикло[2.2.2]окт-1-ил)-5-(3,3,3 трифторэтил)-1,2,4-оксадиазол; 5-(3,3-дифторциклобутил)-3-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3 илбицикло[2.2.2]окт-1-ил)-1,2,4-оксадиазол; 5-(1-фтор-1-метилэтил)-3-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3 илбицикло[2.2.2]окт-1-ил)-1,2,4-оксадиазол; 2-(1,1-дифторэтил)-5-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3 илбицикло[2.2.2]окт-1-ил)-1,3,4-оксадиазол; 2-(3,3-дифторциклобутил)-5-(4-4-метил-5-[2-(трифторметил)фенил]-4H-1,2,4-триазол-3 илбицикло[2.2.2]окт-1-ил)-1,3,4-оксадиазол; 5-(1,1-дифторэтил)-3-(4-4-метил-5-[2-(трифторметил)фенил]-4 Н-1,2,4-триазол-3 илбицикло[2.2,2]окт-1-ил)-1,2,4-оксадиазол и их фармацевтически приемлемые соли. Антагонисты рецептора соматостатина подтипа 3 (SSTR3), которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими: и их фармацевтически приемлемые соли.- 18018613 Активаторы АМФ-активированной протеинкиназы (АМФК), которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими: и их фармацевтически приемлемые соли. Ингибиторы ацетил-CoA карбоксилазы-1 и 2 (АСС-1 и АСС-2), которые могут применяться в сочетании с соединениями формулы (I), включают, но не ограничены ими: 3-1'-[(1-циклопропил-4-метокси-1 Н-индол-6-ил)карбонил]-4-оксоспиро[хроман-2,4'-пиперидин]-6 илбензойная кислота; 5-1'-[(1-циклопропил-4-метокси-1 Н-индол-6-ил)карбонил]-4-оксоспиро[хроман-2,4'-пиперидин]-6 илникотиновая кислота; 1'-[(1-циклопропил-4-метокси-1 Н-индол-6-ил)карбонил]-6-(1 Н-тетразол-5-ил)спиро[хроман-2,4'пиперидин]-4-он; 1'-[(1-циклопропил-4-этокси-3-метил-1 Н-индол-6-ил)карбонил]-6-(1 Н-тетразол-5-ил)спиро[хроман 2,4'-пиперидин]-4-он; 5-1'-[(1-циклопропил-4-метокси-3-метил-1 Н-индол-6-ил)карбонил]-4-оксоспиро[хроман-2,4'пиперидин]-6-илникотиновая кислота; 4'-(6-(5-карбамоилпиридин-2-ил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'-илкарбонил)-2',6'диэтоксибифенил-4-карбоновая кислота; 2',6'-диэтокси-4'-[6-(1-метил-1 Н-пиразол-4-ил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'ил]карбонилбифенил-4-карбоновая кислота; 2',6'-диэтокси-3-фтор-4'-[6-(1-метил-1 Н-пиразол-4-ил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'ил]карбонилбифенил-4-карбоновая кислота; 5-[4-(6-(3-карбамоилфенил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'-илкарбонил)-2,6 диэтоксифенил]никотиновая кислота; натрия 4'-(6-(5-карбамоилпиридин-2-ил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'-илкарбонил)2',6'-диэтоксибифенил-4-карбоксилат; метил 4'-(6-(5-карбамоилпиридин-2-ил)-4-оксоспиро[хроман-2,4'-пиперидин]-1'-илкарбонил)-2',6'диэтоксибифенил-4-карбоксилат;- 19018613 1'-[(4,8-диметоксихинолин-2-ил)карбонил]-6-(1 Н-тетразол-5-ил)спиро[хроман-2,4'-пиперидин]-4-он; пивалат (5-1'-[(4,8-диметоксихинолин-2-ил)карбонил]-4-оксоспиро[хроман-2,4'-пиперидин]-6-ил 2 Н-тетразол-2-ил)метила; 5-1'-[(8-циклопропил-4-метоксихинолин-2-ил)карбонил]-4-оксоспиро[хроман-2,4'-пиперидин]-6 илникотиновая кислота; 1'-(8-метокси-4-морфолин-4-ил-2-нафтоил)-6-(1 Н-тетразол-5-ил)спиро[хроман-2,4'-пиперидин]-4 он; 1'-[(4-этокси-8-этилхинолин-2-ил)карбонил]-6-(1 Н-тетразол-5-ил)спиро[хроман-2,4'-пиперидин]-4 он и их фармацевтически приемлемые соли и сложные эфиры. Соединения в соответствии с данным изобретением могут вводиться перорально, парентерально(например, внутримышечная, внутрибрюшинная, внутривенная, ICV, внутрикишечная инъекция или инфузия, подкожная инъекция или имплантат), ингаляцией, назально, вагинально, ректально, подъязычно или местно и могут быть составлены, по отдельности или вместе, в подходящие лекарственные формы,содержащие обычные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители,подходящие для каждого способа введения. В дополнение к лечению теплокровных животных, таких как мыши, крысы, лошади, домашний скот, овцы, собаки, кошки, обезьяны и т.д., соединения в соответствии с данным изобретением являются эффективными для применения у человека. Фармацевтические композиции для введения соединений в соответствии с данным изобретением обычно могут быть представлены в стандартной лекарственной форме и могут быть получены любыми методами, известными в области фармацевтики. Все способы включают стадию соединения активного ингредиента с носителем, который составляет один или более вспомогательных ингредиентов. В общем,фармацевтические композиции получают однородным и тщательным смешиванием активного ингредиента с жидким носителем или тонкоизмельченным твердым носителем, или обоими, и затем, при необходимости, приданием желаемой формы продукту. В фармацевтической композиции активное рассматриваемое соединение находится в количестве, достаточном для получения желаемого эффекта в отношении способа или состояния заболеваний. В данном описании термин "композиция" охватывает продукт, содержащий определенные ингредиенты в определенных количествах, а также любой продукт, который получается, прямо или косвенно, при сочетании определенных ингредиентов в определенных количествах. Фармацевтические композиции, содержащие активный ингредиент, могут быть в форме, подходящей для перорального введения, например в виде таблеток, пастилок, драже, водных или масляных суспензий, диспергируемых порошков или гранул, эмульсий, твердых или мягких капсул, или сиропов, или эликсиров. Композиции, предназначенные для перорального введения, могут быть получены любым методом, известным в области получения фармацевтических композиций, и такие композиции могут содержать один или более агентов, выбранных из группы, включающей подсластители, вкусовые добавки,красители и консерванты для получения фармацевтически привлекательных препаратов с приятным вкусом. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми наполнителями, которые подходят для получения таблеток. Этими наполнителями могут быть, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующие и разрыхляющие агенты, например кукурузный крахмал или альгиновая кислота; связующие агенты, например крахмал, желатин или аравийская камедь, и смазывающие агенты,например стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без оболочки или могут быть покрыты оболочкой с применением известных методов для замедления разложения и абсорбции в желудочно-кишечном тракте, тем самым обеспечивая замедленное действие в течение длительного периода. Например, может применяться замедляющий материал, такой как моностеарат глицерила или дистеарат глицерила. Они также могут быть покрыты с применением методик, описанных в патентах США 4256108; 4166452 и 4265874, с получением осмотических терапевтических таблеток для контроля выделения. Составы для перорального применения также могут быть представлены в виде твердых желатиновых капсул, где активный ингредиент смешивают с инертным твердым разбавителем, например карбонатом кальция, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, где активный ингредиент смешивают с водной или масляной средой, например арахисовым маслом, жидким парафином или оливковым маслом. Водные суспензии содержат активные материалы в смеси с наполнителями, подходящими для производства водных суспензий. Такими наполнителями являются суспендирующие агенты, например карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакант и аравийская камедь; дисперигрующими или смачивающими агентами могут быть природный фосфатид, например лецитин, или продукты конденсации оксида алкилена с жирными кислотами, например стеарат полиоксиэтилена, или продукты конденсации оксида этилена с длинноцепочечными алифатическими спиртами, например гептадекаэтиленоксиэтанолом, или продукты конденсации оксида этилена с неполными эфирами, полученными из жирных кислот и гексита, такие как- 20018613 моноолеат полиоксиэтиленсорбита, или продукты конденсации оксида этилена с неполными сложными эфирами, полученными из жирных кислот и ангидридов гексита, например моноолеат полиэтиленсорбитана. Водные суспензии также могут содержать один или более консервантов, например этил или н-пропил п-гидроксибензоат, один или более красителей, одну или более вкусовых добавок и один или более подсластителей, таких как сахароза или сахарин. Масляные суспензии могут быть составлены суспендированием активного ингредиента в растительном масле, например арахисовом, оливковом, кунжутном или кокосовом масле, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загущающий агент, например пчелиный воск, твердый парафин или цетиловый спирт. Подсластители, такие как указаны выше, и вкусовые добавки могут быть добавлены для получения перорального препарата с приятным вкусом. Эти композиции могут быть законсервированы добавлением антиоксиданта, такого как аскорбиновая кислота. Диспергируемые порошки и гранулы подходят для получения водных суспензий добавлением воды с получением активного ингредиента в смеси с диспергирующим или смачивающим агентом, суспендирующим агентом и одним или более консервантами. Подходящие диспергирующие или смачивающие агенты представлены теми, которые указаны выше. Дополнительные наполнители, например подсластители, вкусовые добавки и красители, также могут присутствовать. Фармацевтические композиции в соответствии с данным изобретением также могут быть в виде эмульсий масло-в-воде. Масляной фазой может быть растительное масло, например оливковое масло или арахисовое масло, или минеральное масло, например жидкий парафин, или их смеси. Подходящими эмульгирующими агентами могут быть природные камеди, например аравийская камедь или трагакант,природные фосфатиды, например соя, лецитин, и сложные эфиры или неполные сложные эфиры, полученные из жирных кислот и ангидридов гексита, например моноолеат сорбитана, и продукты конденсации указанных неполных сложных эфиров с оксидом этилена, например моноолеат полиоксиэтиленсорбитана. Эмульсии также могут содержать подсластители и вкусовые добавки. Сиропы и эликсиры также могут быть составлены с подсластителями, например глицерином, пропиленгликолем, сорбитом или сахарозой. Такие композиции также могут содержать смягчающие средства, консервант и красители. Фармацевтические композиции могут быть в виде стерильных водной или масляной суспензий. Эта суспензия может быть составлена методами известного уровня техники с применением подходящих диспергирующих или смачивающих агентов, которые указаны выше. Стерильный препарат для инъекций также может быть стерильным раствором или суспензией для инъекций в нетоксичном парентерально приемлемом разбавителе или растворителе, например в виде раствора в 1,3-бутандиоле. К приемлемым носителям и растворителям, которые могут применяться, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно применяют в качестве растворителя или суспендирующей среды. Для этой цели может применяться любое легкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, применяются для получения препаратов для инъекций. Соединения в соответствии с данным изобретением также могут вводиться в виде суппозиториев для ректального введения лекарственного средства. Эти композиции могут быть получены смешиванием лекарственного средства с подходящим нераздражающим наполнителем, который является твердым при обычных температурах, но жидким при ректальной температуре, и поэтому плавится в анальном отверстии для выделения лекарственного средства. Такие материалы включают масло какао и полиэтиленгликоли. Для местного введения применяют кремы, мази, желе, растворы или суспензии и т.д., содержащие соединения в соответствии с данным изобретением. (Для целей данного изобретения местное введение включает полоскания для рта и полоскания для горла). Фармацевтическая композиция и способ в соответствии с данным изобретением могут также включать другие терапевтически активные соединения, указанные здесь, которые обычно применяют при лечении указанных выше патологических состояний. При лечении или предупреждении состояний, которые требуют ингибирования активности фермента дипептидилпептидазы-IV, подходящая доза обычно составляет от около 0,01 до 500 мг/кг массы тела пациента в сутки и может вводиться однократно или многократно. Предпочтительно доза составляет от около 0,1 до около 250 мг/кг в сутки; более предпочтительно от около 0,5 до около 100 мг/кг в сутки. Подходящая доза может быть от около 0,01 до 250 мг/кг в сутки, от около 0,05 до 100 мг/кг в сутки или от около 0,1 до 50 мг/кг в сутки. В этом интервале доза может составлять от 0,05 до 0,5,от 0,5 до 5 или от 5 до 50 мг/кг в сутки. Для перорального введения композиции обычно представлены в виде таблеток, содержащих от 1,0 до 1000 мг активного ингредиента, особенно 1, 5, 10, 15, 20, 25, 50, 75,100, 150, 200, 250, 300, 400, 500, 600, 750, 800, 900 и 1000 мг активного ингредиента для симптоматического доведения дозы для конкретного лечимого пациента. Соединения могут вводиться в режиме от 1 до 4 раз в сутки, предпочтительно 1 или 2 раза в сутки.- 21018613 При лечении или предупреждении сахарного диабета и/или гипергликемии или гипертриглицеридемии или других заболеваний, для которых показаны соединения в соответствии с данным изобретением, обычно удовлетворительные результаты достигаются при суточном введении от около 0,1 до около 100 мг/кг массы тела животного, предпочтительно в виде однократной суточной дозы или от 2 до 6 раз в сутки или в форме с замедленным выделением. Для больших млекопитающих общая суточная доза составляет от около 1 до около 1000 мг, предпочтительно от около 1 до около 50 мг. Для взрослого человека весом 70 кг общая суточная доза обычно составляет от около 7 до около 350 мг. Такой режим введения может быть скорректирован для получения оптимального терапевтического ответа. Должно быть понятно, однако, что конкретный уровень и частота введения для конкретного пациента будут варьироваться и зависят от множества факторов, включая активность конкретного применяемого соединения, метаболическую стабильность и срок действия этого соединения, возраст, массу тела,общее состояние здоровья, пол, режим питания, способ и время введения, скорость выведения, сочетание лекарственных средств, тяжесть конкретного состояния и терапии, которую проходит пациент. Способы синтеза соединений в соответствии с данным изобретением иллюстрированы на представленных ниже схемах и в примерах. Исходные материалы коммерчески доступны или могут быть получены методами, известными в данной области техники или показанными ниже. Соединения в соответствии с данным изобретением могут быть получены из промежуточных соединений, таких как соединения формулы (II) и (III), с применением стандартных условий восстановительного аминирования с последующим снятием защиты: где Ar и V такие, как определены выше; и Р является подходящей защитной группой для азота, такой как трет-бутоксикарбонил (Boc), бензилоксикарбонил (Cbz) или 9-флуоренилметоксикарбонил (Fmoc). Получение этих промежуточных соединений описано на представленных ниже схемах. Схема 1 Промежуточные соединения формулы (II) известны в литератуте или могут быть получены множеством способов, знакомых специалистам в данной области техники. Один из обычных методов показан на схеме 1. Замещенный бензоилгалогенид 1 обрабатывают фенолом в присутствии основания, такого как N,N-диизопропилэтиламин с получением сложного эфира 2. Обработка соединения 2 анионом, полученным из нитрометана с применением гидрида натрия, дает нитрокетон 3. Альтернативно, нитрокетон 3 может быть получен взаимодействием альдегида 1 а с нитрометаном в присутствии основания и окислением полученного нитроспирта 1b окисляющим агентом, таким как реагент Джонса. Нагревание нитрокетона 3 с 3-йодо-2-(йодметил)проп-1-еном дает пиран 4, который, при восстановлении с боргидридом натрия и изомеризацией с основанием, таким как 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ), дает транспиран 5. Энантиомеры 5 могут быть отделены на этой стадии различными методами, известными спе- 22018613 циалистам в данной области техники. Обычно рацемат может быть разделен ВЭЖХ с применением хиральной колонки. Нитрозамещенный пиран 5 затем восстанавливают, например, с применением цинка и кислоты, такой как хлористо-водородная кислота, и полученный амин 6 защищают, например, в виде Boc производного, обработкой ди-трет-бутилдикарбонатом с получением соединения 7. Обработка соединения 7 тетроксидом осмия и N-оксидом N-метилморфолина дает диол 8, который при обработке периодатом натрия дает промежуточный пиранон IIa. Схема 2 Промежуточные соединения формулы (III) известны в литературе или могут быть получены множеством способов, известных специалистам в данной области техники. Один способ получения тетрагидропирролопиразола IIIa показан на схеме 2. Тритил- или Boc-защищенный пирролидинол 9 может быть окислен множеством способов, таких как методика Сверна, обычно известных специалистам в данной области техники, с получением кетона 10, который при обработке и нагревании сN,N-диметилформамидом-диметилацеталем (ДМФ-ДМА) дает соединение 11. Желаемое промежуточное соединение IIIa затем может быть легко получено нагреванием раствора соединения 11 с гидразином 12 в подходящем растворителе, таком как этанол, необязательно в присутствии основания, такого как этоксид натрия, с последующим удалением защитной группы кислотой. Схема 3 Как показано на схеме 3, соединения в соответствии с данным изобретением структурной формулы(I) могут быть получены восстановительным аминированием промежуточного соединения II в присутствии промежуточного соединения III с применением реагентов, таких как цианоборгидрид натрия, декаборан или триацетоксиборгидрид натрия, в растворителях, таких как дихлорметан, тетрагидрофуран или метанол, с получением промежуточного соединения IV. Реакцию проводят необязательно в присутствии кислоты Льюиса, такой как тетрахлорид титана или тетраизопропоксид титана. Реакция также может быть усилена добавлением кислоты, такой как уксусная кислота. В некоторых случаях промежуточное соединение III может быть солью, такой как соль хлористо-водородной кислоты или соль трифторуксусной кислоты, и в этих случаях к реакционной смеси обычно добавляют основание, обычноN,N-диизопропилэтиламин. Защитную группу затем удаляют с применением, например, трифторуксусной кислоты или метанольного гидрохлорида для Boc или палладия на угле и газообразного водорода для Cbz с получением желаемого амина I. Продукт очищают, при необходимости, перекристаллизацией,растиранием, препаративной тонкослойной хроматографией, флэш-хроматографией на силикагеле, такой как на аппарате Biotage, или ВЭЖХ. Соединения, которые очищены ВЭЖХ, могут быть выделены как соответствующая соль. В некоторых случаях продукт I или синтетические промежуточные соединения, показанные на схемах выше, могут быть далее модифицированы, например, манипуляциями заместителей на Ar или V. Эти манипуляции могут включать, но не ограничены ими, восстановление, окисление, алкилирование, ацилирование и гидролиз, которые обычно известны специалистам в данной области техники. В некоторых случаях порядок проведения стадий на представленных выше схемах может быть изменен для усиления реакции или чтобы избежать нежелательных продуктов реакции. Соединения структурной формулы (I) в соответствии с данным изобретением могут быть получены методами, описанными на представленных схемах и в примерах, с применением подходящих материалов, и далее представлены конкретными примерами. Соединения, показанные в примерах, однако, не- 23018613 должны рассматриваться как единственные, считающиеся изобретением. Примеры иллюстрируют детали получения соединения в соответствии с данным изобретением. Специалист в данной области техники легко поймет, что известные вариации условий и процессов представленных ниже методик получения могут применяться для получения этих соединений. Представленные соединения обычно выделяют в виде их фармацевтически приемлемых солей, таких как описаны выше. Свободные аминовые основания,соответствующие выделенным солям, могут быть получены нейтрализацией с подходящим основанием,таким как водный гидрокарбонат натрия, карбонат натрия, гидроксид натрия и гидроксид калия, и экстрагированием выделенного аминового свободного основания в органический растворитель с последующим выпариванием. Аминовое свободное основание, выделенное таким образом, может быть далее превращено в другую фармацевтически приемлемую соль растворением в органическом растворителе с последующим добавлением подходящей кислоты, с последующим выпариванием, осаждением или кристаллизацией. Все температуры даны в C, если не указано иначе. Масс-спектр (МС) измерен ионмассовой спектроскопией с электронным распылением. Далее представлен список аббревиатур, применяемых в описании синтеза промежуточных соединений и примеров ниже. Список аббревиатур:Na2SO4 = сульфат натрия; ЯМР = спектроскопия ядерного магнитного резонанса; ЗГ = защитная группа;Ph = фенил; Кт или КТ = комнатная температура; с = синглет; т = триплет; ТФК = трифторуксусная кислота; ТГФ = тетрагидрофуран. Промежуточное соединение 1. трет-Бутил [(2R,3S)-5-оксо-2-(2,4,5-трифторфенил)тетрагидро-2 Нпиран-3-ил]карбамат Стадия А. Фенил 2,4,5-трифторбензоат. Раствор фенола (13,3 г, 141 ммоль) в сухом дихлорметане (370 мл) охлаждают на ледяной бане и обрабатывают N,N-диизопропилэтиламином (34 мл, 193 ммоль) с последующим добавлением по каплям хлорида 2,4,5-трифторбензоила (25 г, 129 ммоль) в течение 15 мин. Ледяную баню удаляют, перемешивание продолжают в течение 2 ч при комнатной температуре, раствор затем переносят в делительную воронку и органический слой промывают последовательно раствором хлористо-водородной кислоты(2 н., 150 мл), насыщенным водным раствором бикарбоната натрия (150 мл) и насыщенным раствором соли (150 мл), сушат над безводным сульфатом натрия, фильтруют, выпаривают и полученный твердый- 24018613 продукт очищают на силикагеле порциями, элюируя последовательно гексаном и затем 0-5% простым эфиром в гексане с градиентом с получением фенил 2,4,5-трифторбензоата в виде твердого вещества белого цвета. Стадия В. 2-Нитро-1-(2,4,5-трифторфенил)этанон. Гидрид натрия (12 г, 60% в масле, 297 ммоль) промывают гексаном (4100 мл), промывают безводным азотом, суспендируют в N,N-диметилформамиде (350 мл) и затем обрабатывают нитрометаном(44 мл, 81 ммоль). Полученную смесь перемешивают при комнатной температуре в течение 2,5 ч, охлаждают до 0 С и затем обрабатывают раствором фенил 2,4,5-трифторбензоата (22,8 г, 90,0 ммоль) вN,N-диметилформамиде (180 мл) в течение 2 ч. Реакционную смесь хранят при той же температуре в течение ночи и перемешивание продолжают в течение еще 1 ч при комнатной температуре. Смесь выливают на лед (400 г) с концентрированной хлористо-водородной кислотой (48 мл). Водную смесь экстрагируют этилацетатом (3250 мл). Объединенные органические слои промывают насыщенным раствором соли (40 мл), сушат над безводным сульфатом натрия, фильтруют и выпаривают при пониженном давлении. Неочищенный продукт растворяют в простом эфире - гексане (1:1, 240 мл) и воде (200 мл). Органический слой отделяют и кристаллы, которые формируются при выстаивании и охлаждении в холодильнике, отделяют фильтрацией и сушат с получением 2-нитро-1-(2,4,5-трифторфенил)этанона в виде твердого вещества не совсем белого цвета. Стадия С. 3-Метилен-5-нитро-6-(2,4,5-трифторфенил)-3,4-дигидро-2H-пиран. Смесь 3-хлор-2-(хлорметил)проп-1-ена (1,0 г, 8 ммоль) и йодида натрия (6,6 г, 44 ммоль) в ацетоне(60 мл) перемешивают при комнатной температуре в течение 20 ч, выпаривают при пониженном давлении и растворяют в дихлорметане (150 мл) и воде (50 мл). Органический слой сушат над сульфатом натрия, фильтруют и выпаривают с получением 3-йод-2-(йодметил)проп-1-ена в виде красноватого масла(2,45 г). N,N-Диизопропилэтиламин (0,20 мл) добавляют к раствору нитро-1-(2,4,5 трифторфенил)этанона (110 мг, 0,5 ммоль) в N,N-диметилформамиде (3 мл) и 3-йод-2-(йодметил)проп-1 ена (170 мг, 0,55 ммоль) и смесь нагревают при 60 С в течение 2,5 ч, выпаривают и очищают хроматографией на системе Biotage Horizon (двуокись кремния, градиент 0-30% дихлорметан в гексане) с получением 3-метилен-5-нитро-6-(2,4,5-трифторфенил)-3,4-дигидро-2H-пирана. Стадия D. (2R,3S)-5-Метилен-3-нитро-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран. К раствору 3-метилен-5-нитро-6-(2,4,5-трифторфенил)-3,4-дигидро-2H-пирана (798 мг, 2,94 ммоль) в хлороформе (42 мл) и изопропиловом спирте (7,8 мл) добавляют силикагель (5,1 г) и боргидрид натрия(420 мг, 11,1 ммоль) и реакционную смесь перемешивают в течение 30 мин при комнатной температуре. Затем реакционную смесь гасят добавлением по каплям хлористо-водородной кислоты (6 мл, 2 н.) и фильтруют. Полученный остаток промывают этилацетатом (100 мл). Объединенный фильтрат промывают последовательно насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли, сушат над безводным сульфатом натрия и выпаривают. Полученное янтарное масло (802 мг) растворяют в тетрагидрофуране (15 мл) и добавляют 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ, 40 мкл). Раствор перемешивают в течение 105 мин и затем переносят в делительную воронку, содержащую этилацетат(100 мл) и 1 н. хлористо-водородную кислоту (50 мл). Органический слой промывают насыщенным раствором соли и водный слой экстрагируют этилацетатом. Объединенный органический слой сушат над безводным сульфатом натрия, фильтруют и выпаривают с получением неочищенного продукта, который очищают флэш-хроматографией (двуокись кремния, 8-10% простой эфир в гексане) с получением транс 5-метилен-3-нитро-2-(2,4,5-трифторфенил)тетрагидро-2H-пирана. Часть этого продукта (388 мг) разделяют ВЭЖХ (ChiralCel OD, 1,5% изопропилового спирта в гептане) с получением более медленно двигающегося энантиомера, (2R,3S)-5-метилен-3-нитро-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пирана. Стадия Е. (2R,3S)-5-Метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3-амин. К энергично перемешиваемой суспензии(2R,3S)-5-метилен-3-нитро-2-(2,4,5 трифторфенил)тетрагидро-2 Н-пирана (200 мг, 0,73 ммоль) и порошка цинка (561 мг, 8,59 ммоль) в этаноле (7 мл) добавляют 6 н. хлористо-водородную кислоту (2,3 мл, 14 ммоль). Через 1 ч смесь обрабатывают простым эфиром (100 мл) и водным раствором гидроксида натрия (2,5 н., 40 мл). Органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом натрия и выпаривают с получением (2R,3S)-5-метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3-амина, который применяют на следующей стадии без дальнейшей очистки. Стадия[(2R,3S)-5-метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3 ил]карбамат. К раствору (2R,3S)-5-метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3-амина (177 мг,0,73 ммоль) в дихлорметане (5 мл) добавляют ди-трет-бутилдикарбонат (239 мг, 1,1 ммоль) и смесь перемешивают в течение 2,5 ч при комнатной температуре. Раствор выпаривают при пониженном давлении с получением трет-бутил[(2R,3S)-5-метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3 ил]карбамата в виде белого твердого вещества. Его применяют на следующей стадии без дальнейшей очистки.[(2R,3S)-5-метилен-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3 ил]карбамата (203 мг, 0,59 ммоль) в трет-бутиловом спирте (6 мл), ацетоне (3 мл) и воде (1,5 мл) добавляют тетроксид осмия (0,113 мл 2,5% раствора в трет-бутиловом спирте, 0,009 ммоль). Полученную смесь перемешивают при комнатной температуре в течение 10 мин и затем обрабатывают N-оксидомN-метилморфолина (92 мг, 0,79 ммоль) и перемешивают. Через два дня реакционную смесь обрабатывают водным раствором бисульфита натрия (5 мл, 2,0 н.) и затем через 10 мин этилацетатом. Органический слой промывают последовательно 2 н. хлористо-водородной кислотой и насыщенным водным раствором бикарбоната натрия, сушат над безводным сульфатом натрия, фильтруют и выпаривают с получением трет-бутил[(2R,3S)-5-гидрокси-5-(гидроксиметил)-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3 ил]карбамата, который применяют на следующей стадии без дальнейшей очистки. Стадия Н. трет-Бутил [(2R,3S)-5-оксо-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3-ил]карбамат. К раствору трет-бутил [(2R,3S)-5-гидрокси-5-(гидроксиметил)-2-(2,4,5-трифторфенил)тетрагидро 2 Н-пиран-3-ил]карбамата (223 мг, 0,59 ммоль) в тетрагидрофуране (4 мл) добавляют раствор периодата натрия (143 мг, 0,67 ммоль) в воде (1,3 мл) и смесь перемешивают в течение 3 ч. Смесь концентрируют и очищают флэш-хроматографией (двуокись кремния, градиент 5-20% этилацетат в хлороформе) с получением трет-бутил [(2R,3S)-5-оксо-2-(2,4,5-трифторфенил)тетрагидро-2 Н-пиран-3-ил]карбамата в виде твердого вещества белого цвета. Промежуточное соединение 2. трет-Бутил [(2R,3S)-5-оксо-2-(2,5-дифторфенил)тетрагидро-2 Нпиран-3-ил]карбамат Стадия А. 1-(2,5-Дифторфенил)-2-нитроэтанол. К гидроксиду натрия (1 н., 3 л) и метанолу (1500 мл) при 5 С добавляют раствор 2,5-дифторбензальдегида (350 г, 2,46 моль) и нитрометана (157 мл, 2,9 моль) в метаноле (350 мл) по каплям в течение 1 ч. Реакционную смесь затем нейтрализуют ледяной уксусной кислотой (165 мл). Добавляют диэтиловый эфир (1500 мл) и слои разделяют. Органический слой промывают последовательно насыщенным водным раствором карбоната натрия (1000 мл) и насыщенным водным раствором соли(1000 мл). Органический слой сушат над безводным сульфатом магния, фильтруют и концентрируют с получением 1-(2,5-дифторфенил)-2-нитроэтанола, который применяют без дальнейшей очистки на стадии В. Стадия В. 2-Нитро-1-(2,5-дифторфенил)этанон. Раствор периодинана Десса-Мартина (125 г) в дихлорметане (600 мл) добавляют к раствору нитроспирта, полученного на стадии А (46,3 г), при 10 С в течение 30 мин. Перемешивание продолжают в течение 2 ч и реакционную смесь затем выливают в смесь бикарбоната натрия (300 г) и тиосульфата натрия(333 г) в воде (3 л). Полученный продукт экстрагируют метил трет-бутиловым эфиром (МТБЭ) (2 л). Водный слой нейтрализуют HCl (2 н., 1,5 л) и экстрагируют МТБЭ (3 л). Объединенные органические слои сушат над безводным сульфатом магния, фильтруют, выпаривают и остаток очищают хроматографией (силикагель, элюируют дихлорметаном) с получением желаемого нитрокетона. Стадия С. 3-Йод-2-(йодметил)проп-1-ен. Смесь 3-хлор-2-(хлорметил)проп-1-ена (1,0 г, 8 ммоль) и йодида натрия (6,6 г, 44 ммоль) в ацетоне(60 мл) перемешивают при комнатной температуре в течение 20 ч, выпаривают при пониженном давлении и разделяют между дихлорметаном (150 мл) и водой (50 мл). Органический слой сушат над сульфатом натрия, фильтруют и выпаривают с получением 3-йод-2-(йодметил)проп-1-ена в виде красноватого масла. Стадия D. 3-Метилен-5-нитро-6-(2,5-дифторфенил)-3,4-дигидро-2 Н-пиран.(92,7 г, 461 ммоль) в N,N-диметилформамиде (1000 мл) и 3-йод-2-(йодметил)проп-1-ена (156 г,507 ммоль). Смесь нагревают при 60 С в течение 2 ч, выпаривают и очищают хроматографией (силикагель, градиент 0-30% дихлорметан в гексане) с получением 3-метилен-5-нитро-6-(2,5-дифторфенил)-3,4 дигидро-2 Н-пирана. Стадия Е. (2R,3S)-5-Метилен-3-нитро-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран. Это соединение получают по методике, описанной для промежуточного соединения 1, стадия D, с применением 3-метилен-5-нитро-6-(2,5-трифторфенил)-3,4-дигидро-2 Н-пирана. Стадия F. (2R,3S)-5-Метилен-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3-амин. Это соединение получают по методике, описанной для промежуточного соединения 1, стадия Е, с применением (2R,3S)-5-метилен-3-нитро-2-(2,5-дифторфенил)тетрагидро-2 Н-пирана.- 26018613 Стадия G. трет-Бутил [(2R,3S)-5-метилен-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3-ил]карбамат. Это соединение получают по методике, описанной для промежуточного соединения 1, стадия F, с применением (2R,3S)-5-метилен-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3-амина. Стадия Н. трет-Бутил [(2R,3S)-5-гидрокси-5-(гидроксиметил)-2-(2,5-дифторфенил)тетрагидро-2 Нпиран-3-ил]карбамат. Это соединение получают по методике, описанной для промежуточного соединения 1, стадия G, с применением трет-бутил [(2R,3S)-5-метилен-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3-ил]карбамата. Стадия I. трет-Бутил [(2R,3S)-5-оксо-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3-ил]карбамат. К раствору трет-бутил [(2R,3S)-5-гидрокси-5-(гидроксиметил)-2-(2,5-трифторфенил)тетрагидро-2 Нпиран-3-ил]карбамата (10,5 г) в метаноле (100 мл) при 0 С добавляют пиридин (7,8 мл) и тетраацетат свинца (21,7 г). Реакционную смесь перемешивают в течение 20 мин. Водная обработка этилацетатом дает неочищенный продукт, который очищают хроматографией (двуокись кремния, 0-50% этилацетат/гептан) с получением трет-бутил [(2R,3S)-5-оксо-2-(2,5-дифторфенил)тетрагидро-2 Н-пиран-3 ил]карбамата в виде твердого вещества белого цвета. Промежуточное соединение 3(267 г, 2241 ммоль) и нагревают при 105 С в течение 40 мин. Раствор охлаждают и выпаривают при пониженном давлении и полученное оранжевое твердое вещество обрабатывают гексаном (200 мл) и охлаждают в холодильнике в течение 3 дней. Полученное твердое вещество коричневато-желтого цвета как таковое собирают фильтрацией, сушат и применяют на следующей стадии без дальнейшей очистки. Стадия В. 1,4,5,6-Тетрагидропирроло[3,4-с]пиразол. Раствор гидразина (3 мл) и трет-бутил (3Z)-3-[(диметиламино)метилен]-4-оксопирролидин-1 карбоксилата (19,22 г) в этаноле (40 мл) нагревают при 85 С в запечатанной пробирке в течение 4 ч. Растворитель удаляют при пониженном давлении и остаток растирают с дихлорметаном (160 мл) и этилацетатом (15 мл). Полученное твердое вещество фильтруют. Фильтрат концентрируют и полученное твердое вещество снова растирают и фильтруют. Объединенные твердые вещества обрабатывают 4 н. хлористо-водородной кислотой (250 мл) в метаноле и перемешивают в течение 6 ч. Реакционную смесь концентрируют и сушат. Полученное твердое вещество снова обрабатывают в течение 6 ч 4 н. хлористоводородной кислотой (250 мл) в метаноле. После концентрирования и сушки полученный гидрохлорид обрабатывают аммиаком в метаноле (2 н., 300 мл) и раствором гидроксида аммония в воде (28%, 30 мл) и концентрируют досуха. Полученное твердое вещество обрабатывают метанолом (70 мл) и водой (5 мл) и очищают тремя партиями на системе Biotage Horizon (двуокись кремния, градиент 5-17% метанол, содержащий 10% концентрированный гидроксид аммония в этилацетате) с получением 1,4,5,6 тетрагидропирроло[3,4-с]пиразола. 1 Н ЯМР (500 МГц, CD3OD):4,04 (д, 4H), 7,39 (с, 1 Н). Промежуточное соединение 4. 1-(Циклопентилсульфонил)-1,4,5,6-тетрагидропирроло[3,4-с]пиразол. 2-(Циклопентилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол. Стадия А. трет-Бутил 1-(циклопентилсульфонил)-4,6-дигидропирроло[3,4-с]пиразол-5(1 Н)карбоксилат (А) и трет-бутил 2-(циклопентилсульфонил)-2,6-дигидропирроло[3,4-с]пиразол-5(4 Н)карбоксилат (В). К раствору N-Boc-пиразолопирролидина (промежуточное соединение 3, стадия В) (316 мг,1,51 ммоль) в дихлорметане добавляют N,N-диизопропилэтиламин (0,791 мл), затем добавляют хлорид циклопентансульфонила (0,299 мл, 2,265 ммоль). Смесь перемешивают при комнатной температуре в течение 18 ч. Реакционную смесь загружают в колонку Biotage и подвергают хроматографии с 50% этилацетатом в гексане с получением промежуточных соединений А и В, оба в виде твердого вещества не совсем белого цвета. ЖХ-МС: 342,09 (М+1). Стадия В. 1-(Циклопентилсульфонил)-1,4,5,6-тетрагидропирроло[3,4-с]пиразол. Промежуточное соединение А, полученное на предыдущей стадии (84 мг), в дихлорметане (4,0 мл) обрабатывают трифторуксусной кислотой (4,0 мл) при комнатной температуре в течение 2 ч. Реакционную смесь концентрируют и очищают на колонке Biotage, элюируя 2,5-5% метанолом и 0,25-0,5% гидроксидом аммония в дихлорметане с получением указанного в заголовке соединения в виде коричневого сиропа. Н ЯМР (500 МГц, CD3OD):1,60-1,81 (м, 4 Н), 1,92-2,11 (м, 4 Н), 3,92 (м, 2 Н), 4,05 (м, 1 Н), 4,12 (м,2 Н), 7,60 (с, 1 Н). ЖХ-МС: 242,10 (М+1). 2-(Циклопентилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол. Промежуточное соединение В, полученное на стадии А выше (275 мг), в дихлорметане (4,0 мл) обрабатывают трифторуксусной кислотой (4,0 мл) при комнатной температуре в течение 2 ч. Реакционную смесь концентрируют и остаток очищают на колонке с силикагелем, элюируя 5% метанолом и 0,5% гидроксидом аммония в дихлорметане с получением указанного в заголовке соединения в виде коричневого сиропа. 1 Н ЯМР (500 МГц, CD3OD):1,60-1,75 (м, 4 Н), 1,89-2,07 (м, 4 Н), 3,93-4,01 (м, 5 Н), 7,84 (с, 1 Н). ЖХ-МС: 242,05 (М+1). Промежуточное соединение 5. 2-(Метилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол(А) и трет-бутил 2-(метилсульфонил)-2,6-дигидропирроло[3,4-с]пиразол-5(4 Н)-карбоксилат (В). Суспензию N-Boc-пиразолопирролидина (промежуточное соединение 3, стадия В) (27,16 г,130 ммоль) в безводном ацетонитриле (1,0 л) загружают в 2,0 л трехгорлую колбу, оборудованную термометром и добавочной воронкой, и обрабатывают гидридом натрия (60% дисперсия в масле, 6,23 г,156 ммоль) в атмосфере азота одной порцией. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч. Полученную суспензию белого цвета затем охлаждают на ледяной бане и медленно добавляют хлорид метансульфонила (25,2 мл, 324 ммоль) через добавочную воронку. Затем ледяную баню удаляют и смесь перемешивают в течение 1 ч при комнатной температуре. Реакционную смесь гасят водой (500 мл) и слои разделяют. Водный слой затем экстрагируют 2500 мл дихлорметана. Объединенные органические слои сушат над сульфатом натрия и концентрируют при пониженном давлении с получением смеси продуктов А и В в виде бесцветного сиропа. ЯМР в CD3OD показал 1:1 смесь двух продуктов, в которой протон пиразольного кольца в продукте А появляется при 7,70 част./млн, а протон продукта В появляется при 7,95 част./млн. ЖХ-МС: 288,08 (М+1). Стадия В. 2-(Метилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол. Трифторуксусную кислоту (200 мл) медленно добавляют к раствору, содержащему промежуточные соединения А и В, полученные на предыдущей стадии (48,4 г, 168 ммоль), в дихлорметане (400 мл) при 0 С. После добавления охлаждающую баню удаляют и реакционную смесь перемешивают при комнатной температуре в течение 2 ч. Растворитель удаляют при пониженном давлении и полученный трифторацетат затем нейтрализуют 500 мл 25% метанола и 2,5% гидроксида аммония в дихлорметане. После удаления растворителя желаемое промежуточное соединение 5 получают после хроматографии на колонке Biotage (2340 г), элюируя 2,5-12,5% метанолом и 0,25-1,25% гидроксидом аммония в дихлорметане. ЖХ-МС: 109,85 (М+1). Промежуточное соединение 6. 1-(Циклопропилсульфонил)-1,4,5,6-тетрагидропирроло[3,4-с]пиразол. 2-(Циклопропилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол. Стадия А. трет-Бутил 1-(циклопропилсульфонил)-4,6-дигидропирроло[3,4-с]пиразол-5(1 Н)карбоксилат (А) и трет-бутил 2-(циклопентилсульфонил)-2,6-дигидропирроло[3,4-с]пиразол-5(4 Н)карбоксилат (В). Суспензию гидрида натрия (60% дисперсия в масле, 1,55 г, 38,7 ммоль) в безводном ацетонитриле(200 мл) добавляют к N-Boc-пиразолопирролидину (промежуточное соединение 3, стадия В) (5,3 г,25,5 ммоль) одной порцией в атмосфере азота при комнатной температуре. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч. К полученной суспензии белого цвета медленно добавляют хлорид циклопропансульфонила (6,9 г, 49,1 ммоль), смесь перемешивают при комнатной температуре в течение 18 ч, гасят водой (120 мл) и слои разделяют. Водный слой экстрагируют 2100 мл дихлорметана. Объединенные органические слои сушат над сульфатом натрия и концентрируют при пониженном давлении. Неочищенный продукт очищают хроматографией на двуокиси кремния (300 гBiotage колонка) и элюируют 15-80% этилацетатом в гексане с получением соединения А и соединения В в виде твердого вещества белого цвета. ЖХ-МС: 314,21 (М+1).- 28018613 Стадия В. 1-(Циклопропилсульфонил)-1,4,5,6-тетрагидропирроло[3,4-с]пиразол. Раствор соединения А (60 мг, 0,19 ммоль) в дихлорметане (1,0 мл) обрабатывают трифторуксусной кислотой (1,0 мл) при комнатной температуре. Через 1,5 ч реакционную смесь концентрируют и очищают на колонке с силикагелем с применением 5-10% метанола и 0,5-1% NH4OH в дихлорметане с получением указанного в заголовке соединения в виде янтарной пены. 1 Н ЯМР (500 МГц, CD3OD):1,14-1,23 (м, 2 Н), 1,31-1,38 (м, 2 Н), 2,91-2,97 (м, 1 Н), 4,01-4,05 (м,2 Н), 4,20-4,24 (м, 2 Н), 7,60 (с, 1 Н). ЖХ-МС: 214,13 (М+1). 2-(Циклопропилсульфонил)-2,4,5,6-тетрагидропирроло[3,4-с]пиразол. Раствор соединения В (205 мг, 0,65 ммоль) в дихлорметане (4,0 мл) обрабатывают трифторуксусной кислотой (4,0 мл) при комнатной температуре. Через 1,5 ч реакционную смесь концентрируют и нейтрализуют 2 н. гидроксидом аммония в метаноле с получением указанного в заголовке соединения в виде коричневого сиропа. 1 Н ЯМР (500 МГц, CD3OD):1,17-1,23 (м, 2 Н), 1,31-1,38 (м, 2 Н), 2,84-2,91 (м, 1 Н), 3,96-3,99 (м,4 Н), 7,82 (с, 1 Н). ЖХ-МС: 214,13 (М+1). Пример 1.(2R,3S,5R)-2-(2,5-дифторфенил)-5-[2-(метилсульфонил)-2,6 дигидропирроло[3,4-с]пиразол-5(4 Н)-ил]тетрагидро-2 Н-пиран-3-илкарбамат. Смесь промежуточного соединения 2 (26,3 г, 80 ммоль) и 2-(метилсульфонил)-2,4,5,6 тетрагидропирроло[3,4-с]пиразола (промежуточное соединение 5) (15,07 г, 80 ммоль) в безводном метаноле (1,5 л) перемешивают при комнатной температуре в течение 2 ч. К полученной суспензии белого цвета добавляют декаборан (2,95 г, 24,15 ммоль), смесь перемешивают при комнатной температуре в течение ночи. Метанол удаляют и остаток очищают на двух колонках 65i Biotage, элюируя 5-50% этилацетатом в дихлорметане с получением указанного в заголовке соединения в виде твердого вещества белого цвета. ЖХ-МС: 499,10 (М+1). Стадия В.(2R,3S,5R)-2-(2,5-Дифторфенил)-5-[2-(метилсульфонил)-2,6-дигидропирроло[3,4 с]пиразол-5(4 Н)-ил]тетрагидро-2 Н-пиран-3-амин. Удаление Boc-группы в продукте со стадии А (13,78 г, 27,67 ммоль) проводят с применением трифторуксусной кислоты (100 мл) в дихлорметане (200 мл) при комнатной температуре. После перемешивания в течение 2 ч реакционную смесь концентрируют и нейтрализуют 25% MeOH и 2,5% гидроксидом аммония в дихлорметане. Растворители удаляют при пониженном давлении и полученный неочищенный продукт очищают на колонке 65i Biotage, элюируя 1,25-5% MeOH и 0,125-0,5% гидроксидом аммония в дихлорметане. Выделенный продукт далее очищают перекристаллизацией из 5:1EtOAc/CH2Cl2 при 60 С. Кристаллический продукт промывают холодным 2:1 EtOAc/гексаном с получением указанного в заголовке соединения в виде твердого вещества светло-коричневого цвета. 1 Н ЯМР (500 МГц, CD3OD): 1,71 (кв., 1 Н, J=12 Гц), 2,56-2,61 (м, 1 Н), 3,11-3,18 (м, 1 Н), 3,36-3,40 (м,1 Н), 3,48 (т, 1 Н, J=12 Гц), 3,88-3,94 (м, 4 Н), 4,30-4,35 (м, 1 Н), 4,53 (д, 1 Н, J=12 Гц), 7,14-7,23 (м, 2 Н), 7,267,30 (м, 1 Н), 7,88 (с, 1 Н). ЖХ-МС: 399,04 (М+1). Пример 2. (2R,3S,5R)-2-(2,4,5-Трифторфенил)-5-[2-(метилсульфонил)-2,6-дигидропирроло[3,4 с]пиразол-5(4H)-ил]тетрагидро-2 Н-пиран-3-амин
МПК / Метки
МПК: A61P 3/10, A61K 31/4162, C07D 487/04
Метки: предупреждения, лечения, диабета, качестве, дипептидилпептидазы-iv, аминотетрагидропираны, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-18613-aminotetragidropirany-v-kachestve-ingibitorov-dipeptidilpeptidazy-iv-dlya-lecheniya-ili-preduprezhdeniya-diabeta.html" rel="bookmark" title="База патентов Евразийского Союза">Аминотетрагидропираны в качестве ингибиторов дипептидилпептидазы-iv для лечения или предупреждения диабета</a>