Антибиотик 107891, его фармацевтически приемлемые соли, фармацевтическая композиция и применение
Номер патента: 16608
Опубликовано: 30.06.2012
Авторы: Гастальдо Лучано, Кандиани Джанпаоло, Сельва Энрико, Паренти Франко, Маринелли Флавия, Ладзарини Америга, Чичилиато Исмаэла, Лози Даниеле
Формула / Реферат
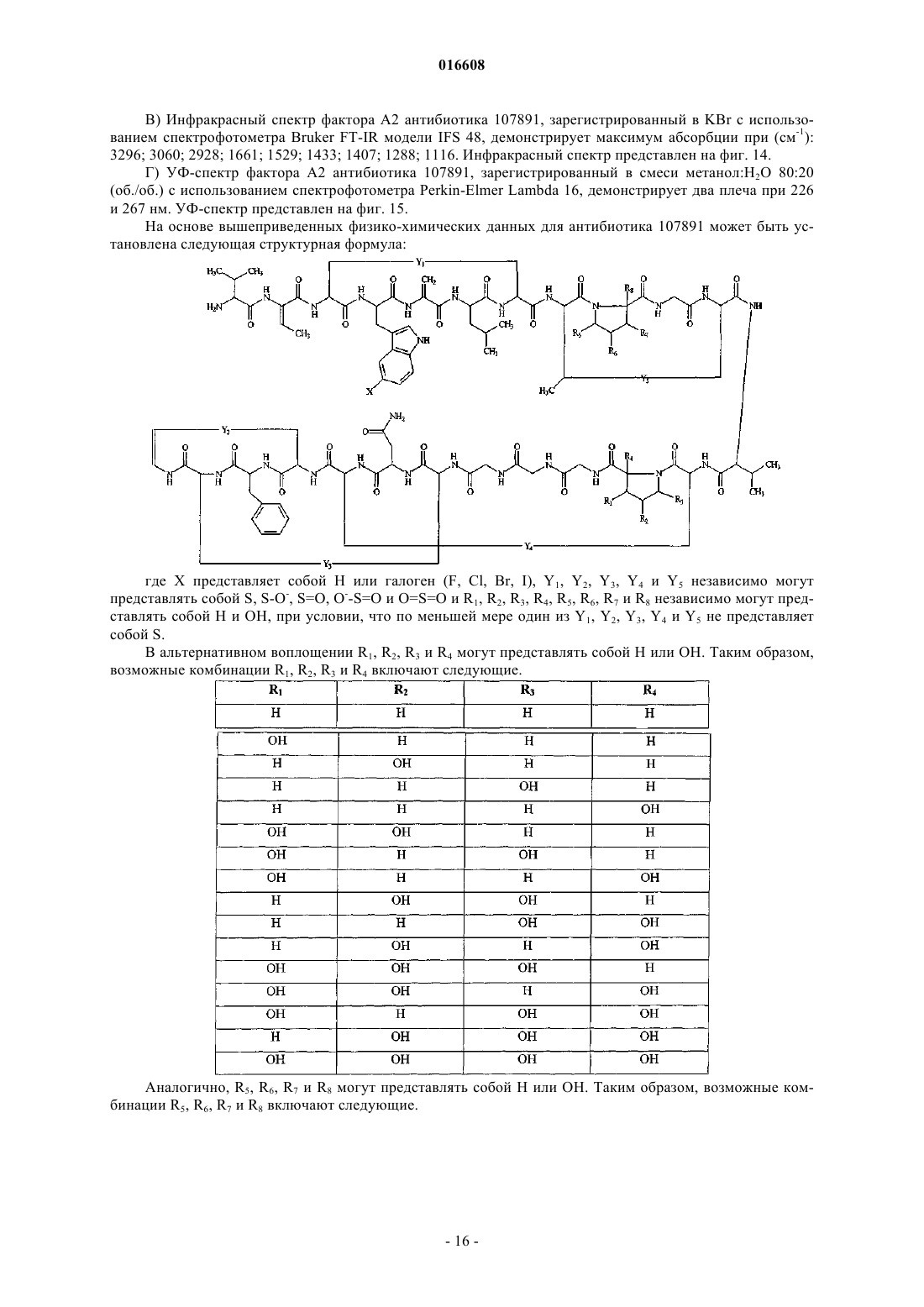
1. Соединение формулы
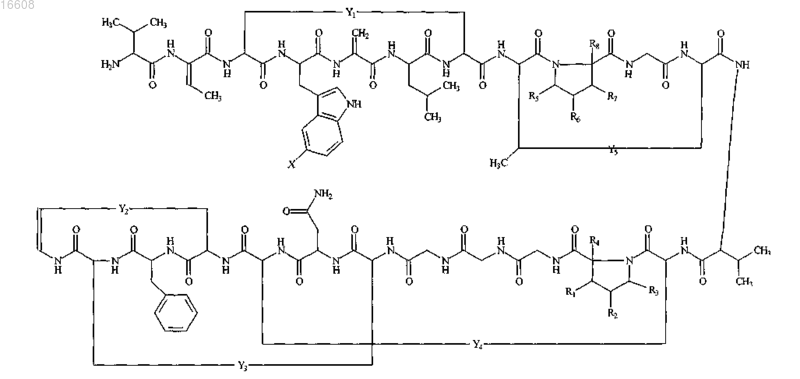
где X выбран из группы, состоящей из H, F, Cl, Br и I;
Y1, Y2, Y3, Y4 и Y5 независимо выбраны из группы, состоящей из S, S-O-, S=O, O--S=O и O=S=O; и
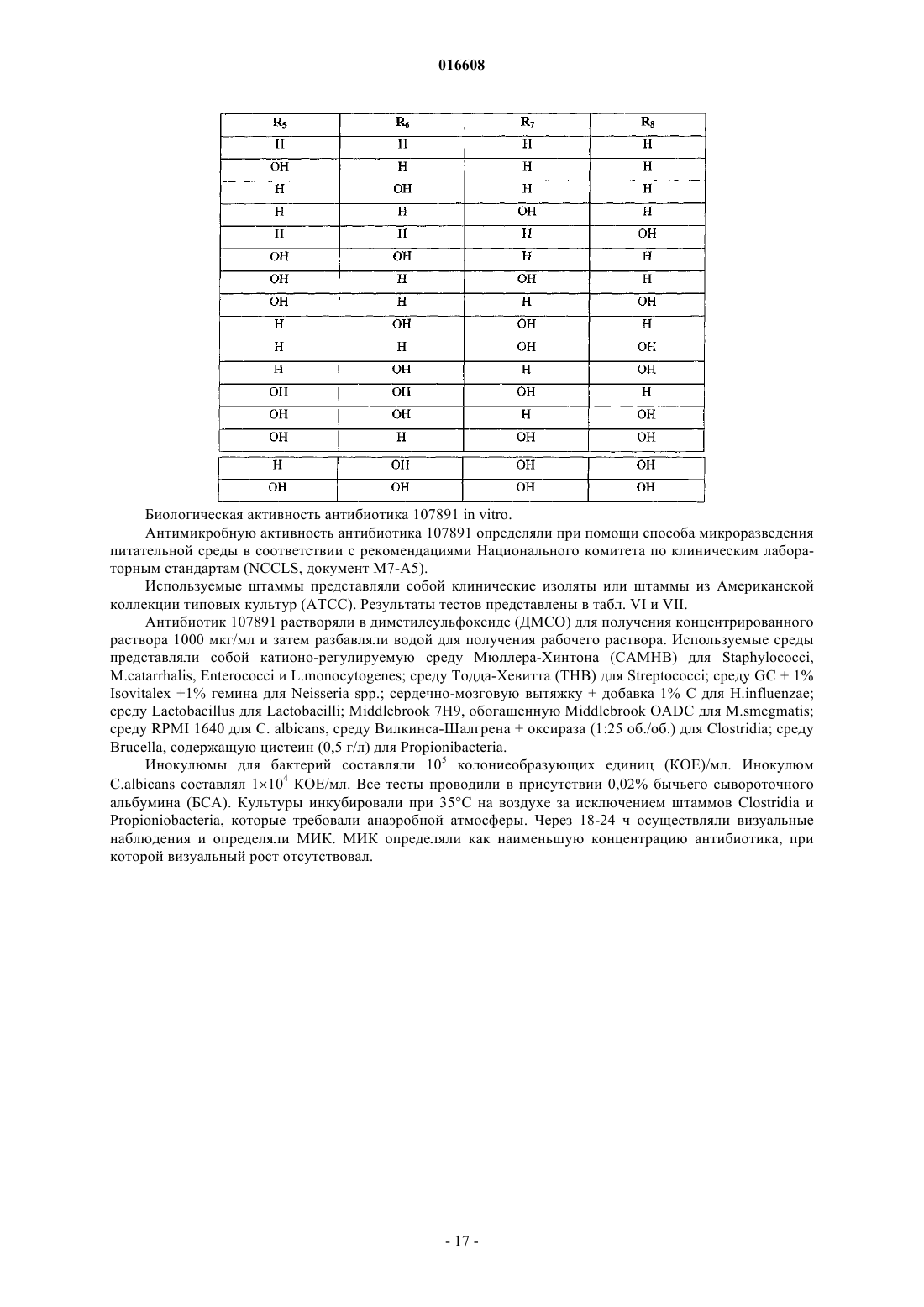
R1, R2, R3, R4, R5, R6, R7 и R8 независимо выбраны из группы, состоящей из H и OH,
при условии, что по меньшей мере один из Y1, Y2, Y3, Y4 и Y5 не представляет собой S.
2. Соединение по п.1, где R4, R5, R6, R7 и R8 представляют собой H.
3. Соединение по п.2, где R1 представляет собой H, R2 представляет собой H и R3 представляет собой H.
4. Соединение по п.2, где R1 представляет собой H, R2 представляет собой H и R3 представляет собой OH.
5. Соединение по п.2, где R1 представляет собой H, R2 представляет собой OH и R3 представляет собой OH.
6. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой OH и R3 представляет собой ОН.
7. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой H и R3 представляет собой Н.
8. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой H и R3 представляет собой ОН.
9. Соединение по п.1, где Y1 выбран из группы, состоящей из S-O-, S=O, O--S=O и O=S=O; а Y2, Y3, Y4 и Y5 представляют собой S.
10. Соединение по п.1, где Y2 выбран из группы, состоящей из S-O-, S=O, O--S=O и O=S=O; a Y1, Y3, Y4 и Y5 представляют собой S.
11. Соединение по п.1, где Y3 выбран из группы, состоящей из S-O-, S=O, O--S=O и O=S=O; a Y1, Y2, Y4 и Y5 представляют собой S.
12. Соединение по п.1, где Y4 выбран из группы, состоящей из S-O-, S=O, O--S=O и O=S=O; a Y1, Y2, Y3 и Y5 представляют собой S.
13. Соединение по п.1, где Y5 выбран из группы, состоящей из S-O-, S=O, O--S=O и O=S=O; a Y1, Y2, Y3 и Y4 представляют собой S.
14. Фармацевтическая композиция, содержащая антибиотик, выбранный из соединений по п.1 или их фармацевтически приемлемой соли с кислотой, и фармацевтически приемлемый носитель.
15. Применение соединений по п.1 или их фармацевтически приемлемой соли с кислотой для изготовления лекарственного средства для лечения или предупреждения бактериальных инфекций.
Текст
АНТИБИОТИК 107891, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ,ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ Изобретение относится к антибиотическому веществу микробного происхождения, произвольно названному 107891, охватываемому общей структурной формулой, приведенной в описании изобретения, продуцируемому путем ферментации Microbispora sp. PTA-5024, его фармацевтически приемлемым солям и фармацевтической композиции и их применению в качестве антибактериального агента, обладающего ингибирующей активностью против чувствительных микробов. Антибиотик 107891 имеет пептидную структуру, содержащую лантионин и метиллантионин в качестве составляющих, которые характерны для антибиотиков группы лантибиотиков. Антибиотик 107891 демонстрирует хорошую антибактериальную активность против грамположительных бактерий, включая штаммы, резистентные к метициллину и ванкомицину, и также активны против некоторых грамотрицательных бактерий, таких как 016608 Заявка на данное изобретение представляет собой международную заявку, основанную на заявке на патент США, поданной 26 января 2005 г., которая представляет собой частично продолжающуюся заявку заявки на патент США 11/035296, поданной 12 января 2005 г., которая представляет собой частично продолжающуюся заявку заявки на патент США 10/521336, поданной 11 января 2005 г., представляющей собой 371 национальной подачи PCT/EP2004/007658, поданной 12 июля 2004 г., заявляющей о приоритете согласно заявке на европейский патент 03016306.7, поданной 18 июля 2003 г., все из которых определенно включены путем ссылки. Настоящее изобретение относится к антибиотическому веществу микробного происхождения, произвольно обозначаемому как антибиотик 107891, его фармацевтически приемлемым солям, фармацевтическим композициям и их применению в качестве антибактериального агента. Согласно изобретению предложено соединение формулыY1, Y2, Y3, Y4 и Y5 независимо выбраны из группы, состоящей из S, S-O-, S=O, OS=O и O=S=O; иR1, R2, R3, R4, R5, R6, R7 и R8 независимо выбраны из группы, состоящей из H и OH,при условии, что по меньшей мере один из Y1, Y2, Y3, Y4 и Y5 не представляет собой S. Предпочтительным является соединение по изобретению, где R4, R5, R6, R7 и R8 представляют собой H. Еще более предпочтительным является соединение, гдеR1 представляет собой OH, R2 представляет собой H и R3 представляет собой OH. Также предпочтительным является соединение по изобретению, гдеY5 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; a Y1, Y2, Y3 и Y4 представляют собой S. Согласно изобретению предложена также фармацевтическая композиция, содержащая антибиотик,выбранный из соединений по изобретению, как они определены выше, или их фармацевтически приемлемой соли с кислотой, и фармацевтически приемлемый носитель. Кроме того, согласно изобретению предложено применение соединений по изобретению или их фармацевтически приемлемой соли с кислотой для изготовления лекарственного средства для лечения или предупреждения бактериальных инфекций. В этом описании термин "антибиотик 107891", если не указано иначе, определяет соединения по изобретению, охватываемые раскрытой выше общей структурной формулой, а термин "факторы A1 и A2 атибиотика 107891" означает два конкретных антибиотических соединения, раскрытых вWO-A-2006075988, которые не входят в объем защиты согласно настоящему изобретению.-1 016608 Антибиотик 107891 представляет собой новый антимикробный агент, имеющий пептидную структуру, содержащий в качестве составляющих лантионин и метиллантионин. Они представляют собой типичные характеристики лантибиотиков и, в частности, подгруппы, действующей прежде всего на биосинтез клеточной стенки. Лантибиотики представляют собой пептиды, содержащие тиоэфирную аминокислоту лантионин, а также несколько других модифицированных аминокислот (H.G. Sahl and G. Bierbaum, (1998):"Lantibiotics: biosynthesis and biological activities of uniquely modified peptides from gram-positive bacteria",Ann. Rev. Microbiol. 52: 41-79). Большая часть известных лантибиотиков обладает антибактериальной активностью, хотя о некоторых сообщалось, что они являются активными в отношении других фармакологических мишеней. Антибактериальные лантибиотики могут быть в общем виде разделены на две группы на основе их структур: лантибиотики типа A представляют собой, как правило, удлиненные амфифильные пептиды, тогда как лантибиотики типа B являются компактными и глобулярнымиMicrob. Rev. 25: 285-308). Низин является типичным представителем лантибиотиков типа A, тогда как актагардин (гардимицин) и мерсацидин относятся к подклассу лантибиотиков типа B. Лантибиотики типа низина и типа мерсацидина взаимодействуют с липидом II, предшественником связанных с мембраной пептидогликанов, хотя эти два класса отличаются действиями, которые они оказывают в процессе бактериальной пролиферации. Лантибиотики низинового типа, прежде всего, убивают бактерии путем пермеабилизации цитоплазматической мембраны (H. Brotz, M. Josten, I. Wiedemann, U. Schneider, F. Gotz,G. Bierbaum and H.G. Sahl, (1998): "Role of lipid-bound peptidoglycan precursors in the formation of pores bynisin, epidermin and other lantibiotics", Mol. Microbiol. 30: 317-27), тогда как лантибиотики мерсацидинового типа прежде всего убивают бактериальную клетку путем ингибирования биосинтеза клеточной стенки (H. Brotz, G. Bierbaum, K. Leopold, P.E. Reynolds and H.G. Sahl, (1998): "The lantibiotic mersacidininhibits peptidoglycan synthesis by targeting lipid II", Antimicrob Agents Chemother. 42: 154-60). Два антибиотика, продуцируемых Microbispora corallina штамм NRRLL 30420, идентифицированные соответственно как антибиотик MF-BA-17681 и MF-BA-17681, описаны в US 6551591 B1. Физико-химические данные, представленные в вышеуказанном патенте (например, данные массспектрометрии, молекулярная масса, содержание аминокислот), и сравнение времен удерживания в экспериментальных анализах путем жидкостной хроматографии/масс-спектрометрии (ЖХ-МС) ясно демонстрируют, что антибиотический комплекс 107891, а также его компоненты фактор A1 и фактор A2 представляют собой химические соединения, отличающиеся от антибиотиков MF-BA-17681 иEP 0592835 А 2 описывает противоопухолевые антибиотики BU-4803TA1, A2, B, C1, C2 и D. Антибиотики BU-4803TA1, A2 и В выделяют из ферментационного бульона Microbispora ATCC 55327(AA 9966), тогда как антибиотики BU-4803TC1, C2 и D представляют собой продукты трансформации антибиотика BU-4803TA1, A2 и B соответственно, когда эти продукты хранят в диметилсульфоксиде. Физико-химические данные, которые сообщаются в EP 0592835 A2 для вышеприведенных антибиотиков(например, поглощение ультрафиолета (УФ), молекулярная масса, противоопухолевая активность), очевидно демонстрируют, что они представляют собой химические вещества, отличающиеся от антибиотического комплекса 107891 и его факторов A1 и A2. Штамм и ферментация.Microbispora sp. 107891 выделили из окружающей среды и 27 февраля 2003 г. депонировали в Американской коллекции типовых культур (American Type Culture Collection) (ATCC), 10801 University Blvd,Manassas VA, 20110-2209 U.S.A., в соответствии с Будапештским договором. Штамму был присвоен номер PTA-5024. Продукцию антибиотика 107891 осуществляют путем культивирования штамма Microbispora sp.,способного продуцировать его, т.е. Microbispora sp. ATCC PTA-5024 или его варианта или мутанта, с сохранением их способности продуцировать указанный антибиотик; выделения получающегося в результате антибиотика из цельного культурального бульона, и/или из выделенного мицелия, и/или из отфильтрованного ферментационного бульона и очистки выделенного антибиотика при помощи хроматографических средств. В любом случае предпочтительно продуцировать антибиотик 107891 в аэробных условиях в водной питательной среде, содержащей легко ассимилируемые источники углерода, азота и неорганические соли. Может быть использовано множество питательных сред, обычно используемых в области ферментации, тем не менее предпочтительны некоторые среды. Предпочтительные источники углерода представляют собой сахарозу, фруктозу, глюкозу, ксилозу и т.п. Предпочтительные источники азота представляют собой соевую муку, пептон, мясной экстракт,дрожжевой экстракт, триптон, аминокислоты, гидролизованный казеин и т.п. Среди неорганических солей, которые могут быть включены в культуральные среды, имеются традиционные растворимые соли,способные к обеспечению ионами натрия, калия, железа, цинка, кобальта, магния, кальция, аммония,хлоридом, карбонатом, сульфатом, фосфатом, нитратом и подобными ионами.-2 016608 Предпочтительно штамм, продуцирующий антибиотик 107891, предварительно культивируют в бродильной трубке или качалочной колбе, затем культуру используют для инокуляции ферментационных сосудов для продуцирования значительных количеств веществ. Среда, используемая для предварительного культивирования, может быть той же самой, что и используемая для более масштабных ферментаций, но также могут быть использованы другие среды. Штамм, продуцирующий антибиотик 107891, можно выращивать при температуре от 17 до 37C, причем оптимальная температура составляет приблизительно 28-30C. Продуцирование антибиотика 107891 в ходе ферментации можно контролировать путем биоанализа на чувствительных микроорганизмах и/или посредством ВЭЖХ (высокоэффективная жидкостная хроматография) анализов. Максимальная продукция антибиотика 107891, как правило, имеет место приблизительно между 90 и 200 ч ферментации. Антибиотик 107891 продуцируют путем культивирования Microbispora sp. ATCC PTA-5024 или его варианта или мутанта, способного продуцировать антибиотик 107891, и он обнаружен в культуральных бульонах и/или в мицелии. Морфологические характеристики Microbispora sp. ATCC PTA-5024.Microbispora sp. ATCC PTA-5024 хорошо растет на различных стандартных твердых средах. Микроскопические размеры измеряли с использованием культуры, выращенной на агаре с гуминовой кислотой и солями микроэлементов (состав в г/л: гуминовая кислота 0,5, FeSO47H2O 0,001, MnCl24H2O 0,001,ZnSO47H2O 0,001, NiSO46H2O 0,001, MOPS 2, агар 20) с добавлением 1 мл/л раствора витаминов (тиамина гидрохлорид 25 мг/л, пантотенат кальция 250 мг/л, никотиновая кислота 250 мг/л, биотин 0,5 мг/л,рибофлавин 1,25 г/л, цианокобаламин 6,25 мг/л, парааминобензойная кислота 25 мг/л, фолиевая кислота 500 мг/л, пиридоксаля гидрохлорид 500 мг/л). В жидкой культуре (среда V6, состав в г/л: декстроза 22, мясной экстракт 5, дрожжевой экстракт 5,казеин 3, NaCl 1,5) не обнаружена фрагментация мицелия после 6 дней роста при 28C. Микроскопическое исследование на агаре с гуминовой кислотой и солями микроэлементов (через 21 день инкубации при 28C) выявляет разветвленный нефрагментированный субстратный мицелий и моноподиально разветвленный воздушный мицелий; также различимо множество длинных, прямых и слаборазветвленных воздушных гиф. Характерные продольные пары спор закачанчиваются короткими спорофорами, латерально происходящими из ветвей или непосредственно из основных воздушных гиф. Споры сферические и неподвижные. Тельца, напоминающие спорангий, или другие особые структуры не обнаружены. Культуральные характеристики Microbispora sp. ATCC PTA-5024.Microbispora sp. ATCC PTA-5024 в течение 6 дней выращивали в жидкой среде AF/MS (см. пример 1) при 28C и 200 об/мин, затем переносили (5% инокулюма) в новую жидкую среду AF/MS и выращивали в течение еще 6 дней и затем инокулировали (7% инокулюма) в 100 мл жидкой среды V6 (см. пример 1). После выращивания в течение 6 дней при 28C и 200 об/мин мицелий собирали путем центрифугирования и трижды промывали стерильным физиологическим раствором, затем разбавляли с получением подходящего инокулюма. Аликвоты суспензии поперечными штрихами наносили на различные среды, рекомендованные Shirling и Gottlieb (E.B. Shirling and D. Gottlieb, (1966): "Method for Characterization(1961): "The Actinomycetes", The Williams and Wilkins Co., Baltimore. Vol. 2: 328-334). Способность использовать различные углеводы в качестве источника углерода и энергии определяли с использованием среды ISP 4 без крахмала с добавлением 1 мл/л описанного выше раствора витаминов в качестве базовой среды; каждый источник углерода добавляли в конечной концентрации 1%(мас./об.). Устойчивость к NaCl, диапазон pH для роста, а также способность расти при различных температурах определяли на среде ISP 2. Все среды инкубировали при 28C в течение трех недель; если не указано иначе, описания относятся к 21 дню. Окраску оценивали при естественном свете с использованием Атласа окрашивания Maerz и Paul (A. Maerz and M.R. Paul, 1950. - A Dictionary of Colour, 2nd edition.McGraw-Hill Book Co. Inc., New York). Способность восстанавливать нитраты до нитритов оценивали в жидкой нитратной среде в соответствии со способом, описанным Williams et al.(S.T. Williams, M. Goodfellow, G. Alderson, E.M.H. Wellington, P.H.A. SneathM.J. Sackin, 1983. Numerical classification of Streptomyces and related genera. - J. Gen. Microbiol. 129, 1743-1813). Рост, внешний вид колоний, окраска субстратного и воздушного мицелия и продукция пигмента для штамма Microbispora sp. ATCC PTA-5024 представлены в табл. I. Вегетативный рост присутствует на большей части используемых сред в отличие от воздушного мицелия, который присутствует только на некоторых из них. На всех использованных средах пигментация отсутствовала. Физиологические характеристики штамма представлены в табл. II. Рост и продуцирование воздушного мицелия происходят при 17C, но не при 43C. Продуцирование воздушного мицелия на ISP 2 происходит при pH больше 6 и отсутствует в присутствии 1% NaCl.-3 016608 Способность использовать различные углеводы для роста представлена в табл. III. Таблица I Характеристики роста Microbispora sp. ATCC PTA-5024 Таблица III Использование источников углерода Microbispora sp. ATCC PTA-5024- отсутствие роста; воздушный мицелий всегда отсутствует.Microbispora sp. ATCC PTA-5024 выращивали в среде GYM (глюкоза 4 г/л; дрожжевой экстракт 4 г/л; солодовый экстракт 10 г/л) при 28C на роторной качалке, мицелий собирали, дважды промывали стерильной дистиллированной водой и затем сушили замораживанием. Анализы аминокислот осуществляли в соответствии со способом Staneck и Roberts (J.L. Staneck and G.D. Roberts, (1974): "Simplifiedapproach to identification of aerobic actinomycetes by thin-layer chromatography", Appl. Microbiol. 28: 226231). Менахиноны и полярные липиды экстрагировали в соответствии со способом Minnikin et al."An integrated procedure of isoprenoid quinones and polar lipids", J. Microbiol. Meth. 2: 233-241). Полярные липиды анализировали соответственно посредством тонкослойной хроматографии (D.E. Minnikin,V. Patel, L. Alshamaony, and M. Goodfellow, (1977): "Polar lipid composition in the classification of Nocardiaand related bacteria", Int. J. Syst. Bacteriol. 27: 104-117), менахиноны - посредством высокоэффективной жидкостной хроматографии (ВЭЖХ) (R.M. Kroppenstedt, (1982): "Separation of bacterial menaquinones byGoodfellow and D.E. Minnikin eds, Academic Press, London), а метиловые эфиры жирных кислот - посредством газожидкостной хроматографии (L.Т. Miller, (1982): "A single derivatization method for bacterial fattyof bacteria by gas chromatography of cellular fatty acids", USFCC News Letters. 20: 1-6). Присутствие миколовых кислот проверяли с помощью метода, предложенного Minnikin et al. (D.E. Minnikin,L. Alshamaony, and M. Goodfellow, (1975): "Differentiation of Mycobacterium, Nocardia and related taxa bythin layer chromatographic analysis of whole organism methanolyzates", J. Gen. Microbiol. 88: 200-204). Гидролизаты целых клеток штамма Microbispora sp. ATCC PTA-5024 содержат мезодиаминопимелиновую кислоту в виде диаминокислоты пептидогликана. Преобладающие менахиноны представляют собой MK-9 (III, VIII-H4), MK-9 (H2) и MK-9 (H0). Картина полярных липидов характеризуется наличием фосфолипида, содержащего фосфатидилэтаноламин, метилфосфатидилэтаноламин,фосфатидилглицерин, дифосфатидилглицерин, фосфатидилинозит, фосфатидилинозитманнозиды иcomposition", Biochem. Syst. Ecol. 5: 246-260). Основные компоненты паттерна жирных кислот представляют собой anteiso 15:0, iso 16:0, n-16:0, anteiso 17:0 и 10-метилгептадекановую (10-Me-17:0) кислоты,т.е. 3c sensu Kroppenstedt (R.M. Kroppenstedt, (1985): "Fatty acid and menaquinone analysis of actinomycetesand related organisms", in: Chemical Methods in Bacterial Systematics. No 20 SAB Technical Series, p. 173199. M. Goodfellow and D.E. Minnikin eds, Academic Press, London). Миколовые кислоты не обнаружены. Определение последовательности 16S рДНК MICROBISPORA sp. ATCC PTA-5024. Частичную последовательность гена 16 рРНК (16S рДНК), т.е. 1443 нуклеотида, соответствующей 95% полноразмерной рРНК штамма Microbispora sp. ATCC PTA-5024, получили в соответствии с опубликованными методами (P. Mazza, P. Monciardini, L. Cavaletti, M. Sosio and S. Donadio, (2003): "DiversitySEQ ID NO: 1. Эту последовательность сравнивали с последовательностью штамма Microbispora corallina NRRL 30420 (MF-BA-1768), которая приведена в US 6551591 B1. Две последовательности выравнивали и различия обнаружили в 31 из 1456 выровненных позиций, что составляло общее различие в последовательности 2,13%. Любые два штамма, имеющие менее чем 97,5%-ную идентичность последовательностей,обычно относятся к различным видам (Stackebrandt, E. and Embley, M.T. (2000): "Diversity of UnculteredD.J. Grimes (eds). ASM, Press, Washington DC, p. 57-75). Таким образом, 2%-ный уровень различия последовательностей является весьма высоким (Rossell-Mora, R., and Amann, R. (2001): "The Species Conceptfor Prokaryotes". FEMS Microbiol. Rev. 25: 39-67) и указывает на то, что Microbispora sp. ATCC PTA-5024 и Microbispora corallina NRRL 30420 (MF-BA-1768) представляют собой различные штаммы. Идентификация штамма MICROBISPORA sp. ATCC PTA-5024. Штамм, продуцирующий антибиотик 107891, относят к роду Microbispora, семействоStreptosporangiaceae, в силу следующих хемотаксономических и морфологических характеристик: присутствие мезодиаминопимелиновой кислоты в клеточной стенке; большое количество MK-9 (III, VIII-H4) и фосфолипидов IV типа в соответствии с Lechevalier et al.phospholipid composition", Biochem. Syst. Ecol. 5: 246-260); профиль жирных кислот 3c sensu Kroppenstedt (R.M. Kroppenstedt, (1992): "The genus Nocardiopsis",in: The Prokariotes, Vol II, p. 1139-1156, A. Balows, H. Truper, M. Dworkin, W. Harder and K.H. Schleifereds; New York, Springer-Verlag); отсутствие миколовых кислот; образование характерных продольных пар спор на верхушках коротких спорофоров, латерально ветвящихся от воздушных гиф. Неподвижные споры; частичная последовательность гена 16 рРНК (16S рДНК), т.е. 1443 нуклеотидов, соответствующая 95% полноразмерной рРНК, представленная в SEQ ID NO: 1, демонстрирующая более чем 97%-ную идентичность с последовательностями 16S рДНК описанных видов Microbispora.-6 016608 Как с другими микроорганизмами, характеристики штамма, продуцирующего антибиотик 107891,подвержены вариации. Например, искусственные варианты и мутанты штамма могут быть получены путем обработки различными известными мутагенами, такими как ультрафиолетовые (УФ) лучи, химические вещества, такие как азотистая кислота, N-метил-N'-нитро-N-нитрозогуанидин, и множество других. Все природные и искусственные варианты и мутанты штамма Microbispora sp. ATCC PTA-5024, способные продуцировать антибиотик 107891, считаются эквивалентными ему для целей данного изобретения и, таким образом, входят в объем изобретения. Экстракция и очистка антибиотика 107891. Как упомянуто выше, обнаружено, что антибиотик 107891 почти равным образом распределен как в мицелии, так и в отфильтрованной фракции ферментационного бульона. Собранный бульон может быть подвергнут отделению мицелия от супернатанта ферментационного бульона и мицелий может быть экстрагирован смешивающимся с водой растворителем с получением раствора, содержащего антибиотик 107891, после удаления истощенного мицелия. Этот экстракт мицелия затем может быть обработан отдельно или вместе с супернатантом в соответствии со способами, которые приведены далее для фракции супернатанта. Когда смешивающийся с водой растворитель может оказывать влияние на операции выделения антибиотика из экстракта мицелия, этот смешивающийся с водой растворитель может быть удален путем отгонки или может быть разбавлен водой до концентрации, которая не оказывает влияния. Используемый в данном описании термин "смешивающийся с водой растворитель" имеет значение,в настоящее время присвоенное в области техники этому термину, и относится к растворителям, которые в условиях применения смешиваются с водой в достаточно широком диапазоне концентраций. Примеры смешивающихся с водой органических растворителей, которые могут быть использованы в экстракции соединений по изобретению, представляют собой низшие алканолы, например (C1-C3)алканолы,такие как метанол, этанол и пропанол; фенил(C1-C3)алканолы, такие как бензиловый спирт; низшие кетоны, например (C3-C4)кетоны, такие как ацетон и этилметилкетон; циклические эфиры, такие как диоксан и тетрагидрофуран; гликоли и их продукты частичной этерификации, такие как этиленгликоль, пропиленгликоль и монометиловый эфир этиленгликоля, низшие амиды, такие как диметилформамид и диэтилформамид; диметилсульфоксид уксусной кислоты и ацетонитрил. Выделение соединения из супернатанта ферментационного бульона продуцирующего микроорганизма осуществляют в соответствии с известными методами, включающими экстракцию растворителями, осаждение путем добавления нерастворителей или путем изменения pH раствора, путем распределительной хроматографии, распределительной хроматографии с обращенной фазой, ионообменной хроматографии, молекулярной вытеснительной хроматографии и т.п. или комбинации двух или более чем двух из указанных способов. Процедура выделения соединений по изобретению из профильтрованного ферментационного бульона включает экстракцию антибиотика 107891 смешивающимися с водой органическими растворителями с последующим осаждением из концентрированных экстрактов, возможно путем добавления осаждающего агента. Также в этом случае используемый в описании термин "несмешивающийся с водой растворитель" имеет значение, в настоящее время присвоенное в области техники указанному термину, и относится к растворителям, которые в условиях применения слабо смешиваются или практически не смешиваются с водой в достаточно широком диапазоне концентраций, подходящих для предполагаемого применения. Примеры не смешивающихся с водой органических растворителей, которые могут быть использованы в экстракции соединений по изобретению из ферментационного бульона, представляют собой алканолы, состоящие по меньшей мере из четырех атомов углерода, которые могут быть линейными, разветвленными или циклическими, такие как н-бутанол, 1-пентанол, 2-пентанол, 3-пентанол, 1-гексанол,2-гексанол, 3-гексанол, 3,3-диметил-1-бутанол, 4-метил-1-пентанол, 3-метил-1-пентанол, 2,2-диметил-3 пентанол, 2,4-диметил-3-пентанол, 4,4-диметил-2-пентанол, 5-метил-2-гексанол, 1-гептанол, 2-гептанол,5-метил-1-гексанол, 2-этил-1-гексанол, 2-метил-3-гексанол, 1-октанол, 2-октанол, циклопентанол,2-циклопентилэтанол, 3-циклопентил-1-пропанол, циклогексанол, циклогептанол, циклооктанол,2,3-диметилциклогексанол, 4-этилциклогексанол, циклооктилметанол, -метил-5-гептен-2-ол, 1-нонанол,2-нонанол, 1-деканол, 2-деканол и 3-деканол; кетоны, состоящие по меньшей мере из пяти атомов углерода, такие как метилизопропилкетон, метилизобутилкетон, метил-н-амилкетон, метилизоамилкетон и их смеси. Как известно в области техники, экстракция продукта из профильтрованного ферментационного бульона может быть улучшена путем доведения pH до подходящего значения и/или путем добавления подходящей органической соли, образующей ионную пару с антибиотиком, растворимым в экстрагирующем растворителе. Как известно в области техники, фазовое разделение может быть улучшено путем высаливания водной фазы. Когда после экстракции выделенная органическая фаза содержит большое количество воды, может быть удобным азеотропно отгонять из нее воду. Как правило, для этого требуется добавление растворителя, способного образовывать минимальные азеотропные смеси с водой, с последующим добавлением-7 016608 осаждающего агента для осаждения при необходимости желаемого продукта. Типичные примеры органических растворителей, способных образовывать минимальные азеотропные смеси с водой, представляют собой н-бутанол, бензол, толуол, бутиловый эфир, тетрахлорид углерода, хлороформ, циклогексан,2,5-диметилфуран, гексан и м-ксилол; предпочтительный растворитель представляет собой н-бутанол. Примеры осаждающих агентов представляют собой петролейный эфир, низшие алкиловые эфиры,такие как этиловый эфир, пропиловый эфир и бутиловый эфир, и низшие алкилкетоны, такие как ацетон. В соответствии с предпочтительным способом выделения антибиотика 107891 профильтрованный ферментационный бульон может быть приведен в контакт с адсорбирующей матрицей с последующей элюцией полярным смешивающимся с водой растворителем или их смесью, концентрированием до маслянистого остатка при пониженном давлении и осаждением осаждающим агентом, имеющим тип, уже упомянутый выше. Примеры адсорбирующих матриц, которые могут быть удобным образом использованы при выделении соединений по изобретению, представляют собой полистирольные или смешанные полистиролдивинилбензольные смолы (например, M112 или S112, Dow Chemical Co.; Amberlite XAD2 или XAD4,RohmHaas; Diaion HP 20, Mitsubishi), акриловые смолы (например, XAD7 или XAD8, RohmHaas),полиамиды, такие как поликапролактамы, нейлоны и поперечно-сшитые поливинилпирролидоны (например, полиамид-CC 6, полиамид-SC 6, полиамид-CC 6.6, полиамид-CC 6AC и полиамид-SC 6AC,Macherey-NagelCo., Germany; PA 400, M. Woelm AG, Germany); и поливинилпирролидоновую смолуPVP-CL (Aldrich Chemie GmbHCo., KG, Germany) и поперечно-сшитые декстраны с контролируемыми порами (например, Sephadex LH-20, Pharmacia Fine Chemicals, AB). Предпочтительно используют полистирольные смолы, особенно предпочтительна смола Diaion HP 20. В случае полистирольных смол, полистиролдивинилбензольных смол, полиамидных смол или акриловых смол предпочтительный элюент представляет собой смешивающийся с водой растворитель или его водные смеси. Водные смеси могут содержать буферы при подходящем значении pH. Также в этом случае используемый в этом описании и формуле изобретения термин "смешивающийся с водой растворитель" имеет значение, присвоенное в настоящее время в области техники указанному термину, как описано выше. Успешные процедуры выделения и очистки антибиотика могут быть осуществлены в объединенных экстрактах из супернатанта бульона и из мицелия. Например, когда часть антибиотического продукта, содержащегося в профильтрованном ферментационном бульоне или супернатанте, выделяют путем абсорбции на абсорбирующей смоле, а часть антибиотического продукта, содержащегося в мицелии,экстрагируют из него смешивающимся с водой растворителем с последующей адсорбцией на абсорбирующей смоле, элюированные фракции с каждого из двух наборов абсорбирующих смол могут быть объединены, возможно после концентрирования, и затем дополнительно обработаны в виде единой партии. Альтернативно, когда два набора абсорбирующих смол, использованных для отдельных стадий экстракции, имеют одинаковый тип и обладают одинаковыми функциональными характристиками, они могут быть объединены вместе и смесь может быть подвергнута единой стадии элюции, например смешивающимся с водой растворителем или его смесью с водой. В любом случае, независимо от того, какая процедура адаптирована для выделения сырого антибиотика 107981, успешную стадию очистки обычно осуществляют из смеси сырых веществ, являющейся результатом объединения продуктов с отдельных стадий экстракции. Очистка сырого антибиотика 107891 может быть осуществлена при помощи любого из известных способов, но предпочтительно ее осуществляют при помощи хроматографических процедур. Примеры этих хроматографических процедур представляют собой способы, о которых сообщали в связи со стадией выделения, и включают также хроматографию на стационарных фазах, таких как хроматография на силикагеле, оксиде алюминия, активированном силикате магния и т.п., или хроматографию с обращенной фазой на силанизированном силикагеле, имеющем различные функциональные дериватизации, и элюцию смешивающимися с водой растворителями или водной смесью смешивающихся с водой растворителей, имеющих упомянутый выше тип. Например, может быть использована препаративная ВЭЖХ хроматография с использованием RP-8 или RP-18 в качестве стационарной фазы и смеси буфер HCOONH4:CH3CN в качестве системы элюции. Активные фракции, выделенные на стадии очистки, объединяют, концентрируют в вакууме, осаждают путем добавления осаждающего агента упомянутых выше типов и сушат или лиофилизируют в единичном или повторяющихся циклах. В случае, когда продукт содержит остаточные количества формиата аммония или других буферных солей, они могут быть удалены путем абсорбции антибиотика 107891 на колонке для твердофазной экстракции, например колонке с обращено-фазовой смолой, такой как SPE Superclean LCP18 Supelco (Bellefonte PA, USA), с последующей промывкой дистиллированной водой и элюцией подходящей водной смесью растворителей, например этанол:вода. Затем антибиотик выделяют путем удаления элюирующих растворителей. Соответственно получают высушенный препарат очищенного антибиотического комплекса 107891 в виде белого порошка.-8 016608 Как обычно в этой области техники, стадию продуцирования, а также выделения и очистки можно контролировать при помощи различных аналитических процедур, включающих ингибиторный анализ против чувствительных микроорганизмов и аналитический контроль с использованием ВЭЖХ или ВЭЖХ в сочетании с масс-спектрометрией. Предпочтительный аналитический метод ВЭЖХ осуществляют на аппарате Waters (Waters(2504,6 мм), элюируя со скоростью потока 1 мл/мин при температуре 50C. Элюцию осуществляли в соответствии с многостадийной программой: время=0 (30% фаза Б); время=8 мин (30% фаза Б); время =28 мин (40% фаза Б). Фаза А представляла собой ацетонитрил: 100 мМ буфер формиата аммония (pH:5,0) 5:95 (об./об.), и фаза Б представляла собой ацетонитрил. УФ-детектор установлен на 282 нм. Вытекающий поток с колонки разделяли в отношении 5:95 и большую часть (приблизительно 950 мкл/мин) направляли в детектор на основе фотодиодной матрицы. Оставшееся количество(50 мкл/мин) направляли в интерфейс ESI (электрораспылительная ионизация) масс-спектрометра с ионной ловушкой Finnigan LCQ (Thermoquest, Finnigan MAT, San Jose CA). Масс-спектрометрический анализ осуществляли в следующих условиях. Условия при введении образца: струя газа (N2) 413,7 кПа (60 фунт-сила/кв.дюйм); вспомогательный газ (N2) 34,45 кПа (5 фунт-сила/кв.дюйм); нагрев капилляра 250C. Установки потенциала при введении образца: полярность положительная и отрицательная; потенциал ионораспыления 5 кВ; капиллярный потенциал 19 В. Условия сканирования: максимальное ионное время 200 мс; ионное время 5 мс; полное микросканирование 3; сегмент: длительность 30 мин, сканы положительные (150-2000 m/z) и отрицательные(150-2000 m/z). В этих аналитических условиях ВЭЖХ факторы A1 и A2 антибиотика 107891 демонстрировали времена удерживания соответственно 13,2 и 13,9 мин. В той же самой системе ВЭЖХ фактор A2 рамопланина (L. Gastaldo, R. Ciabatti, F. Assi, E. Restelli, J.K. Kettenring, L.F. Zerilli, G. Romano, M. Denaro andA'3 glycolipodepsipeptide antibiotics", J. Ind. Microbiol. 11: 13-18), элюировался с временем удерживания 7,5 мин. Факторы A1 и A2 антибиотика 107891 могут быть выделены из очищенного образца антибиотического комплекса 107891 посредством препаративной ВЭЖХ. Фактор A1 выделяли и очищали на колонке Symmetry Prep. C18 из очищенного антибиотического комплекса 107891, растворенного в смеси диметилсульфоксид (ДМСО):муравьиная кислота 95:5 (об./об.) с использованием линейного градиента элюции длительностью 25 мин от 30 до 45% фазы Б со скоростью потока 3,5 мл. Фаза Б представляла собой ацетонитрил. Фаза А представляла собой смесь 25 мМ буфер формиата аммония pH 4,5:ацетонитрил 95:5 (об./об.). Элюируемые фракции, содержащие чистый фактор A1 антибиотика 107891, объединяли и концентрировали в вакууме. Оставшийся раствор лиофилизировали с получением чистого фактора A1 в виде белого порошка. Фактор A2 выделяли и очищали посредством изократической элюции на колонке Symmetry Prep.C18 из образца очищенного антибиотического комплекса 107891, растворенного в смеси уксусная кислота:ацетонитрил: 100 мМ буфер формиат аммония (pH 4) 50:120:80 (об./об.). Изократическую элюцию осуществляли со скоростью потока 7 мл смесью 100 мМ буфер формиат аммония pH 4:ацетонитрил в отношении 82,5:17,5 (об./об.). Элюированные фракции, содержащие чистый фактор A2 антибиотика 107891, объединяли и концентрировали в вакууме. Оставшийся раствор лиофилизировали с получением чистого фактора A2 в виде белого порошка. Поскольку в соответствии с результатами кислотного/основного титрования в смеси 2-метоксиэтанол (MCS):H2O 12:3 (об./об.) антибиотик 107891 содержит основную функцию, он способен образовывать соли с подходящими кислотами в соответствии с обычными способами и может существовать также в форме свободного основания. Антибиотик 107891, полученный в форме свободного основания, может быть превращен с использованием кислот в соответствующие соли, включающие нетоксичные фармацевтически приемлемые соли. Подходящие соли включают соли, образованные путем стандартной реакции с органическими и неорганическими кислотами, такими как, например, соляная, бромисто-водородная, серная, ортофосфор-9 016608 ная, уксусная, трифторуксусная, трихлоруксусная, янтарная, лимонная, аскорбиновая, молочная, малеиновая, фумаровая, пальмитиновая, холевая, памоевая, муциновая, глутамовая, камфорная, глутаровая,гликолевая, фталевая, винная, лауриновая, стеариновая, салициловая, метансульфоновая, бензолсульфоновая, сорбиновая, пикриновая, бензойная, коричная кислоты и т.п. Соли присоединения кислот антибиотика 107891 могут быть получены в соответствии с обычными способами. В качестве примера антибиотик 107891 в форме свободного основания растворяют в минимальном количестве подходящего растворителя, типично низшего алканола, или смеси низший алканол/вода, стехиометрическое количество подходящей выбранной кислоты постепенно добавляют к полученному раствору и полученную соль осаждают путем добавления нерастворителя. Образовавшуюся соль присоединения затем выделяют путем фильтрации или выпаривания растворителей. Альтернативно, эти соли могут быть получены, по существу, в безводной форме путем лиофилизации; в этом случае соль антибиотика 107891 с летучей кислотой растворяют в подходящем количестве нелетучей кислоты. Затем из раствора отфильтровывают все нерастворимые вещества и раствор лиофилизируют в течение единичного или повторяющихся раундов. Конкретная соль присоединения также может быть получена из раствора другой солевой формы антибиотика 107891, если желаемая соль осаждается при добавлении подходящего аниона. Превращение несолевого соединения по изобретению в соответствующие соли присоединения, и наоборот, т.е. превращение соли присоединения соединения по изобретению в несолевую форму, находятся в пределах знаний специалиста в данной области техники и охвачены настоящим изобретением. Образование солей антибиотика 107891 может решать несколько задач, включая выделение, очистку указанного антибиотика 107891 и его применение в качестве терапевтических агентов или промоторов роста животного. Для терапевтических задач обычно используют фармацевтически приемлемые соли. Термин "фармацевически приемлемые соли" относится к нетоксичным солям, которые могут быть использованы в терапии теплокровных животных. Антибиотик 107981 может быть введен сам по себе или в смесях с фармацевтически приемлемыми носителями и также может быть введен в сочетании с другими антимикробными агентами, такими как пенициллины, цефалоспорины, аминогликозиды и гликопептиды. Таким образом, комбинированная терапия включает последовательное, одновременное и раздельное введение активного соединения таким образом, что терапевтические эффекты первого вводимого соединения полностью не исчезают к тому моменту, когда вводят последующее. Соединения по изобретению или их фармацевтически приемлемые соли присоединения могут быть приготовлены в формах, подходящих для парентерального, перорального или местного введения. Для внутривенного (в.в.) введения при лечении любой инфекции, включающей микроорганизм, чувствительный к антибиотику, препарат для парентерального введения находится, например, в воде с подходящим солюбилизирующим агентом, таким как полипропиленгликоль или диметилацетамид, и поверхностноактивным агентом (например, полиоксиэтиленсорбитана моноолеатом или полиэтокилированным касторовым маслом) или в композициях на основе циклодекстринов или фосфолипидов в стерильнойводе для инъекции. Инъецируемый препарат также может быть приготовлен с подходящим циклодекстрином. Антибиотик 107981 также может быть использован в подходящей фармацевтической форме, такой как капсула, таблетка или водная суспензия для перорального введения, или с обычными кремами или гелями для местных применений. Помимо применения в качестве лекарственных средств в терапии и ветеринарии, соединения по изобретению также могут быть использованы в качестве промотора роста животных. Для этой задачи соединение по изобретению вводят перорально в подходящем корме. Точная используемая концентрация представляет собой концентрацию, которая требуется для обеспечения активного агента в количестве, эффективном для стимуляции роста, когда потребляют нормальные количества корма. Добавление активного соединения по изобретению в корм животных предпочтительно осуществляют путем приготовления подходящего кормового премикса, содержащего активное соединение в эффективном количестве, и включения премикса в полный рацион. Альтернативно, промежуточный концентрат или пищевая добавка, содержащая активный ингредиент, может быть смешана с кормом. Способ, при помощи которого такие кормовые премиксы и полные рационы могут быть приготовлены и введены, описаны в книгах (таких как "Applied Animal Nutrition", W.H. Freedman and CO., S. Francisco,U.S.A., 1969 или "Livestock Feeds and Feeding" 0 и B books, Corvallis, Ore., U.S.A., 1977). Физико-химические характеристики антибиотика 107891. А) Масс-спектрометрия. В экспериментах с использованием масс-спектрометрии (MC) на аппарате Thermofinnigan LCQdeca, оборудованном источником электрораспыления, с использованием калибровочной смеси Thermofinnigan антибиотик 107891 давал два дважды протонированных иона с m/z = 1124 и m/z = 1116, соответствующие низшей изотопной композиции факторов A1 и A2 комплекса соответственно.- 10016608 Условия электрораспыления: напряжение при распылении: 4,7 кВ; температура капилляра: 220C; капиллярное напряжение: 3B; режим введения 10 мкл/мин. Спектры регистрировали в растворе с концентрацией 0,2 мг/мл в смеси метанол/вода 80/20 (об./об.) с трифторуксусной кислотой 0,1% и они представлены на фиг. 1 А (спектр низкого разрешения при полном сканировании) и фиг. 1 Б (спектр высокого разрешения при сканировании с масштабированием). Б) Инфракрасный спектр антибиотика 107891, снятый в KBr с использованием спектрофотометра для инфракрасной спектрометрии с преобразованием Фурье Bruker FT-IR модель IFS 48, демонстрирует максимумы абсорбции при (см-1): 3263; 2929; 1661; 1533; 1402; 1114; 1026; инфракрасный спектр представлен на фиг. 2. Полосы абсорбции при 1631, 1596 и 1346 относятся к остаточным количествам формиата аммония. В) УФ-спектр антибиотика 107891 в смеси метанол/H2O (в отношении 80:20) с использованием спектрофотометра Perkin-Elmer Lambda 16 демонстрирует два плеча при 226 и 267 нм. УФ-спектр представлен на фиг. 3. Г) Спектр 1H-ядерного магнитного резонанса (ЯМР) регистрировали в смеси метанол-d4:H2O (pH 4,3 HCl) 40:10 (об./об.) при 40C на спектрометре Bruker AMX 600 с применением последовательности вытеснения воды. В качестве внутреннего стандарта рассматривали остаточный сигнал метанол-d4 при 3,31 м.д. 1H-ЯМР спектр антибиотика 107891 представлен на фиг. 4. 1H-ЯМР спектр антибиотика 107891,растворенного в смеси метанол-d4:H2O (0,01 н. HCl) 40:10 (об./об.) демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием MeOH-d4 в качестве внутреннего стандарта (3,31 м.д.)(перекрывающиеся CH3), 1,26 s (CH3), 1,30 t (перекрывающиеся CH3), 1,62-1,74 m (CH2), 1,78 d (CH3),1,80 d (CH3), 2,03 m (CH2), 2,24 m (CH), 2,36 m (CH2), 2,72-3,8 m (пептидные альфа CH), 3,8-5,2 m (пептидные альфа CH), 5,53-6,08 s (CH2), 5,62 d (CH двойной связи), 6,42 m (CH), 6,92 d (CH двойной связи),7,0-7,55 m (ароматические CH), 7,62-10,4 d и m (ароматические и пептидные NH). Д) 13C-ЯМР спектр регистрировали в смеси метанол-d4:H2O (pH 4,3 HCl) 40:10 (об./об.) при 40C на спектрометре Bruker AMX 600, с использованием в качестве внутреннего стандарта остаточного сигнала метанол-d4 при 49,15 м.д. 13C-ЯМР bb-несвязанный спектр антибиотика 107891 представлен на фиг. 5. 13(об./об.), демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием MeOH-d4 в качестве внутреннего стандарта (49,15 м.д.), [=м.д.; (соотнесение)]: 13,6-23,2 (алифатические CH3),26,16-73 (алифатические CH2 и пептидные альфа CH), 105-136 (ароматические CH и CH двойных связей и четвертичные атомы углерода), 164,3-176,3 (пептидные карбонилы). Е) Антибиотик 107891 растворяли в смеси 2-метоксиэтанол (MCS):H2O 12:3 (об./об.), содержащей молярный избыток 0,01 М соляной кислоты. Раствор затем вновь титровали раствором 0,01 н. гидроксида калия. Получающаяся в результате кривая титрования демонстрировала одну основную ионизируемую функцию. Аминокислотный состав антибиотика 107891. А) Определение "кислотоустойчивых" аминокислот в антибиотике 107891. Антибиотик 107891 подвергали полному кислотному гидролизу (HCl 6 н., 105C, 24 ч) и идентифицировали аминокислотные компоненты антибиотика, устойчивые к обработке кислотой. Кислотолабильные аминокислоты при использовании этого подхода не обнаружимы. Гидролизат исследовали при помощи анализа путем ВЭЖХ-MC и газовой хроматографии/масс-спектрометрии (ГХ-МС) после соответствующей дериватизации в сравнении со смесью стандартных аминокислот, дериватизированных аналогичным образом. Для анализа путем ВЭЖХ гидролизованный образец обрабатывали 6-аминохинолил-Nгидроксисукцинимидилкарбаматом (набор реагентов AccQ-Tag Fluor), для анализа путем ГХ - смесью 3 н. HCl в безводном метаноле и трифторуксусном ангидриде. Количественный анализ путем ВЭЖХ осуществляли на системе жидкостной хроматографии с одновременной детекцией с помощью диодной матрицы (ДДМ) и MC. Условия для ВЭЖХ: колонка: AccQ-Tag (Waters C18 NovoPak 4 мкм 3,9150 мм); температура колонки: 37C; поток: 1 мл/мин; фаза А: ацетат аммония 140 мМ pH 5 (уксусная кислота); фаза Б: вода:ацетонитрил 60:40 (об./об.). УФ-детекция: 254 нм. Условия МС: спектрометр: Finnigan LCQ Deca, оборудованный стандартным источником электрораспыления; температура капилляра: 250C; напряжение источника: 4,70 кВ; ток источника: 80 мкА; капиллярное напряжение: -15 В; Количественный анализ путем ГХ осуществляли на газовом хроматографе с МС-ЭИ (электрораспыление) детекцией. Условия ГХ: колонка: JW Scientific DB-5, 30 м 0,254 мм внутренний диаметр (В.Д.)0,25 мкм FT; газ-носитель: гелий; режим инъекции: без разделения; температура инжектора: 200C; температура трубок: 300C; температурная программа: от 50 до 100C со скоростью 2,5C/мин (10 мин), от 100 до 250C со скоростью 10C/мин (15 мин), 15 мин при 250C; инъецируемый объем: 1 мкл. Условия МС: спектрометр: Finnigan TSQ700; режим ионизации: электронный удар; параметры напряжения: ток накала: 400 мА; электронный умножитель: 1400 В; энергия электрона: 70 эВ; Режим положительных ионов Условия сканирования: диапазон сканирования: 40-650 amu: время сканирования: 1 с. В хроматограммах ЖХ/МС и ГХ/МС, полученных на гидролизате антибиотика 107891, вместе с другими неидентифицированными пиками были идентифицированы следующие аминокислоты: лантионин, метиллантионин, глицин, пролин, валин, аспарагиновая кислота (исследования путем ЯМР указывают на то, что она представляет собой продукт превращения аспарагина, приводящего к образованию аспарагиновой кислоты путем гидролиза), фенилаланин и лейцин. Факторы A1 и A2 антибиотика 107891 подвергали полному кислотному гидролизу в тех же самых условиях (дериватизация и ВЭЖХ-МС), которые приведены для комплекса. Анализ путем ГХ-МС проводили на приборе для ГХ/МС Thermo Finnigan Trace, оборудованном инжектором-испарителем с программируемой температурой (PTV). Способ путем ГХ осуществляли в следующих условиях: колонка: Restek RTX-5MS, 15 м 0,25 мм В.Д.0,25 мкм FT; гз-носитель: гелий; температура границы: 250C; температурная программа: 1,5 мин при 50C, от 50 до 100C при 20C/мин, 1 мин при 100C, от 100 до 135C при 20C/мин, 1 мин при 135C, от 135 до 250C при 20C/мин, 1 мин при 250C; инъецируемый объем: 1 мкл; инжектор: режим без разделения, базовая температура 50C, температура переноса 280C, скорость увеличения температуры 14,5C/мин. Условия МС: режим ионизации: электронный удар. Установки напряжения: ток накала: 149 мкА; электронный умножитель: 200 В; энергия электрона: 70 эВ. Режим положительных ионов.- 12016608 Условия сканирования: диапазон сканирования: 33-500 amu; время сканирования: 0,6 с. В гидролизате фактора A1 антибиотика 107891 хроматограммы ВЭЖХ/МС и ГХ/МС демонстрировали вместе с другими неидентифицированными пиками присутствие следующих аминокислот: лантионина, метиллантионина, глицина, пролина, валина, аспарагиновой кислоты (исследования путем ЯМР указывают на то, что она представляет собой продукт превращения аспарагина, приводящего к образованию аспарагиновой кислоты путем гидролиза), фенилаланина и лейцина. Вышеприведенный способ, использованный для фактора A2, выявил вместе с другими неидентифицированными пиками присутствие следующих аминокислот: лантионина, метиллантионина, глицина,пролина, валина, аспарагиновой кислоты (исследования путем ЯМР указывают на то, что она представляет собой продукт превращения аспарагина, приводящего к образованию аспарагиновой кислоты путем гидролиза), фенилаланина и лейцина. Б) Определение 5-хлортриптофана в антибиотике 107891 и в его факторе A1 и факторе A2. Полный гидролиз очищенного антибиотика 107891 и его отдельных факторов A1 и A2 осуществляли в соответствии со способом, описанным Simpson R.J., Neuberger M.R., Liu T.Y., "Complete AminoacidAnalysis of Proteins from a Single Hydrolysate". Journal Biol. Chem. (United States), April 10, 1976, 251 (7),1936-40. Эта процедура гидролиза позволяет предотвратить деградацию аминокислот, обычно нестабильных во время расщепления неорганическими кислотами, и таким образом дает возможность для определения этих аминокислот, включающих триптофан, из гидролизата пептида. Стандартный образец 5-хлор-DLтриптофана был приобретен в Biosynt A.G., Staad, Switzerland и его структура подтверждена при помощи анализа путем ЯМР; DL-триптофан был приобретен в Merck KGaA, Darmstadt, Germany. Фактор A1 (1,5 мг) суспендировали в 0,6 мл 4 н. метансульфоновой кислоты, содержащей 0,2%(мас./об.) 3-(2-аминоэтил)индола в качестве катализатора для гидролиза. Гидролиз осуществляли при 115C в течение 16 ч. Гидролизат затем нейтрализовали 5 н. NaOH и разбавляли равным количеством дистиллированной воды. 100 мкл этого раствора анализировали путем ЖХ/МС. Разделение осуществляли на колонке Symmetry C18 (5 мкм) 4,6250 мм (Waters Co. Milford MA, USA), оборудованной предколонкой Symmetry C18 (5 мкм) 3,920 мм. Элюцию осуществляли при скорости потока 1 мл/мин в течение 25 мин. Линейный градиент от 0 до 50% фазы Б. Фаза A представляла собой смесь 25 мМ буферHCOONH4 pH 4,5:CH3CN 95:5 (об./об.), и фаза Б представляла собой CH3CN. УФ-обнаружение проводили при 280 нм. Оборудование для ВЭЖХ находилось в тандеме с масс-спектрометром с ионной ловушкой Finnigan LCQ (Thermoquest, Finnigan MAT, San Jose, CA, USA). 50 мкл/мин вытекающего потока с колонки направляли в интерфейс ионизации электрораспылением (ИЭР) масс-спектрометра LCQ. Анализ путем MC осуществляли в следующих условиях: ввод образца: газ-носитель (N2) 413,7 кПа (60 фунтсила/кв.дюйм); нагрев капилляра 210C; полярность напряжения при вводе образца: положительная и отрицательная; напряжение распыления ионов 4,5 кВ; напряжение капилляра 21 В; условия сканирования: максимальное ионное время 50 мс; полное микро: скан 3. Стандарты триптофана и 5-хлортриптофана элюировали с временами удерживания 8,1 и 11,5 мин,соответствующими M+H+ с m/z 205 и 239 соответственно. В гидролизате фактора A1 антибиотика 107891 присутствие пика на 11,5 мин для m/z с 238,97 указывало на присутствие 5-хлортриптофана. Стандарт триптофана обнаруживали при помощи хроматографической системы с пределом обнаружения 0,3 мкг/мл. Это значение было ниже значения, которое указывало бы на присутствие указанной аминокислоты в тестируемом образце антибиотика. Триптофан не был обнаружен выше указанного предела на хроматограмме гидролизата фактора A1 антибиотика 107891. Идентичные результаты были получены в результате анализа путем ЖХ/МС гидролизата фактора A2 и гидролизата очищенного образца антибиотического комплекса 107891. Масс-спектрометрия фактора A1 и фактора A2 антибиотика 107891. Фактор A1 антибиотика 107891 дает дважды протонированный ион с m/z=1124, а фактор A2 - сm/z = 1116, соответствующим наименьшей изотопоной композицией в экспериментах MC на прибореThermoflnnigan LCQ deca, оборудованном источником электрораспыления, с использованием калибровочной смеси Thermofinnigan. Условия электрораспыления: напряжение распыления: 4,7 кВ; температура капилляра: 250C; напряжение капилляра: 8 В; режим введения: 10 мкл/мин. Спектры регистрировали в растворе 0,1 мг/мл в смеси ацетонитрил:вода 50:50 (об./об.) с 0,5% уксусной кислоты, и они представлены на фиг. 6A (полный спектр низкого разрешения) и фиг. 6 Б (масштабированный спектр высокого разрешения), а также на фиг. 7 А (полный спектр низкого разрешения) и фиг. 7 Б (масштабированный спектр высокого разрешения). Точную массу фактора A1 и фактора A2 антибиотика определяли путем использования спектрометра Bruker Daltonics APEX II, 4.7 Tesla, оборудованного источником электрораспыления. На основе этих данных для фактора A1 установлена молекулярная масса 2246,710,06, рассчитанная моноизотопная масса от [M+2H]2+ с m/z 1124,36124 (точность 30 м.д.), определенная при помощи ИЭР-масс- 13016608 спектрометрии с преобразованием Фурье (МСПФ). Для фактора A2 установлена молекулярная масса 2230,710,06, рассчитанная моноизотопная масса от [M+2H]2+ с m/z 1116,36260 (точность 30 млн-1), определенная при помощи ИЭР-МСПФ. Сравнение факторов A1 и A2 антибиотика 107891 с антибиотиками MF-BA-17681 иA) Microbispora corallina NNRL 30420 (MF-BA-1768), описанный в US 6551591 B1, приобрели из коллекции NNRL. В пробном эксперименте штамм M.corallina NNRL 30420 (MF-BA-1768) ферментировали в колбе Эрленмейера в условиях, описанных в US 6551591 B1. Собранный бульон экстрагировали путем разведения метанолом. После отделения мицелия центрифугированием супернатант наносили на полистирольную абсорбирующую смолу HP20, элюировали смесью метанол:вода 70:30, объем которой уменьшали до небольшого объема и затем лиофилизировали. На хроматограмме два пика демонстрировали сигналы 1091 и 1108 [M+2H]2+, соответствующие[M+2H]2+, о которых сообщали в US 6551581 B1 для MF-BA-17681 и MF-BA-17681 соответственно. В вышеприведенный экстракт затем добавляли факторы A1 и A2 антибиотика 107891 и смесь анализировали путем ЖХ/МС. Обнаружили, что пики антибиотиков MF-BA-17681 и MF-BA-17681 и факторов A1 и A2 антибиотика 107891 обладают различными временами удерживания и различными MC фрагментами [M+2H]+. Б) В еще одном эксперименте ферментацию Microbispora sp. штамм NRRL 30420 (MF-BA-1768) проводили в танке объемом 30 л и собранный бульон обрабатывали в соответствующим с описаниемUS 6551591 B1. После стадий последовательной очистки на полистирольной смоле HP20 и полиамидной смоле CC 6 0,1-0,3 мм (Macherey-Nagel) получали два индивидуальных вещества в чистой форме при помощи препаративной ВЭЖХ на колонке C18 Phenomenex (Torrance CA, USA) Luna (25012,2 мм) с размером частиц 10 мкм, элюируя при скорости потока 27 мл/мин в соответствии со следующей многостадийной программой: время=0 мин (32% фазы Б); время=8 мин (32% фазы Б); время=20 мин (36% фазы Б); время=32 мин (90% фазы Б). Фаза А представляла собой 0,05%-ную (об./об.) муравьиную кислоту в воде, фаза Б представляла собой CH3CN. Эти вещества демонстрировали антибактериальную активность против стафилококков и энтерококков, как представлено в табл. IV. В экспериментах с использованием ЖХ/МС эти два вещества продемонстрировали сигналы для двойных протонированных ионов [M+2H], соответствующие антибиотику Экспериментальные условия антимикробных тестов были теми же, что и используемые для тестов,представленных в табл. VI. Анализы путем ЖХ/МС выделенных антибиотиков MF-BA-17681 и MF-BA-17681 проводили на колонке Symmetry C18 (5:м) 4,6250 мм (Waters; Milford MA, USA), оборудованной предколонкойSymmetry C18 (5:м) 3,920 мм (обе держали в термостате при температуре 50C). Элюцию осуществляли при скорости потока 1 мл/мин со следующей многостадийной программой элюции: время=0 мин (30% фазы Б); время=8 мин (30% фазы Б); время=20 мин (45% фазы В); время=24 мин (90% фазы Б) и время=28 мин (90% фазы Б). Фаза А представляла собой смесь 25 мМ буфер HCOONH4 pH 4,5:CH3CN 95:5 (об./об.), и фаза Б представляла собой CH3CN. Оборудование ВЭЖХ находилось в тандеме с массспектрометром с ионной ловушкой Finnigan LCQ (Thermoquest, Finnigan MAT, San Jose CA, USA). 100 мкл/мин выходного потока из колонки направляли в ИЭР интерфейс масс-спектрометра LCQ. Анализ путем MC осуществляли в следующих условиях: ввод образца: газ-носитель (N2) 172,375 кПа(25 фунт-сила/кв.дюйм); поток вспомогательного газа 34,475 кПа (5 фунт-сила/кв.дюйм); нагрев капилляра 210C; полярность напряжения при вводе образца: положительная и отрицательная; напряжение- 14016608 распыления ионов 4,75 кВ; напряжение капилляра 12 В; условия сканирования: максимальное время ионов 50 мс; полный микро: скан 3. Индивидуальные антибиотические факторы MF-BA-17681 и MF-BA-17681 и факторы A1 и A2 антибиотика 107891 анализировали индивидуально и в смеси. Результаты собраны в табл. V. Таблица V В той же самой хроматографической системе фактор A2 рамопланина (L. Gastaldo, R. Ciabatti,F. Assi, E. Restelli, J.K. Kettenring, L.F. Zerilli, G. Romano, M. Denaro and B. Cavalleri, (1992): "Isolation,structure determination and biological activity of A-16686 Factors A'1, A'2 и A'3 glycolipodepsipeptideCD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600 с применением последовательности вытеснения воды. В качестве внутреннего стандарта рассматривали остаточный сигнал ацетонитрил-d3 при 1,94 м.д. А) 1H-ЯМР спектр фактора A1 антибиотика 107891 представлен на фиг. 8. 1H-ЯМР спектр фактора A1 антибиотика 107891, растворенного в смеси CD3CN:DH2O (1:1) демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием CD3CN в качестве внутреннего стандарта (1,94 м.д.) [=м.д. мультиплетность; (соотнесение)]: 0,84 d (CH3), 0,89 d (CH3), 0,94 t(CH3), 1,75 m (CH2), 2,11 m (CH), 2,26 m (CH), 2,5 m (CH2), 2,68-3,8 m (пептидные CH), 3,8-5,0 m (пептидные CH), 5,45-6,17 s (CH2), 5,58 d (CH двойной связи), 6,36 m (CH), 6,86 d (CH двойной связи), 7,07,45 m (ароматические CH). В качестве примесей присутствуют сигнал для диметилсульфоксида при 2,58 м.д. и сигнал для формиата при 8,33 м.д. Б) 1H-ЯМР bb несвязанный спектр фактора A2 антибиотика 107891 представлен на фиг. 9. 1H-ЯМР спектр фактора A2 антибиотика 107891, растворенного в смеси CD3CN:D2O (1:1), демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием CD3CN в качестве внутреннего стандарта (1,94 м.д.), [=м.д., мультиплетность; (соотнесение)]: 0,84 d (CH3), 0,88 d (CH3), 0,94 d(CH3), 1,06 d (CH3), 1,14 d (CH3), 148 m (CH2), 1,65-1,75 m (CH2), 1,67 d (CH3), 2,15 m (CH), 2,25 m (CH),2,5 m (CH2), 2,77-3,8 m (пептидные CH), 3,8-4,9 m (пептидные CH), 5,45-6,14 s (CH2), 5,59 d (CH двойной связи), 6,34 m (CH), 6,84 d (CH двойной связи), 7,0-7,42 m (ароматические CH). В качестве примесей также присутствуют сигнал для диметилсульфоксида при 2,58 м.д. и сигнал для формиата при 8,32 м.д. 13CD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600 с применением в качестве внутреннего стандарта остаточного сигнала ацетонитрил-d3 при 1,39 м.д. В) 13C-ЯМР спектр фактора A1 антибиотика 107891 представлен на фиг. 10. 13 С-ЯМР спектр фактора A1 антибиотика 107891, растворенного в смеси CD3CN:D2O (1:1), демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием CD3CN в качестве внутреннего стандарта (1,39 м.д.), [=м.д.; (соотнесение)]: 13,6-23,03 (алифатические CH3), 25,69-77,9 (алифатические CH2 и пептидные CH), 105-137,3 (ароматические и двойные связи CH и четвертичные атомы углерода), 165,6-176,6 (пептидные карбонилы). Г) 13C-ЯМР bb несвязанный спектр фактора A2 антибиотика 107891 представлен на фиг. 11. 13C-ЯМР спектр фактора A2 антибиотика 107891, растворенного в смеси CD3CN:D2O (1:1), демонстрирует следующие группы сигналов (в м.д.) при 600 МГц с использованием CD3CN в качестве внутреннего стандарта (1,39 м.д.), [=м.д.; (соотнесение)]: 13,6-22,9 (алифатические CH3), 25,65-73 (алифатические CH2 и пептидные CH), 105-137,3 (ароматические CH и CH двойных связей и четвертичные атомы углерода), 165,7-176,1 (пептидные карбонилы). УФ и инфракрасные (ИК) спектры фактора A1 и фактора A2 антибиотика 107891. А) Инфракрасный спектр фактора A1 антибиотика 107891, зарегистрированный в KBr с использованием спектрофотометра Bruker FT-IR модели IFS 48, демонстрирует максимумы абсорбции при (см-1): 3294; 3059; 2926; 1661; 1529; 1433; 1407; 1287; 1114; 1021. Инфракрасный спектр представлен на фиг. 12. Б) УФ-спектр фактора A1 антибиотика 107891, зарегистрированный в смеси метанол:H2O 80:20(об./об.) с использованием спектрофотометра Perkin-Elmer Lambda 16, демонстрирует два плеча при 226 и 267 нм. УФ-спектр представлен на фиг. 13.- 15016608 В) Инфракрасный спектр фактора A2 антибиотика 107891, зарегистрированный в KBr с использованием спектрофотометра Bruker FT-IR модели IFS 48, демонстрирует максимум абсорбции при (см-1): 3296; 3060; 2928; 1661; 1529; 1433; 1407; 1288; 1116. Инфракрасный спектр представлен на фиг. 14. Г) УФ-спектр фактора A2 антибиотика 107891, зарегистрированный в смеси метанол:H2O 80:20(об./об.) с использованием спектрофотометра Perkin-Elmer Lambda 16, демонстрирует два плеча при 226 и 267 нм. УФ-спектр представлен на фиг. 15. На основе вышеприведенных физико-химических данных для антибиотика 107891 может быть установлена следующая структурная формула: где X представляет собой H или галоген (F, Cl, Br, I), Y1, Y2, Y3, Y4 и Y5 независимо могут представлять собой S, S-O-, S=O, OS=O и O=S=O и R1, R2, R3, R4, R5, R6, R7 и R8 независимо могут представлять собой H и OH, при условии, что по меньшей мере один из Y1, Y2, Y3, Y4 и Y5 не представляет собой S. В альтернативном воплощении R1, R2, R3 и R4 могут представлять собой H или OH. Таким образом,возможные комбинации R1, R2, R3 и R4 включают следующие. Аналогично, R5, R6, R7 и R8 могут представлять собой H или OH. Таким образом, возможные комбинации R5, R6, R7 и R8 включают следующие. Биологическая активность антибиотика 107891 in vitro. Антимикробную активность антибиотика 107891 определяли при помощи способа микроразведения питательной среды в соответствии с рекомендациями Национального комитета по клиническим лабораторным стандартам (NCCLS, документ M7-A5). Используемые штаммы представляли собой клинические изоляты или штаммы из Американской коллекции типовых культур (ATCC). Результаты тестов представлены в табл. VI и VII. Антибиотик 107891 растворяли в диметилсульфоксиде (ДМСО) для получения концентрированного раствора 1000 мкг/мл и затем разбавляли водой для получения рабочего раствора. Используемые среды представляли собой катионо-регулируемую среду Мюллера-Хинтона (CAMHB) для Staphylococci,M.catarrhalis, Enterococci и L.monocytogenes; среду Тодда-Хевитта (THB) для Streptococci; среду GC + 1%Brucella, содержащую цистеин (0,5 г/л) для Propionibacteria. Инокулюмы для бактерий составляли 105 колониеобразующих единиц (КОЕ)/мл. ИнокулюмC.albicans составлял 1104 КОЕ/мл. Все тесты проводили в присутствии 0,02% бычьего сывороточного альбумина (БСА). Культуры инкубировали при 35C на воздухе за исключением штаммов Clostridia иPropioniobacteria, которые требовали анаэробной атмосферы. Через 18-24 ч осуществляли визуальные наблюдения и определяли МИК. МИК определяли как наименьшую концентрацию антибиотика, при которой визуальный рост отсутствовал.- 17016608 Таблица VI Антимикробная активность антибиотика 107891- 18016608 Таблица VII Антимикробная активность антибиотика 107891 против анаэробных бактерий Антибиотик 107891 демонстрирует хорошую антибактериальную активность против грамположительных бактерий. Диапазон МИК против Staphylococcus spp., включая штаммы, резистентные к метициллину (MRSA) и гликопептидным промежуточным соединениям (GISA), составляет 0,13-4 мкг/мл, а против полученных недавно клинических изолятов Enterococcus spp., включая резистентные к ванкомицину (VRE), составляет 0,5-4 мкг/мл. МИК против Streptococcus spp. составляют не более 0,13 мкг/мл. Антибиотик 107891 также активен против анаэробных грамположительных штаммов; величины МИК составляют не более 0,13 мкг/мл против Clostridia и не более 0,004-4 мкг/мл противPropionibacteria. Антимикробные активности продемонстрированы против L.monocytogenes (МИК 0,125 мкг/мл) и штаммов Lactobacilli (диапазон МИК не более 0,13-4 мкг/мл). Некоторые грамотрицательные бактерии чувствительны к антибиотику 107891; МИК составляют 1-0,25 мкг/мл против М.catharralis, 0,5-0,25 мкг/мл против Neisseria spp. и 32 мкг/мл против H.influenzae. Антибиотик 107891 не активен против тестированных штаммов E.coli и C.albicans. В экспериментах с киллингом в зависимости от времени антибиотик 107891 демонстрирует бактерицидную активность против штамма S.aureus GISA и E.faecalis VanA; через 24 ч бактерицидная концентрация представляет собой значение МИК в среде Мюллера-Хинтона.S.aureus может вызывать угрожающие жизни инфекции, и MRSA имеет особенную клиническую значимость, поскольку он резистентен ко всем пенициллинам и цефалоспоринам, а также к множеству других антибиотиков; дополнительно он легко передается от пациента к пациенту, вызывая вспышку инфекции с серьезными осложнениями для здравоохранения (W. Witte, (1999): "Antibiotic resistance inGram-positive bacteria: epidemiological aspects", Journal of Antimicrobial Chemotherapy. 44: 1-9). Центр по контролю за заболеваниями (CDC) Национальной системы по контролю за нозокомиальными инфекциями (NNIS) сообщает, что резистентность к метициллину у S.aureus в госпиталях США увеличилась с 2,4% в 1975 г. до 29% в 1991 г., с большей степенью резистентности в отделениях интенсивной терапииcare unit", Clinic Infect. Dis. 24: 211-5). Нозокомиальные стафилококковые инфекции ассоциируются со значительной заболеваемостью и смертностью, увеличивая длительность пребывания в госпитале и повышая стоимость госпитализации. Большая часть штаммов MRSA резистентна к нескольким из наиболее часто используемых антимикробных агентов, включая используемые в настоящее время макролиды,аминогликозидные и -лактамовые антибиотики, включая самое последнее поколение цефалоспоринов. Приобретаемые в госпитале резистентные к ванкомицину патогены, ответственные за инфекции(такие как эндокардит, менингит и септицемия), составляют прогрессирующую терапевтическую проблему (Y. Cetinkaya, P. FaIk and C.G. Mayhall, (2000): "Vancomycin-resistant enterococci", Clin. Microbiol.S.pneumoniae и M.catarrhalis представляют собой известные серьезные патогены людей. Они являются распространенной причиной инфекций респираторного тракта, в частности отита среднего уха у детей и инфекций нижнего отдела респираторного тракта у пожилых людей. M.catarrhalis и S.pneumoniae недавно были признаны самыми распространенными патогенами респираторного тракта (M.C. EnrightClostridia ответственны за различные заболевания: газовую гангрену и родственные раневые инфекции, столбняк, ботулизм, диарею, ассоциирующуюся с антибиотиками (CDAD), и псевдомембранозный колит. Большая часть этих микроорганизмов продуцирует экзотоксины, играющие важную роль в патогенезе заболеваний. C.difficile представляет собой возбудитель, ответственный за 25% случаевCDAD и, по существу, за все случаи псевдомембранозного колита. В течение последних нескольких лет случаи коинфекции C.difficile наблюдали у пациентов, страдающих от резистентной к ванкомицину энтерококковой инфекции или колонизации (J.G. Bartlett, (1992): "Antibiotic associated diarrhea", Clinic.Infect. Dis. 15: 573-581). Биологическая активность факторов A1 и A2 антибиотика 107891 in vitro. В табл. VIII представлены антимикробные активности индивидуальных факторов A1 и A2 антибиотика 107891. МИК определяли при помощи способа микроразведения среды, как описано выше. Таблица VIII Антимикробная активность факторов A1 и A2 антибиотика 107891 Биологическая активность антибиотика 107891 in vivo. Самок мышей ICR (Harlan Italia SpA - S. Pietro al Natisone, Italy) массой 23-25 г использовали в экспериментах с острой летальной инфекцией у иммунокомпетентных мышей или мышей, страдающих нейтропенией. Нейтропению вызывали путем интраперитонеальных введений циклофосфамида, 200 и 100 мг/кг, за четыре и одни сутки перед инфицированием мышей соответственно. Инфекцию вызывали путем интраперитонеальной инокуляции иммунокомпетентных мышей (8 животных/дозу/обрабатываемую группу) бактериальной суспензией клинического изолята стафилококка,резистентного к метициллину (Staph. aureus SA3817), или стандартного штамма, чувствительного к метициллину (Staph. aureus Smith ATCC19636), или путем инокуляции мышей, страдающих нейтропенией,клиническим изолятом энтерококка, резистентного к гликопептидам (Ent. faecalis A533). Бактериальные инфицирующие дозы (приблизительно 106 клеток/мышь) давали в виде суспензии в 0,5 мл 5%-ного бактериологического муцина (Difco). Необработанные животные погибали в течение 24-72 ч после инфицирования. Обработку антибиотиком начинали в течение 10-15 мин после инфицирования. Антибиотик 107891 вводили один раз внутривенно или подкожно в различных водных препаратах. 50%-ную эффективную дозу (ЭД 50) и 95%-ные доверительные интервалы рассчитывали методом Спирмана-Карбераassay, p. 524-530, Charles GriffinCo., Ltd., London), исходя из процентной доли животных, выживших- 20016608 на 7-е сутки. Результаты представлены в табл. IX. Антибиотик 107891 не токсичен вплоть до максимальной тестируемой дозы 200 мг/кг. Таблица IX ЭД 50 антибиотика 107891 при острых летальных инфекциях у мышейIII. VanA: Ent. faecalis A533, клинический изолят, у мышей с нейтропенией. Краткое описание графических материалов Фиг. 1 А (спектр низкого разрешения при полном сканировании) и фиг. 1 Б (масштабированный спектр высокого разрешения) представляют масс-спектры антибиотика 107891, демонстрирующие дважды протонированный ион с m/z 1124 и m/z 1116. Фиг. 2 представляет спектр ИК абсорбции антибиотика 107891, диспергированного в KBr. Фиг. 3 представляет УФ-спектр антибиотика 107891, растворенного в смеси метанол:H2O. Фиг. 4 представляет 1H-ЯМР спектр, зарегистрированный в смеси метанол-d4:H2O (pH 4,3 HCl) 40:10 (об./об.) при 40C на спектрометре Bruker AMX 600 с применением последовательности вытеснения воды. Фиг. 5 представляет 13C-ЯМР спектр, зарегистрированный в смеси метанол-d4:H2O (pH 4,3 HCl) 40:10 (об./об.) при 40C на спектрометре Broker AMX 600. Фиг. 6 А (спектр низкого разрешения при полном сканировании) и фиг. 6 Б (масштабированный спектр высокого разрешения) представляют масс-спектры фактора A1 антибиотика 107891, демонстрируя дважды протонированные ионы [M+2H]2+ с m/z 1124. Фиг. 7 А (спектр низкого разрешения при полном сканировании) и фиг. 7 Б (масштабированный спектр высокого разрешения) представляют масс-спектры фактора A2 антибиотика 107891, демонстрируя дважды протонированные ионы [M+2H] 2+ с m/z 1116. Фиг. 8 представляет 1H-ЯМР спектр фактора A1 антибиотика 107891, зарегистрированный в смесиCD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600 с применением последовательности вытеснения воды. Фиг. 9 представляет 1H-ЯМР спектр фактора A2 антибиотика 107891, зарегистрированный в смесиCD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600 с применением последовательности вытеснения воды. Фиг. 10 представляет 13C-ЯМР спектр фактора A1 антибиотика 107891, зарегистрированный в смеси CD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600. Фиг. 11 представляет 13C-ЯМР спектр фактора A2 антибиотика 107891, зарегистрированный в смеси CD3CN:D2O (1:1) при 298 К на спектрометре Bruker AMX 600. Фиг. 12 представляет спектр ИК абсорбции фактора A1 антибиотика 107891, диспергированного вKBr. Фиг. 13 представляет УФ-спектр фактора A1 антибиотика 107891, растворенного в смеси метанол:H2O. Фиг. 14 представляет спектр ИК абсорбции фактора A2 антибиотика 107891, диспергированного вMicrobispora sp. штамм ATCC PTA-5024 поддерживали на косяках из агара на основе овсяной муки в течение 2-3 недель при 28C. Содержимое с микробами с одного косяка смывали 5 мл стерильной воды и инокулировали в колбы Эрленмейера объемом 500 мл, содержащие 100 мл посевной среды (AF/MS),состоящей из (г/л): дектроза 20, дрожжевой экстракт 2, соевая мука 8, NaCl 1 и карбонат кальция 4. Среду готовили в дистиллированной воде и pH доводили до 7,3 перед стерилизацией при 121C в течение 20 мин. Инокулированное содержимое колб выращивали при 28C на роторной качалке, функционирующей при 200 об/мин. Через 4-6 дней 5% этой культуры инокулировали во вторую серию колб, содержащих ту же самую ферментационную среду. После инкубации в течение 72 ч 200 мл переносили в биореактор объемом 4 л, содержащий 3 л той же самой вегетативной среды. Ферментацию осуществляли при 30C с перемешиванием при 700 об/мин и аэрации 0,5 vvm (отношение количества подводимого воздуха к емкости реактора). Через 72 ч культуру (1,5 л) переносили в биореактор объемом 20 л, содержащий 15 л той же самой вегетативной среды. Ферментацию осуществляли в течение 48 ч при 30C при перемешивании при 500 об/мин и аэрации 0,5 vvm и затем переносили в производственный танк. Продукцию антибиотика 107891 осуществляли в ферментаторе объемом 300 л, содержащем 200 л продуцирующей среды M8, состоящей из (г/л): крахмал 20, глюкоза 10, дрожжевой экстракт 2, гидролизованный казеин 4, мясной экстракт 2 и карбонат кальция 3. Среду готовили в деионизированной воде,pH доводили до 7,2 перед стерилизацией при 121C в течение 25 мин. После охлаждения ферментатор инокулировали приблизительно 14 л (7%) предкультуры. Ферментатор запускали при 29C, при перемешивании 180 об/мин и аэрации 0,5 vvm при давлении на выходе 36 кПа (0,36 бар). Содержимое ферментатора собирали после 98 ч ферментации. Продукцию антибиотика 107891 контролировали путем ВЭЖХ, как описано ранее, после экстракции цельной культуральной жидкости таким же объемом метанола. Экстракцию проводили при комнатной температуре при перемешивании в течение 1 ч. Пример 2. Альтернативный способ ферментации Microbispora sp. ATCC PTA-5024.Microbispora sp. ATCC PTA-5024 инокулировали в колбы Эрленмейера объемом 500 мл, содержащие 100 мл ростовой среды (G1), состоящей из г/л: глюкоза 10, мальтоза 10, соевое масло 10, соевая мука 8, дрожжевой экстракт 2 и карбонат кальция 4. Среду готовили в деионизированной воде и стерилизовали при 120C20 мин без доведения pH. Инокулированные колбы инкубировали в течение 120-168 ч при 28C с перемешиванием при 200 об/мин до тех пор, пока не будет обнаружен хороший рост. Колбы затем использовали для инокуляции (3%) биореактора объемом 4 л, содержащего 3 л посевной среды AF/MS,приготовленной, как описано в примере 1. После ферментации в течение 120 ч при 30C с перемешиванием при 700 об/мин и аэрацией 0,5 vvm 1,5 л культуры переносили в биореактор объемом 20 л, содержащий 15 л такой же вегетативной среды. Ферментацию осуществляли в течение 96 ч при 30C при перемешивании при 600 об/мин и аэрации 0,5 vvm и затем переносили в производственный танк. Продукцию антибиотика осуществляли в ферментаторе объемом 300 л, содержащем 200 л продуцирующей среды (V6), состоящей из (г/л): дектроза 20, дрожжевой экстракт 5, мясной экстракт 5, гидролизованный казеин 3, пептон 5 и NaCl 1,5. Среду готовили в деионизированной воде с рН, доведенным до 7,5 с помощью NaOH, и стерилизовали при 121C в течение 20 мин. Ферментатор инокулировали 14 л посевной культуры (7%) и ферментацию осуществляли при 29C,перемешивали при 180 об/мин, аэрировали 100 л обычного воздуха в минуту (0,5 vvm). Продукцию антибиотика 107891 контролировали путем ВЭЖХ, как описано ранее. Ферментационную среду собирали приблизительно через 160 ч. Пример 3. Выделение антибиотика 107891. Ферментационный бульон, описанный в примере 1, фильтровали при помощи системы тангенциальной фильтрации (размер пор мембраны 0,1 мкм, Koch Carbo-Cor, Koch Wilmington, USA) с получением 170 л супернатанта и 30 л концентрированного мицелия. Антибиотический комплекс 107891 был обнаружен в фильтрате (А) и в мицелии (Б).(А) Профильтрованный бульон перемешивали в течение ночи при комнатной температуре в присутствии полистирольной смолы Diaion HP-20 (4 л). Смолу затем отделяли, промывали 10 л смеси метанол:вода 4:6 (об./об.) и партиями элюировали сначала 10 л смеси метанол:вода 9:1 (об./об.), а затем 10 л смеси метанол:бутанол:вода 9:1:1 (об./об.). Объединенные элюированные фракции, содержащие антибиотик 107891, концентрировали до небольшого объема на роторном испарителе и затем сушили замораживанием с получением 32 г неочищенного материала. Этот неочищенный материал растворяли в н-бутаноле (1 л) и затем трижды последовательно экстрагировали 800 мл воды. Органический слой концентрировали при пониженном давлении до маслянистого остатка, который растворяли в метаноле. После добавления петролейного эфира путем осаждения получали 5 г неочищенного препарата антибиотика.(Б) После добавления 25 л метанола порцию ретентата, содержащего мицелий, перемешивали в течение 1 ч и фильтровали с получением 45 л экстракта мицелия. Этот раствор затем разбавляли водой(20 л) и перемешивали в течение ночи при комнатной температуре с полистирольной смолой DiaionHP-20 (1 л). Затем смолу отделяли, промывали 2 л смеси метанол:вода 40:60 (об./об.) и партиями последовательно элюировали 3 л смеси метанол:вода 85:15 (об./об.) и затем 2 л смеси метанол:вода 90:10(об./об.). Элюируемые фракции контролировали в отношении присутствия антибиотика 107891 при помощи анализа диффузии на агаре с Staphylococcus aureus и при помощи способа аналитической ВЭЖХ,как сообщали ранее. Элюированные фракции, содержащие антибиотик 107891, объединяли, концентрировали при пониженном давлении и сушили замораживанием с получением 8,1 г неочищенного антибиотика 107891. Пример 4. Альтернативное выделение антибиотика 107891. Собранную среду из описанного в примере 2 ферментационного танка объемом 200 л доводили доpH 6,8 и фильтровали путем тангенциальной фильтрации (размер пор мембраны 0,1 мкм, KochCarbo-Cor). Фильтрат (180 л) партиями перемешивали в течение ночи при комнатной температуре с 2 л смолы Diaion HP20 (Mitsubishi Chemical) и смолу затем собирали. К порции ретентата, содержащего концентрированный мицелий, в аппарате для тангенциальной фильтрации (приблизительно 20 л) добавляли метанол (25 л). Эту суспензию перемешивали в течение 1 ч и затем фильтровали при помощи системы микрофильтрации до остаточного объема ретентата приблизительно 20 л. Затем добавляли дополнительную порцию метанола (25 л) и вышеприведенный способ последовательно повторяли в течение в общей сложности 5 циклов. Объединенные метанольные экстракты (приблизительно 125 л) разбавляли 160 л деминерализованной воды и партиями в течение ночи перемешивали при комнатной температуре с 3 л смолы Diaion HP 20. Смолу затем собирали и объединяли со смолой Diaion HP 20, использованной для экстракции фильтрата среды в соответствии с вышеописанным способом. Объединенную смолу промывали в хроматографической колонке 20 л смеси вода:метанол 6:4 (об./об.). Антибиотик 107891 элюировали 23 л смеси метанол:50 мМ буфер формиата аммония pH 3,5:н-бутанол 9:1:1 (об./об.). Этот элюат затем концентрировали в вакууме до конечного объема 3 л. Затем концентрированный раствор при pH 4,5 наносили на колонку 2,5 л полиамида CC 6 0,1-0,3 мм (Macherey-Nagel), уравновешенную смесью вода:метанол 7:3 (об./об.). Колонку промывали смесью вода:метанол 7:3 (об./об.) и затем смесью 25 мМ буфер формиата аммония pH 3,5:метанол 7:3(об./об.). Антибиотик элюировали смесью вода:метанол 3:7 (об./об.) и затем смесью 1:9 (об./об.). Элюцию завершали смесью 25 мМ буфер формиата аммония pH 2,8:метанол в отношении 1:9 (об./об.). Элюаты, содержащие антибиотик 107891, объединяли и концентрировали в вакууме до конечного объема 1 л.pH концентрированного раствора доводили до величины от 4 до 5,7 с использованием 7 M гидроксида аммония и затем смесь центрифугировали для сбора осадка. Это твердое вещество суспендировали в воде и сушили замораживанием с получением 6,96 г препарата антибиотика 107891. Пример 5. Очистка антибиотика 107891. Неочищенный антибиотик 107891 (3,6 г), полученный в соответствии с описанным в примере 3,очищали путем хроматографии среднего давления на 100 г частиц размера 40-70 мкм обращенной фазыC8 (EC), размер пор 60 A, IST (International Sorbent Technology, MidGlamorgan, UK) путем использования системы хроматографии среднего давления Buchi B-680 (Buchi laboratoriums-technik AG, FlawilSwitzerland), оборудованной градиентообразователем B-687, коллектором фракций B-684, стеклянной колонкой B-685 70460 мм. Смолу предварительно уравновешивали смесью фаза А:фаза Б 8:2 (об./об.) и затем элюировали при скорости 25 мл/мин с использованием линейного градиента от 20 до 60% фазы Б в течение 60 мин. Фаза А представляла собой смесь ацетонитрил:20 мМ буфер формиата аммония (pH 6,6) 10:90(об./об.); а фаза Б представляла собой смесь ацетонитрил:20 мМ буфер формиата аммония (pH 6,6) 90:10(об./об.). Фракции, содержащие антибиотик 107891, объединяли, концентрировали в вакууме и дважды лиофилизировали из воды с получением 430 мг очищенного антибиотика 107891. Пример 6. Очистка антибиотика 107891 путем препаративной ВЭЖХ. Антибиотик 107891 дополнительно очищали путем препаративной ВЭЖХ на колонке RT Hibar,предварительно упакованной лихросорбом RP8 (размер частиц 7 мкм) 250-25 мм, Merck, путем использования линейного элюирующего градиента от 30 до 45% фазы Б при скорости 30 мл/мин в течение 25 мин. Фаза А представляла собой смесь 25 мМ буфер формиата аммония pH 4,5:ацетонитрил 95:5(об./об.), а фаза Б представляла собой ацетонитрил. Образец антибиотика 107891 по примеру 5 (300 мг) растворяли в 1,5 мл 350:л смеси ДМСО:муравьиная кислота 95:5 (об./об.) и 300 мкл подвергали хроматографическому разделению. Антибиотик 107891, как правило, элюировали в течение 15-16 мин. Элюируемые фракции с 5 хроматографических разделений, содержащих антибиотик 107891, объединяли и концентрировали в вакууме. Оставшийся раствор последовательно трижды лиофилизировали из воды с получением 31 мг антибиотика 107891 в виде белого порошка.- 23016608 Пример 7. Разделение и очистка индивидуальных факторов A1 и A2 антибиотика 107891. Факторы A1 и A2 разделяли и очищали из антибиотического комплекса 107891 по примеру 5 при помощи препаративной ВЭЖХ на колонке Symmetry Prep C18 (размер частиц 7 мкм) 7,8300 мм Waters(Mildfold USA) с использованием различных программ элюции. А) Фактор A1 очищали при помощи линейного элюирующего градиента от 30 до 45% фазы Б при скорости потока 3,5 мл в течение 25 мин. Фаза А представляла собой 25 мМ буфер формиата аммония pH 4,5:ацетонитрил 95:5 (об./об.), а фаза Б представляла собой ацетонитрил. Очищенный антибиотический комплекс 107891 (15 мг) растворяли в 350 мкл смеси ДМСО:муравьиная кислота 95:5 (об./об.) и подвергали хроматографическому разделению. Факторы A1 и A2, как правило, элюировали во временном интервале 11-13 мин. Элюированные фракции затем анализировали при помощи ВЭЖХ в вышеописанных аналитических условиях. Фракции после 14 хроматографических разделений, содержащие чистый фактор A1 антибиотика 107891, объединяли и концентрировали в вакууме. Оставшийся раствор трижды последовательно лиофилизировали из воды с получением 15 мг чистого фактора A1 в виде белого порошка. Б) Фактор A2 очищали путем изократической элюции при скорости потока 7 мл смесью 100 мМ буфер формиата аммония pH 4:ацетонитрил 82,5:17,5 (об./об.). Очищенный антибиотитический комплекс 107891 (5 мг) растворяли в 250 мкл смеси уксусная кислота:ацетонитрил:100 мМ буфер формиата аммония pH 4 50:120:80 (об./об.) и подвергали хроматографическому разделению. Факторы A1 и A2, как правило, элюировали в течение временного интервала 9-10 мин. Элюированные фракции затем анализировали путем ВЭЖХ в вышеописанных аналитических условиях. Фракции после 20 хроматографических разделений, содержащие чистый фактор A2 антибиотика 107891, объединяли и концентрировали в вакумме. Оставшийся раствор дважды лиофилизировали из воды с получением 8 мг чистого фактора A2 в виде белого порошка. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулыY1, Y2, Y3, Y4 и Y5 независимо выбраны из группы, состоящей из S, S-O-, S=O, OS=O и O=S=O; иR1, R2, R3, R4, R5, R6, R7 и R8 независимо выбраны из группы, состоящей из H и OH,при условии, что по меньшей мере один из Y1, Y2, Y3, Y4 и Y5 не представляет собой S. 2. Соединение по п.1, где R4, R5, R6, R7 и R8 представляют собой H. 3. Соединение по п.2, где R1 представляет собой H, R2 представляет собой H и R3 представляет собой H. 4. Соединение по п.2, где R1 представляет собой H, R2 представляет собой H и R3 представляет собой OH. 5. Соединение по п.2, где R1 представляет собой H, R2 представляет собой OH и R3 представляет собой OH. 6. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой OH и R3 представляет собой ОН. 7. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой H и R3 представляет собой Н. 8. Соединение по п.2, где R1 представляет собой OH, R2 представляет собой H и R3 представляет собой ОН. 9. Соединение по п.1, где Y1 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; а Y2, Y3,Y4 и Y5 представляют собой S.- 24016608 10. Соединение по п.1, где Y2 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; a Y1, Y3,Y4 и Y5 представляют собой S. 11. Соединение по п.1, где Y3 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; a Y1, Y2,Y4 и Y5 представляют собой S. 12. Соединение по п.1, где Y4 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; a Y1, Y2,Y3 и Y5 представляют собой S. 13. Соединение по п.1, где Y5 выбран из группы, состоящей из S-O-, S=O, OS=O и O=S=O; a Y1, Y2,Y3 и Y4 представляют собой S. 14. Фармацевтическая композиция, содержащая антибиотик, выбранный из соединений по п.1 или их фармацевтически приемлемой соли с кислотой, и фармацевтически приемлемый носитель. 15. Применение соединений по п.1 или их фармацевтически приемлемой соли с кислотой для изготовления лекарственного средства для лечения или предупреждения бактериальных инфекций.
МПК / Метки
МПК: A61P 31/04, C07K 14/195, A61K 38/16, C07K 1/14, A61P 31/14, C12P 1/04
Метки: композиция, 107891, применение, фармацевтически, соли, антибиотик, приемлемые, фармацевтическая
Код ссылки
<a href="https://eas.patents.su/30-16608-antibiotik-107891-ego-farmacevticheski-priemlemye-soli-farmacevticheskaya-kompoziciya-i-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Антибиотик 107891, его фармацевтически приемлемые соли, фармацевтическая композиция и применение</a>
Предыдущий патент: Поверхностно-активное вещество для получения латекса, композиция покрытия, латекс, способ получения латекса и эмульгатор для эмульсионной полимеризации
Следующий патент: Рекомбинантные моновалентные антитела и способы их получения
Случайный патент: Беспроводное передающее устройство