Способы, соединения, композиции и носители для доставки 3-амино-1-пропансульфоновой кислоты
Номер патента: 16568
Опубликовано: 30.05.2012
Авторы: Боузиде Абдеррахим, Ву Ксинфу, Валаде Исабель, Мигнолт Дэвид, Левеск Софи, Сиблат Стефан, Бачанд Бенуа, Конг Ксянки, Атфани Мохамед, Делорме Даниэль
Формула / Реферат
1. Соединение формулы (IV) или его фармацевтически приемлемая соль, выбранное из
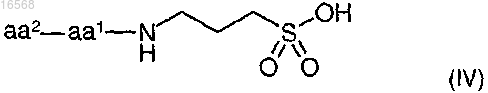
при этом аа1 представляет собой остаток природной или неприродной аминокислоты;
аа2 представляет собой остаток природной или неприродной аминокислоты, или отсутствует;
при этом указанные аа1 и аа2 представляют собой остатки аминокислот, соответствующие формуле (VI)
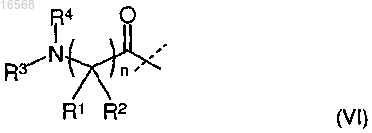
при этом R1 представляет собой замещенную или незамещенную группу, выбранную из следующих: C1-C12-алкил, C3-C15-циклоалкил, гетероциклоалкил, имеющий от 3 до 8 атомов в кольце, включая от 1 до 4 гетероатомов, выбранных из азота, кислорода и серы, и гетероциклоалкил, имеющий от 5 до 8 атомов в кольце, включая от 1 до 4 гетероатомов, при этом когда указанная группа замещена, она замещена группой, выбранной из NH2, ОН, карбокси, C1-C6-алкокси, C1-C6-алкилтио, бензилокси, бензилоксикарбонил;
R2 представляет собой водород;
R3 представляет собой водород или связь между двумя остатками аминокислот, когда оба аа1 и аа2 представляют собой остатки аминокислот;
R4 представляет собой Н; или
R1 и R4 вместе с соседними атомами углерода и азота образуют C3-C10-гетероциклоалкил; и
n равно 1.
2. Соединение по п.1, отличающееся тем, что указанное соединение представляет собой соединение формулы (V) или его фармацевтически приемлемую соль
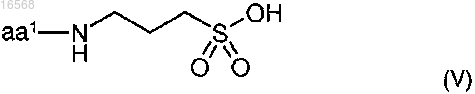
при этом аа1 представляет собой природную или неприродную аминокислоту в соответствии с определением в п.1.
3. Соединение по п.1 или 2, отличающееся тем, что указанный остаток аминокислоты находится в L-конфигурации.
4. Соединение по любому из пп.1 или 2, отличающееся тем, что указанный остаток аминокислоты является остатком природной аминокислоты.
5. Соединение по любому из пп.1 или 2, отличающееся тем, что R1 представляет собой замещенную или незамещенную C1-C12-алкильную группу.
6. Соединение по п.5, отличающееся тем, что R1 представляет собой незамещенную C1-C12-алкильную группу.
7. Соединение по п.6, отличающееся тем, что R1 представляет собой замещенную C1-C12-алкильную группу.
8. Соединение по п.7, отличающееся тем, что R1 выбран из метила, этила, н-пропила, изопропила, изобутила и вторбутила.
9. Соединение по п.5, отличающееся тем, что R1 представляет собой C1-C12-алкильную группу, замещенную группой, выбранной из гидроксила, C1-C6-алкокси и бензоксигрупп.
10. Соединение по п.3, отличающееся тем, что аа1 и аа2, каждый независимо, выбраны из следующих остатков аминокислот: L-валин, L-лизин, L-лейцин, L-серин, L-аланин, L-изолейцин, L-гистидин и L-O-бензилсерин, или их фармацевтически приемлемые соли.
11. Соединение по п.1 или 2, отличающееся тем, что указанное соединение выбрано из группы, состоящей из
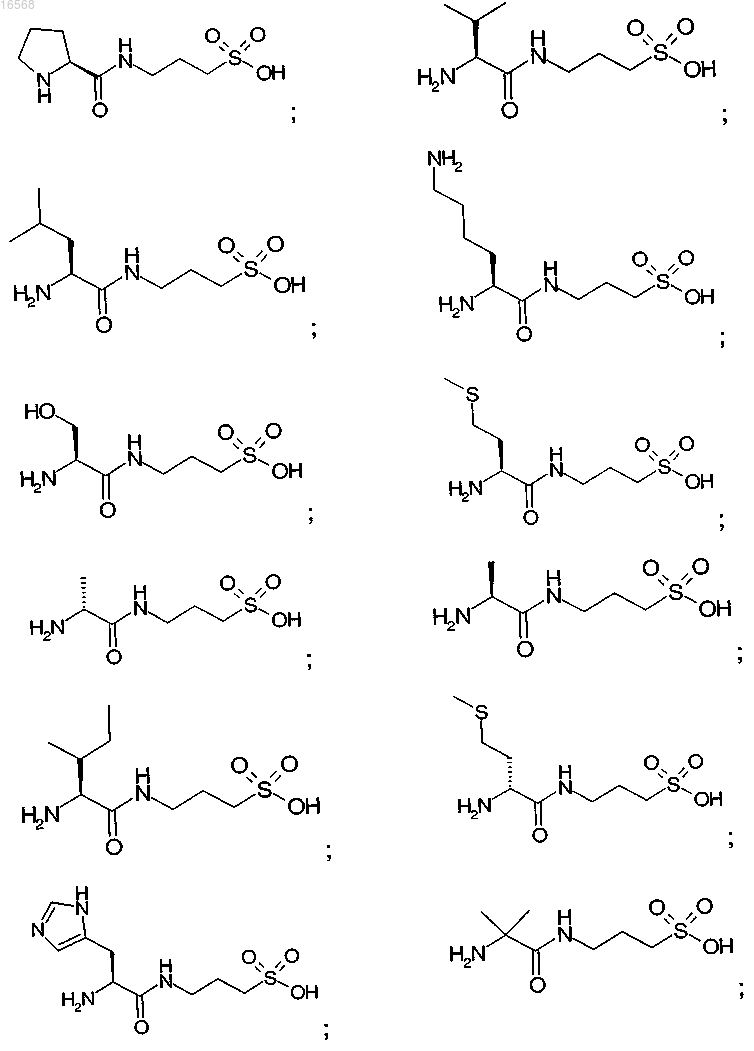
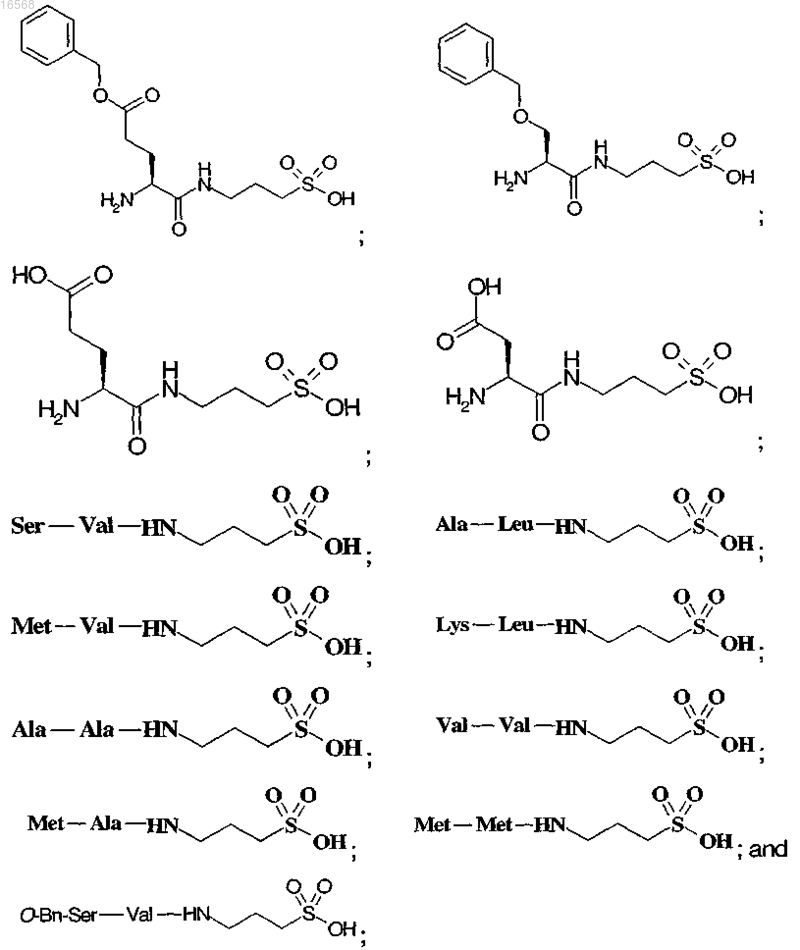
или его фармацевтически приемлемые соли.
12. Соединение по п.1 или 2, отличающееся тем, что указанное соединение выбрано из
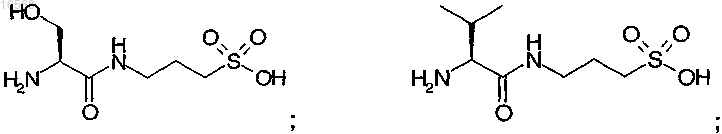
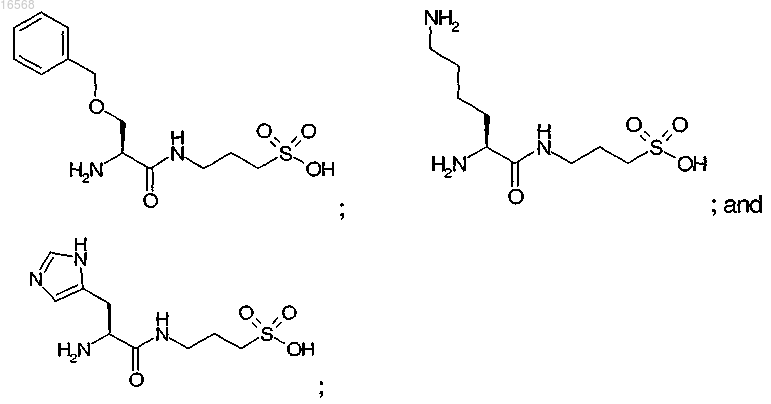
или его фармацевтически приемлемые соли.
13. Соединение по п.4, отличающееся тем, что указанное соединение представляет собой
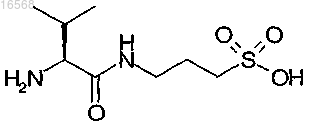
или его фармацевтически приемлемую соль.
14. Фармацевтическая композиция, содержащая соединение по любому из пп.1-13 вместе с фармацевтически приемлемым носителем.
15. Применение соединений по любому из пп.1-13 в качестве лекарственного средства.
16. Способ лечения или предотвращения болезни или состояния, выбранного из болезни Альцгеймера, умеренных когнитивных нарушений, синдрома Дауна, наследственной церебральной геморрагии с амилоидозом голландского типа, церебральной амилоидной ангиопатии, дегенеративного слабоумия, слабоумия смешанного сосудистого и дегенеративного происхождения, слабоумия, связанного с болезнью Паркинсона, слабоумия, связанного с прогрессирующим супрануклеарным параличом, слабоумия, связанного с кортико-базальной дегенерацией, или болезни Альцгеймера с диффузными тельцами Леви, включающий введение терапевтически эффективного количества соединения по любому из пп.1-13 нуждающемуся в этом субъекту.
17. Способ лечения или предотвращения болезни или состояния, выбранного из болезни Альцгеймера, умеренных когнитивных нарушений, наследственной церебральной геморрагии с амилоидозом голландского типа или церебральной амилоидной ангиопатии, включающий введение терапевтически эффективного количества соединения по любому из пп.1-13 нуждающемуся в этом субъекту.
18. Способ по п.17, отличающийся тем, что указанная болезнь представляет собой болезнь Альцгеймера.
19. Способ лечения или предотвращения заболевания, связанного с бета-амилоидом, включающий введение терапевтически эффективного количества соединения по любому из пп.1-13 нуждающемуся в этом субъекту.
20. Способ лечения или предотвращения нейродегенеративного заболевания, включающий введение терапевтически эффективного количества соединения по любому из пп.1-13 нуждающемуся в этом субъекту.
21. Способ лечения или предотвращения нейродегенеративного заболевания по п.20, где нейродегенеративное заболевание представляет собой болезнь Паркинсона.
22. Применение соединения по любому из пп.1-13 в производстве нейропротекторного лекарственного средства для лечения или предотвращения заболевания, связанного с бета-амилоидом.
23. Применение соединения по любому из пп.1-13 в производстве лекарственного средства для лечения или предотвращения болезни или состояния, выбранного из болезни Альцгеймера, умеренных когнитивных нарушений, синдрома Дауна, наследственной церебральной геморрагии с амилоидозом голландского типа, церебральной амилоидной ангиопатии, дегенеративного слабоумия, слабоумия смешанного сосудистого и дегенеративного происхождения, нейродегенеративного заболевания, болезни Паркинсона, слабоумия, связанного с болезнью Паркинсона, слабоумия, связанного с прогрессирующим супрануклеарным параличом, слабоумия, связанного с кортико-базальной дегенерацией, или болезни Альцгеймера с диффузными тельцами Леви.
24. Применение соединения по п.23 в производстве лекарственного средства для лечения или предотвращения заболевания или состояния, выбранного из болезни Альцгеймера, умеренных когнитивных нарушений, наследственной церебральной геморрагии с амилоидозом голландского типа или церебральной амилоидной ангиопатии.
25. Применение по п.23, причем указанная болезнь представляет собой болезнь Альцгеймера.
26. Применение соединения по п.23 в производстве лекарственного средства для лечения или предотвращения нейродегенеративного заболевания.
27. Применение соединения по п.22 в производстве лекарственного средства для лечения или предотвращения болезни Паркинсона.
Текст
СПОСОБЫ, СОЕДИНЕНИЯ, КОМПОЗИЦИИ И НОСИТЕЛИ ДЛЯ ДОСТАВКИ 3-АМИНО-1-ПРОПАНСУЛЬФОНОВОЙ КИСЛОТЫ Изобретение относится к способам, соединениям, композициям и носителям для введения 3 амино-1-пропансульфоновой кислоты (3-АПС) субъекту, предпочтительно субъекту - человеку. Изобретение включает соединения, которые превращаются в 3-АПС или образуют in vitro или invivo. Предпочтительные соединения включают аминокислотные пролекарства 3-АПС, подходящие для применения, неограничивающие примеры которого включают предотвращение или лечение болезни Альцгеймера. 016568 Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США 60/851039 от 12 октября 2006 г. и предварительной заявке на патент США 60/911459 от 12 апреля 2007 г., содержание которых включено в настоящее описание по ссылке. Область техники Изобретение относится к способам, соединениям, композициям и носителям для доставки 3-амино 1-пропансульфоновой кислоты (3-АПС) субъекту, предпочтительно человеку. Изобретение включает соединения, которые превращаются в или образуют 3-АПС либо in vitro, либо in vivo. Предпочтительные соединения включают аминокислотные пролекарства 3-АПС, пригодные для применения, неограничивающие примеры которого включают предотвращение или лечение болезни Альцгеймера. Существующий уровень техники Болезнь Альцгеймера (БА) представляет собой прогрессирующее дегенеративное заболевание мозга, связанное, в первую очередь, со старением. Количество страдающих этим заболеванием в Соединенных Штатах в 2000 году было близко к 4,5 миллионам человек. Было подсчитано, что приблизительно один из десяти индивидуумов в возрасте старше 65 лет и почти половина людей в возрасте старше 85 лет страдают болезнью Альцгеймера. Предположительно, каждый год только в Соединенных Штатах диагноз БА будет установлен приблизительно у 360000 пациентов. Клиническая картина БА характеризуется ухудшением памяти, когнитивной способности, логического мышления, способности к умозаключениям и способности к ориентации. По мере прогрессирования болезни происходит ухудшение моторных, сенсорных и речевых способностей, которое приводит к общему нарушению различных когнитивных функций. Указанное ухудшение когнитивных способностей происходит постепенно, но обычно приводит к тяжелым нарушениям и, в конечном итоге, к смерти в течение периода, составляющего от четырех до двенадцати лет. Болезнь Альцгеймера характеризуется двумя основными наблюдаемыми патологическими изменениями, происходящими в мозге: образованием нейрофибриллярных клубков и бета-амилоидных (или нейритных) бляшек, в основном состоящих из агрегатов фрагмента пептида, известного как А. Нейрофибриллярные клубки, а также характерные отложения бета-амилоида (бета-амилоидные бляшки) обнаружены в мозге и в сосудах головного мозга (бета-амилоидная ангиопатия) индивидуумов, страдающих БА. Нейрофибриллярные клубки обнаружены не только у индивидуумов, страдающих болезнью Альцгеймера, но и у людей, страдающих другими нарушениями, вызывающими слабоумие. 3-амино-1-пропансульфоновая кислота (3-АПС, Tramiprosate, Alzhemed) представляет собой перспективный продукт, который проходит исследования для определения возможности его применения для лечения болезни Альцгеймера; и в настоящее время находится на третьей фазе клинических испытаний в Северной Америке и Европе (Wright, Т. М., Drugs of Today (2006), 42(5): 291-298). Это соединение было разработано Компанией Neurochem Inc. (Лаваль, QC, Канада), и полагают, что оно способно уменьшать образование отложений и/или амилоидную нагрузку на мозг посредством связывания с растворимым пептидом A. Для повышения терапевтической эффективности 3-АПС желательно повысить ее биодоступность, стабильность и/или способность к прохождению через гематоэнцефалический барьер. Эти и другие задачи могут быть решены путем реализации настоящего изобретения, которое относится к пролекарственной форме 3-амино-1-пропансульфоновой кислоты (3-АПС), фармацевтическим композициям, содержащим такую форму, и применению этой формы для лечения различных медицинских нарушений. Проведенные ранее исследования метаболической стабильности показали отсутствие метаболизма 3-АПС in vitro. Указанные исследования включали исследования метаболической стабильности 3-АПС в объединенных гепатоцитах человека, микросомах печени человека, крысы и собаки, кишечной микрофлоре человека, объединенных цитозолях печени человека и ариламин-N-ацетилтрансферазе человека(см. примеры 4 и 5). Краткое описание изобретения Неожиданно было обнаружено, что 3-АПС подвергается метаболизму как in vitro, так и in vivo. В самом деле, как будет более подробно описано ниже, недавние исследования in vivo указывают на интенсивный метаболизм, в частности пресистемный метаболизм (эффект первого прохождения) и/или системный метаболизм 3-АПС. Были идентифицированы три потенциальных метаболита по меньшей мере одного типа биологических молекул: 2-карбоксиэтансульфоновая кислота, 3-гидрокси-1-пропансульфоновая кислота и 3-ацетиламино-1-пропансульфоновая кислота. Дальнейшие исследования показали, что единственным основным метаболитом 3-АПС у мышей, крыс, собак и людей является 2-карбоксиэтансульфоновая кислота.-1 016568 Не прибегая к какой-либо теории, можно предположить, что метаболизм 3-АПС в основном осуществляется трансаминазой и/или моноаминоксидазой, которая в качестве основного метаболита образует 2-карбоксиэтансульфоновую кислоту, а в качестве второстепенного метаболита-3-гидрокси-1 пропансульфоновую кислоту. Другим возможным второстепенным метаболитом является N-ацетил-3 аминопропансульфоновая кислота, при этом предположительно ее образует фермент, ацетилирующий 3 АПС. Указанные гипотезы подтверждаются экспериментами in vitro (см., например, пример 5), показывающими, что превращение 3-АПС в 2-карбоксиэтансульфоновую кислоту в культуральной среде первичных нейронов в значительной степени ингибируется вигабатрином, классическим ингибитором трансаминазы ГАМК (гамма-аминомасляную кислоту). Ниаламид, ингибитор моноаминоксидазы, также уменьшает образование 2-карбоксиэтансульфоновой кислоты (из 3-АПС), но в меньшей степени. Соответственно, один из аспектов изобретения относится к соединениям и композициям, которые обеспечивают доставку 3-АПС при минимизации метаболизма, например пресистемного метаболизма,связанного с данным медикаментом, и, более конкретно, к соединениям, которые блокируют или защищают аминогруппу в 3-АПС таким образом, что она не подвергается метаболическим превращениям,например, под действием трансаминаз и/или моноаминоксидаз. Изобретение относится к способам, соединениям, композициям и носителям для доставки субъекту,предпочтительно человеку, 3-амино-1-пропансульфоновой кислоты или ее солей. 3-Амино-1-пропансульфоновая кислота (также называемая 3-АПС, Tramiprosate, Alzhemed) имеет следующую структуру: В соответствии с одним из аспектов настоящего изобретения изобретение относится к соединениям или композициям, которые способны к образованию или превращению в 3-АПС после введения указанных соединений или композиций субъекту. В одном из примеров реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой аминокислотное пролекарство 3-АПС. В другом варианте реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой пролекарство 3-АПС, являющееся карбаматом. В другом варианте реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой пролекарство 3-АПС,являющееся амидом. В другом варианте реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой пролекарство 3-АПС, являющееся производным углевода. В другом варианте реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой пролекарство 3-АПС, являющееся N-гидроксипроизводным. В другом варианте реализации соединение, которое может образовывать или превращаться в 3-АПС, представляет собой циклическое пролекарство, имеющее двойную защиту. В другом варианте реализации, соединение, которое образует или превращается в 3-АПС, представляет собой 3-АПС полимер (например, молекулу, состоящую из двух или более молекул 3-АПС, соединенных друг с другом). В другом варианте реализации соединение, которое образует или превращается в 3-АПС, представляет собой димер, состоящий из двух молекул 3-АПС. В некоторых примерах реализации аминокислотные пролекарства 3-АПС, которые могут образовывать или превращаться в 3-АПС либо in vitro, либо in vivo, имеют одну из общих или конкретных формул или структур, представленных в настоящем описании. Настоящее изобретение также включает указанные соединения, фармацевтические композиции, содержащие указанные соединения, и способы лечения различных медицинских нарушений, например болезни Альцгеймера, в которых используют такие соединения или композиции. Настоящее изобретение также относится к фармацевтическим композициям, включающим соединение согласно настоящему изобретению. Настоящее изобретение также относится к способу повышения терапевтической эффективности 3 АПС, включающему введение субъекту, предпочтительно субъекту-человеку, эффективного количества пролекарства согласно настоящему изобретению. Настоящее изобретение также относится к способам превращения соединения согласно настоящему изобретению в 3-АПС. Превращение и/или получение 3-АПС включает контакт любого из соединений согласно настоящему изобретению, например, с кровью, плазмой и/или клетками мозга. Превращение может происходить in vitro или in vivo. Превращение также может происходить в присутствии ферментов, способных расщеплять аминные связи, например, пептидаз, или других ферментов, пригодных для других рассматриваемых в настоящем описании структур, включающих структуры, находящиеся в крови, плазме и/или мозге. Изобретение также относится к применению соединения согласно настоящему изобретению для изготовления лекарственного средства. Изобретение также относится к применению соединения согласно настоящему изобретению для лечения или предотвращения болезни Альцгеймера, умеренных когнитивных нарушений, синдрома Дауна, наследственной церебральной геморрагии с амилоидозом голландского типа, церебральной амилоидной ангиопатии, других типов дегенеративного слабоумия, слабоумия смешанного сосудистого и дегенеративного происхождения, слабоумия, связанного с болезнью Паркин-2 016568 сона, слабоумия, связанного с синдромом прогрессирующего супрануклеарного паралича, слабоумия,связанного с кортикально-базальной дегенерацией, или болезни Альцгеймера диффузного типа с тельцами Леви. Изобретение также относится к способам лечения или предотвращения указанных заболеваний,включающим введение терапевтически эффективного количества соединения согласно настоящему изобретению, или композиции, включающей указанное соединение, субъекту, предпочтительно субъектучеловеку, нуждающемуся в таком введении. Более предпочтительно заболевание представляет собой болезнь Альцгеймера. Таким образом, соответствующий аспект изобретения относится к предотвращению и/или лечению болезни Альцгеймера у субъекта-человека посредством введения эффективного количества соединения или композиции, предлагаемых согласно настоящему изобретению субъектучеловеку, нуждающемуся в таком предотвращении и/или лечении. Другой пример реализации изобретения включает введение 3-АПС через или под слизистые оболочки, носовую полость (интраназально), ротовую полость или глаз, например, при помощи назального спрея, жевательной резинки или глазных капель, через ушную полость, например, при помощи ушных капель, с применением имплантанта, ректально, например, при помощи суппозитория или клизмы, первагинально, например, при помощи крема или лосьона, или через дыхательную систему, например, при помощи ингаляции, интраназально или интратрахеально. Другие аспекты изобретения включают введение соединений согласно настоящему изобретению при помощи любого способа и/или носителя, включая все способы и/или носители, рассмотренные в настоящем описании, например, введение пролекарств 3-АПС через носовую полость, слизистые оболочки,трансдермально, при помощи пластыря и т.д. Различные аспекты настоящего изобретения относятся к следующим пронумерованным аспектам: Аспект 1. Соединение, отвечающее формулам (IV), (V), (VI), представленным ниже, или фармацевтически приемлемая соль указанного соединения. Аспект 2. Фармацевтическая композиция, включающая соединение аспекта 1 и фармацевтически приемлемый носитель. Аспект 3. Способ лечения или предотвращения болезни Альцгеймера, умеренных когнитивных нарушений, синдрома Дауна, наследственной церебральной геморрагии с амилоидозом голландского типа,церебральной амилоидной ангиопатии, дегенеративного слабоумия, слабоумия смешанного сосудистого и дегенеративного происхождения, слабоумия, связанного с болезнью Паркинсона, слабоумия, связанного с прогрессирующим супрануклеарным параличом, слабоумия, связанного с кортикально-базальной дегенерацией, или болезни Альцгеймера с диффузными тельцами Леви, включающий введение терапевтически эффективного количества соединения аспекта 1 нуждающемуся в этом субъекту-человеку. Аспект 4. Способ в соответствии с аспектом 3, в котором указанная болезнь представляет собой болезнь Альцгеймера. Аспект 5. Способ лечения или предотвращения заболевания, связанного с бета-амилоидом, включающий введение терапевтически эффективного количества соединения в соотвествии с аспектом 1 нуждающемуся в этом субъекту. Аспект 6. Способ лечения или предотвращения нейродегенеративного заболевания, включающий введение терапевтически эффективного количества соединения в соотвествии с аспектом 1 нуждающемуся в этом субъекту. Аспект 7. Способ лечения или предотвращения нейродегенеративного заболевания в соотвествии с аспектом 6, где нейродегенеративное заболевание представляет собой болезнь Паркинсона. Аспект 8. Применение соединения в соотвествии с аспектом 1 в производстве нейропротекторного лекарственного средства для лечения или предотвращения заболевания, связанного с бета-амилоидом. Аспект 9. Применение соединения в соотвествии саспектом 1 в производстве лекарственного средства для лечения или предотвращения болезни или состояния, выбранного из: болезни Альцгеймера,умеренных когнитивных нарушений, синдрома Дауна, наследственной церебральной геморрагии с амилоидозом голландского типа, церебральной амилоидной ангиопатии, дегенеративного слабоумия, слабоумия смешанного сосудистого и дегенеративного происхождения, нейродегенеративного заболевания,болезни Паркинсона, слабоумия, связанного с болезнью Паркинсона, слабоумия, связанного с прогрессирующим супрануклеарным параличом, слабоумия, связанного с кортико-базальной дегенерацией, или болезни Альцгеймера с диффузными тельцами Леви. Аспект 10. Применение соединения в соотвествии с аспектом 9 в производстве лекарственного средства для лечения или предотвращения заболевания или состояния выбранного из: болезни Альцгеймера, умеренных когнитивных нарушений, наследственной церебральной геморрагии с амилоидозом голландского типа или церебральной амилоидной ангиопатии. Аспект 11. Применение в соотвествии с аспектом 9 причем указанная болезнь представляет собой болезнь Альцгеймера. Аспект 12. Применение соединения в соотвествии с аспектом 9 в производстве лекарственного средства для лечения или предотвращения нейродегенеративного заболевания. Аспект 13. Применение соединения в соотвествии с аспектом 9 в производстве лекарственного средства для лечения или предотвращения болезни Паркинсона.-3 016568 Другие задачи, преимущества и признаки настоящего изобретения подробно разъяснены в нижеследующем неограничивающем описании предпочтительных примеров реализации, которые приведены для иллюстрации изобретения и никоим образом не ограничивают область его применения.I. Определения. Все технические и научные термины, приведенные в настоящем описании, имеют значение, которое обычно известно среднему специалисту в данной области техники, к которой относится настоящее изобретение. Для удобства значения некоторых терминов и фраз, используемых в настоящем описании,приведены ниже. Если определения терминов, приведенные в публикациях, патентах и патентных заявках, цитируемых в настоящем описании, противоречат определениям, данным в настоящем описании, то определения, данные в настоящем описании, имеют приоритет. Названия разделов настоящего описания приведены лишь для удобства и не должны расцениваться как ограничивающие предмет настоящего описания. Следует отметить, что единственное число понятий включает множественное, если контекст не указывает однозначно на обратное. Так, например, указание композиции, содержащей "соединение", включает смесь двух или более соединений. Также следует отметить, что термин "или" обычно означает"и/или", если из контекста однозначно не следует обратное. Химические структуры, приводимые в настоящем описании, изображены в соответствии с традиционными стандартами, известными в данной области техники. Так, если атом, например атом углерода,изображен имеющим ненасыщенную валентность, то эта валентность должна быть заполнена атомом водорода, даже если атом водорода не изображен в явной форме. Следует понимать, что атомы водорода представляют собой часть соединения. Символ "-" в общем случае означает связь между атомами в цепочке. Так, CH3-О-СН 2-СН(Ri)-CH3 представляет собой 2-замещенный-1-метоксипропан. Кроме того, символ "-" также означает точку присоединения заместителя к соединению. Так, например, арил(C1-C6)-алкил означает арилалкильную группу, например бензильную, присоединенную к соединению по алкильному фрагменту. Если указано, что к структуре присоединены несколько заместителей, то следует понимать, что эти заместители могут быть как одинаковыми, так и различными. Так, например, "Rm, возможно содержащий 1, 2 или 3 заместителя Rq" указывает на то, что Rm содержит в качестве заместителей 1, 2, или 3 группыRq, причем группы Rq могут быть как одинаковыми, так и различными. В соответствии с настоящим описанием термин "соединения согласно настоящему изобретению" и эквивалентные обозначения означают соединения, указанные в настоящем описании и пригодные для осуществления по меньшей мере одного из назначений настоящего изобретения, например соединения,описываемые, например, структурными формулами (I), (I-A), (I-C), (I-D), (I-Е), (1-Р), (I-P2), (II), (III),(IV), (V), (VI), (VII), (VIII), (IX), (X), (XI), (XII), (XII-А) и (XIII), и включают конкретные указанные в описании соединения, например, от А 1 до А 35, от С 1 до С 26, от В 1 до В 14, от Н 1 до Н 4, от G1 до G11, отS1 до S14 и от D1 до D8, и т.д., а также их фармацевтически приемлемые соли и сольваты. Описанные примеры реализации могут исключать одно или несколько соединений согласно настоящему изобретению. Соединения могут быть идентифицированы или по их химической структуре и/или химическому названию. Если имеет место противоречие химической структуры и химического названия, то идентификацию соединения производят в соответствии с химической структурой. Соединения, рассматриваемые в настоящем описании, могут содержать один или несколько хиральных центров и/или двойных связей и,таким образом, могут существовать в виде стереоизомеров, например изомеров по двойной связи (т.е.,геометрических изомеров), энантиомеров или диастереомеров. Соответственно, химические структуры,рассмотренные в настоящем описании, включают все возможные энантиомеры и стереоизомеры показанных соединений, включая стереоизомерно чистые формы (например, геометрически чистые, энантиомерно чистые или диастереомерно чистые) и смеси энантиомеров и стереоизомеров. Смеси энантиомеров и стереоизомеров могут быть разделены на составляющие энантиомеры или стереоизомеры при помощи известных методик разделения или методик хирального синтеза, хорошо известных специалисту в данной области техники, например при помощи хиральной хроматографии (например, хиральной ЖХВР), методик иммунологического анализа или применения ковалентно (например, эфиры Мошера) и нековалентно (например, хиральные соли) связанных с ними хиральных реагентов, которые, соответственно, образуют смесь диастереомеров, которая может быть разделена традиционными способами, например хроматографией, перегонкой, кристаллизацией или сублимацией, после чего хиральную соль или сложный эфир подвергают реакции обмена или расщепления традиционными способами и выделяют желаемые изомеры. Соединения также могут существовать в нескольких таутомерные формах, включающих енольную форму, кетонную форму и их смеси. Соответственно, химические структуры, рассматриваемые в настоящем описании, включают все возможные таутомерные формы показанного соединения. Описываемые соединения также включают меченые изотопами соединения, в которых один или несколько атомов имеют атомную массу, отличающуюся от наиболее распространенного в природе значения атомной массы. Неограничивающие примеры изотопов, которые могут быть введены в соединения, предлагаемые согласно настоящему изобретению, включают 2 Н (D), 3 Н (Т), 11 С, 13 С, 14 С, 15N, 18O,17 О и т.д. Соединения могут существовать в несольватированных формах, а также в сольватированных фор-4 016568 мах, включающих гидратированные формы. В общем случае соединения могут быть гидратированы или сольватированы. Некоторые соединения могут существовать в нескольких кристаллических формах или аморфных формах. В общем случае все физические формы эквивалентны по отношению к использованию, рассматриваемому в настоящем описании, и включены в область, защищаемую настоящим изобретением. Кроме того, если показаны частичные структуры соединений, то скобки или эквиваленты указывают току присоединения частичной структуры к остальной части молекулы. Термин "пролекарство" и эквивалентные обозначения означают вещества, которые могут быть переведены в активную форму in vitro или in vivo прямо или опосредованно (см., например, R. В. Silverman,1992, "The Organic Chemistry of Drug Design and Drug Action" Academic Press, глава 8; Bundgaard, Hans;Springer). Пролекарства можно использовать для изменения биораспределения (например, вещества, которые обычно не достигают реакционного центра протеазы, могут быть доставлены к этому центру) или фармакокинетики конкретного вещества. Для модификации соединений с целью получения пролекарств применяют различные группы, например сложные эфиры, простые эфиры, фосфаты и т.д. При введении пролекарства субъекту такие группы отщепляются под действием ферментов или без участия ферментов,по механизму восстановления, окисления, гидролиза или другому механизму, с образованием активной формы. В соответствии с настоящим описанием термин "пролекарство" включает фармацевтически приемлемые соли вещества или фармацевтически приемлемые сольваты, а также кристаллические формы любой из указанных выше форм. Часто, хотя и не обязательно, пролекарства фармакологически неактивны до превращения в исходное лекарственное средство. Термин "двойной (бивалентный) димер" и эквивалентные обозначения означают синтетическое соединение, включающее по меньшей мере два фрагмента одного и того же вещества или лекарственного средства, соединенные друг с другом. Описание двойных димеров дано, например, в следующих публикациях: Hammell D. С., Hamad M., Vaddi H. K., Crooks P. А., Stinchcomb A. L. A duplex "Gemini" prodrugof naltrexone for transdermal delivery. J Control Release. 2004. 97(2):283-90. В предпочтительном варианте реализации двойные димеры согласно настоящему изобретению изготовлены из двух соединенных молекул 3-АПС, которые in vitro или in vivo непосредственно или опосредованно могут образовывать по меньшей мере одну, предпочтительно две, фармацевтически активные молекулы 3-АПС. Термин "карбамат" означает оксикарбонильный остаток (OC(O)-), присоединенный к аминогруппе с образованием группы, включающей радикал (-ОС(О)N(или NH)-). Карбаматная группа может быть вторичной (NH) или третичной (N). Более подробное определение этого термина дано ниже в разделе IIВ(а). Термин "амид" означает органическое соединение, содержащее карбонильную группу (-С(О)-),присоединенную к аминогруппе с образованием группы, включающей радикал (-С(О)N(или NH)-). Амидная группа может быть вторичной (NH) или третичной (N). Более подробное определение этого термина дано ниже в разделе II-А. Термин "неаминокислотный амид" означает амидную группу, в которой карбонил (-С(О)-) не образует часть аминокислотного остатка. Более подробное определение этого термина дано ниже в разделе II-В(b). Термин "производное углевода (полученный из углевода)" означает соединения, в которых группа,присоединенная, например, к 3-АПС, представляет собой органическую группу, которая представляет собой или получена из полигидроксиальдегида, полигидроксикетона или полиола, или может превращаться в указанные группы при проведении простых химических превращений, например гидролиза,окисления или восстановления. Такие группы включают, например, сахара, крахмалы, целлюлозы и камеди. Более подробное определение этого термина дано ниже в разделе II-С. Термин "N-гидроксипроизводное" означает соединения, содержащие гидроксигруппу или полученные из гидроксигруппы(например, алкокси-, бензилокси-, фенокси-, ацилоксигруппу и подобные группы) с образованием группы (RO-N(или NH)-). Более подробное определение этого термина дано ниже в разделе II-D(a). Термин "циклический с двойной защитой" означает соединение, в котором защитная группа присоединена и к амину, и к сульфоновой кислоте 3-АПС. Более подробное определение этого термина дано ниже в разделе II-D(b). Термин "сложный эфир" означает соединения, которые могут быть представлены формулойRCOOR (карбоновый сложный эфир) или формулой RSO3R' (сульфонатный сложный эфир), в которых группа R может представлять собой, например, 3-АПС или 3-аминопропановую часть 3-АПС, а группа R' может представлять собой другую органическую группу. Указанные соединения обычно получают в соответствующих реакциях между карбоновой или сульфоновой кислотой и спиртом, обычно с отщеплением воды. Термин "аминокислота" в общем случае означает органическое соединение, включающее как группу карбоновой кислоты, так и аминогруппу. Термин "аминокислота" включает как "природные", так и"неприродные" аминокислоты. Кроме того, термин аминокислота включает О-алкилированные или Nалкилированные аминокислоты, а также аминокислоты, включающие азот- или кислородсодержащие боковые цепи (например, Lys, Orn или Ser), в которых атом азота или кислорода был ацилирован или-5 016568 алкилирован. Аминокислоты могут быть чистыми и представлять собой L или D изомеры или смеси L иD изомеров, включающие рацемические смеси. В общем случае, аминокислоты представлены остатком формулы V. Термин "природная аминокислота" и эквивалентные обозначения означают L-аминокислоты, обычно встречающиеся в белках в природе. Неограничивающие примеры природных аминокислот включают аланин (Ala), цистеин (Cys), аспарагиновую кислоту (Asp), глютаминовую кислоту (Glu), фенилаланин(Trp), тирозин (Tyr), -аланин (-ALA) и -аминомасляную кислоту (ГАМК). Термин "неприродная аминокислота" означает любое производное природной аминокислоты,включающее D-формы, и производные - и -аминокислот. Следует отметить, что некоторые аминокислоты, например гидроксипролин, которые в соответствии с настоящим описанием рассматриваются как неприродные аминокислоты, могут встречаться в природе и содержаться в некоторых организмах или конкретных белках. В настоящее время коммерчески доступны аминокислоты, включающие множество различных защитных групп, пригодные для немедленного использования в твердофазном синтезе пептидов. Помимо двадцати наиболее распространенных природных аминокислот в соответствии с настоящим изобретением могут быть использованы следующие примеры неприродных аминокислот и производных аминокислот: (в скобках указаны общепринятые сокращения): 2-аминоадипиновая кислота (Aad), 3 аминоадипиновая кислота (-Aad), 2-аминомасляная кислота (2-Abu), ,-дегидро-2-аминомасляная кислота (8-AU), 1-аминоциклопропан-1-карбоновая кислота (АСРС), аминоизомасляная кислота (Aib), 3 аминоизомасляная кислота (-Aib), 2-аминотиазолин-4-карбоновая кислота, 5-аминовалериановая кислота (5-Ava), 6-аминогексановая кислота (6-Ahx), 2-аминогептановая кислота (Ahe), 8-аминооктановая кислота (8-Аос), 11-аминоундекановая кислота (11-Aun), 12-аминододекановая кислота (12-Ado), 2 аминобензойная кислота (2-Abz), 3-аминобензойная кислота (3-Abz), 4-аминобензойная кислота (4-Abz),4-амино-3-гидрокси-6-метилгептановая кислота (Statine, Sta), аминооксиуксусная кислота (Аоа), 2 аминотетралин-2-карбоновая кислота (АТС), 4-амино-5-циклогексил-3-гидроксипентановая кислота(Tic), тиенилаланин и тиазолидин-4-карбоновая кислота (тиопролин, Th). В соответствии с настоящим описанием термин "ациклический" означает органический фрагмент,не содержащий систем колец. Термин "алифатическая группа" включает органические фрагменты, включающие неразветвленные и разветвленные цепочки, обычно содержащие от 1 до 15 атомов углерода. Алифатические группы включают нециклические алкильные группы, алкенильные группы и алкинильные группы. В соответствии с настоящим описанием термин "алкил" означает насыщенный углеводород, содержащий от одного до двенадцати атомов углерода, включающий неразветвленные, разветвленные и циклические алкильные группы. Неограничивающие примеры алкильных групп включают следующие радикалы: метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, изопропил, трет-бутил,втор-бутил, изобутил, циклопропил, циклопентил, циклогексил, циклогептил, циклооктил и подобные им радикалы. Термин алкил включает как незамещенные алкильные группы, так и замещенные алкильные группы. Термин "C1-Cn-алкил", в котором n равен целому числу, составляющему от 2 до 12, означает алкильную группу, содержащую от 1 до указанного числа "n" атомов углерода. В соответствии с настоящим описанием термин "алкенил" означает ненасыщенный углеводород,содержащий от двух до двенадцати атомов углерода, включающий неразветвленные, разветвленные и циклические неароматические алкенильные группы и включающий от одной до шести углеродуглеродных двойных связей. Неограничивающие примеры алкенильных групп включают следующие-6 016568 радикалы: винил, аллил, 1-пропен-2-ил, 1-бутен-3-ил, 1-бутен-4-ил, 2-бутен-4-ил, 1-пентен-5-ил, 1,3 пентадиен-5-ил, циклопентенил, циклогексенил, этилциклопентенил, этилциклогексенил и подобные им радикалы. Термин алкенил включает как незамещенные алкенильные группы, так и замещенные алкенильные группы. Термин "C2-Cn-алкенил", в котором n равен целому числу, составляющему от 3 до 12,означает алкенильную группу, содержащую от 1 до указанного числа "n" атомов углерода. В соответствии с настоящим описанием термин "алкинил" означает ненасыщенный углеводород,содержащий от двух до двенадцати атомов углерода, включающий неразветвленные, разветвленные и циклические неароматические алкинил группы и включающий от одной до шести углерод-углеродных тройных связей. Неограничивающие примеры алкинильных групп включают следующие радикалы: этилин, 1-пропин-3-ил, 1-бутин-4-ил, 2-бутин-4-ил, 1-пентин-5-ил, 1,3-пентадиин-5-ил и подобные им радикалы. Термин алкинил включает как незамещенные алкинильные группы, так и замещенные алкинильные группы. Термин "C2-Cn-алкинил", в котором n равен целому числу, составляющему от 3 до 12, означает алкинильну группу, содержащую от 1 до указанного числа "n" атомов углерода. Если количество атомов углерода не указано особо, "низший", например, в выражении "низшая алифатическая группа", "низший алкил", "низший алкенил" и "низший алкнил" в соответствии с настоящим описанием означают, что фрагмент содержит по меньшей мере один атом углерода (два для алкенила и алкинила) и менее или равен 6 атомам углерода. Термины "циклоалкил", "алициклический", "карбоциклический" и эквивалентные обозначения означают группу, включающую насыщенный или частично ненасыщенный карбоциклический цикл в одноядерной, спироциклической (с одним общим атомом) или конденсированной (с по меньшей мере одной общей связью) карбоциклической кольцевой системе, содержащей от трех до пятнадцати циклических членов. Неограничивающие примеры циклоалкильных групп включают следующие радикалы: циклопропил, циклобутил, циклопентил, циклопентен-1-ил, циклопентен-2-ил, циклопентен-3-ил, циклогексил, циклогексен-1-ил, циклогексен-2-ил, циклогексен-3-ил, циклогептил, бицикло[4,3,0]нонанил, норборнил и подобные им радикалы. Термин циклоалкил включает как незамещенные циклоалкильные группы, так и замещенные циклоалкильные группы. Термин "C3-Cn-циклоалкил", в котором n равен целому числу, составляющему от 4 до 15, означает циклоалкильную группу, содержащую от 3 до указанного числа "n" атомов углерода в циклической структуре. Если количество атомов углерода не указано особо, "низшая циклоалкильная" группа, упоминаемая в настоящем описании, содержит по меньшей мере 3 и меньше или равно 8 атомов углерода в своей циклической структуре. Термин "гетероциклоалкил" и эквивалентные обозначения означают группу, включающую насыщенный или частично ненасыщенный карбоциклический цикл в одноядерной, спироциклической (с одним общим атомом) или конденсированной (с по меньшей мере одной общей связью) карбоциклической кольцевой системе, содержащей от трех до пятнадцати циклических членов, включающую от одного до шести гетероатомов (например N, О, S, P), или группы, содержащие указанные гетероатомы (например,NH, NRx (Rx представляет собой алкил, ацил, арил, гетероарил или циклоалкил), РО 2, SO, SO2 и подобные им группы). Гетероциклоалкильные группы могут быть присоединены к атому С или гетероатому(например через атом азота), если это возможно. Неограничивающие примеры гетероциклоалкильных группы включают следующие радикалы: пирролидино, тетрагидрофуранил, тетрагидродитиенил, тетрагидропиранил, тетрагидротиопиранил, пиперидино, морфолино, тиоморфолино, тиоксантил, пиперазинил, азетидинил, оксэтанил, тиэтанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил,тиазепинил, 1,2,3,6-тетрагидропиридинил, 2-пирролинил, 3-пирролинил, индолинил, 2 Н-пиранил, 4 Нпиранил, диоксантил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3,1,0]гексанил,3-азабицикло[4,1,0] гептанил, 3H-индолил, хинолизинил и сахара и подобные им вещества. Термин гетероциклоалкил включает как незамещенные гетероциклоалкил группы, так и замещенные гетероциклоалкил группы. Термин "C3-Cn-гетероциклоалкил", в котором n равен целому числу, составляющему от 4 до 15, означает гетероциклоалкильную группу, содержащую от 3 до указанного числа "n" атомов углерода в циклической структуре, включающей по меньшей мере одну гетерогруппу или гетероатом, определение которых дано выше. Если количество атомов углерода не указано особо, "низшая гетероциклоалкильная" группа, упоминаемая в настоящем описании, содержит по меньшей мере 3 и меньше или 8 атомов углерода в своей циклической структуре. Термины "арил" и "арильный цикл" означают ароматическую группу, имеющую "4n+2" (пи) электронов, в которой n равен целому числу, составляющему от 1 до 3, в сопряженной моноциклической или полициклической системе (конденсированной или неконденсированной), и включающую от шести до четырнадцати атомов в цикле. Полициклическая система ядер включает по меньшей мере один ароматический цикл. Арил может быть присоединен непосредственно, или соединен через C1-C3-алкильную группу (группа также называется арилалкильной или аралкильной). Неограничивающие примеры арильных групп включают следующие радикалы: фенил, бензил, фенэтил, 1-фенилэтил, толил, нафтил, бифенил, третфенил, инденил, бензоциклооктенил, бензоциклогептенил, азуленил, аценафтиленил, флуоренил, фенантренил, антраценил и подобные им радикалы. Термин арил включает как незамещенные арильные группы, так и замещенные арильные группы. Термин "C6-Cn-арил", в котором n равен целому-7 016568 числу, составляющему от 6 до 15, означает арильную группу, содержащую от 6 до указанного числа "n" атомов углерода в циклической структуре, включающей по меньшей мере одну гетерогруппу или гетероатом, определение которых дано выше. Термины "гетероарил" и "гетероарильный цикл" означают ароматическую группу, имеющую"4n+2" (пи) электронов, в которой n равен целому числу, составляющему от 1 до 3, в сопряженной моноциклической или полициклической системе (конденсированной или неконденсированной), и включающую от пяти до четырнадцати атомов в цикле, включающем от одного до шести гетероатомов (например N, О, S), или группы, содержащие указанные гетероатомы (например, NH, NRx (Rx представляет собой алкил, ацил, арил, гетероарил или циклоалкил), SO и подобные им группы). Полициклическая система ядер включает по меньшей мере один гетероароматический цикл. Гетероарил может быть присоединен непосредственно, или соединен через C1-C3-алкильную группу (группа также называется гетероарилалкильной или гетероаралкильной). Гетероарильные группы могут быть присоединены к атому С или гетероатому (например, через атом азота), если это возможно. Неограничивающие примеры гетероарильных групп включают следующие радикалы: пиридил, имидазолил, пиримидинил, пиразолил, триазолил, тетразолил, фурил, тиенил, изооксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, изоиндолил, хроменил, изохроменил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, пиразинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиенил,бензотиазолил, бензоксазолил, хиназолинил, хинолизинил, хинолонил, изохинолонил, хиноксалинил,нафтиридинил, фуропиридинил, карбазолил, фенантридинил, акридинил, перимидинил, фенантролинил,феназинил, фенотиазинил, фенохазинил, дибензофуранил и подобные им радикалы. Термин гетероарил включает как незамещенные гетероарильные группы, так и замещенные гетероарильные группы. Термин"C5-Cn-гетероарил", в котором n равен целому числу, составляющему от 6 до 15, означает гетероарильную группу, содержащую от 5 до указанного числа "n" атомов углерода в циклической структуре, включающей по меньшей мере одну гетерогруппу или гетероатом, определение которых дано выше. Термины "гетероцикл" или "гетероциклический" включают гетероциклоалкильные и гетероарильные группы. Неограничивающие примеры гетероциклов включают: акридинил, азоцинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, бензимидазолинил, карбазолил, 4 Н-карбазолил, карболинил, хроманил, хроменил, циннолинил, декагидрохинолинил, 2 Н,6 Н-1,5,2-дитиазинил, дигидрофуро[2,3-b]тетрагидрофуран, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1 Ниндазолил, индолил, индолинил, индолизинил, индолил, 3H-индолил, изобензофуранил, изохроманил,изоиндазолил, изоиндолинил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, метилендиоксифенил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4 оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, оксазолидинил, оксазолил, оксазолидинил, пиримидинил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатиинил, феноксазинил,фталазинил, пиперазинил, пиперидинил, пиперидонил, 4-пиперидонил, пиперонил, птеридинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазол, пиридоимидазол, пиридотиазол, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, 2 Нпирролил, пирролил, хиназолинил, хинолинил, 4 Н-хинолизинил, хиноксалинил, хинуклидинил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, тетразолил, 6 Н-1,2,5-тиадиазинил, 1,2,3 тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, тиазолил, тиенил,тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиофенил, триазинил, 1,2,3-триазолил, 1,2,4 триазолил, 1,2,5-триазолил, 1,3,4-триазолил, ксантенил и подобные им радикалы. Термин гетероцикл включает как незамещенные гетероциклические группы, так и замещенные гетероциклические группы. В соответствии с настоящим описанием термин "амин" или "амино" означает незамещенный или замещенный фрагмент, отвечающий формуле -NRaRb, в которой каждый из Ra и Rb независимо представляет собой атом водорода, алкил, арил или гетероциклический радикал, или Ra и Rb, вместе с атомом азота, к которому они присоединены, образуют гетероцикл. Термин амино включает соединения или фрагменты, в которых атом азота ковалентно связан по меньшей мере с одним атомом углерода или гетероатомом. Таким образом, в соответствии с настоящим описанием термины "алкиламино" и "диалкиламино" означают аминогруппу, включающую, соответственно, одну и по меньшей мере две C1-C6-алкильные группы, присоединенных к аминогруппе. Термин "ариламино" и "диариламино" включают группы, в которых атом азота присоединен к по меньшей мере одной или двум арильным группам, соответственно. Термин "амид" или "аминокарбонил" включает соединения или фрагменты, которые содержат атом азота, который присоединен к атому углерода карбонильной или тиокарбонильной группы. Термин "ациламино" означает аминогруппу, непосредственно присоединенную к ацильной группе, рассматриваемой в настоящем описании. Термин "нитро" означает -NO2; термины "галогено" и "галоген" означают заместители, представляющие собой бром, хлор, фтор или йод; термины "тиол", "тио" или "меркапто" означают SH; и термин-8 016568 присоединена сульфгидрильная группа. Подходящие алкилтиогруппы включают группы, содержащие от 1 и приблизительно до 12 атомов углерода, предпочтительно от 1 и приблизительно до 6 атомов углерода. В соответствии с настоящим описанием термин "алкилкарбоксил" означает алкильную группу, к которой присоединена карбоксильная группа. Термин "алкокси(группа)" или "низшая алкоксигруппа" в соответствии с настоящим описанием означает алкильную группу, к которой присоединен атом кислорода. Некоторые примеры алкоксигрупп включают группы, содержащие от 1 и приблизительно до 6 атомов углерода, например метокси-, этокси-,пропокси-, трет-бутоксигруппу и подобные им группы. Примеры алкоксигрупп включают метокси-,этокси-, изопропилокси-, пропокси-, бутокси-, пентокси-, фторметокси-, дифторметокси-, трифторметокси-, хлорметокси-, дихлорметокси-, трихлорметоксигруппу и подобные им группы. Термин алкоксигруппа включает как незамещенные, так и замещенные алкоксигруппы и т.д., а также пергалогенированные алкилоксигруппы. Термин "карбонил" или "карбокси(группа)" включает соединения и фрагменты, которые содержат атом углерода, присоединенный посредством двойной связи к атому кислорода. Примеры частиц, которые содержат карбонил, включают альдегиды, кетоны, карбоновые кислоты, амиды, сложные эфиры,ангидриды и т.д. Термин "ацил" означает карбонильную группу, которая присоединена посредством имеющегося в ней атома углерода к атому водорода (т.е., формильная группа), алифатической группе (C1-C6-алкил, C1C6-алкенил, C1-С 6-алкинил, например, ацетил), циклоалкильной группе (C3-C8-циклоалкил), гетероциклической группе (С 3-С 8-гетероциклоалкил и C5-C6-гетероарил), ароматической группе (С 6-арил, например, бензоил) и подобным им группам. Ацильные группы могут быть незамещенными или замещенными ацильными группами (например, салицилоильная группа). Следует понимать, что термины "замещение" или "замещенный" включают явное предположение,что такое замещение происходит в соответствии с разрешенной валентностью замещаемого атома и заместителя и что такое замещение приводит к образованию стабильного соединения, например, такого,которое не подвергается спонтанным трансформациям, таким как перегруппировка, циклизация, элиминирование и т.д. В соответствии с настоящим описанием термин "замещенный" должен включать все возможные заместители органического соединения. В широком смысле, возможные заместители включают ациклические и циклические, разветвленные и неразветвленные, карбоциклические и гетероциклические, ароматические и неароматические заместители органического соединения. Возможный заместитель может быть один или их может быть несколько. Термин "замещенный", применяемый в сочетании с любой из вышеуказанных групп, означает группу, в одном или нескольких положениях которой имеется заместитель, например ацил, аминогруппа (включая простые аминогруппы, моно- и диалкиламиногруппы, моно- и диариламиногруппы и алкилариламиногруппы), ациламиногруппа (включая карбамоильную и уреидогруппы), алкилкарбонилоксигруппа, арилкарбонилоксигруппа, алкоксикарбонилоксигруппа,алкоксикарбонильная, карбоксигруппа, карбоксилат, аминокарбонильная, моно- и диалкиламинокарбонильная, цианогруппа, азидогруппа, галоген, гидроксильная группа, нитрогруппа, трифторметильная,тиогруппа, алкилтиогруппа, арилтиогруппа, алкилтиокарбонильная группа, тиокарбоксилат, низший алкил, низший алкенил, низший алкинил, циклоалкил, гетероциклоалкил, арил, гетероарил, низшая алкоксигруппа, арилоксигруппа, арилоксикарбонилоксигруппа, бензилоксигруппа, бензил, сульфинил, алкилсульфинил, сульфонил, сульфат, сульфонат, сульфонамид, фосфат, фосфонатную группу, фосфинатную группу, оксо, гуанидин, иминогруппу, формильную группу и подобные им группы. Любые из вышеуказанных заместителей также могут быть замещены, если это возможно, например, группа может содержать алкильную группу, арильную группу или другие группы. Термин "сольват" означает физическую ассоциацию соединения согласно настоящему изобретению с одной или несколькими молекулами растворителя, как органического, так и неорганического. Такая физическая ассоциация включает водородные связи. В некоторых примерах сольват может быть выделен, например, если одна или несколько молекул растворителя находятся в кристаллической решетке твердого кристаллического вещества. Термин "сольват" включает как находящиеся в растворе, так и выделяемые сольваты. Некоторые примеры сольватов включают гидраты, этаноляты, метаноляты, полуэтаноляты и подобные им объединения."Фармацевтически приемлемая соль" соединения означает соль соединения, которая является фармацевтически приемлемой. Желательным является использование солей, которые сохраняют или улучшают биологическую эффективность и свойства свободных кислот и оснований исходного соединения,рассматриваемого в настоящем описании, или те, в которых используется присущая молекуле функциональность - кислотность, основность или заряд, и которые не являются нежелательными с биологической или иной точки зрения. Примеры фармацевтически приемлемых солей описаны, например, в публикации(1) соли присоединения кислоты, образованные в результате присоединения к основной или положительно заряженной функциональной группе неорганических кислот: например, соляной кислоты,бромоводородной кислоты, йодоводородной кислоты, серной кислоты, сульфаминовой кислоты, азотной кислоты, фосфороной кислоты, веществ, образующих карбонаты, и подобных им веществ; или образо-9 016568 ванные органическими кислотами, например, уксусной кислотой, пропионовой кислотой, молочной кислотой, щавелевой кислотой, гликолевой кислотой, пивалиновой кислотой, терт-бутилуксусной кислотой, -гидроксимасляной кислотой, валериановой кислотой, гексановой кислотой, циклопентанпропионовой кислотой, винной кислотой, малоновой кислотой, яблочной кислотой, янтарной кислотой, малеиновой кислотой, фумаровой кислотой, винной кислотой, лимонной кислотой, бензойной кислотой, 3-(4 гидроксибензоил)бензойной кислотой, коричной кислотой, миндальной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, 1,2-этандисульфоновой кислотой, 2-гидроксиэтансульфоновой кислотой, циклогексиламиносульфоновой кислотой, бензолсульфоновой кислотой, сульфаниловой кислотой, 4-хлорбензолсульфоновой кислотой, 2-нафталинсульфоновой кислотой, 4-толуолсульфоновой кислотой, камфорсульфоновой кислотой, 3-фенилпропионовой кислотой, лаурилсульфоновой кислотой,лаурилсерной кислотой, олеиновой кислотой, пальмитиновой кислотой, стеариновой кислотой, лауриновой кислотой, эмбоновой (памовой) кислотой, пальмоиновой кислотой, пантотеновой (витамин В 3) кислотой, лактобионовой кислотой, альгиновой кислотой, галактаровой кислотой, галактоуроновой кислотой, глюконовой кислотой, глюкогептоновой кислотой, глютаминовой кислотой, нафтойной кислотой,гидроксинафтойной кислотой, салициловой кислотой, аскорбиновой кислотой, стеариновой кислотой,муконовой кислотой и подобными им кислотами;(2) соли присоединения основания, образованные при замещении кислотного фрагмента исходного соединения ионами металла, включающими ионы щелочных металлов (например, лития, натрия, калия),ионами щелочноземельных металлов (например, магния, кальция, бария) или ионами других металлов,например, алюминия, цинка, железа и подобных им металлов; или при координировании кислотной части органическим основанием, например, аммиаком, этиламином, диэтиламином, этилендиамином, N,N'дибензилэтилендиамином, этаноламин, диэтаноламин, триэтаноламином, трометамином, N-метилглюкамином, пиперазином, хлорпрокаином, прокаином, холином, лизином и подобными основаниями. Фармацевтически приемлемые соли могут быть синтезированы стандартными химическими методами из исходного соединения, которое содержит основной или кислотный фрагмент. В общем случае,такие соли готовят в соответствии с реакцией свободных кислотных или основных форм указанных веществ со стехиометрическим количеством подходящего основания или кислоты в воде или в органическом растворителе или в их смеси. Соли могут быть приготовлены in situ, во время окончательного выделения или очистки вещества или путем проведения отдельной реакции очищенного соединения согласно настоящему изобретению, в форме свободной кислоты основания с необходимым соответствующим основанием или кислотой, и выделения полученной таким образом соли. Термин "фармацевтически приемлемые соли" также включает цвиттер-ионные соединения, содержащие катионную группу, ковалентно связанную с анионной группой, поскольку они представляют собой "внутренние соли". Все кислотные, солевые, основные и другие ионные и неионные формы описанных соединений представляют собой соединения, предлагаемые согласно настоящему изобретению. Например, если в настоящем описании соединение показано в виде кислоты, то изобретение также включает солевые формы соединения. Аналогично, если соединение показано в виде соли, то изобретение также включает кислотные и/или основные формы соединения. В соответствии с настоящим описанием понятия "А-бета", "А" или "-амилоид" означают любой пептид, полученный при расщеплении бета-амилоидного предшественника белка (АПП) под действием бета-секретазы, включая, например, пептиды, состоящие из 37, 38, 39, 40, 41, 42 и 43 аминокислот, и включающий аминокислоты от сайта отщепления под действием бета-секретазы до аминокислот 37, 38,39, 40, 41, 42 или 43. Он также включает N-терминальные усеченные молекулы указанных пептидов, например пироглютаминовые формы рЕ 3-40, рЕ 3-42, рЕ 3-43, рЕ 11-42, рЕ 11-43 и подобные им белки. Для упрощения номенклатуры "А 1-42" в настоящем описании может быть обозначен как "А(1-42)" или просто как "АВ 42" (и аналогично может обозначаться любой другой амилоидный пептид, рассматриваемый в настоящем описании). В соответствии с настоящим описанием термины "А-бета", "А", "-амилоид","амилоид-р" представляют собой синонимы, совместно обозначающие усеченные и неусеченные молекулы пептидов, содержащие последовательность между сайтами - и -расщепления АПП. Термин "-амилоидное заболевание" или "заболевание, связанное с амилоидом-" могут обозначать умеренные когнитивные нарушения; сосудистое слабоумие; раннюю болезнь Альцгеймера; болезнь Альцгеймера, включая спорадическую (ненаследственную) болезнь Альцгеймера и семейную (наследственную) болезнь Альцгеймера; старческое ухудшение когнитивной функции; церебральную амилоидную ангиопатию ("ЦАА"); наследственную церебральную геморрагию; старческое слабоумие; синдром Дауна; миозит с включенными тельцами ("МВТ"); или старческую дистрофию желтого пятна ("СДЖП"),умеренные когнитивные нарушения ("УКН"), церебральную амилоидную ангиопатию ("ЦАА")."ППК (ППК, AUC)" означает площадь под кривой, отражающую концентрацию соединения в биологическом образце, взятом у субъекта, в виде функции от времени после введения субъекту соединения. Примеры биологических образцов включают биологические жидкости, например плазму и кровь, или гомогенаты органов, например гомогенаты мозга или печени. ППК может быть определена путем измерения концентрации соединения в биологическом образце, например в плазме, крови или гомогенате- 10016568 ткани мозга, с использованием таких методов, как жидкостная хроматография - тандемная массспектрометрия (ЖХ/МС/МС), через различные интервалы времени, и вычисления площади под кривой зависимости концентрации от времени. Подходящие способы расчета ППК зависимости концентрации лекарственного средства от времени хорошо известны в данной области техники. В соответствии с настоящим описанием ППК для 3-АПС может быть определена путем измерения концентрации 3-АПС в плазме, крови или гомогенате мозга субъекта после перорального введения субъекту соединений, имеющих формулы (IV), (V), (VI). Если не указано особо, в соответствии с настоящим описанием ППК означает ППК 0-, как описано ниже в примере 4."Биодоступность" означает скорость и количество лекарственного средства, которое попадает в системное кровообращение (большого круга) субъекта после введение субъекту лекарственного средства или его пролекарства, и может быть оценена путем определения, например, профиля зависимости концентрации лекарственного средства в плазме или крови от времени. Параметры, используемые для характеристики кривой зависимости концентрации лекарственного средства в плазме или крови от времени, включают площадь под кривой (ППК), время достижения пиковой концентрации (Tmax) и максимальную концентрацию лекарственного средства (Cmax). Биодоступность часто выражают в форме F(%), означающего отношение процентной доли ППК соединения для конкретного способа введения (например,перорального) к ППК соединения после IV (внутривенного) введения."Биоэквивалентность" означает эквивалентность скорости и степени абсорбции лекарственного средства введения равных доз лекарственного средства или пролекарства субъекту. В соответствии с настоящим описанием два профиля концентрации в плазме или крови считаются биоэквивалентными, если 90% доверительного интервала, полученного для соотношения средних ответных реакций для двух профилей, находится в диапазоне от 0,8 до 1,25. Средняя ответная реакция включает по меньшей мере один из характеристических параметров профиля, например, Cmax, Tmax и ППК."Cmax" представляет собой максимальную концентрацию лекарственного средства в биологическом образце, взятом у субъекта, после введения субъекту дозы лекарственного средства или пролекарства."Tmax" представляет собой время достижения максимальной концентрации (Cmax) лекарственного средства в биологическом образце, взятом у субъекта, после введения субъекту дозы лекарственного средства или пролекарства. В соответствии с настоящим описанием термин "эффективное количество" означает количество или дозу соединения, при введении субъекту однократной или многократной дозы, которое обеспечивает у субъекта желаемый эффект при диагностике или лечении. Эффективное количество может быть легко определено лечащим врачом-диагностом, который является специалистом в данной области техники, при помощи известных методик и с учетом результатов, полученных при аналогичных обстоятельствах. При определении эффективного количества или дозы вводимого соединения лечащий врач-диагност должен учитывать ряд факторов, неограничивающие примеры которых включают размеры, возраст и общее состояние здоровья субъекта; конкретное заболевание, подвергаемое лечению; стадию или прогресс или тяжесть заболевания; ответную реакцию конкретного субъекта; конкретное вводимое соединение; способ введения; характеристики биодоступности вводимого препарата; выбранный режим дозирования; применение сочетательной терапии; и другие важные обстоятельства. В соответствии с настоящим описанием термин "терапевтическое биораспределение 3-АПС" означает один или несколько фармакокинетических параметров 3-АПС, которые влияют на терапевтическое действие 3-АПС. Неограничивающие примеры таких фармакокинетических (ФК) параметров включают: биодоступность 3-АПС, ППК (площадь под кривой), рассчитанную для 3-АПС, концентрации 3-АПС в мозге, ЦСЖ уровни 3-АПС, Cmax для 3-АПС, Tmax для 3-АПС и/или биоабсорбцию 3-АПС и т.д. В соответствии с настоящим описанием термины "повышение (или подобные термины, например,повышенный и т.д.) терапевтической эффективности 3-АПС" и "усиление (или подобные термины, например, усиленный и т.д.) терапевтической эффективности 3-АПС" означают повышение эффективности 3-АПС, измеренное, например, в соответствии с одним или несколькими параметрами, перечисленными в разделе "Терапевтическое биораспределение 3-АПС", например на 5, 10, 20, 30, 40, 50, 60, 70, 80, 90,95, 99, 125% и т.д. или более, например в 2 или 4 раза или более, при введении субъекту, например животному или человеку, которая увеличивается по сравнению с эффектом той же эквивалентной молярной дозы 3-АПС, вводимой перорально в водном растворе. Предпочтительно такое же % повышение достигают также по сравнению с пероральным введением 3-АПС в композициях, указанных в табл. 3 USSN 11/103656 от 12 апреля 2005 г. Эффективность также может быть определена, например, по воздействию на характеристики заболевания, например болезни Альцгеймера, например, по снижению количества бляшек или нагрузки A в мозге, или по улучшениям в выбранных проявлениях заболевания, например,по снижению ухедшения памяти, улучшению когнитивных способностей, улучшению логического мышления, способности к рассуждениям, способности к ориентации и т.д. Подробности определения воздействия лекарственного средства на характеристики таких заболеваний можно найти в USSN 11/103656 от 12 апреля 2005 г. Термин "снижение метаболизма 3-АПС" (или схожие термины, например, "уменьшение, ниже, по- 11016568 нижение" и т.д.) означает снижение степени/количественной меры пресистемного метаболизма 3-АПС в ЖКТ или печени (при введении его субъекту не пероральным способом или в составе конкретных композиций для перорального введения или в виде пролекарства), например, на 5, 10, 20, 30, 40, 50, 60, 70,80, 90, 95, 99 или даже на 100%, т.е. снижение степени/количественной меры или метаболизма 3-АПС,который наблюдается при пероральном введении той же эквивалентной молярной дозы 3-АПС в водном растворе. Предпочтительно такое % снижение также достигают по сравнению с пероральным введением 3-АПС в композициях, указанных в табл. USSN 11/103656 от 12 апреля 2005 г. Термин "уменьшение побочных эффектов 3-АПС" означает уменьшение количества или тяжести одного или более побочных эффектов 3-АПС, например, на 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 95, 99, или 99,9 или даже на 100%, т.е. снижение по сравнению с количеством или тяжестью побочных эффектов 3 АПС, появляющихся при пероральном введении той же эквивалентной молярной дозы 3-АПС в водном растворе. Предпочтительно такого % снижения также достигают по сравнению с пероральным введением 3-АПС в композициях, указанных в табл. 3 USSN 11/103656 от 12 апреля 2005 г. В более общем случае, в контексте настоящего описания термины уменьшение и т.д., повышение и т.д. означают процентные изменения, например, на 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 95, 99, 125% и т.д. или более, например в 2 раза или даже более. Все фармакокинетические данные, приведенные в USSN 11/103656 от 12 апреля 2005 г., полностью включены в настоящее описание по ссылке, включая данные,приведенные, например, в табл. 1 и 3, например, для получения параметров сравнения для оценки воздействия соединений согласно настоящему изобретению. Под получением (например, высвобождении из лекарственной формы или пролекарства) "3-АПС" подразумевают все формы 3-АПС, например сольваты данного соединения, ионные диссоциированные формы данного соединения, заряженные формы данного соединения и т.д. Термин "фармацевтически приемлемый" относится к лекарствам, лекарственным средствам, инертным ингредиентам и т.д. и описывает вещества, подходящие для использования в контакте с биологическими тканями человека и низших животных без нежелательного токсического воздействия, несовместимости, нестабильности, не вызывающие раздражения, аллергических реакций и подобных реакций и имеющие разумное соотношение пользы и риска. Это предпочтительно означает соединение или композицию, одобренную или проходящую процедуру одобрения Федеральным или Государственным правительственным органом регулирования, или указанную в руководстве Фармакопее США или другой общепризнанной фармакопее, в котором указаны медикаменты, разрешенные к использованию для лечения животных и, в частности, человека."Фармацевтически приемлемый носитель" означает разбавитель, вспомогательное вещество, наполнитель или носитель, с которым вводят соединение. "Фармацевтическая композиция" включает по меньшей мере одно соединение и по меньшей мере один фармацевтически приемлемый носитель, с которым соединение вводят субъекту. Термины "предотвращать" или "предотвращение" означают по меньшей мере снижение вероятности риска (или предрасположенности) развития заболевания или нарушения (т.е., препятствование возникновению по меньшей мере одного из клинических симптомов заболевания у субъекта, который может быть подвержен или предрасположен к указанному заболеванию, но пока еще не страдает от заболевания или не проявляет симптомов заболевания). В некоторых примерах реализации термины "лечить" или "лечение" любого заболевания или нарушения означают смягчение течения по меньшей мере одного заболевания или нарушения (т.е., остановку или уменьшение развития заболевания или по меньшей мере одного из клинических симптомов заболевания). В некоторых примерах реализации термины "лечить" или "лечение" означают улучшение по меньшей мере одного физического параметра, который может быть или может не быть отмечен субъектом. В некоторых примерах реализации термины "лечить" или "лечение" означают ингибирование заболевания или нарушения как физически (например, стабилизация явного симптома), так и физиологически(например, стабилизация физического параметра) или и физически, и физиологически. В некоторых примерах реализации термины "лечить" или "лечение" означают отсрочку начала развития заболевания или нарушения. Термин "лечение" означает любые показатели успеха в лечении или облегчении повреждения, патологии или состояний, включающие любые объективные или субъективные показатели субъекта, например ослабление; ремиссию; уменьшение интенсивности симптомов или превращение повреждения, патологии или состояния до лучше переносимого субъектом состояния; замедление скорости дегенерации или истощения; изменение результата дегенерации на менее тяжелый; улучшение физического или душевного состояния субъекта; или, в некоторых ситуациях, предотвращение возникновения слабоумия. Лечение или снижение выраженности симптомов может быть основано на объективных параметрах или субъективном самочувствии субъекта, которые включают результаты физического обследования, психиатрической оценки или проверки когнитивных способностей, например, CDR, MMSE, DAD,ADAS-Cog, или иных тестов, известных в данной области техники. Например, способы, предлагаемые согласно настоящему изобретению, пригодны для успешного лечения слабоумия субъекта, поскольку позволяют снижать скорость или уменьшать степень ослабления когнитивных способностей субъекта.- 12016568 субъекту для лечения или предотвращения заболевания достаточно для осуществления указанного лечения или предотвращения заболевания. "Терапевтически эффективное количество" может быть различным в зависимости от типа соединения, типа заболевания и его тяжести, а также возраста, массы и т.д. субъекта, страдающего заболеванием, которое следует лечить или предотвращать. Ниже будут подробно рассмотрены некоторые примеры реализации соединений и способов согласно настоящему изобретению. Рассмотренные примеры реализации не предназначены для ограничения настоящего изобретения. Другой аспект изобретения включает введение 3-АПС, которое не включает введение через трансдермальный пластырь или топическое введение соединения в виде композиций, например, лосьонов,кремов, растворов, гелей или твердых веществ, или не включает введение 3-АПС посредством подкожной, внутривенной или внутрибрюшинной инъекции или введением в спинномозговой канал или внутримозговым введением.II. Соединения согласно настоящему изобретению. Настоящее изобретение относится к способам, соединениям и композициям для доставки в организм субъекта, предпочтительно субъекта-человека, 3-амино-1-пропансульфоновой кислоты или ее солей, которые в настоящей заявке также обозначаются 3-АПС. Изобретение включает соединения, которые могут превращаться в или образовывать 3-АПС как in vitro, так и in vivo. В предпочтительном варианте реализации соединения согласно настоящему изобретению включают пролекарства, которые могут превращаться в или образовывать 3-АПС при введении человеку. В соответствии с предпочтительными примерами реализации соединения, предлагаемые согласно настоящему изобретению, проявляют различные полезные свойства. В одном из примеров реализации соединение представляет собой пролекарство, которое, по существу, не подвергается пресистемному метаболизму в печени и/или пищеварительном тракте (например, кишечнике, желудке или тонком кишечнике), связанному с введением 3-АПС, и, таким образом, повышает биораспределение и/или биодоступность 3-АПС по сравнению с введением молярного эквивалента 3-АПС. Избежание пресистемного метаболизма в печени модифицирует, улучшает или повышает фармакокинетические параметры 3-АПС, например ППК,Cmax и/или Tmax 3-АПС. В одном из примеров реализации соединение представляет собой пролекарство,которое, по существу, проявляет повышенную абсорбцию в желудочно-кишечном тракте по сравнению с введением молярного эквивалента 3-АПС. В одном из примеров реализации соединение представляет собой пролекарство, которое обеспечивает замедленное высвобождение 3-АПС в течение некоторого времени. В другом варианте реализации соединение представляет собой пролекарство, которое по существу повышает концентрации 3-АПС в мозге по сравнению с введением молярного эквивалента 3-АПС. В другом варианте реализации, соединение представляет собой пролекарство, которое по существу уменьшает обычные побочные эффекты, связанные с введением 3-АПС. Например, в предпочтительном варианте реализации пролекарство имеет лучшую желудочно-кишечную толерантность по сравнению с 3-АПС. В предпочтительных примерах реализации соединения и/или композиции, предлагаемые согласно настоящему изобретению, имеют одно или несколько следующих преимуществ: (1) снижение молярной дозы 3-АПС, вводимой субъекту (например, благодаря улучшению абсорбции по сравнению 3-АПС или благодаря ослаблению пресистемного метаболизма 3-АПС); (2) отсутствие обычных побочных эффектов,например желудочно-кишечного раздражения, при пероральном введении 3-АПС; (3) улучшение проникновения 3-АПС через гематоэнцефалический барьер; (4) ослабление побочных эффектов, связанных с приемом 3-АПС (например, ослабление желудочно-кишечных проблем или повышение относительного количества 3-АПС, достигающего мозга; (5) повышение концентрации или уровней 3-АПС в целевых тканях или жидкостях (например, мозге, цереброспинальной жидкости (CSF. Другие преимущества должны быть понятны специалистам в данной области техники. Изобретение включает солевые формы и кислотные и/или основные формы соединений согласно настоящему изобретению. Например, изобретение включает не только конкретные солевые формы соединения, рассматриваемые в настоящем описании как соли, но, кроме того, изобретение включает другие фармацевтически приемлемые соли, и кислотные и/или основные формы соединений. Изобретение также относится к солевым формам соединений, рассматриваемых в настоящем описании. Соединения,предлагаемые согласно настоящему изобретению, представлены ниже в табл. 1, табл. 2, табл. 3, табл. 4 и табл. 4 В. Соединения, предлагаемые согласно настоящему изобретению, могут проявлять полиморфизм. Полиморфные формы соединений согласно настоящему изобретению могут быть приготовлены кристаллизацией в различных условиях. Например, для перекристаллизации используют различные растворители или различные смеси растворителей; используют кристаллизацию при различных температурах; используют различные способы охлаждения во время кристаллизации, начиная от очень медленного и заканчивая самым быстрым. Полиморфные формы также могут быть получены нагреванием или плавлением пролекарства с последующим постепенным или быстрым охлаждением. Наличие полиморфных форм может быть определено при помощи ЯМР спектроскопии с твердым зондом, ИК спектроскопии,дифференциальной сканирующей калориметрии, порошкового рентгеноструктурного анализа или других подобных методик.II-А. Аминокислотные пролекарства. В предпочтительном варианте реализации соединения, предлагаемые согласно настоящему изобретению, представляют собой аминокислотные пролекарства (т.е. пролекарства, в которых основное соединение связано с аминокислотой), которые могут превращаться в или образовывать 3-АПС после введения в организм человека. Предпочтительные пролекарства содержат остаток аминокислоты, присоединенный к аминогруппе 3-АПС амидной связью. Остаток аминокислоты может быть отщеплен in vivo под действием ферментов, например пептидазы, или в соответствии с любым другим механизмом, с высвобождением аминогруппы 3-АПС. Более конкретно, один из аспектов изобретения относится к соединению, имеющему формулу (IV),и к фармацевтически приемлемым солям указанного соединения: в котором аа 1 представляет собой остаток природной или неприродной аминокислоты; аа 2 представляет собой остаток природной или неприродной аминокислоты или отсутствует. Другие аспекты настоящего изобретения относятся к соединению, соответствующему формуле (V),и к фармацевтически приемлемым солям, сложным эфирам или сольватам указанного соединения: в котором аа 1 представляет собой остаток природной или неприродной аминокислоты. Остатки природной или неприродной аминокислот в формуле IV могут быть представлены формулой (VI): в которой R1 представляет собой замещенную или незамещенную группу, выбранную из следующих C1-C12-алкил, C3-C15-циклоалкил, гетероциклоалкил, имеющий от 3 до 8 атомов в кольце, включая от 1 до 4 гетероатомов, выбранных из азота, кислорода и серы, и гетероциклоалкил, имеющий от 5 до 8 атомов в кольце, включая от 1 до 4 гетероатомов, при этом когда указанная группа замещена, она замещена группой выбранной из NH2, ОН, карбокси, C1-C6 алкокси, C1-C6-алкилтио, бензилокси, бензилоксикарбонил;R3 представляет собой водород или связь между двумя остатками аминокислот, когда оба аа 1 и аа 2 представляют собой остатки аминокислот;R4 представляет собой Н; или R1 и R4 вместе с соседними атомами углерода и азота образуют C3-C10-гетероциклоалкил; иn равен 1. В одном из примеров реализации соединение согласно настоящему изобретению включает остаток аминокислоты, представленный формулой VI, в котором R2 представляет собой Н, и все остальные группы описаны выше. В другом варианте реализации соединение согласно настоящему изобретению включает остаток аминокислоты, представленный формулой VI, в котором каждый из R2 и R3 представляет собой Н, и все остальные группы описаны выше. В другом варианте реализации соединение согласно настоящему изобретению включает остаток аминокислоты, представленный формулой VI, в котором,если каждый из R2 и R3 представляет собой Н, то R1 не представляет собой арилзамещенный C1-алкил. В другом варианте реализации соединение согласно настоящему изобретению, включает остаток аминокислоты, представленный формулой VI, в котором, если каждый из R2 и R3 представляет собой Н, то R1 не представляет собой группу -СН 2 арил. В другом варианте реализации соединение согласно настоящему изобретению включает остаток аминокислоты, представленный формулой VI, в котором, если R2 представляет собой Н, и R3 представляет собой Н или связь, то R1 не представляет собой группу -СН 2 фенил. В другом варианте реализации изобретение включает соединения, отвечающие формуле V, при условии, что аа 1 не представляет собой фенилаланин. В другом варианте реализации изобретение включает соединения, отвечающие формуле IV, при условии, что аа 1 и аа 2 не представляют собой Dфенилаланин. В другом варианте реализации, изобретение включает соединения, отвечающие формулеIV, при условии, что аа 1 и аа 2 не представляют собой L-фенилаланин. В другом варианте реализации изобретение включает соединения, отвечающие формуле IV, при условии, что, если один из аа 1 или аа 2 представляет собой D-фенилаланин, то другой фрагмент не представляет собой D-фенилаланин или Dтирозин. В еще одном варианте реализации изобретение включает соединения, отвечающие формуле IV,при условии, что если один из аа 1 или аа 2 представляет собой L-фенилаланин, то другой фрагмент не представляет собой D-фенилаланин или L или D-тирозин.- 14016568 Таблица 1. Примеры аминокислотных пролекарств согласно настоящему изобретению- 15016568 Предпочтительные аминокислотные пролекарства, предлагаемые согласно настоящему изобретению, представляют собой соединения А 2, А 4, А 6, А 7 и А 18 (описанные выше) и фармацевтически приемлемые соли и сольваты указанных соединений.III. Синтез соединений согласно настоящему изобретению. В общем случае все соединения согласно настоящему изобретению могут быть приготовлены в соответствии со способами, рассмотренными в примерах, описанных ниже, и/или в соответствии с другими стандартными методами, с использованием доступных готовых исходных материалов и/или исходных материалов и реагентов, приготавливаемых традиционными способами, и традиционных методик синтеза. В указанных реакциях могут быть использованы уже известные варианты, которые, тем не менее, не рассмотрены в настоящем описании. Некоторые новые способы и примеры способов приготовления соединений согласно настоящему изобретению описаны в разделе "Примеры". Такие способы также включены в настоящее изобретение. Настоящее изобретение также включает функциональные или структурные эквиваленты соединений, рассматриваемых в настоящем описании, имеющие описанные общие свойства, а также имеющие один или несколько простых вариантов заместителей, которые не оказывают отрицательного влияния на существенные свойства соединений. Более конкретно, аминокислотные пролекарства, предлагаемые согласно настоящему изобретению,могут быть приготовлены в соответствии со способами, рассмотренными в примере 1-А, описанном ниже, и в соответствии с общими схемами реакций, например схемами 1 и 2, или в соответствии с вариантами указанных схем. Карбаматные пролекарства, предлагаемые согласно настоящему изобретению, могут быть получены в соответствии со способами, рассмотренными в примере 1-В, описанном ниже, или в соответствии с вариантами указанного примера. Неаминокислотные пролекарства, предлагаемые согласно настоящему изобретению, могут быть получены в соответствии со способами, рассмотренными в примере 1-С, описанном ниже, и в соответствии с общими схемами реакций, например реакцией амидного сочетания, показанной на схемах 1 и 2,или в соответствии с вариантами указанных схем. Пролекарства на основе производных углеводов могут быть получены в соответствии со способами, рассмотренными в примере 1-D, описанном ниже, или при помощи известных реакций, в зависимости от используемого соединительного фрагмента (карбамата, мочевины, амида и подобных фрагментов), или в соответствии с вариантами указанного примера. Пролекарства на основе N-гидроксипроизводных и их производных могут быть получены окислением аминогруппы и, при необходимости, алкилированием указанной N-гидроксигруппы. Методики выполнения указанных реакций доступны и хорошо известны специалистам в данной области техники. Циклические пролекарства с двойной защитой готовят в соответствии со стандартными способами циклизации указанных групп, в зависимости от используемых групп D и X. Соединения согласно настоящему изобретению могут быть легко получены в соответствии со схемами синтеза и протоколами, рассматриваемыми в настоящем описании, и в соответствии с предлагаемыми процедурами. Тем не менее, специалистам в данной области техники должно быть понятно, что существуют и другие способы синтеза предлагаемых соединений и что приведенные методики даны лишь для примера и не ограничивают область, защищаемую настоящим изобретением. См., например,"Comprehensive Organic Transformations", R. Larock, VCH Publishers (1989). Также следует понимать, что могут быть использованы различные способы защиты и снятия защиты, хорошо известные в данной области техники (см., например, "Protective Groups in Organic Synthesis", Greene and Wuts (1991. Специалисты в данной области техники должны понимать, что выбор любой конкретной защитной группы (например, аминогруппы, гидроксила, тиогруппы и карбоксильной защитной группы) зависит от стабильности защищаемого фрагмента в условиях конкретной проводимой реакции, и смогут выбрать подходящий способ защиты. Другие примеры методик, известных специалистам в данной области техники, приведены, например, в следующей химической литературе: "Chemistry of the Amino Acids", J.P. Greenstein, M. Winitz, JohnBailey, John WileySons, Inc., New York (1992). Синтез соединений согласно настоящему изобретению предпочтительно проводят в растворителе. Подходящие растворители представляют собой жидкости при обычной комнатной температуре и обычном давлении или остаются в жидком состоянии при температуре и давлении, применяемых в реакции. Выбор растворителя доступен обычному специалисту в данной области техники и зависит от условий реакции, например температуры, природы реагентов и исходного материала, растворимости и стабильности реагентов и исходного материала, типа реакции и подобных соображений. В зависимости от об- 16016568 стоятельств, растворители могут быть дистиллированными или дегазированными. Растворители могут представлять собой, например, алифатические углеводороды (например, гексаны, гептаны, лигроин, петролейный эфир, циклогексан или метилциклогексан) и галогенированные углеводороды (например, метиленхлорид, хлороформ, четыреххлористый углерод, дихлорэтан, хлорбензол или дихлорбензол); ароматические углеводороды (например, бензол, толуол, тетрагидронафталин, этилбензол или ксилол); простые эфиры (например, диглим, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, этил-третбутиловый эфир, диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран или метилтетрагидрофураны, диоксан, диметоксиэтан или диметиловый эфир диэтиленгликоля); амиды (например, N,Nдиметилформамид, N,N-диметилацетамид); нитрилы (например, ацетонитрил); кетоны (например, ацетон); сложные эфиры (например, метилацетат или этилацетат); спирты (например, метанол, этанол, изопропанол); воду и смеси указанных веществ."Активированные сложные эфиры" и эквивалентные обозначения могут быть представлены Формулой СОХ, в которой X представляет собой отделяемую группу, типичные примеры которой включаютN-гидроксисульфосукцинимидил и N-гидроксисукцинимидил; арилоксигруппы, имеющие электроноакцепторные заместители (например, п-нитро-, пентафтор-, пентахлор-, п-циано- или п-трифторметил-); и карбоновые кислоты, активированные карбодиимидом или другим традиционным сочетающим реагентом с образованием ангидрида или смешанного ангидрида, например, группы -OCORa или -OCNRaNHRb,в которых Ra и Rb независимо представляют собой C1-C6-алкил, C5-C8-алкил (например, циклогексил),C1-C6-перфторалкил или C1-C6-алкоксигруппы. Активированный сложный эфир может быть образован insitu или может представлять собой выделяемый реагент. Сложноэфирные отделяемые группы могут представлять собой, например, сложные эфиры сульфосукцинимидила, сложные эфиры пентафтортиофенола, сульфотетрафторфенола, замещенные или незамещенные C1-C6-алкилы (например, метил, этил,пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил или гексил), или замещенные или незамещенные C6-C14-арильные группы или гетероциклические группы, например, следующие фрагменты: 2-фторэтил, 2-хлорэтил, 2-бромэтил, 2,2-дибромэтил, 2,2,2-трихлорэтил, 3-фторпропил, 4-хлорбутил,метоксиметил, 1,1-диметил-1-метоксиметил, этоксиметил, N-пропоксиметил, изопропоксиметил, Nбутоксиметил, трет-бутоксиметил, 1-этоксиэтил, 1-метил-1-метоксиэтил, 1-(изопропокси)этил, 3 метоксипропил-4-метоксибутил, фторметоксиметил, 2,2,2-трихлорэтоксиметил, бис(2-хлорэтокси)метил,3-фторпропоксиметил, 4-хлорбутоксиэтил, дибромметоксиэтил, 2-хлорэтоксипропил, фторметоксибутил,2-метоксиэтоксиметил, этоксиметоксиэтил, метоксиэтоксипропил, метоксиэтоксибутил, бензил, фенэтил,3-фенилпропил, 4-фенилбутил, -нафтилметил, -нафтилметил, дифенилметил, трифенилметил, нафтилдифенилметил, 9-антрилметил, 4-метилбензил, 2,4,6-триметилбензил, 3,4,5-триметилбензил, 4 метоксибензил, 4-метоксифенилдифенилметил, 2-нитробензил, 4-нитробензил, 4-хлорбензил, 4 бромбензил, 4-цианобензил, 4-цианобензилдифенилметил или бис(2-нитрофенил)метил.III. Примеры синтеза аминокислотных пролекарств согласно настоящему изобретению. Следующие схемы приведены для иллюстрации, но не для ограничения настоящего изобретения. Сочетание 3-амино-1-пропансульфоновой кислоты с первой аминокислотой может быть в общем случае представлено схемой 1. Схема 1 в которой R1, R2 и R4 описаны выше, Rz представляет собой R3 или защитную группу и X представляет собой покидающую группу активированного сложного эфира. На схеме 1 моноаминокислотное пролекарство 3-амино-1-пропансульфоновой кислоты получают по реакции свободной аминогруппа молекулы (или защищенного сульфонатного эфира) с активированным сложным эфиром требуемой аминокислоты (которая может быть N-защищенной). Группа С(О)Х активированного сложного эфира может представлять собой ацилгалогенид, смешанный ангидрид,сложный эфир сукцинимида или может представлять собой карбоновую кислоту, активированную пептидным сочетающим агентом (например, карбодиимидами (например, EDC (1-(3-диметиламинопропил)3-диизопропилэтилкарбодиимидом и солями урония (например, HATU (О-(7-азабензотриазол-1-ил)N,N,N',N'-тетраметилуронийгексафторфосфатом, в присутствии основания (например, аминов (например, DIPEA (N,N-диизопропилэтиламина), гидроксидов (например, гидроксида натрия), карбонатов (например, карбоната калия) и т.д.), и, возможно, катализатора (например 4-(диметиламино)пиридина(DMAP), 1-гидроксибензотриазола (HOBt. Выбор основания и катализатора в основном зависит от при- 17016568 роды активированного сложного эфира. На этом этапе защитные группы (Rz на аминогруппе или защитные группы, присутствующие на гетероатомах в группах R1 и R2) могут быть удалены. Защитные группы на гетероатомах, отличные от аминогрупп, могут быть оставлены, если проводят дальнейшие сочетания аминокислот (см. схему 2). Защитные группы на атомах кислорода могут включать бензиловые и силильные простые эфиры, ацетали и сложные эфиры, защитные группы на атоме азота могут включать карбаматы и производные флуорена. Их отщепляют при помощи широко используемых процедур (см., например, Greene and WutsR , показанными в вышеуказанной схеме, и R1, R2, R4, Rz и X описаны выше. В соответствии со схемой 2 получают пролекарства, включающие две или более аминокислоты,присоединенные к 3-АПС. Условия сочетания в общем случае аналогичны условиям, описанным для схемы 1. Последующие аминокислоты присоединяют аналогичным образом, проводя снятие защиты с аминогруппы после проведения каждой операции сочетания. Если на гетероатомах остатков присутствуют другие защитные группы, то они могут быть удалены в последней операции химической обработки. В общем случае, после завершения реакции, продукт выделяют из реакционной смеси в соответствии со стандартными методиками. Например, растворитель удаляют испарением или фильтрованием,если продукт твердый, возможно, под уменьшенным давлением. После завершения реакции к остатку может быть добавлена вода, и водный слой может быть подкислен или подщелочен, и выпавшее соединение отфильтровано; при этом следует с осторожностью обращаться с соединениями, чувствительными к воде. Аналогично, к реакционной смеси может быть добавлена вода с гидрофобным растворителем с целью экстракции целевого соединения. Органический слой может быть промыт водой, высушен над безводным сульфатом магния или сульфатом натрия и растворитель испарен с получением целевого соединения. Полученное таким образом целевое соединение при необходимости может быть очищено, например, перекристаллизацией, переосаждением, хроматографией или превращением его в соль при добавлении кислоты или основания.IV. Альтернативные пути и средства для доставки 3-АПС, позволяющие сводить к минимуму или снижать пресистемный метаболизм в печени. Как было отмечено выше, один из аспектов настоящего изобретения относится к новым путям введения (например, трансдермальным, подкожным, интраназальным и т.д.) и новым фармацевтическим носителям (например, пластырям, имплантантам, спреям, композициям (включающим композиции для перорального введения позволяющим уменьшать пресистемный метаболизм 3-АПС в печени. Устройства для трансдермальной доставки лекарственного средства Доставка медикаментов трансдермальным способом привлекает растущий интерес, поскольку преимуществом указанного способа является продолжительное и постоянное введение лекарственного средства в кровь. Трансдермальная доставка 3-АПС представляет собой один из предпочтительных примеров реализации настоящего изобретения, поскольку позволяет избежать пресистемного метаболизма в печени при введении 3-АПС и, таким образом, повышает терапевтический эффект 3-АПС. Трансдермальная доставка также позволяет избежать болевых ощущений, связанных с инъекциями, и может повышать гибкость режима дозирования. Соответственно, некоторые аспекты настоящего изобретения относятся к способу доставки соединений согласно настоящему изобретению, предпочтительно 3-АПС, которые улучшают эффективность соединения при лечении когнитивных нарушений. Изобретение также относится к способу доставки соединения согласно настоящему изобретению, предпочтительно 3-АПС, в котором соединение может быть введено посредством трансдермального пластыря. Устройства трансдермальной доставки лекарственного средства, предлагаемые согласно настоящему изобретению, могут быть изготовлены с использованием способов и компонентов, хорошо известных специалисту в данной области техники. Устройство трансдермальной доставки лекарственного средства обычно включает защитный слой, который возможно состоит из пигментированной пленки полиэстера,4- 18016568 резервуар с лекарственным средством, микропористой мембраной, которая контролирует скорость доставки лекарственного средства из системы на поверхность кожи, и адгезионной композиции, предназначенной для фиксации системы доставки на теле субъекта. Возможно, адгезионная композиция может включать лекарственное средство, таким образом, ускоренное выделение дозы после фиксации пластыря на теле субъекта. Устройства трансдермальной доставки лекарственного средства также обычно включают носитель(например, жидкость, гель или твердую матрицу или адгезионный агент, чувствительный к давлению), в который введено действующее лекарственное средство. Носитель, содержащий лекарственное средство,затем наносят на кожу, и лекарственное средство, вместе с любыми вспомогательными веществами и наполнителями, попадает на кожу. Обычно части носителя, не контактирующие с кожей субъекта, закрыты защитным слоем. Защитный слой нужен для защиты носителя (и компонентов, содержащихся в носителе, включая медикамент) от воздействия окружающей среды и предотвращения утечки ингредиентов устройства доставки лекарственного средства в окружающую среду. Поскольку известно, что гидратация рогового слоя усиливает транспорт некоторых медикаментов через кожный покров, иногда желательно, чтобы защитный слой имел относительно низкую скорость пропускания паров влаги с целью удержания влаги на участке, закрытом устройством доставки лекарственного средства. Для поддержания здорового состояния закрытого участка кожи при долговременном ношении устройства (например, в течение времени, превышающего одни сутки), чтобы позволить коже дышать, также желательно, чтобы защитный слой имел относительно высокую проницаемость по отношению к кислороду. Кроме того,поскольку защитный слой находится в контакте с компонентами носителя, включая медикамент и любые вспомогательные вещества и наполнители, важно, чтобы защитный слой был стабильным по отношению к указанным компонентам, чтобы защитный слой оставался структурно целостным, имел постоянный предел прочности и хорошо прилегал к телу. Также желательно, чтобы защитный слой не впитывал из носителя медикамент или другие наполнители. При изготовлении некоторых устройств трансдермальной доставки лекарственного средства типа резервуаров также желательно, чтобы защитный слой был удобен для термосклеивания при относительно низкой температуре как с самим собой, так и с рядом других полимерных подложек. Материалы защитного слоя, применяемые для изготовления устройств трансдермальной доставки лекарственного средства, включают металлические фольги, металлизированные пластиковые пленки и однослойные и многослойные полимерные пленки (см. патент США 5264219). Мембраны, пригодные для изготовления трансдермального пластыря, известны в данной области техники, и их неограничивающие примеры включают мембраны CoTran, коммерчески поставляемые 3M, например, мембраны COTRAN 9701, 9702, 9705, 9706, 9715, 9716, 9726 и COTRAN 9728. Защитный слой, пригодный для изготовления трансдермального пластыря, известен в данной области техники, и неограничивающие примеры такого слоя включают материал защитного слоя, коммерчески поставляемые 3M, например, защитные слои COTRAN и SCOTCHPAK. Аналогично, прокладочные материалы хорошо известны в данной области техники и могут быть получены из ряда коммерческих источников. Возможно, могут быть добавлены желирующие агенты в количестве до 20 об.%. Неограничивающие примеры желирующих агентов включают: сшитые полимеры акриловой кислоты, например семейство полимеров типа "карбомер", например, карбоксиполиалкилены, которые могут быть получены из коммерческих источников под торговой маркой KAPBOPOL; гидрофильные полимеры, например полиэтиленоксиды, полиоксиэтилен- полиоксипропиленовые сополимеры и поливиниловый спирт; целлюлозные полимеры, например гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилметилцеллюлозу, фталат гидроксипропилметилцеллюлозы, метилцеллюлозу; камеди, например трагакантовую камедь и ксантановую камедь; альгинат натрия; и желатин. Специалист в данной области техники легко определит подходящее сочетание и/или концентрацию защитного слоя, резервуара с лекарственным средством, мембраны, носителя, защитного слоя, усилителя проникновения, желирующего агента и т.д. При необходимости, можно обратиться к многочисленным публикациям по этой теме, включающим патентную литературу, например, заявки ЕР 1602367, US 2005/019384, US 2005/0074487 и US 2005/175680, в каждой из которых описаны устройства трансдермальной доставки лекарственного средства и аналогичные устройства. Например, для определения пригодности трансдермальной доставки при помощи конкретного носителя или носителей может быть использовано определение абсорбции лекарственного средства через кожу человека. Например, проницаемость соединений согласно настоящему изобретению, предпочтительно 3-АПС, через эпидермис человека может быть определена in vitro при помощи диффузии клеток через стекло. Таким образом, оптимизация абсорбции соединений достигается при использовании композиций, рассмотренных в настоящем описании и известных в данной области техники как усилители проникновения. Дополнительные хорошо известные тесты и анализы включают исследования скорости проникновения, исследования абсорбции, диффузионные анализы, исследования временных профилей проникновения через человеческий эпидермис, исследования возникновения раздражений и т.д. Клинические исследования указывают на то, что доза 3-АПС, введенная перорально и составляющая приблизительно 100 и/или 150 мг bid (bis in die (2 раза в сутки, может создавать благоприятный- 19016568 эффект при лечении когнитивных нарушений, например, БА. Таким образом, трансдермально введенные соединения согласно настоящему изобретению, предпочтительно 3-АПС, подвергаются сниженному пресистемному метаболизму, дозировка 3-АПС при трансдермальном введении может быть снижена. С другой стороны, трансдермальное введение может способствовать повышению дозировки 3-АПС, поскольку исключает появление обычных побочных эффектов, например раздражения желудочнокишечного тракта, связанного с пероральным введением этого лекарственного средства. Преимущества трансдермального введения лекарственной формы включают улучшенное состояние субъекта благодаря возможности снижения количества введений. Например, трансдермальный пластырь согласно настоящему изобретению, может быть изготовлен таким образом, чтобы он обеспечивал введение лекарственного средства в течение одних, двух, трех, четырех, пяти, шести или семи суток. В одном из примеров реализации трансдермальный пластырь обеспечивает введение лекарственного средства в течение приблизительно трех суток, после чего пластырь желательно заменить. В другом возможном варианте реализации трансдермальный пластырь обеспечивает введение лекарственного средства в течение семи суток, после чего пластырь желательно заменить. Кроме того, в трансдермальные лекарственные формы могут быть введены любые желательные дозировки соединений согласно настоящему изобретению. Например, трансдермальная лекарственная форма может обеспечивать дозировку, эквивалентную пероральному введению 100 мг bid (bis in die (2 раза в сутки, 150 мг bid, 200 мг bid, 250 мг bid,300 мг bid, 350 мг bid или 400 мг bid. Соответственно, трансдермальный пластырь (пластыри), содержащий дозировку, эквивалентную пероральному введению 150 мг bid, может быть зафиксирован на теле субъекта в течение желательного периода времени, например четырех недель, а затем в течение желательного периода времени на теле субъекта может быть зафиксирован трансдермальный пластырь или пластыри, включающие дозировку, эквивалентную пероральному введению 200 мг bid. Изобретение также включает набор, который может содержать желаемый запас пластырей, например месячный запас трансдермальных пластырей. Возможно, набор может быть выполнен в виде нескольких, например, трех по-разному обозначенных (пронумерованных, разного цвета и т.д.) частей,причем сначала вводят содержимое первой части, затем - содержимое второй части и затем - содержимое третьей части. В альтернативном случае набор может содержать комбинацию пластырей и композиций для перорального введения.V. Субъекты и популяции пациентов. Термин "субъект" включает живые организмы, у которых может возникать А-амилоидоз, или которые подвержены А-амилоидным заболеваниям, например болезни Альцгеймера и т.д. Примеры субъектов включают человека, кур, уток, уток пекинской породы, гусей, обезьян, оленей, коров, кроликов,овец, коз, собак, кошек, мышей, крыс и трансгенных видов указанных животных. Термин "субъект" предпочтительно включает животных, которые подвержены состояниям, характеризующимся гибелью нейронных клеток, например, млекопитающих, например, людей. Животное может представлять собой подопытное животное, имеющее требуемое нарушение, например трансгенную мышь, страдающую нейропатологией типа болезни Альцгеймера. В предпочтительных примерах реализации субъект представляет собой млекопитающее, более предпочтительно субъект представляет собой человека. Термин "субъект-человек" включает людей, которые могут получить пользу от введения 3-АПС, и,более конкретно, людей, которые подвержены риску развития или которым поставлен диагноз заболевания, связанного с амилоидом-, и/или страдающих нейродегенеративным заболеванием, например, болезнью Альцгеймера, болезнью Паркинсона и т.д. В некоторых примерах реализации настоящего изобретения субъект-человек нуждается в лечении,осуществляемом способами согласно настоящему изобретению, и на основании этой необходимости он выбран для проведения лечения. Субъекты, нуждающиеся в лечении, известны в данной области техники и включают субъектов, у которых было обнаружено заболевание или нарушение, связанное с образованием -амилоидных бляшек, обнаружен симптом такого заболевания или нарушения, или обнаружен риск развития такого заболевания или нарушения, и на основании диагноза, например медицинского диагноза, следует ожидать, что состояние указанного субъекта улучшится в результате лечения (например,произойдет излечение, лечение, предотвращение, снижение выраженности, облегчение, изменение, ослабление, улучшение или изменение в течении заболевания или нарушения, симптома заболевания или нарушения или риска развития заболевания или нарушения). Например, субъект-человек может быть человеком в возрасте старше 30 лет, человеком в возрасте старше 40 лет, человеком в возрасте старше 50 лет, человеком в возрасте старше 60 лет, человеком в возрасте старше 70 лет, человеком в возрасте старше 80 лет, человеком в возрасте старше 85 лет, человеком в возрасте старше 90 лет или человеком в возрасте старше 95 лет. Субъект может быть женщиной, включая женщин в постклимактерическом возрасте, которые могут получать гормонозаместительную терапию (эстроген). Субъект также может быть мужчиной. В другом варианте реализации возраст субъекта составляет менее 40 лет. В предпочтительных примерах реализации субъект представляет собой субъекта-человека, страдающего нейропатологией типа болезни Альцгеймера. Индивидуумы, в настоящее время страдающие- 20016568 болезнью Альцгеймера, могут быть выявлены по наличию характерного слабоумия, а также наличия факторов риска, описанных ниже. Кроме того, для идентификации индивидуумов, страдающих БА, разработан ряд тестов, основанных на когнитивных и неврологических испытаниях. Например, диагноз индивидуумам, страдающим болезнью Альцгеймера, может быть поставлен в соответствии со Шкалой Клинического Слабоумия (Clinical Dementia Rating, CDR), Краткой шкалой оценки психического статуса(MMSE), Когнитивной субшкалой шкалы оценки болезни Альцгеймера (ADAS-Cog) или в соответствии с другими тестами, известными в данной области, рассматриваемыми в настоящем описании. Для выявления популяции с риском развития сказанных заболеваний могут быть использованы подходящие базовые оценки, включая MMSE и ADAS, совместно с другими оценками, разработанными для исследования более нормальной популяции. Другой способ идентификации группы риска включает исследования нейронного ниточного белка, найденного в моче; см., например, Munzar et al., Neurology and Clinical Neurophysiology, Vol. 2002, No. 1. Пациенты с высоким риском развития болезни Альцгеймера могут быть выявлены среди населения путем исследования наличия ранних симптомов потери памяти или других проблем, связанных с симптоматикой периода, предшествующего развитию болезни Альцгеймера, исследования семейной истории, включающей болезнь Альцгеймера, пациентов с умеренными когнитивными нарушениями (УГН), генетическими факторами риска, определенного возраста, пола и других особенностей, которые используют для предсказания высокого риска развития болезни Альцгеймера. Термины "предотвращать" или "предотвращение" также означают введение соединения или композиции, предлагаемой согласно настоящему изобретению, субъекту с риском развития (или подверженного) таким заболеваниям или состояниям. Пациенты, поддающиеся лечению, нацеленному на предотвращение заболевания или состояния, включают индивидуумов с риском развития заболевания или состояния, но не проявляющих симптомов, а также пациентов, уже проявляющих симптомы. В случае болезни Альцгеймера, буквально каждый может заболеть болезнью Альцгеймера, если она или он проживут достаточно долго. Таким образом, предлагаемые способы могут быть введены профилактически основному населению без оценки риска пациента, подвергаемого лечению. Однако предлагаемые способы особенно полезны для индивидуумов, у которых выявлен известный риск развития болезни Альцгеймера. Такие индивидуумы включают индивидуумов, родственники которых страдают указанным заболеванием, и индивидуумов, у которых выявлен риск развития заболевания путем анализа генетических или биохимических маркеров, включающих бляшки в мозге, обнаруженные томографическими способами, например ЯМР-томографией, позитронно-эмиссионной томографией, однофотонной эмиссионной компьютерной томографией и т.д. Примеры таких томографических способов описаны в публикациях Burggren et al.,Current Topics in Medicinal Chemistry, vol. 2002, no. 2, pp. 385-393, и Sair et al., Neuroradiology, vol. 46, pp. 93-104 (2002). Факторы предрасположенности к болезни Альцгеймера, указанные или предложенные в научной литературе, включают, например, генотипическую предрасположенность субъекта к развитию болезни Альцгеймера; факторы предрасположенности субъекта к развитию болезни Альцгеймера, зависящие от окружающей среды; перенесенные вирусные и бактериальные заболевания, усиливающие предрасположенность субъекта к развитию болезни Альцгеймера; и сосудистые факторы, усиливающие предрасположенность субъекта к развитию болезни Альцгеймера. Генетические маркеры риска развития болезни Альцгеймера включают мутации в гене АРР (Amyloid Precursor Protein = белок-предшественник амилоида), в частности мутации в положении 717 и положениях 670 и 671, называемые соответственно мутациями Hardy и Swedish (см. Hardy et al., TINS 20, 154-158 (1997. Другие маркеры риска представляют собой мутации в генах пресенилинов, PS1 и PS2, и АроЕ 4, семейную историю заболеваний БА, гиперхолестеринемию или атеросклероз. Риск развития заболевания у субъекта может быть обнаружен при диагностике мозга томографическими способами, например, измеряющими активность мозга, образование бляшек или атрофию мозга. Риск развития заболевания у субъекта-человека также может быть обнаружен при помощи когнитивных тестов, например, в соответствии со Шкалой Клинического Слабоумия("CDR"), Когнитивной субшкалой оценочной шкалы болезни Альцгеймера ("ADAS-Cog"), Оценки непригодности в результате наступления слабоумия (Disability Assessment for Dementia, "DAD") или Краткой шкалой оценки психического статуса ("MMSE") и/или в соответствии с другими тестами, известными в данной области техники. В другом варианте реализации субъект-человек не проявляет симптомов болезни Альцгеймера. В другом варианте реализации возраст субъекта составляет по меньшей мере 40 лет и субъект-человек не проявляет симптомов болезни Альцгеймера. В другом варианте реализации возраст субъекта составляет по меньшей мере 40 лет и он проявляет один или несколько симптомов болезни Альцгеймера. При помощи способов и соединений согласно настоящему изобретению уровни амилоидныхпептидов в плазме крови или цереброспинальной жидкости субъекта (ЦСЖ) могут быть в значительной степени снижены по сравнению с уровнями, имевшимися перед лечением, приблизительно на 10-100% или даже приблизительно на 50-100 процентов, например, на 15, 25, 40, 60, 70, 75, 80, 90, 95 или 99%. Соответственно, в некоторых примерах реализации, перед проведением лечения в соответствии с предлагаемыми способами у субъекта-человека может наблюдаться повышенный уровень амилоидных пептидов А 40 и А 42 в крови и/или ЦСЖ, например уровни А 40, превышающие приблизительно 10 пг/мл, или- 21016568 превышающие приблизительно 20 пг/мл, или превышающие приблизительно 35 пг/мл, или даже превышающие приблизительно 40 пг/мл; и уровни А 42 от 30 пг/мл приблизительно до 200 пг/мл, или даже до приблизительно 500 пг/мл. Аналогично, в соответствии с некоторыми примерами реализации способы и соединения согласно настоящему изобретению позволяют снизить размер и/или количество бляшек А или А в мозге приблизительно на 10-100 процентов, или даже приблизительно на 50-100 процентов,например на 15, 25, 40, 60, 70, 75, 80, 90, 95 или 99% по сравнению уровнями перед лечением.VI. Фармацевтические композиции. Предпочтительно соединения согласно настоящему изобретению перед введением в фармацевтические композиции получают при помощи способов и методик, хорошо известных в данной области техники. Соответственно, другой пример реализации настоящего изобретения относится к фармацевтическим композициям (например растворам, суспензиям или эмульсиям), включающим эффективные количества одного или нескольких соединений, соответствующих любой из формул, рассматриваемых в настоящем описании, и фармацевтически приемлемый носитель, а также к способам применения и изготовления указанных фармацевтических композиций. Фармацевтические композиции готовят для подходящего пути введения (перорального, парентерального, (внутривенного (ВВ), внутримышечного (ВМ), депо-ВМ, ПК и депо-ПК), подъязычного, интраназального (ингаляция), внутриоболочечного, топического (местного) или ректального). Неограничивающие примеры подходящих фармацевтически приемлемых носителей включают любые неиммуногенные фармацевтические носители или разбавители, подходящие для перорального, парентерального, назального, мукозального, трансдермального, топического, мукозального (в/через слизистую оболочку),ректального, внутрисосудистого (ВВ), внутриартериального (ВА), внутримышечного (ВМ) и подкожного(ПК) введения, например фосфатно-солевой буферный раствор (ФСБ). Также, настоящее изобретение включает такие соединения, которые были лиофилизованы и могут быть восстановлены с образованием фармацевтически приемлемых композиций, пригодных для введения, например, путем внутривенной,внутримышечной или подкожной инъекции. Введение также может быть осуществлено внутрикожно или трансдермально. Носитель может быть растворителем или дисперсионной средой, содержащей, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и подобные им вещества), подходящие смеси указанных веществ и растительные масла. Подходящая текучесть может быть достигнута, например, путем применения покрытия, например лецитина, поддержанием требуемого размера частиц в случае дисперсии и при помощи применения поверхностно-активных веществ. Предотвращение воздействия микроорганизмов может быть достигнуто добавлением различных антибактериальных и противогрибковых агентов, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты, тимерозаля и подобных веществ. Во многих случаях в композицию включают изотонические добавки, например сахара, хлорид натрия или полиспирты, например маннитол и сорбит. Продолжительная абсорбция инъецируемой композиции может быть достигнута за счет включения в композицию вещества, которое замедляет абсорбцию, например моностеарата алюминия или желатина. Предпочтительно соединение (соединения) согласно настоящему изобретению может быть введено перорально. Композиции согласно настоящему изобретению включают составы, подходящие для перорального введения. Композиции могут быть легко приготовлены в виде стандартных лекарственных форм и могут быть приготовлены любыми способами, хорошо известными в области фармакологии. Способы приготовления указанных композиций или составов включают операцию объединения соединения согласно настоящему изобретению, с фармацевтически приемлемым носителем (например, с инертным разбавителем или усвояемым съедобным носителем) и, возможно, одним или несколькими вспомогательными ингредиентами. В общем случае, композиции готовят путем равномерного и тщательного смешивания соединения согласно настоящему изобретению, с жидкими носителями и/или мелко измельченными твердыми носителями, и затем, при необходимости, придания продукту нужной формы. Количество терапевтического вещества в таких терапевтически пригодных композициях должно быть таким, которое обеспечивает получение подходящей дозировки. Композиции согласно настоящему изобретению, подходящие для перорального введения, могут быть изготовлены в виде капсул (например, капсул с твердой или мягкой желатиновой оболочкой),крахмальных капсул, пилюль, таблеток, пастилок, порошков, гранул, горошин, драже, например, имеющих покрытие (например, покрытых растворяющейся в кишечнике оболочкой) или не имеющих покрытия, или в виде раствора или суспензии в водной или неводной жидкости, или в виде жидкой эмульсии типа масло-в-воде или вода-в-масле, или в виде эликсира или сиропа, или в виде пастилок (с инертной основой, например, в желатине и глицерине или сахарозе и камеди), или в виде полосканий для рта и подобных составов, каждый из которых содержит заранее определенное количество соединения согласно настоящему изобретению, в качестве активного ингредиента. Соединения согласно настоящему изобретению также могут быть введены в виде болюса, электуария (лекарственной кашки) или пасты или непосредственно введены в пищу субъекта. Кроме того, в некоторых примерах реализации указанные гранулы могут быть изготовлены таким образом: (а) чтобы обеспечивать мгновенное или быстрое высвобож- 22016568 дение лекарственного средства (т.е., без покрытия); (b) с покрытием, например, обеспечивающим замедленное высвобождение лекарственного средства в течение некоторого времени; или (с) с оболочкой, растворяющейся в кишечнике, для обеспечения лучшей желудочно-кишечной переносимости. В твердых лекарственных формах согласно настоящему изобретению для перорального введения активный ингредиент смешивают с одним или несколькими фармацевтически приемлемыми носителями,например цитратом натрия или фосфатом дикальция, или любым другим из следующих веществ: наполнителями или сухими разбавителями, например крахмалами, лактозой, сахарозой, глюкозой, маннитом или кремниевой кислотой; связующими веществами, например карбоксиметилцеллюлозой, альгинатами,желатином, поливинилпирролидоном, сахарозой или камедью; увлажняющими веществами, например,глицерином; дезинтегрирующими веществами, например агар-агаром, карбонатом кальция, картофельным или маниоковым крахмалом, альгининовой кислотой, некоторыми силикатами и карбонатом натрия; веществами, замедляющими растворение, например парафином; ускорителями абсорбции, например,четвертичными аммонийными соединениями; смачивающими агентами, например цетиловым спиртом и моностеаратом глицерина; абсорбентами, например каолином и бентонитовой глиной; скользящими веществами, например тальком, стеаратом кальция, стеаратом магния, твердыми полиэтиленгликолями,лаурилсульфатом натрия, и смесями указанных соединений; а также окрашивающими добавками. В случае капсул, таблеток и пилюль фармацевтические композиции также могут включать буферные агенты. Твердые композиции аналогичного типа также могут быть использованы в качестве наполнителей капсул с мягкой и твердой желатиновой оболочкой с добавлением таких вспомогательных наполнителей,как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и подобных им веществ. Композиции для перорального введения обычно включают жидкие растворы, эмульсии, суспензии и подобные им рецептуры. Фармацевтически приемлемые носители, подходящие для приготовления таких композиций, хорошо известны в данной области техники. Типичные компоненты носителей, применяемых для приготовления сиропов, эликсиров, эмульсий и суспензий, включают этанол, глицерин, пропиленгликоль, полиэтиленгликоль, жидкую сахарозу, сорбит и воду. Для приготовления суспензий, типичные суспензирующие агенты включают метилцеллюлозу, натрий-карбоксиметилцеллюлозу, трагакантовую камедь и альгинат натрия; типичные смачивающие вещества включают лецитин и полисорбат 80; и типичные консерванты включают метилпарабен и бензоат натрия. Жидкие композиции для перорального ведения также могут содержать один или несколько компонентов, например подсластителей,вкусовых добавок и окрашивающих веществ, описанных выше. Фармацевтические композиции, подходящие для введения в виде инъекций, включают стерильные водные растворы (если вещества водорастворимы) или дисперсии и стерильные порошки, препараты для немедленного приготовления стерильных инъецируемых растворов или дисперсий. Во всех случаях,композиция должна быть стерильной и должна быть жидкой до такой степени, чтобы ее было легко вводить при помощи шприца. Композиция должна быть стабильной в условиях изготовления и хранения и должна быть защищена от загрязняющего воздействия микроорганизмов, например бактерий и грибков. Стерильные инъецируемые растворы могут быть приготовлены путем введения требуемого количества терапевтического агента в подходящий растворитель и, при необходимости, добавления одного из сочетаний ингредиентов, описанных выше, с последующим проведением стерилизационного фильтрования. В общем случае, дисперсии готовят путем введения терапевтического агента в стерильный носитель,который содержит основную дисперсионную среду и другие необходимые ингредиенты из перечисленных выше. В случае приготовления стерильных порошков для получения стерильных инъецируемых растворов способы приготовления включают вакуумную сушку и сушку замораживанием, которые обеспечивают получение порошка активного ингредиента (т.е., терапевтического агента) плюс любой другой необходимый ингредиент, полученный из приготовленного ранее раствора компонентов, стерилизованного фильтрованием. Изобретение также включает фармацевтические композиции, пригодные для введения в виде аэрозоля посредством ингаляции. Такие композиции включают раствор или суспензию нужного соединения,отвечающего любой Формуле, рассматриваемой в настоящем описании, или множество частиц такого соединения (соединений). Целевая композиция может быть помещена в небольшой объем и распылена. Распыление может осуществляться при помощи сжатого воздуха или ультразвука, приводящего к образованию множества капель жидкости или твердых частиц, включающих агенты или их соли. Размеры капель жидкости или твердых частиц должны находиться в диапазоне приблизительно от 0,5 до 5 мкн. Твердые частицы могут быть получены путем обработки твердого соединения, отвечающего любой из Формул, рассматриваемых в настоящем описании, или его соли, любым подходящим способом, известным в данной области техники, например измельчением. Размеры капель или твердых частиц могут составлять, например, приблизительно от1 до 2 мкн. Для получения указанных частиц могут быть использованы коммерчески доступные распылители. Фармацевтическая композиция, подходящая для введения в виде аэрозоля, может быть в форме жидкости, и такая композиция включает водорастворимое вещество, отвечающее любой формуле, рассматриваемой в настоящем описании, или его соль в носителе, который включает воду. Композиция мо- 23016568 жет включать поверхностно-активное вещество, которое понижает поверхностное натяжение композиции до такой степени, что при распылении композиция может образовывать капли желаемых размеров. Композиции согласно настоящему изобретению также могут быть введены субъекту топически, например, непосредственным наложением или распределением композиции по эпидермальной или эпителиальной ткани субъекта, или трансдермальным способом при помощи "пластыря". Такие композиции включают, например, лосьоны, кремы, растворы, гели и твердые вещества. Указанные топические композиции могут включать эффективное количество, обычно по меньшей мере приблизительно 0,1%, или даже приблизительно от 1 до 5%, вещества согласно настоящему изобретению. Носители, подходящие для топического введения, обычно фиксируют на участке кожи в виде непрерывной пленки; такие носители должны быть устойчивы к отклеиванию под действием потоотделения или при погружении в воду. В общем случае, носитель имеет органическую природу и в нем возможно диспергировать или растворять рассматриваемые в настоящем описании терапевтические вещества. Носитель может включать фармацевтически приемлемые смягчающие вещества, эмульгаторы, загустители, растворители и подобные добавки. Другие композиции, пригодные для системной доставки рассматриваемых веществ, включают подъязычные, буккальные и назальные лекарственные формы. Такие композиции обычно включают один или несколько растворимых наполнителей, например сахарозу, сорбит и маннитот; и связующих веществ, например камедь, микрокристаллическую целлюлозу, карбоксиметилцеллюлозу и гидроксипропилметилцеллюлозу. Композиции также могут включать вещества, обеспечивающие скольжение,смазывающие вещества, подсластители, окрашивающие вещества, антиоксиданты и вкусовые добавки,рассмотренные в настоящем описании. Соединение (соединения) согласно настоящему изобретению также может быть введено парентеральным, внутрибрюшинным, интраспинальным или интрацеребральным путем. Для приготовления таких композиций соединение (соединения) согласно настоящему изобретению может быть приготовлено в глицерине, жидких полиэтиленгликолях и смесях указанных веществ, а также в маслах. При обычных условиях хранения и применения эти препараты могут содержать консервант, предотвращающий рост микроорганизмов. Для способа введения соединения (соединений) согласно настоящему изобретению, отличного от парентерального введения, на соединение (соединения) может быть нанесено покрытие, или соединение(соединения) могут быть введены совместно с материалом, предотвращающим его дезактивацию. Например, соединение (соединения), предлагаемое согласно настоящему изобретению, может быть введено субъекту в подходящем носителе, например липосомах, или разбавителе. Фармацевтически приемлемые разбавители включают солевые и водные буферные растворы. Липосомы включают CGF эмульсии типа вода-в-масле-в-воде, а также традиционные липосомы. На фармацевтические композиции, предлагаемые согласно настоящему изобретению, может быть традиционными способами нанесено покрытие, обычно покрытие, регулирующее рН, или растворяющееся с течением времени таким образом, что соединение (соединения), предлагаемое согласно настоящему изобретению, высвобождается вблизи целевого участка или спустя различное время, что позволяет продлить период его действия. Неограничивающие примеры таких лекарственных форм обычно включают один или несколько ацетатфталатов целлюлозы, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы, этилцеллюлозу, воски и шеллак. Соединение (соединения) согласно настоящему изобретению может быть упаковано в набор, возможно включающий контейнер (например, упаковку, коробку, флакон и т.д.). Набор может быть использован коммерчески в соответствии со способами, рассматриваемыми в настоящем описании, и может включать инструкции по применению в соответствии со способом согласно настоящему изобретению. Дополнительные компоненты набора могут включать кислоты, основания, буферные агенты, неорганические соли, растворители, антиоксиданты, консерванты или агенты, хелатирующие металлы. Дополнительные компоненты набора могут представлять собой чистые композиции или водные или органические растворы, которые включают один или несколько дополнительных компонентов набора. Любой или все компоненты набора могут также включать буферные вещества.VII. Дозировка. При высвобождении соединения согласно настоящему изобретению лекарственные формы могут обеспечивать образование in vivo соответствующих форм 3-АПС при введении субъекту-человеку. Очевидно, что подходящие дозировки зависят от ряда факторов, которые известны врачу, ветеринару или исследователю обычной квалификации (см., например, Wells et al. eds., Pharmacotherapy Handbook, 2ndEdition, Appleton and Lange, Stamford, Conn. (2000); PDR Pharmacopoeia, Tarascon Pocket Pharmacopoeia 2000, Deluxe Edition, Tarascon Publishing, Loma Linda, Calif. (2000. Доза (дозы) соединения (соединений) согласно настоящему изобретению могут быть разными, например, в зависимости от ряда факторов,включающих действие конкретного применяемого вещества, возраст, массу тела, общее состояние здоровья, пол и диету субъекта, время введения, способ введения, скорость выведения и, если возможно,любое сочетание лекарственных средств, ожидаемое специалистом действие на субъекта после введения соединения, и свойства соединений (например, биодоступность, стабильность, эффективность, токсичность и т.д.). Указанные подходящие дозировки могут быть определены при помощи исследований, рас- 24016568 сматриваемых в настоящем описании. Если человеку вводят одно или несколько соединений согласно настоящему изобретению, то врач может, например, сначала выписать относительно низкую дозировку и затем постепенно повышать дозировку до получения подходящей ответной реакции. Примеры дозировок включают миллиграммовые или микрограммовые количества соединения на килограмм массы субъекта или образца (например, от приблизительно 50 мкг/кг до приблизительно 500 мг/кг, от приблизительно 1 мг/кг до приблизительно 100 мг/кг, от приблизительно 1 мг/кг до приблизительно 50 мг/кг, от приблизительно 1 мг/кг до приблизительно 10 мг/кг или от приблизительно 3 мг/кг до приблизительно 5 мг/кг). Другие примеры дозировок включают дозы, составляющие от приблизительно 5 до приблизительно 500 мг, или от приблизительно 25 до приблизительно 300 мг, или от приблизительно 25 до приблизительно 200 мг, предпочтительно от приблизительно 50 до приблизительно 150 мг, более предпочтительно приблизительно 50, приблизительно 100, приблизительно 150 мг, приблизительно 200 мг или приблизительно 250 мг и предпочтительно ежесуточно или дважды в сутки, или меньшие или большие количества. Для сравнения, примеры дозировок 3-АПС как таковой включают приблизительно 2-3 миллиграмм 3-АПС на килограмм массы субъекта (дважды в сутки). См. также заявку US 11/103656 от 12 апреля 2005 г., полностью включенную в настоящее описание по ссылке. В общем случае композиции для парентерального введения удобно приготавливать в виде стандартных лекарственных форм, что облегчает введение и способствует равномерному распределению дозировки. Термин "стандартная лекарственная форма" означает физически раздельные единицы, подходящие в качестве единичных дозировок для введения субъекту-человеку и другим млекопитающим; при этом каждая стандартная форма содержит определенное количество активного материала, рассчитанное таким образом, чтобы обеспечить достижение желаемого терапевтического эффекта, совместно с подходящим фармацевтическим носителем. В одном из примеров реализации композиции, предлагаемые согласно настоящему изобретению, готовят в виде стандартной лекарственной формы, и при этом каждая единица содержит приблизительно от 50 мг до 500 мг, более предпочтительно приблизительно от 100 мг до 300 мг соединения согласно настоящему изобретению. См. также заявку US 11/103656 от 12 апреля 2005 г., которая полностью включена в настоящее описание по ссылке. Конкретные характеристики стандартных лекарственных форм согласно настоящему изобретению могут быть различными и непосредственно зависят от (а) уникальных характеристик терапевтического агента и конкретного терапевтического эффекта, который должен быть достигнут, и (b) ограничений, имеющихся в данной области техники для получения композиции, включающей терапевтический агент для лечения амилоидных отложений у субъектов. Доставку соединений и композиций согласно настоящему изобретению субъекту, подвергаемому лечению, проводят с использованием известных процедур, применяя дозировки и в течение периода времени, достаточного для достижения желаемой цели (например, предотвращения или лечения БА, получения конкретных уровней 3-АПС и т.д.). Режимы дозирования могут быть выбраны таким образом, чтобы обеспечивать оптимальную терапевтическую ответную реакцию. Например, ежесуточно могут быть введены несколько разделенных дозировок, или доза может быть пропорционально снижена в соответствии с требованиями терапевтической ситуации. В одном из примеров реализации соединение (соединения) согласно настоящему изобретению, вводят в терапевтически эффективной дозировке, достаточной для ингибирования амилоидных отложений у субъекта, предпочтительно субъекта-человека. Применительно к амилоидным отложениям "терапевтически эффективная" дозировкаингибирует амилоидные отложения, например, по меньшей мере приблизительно на 20% или по меньшей мере приблизительно на 40%, или даже по меньшей мере приблизительно на 60%, или по меньшей мере приблизительно на 80% по сравнению с показателями у субъектов, не подвергаемых лечению. В одном из примеров реализации соединение (соединения) согласно настоящему изобретению, вводят в терапевтически эффективной дозировке с целью предотвращения или лечения болезни Альцгеймера. Применительно к болезни Альцгеймера, "терапевтически эффективная" дозировка стабилизирует когнитивные функции или предотвращает дальнейшее снижение когнитивных функций (т.е., предотвращение, замедление или остановку развития заболевания).VII. Применение соединений, композиций и лекарственных форм. Другой аспект настоящего изобретения относится к способу ингибирования гибели нейронных клеток посредством введения эффективного количества соединения согласно настоящему изобретению. Другой аспект изобретения относится к способу обеспечения нейрозащиты субъекту, имеющему заболевание, связанное с А-амилоидом, например болезнь Альцгеймера, который включает введение субъекту эффективного количества соединения согласно настоящему изобретению, которое обеспечивает нейрозащиту. В соответствии с настоящим описанием термин "нейрозащита" включает защиту нейронных клеток субъекта от клеточной гибели, которая может быть вызвана началом процессов, неограничивающие примеры которых включают: дестабилизацию цитоскелета; фрагментацию ДНК; активацию гидролитических ферментов, например, фосфолипазы А 2; активацию каспаз, активируемых кальцием протеаз и/или активируемых кальцием эндонуклеаз; воспаление, медиатором которого являются макрофаги; инфлюкс кальция в клетки; потенциальные изменения мембран клеток; разрыв соединения клеток, ведущий- 25016568 к пониженной или отсутствующей коммуникации типа "клетка-клетка"; и активацию экспрессии генов,участвующих в гибели клеток. В соответствии с предпочтительным примером реализации соединения и композиции согласно настоящему изобретению используют для получения одного или нескольких из следующих эффектов: предотвращения болезни Альцгеймера, лечения болезни Альцгеймера или снижения выраженности симптомов болезни Альцгеймера, для регулирования выработки уровней пептидов амилоида(А), предотвращения, уменьшения или подавления отложения амилоида у субъекта и для лечения или предотвращения заболеваний, связанных с амилоидом. Действие соединений и фармацевтических композиций согласно настоящему изобретению может облегчать течение заболевания, связанного с -амилоидом, в соответствии с любым из следующих механизмов (следующий список приведен для иллюстрации, а не в целях ограничения изобретения): замедление скорости образования или отложения -амилоидных фибрилл (волокон); уменьшение степени накопления -амилоида, подавление, уменьшение или предотвращение образования амилоидных фибрилл; подавления нейродегенераци или клеточной токсичности, вызываемой -амилоидом; подавление воспаления вызываемого амилоидом; усиление клиренса -амилоида из мозга; усиление разрушения А в мозге; или усиление клиренса амилоидного белка перед его сборкой в фибриллы, и снижение отношения А 42:А 40 в ЦСЖ или плазме крови. В другом варианте реализации изобретение относится к способу улучшения когнитивной способности у субъекта, страдающего БА. Способ включает введение эффективного количества терапевтического соединения согласно настоящему изобретению, в результате которого улучшаются когнитивные способности субъекта. Когнитивные способности субъекта могут быть протестированы в соответствии со способами, известными в данной области техники, например в соответствии со Шкалой Клинического Слабоумия ("CDR"), Краткой шкалой оценки психического статуса("MMSE"), Оценки инвалидности в результате слабоумия ("DAD") и Когнитивной субшкалой оценочной шкалы болезни Альцгеймера ("ADAS-Cog"). В соответствии с настоящим изобретением улучшение когнитивных способностей наблюдается, если имеется измеримое различие между результатами тестов, которые выполнил субъект, подвергаемый лечению способами согласно настоящему изобретению, по сравнению с членами группы, получающей плацебо, группой исторического контроля или между последовательно проведенными тестами одного и того же субъекта. Изобретение также относится к способу лечения, замедления или купирования заболевания, связанного с -амилоидом, вызывающего нарушение когнитивной функции, включающему введение субъекту эффективного количества терапевтического соединения согласно настоящему изобретению, при котором снижается ежегодное ухудшение когнитивных способностей субъекта, измеренное при помощи любого из перечисленных выше тестов. Следует понимать, что объем настоящего изобретения включает любые значения и диапазоны, рассматриваемые в настоящем описании, например возраст популяции больных, дозировки и уровни веществ в крови, все значения и диапазоны, включаемые в указанные значения и диапазоны. Кроме того,все значения, входящие в указанные значения и диапазоны, также могут составлять верхний или нижний пределы диапазонов.VIII. Комбинированная терапия. В некоторых примерах реализации соединения и композиции согласно настоящему изобретению могут быть использованы для лечения в комбинации с по меньшей мере одним другим терапевтическим агентом. Соединения-пролекарства согласно настоящему изобретению и по меньшей мере одно другое терапевтическое вещество (вещества) могут оказывать аддитивное или, в некоторых примерах реализации, синергетическое воздействие. В некоторых примерах реализации соединения согласно настоящему изобретению можно вводить одновременно с введением другого терапевтического вещества. В некоторых примерах реализации соединения согласно настоящему изобретению могут быть введены до или после введения другого терапевтического вещества. Указанное по меньшей мере одно другое терапевтическое вещество может быть эффективно для лечения того же или иного заболевания, нарушения или состояния. Способы согласно настоящему изобретению включают введение одного или нескольких соединений или фармацевтических композиций согласно настоящему изобретению и одного или нескольких других терапевтических веществ при условии, что комбинированное введение не приводит к подавлению терапевтического эффекта одного или более соединений согласно настоящему изобретению и/или не приводит к отрицательному эффекту комбинации. В некоторых примерах реализации композиции, предлагаемые согласно настоящему изобретению,можно вводить одновременно с введением другого терапевтического вещества, которое может составлять часть той же фармацевтической композиции, которая содержит соединения, предлагаемые согласно настоящему изобретению, или находиться в другой композиции. В некоторых примерах реализации соединения, предлагаемые согласно настоящему изобретению, можно вводить до или после введения другого терапевтического вещества. В некоторых примерах реализации комбинированной терапии комбинированная терапия включает попеременное введение композиции, предлагаемой согласно настоящему изобретению, и композиции, включающей другое терапевтическое вещество, например, с целью мини- 26016568 мизации отрицательных побочных эффектов, связанных с действием конкретного лекарственного средства. Если соединение согласно настоящему изобретению вводят одновременно с другим терапевтическим веществом, которое потенциально может вызывать отрицательные побочные эффекты, неограничивающий пример которых представляет токсичность, то такое терапевтическое вещество удобно вводить в дозировке, значение которой ниже порогового значения, вызывающего отрицательные побочные эффекты. В некоторых примерах реализации фармацевтическая композиция также может включать вещества,которые усиливают, модулируют и/или регулируют высвобождение, биодоступность, терапевтическую эффективность, терапевтическое воздействие, стабильность и подобные показатели активного вещества. Например, для усиления терапевтической эффективности соединения согласно настоящему изобретению это соединение может быть введено совместно с одним или несколькими активными веществами, повышающими абсорбцию или диффузию соединения в желудочно-кишечном тракте или замедляющими разрушение лекарственного средства в кровеносной системе. В некоторых примерах реализации по меньшей мере одно соединение согласно настоящему изобретению может быть введено совместно с активными веществами, фармакологическое воздействие которых заключается в усилении терапевтической эффективности 3-АПС. В некоторых примерах реализации соединения или фармацевтические композиции, предлагаемые согласно настоящему изобретению, включают или могут быть введены субъекту вместе с другим терапевтическим лекарственным средством, который может быть доступен как без рецепта, так и по рецепту. Заявка на патент США No. 2005/0031651 (полностью включенной в настоящее описание по ссылке) содержит обширный, но не исчерпывающий перечень "терапевтических лекарственных средств", пригодных для введения в сочетании с веществами, предлагаемыми согласно настоящему изобретению. Предпочтительные терапевтические лекарственные средства можно использовать совместно с соединениями или фармацевтическими композициям, предлагаемыми согласно настоящему изобретению, представляют собой терапевтические медикаменты, пригодные для предотвращения или лечения болезни Альцгеймера или ее симптомов; неограничивающие примеры таких лекарств включают: донепецил (Aricept),мемантин (Namenda), ривастигмин (Exelon), галантамин (Reminyl и R-флурбипрофен (Flurizan. Соединения и композиции, предлагаемые согласно настоящему изобретению, также могут использоваться в сочетании с вакцинами и антителами, пригодными для предотвращения или лечения БА. В другом варианте реализации соединения, предлагаемые согласно настоящему изобретению, можно вводить совместно с 3-АПС.IX. Стандартные способы тестирования соединений согласно настоящему изобретению. Соединения согласно настоящему изобретению можно дополнительно тестировать, исследовать и оценивать при помощи ряда in vitro или in vivo анализов, подтверждающих их безопасность, биодоступнойсть, нейропротекторные свойства, их способность к доставке 3-АПС и т.д далее представлены иллюстративные примеры некоторых биологических тестов, которые применяли для оценки некоторых из предлагаемых соединений.i) Определение ферментного расщепления пролекарств in vitro. Для перорально вводимых пролекарств в общем случае желательно, чтобы пролекарство оставалось неизменным (т.е., нерасщепленным) во время пребывания в желудочно-кишечном тракте и расщеплялось(т.е., высвобождало исходный медикамент) в кровеносной системе. Подходящий уровень стабильности может быть, по меньшей мере, частично определен механизмом и кинетикой абсорбции пролекарства в желудочно-кишечном тракте. Подходящий уровень лабильности может быть, по меньшей мере, частично определен фармакокинетикой пролекарства и исходного лекарственного средства в кровеносной системе. В общем случае, пролекарства, оказывающиеся более стабильными при определении Сасо-2 S9 и/или панкреатина и более лабильными в плазме крови крыс, плазме крови человека, препаратах печени крысS9 и/или печени человека S9, могут быть пригодными в качестве пролекарств для перорального введения. Для выбора пролекарств, пригодных для последующего тестирования in vivo, могут быть использованы результаты тестов по определению ферментного расщепления пролекарств in vitro.ii) Биодоступность пролекарств in vivo. Пролекарства, которые обеспечивают биодоступность соответствующего исходного лекарственного средства, которая превышает биодоступность, обеспечиваемую эквимолярной дозой исходного лекарственного средства, вводимой субъекту тем же путем (например, пероральное введение), можно применять в качестве терапевтических веществ. Биодоступность соединений согласно настоящему изобретению, и высвобожденной 3-АПС можно измерить in vivo (у людей и лабораторных животных) методами, хорошо известными в данной области техники. Пример способа определения биодоступности в организме мышей рассмотрен в настоящем описании в примере 3.iii) Тесты in vivo: Модели на подопытных животных. Для оценки эффективности и/или степени воздействия соединений согласно настоящему изобретению можно применять различные модели с использованием животных. Например, исследования, проведенные на некоторых трансгенных животных, описаны, например, в патентах США No. 5877399;- 27016568 5612486; 5387742; 5720936; 5850003; 5877015 и 5811633 и в публикации Ganes et al., (Nature 1995,373:523). Предпочтительными являются модели на животных, которые демонстрируют характеристики,связанные с патофизиологией БА. Введение ингибиторов согласно настоящему изобретению трансгенным мышам, рассматриваемое в настоящем описании, представляет собой альтернативный способ демонстрации ингибиторной активности соединений. Предпочтительным также является введение соединений в фармацевтически эффективном носителе и таким путем введения, который обеспечивает достижение лекарственным средством целевой ткани в подходящем терапевтическом количестве.iv) Токсичность. Для оценки токсичности может быть использован ряд различных параметров. Неограничивающие примеры таких параметров включают пролиферацию клеток, мониторинг активации клеточных путей токсикологических ответных реакций при проведении генного или белкового экспрессионного анализа,фрагментацию ДНК, изменения в составе клеточных мембран, проницаемость мембран, активацию компонентов рецепторов гибели или сигнальных путей в прямом направлении (в направлении экспрессии)(например, каспаз), ответные реакции на генный стресс, активацию NF-каппаВ и ответные реакции на митогены. Аналогичные способы анализа используют для исследования апоптоза (процесс запрограммированной гибели клеток) и некроза, включая образование цГМФ и образование NO. Токсичность и терапевтическая эффективность соединения (соединений) и композиции (композиций) согласно настоящему изобретению могут быть определены при помощи стандартных фармацевтических анализов с использованием клеточных культур или животных, например, пригодных для определения LD50 (доза, летальная для 50% популяции) и ED50 (доза, терапевтически эффективная для 50% популяции). Отношение доз между токсическим и терапевтическим эффектами представляет собой терапевтический индекс и может быть выражено в виде отношения LD50/ED50, и обычно более высокий терапевтический индекс означает большую эффективность. Несмотря на то что можно использовать вещества, оказывающие токсические побочные эффекты, получение систем для доставки таких веществ к целевому участку поврежденной ткани должно проводиться с осторожностью с целью сведения к минимуму потенциальной опасности воздействия на неповрежденные клетки и, таким образом, снижения побочных эффектов.v) Нейропротекторное действие. Ниже показаны иллюстративные примеры биологических тестов, которые могут быть использованы для оценки существования защитного эффекта, оказываемого ингибирующим веществом по отношению к повреждению нейронов или заболеванию. а. Морфологические изменения. Апоптоз в клетках многих типов коррелирует с измененными морфологическими признаками. Неограничивающие примеры таких изменений включают образование пузырьков плазмы в мембране, изменение формы клеток, потерю адгезионных свойств субстрата. Такие изменения хорошо видны в оптический микроскоп. Клетки, претерпевающие апоптоз, также можно определить по фрагментации и дезинтеграции хромосом. Указанные изменения можно увидеть в оптический микроскоп и/или при окрашивании красителями, специфичными для ДНК или хроматина.b. Изменение проницаемости мембран. Часто мембраны клеток, подвергающихся апоптозу, становятся чрезвычайно проницаемыми. Это изменение в свойствах мембран может быть легко определено при помощи витальных красителей (например, пропидиумйодида и трипанового синего). Красители можно использовать для определения присутствия мертвых клеток. Например, в некоторых способах используют набор зеленых флуоресцентных красителей LIVE/DEAD Cytotoxicity Kit 2, поставляемый Molecular Probes. Краситель специфичным образом реагирует с аминогруппами клетки. В мертвых клетках для реакции с красителем доступны все аминогруппы, что приводит к образованию интенсивной флуоресцентной окраски. Напротив, в живых клетках с красителем могут реагировать только поверхностные аминогруппы. Таким образом, интенсивность флуоресценции живых клеток оказывается ниже, чем у омертвевших (см., например, Haugland,1996 Handbook of Fluorescent Probes and Research Chemicals, 6th ed., Molecular Probes, OR).c. Нарушение потенциала мембран митохондрий. Митохондрии осуществляют непосредственное и опосредованное биохимическое регулирование разнообразных процессов в клетке, являясь важным источником энергии в клетках высших организмов. Такие процессы включают механизмы цепи переноса электронов, которые обусловливают окислительное фосфорилирование, приводящее к выработке метаболической энергии в форме аденозинтрифосфата (т.е.,АТФ). Изменение или нарушение активности митохондрий может привести к митохондриальному коллапсу, называемому "изменением проницаемости" (permeability transition) или изменением проницаемости митохондрий. Правильное функционирование митохондрий требует поддержания мембранного потенциала, т.е. разности потенциалов между разными сторонами мембраны. Потеря мембранного потенциала ухудшает синтез АТФ и, таким образом, приводит к остановке или затруднению образования источника жизненной биохимической энергии. Таким образом, разнообразные тесты, разработанные для оценки токсичности и гибели клеток,включают мониторинг воздействия проявляющего вещества на потенциалы мембран митохондрий или- 28016568 на проницаемость мембран митохондрий. Один из подходов включает использование флуоресцентных индикаторов (см., например, Haugland, 1996 Handbook of Flourescent Probes Probes and Research Chemicals, 6th ed., Molecular Probes, OR, pp. 266-274 and 589-594). Кроме того, используют ряд нефлуоресцентных зондов (см., например, Kamo et al. (1979) J. Membrane Biol. 49:105). Потенциалы митохондриальных мембран также могут быть определены опосредовано по значениям проницаемости мембран митохондрий (см., например, Quinn (1976) The Molecular Biology of Cell Membranes, University Park Press, Baltimore, Md., pp. 200-217). Другие указания по способам проведения таких анализов представлены в заявке РСТ WO 00/19200, заявленной Dykens et al.d. Активация каспазы. Апоптоз представляет собой процесс запрограммированной гибели клеток и включает активацию генетических программ, в случае, когда необходимость в клетках отпадает или они серьезно повреждены. Апоптоз включает каскад биохимических событий, и этот процесс регулирует ряд различных генов. Одна группа генов представляет собой эффекторы апоптоза и называется семейством генов интерлейкин-1-конвертирующего фермента (ICE). Эти гены кодируют семейство цистеиновых протеаз, активность которых при апоптозе увеличивается. Семейство протеаз ICE в общем называют ферментамикаспазами (caspase). Буква "С" в названии означает тот факт, что ферменты представляют собой протеазы цистеина (cysteine), в то время как "каспаза" означает способность этих ферментов осуществлять отщепление после остатков аспарагиновой кислоты. Таким образом, некоторые тест-системы для анализа апоптоза основаны на том наблюдении, что во время апоптоза вырабатываются каспазы. Образование этих ферментов можно определить путем мониторинга расщепления субстратов, специфично распознаваемых указанными ферментами. Известны несколько природных и синтетических белковых субстратов (см., например, Ellerby et al. (1997) J. Neurosci. 17:6165; Kluck, et al. (1997) Science 275:1 132; Nicholson et al. (1995) Nature 376:37; и Rosen and CasciolaRosen (1997) J. Cell Biochem. 64:50). Способы приготовления ряда различных субстратов, которые могут быть использованы в таких тестах, описаны в заявке США No. 5976822. В этом патенте также описаны тесты, которые можно проводить с использованием целых клеток, подходящих для исследований при помощи некоторых описанных микроструйных устройств. Другие способы, включающие использование методик резонансного переноса энергии флуоресценции (fluorescence resonance energy transfer = FRET),описаны в публикации Mahajan, et al. (1999) Chem. Biol. 6:401-9; and Xu, et al. (1998) Nucl. Acids. Res. 26:2034-5.e. Высвобождение цитохрома С. Внутренняя мембрана митохондрий здоровых клеток непроницаема для макромолекул. Таким образом, один из индикаторов апоптоза клеток представляет собой высвобождение или выделение цитохрома С из митохондрий. Определение цитохрома С может осуществлять методами спектроскопии, поскольку этот белок обладает определенными параметрами поглощения. Таким образом, один из доступных способов анализа включает помещение клеток в зону для приемной камеры и детектирование поглощения при характеристической длине волны цитохрома С. В альтернативном случае этот белок может быть определен при помощи стандартных иммунологических способов (например, твердофазный) и с использованием антитела, которое специфично связывает цитохром С (см., например, Liu et al. (1996) Cell 86:147).f. Тесты на лизис клеток. Конечная стадия гибели клеток обычно представляет собой лизис клетки. При гибели клеток они обычно высвобождают в окружение смесь химических веществ, включающую нуклеотиды и ряд других веществ (например, белков и углеводов). Некоторые из высвобождаемых веществ включают АДФ и АТФ, а также фермент аденилатциклазу, который катализирует превращение АДФ в АТФ в присутствии избытка АДФ. Таким образом, некоторые тесты включают создание концентрации АДФ в среде для анализа, достаточной для смещения равновесия в сторону наработки АТФ, которую затем можно детектировать рядом способов. Один из таких подходов включает использование системы люциферин/люцифераза, хорошо известной специалистам в данной области техники, в которых фермент люцифераза действует на АТФ и субстрат люциферин с образованием сигнала, который можно детектировать фотометрическим методом. Более подробно некоторые способы анализа лизиса клеток описаны в патентной публикации РСТ WO 00/70082.g. Системы моделей ишемии. Способы определения того, оказывает ли соединение защитное нейрологическое действие против ишемии и инсульта, описаны в публикации Aarts, et al. (Science 298:846-850, 2002). В общем случае, такие тесты включают создание у крыс окклюзии средней церебральной артерии (ОСЦА) в течение относительно короткого времени (например, приблизительно 90 мин). ОСЦА может быть индуцирована различными методами, включая сшивание просвета артерии (см., например, Longa, E. Z. et al. (1989) Stroke 20:84; and Belayev, L, et al. (1996) Stroke 27:1616). Композицию, содержащую предполагаемый ингибитор, вводят крысе традиционными путями (например, путем внутривенной инъекции). Для оценки профилактического эффекта композиции композицию вводят до выполнения ОСЦА. Если оценивают способность соединения уменьшать последствия уже произошедших ишемических нарушений, то компози- 29
МПК / Метки
МПК: C07D 207/16, C07D 209/20, C07D 333/24, C12P 11/00, A61K 38/08, A61K 38/07, C07C 309/15, C07D 233/64, C07D 291/02, A61P 25/28, C07D 217/24, C07K 5/08, C07K 5/06
Метки: 3-амино-1-пропансульфоновой, доставки, кислоты, соединения, способы, носители, композиции
Код ссылки
<a href="https://eas.patents.su/30-16568-sposoby-soedineniya-kompozicii-i-nositeli-dlya-dostavki-3-amino-1-propansulfonovojj-kisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Способы, соединения, композиции и носители для доставки 3-амино-1-пропансульфоновой кислоты</a>
Предыдущий патент: Ингибиторы матриксных металлопротеиназ
Следующий патент: Способ и установка для термической обработки зернистых твердых частиц
Случайный патент: Фармацевтические композиции лекарственных веществ с быстрым высвобождением












