Способы получения замещенных пиримидинов
Номер патента: 15990
Опубликовано: 30.01.2012
Авторы: Мадзей Франческа, Шаррьер Жан-Дамиен, Кэй Дэвид, Миллер Эндрю
Формула / Реферат
1. Способ получения соединения формулы I
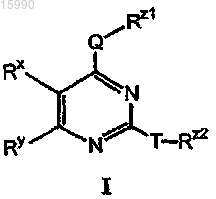
где Q и Т, каждый независимо, выбраны из кислорода, серы или N(R);
каждый R независимо выбран из водорода или C1-6алифатической группы, необязательно замещенной одним или несколькими заместителями, выбранными из галогена, -R°, -OR°, -SR°, 1,2-метилендиокси, 1,2-этилендиокси, фенила (Ph), необязательно замещенного R°, -О(Ph) необязательно замещенного R°,
-CH2(Ph), необязательно замещенного R°, -CH2CH2(Ph), необязательно замещенного R°, -NO2, -CN, -N(R°)2, NR°C(O)R°, -NR°C(O)N(R°)2, -NR°CO2R°, -NR°NR°C(O)R°, -NR°NR°C(O)N(R°)2, -NR°NR°CO2R°,
-C(O)C(O)R°, C(O)CH2C(O)R°, -CO2R°, -C(O)R°, -C(O)N(R°)2, -ОС(O)N(R°)2, -S(O)2R°, -SO2N(R°)2, -S(O)R°,
-NR°SO2N(R°)2, -NR°SO2R°, C(=S)N(R°)2, -C(=NH)-N(R°)2 или -(CH2)yNHC(O)R°, где
каждый R° независимо выбран из водорода, необязательно замещенной C1-6алифатической группы, незамещеннного 5-6-членного гетероарильного или гетероциклического кольца, фенила, -О(Ph) или СН2(Ph),
необязательные заместители алифатической группы R° выбраны из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, CO2H, CO2(C1-4алифатической группы), О(галоген-C1-4алифатической группы) или галоген(C1-4 алифатической группы), =O, =S, =NNHR*, =NN(R*)2, =NNHC(O)R*, =NNHCO2(алкила), =NNHSO2(алкила) или =NR*, где каждый R* независимо выбран из водорода или необязательно замещенной C1-6 алифатической группы; и
необязательные заместители алифатической группы R* выбраны из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, СО2Н, CO2(С1-4алифатической группы), О(галоген-C1-4алифатической группы) или галоген(С1-4 алифатической группы),
где два R, связанные с одним и тем же атомом азота, необязательно взяты вместе с этим атомом азота с образованием необязательно замещенного 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-3 гетероатома, наряду со связанным с ними азотом, независимо выбранных из азота, кислорода или серы;
Rx обозначает U-R5;
R5 выбран из галогена, NO2, CN, R или Ar;
каждый U независимо выбран из валентной связи или С1-4алкилиденовой цепи, где до двух метиленовых звеньев в U необязательно и независимо заменены на -O-, -S-, -SO-, -SO2-, -N(R)SO2-, -SO2N(R)-, -N(R)-,
-C(O)-, -CO2-, -N(R)C(O)-, -N(R)C(O)O-, -N(R)CON(R)-, -N(R)SO2N(R)-, -N(R)N(R)-, -C(O)N(R)-,
-OC(O)N(R)-, C(R)=NN(R)- или -C(R)=N-O-;
каждый Ar независимо выбран из необязательно замещенного кольца, выбранного из 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы;
Ry обозначает -N(R1)2, -OR1 или -SR1;
каждый R1 независимо выбран из R или 3-8-членного моноциклического, 8-10-членного бициклического или 10-12-членного трициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, и где каждый R1 необязательно и независимо содержит до четырех заместителей, независимо выбранных из R2;
каждый R2 независимо выбран из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2, -C(O)R3, -OC(O)R3,
-CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3), -ОС(O)N(R3)2,
-NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2(R3);
каждый R3 выбран независимо из R или Ar;
Rz1 выбран из C1-6алифатической группы или 3-8-членного моноциклического, 8-10-членного бициклического или 10-12-членного трициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, где Rz1 замещен 0-4 независимо выбранными группами R2;
Rz2 обозначает 3-8-членное моноциклическое или 8-10-членное бициклическое насыщенное, частично ненасыщенное или полностью ненасыщенное кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, где Rz2 замещен 0-4 заместителями, независимо выбранными из оксо или U-R5;
где указанный способ включает
первую стадию, на которой связывают соединения формулы IV с соединением формулы Rz2-T-H в первой подходящей среде с получением соединения формулы III,
вторую стадию, на которой связывают соединения формулы III с соединением формулы Rz1-Q-H во второй подходящей среде с получением соединения формулы II, и
третью стадию, на которой связывают соединения формулы II с соединением формулы RY-H в третьей подходящей среде
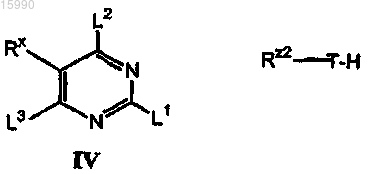

где каждая первая, вторая и третья подходящая среды независимо содержат:
i) подходящий растворитель, выбранный из протонного растворителя, галогенированный углеводород, простой эфир, ароматический углеводород, полярный или неполярный апротонный растворитель или любую их смесь,
ii) необязательно подходящее основание, выбранное из органического амина, карбоната щелочно-земельного металла, гидрида щелочно-земельного металла или гидроксида щелочно-земельного металла; и
L1, L2, L3 независимо выбраны из глогена, алкокси, сульфонилокси, необязательно замещенного алкилсульфонила, необязательно замещенного алкенилсульфонила, необязательно замещенного арилсульфонила, и диазониевый фрагмент.
2. Способ по п.1, где L3 выбран из галогена, необязательно замещенного арилсульфонила или необязательно замещенного алкилсульфонила, предпочтительно L3 обозначает фтор, хлор, бром, йод, паратолуолсульфонил, метансульфонил, паранитрофенилсульфонил, парабромфенилсульфонил или трифторметансульфонат, более предпочтительно L3 обозначает хлор или йод.
3. Способ по п.1, где L2 обозначает галоген, необязательно замещенный арилсульфонил или необязательно замещенный алкилсульфонил, предпочтительно L2 обозначает фтор, хлор, бром, йод, паратолуолсульфонил, метансульфонат, паранитрофенилсульфонил, парабромфенилсульфонил или трифторметансульфонат, более предпочтительно L2 обозначает хлор или йод.
4. Способ по п.1, где L1 обозначает галоген, необязательно замещенный арилсульфонил или необязательно замещенный алкилсульфонил, предпочтительно L1 обозначает необязательно замещенный алкилсульфонил, более предпочтительно L1 обозначает метансульфонил.
5. Способ по п.1, где Q обозначает N(R).
6. Способ по п.1, где Т обозначает кислород или серу, предпочтительно Т обозначает серу.
7. Способ по п.1, где Ry обозначает -OR1 или -N(R1)2.
8. Способ по п.7, где Ry обозначает -N(R1)2 и где R1 выбран из R или 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, или
каждый R1 обозначает R, так что эти два R на одном атоме азота взяты вместе с образованием необязательно замещенного 4-7-членного насыщенного кольца, содержащего до двух дополнительных гетероатомов, независимо выбранных из азота, кислорода или серы, и где
каждый R1 необязательно и независимо замещен до четырех заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2, -C(O)R3, -OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3,
-C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3), -OC(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2(R3),
предпочтительно Ry обозначает -N(R1)2 и каждый R1 независимо выбран из R, где R обозначает водород или C1-4алифатическую группу, необязательно замещенную одним или несколькими заместителями, выбранными из
галогена, -R°, -OR°, -SR°, 1,2-метилендиокси, 1,2-этилендиокси, фенила (Ph), необязательно замещенного R°, -O(Ph), необязательно замещенного R°, -CH2(Ph), необязательно замещенного R°, -CH2CH2(Ph), необязательно замещенного R°, -NO2, -CN, -N(R°)2, -NR°C(O)R°, -NR°C(O)N(R°)2, -NR°CO2R°,
-NR°NR°C(O)R°, -NR°NRoC(O)N(R°)2, -NR°NR°CO2Ro, -C(O)C(O)R°, -C(O)CH2C(O)R°, -CO2R°, -C(O)R°,
-C(O)N(R°)2, -ОС(O)N(R°)2, -S(O)2R°, -SO2N(R°)2, -S(O)R°, -NR°SO2N(R°)2, -NR°SO2R°, -C(=S)N(R°)2,
-C(=NH)-N(R°)2 или -(CH2)yNHC(О)R°, где
R° независимо выбран из водорода, необязательно замещенной C1-6алифатической группы, незамещеннного 5-6-членного гетероарильного или гетероциклического кольца, фенила, -O(Ph) или СН2(Ph),
необязательные заместители алифатической группы R° выбраны из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, CO2H, CO2(C1-4алифатической группы), О(галоген-C1-4алифатической группы) или галоген(C1-4 алифатической группы), =O, =S, =NNHR*, =NN(R*)2, =NNHC(O)R*, =NNHCO2(алкила), =NNHSO2(алкила) или =NR*, где каждый R* независимо выбран из водорода или необязательно замещенной C1-6алифатической группы; и
алифатическая группа R* выбрана из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, СО2Н, CO2(C1-4алифатической группы), O(галоген-C1-4алифатической группы) или галоген(C1-4алифатической группы).
9. Способ по п.8, где Ry обозначает -N(R1)2, где каждый R1 обозначает R, так что эти две R группы взяты вместе с образованием необязательно замещенного 4-7-членного насыщенного кольца, содержащего до двух дополнительных гетроатомов, независимо выбранных из азота, кислорода или серы, предпочтительно Ry выбран из пирролидин-1-ила, пиперидин-1-ила, морфолин-4-ила, тиоморфолин-4-ила, пиперазин-1-ила, диазепанила или тетрагидроизохинолинила, где каждое кольцо необязательно замещено одной или двумя группами, независимо выбранными из метила, этила, метилсульфонила, (СН2)2SO2CH3, циклопропила, СН2циклопропила, (СН2)2ОН, CO2-трет-бутила, СН2фенила, фенила, NH2, NH(CH3), N(CH3)2, (CH2)2NH2, (CH2)2морфолин-4-ила, (CH2)2N(CH3)2, изопропила, пропила, трет-бутила, (CH2)2CN или (СН2)2С(О)морфолин-4-ила.
10. Способ по п.1, где Rz1 обозначает 3-7-членное моноциклическое или 8-10-членное бициклическое насыщенное, частично ненасыщенное или полностью ненасыщенное кольцо, содержащее 0-4 гетероатома, независимо выбранных из кислорода, азота или серы, где указанное кольцо необязательно и независимо замещено тремя заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2, -C(O)R3, -OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3),
-ОС(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2R3,
предпочтительно Rz1 обозначает 5-6-членное полностью ненасыщенное кольцо, содержащее 1-3 гетероатома, независимо выбранных из азота, кислорода или серы, где указанное кольцо необязательно и независимо замещено тремя заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена,
-N(R3)2, -C(O)R3, -OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2,
-OC(O)NR(R3), -OC(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2R3;
более предпочтительно Rz1 обозначает необязательно замещенное кольцо, выбранное из пиразола или любого из следующих 5-6-членных колец:
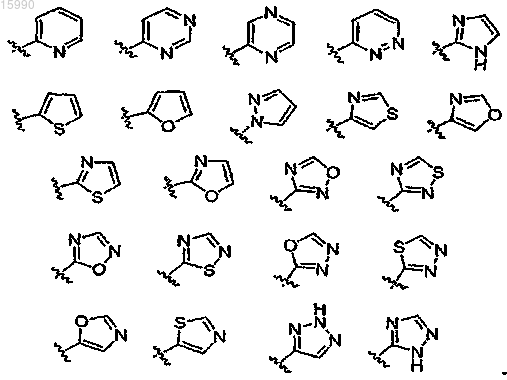
наиболее предпочтительно Rz1 обозначает пиразольное кольцо, содержащее до двух заместителей, независимо выбранных из -N(R3)2, -OR3 или C1-4алифатической группы, например Rz1 обозначает пиразол, необязательно замещенный одним заместителем, выбранным из метила, этила, пропила, изопропила, трет-бутила, циклопропила или фенила.
11. Способ по п.1, где Rz2 обозначает необязательно замещенное кольцо, выбранное из 5-6-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, где указанное кольцо необязательно замещено до трех заместителями, независимо выбранными из галогена, -CN, -NO2, -C(O)R3, -CO2R3, -C(O)NR(R3), -NR3C(O)R3, -N(R3)2, -N(R3)SO2R3,
-NR3C(O)N(R3)2 или -NR3CO2R3;
предпочтительно Rz2 выбран из фенила, имидазолила, пиразолила, пиридила, пиридазинила, пиразинила, нафтила, тетрагидронафтила, бензимидазолила, бензтиазолила, хинолинила, хиназолинила, бензодиоксинила, изобензофурана, инданила, индолила, индолинила, индазолила или изохинолинила, где
Rz2 необязательно замещен до трех заместителями, независимо выбранными из -Cl, -Br, -F, -CN, -CF3,
-COOH, -CONHMe, -CONHEt, -NH2, -NHAc, -NHSO2Me, -NHSO2Et, -NHSO2(н-пропила), -NHSO2 (изопропила), -NHCOEt, -NHCOCH2NHCH3, -NHCOCH2N(CO2t-Bu)CH3, -NHCOCH2N(CH3)2,
-NHCOCH2CH2N(CH3)2, -NHCOCH2CH2CH2N(CH3)2, -NHCO(циклопропила), -NHCO(изопропила), -NHCO (изобутила), -NHCOCH2(морфолин-4-ила), -NHCH2COCH2(морфолин-4-ила), -NHCH2COCH2CH2(морфолин-4-ила), -NHCO2(трет-бутила), -NH(циклогексила), -NHMe, -NMe2, -ОН, -ОМе, метила, этила, циклопропила, изопропила или трет-бутила;
более предпочтительно Rz2 содержит один заместитель, выбранный из -NR3C(O)R3, где
каждый R3 независимо выбран из R или Ar и где
R обозначает водород или C1-4алифатическую группу, необязательно замещенную одним или несколькими заместителями, выбранными из галогена, -R°, -OR°, -SR°, 1,2-метилендиокси, 1,2-этилендиокси, фенила (Ph), необязательно замещенного R°, -O(Ph), необязательно замещенного R°, -CH2(Ph), необязательно замещенного R°, -CH2CH2(Ph), необязательно замещенного R°, -NO2, -CN, -N(R°)2, -NR°C(O)R°,
-NR°C(O)N(R°)2, -NR°CO2R°, -NR°NR°C(O)R°, -NR°NR°C(O)N(R°)2, -NR°NR°CO2R°, -C(O)C(O)R°,
-C(O)CH2C(O)R°, -CO2R°, -C(O)R°, -C(O)N(R°)2, -ОС(О)N(R°)2, -S(O)2R°, -SO2N(R°)2, -S(O)R°,
-NR°SO2N(R°)2, -NR°SO2R°, -C(=S)N(R°)2, -C(=NH)-N(R°)2 или -(CH2)yNHC(O)R°, где
каждый R° независимо выбран из водорода, необязательно замещенной C1-6алифатической группы, незамещеннного 5-6-членного гетероарильного или гетероциклического кольца, фенила, -O(Ph) или CH2(Ph),
алифатическая группа R° выбрана из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, СО2Н, CO2(C1-4алифатической группы), О(галоген-C1-4алифатическойгруппы) или галоген(C1-4алифатической группы), =O, =S, =NNHR*, =NN(R*)2, =NNHC(O)R*, =NNHCO2(алкила), =NNHSO2(алкила) или =NR*,
где каждый R* независимо выбран из водорода или необязательно замещенной C1-6алифатической группы; и
алифатическая группа R* выбрана из NH2, NH(C1-4алифатической группы), N(C1-4алифатической группы)2, галогена, C1-4алифатической группы, ОН, O(C1-4алифатической группы), NO2, CN, СО2Н, СО2(С1-4алифатической группы), О(галоген-C1-4алифатической группы) или галоген(C1-4алифатической группы).
12. Способ по п.1, где указанным подходящим растворителем является C1-5прямой или разветвленный алкиловый спирт, простой эфир или полярный или неполярный растворитель.
13. Способ по п.1, где указанное подходящее основание выбрано из триалкиламина, карбоната натрия, карбоната калия, гидрида натрия, гидрида калия, гидроксида натрия или гидроксида натрия.
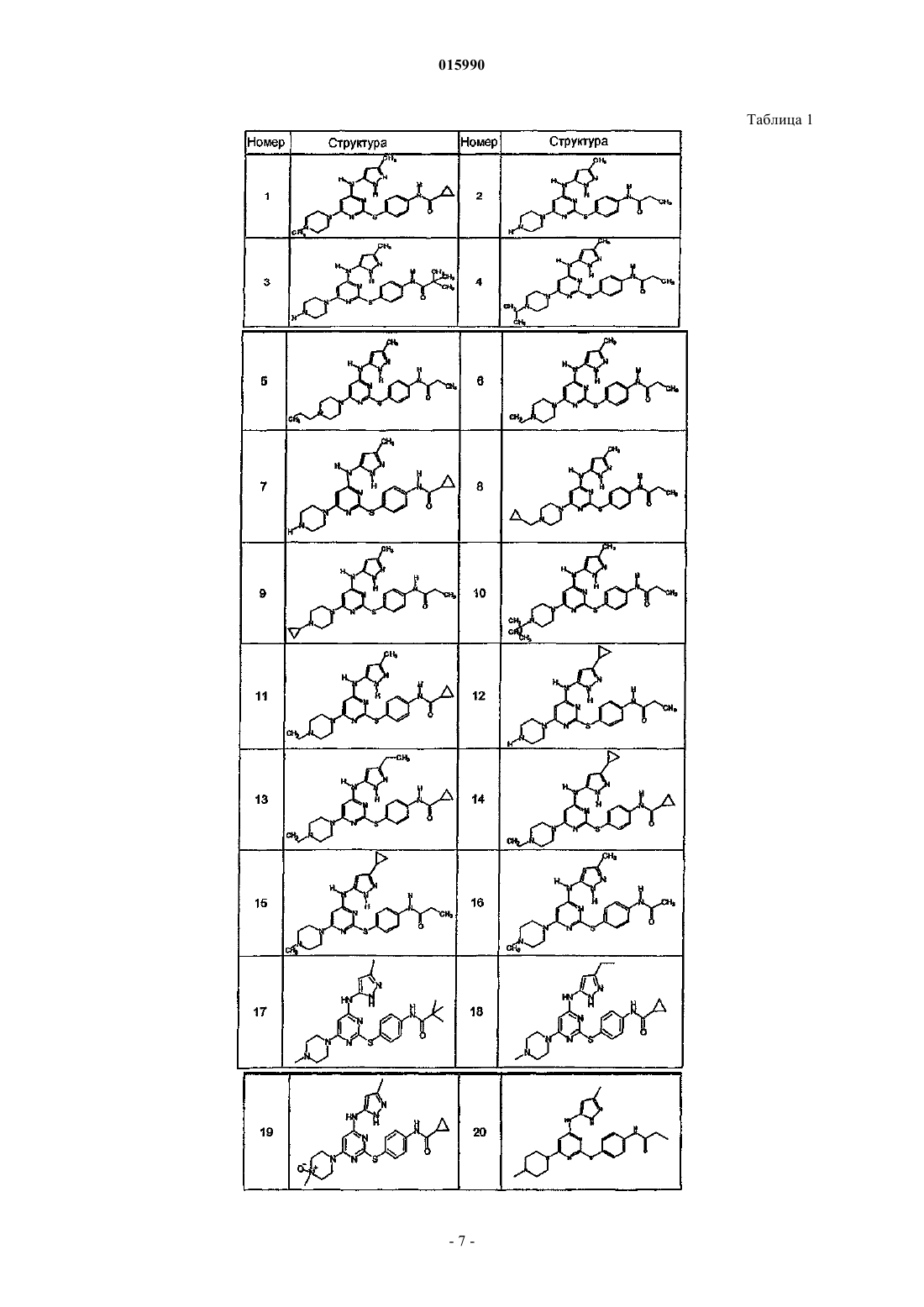
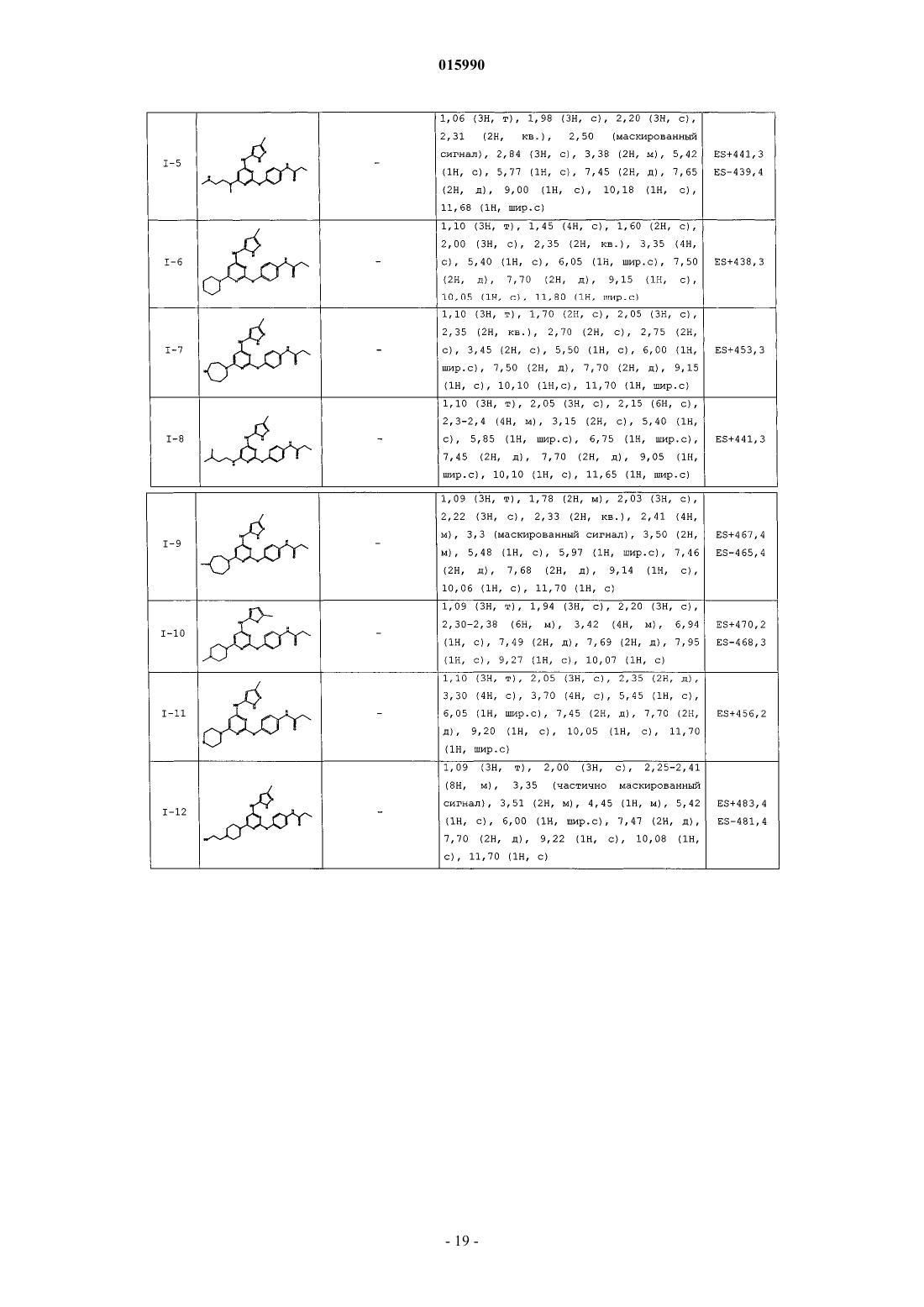
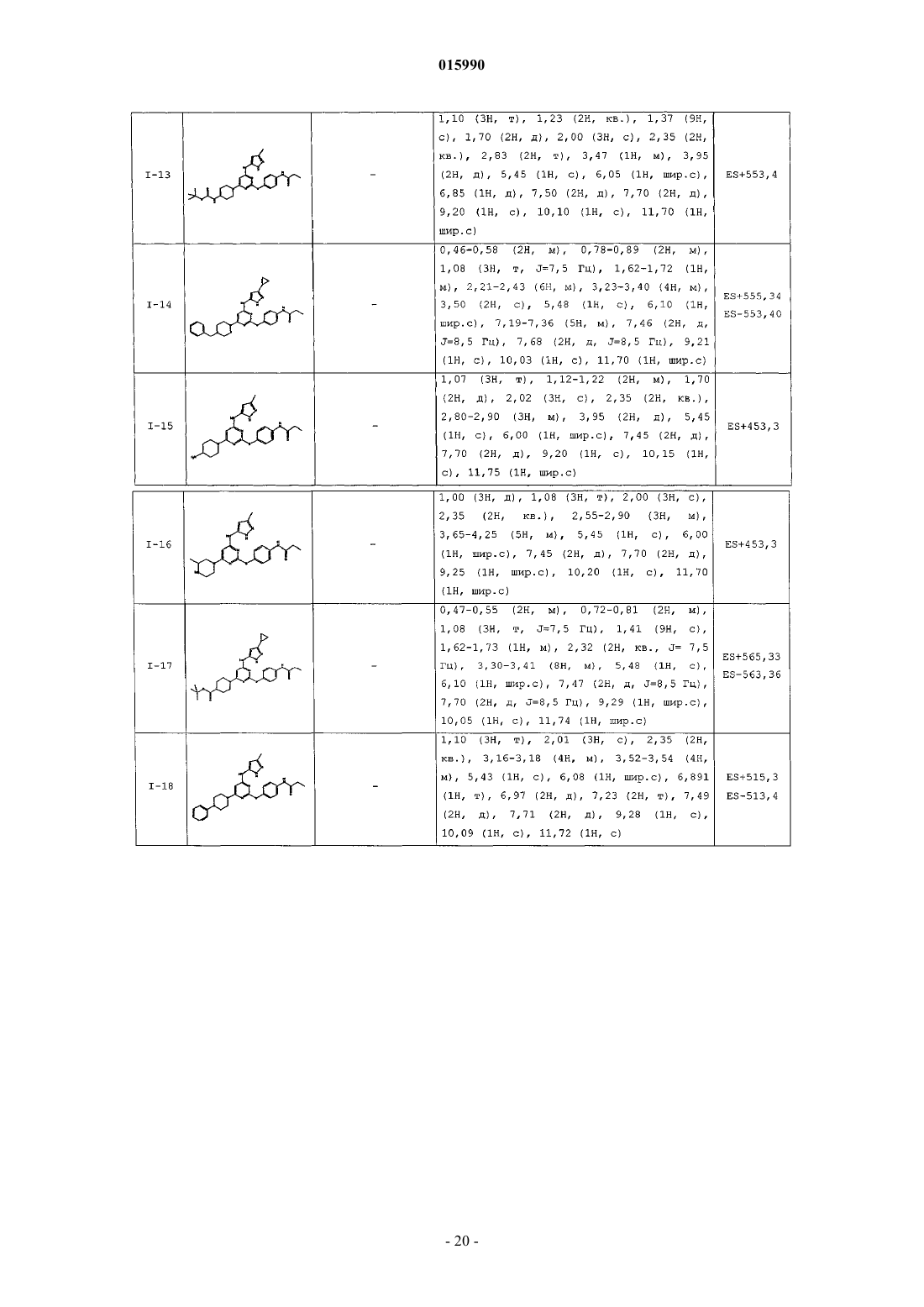
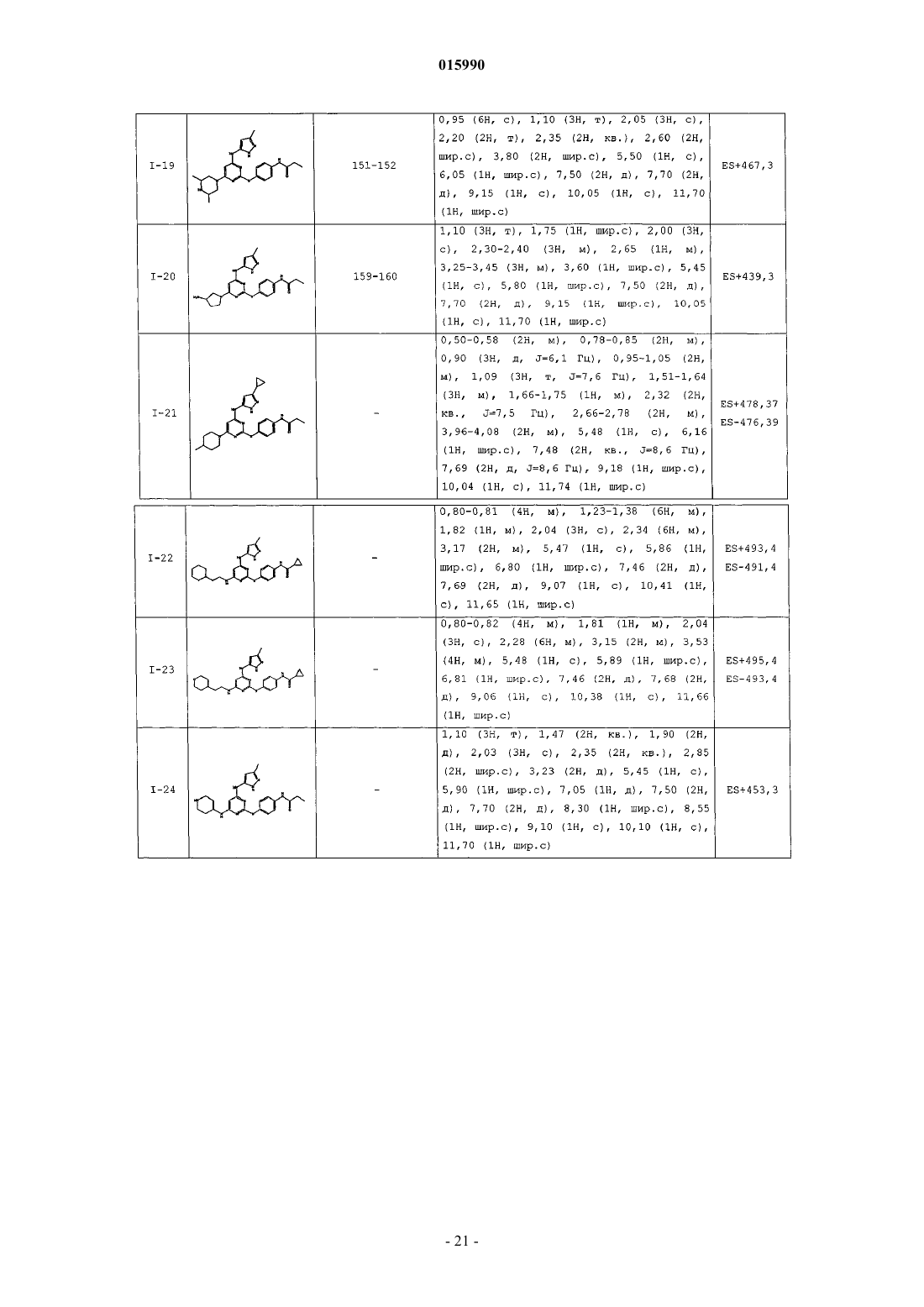
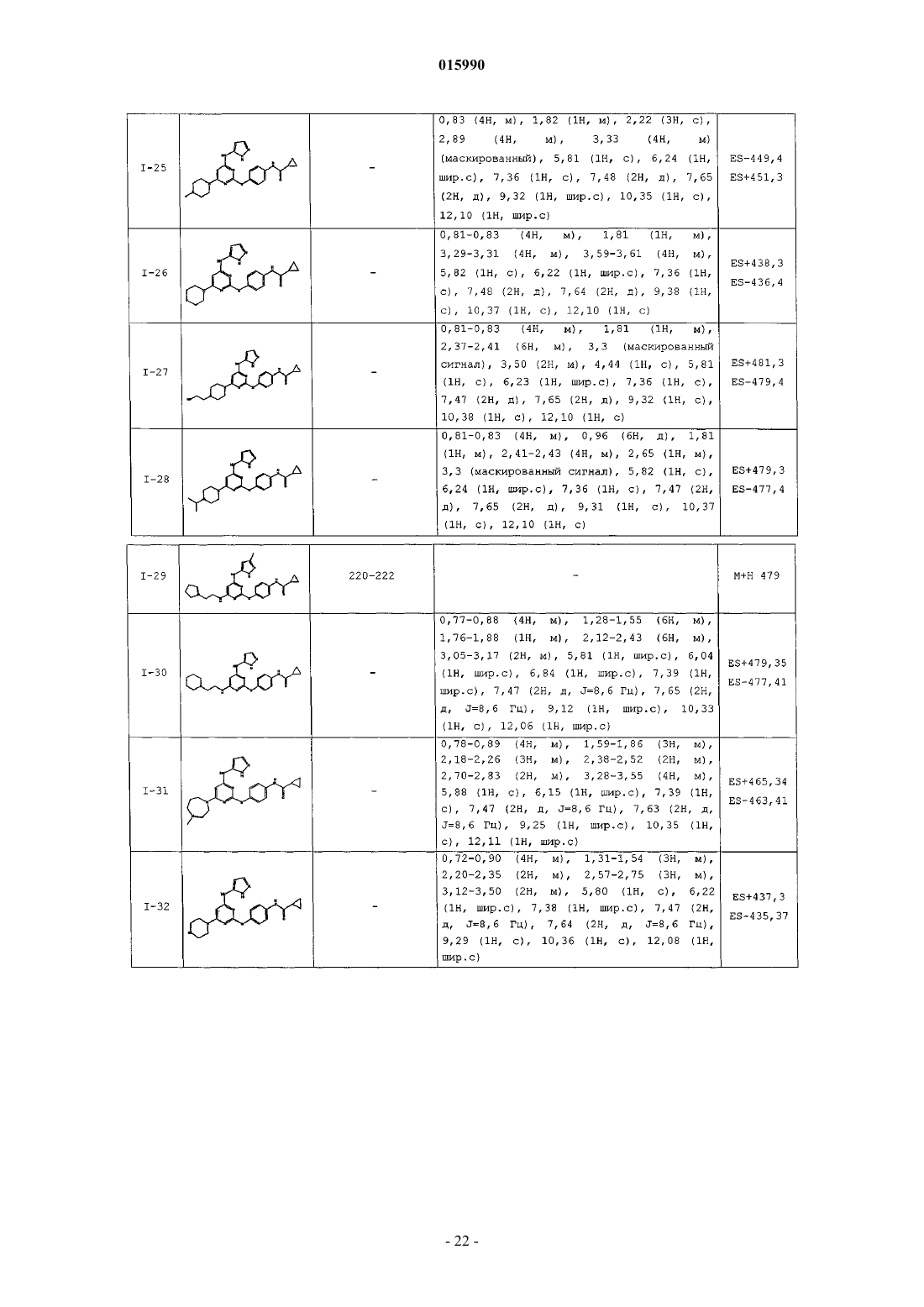
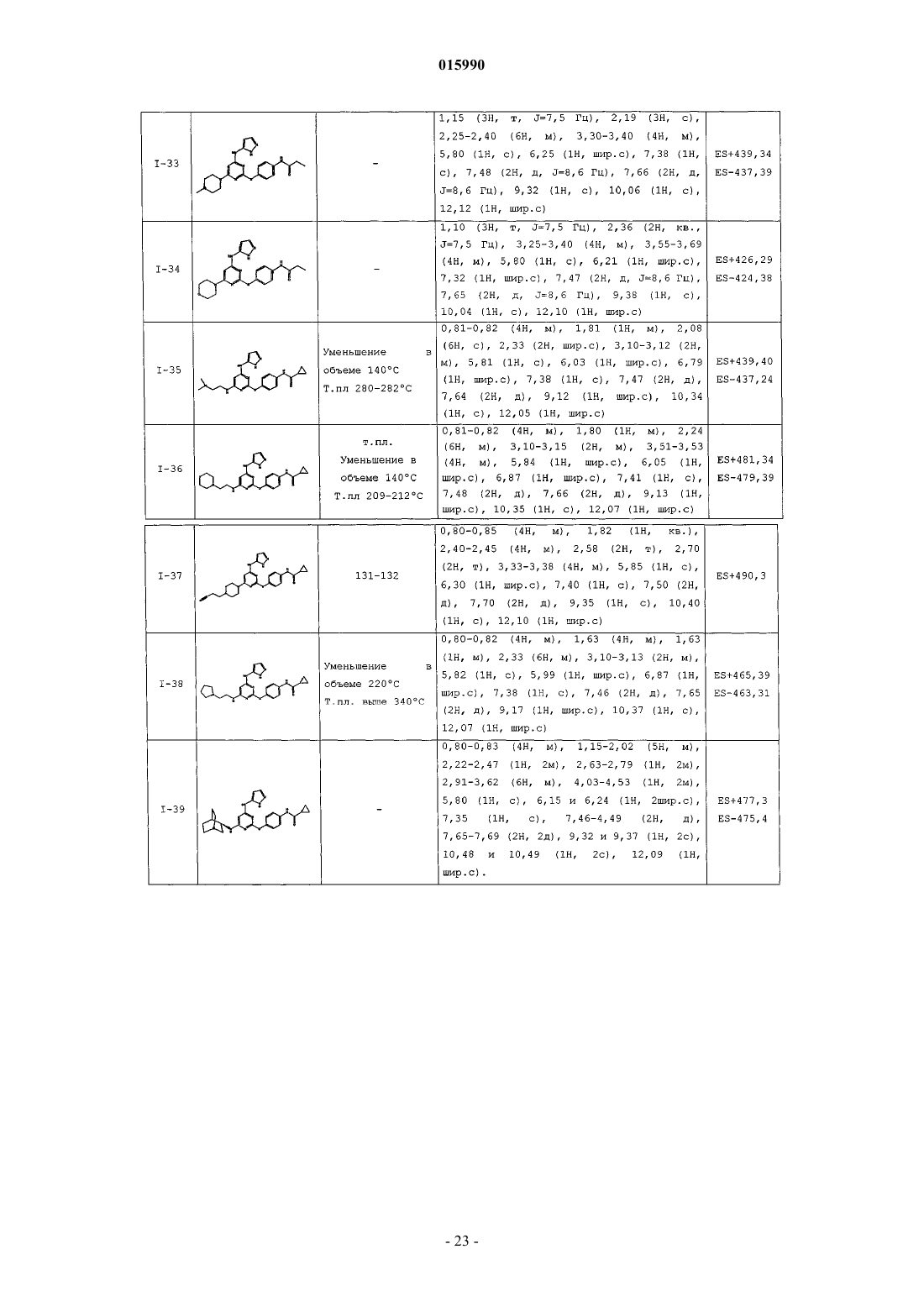
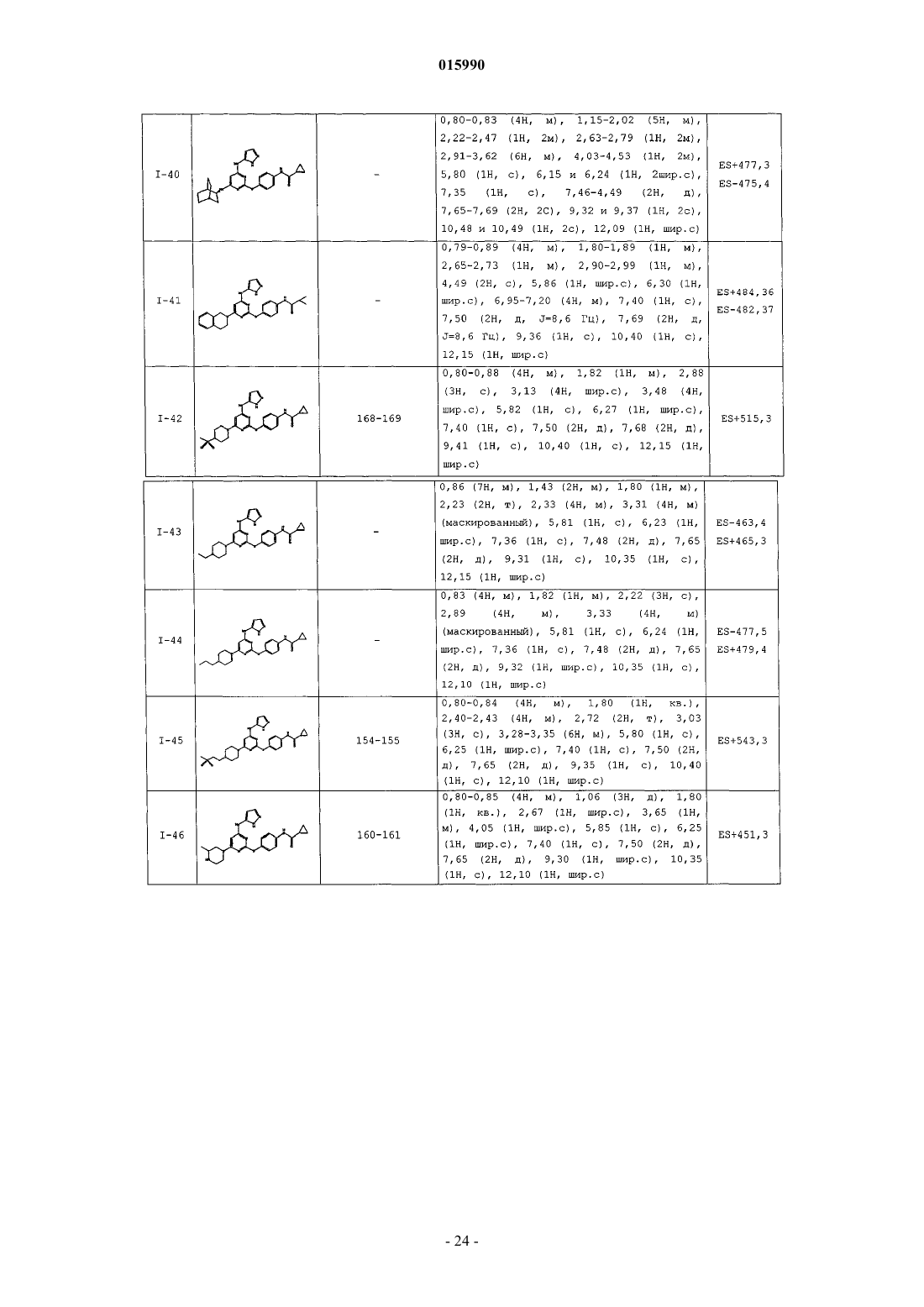
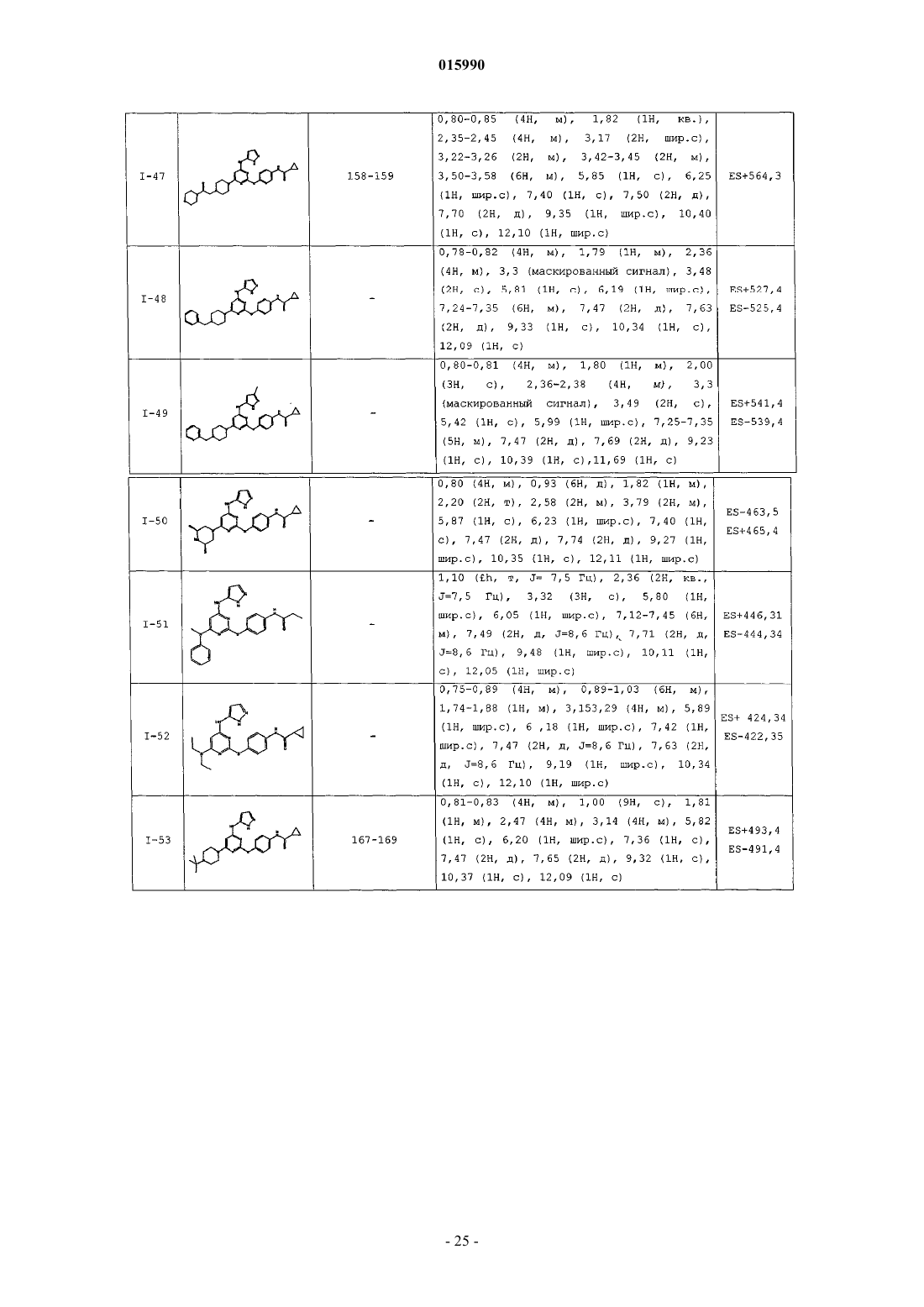
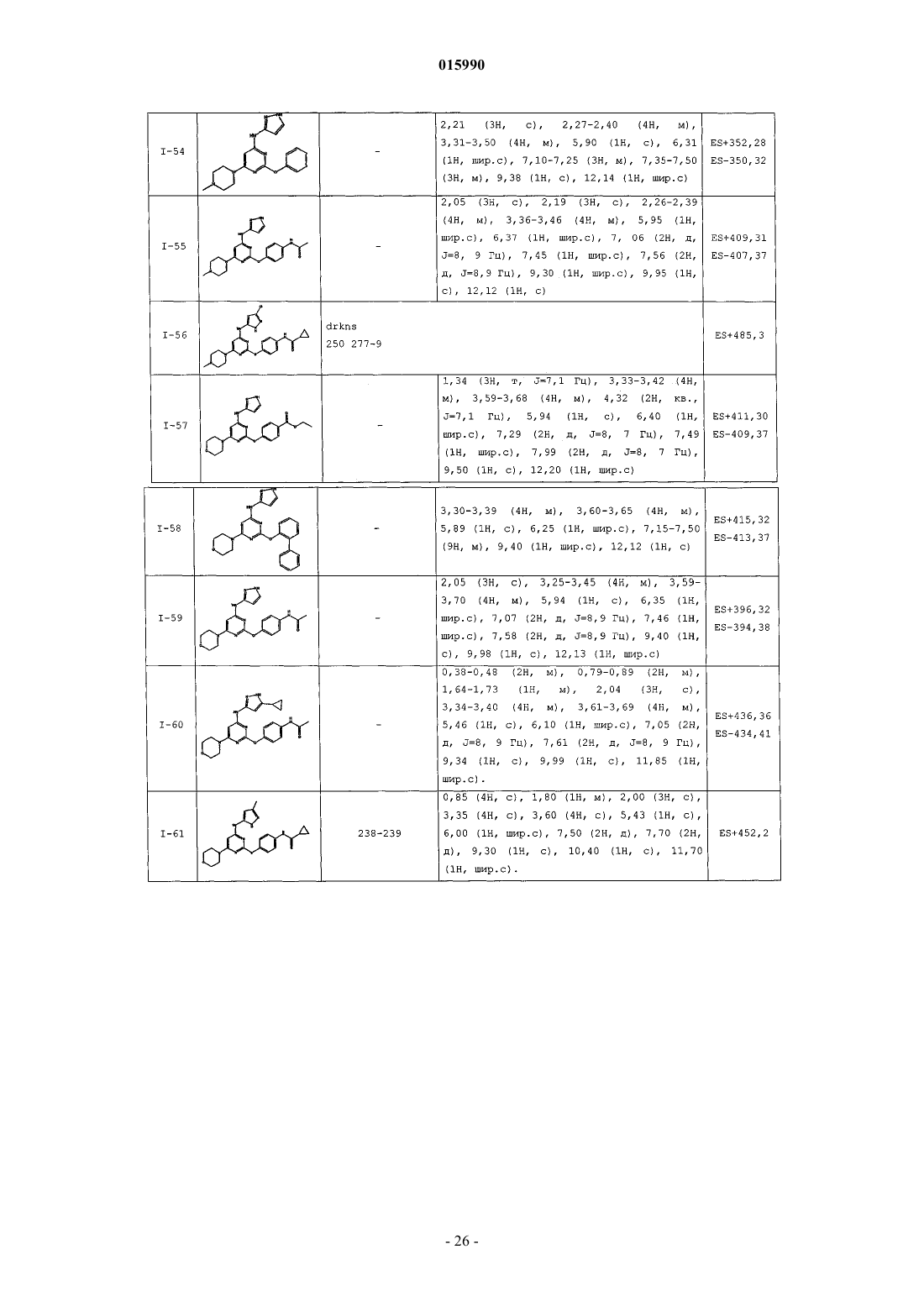
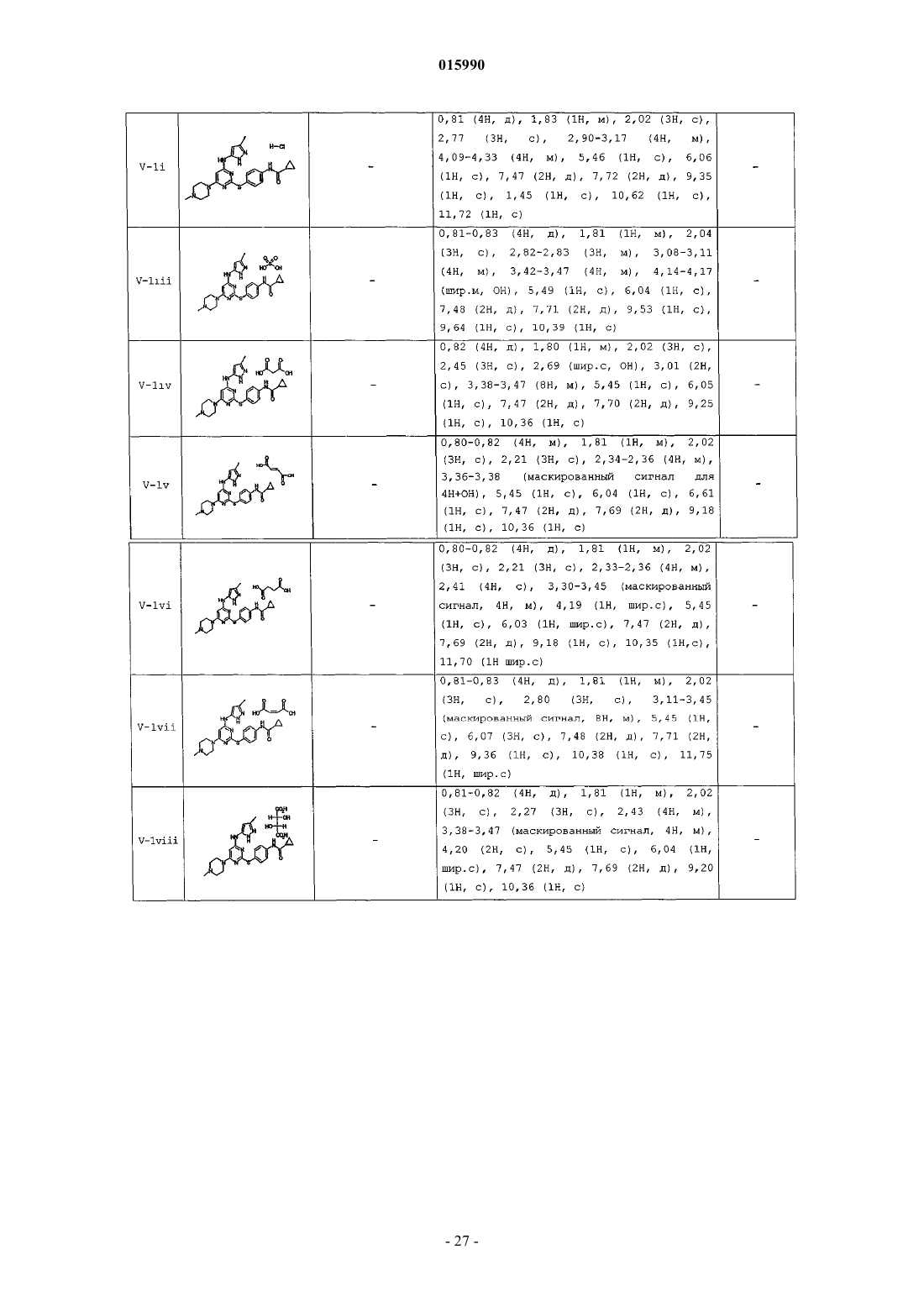
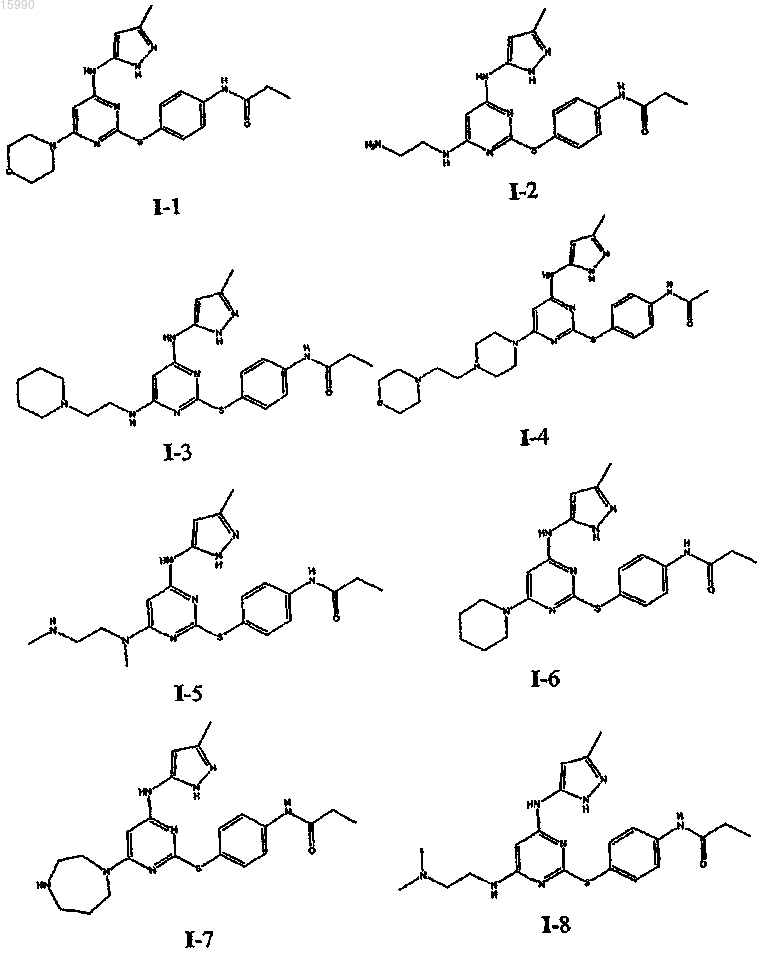
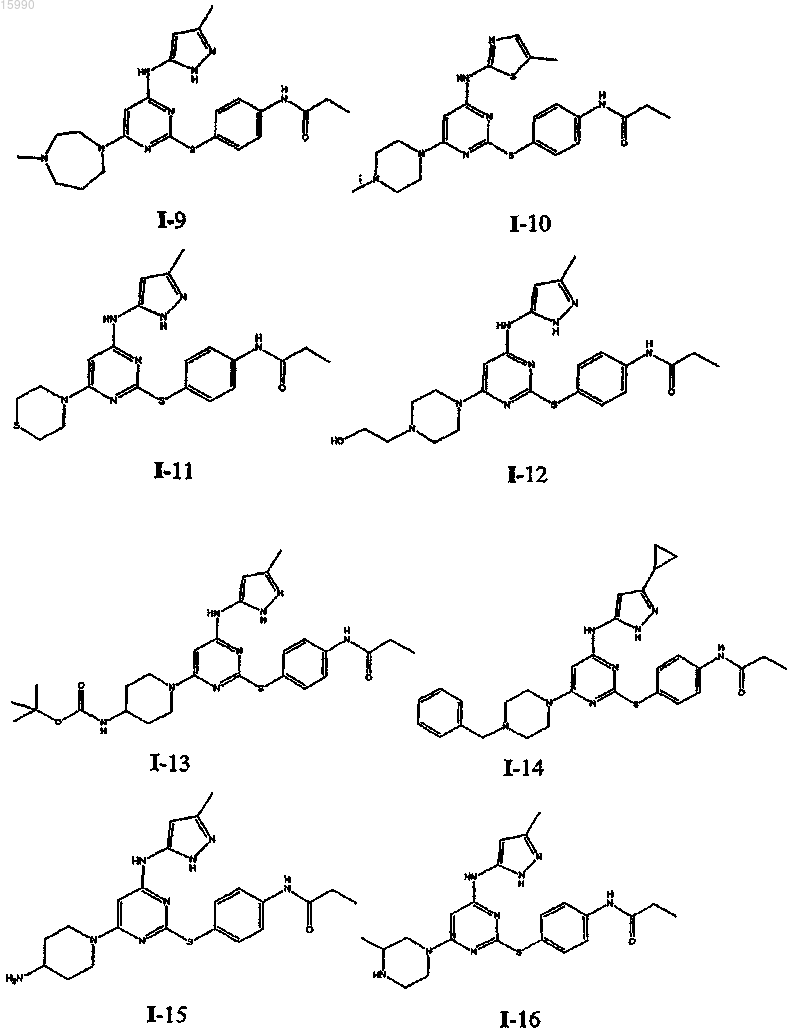
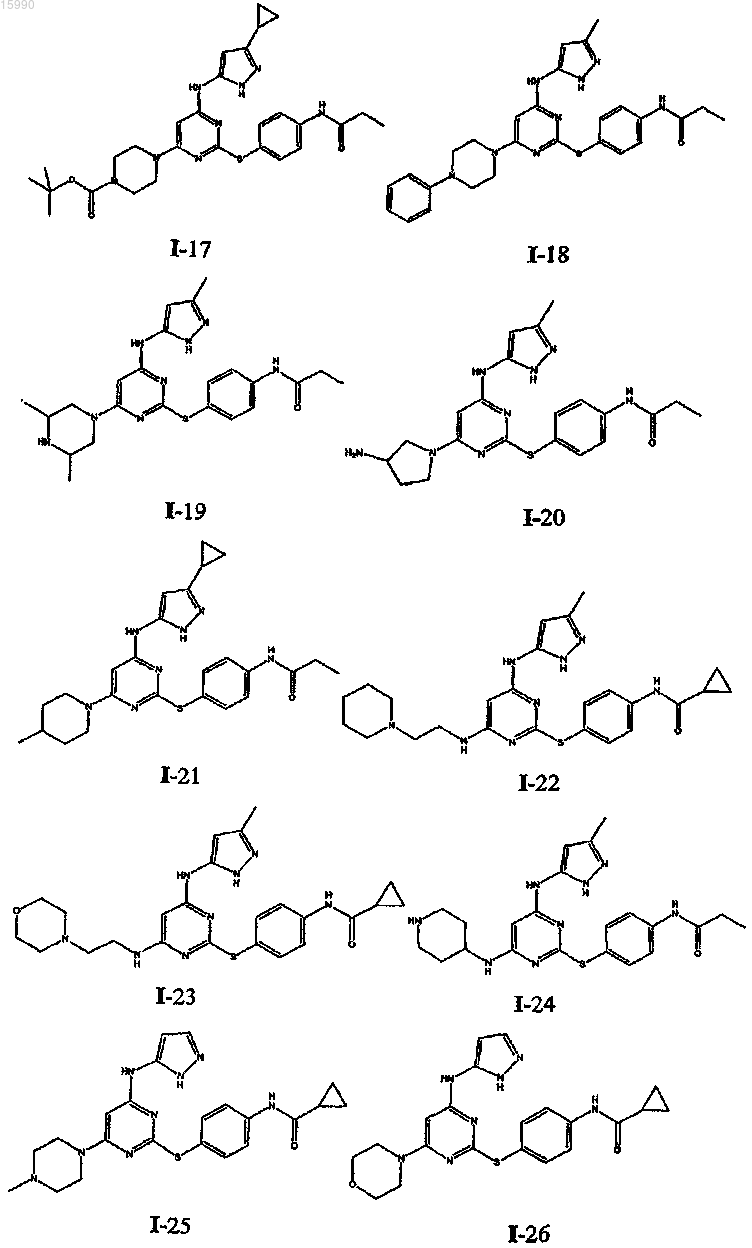
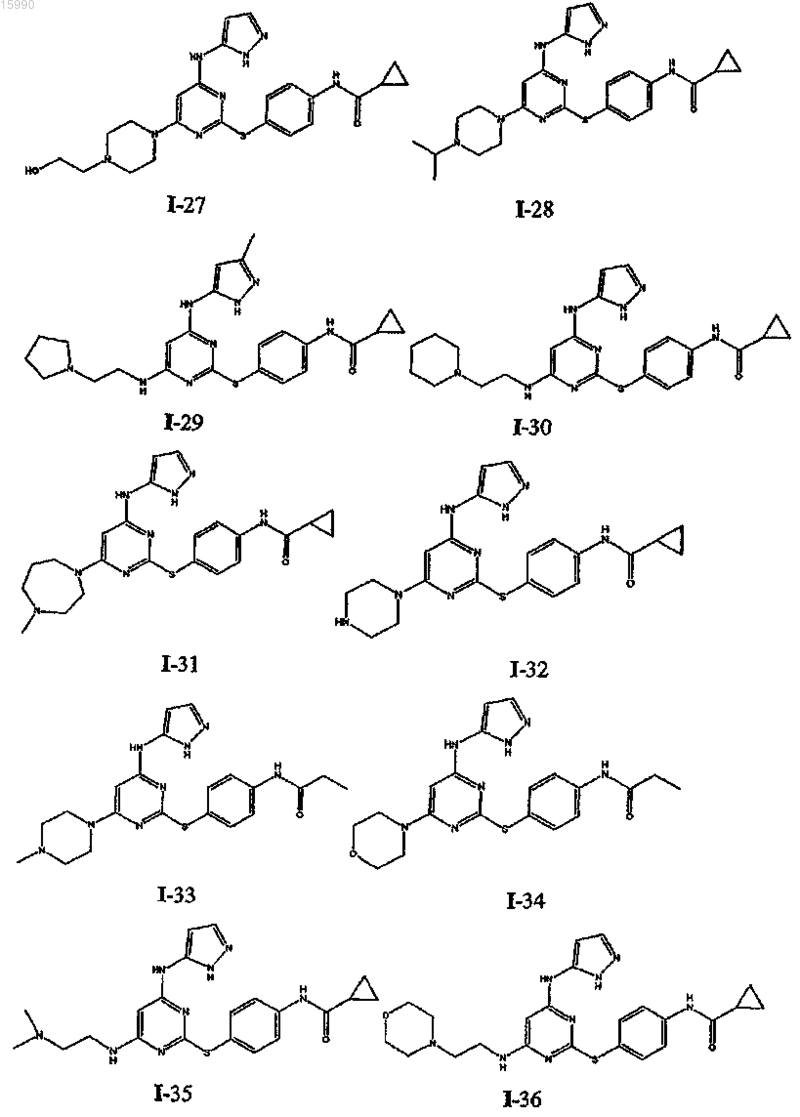
14. Способ по п.1, где указанный способ используют для получения соединения, выбранного из следующих соединений табл. 1 и 2:
Таблица 1
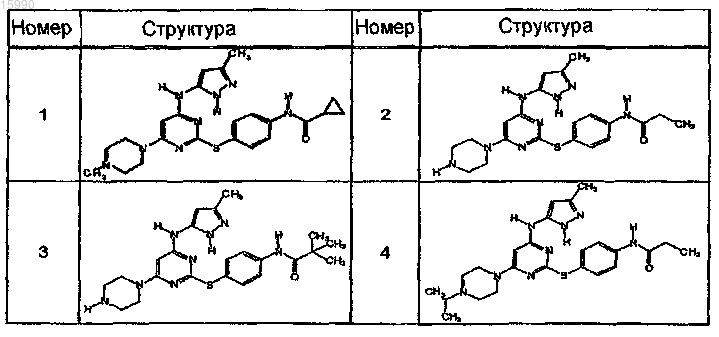
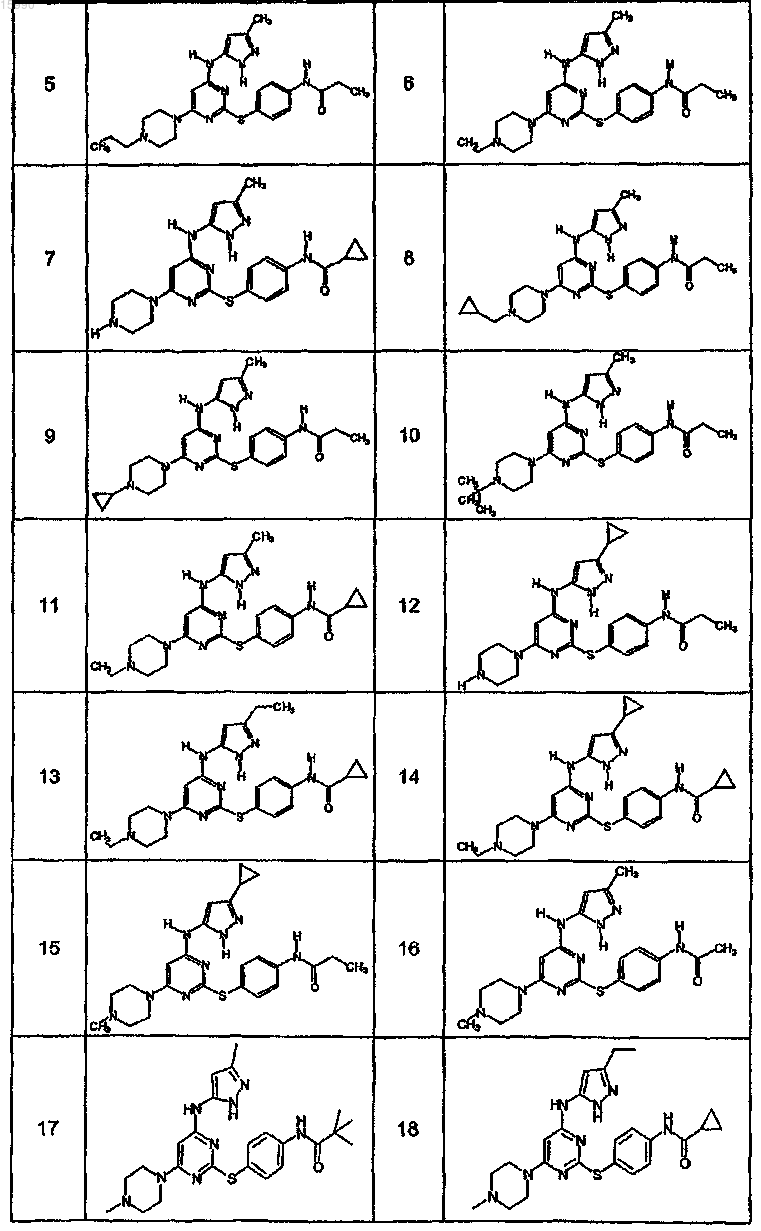
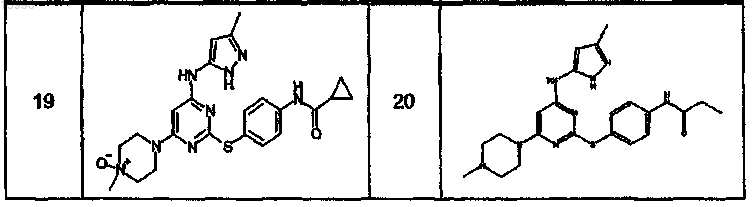
Таблица 2
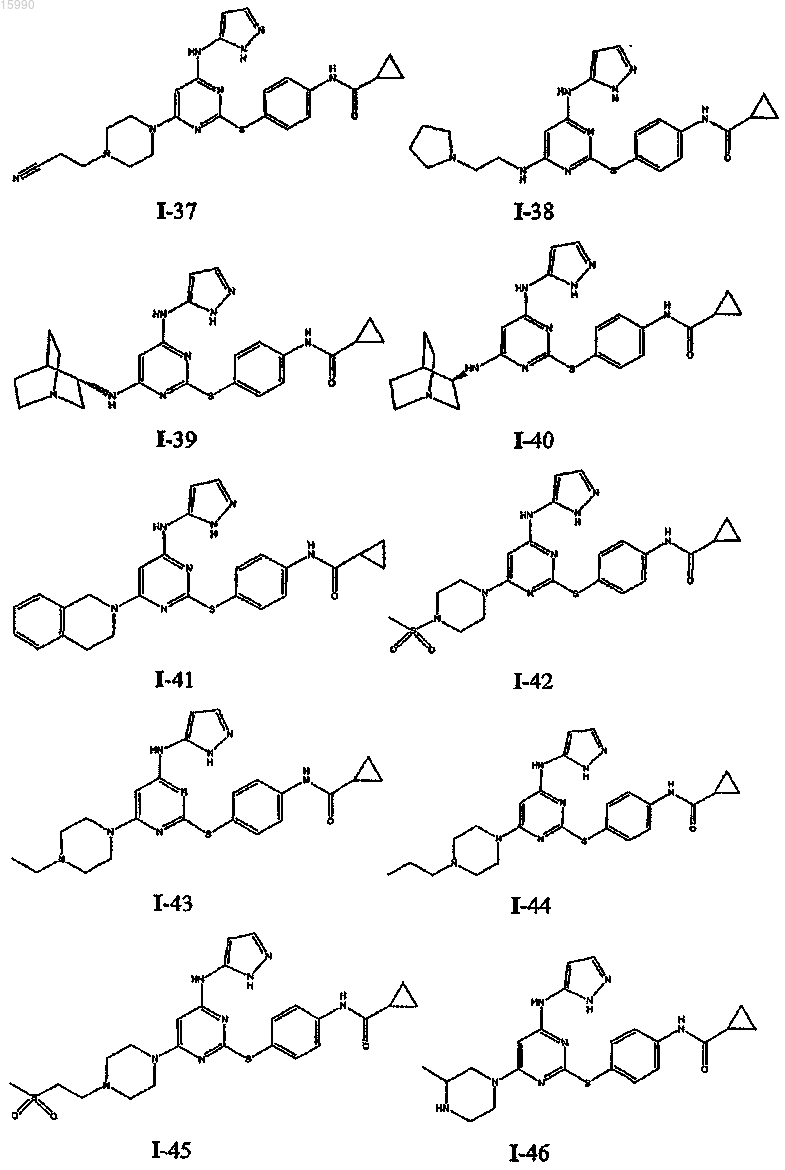

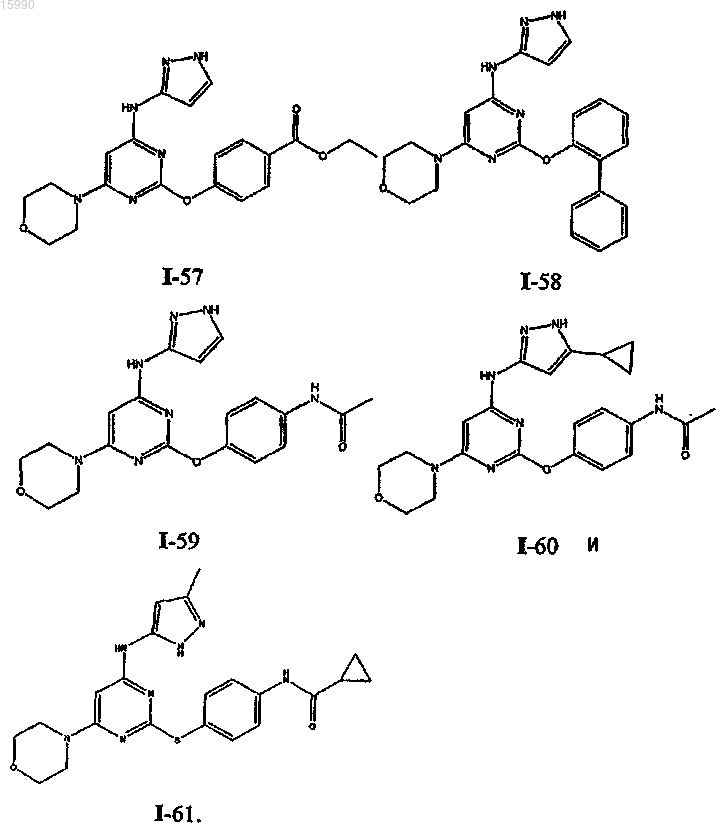
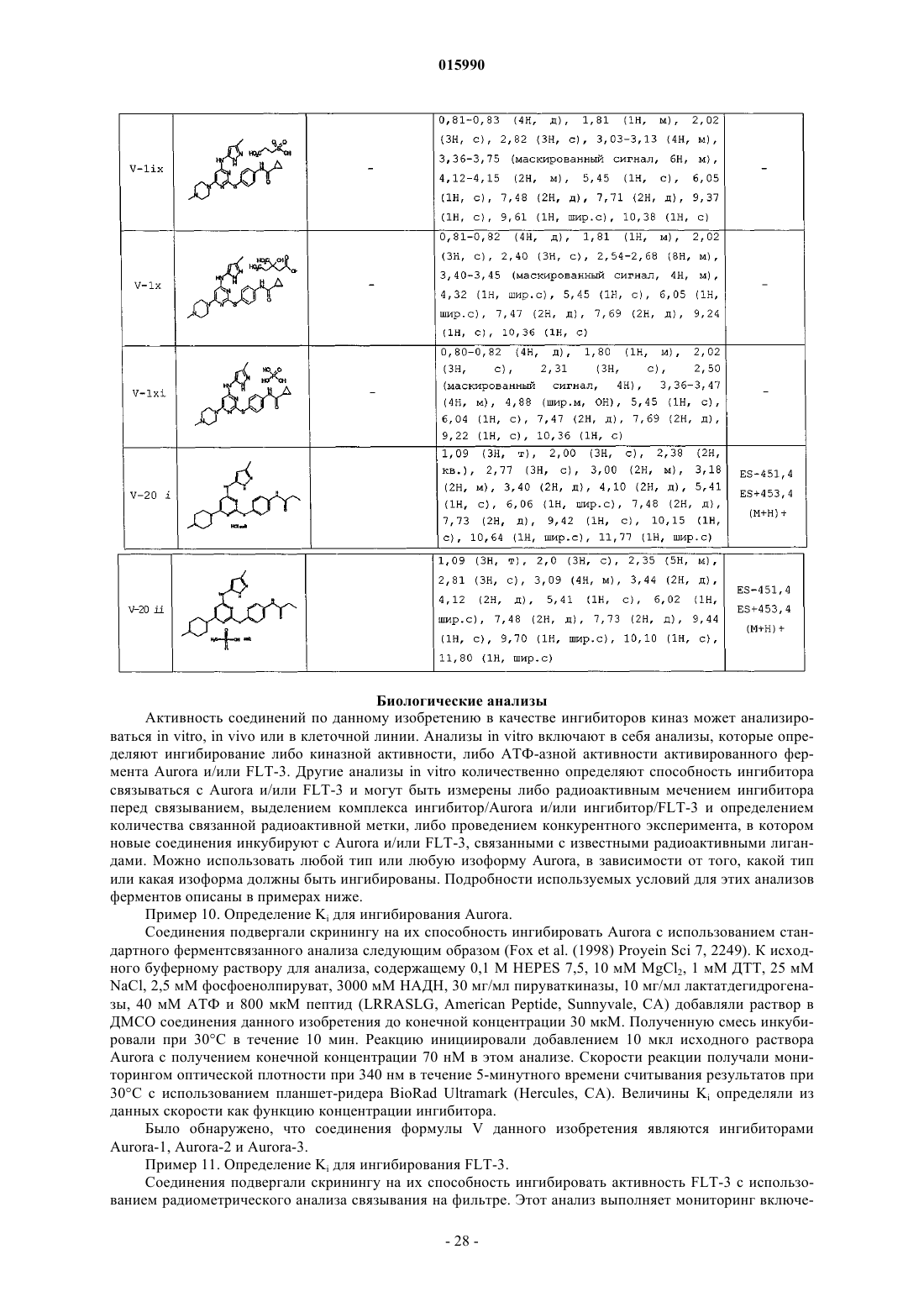
Текст
СПОСОБЫ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ПИРИМИДИНОВ Данное изобретение относится к усовершенствованному тетразамещенных пиримидинов общей формулы которые могут быть использованы в качестве ингибиторов протеинкиназ для лечения или ослабления опосредованных Aurora заболеваний или состояний.(71)(73) Заявитель и патентовладелец: ВЕРТЕКС ФАРМАСЬЮТИКАЛЗ ИНКОРПОРЕЙТЕД (US) 015990 Перекрестная ссылка на родственные заявки Поданной заявке испрашивается приоритет в соответствии с предварительной заявкой на патент США 60/390658, поданной 20 июня 2002 г., и предварительной заявкой на патент США 60/411609, поданной 18 сентября 2002 г., содержания которых включены здесь в качестве ссылки. Область техники, к которой относится изобретение Данное изобретение относится к легкому способу получения замещенных пиримидинов. Этот способ применим для получения ингибиторов протеинкиназ, в частности FLT-3 и киназ семейства Aurora,серин/треонинпротеинкиназ. Данное изобретение относится также к ингибиторам протеинкиназ FLT-3,Aurora-1, Aurora-2 и Aurora-2 и их композициям. Уровень техники Поиск новых терапевтических средств был в значительной степени облегчен в последние годы лучшим пониманием структуры ферментов и других биомолекул, ассоциированных с представляющими интерес заболеваниями. Одним важным классом ферментов, который был предметом интенсивного исследования, являются протеинкиназы. Протеинкиназы опосредуют внутриклеточную трансдукцию сигналов. Они осуществляют это путем переноса фосфорила от нуклеозидтрифосфата к белковому акцептору, который участвует в пути передачи сигнала. Имеется ряд киназ и путей, посредством которых внеклеточные и другие стимулы индуцируют различные клеточные реакции внутри клетки. Примеры таких стимулов включают в себя сигналы окружающей среды и химического стресса (например, осмотический шок, тепловой шок, ультрафиолетовую радиацию, бактериальный эндотоксин и Н 2 О 2), цитокины (например, интерлейкин-1 (IL-1) и фактор некроза опухолей альфа (TNF- и факторы роста (например, колониестимулирующий фактор гранулоцитов и макрофагов (GM-CSF) и фактор роста фибробластов (FGF. Внеклеточный стимул может действовать на одну или несколько клеточных реакций, связанных с ростом, миграцией, дифференцировкой клеток, секрецией гормонов, активацией факторов транскрипции, мышечным сокращением,метаболизмом глюкозы, регуляцией синтеза белка и регуляцией клеточного цикла. Многие заболевания ассоциированы с нарушенными клеточными реакциями, запускаемыми опосредуемыми протеинкиназами событиями. Эти заболевания включают в себя аутоиммунные заболевания, воспалительные заболевания, костные заболевания, метаболические заболевания, неврологические и нейродегенеративные заболевания, рак, сердечно-сосудистые заболевания, аллергии и астму, болезнь Альцгеймера и связанные с гормонами заболевания. Таким образом, в медицинской химии прилагались существенные усилия для нахождения ингибиторов протеинкиназ, которые являются эффективными в качестве терапевтических агентов. Семейство Aurora серин/треонинкиназ является важным для пролиферации клеток [Bischoff J.R.as regulators of cell divisions and its checkpoints) Nat. Rev. Mol. Cell Biol. 2, 21-32 (2001); Adams R.R., Carmena M. and Earnshaw W.C. (Chromosomal passengers and the (aurora) ABC of mitosis) Trends in Cell Biology 11, 49-54 (2001)]. Таким образом, ингибиторы семейства киназ Aurora имеют потенциал блокирования роста всех типов опухолей. Три известных члена семейства млекопитающих, Aurora-A (1), В (2) и С (3) являются высокогомологичными белками, ответственными за хромосомное расщепление, функцию митотического веретена и цитокинез. Экспрессия Aurora является низкой или недетектируемой в покоящихся клетках, с повышением экспрессии и активности до максимума во время фазы G2 и митотической фазы в клеточном цикле. В клетках млекопитающих предполагаемые субстраты Aurora включают в себя гистон Н 3, белок, участвующий в конденсации хромосом, и CENP-A, регуляторную легкую цепь миозина II, протеинфосфатазу 1, ТРХ 2, которые все необходимы для деления клеток. С его открытия в 1997 г. семейство киназ Aurora тесно связывали с онкогенезом. Наиболее привлекающим внимание доказательством этой связи является то, что сверхэкспрессия Aurora-A вызывает перерождение фибробластов грызунов (Bischoff J.R., et al., A homologue of Drosophila aurora kinase is oncogenic and amplified in human colorectal cancers. EMBO J. 17, 3052-3065 (1998. Клетки с повышенными уровнями этой киназы содержат множественные центросомы и мультиполярные веретена и быстро становятся анеуплоидными. Онкогенная активность киназ Aurora, по-видимому, связана с генерированием такой генетической нестабильности. Действительно, наблюдали корреляцию между амплификацией локуса Aurora-A и хромосомной нестабильностью в опухолях молочной железы и желудка (Miyoshi Y.,Iwao K., Egawa С. and Noguchi S. Association of centrosomal kinase STK15/BTAK mRNA expression withchromosomal instability in human breast cancers. Int. J. Cancer 92, 370-373 (2001). (Sakakura С. et al. Timoramplified kinase BTAK is amplified and overexpressed in gastric cancers with possible involvement in aneuploid formation. British Journal of Cancer 84, 824-831 (2001. Сообщалось, что киназы Aurora сверхэкспрессируются в большом диапазоне опухолей человека. Повышенная экспрессия Aurora-A была обнаружена в более чем 50% колоректальных опухолей (Bischoff J.R. et al. A homologue of Drosophila auroraof centrosome kinase BTAK/Aurora-A in human ovarian cancer. Clinical Cancer Research 9, 1420-1426 (2003 и опухолей желудка (Sakakura С. et al. Timor-amplified kinase BTAK is amplified and overexpressed in gastric cancers with possible involvement in aneuploid formation. British Journal of Cancer 84, 824-831 (2001 и в 94% инвазивных аденокарцином млечных протоков молочной железы (Tanaka Т. et al. Centrosomal kinaseAIK1 is overexpressed in invasive ductal carcinoma of the breast. Cancer Research, 59, 2041-2044 (1999. Высокие уровни Aurora-A сообщались также в почечных, цервикальных, нейробластомных, меланомных,лимфомных, панкреатических линиях опухолевых клеток и линиях клеток опухоли предстательной железы (Bischoff J.R. et al. A homologue of Drosophila aurora kinase is oncogenic and amplified in human colorectal cancers. EMBO J. 17, 3052-3065 (1998, (Kimura M., Matsuda Y., Yoshioka Т. and Okano Y. Cell cycle-dependent expression and centrosomal localization of a third human Aurora/Ipl1-related protein kinase,AIL3, Journal of Biological Chemistry 274, 7334-7340 (1999, (Zhou et al. Tumour amplifiec kinaseClin Cancer Res. 9(3):991-7 (2003. Амплификацию/сверхэкспрессию Aurora-A наблюдают в раках мочевого пузыря человека, и амплификация Aurora-A связана с анеуплоидией и агрессивным клиническим поведением (Sen S. et al. Amplification/overexpression of mitotic kinase gene in human bladder cancer. J. Natl.Cancer Inst. 94(17):132909 (2002. Кроме того, амплификация локуса Aurora-A (20q13) коррелирует с плохим прогнозом для пациентов с лимфоузел-отрицательным раком молочной железы (Isola J.J. et al.cancer. American Journal of Pathology 147, 905-911 (1995. Aurora-B экспрессируется на высоком уровне во множественных линиях опухолевых клеток человека, в том числе лейкозных клетках (Katayama et al.Human AIM-1: cDNA cloning and reduced expression during endomitosis in megakaryocyte-lineage cells. Gene 244:1-7. Уровни этого фермента увеличиваются как функция стадии Duke в первичных колоректальных раках (Katayama Н. et al. Mitotic kinase expression and colorectal cancer progression. Journal of the NationalCancer Institute 91, 1160-1162 (1999. Aurora-C, которая обычно обнаруживается только в зародышевых клетках, сверхэкспрессируется также в высоком проценте первичных колоректальных раков и в различных линиях опухолевых клеток, в том числе клетках цервикальной аденокарциномы и карциномы молочной железы (Kimura М., Matsuda Y., Yoshioka Т. and Okano Y. Cell cycle-dependent expression and centrosomal localization of a third human Aurora/Ipl1-related protein kinase, AIK3, Journal of Biological Chemistry 274, 7334-7340 (1999, (Takahashi Т. et al. Centrosomal kinases, HsAIRk1 and HsAIRK3, are overexpressedin primary colorectal cancers. Jpn. J. Cancer Res. 91, 1007-1014 (2000. На основе известного действия киназ Aurora ингибирование их активности должно нарушать митоз,приводя к остановке клеточного цикла. Таким образом, in vivo ингибитор Aurora замедляет рост и индуцирует регресс опухоли. Повышенные уровни всех членов семейства Aurora наблюдаются в широком разнообразии линий опухолевых клеток. Киназы Aurora сверхэкспрессируются во многих опухолях человека и, как сообщается, ассоциированы с хромосомной нестабильностью в опухолях молочной железы (Miyoshi et al. 2001, 92,370-373).Aurora-2 экспрессируется на высоком уровне во множественных линиях опухолевых клеток человека, и уровни увеличиваются как функция стадии Duke в первичных колоректальных раках [Katayama Н.et al. Mitotic kinase expression and colorectal cancer progression. Journal of the National Cancer Institute 91,1160-1162 (1999)]. Aurora-2 играет роль в регуляции точного расщепления хромосом во время митоза. Ошибочная регуляция клеточного цикла может привести к клеточной пролиферации и другим нарушениям. Было обнаружено, что в ткани рака ободочной кишки человека сверхэкспрессируется белок(1998); Kimura et al., J. Biol. Chem., 272, 13766-13771 (1997)]. Aurora-2 сверхэкспрессируется в большинстве трансформированных клеток. Bischoff et al. обнаружил высокие уровни Aurora-2 в 96% клеточных линий, полученных из опухолей легкого, ободочной кишки, почки, меланомы и молочной железы(Bischoff et al., EMBO J., 1998, 17, 3052-3065). Два интенсивных исследования показывают повышенный уровень Aurora-2 в 54 и 68% (Bischoff et al., EMBO J., 1998, 17, 3052-3065) (Takahashi et al. 2000, Jpn. J.Cancer Res. 91, 1007-1014) колоректальных опухолей и в 94% инвазивных аденокарцином млечных протоков молочной железы (Tanaka et al., 1999, 59, 2041-2044). Экспрессия Aurora-1 является повышенной в клеточных линиях, полученных из опухолей ободочной кишки, молочной железы, легкого, меланомы, печени, яичника, поджелудочной железы, ЦНС, желудочно-кишечного тракта и лейкозов (Tatsuka et al., 1998, 58, 4811-4816). Высокие уровни Aurora-3 были обнаружены в нескольких линиях опухолевых клеток, хотя она ограничена яичком в нормальных тканях (Kiraura et al., 1999, 274, 7334-7340). Сверхэкспрессия Aurora-3 в высоком проценте (приблизительно 50%) колоректальных раков также была документирована (Takahashiet al., 2000, Jpn. J. Cancer Res. 91, 1007-1014). В противоположность этому семейство Aurora экспрессируется при низком уровне в большинстве нормальных тканей, за исключением тканей с высокой долей-2 015990 делящихся клеток, таких как вилочковая железа и яичко (Bischoff et al., EMBO J., 1998, 17, 3052-3065). В отношении дополнительного обзора роли киназ Aurora, которую они играют в пролиферативных нарушениях, см. Bischoff J.R.Plowman G.D. (The Aurora/Ipl1p kinase family: regulators of chromosomeof aurora-A in centrosome function) Oncogene 21, 6175-6183 (2002). Рецепторная тирозинкиназа типа III, Flt3, играет важную роль в поддержании, росте и развитии гемопоэтических и негемопоэтических клеток [Scheijen В., Griffin J.D., Oncogene, 2002, 21, 3314-3333 иReilly J.T., British Journal of Haematology, 2002, 116, 744-757]. FLT-3 регулирует поддержание пулов стволовых клеток/клеток-предшественников, а также развитие зрелых лимфоидных и миелоидных клеток[Lyman S., Jacobsen S., Blood, 1998, 91, 1101-1134]. FLT-3 содержит внутренний киназный домен, который активируется после опосредованной лигандом димеризации этих рецепторов. После активации киназный домен индуцирует аутофосфорилирование рецептора, а также фосфорилирование различных цитоплазматических белков, которые способствуют размножению сигнала активации, приводящего к росту, дифференцировке и выживанию. Некоторые из стоящих далее по ходу процесса регуляторов передачи сигнала FLT-3-рецептора включают в себя PLC, PI3-киназу, Grb-2, SHIP и Src-родственные киназы[Scheijen В., Griffin J.D., Oncogene, 2002, 21, 3314-3333]. Киназа FLT-3 играет роль во многих гемопоэтических и негемопоэтических злокачественностях. Считают, что мутации, которые индуцируют лиганднезависимую активацию FLT-3, участвуют в остром миелогенном лейкозе (AML), остром лимфоцитарном лейкозе (ALL), мастоцитозе и желудочно-кишечной стромальной опухоли (GIST). Эти мутации включают в себя изменения единственной аминокислоты в киназном домене или внутренних тандемных удвоениях, точковые мутации или делеции в рамке считывания юкстамембранного района этих рецепторов. Кроме активации мутаций, лигандзависимая (аутокринная или паракринная) стимуляция сверхэкспрессируемой киназы FLT-3 дикого типа вносит вклад в злокачественный фенотип [Scheijen В., Griffininhibitor therapy for acute myeloid leukaemia) Cancer Cell. 1, 413-415 (2002). Три- или тетразамещенные производные пиримидинов, применимые в качестве ингибиторов киназ,известны в данной области. Обычно эти производные пиримидинов являются 2,4,6- или 2,4,5,6 замещенными, как показано ниже 2,4,6-замещенный пиримидин 2,4,5,6-замещенный пиримидин Известные способы получения таких производных пиримидинов обладают родом недостатков синтеза, такими как отсутствие возможности региоселективного введения заместителей в положении 2, 4 или 6 с высокими выходами. См. М. Botta, Nucleosides Nucleotides, 13, 8, 1994, 1769-78; М. Ban, Bioorg.Het. Chem., 35, 2, 1998, 269-74; H. Uchel, Tetrahedron Lett., 36, 52, 1995, 9457-60 и Y. Nezu, Pestic. Sci., 47,2, 1996, 115-24. Существует потребность в синтетическом способе, который может быть легко использован для получения три- или тетразамещенных производных пиримидинов в крупном масштабе. Существует также потребность в способе, в котором имеется минимальное количество стадий и в котором используются легкодоступные исходные материалы и простые реакционные среды. В идеале, такой способ будет легко осуществим в крупном масштабе и он не будет дорогостоящим. Существует также потребность в способе, который не будет приводить к промежуточным региоизомерным смесям, которые требуют разделения, например, хроматографическими способами. Такие разделения снижают общие выходы. Было бы желательно иметь синтетический способ получения три- или тетразамещенных производных пиримидинов, который обладает указанными выше преимуществами и, следовательно, является улучшенным в сравнении с доступными в настоящее время способами. Сущность изобретения Настоящее изобретение относится к способу получения соединения формулы I где Q и Т, каждый независимо, выбраны из кислорода, серы или N(R); каждый R независимо выбран из водорода или необязательно замещенной C1-6 алифатической группы, где два R, связанные с одним и тем же атомом азота, необязательно взяты вместе с этим атомом азота с образованием необязательно замещенного 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 03 гетероатома, наряду со связанным с ними азотом, независимо выбранных из азота, кислорода или серы;R5 выбран из галогена, NO2, CN, R или Ar; каждый U независимо выбран из валентной связи или C1-4 алкилиденовой цепи, где до двух метиленовых звеньев в U необязательно и независимо заменены на -О-, -S-, -SO-, -SO2-,-N(R)SO2-, -SO2N(R)-, -N(R)-, -C(O)-, -CO2-, -N(R)C(O)-, -N(R)C(O)O-, -N(R)CON(R)-, -N(R)SO2N(R)-,-N(R)N(R)-, -C(O)N(R)-, -OC(O)N(R)-, -C(R)=NN(R)- или -C(R)=N-O-; каждый Ar независимо выбран из необязательно замещенного кольца, выбранного из 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы;Ry обозначает -N(R1)2, -OR1 или -SR1; каждый R1 независимо выбран из R или 3-8-членного моноциклического, 8-10-членного бициклического или 10-12-членного трициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, и где каждый R1 необязательно и независимо содержит до четырех заместителей, независимо выбранных 2 из R ; каждый R2 независимо выбран из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2, -C(O)R3,-OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3),-OC(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2(R3); каждый R3 выбран независимо из R или Ar;Rz1 выбран из C1-6 алифатической группы или 3-8-членного моноциклического, 8-10-членного бициклического или 10-12-членного трициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, гдеRz1 замещен 0-4 независимо выбранными группами R2;Rz2 обозначает 3-8-членное моноциклическое или 8-10-членное бициклическое насыщенное, частично ненасыщенное или полностью ненасыщенное кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, гдеRz2 замещен 0-4 заместителями, независимо выбранными из оксо или U-R5; где указанный способ включает первую стадию связывания соединения формулы IV с соединением формулы Rz2-T-H в первой подходящей среде с получением соединения формулы III,вторую стадию связывания соединения формулы III с соединением формулы Rz1-Q-H во второй подходящей среде с получением соединения формулы II и третью стадию связывания соединения формулы II с соединением формулы RY-H в третьей подходящей среде где каждая первая, вторая и третья подходящая среды независимо содержат:L1, L2, L3 обозначают подходящую уходящую группу. В предпочтительном варианте L3 выбран из галогена, необязательно замещенного арилсульфонила или необязательно замещенного алкилсульфонила, предпочтительно L3 обозначает фтор, хлор, бром,йод, паратолуолсульфонил, метансульфонил, паранитрофенилсульфонил, парабромфенилсульфонил или трифторметансульфонат, более предпочтительно L3 обозначает хлор или йод. В другом варианте L2 обозначает галоген, необязательно замещенный арилсульфонил или необязательно замещенный алкилсульфонил, предпочтительно L2 обозначает фтор, хлор, бром, йод, паратолуолсульфонил, метансульфонат, паранитрофенилсульфонил, парабромфенилсульфонил или трифторметансульфонат, более предпочтительно L2 обозначает хлор или йод. В другом предпочтительном варианте L1 обозначает галоген, необязательно замещенный арилсульфонил или необязательно замещенный алкилсульфонил, предпочтительно L1 обозначает необязательно замещенный алкилсульфонил, более предпочтительно L1 обозначает метансульфонил. В предпочтительном варианте Q обозначает N(R). В другом предпочтительном варианте Т обозначает кислород или серу, предпочтительно Т обозначает серу. В одном из предпочтительных вариантов Ry обозначает -OR1 или -N(R1)2-. Предпочтительно Ry обозначает -N(R1)2 и где R1 выбран из R или 3-7-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, или каждый R1 обозначает R, так что эти два R на одном атоме азота взяты вместе с образованием необязательно замещенного 4-7-членного насыщенного кольца, содержащего до двух дополнительных гетроатомов, независимо выбранных из азота, кислорода или серы, и где каждый R1 необязательно и независимо замещен до четырех заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена,-N(R3)2, -C(O)R3, -OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2,-ОС(O)NR(R3), -ОС(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2(R3), предпочтительно Ry обозначает -N(R1)2, и каждый R1 независимо выбран из R, где R обозначает водород или необязательно замещенную C1-4 алифатическую группу. Более предпочтительно Ry обозначает -N(R1)2, где каждый R1 обозначает R, так что эти две R группы взяты вместе с образованием необязательно замещенного 4-7-членного насыщенного кольца, содержащего до двух дополнительных гетроатомов, независимо выбранных из азота, кислорода или серы,предпочтительно Ry выбран из пирролидин-1-ила, пиперидин-1-ила, морфолин-4-ила, тиоморфолин-4 ила, пиперазин-1-ила, диазепанила или тетрагидроизохинолинила, где каждое кольцо необязательно замещено одной или двумя группами, независимо выбранными из метила, этила, метилсульфонила,(СН 2)2SO2CH3, циклопропила, СН 2 циклопропила, (СН 2)2 ОН, СО 2-трет-бутила, СН 2 фенила, фенила, NH2,-5 015990NH(СН 3), N(СН 3)2, (СН 2)2NH2, (СН 2)2 морфолин-4-ила, (CH2)2N(СН 3)2, изопропила, пропила, трет-бутила,(CH2)2CN или (СН 2)2 С(О)морфолин-4-ила. В частном варианте Rz1 обозначает 3-7-членное моноциклическое или 8-10-членное бициклическое насыщенное, частично ненасыщенное или полностью ненасыщенное кольцо, содержащее 0-4 гетероатома, независимо выбранных из кислорода, азота или серы, где указанное кольцо необязательно и независимо замещено тремя заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2,-C(O)R3, -OC(O)R3, -CO2R3, -SO2R3, -SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3),-OC(O)N(R3)2, -NR3C(O)R3, -NR3C(O)N(R3)2 или -NR3CO2R3, предпочтительно Rz1 обозначает 5-6-членное полностью ненасыщенное кольцо, содержащее 1-3 гетероатома, независимо выбранных из азота, кислорода или серы, где указанное кольцо необязательно и независимо замещено тремя заместителями, выбранными из -R3, -OR3, -SR3, -CN, -NO2, оксо, галогена, -N(R3)2, -C(O)R3, -OC(O)R3, -CO2R3, -SO2R3,-SO2N(R3)2, -N(R3)SO2R3, -C(O)NR(R3), -C(O)N(R3)2, -ОС(O)NR(R3), -ОС(O)N(R3)2, -NR3C(O)R3,-NR3C(O)N(R3)2 или -NR3CO2R3; более предпочтительно Rz1 обозначает необязательно замещенное кольцо, выбранное из пиразола или любого из следующих 5-6-членных колец: Наиболее предпочтительно Rz1 обозначает пиразольное кольцо, содержащее до двух заместителей,независимо выбранных из -N(R3)2, -OR3 или C1-4 алифатической группы, например Rz1 обозначает пиразол, необязательно замещенный одним заместителем, выбранным из метила, этила, пропила, изопропила,трет-бутила, циклопропила или фенила. Кроме того, в одном из вариантов Rz2 обозначает необязательно замещенное кольцо, выбранное из 5-6-членного моноциклического или 8-10-членного бициклического насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, где указанное кольцо необязательно замещено до трех заместителями, независимо выбранными из галогена, -CN, -NO2, -C(O)R3, -CO2R3, -C(O)NR(R3), -NR3C(O)R3, -N(R3)2,-N(R3)SO2R3, -NR3C(O)N(R3)2 или -NR3CO2R3; предпочтительно Rz2 выбран из фенила, имидазолила, пиразолила, пиридила, пиридазинила, пиразинила, нафтила, тетрагидронафтила, бензимидазолила, бензтиазолила, хинолинила, хиназолинила, бензодиоксинила, изобензофурана, инданила, индолила, индолинила,индазолила или изохинолинила, где Rz2 необязательно замещен до трех заместителями, независимо выбранными из -Cl, -Br, -F, -CN, -CF3, -СООН, -CONHMe, -CONHEt, -NH2, -NHAc, -NHSO2Me, -NHSO2Et,-NHSO2(н-пропил), -NHSO2(изопропила), -NHCOEt, -NHCOCH2NHCH3, -NHCOCH2N(CO2t-Bu)CH3,-NHCOCH2N(CH3)2,-NHCOCH2CH2N(CH3)2,NHCOCH2CH2CH2N(CH3)2,-NHCO(циклопропила),-NHCO(изопропила), NHCO(изобутила), -NHCOCH2(морфолин-4-ила), -NHCH2COCH2(морфолин-4-ила),-NHCH2COCH2CH2(морфолин-4-ила), -NHCO2(трет-бутила), NH(циклогексила), -NHMe, -NMe2, -ОН,-OMe, метила, этила, циклопропила, изопропила или трет-бутила; более предпочтительно Rz2 содержит один заместитель, выбранный из -NR3C(O)R3, где каждый R3 независимо выбран из R или Ar и где R обозначает водород или необязательно замещенную C1-4 алифатическую группу. При реализации одного из вариантов способа подходящим растворителем является протонный растворитель, галогенированный углеводород, простой эфир, ароматический углеводород, полярный или неполярный апротонный растворитель или любая их смесь, предпочтительно указанным растворителем является C1-5 прямой или разветвленный алкиловый спирт, простой эфир или полярный или неполярный растворитель. При реализации одного из вариантов подходящее основание выбрано из органического амина, карбоната щелочно-земельного металла, гидрида щелочно-земельного металла или гидроксида щелочноземельного металла, предпочтительно указанное подходящее основание выбрано из триалкиламина, карбоната натрия, карбоната калия, гидрида натрия, гидрида калия, гидроксида натрия или гидроксида натрия. В одном из вариантов способа используют для получения соединения, выбранные из следующих соединений табл. 1 и 2: Подходящим растворителем является растворитель или смесь растворителей, которые в сочетании со связываемыми соединениями могут облегчать протекания реакции между ними. Подходящий растворитель может солюбилизировать одно или несколько реакционных компонентов или, альтернативно,подходящий растворитель может облегчать перемешивание суспензии одного или нескольких реакционных компонентов. Примерами подходящих растворителей, применимых в данном изобретении, являются протонный растворитель, галогенированный углеводород, простой эфир, ароматический углеводород,полярный или неполярный апротонный растворитель или любые их смеси. Эти и другие подобные подходящие растворители хорошо известны в данной области, например, см. "Advanced Organic Chemistry",Jerry March, 4th edition, John Wiley and Sons, N.Y. (1992). Предпочтительно подходящим растворителем является C1-7 прямой или разветвленный алкиловый спирт, простой эфир или полярный или неполярный растворитель. Для реакции между соединением формулы II и соединением Ry-H более предпочтительный подходящий растворитель выбран из этанола, изопропанола, трет-бутанола, н-бутанола или тетрагидрофурана. Для реакции между соединением формулы III и соединением Rz1-Q-H более предпочтительный подходящий растворитель выбран из этанола, изопропанола, трет-бутанола, н-бутанола, N,Nдиметилформамида, диметилсульфоксида или тетрагидрофурана. Для реакции между соединением формулы IV и соединением Rz2-T-H более предпочтительный подходящий растворитель выбран из N,N-диметилформамида, диметилсульфоксида или тетрагидрофурана. В соответствии с альтернативным вариантом осуществления подходящим растворителем являетсяRy-H. Таким образом, в таком варианте осуществления реагент Ry-H действует, частично, в качестве подходящего растворителя в сочетании с соединением формулы II, а также действует, частично, в качестве реагента и взаимодействует с соединением формулы II с образованием соединения формулы I. В соответствии с другим альтернативным вариантом осуществления подходящим растворителем является Rz1-Q-H. Таким образом, в таком варианте осуществления, реагент Rz1-Q-H действует, частично,в качестве подходящего растворителя в сочетании с соединением формулы III, а также действует, частично, в качестве реагента и взаимодействует с соединением формулы III с образованием соединения формулы II. В соответствии с другим альтернативным вариантом осуществления подходящим растворителем- 10015990 является Rz2-T-H. Таким образом, в таком варианте осуществления реагент Rz2-T-H действует, частично,в качестве подходящего растворителя в сочетании с соединением формулы IV, а также действует, частично, в качестве реагента и взаимодействует с соединением формулы IV с образованием соединения формулы III. Подходящее основание является химическим соединением, которое способно быть акцептором протонов. Примеры включают в себя органические амины, карбонаты щелочно-земельных металлов,гидриды щелочно-земельных металлов и гидроксиды щелочно-земельных металлов. Эти и другие такие подходящие основания хорошо известны в данной области, например, см. "Advanced Organic Chemistry",Jerry March, 4th, edition, 248-253, John Wiley and Sons, N.Y. (1992). Предпочтительные подходящие основания включают в себя триалкиламины, карбонат натрия, карбонат калия, гидрид натрия, гидрид натрия,гидроксид натрия или гидроксид калия. Более предпочтительно таким подходящим основанием является диизопропилэтиламин или триэтиламин. Подходящей удаляемой группой является химическая группа, которая легко вытесняется желаемой присоединяемой химической группой. Таким образом, выбор конкретной подходящей удаляемой группы определяется ее способностью легко вытесняться присоединяемой химической группой Ry в Ry-H, Rz1-Q в Rz1-Q-H или Rz2-T в Rz2-T-H. Подходящие удаляемые группы хорошо известны в данной области, например, см. "Advanced Organic Chemistry", Jerry March, 4th edition, 351-352, John Wiley and Sons, N.Y.(1992). Такие удаляемые группы включают в себя, но не ограничиваются ими, галоген, алкокси, сульфонилокси, необязательно замещенный алкилсульфонил, необязательно замещенный алкенилсульфонил,необязательно замещенный арилсульфонил и диазониевые группы. Примеры подходящих удаляемых групп включают в себя хлор, йод, бром, фтор, метансульфонил (мезил), тозил, трифлат, нитрофенилсульфонил (нозил) и бромфенилсульфонил (брозил). Например, в способе получения соединения формулы I L3 вытесняется присоединяемой группой Ryy из R -H. Таким образом, если Ry-H обозначает, например, пиперазин, то L3 является удаляемой группой,которая легко вытесняется группой -NH- в пиперазине. Предпочтительные удаляемые группы L3 выбраны из галогена, необязательно замещенного арилсульфонила или необязательно замещенного алкилсульфонила. Более предпочтительно L3 обозначает хлор, йод или метансульфонил. Наиболее предпочтительно L3 обозначает хлор. Например, в способе получения соединения формулы II L2 вытесняется присоединяемой группойR -Q из Rz1-Q-H. Таким образом, если Rz1-Q-H обозначает, например, 3-аминопиразол, то L2 является удаляемой группой, которая легко вытесняется 3-аминопиразолом. Предпочтительные удаляемые группы L2 выбраны из галогена, необязательно замещенного арилсульфонила или необязательно замещенного алкилсульфонила. Более предпочтительно L2 обозначает хлор, йод или фтор. Наиболее предпочтительно L2 обозначает хлор. Например, в способе получения соединения формулы III, L1 вытесняется присоединяемой группойR -T из Rz2-T-H. Таким образом, если Rz2-T обозначает, например, необязательно замещенный арилтиол,то L1 является удаляемой группой, которая легко вытесняется необязательно замещенным арилтиолом. Предпочтительные удаляемые группы L1 выбраны из галогена, необязательно замещенного арилсульфонила или необязательно замещенного алкилсульфонила. Более предпочтительно L1 обозначает хлор, йод или метансульфонил. Наиболее предпочтительно L1 обозначает метансульфонил. В соответствии с другим вариантом осуществления подходящая удаляемая группа может образовываться in situ в реакционной среде. Например, L3 в соединении формулы II может быть образован in situ из предшественника соединения формулы II, где указанный предшественник содержит группу, легко вытесняемую L3 in situ. В конкретном примере такого вытеснения указанный предшественник соединения формулы II содержит группу (например, группу хлор или гидроксильную группу), которая вытесняется in situ L3, таким как йод-группа. Источником йод-группы может быть, например, йодид натрия. В соответствии с этим L2 и L1 могут быть также образованы in situ аналогичным образом. Такое образование in situ подходящей удаляемой группой хорошо известно в данной области, например, см. "AdvancedOrganic Chemistry", Jerry March, 4th edition, 430-431, John Wiley and Sons, N.Y. (1992). В соответствии с еще одним альтернативным вариантом осуществления анион любого из Ry в Ry-H,z1R -Q в Rz1-Q-H или Rz2-Т в Rz2-T-H может быть образован перед добавлением к реакционной среде. Получение указанного аниона хорошо известно в данной области. Например, когда Т является кислородом,анион Rz2-T-H легко образуется при обработке Rz2-T-H основанием, таким как гидрид натрия. Затем этот кислородный анион может быть объединен с соединением формулы IV с образованием соединения формулы III. В соответствии с другим вариантом осуществления описанные здесь реакции проводят при температуре, меньшей или равной температуре дефлегмации реакционной среды. В соответствии с другим вариантом осуществления указанная реакционная среда имеет температуру, меньшую, чем точка кипения указанного подходящего растворителя, или температуру, достигаемую при дефлегмации указанного подходящего растворителя в указанной реакционной среде. В другом варианте осуществления указанная реакционная среда имеет температуру между приблизительно 0 и приблизительно 190 С. В соответствии с еще одним вариантом осуществления указанная реакционная среда имеет температуру между прибли- 11015990 зительно 40 и приблизительно 120 С. В соответствии с другим аспектом данного изобретения указанная реакционная среда имеет температуру между приблизительно 70 и приблизительно 115 С. В данном контексте будут применяться следующие определения, если нет других указаний. Термин "Aurora" относится к любой изоформе семейства Aurora протеинкиназ, в том числе Aurora1, Aurora-2 и Aurora-3. Термин "Aurora" относится также к изоформам семейства Aurora протеинкиназ,известных как Aurora-A, Aurora-B и Aurora-C. Фраза "необязательно замещенный" используется здесь взаимозаменяемо с фразой "замещенный или незамещенный". Если нет других указаний, необязательно замещенная группа может иметь заместитель в каждом замещаемом положении этой группы, и каждое замещение является независимым от другого. Термин "алифатическая" или "алифатическая группа" в данном контексте обозначает прямую или разветвленную С 1-С 8 углеводородную цепь, которая является полностью насыщенной или которая содержит одно или несколько ненасыщенных звеньев, или моноциклический С 3-С 8 углеводород, или бициклический С 8-С 12 углеводород, который является полностью насыщенным или который содержит одно или несколько ненасыщенных звеньев, но который не является ароматическим (также называемый "карбоциклом" или "циклоалкилом"), который имеет единственную точку присоединения к остальной молекуле, где любое индивидуальное кольцо в указанной бициклической кольцевой системе состоит из 3-7 членов. Например, подходящие алифатические группы включают в себя, но не ограничиваются ими, линейные или разветвленные алкильную, алкенильную, алкинильную группы и их гибриды, такие как(циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил. Термины "алкил", "алкокси", "гидроксиалкил", "алкоксиалкил" и "алкоксикарбонил", используемые отдельно или в виде части большего радикала, включают в себя как прямые, так и разветвленные цепи,содержащие 1-12 атомов углерода. Термины "алкенил" и "алкинил", используемые отдельно или в виде части большего радикала, будут включать в себя как прямые, так и разветвленные цепи, содержащие от 2 до 12 атомов углерода. Термин "гетероатом" обозначает азот, кислород или серу и включает в себя любую окисленную форму азота и серы и кватернизованную форму любого основного азота. Термин "азот" включает в себя также замещаемый азот гетероциклического кольца. Например, в насыщенном или частично ненасыщенном кольце, имеющем 0-3 гетероатома, выбранных из кислорода, серы или азота, этот азот может быть N(как в 3,4-дигидро-3 Н-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле). Термин "арил" или "арильное кольцо" обозначает моноциклические, бициклические или трициклические кольцевые системы, имеющие в целом от 5 до 14 кольцевых атомов углерода, где по меньшей мере одно кольцо является ароматическим и где каждое кольцо в этой системе содержит от 3 до 7 членов кольца. Термин "арил" может быть использован взаимозаменяемо с термином "арильное кольцо". Примеры включают в себя фенил, инданил, 1-нафтил, 2-нафтил, 1-антрацил, 2-антрацил и бицикло[2.2.2]окт 3-ил. Более предпочтительные размеры колец для арильных колец приведены ниже для различных предпочтительных вариантов соединений формулы I. Термин "арил", используемый отдельно или в виде части большего радикала, как в "аралкиле","аралкокси" или "арилоксиалкиле", обозначает моноциклические, бициклические или трициклические кольцевые системы, имеющие в целом от 5 до 14 членов кольца, где по меньшей мере одно кольцо в этой системе является ароматическим и где каждое кольцо в этой системе состоит из 3-7 членов кольца. Термин "арил" может быть использован взаимозаменяемо с термином "арильное кольцо". Термин "арил" относится также к гетероарильным кольцевым системам, определенным ниже. Термин "гетероцикл", "гетероциклил" или "гетероциклический" в данном контексте обозначает неароматические, моноциклические, бициклические или трициклические системы, имеющие от 5 до 14 членов кольца, в которых один или несколько членов кольца являются гетероатомами, где каждое кольцо в этой системе содержит 3-7 членов кольца. Термин "гетероарил", используемый отдельно или в виде части большего радикала, как в "гетероаралкиле" или "гетероарилалкокси", обозначает моноциклические, бициклические и трициклические кольцевые системы, имеющие от 5 до 14 членов кольца, где по меньшей мере одно кольцо в этой системе является ароматическим, по меньшей мере одно кольцо в этой системе содержит один или несколько гетероатомов и где каждое кольцо в этой системе состоит из 3-7 членов кольца. Термин "гетероарил" может быть использован взаимозаменяемо с термином "гетероарильное кольцо" или с термином "гетероароматический". Арильная (в том числе аралкильная, аралкокси, арилоксиалкильная и т.п.) или гетероарильная (в том числе гетероаралкильная и гетероарилалкокси и т.п.) группа может содержать один или несколько заместителей. Подходящие заместители ненасыщенного атома углерода арильной, гетероарильной, аралкильной или гетероаралкильной группы выбраны из галогена, -R, -OR, -SR, 1,2-метилендиокси, 1,2 этилендиокси, фенила (Ph), необязательно замещенного R, -O(Ph), необязательно замещенного R,-CH2(Ph), необязательно замещенного R, -CH2CH2(Ph), необязательно замещенного R, -NO2, -CN,- 12015990R независимо выбран из водорода, необязательно замещенной C1-6 алифатической группы, незамещеннного 5-6-членного гетероарильного или гетероциклического кольца, фенила, -O(Ph) или СН 2(Ph). Необязательные заместители на алифатической группе R выбраны из NH2, NH(C1-4 алифатической группы),N(C1-4 алифатической группы)2, галогена, C1-4 алифатической группы, ОН, O(C1-4 алифатической группы),NO2, CN, CO2H, CO2(C1-4 алифатической группы), О(галоген C1-4 алифатической группы) или галоген(C1-4 алифатической группы). Алифатическая группа или неароматическое гетероциклическое кольцо могут содержать один или несколько заместителей. Подходящие заместители насыщенного углерода алифатической группы или неароматического гетероциклического кольца выбраны из заместителей, перечисленных выше для ненасыщенного углерода арильной или гетероарильной группы, и следующих: =O, =S,=NNHR, =NN(R)2, =NNHC(O)R, =NNHCO2(алкила), =NNHSO2(алкила) или =NR, где каждый R независимо выбран из водорода или необязательно замещенной C1-6 алифатической группы. Необязательные заместители алифатической группы R выбраны из NH2, NH(C1-4 алифатической группы), N(C1-4 алифатической группы)2, галогена, C1-4 алифатической группы, ОН, O(C1-4 алифатической группы) NO2,CN, СО 2 Н, CO2(C1-4 алифатической группы), О(галоген C1-4 алифатической группы) или галоген (C1-4 алифатической группы). Необязательные заместители азота неароматического гетероциклического кольца выбраны из -R+,+-CH2(Ph), необязательно замещенный -CH2CH2(Ph) или незамещенное 5-6-членное гетероарильное или гетероциклическое кольцо. Необязательные заместители алифатической группы или фенильного кольцаR+ выбраны из NH2, NH(C1-4 алифатической группы), N(C1-4 алифатической группы)2, галогена, C1-4 алифатической группы, ОН, O(C1-4 алифатической группы) NO2, CN, CO2H, CO2(C1-4 алифатической группы),О(галоген C1-4 алифатической группы) или галоген(C1-4 алифатической группы). Термин "алкилиденовая цепь" обозначает прямую или разветвленную углеродную цепь, которая может быть полностью насыщенной или иметь одно или несколько ненасыщенных звеньев и имеет две точки присоединения к остальной части молекулы. Комбинация заместителей или переменных является допустимой только в том случае, если такая комбинация приводит к стабильному или химически возможному соединению. Стабильным соединением или химически возможным соединением является соединение, которое, по существу, не изменяется при хранении при температуре 40 С или менее, в отсутствие влаги или других химически реакционноспособных условий, в течение по меньшей мере недели. Обычному специалисту в данной области понятно, что некоторые соединения данного изобретения могут существовать в таутомерных формах, причем все такие таутомерные формы находятся в рамках данного изобретения. Если нет других указаний, предполагается, что структуры, изображенные здесь, включают в себя все стереохимические формы такой структуры; т.е. R- и S-конфигурации для каждого асимметричного центра. Таким образом, как отдельные стереохимические изомеры, так и энантиомерные и диастереомерные смеси данных соединений входят в рамках данного изобретения. Если нет других указаний,предполагается, что структуры, изображенные здесь, включают в себя соединения, которые отличаются только присутствием одного или нескольких изотопно обогащенных атомов. Например, соединения,имеющие приведенные структуры, за исключением замены водорода дейтерием или тритием, или замены углерода обогащенным 13 С- или 14 С-углеродом, входят в объем данного изобретения. Такие соединения могут использоваться, например, в качестве аналитических инструментов или зондов в биологических анализах. Для более полного понимания описанного здесь изобретения приводятся следующие примеры. Следует учесть, что эти примеры приведены только для иллюстративных целей и не должны рассматриваться как ограничивающие каким-либо образом данное изобретение. Пример 1. 4,6-Дихлорпиримидин-2-метилсульфон (А), полученный способами, по существу, одинаковыми со способами, приведенными в Koppel et al., JOC, 26, 1961, 792, следующим образом. К перемешиваемому раствору 4,6-дихлор-2-(метилтио)пиримидина (50 г, 0,26 моль) в дихлорметане (1 л) при 0 С добавляли метахлорпероксибензойную кислоту (143,6 г, 0,64 моль) в течение 20 мин. Раствору давали нагреться до комнатной температуры и перемешивали в течение 4 ч. Смесь разбавляли дихлорметаном(1,5 л) и затем обрабатывали последовательно 50% раствором Na2S2O3/NaHCO3 (2200 мл), насыщенным раствором NaHCO3 (4300 мл) и солевым раствором (200 мл), затем сушили (MgSO4). Растворитель удаляли в вакууме с получением твердого вещества не совсем белого цвета, которое вновь растворяли вEtOAC (1 л) и обрабатывали последовательно насыщенным водным раствором NaHCO3 (3300 мл) и солевым раствором (100 мл), затем сушили (MgSO4). Растворитель удаляли в вакууме с получением указанного в заголовке соединения (А) в виде белого твердого вещества (55,6 г, выход 96%). 1(С). Суспензию соединения А (10 г, 44,04 ммоль) и (4-меркаптофенил)амид циклопропанкарбоновой кислоты (В, 8,51 г, 44,04 ммоль) в трет-бутаноле (300 мл) дегазировали откачиванием воздуха с последующей продувкой азотом. Смесь перемешивали при 90 С в атмосфере азота в течение 1 ч, затем растворитель удаляли в вакууме. Остаток растворяли в этилацетате (600 мл) и промывали водным раствором карбоната калия и хлорида натрия. Органический экстракт сушили над сульфатом магния, концентрировали до малого объема и давали кристаллизоваться. Продукт С собирали в виде бесцветных кристаллов (11,15 г, 74%). 1 Н-ЯМР ДМСО-d6,0,82-0,89 (4 Н, м), 1,80-1,88 (1 Н, м), 7,55 (2 Н, д), 7,70-7,76 (3 Н, м), 10,49 (1 Н, с); М+Н, 340. Пример 3. 4-[4-Хлор-6-(5-метил-2 Н-пиразол-3-иламино)пиримидин-2-илсульфанил]фениламид циклопропанкарбоновой кислоты (D). Смесь соединения С (1,0 г, 2,94 ммоль) и 3-амино-5-метилпиразола (314 мг, 3,23 ммоль) в диметилформамиде (6 мл) обрабатывали диизопропилэтиламином (0,614 мл, 3,53 ммоль) и йодидом натрия (530 мг, 3,53 ммоль). Смесь перемешивали в атмосфере азота при 85 С в течение 4 ч, охлаждали до комнатной температуры и разбавляли этилацетатом. Раствор промывали водой (4), сушили над сульфатом магния и концентрировали до 5 мл с получением после кристаллизации и сбора бесцветных кристаллов указанного в заголовке соединения D (920 мг, 78%). 1 Н-ЯМР ДМСО-d6,0,80-0,87 (4 Н, м), 1,77-1,85 (1 Н, м), 1,92 (1 Н, с), 5,24 (1 Н, шир.с), 6,47 (1 Н,шир.с), 7,55 (2 Н, д), 7,70-7,80 (2 Н, м), 10,24 (1 Н, с), 10,47 (1 Н, с), 11,92 (1 Н, с). Пример 4. 4-[4-(4-Метилпиперазин-1-ил)-6-(5-метил-2 Н-пиразол-3-иламино)пиримидин-2-илсульфанил]фениламид циклопропанкарбоновой кислоты (V-1). Соединение D (2,373 г, 5,92 ммоль) обрабатывали N-метилпиперазином (10 мл) и смесь перемешивали при 110 С в течение 2 ч. Избыток N-метилпиперазина удаляли в вакууме, затем остаток растворяли в этилацетате, промывали водным раствором бикарбоната натрия, сушили над сульфатом магния и концентрировали. Остаток кристаллизовали из метанола с получением бесцветных кристаллов желаемого продукта V-1 (1,82 г, 66%). 1 Н-ЯМР ДМСО-d6,0,81 (4 Н, д), 1,79 (1 Н, м), 2,01 (3 Н, с), 2,18 (3 Н, с), 2,30 (4 Н, м), 3,35 (маскированный сигнал), 5,42 (1 Н, с), 6,02 (1 Н, шир.с), 7,47 (2 Н, д), 7,69 (2 Н, д), 9,22 (1 Н, с), 10,39 (1 Н, с), 11,69N-4-[4-(5-Метил-2 Н-пиразол-3-илметил)-6-(4-пропилпиперазин-1-ил)пиримидин-2-илсульфанил] фенилпропионамид (V-5). 4-[4-Хлор-6-(5-метил-2 Н-пиразол-3-иламино)пиримидин-2-илсульфанил]фениламид этанкарбоновой кислоты (119 мг, 0,306 ммоль), полученный способами, аналогичными способам, приведенным в примерах 1, 2 и 3, в н-BuOH (5 мл) обрабатывали дигидробромидом N-пропилпиперазина (887 мг, 3,06 ммоль), затем диизопропилэтиламином (1,066 мл, 6,12 ммоль). Полученную смесь перемешивали при 110 С в течение 20 ч. Растворитель удаляли при пониженном давлении и остаток очищали с использованием препаративной ВЭЖХ с получением указанного в заголовке соединения. 1N-[4-(4,6-Дихлорпиримидин-2-илокси)фенил]ацетамид. Раствор 4-ацетамидофенола (666 мг, 4,40 ммоль) в безводном ТГФ (40 мл), перемешивающийся при температуре окружающей среды, обрабатывали 60% дисперсией гидрида натрия в минеральном масле(176 мг, 4,40 ммоль). Затем реакционной смеси давали перемешиваться в течение 30 мин при температуре окружающей среды и добавляли 4,6-дихлор-2-метансульфонилпиримидин (1,0 г, 4,40 ммоль). Затем реакционную смесь перемешивали в течение еще 3 ч и разбавляли реакционную смесь насыщенным водным раствором NH4Cl и EtOAC. Органический слой отделяли, промывали насыщенным водным раствором NaCl и сушили над сульфатом натрия и затем концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, MeOH:CH2Cl2, 5:95) с получением указанного в заголовке соединения 1,25 г (95%) в виде твердого вещества. 1H-ЯМР (400 МГц, ДМСО-d6):2,06 (3 Н, с), 7,18 (2 Н, д, J=8,5 Гц), 7,62 (2 Н, д, J=8,5 Гц), 10,05 (1 Н,с), LS-MC: ES+=298,16, ES-=296,18). Пример 7. 4-[4-(4-Метил-4-оксипиперазин-1-ил)-6-(5-метил-2 Н-пиразол-3-иламино)пиримидин-2 илсульфанил]фениламид циклопропанкарбоновой кислоты (V-19). Соединение V-1 (1 г, 2,1 ммоль) суспендировали в дихлорметане (20 мл), охлаждали до 0 С и обрабатывали раствором дихлорметана в mCPBA в 10 аликвотах при 10-минутных интервалах (каждая аликвота состояла из 100 мг, 0,44 ммоль) в 1 мл ДХМ. Каждый раз при добавлении аликвоты этот раствор становился коричневым и постепенно возвращался к желтому цвету по мере расходования mCPBA. После расходования всего исходного материала растворитель удаляли в вакууме и полученное оранжевое масло очищали препаративной ВЭЖХ с получением указанного в заголовке соединения в виде твердого вещества не совсем белого цвета (69 мг, 7%). 1(1 Н, с), 11,82 (1 Н, шир.с). Пример 8. Метансульфонат 4-[4-(4-метилпиперазин-1-ил)-6-(5-метил-2 Н-пиразол-3-иламино)пиримидин-2-илсульфанил]фениламида циклопропанкарбоновой кислоты (V-1ii). Соединение V-1 (515 мг, 1,11 ммоль) суспендировали в этаноле (80 мл) и нагревали с обратным холодильником при кипичении. К прозрачному раствору добавляли метансульфоновую кислоту (106 мг,1,11 ммоль) и реакционную смесь нагревали с обратным холодильником при кипичении в течение еще 10 мин. Смеси давали остыть до комнатной температуры и растворитель выпаривали, пока не начинал образовываться осадок. Затем смесь охлаждали до 0 С и полученный осадок собирали фильтрацией и затем сушили в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества(2 Н, д), 9,61 (1 Н, с), 10,41 (1 Н, шир.с), 10,80 (1 Н, с). Пример 9. Следующие соединения, представленные в табл. 4 ниже, получали в соответствии со способами по данному изобретению и способами, по существу, одинаковыми с приведенными в примерах 1-8 выше. Данные, характеризующие эти соединения, суммированы в табл. 4 ниже и включают в себя 1 Н-ЯМР,точку плавления (т. пл.) и данные масс-спектрометрии (MS). Если нет других указаний, все представленные данные 1 Н-ЯМР, приведенные в табл. 4, были получены при 400 МГц в дейтерированном диметилсульфоксиде (ДМСО-d6). Таблица 4 Данные характеристики представительных соединений Биологические анализы Активность соединений по данному изобретению в качестве ингибиторов киназ может анализироваться in vitro, in vivo или в клеточной линии. Анализы in vitro включают в себя анализы, которые определяют ингибирование либо киназной активности, либо АТФ-азной активности активированного фермента Aurora и/или FLT-3. Другие анализы in vitro количественно определяют способность ингибитора связываться с Aurora и/или FLT-3 и могут быть измерены либо радиоактивным мечением ингибитора перед связыванием, выделением комплекса ингибитор/Aurora и/или ингибитор/FLT-3 и определением количества связанной радиоактивной метки, либо проведением конкурентного эксперимента, в котором новые соединения инкубируют с Aurora и/или FLT-3, связанными с известными радиоактивными лигандами. Можно использовать любой тип или любую изоформу Aurora, в зависимости от того, какой тип или какая изоформа должны быть ингибированы. Подробности используемых условий для этих анализов ферментов описаны в примерах ниже. Пример 10. Определение Ki для ингибирования Aurora. Соединения подвергали скринингу на их способность ингибировать Aurora с использованием стандартного ферментсвязанного анализа следующим образом (Fox et al. (1998) Proyein Sci 7, 2249). К исходного буферному раствору для анализа, содержащему 0,1 М HEPES 7,5, 10 мМ MgCl2, 1 мМ ДТТ, 25 мМNaCl, 2,5 мМ фосфоенолпируват, 3000 мМ НАДН, 30 мг/мл пируваткиназы, 10 мг/мл лактатдегидрогеназы, 40 мМ АТФ и 800 мкМ пептид (LRRASLG, American Peptide, Sunnyvale, СА) добавляли раствор в ДМСО соединения данного изобретения до конечной концентрации 30 мкМ. Полученную смесь инкубировали при 30 С в течение 10 мин. Реакцию инициировали добавлением 10 мкл исходного раствораAurora с получением конечной концентрации 70 нМ в этом анализе. Скорости реакции получали мониторингом оптической плотности при 340 нм в течение 5-минутного времени считывания результатов при 30 С с использованием планшет-ридера BioRad Ultramark (Hercules, СА). Величины Ki определяли из данных скорости как функцию концентрации ингибитора. Было обнаружено, что соединения формулы V данного изобретения являются ингибиторамиAurora-1, Aurora-2 и Aurora-3. Пример 11. Определение Ki для ингибирования FLT-3. Соединения подвергали скринингу на их способность ингибировать активность FLT-3 с использованием радиометрического анализа связывания на фильтре. Этот анализ выполняет мониторинг включе- 28015990 ния 33 Р в субстрат поли(Glu,Tyr)4:1 (pE4Y). Реакции проводили в растворе, содержащем 100 мМ HEPES(рН 7,5), 10 мМ MgCl2, 25 мМ NaCl, 1 мМ ДТТ, 0,01% БСА и 2,5% ДМСО. Конечные концентрации субстрата в этом анализе были 90 мкМ АТФ и 0,5 мг/мл pE4Y (оба из Sigma Chemicals, St Louis, МО). Конечная концентрация соединения данного изобретения обычно была между 0,01 и 5 мкМ. Обычно проводили титрование с 12 точками приготовлением серийных разведений из исходного ДМСО-раствора тест-соединения. Реакции проводили при комнатной температуре. Готовили два раствора для анализа. Раствор 1 содержит 100 мМ HEPES (рН 7,5), 10 мМ MgCl2, 25 мМ NaCl, 1 мг/мл pE4Y и 180 мкМ АТФ (содержащий 0,3 мкКи [-33 Р]АТФ для каждой реакции). Раствор 2 содержит 100 мМ HEPES (рН 7,5), 10 мМ MgCl2, 25 мМ NaCl, 2 мМ ДТТ, 0,02% БСА и 3 нМ FLT-3. Анализ проводили на 96-луночном планшете смешиванием 50 мкл каждого из раствора 1 и 2,5 мл соединения данного изобретения. Реакцию инициировали раствором 2. После инкубирования в течение 20 мин при комнатной температуре реакцию останавливали 50 мкл 20% ТХУ, содержащей 0,4 мМ АТФ. Затем весь объем реакции переносили на фильтрующий планшет и промывали 5% ТХУ с использованием харвестера 9600 из ТОМТЕС (Hamden, СТ). Количество включения 33 Р в pE4Y анализировали сцинтилляционным счетчиком для счета в микропланшетах Packard Top Count Microplate Scintillation Counter(Meriden, СТ). Данные строили с использованием программы Prism с получением IC50 или Ki. Было обнаружено, что соединения формулы V данного изобретения являются ингибиторами FLT-3. Пример 12. Определение IC50 для ингибирования Aurora в анализе с клетками Colo205. Соединения анализировали также на ингибирование пролиферации клеток. В этом анализе полную среду готовили добавлением 10% фетальной бычьей сыворотки, L-глутамина и раствора пенициллина/стрептомицина к среде RPMI 1640 (Sigma). Клетки рака ободочной кишки (клеточной линии COLO205) добавляли в 96-луночный планшет при плотности посева 1,25104 клеток/лунка/150 мкл. Раствор тест-соединения готовили в полной среде серийным разведением, тест-соединение (50 мкл) добавляли в каждую лунку. Каждый планшет содержал ряд лунок, в которые добавляли только полную среду (200 мкл), для образования контрольной группы для измерения максимальной пролиферации. Контрольную группу с носителем также добавляли на каждом планшете. Планшеты инкубировали при 37 С в течение 2 дней. Исходный раствор 3 Н-тимидина (1 мКи/мл, Amersham Pharmacia UK) разбавляли до 20 мкКи/мл в средеRPMI 1640, затем 25 мкл этого раствора добавляли в каждую лунку. Планшеты инкубировали дополнительно при 37 С в течение 3 ч и анализировали на поглощение 3 Н-тимидина с использованием жидкостного сцинтилляционного счетчика. Было обнаружено, что соединения формулы V являются ингибиторами пролиферации раковых клеток Colo205. Пример 13. Измерение пролиферации клеток в панели опухолевых и нормальных типов клеток: анализ включения 3 Н-тимидина. Анализ включения 3 Н-тимидина был выбран в качестве хорошо охарактеризованного способа определения пролиферации клеток. Клетки из нормальных тканей и большое разнообразие различных типов опухолей были выбраны для анализа. Многие опухолевые клетки были выбраны потому, что они экспрессируют высокие уровни белков Aurora (например, MCF-7, PC3, А 375, А 549) (см. раздел 5.3.5 и Bischoff et al. EMBO J. 1998, 17,3052-3065) и/или способны образовывать опухоли в голых мышах или крысах (например, НСТ 116, MCF7 и MDA-MB-231). Логарифмически растущие клетки инкубировали с соединением в течение 96 ч. Для измерения пролиферации клеток за 3 ч перед окончанием этого эксперимента в каждую лунку добавляли 0,5 мкКи 3 Нтимидина. Затем клетки собирали, промывали и включенную радиоактивность считали на -счетчике для микропланшетов Wallac. Для определения ингибирования пролиферации, имп/мин строили в зависимости от концентрации соединения и определяли графически IC50. В табл. 5 ниже представлены клеточные линии, использованные в описанном выше анализе пролиферации клеток. Для каждой клеточной линии определяли ингибирование пролиферации клеток и включение 3 Н-тимидина (временная точка 96 ч).
МПК / Метки
МПК: C07D 401/14, C07D 403/14, C07D 403/12, A61K 31/506
Метки: способы, замещенных, пиримидинов, получения
Код ссылки
<a href="https://eas.patents.su/30-15990-sposoby-polucheniya-zameshhennyh-pirimidinov.html" rel="bookmark" title="База патентов Евразийского Союза">Способы получения замещенных пиримидинов</a>
Предыдущий патент: Лечение воспалительного заболевания кишечника
Следующий патент: Закрепленные на матрице пептидомиметики
Случайный патент: Энтомопатогенный препарат против личинок комаров на основештамма bacillus thuringiensis var. israelensis h-14 вкпм в-7572