Новый способ получения пиперазинильных производных бензамида
Номер патента: 14905
Опубликовано: 28.02.2011
Авторы: Ческо-Канчиан Серджио, Рейес Майра Б., Мани Неелакандха С., Палмер Дэвид К., Пандит Ченнагири Р., Сяо Тонг
Формула / Реферат
1. Способ получения соединения формулы (I)
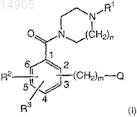
и его фармацевтически приемлемых солей, сложных эфиров, таутомеров, сольватов или амидов,
где R1выбирают из группы, состоящей из C1-10-алкила, С3-8-алкенила, С3-8-циклоалкила, (С3-8-циклоалкил)-С1-6-алкила, (С3-8-циклоалкил)-С3-8-алкенила и (C1-8-алкилкарбонил)-C1-8-алкила;
n означает целое число от 1 до 2;
R2 и R3, каждый, независимо выбирают из группы, состоящей из водорода, фтора, хлора, брома, нитро, трифторметила, метила или C1-3-алкокси;
m означает целое число от 1 до 7;
Q означает NR8R9;
где R8выбирают из группы, состоящей из водорода, C1-6-алкила, С3-6-алкенила, 3-9-членного карбоциклила, 3-12-членного гетероциклила, фенила, (6-9-членный гетероциклил)-C1-6-алкилена и (фенил)-C1-6-алкилена;
R9 выбирают из группы, состоящей из C1-6-алкила, С3-6-алкенила, 6-9-членного карбоциклила, 3-12-членного гетероциклила, фенила, (6-9-членный гетероциклил)-C1-6-алкилена и (фенил)-C1-6-алкилена;
альтернативно, Q представляет собой насыщенный 3-12-членный N-связанный гетероциклил, где в дополнение к N-связывающему атому азота 3-12-членный гетероциклил необязательно может содержать 1-3 дополнительных гетероатома, независимо выбираемых из О, S и NH;
Q (когда Q представляет собой насыщенный 3-12-членный N-связанный гетероциклил) необязательно замещен 1-3 заместителями, независимо выбираемыми из группы, состоящей из гидрокси, галогена, карбоксамида, C1-6-алкила, 5-9-членного или 6-9-членного гетероциклила, -N-(C1-6-алкил)(5-9-членного или 6-9-членного гетероциклила), -NH-(5-9-членного или 6-9-членного гетероциклила), -О-(5-9- или 6-9-членного гетероциклила), (5-9-членный или 6-9-членный гетероциклил)-C1-3-алкилена, C1-6-алкокси, (С3-6-циклоалкил)-O-, фенила, (фенил)-C1-3-алкилена и (фенил)-C1-3-алкилен-О-;
каждая из вышеуказанных гетероциклильных, фенильных и алкильных групп может быть далее необязательно замещена 1-3 заместителями, независимо выбираемыми из группы, состоящей из трифторметила, метокси, галогена, нитро, циано, гидрокси и C1-3-алкила;
при условии, что 5 и 6 положения в фенильном цикле не замещены;
далее, при условии, что когда R1 означает метил, то -(CH2)m-Q не означает пиперидин-1-илметил;
каждая из вышеуказанных алкильных, алкиленовых, алкенильных, гетероциклильных, циклоалкильных, карбоциклильных и арильных групп может быть независимо и необязательно замещена 1-3 заместителями, независимо выбираемыми из группы, состоящей из трифторметила, метокси, галогена, амино, нитро, гидрокси и C1-3-алкила;
включающий
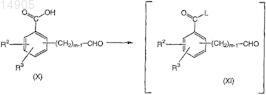
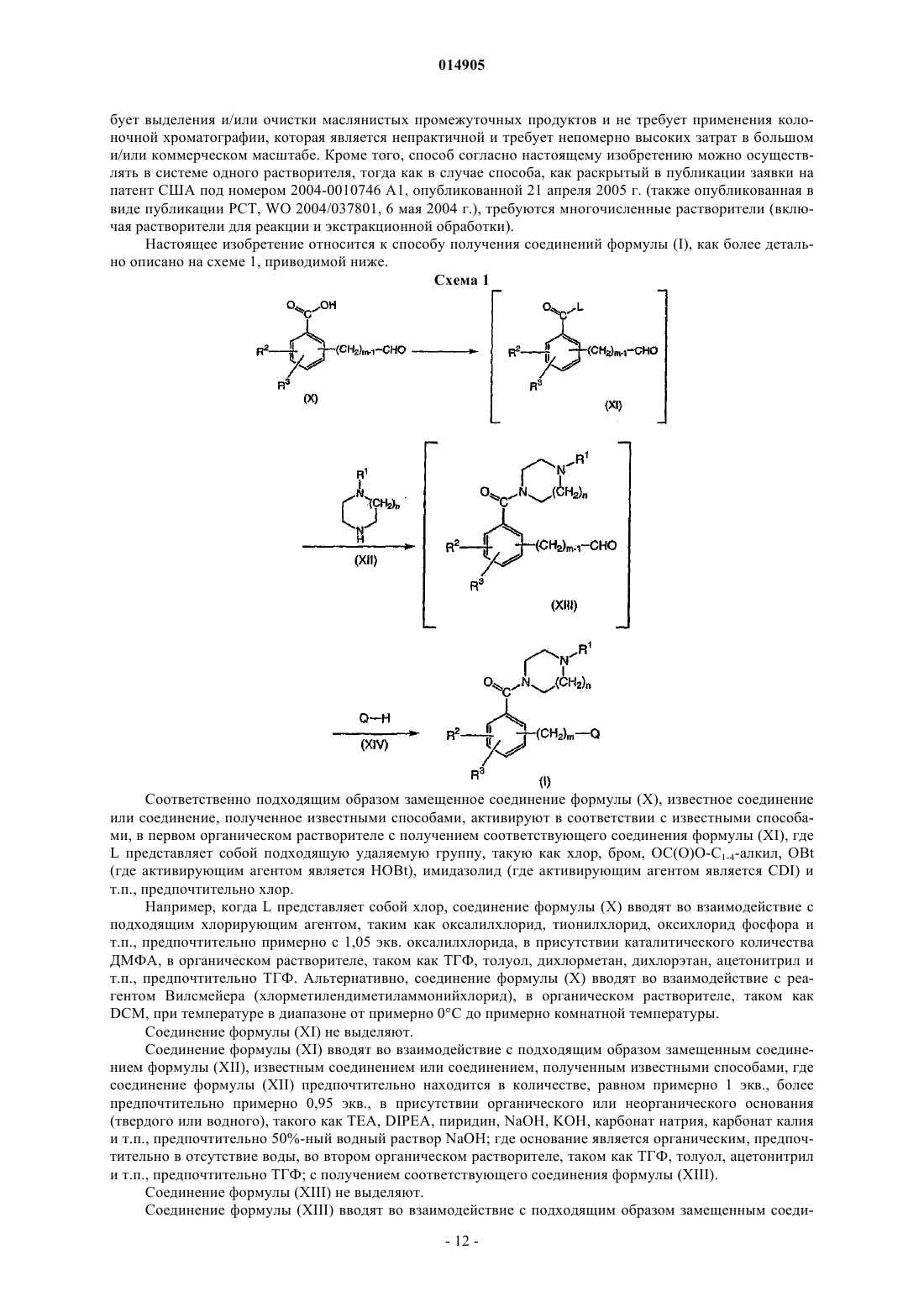
введение во взаимодействие соединения формулы (X) в первом органическом растворителе с получением соответствующего соединения формулы (XI), где L представляет собой удаляемую группу и соединение формулы (XI) не выделяют;
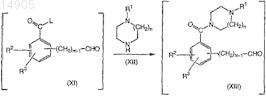
введение во взаимодействие соединения формулы (XI) с соединением формулы (XII) в присутствии органического или неорганического основания во втором органическом растворителе с получением соответствующего соединения формулы (XIII), где соединение формулы (XIII) не выделяют;
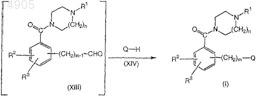
и введение во взаимодействие соединения формулы (XIII) с соединением формулы (XIV) в присутствии восстановителя в третьем органическом растворителе с получением соответствующего соединения формулы (I).
2. Способ по п.1, где первый органический растворитель, второй органический растворитель и третий органический растворитель являются одинаковыми.
3. Способ по п.1, где L означает хлор.
4. Способ по п.1, включающий далее введение во взаимодействие соединения формулы (I) с получением соответствующей фармацевтически приемлемой соли соединения формулы (I).
5. Способ по п.4, где фармацевтически приемлемую соль выбирают из группы, состоящей из сукцината, фумарата, малеата, гидрохлорида или гидробромида.
6. Способ по п.1, где соединением формулы (I) является соединение формулы (Ia)
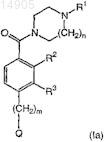
или его энантиомер, диастереомер, гидрат, сольват или фармацевтически приемлемая соль, сложный эфир или амид.
7. Способ по п.1, где R1 означает изопропил, n означает 1, R2означает водород, R3 означает водород и R4 означает 4-морфолинилметил.
8. Способ получения соединения формулы (Is)
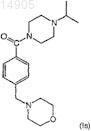
или его энантиомера, диастереомера, гидрата, сольвата или фармацевтически приемлемой соли, сложного эфира или амида,
включающий
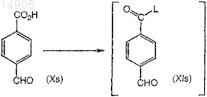
введение во взаимодействие соединения формулы (Xs) в первом органическом растворителе с получением соответствующего соединения формулы (XIs), где L представляет собой удаляемую группу и соединение формулы (XIs) не выделяют;
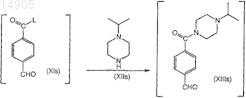
введение во взаимодействие соединения формулы (XIs) с соединением формулы (XIIs) в присутствии органического или неорганического основания во втором органическом растворителе с получением соответствующего соединения формулы (XIIIs), где соединение формулы (XIIIs) не выделяют;
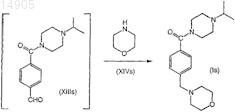
и введение во взаимодействие соединения формулы (XIIIs) с соединением формулы (XIVs) в присутствии восстановителя в третьем органическом растворителе с получением соответствующего соединения формулы (Is).
9. Способ по п.8, где первый органический растворитель, второй органический растворитель и третий органический растворитель являются одинаковыми.
10. Способ по п.8, где L означает хлор.
11. Способ по п.8, где соединение формулы (XIIs) находится в количестве, равном примерно 1 экв.
12. Способ по п.8, где соединение формулы (XIVs) находится в количестве более чем примерно 1 экв. и восстановитель находится в количестве в диапазоне от примерно 1 до примерно 2 экв.
13. Способ по п.8, включающий далее введение во взаимодействие соединения формулы (Is) с получением соответствующей фармацевтически приемлемой соли соединения формулы (Is).
14. Способ по п.13, где фармацевтически приемлемую соль выбирают из группы, состоящей из сукцината, фумарата, малеата, гидрохлорида или гидробромида.
15. Способ по п.13, где фармацевтически приемлемой солью является моносукцинат.
Текст
НОВЫЙ СПОСОБ ПОЛУЧЕНИЯ ПИПЕРАЗИНИЛЬНЫХ ПРОИЗВОДНЫХ БЕНЗАМИДА Настоящее изобретение относится к новому способу получения замещенных пиперазинильных бензамидов, пригодных для лечения нарушений и состояний, опосредуемых рецептором гистамина. 014905 Область техники, к которой относится изобретение Настоящее изобретение относится к способам получения пиперазинильных производных бензамида, пригодных для лечения нарушений и состояний, опосредуемых рецептором гистамина. Предпосылки создания изобретения В публикации заявки на патент США под номером 2004-0110746 А 1, опубликованной 21 апреля 2005 г. (также опубликованная в виде публикации РСТ, WO 04/037801, 6 мая 2004 г.), которая включена в данный контекст путем ссылки, раскрываются новые пиперазинильные и диазепанильные производные бензамида, пригодные для лечения нарушений, опосредуемых рецептором гистамина. В особенности,соединения пригодны для лечения нарушений и состояний, опосредуемых H3-рецептором. Более конкретно, соединения пригодны для лечения или предупреждения неврологических нарушений, включая нарушения сон/бодрствование и нарушения возбуждение/бессонница (например, инсомния и нарушение суточного ритма организма), нарушения гиперактивности в отношении дефицита внимания (ADHD),нарушения в отношении обучения и запоминания, когнитивную дисфункцию, мигрень, нейрогенное воспаление, деменцию, легкое когнитивное ухудшение (преддеменция), болезнь Альцгеймера, эпилепсию,нарколепсию, нарушения аппетита, ожирение, морскую болезнь, головокружение, шизофрению, злоупотребление веществом, биполярные нарушения, маниакальные расстройства и депрессию, а также другие нарушения, опосредуемые H3-рецептором гистамина, такие как аллергический ответ верхних дыхательных путей, астма, зуд, закупорка носового канала и аллергический ринит, в случае субъекта, нуждающегося в этом; например, способы предупреждения, ингибирования прогрессирования или лечения аллергического ответа верхних дыхательных путей, астмы, зуда, закупорки носового канала и аллергического ринита. В публикации заявки на патент США под номером 2004-0110746 А 1, опубликованной 21 апреля 2005 г. (также опубликованная в виде публикации РСТ, WO 04/037801, 6 мая 2004 г.), раскрывается способ получения пиперазинил- и диазепанилбензамидов. Однако остается необходимость в способах получения пиперазинильных и диазепанильных производных бензамида, которые пригодны для крупномасштабных/коммерческих применений. Краткое изложение сущности изобретения Настоящее изобретение относится к способу получения соединений формулы (I) и их фармацевтически приемлемых солей, сложных эфиров, таутомеров, сольватов или амидов; где R1 выбирают из группы, состоящей из C1-10-алкила, C3-8-алкенила, C3-8-циклоалкила, (C3-8 циклоалкил)-C1-6-алкила, (C3-8-циклоалкил)-С 3-8-алкенила и (C1-8-алкилкарбонил)-C1-8-алкила;n означает целое число от 1 до 2;R2 и R3, каждый, независимо выбирают из группы, состоящей из водорода, фтора, хлора, брома,нитро, трифторметила, метила или C1-3-алкокси;m означает целое число от 1 до 7 (предпочтительно m означает целое число от 1 до 4, более предпочтительно m означает 1);R9 выбирают из группы, состоящей из C1-6-алкила, С 3-6-алкенила, 6-9-членного карбоциклила, 3-12 членного гетероциклила (предпочтительно 5-9- или 5-8-членный гетероциклил), фенила, (6-9-членный гетероциклил)-С 1-6-алкилена и (фенил)-C1-6-алкилена; альтернативно, Q представляет собой насыщенный 3-12-членный N-связанный гетероциклил, где в дополнение к N-связывающему атому азота 3-12-членный гетероциклил необязательно может содержать 1-3 дополнительных гетероатома, независимо выбираемых из О, S и NH; где Q (когда Q представляет собой насыщенный 3-12-членный N-связанный гетероциклил) необязательно замещен 1-3 заместителями, независимо выбираемыми из группы, состоящей из гидрокси, галогена, карбоксамида, C1-6-алкила, 5-9-членного или 6-9-членного гетероциклила, -N-(C1-6-алкил)(5-9 членного или 6-9-членного гетероциклила), -NH-(5-9-членного или 6-9-членного гетероциклила), -О-(59- или 6-9-членного гетероциклила), (5-9-членный или 6-9-членный гетероциклил)-C1-3-алкилена, C1-6 алкокси, (C3-6-циклоалкил)-O-, фенила, (фенил)-C1-3-алкилена и (фенил)-C1-3-алкилен-О-; каждая из вышеуказанных гетероциклильных, фенильных и алкильных групп может быть далее необязательно замещена 1-3 заместителями, независимо выбираемыми из группы, состоящей из трифторметила, метокси, галогена, нитро, циано, гидрокси и C1-3-алкила;-1 014905 при условии, что 5- и 6-е положения в фенильном цикле не замещены (т.е. R2, R3 и -(CH2)m-Q связаны с положениями 2, 3 и 4 фенильного цикла); далее, при условии, что когда R1 означает метил, то -(CH2)m-Q не означает пиперидин-1-илметил; и где каждая из вышеуказанных алкильных, алкиленовых, алкенильных, гетероциклильных, циклоалкильных, карбоциклильных и арильных групп может быть независимо и необязательно замещена 1-3 заместителями, независимо выбираемыми из группы, состоящей из трифторметила, метокси, галогена,амино, нитро, гидрокси и C1-3-алкила; включающему введение во взаимодействие соединения формулы (X) в первом органическом растворителе с получением соответствующего соединения формулы (XI), где L представляет собой удаляемую группу и соединение формулы (XI) не выделяют; введение во взаимодействие соединения формулы (XI) с соединением формулы (XII) в присутствии органического или неорганического основания во втором органическом растворителе с получением соответствующего соединения формулы (XIII), где соединение формулы (XIII) не выделяют; и введение во взаимодействие соединения формулы (XIII) с соединением формулы (XIV) в присутствии восстановителя в третьем органическом растворителе с получением соответствующего соединения формулы (I). В одном воплощении настоящее изобретение относится к способам получения соединений формулы (Ia) и их фармацевтически приемлемых солей, сложных эфиров, таутомеров, сольватов или амидов. В другом воплощении настоящее изобретение относится к способам получения соединения формулы (Is) также известного как (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанон, или его фармацевтически приемлемой соли, сложного эфира, таутомера, сольвата или амида. Настоящее изобретение далее относится к новым кристаллическим солям соединения формулы (I). В одном воплощении настоящее изобретение относится к малеату, сукцинату, фумарату, гидрохлориду или гидробромиду соединения формулы (I). В одном воплощении настоящее изобретение относится к новым кристаллическим солям соединения формулы (Is). В одном воплощении настоящее изобретение относится к малеату, сукцинату, фумарату, гидрохлориду или гидробромиду соединения формулы (Is). В другом воплощении настоящее изобретение относится к кристаллическому сукцинату соединения формулы (Is). В другом воплощении настоящее изобретение относится к кристаллическому моносукцинату соединения формулы (Is). Подробное описание данного изобретения Настоящее изобретение относится к способу получения соединений формулы (I) где n, R1, R2, R3, m и Q имеют значения, как описано в данном контексте,пригодных для лечения нарушений и состояний, модулируемых рецептором гистамина. Как используется в данном контексте, термин "Са-b" (где а и b являются целыми числами) относится к радикалу, содержащему от а до b атомов углерода включительно. Например, C1-3- означает радикал,содержащий 1, 2 или 3 атома углерода. Как используется в данном контексте, термин "гало" или "галоген" означает одновалентные радикалы хлора, брома, фтора и йода. Как используется в данном контексте, термин "алкил", используемый отдельно или как часть замещающей группы, включает линейные или разветвленные насыщенные углеродные цепи. Например, алкильные радикалы включают метил, этил, пропил, изопропил, бутил, изобутил, вторбутил, трет-бутил, пентил и т.п. За исключением иначе указанного, термин "низший", когда используется вместе с алкилом, означает состав углеродной цепи из 1-4 атомов углерода. Термин "алкилен" относится к двухвалентному углеводородному остатку, такому как метилен (-СН 2-), этилен (-СН 2-СН 2-) или пропилен (-СН 2 СН 2 СН 2-) и т.п. Как используется в данном контексте, термин "алкилен" относится к двухвалентной алкильной группе с линейной или разветвленной цепью. Подходящие примеры включают, но не ограничиваясь этим, метилен, этилен, н-пропилен и т.п. Как используется в данном контексте, за исключением иначе указанного, термин "алкенил" означает алкиленовую группу по меньшей мере с двумя атомами водорода, замененными пи-связью с образованием двойной связи "углерод-углерод", такую как пропенил, бутенил, пентенил и т.п. Там, где алкенильная группа означает R8 или R9, свободный радикал (место присоединения остатка к молекуле) представляет собой sp3-углерод, как проиллюстрировано с помощью аллила, и двойная связь или связи, следовательно, находятся, по меньшей мере, в альфа-положении (не бета-, гамма-положении и т.д.) к свободному радикалу. Как используется в данном контексте, термин "алкилиден" относится к насыщенному или ненасыщенному, с разветвленной, линейной цепью или циклическому двухвалентному углеводородному радикалу, получаемому путем удаления двух атомов водорода от одного и того же атома углерода исходного алкана, алкена или алкина. Центр двухвалентного радикала образует двойную связь с одним атомом остатка молекулы. Типичные алкилидены включают, но не ограничиваясь этим, этанилиден, пропилидены,такие как пропан-1-илиден, пропан-2-илиден, циклопропан-1-илиден, бутилидены, такие как бутан-1 илиден, бутан-2-илиден, 2-метилпропан-1-илиден, циклобутан-1-илиден и т.п. Как используется в данном контексте, за исключением иначе указанного, термин "алкокси" означа-3 014905 ет содержащий кислород простого эфира радикал вышеописанных, с линейной или разветвленной цепью алкильных групп, например метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и т.п. Как используется в данном контексте, за исключением иначе указанного, термин "циклоалкил" означает 3-8-членную, насыщенную, моноциклическую, карбоциклическую, циклическую структуру. Подходящие примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Как используется в данном контексте, за исключением иначе указанного, термин "циклоалкенил" означает 3-8-членную, частично ненасыщенную, моноциклическую, карбоциклическую, циклическую структуру, где циклическая структура содержит по меньшей мере одну двойную связь. Подходящие примеры включают циклогексенил, циклопентенил, циклогептенил, циклооктенил, циклогекс-1,3-диенил и т.п. Как используется в данном контексте, за исключением иначе указанного, термин "арил" относится к карбоциклическим ароматическим группам, таким как фенил, нафтил и т.п. Двухвалентные радикалы включают фенилен (-С 6 Н 4-), который представляет собой предпочтительно фен-1,4-диил, но также может означать фен-1,3-диил. Как используется в данном контексте, за исключением иначе указанного, термин "аралкил" означает любую алкильную группу, замещенную арильной группой, такой как фенил, нафтил и т.п. Примеры аралкилов включают бензил, фенетил и фенилпропил. Как используется в данном контексте, за исключением иначе указанного, термин "карбоциклил" означает любую циклическую группу, содержащую 3-12 атомов углерода и предпочтительно 6-9 атомов углерода, в цикле или циклах структуры, если карбоцикл является конденсированной или спиробициклической или трициклической группой. Карбоцикл может быть насыщенным, ненасыщенным, частично ненасыщенным или ароматическим. Примеры включают циклоалкил, циклоалкенил, циклоалкинил; отдельные примеры включают фенил, бензил, инданил и бифенил. Карбоцикл может иметь заместители, которые не являются атомами углерода или водорода, такие как гидрокси, галоген, галогенметил и т.п., как показано где-нибудь в другом месте данного контекста. Как используется в данном контексте, за исключением иначе указанного, термины "гетероцикл","гетероциклил" и "гетероцикло" означают 3-, 4-, 5-, 6-, 7- или 8-членную моноциклическую, 9- или 10 членную бициклическую либо 13- или 14-членную трициклическую циклическую структуру, содержащую по меньшей мере один гетероатомный остаток, выбираемый из группы, состоящей из NH, О, SO,SO2(C=O) и S, предпочтительно NH, О или S, необязательно содержащую 1-4 дополнительных гетероатомов в каждом цикле. В некоторых воплощениях гетероциклил содержит 1-3 или 1-2 дополнительных гетероатомов. За исключением иначе указанного, гетероциклил может быть насыщенным, частично ненасыщенным, ароматическим или частично ароматическим. Гетероциклильная группа может быть присоединена к любому гетероатому или атому углерода, что приводит в результате к созданию стабильной структуры. Типичные моноциклические гетероциклические группы могут включать пирролидинил, пирролил,индолил, пиразолил, оксетанил, пиразолинил, имидазолил, имидазолинил, имидазолидинил, оксазолил,оксазолидинил, изоксазолинил, изоксазолил, тиазолил, тиадиазолил, тиазолидинил, изотиазолил, изотиазолидинил, фурил, тетрагидрофурил, тиенил, оксадиазолил, пиперидинил, пиперазинил, 2 оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксазепинил, азепинил, гексагидроазепинил, 4-пиперидинил, пиридил, N-оксопиридил, пиразинил, пиримидинил, пиридазинил, тетрагидропиранил, тетрагидротиопиранил, тетрагидротиопиранилсульфон, морфолинил, тиоморфолинил, тиоморфолинилсульфоксид, тиоморфолинилсульфон, 1,3-диоксолан и тетрагидро-1,1-диоксотиенил, диоксанил, изотиазолидинил, тиетанил, тииранил, триазинил, триазолил, тетразолил, азетидинил и т.п. Например, когда Q представляетсобой насыщенный, 3-12-членный, N-связанный гетероциклил, Q обязательно содержит по меньшей мере один атом азота, и атомы углерода являются sp3 гибридизированными. Когда Q представляет собой конденсированный бициклический гетероциклил,атомы углерода цикла, связанные с L, являются sp3-гибридизированными при условии, что смежный цикл (и общие атомы углерода) может быть sp2-гибридизации, как, например, инданил, где один из атомов углерода заменен атомом азота. Вообще, типичные бициклические гетероциклилы включают бензтиазолил, бензоксазолил, бензоксазинил, бензотиенил, хинуклидинил, хинолинил, хинолинил-N-оксид, тетрагидроизохинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофурил, хромонил, кумаринил, циннолинил,хиноксалинил, индазолил, пирролопридил, фуропиридинил (такой как фуро 2,3-спиридинил, фуро 3,1bпиридинил или фуро 2,3-bпиридинил), дигидроизоиндолил, дигидрохиназолинил (такой как 3,4 дигидро-4-оксохиназолинил), тетрагидрохинолинил (такой как 1,2,3,4-тетрагидрохинолинил), тетрагидроизохинолинил (такой как 1,2,3,4-тетрагидроизохинолинил), бензизотиазолил, бензизоксазолил, бензодиазинил, бензофуразанил, бензотиопиранил, бензотиазолил, бензпиразолил, дигидробензофурил, дигидробензотиенил, дигидробензотиопиранил, дигидробензотиопиранилсульфон, дигидробензопиранил,индолинил, изоиндолил, тетрагидроиндазолил (такой как 4,5,6,7-тетрагидроиндазолил), изохроманил,изоиндолинил, нафтиридинил, фталазинил, пиперонил, пуринил, пуридопиридил, хиназолинил, тетра-4 014905 и т.д. гидрохинолинил, тиенофурил, тиенопиридил, тиенотиенил,Типичные трициклические гетероциклические группы включают акридинил, феноксазинил, феназинил, фенотиазинил, карбозолил, перминидинил, фенантролинил, карболинил, нафтотиенил, тиантренил и т.п. Предпочтительные гетероциклильные группы включают морфолинил, тиоморфолинил, пиперидинил, пиперазинил, пирролидинил, пиримидинил, пиридил, пирролил, имидазолил, оксазолил, изоксазолил, акридинил, азепинил, гексагидроазепинил, азетидинил, индолил, изоиндолил, тиазолил, тиадиазолил, хинолинил, изохинолинил, 1,2,3,4-тетрагидрохинолинил, 1,3,4-тригидроизохинолинил, 4,5,6,7 тетрагидроиндадолил, бензоксазинил, бензоксазолил, бензтиазолил, бензимидазолил, тетразолил, оксадиазолил,Как используется в данном контексте, за исключением иначе указанного, термины "гетероциклилалкил" или "гетероциклилалкилен" означают любую алкильную группу, замещенную гетероциклильной группой, где гетероциклилалкильная группа связана через алкильную часть с центральной частью молекулы. Подходящие примеры гетероциклилалкильных групп включают, но не ограничиваясь этим, пиперидинилметил, пирролидинилметил, пиперидинилэтил, пиперазинилметил, пирролилбутил, пиперидинилизобутил, пиридилметил, пиримидилэтил и т.п. Когда отдельная группа является "замещенной" (например, алкил, алкилен, циклоалкил, арил, гетероциклил, гетероарил), то группа может иметь один или более заместителей, предпочтительно 1-5 заместителей, более предпочтительно 1-3 заместителя, наиболее предпочтительно 1, 2 заместителя, независимо выбираемых из перечня заместителей. Подразумевают, что определение любого заместителя или переменной в конкретном положении в молекуле не зависит от его определений где-нибудь в другом месте этой молекулы. Подразумевают, что заместители и замещенные структуры в случае соединений согласно данному изобретению могут быть выбраны квалифицированным специалистом в данной области для получения соединений, которые химически стабильны и которые можно без труда синтезировать способами, известными в данной области,а также теми способами, которые указаны в данном контексте. Согласно стандартной номенклатуре, используемой на протяжении всего этого описания, концевая часть указываемой боковой цепи описывается первой, с последующей смежной функциональностью по отношению к месту присоединения. Таким образом, например, заместитель "фенил(алкил)амидо(алкил)" относится к группе формулы За исключением иначе указанного, положение в случае центрального фенильного цикла соединений формулы (I), с которым связаны замещающие группы R2, R3 и -(CH2)m-Q, должно быть определено, как пронумеровано в направлении по часовой стрелке вокруг фенильного цикла, начиная от атома углерода,с которым связана группа -С(О)-, как показано ниже В соединениях формулы (I) настоящего изобретения R2, R3 и -(CH2)m-Q могут быть связаны только с положениями 2, 3 и/или 4. Далее, 5- и 6-е положения не замещены. Таким образом, в соединениях формулы (I) положения, с которыми связаны R2, R3 и -(CH2)m-Q, могут быть такими, как перечислено ниже. Термин "субъект", как используется в данном контексте, относится к животному, предпочтительно к млекопитающему, более предпочтительно к человеку, который является объектом лечения, наблюдения или эксперимента.-5 014905 Термин "терапевтически эффективное количество", как используется в данном контексте, означает такое количество активного соединения или фармацевтического агента, которое вызывает биологический или медицинский ответ в тканевой системе животного или человека, т.е. искомый исследователем,ветеринаром, лечащим врачом или другим клиницистом, который включает предупреждение, ингибирование начала болезни или ослабление симптомов заболевания или нарушения, которое подвергают лечению. Как используется в данном контексте, подразумевают, что термин "композиция" включает продукт,содержащий указанные ингредиенты в указанных количествах, а также любой продукт, который образуется, прямо или непрямо, в результате комбинаций указанных ингредиентов в указанных количествах. Аббревиатуры, используемые в данном описании, частично в схемах и примерах, представляют собой следующее:XRD=дифракция рентгеновских лучей. Для предоставления более краткого описания, некоторые из количественных выражений, указанных в данном контексте, не ограничены термином "примерно". Подразумевают, что используют ли термин "примерно" однозначно или нет, любое количество, указанное в данном контексте, означает, что оно относится к реально полученному значению, и также означает, что оно относится к приблизительному соответствию такому полученному значению, что должно быть достаточно ясно квалифицированному специалисту в данной области, включая приближения, вызываемые экспериментальными условиями и/или условиями измерения, к такому полученному значению. Как используется в данном контексте, за исключением иначе указанного, термин "удаляемая группа" означает заряженный или незаряженный атом или группу, который(ую) удаляют во время реакции замещения или реакции обмена. Подходящие примеры включают, но не ограничиваясь этим, Br, Cl, имидазолил и т.п. Когда соединения согласно данному изобретению имеют по меньшей мере один хиральный центр,они могут соответственно существовать в виде энантиомеров. Когда соединения имеют два или более хиральных центров, они могут дополнительно существовать в виде диастереомеров. Подразумевают, что все такие изомеры и их смеси входят в рамки настоящего изобретения. Предпочтительно, что когда соединение находится в виде энантиомера, то энантиомер представлен в энантиомерном избытке более чем или равном примерно 80%, более предпочтительно в энантиомерном избытке более чем или равном примерно 90%, еще более предпочтительно в энантиомерном избытке более чем или равном примерно 95%, еще более предпочтительно в энантиомерном избытке более чем или равном примерно 98%, в высшей степени предпочтительно в энантиомерном избытке более чем или равном примерно 99%. Подобным образом, когда соединение находится в виде диастереомера, то диастереомер представлен в диастереомерном избытке более чем или равном примерно 80%, более предпочтительно в диастереомерном избытке более чем или равном примерно 90%, еще более предпочтительно в диастереомерном избытке более чем или равном примерно 95%, еще более предпочтительно в диастереомерном избытке более чем или равном примерно 98%, в высшей степени предпочтительно в диастереомерном избытке более чем или равном примерно 99%. Кроме того, некоторые из кристаллических форм соединений согласно настоящему изобретению могут существовать в виде полиморфов и подразумевают, что как таковые входят в рамки настоящего изобретения. В дополнение, некоторые из соединений согласно настоящему изобретению могут образо-6 014905 вывать сольваты с водой (т.е. гидраты) или с обычными органическими растворителями и подразумевают, что такие сольваты также входят в рамки данного изобретения. Квалифицированному специалисту в данной области понятно, что там, где реакционную стадию согласно настоящему изобретению можно осуществлять во множестве растворителей или в системах растворителей, вышеуказанную реакционную стадию также можно осуществлять в смеси подходящих растворителей или в системах растворителей. В случаях, где способы получения соединений согласно данному изобретению приводят к смеси стереоизомеров, эти изомеры можно разделять стандартными методами, как, например, препаративная хроматография. Соединения могут быть получены в рацемической форме или индивидуальные энантиомеры могут быть получены либо путем энантиоспецифического синтеза, либо путем разделения. Эти соединения можно, например, разделять на их энантиомерные компоненты стандартными способами,как, например, образование диастереомерных пар путем образования соли с оптически активной кислотой, такой как (-)-ди-п-толуол-D-винная кислота и/или (+)-ди-п-толуол-L-винная кислота, с последующей фракционной кристаллизацией и регенерацией свободного основания. Соединения также можно разделять путем образования диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного агента. Альтернативно, соединения можно разделять, используя ВЭЖХ при применении колонки с хиральной фазой. Во время любого из способов получения соединений согласно настоящему изобретению может быть необходима и/или желательна защита чувствительных или реакционноспособных групп в случае любой из связанных с ними молекул. Это может быть достигнуто посредством обычных защитных групп, таких как таковые, описанные в руководстве "Protective Groups in Organic Chemistry", под ред.J.F.W. McOmie, Plenum Press, 1973; и руководстве T.W. GreeneP.G.M. Wuts, "Protective Groups in Organic Chemistry", John WileySons, 1991. Защитные группы можно удалять на подходящей последующей стадии, используя способы, известные в данной области. Например, квалифицированному специалисту в данной области понятно, что в случае способов согласно настоящему изобретению может быть необходимо и/или желательно осуществлять защиту замещающих групп, таких как (C1-8-алкилкарбонил)C1-8-алкил. Настоящее изобретение включает в свои рамки пролекарства соединений согласно данному изобретению. Вообще, такие пролекарства должны быть функциональными производными соединений, которые без труда превращаются in vivo в необходимое соединение. Таким образом, в случае способов лечения согласно настоящему изобретению термин "введение" включает лечение различных описанных нарушений с помощью конкретно описанного соединения или с помощью соединения, которое не может быть конкретно описано, но которое превращается in vivo в конкретное соединение после введения пациенту. Стандартные способы селекции и получения подходящих пролекарственных производных описаны, например, в "Design of Prodrugs", ред. Н. Bundgaard, Elsevier, 1985. Для применения в медицине соли соединений согласно данному изобретению относятся к нетоксичным "фармацевтически приемлемым солям". Другие соли, однако, могут быть пригодны при получении соединений согласно данному изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений включают аддитивные соли кислот, которые, например, могут быть образованы путем смешения раствора соединения с раствором фармацевтически приемлемой кислоты, такой как соляная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, карбоновая кислота или фосфорная кислота. Кроме того, когда соединения согласно данному изобретению содержат кислотный остаток, их подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов, например соли натрия или калия, соли щелочно-земельных металлов, например соли кальция или магния, и соли, образованные с подходящими органическими лигандами, например соли четвертичного аммония. Таким образом, типичные фармацевтически приемлемые соли включают следующие: ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, эдетат кальция, камсулат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликоллиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, иодид, изотионат, лактат, лактобионат, лаурат, малат, малеат,манделят, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, Nметилглюкаминаммониевая соль, олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат. Типичные кислоты и основания, которые можно использовать для получения фармацевтически приемлемых солей, включают следующее: кислоты включают уксусную кислоту, 2,2-дихлоруксусную кислоту, ацилированные аминокислоты,адипиновую кислоту, альгиновую кислоту, аскорбиновую кислоту, L-аспарагиновую кислоту, бензолсульфокислоту, бензойную кислоту, 4-ацетамидобензойную кислоту, (+)-камфорную кислоту, камфорсульфокислоту, (+)-(1S)-камфор-10-сульфоновую кислоту, каприновую кислоту, капроновую кислоту,каприловую кислоту, коричную кислоту, лимонную кислоту, цикламеновую кислоту, додецилсерную-7 014905 кислоту, этан-1,2-дисульфоновую кислоту, этансульфокислоту, 2-гидроксиэтансульфокислоту, муравьиную кислоту, фумаровую кислоту, галактаровую кислоту, гентизиновую кислоту, глюкогептоновую кислоту, D-глюконовую кислоту, D-глюкуроновую кислоту, L-глутаминовую кислоту, -оксоглутаровую кислоту, гликолевую кислоту, гиппуровую кислоту, бромоводородную кислоту, соляную кислоту, (+)-Lмолочную кислоту, -DL-молочную кислоту, лактобионовую кислоту, малеиновую кислоту, (-)-Lяблочную кислоту, малоновую кислоту, -DL-миндальную кислоту, метансульфокислоту, нафталин-2 сульфоновую кислоту, нафталин-1,5-дисульфоновую кислоту, 1-гидрокси-2-нафтойную кислоту, никотиновую кислоту, азотную кислоту, олеиновую кислоту, оротовую кислоту, щавелевую кислоту, пальмитиновую кислоту, памоевую кислоту, фосфорную кислоту, L-пироглутаминовую кислоту, салициловую кислоту, 4-аминосалициловую кислоту, себациновую кислоту, стеариновую кислоту, янтарную кислоту,серную кислоту, дубильную кислоту, (+)-L-винную кислоту, тиоциановую кислоту, птолуолсульфокислоту и ундециленовую кислоту; и основания включают аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, деанол,диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин, 1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин, пиперазин, гидроксид калия, 1-(2-гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. В одном воплощении настоящее изобретение относится к способам получения соединений формулы (I), где R1 выбирают из группы, состоящей из C1-6-алкила (предпочтительно изопропил) и C3-8 циклоалкила (предпочтительно циклопропил или циклобутил); n означает 1; R2 и R3, каждый, означают водород; R4 означает -(СН 2)-Q и Q означает 5- или 6-членный N-связанный гетероциклил, где в дополнение к N-связывающему азоту гетероциклил может необязательно содержать 1, 2 дополнительных гетероатома, независимо выбираемых из О, S и NH. В одном воплощении настоящее изобретение относится к способам получения соединений формулы (I), где:(f) L означает неразветвленный -(СН 2)m-, где m означает целое число от 1 до 4;(i) Q означает замещенный или незамещенный пиперидинил, диазепанил, азепанил, декагидроизохинолин-2-ил, пиперазинил, пирролинил, пирролидинил, тиоморфолинил или морфолинил;(l) Q означает одновалентный радикал амина, выбираемого из группы, состоящей из азиридина,1,4,7-триокса-10-азациклододекана, тиазолидина, 1-фенил-1,3,8-триазаспиро 4.5 декан-4-она, диэтиламида пиперидин-3-карбоновой кислоты,1,2,3,4,5,6-гексагидро 2,3'бипиридинила,4-(3 трифторметилфенил)пиперазина, 2-пиперазин-1-илпиримидина, амида пиперидин-4-карбоновой кислоты, метил(2-пиридин-2-илэтил)амина, 2-(3,4-диметоксифенил)этилметиламина, тиоморфолинила, аллилциклопентиламина,2-(1 Н-индол-3-ил)этилметиламина,1-пиперидин-4-ил-1,3-дигидробензоимидазол-2-она, 2-(пиперидин-4-илокси)пиримидина, пиперидин-4-илпиридин-2-иламина, фениламина и пиридин-2-иламина;(m) Q выбирают из группы, состоящей из диазепанила, азепанила, морфолинила, пиперидинила и пирролидинила, необязательно замещенных 1-3 заместителями, независимо выбираемыми из группы,состоящей из гидрокси, галогена, карбоксамида, C1-6-алкила, 5-9-членного или 6-9-членного гетероциклила, -N-(С 1-6-алкил)(5-9-членного или 6-9-членного гетероциклила), -NH-(5-9-членного или 6-9 членного гетероциклила), -О-(5-9- или 6-9-членного гетероциклила), (5-9-членного или 6-9-членного гетероциклил)-С 1-3-алкилена, C1-6-алкокси, (C3-6-циклоалкил)-O-, фенила, (фенил)-С 1-3-алкилена и (фенил)C1-3-алкилен-О-, где каждая из вышеуказанных гетероциклильных, фенильных и алкильных групп может быть необязательно замещена 1-3 заместителями, независимо выбираемыми из группы, состоящей из трифторметила, метокси, галогена, нитро, циано, гидрокси и С 1-3-алкила;(r) R9 означает незамещенный или замещенный фенил;(v) R9 выбирают из фенила или 5-9-членного ароматического гетероциклила, где вышеуказанный фенил или ароматический гетероциклил необязательно замещен 1-3 заместителями, выбираемыми из метокси, гидрокси, галогена, нитро, циано, трифторметила и C1-3-алкила;(w) R9 выбирают из замещенного или незамещенного фенила, пиридила, пиримидила, фурила, тиофурила, имидазолила, (имидазолил)-C1-6-алкилена, оксазолила, тиазолила, 2,3-дигидроиндолила, бензимидазолила, 2-оксобензимидазолила, (тетразолил)-C1-6-алкилена, тетразолила, (триазолил)-C1-6-алкилена,триазолила, (пирролил)-С 1-6-алкилена, пирролидинила и пирролила;(х) R9 означает замещенный или незамещенный пиридил;(z) комбинации (a)-(z), указанные выше. В другом воплощении настоящее изобретение относится к способам получения соединений формулы (I), выбираемых из группы, состоящей из-9 014905 4-(1-этилпропил)пиперазин-1-ил-(4-морфолин-4-илметилфенил)метанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-(4-фениламинометилфенил)метанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-(4-пиперидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-(4-пирролидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-4-(3-трифторметилпиперидин-1-илметил)фенилметанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-4-(декагидроизохинолин-2-илметил)фенилметанона; 4-(1-этилпропил)пиперазин-1-ил-4-(4-трифторметилфениламино)метилфенилметанондигидрохлорида; 4-(1-метилгептил)пиперазин-1-ил-(4-морфолин-4-илметилфенил)метанона; 4-(1-метилгептил)пиперазин-1-ил-(4-пиперидин-1-илметилфенил)метанона; 4-(бензиламинометил)фенил-(4-изопропилпиперазин-1-ил)метанондигидрохлорида; 4-(бензиламинометил)фенил-4-(1-этилпропил)пиперазин-1-илметанона и 4-(5-хлорпиридин-2-иламино)метилфенил-(4-изопропилпиперазин-1-ил)метанондигидрохлорида. Предпочтительно с помощью способов согласно настоящему изобретению получают соединения,выбираемые из группы, состоящей из- 10014905 4-(5-хлорпиридин-2-иламино)метилфенил-(4-изопропилпиперазин-1-ил)метанондигидрохлорида. Предпочтительно настоящее изобретение относится к способам получения соединения формулы (I),выбираемого из группы, состоящей из(4-втор-бутилпиперазин-1-ил)-(4-пирролидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-(4-морфолин-4-илметилфенил)метанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-(4-пиперидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-(4-пирролидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-4-(3-трифторметилпиперидин-1 илметил)фенилметанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-4-(декагидроизохинолин-2-илметил)фенилметанона; 4-(бензиламинометил)фенил-(4-изопропилпиперазин-1-ил)метанондигидрохлорида и 4-(бензиламинометил)фенил-4-(1-этилпропил)пиперазин-1-илметанона. Более предпочтительно настоящее изобретение относится к способам получения соединения формулы (I), выбираемого из группы, состоящей из(4-втор-бутилпиперазин-1-ил)-(4-пирролидин-1-илметилфенил)метанона; 4-(1-этилпропил)пиперазин-1-ил-(4-морфолин-4-илметилфенил)метанондигидрохлорида; 4-(1-этилпропил)пиперазин-1-ил-(4-пиперидин-1-илметилфенил)метанона и 4-(1-этилпропил)пиперазин-1-ил-(4-пирролидин-1-илметилфенил)метанона. Еще более предпочтительно настоящее изобретение относится к способам получения соединения формулы (I), выбираемого из группы, состоящей из(4-втор-бутилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанондигидрохлорида и 4-(1-этилпропил)пиперазин-1-ил-(4-морфолин-4-илметилфенил)метанондигидрохлорида. Настоящее изобретение относится к способу получения соединений формулы (I). Способ согласно настоящему изобретению выгоден для крупномасштабных и/или коммерческих целей, так как он не тре- 11014905 бует выделения и/или очистки маслянистых промежуточных продуктов и не требует применения колоночной хроматографии, которая является непрактичной и требует непомерно высоких затрат в большом и/или коммерческом масштабе. Кроме того, способ согласно настоящему изобретению можно осуществлять в системе одного растворителя, тогда как в случае способа, как раскрытый в публикации заявки на патент США под номером 2004-0010746 А 1, опубликованной 21 апреля 2005 г. (также опубликованная в виде публикации РСТ, WO 2004/037801, 6 мая 2004 г.), требуются многочисленные растворители (включая растворители для реакции и экстракционной обработки). Настоящее изобретение относится к способу получения соединений формулы (I), как более детально описано на схеме 1, приводимой ниже. Схема 1 Соответственно подходящим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными способами, активируют в соответствии с известными способами, в первом органическом растворителе с получением соответствующего соединения формулы (XI), гдеL представляет собой подходящую удаляемую группу, такую как хлор, бром, ОС(О)O-C1-4-алкил, OBt(где активирующим агентом является HOBt), имидазолид (где активирующим агентом является CDI) и т.п., предпочтительно хлор. Например, когда L представляет собой хлор, соединение формулы (X) вводят во взаимодействие с подходящим хлорирующим агентом, таким как оксалилхлорид, тионилхлорид, оксихлорид фосфора и т.п., предпочтительно примерно с 1,05 экв. оксалилхлорида, в присутствии каталитического количества ДМФА, в органическом растворителе, таком как ТГФ, толуол, дихлорметан, дихлорэтан, ацетонитрил и т.п., предпочтительно ТГФ. Альтернативно, соединение формулы (X) вводят во взаимодействие с реагентом Вилсмейера (хлорметилендиметиламмонийхлорид), в органическом растворителе, таком какDCM, при температуре в диапазоне от примерно 0 С до примерно комнатной температуры. Соединение формулы (XI) не выделяют. Соединение формулы (XI) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XII), известным соединением или соединением, полученным известными способами, где соединение формулы (XII) предпочтительно находится в количестве, равном примерно 1 экв., более предпочтительно примерно 0,95 экв., в присутствии органического или неорганического основания(твердого или водного), такого как TEA, DIPEA, пиридин, NaOH, KOH, карбонат натрия, карбонат калия и т.п., предпочтительно 50%-ный водный раствор NaOH; где основание является органическим, предпочтительно в отсутствие воды, во втором органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно ТГФ; с получением соответствующего соединения формулы (XIII). Соединение формулы (XIII) не выделяют. Соединение формулы (XIII) вводят во взаимодействие с подходящим образом замещенным соеди- 12014905 нением формулы (XIV), известным соединением или соединением, полученным известными способами,где соединение формулы (XIV) предпочтительно находится в количестве более чем примерно 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 5 экв., еще более предпочтительно в количестве в диапазоне от примерно 1,5 до примерно 2,5 экв., наиболее предпочтительно в количестве в диапазоне от примерно 1,5 до примерно 2 экв., в присутствии восстановителя, такого какNaBH(OAc)3, NaBH4, цианоборгидрид натрия и т.п., предпочтительно NaBH(OAc)3; где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв.; в третьем органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно ТГФ, с получением соответствующего соединения формулы (I). Предпочтительно соединение формулы (I) не выделяют и/или очищают. Более предпочтительно соединение формулы (I) вводят во взаимодействие в соответствии с известными способами с получением соответствующей фармацевтически приемлемой соли соединения формулы (I). Необязательно, соединение формулы (I) выделяют и/или очищают в соответствии с известными способами. Предпочтительно первый органический растворитель, второй органический растворитель и третий органический растворитель являются одинаковыми. Предпочтительно конверсия соединения формулы(X) в соответствующее соединение формулы (I) завершается в системе одного растворителя. В одном воплощении настоящего изобретения соединение формулы (I) далее вводят во взаимодействие с подходящим образом выбранной фармацевтически приемлемой кислотой, получая соответствующую фармацевтически приемлемую соль соединения формулы (I). В одном воплощении настоящего изобретения соединение формулы (I) не выделяют и вводят во взаимодействие с подходящим образом выбранной фармацевтически приемлемой кислотой, получая соответствующую фармацевтически приемлемую соль соединения формулы (I). Квалифицированному специалисту в данной области понятно, что при синтезе соединений формулы (I), где замещающая группа -(СН 2)m-Q связана с положением 2 фенильного цикла, альдегидную группу соединения формулы (X) предпочтительно защищают с помощью подходящих защитных групп в соответствии с известными способами до реакции с соединением формулы (XII) и затем после снятия защиты вводят во взаимодействие с соединением формулы (XIV). В одном воплощении настоящее изобретение относится к способу получения соединения формулы(Is), также известного как (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанон, как более детально описано на схеме 2, приводимой ниже. Схема 2 Соответственно подходящим образом замещенное соединение формулы (Xs), также известное как 4-формилбензойная кислота, известное соединение, активируют в соответствии с известными способами в первом органическом растворителе с получением соответствующего соединения формулы (XIs), где L представляет собой подходящую удаляемую группу, такую как хлор, бром, ОС(О)O-C1-4-алкил, OBt (где активирующим агентом является HOBt), имидазолид (где активирующим агентом является CDI) и т.п.,предпочтительно хлор. Например, когда L представляет собой хлор, соединение формулы (Xs) вводят во взаимодействие с подходящим хлорирующим агентом, таким как оксалилхлорид, тионилхлорид, оксихлорид фосфора и т.п., предпочтительно примерно с 1,05 экв. оксалилхлорида, в присутствии каталитического количества ДМФА, в органическом растворителе, таком как ТГФ, толуол, дихлорметан, дихлорэтан, ацетонитрил и т.п., предпочтительно ТГФ. Альтернативно, соединение формулы (Xs) вводят во взаимодействие с реагентом Вилсмейера (хлорметилендиметиламмонийхлорид) в органическом растворителе, таком какDCM, при температуре в диапазоне от примерно 0 С до примерно комнатной температуры.- 13014905 Соединение формулы (XIs) не выделяют. Соединение формулы (XIs) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIIs), также известным как N-изопропилпиперазин, известным соединением, где соединение формулы (XIIs) предпочтительно находится в количестве, равном примерно 1 экв., более предпочтительно примерно 0,95 экв.; в присутствии органического или неорганического основания (твердого или водного), такого как TEA, DIPEA, пиридин, NaOH, KOH, карбонат натрия, карбонат калия и т.п.,предпочтительно 50%-ный водный раствор NaOH; где основание является органическим, предпочтительно в отсутствие воды, во втором органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно ТГФ, с получением соответствующего соединения формулы (XIIIs), также известного как 4-(4-изопропилпиперазин-1-карбонил)бензальдегид. Соединение формулы (XIIIs) не выделяют. Соединение формулы (XIIIs) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIVs), также известным как морфолин, известным соединением, где соединение формулы (XIVs) предпочтительно находится в количестве более чем примерно 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 5 экв., еще более предпочтительно в количестве в диапазоне от примерно 1,5 до примерно 2,5 экв., наиболее предпочтительно в количестве в диапазоне от примерно 1,5 до примерно 2 экв., в присутствии восстановителя, такого как NaBH(OAc)3, NaBH4, цианоборгидрид натрия и т.п., предпочтительно NaBH(ОАс)3, где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв., в третьем органическом растворителе, таком как ТГФ,толуол, ацетонитрил и т.п., предпочтительно ТГФ, с получением соответствующего соединения формулы (Is), также известного как (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанон. Предпочтительно соединение формулы (Is) не выделяют и/или очищают. Более предпочтительно соединение формулы (Is) вводят во взаимодействие в соответствии с известными способами, получая соответствующую фармацевтически приемлемую соль соединения формулы (Is), еще более предпочтительно моносукцинат соединения формулы (Is). Необязательно, соединение формулы (Is) выделяют и/или очищают в соответствии с известными способами. В одном воплощении настоящего изобретения соединение формулы (Is) далее вводят во взаимодействие с подходящим образом выбранной фармацевтически приемлемой кислотой, получая соответствующую фармацевтически приемлемую соль соединения формулы (Is). В одном воплощении настоящего изобретения соединение формулы (Is) не выделяют и вводят во взаимодействие с подходящим образом выбранной фармацевтически приемлемой кислотой, получая соответствующую фармацевтически приемлемую соль соединения формулы (Is). В публикации заявки на патент США под номером 2004-0010746 А 1, опубликованной 21 апреля 2005 г. (также опубликованная в виде публикации РСТ, WO 2004/037801, 6 мая 2004 г.), раскрывается способ получения соединений формулы (I). В одном воплощении настоящее изобретение относится к усовершенствованиям в отношении способа получения соединений формулы (I), как раскрытый в публикации заявки на патент США под номером 2004-0010746 А 1. Более конкретно, усовершенствованием согласно настоящему изобретению является получение бисульфитного промежуточного продукта (соединение формулы (XVII) на схемах, которые следуют ниже в данном контексте), который может быть выделен в виде твердого вещества, таким образом обеспечивая улучшенный способ очистки (в способе, описанном в публикации заявки на патент США под номером 2004-0010746 А 1, альдегидный промежуточный продукт формулы (XIII) выделяют в виде масла и затем очищают с помощью колоночной хроматографии). Кроме того, бисульфитный промежуточный продукт обладает улучшенными стабильностью и сроком хранения относительно альдегидного промежуточного продукта. В одном воплощении настоящее изобретение относится к способу очистки альдегидного промежуточного продукта, соединения формулы (XII), включающему получение его соответствующего бисульфитного производного, выделение вышеуказанного бисульфитного производного в виде твердого вещества, например, путем фильтрации и, необязательно, очистку в соответствии с известными методами,например, путем перекристаллизации из подходящего растворителя, такого как метанол, этанол, изопропанол, ацетонитрил и т.п., предпочтительно этанол. Бисульфитное производное затем может быть далее введено во взаимодействие, как описано в данном контексте, с получением желательного соединения формулы (I) или, альтернативно, может быть введено во взаимодействие до образования снова соединения формулы (XIII), которое затем вводят во взаимодействие в соответствии со способами, как описанные в данном контексте, с получением желательного соединения формулы (I). Усовершенствованный способ согласно настоящему изобретению более детально описан на схеме 3, приводимой далее. Соответственно подходящим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными способами, активируют в соответствии с известными способами с получением соответствующего соединения формулы (XI), где L представляет собой подходящую удаляемую группу, такую как хлор, бром, -ОС(О)O-C1-4-алкил, OBt (где активирующим агентом являетсяHOBt), имидазолид (где активирующим агентом является CDI) и т.п., предпочтительно хлор. Например, когда L представляет собой хлор, соединение формулы (X) вводят во взаимодействие с подходящим хлорирующим агентом, таким как оксалилхлорид, тионилхлорид, оксихлорид фосфора и т.п., предпочтительно примерно с 1,05 экв. тионилхлорида, в присутствии каталитического количества ДМФА, в органическом растворителе, таком как ТГФ, толуол, дихлорметан, дихлорэтан, ацетонитрил и т.п., предпочтительно ТГФ. Альтернативно, соединение формулы (X) вводят во взаимодействие с реагентом Вилсмейера (хлорметилендиметиламмонийхлорид) в органическом растворителе, таком какDCM, при температуре в диапазоне от примерно 0 С до примерно комнатной температуры. Предпочтительно соединение формулы (XI) не выделяют. Соединение формулы (XI) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XII), известным соединением или соединением, полученным известными способами, где соединение формулы (XII) предпочтительно находится в количестве, равном примерно 1 экв., более предпочтительно примерно 0,95 экв., в присутствии органического или неорганического основания(твердого или водного), такого как TEA, DIPEA, пиридин, NaOH, KOH, карбонат натрия, карбонат калия и т.п., предпочтительно TEA; где основание является органическим, предпочтительно в отсутствие воды,в органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно ТГФ, с получением соответствующего соединения формулы (XIII). Предпочтительно соединение формулы (XIII) не выделяют. Соединение формулы (XIII) вводят во взаимодействие с подходящим источником бисульфита, таким как NaHSO3, KHSO3 и т.п., предпочтительно водный раствор NaHSO3, где источник бисульфита предпочтительно находится в количестве более чем или равном примерно 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., еще более предпочтительно в количестве,равном примерно 1,2 экв., в полярном органическом растворителе, таком как метанол, этанол, ТГФ,ДМФА, ацетонитрил и т.п., предпочтительно этанол, с получением соответствующего бисульфита, соединения формулы (XVII). Предпочтительно соединение формулы (XVII) выделяют известными способами, например путем фильтрации и промывки подходящим органическим растворителем, таким как этанол, гексан и т.п., и затем, далее, необязательно очищают известными методами, например путем перекристаллизации из подходящего растворителя, такого как метанол, этанол, изопропанол, ацетонитрил и т.п., предпочтительно этанол. Соединение формулы (XVII) вводят во взаимодействие на 2-й или 1-й стадии способа, где бисульфит вводят во взаимодействие для высвобождения соответствующего альдегида, соединения формулы(XIII), и альдегид формулы (XIII) вводят во взаимодействие с соединением формулы (XVI), получая соответствующее соединение формулы (I). Более конкретно соединение формулы (XVII) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIV), известным соединением или соединением, полученным известными способами, где соединение формулы (XIV) предпочтительно находится в количестве более чем примерно 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., еще более предпочтительно примерно 2 экв.; в присутствии восстановителя, такого как NaBH(OAc)3, NaBH4,цианоборгидрид натрия и т.п., предпочтительно NaBH(OAc)3, где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв., в присутствии органического или неорганического основания, такого как TEA, DIPEA, пиридин, NaOH, KOH и т.п., предпочтительно 10%-ный водный раствор NaOH; в органическом растворителе, таком как дихлорэтан, ТГФ, толуол, ацетонитрил и т.п., предпочтительно дихлорэтан, необязательно в присутствии источника кислоты, такого как отбеливающая глина, активированная кислотой, монтмориллонит К-10 (выпускается фирмой Aldrich), Nafion-H (регистрационный номер по каталогу 63937-00-8) и т.п., с получением соответствующего соединения формулы(I). Квалифицированному специалисту в данной области понятно, что когда количество соединения формулы (XIV) является более чем или равным примерно 2 экв., то 1 экв. соединения формулы (XIV) действует в качестве органического или неорганического основания для высвобождения альдегида, соединения формулы (XIII), и, кроме того, нет необходимости в дополнительном органическом или неорганическом основании. Альтернативно, соединение формулы (XVII) вводят во взаимодействие с органическим или неорганическим основанием, таким как TEA, DIPEA, пиридин, NaOH, KOH и т.п., предпочтительно 10%-ный водный раствор NaOH, где основание предпочтительно находится в количестве более чем или равном 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв.; в соответствии с известными способами удаления бисульфита и высвобождения соответствующего соединения формулы (XIII). Соединение формулы (XIII) затем вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIV), где соединение формулы (XIV) предпочтительно находится в количестве более чем или равном примерно 1 экв., предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., в присутствии восстановителя, такого как NaBH(ОАс)3, NaBH4, цианоборгидрид натрия и т.п., предпочтительно NaBH(OAc)3, где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв.; необязательно в присутствии источника кислоты, такого как отбеливающая глина, активированная кислотой, монтмориллонит К-10 (выпускаемая фирмой Aldrich), Nafion-H(регистрационный номер по каталогу 63937-00-8) и т.п., в органическом растворителе, таком как ТГФ,толуол, ацетонитрил и т.п., предпочтительно ТГФ; с получением соответствующего соединения формулы (I). Альтернативно, соединение формулы (XIII) вводят во взаимодействие с соответствующим образом замещенным соединением формулы (XIV) в соответствии со способами, как описанные в данном контексте или как описано в публикации заявки на патент США под номером 2004-0010746 А 1, с получением соответствующего соединения формулы (I). Предпочтительно соединение формулы (I) выделяют в соответствии с известными способами, например путем выпаривания растворителя. Соединение формулы (I) затем, далее, может быть, необязательно, введено во взаимодействие в соответствии с известными способами, получая его соответствующую фармацевтически приемлемую соль. В одном воплощении настоящее изобретение относится к усовершенствованиям способа, описанного в публикации заявки на патент США под номером 2004-0010746 А 1, для получения соединения формулы (Is), также известного как (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанон,как более детально описано на схеме 4, приводимой далее. Соответственно подходящим образом замещенное соединение формулы (Xs), также известное как 4-формилбензальдегид, известное соединение, активируют в соответствии с известными способами с получением соответствующего соединения формулы (XIs), где L представляет собой подходящую удаляемую группу, такую как хлор, бром, -ОС(О)O-С 1-4-алкил, OBt (где активирующим агентом являетсяHOBt), имидазолид (где активирующим агентом является CDI) и т.п., предпочтительно хлор. Например, когда L представляет собой хлор, соединение формулы (Xs) вводят во взаимодействие с подходящим хлорирующим агентом, таким как оксалилхлорид, тионилхлорид, оксихлорид фосфора и т.п., предпочтительно примерно с 1,05 экв. тионилхлорида, в присутствии каталитического количества ДМФА, в органическом растворителе, таком как ТГФ, толуол, дихлорметан, дихлорэтан, ацетонитрил и т.п., предпочтительно ТГФ. Альтернативно, соединение формулы (Xs) вводят во взаимодействие с реагентом Вилсмейера (хлорметилендиметиламмонийхлорид) в органическом растворителе, таком какDCM, при температуре в диапазоне от примерно 0 С до примерно комнатной температуры. Предпочтительно соединение формулы (XIs) не выделяют. Соединение формулы (XIs) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIIs), также известным как 4-изопропилпиперазин, известным соединением, где соединение формулы (XIIs) предпочтительно находится в количестве, равном примерно 1 экв., более предпочтительно примерно 0,95 экв., в присутствии органического или неорганического основания (твердого или водного), такого как TEA, DIPEA, пиридин, NaOH, KOH, карбонат натрия, карбонат калия и т.п.,предпочтительно TEA; где основание является органическим, предпочтительно в отсутствие воды, в органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно ТГФ; с получением соответствующего соединения формулы (XIIIs). Предпочтительно соединение формулы (XIIIs) не выделяют. Соединение формулы (XIIIs) вводят во взаимодействие с подходящим источником бисульфита, таким как NaHSO3, KHSO3 и т.п., предпочтительно водный раствор NaHSO3, где источник бисульфита предпочтительно находится в количестве более чем или равном примерно 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв, еще более предпочтительно в количестве,равном примерно 1,2 экв, в полярном органическом растворителе, таком как метанол, этанол, ТГФ,ДМФА, ацетонитрил и т.п., предпочтительно этанол, с получением соответствующего бисульфита, соединения формулы (XVIIs). Предпочтительно соединение формулы (XVIIs) выделяют известными способами, например путем фильтрации и промывки подходящим органическим растворителем, таким как этанол, гексан и т.п., и затем необязательно очищают известными способами, например путем перекристаллизации из подходящего растворителя, такого как метанол, этанол, изопропанол, ацетонитрил и т.п., предпочтительно этанол. Соединение формулы (XVIIs) вводят во взаимодействие на 2-й или 1-й стадии способа, где бисульфит подвергают реакции с высвобождением соответствующего альдегида, соединения формулы (XIIIs), и альдегидное соединение формулы (XIIIs) вводят во взаимодействие с соединением формулы (XIVs) с получением соответствующего соединения формулы (Is). Более конкретно, соединение формулы (XVIIs) вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIVs), также известным как морфолин, известным соединением,- 17014905 где соединение формулы (XIVs) предпочтительно находится в количестве более чем примерно 1 экв.,более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., еще более предпочтительно примерно 2 экв.; в присутствии восстановителя, такого как NaBH(ОАс)3, NaBH4, цианоборгидрид натрия и т.п., предпочтительно NaBH(OAc)3, где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв.; в присутствии органического или неорганического основания,такого как TEA, DIPEA, пиридин, NaOH, KOH и т.п., предпочтительно 10%-ный водный раствор NaOH,в органическом растворителе, таком как дихлорэтан, ТГФ, толуол, ацетонитрил и т.п., предпочтительно дихлорэтан; необязательно в присутствии источника кислоты, такого как отбеливающая глина, активированная кислотой, монтмориллонит К-10 (выпускается фирмой Aldrich), Nafion-H (регистрационный номер по каталогу 63937-00-8) и т.п., с получением соответствующего соединения формулы (Is). Квалифицированному специалисту в данной области понятно, что когда количество соединения формулы (XIVs) является более чем или равным примерно 2 эквивалентам, то 1 экв. соединения формулы (XIVs) действует в качестве органического или неорганического основания для высвобождения альдегида, соединения формулы (XIIIs), и, кроме того, нет необходимости в дополнительном органическом или неорганическом основании. Альтернативно, соединение формулы (XVIIs) вводят во взаимодействие с органическим или неорганическим основанием, таким как TEA, DIPEA, пиридин, NaOH, KOH и т.п., предпочтительно 10%-ный водный раствор NaOH, где основание предпочтительно находится в количестве более чем или равном 1 экв., более предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., в соответствии с известными способами удаления бисульфита и высвобождения соответствующего соединения формулы (XIIIs). Соединение формулы (XIIIs) затем вводят во взаимодействие с подходящим образом замещенным соединением формулы (XIVs), где соединение формулы (XIVs) предпочтительно находится в количестве более чем или равном примерно 1 экв., предпочтительно в количестве в диапазоне от примерно 1 до примерно 2 экв., в присутствии восстановителя, такого как NaBH(ОАс)3, NaBH4, цианоборгидрид натрия и т.п., предпочтительно NaBH(OAc)3, где восстановитель предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно в количестве в диапазоне от примерно 1,25 до примерно 1,5 экв.; необязательно в присутствии источника кислоты, такого как отбеливающая глина, активированная кислотой, монтмориллонит К-10 (выпускается фирмой Aldrich), Nafion-H(регистрационный номер по каталогу 63937-00-8) и т.п., в органическом растворителе, таком как ТГФ,толуол, ацетонитрил и т.п., предпочтительно ТГФ, с получением соответствующего соединения формулы (Is). Альтернативно, соединение формулы (XIIIs) вводят во взаимодействие с соответствующим образом замещенным соединением формулы (XIVs) в соответствии со способами, как описанные в данном контексте или как описано в публикации заявки на патент США под номером 2004-0010746 А 1, с получением соответствующего соединения формулы (Is). Предпочтительно соединение формулы (Is) выделяют в соответствии с известными способами, например путем выпаривания растворителя. Соединение формулы (Is) далее может быть необязательно введено во взаимодействие в соответствии с известными способами, получая его соответствующую фармацевтически приемлемую соль, предпочтительно его соответствующий моносукцинат. Настоящее изобретение далее относится к новым кристаллическим солям соединения формулы (I). В одном воплощении настоящее изобретение относится к малеату, фумарату, сукцинату, гидрохлориду или гидробромиду соединения формулы (I). Настоящее изобретение далее относится к новым кристаллическим солям соединения формулы (Is). В одном воплощении настоящее изобретение относится к малеату, фумарату, сукцинату, гидрохлориду или гидробромиду соединения формулы (Is). В одном воплощении настоящее изобретение относится к кристаллическому сукцинату соединения формулы (Is). В другом воплощении кристаллический сукцинат соединения формулы (Is) является моносукцинатом. Кристаллический моносукцинат соединения формулы (Is) является негигроскопическим. Установлено, что моносукцинат соединения формулы (Is) является кристаллическим согласно XRD и DSC и негигроскопическим согласно DVS. Кристаллический моносукцинат соединения формулы (Is) может быть представлен следующей химической структурой: Кристаллический сукцинат соединения формулы (Is) можно получать путем введения во взаимодействие соединения формулы (Is) с янтарной кислотой, где янтарная кислота предпочтительно находится в количестве в диапазоне от примерно 1 до примерно 2 экв., более предпочтительно примерно 1,3 экв.; в органическом растворителе, таком как ТГФ, толуол, ацетонитрил и т.п., предпочтительно в органическом растворителе, в котором янтарная кислота является растворимой, более предпочтительно в ТГФ. Кристаллический сукцинат соединения формулы (Is) предпочтительно очищают в соответствии с известными способами, более предпочтительно путем перекристаллизации из подходящего растворителя, такого как абсолютный этанол, метанол, изопропиловый спирт, ацетонитрил и т.п., предпочтительно абсолютный этанол. Настоящее изобретение далее относится к фармацевтически приемлемой соли соединения формулы(Is), где солью является малеат, фумарат, гидрохлорид или гидробромид соединения формулы (Is). В другом воплощении солью соединения формулы (Is) является бисмалеат, монофумарат, дигидрохлорид или дигидробромид соединения формулы (Is). Бисмалеат, монофумарат, дигидрохлорид или дигидробромид соединения формулы (Is) могут быть получены путем введения во взаимодействие соединения формулы (Is) с соответствующей кислотой (т.е. малеиновой кислотой, фумаровой кислотой, HCl и HBr соответственно), как более детально описано в примерах, которые следуют ниже в данном контексте. Установлено, что бисмалеат соединения формулы (Is) является кристаллическим согласно XRD иDSC и гигроскопическим согласно DVS. Установлено, что фумарат соединения формулы (Is) является кристаллическим согласно XRD и DSC и стабильным при относительной влажности вплоть до примерно 70% согласно DVS. Установлено, что дигидрохлорид соединения формулы (Is) является частично кристаллическим согласно XRD и DSC, представляет собой моногидрат согласно Карлу Фишеру и является гигроскопическим согласно DVS. Установлено, что дигидробромид соединения формулы (Is) является частично кристаллическим согласно XRD и DSC, представляет собой полугидрат согласно Карлу Фишеру и является гидроскопическим при относительной влажности (RH) выше примерно 10% согласно DVS. Соли соединения формулы (Is) могут быть охарактеризованы по их соответствующей порошковой рентгенограмме. Рентгенограммы, перечисленные в данном контексте, получали при использовании детектора XCelerator. Образец помещали в стандартный держатель аппарата рентгеновского излучения и сканировали в положениях от 3 до 352, с величиной шага 0,01652 и временем на шаг 10,16 с. Эффективная скорость сканирования составляла 0,2067/с. Напряжение измерителя и фиксации тока составляли 45 кВ и 40 мА. Кристаллический моносукцинат соединения формулы (Is) можно охарактеризовать по его ренгтенограмме, включающей пики, как перечисленные в нижеприводимой табл. 1. Таблица 1 Предпочтительно кристаллический моносукцинат соединения формулы (Is) характеризуют по его рентгенограмме, которая включает пики, имеющие относительную интенсивность более чем или равную В одном воплощении кристаллический моносукцинат соединения формулы (Is) характеризуют по положениям пиков (в 2) в его рентгеновских спектрах для пиков с относительной интенсивностью более чем примерно 10%, предпочтительно с относительной интенсивностью более чем примерно 25%. Кристаллический монофумарат соединения формулы (Is) можно охарактеризовать по его рентгенограмме, включающей пики, перечисленные в нижеприводимой табл. 3. Таблица 3 Предпочтительно кристаллический монофумарат соединения формулы (Is) характеризуют по его рентгенограмме, которая включает пики, имеющие относительную интенсивность более чем или равную примерно 25%, как перечислено в нижеприводимой табл. 4. Таблица 4 В одном воплощении кристаллический монофумарат соединения формулы (Is) характеризуют по положениям пиков (в 2) в его рентгеновских спектрах для пиков с относительной интенсивностью более чем примерно 10%, предпочтительно с относительной интенсивностью более чем примерно 25%. Кристаллический дигидрохлорид соединения формулы (Is) можно охарактеризовать по его рентгенограмме, включающей пики, перечисленные в нижеприводимой табл. 5. Предпочтительно кристаллический дигидрохлорид соединения формулы (Is) характеризуют по его рентгенограмме, которая включает пики, имеющие относительную интенсивность более чем или равную примерно 25%, как перечислено в нижеприводимой табл. 6. Таблица 6 В одном воплощении кристаллический дигидрохлорид соединения формулы (Is) характеризуют по положениям пиков (в 2) в его рентгеновских спектрах для пиков с относительной интенсивностью более чем примерно 10%, предпочтительно с относительной интенсивностью более чем примерно 25%. Кристаллический дигидробромид соединения формулы (Is) можно охарактеризовать по его рентгенограмме, включающей пики, как перечисленные в нижеприводимой табл. 7. Предпочтительно кристаллический дигидробромид соединения формулы (Is) характеризуют по его рентгенограмме, которая включает пики, имеющие относительную интенсивность более чем или равную примерно 25%, как перечислено в нижеприводимой табл. 8. Таблица 8 В одном воплощении кристаллический дигидробромид соединения формулы (Is) характеризуют по положениям пиков (в 2) в его рентгеновских спектрах для пиков с относительной интенсивностью более чем примерно 10%, предпочтительно с относительной интенсивностью более чем примерно 25%. Соединения или композиции согласно данному изобретению могут быть получены и введены субъекту любым стандартным путем введения, включая, но не ограничиваясь этим, внутривенное, пероральное, подкожное, внутримышечное, интрадермальное и парентеральное введение. Количество соединения, которое эффективно для лечения каждого состояния, можно варьировать и может быть определено квалифицированным специалистом в данной области. Настоящее изобретение также относится к фармацевтическим композициям, содержащим одно или более соединений согласно данному изобретению, в сочетании с фармацевтически приемлемым носителем и, необязательно, дополнительными фармацевтическими агентами, такими как H1-антагонисты илиSSRIs (селективные ингибиторы повторного поглощения серотонина). Предпочтительно эти композиции находятся в унифицированных разовых лекарственных формах, таких как пилюли, таблетки, каплеты,капсулы (каждая включает готовые лекарственные формы с немедленным высвобождением, высвобождением по времени и с пролонгированным высвобождением), порошки, гранулы, стерильные паренте- 22014905 ральные растворы или суспензии (включая сиропы и эмульсии), дозированные аэрозоли или жидкие спреи, капли, ампулы, автоинжекторные устройства или суппозитории; для перорального, парентерального, интраназального, сублингвального или ректального введения или введения путем ингаляции или инсуффляции. Альтернативно, композиция может находиться в форме, пригодной для введения один раз в неделю или один раз в месяц, например нерастворимую соль активного соединения, такую как деканоат, можно адаптировать для получения препарата пролонгированного действия для внутримышечной инъекции. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например со стандартными ингредиентами для таблетирования, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальцийфосфат или смолы, и другими фармацевтическими разбавителями, как, например, вода, для образования твердой, предварительно приготовленной композиции, содержащей гомогенную смесь, включающую соединение согласно настоящему изобретению или его фармацевтически приемлемую соль. Когда ссылаются на эти предварительно приготовленные композиции как на гомогенные, это означает, что активный ингредиент равномерно диспергирован по всей композиции, так что композицию можно без труда подразделять на равные эффективные лекарственные формы, такие как таблетки, пилюли и капсулы. Эту твердую, предварительно приготовленную композицию затем подразделяют на унифицированные разовые лекарственные формы типа, описанного выше, содержащие от 5 до примерно 1000 мг активного ингредиента согласно настоящему изобретению. Примеры включают 5, 7, 10, 15, 20,35, 50, 75, 100, 120, 150 мг и т.д. На таблетки или пилюли из описанных композиций может быть нанесено покрытие или они могут быть компаундированы иным способом для получения лекарственной формы, обладающей преимуществом пролонгированного действия. Например, таблетка или пилюля может содержать внутренний дозированный компонент и внешний дозированный компонент, причем последний находится в форме покрытия для первого. Два компонента можно разделять с помощью энтеросолюбильного слоя, который служит для препятствования дезинтеграции в желудке и дает возможность внутреннему компоненту неповрежденным проходить в двенадцатиперстную кишку или высвобождаться пролонгированно. Можно использовать множество веществ для таких энтеросолюбильных слоев или покрытий, причем такие вещества включают некоторое количество полимерных кислот с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которых соединения и композиции согласно настоящему изобретению могут быть комбинированы для введения перорально или путем инъекции, включают водные растворы, пригодные ароматизированные сиропы, водные или масляные суспензии и ароматизированные эмульсии с пищевыми маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические среды. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические и природные смолы, такие как трагакант, гуммиарабик, альгинат, декстран, натрийкарбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин. Преимущественно соединения согласно настоящему изобретению можно вводить в унифицированной разовой суточной дозе, или общая суточная доза может быть введена в виде разделенных доз два,три или четыре раза в сутки. Кроме того, соединения согласно настоящему изобретению можно вводить в интраназальной форме при местном применении подходящих интраназальных сред или с помощью трансдермальных кожных пластырей, хорошо известных квалифицированному специалисту в данной области. Для введения в форме трансдермальной системы доставки введение дозировки, конечно, должно быть предпочтительнее непрерывным, чем прерывистым, на всем протяжении схемы приема. Например, для перорального введения в форме таблетки или капсулы активный лекарственный компонент можно комбинировать с пероральным нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и т.п. Кроме того, когда желательно или необходимо, также можно вводить в смесь подходящие связующие вещества, смазки, дезинтегрирующие агенты и красители. Подходящие связующие вещества включают, без ограничения этим, крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, сахаристые вещества из кукурузы, природные и синтетические смолы, такие как гуммиарабик, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтегрирующие агенты включают, без ограничения этим,крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п. Соединение согласно настоящему изобретению также можно вводить в форме липосомных систем доставки, таких как малые моноламеллярные везикулы, большие моноламеллярные везикулы и мультиламеллярные везикулы. Липосомы могут быть образованы из множества фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины. Соединения согласно настоящему изобретению также можно доставлять за счет использования моноклональных антител в качестве индивидуальных носителей, с которыми связаны молекулы соединения. Соединения согласно настоящему изобретению также можно связывать с растворимыми полимерами в качестве нацеливаемых лекарственных носителей. Такие полимеры могут включать поливинипирролидон, пирановый сополимер, полигидроксипропилметакриламидфенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный пальмитоиловым остатком. Кроме того, соеди- 23014905 нения согласно настоящему изобретению могут быть связаны с классом биоразлагаемых полимеров,пригодных для достижения контролируемого высвобождения лекарственного средства, например полимолочная кислота, полиэпсилонкапролактон, полигидроксимасляная кислота, сложные полиэфиры, полиацетали, полидигидропираны, полицианоакрилаты сшитые или амфипатические блок-сополимеры гидрогелей. Соединения согласно данному изобретению могут быть введены в любых из вышеуказанных композиций и в соответствии со схемами приема, установленными в данной области, всякий раз, когда требуется лечение. Суточная доза продуктов может варьироваться в широком диапазоне от 1 до 1000 мг на взрослого человека в сутки. Для перорального введения композиции предпочтительно получают в форме таблеток,содержащих 1,0, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 250 и 500 мг активного ингредиента, для симптоматического регулирования дозы для субъекта, которого подвергают лечению. Эффективное количество лекарственного средства обычно обеспечивается при уровне дозировки от примерно 0,01 до примерно 20 мг/кг массы тела в сутки. Предпочтительно диапазон составляет от примерно 0,02 до примерно 10 мг/кг массы тела в сутки и, в особенности, от примерно 0,05 до примерно 10 мг/кг массы тела в сутки. Соединения можно вводить в режиме от 1 до 4 раз в сутки. Оптимальные дозы для введения могут быть без труда определены квалифицированным специалистом в данной области, и они могут варьироваться в зависимости от конкретного используемого соединения, способа введения, эффективности препарата, пути введения и прогрессирования болезненного состояния. В дополнение, факторы, связанные с конкретным пациентом, которого подвергают лечению,включающие возраст пациента, массу тела, диету и время введения, приводят к необходимости регулировки доз. Следующие примеры приводятся для способствования пониманию данного изобретения и не предназначены и не могут быть истолкованы как ограничивающие каким-либо образом данное изобретение,изложенное в формуле изобретения, которая представлена далее. В нижеследующих примерах некоторые синтетические продукты перечислены в виде выделенных в качестве остатка. Квалифицированному специалисту в данной области понятно, что термин "остаток" не ограничен физическим состоянием, в котором выделяют продукт, и может включать, например, твердое вещество,масло, пену, смолу, сироп и т.п. Пример 1. 4-Формилбензоилхлорид К тонкой суспензии 4-карбоксибензальдегида (600 г, 3,92 моль) в тетрагидрофуране (2664 г,36,57 моль) добавляют диметилформальдегид (11,48 г, 0,16 моль) и реакционную смесь охлаждают до температуры 0-5 С на ледяной бане. Реакционную смесь затем перемешивают при температуре 0 С при медленном добавлении оксалилхлорида (608,69 г, 4,70 моль). Реакционную смесь перемешивают до тех пор, пока реакция по 1 Н-ЯМР не завершится, получая указанное в заголовке соединение. Реакционную смесь используют на следующей стадии без дальнейшей обработки. 1(43,3 г, 469,39 ммоль) медленно добавляют к раствору NaHCO3 (0,8 г, 9,52 ммоль) и 4 изопропилпиперазина (2,50 г, 18,35 ммоль) в воде (5 г, 277 ммоль) при температуре 0 С. Реакционную смесь энергично перемешивают до тех пор, пока полностью не завершится реакция. Слои разделяют и толуольную фазу концентрируют, получая указанное в заголовке соединение в виде масла желтого цвета. 1 4-Изопропилпиперазин (79,53 г, 0,620 моль), ТГФ (444 г, 5,04 моль), воду (36 г, 2 моль) и 50%-ный раствор гидроксида натрия (130,6 г, 1,63 моль) вводят в реакционный сосуд и охлаждают до температуры 0-5 С. 4-Формилбензоилхлорид в ТГФ (110,08 г, 0,630 моль) добавляют к содержащей 4 изопропилпиперазин реакционной смеси, в то время как поддерживают температуру ниже примерно 10 С. Полученную суспензию белого цвета перемешивают при комнатной температуре до тех пор, пока реакция полностью не завершится. К реакционной суспензии добавляют воду и полученный мутный раствор отфильтровывают через целит, удаляя нерастворимые вещества. Отфильтрованный реакционный раствор отстаивают и водный слой удаляют. Слой продукт/ТГФ последовательно сушат над сульфатом магния и молекулярными ситами. Раствор продукта (KF0,5%) хранят при температуре 5 С для использования без дальнейших обработок. Пример 4. (4-Изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанон К раствору 4-(4-изопропилпиперазин-1-карбонил)бензальдегида (4,0 г, 15,38 ммоль) в ТГФ (40 мл) добавляют морфолин (2,9 г, 33,83 ммоль) и полученную смесь перемешивают при комнатной температуре в течение 1 ч перед охлаждением до температуры 0 С на ледяной бане. Реакционную смесь затем обрабатывают с помощью NaBH(OAc)3 (4,56 г, 21,53 ммоль) в виде порций, в течение 15 мин. Полученную суспензию перемешивают при комнатной температуре до тех пор, пока реакция согласно ВЭЖХ не завершится. После завершения реакции добавляют 10%-ный раствор NaOH (25 мл) и реакционную смесь энергично встряхивают в течение 15 мин. Фазы разделяют и водный слой экстрагируют с помощью ТГФ(20 мл). Органические слои объединяют, сушат (MgSO4), отфильтровывают и концентрируют, получая указанное в заголовке соединение в виде масла желтого цвета. 1 Раствор 1-(4-формилбензоил)-4-изопропилпиперазина в ТГФ (содержащий 945 г 1-(4 формилбензоил)-4-изопропилпиперазина и 3879 г ТГФ) вводят в реакционный сосуд с последующим добавлением морфолина (576,3 г, 6,55 моль). Спустя 20 мин реакционную смесь охлаждают до температуры примерно 0-10 С и в виде порций добавляют триацетоксиборгидрид натрия (1167,3 г, 5,23 моль). После завершения реакции медленно добавляют 10%-ный раствор гидроксида натрия (3623,2 мл,9,06 моль) и реакционную смесь перемешивают в течение 20 мин. Слои разделяют и водный слой промывают с помощью ТГФ. Объединенные органические слои сушат над сульфатом магния. После сушки раствор (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона в ТГФ используют без дальнейших обработок. Раствор сырого (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона (59,4 г,0,179 моль) в ТГФ (278,0 г) нагревают до температуры 40 С и добавляют янтарную кислоту (27,53 г,0,233 моль). Реакционную смесь нагревают до температуры 60 С и отфильтровывают в чистую колбу. Полученный раствор повторно нагревают до температуры 60 С и затем медленно охлаждают сначала до комнатной температуры, а затем до температуры -7 С. Полученную суспензию поддерживают при температуре -7 С и отфильтровывают. Фильтровальный осадок промывают с помощью ТГФ (60 мл) и твердое вещество высушивают в течение ночи при температуре 50 С в полном вакууме, получая сырой моносукцинат в виде твердого вещества белого цвета. Суспензию сырого моносукцината (701,3 г, 1,56 моль) в этаноле (7,01 л) нагревают до температуры 60-65 С. Любое нерастворимое вещество удаляют путем фильтрации. Полученный прозрачный раствор медленно охлаждают до температуры -7 С. Суспензию отфильтровывают и промывают этанолом(700 мл). Фильтровальный осадок высушивают в течение ночи при температуре 50 С в полном вакууме,получая моносукцинат в виде кристаллического твердого вещества белого цвета. Температура плавления: 154-156 С; Элементный анализ для C19H29N3O2C4H6O2: Рассчитано: С 61,45; Н 7,85; N 9,35; H2O 0,1%; Найдено: С 61,42; Н 7,84; N 9,29; H2O 0,1%; МС: [М+Н]+=332; [2 М+Н]+=685. Пример 7. Монофумарат (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона К раствору (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона (3,0 г, 9,0 ммоль) в ТГФ (40 мл) добавляют ТГФ (40 мл) и фумаровую кислоту (3,3 г, 28,4 ммоль). Полученную смесь нагревают при температуре 60 С и перемешивают в течение 0,5 ч. Полученную суспензию охлаждают до температуры 0 С и полученный осадок собирают путем фильтрации, промывают с помощью ТГФ(20 мл) и высушивают в вакуумном сушильном шкафу при температуре 65 С в течение 20 ч, получая сырое, указанное в заголовке соединение в виде твердого вещества белого цвета. Суспензию сырого монофумарата(4-изопропилпиперазин-1-ил)-(4-морфолин-4 илметилфенил)метанона (5,7 г, 12,7 ммоль) в абсолютном EtOH (110 мл) нагревают до температуры 70 С. Любое нерастворимое вещество удаляют путем фильтрации через слой целита. Фильтрат повторно нагревают до температуры 65 С и затем охлаждают до температуры 0 С. Осадок собирают путем фильтрации и промывают с помощью МТВЕ (20 мл). Твердые вещества высушивают в вакуумном сушильном шкафу при температуре 65 С в течение 20 ч, получая указанное в заголовке соединение в виде твердого вещества белого цвета. Температура плавления: 196-198 С; Элементный анализ для C19H29N3O2C4H4O4: Рассчитано: С 61,73; Н 7,43; N 9,39; Найдено: С 61,44; Н 7,50; N 9,30. Пример 8. Моногидрат (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанондигидрохлорида Раствор (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона (2,0 г, 6,0 ммоль) в абсолютном EtOH (20 мл) обрабатывают с помощью газообразного HCl (0,5 г, 13,7 ммоль) при комнатной температуре. Полученную суспензию перемешивают в течение 1 ч и затем добавляют МТВЕ (5 мл).- 26014905 Суспензию охлаждают до температуры 0 С и отфильтровывают. Фильтровальный осадок промывают с помощью МТВЕ (20 мл) и твердое вещество высушивают в вакуумном сушильном шкафу при температуре 60 С в течение 20 ч, получая сырое, указанное в заголовке соединение в виде твердого вещества белого цвета. Суспензию сырого (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанондигидрохлорида (2,1 г, 5,2 ммоль) в абсолютном EtOH (30 мл) нагревают до температуры 78 С и добавляют воду(2,2 мл). Полученный раствор охлаждают до комнатной температуры и добавляют МТВЕ (5 мл). Полученную суспензию охлаждают до температуры 0 С и отфильтровывают. Фильтровальный осадок промывают с помощью МеОН (15 мл). Твердые вещества высушивают в вакуумном сушильном шкафу при температуре 105 С в течение 20 ч, получая указанное в заголовке соединение в виде твердого вещества белого цвета. Температура плавления: разложение при 220 С; Элементный анализ для C19H29N3O22HClH2O: Рассчитано: С 53,97; Н 7,81; N 9,94; Cl 16,81; Найдено: С 54,13; Н 7,50; N 9,90; Cl 16,68; К раствору (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона (3,0 г, 9,0 ммоль) в ТГФ (40 мл) добавляют ТГФ (40 мл) и 30%-ный раствор бромоводорода в уксусной кислоте (3,7 мл,18,6 ммоль) при поддерживании температуры в интервале между 15 и 20 С. Полученную суспензию перемешивают в течение 1 ч и затем охлаждают до температуры 0 С. Осадок собирают путем фильтрации,промывают с помощью ТГФ (20 мл) и высушивают в вакуумном сушильном шкафу при температуре 65 С в течение 20 ч, получая сырое, указанное в заголовке соединение в виде твердого вещества белого цвета. Суспензию сырого(4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанондигидробромида (4,9 г, 9,9 ммоль) в МеОН (50 мл) нагревают до температуры 65 С. Полученный раствор охлаждают до температуры 0 С и осадок собирают путем фильтрации и промывают с помощью МеОН(15 мл). Твердые вещества высушивают в вакуумном сушильном шкафу при температуре 65 С в течение 20 ч, получая указанное в заголовке соединение в виде твердого вещества белого цвета. Температура плавления: разложение 290 С; Элементный анализ для C19H29N3O22HBr0,5 Н 2 О: Рассчитано: С 45,39; Н 6,37; N 8,36; Br 31,85; Найдено: С 45,60; Н 6,32; N 8,36; Br 33,41;(3,0 г,9,05 ммоль) в абсолютном EtOH (20 мл) добавляют при использовании капельной воронки раствор малеиновой кислоты (3,3 г, 19,8 ммоль) в абсолютном EtOH (20 мл) в течение 10 мин. Полученную суспензию перемешивают при комнатной температуре в течение 15 мин, при температуре 75 С в течение 30 мин и затем оставляют охлаждаться до комнатной температуры в течение 15 ч. Реакционную смесь после этого охлаждают до температуры 0 С и затем перемешивают в течение 2 ч. Полученный осадок собирают путем вакуумной фильтрации и промывают холодным EtOH (20 мл). Влажное твердое вещество высушивают в вакуумном сушильном шкафу при температуре 40 С в течение 6 ч, получая указанное в заголовке соединение в виде сырого продукта, в виде твердого вещества белого цвета. Суспензию сырого бисмалеата (4-изопропилпиперазин-1-ил)-(4-морфолин-4-илметилфенил)метанона (3,0 г) в абсолютном EtOH (30 мл) нагревают при температуре 75 С в течение 1 ч и полученный раствор отфильтровывают через тонкопористый стеклянный фильтр. Фильтрат нагревают при температуре 75 С, затем охлаждают до комнатной температуры в течение 2 ч при перемешивании и добавляют Et2O (10 мл). Полученную суспензию охлаждают до температуры 0 С в течение 2 ч, осадок соби- 27014905 рают путем вакуумной фильтрации и промывают с помощью Et2O (20 мл) в защитной атмосфере азота. Твердые вещества высушивают в вакуумном сушильном шкафу при температуре 45 С в течение 20 ч,получая указанное в заголовке соединение в виде кристаллического твердого вещества белого цвета. Температура плавления: 154,1 С; Элементный анализ для C27H37N3O10: Рассчитано: С 57,54; Н 6,62; N 7,46; Найдено: С 57,44; Н 6,66; N 7,33. Пример 11. Протокол анализов для соединений, полученных в примерах 12-29. ВЭЖХ, прибор Hewlett Packard, фаза Zorbax Eclipse XDB-C8, 5 мкм, колонка размером 4,6150 мм; используемыми растворителями являются H2O/CH3CN/0,05% трифторуксусная кислота; градиентные условия представляют собой: градиент 1-99% CH3CN в течение 8 мин, 99% CH3CN в течение 2 мин. Все реакции осуществляют в атмосфере азота. Масс-спектр получают на приборе Agilent серии 1100 MSD, используя ионизацию электронным распылением (ESI) методами образования или положительных или отрицательных ионов, как указано. Тонкослойную хроматографию осуществляют, используя пластинки, предварительно покрытые силикагелем Merck 60 F254, размером 2,5 см 7,5 см, 250 мкм или размером 5,0 см 10,0 см, 250 мкм. Препаративную тонкослойную хроматографию осуществляют, используя пластинки, предварительно покрытые силикагелем ЕМ Science 60 F254, размером 20 см 20 см, 0,5 мм, с зоной концентрации размером 20 см 4 см. ЯМР-спектры получают или на спектрометре Bruker модели DPX400 (400 МГц), или на спектрометре Bruker модели DPX500 (500 МГц). Вид данных ЯМР представлен ниже: химический сдвиг в м.д.(миллионных долях) в сторону нижнего поля от тетраметилсилана в качестве стандарта (мультиплетность, константа взаимодействия J в Гц, интеграция). Пример 12. 1-Изопропилпиперазиндигидрохлорид К раствору трет-бутилпиперазин-1-карбоксилата (100 г) и ацетона (48 мл) в CH2Cl2 (1 л) добавляют уксусную кислоту (31 мл) и NaBH(OAc)3 (170 г). Реакционную смесь перемешивают в течение 18 ч, затем разбавляют 1 н. раствором NaOH (500 мл) и экстрагируют с помощью CH2Cl2 (2 раза по 500 мл). Объединенные органические слои сушат (Na2SO4) и концентрируют до получения остатка. Остаток растворяют в МеОН (200 мл) и к реакционной смеси добавляют 4 М раствор HCl в 1,4-диоксане (700 мл) в течение нескольких часов. Спустя 18 ч реакционную смесь концентрируют до получения твердого вещества, которое промывают с помощью Et2O (2 раза по 500 мл) и высушивают в течение ночи, получая указанное в заголовке соединение в виде твердого вещества белого цвета. 1CH2Cl2 (300 мл) при температуре 0 С обрабатывают с помощью 4-карбоксибензальдегида (40,0 г,267 ммоль) в виде одной порции. Реакционную смесь перемешивают при температуре 0 С в течение 30 мин, затем при комнатной температуре в течение 2 ч. Анализ ВЭЖХ аликвоты реакционной смеси,погашенной с помощью МеОН, показывает полный расход 4-карбоксибензальдегида. Реакционную смесь отфильтровывают через пористый стеклянный фильтр. Фильтрат, содержащий указанное в заголовке соединение, хранят при температуре 0 С и используют на следующей стадии без дальнейшей обработки. Пример 14. 4-(4-Изопропилпиперазин-1-карбонил)бензальдегид К суспензии изопропилпиперазиндигидрохлорида (52,5 г, 262 ммоль) (получен согласно вышеприведенному примеру 12) в CH2Cl2 добавляют Et3N (83,5 г, 827 ммоль) и полученную суспензию перемешивают при комнатной температуре в течение 1 ч, затем при температуре 0 С в течение 30 мин. Реакционную смесь отфильтровывают через пористый стеклянный фильтр и фильтрат охлаждают до темпера- 28014905 туры 0 С. Раствор 4-формилбензоилхлорида в CH2Cl2 добавляют при использовании капельной воронки в виде медленного потока в течение 30 мин. Полученную смесь перемешивают при температуре 0 С в течение 30 мин, затем при комнатной температуре в течение 2 ч. Реакционную смесь охлаждают до температуры 0 С и отфильтровывают через пористый стеклянный фильтр. Фильтрат промывают водой, 0,5 н. раствором NaOH и насыщенным солевым раствором (1 раз по 400 мл каждого). Органический слой сушат (Na2SO4) и концентрируют, получая масло (59,8 г). Это масло растирают в безводном Et2O (275 мл) с последующим удалением растворителя при использовании роторного испарителя, получая указанное в заголовке соединение в виде масла бледного желто-коричневого цвета. ВЭЖХ: RT=5,43 мин. Пример 15. Натриевая соль гидрокси[4-(4-изопропилпиперазин-1-карбонил)фенил]метансульфоновой кислоты Раствор 4-(4-изопропилпиперазин-1-карбонил)бензальдегида (20,0 г, 76,9 ммоль) в EtOH (200 мл) перемешивают при комнатной температуре в течение 15 мин. К полученному раствору по каплям добавляют раствор NaHSO3 (9,6 г) в H2O (25 мл) в течение 30 мин. Полученную суспензию перемешивают при комнатной температуре в течение 2 ч, затем охлаждают до температуры 0 С и перемешивают в течение 3 ч, периодически добавляя EtOH (общее количество 200 мл) для способствования перемешиванию. Выпавший осадок собирают путем вакуумной фильтрации через стеклянный фильтр, снабженный изнутри фильтровальной бумагой. Фильтровальный осадок промывают гексаном (1 раз по 50 мл) и высушивают в вакууме в течение 16 ч, получая указанное в заголовке соединение в виде твердого вещества белого цвета. Температура плавления: 275 С (разложение). Чистоту соединения определяют путем растворения бисульфитного аддукта в смеси 1 н. растворNaOH/MeOH в соотношении 1:1 и анализа путем ВЭЖХ. Кроме того, выделенный продукт экстрагируют с помощью EtOAc и органический слой анализируют путем ТСХ (MeOH/CH2Cl2, 1:9). Продолжительное выдерживание в йодной камере показывает одно пятно (Rf=0,71). Пример 16. 4-(4-Изопропилпиперазин-1-карбонил)бензальдегид К суспензии натриевой соли гидрокси[4-(4-изопропилпиперазин-1-карбонил)фенил]метансульфоновой кислоты (49,0 г, 135 ммоль) в деионизированной воде (490 мл) при температуре 0 С добавляют 1 н. раствор NaOH (100 мл) в виде порций по 10 мл при энергичном перемешивании. Получают прозрачный раствор (pH 12), который перемешивают при температуре 0 С в течение 1 ч, затем при комнатной температуре в течение 30 мин. Водный раствор экстрагируют с помощью EtOAc (3 раза по 200 мл),затем CH2Cl2 (3 раза по 200 мл). Органические слои объединяют, промывают насыщенным солевым раствором (1 раз по 300 мл), сушат (Na2SO4) и концентрируют, получая указанное в заголовке соединение в виде масла бледно-желтого цвета. ВЭЖХ: RT=5,43 мин. К раствору 4-(4-изопропилпиперазин-1-карбонил)бензальдегида (32,0 г, 123 ммоль) в ТГФ (650 мл) добавляют морфолин (21,4 г, 246 ммоль) в виде медленного потока при использовании капельной воронки в течение 15 мин и полученную смесь перемешивают при комнатной температуре в течение 40 мин. Реакционную смесь обрабатывают с помощью NaBH(ОАс)3 (38,4 г, 172 ммоль) в виде порций в течение 40 мин, перемешивают при комнатной температуре в течение 16 ч и затем концентрируют до получения остатка. Остаток разбавляют с помощью EtOAc (400 мл), охлаждают до температуры 0 С и обрабатывают 1 н. раствором NaOH (250 мл). Двухфазный раствор перемешивают при температуре 0 С в течение 30 мин. Фазы разделяют и водный слой экстрагируют с помощью EtOAc (2 раза по 200 мл) и CH2Cl2(2 раза по 100 мл). Органические слои объединяют, промывают насыщенным солевым раствором (1 раз
МПК / Метки
МПК: C07D 295/18, C07D 211/14, C07D 207/06
Метки: новый, производных, пиперазинильных, бензамида, получения, способ
Код ссылки
<a href="https://eas.patents.su/30-14905-novyjj-sposob-polucheniya-piperazinilnyh-proizvodnyh-benzamida.html" rel="bookmark" title="База патентов Евразийского Союза">Новый способ получения пиперазинильных производных бензамида</a>
Предыдущий патент: Новые гетероциклические соединения в качестве положительных аллостерических модуляторов метаботропных глутаматных рецепторов
Следующий патент: 5-(арилсульфонил)пиразолопиперидины
Случайный патент: Способ и устройство для загрузки направленных вверх шпуров поддающимся насосной перекачке материалом