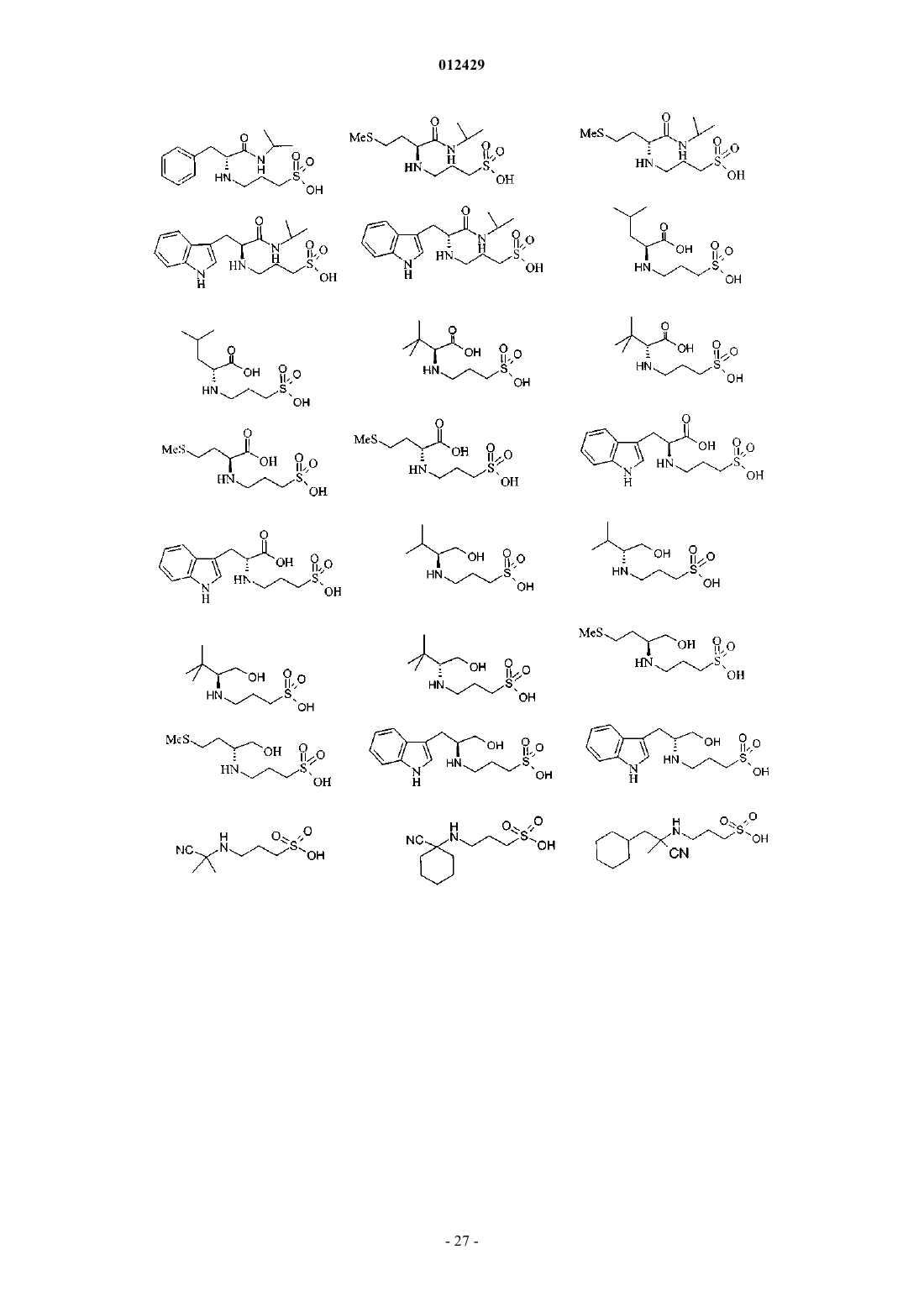Способы и композиции для лечения амилоидных заболеваний
Номер патента: 12429
Опубликовано: 30.10.2009
Авторы: Ву Ксинфу, Валяд Изабелль, Конг Ксианки, Жерве Франсин, Мигнол Дэвид
Формула / Реферат
1. Применение соединения формулы (I)
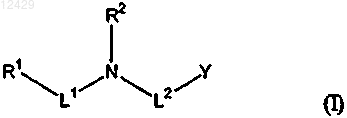
где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3; L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства для лечения или предупреждения связанного с амилоидом заболевания или состояния.
2. Применение по п.1, отличающееся тем, что заболевание или состояние характеризуется отложением b-амилоида.
3. Применение соединения формулы (I)
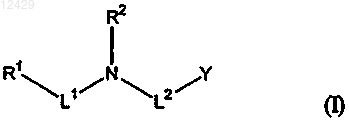
где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства для лечения или предупреждения отложения амилоида.
4. Применение соединения формулы (I)
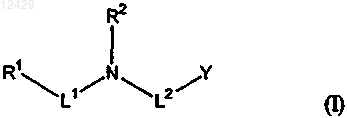
где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства для лечения или предупреждения заболевания, выбранного из группы, включающей болезнь Альцгеймера, церебральную амилоидную ангиопатию, миозит телец включений, дегенерацию желтого пятна, MCI или синдром Дауна.
5. Применение по п.4, отличающееся тем, что заболевание представляет собой болезнь Альцгеймера.
6. Применение соединения формулы (I)

где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и Y обозначрхт SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства для изготовления лекарственного средства для лечения или предупреждения связанных с амилоидом заболеваний и состояний.
7. Применение по п.6, отличающееся тем, что заболевание или состояние характеризуется отложением b-амилоида.
8. Применение соединения формулы (I)

где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства для изготовления лекарственного средства для лечения или предупреждения заболевания, выбранного из группы, включающей болезнь Альцгеймера, церебральную амилоидную ангиопатию, миозит телец включений, дегенерацию желтого пятна, MCI или синдром Дауна.
9. Применение по п.8, отличающееся тем, что заболевание представляет собой болезнь Альцгеймера.
10. Применение по пп.1-9, отличающееся тем, что R1 обозначает водород.
11. Применение по п.1, отличающееся тем, что R1 обозначает линейный C2-C10-алкил.
12. Применение по п.11, отличающееся тем, что R1 обозначает этил, н-пентил, н-гептил, н-октил или н-нонил.
13. Применение по пп.1-9, отличающееся тем, что R1 обозначает трет-бутил.
14. Применение по п.13, отличающееся тем, что соединение представляет собой 3-(трет-бутил)амино-1-пропансульфоновую кислоту или ее фармацевтически приемлемую соль, сложный эфир или пролекарство.
15. Применение по пп.1-9, отличающееся тем, что R1 обозначает C4-C10-циклоалкил.
16. Применение по п.15, отличающееся тем, что R1 обозначает циклоалкил, содержащий 2 или 3 конденсированных кольца.
17. Применение по п.16, отличающееся тем, что R1 обозначает C7-C10-циклоалкил, содержащий 2 конденсированных кольца.
18. Применение по п.16, отличающееся тем, что R1 обозначает циклоалкил, содержащий 2 конденсированных кольца.
19. Применение по п.17, отличающееся тем, что R1 обозначает трицикло[3.3.1.03,7]децил или адамантил.
20. Применение по п.19, отличающееся тем, что R1 обозначает бицикло[2.1.2]гептил.
21. Применение по п.19, отличающееся тем, что соединение представляет собой 3-(1-адамантил)амино-1-пропансульфоновую кислоту или ее фармацевтически приемлемую соль, сложный эфир или пролекарство.
22. Применение по любому из пп.1-21, отличающееся тем, что L2 обозначает (СН2)3.
23. Применение по любому из пп.1-22, отличающееся тем, что L2 обозначает замещенный C2-C5-алкил.
24. Применение по п.23, отличающееся тем, что L2 выбран из -CH2CH2CH(CH3)- и -CH2CH(OH)CH2-.
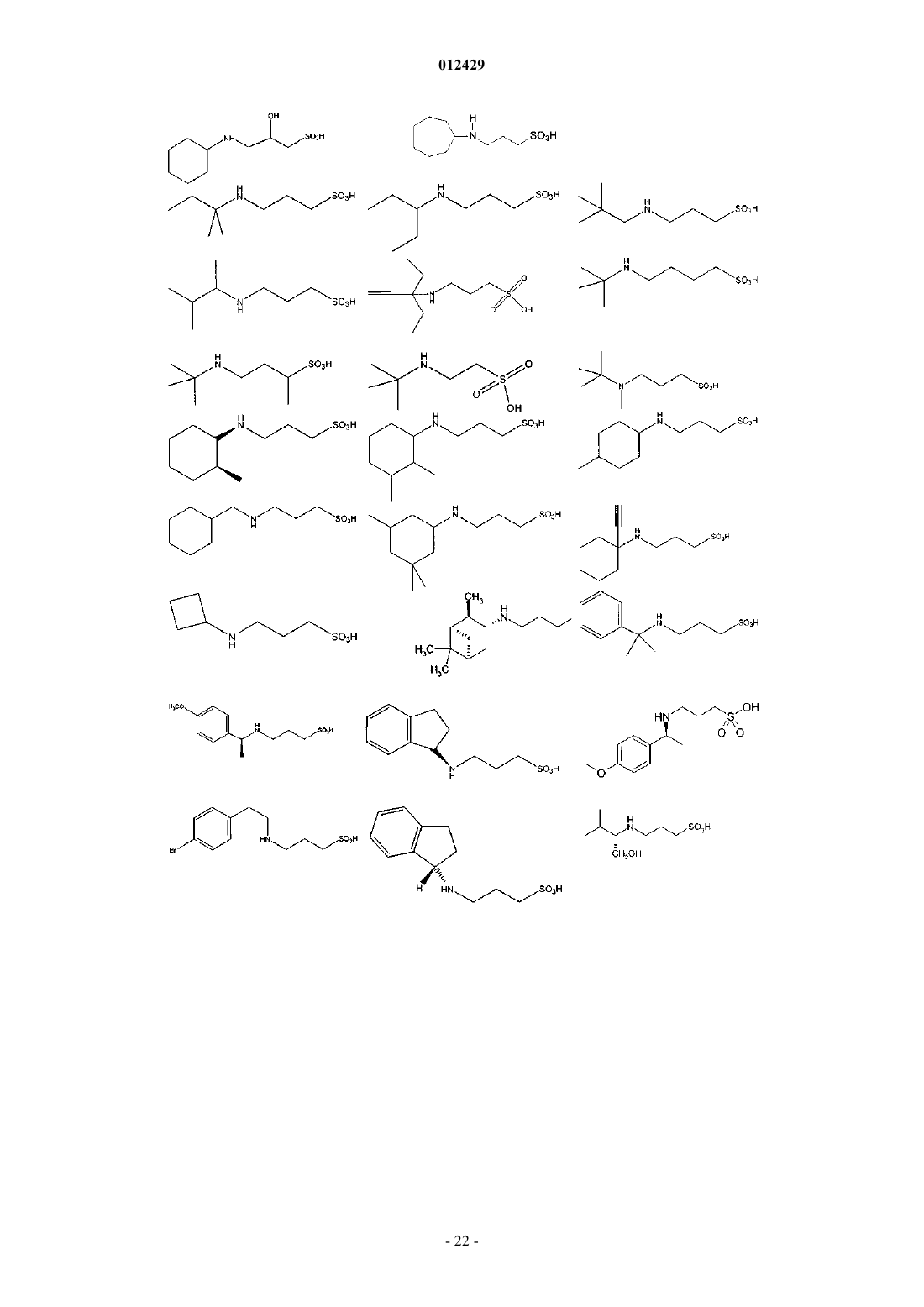
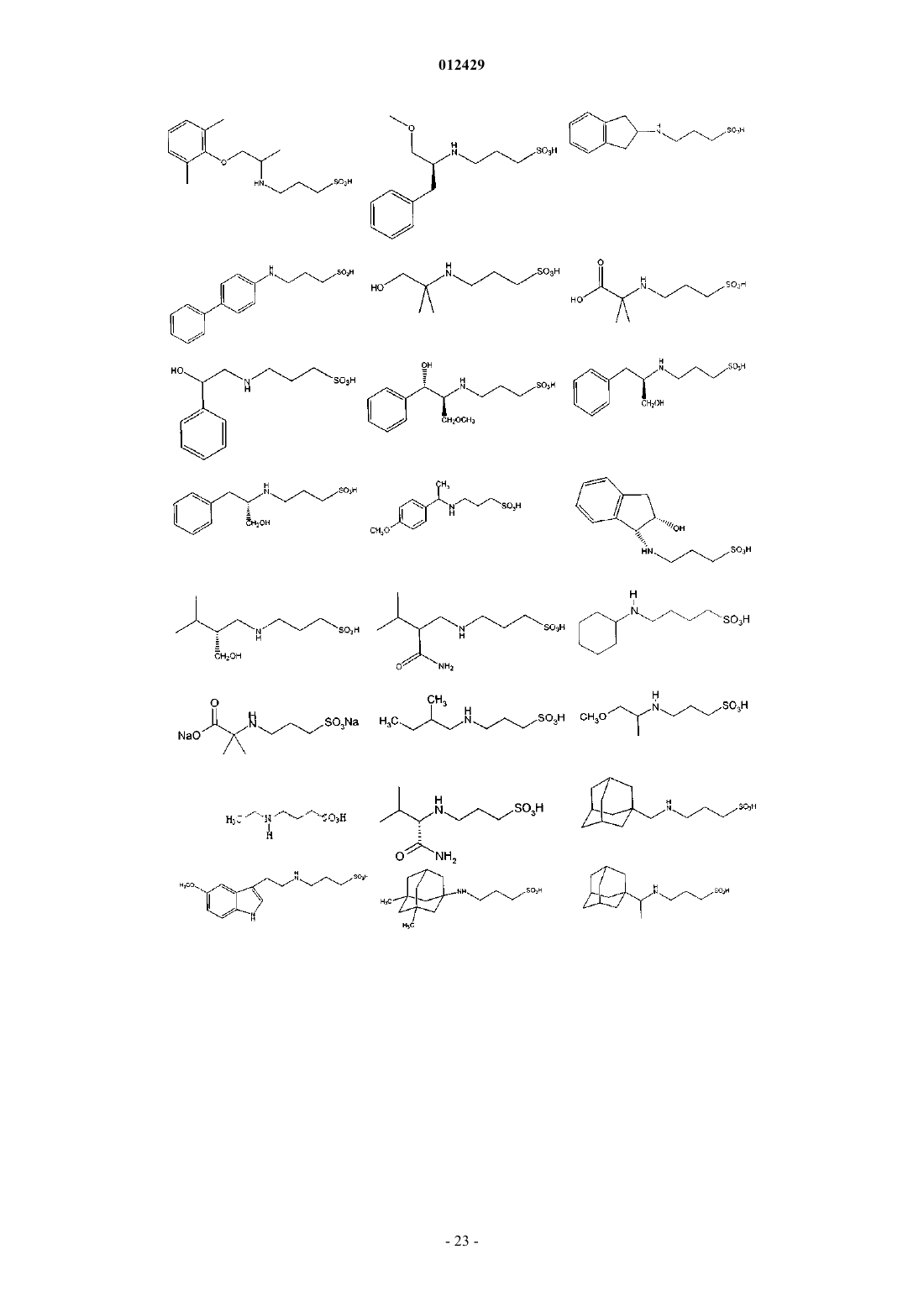
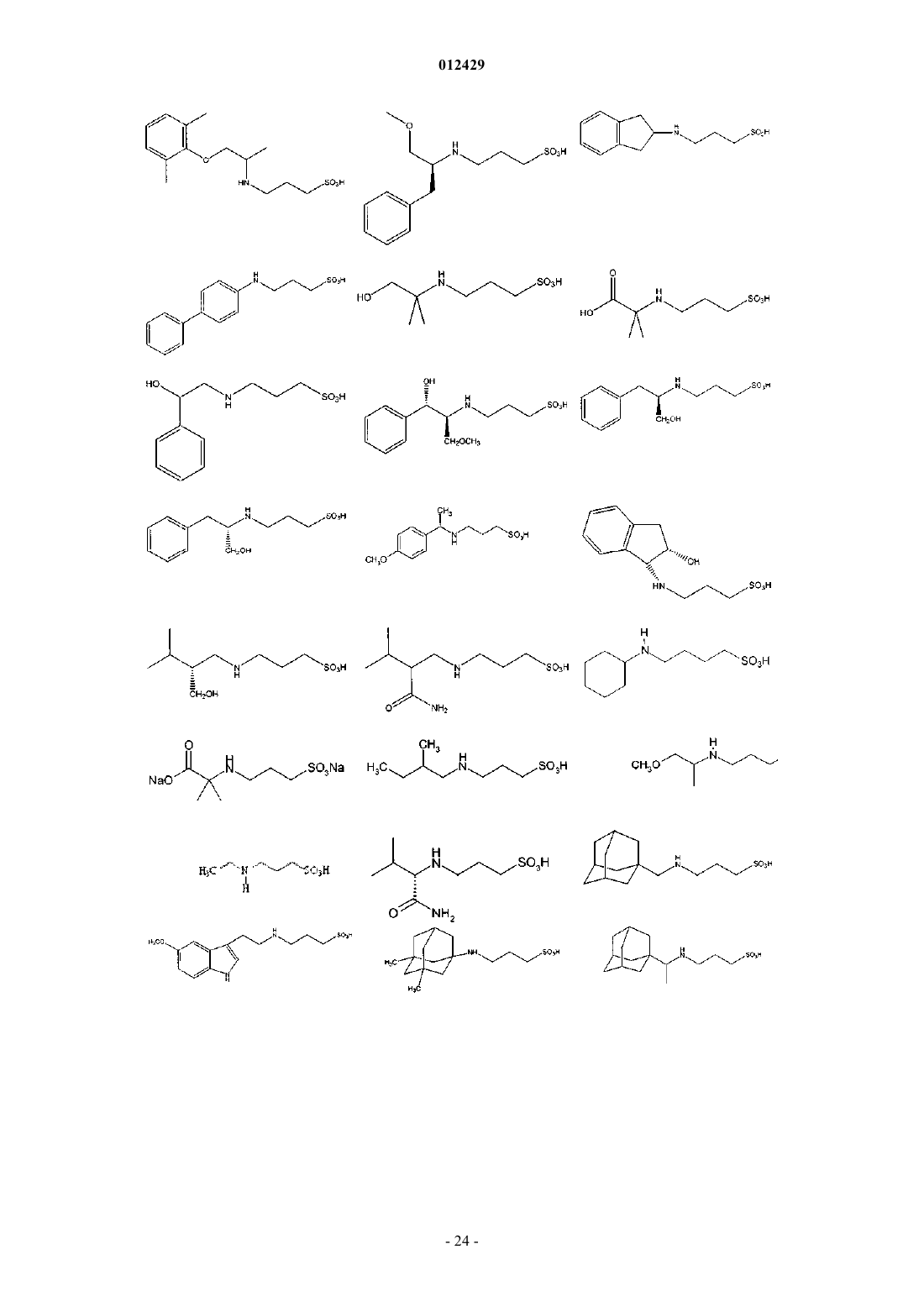
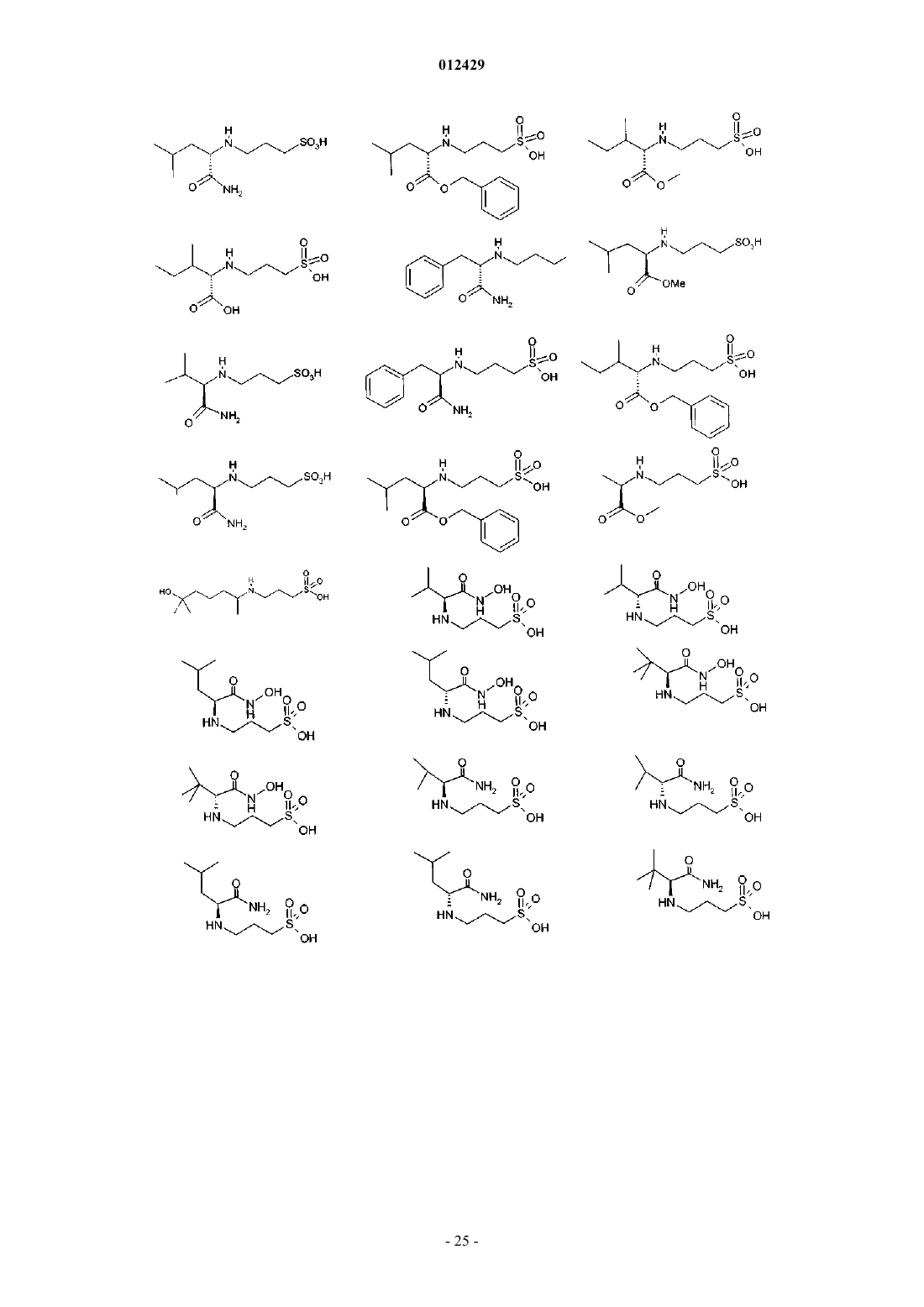
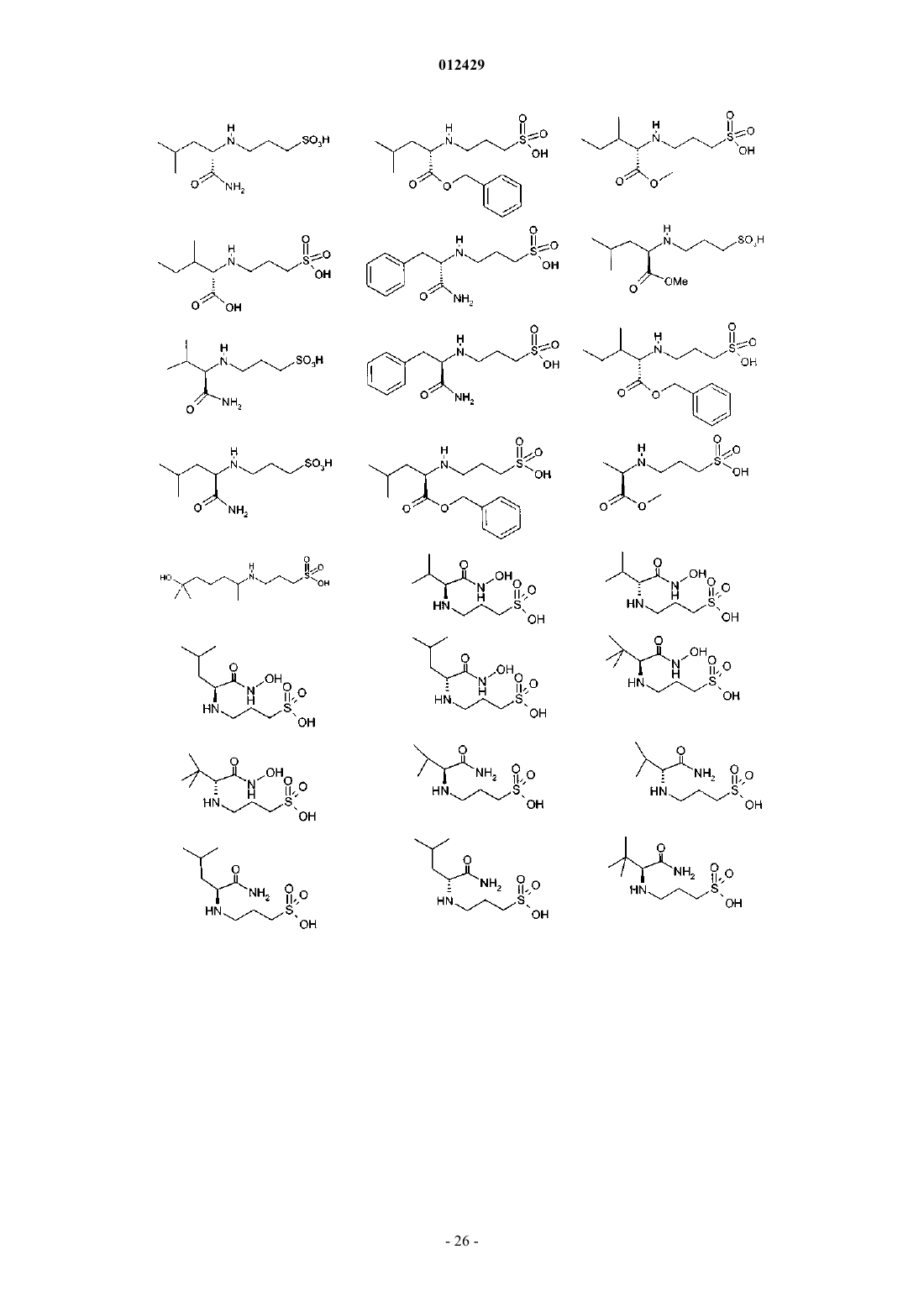
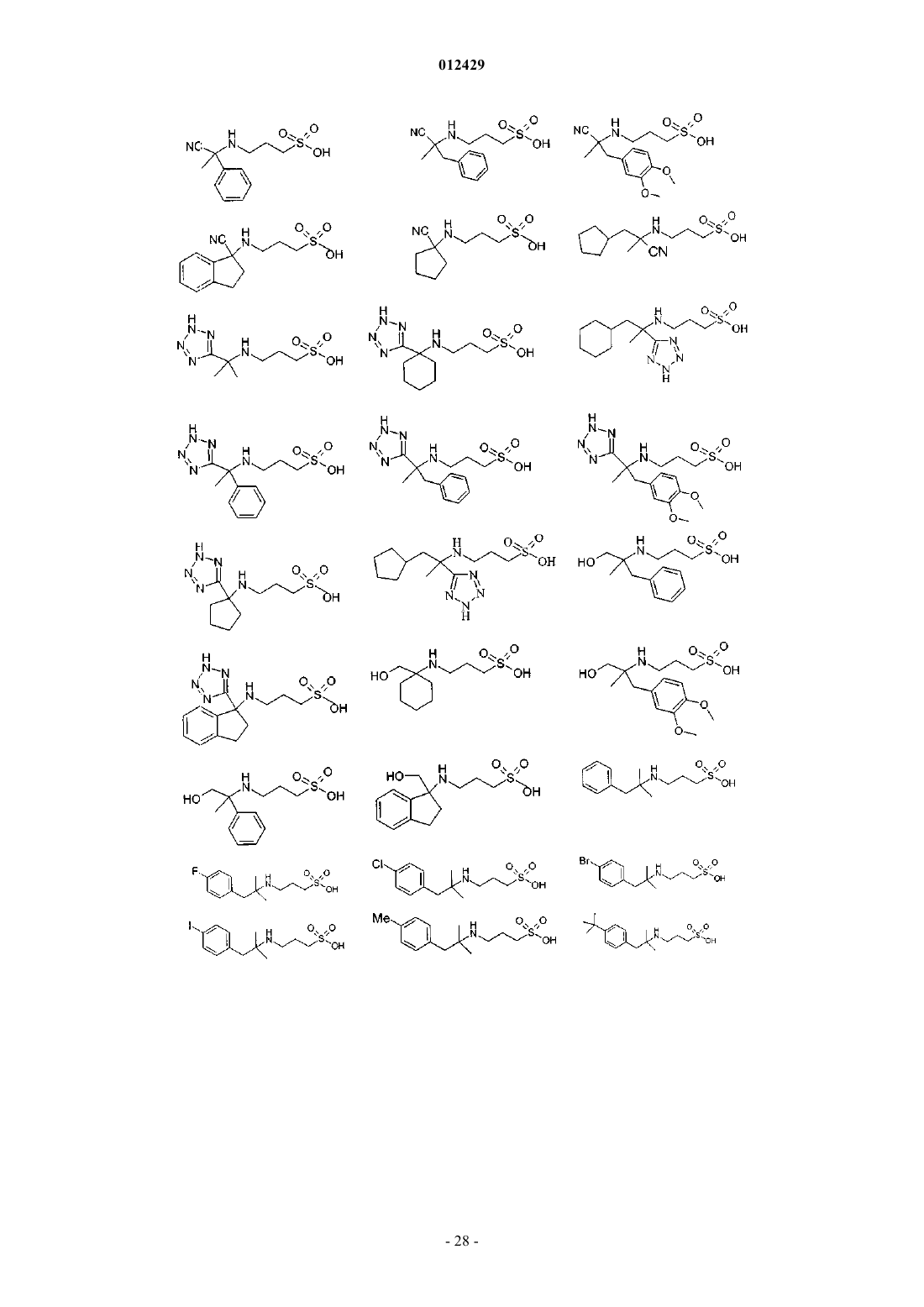
25. Применение по пп.1-9, отличающееся тем, что соединение выбрано из



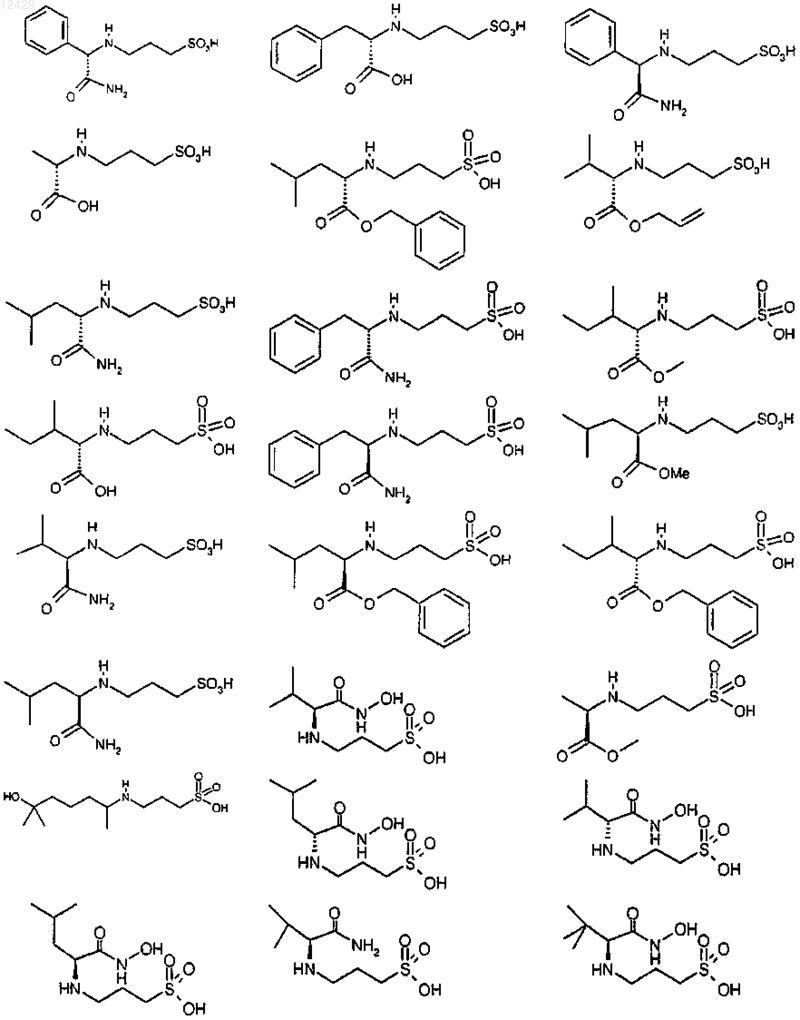
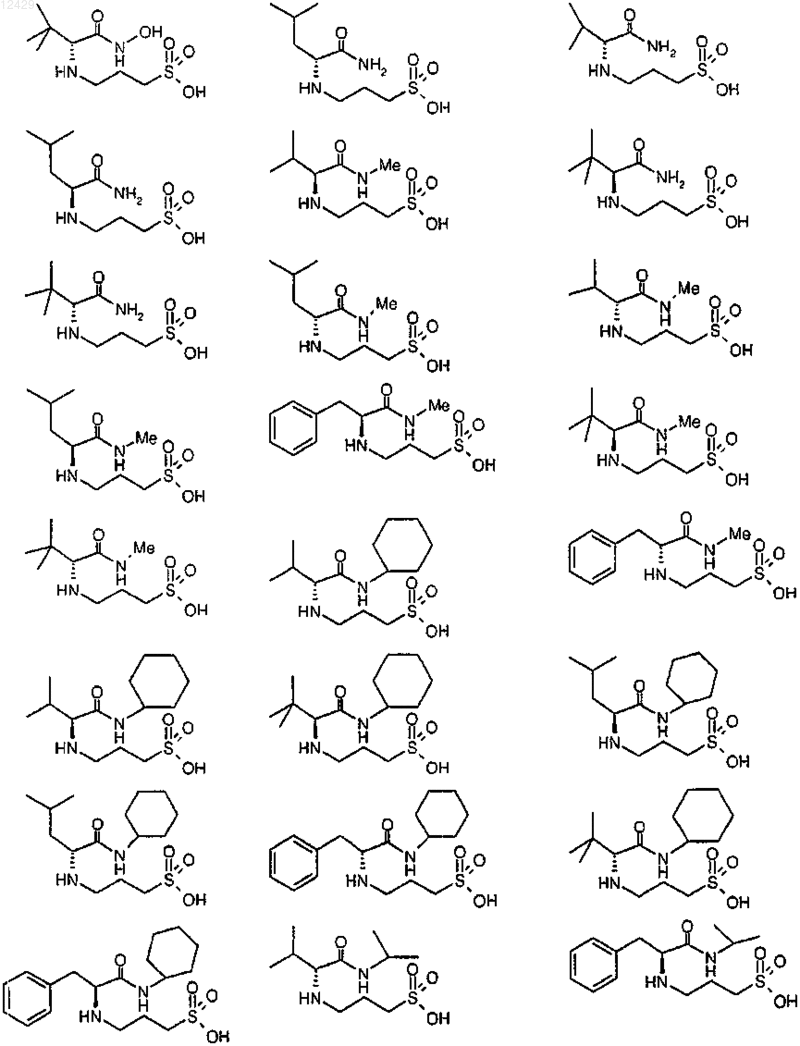
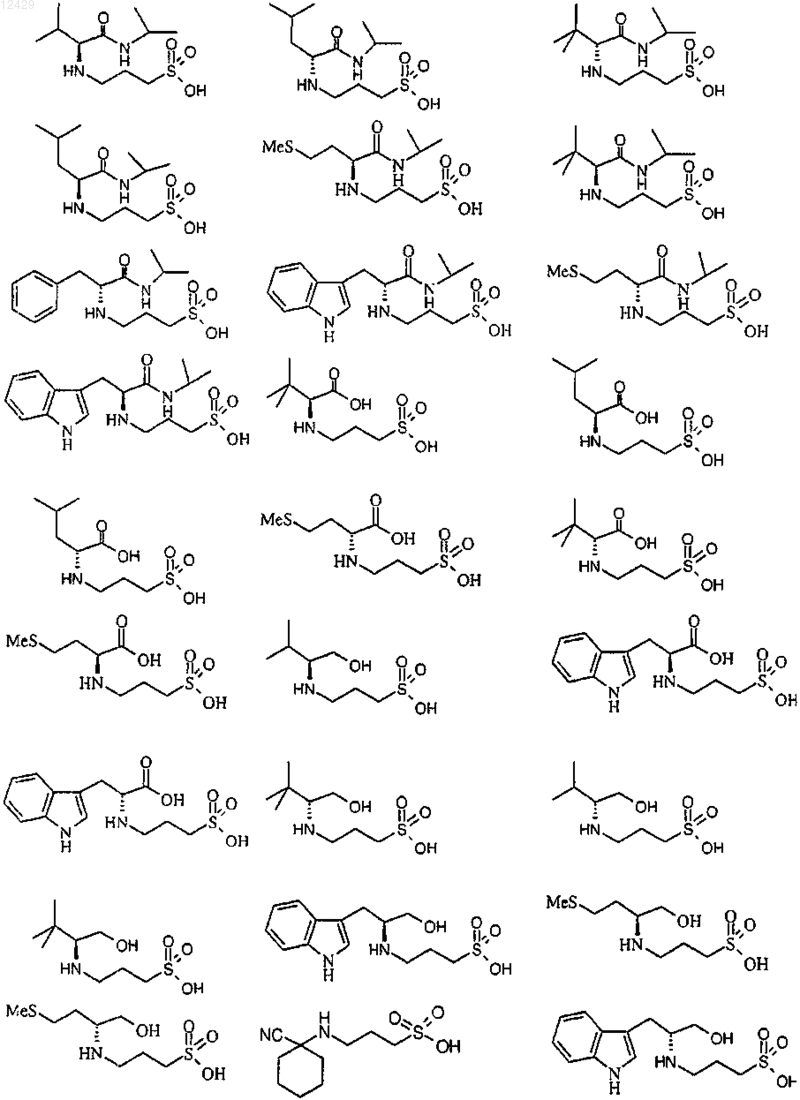
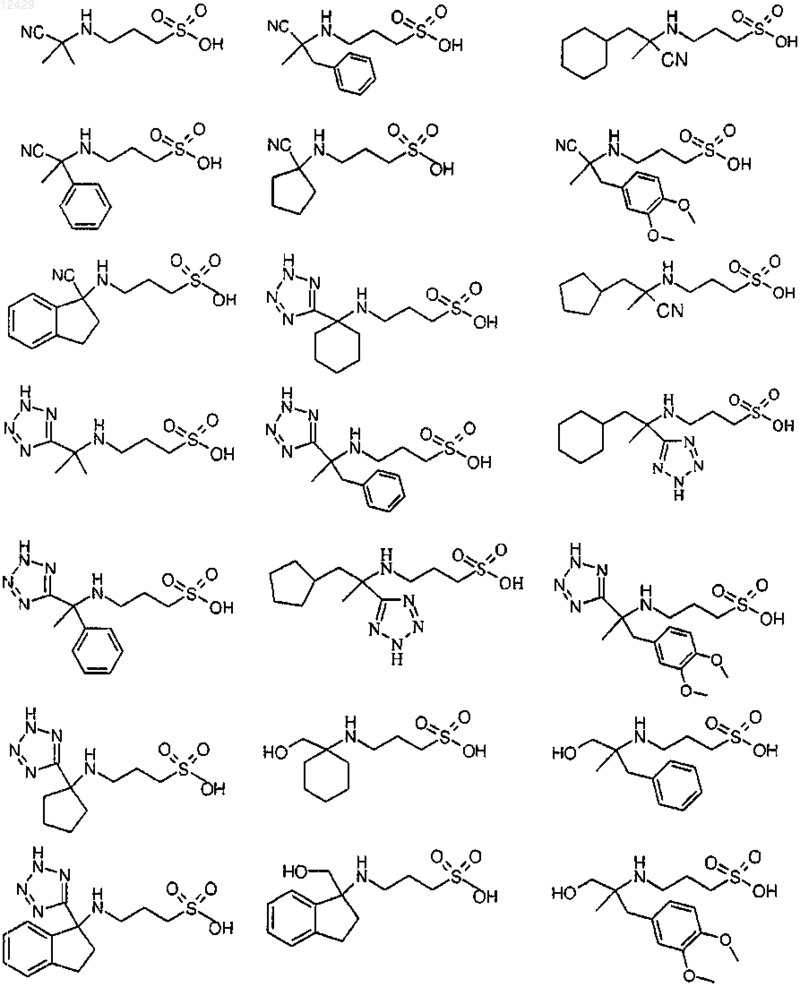
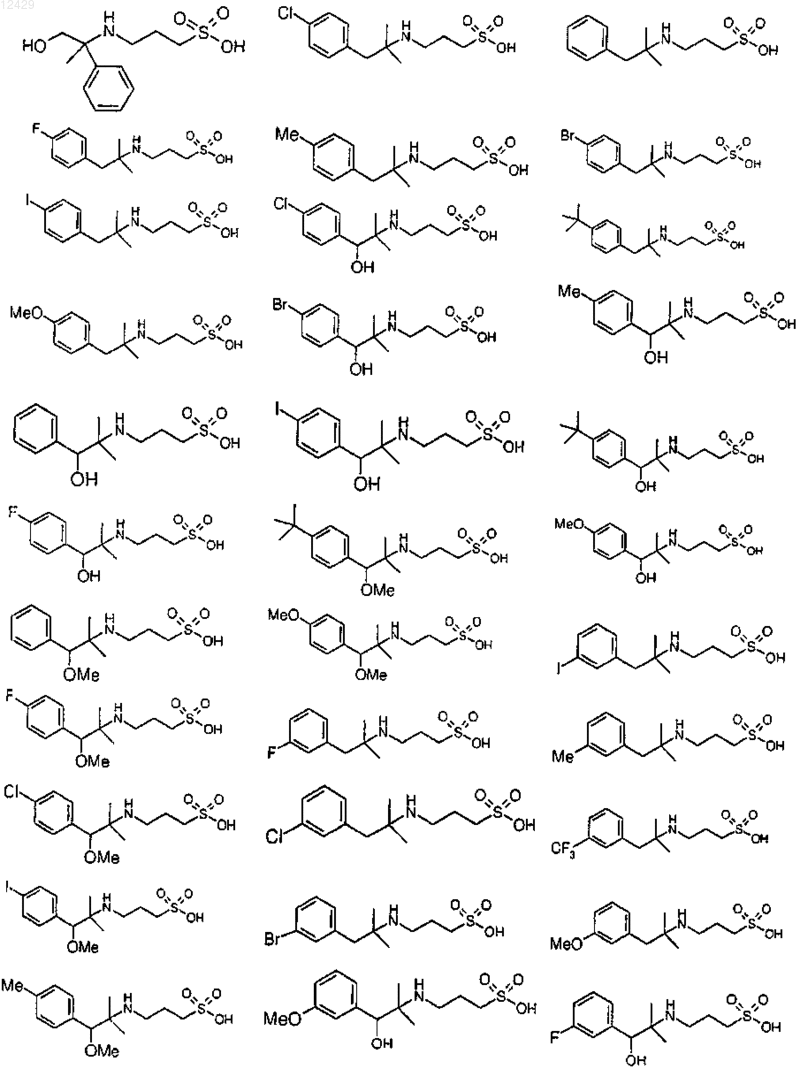
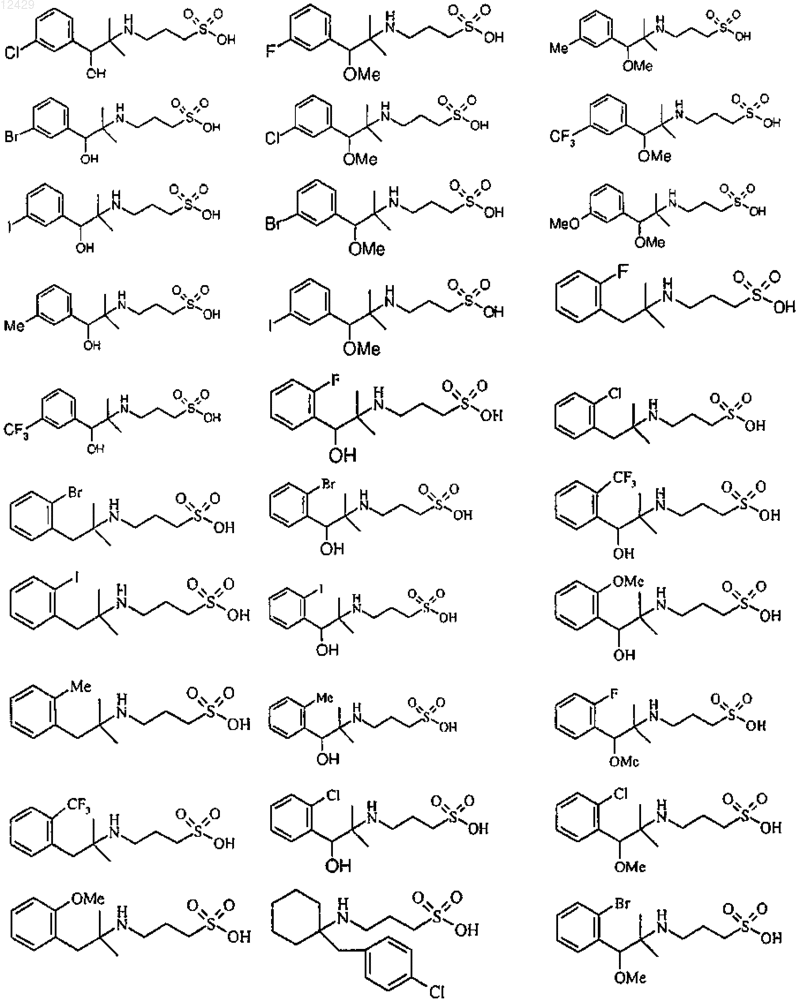
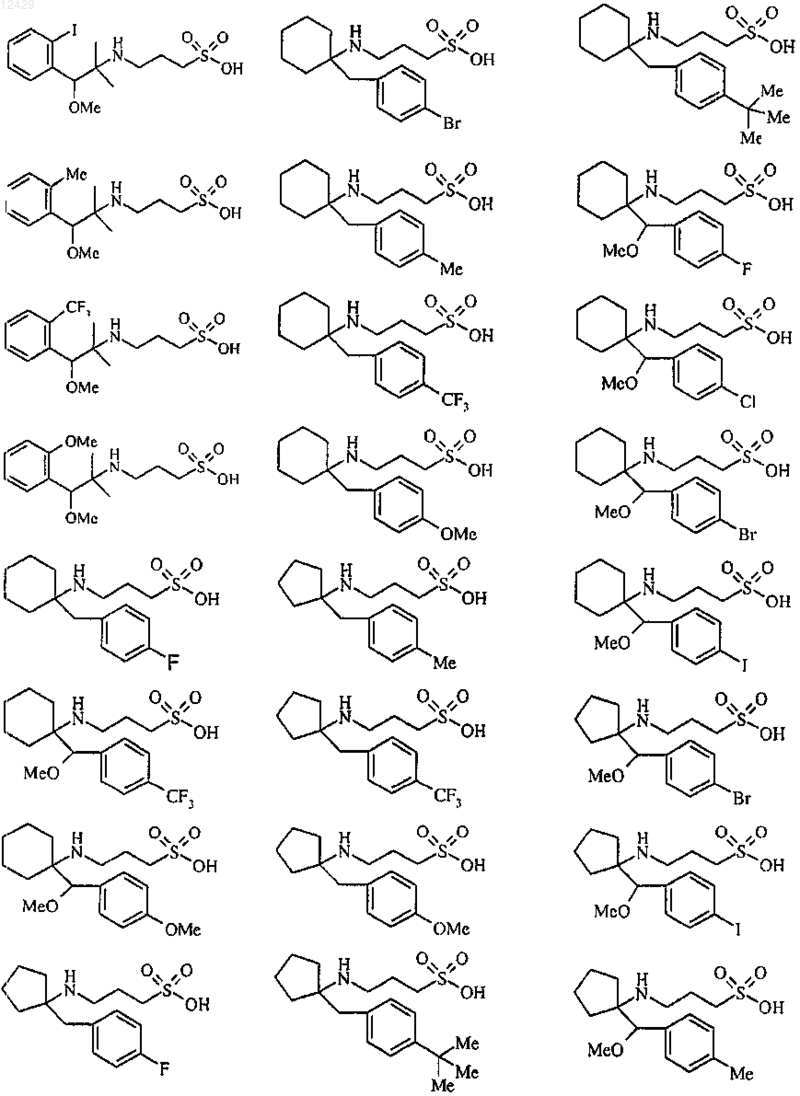
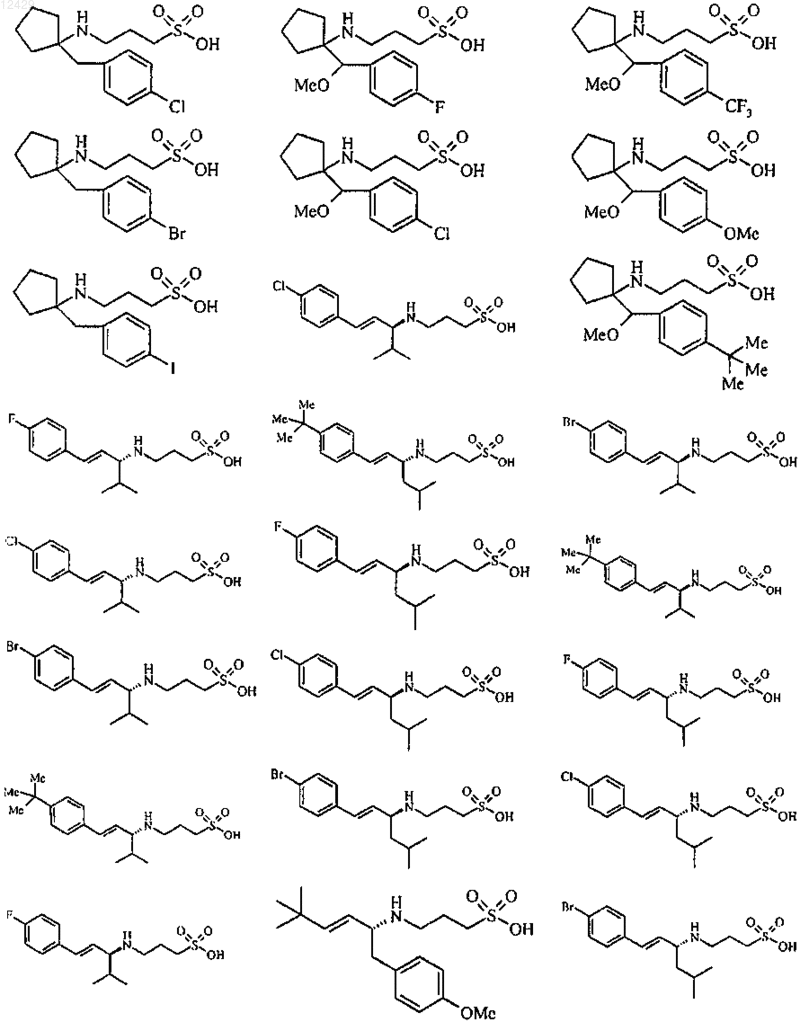
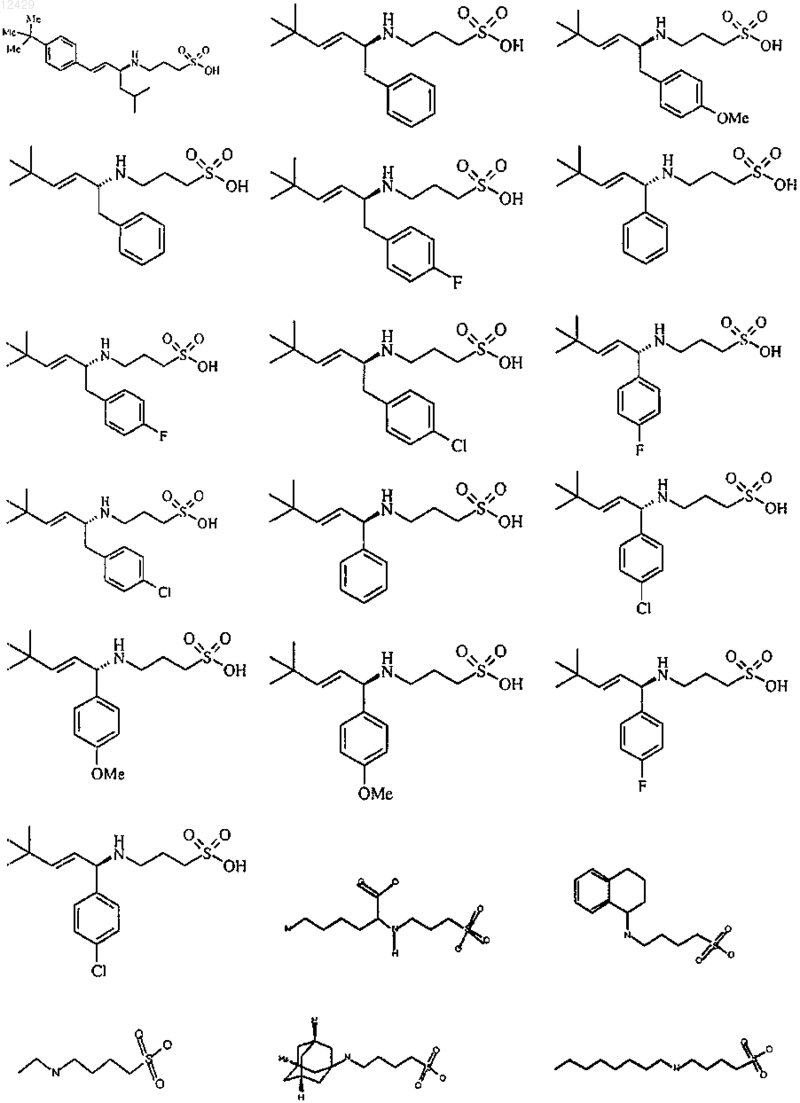
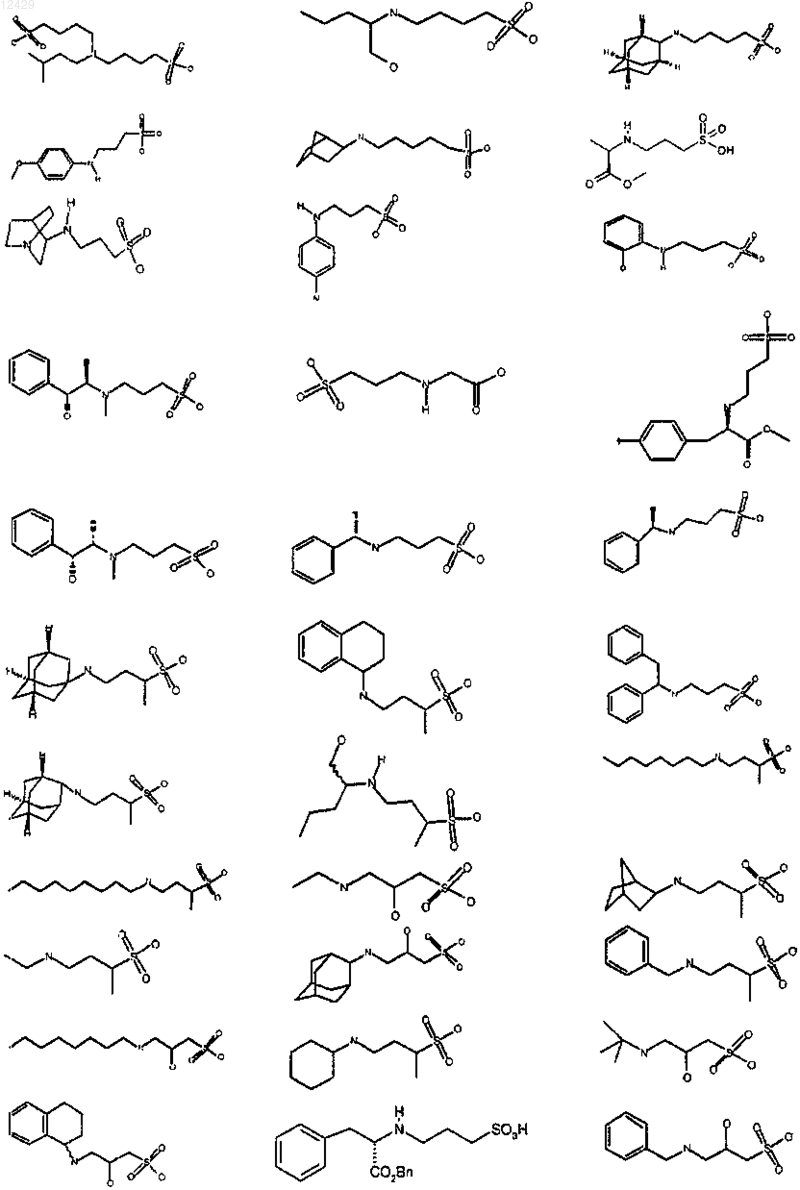
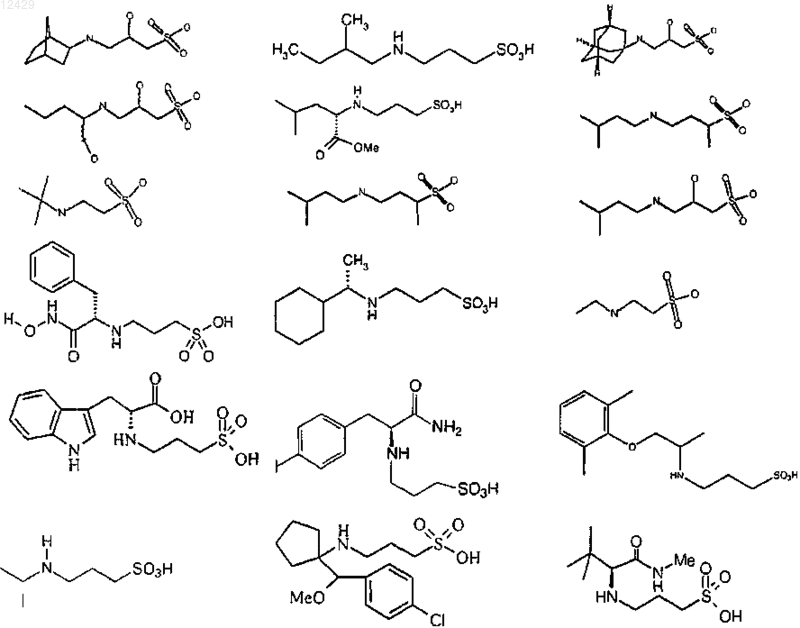
или его фармацевтически приемлемых соли, сложного эфира или пролекарства.
26. Способ лечения или предупреждения связанного с амилоидом заболевания, включающий введение субъекту эффективного количества соединения формулы (I)
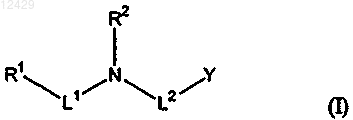
где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов, выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных колец;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;
L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,
при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН2)3- и Y обозначает SO3-Х+; R1 не обозначает фенил, 1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептшы, н-октил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил, 1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил, 5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2-(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,
или его фармацевтически приемлемой соли, сложного эфира или пролекарства.
27. Способ по п.26, отличающийся тем, что связанное с амилоидом заболевание характеризуется отложением b-амилоида.
28. Способ по п.26 или 27, отличающийся тем, что R1 обозначает водород.
29. Способ по п.26 или 27, отличающийся тем, что R1 обозначает линейный C2-C10-алкил.
30. Способ по п.29, отличающийся тем, что R1 обозначает этил, н-пентил, н-гептил, н-октил или н-нонил.
31. Способ по п.26 или 27, отличающийся тем, что R1 обозначает трет-бутил.
32. Способ по п.31, отличающийся тем, что соединение представляет собой 3-(трет-бутил)амино-1-пропансульфоновую кислоту или ее фармацевтически приемлемую соль, сложный эфир или пролекарство.
33. Способ по п.26 или 27, отличающийся тем, что R1 обозначает C4-C10-циклоалкил.
34. Способ по п.33, отличающийся тем, что R1 обозначает циклоалкил, содержащий 2 или 3 конденсированных кольца.
35. Способ по п.34, отличающийся тем, что R1 обозначает С7-С10-циклоалкил, содержащий 2 конденсированных кольца.
36. Способ по п.34, отличающийся тем, что R1 обозначает циклоалкил, содержащий 2 конденсированных кольца.
37. Способ по п.36, отличающийся тем, что R1 обозначает трицикло[3.3.1.03,7]децил или адамантил.
38. Способ по п.35, отличающийся тем, что R1 обозначает бицикло[2.1.2]гептил.
39. Способ по п.37, отличающийся тем, что соединение представляет собой 3-(1-адамантил)амино-1-пропансульфоновую кислоту или ее фармацевтически приемлемую соль, сложный эфир или пролекарство.
40. Способ по любому из пп.26-39, отличающийся тем, что L2 обозначает (СН2)3.
41. Способ по любому из пп.26-39, отличающийся тем, что L2 обозначает замещенный C2-C5-алкил.
42. Способ по п.41, отличающийся тем, что L2 выбран из -CH2CH2CH(CH3)- и CH2CH(OH)CH2-.
43. Способ по п.26 или 27, отличающийся тем, что соединение выбрано из
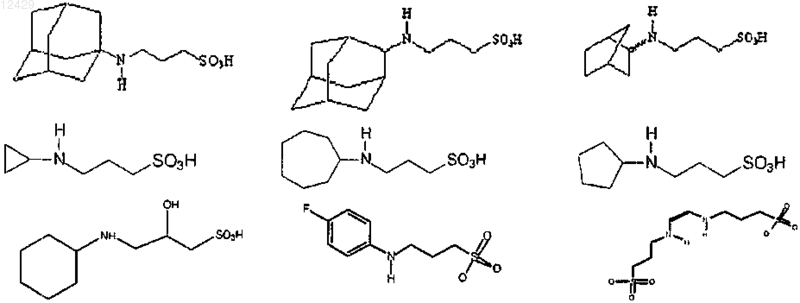
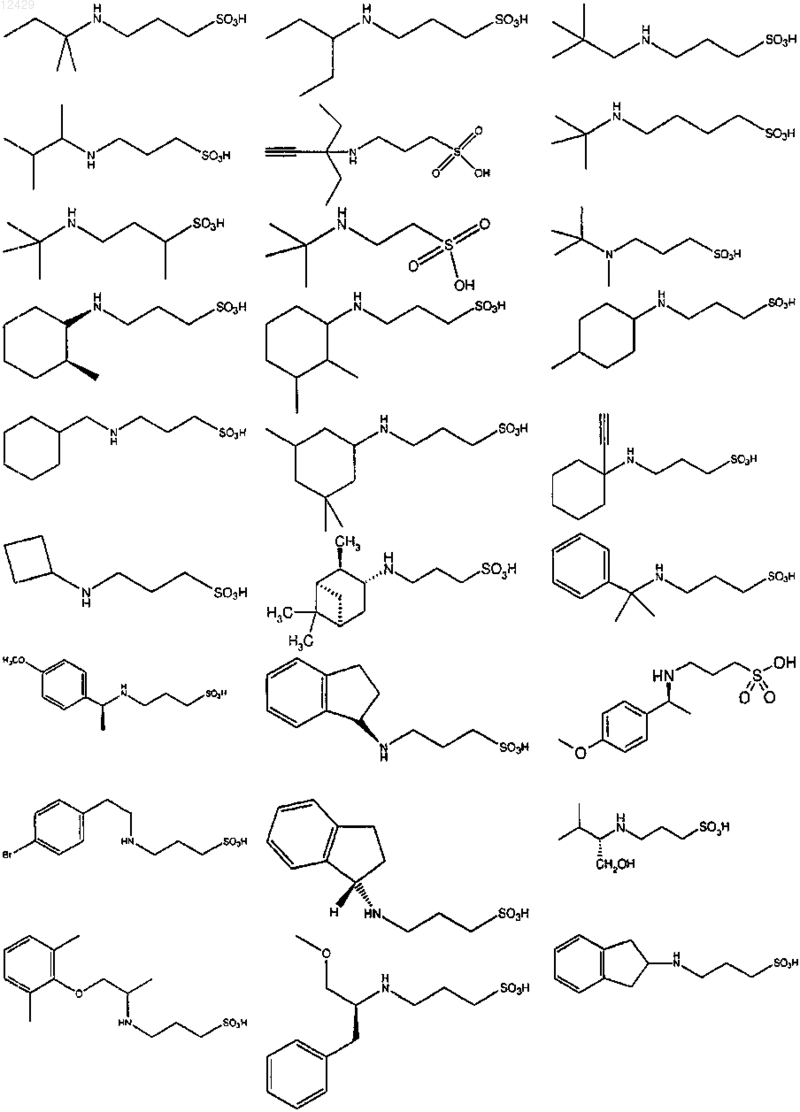
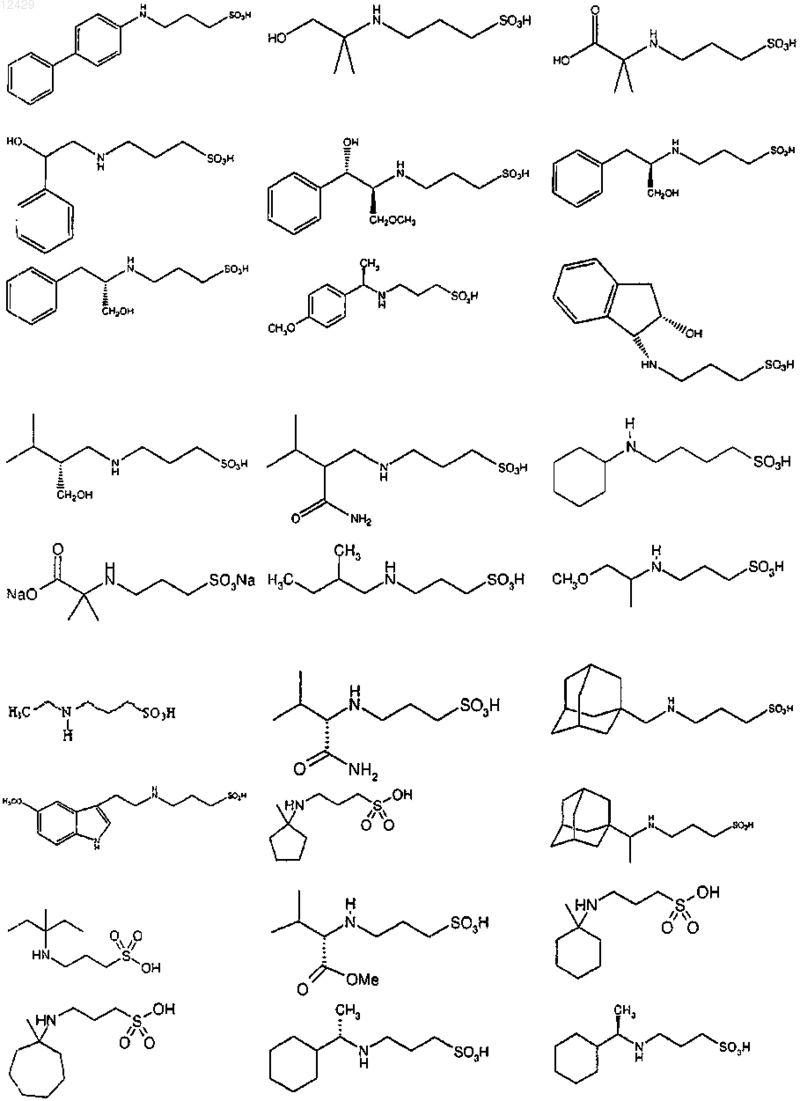
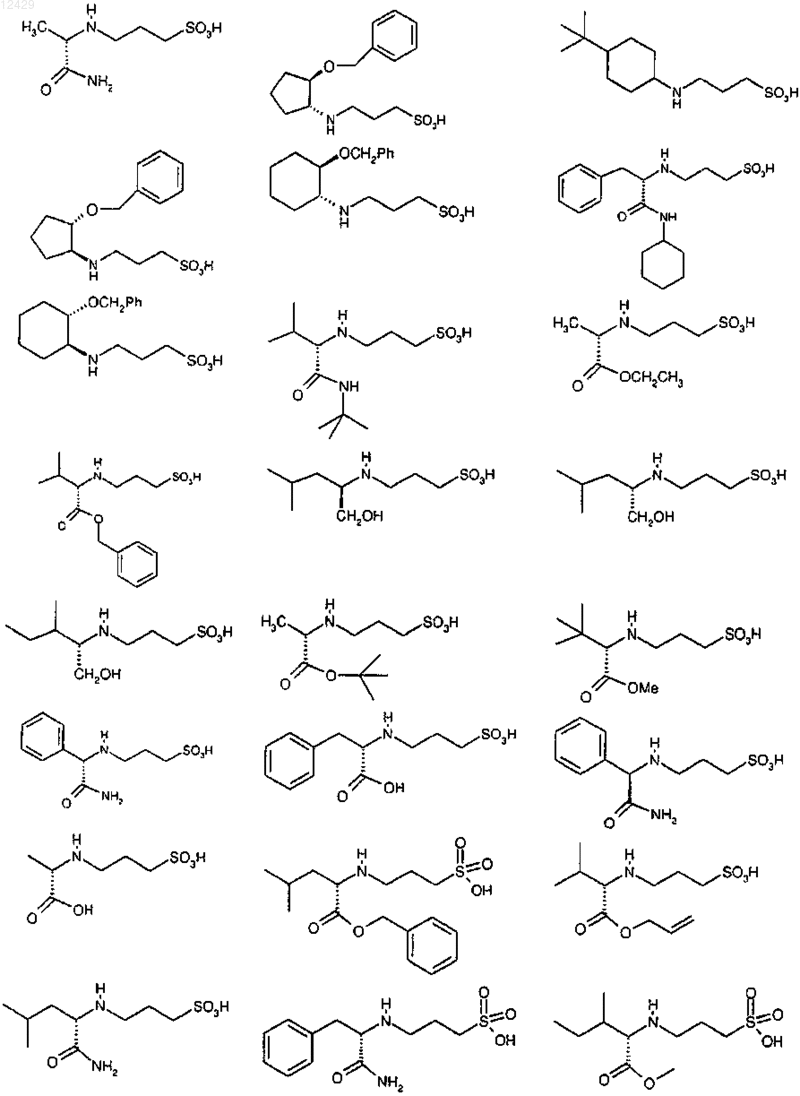
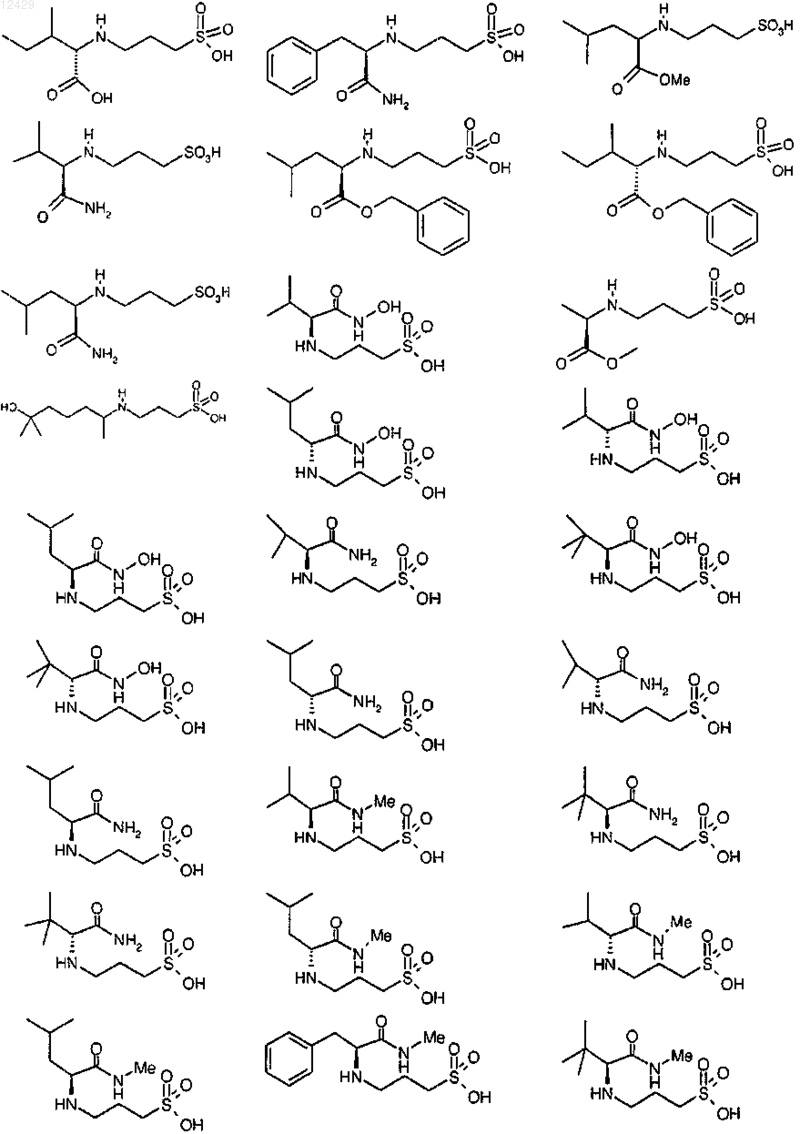
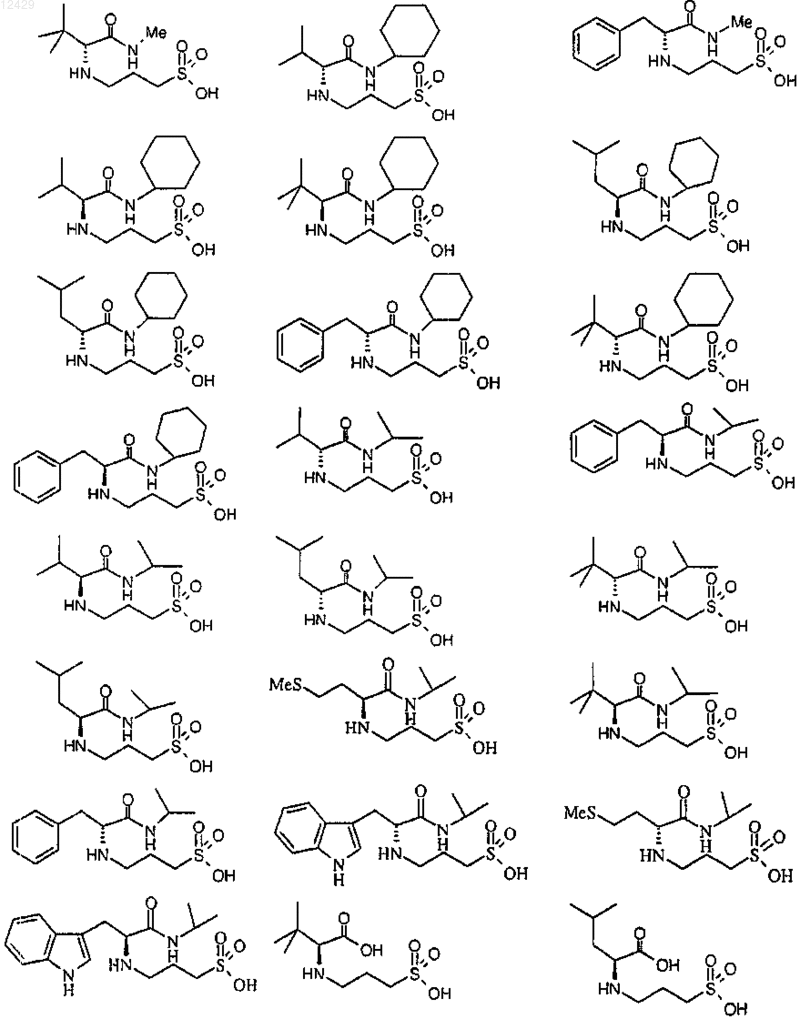
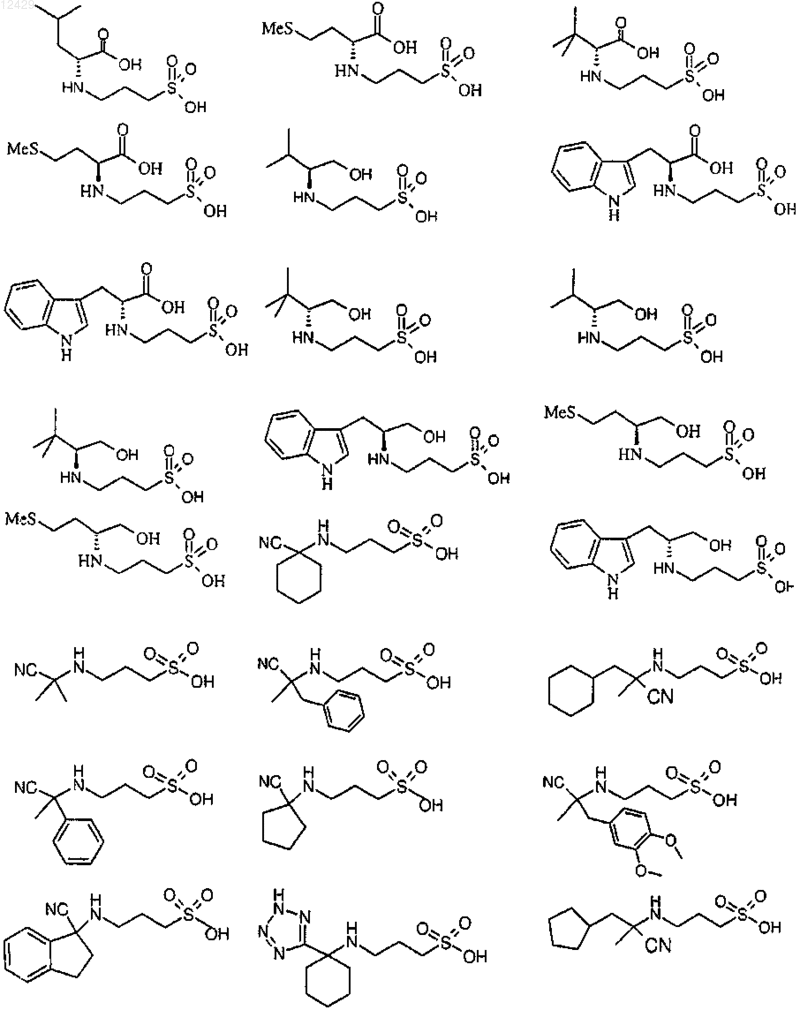
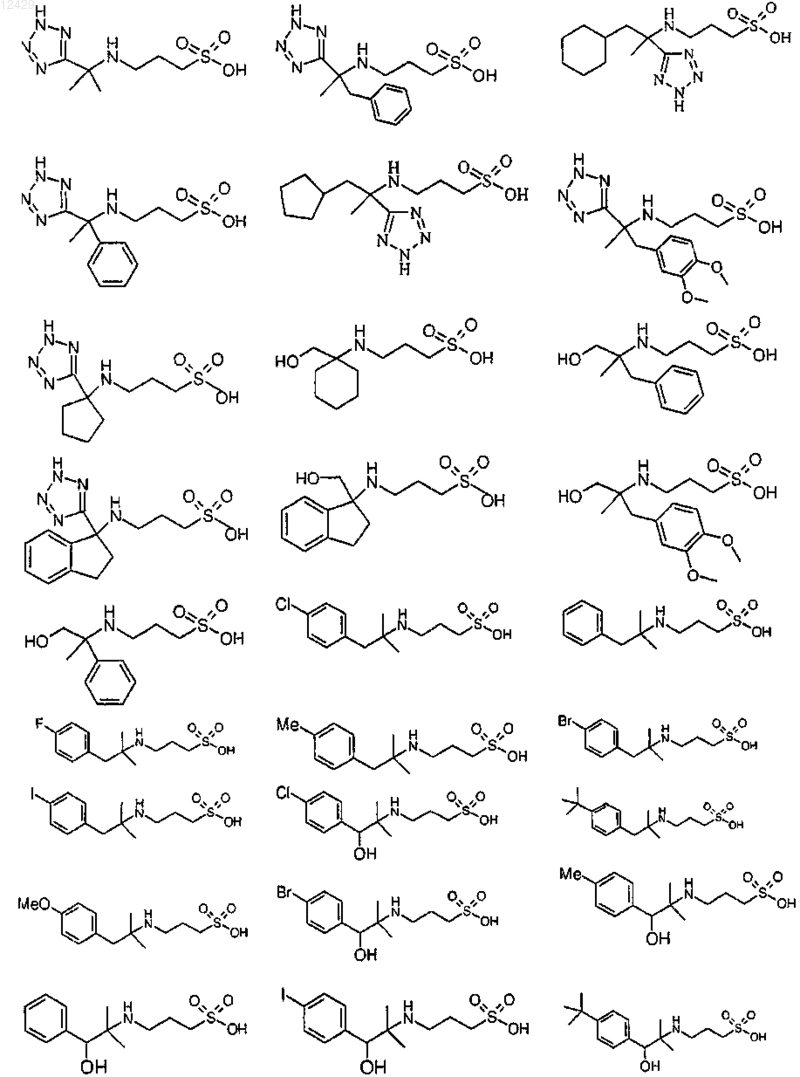
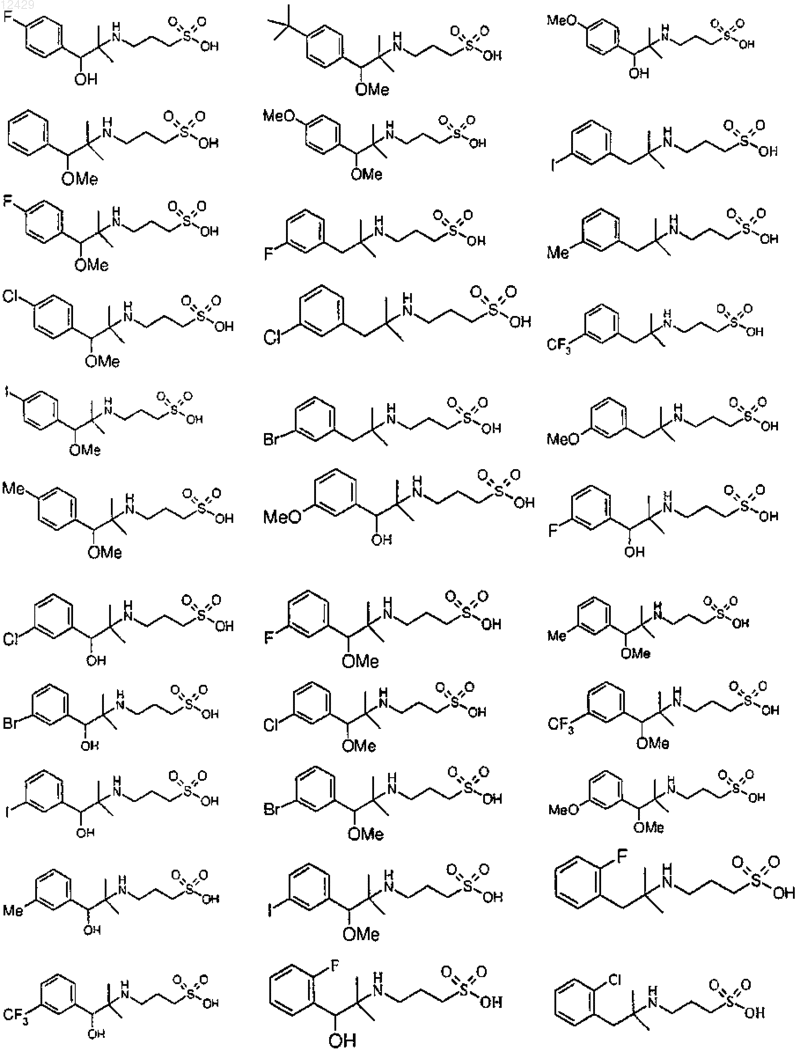
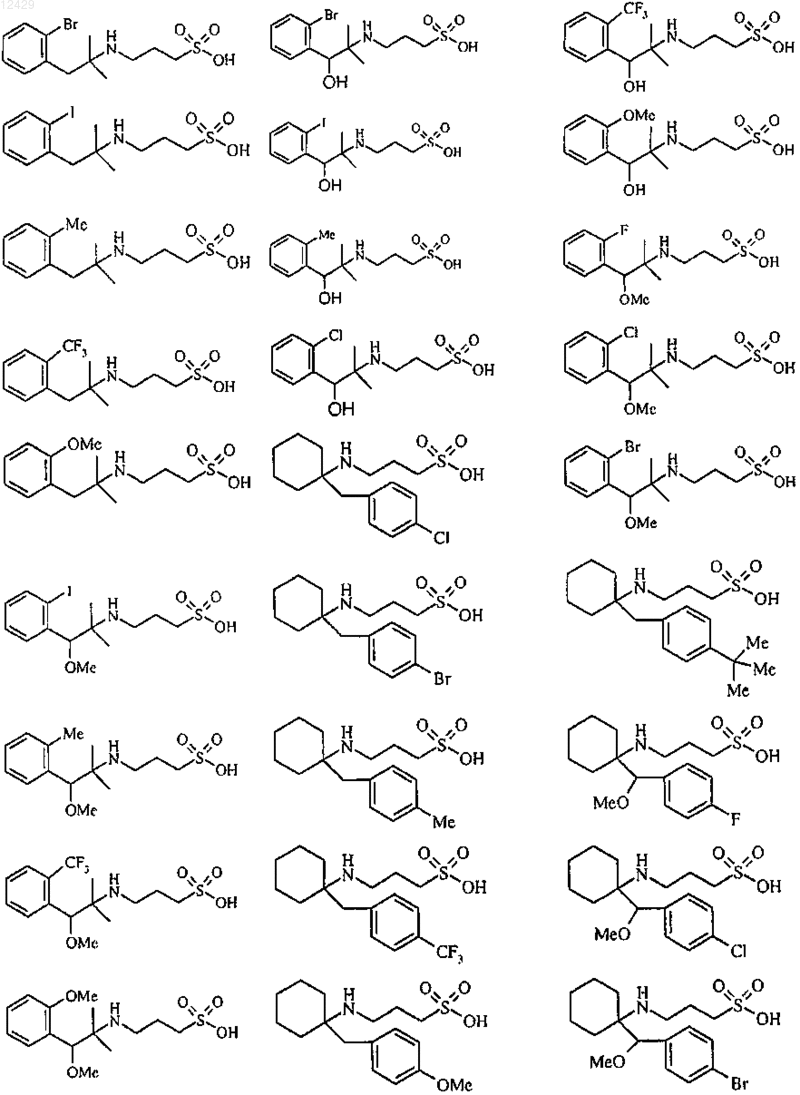
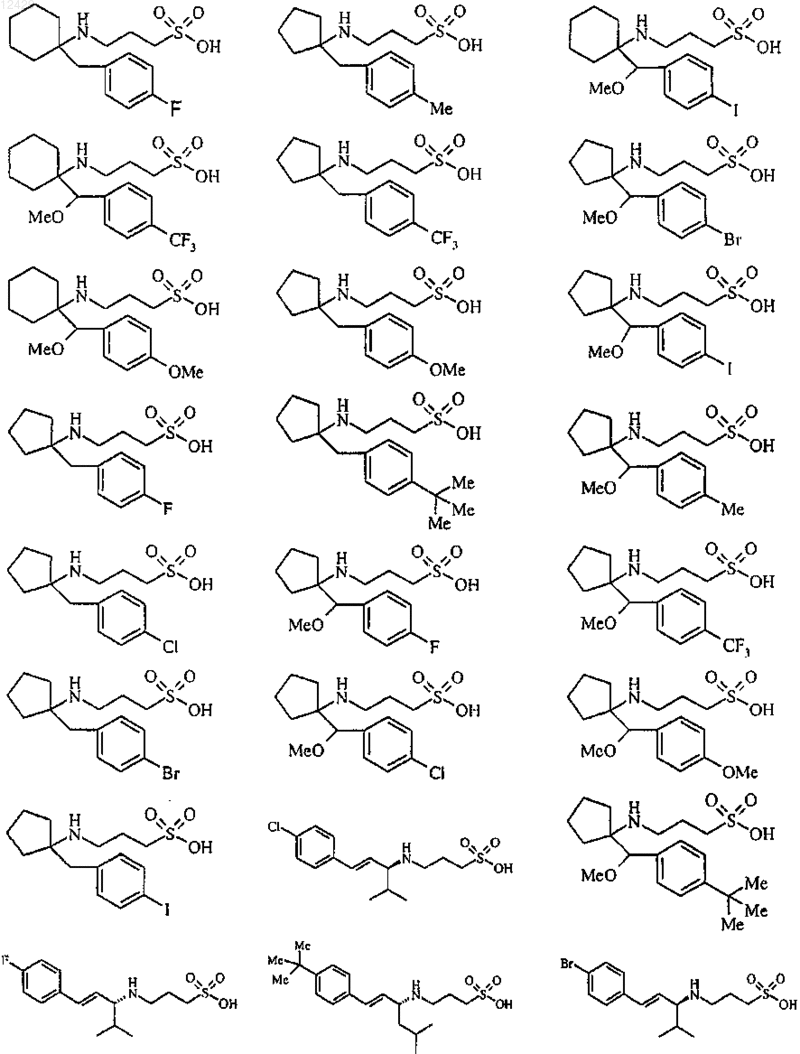
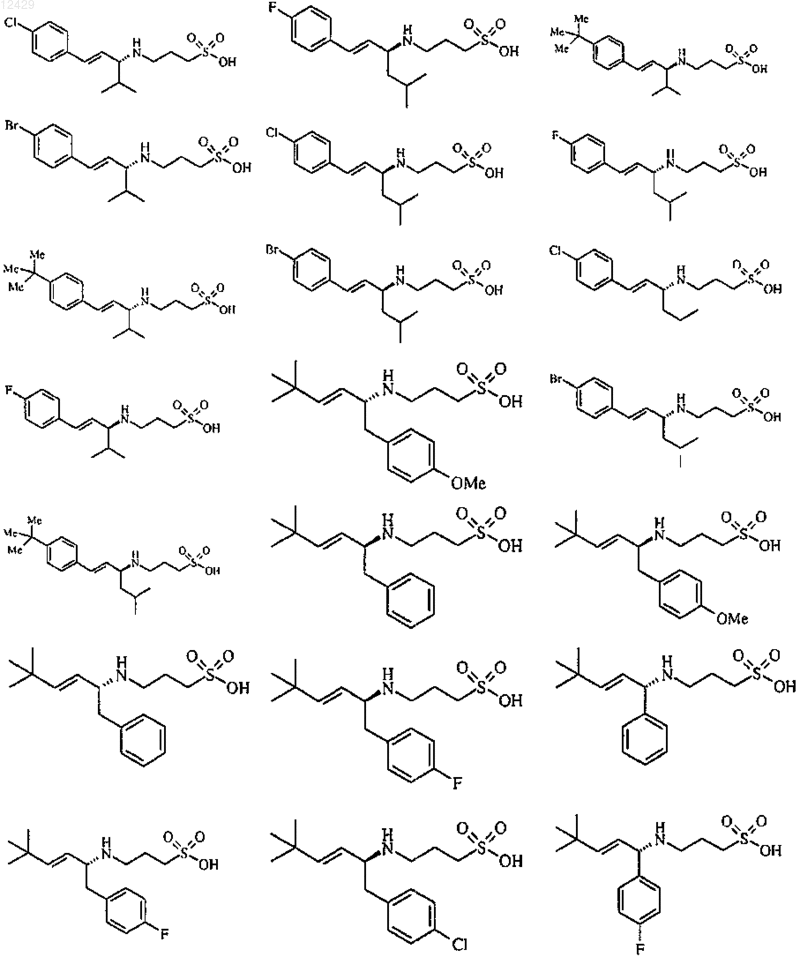
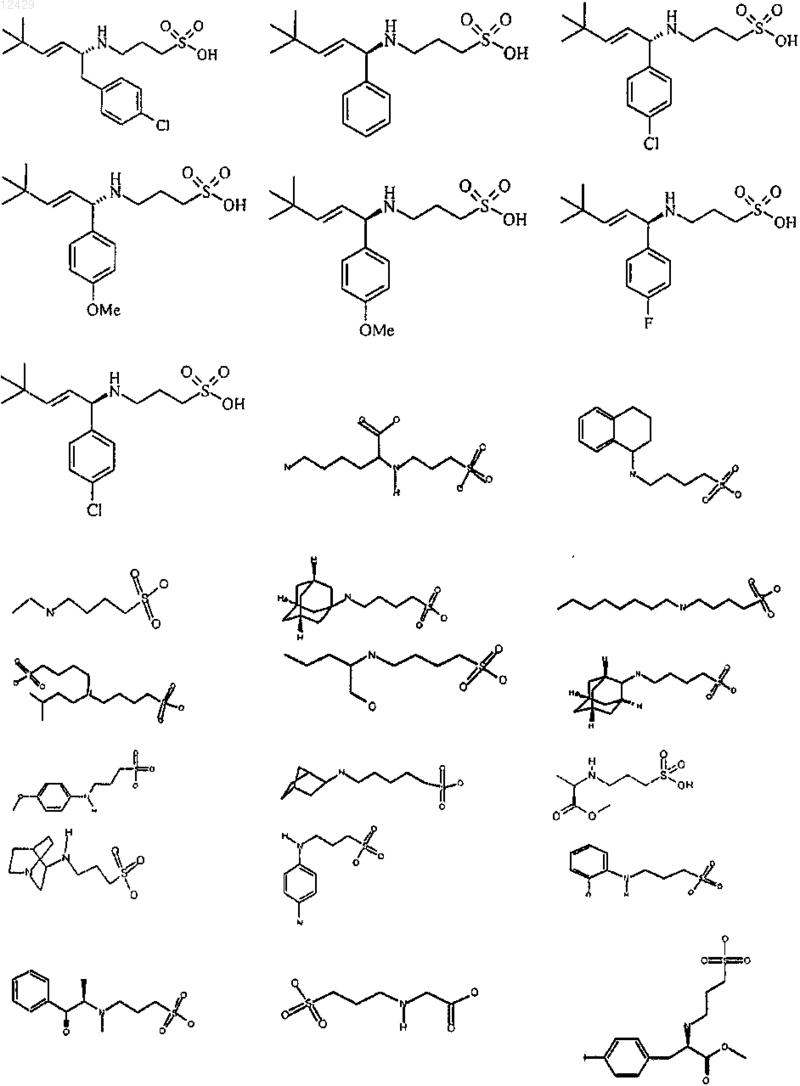
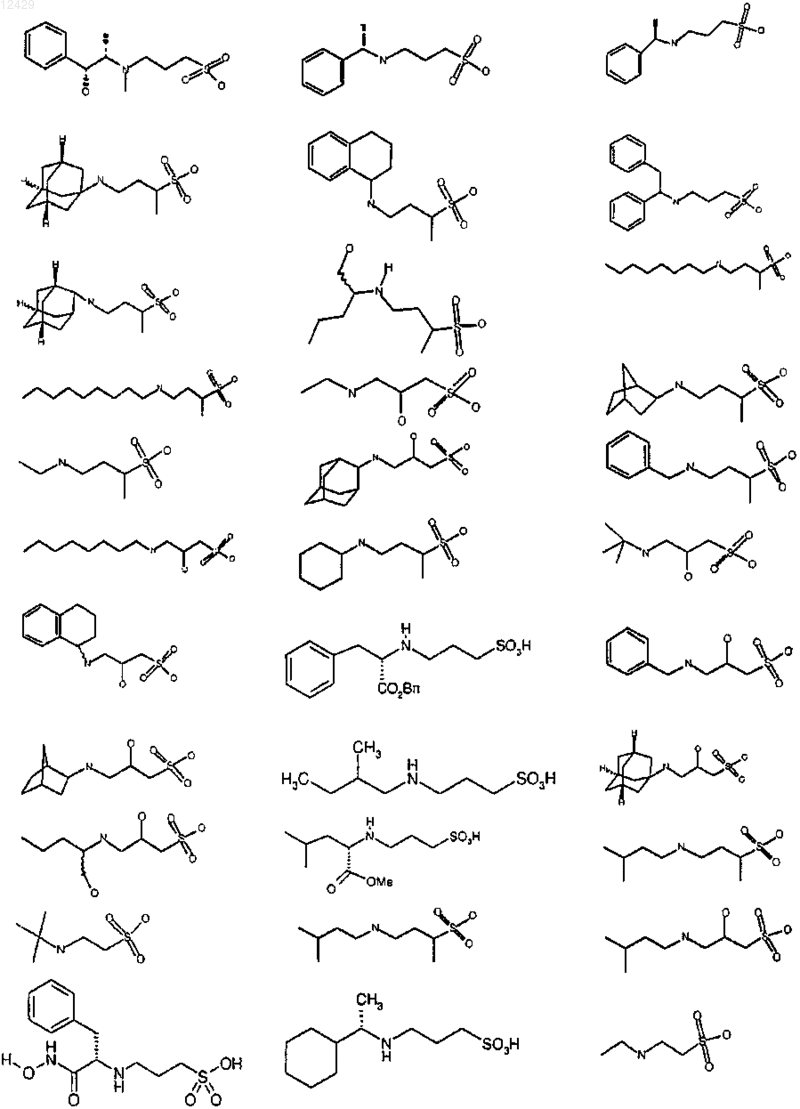
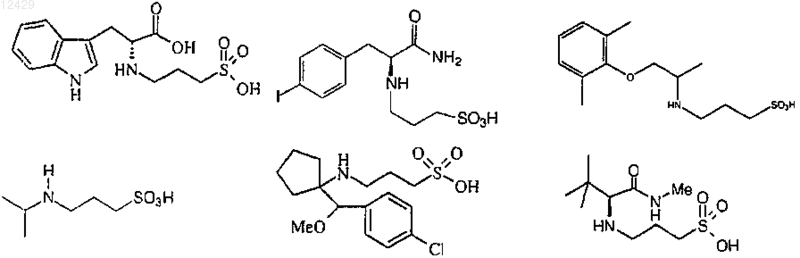
или его фармацевтически приемлемой соли, сложного эфира или пролекарства.
44. Соединение формулы (I), как определено в п.1, или его фармацевтически приемлемая соль, сложный эфир или пролекарство, выбранное из группы, включающей
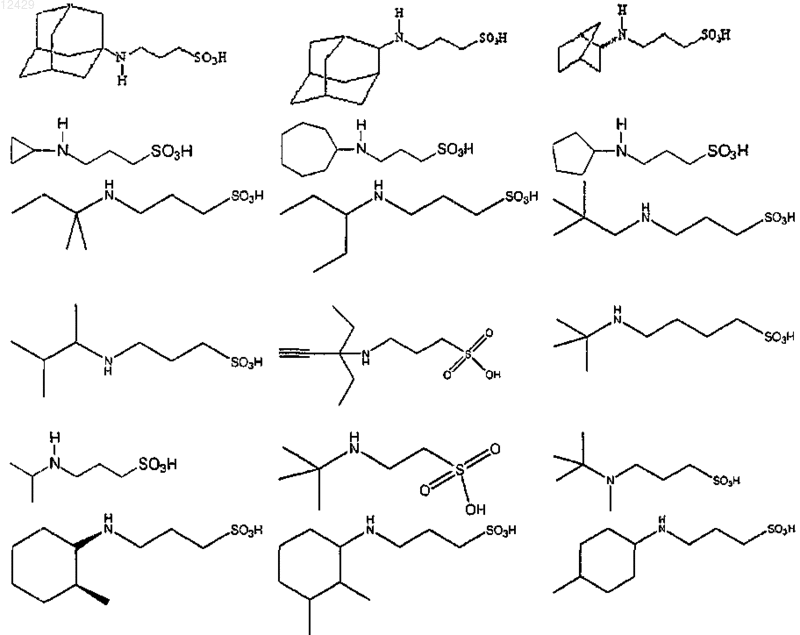
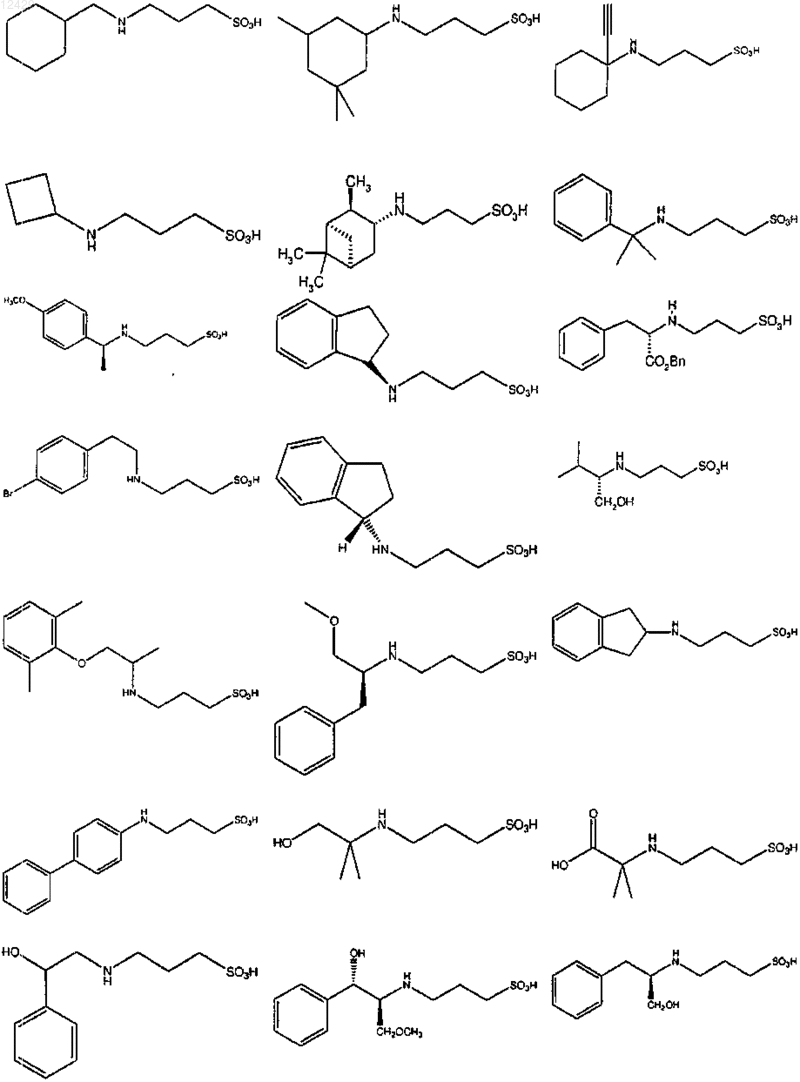
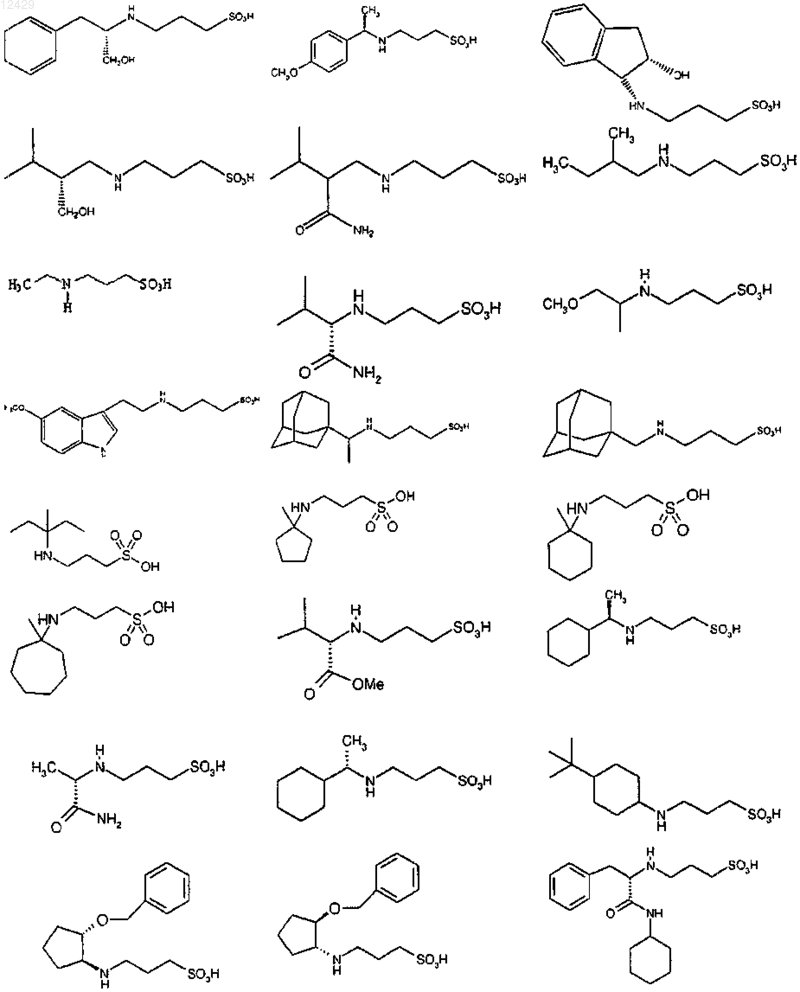
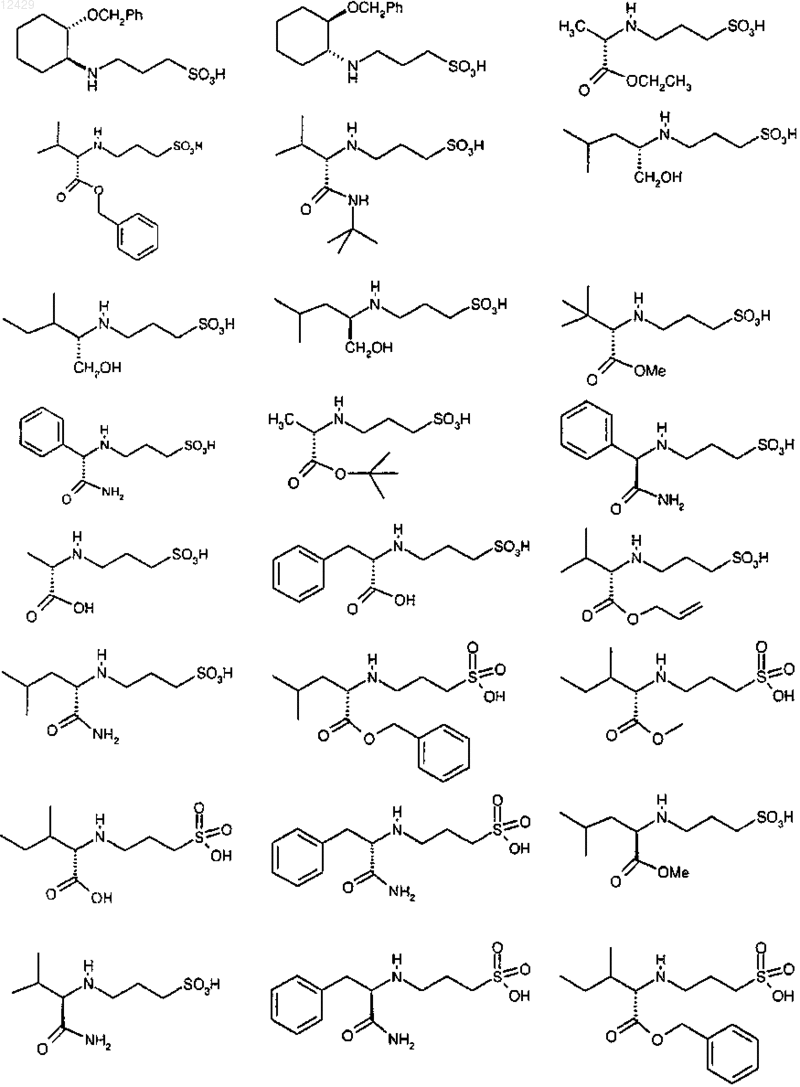
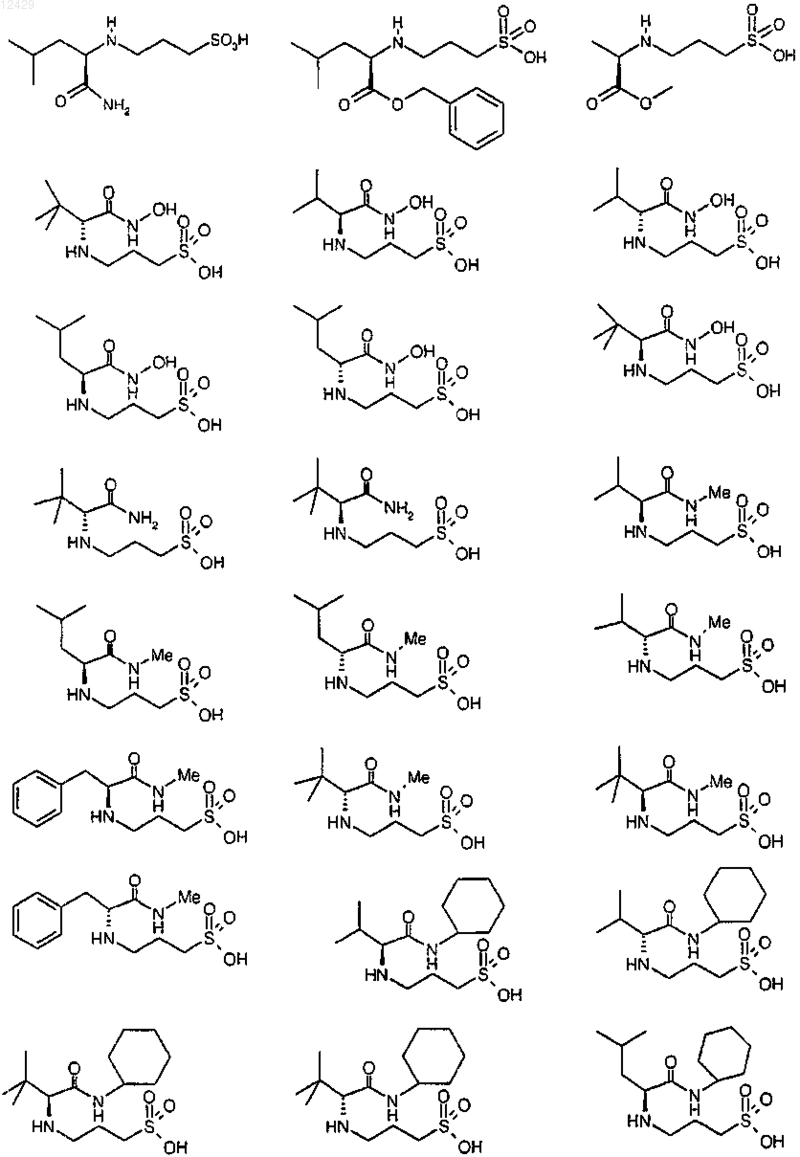
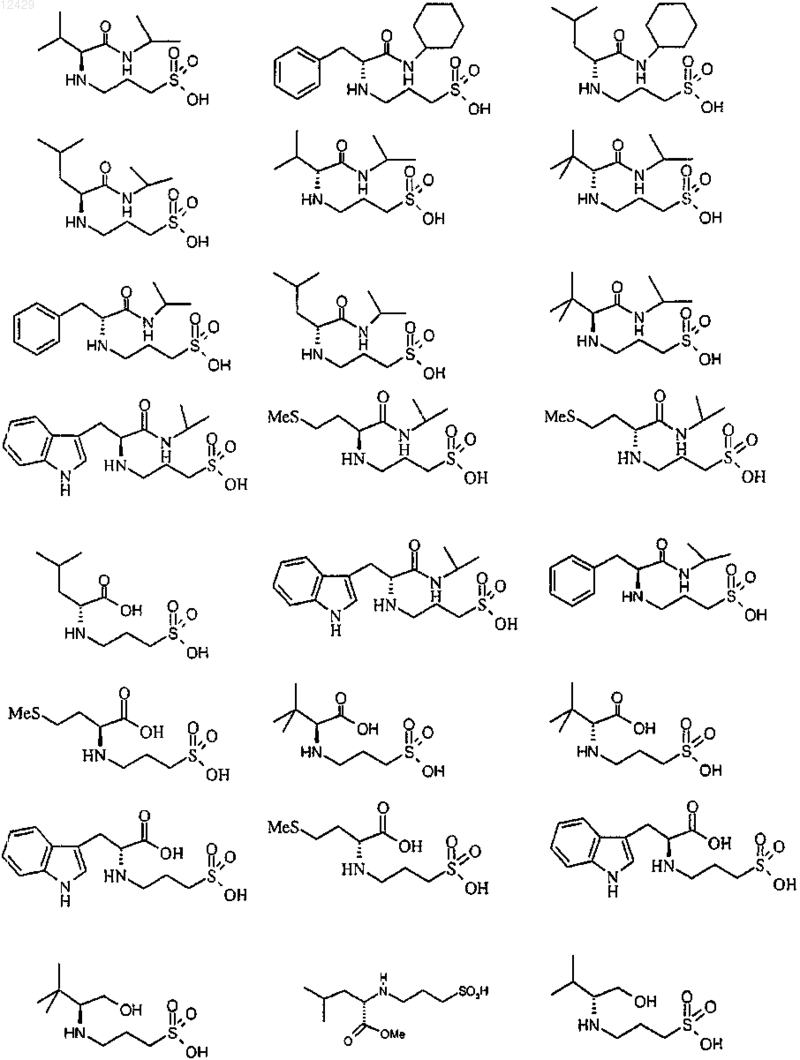
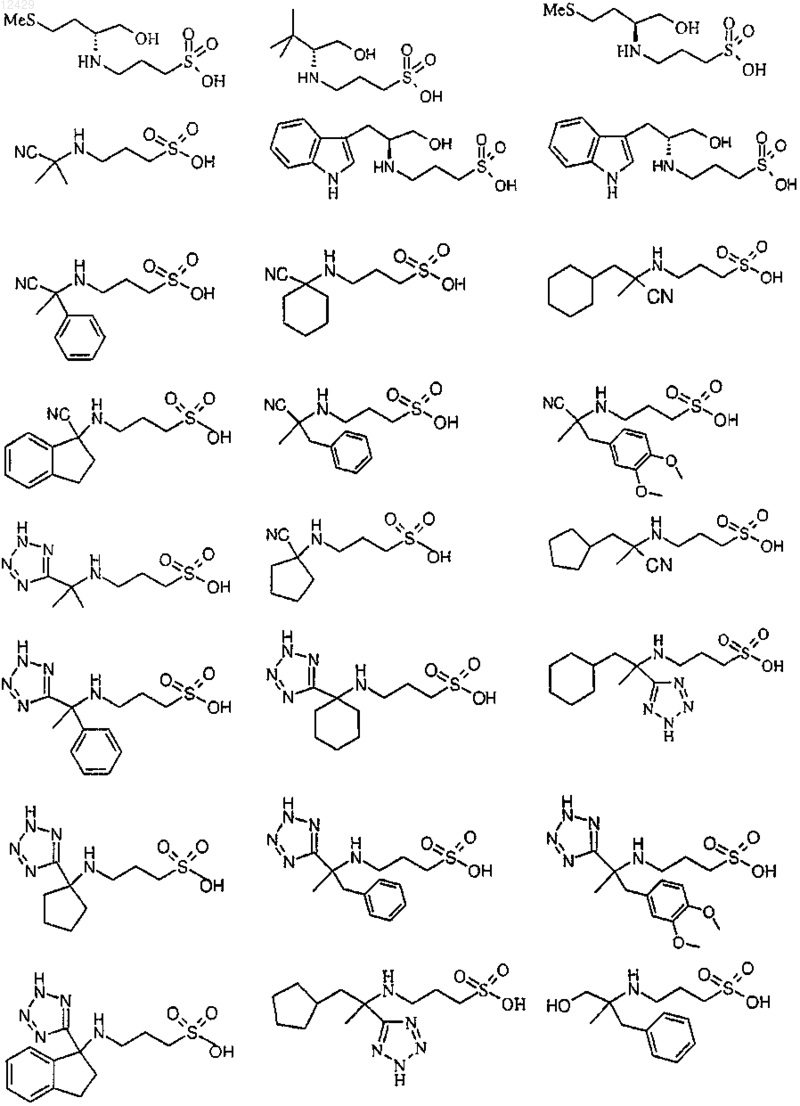
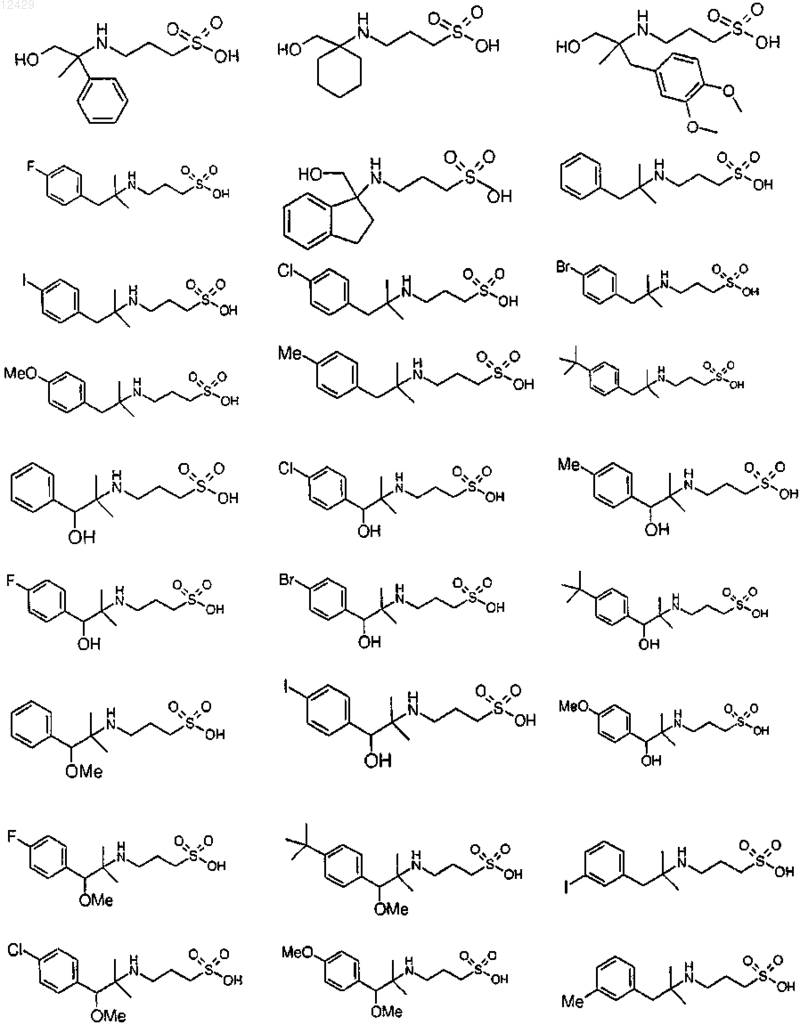
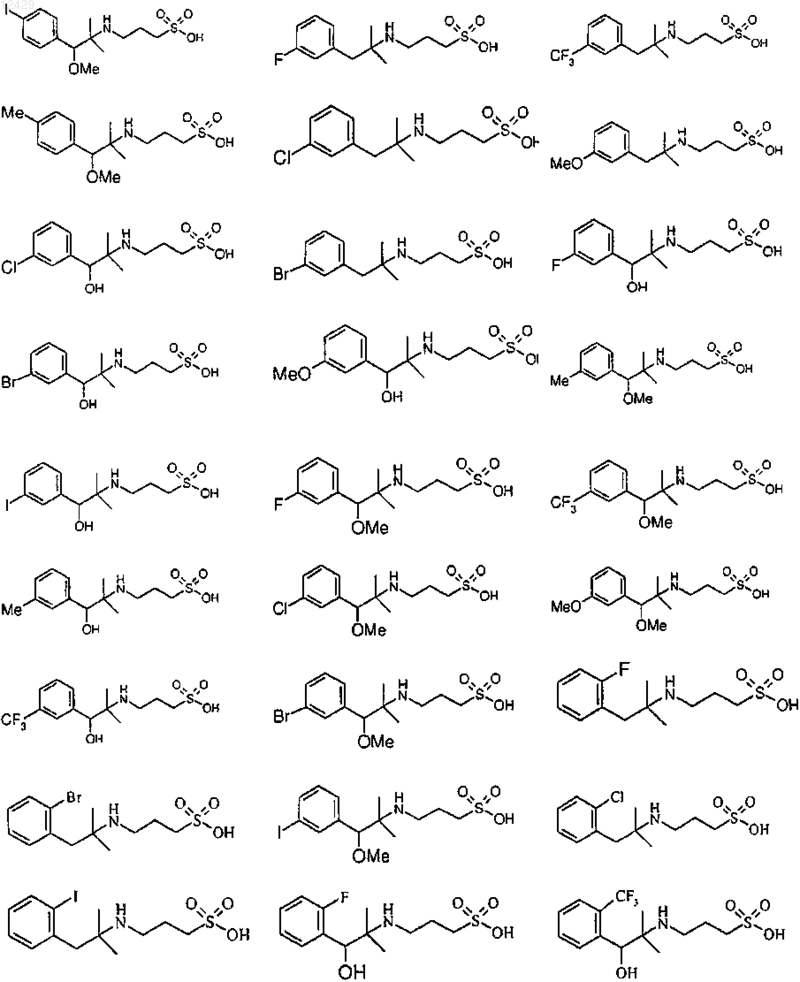
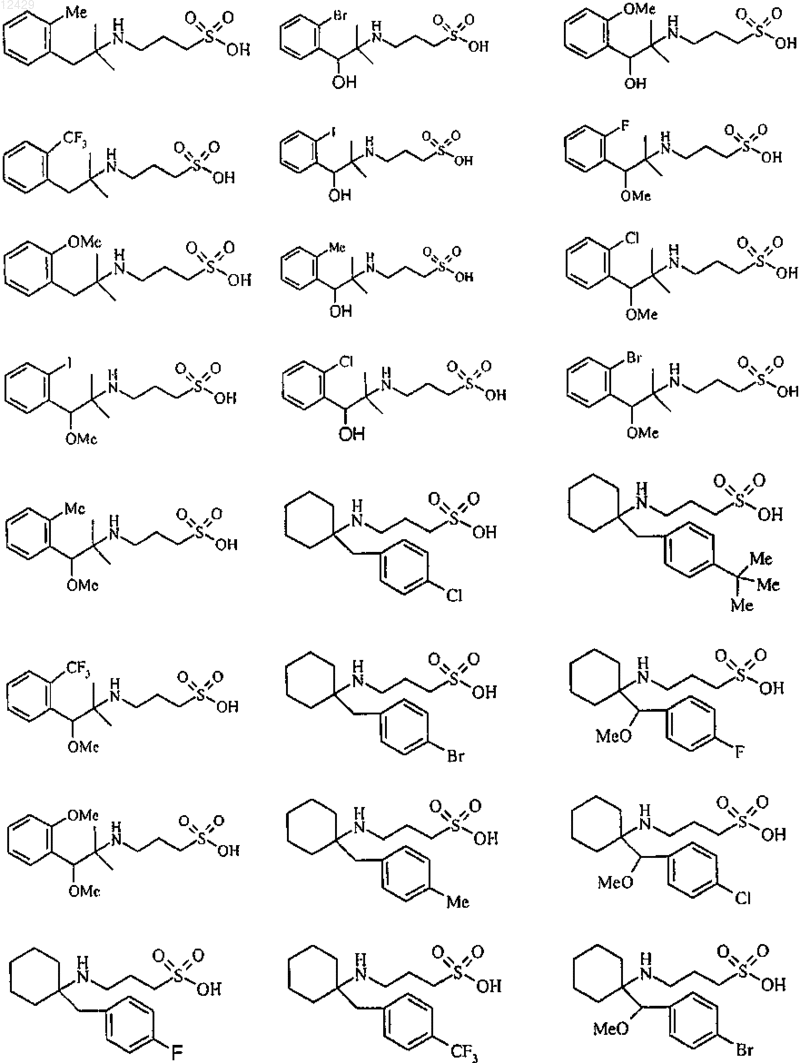
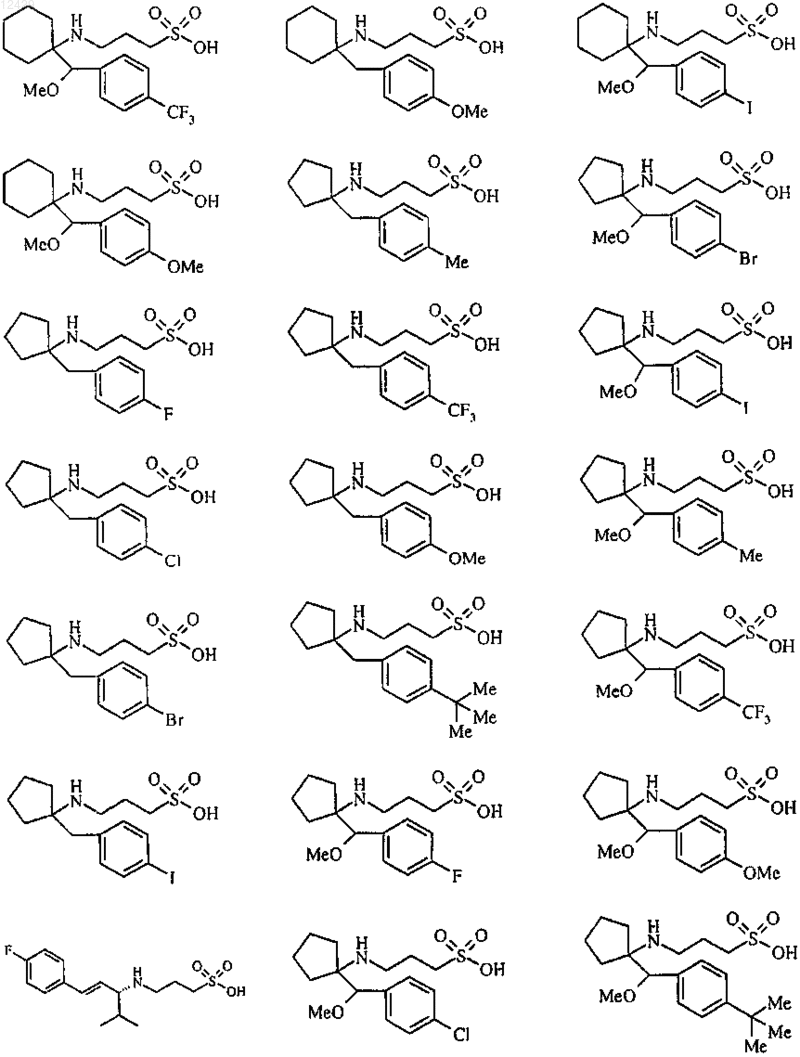
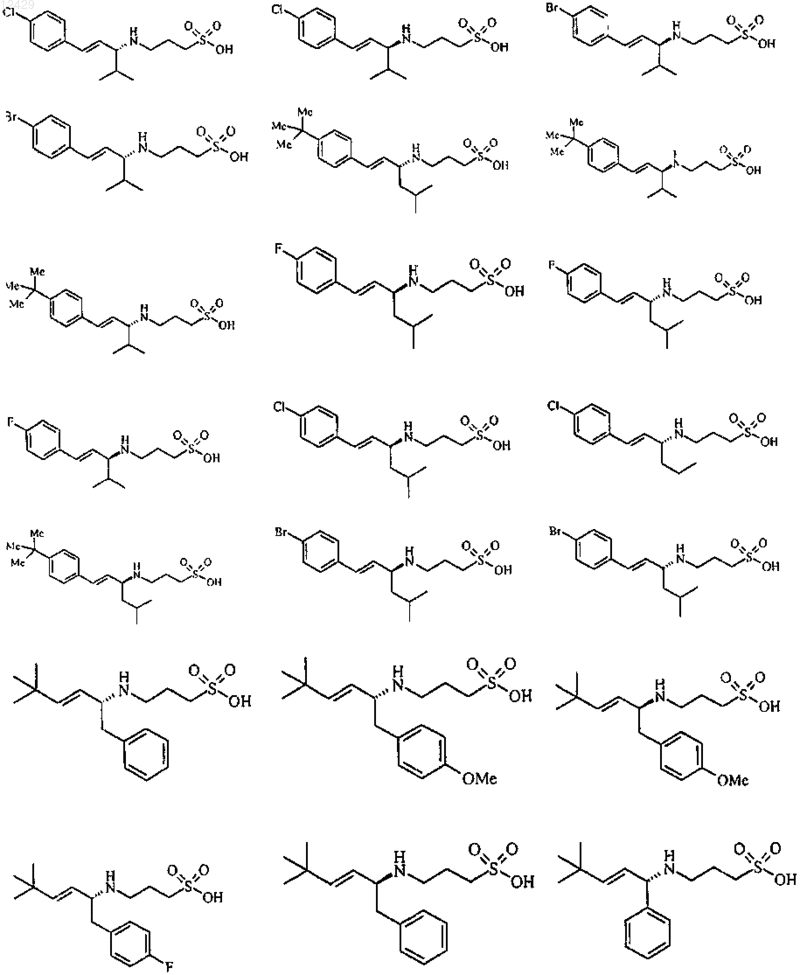
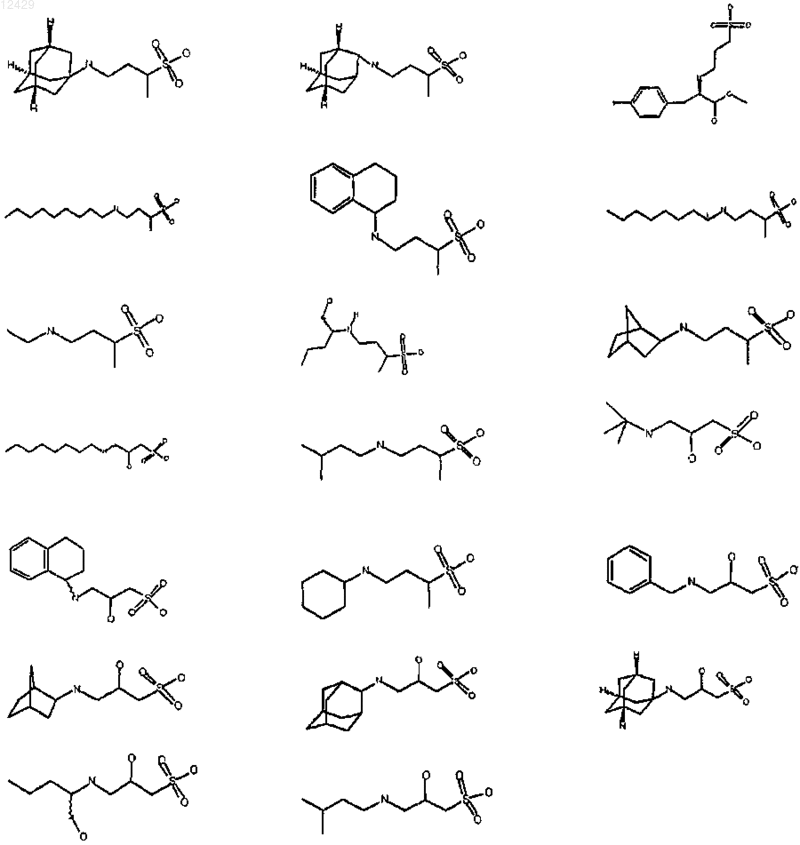
45. Соединение формулы (I)
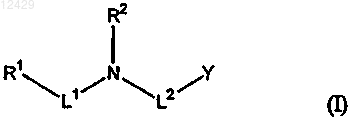
где R1 обозначает замещенный или незамещенный бицикло[2.1.2]гептил или замещенный или незамещенный адамантил;
R2 обозначает водород или C1-C10-алкил;
Y обозначает SO3H;
L1 обозначает замещенный или незамещенный C2-C5-алкил или отсутствует;
L2 обозначает замещенный или незамещенный C2-C5-алкил или отсутствует; при условии, что R2 обозначает водород, L2 обозначает -(СН2)3-, L1 отсутствует и что R1 не является 3,4-диметил-1-адамантилом или 3,5-диметил-1-адамантилом;
или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
46. Соединение по п.44, выбранное из группы

или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
47. Соединение по п.46, представляющее собой
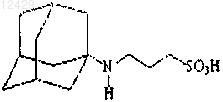
или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
48. Соединение, выбранное из
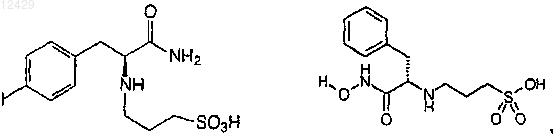
или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
49. Фармацевтическая композиция для лечения или предупреждения амилоидного заболевания, содержащая соединение по любому из пп.44-48 с фармацевтически приемлемым носителем.
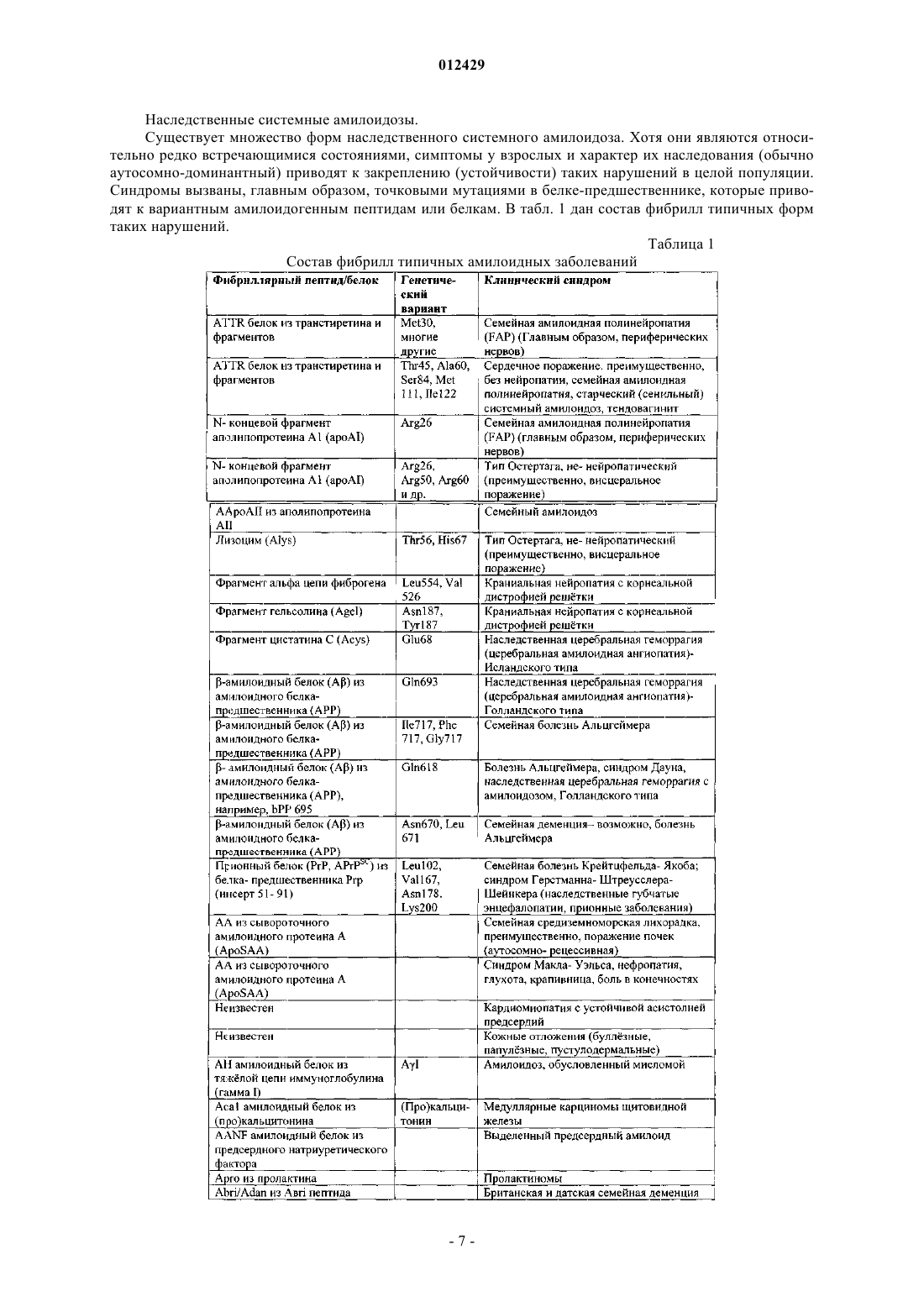
Текст
012429 Родственные заявки Заявка на данный патент претендует на приоритет патентной заявки США 10/871514, поданной 18 июня 2004 г., патентной заявки США 10/871365, поданной 18 июня 2004 г., предварительной патентной заявки США 60/512047, поданной 17 октября 2003 г., предварительной патентной заявки США 60/480906, поданной 23 июня 2003 г., все озаглавлены Способы и композиции для лечения амилоидных заболеваний. Заявка на данный патент также родственна предварительной патентной заявке США 60/512017,поданной 17 октября 2003 г., предварительной патентной заявке США 60/480918, поданной 23 июня 2003 г., и патентной заявке США 10/874805, поданной 18 июня 2004 г., все озаглавлены Способы лечения нарушений, вызванных агрегацией белков. Заявка на данный патент родственна предварительной патентной заявке США 60/512116, поданной 17 октября 2003 г., предварительной патентной заявке США 60/480984, поданной 23 июня 2003 г.,и патентной заявке США 10/871549, поданной 18 июня 2004 г., все озаглавлены Фармацевтические препараты соединений, ингибирующих амилоиды. Заявка на данный патент родственна предварительной патентной заявке США 60/436379, поданной 24 декабря 2002 г., предварительной патентной заявке США 60/482214, поданной 23 июня 2003 г.,озаглавленным Комбинированная терапия для лечения болезни Альцгеймера, патентной заявке США 10/746138, поданной 24 декабря 2003 г., международной патентной заявке РСТ/СА 2003/002011, и патентной заявке США 10/871537, поданной 18 июня 2004 г., все озаглавлены Терапевтические препараты для лечения заболеваний, связанных с -амилоидными пептидами. Заявка на данный патент родственна предварительной патентной заявке США 60/512135, поданной 17 октября 2003 г., предварительной патентной заявке США 60/482058, поданной 23 июня 2003 г.,обе озаглавлены Синтетический способ получения соединений для лечения амилоидоза, и патентной заявке США 10/871543, поданной 18 июня 2004 г., озаглавленной Улучшенные фармацевтические препараты-кандидаты и способ их получения. Заявка на данный патент родственна предварительной патентной заявке США 60/512018, поданной 17 октября 2003 г., предварительной патентной заявке США 60/482928, поданной 23 июня 2003 г.,и патентной заявке США 10/871512, поданной 18 июня 2004 г., все озаглавлены Способы и композиции для лечения заболеваний, связанных с амилоидами и эпилептогенезом. Заявка на данный патент родственна патентной заявке США 08/463548, в настоящее время патент США 5972328 под названием Способ лечения амилоидоза. Полное содержание каждой из этих патентных заявок и патента тем самым вводятся специально в данное описание ссылкой, включая, без ограничения, описание, формулу изобретения и реферат, а также любые фигуры, таблицы или рисунки в них. Предпосылки создания изобретения Амилоидоз относится к патологическому состоянию, характеризующемуся наличием амилоидных фибрилл. Амилоид является родовым названием, относящимся к группе разнообразных, но специфичных белковых отложений (внутриклеточных или внеклеточных), которые наблюдаются при различных заболеваниях. Будучи различными по местонахождению, все амилоидные отложения имеют общие морфологические свойства, окрашиваются специфичными красителями (например, конго красным) и после окрашивания имеют характерное красно-зеленое двойное лучепреломление в поляризованном свете. Они также имеют общие обычные ультраструктурные признаки и обычные рентгеновские и ИК-спектры. Заболевания, связанные с амилоидами, могут либо ограничиваться одним органом, либо распространяться на несколько органов. Первый пример называют "локализованным амилоидозом", тогда как второй называют "системным амилоидозом". Некоторые амилоидные заболевания могут быть идиопатическими, но большинство этих заболеваний проявляются как осложнения предыдущего заболевания. Например, первичный амилоидоз (AL амилоид) может появиться без какой-либо другой патологии или может быть последствием дискразии плазматических клеток или множественной миеломы. Обычно вторичный амилоидоз наблюдается как ассоциированный с хронической инфекцией (такой как туберкулез) или хроническим воспалением (таким как ревматоидный артрит). Семейная форма вторичного амилоидоза также наблюдается в других типах семейного амилоидоза, например семейная средиземноморская лихорадка (FMF). Этот семейный тип амилоидоза является генетически наследственным и обнаруживается в специфичных популяционных группах. Как при первичном, так и при вторичном амилоидозе отложения обнаруживают в некоторых органах и, следовательно, оба амилоидоза рассматриваются как системные амилоидные заболевания."Локализованные амилоидозы" представляют собой такие заболевания, которые включают систему единичного органа. Различные амилоиды также характеризуются типом белка, присутствующего в отложении. Например, нейродегенеративные заболевания, такие как скрепи, бычий губчатый энцефалит (болезнь коровьего бешенства), болезнь Крейтцфельда-Якоба и т.п., характеризуются появлением и аккумуляцией, устойчивой к протеазам формы прионного белка (называемого AScr или PrP-27). Аналогично,болезнь Альцгеймера, другое нейродегенеративное заболевание, характеризуется нейритными бляшками-1 012429 и нейрофибриллярными клубками. В данном случае амилоидные бляшки, обнаруживаемые в паренхиме и кровеносном сосуде, образуются отложением фибриллярного А-амилоидного белка. Другие заболевания, такие как диабет взрослых (диабет типа II), характеризуются локализованной аккумуляцией амилоидных фибрилл в поджелудочной железе. В случае образования амилоидов отсутствует известная, общепринятая терапия, или лечение, в результате которой происходило бы заметное растворение амилоидных отложений in situ, которая предупреждала бы дальнейшие амилоидные отложения или предупреждала инициирование амилоидного отложения. Каждый амилоидогенный белок способен претерпевать конформационное изменение и создавать складки и образовывать нерастворимые фибриллы, которые могут отлагаться вне или внутри клетки. Все амилоидогенные белки имеют различную аминокислотную последовательность, но одинаковое свойство образовывать фибриллы и связываться с другими элементами, такими как протеогликан, амилоид Р и компонент комплемента. Кроме того, все амилоидогенные белки имеют аминокислотные последовательности,которые будучи различными имеют сходство, такое как области, способные связываться с гликозаминогликановым (GAC) участком протеогликана (называемым сайт связывания GAC), а также другие области,которые промотируют образование -складок. Протеогликаны представляют собой макромолекулы различного размера и различной структуры, которые распространены почти по всему организму. Их можно обнаружить в межклеточном компартменте, на поверхности клетки и как часть внеклеточной матрицы. Основная структура всех протеогликанов состоит из ядерного белка и по меньшей мере одной, но часто большего числа, полисахаридных цепей (GAC), соединенных с ядерным белком. Открыто множество различных GAC, включая хондроитин сульфат, дерматан сульфат, кератан сульфат, гепарин и гиалуронан. В специфических случаях амилоидные фибриллы, если только они образовались, могут стать токсичными по отношению к окружающим клеткам. Например, показано, что А-фибриллы, организованные в виде сенильных бляшек, ассоциируются с мертвыми нейронными клетками, дистрофическими нейритами, астроцитозом и микроглиозом у больных болезнью Альцгеймера. При испытании in vitro показано, что олигомерный (растворимый), а также фибриллярный А-пептид способен инициировать процесс активации микроглии (макрофагов мозга), что объясняет микроглиоз и воспаление мозга, обнаруженные в мозге больных болезнью Альцгеймера. Как олигомерный, так и фибриллярный А-пептид могут также индуцировать гибель нейронных клеток in vitro. См., например, М.Р. Lampert, et al., Proc.Natl. Acad. Set USA 95, 6448-53 (1998). Показано, что при другом типе амилоидоза, наблюдаемом у больных диабетом типа II, амилоидогенный белок IAPP, если организован в олигомерные формы или в фибриллы, индуцирует токсичность островковых -клеток in vitro. Следовательно, появление IAPP фибрилл в поджелудочной железе больных диабетом типа II способствует утрате островковых -клеток (клеток Лангерганса) и дисфункции органа, которая может привести к инсулинемии. Другой тип амилоидоза связан с 2-микроглобулином и встречается у больных, проходящих длительный курс гемодиализа. У пациентов, проходящих продолжительный курс гемодиализа, появляются фибриллы из 2-микроглобулина в запястном туннеле и в богатых коллагеном тканях в некоторых суставах. Это вызывает сильные боли, тугоподвижность и опухание суставов. Амилоидоз также характерен для болезни Альцгеймера. Болезнь Альцгеймера является заболеванием,разрушающим мозг, которое приводит к прогрессирующей потере памяти, ведущей к слабоумию, психической нетрудоспособности и смерти через относительно продолжительное время. В процессе старения популяций в развитых странах число больных болезнью Альцгеймера достигает размера эпидемии. У людей, страдающих болезнью Альцгеймера, развивается прогрессирующее слабоумие в состоянии зрелости, сопровождающееся тремя основными структурными изменениями в мозге: диффузная гибель нейронов во многих участках мозга; аккумуляция внутриклеточных отложений белка, называемых нейрофибриллярными клубками; и аккумуляция внеклеточных отложений белка, называемых амилоидными или сенильными бляшками, окруженных деформированными нервными окончаниями (дистрофические нейриты) и активированной микроглией (микроглиоз и астроцитоз). Основным составляющим этих амилоидных бляшек является амилоидный -пептид (А), белок из 39-43 аминокислот, который образуется расщеплением -амилоидного белка-предшественника (АРР). Интенсивное исследование проводилось по изучению релевантности А-отложений при болезни Альцгеймера, см., например,Selkoe, Trends in Cell Biology 8, 447-453 (1998). А легко образуется при метаболическом процессировании амилоидного белка-предшественника ("АРР") в эндоплазматическом ретикулуме ("ER"), аппарате Гольджи, или в эндосомно-лизосомном метаболическом пути (системе), и, наиболее обычно, секретируется в виде пептида, содержащего 40 ("A1-40") или 42 ("А-42") аминокислот (Selkoe, Annu. Rev. CellBiol. 10, 373-403 (1994. Роль А как основной причины болезни Альцгеймера подтверждается присутствием внеклеточных отложений А в сенильных бляшках, характерных для болезни Альцгеймера, повышенным продуцированием А в клетках, содержащих мутантные гены, ассоциированные с болезнью Альцгеймера, например, амилоидного белка-предшественника, пресенилина I и пресенилина II; и токсичность растворимого (олигомерного) или фибриллярного А в отношении клеток в культуре. См., на-2 012429 пример, Gervais, Eur. Biopharm. Review, 40-42 (Autumn 2001); May, DDT, 459-62 (2001). Хотя существует симптоматическое лечение болезни Альцгеймера, в настоящее время это заболевание нельзя предупредить или лечить. Болезнь Альцгеймера характеризуется диффузными и нейритными бляшками, церебральной ангиопатией и нейрофибриллярными клубками. Полагают, что амилоид бляшек и кровеносных сосудов образуется за счет отложения нерастворимого А-амилоидного белка, который можно описать как диффузный или фибриллярный. Полагают также, что как растворимый олигомерный А, так и фибриллярный А являются нейротоксическими и воспалительными. Другим типом амилоидоза является церебральная амилоидная ангиопатия (САА). САА представляет собой специфичное отложение амилоидных -фибрилл на стенках липтоменингеальной и корковой артерий, артериол и вен. Она обычно ассоциируется с болезнью Альцгеймера, синдромом Дауна и нормальным старением, а также с различными семейными состояниями, связанными с ударом или деменцией (см. Frangione et al., Amiloid: J. Protein Folding Disord. 8, Suppl. 1, 36-42 (2001. Общедоступные в настоящее время методы лечения -амилоидных заболеваний, почти все, являются лишь симптоматическими, дающими лишь временное или частичное клиническое улучшение. Хотя описаны некоторые фармацевтические агенты, которые предлагают ослабление симптомов, в настоящее время отсутствует комплексная фармакологическая терапия для предупреждения или лечения, например,болезни Альцгеймера. Сущность изобретения Настоящее изобретение относится к применению соединений формулы (I) для лечения амилоидных заболеваний. В частности, данное изобретение относится к способу лечения или предупреждения амилоидного заболевания у субъекта, заключающемуся во введении субъекту терапевтического количества соединения по изобретению. Изобретение также относится к каждому из новых соединений по изобретению, представленных в данном описании. Среди соединений для применения по изобретению при введении соединений нижеприведенной формулы (I) уменьшается или ингибируется образование амилоидных фибрилл, специфичная дисфункция органов (например, нейродегенерация) или клеточная токсичность. В одном варианте изобретение относится к применению соединения формулы (I) где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов,выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных или конденсированных колец;R2 обозначает водород или C1-C10-алкил;L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН 2)3- и Y обозначает SO3-X+; R1 не обозначает фенил,1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН 2)3-, L1 отсутствует и Y обозначает SO3-X+, R1 не обозначает н-пентил, н-гексил, н-гептил, ноктил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил,1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил,5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,или его фармацевтически приемлемой соли, сложного эфира или пролекарства для лечения или предупреждения связанного с амилоидом заболевания или состояния, в том числе, если заболевание или состояние характеризуется отложением -амилоида. В соответствии с изобретением соединение формулы (I) или его фармацевтически приемлемая соль,сложный эфир или пролекарство также применимо для лечения или предупреждения отложения амилоида или заболевания, выбранного из группы, включающей болезнь Альцгеймера, церебральную амилоидную ангиопатию, миозит телец включений, дегенерацию желтого пятна, MCI или синдром Дауна. В другом варианте изобретения соединения формулы (I) или его фармацевтически приемлемая соль, сложный эфир или пролекарство применяются для изготовления лекарственного средства для лечения или предупреждения связанных с амилоидом заболеваний и состояний, в том числе заболеваний или состояний, которые характеризуется отложением -амилоида, а также для лечения или предупреждения заболевания, выбранного из группы, включающей болезнь Альцгеймера, церебральную амилоидную ангиопатию, миозит телец включений, дегенерацию желтого пятна, MCI или синдром Дауна.-3 012429 В другом аспекте изобретение относится к способу лечения или предупреждения связанного с амилоидом заболевания, в том числе отложения -амилоида, включающему введение субъекту эффективного количества соединения формулы (I) где R1 обозначает замещенный или незамещенный 3-10-членный, содержащий от 1 до 4 гетероатомов,выбранных из N, О и S, гетероциклил, 6-10-членный арил, 8-15-членный арилциклоалкил или замещенную или незамещенную C2-C10-алкильную группу; причем замещенный или незамещенный гетероциклил, арил или арилциклоалкил содержат от 1 до 3 отдельных колец;R2 обозначает водород или C1-C10-алкил;L1 обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует;L2 обозначает замещенную или незамещенную C2-C5-алкильную группу,при условии, что, когда R1 обозначает алкил, L1 отсутствует; при условии, что, когда R2 обозначает водород, L1 обозначает метилен, L2 обозначает -(СН 2)3-, и Y обозначает SO3-Х+; R1 не обозначает фенил,1,3-бензодиоксол-5-ил или 3,4-диметоксифенил, и при условии, что, когда R2 обозначает водород, L2 обозначает -(СН 2)3-, L1 отсутствует и Y обозначает SO3-Х+, R1 не обозначает н-пентил, н-гексил, н-гептил, ноктил, н-нонил, н-децил, циклогексил, 1-гидрокси-2-пропил, 1-гидрокси-2-бутил, 2-гидрокси-1-пропил,1-гидрокси-4-пентил, 1-гидрокси-5-гексил, 2-гидрокси-1-этил, 3-гидрокси-1-пропил, 4-гидрокси-1-бутил,5-гидрокси-1-пентил, 6-гидрокси-1-гексил, 3,5-диметил-1-адамантил, 1-гидроксиметил-1-циклопентил, 2(2-деокси-D-глюкозу), фенил, 4-гидроксифенил или 4-пиридил, 1-гидрокси-2-пентил, 3-метилмасляную кислоту, метиловый эфир 4-метилпентановой кислоты или 2,2-дифенилэтил,или его фармацевтически приемлемой соли, сложного эфира или пролекарства. Соединения по изобретению включают также соединение формулы (I) ге R1 обозначает замещенный или незамещенный бицикло[2.1.2]гептил или замещенный или незамещенный адамантил;R2 обозначает водород или C1-C10-алкил;L1 обозначает замещенный или незамещенный C1-C5-алкил или отсутствует; иL2 обозначает замещенный или незамещенный C2-C5-алкил или отсутствует; при условии, что R2 обозначает водород, L2 обозначает -(СН 2)3-, L1 отсутствует и что R1 не является 3,4-диметил-1-адамантилом или 3,5-диметил-1-адамантилом; или его фармацевтически приемлемую соль, сложный эфир или пролекарство. Еще в одном аспекте соединения по изобретению представляют собой Данное изобретение предусматривает также фармацевтическую композицию для лечения или предупреждения амилоидного заболевания, содержащую соединение по изобретению и фармацевтически приемлемый носитель. Соединения по изобретению могут действовать по одному из ниже следующих механизмов. В одном варианте изобретения соединения по данному описанию предупреждают или ингибируют сборку амилоидного белка в нерастворимые фибриллы, которые, in vivo, отлагаются в различных органах, или они способствуют клиренсу ранее образовавшихся отложений или замедляют отложение у пациентов, уже имеющих отложения. В другом варианте изобретения соединение может также предупреждать связывание амилоидного белка, в его растворимой, олигомерной форме или в его фибриллярной форме, с клеточной поверхностью или адгезию этого белка к клеточной поверхности. Еще в одном варианте изобретения соединение может блокировать вызванные амилоидами клеточную токсичность или активацию макрофага. В другом варианте изобретения соединение может блокировать вызванные амилоидами нейротоксичность или микроглиальную активацию. В другом варианте изобретения соединение защищает клетки от вызванной амилоидом цитотоксичности островковых В-клеток. В другом варианте изобретения соединение может повышать клиренс из конкретного органа, например, мозга, или оно понижает концентрацию амилоидного белка таким образом, в нацеленном органе предупреждается образование фибрилл.-4 012429 Соединения по изобретению можно применять терапевтически или профилактически для лечения заболеваний, ассоциированных с образованием, агрегацией или отложением амилоидных фибрилл. Соединения по изобретению могут действовать, облегчая течение амилоидного заболевания, по любому из приведенных ниже механизмов (предполагается, что этот перечень является иллюстративным и не лимитирующим): замедление скорости образования или отложения амилоидных фибрилл; уменьшение степени амилоидного отложения; ингибирование, уменьшение или предупреждение образования амилоидных фибрилл; ингибирование нейродегенерации или клеточной токсичности, вызванной амилоидом; ингибирование воспаления, индуцированного амилоидом; повышение клиренса амилоида; или содействие расщеплению (разрушению) амилоидного белка до его объединения в фибриллы. Соединения по изобретению можно применять терапевтически или профилактически для лечения заболеваний, ассоциированных с образованием, агрегацией или отложением фибрилл -амилоида. Соединения по изобретению могут действовать, облегчая течение заболевания, связанного с -амилоидом,по любому из приведенных ниже механизмов (предполагается, что этот перечень является иллюстративным и не лимитирующим): замедление скорости образования или отложения -амилоидных фибрилл; уменьшение степени -амилоидного отложения; ингибирование, уменьшение или предупреждение образования -амилоидных фибрилл; ингибирование нейродегенерации или клеточной токсичности, вызванной -амилоидом; ингибирование воспаления, индуцированного -амилоидом; повышение клиренса амилоида из мозга; или содействие расщеплению (разрушению) -амилоидного белка до его объединения в фибриллы. Терапевтические соединения по изобретению могут быть эффективны при контроле -амилоидного отложения либо после их проникновения в мозг (после прохождения через гематоэнцефалический барьер), либо с периферии. При действии с периферии соединение может изменять равновесие А между мозгом и плазмой таким образом, который содействует удалению А из мозга. Оно может также повышать катаболизм нейронного А и изменять скорость удаления из мозга. Увеличение выхода А из мозга приводит к понижению концентрации А в мозге и в спинно-мозговой жидкости (CSF) и, следовательно,способствует уменьшению А отложения. Или же, соединения, которые проникают в мозг, могли бы регулировать отложение, действуя непосредственно на А в мозге, например, сохраняя его в нефибриллярной форме, способствуя его клиренсу из мозга или замедляя процессирование АРР. Эти соединения могли бы также предупреждать взаимодействие А в мозге с клеточной поверхностью и, следовательно,предупреждать нейротоксичность, нейродегенерацию и воспаление. Они также могут снижать продуцирование А активированной микроглией. Эти соединения могут также повышать разрушение при использовании макрофагов или нейронных клеток. В одном варианте изобретения применяется способ лечения болезни Альцгеймера (например, спорадической формы, семейной или ранней AD). Способ также можно применять профилактически или терапевтически для лечения других случаев -амилоидного отложения, таких как у больных с синдромом Дауна или у больных церебральной амилоидной ангиопатией ("САА"). В другом варианте изобретения применяют способ лечения легкой когнитивной недостаточности. Легкая когнитивная недостаточность ("MCI") представляет собой состояние, характеризующееся легкой,но заметной утратой мыслительного навыка, квалификации, умения, которая необязательно связана с наличием деменции. MCI часто, но не всегда, предшествует болезни Альцгеймера. Кроме того, аномальная аккумуляция АРР и -амилоидного белка в мышечных волокнах влечет за собой патологию случайного миозита телец включений (IBM) (Askanas et al., Pros. Natl. Acad. Sci. USA 93, 1314-1319 (1996); Askanas et al., Current Opinion in Rheumathology 7, 486-496 (1995. Соответственно,соединения по изобретению можно применять профилактически или терапевтически при лечении нарушений, при которых -амилоидный белок аномально отлагается в ненейрологических участках, например, для лечения IBM доставкой соединений к мышечным волокнам. Кроме того, было показано, что А ассоциируется с аномальными внеклеточными отложениями,известными как друзы, которые аккумулируются вдоль базальной поверхности ретинального пигментированного эпителия у субъектов с возрастной дегенерацией желтого пятна (AMD). AMD является причиной необратимой потери зрения у людей старшего возраста. Полагают, что отложение А может являться важным компонентом локальных воспалительных событий, которые способствуют атрофии ретинального пигментированного эпителия, биогенезу друз и патогенезу AMD (Johnson, et al., Pros. Natl.Acad. Sci. USA 99(18), 11830-5 (2002. Следовательно, настоящее изобретение относится к применению соединений формулы (I) по данному описанию для предупреждения или лечения амилоидных заболеваний, включая, среди прочих, болезнь Альцгеймера, церебральную амилоидную ангиопатию, легкую когнитивную недостаточность, миозит телец включений, синдром Дауна, дегенерацию желтого пятна, а также другие типы амилоидоза,обусловленного IAPP (например, диабет), первичный (AL) амилоидоз, вторичный (АА) амилоидоз и амилоидозы, обусловленные 2-микроглобулином (диализные). При амилоидозе, связанном с диабетом типа II (диабетическом) (IAPP), амилоидогенный белок IAPP-5 012429 индуцирует токсичность островковых -клеток при объединении в олигомерные формы или в фибриллы. Следовательно, появление IAPP фибрилл в поджелудочной железе больных диабетом типа II способствует утрате островковых -клеток (Лангерганса) и дисфункции органа, которая ведет к инсулинемии. Известно, что обычно первичный амилоидоз (AL амилоид) ассоциирован с дискразией плазматических клеток и множественной миеломой. Его также можно наблюдать в качестве идиопатического заболевания. Вторичный (АА) амилоидоз обычно наблюдается в связи с хронической инфекцией (такой как туберкулез) или хроническим воспалением (таки как ревматоидный артрит). Семейную форму вторичного амилоидоза наблюдают также при семейной средиземноморской лихорадке (FMF). Амилоидоз, обусловленный 2-микроглобулином (диализный), наблюдают у пациентов при продолжительном курсе гемодиализа. У больных, проходящих длительный курс гемодиализа, появляются фибриллы из 2-микроглобулина в запястном туннеле и в тканях, обогащенных коллагеном, в некоторых суставах. Это вызывает сильные боли, тугоподвижность и опухание суставов. Эти отложения вызваны неспособностью сохранять низкие уровни 2 М в плазме больных, подвергающихся гемодиализу. Повышенные концентрации белка 2 М вызывают структурные изменения и могут привести к отложению модифицированного 2 М в суставах в виде нерастворимых фибрилл. Подробное описание изобретения Настоящее изобретение относится к применению соединений формулы (I) по данному описанию для лечения амилоидных заболеваний. Для удобства некоторые определения или термины, на которые есть ссылки в данном описании, представлены ниже. Амилоидные заболевания АА (реактивный) амилоидоз. Обычно АА амилоидоз представляет собой проявление ряда заболеваний, которые вызывают продолжительную реакцию в острой фазе. Такие заболевания включают хронические воспалительные нарушения, хронические местные или системные микробные инфекции и злокачественные новообразования. Наиболее обычную форму реактивного или вторичного (АА) амилоидоза наблюдают в результате продолжительных воспалительных состояний. Например, у больных ревматоидным артритом или семейной средиземноморской лихорадкой (которая является генетическим заболеванием) может развиться АА амилоидоз. Термины "АА амилоидоз" и "вторичный (АА) амилоидоз" применяются поочередно (взаимозаменяемо). АА фибриллы обычно состоят из фрагментов размером 8000 Дальтон (Да) (АА пептид или белок),образующихся при протеолитическом расщеплении сывороточного амилоидного протеина A (ApoSAA),циркулирующего аполипопротеина, который синтезируется, главным образом, в гепатоцитах в ответ на такие цитокины, как IL-1, IL-6 и TNF. Секретированный ApoSAA образует комплексы с HDL. Отложение АА фибрилл может быть распространено в организме, преимущественно в паренхимных органах. Обычно местом, где находятся отложения, являются почки, также могут быть задеты печень и селезенка. Отложение также наблюдают в сердце, желудочно-кишечном тракте и коже. Основные заболевания, которые могут привести к развитию АА амилоидоза, включают, но без ограничения, воспалительные заболевания, такие как ревматоидный артрит, ювенильный хронический артрит, анкилоизирующий спондилоартрит, псориаз, псориатическая артропатия, синдром Рейтера, болезнь Стилла у взрослых, синдром Бехчета и болезнь Крона. АА отложения также могут возникать в результате хронических микробных инфекций, таких как проказа, туберкулез, бронхоэктаз, декубитальные язвы,хронический пиелонефрит, остеомиелит и болезнь Уиппла. Некоторые злокачественные новообразования также могут вызвать отложения АА фибриллярного амилоидного белка. Эти злокачественные новообразования включают лимфому Ходжкина, рак почки, рак кишки, легкого и мочеполовой системы, базалиому и вилосистоклеточную лейкемию. Другими основными состояниями, которые могут обусловливать АА амилоидоз, являются болезнь Кастльмана и синдром Шнитцлера.AL Амилоидоз (первичный амилоидоз). Отложение AL амилоида обычно связано почти с любой дискразией линии В лимфоцитов, от злокачественного развития плазматических клеток (множественная миелома) до доброкачественной моноклональной гаммапатии. Иногда присутствие амилоидных отложений может быть непосредственным показателем основной дискразии. AL амилоидоз также подробно описан в Current Drug Targets, 2004, 5 159-171. Фибриллы AL амилоидных отложений состоят из легких цепей моноклонального иммуноглобулина или их фрагментов. Более конкретно, фрагменты образованы из N-концевого участка легкой цепи ( или) и содержат целый вариабельный домен (VL) или его часть. Отложения встречаются, главным образом,в мезенхимных тканях, вызывая периферическую и автономную нейропатию, туннельный запястный синдром, макроглоссию, рестриктивную кардиомиопатию, артропатию больших суставов, иммунные дискразии, миеломы, а также дискразии неизвестного происхождения. Однако следует отметить, что могут быть затронуты почти все ткани, в особенности внутренние органы, такие как почка, печень, селезенка и сердце.-6 012429 Наследственные системные амилоидозы. Существует множество форм наследственного системного амилоидоза. Хотя они являются относительно редко встречающимися состояниями, симптомы у взрослых и характер их наследования (обычно аутосомно-доминантный) приводят к закреплению (устойчивости) таких нарушений в целой популяции. Синдромы вызваны, главным образом, точковыми мутациями в белке-предшественнике, которые приводят к вариантным амилоидогенным пептидам или белкам. В табл. 1 дан состав фибрилл типичных форм таких нарушений. Таблица 1 Состав фибрилл типичных амилоидных заболеваний-7 012429 Данные взяты из Tan SY, Pepys MB. Amyloidosis. Histopathology, 25(5), 403-414 (Nov 1994),WHO/IUIS Nomenclature Subcommittee, Nomenclature of Amyloid and Amyloidosis. Bulletin of the WorldHealth Organization 1993; 71: 10508; и Merlini et al., Clin Chem Lab Med 2001; 39(11): 1065-75. Данные в табл. 1 приведены в качестве примеров и не претендуют на ограничение объема изобретения. Например, описано более 40 отдельных точковых мутаций в гене транстиретина, каждая из которых дает клинически сходные формы семейной амилоидной полинейропатии. Как правило, любое наследственное амилоидное нарушение может встречаться также в спорадической форме, и как наследственная, так и спорадическая (случайная) форма заболевания имеют одинаковые особенности в том, что касается амилоида. Например, наиболее распространенная форма вторичного АА амилоидоза встречается случайно, например как результат постоянного воспаления, и не связана с семейной средиземноморской лихорадкой. Таким образом, общие сведения, касающиеся наследственных амилоидных нарушений, можно также отнести к спорадическим (случайным) амилоидозам. Транстиретин (TTR) представляет собой белок протяженностью 14 килодальтон (кДа), который иногда называют преальбумин. Он продуцируется печенью и сосудистым сплетением и функционирует в процессе транспорта тироидных гормонов и витамина А. По меньшей мере 50 вариантных форм белка,каждый из которых характеризуется единственной аминокислотной заменой, ответственны за различные формы семейной амилоидной полинейропатии. Например, замена пролин вместо лейцина в положении 55 приводит, главным образом, к прогрессирующей форме нейропатии; замена лейцина на метионин в положении 111 вызывает тяжелую кардиопатию у голландских пациентов. На амилоидных отложениях, выделенных из тканей сердца пациентов с системным амилоидозом,видно, что отложения состоят из гетерогенной смеси TTR и его фрагментов, в целом называемых ATTR,полноразмерные последовательности которых охарактеризованы. Компоненты ATTR фибрилл можно извлечь (экстрагировать) из таких бляшек и методами, известными в уровне техники, можно определить их структуру и последовательность (например, Gustavson, A., et al., Laboratory Invest. 73: 703-708, 1995;TrpArg50; LeuArg60) наблюдается форма амилоидоза ("тип stertag"), характеризующаяся отложениями белка аполипопротеина AI или его фрагментов (AapoAI). У этих больных наблюдаются низкие уровни липопротеина высокой плотности (HDL) и периферическая нейропатия или почечная недостаточность. Мутация в -цепи фермента лизоцима (например, IleThr56 или AspHis57) лежит в основе другой формы ненейропатического наследственного амилоида типа stertag, наблюдаемого в английских семьях. В данном случае отлагаются фибриллы мутантного белка лизоцима (Alys) и у пациентов, как правило, наблюдается недостаточность почечной функции. Этот белок в отличие от большинства белков,образующих фибриллы, по данному описанию обычно присутствует в полной (нефрагментированной) форме (Benson, M.D., et al. CIBA Fdn. Symp. 199: 104-131, 1996). Легкие цепи иммуноглобулинов имеют тенденцию образовывать агрегаты различной морфологии,включая фибриллярную (например, AL амилоидоз и АН амилоидоз), гранулярную (например, болезнь легких цепей (БЛЦ, LCDD), болезнь тяжелых цепей (БТЦ, HCDD) и болезнь легких-тяжелых цепей(например, криоглобулинемия). Образование нерастворимых фибрилл легких цепей и тяжелых цепей иммуноглобулинов и/или их фрагментов является показателем AL и АН амилоидоза, соответственно. ВAL фибриллах лямбда-цепи, такие как VI-цепи (6-цепи), обнаружены в более высоких концентрациях, чем каппа-цепи. Merlini et al., Clin Chem Lab Med 39(11): 1065-75 (2001). Амилоидоз тяжелых цепей (АН) характеризуется агрегатами амилоидных белков -цепи IgGl подкласса. Eulitz et al., Proc.Natl. Acad. Sci. USA 87: 6542-46 (1990). Сравнение амилоидогенных легких цепей с неамилоидогенными показало, что первые могут включать замены, которые, по-видимому, дестабилизируют скручивание белка или стимулируют агрегацию.AL и LCDD были определены из других амилоидных заболеваний благодаря их относительно малой популяции моноклональных легких цепей, которые образуются за счет неопластического роста продуцирующей антитело В клетки. Как правило, AL агрегаты представляют собой хорошо организованные фибриллы -цепей. Агрегаты LCDD являются относительно аморфными агрегатами как -, так и цепей, в основном , иногда IV. Bellotti et al., Journal of Structural Biology 13: 280-89 (2000). Сравнение амилоидогенных и неамилоидогенных тяжелых цепей у пациентов с АН амилоидозом выявило недостающие и/или измененные компоненты. Eulitz et al., Proc. Natl. Acad. Sci. USA 87: 6542-46 (1990) (патогенные тяжелые цепи, отличающиеся значительно более низкой молекулярной массой, чем неамилоидогенные тяжелые цепи); и Solomon et al., Am J Hemat 45(2) 171-6 (1994) (амилоидогенные тяжелые цепи,отличающиеся тем, что состоят исключительно из VH-D участка неамилоидогенной тяжелой цепи). Следовательно, возможные способы обнаружения и мониторинга лечения субъектов с повышенным риском наличия AL, LCDD, АН и т.п. включают, но без ограничения, иммуноанализ плазмы или мочи на-8 012429 присутствие или пониженное отложение амилоидогенных легкой или тяжелой цепей, например, амилоида , амилоида , амилоида VI, амилоидаили амилоида 1. Амилоидоз мозга. Наиболее часто встречающийся тип амилоида в мозге состоит, главным образом, из А-пептидных фибрилл, приводящих к деменции, ассоциированной со случайной (не наследственной) болезни Альцгеймера. На самом деле, частота спорадической (случайной) болезни Альцгеймера значительно превышает формы, которые, как показано, являются наследственными. Тем не менее, фибриллярные пептиды,образующие бляшки, у обоих типов очень похожи. Амилоидоз мозга включает такие заболевания, состояния, патологии и другие аномалии структуры или функции мозга, включая его компоненты, причиной которых является амилоид. Областью мозга, пораженной амилоидным заболеванием, может быть строма, включающая сосудистую сеть, или паренхима, включающая функциональные или анатомические области, или их нейроны. Больному необязательно поставлен точный диагноз конкретного определенного амилоидного заболевания. Термин "амилоидное заболевание (заболевание, связанное с амилоидом)" включает амилоидоз мозга.-амилоидный пептид ("А") представляет собой пептид из 39-43 аминокислот, образующийся протеолизом большого белка, известного как -амилоидный белок-предшественник ("АРР"). Мутации в АРР вызывают семейные формы болезни Альцгеймера, синдром Дауна, церебральную амилоидную ангиопатию и старческую деменцию, характеризующуюся церебральным отложением бляшек, состоящих из А-фибрилл и других компонентов, которые более подробно описаны ниже. Известные мутации в АРР, ассоциированные с болезнью Альцгеймера, происходят непосредственно близ сайтов расщепления - или -секретазой или в А. Например, положение 717 - ближайшее к сайту расщепления секретазой АРР при его процессировании в А, а положения 670/671 - ближайшие к сайту расщепления-секретазой. Мутации в любом из этих остатков могут привести к болезни Альцгеймера, предположительно, за счет повышение количества формы А из 42/43 аминокислот, образующейся из АРР. Семейная форма болезни Альцгеймера составляет только 10% испытуемой популяции. Большинство случаев болезни Альцгеймера являются спорадическими, в которых АРР и А не содержат никакой мутации. Структура и последовательность А-пептидов различной длины общеизвестны в уровне техники. Такие пептиды можно получать методами, известными в технике, или можно выделить из мозга известными методами (например, Glenner and Wong, Biochem. Biophys. Res. Comm. 129, 885-90 (1984); Glenner andWong, Biochem. Biophys. Res. Comm. 122, 1131-35 (1984. Кроме того, различные формы пептидов являются продажными. АРР экспрессируется и конститутивно катаболизируется в большинстве клеток. По-видимому, доминантный катаболитический путь представляет собой расщепление АРР внутри последовательности А ферментом, предварительно названным -секретазой, который приводит к высвобождению растворимого фрагмента эктодомаина, известного как APPs. Это расщепление мешает образованию А-пептида. В отличие от этого неамилоидогенного каскада реакций АРР может также расщепляться ферментами, известными как - и -секретаза, по N- и С-концам А, соответственно, с последующим выделением А во внеклеточное пространство. К настоящему времени ВАСЕ идентифицирован как(De Strooper et al., Nature 391, 387-90 (1998. А-пептид, содержащий 39-43 аминокислоты, продуцируется при последовательном протеолитическом расщеплении амилоидного белка-предшественника (АРР)- и -секретазами. Хотя преимущественно продуцируется А 40 форма, 5-7% тотального А существует в виде А 42 (Cappai et al., Int. J. Biochem. Cell Biol. 31. 885-89 (1999. По-видимому, длина А-пептида решающим образом изменяет его биохимические/биофизические свойства. Конкретно, дополнительные две аминокислоты на С-конце А 42, являясь сильно гидрофобными, по-видимому, повышают предрасположенность А 42 к агрегации. Например, Jarrett, et al. показали,что А 42 агрегируется очень быстро in vitro по сравнению с А 40, это наводит на мысль, что более протяженные формы А могут быть важными патологическими белками, которые участвуют в начальном посеве нейритных бляшек при болезни Альцгеймера (Jairrett, et al., Biochemistry 32, 4693-97 (1993);Jarrett, et al., Ann. N.Y. Acad. Sci. 695, 144-48 (1993. Эта гипотеза дополнительно подтверждается недавними анализами вклада конкретных форм А в генетических семейных формах болезни Альцгеймера("FAD"). Например, мутантная форма АРР (APPV7171) "Лондон", связанная с FAD, селективно повышает продуцирование А 42/43 форм по сравнению с А 40 (Suzuki, et al., Science 264, 1336-40 (1994, тогда как мутантная форма АРР "Шведский" (APPK670N/M671L) повышает уровни как А 40, так и А 42/43 (Citron, et al., Nature 360, 672-674 (1992); Cai, et al., Science 259, 514-16, (1993. Также наблюдали, что FAD-связанные мутации в генах пресенилин-1 ("PS1) или пресенилин-2 ("PS2") приводит к селективному повышению продуцирования АР 42/43, но не А 40 (Borchelt, et al., Neuron 17, 1005-13(1996. Это открытие подтверждено на трансгенных мышиных моделях, экспрессирующих PS мутанты,которые демонстрируют селективное увеличение в мозге А 42 (Borchelt, см. выше; Duff, et al., Neurodegeneration 5(4), 293-98 (1996. Таким образом, основной гипотезой об этиологии болезни Альцгеймера-9 012429 является то, что увеличение концентрации А 42 в мозге вследствие повышенного продуцирования и выделения А 42, либо пониженного клиренса (расщепление или клиренс из тканей мозга) - событие, являющееся причиной патологии заболевания. Многие сайты мутации либо в А, либо в АРР гене были идентифицированы и клинически ассоциированы либо с деменцией, либо с церебральной геморрагией. Типичные САА нарушения включают,но без ограничения, наследственную церебральную геморрагию с амилоидозом исландского типа(HCHWA-I); голландский вариант HCHWA (HCHWA-D; мутация в A); фламандскую мутацию А; арктическую мутацию А; итальянскую мутацию А; мутацию А вариант Айова; семейную британскую деменцию; и семейную датскую деменцию. САА также может быть спорадическим (случайным). Применяемые в данном описании термины "-амилоид", "амилоид-" и т.п., если не указано иначе,относятся к белкам и пептидам -амилоида, амилоидным- белкам- или пептидам-предшественникам, их интермедиатам и модификациям и фрагментам. В частности, "А" относится к любому пептиду, продуцированному протеолитическим процессированием генного продукта АРР, особенно к пептидам, которые ассоциированы с амилоидными патологиями, включая А 1-39, А 1-40, А 1-41, А 1-42 и А 1-43. Для удобства номенклатуры "А 1-42" может в данном описании называться "А 1-42" или просто"А 42" или "А 42" (и аналогично для любых других амилоидных пептидов, обсуждаемых в данном описании). Применяемые в данном описании термины "-амилоид", "амилоид-" и "а" являются синонимами. Если не указано иначе, термин "амилоид" относится к амилоидогенным белкам, пептидам или их фрагментам, которые могут быть растворимыми (например, мономерными или олигомерными) или нерастворимыми (например, имеющими фибриллярную структуру или находящимися в виде амилоидных бляшек). См, например, М.Р. Lampert, et al., Proc. Natl. Acad. Sci. USA 95, 6448-53 (1998). "Амилоидоз" или "амилоидное заболевание" или "заболевание, связанное с амилоидом" относится к патологическому состоянию, отличающемуся присутствием амилоидных волокон. "Амилоид" является родовым термином, относящимся к группе различных, но специфичных белковых отложений (внутриклеточных или внеклеточных), которые наблюдаются при многих различных заболеваниях. Встречаясь в различных местах, все амилоидные отложения имеют общие морфологические свойства, окрашиваются специфичными красителями (например, конго красным) и после окрашивания имеют характерное красно-зеленое двойное лучепреломление в поляризованном свете. Они также имеют общие обычные ультраструктурные признаки и обычные рентгеновские и ИК-спектры. Гельсолин является связывающим кальций белком, который связывается с фрагментами и филаментами актина. Мутации в положении 187 (например, AspAsn; AspTyr) белка приводят к форме наследственного системного амилоидоза, обычно обнаруживаемого у пациентов из Финляндии, а также у выходцев из Голландии и Японии. У пораженных болезнью людей фибриллы, образованные из фрагментов гельсолина (Agel), обычно состоят из аминокислот 173-243 (карбоксиконцевой фрагмент длиной 68 кДа) и отлагаются в кровеносных сосудах и базальных мембранах, вызывая корнеальную дистрофию и краниальную нейропатию, которая прогрессирует в периферическую нейропатию, дистрофические кожные изменения и отложения в других органах (Kangas, H., et al. Human Mol. Genet. 5(9): 1237-1243,1996. Другие мутантные белки, такие как мутантная -цепь фибриногена (AfibA) и мутантный цистатин С (Acys), также образуют фибриллы и вызывают характерные наследственные нарушения. ФибриллыAfibA образуют отложения, характерные для наследственной церебральной амилоидной ангиопатии,обнаруженной в Исландии (Isselbacher, Harrison's Principles of Internal Medicine, McGraw-Hill, San Francisco, 1995; Benson et al.). Показано, что, по меньшей мере, в нескольких случаях у пациентов с церебральной амилоидной ангиопатией (САА) имеются амилоидные фибриллы, содержащие немутантную форму цистатина С, связанную с -амилоидным белком (Nagai, A., et al. Molec. Chem. Neuropathol. 33: 63-78, 1998). В настоящее время считают, что некоторые формы прионного заболевания, которые ранее полагали преимущественно инфекционными по своей природе, являются наследственными, насчитывающими до 15% случаев. (Baldwin, et al., в Research Advances in Alzheimer Disease and Related Disorders, John Wileyand Sons, New York, 1995). При наследственных и случайных (спорадических) прионных заболеваниях у больных появляются бляшки, состоящие из аномальных изоформ нормального прионного белка (PrPSc). Преимущественная мутантная изоформа, PrPSc, также называемая AScr, отличается от нормального клеточного белка своей резистентностью к расщеплению протеазой, нерастворимостью после экстракции детергентом, отложением во вторичных лизосомах, посттрансляционным синтезом и высоким содержанием -складок. Генетическая связь установлена по меньшей мере для пяти мутаций, вызывающих болезнь Крейтцфельда-Якоба (CJD), синдром Герстманна-Штреусслера-Шейнкера (GSS) и летальную семейную бессонницу (FFI). (Baldwin, см. выше). Способы извлечения фибриллярных пептидов из фибрилл скрепи, определение последовательностей и получение таких пептидов известны в технике (например, Beekes, M., et al. J. Gen. Virol. 76: 2567-76, 1995). Например, одна форма GSS связана с PrP мутацией в кодоне 102, тогда как GSS конечного мозга- 10012429 отличается мутацией в кодоне 117. Мутации в кодонах 198 и 218 приводят к появлению формы GSS, при которой нейритные бляшки, характерные для болезни Альцгеймера, содержат PrP вместо A-пептида. Некоторые формы семейной CJD ассоциируются с мутациями в кодонах 200 и 210; мутации в кодонах 129 и 178 обнаружены как при семейной CJD, так и при FFI (Baldwin, см. выше). Церебральный амилоидоз (Амилоидоз мозга). Локальное отложение амилоида обычно встречается в мозге, в частности, у людей старшего возраста. Наиболее часто встречающийся тип амилоида в мозге состоит, главным образом, из А-пептидных фибрилл, которые вызывают деменцию или спорадическую (случайную, ненаследственную) болезнь Альцгеймера. Наиболее часто встречаются случаи спорадического, а не наследственного церебрального амилоидоза. Например, частота случайной болезни Альцгеймера и случайной САА значительно превышает частоту семейной AD и семейной САА. Кроме того, случайные и семейные формы заболевания нельзя отличить друг от друга (они отличаются только наличием или отсутствием наследственной генетической мутации); например, клинические симптомы и амилоидные бляшки, образующиеся как при случайной, так и при семейной AD, очень похожи, если не идентичны. Церебральная амилоидная ангиопатия (САА) относится к специфичному отложению амилоидных фибрилл на стенках лептоменингеальной и кортикальной артерий, артериол и вен. Ее обычно ассоциируют с болезнью Альцгеймера, синдромом Дауна и обычным старением, а также с рядом семейных состояний, связанных с ударом или деменцией (см. Frangione et al., Amiloid: J. Protein Folding Disord. 8,Suppl. 36-42 (2001. САА может быть спорадической (случайной) или семейной. Старческий (сенильный) системный амилоидоз. Амилоидные отложения, либо системные, либо очаговые, увеличиваются с возрастом. Например,фибриллы транстиретина (TTR) дикого типа обычно обнаруживают в тканях сердца старых людей. Они могут быть бессимптомными, клинически скрытыми, или могут вызывать сердечную недостаточность. Бессимптомные фибриллярные очаговые отложения могут находиться в мозге (А), крахмалистом теле простаты (2-микроглобулин), суставах и семенных пузырьках. Диализный амилоидоз. Бляшки, состоящие из фибрилл 2-микроглобулина (2 М), обычно появляются у пациентов, проходящих длительный курс гемодиализа или перитонеального диализа. 2-микроглобулин представляет собой полипептид длиной 11,8 кДа и является легкой цепью антигенов класса I MHC, которые присутствуют во всех ядерных клетках. В нормальных обстоятельствах 2 М обычно находится во внеклеточном пространстве, если нет почечной недостаточности, в этом случае 2 М переносится в ткани, где он полимеризуется с образованием амилоидных фибрилл. Недостаточный клиренс, как в случае почечной недостаточности, приводит к отложению в запястном туннеле и других местах (главным образом, в богатых коллагеном тканях суставов). В отличие от других фибриллярных белков молекулы 2 М не продуцируются при расщеплении более протяженного белка-предшественника и обычно присутствуют в нефрагментированной форме в фибриллах. (Benson, см. выше). Показано, что сохранение и аккумуляция этого амилоидного белка-предшественника является основным патогенным процессом, лежащим в основеDRA. DRA характеризуется остеоартропатией периферических суставов (например, тугоподвижностью суставов, болью, опуханием и т.д.). Изоформы 2 М, гликированный 2 М или полимеры 2 М в ткани являются наиболее амилоидогенной формой (в противоположность нативному 2 М). В отличие от других типов амилоидоза 2 М в основном ограничивается костно-суставными тканями. Висцеральные отложения наблюдаются редко. Изредка эти отложения могут находиться в кровеносных сосудах и других важных анатомических положениях. Несмотря на усовершенствованные с точки зрения удаления 2 М методы диализа, у большинства пациентов наблюдаются высокие концентрации 2 М в плазме, которые остаются значительно выше нормы. Эти повышенные концентрации 2 М обычно вызывают диабетический амилоидоз (DRA) и сопутствующее распространение заболевания, ведущее к смерти. Островковый амилоидный полипептид и диабет. Гиалиноз островков (амилоидное отложение) описан впервые более века назад как присутствие агрегатов фиброзного белка в поджелудочной железе больных тяжелой гипергликемией (Opie, E.L., J. Exp.Med. 5: 397-428, 1901). В настоящее время островковый амилоид, состоящий преимущественно из островкового амилоидного полипептида (IAPP), или амилина, является характерным гистопатологическим маркером более чем в 90% случаев диабета типа II (также известного как инсулиннезависимый диабет,или NIDDM). Эти фибриллярные скопления возникают в результате агрегации островкового амилоидного полипептида (IAPP), или амилина, который представляет собой пептид из 37 аминокислот, образующийся из более протяженного пептида-предшественника, называемого (про)Pro-IAPP.IAPP секретируется вместе с инсулином в ответ на стимуляторы секреции -клетками. Этот патологический признак не ассоциирован с инсулинзависимым (типа I) диабетом и является общим (объединяющим) характерным признаком для гетерогенных клинических фенотипов, диагностированных какNIDDM. Продолжительные исследования на кошках и иммуноцитохимические исследования на обезьянах- 11012429 показали, что прогрессирующее увеличение островкового амилоида связано с резким уменьшением популяции секретирующих инсулин -клеток и увеличивает тяжесть заболевания. Позднее трансгенные исследования подтвердили связь между образованием IAPP бляшек и апоптозом -клеток и дисфункцией, это показывает, что амилоидное отложение является главным фактором, определяющим повышение тяжести диабета типа II. Также было показано, что IAPP индуцирует токсичность островковых -клеток in vitro, указывая,что появление IAPP фибрилл в поджелудочной железе больных диабетом типа II и типа I (посттрансплантация островков) может способствовать утрате островковых -клеток (Лангерганса) и дисфункции органа. У больных диабетом типа II накопление IAPP в поджелудочной железе вызывает образование олигомерного IAPP, приводя к созданию IAPP-амилоида в виде нерастворимых отложений, которые в конечном счете разрушают продуцирующие инсулин -клетки островков, вызывая истощение и недостаточность -клеток. (Westermark, P., Grimelius, L., Ada Path. Microbiol. Scand., sect. A. 81: 291-300, 393; deKoning, EJP., et al., Diabetologia 36: 378-384, 1993; и Lorenzo, A., et al., Nature 368: 756-760, 1994). Аккумуляция IAPP в виде фиброзных отложений также может оказывать влияние на обычное отношение проIAPP к IAPP в плазме, повышая это отношение за счет попадания (захвата) IAPP в отложения. Уменьшение массы -клеток может проявляться в виде гипергликемии и инсулинемии. Эта потеря массы -клеток может привести к необходимости лечения инсулином. Заболевания, вызванные гибелью или недостаточным функционированием конкретного типа или конкретных типов клеток, можно лечить трансплантацией пациенту здоровых клеток релевантного типа. Этот метод был использован для лечения больных диабетом типа I. Часто островковые клетки поджелудочной железы донора выращивают in vitro перед трансплантацией для того, чтобы использовать их после выделения для лечения, или для того, чтобы уменьшить их иммуногенность. Однако во многих случаях трансплантация островковых клеток не является успешной вследствие гибели трансплантированных клеток. Одной из причин такого малой доли успешных попыток является IAPP, который объединяется в токсические олигомеры. Токсическое действие может возникать вследствие внутриклеточной и внеклеточной аккумуляции фибриллярных олигомеров. Олигомеры IAPP могут образовывать фибриллы и становиться токсическими в отношении клеток in vitro. Кроме того, IAPP фибриллы, по-видимому, продолжают расти после трансплатации клеток и вызывают гибель или дисфункцию клеток. Это может происходить даже когда в клетках здорового донора и у получающего трансплантат пациента не наблюдается болезнь, характеризующаяся присутствием фибрилл. Например, соединения по настоящему изобретению можно использовать для получения тканей или клеток для трансплантации по методу, описанному в международной заявке (РСТ) WO 01/003680. Соединения по изобретению могут также стабилизировать отношение концентраций ProIAPP/IAPP, проинсулин/инсулин и уровни С-пептида. Помимо этого, в качестве биологических маркеров эффективности, результатов различных тестов, таких как тест секреции аргинина-инсулина, тест переносимости глюкозы и тесты чувствительности, все могут использоваться в качестве маркеров пониженной массы -клеток и/или аккумуляции амилоидных отложений. Такой класс лекарственных препаратов можно использовать вместе с другими лекарственными веществами, нацеленными на резистентность к инсулину, продуцирование печеночной глюкозы. Такие соединения могут предупреждать терапию инсулином, сохраняя функцию -клеток, и могут применяться для сохранения трансплантантов островков. Амилоидоз гормонального происхождения. Эндокринные органы могут накапливать амилоидные отложения, в особенности у старых людей. Опухоли, секретирующие гормоны, могут также содержать амилоидные бляшки гормонального происхождения, фибриллы которых состоят из полипептидных гормонов, таких как кальцитонин (медуллярный рак щитовидной железы), предсердный натриуретический пептид (выделенный амилоидоз предсердий). Последовательности и структуры этих белков хорошо известны в уровне техники. Смешанный амилоидоз. Существует множество других форм амилоидного заболевания, которые обычно проявляются как локализованные отложения амилоида. Эти заболевания являются результатом, главным образом, локализованным продуцированием или отсутствием катаболизма конкретных фибриллярных предшественников или предрасположением конкретной ткани (такой как суставная) к фибриллярному отложению. Примеры такого идиопатического отложения включают узелковый AL амилоид, кожный амилоид, эндокринный амилоид и амилоид, связанный с опухолью. Другие заболевания, связанные с амилоидом, включают заболевания, описанные в табл. 1, такие как семейная амилоидная полинейропатия (FAP), старческий (сенильный) системный амилоидоз, тендовагинит, семейный амилоидоз, типа Остертаг, ненейропатический амилоидоз, краниальную нейропатию, наследственную церебральную геморрагию, семейную деменцию,хронический диализ, семейную болезнь Крейтцфельда-Якоба; синдром Герстманна-ШтреусслераШейнкера, наследственный губчатый энцефалит, прионные заболевания, семейную средиземноморскую лихорадку, синдром Макла-Уэльса, нефропатию, глухоту, крапивницу, боль в конечностях, кожные отложения, множественную миелому, доброкачественную моноклональную гаммапатию, макроглобулинемию, амилоидоз, обусловленный миеломой, медуллярный рак щитовидной железы, изолированный ами- 12012429 лоидоз предсердий и диабет. Соединения по изобретению можно применять терапевтически или профилактически для лечения заболеваний, ассоциированных с образованием, агрегацией или отложением амилоидных фибрилл, вне зависимости от клинической картины. Соединения по изобретению могут облегчать течение амилоидного заболевания по любому из приведенных ниже механизмов, но без ограничения: замедление скорости образования или отложения амилоидных фибрилл; уменьшение степени амилоидного отложения; уменьшение степени амилоидного образования; ингибирование, уменьшение или предупреждение образования амилоидных фибрилл; ингибирование воспаления, индуцированного амилоидом; повышение клиренса амилоида, например, из мозга; или защита клеток от индуцированной амилоидом (олигомерным или фибриллярным) токсичности. В одном варианте изобретения соединения по изобретению можно применять терапевтически или профилактически для лечения заболеваний, ассоциированных с образованием, агрегацией или отложением -амилоидных фибрилл. Соединения по изобретению могут облегчать течение заболевания, связанного с -амилоидом, по любому из приведенных ниже механизмов (предполагается, что этот перечень является иллюстративным и не лимитирующим): замедление скорости образования или отложения амилоидных фибрилл; уменьшение степени -амилоидного отложения; ингибирование, уменьшение или предупреждение образования -амилоидных фибрилл; ингибирование нейродегенерации или клеточной токсичности, вызванной -амилоидом; ингибирование воспаления, индуцированного -амилоидом; повышение клиренса -амилоида из мозга; или содействие расщеплению (разрушению) А. Соединения по изобретению могут быть эффективны при контроле -амилоидного отложения либо после их проникновения в мозг (после прохождения через гематоэнцефалический барьер), либо с периферии. При действии с периферии соединение может изменять равновесие А между мозгом и плазмой таким образом, чтобы содействовать удалению А из мозга. Увеличение выхода А из мозга приводит к понижению концентрации А в мозге и, следовательно, способствует уменьшению А отложения. Кроме того, соединения, которые проникают в мозг, могут регулировать отложение, действуя непосредственно на А в мозге, например, сохраняя его в нефибриллярной форме или способствуя его клиренсу из мозга. Соединения могут замедлять процессирование АРР; могут увеличивать расщепление при использовании макрофагов или нейронных клеток; или могут снижать продуцирование А активированной микроглией. Эти соединения могли бы также предупреждать взаимодействие А в мозге с клеточной поверхностью и,следовательно, предупреждать нейротоксичность, нейродегенерацию и воспаление. В предпочтительном варианте изобретения применяется способ лечения болезни Альцгеймера (например, спорадической или семейной AD). Способ также можно применять профилактически или терапевтически для лечения других клинических случаев -амилоидного отложения, таких как у больных с синдромом Дауна и у больных церебральной амилоидной ангиопатией ("САА") или у больных с наследственной церебральной геморрагией, или больных ранней болезнью Альцгеймера. В другом варианте изобретения применяют способ лечения легкой когнитивной недостаточности. Легкая когнитивная недостаточность ("MCI") представляет собой состояние, характеризующееся легкой,но заметной утратой мыслительных способностей, которая необязательно связана с наличием деменции.MCI часто, но не всегда, предшествует болезни Альцгеймера. Кроме того, аномальная аккумуляция АРР и -амилоидного белка в мышечных волокнах влечет за собой патологию случайного миозита телец включений (IBM) (Askanas et al., Pros. Natl. Acad. Sci. USA 93, 1314-1319 (1996); Askanas et al., Current Opinion in Rheumathology 7, 486-496 (1995. Соответственно,соединения по изобретению можно применять профилактически или терапевтически при лечении нарушений, при которых -амилоидный белок аномально отлагается в ненейрологических участках, например, для лечения IBM доставкой соединений к мышечным волокнам. Кроме того, было показано, что А ассоциируется с аномальными внеклеточными отложениями,известными как друзы, которые аккумулируются вдоль базальной поверхности ретинального пигментированного эпителия у субъектов со старческой дегенерацией желтого пятна (ARMD). ARMD является причиной необратимой потери зрения у людей старшего возраста. Полагают, что отложение А может являться важным компонентом локальных воспалительных событий, которые способствуют атрофии ретинального пигментированного эпителия, биогенезу друз и патогенезу AMD (Johnson, et al., Pros. Natl.Acad. Sci. USA 99(18), 11830-5 (2002. В другом варианте изобретение относится к способу лечения или предупреждения амилоидного заболевания у субъекта (предпочтительно, у человека), заключающемуся в введении субъекту терапевтического количества соединения по нижеприведенным формулам или иным образом представленного в данном описании, так что уменьшается или ингибируется образование или отложение фибрилл, нейродегенерация или клеточная токсичность. В другом варианте изобретение относится к способу лечения или предупреждения амилоидного заболевания у субъекта (предпочтительно, у человека), заключающемуся в введении субъекту терапевтического количества соединения по нижеприведенным формулам или иным образом представленного в данном описании, так что у пациентов с амилоидозом мозга, например, у- 13012429 больных болезнью Альцгеймера, синдромом Дауна или церебральной амилоидной ангиопатией, когнитивная функция повышается или стабилизируется или дальнейшее ухудшение когнитивной функции предупреждается, замедляется или прекращается. Эти соединения могут также повысить качество повседневной жизни этих субъектов. Терапевтические соединения по изобретению могут лечить амилоидоз, связанный с диабетом типаII, например, стабилизируя гликемию, предупреждая или уменьшая потерю -клеточной массы, снижая или предупреждая гипергликемию вследствие потери -клеточной массы, и модулируя (например, повышая или стабилизируя) продуцирование инсулина. Соединения по изобретению могут также стабилизировать отношение концентраций про-IAPP/IAPP. Терапевтические соединения по изобретению могут лечить АА (вторичный) амилоидоз и/или AL(первичный) амилоидоз, стабилизируя почечную функцию, снижая протеинурию, повышая клиренс креатинина (например, по меньшей мере на 50% и более или по меньшей мере на 100% и более), способствуя ремиссии хронической диареи или прибавке в весе (например, на 10% или более) или снижая сывороточный креатинин. Можно также уменьшить висцеральное содержание амилоида, определяемое,например, SAP сцинтиграфией. Соединения по изобретению Настоящее изобретение относится, по меньшей мере частично, к применению некоторых химических соединений (и их фармацевтических препаратов) для предупреждения или лечения амилоидных заболеваний, включая, среди прочего, болезнь Альцгеймера, церебральную амилоидную ангиопатию,миозит телец включений, синдром Дауна, амилоидоз, связанный с диабетом, амилоидоз, связанный с гемодиализом (2 М), первичный амилоидоз (например, связанный с - или -цепью), семейную амилоидную полинейропатию (FAP), старческий (сенильный) системный амилоидоз, семейный амилоидоз,типа Остертаг ненейропатический амилоидоз, краниальную нейропатию, наследственную церебральную геморрагию, семейную деменцию, хронический диализ, семейную болезнь Крейтцфельда-Якоба; синдром Герстманна-Штреусслера-Шейнкера, наследственный губчатый энцефалит, прионные заболевания,семейную средиземноморскую лихорадку, синдром Макла-Уэльса, нефропатию, глухоту, крапивницу,боль в конечностях, кардиомиопатию, кожные отложения, множественную миелому, доброкачественную моноклональную гаммапатию, макроглобулинемию, амилоидоз, обусловленный миеломой, медуллярный рак щитовидной железы и изолированный амилоидоз предсердий. Химические структуры по данному описанию изображены в соответствии с известными в технике стандартами. Поскольку атом, такой как углеродный атом, так как он изображен, имеет недостающую валентность, предполагается, что эта валентность связана с водородом, даже если этот атом водорода не обязательно изображен. Структуры некоторых соединений по данному изобретению включают стереогенные атомы углерода. Следует отдавать отчет, что изомеры, возникающие вследствие такой асимметрии (например, все энантиомеры и диастереомеры), входят в объем настоящего изобретения, если не указано иначе. Т.е., если не указано иначе, любой хиральный углеродный центр может иметь либо (R)-, либо(S)-стереохимию. Такие изомеры можно получать в практически чистом виде классическими методами разделения или с помощью стереохимически контролируемого синтеза. Кроме того, когда это целесообразно, алкены могут иметь либо Е-, либо Z-геометрию. Помимо этого, соединения по настоящему изобретению могут существовать в несольватированной, а также в сольватированной с помощью соответствующих растворителей, таких как вода, ТГФ, этанол и т.п., форме. В целом сольвагированные формы считаются эквивалентными несольватированным формам для целей настоящего изобретения. Термин "малая молекула" относится к соединению, которое, само по себе, не является продуктом генной транскрипции или трансляции (например, белком, РНК или ДНК) и предпочтительно имеет низкую молекулярную массу, например менее примерно 2500 а.е.м. Термин "нуклеофил" является обычно общепринятым в технике термином для обозначения химической группы, содержащей реакционноспособную пару электронов, которая реагирует с соединением,замещая уходящую группу (обычно другой нуклеофил), как это обычно происходит в химии алифатических соединений по мономолекулярному (известному как "SN1") или бимолекулярному ("SN2") механизму. Примеры нуклеофилов включают не несущие заряд соединения, такие как амины, меркаптаны и спирты, и группы, имеющие заряд, такие как алкоксиды, тиолаты, карбанионы и ряд органических и неорганических анионов. Примеры анионных нуклеофилов включают, среди прочих, простые анионы, такие как азид, цианид, тиоцианат, формиат или хлорформиат и бисульфит. Металлоорганические реагенты, такие как медьорганические, цинкорганические, литийорганические соединения, реагенты Гриньяра,еноляты и ацетилиды, которые в соответствующих условиях являются подходящими нуклеофилами. Аналогично, термин "электрофил" означает атом, молекулу или ион, способные принимать электронную пару, в частности пару электронов от нуклеофила, как это обычно происходит в реакции электрофильного замещения. В реакции электрофильного замещения электрофил связывается с субстратом с удалением другого электрофила, например, замещение протона на другой электрофил, такой как ион нитрония, в ароматическом субстрате (например, бензоле). Электрофилы включают циклические соединения, такие как эпоксиды, азиридины, эписульфиды, циклические сульфаты, карбонаты, лактоны и лак- 14012429 тамы; а нециклические электрофилы включают сульфаты, сульфонаты (например, тозилаты), хлориды,бромиды и йодиды. Электрофил, как правило, может быть насыщенным углеродным атомом (например,метиленовая группа), связанным с уходящей группой; однако, электрофил может также быть ненасыщенной группой, такой как альдегидная, кето-, сложноэфирная группа, или их сопряженный (,ненасыщенный) аналог, который при реакции с нуклеофилом образует аддукт. Термин "уходящая группа", как правило, относится к группе, которая легко вытесняется и замещается нуклеофилом (например, амином, тиолом, спиртом или цианидом). Такие уходящие группы общеизвестны и включают карбоксилаты, N-гидроксисукцинимид ("NHS"), N-гидроксибензотриазол, галоген(фтор, хлор, бром или йод), алкоксиды и тиоалкоксиды. Обычно в химическом синтезе используют ряд серосодержащих уходящих групп, включая алкансульфонилоксигруппы (например, C1-C4-алкан, такие как метансульфонилокси-, этансульфонилокси-, пропансульфонилокси- и бутансульфонилоксигруппы) и галогенированные аналоги (например, галогенов(C1-C4-алкан)сульфонилоксигруппы, такие как трифторметансульфонилокси- (т.е. трифлат), 2,2,2-трихлорэтансульфонилокси-, 3,3,3-трибромпропансульфонилокси- и 4,4,4-трифторбутансульфонилоксигруппы), а также арилсульфонилоксигруппы (например,C6-C10-арил, необязательно замещенный 1-3 C1-C4-алкильными группами, такие как бензолсульфонилокси-, -нафтилсульфонилокси-, -нафтилсульфонилокси-, п-толуолсульфонилокси- (т.е. тозилаты), 4-третбутилбензолсульфонилокси-, мезитиленсульфонилокси- и 6-этилнафтилсульфонилоксигруппы)."Активированные сложные эфиры" можно представить формулой -COL, где L обозначает уходящую группу, типичные примеры которой включают N-гидроксисульфосукцинимидильная и Nгидроксисукцинимидильная группы; группы, замещенные электроноакцепторными группами (например,п-нитро, пентафтор, пентахлор, п-циано или п-трифторметил); и карбоновые кислоты, активированные карбодиимидом с образование ангидрида или смешанного ангидрида, например, -OCORa или OCNRaNHRb, где Ra и Rb, независимо, обозначают C1-C6-алкильная, C5-C8-алкильная (например, циклогексильная), C1-C6-перфторалкильная или C1-C6-алкоксильная группы. Активированный сложный эфир можно получать in situ или может быть отдельным реагентом. Сульфосукцинимидиловые сложные эфиры, пентафтортиофеноловые сложные эфиры и сульфотетрафторфеноловые сложные эфиры являются предпочтительными активированными сложными эфирами. Однако сложноэфирной уходящей группой может быть, например, замещенная или незамещенная C1-C6-алкильная (такая как метильная, этильная,пропильная, изопропильная, бутильная, изобутильная, втор-бутильная, трет-бутильная, пентильная или гексильная) группа, или замещенная C6-C14-арильная или гетероциклическая группа, такая как 2 фторэтильная, 2-хлорэтильная, 2-бромэтильная, 2,2-дибромэтильная, 2,2,2-трихлорэтильная, 3 фторпропильная, 4-хлорбутильная, метоксиметильная, 1,1-диметил-1-метоксиметильная, этоксиметильная, N-пропоксиметильная, изопропоксиметильная, N-бутоксиметильная, трет-бутоксиметильная, 1 этоксиэтильная, 1-метил-1-метоксиэтильная, 1-(изопропокси)этильная, 3-метоксипропил-4-метоксибутильная, фторметоксиметильная, 2,2,2-трихлорэтоксиметильная, бис-(2-хлорэтокси)метильная, 3 фторпропоксиметильная, 4-хлорбутоксиэтильная, дибромметоксиэтильная, 2-хлорэтоксимпропильная,фторметоксибутильная, 2-метоксиэтоксиметильная, этоксиметоксиэтильная, метоксиэтоксипропильная,метоксиэтоксибутильная, бензильная, фенетильная, 3-фенилпропильная, 4-фенилбутильная, нафтилметильная, -нафтилметильная, дифенилметильная, трифенилметильная, -нафтилдифенилметильная, 9-антранилметильная, 4-метилбензильная, 2,4,6-триметилбензильная, 3,4,5-триметилбензильная, 4-метоксибензильная, 4-метоксифенилдифенилметильная, 2-нитробензильная, 4-нитробензильная, 4-хлорбензильная, 4-бромбензильная, 4-цианобензильная, 4-цианобензилдифенилметильная или бис-(2-нитрофенил)метильная группы. Термин "электроноакцепторная группа" является общепринятой в уровне техники и описывает способность заместителя оттягивать на себя валентные электроны (например,(пи) электроны) от соседних атомов, например, заместитель является более электроотрицательным, чем соседние атомы, или он оттягивает на себя электроны сильнее, чем атом водорода в том же самом положении. Величина константы Гаммета сигмаявляется общепринятой мерой электронодонорной и электроноакцепторной способности группы, особенно значение сигма пара (р). См., например, "Advanced Organic Chemistry" by J. March,5th Ed., John WileySons, Inc., New York, pp.368-75 (2001). Значения константы Гаммета обычно отрицательны для электронодонорных групп (р=-0,66 для NH2) и положительны для электроноакцепторных групп (р=0,78 для нитрогруппы), причем р указывает на замещение в пара-положении. Примеры электроноакцепторных групп включают, среди прочих, нитро, ацильную (кетон), формильную (альдегид),сульфонильную, трифторметильную, галогено (например, хлор или фтор) и цианогруппы. Напротив,"электронодонорная группа" обозначает заместитель, который отдает электроны легче, чем водород, в случае, если он занимает то же самое положение в молекуле. Примеры включают, среди прочих, амино(включая алкиламино и диалкиламино), арильную, алкокси (включая аралкокси), арилокси, меркапто и алкилтио и гидроксильные группы. Применяемое в данном описании понятие "арильные" группы включает насыщенные углеводороды, содержащие один или более углеродный атом, включая линейные алкильные группы (например, метильную, этильную, пропильную, бутильную, пентильную, гексильную, гептильную, октальную, но- 15012429 нильную, децильную и т.д.), циклические алкильные группы (или "циклоалкильные", или "алициклические", или "карбоциклические" группы) (например, циклопропильную, циклопентильную, циклогексильную, циклогептильную, циклооктильную и т.д.), разветвленные алкильные группы (изопропильную,трет-бутильную, втор-бутильную, изобутильную и т.д.) и алкилзамещенные алкильные группы (например, алкилзамещенные циклоалкильные группы и циклоалкилзамещенные алкильные группы). Термин"алифатическая группа" включает органические частицы (фрагменты), для которых характерны линейные или разветвленные цепи, содержащие, как правило, 1-22 атома углерода. В сложных структурах цепи могут быть разветвленными, мостиковыми или сшитыми. Алифатические группы включают алкильные группы, алкенильные группы и алкинильные группы. В некоторых вариантах изобретения линейная или разветвленная алкильная группа может содержать в основной цепи 30 или меньше углеродных атомов, например C1-C30 для линейной цепи или C3-C30 для разветвленной цепи. В некоторых вариантах изобретения линейная или разветвленная алкильная группа может содержать 20 или менее углеродных атомов в основной цепи, например C1-C20 для линейной цепи или C3-C20 для разветвленной цепи, и более предпочтительно 18 углеродных атомов или менее. Аналогично, предпочтительные циклоалкильные группы содержат 4-10 углеродных атомов в циклической структуре и более предпочтительно 4-7 углеродных атомов в циклической структуре. Термин "низший алкил" относится к алкильным группам, содержащим 1-6 углеродных атомов в цепи, и к циклоалкильным группам, содержащим 3-6 углеродных атомов в циклической структуре. Если число углеродных атомов иначе не указано, "низший", как в "низший алифатический", "низший алкил", "низший алкенил" и т.д., по данному описанию означает, что группа (фрагмент) содержит по меньшей мере один и примерно менее 8 углеродных атомов. В некоторых вариантах изобретения линейная или разветвленная низшая алкильная группа содержит 6 или менее углеродных атомов в основной цепи (например, C1-C6 для линейной цепи, C3-C6 для разветвленной цепи) и более предпочтительно 4 или менее. Аналогично, предпочтительные циклоалкильные группы содержат 3-8 углеродных атомов в циклической структуре и более предпочтительно 5-6 углеродных атомов в циклической структуре. Термин "C1-C6", как в "C1-C6-алкил", означает алкильные группы, содержащие 1-6 углеродных атомов. Кроме того, если не указано иначе, термин "алкил" включает как "незамещенные алкилы", так и"замещенные алкилы", последний термин относится к алкильным группам, содержащие заместители,замещающие один или более атомов водорода при одном или более углеродных атомов в основной цепи углеводорода. Такие заместители могут включать, например, алкенильную, алкинильную, галогено, гидроксильную группы, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилокси, арилоксикарбонилокси, карбоксилатную, алкилкарбонильную, арилкарбонильную, алкоксикарбонильную, аминокарбонильную, алкиламинокарбонильную, диалкиламинокарбонильную, алкилтиокарбонильную, алкоксильную, фосфатную, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), имино, сульфгидрильную, алкилтио, арилтио, тиокарбоксилатную, сульфатную алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметильную, циано, азидо, гетероциклическую, алкиларильную или ароматическую (включая гетероароматическую) группы."Арилалкильная" группа обозначает алкильную группу, замещенную арильной группой (например,фенилметильной (т.е. бензильной. "Алкиларильная" группа обозначает арильную группу, замещенную алкильной группой (например, п-метилфенильной (т.е. п-толильной. Термин "н-алкил" означает линейную (т.е. неразветвленную) незамещенную алкильную группу. "Алкиленовая" группа обозначает двухвалентный аналог соответствующей алкильной группы. Термины "алкенил" и "алкинил" относятся к ненасыщенным алифатическим группам, аналогичным алкила, но содержащим по меньшей мере одну двойную или тройную углерод-углеродную связь, соответственно. Соответствующие алкенильная и алкинильная группы включают группы, содержащие около 2-12 углеродных атомов, предпочтительно от 2 примерно до 6 углеродных атомов. Термин "ароматическая группа" или "арильная группа" включает ненасыщенные и ароматические циклические углеводороды, а также ненасыщенные и ароматические гетероциклы, содержащие один или более циклов. Арильные группы могут быть также конденсированными или мостиковыми с алициклическими или гетероциклическими циклами, которые не являются ароматическими, так что образуется полициклическая система (например, тетралин). "Ариленовая" группа является двухвалентным аналогом арильной группы. Арильные группы могут быть также конденсированными или мостиковыми с алициклическими или гетероциклическими циклами, которые не являются ароматическими, так что образуется полициклическая система (например, тетралин). Термин "гетероциклическая группа" включает замкнутые циклические структуры, аналогичные карбоциклическим группам, в которых один или более углеродных атомов в цикле представляет собой иной атом, нежели углеродный, например, атом азота, серы или кислорода. Гетероциклические группы могут быть насыщенными или ненасыщенными. Кроме того, гетероциклические группы (такие как пирролил, пиридил, изохинолил, хинолил, пуринил и фурил) могут иметь ароматический характер, в этом случае их можно называть "гетероарильная" или "гетероароматическая" группы. Если не указано иначе, арильная и гетероциклическая группы (включая гетероарильную) могут- 16012429 также быть замещенными по одному или более структурных атомов. Примеры гетероароматических и гетероалициклических групп могут содержать 1-3 раздельных или конденсированных цикла с 3-8 членами в цикле и один или более гетероатом N, О или S. Обычно термин "гетероатом" включает иные атомы,нежели атомы углерода и водорода, предпочтительные примеры гетероатомов включают азот, кислород,серу или фосфор. Гетероциклические группы могут быть насыщенными, или ненасыщенными, или ароматическими. Примеры гетероциклов включают, но без ограничения, акридинил; азоцинил; бензимидазолил; бензофуранил; бензотиофуранил; бензотиофенил; бензоксазолил; бензотиазолил; бензотриазолил; бензотетразолил; бензизоксазолил; бензизотиазолил; бензимидазолинил; карбазолил; 4 аН-карбазолил; карболинил; хроманил; хроменил; циннолинил; декагидрохинолинил; 2 Н,6 Н-1,5,2-дитиазинил; дигидрофуро[2,3b]тетрагидрофуран; фуранил; фуразанил; имидазолидинил; имидазолинил; имидазолил; 1 Н-имидазолил; индоленил; индолинил; индолизинил; индолил; 3 Н-индолил; изобензофуранил; изохроманил; изоиндазолил; изоиндолинил; изоиндолил; изохинолинил; изотиазолил; изоксазолил; метилендиоксифенил; морфолинил; нафтаридинил; октагидроизохинолинил; оксадиазолил; 1,2,3-оксадиазолил; 1,2,4-оксадиазолил; 1,2,5-оксадиазолил; оксалидинил; оксазолил; оксалидинил; пиримидинил; фенантридинил; фенантролинил; феназинил; фенотиазинил; феноксатиинил; феноксазинил; фталазинил; пиперазинил; пиперидонил; 4-пиперидонил; пиперонил; птеридинил; пуринил; пиранил; пиразолидинил; пиразолинил; пиразолил; пиридазинил; пиридоксазол; пиридоимидазол; пиридотиазол; пиридинил; пиридил; пиримидинил; пирролидинил; пирролинил; 2 Н-пирролил; пирролил; хиназолинил; хинолинил; 4 Н-хинолизинил; хиноксалинил; хинуклидинил; тетрагидрофуранил; тетрагидроизохинолинил; тетрагидрохинолинил; тетразолил; 6 Н-1,2,5-тиадиазинил; 1,2,3-тиадиазолил; 1,2,4-тиадиазолил; 1,2,5-тиадиазолил; 1,3,4-тиадиазолил; тиантренил; тиазолил; тиенил; тиенотиазолил; тиенооксазолил; тиеноимидазолил; тиофенил; триазинил; 1,2,3-триазолил; 1,2,4-триазолил; 1,2,5-триазолил; 1,3,4-триазолил и ксантенил. Предпочтительные гетероциклы включают, но без ограничения, пиридинильную; фуранильную; тиенильную; пирролильную; пиразолильную; пирролидинильную; имидазолильную; индолильную; бензимидазолильную; 1 Ниндазолильную; оксазолидинильную; бензотриазолильную; бензизоксазолильную; оксиндолильную; бензоксазолинильную и изатиноильную группы. Также включаются конденсированные циклические и спиросоединения, содержащие, например, вышеприведенные гетероциклы. Обычной углеводородной арильной группой является фенильная группа, имеющая один цикл. Бициклические углеводородные арильные группы включают нафтильную, инденильную, бензоциклооктенильную, бензоциклогептенильную, пенталенильную и азуленильную группы, а также их частично гидрированные аналоги, такие как инданил и тетрагидронафтил. Типичные трициклические углеводородные арильные группы включают ацефтиленильную, флуоренильную, феналенильную, фенантренильную и антраценильную группы. Арильные группы также включают гетеромоноциклические арильные группы, т.е. одноциклические гетероарильные группы, такие как тиенильная, фурильная, пиранильная, пирролильная, имидазолильная,пиразолильная, пиридинильная, пиразинильная, пиримидинильная и пиридазинильная группы; и их окисленные аналоги, такие как пиридонильная, оксазолонильная, пиразолонильная, изоксазолонильная и тиазолонильная группы. Соответствующие гидрированные (т.е. неароматические) гетеромоноциклические группы включают пирролидинильную, пирролинильную, имидазолидинильную, имидазолинильную, пиразолидинильную, пиразолинильную, пиперидильную и пиперидино, пиперазинильную, и морфолино и морфолинильную группы. Арильные группы также включают бициклические гетероарилы, такие как индолильная, изоиндолильная, индолизинильная, индазолинильная, хинолинильная, изохнолинильная, фталазинильная, хиноксалинильная, хиназолинильная, циннолинильная, хроменильная, изохроменильная, бензотиенильная,бензимидазолильная, бензотиазолильная, пуринильная, хиназолинильная, изохинолонильная, хинолонильная, нафтиридинильная и птеридинильная группы, а также частично гидрированные аналоги, такие как хроманильная, изохроманильная, индолинильная, изоиндолинильная и тетрагидроиндолинильная группы. Арильные группы также включают конденсированные трициклические группы, такие как феноксатиинильная, карбазолильная, фенантридинильная, акридинильная, перимидинильная, фенантролинильная, феназинильная, фенотиазинильная, феноксазинильная и дибензофуранильная группы. Некоторые типичные арильные группы включают насыщенные или ненасыщенные 5- и 6-членные моноциклические группы. В другом аспекте каждая Ar группа может выбираться из группы, состоящей из замещенной или незамещенной фенильной, пирролильной, фурильной, тиенильной, тиазолильной,изотиазолильной, имидазолильной, тиазолильной, триазолильной, тетразолильной, пиразолильной, оксазолильной, изоксаозолильной, пиридинильной, пиразинильной и пиримидинильной групп. Другие примеры включают замещенные или незамещенные фенильную, 1-нафтильную, 2-нафтильную, бифенильную, 1-пирролильную, 2-пирролильную, 3-пирролильную, 3-пиразолильную, 2-имидазолильную, 4 имидазолильную, пиразинильную, 2-оксазолильную, 4-оксазолильную, 5-оксазолильную, 3 изоксазолильную, 4-изоксазолильную, 5-изоксазолильную, 2-тиазолильную, 4-тиазолильную, 5 тиазолильную, 2-фурильную, 3-фурильную, 2-тиенильную, 3-тиенильную, 2-пиридильную, 3 пиридильную, 4-пиридильную, 2-пиримидильную, 4-пиримидильную, 5-бензотиазолильную, пуриниль- 17012429 ную, 2-бензимидазолильную, 5-индолильную, 1-изохинолинильную, 5-изохинолинильную, 2 хиноксалинильную, 5-хиноксалинильную, 3-хинолинильную и 6-хинолинильную группы. Термин "амин" или "амино" по данному описанию относится к незамещенной или замещенной группе формулы -NRaRb, где Ra и Rb, каждый независимо, обозначают водород, алкил, арил или гетероциклил, или Ra и Rb вместе с атомом азота, с которым они связаны, образуют циклическую группу, содержащую 3-8 атомов в цикле. Таким образом, если не указано иначе, термин "амино" включает циклические аминогруппы, такие как пиперидинильная или пирролидинильная группы. Таким образом, термин "алкиламино" по данному описанию обозначает алкильную группу, содержащую соединенную с ней аминогруппу. Подходящие алкиламиногруппы включают группы, содержащие от 1 примерно до 12 углеродных атомов, предпочтительно от 1 примерно до 6 углеродных атомов. Термин "амино" включает соединения или группы, в которых атом азота ковалентно связан по меньшей мере с одним углеродным атомом или гетероатомом. Термин "диалкиламино" включает группы, в которых атом азота связан по меньшей мере с двумя алкильными группами. Термин "ариламино" и "диариламино" включает группы, в которых атом азота связан по меньшей мере с одной или двумя арильными группами, соответственно. Термин "алкилариламино" относится к аминогруппе, которая связана по меньшей мере с одной алкильной группой и по меньшей мере с одной арильной группой. Термин "алкиламиноалкил" относится к алкильной, алкенильной или алкинильной группе, замещенной алкиламиногруппой. Термин "амид" или"аминокарбонил" включает соединения или группы, которые содержат атом азота, связанный с углеродом карбонильной или тиокарбонильной группы. Термин "алкилтио" относится к алкильной группе, содержащей соединенную с ней сульфгидрильную группу. Подходящие алкилтиогруппы включают группы, содержащие от 1 примерно до 12 углеродных атомов, предпочтительно от 1 примерно до 6 углеродных атомов. Термин "алкилкарбоксил" по данному описанию обозначает алкильную группу, содержащую соединенную с ней карбоксильную группу. Термин "алкокси" по данному описанию означает алкильную группу, содержащую соединенный с ней атом кислорода. Типичные алкоксигруппы включают группы, содержащие от 1 примерно до 12 углеродных атомов, предпочтительно от 1 примерно до 6 углеродных атомов, например метокси, этокси,пропокси, трет-бутокси и т.п. Примеры алкоксигрупп включают метокси, этокси, изопропилокси, пропокси, бутокси и пентоксигруппы. Алкоксигруппы могут быть замещены такими группами, как алкенильная, алкинильная, галоген, гидроксильная, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилатная, алкилкарбонильная, арилкарбонильная, алкоксикарбонильная, диалкиламинокарбонильная, алкилтиокарбонильная, алкоксильная, фосфатная, фосфонато,фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), имино,сульфгидрильная, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинильная, сульфонато,сульфамоил, сульфонамидо, нитро, трифторметильная, циано, азидо, гетероциклильная, алкиларильная или ароматическая или гетероароматическая группы. Примеры галогензамещенных алкоксигрупп включают, но без ограничения, фторметокси, дифторметокси, трифторметокси, хлорметокси, дихлорметокси,трихлорметокси и т.д., а также пергалогенированные алкоксигруппы. Термин "ациламино" включает группы, в которых аминогруппа связана с ацильной группой. Например, ациламиногруппа включает алкилкарбониламино, арилкарбониламино, карбамоильную и уреидогруппы. Термины "алкоксиалкил", "алкиламиноалкил" и "тиоалкоксиалкил" включают вышеописанные алкильные группы, которые дополнительно включают атомы кислорода, азота или серы, замещающие один или более углеродных атомов углеводородного скелета. Термин "карбонил" или "карбокси" включает соединения и группы, которые содержат атом углерода, соединенный двойной связью с атомом кислорода. Примеры групп, которые содержат карбонил,включают альдегиды, кетоны, карбоновые кислоты, амиды, сложные эфиры, ангидриды и т.д. Термин "простой эфир" или "эфирный" включает соединения или группы, которые содержат атом кислорода, соединенный с двумя углеродными атомами. Например, простой эфир или простая эфирная группа включает "алкоксиалкил", который относится к алкильной, алкенильной или алкинильной группе,замещенной алкоксигруппой."Сульфонатная" группа обозначает группу -SO3H или -SO3-X+, связанную с углеродным атомом, где+ Х обозначает катионную противоионную группу. Аналогично, "сульфоновая кислота" содержит группу"сульфат" по данному описанию обозначает группу -OSO3H или -OSO3-X+, связанную с углеродным атомом, а "сульфокислота" обозначает группу -OSO3H или -OSO3-X+, связанную с углеродным атомом, где Х+ обозначает катионную группу. Согласно данному изобретению подходящей катионной группой может быть атом водорода. В некоторых случаях катионная группа на самом деле может быть иной группой в терапевтическом соединении, которая положительно заряжена при физиологическом pH, например, аминогруппой."Противоион" требуется для сохранения нейтрального общего заряда. Примеры анионных противо- 18012429 ионов включают галоген, трифлат, сульфат, нитрат, гидроксид, карбонат, бикарбонат, ацетат, фосфат,оксалат, цианид, алкилкарбоксилат, N-гидроксисукцинимид, N-гидроксибензотриазол, алкоксид, тиоалкоксид, алкансульфонилокси, галогенированный алкансульфонилокси, арилсульфонилокси, бисульфат,оксалат, валерат, олеат, пальмитат, стеарат, лаурат, борат, бензоат, лактат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат мезилат, глюкогептонат или лактобионат. Соединения, содержащие катионную группу, ковалентно связанную с анионной группой, можно называть "внутренними солями". Термин "нитро" обозначает -NO2; термин "галоген" или "галогено", или "галоид" ("гало") обозначает -F, -Cl, -Br или -I; термин "тиол", "тио" или "меркапто" обозначает SH; и термин "гидроксил" или"гидрокси" обозначает -ОН. Термин "ацил" относится к карбонильной группе, через свой углеродный атом соединенной с водородом (т.е. формил), алифатической группой (например, ацетил), ароматической группой (например,бензоил) и т.п. Термин "замещенный ацил" включает группы, в которых один или более атомов водорода при одном или более углеродных атомов замещены, например, на алкильную группу, алкинильную группу, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано,амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино(включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, циано, азидо, гетероциклил, алкиларил или ароматическую или гетероароматическую группу. Если не указано иначе, химические группы (фрагменты) соединений по изобретению, включая группы, обсуждавшиеся выше, могут быть "замещенными или незамещенными". В некоторых вариантах изобретения термин "замещенный" означает, что группа имеет заместители, отличные от водорода (т.е. в большинстве случаев замещают водород), которые содействуют осуществлению молекулой предполагаемой функции. Примеры заместителей включают фрагменты (группы), выбранный из линейного или разветвленного алкила (предпочтительно, C1-C5), циклоалкила (предпочтительно, C3-C8), алкокси (предпочтительно, C1-C6), тиоалкила (предпочтительно, C1-C6), алкенила (предпочтительно, C2-C6), алкинила(предпочтительно, C2-C6), гетероцикличеческой, карбоциклической, арильной (например, фенильной) групп, арилокси (например, фенокси), аралкила (например, бензила), арилоксиалкила (например,фен(ил)оксиалкила)арилацетамидоила, алкиларила, гетероаралкила, алкилкарбонила и арилкарбонила или другой подобной ацильной группы, гетероарилкарбонильной и гетероарильной групп, а такжеR' и R", каждый независимо, обозначает водород, C1-C5-алкильную, C2-C5-алкенильную, C2-C5 алкинильную или арильную группу; или боковую цепь любой природной аминокислоты. В другом варианте изобретения заместитель можно выбирать из линейного или разветвленного алкила (предпочтительно, C1-C5), циклоалкила (предпочтительно, C3-C8), алкокси (предпочтительно, C1C6), тиоалкила (предпочтительно, C1-C6), алкенила (предпочтительно, C2-C6), алкинила (предпочтительно, C2-C6), гетероциклической, карбоциклической, арильной (например, фенильной) групп, арилокси(например, фенокси), аралкила (например, бензила), арилоксиалкила (например, фен(ил)оксиалкила),арилацетамидоила, алкиларила, гетероаралкила, алкилкарбонила и арилкарбонила или другой подобной ацильной группы, гетероарилкарбонильной или гетероарильной групп, а также (CR'R")0-10NR'R" (например, NH2), (CR'R")0-10CN (например, -CN), -NO2, галогена (например, -F, -Cl, -Br или -I), (CR'R")0-10C(галоген)3(например, -CF3), (CR'R")0-10 СН(галоген)2, (CR'R")0-10CH2(галоген), (CR'R")0-10CONR'R", (CR'R")0-10(CNH)NR'R",(CR'R")0-10S(O)1-2NR'R", (CR'R")0-10CHO, (CR'R")0-10O(CR'R")0-10H, (CR'R")0-10S(O)0-3R' (например, -SO3H),(CR'R")0-10O(CR'R")0-10H (например, -СН 2 ОСН 3 и -ОСН 3), (CR'R")0-10S(CR'R")0-3H (например, -SH и -SCH3),(CR'R")0-10OH (например, -ОН), (CR'R")0-10COR', (CR'R")0-10(замещенный или незамещенный фенил),(CR'R")0-10(C3-C8-циклоалкил), (CR'R")0-10CO2R' (например, -CO2H) и (CR'R")0-10OR' группы, или боковой цепи любой природной аминокислоты; где R' и R", каждый независимо, обозначает водород, C1-C5 алкильную, C2-C5-алкенильную, C2-C5-алкинильную или арильную группу, или R' и R" вместе обозначают бензилиденовую группу или -(СН 2)2 О(СН 2)2-группу. Следует понимать, "замещение" или "замещенный на" включает подразумеваемое условие, что такое замещение осуществляется в соответствии с валентностью замещаемого атома и заместителя и что замещение в результате приводит к устойчивому соединению, такому, например, которое не претерпевает самопроизвольного превращения, такого как перегруппировка, циклизация, элиминирование и т.д. Предполагается, что применяемый в данном описании термин "замещенный" включает все допустимые заместители органического соединения. В широком аспекте допустимые заместители включают ацикли- 19012429 ческие и циклические, разветвленные и неразветвленные, карбоциклические и гетероциклические, ароматические и неароматические заместители органических соединений. Допустимых заместителей может быть один или более. В некоторых вариантах изобретения "заместитель" может выбираться из группы, состоящей, например, из C1-C6-алкильной, C2-C6-алкенильной, C2-C6-алкинильной, C1-C6-алкилкарбонилокси, арилкарбонилокси, C1-C6-алкоксикарбонилокси, арилоксикарбонилокси, C1-C6-алкилкарбонильной, C1-C6 алкоксикарбонильной, C1-C6-алкокси, C1-C6-алкилтио, арилтио, гетероциклильной, арилалкильной(включая гетероарильную) групп. В одном варианте изобретение относится к соединениям формулы (I) где R1 обозначает замещенный или незамещенный циклоалкил, гетероциклил, арил, арилциклоалкил,бициклическую или трициклическую группу, конденсированную бициклическую или трициклическую группу или замещенную или незамещенную C2-C10-алкильную группу;Y обозначает SO3-X+, OSO3-Х+ или S SO3-Х+; Х+ обозначает водород, катионную группу или группу, образующую сложный эфир; и каждый из L1 и L2 обозначает, независимо, замещенную или незамещенную C1-C5-алкильную группу или отсутствует,или к их фармацевтически приемлемой соли, при условии, что, когда R1 обозначает алкил, L1 отсутствует. В другом варианте изобретение относится к соединениям формулы (II) где R1 обозначает замещенную или незамещенную циклическую, бициклическую, трициклическую или бензогетероциклическую группу или замещенную или незамещенную C2-C10-алкильную группу;Y обозначает SO3-X+, OSO3-X+ или S SO3-X+; Х+ обозначает водород, катионную группу или группу, образующую сложный эфир;L обозначает замещенную или незамещенную C1-C5-алкильную группу или отсутствует,или к их фармацевтически приемлемой соли, при условии, что, когда R1 обозначает алкил, L отсутствует. В другом варианте изобретения R2 обозначает водород. Еще в одном варианте изобретения R1 обозначает линейный алкил, например, этил, н-пентил, н-гептил или н-октил. В другом варианте изобретения R1 обозначает трет-бутил. Еще в одном альтернативном варианте изобретения R1 обозначает C7-C10 бициклоалкил или трициклоалкил, например, такой как трицикло[3.3.1.03,7]децил (или адамантил), бицикло[2.1.2]гептил или индолил. В другом альтернативном варианте изобретения R1 обозначает тетрагидронафтил. В одном варианте изобретения L2 обозначает -(СН 2)3-. В другом дополнительном варианте L2 обозначает -(СН 2)4- или -(СН 2)5-. Еще в одном дополнительном варианте изобретения L2 обозначает -(СН 2)2. Еще в одном дополнительном варианте изобретения L2 обозначает замещенный алкил, например -СН 2(CHOH)-СН 2-. В другом варианте изобретения L2 обозначает СН 2 СН 2 или отсутствует. В другом варианте изобретения R1 обозначает разветвленный алкил, например трет-бутил. В другом варианте изобретения R1 обозначает адамантил. В другом варианте изобретения R1 обозначает циклический алкил, например, циклопропил, циклогексил, циклогептил, циклооктил и т.д. Циклоалкильные группы могут быть далее замещенными, например, дополнительными алкильными группами или другими группами, которые содействуют осуществлению молекулой предполагаемой функции. В другом варианте изобретения R1 обозначает алкил, замещенный пропаргильным фрагментом (например -НСС-). В другом варианте изобретения R1 обозначает циклогексил, замещенный одной или более метильной или пропаргильной группами. В других вариантах изобретения L1 обозначает C1-C2-алкильную линкерную группу (например,-СН(СН 3)- или -(СН 2)2-). В другом варианте изобретения R1 обозначает фенил. В некоторых вариантах изобретения R1 замещен метоксигруппой. В других вариантах изобретения L1 обозначает С 3, например-(СН 2)3- или С(СН 3)2-. В некоторых вариантах изобретения L1 замещен, например, алкокси, карбоксилатной (-СООН), бензильной, амидо (-C=O-NH-) или сложноэфирной (С=О-С-О) группой. В некоторых вариантах изобретения сложноэфирная группа представляет собой метиловую, этиловую, пропиловую,бутиловую, циклогексиловую сложноэфирную группу. В других вариантах изобретения сложноэфирная группа может быть пропенильной группой. В других вариантах изобретения L1 замещен карбоксилатной группой. В другом варианте изобретения R1 замещен замещенной амидной группой, где амидная группа замещена алкильной, например, метильной, этильной, пропильной, бутильной, пентильной или гексильной группой. В другом варианте изобретения алкильная R1 группа замещена -C=O-NH-OH, C=O-NH2 или амидогруппой. В некоторых вариантах изобретения амидогруппа замещена алкильной (например, метильной, этильной, пропильной, бутильной, пентильной, гексильной, циклогексильной и т.д.), бензильной или арильной группой. В другом варианте изобретения амидогруппа замещена -СН(СН 2)2- группой. Сам R' может быть замещен фенилом или может быть разветвленным или линейным алкилом. В некоторых вариантах изобретения R' может быть также замещен тиоэфирной группой. Примеры тиоэфиров включают S-Me, S-Et и т.д. В некоторых вариантах изобретения алкильная R1 группа замещена как арильной, так и тиоэфирной группой и амидогруппой. В других вариантах изобретения алкильная R1 группа может быть замещена как тиоэфирной, так и карбоксилатной группой. В других вариантах изобретения алкильные R1 группы замещены гидроксилом. R1 группы, например, алкильные R1 группы, могут быть также замещены как тиоэфирной, так и гидроксильной группой. В других вариантах изобретения R1 группы, например, алкильные R1 группы, замещены цианогруппой. Примеры R1 групп, содержащих -CN фрагменты, включают C(CH3)2CN, циклогексил, замещенный одной или более цианогруппой и т.д. В других вариантах изобретения алкильные R1 группы замещены арильными группами. Арильные группы могут представлять собой, например, замещенный фенил. Замещенный фенил может быть замещен одним или более заместителей, таких как гидрокси, циано и алкокси. В других вариантах изобретения алкильные R1 группы замещены тетразолилом или замещенным или незамещенным бензилом. В других вариантах изобретения L1 обозначает -С(СН 3)2-СНОН. Еще в одном варианте изобретения 1L обозначает -С(СН 3)2 СН(ОМе)-. В другом варианте изобретения R1 обозначает замещенный или незамещенный фенил. Еще в одном варианте изобретения R1 обозначает паразамещенный фенил. Примеры заместителей включают, но без ограничения, фтор, хлор, бром, йод, метил, трет-бутил, алкокси, метокси и т.д. В другом варианте изобретения R1 замещен в мета-положении. Примеры заместителей включают метокси, хлор, метил, трет-бутил, фтор, алкил, алкокси, йод, трифторалкил, метокси, и т.д. В другом варианте изобретения R1 обозначает фенил, замещенный аналогичными заместителями в орто-положении. В другом варианте изобретения L1 содержит циклоалкильный фрагмент, например, циклопентил. В другом варианте изобретения L1 содержит алкенильную группу и, необязательно, замещенную арильную группу с заместителями, аналогичными вышеописанным. В некоторых вариантах изобретения R1 обозначает циклопропил или циклогексил. В некоторых вариантах изобретения циклопропильная или циклогексильная группа замещена простой эфирной группой или алкильной группой. В некоторых дополнительных вариантах изобретения простая эфирная группа представляет собой группу простого бензилового эфира. В другом варианте изобретения, в которых R1 обозначает алкил, он замещен группами, такими как фенил или гидрокси. В других вариантах изобретения соединение по изобретению выбирают из группы, состоящей из
МПК / Метки
МПК: A61P 25/28, A61K 31/185, C07C 309/14
Метки: амилоидных, способы, лечения, композиции, заболеваний
Код ссылки
<a href="https://eas.patents.su/30-12429-sposoby-i-kompozicii-dlya-lecheniya-amiloidnyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Способы и композиции для лечения амилоидных заболеваний</a>
Предыдущий патент: Устройство для наполнения контейнера складного типа
Следующий патент: Производные пропионамида, полезные в качестве модуляторов андрогенных рецепторов
Случайный патент: Ингибиторы протеина, активирующего 5-липоксигеназу (flap)