Лечение доброкачественной гиперплазии простаты селективным модулятором рецептора андрогенов ( sarm )
Номер патента: 13399
Опубликовано: 30.04.2010
Авторы: Стейнер Митчелл С., Веверка Карен А., Джао Венквинг, Миллер Дуэйн Д., Долтон Джеймс Т.
Формула / Реферат
1. Способ блокирования способности дигидротестостерона (DHT) индуцировать гиперплазию, который включает стадию контактирования рецептора андрогенов с соединением - селективным модулятором рецептора андрогенов (SARM) формулы I

в которой G представляет собой О или S;
X представляет собой связь, О, CH2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, СООН, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН, и
R1 представляет собой СН3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода;
или изомером, фармацевтически приемлемой солью, гидратом или N-оксидом указанного соединения SARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию.
2. Способ ингибирования митогенного действия тестостерона и DHT, который включает стадию контактирования рецептора андрогенов с соединением SARM формулы I

в которой G представляет собой О или S;
X представляет собой связь, О, СН2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, СООН, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН, и
R1 представляет собой СН3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода, тем самым ингибируя митогенную активность тестостерона и DHT.
3. Способ ингибирования рекрутирования коактиваторов или корегуляторов андроген-респонсивной ДНК, который включает стадию контактирования рецептора андрогенов с соединением SARM формулы I
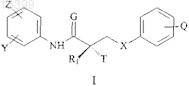
в которой G представляет собой О или S;
X представляет собой связь, О, СН2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, COOH, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН, и
R1 представляет собой CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода;
тем самым ингибируя рекрутирование коактиваторов или корегуляторов андроген-респонсивной ДНК.
4. Способ лечения пациентов-мужчин, страдающих от доброкачественной гиперплазии простаты, который включает стадию введения указанному пациенту соединения - селективного модулятора рецептора андрогенов (SARM) формулы I
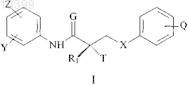
в которой G представляет собой О или S;
X представляет собой связь, О, СН2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, СООН, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН, и
R1 представляет собой СН3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3,
где алкил содержит 1-12 атомов углерода.
5. Способ по п.1, который предусматривает введение изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного SARM или любого их сочетания.
6. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой II
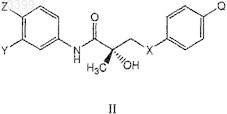
в которой X представляет собой связь, О, СН2, NH, Se или NO;
Z представляет собой NO2, CN, COOH, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, С(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, С(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН,
где алкил содержит 1-12 атомов углерода.
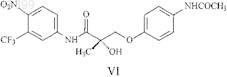
7. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VI
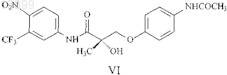
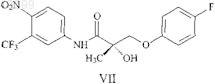
8. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VII

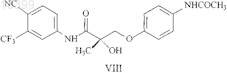
9. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VIII
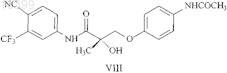
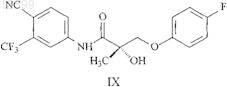
10. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой IX
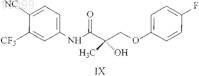
11. Способ по п.1, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5a-редуктазы.
12. Способ по п.1, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5a-редуктазы.
13. Способ по п.12, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 1.
14. Способ по п.12, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 2.
15. Способ по п.1, в котором фермент 5a-редуктаза представляет собой фермент тестостерон-5a-редуктазу.
16. Способ по п.4, в котором указанное введение включает внутривенную, внутриартериальную или внутримышечную инъекцию указанному пациенту указанного соединения SARM в жидкой форме; подкожную имплантацию указанному пациенту гранулы, содержащей указанное соединение SARM; оральное введение указанному пациенту указанного соединения SARM в жидкой или твердой форме; или местное нанесение на поверхность кожи указанного пациента указанного соединения SARM.
17. Способ предупреждения, подавления, ингибирования или снижения заболеваемости доброкачественной гиперплазией простаты у пациентов-мужчин, который включает стадию введения указанному пациенту соединения SARM формулы I

в которой G представляет собой О или S;
X представляет собой связь, О, СН2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, СООН, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН, и
R1 представляет собой CH3, CH2F, CHF2, CF3, CH2CH3, или CF2CF3,
где алкил содержит 1-12 атомов углерода;
или изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного соединения SARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию.
18. Способ по п.17, который включает введение изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного SARM или любого их сочетания.
19. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой II
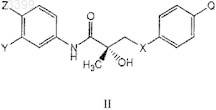
в которой X представляет собой связь, О, СН2, NH, Se или NO;
Z представляет собой NO2, CN, COOH, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН,
где алкил содержит 1-12 атомов углерода.
20. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой VI

21. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой VII
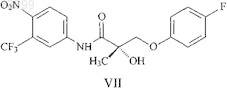
22. Способ по п.17, в котором соединение SARM представлено структурной формулой VIII
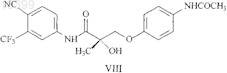
23. Способ по п.17, в котором соединение SARM представлено структурной формулой IX
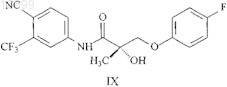
24. Способ по п.17, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5a-редуктазы.
25. Способ по п.17, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5a-редуктазы.
26. Способ по п.25, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 1.
27. Способ по п.25, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 2.
28. Способ по п.25, в котором фермент 5a-редуктаза представляет собой фермент тестостерон-5a-редуктазу.
29. Способ по п.17, в котором указанное введение включает внутривенную, внутриартериальную или внутримышечную инъекцию указанному пациенту указанного соединения SARM в жидкой форме; подкожную имплантацию указанному пациенту гранулы, содержащей указанное соединение SARM; оральное введение указанному пациенту указанного соединения SARM в жидкой или твердой форме; или местное нанесение на поверхность кожи указанного пациента указанного соединения SARM.
30. Способ ингибирования фермента 5a-редуктазы, который включает контактирование указанного фермента с эффективным ингибирующим 5a-редуктазу количеством соединения SARM формулы I
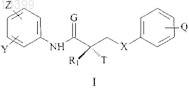
в которой G представляет собой О или S;
X представляет собой связь, О, СН2, NH, Se или NO;
Т представляет собой ОН, OR, -NHCOCH3 или NHCOR;
Z представляет собой NO2, CN, СООН, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, C(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН и
R1 представляет собой СН3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3,
где алкил содержит 1-12 атомов углерода;
или изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного соединения SARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию.
31. Способ по п.30, который включает введение изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного SARM или любого их сочетания.
32. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой II
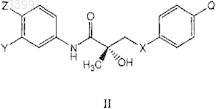
в которой X представляет собой связь, О, СН2, NH, Se или NO;
Z представляет собой NO2, CN, COOH, COR, NHCOR или CONHR;
Y представляет собой CF3, F, I, Br, Cl, CN, С(R)3 или Sn(R)3;
Q представляет собой алкил, галоген, CF3, CN, C(R)3, Sn(R)3, N(R)2, NHCOCH3, NHCOCF3, NHCOR, NHCONHR, NHCOOR, OCONHR, CONHR, NHCSCH3, NHCSCF3, NHCSR, NHSO2CH3, NHSO2R, OR, COR, OCOR, OSO2R, SO2R, SR;
R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, галоген, алкенил или ОН,
где алкил содержит 1-12 атомов углерода.
33. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой VI
34. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой VII
35. Способ по п.30, в котором соединение SARM представлено структурной формулой VIII
36. Способ по п.30, в котором соединение SARM представлено структурной формулой IX
37. Способ по п.30, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5a-редуктазы.
38. Способ по п.30, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5a-редуктазы.
39. Способ по п.30, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 1.
40. Способ по п.30, в котором фермент 5a-редуктаза представляет собой фермент 5a-редуктазу типа 2.
41. Способ по п.30, в котором фермент 5a-редуктаза представляет собой фермент тестостерон-5a-редуктазу.
Текст
013399 Область техники, к которой относится изобретение Это изобретение относится к предупреждению и/или лечению доброкачественной гиперплазии простаты (ДГП). Более конкретно, это изобретение относится к способу лечения, предупреждения, подавления, ингибирования или ослабления доброкачественной гиперплазии простаты у пациентов-мужчин,страдающих от доброкачественной гиперплазии простаты, который заключается во введении указанному пациенту селективного модулятора рецептора андрогенов (SARM) и/или его аналога, производного, изомера, метаболита, фармацевтически приемлемой соли, фармацевтического продукта, гидрата, N-оксида или их смесей. Уровень техники Доброкачественная гиперплазия простаты (ДГП) представляет собой незлокачественное увеличение предстательной железы. ДГП является наиболее частым незлокачественным пролиферативным,встречающимся среди внутренних органов, и главной причиной заболеваемости взрослых мужчин. Первоначальное развитие ДГП начинается уже в возрасте от 30 до 40 лет, причем распространенность заболевания в этой возрастной группе составляет приблизительно 10%. С увеличением возраста распространенность ДГП постепенно возрастает. Для мужчин в возрасте свыше 50 лет она составляет более 75%,причем на девятом десятке лет распространенность ДГП достигает 88%. Предполагается, что общее старение населения США, а также увеличение продолжительности жизни способствуют продолжающемуся росту числа пациентов с ДГП. Зачастую ДГП приводит к постепенному сжатию части мочеиспускательного канала, который проходит через простату (простатическая уретра). Это приводит к ситуации, когда пациент испытывает побуждение к частому мочеиспусканию, из-за неполного опорожнения мочевого пузыря, и ощущение жжения или аналогичного дискомфорта при мочеиспускании. Препятствие току мочи также может привести к общей потере контроля мочеиспускания, в том числе к затруднению начала мочеиспускания при его побуждении, а также к затруднению удержания мочи из-за закупорки выхода из мочевого пузыря и неконтролируемому удерживанию мочи из-за остаточной мочи - состоянию, известному как избыточное недержание мочи. Известны две составляющие ДГП. Первая составляющая обусловлена увеличением предстательной железы, что может привести к сжатию уретры и препятствию току мочи из мочевого пузыря. Вторая составляющая обусловлена повышенным тонусом гладких мышц шейки мочевого пузыря и самой простаты, что мешает опорожнению мочевого пузыря, и регулируется l-адрэнергическими рецепторами (lAR). Андрогены тестостерон и дигидротестостерон (DHT) представляют собой факторы, дающие вклад в развитие ДГП в простате. Под действием 5-альфа-редуктазы (5-редуктазы) тестостерон превращается в дигидротестостерон, который приблизительно в 5 раз более активен, чем тестостерон, в связи с большей связывающей способностью с рецептором андрогенов. Дигидротестостерон связывается с цитоплазменными рецепторами в простате, где DHT инициирует синтез РНК и ДНК. В свою очередь, это индуцирует синтез белка и аномальный рост простаты. У млекопитающих, в частности у людей, существуют две изоформы 5-редуктазы. Первый тип изофермента сильно экспрессируется в печени и коже, обладает пониженным сродством к тестостерону и его поведение больше напоминает катаболический реагент. Напротив, второй тип изофермента экспрессируется, главным образом, в тканях-мишенях андрогенов,обладает повышенным сродством к тестостерону и усиливает андрогенное действие тестостерона, превращая его в DHT. Андрогенная недостаточность может ослабить обструктивные симптомы ДГП. Более того, текущие клинические данные указывают на то, что при ингибировании 5-редуктазы проходят симптомы ДГП у мужчин (Strauch G. Eur. Urol., v. 26, p. 247-252 (1994); Rhodes L. Prostate, v. 22, p.43-51 (1993. Кроме того, оказалось, что активность 5-редуктазы выше в клетках, полученных из ткани ДГП, чем в клетках,полученных из нормальной ткани простаты (Bone К. Eur. J. of Herbal Medicine, v. 4 (1), p. 15-24 (1998). Знание механизма регулирования роста простаты 5-редуктазой привело к разработке лекарственных препаратов, таких как селективный ингибитор 5-редуктазы типа 2-финастерид, для использования при регулировании симптомов ДГП и предупреждения задержки мочеиспускания. Финастерид (PROSCAR) блокирует превращение тестостерона в DHT, причем установлено, что он уменьшает размер простаты, что приводит к увеличению максимальной скорости мочетока и ослаблению симптомов (StrauchG. 1994; Rhodes L. 1993; Russel (1994), Annu. Rev. Biochem. v. 63, p. 25-61). Обычно имеется несколько вариантов лечения пациентов с диагнозом ДГП, в том числе выжидательное наблюдение, хирургическое вмешательство, простатэктомия с использованием лазера, теплотерапия и лекарственная терапия. Выжидательное наблюдение часто выбирают для пациентов, у которых нет симптомов ДГП (или они минимально проявляются); оно включает регулярное обследование и мониторинг, для того чтобы определить, остается ли состояние пациента терпимым. В настоящее время хирургическое вмешательство является принятым методом лечения ДГП, и обычно оно применяется для пациентов с непереносимыми симптомами или с ожидаемыми сильными симптомами при остановке лечения. В настоящее время только незначительная часть пациентов, страдающих от ДГП, подвергается-1 013399 хирургическому лечению. Хирургическая терапия включает в том числе трансуретральную резекцию простаты (TURP), трансуретральный разрез простаты (TUIP) и открытую хирургию. Хирургические методы, хотя и эффективны для ослабления симптомов ДГП, приводят к существенному повреждению,которому подвергается простатическая уретра. Хотя простатэктомия с помощью лазера и тепловая абляционная терапия являются менее инвазивными, и в этом случае имеет место существенное повреждение простатической уретры. Кроме того, затраты на хирургическое лечение ДГП оцениваются в сумме более 1 миллиарда долларов в год, при этом прогнозируется рост этих затрат по мере старения мужского населения. Применяемые для лечения ДГП лекарственные препараты предназначаются для лечения увеличения простаты, что характерно при ДГП, путем уменьшения простаты или путем ингибирования или замедления роста клеток простаты. Финастерид (PROSCAR, RTM., Merck) представляет собой один вид такой терапии, которая показана для лечения симптоматической ДГП. Финастерид является конкурентным ингибитором фермента 5-редуктазы типа 2, который ответственен за превращение тестостерона в дигидротестостерон в предстательной железе. Другие лекарственные препараты предназначены для расслабления мышц в простате и шейке мочевого пузыря, для того чтобы ослабить непроходимость уретры. Теразозин (Hytrin, Abbott) представляет собой блокирующий агент адрэнергического рецептора (блокатор l-AR), который действует путем ослабления тонуса гладких мышц внутри предстательной железы,уретры и мочевого пузыря. Если доброкачественная гиперплазия простаты не прекращается, то она может иметь тяжелые последствия для здоровья. ДГП может привести к острой задержке мочеиспускания (полная неспособность мочеиспускания), инфекционным заболеваниям мочевых путей, серьезно угрожающим жизни, и уросепсису, и постоянному поражению мочевого пузыря и почек. Для лечения ДГП срочно требуются инновационные подходы как на уровне фундаментальной науки, так и на клиническом уровне. Разработка новых неинвазивных терапевтических подходов может привести к существенному увеличению числа ДГП пациентов, выбирающих лечение. Настоящее изобретение посвящено удовлетворению этой потребности. Раскрытие изобретения В одном варианте осуществления изобретение относится к способу лечения пациентов-мужчин,страдающих от доброкачественной гиперплазии простаты, который включает стадию введения этому пациенту селективного модулятора рецептора андрогенов (SARM) и/или его аналога, производного, изомера, метаболита, фармацевтически приемлемой соли, фармацевтического продукта, гидрата, N-оксида или их любого сочетания. В другом варианте осуществления изобретение относится к способу предупреждения, подавления,ингибирования или уменьшения заболеваемости доброкачественной гиперплазией простаты у пациентов-мужчин, который включает стадию введения этому пациенту селективного модулятора рецептора андрогенов (SARM) и/или его аналога, производного, изомера, метаболита, фармацевтически приемлемой соли, фармацевтического продукта, гидрата, N-оксида или их любого сочетания. Кроме того, это изобретение относится к способу ингибирования фермента 5-редуктазы, который включает контактирование фермента с эффективным, ингибирующим 5-редуктазу количеством селективного модулятора рецептора андрогенов (SARM) и/или его аналога, производного, изомера, метаболита, фармацевтически приемлемой соли, фармацевтического продукта, гидрата, N-оксида или их любого сочетания. В одном варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет доброкачественную гиперплазию простаты; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой IR1 представляет собой CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой II.R представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН,где алкил содержит 1-12 атомов углерода. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой VI В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой VII В одном варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой VIIIB одном варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой IX В другом варианте осуществления SARM представляет собой агонист рецептора андрогенов. В другом варианте осуществления SARM представляет собой антагонист рецептора андрогенов. В другом варианте осуществления SARM представляет собой ингибитор фермента 5-редуктазы. В другом варианте осуществления SARM представляет собой конкурентный ингибитор фермента 5-редуктазы. В одном варианте осуществления фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 1. В другом варианте осуществления фермент 5-редуктаза представляет собой фермент 5 редуктазу типа 2. В другом варианте осуществления фермент 5-редуктаза представляет собой фермент-3 013399 тестостерон 5-редуктазу, т.е., фермент, который превращает тестостерон (Т) в дигидротестостерон(DHT). В одном варианте осуществления изобретение обеспечивает способ блокирования способности дигидротестостерона индуцировать гиперплазию, который заключается в том, что рецептор андрогенов приводят в контакт с любым одним или несколькими соединениями I, II, VI-IX, или с композицией, содержащей любое одно или несколько соединений I, II, VI-IX, тем самым блокируя способность дигидротестостерона вызывать гиперплазию. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX является частичным агонистом и селективным агонистом, который при контакте с рецептором андрогенов или при введении субъекту предотвращает митогенное действие тестостерона и дигидротестостерона путем блокирования способности эндогенных лигандов связываться с рецептором. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает рекрутирование коактиваторов и корегуляторов андроген-респонсивной ДНК и предотвращает рост клеток, зависящих от рецептора андрогенов (таких как железистый эпителий в простате). В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает рекрутирование корепрессоров андроген-респонсивной ДНК и предотвращает рост клеток, зависящих от рецептора андрогенов(таких как железистый эпителий в простате). В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает митогенное действие тестостерона и дигидротестостерона путем блокирования способности эндогенных лигандов связываться с рецептором и индуцировать транскрипцию других гормонов и факторов роста, сигнал которых паракринным образом вызывает пролиферацию эпителиальных клеток простаты. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает митогенное действие тестостерона и дигидротестостерона путем блокирования способности эндогенных лигандов связываться с рецептором и индуцировать последующую передачу молекулярного сигнала, который вызывает программированную гибель клеток железистого эпителия. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. Настоящее изобретение предоставляет безопасный и эффективный способ лечения, предупреждения, подавления, ингибирования или уменьшения заболеваемости доброкачественной гиперплазией простаты и, в частности, применяется при лечении пациентов-мужчин, страдающих от симптомов и признаков ДГП. Краткое описание чертежей Фиг. 1. Влияние соединения VI, SARM, на метаболизм тестостерона под действием 5-редуктазы типа 1 и типа 2 (n=3). Данные нормализованы по величинам УФ-поглощения, полученным при анализе-галактозидазы. Фиг. 2. Влияние соединения VI, SARM, на размер простаты, семенных пузырьков и поднимающей мышцы ануса (levator ani muscle) крыс с различным гормональным статусом. Фиг. 3. Фармакологическое действие гидроксифлутамида, соединения VII и финастерида на вес вентральной простаты здоровых самцов крысы после различных периодов обработки (n=5). Фиг. 4. Фармакологическое действие гидроксифлутамида, соединения VII и финастерида на вес семенных пузырьков здоровых самцов крысы после различных периодов обработки (n=5). Фиг. 5. Фармакологическое действие гидроксифлутамида, соединения VII и финастерида на вес поднимающей мышцы ануса здоровых самцов крысы после различных периодов обработки (n=5). Фиг. 6. Соединение VII уменьшает простату у здоровых крыс линии Sprague-Dawley. Осуществление изобретения В одном варианте осуществления настоящее изобретение обеспечивает способ предупреждения,подавления, ингибирования или уменьшения заболеваемости доброкачественной гиперплазией простаты у пациентов-мужчин путем введения этому пациенту селективного модулятора рецептора андрогенов(SARM). В другом варианте осуществления способ включает введение изомера SARM. В другом варианте осуществления способ включает введение фармацевтически приемлемой соли SARM. В другом варианте осуществления способ включает введение гидрата SARM. В другом варианте осуществления способ включает введение N-оксида SARM. Это изобретение обеспечивает в одном варианте осуществления способ блокирования способностиDHT индуцировать гиперплазию, который заключается в том, что рецептор андрогенов приводят в контакт с любым одним или несколькими соединениями I, II, VI-IX, или с композицией, содержащей любое-4 013399 одно или несколько соединений I, II, VI-IX, тем самым блокируя способность DHT вызывать гиперплазию. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX является частичным агонистом и селективным агонистом, который при контакте с рецептором андрогенов или при введении субъекту предотвращает митогенное действие тестостерона и DHT путем блокирования способности эндогенных лигандов связываться с рецептором. В одном варианте осуществления это соединение является соединениемVII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает рекрутирование коактиваторов и корегуляторов андроген-респонсивной ДНК и предотвращает рост клеток, зависящих от рецептора андрогенов (таких как железистый эпителий в простате). В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает рекрутирование корепрессоров андроген-респонсивной ДНК и предотвращает рост клеток, зависящих от рецептора андрогенов(таких как железистый эпителий в простате). В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает митогенное действие тестостерона и DHT путем блокирования способности эндогенных лигандов связываться с рецептором и индуцировать транскрипцию других гормонов и факторов роста, сигнал которых паракринным образом вызывает пролиферацию эпителиальных клеток простаты. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX предотвращает митогенное действие тестостерона и DHT путем блокирования способности эндогенных лигандов связываться с рецептором и индуцировать последующую передачу молекулярного сигнала, который вызывает программированную гибель клеток железистого эпителия. В одном варианте осуществления это соединение является соединением VII. В другом варианте осуществления это соединение является соединением VI. В одном варианте осуществления соединение I, II, VI-IX является селективным агонистом в мышцах и частичным агонистом в простате. Действие андрогена опосредуется через рецептор андрогенов(AR). AR представляет собой зависящий от лиганда транскрипционный фактор, который регулирует экспрессию андроген-респонсивных генов путем связывания с андроген-респонсивными элементами в ДНК. Андроген-респонсивные гены ответственны за андроген-зависимую пролиферацию, а также за андрогензависимую гибель клеток. Кроме того, другие гены в каскадах передачи клеточных сигналов вносят вклад в клеточную пролиферацию или подавление путем передачи сигнала через рецептор андрогенов и последовательно с рецептором андрогенов (повышающе регулируемым через взаимодействие с ARзависимой ДНК), однако являются митогенными через альтернативный рецептор, вовлеченный в клеточную пролиферацию (например, IGF-I). Простата представляет собой чувствительную к андрогену ткань; таким образом, тестостерон и дигидротестостерон поддерживают нормальную структурную и функциональную целостность простаты (через рецептор андрогенов). Однако Т и DHT также являются сильными митогенами в простате и могут приводить к аномальному росту андроген-зависимых клеток (таких как железистые эпителиальные клетки предстательной железы), причем окончательным результатом будет заболевание простаты, такое как ДГП и рак. Лишение андрогенной поддержки путем кастрации или ингибирования эндогенных лигандов для рецептора андрогенов (например, частичные агонисты, такие как соединение I, II, VI-IX) предупреждает метаболические изменения, зависящие от тестостерона и DHT. Кроме того, в другом варианте осуществления это изобретение обеспечивает способ ингибирования фермента 5-редуктазы типа 1 и/или типа 2, который включает контактирование фермента с эффективным ингибирующим 5-редуктазу количеством селективного модулятора рецептора андрогенов (SARM). В другом варианте осуществления способ включает введение изомера SARM. В другом варианте осуществления способ включает введение фармацевтически приемлемой соли SARM. В другом варианте осуществления способ включает введение гидрата SARM. В другом варианте осуществления способ включает введение N-оксида SARM. Селективные модуляторы рецептора андрогенов (SARM) представляют собой класс агентов, направленных на рецептор андрогенов (ARTA), которые демонстрируют андрогенную и анаболическую активность нестероидных лигандов для рецептора андрогенов. Эти новые агенты применяются для лечения различных связанных с гормонами состояний у мужчин и женщин, таких как гипогонадизм, саркопения, эритропоэз, дисфункция эрекции, отсутствие полового влечения, остеопороз и бесплодие. Кроме того, SARM применяется при оральной тестостерон-заменительной терапии, лечении рака предстательной железы, визуализации рака предстательной железы и для сохранения полового влечения у женщин. В одном варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет доброкачественную гиперплазию простаты; и/или b) лечит выпадение волос; и/или с) ингибирует-5 013399 фермент 5-редуктазу; и/или d) является антагонистом рецептора андрогенов, является соединением,представленным структурной формулой IR1 представляет собой CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода. В одном варианте осуществления SARM представляет собой изомер соединения формулы I. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы I. В другом варианте осуществления SARM представляет собой гидрат соединения формулы I. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы I. В другом варианте осуществления SARM представляет собой сочетание любого из изомера, фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы I. В одном варианте осуществления SARM представляет собой соединение формулы I, в которой X означает атом кислорода. В одном варианте осуществления SARM представляет собой соединение формулы I, в которой G означает атом кислорода. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой Z означает NO2. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой Z означает CN. В другом варианте осуществленияSARM представляет собой соединение формулы I, в которой Y представляет собой CF3. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой Q представляет собойNHCOCH3. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой Q представляет собой атом фтора. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой Т означает группу ОН. В другом варианте осуществления SARM представляет собой соединение формулы I, в которой R1 означает метил. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой IIR представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН, где алкил содержит 1-12 атомов углерода. В одном варианте осуществления SARM представляет собой изомер соединения формулы II. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы II. В другом варианте осуществления SARM представляет собой гидрат соединения формулыII. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы II. В другом варианте осуществления SARM представляет собой сочетание любого из изомера, фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы II. В одном варианте осуществления SARM представляет собой соединение формулы II, в которой X означает атом кислорода. В другом варианте осуществления SARM представляет собой соединение формулы II, в которой Z означает NO2. В другом варианте осуществления SARM представляет собой соединение формулы II, в которой Z означает CN. В другом варианте осуществления SARM представляет со-6 013399 бой соединение формулы II, в которой Y представляет собой CF3. В другом варианте осуществленияSARM представляет собой соединение формулы II, в которой Q представляет собой NHCOCH3. В другом варианте осуществления SARM представляет собой соединение формулы II, в которой Q представляет собой атом фтора. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой VI. В одном варианте осуществления SARM представляет собой изомер соединения формулы VI. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы VI. В другом варианте осуществления SARM представляет собой гидрат соединения формулы VI. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы VI. В другом варианте осуществления SARM представляет собой сочетание любого из изомера, фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы VI. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой В одном варианте осуществления SARM представляет собой изомер соединения формулы VII. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы VII. В другом варианте осуществления SARM представляет собой гидрат соединения формулы VII. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы VII. В другом варианте осуществления SARM представляет собой сочетание любого из изомера, фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы VII. В другом варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой В одном варианте осуществления SARM представляет собой изомер соединения формулы VIII. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы VIII. В другом варианте осуществления SARM представляет собой гидрат соединения формулы VIII. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы VIII. В другом варианте осуществления SARM представляет собой сочетание любого из изомера,фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы VIII. В одном варианте осуществления SARM, который: а) лечит, предупреждает, ингибирует или подавляет ДГП; и/или b) лечит выпадение волос; и/или с) ингибирует фермент 5-редуктазу; и/или d) противодействует рецептору андрогенов, является соединением, представленным структурной формулой IX. В одном варианте осуществления SARM представляет собой изомер соединения формулы IX. В другом варианте осуществления SARM представляет собой фармацевтически приемлемую соль соединения формулы IX. В другом варианте осуществления SARM представляет собой гидрат соединения-7 013399 формулы IX. В другом варианте осуществления SARM представляет собой N-оксид соединения формулы IX. В другом варианте осуществления SARM представляет собой сочетание любого из изомера, фармацевтически приемлемой соли, гидрата или N-оксида соединения формулы IX. В соединениях изобретения формул I и II заместитель R определен как алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3, CF2CF3, фенил, атом галогена, алкенил или ОН. Термин алкильная группа относится к насыщенному алифатическому углеводороду, в том числе алкильным группам с прямой цепочкой, разветвленной цепочкой и циклическим алкильным группам. В одном варианте осуществления алкильная группа имеет 1-12 атомов углерода. В другом варианте осуществления алкильная группа имеет 1-7 атомов углерода. В другом варианте осуществления алкильная группа имеет 1-6 атомов углерода. В другом варианте осуществления алкильная группа имеет 1-4 атома углерода. Алкильная группа может быть незамещенной или замещенной одной или несколькими группами, выбранными из атома галогена, гидрокси, алкокси, карбонила, амидо, алкиламидо, диалкиламидо,нитро, амино, алкиламино, диалкиламино, карбоксила, тио и тиоалкила. Термин алкенильная группа относится к ненасыщенному алифатическому углеводороду, включая группы с прямой цепочкой, разветвленной цепочкой, и циклические группы, имеющие одну или несколько двойных связей. Алкенильная группа может иметь одну двойную связь, две двойные связи, три двойные связи и т.д. Примеры алкенильных групп представляют собой этенил, пропенил, бутенил, циклогексенил и т.д. Алкенильная группа может быть незамещенной или замещенной одной или несколькими группами, выбранными из атома галогена, гидрокси, алкокси, карбонила, амидо, алкиламидо, диалкиламидо, нитро, амино, алкиламино, диалкиламино, карбоксила, тио и тиоалкила. Термин галоидалкильная группа относится к алкильной группе, которая определена выше и замещена одним или несколькими атомами галогена, например F, Cl, Br или I. Термин арильная группа относится к ароматической группе, имеющей по меньшей мере одну карбоциклическую ароматическую группу или гетероциклическую ароматическую группу, которая может быть незамещенной или замещенной одной или несколькими группами, выбранными из атома галогена, галоидалкила, гидрокси, алкокси, карбонила, амидо, алкиламидо, диалкиламидо, нитро, амино, алкиламино, диалкиламино, карбоксила, или тио, или тиоалкила. Неограничивающими примерами арильных циклов являются фенил, нафтил, пиранил, пирролил, пиразинил, пиримидинил, пиразолил, пиридинил, фуранил, тиофенил, тиазолил, имидазолил, изоксазолил и т.п. Термин гидроксильная группа относится к группе ОН. Термин алкенильная группа относится к группе, имеющей по меньшей мере одну углерод-углеродную двойную связь. Галоидная группа относится к F, Cl, Br или I. Термин арилалкильная группа относится к алкилу, связанному с арилом, в которой алкил и арил такие, как определено выше. Примером арилалкильной группы является бензильная группа. Как предполагается, это изобретение обеспечивает способ лечения, предупреждения, подавления,ингибирования или снижение заболеваемости доброкачественной гиперплазией простаты у пациентовмужчин путем введения этому пациенту селективного модулятора рецептора андрогенов (SARM). В другом варианте осуществления способ включает введение изомера указанного SARM. В другом варианте осуществления способ включает введение фармацевтически приемлемой соли указанного SARM. В другом варианте осуществления способ включает введение гидрата указанного SARM. В другом варианте осуществления способ включает введение N-оксида указанного SARM. Указанный в изобретении термин изомер включает, но не ограничивается оптическими изомерами и их аналогами, структурными изомерами и их аналогами, конформационными изомерами и их аналогами и т.п. В одном варианте осуществления это изобретение охватывает применение различных оптических изомеров соединения SARM. Специалисты в этой области техники могут оценить, что соединенияSARM настоящего изобретения содержат по меньшей мере один хиральный центр. Соответственно,применяемые в способе настоящего изобретения SARM могут существовать и могут быть выделены в оптически активной или рацемической формах. Для некоторых соединений также может проявляться полиморфизм. Следует понимать, что настоящее изобретение охватывает любые рацемические, оптически активные, полиморфные или стереоизомерные формы или любые их сочетания, которые обладают свойствами, которые эффективны при лечении ДГП, описанной в этом изобретении. В одном варианте осуществления SARM представляют собой чистые (R)-изомеры. В другом варианте осуществленияSARM представляют собой чистые (S)-изомеры. В другом варианте осуществления SARM представляют собой смесь (R)- и (S)-изомеров. В другом варианте осуществления SARM представляют собой рацемическую смесь, содержащую равные количества (R)- и (S)-изомеров. Из уровня техники хорошо известны методы получения оптически активных форм (например, путем разделения рацемических форм способом перекристаллизации, путем синтеза из оптически активных исходных материалов, путем хирального синтеза или путем хроматографического разделения с использованием хиральной стационарной фазы). Это изобретение включает фармацевтически приемлемые соли аминозамещенных соединений с органическими или неорганическими кислотами, например лимонной кислотой и хлористо-водородной кислотой. Кроме того, изобретение включает N-оксиды описанных здесь аминозамещенных соединений.-8 013399 Фармацевтически приемлемые соли также могут быть получены из фенольных соединений путем их обработки неорганическими основаниями, например гидроксидом натрия. Кроме того, могут быть получены сложные эфиры фенольных соединений путем взаимодействия с алифатическими и ароматическими карбоновыми кислотами, например сложные эфиры уксусной кислоты и бензойной кислоты. Кроме того, это изобретение дополнительно включает гидраты соединений SARM. Термин гидраты включает, но не ограничивается, полугидрат, моногидрат, дигидрат, тригидрат и т.п. Биологическая активность соединений - селективных андрогенных модуляторов Как предполагается в изобретении, соединения SARM, которые используются для предупреждения и лечения ДГП, классифицируются как агонисты рецептора андрогенов (агонисты AR) или антагонисты рецептора андрогенов (антагонисты AR). Рецептор андрогенов представляет собой активируемый лигандами регулирующий транскрипцию белок, который опосредует индукцию полового развития мужчины и функционирует через взаимодействие с эндогенными андрогенами (мужские половые гормоны). Андрогенные гормоны представляют собой стероиды, которые продуцируются в организме в яичках и в кортикальном слое надпочечной железы. Андрогенные стероиды играют важную роль во многих физиологических процессах, в том числе развитии и поддержании таких половых признаков мужчин, как мышечная и костная масса, рост предстательной железы, сперматогенез, и характер волосяного покрова мужчины (Matsumoto, Endocrinol. MetClin. N. Am. 23:857-75 (1994). Эндогенные стероидные андрогены включают тестостерон и дигидротестостерон ("DHT"). Другие стероидные андрогены включают сложные эфиры тестостерона, такие как ципионат, пропионат, фенилпропионат, циклопентилпропионат, изокапроат, эфир энантовой кислоты, и эфиры декановой кислоты, и другие синтетические андрогены, такие как 7-метил-нортестостерон("MENT1") и его сложный эфир с уксусной кислотой (Sundaram и др., "7 Alpha-Methyl-Nortestosterone(MENT): The Optimal Androgen For Male Contraception," Ann. Med., 25:199-205 (1993) ("Sundaram"). Агонист рецептора представляет собой вещество, которое связывает и активирует рецептор. Антагонист рецептора представляет собой вещество, которое связывает и инактивирует рецептор. В одном варианте осуществления соединения SARM, которые применяются при лечении и предупреждении ДГП,представляют собой агонисты AR, и поэтому применяются для связывания с и активации AR. В другом варианте осуществления соединения SARM, которые применяются при лечении и предупреждении ДГП,представляют собой антагонисты рецептора и поэтому применяются для связывания с и инактивацииAR. Анализы с целью определения, являются ли соединения настоящего изобретения агонистами или антагонистами AR, хорошо известны специалистам в этой области техники. Например, активность агониста AR может быть определена путем регистрации способности соединений SARM поддерживать и/или стимулировать рост ткани, содержащей AR, такой как простата и семенные пузырьки, что измеряется по весу. Активность антагониста AR может быть определена путем регистрации способности соединений SARM ингибировать рост ткани, содержащей AR. В еще одном варианте осуществления соединения SARM настоящего изобретения могут быть классифицированы как частичные агонисты/антагонисты рецептора андрогенов. В некоторых тканях SARM представляют собой агонисты рецептора андрогенов, которые вызывают повышенную транскрипциюSARM играют роль конкурентных ингибиторов тестостерона/дигидротестостерона в отношении AR,предупреждая агонистическое действие природных андрогенов. Соединения настоящего изобретения связываются или обратимо, или необратимо с рецептором андрогенов. В одном варианте осуществления соединения SARM связываются обратимо с рецептором андрогенов. В другом варианте осуществления соединения SARM связываются необратимо с рецептором андрогенов. Соединения настоящего изобретения могут содержать функциональную группу (аффинная метка), что позволяет алкилировать рецептор андрогенов (то есть образование ковалентной связи). Таким образом, в этом случае соединения связываются необратимо с рецептором и соответственно не могут быть вытеснены стероидом, таким как эндогенные лиганды дигидротестостерон и тестостерон. Как продемонстрировано в описании, соединения SARM настоящего изобретения являются сильными ингибиторами фермента 5-редуктазы. Таким образом, в одном варианте осуществления это изобретение предоставляет способ ингибирования фермента 5-редуктазы, который включает контактирование фермента с эффективным ингибирующим 5-редуктазу количеством селективного модулятора рецептора андрогенов (SARM), и/или его изомера, фармацевтически приемлемой соли, гидрата, Nоксида или любого их сочетания, как описано в изобретении. В одном варианте осуществления соединение SARM, которое, как показано, является сильным ингибитором фермента 5-редуктазы, представляет собой соединение формулы I. В другом варианте осуществления соединение SARM, которое, как показано, является сильным ингибитором фермента 5-редуктазы, представляет собой соединение формулы II. В другом варианте осуществления соединение SARM, которое, как показано, является сильным ингибитором фермента 5-редуктазы, представляет собой соединение формулы VI. В другом варианте осуществления соединение SARM, которое, как показано, является сильным ингибитором фермента 5 редуктазы, представляет собой соединение формулы VII. В другом варианте осуществления соединениеSARM, которое, как показано, является сильным ингибитором фермента 5-редуктазы, представляет собой соединение формулы VIII. В другом варианте осуществления соединение SARM, которое, как показано, является сильным ингибитором фермента 5-редуктазы, представляет собой соединение формулы IX. В одном варианте осуществления настоящего изобретения фермент 5-редуктаза представляет собой фермент тестостерон 5-редуктазу. Фермент тестостерон-5-редуктаза представляет собой фермент,который превращает тестостерон (Т) в дигидротестостерон (DHT). Полагают, что DHT, который связывается с рецептором андрогенов человека с в 5 раз большим сродством, является медиатором андрогенного действия во многих тканях. Дигидротестостерон вызывает пролиферацию ткани предстательной железы, которая, в свою очередь, сопровождается увеличением простаты. Путем ингибирования тестостерон-5-редуктазы соединением SARM настоящего изобретения можно сократить образование DHT, и можно ожидать, что увеличение предстательной железы будет блокировано. Существуют две изоформы 5-редуктазы - изозим типа 1 преимущественно экспрессируется в печени и коже, и изозим типа 1 преимущественно экспрессируется в предстательной железе. Как продемонстрировано в описании соединения SARM настоящего изобретения эффективны при ингибировании 5-редуктазы как типа 1, так и типа 2. Таким образом, в одном варианте осуществления соединениеSARM, которое, как продемонстрировано, является сильным ингибитором фермента 5-редуктазы, представляет собой сильный ингибитор фермента 5-редуктазы типа 1. В другом варианте осуществления соединение SARM, которое, как продемонстрировано, является сильным ингибитором фермента 5 редуктазы, представляет собой сильный ингибитор фермента 5-редуктазы типа 2. В другом варианте осуществления, как показано в описании, соединение SARM, которое, как продемонстрировано, является сильным ингибитором фермента 5-редуктазы, представляет собой конкурентный ингибитор фермента 5-редуктазы. Определение термина контактирование в описании означает, что соединение SARM настоящего изобретения вводят в образец, содержащий фермент, в пробирке, колбе, культуре ткани, на чипе, матрице, на планшете, микропланшете, в капилляре или т.п., и инкубируют при температуре и времени, которые достаточны, чтобы обеспечить связывание SARM с ферментом. Способы контактирования проб сSARM или другими специфическими связывающими компонентами известны специалистам в этой области техники и могут быть выбраны в зависимости от типа протокола анализа, который будет проводиться. Способы инкубации также являются общепринятыми и известны специалистам в этой области техники. В другом варианте осуществления термин контактирование означает, что соединение SARM настоящего изобретения вводят субъекту, подвергающемуся лечению, и обеспечивают контакт соединенияSARM с рецептором андрогенов in vivo. Используемый здесь термин лечение включает лечение, направленное на ослабление нарушений. Это изобретение обеспечивает применение композиции и фармацевтической композиции для лечения, предупреждения, подавления, ингибирования или снижения заболеваемости доброкачественной гиперплазией простаты у пациентов-мужчин, причем композиция содержит селективный модулятор рецептора андрогенов (SARM) и/или его изомер, фармацевтически приемлемую соль, гидрат, N-оксид или их любое сочетание, как описано в изобретении, в фармацевтическом препарате, который дополнительно содержит подходящий носитель или разбавитель. Настоящее изобретение предоставляет безопасный и эффективный способ лечения, предупреждения, подавления, ингибирования или ослабления доброкачественной гиперплазии простаты (ДГП) и, в частности, применяется при лечении симптомов и признаков, связанных с ДГП, у субъектов, страдающих от ДГП. В одном варианте осуществления субъект представляет собой млекопитающее. В другом варианте субъект представляет собой человека. В другом варианте осуществления этот субъект представляет собой мужчину. Фармацевтические композиции Используемый здесь термин фармацевтическая композиция означает терапевтически эффективное количество активного компонента, то есть соединения SARM вместе с фармацевтически приемлемым носителем или разбавителем. Используемый здесь термин терапевтически эффективное количество относится к такому количеству, которое обеспечивает терапевтический эффект при данном состоянии и режиме введения. Фармацевтические композиции, содержащие соединение SARM, могут быть введены субъекту любым способом, известным специалистам в этой области техники, таким как парентеральным, около опухоли, через слизистую, через кожу, внутримышечно, внутривенно, внутрикожно, подкожно, внутрибрюшинно, интравентрикулярно, внутричерепно, интравагинально или внутрь опухоли. В одном варианте осуществления фармацевтические композиции вводят перорально и, таким образом, составляют в форме, подходящей для орального введения, то есть как твердый или жидкий препарат. Подходящие твердые оральные рецептуры включают таблетки, капсулы, пилюли, гранулы, подушечки и т.п. Подходящие жидкие оральные рецептуры включают растворы, суспензии, дисперсии,- 10013399 эмульсии, масла и т.п. В одном варианте осуществления настоящего изобретения соединения SARM составляются в виде капсулы. В соответствии с этим вариантом осуществления композиции настоящего изобретения, кроме активного соединения SARM и инертного носителя или разбавителя, содержат желатиновую капсулу. Кроме того, в другом варианте осуществления фармацевтические композиции вводятся путем внутривенной, внутриартериальной или внутримышечной инъекции жидкого препарата. Подходящие жидкие рецептуры включают растворы, суспензии, дисперсии, эмульсии, масла и т.п. В одном варианте осуществления фармацевтические композиции вводятся внутривенно, и, таким образом, составляются в форме,подходящей для внутривенного введения. В другом варианте осуществления фармацевтические композиции вводятся внутриартериально, и, таким образом, составляются в форме, подходящей для внутриартериального введения. В другом варианте осуществления фармацевтические композиции вводятся внутримышечно, и таким образом, составляются в форме, подходящей для внутримышечного введения. Кроме того, в другом варианте осуществления фармацевтические композиции вводят местно на поверхность тела и, таким образом, составляют в форме, подходящей для местного введения. Рецептуры,подходящие для местного введения, включают гели, мази, кремы, лосьоны, капли и т.п. Для местного введения соединения SARM или их физиологически допустимые производные, такие как соли, сложные эфиры, N-оксиды и т.п., готовят и наносят в виде растворов, суспензий или эмульсий в физиологически приемлемом разбавителе с фармацевтическим носителем или без него. Кроме того, в другом варианте осуществления фармацевтические композиции вводят в виде суппозитория, например ректальной свечи или уретрального суппозитория. Кроме того, в другом варианте осуществления фармацевтические композиции вводят путем подкожной имплантации гранулы. В дополнительном варианте осуществления эта гранула обеспечивает контролируемое высвобождение соединения SARM в течение некоторого времени. В другом варианте осуществления активное соединение может быть доставлено в виде везикулы, в частности липосомы (см. статью Langer, Science, т. 249, с. 1527-1533 (1990); Treat и др., в книге Liposomes in the Therapy of Infectious Disease и Cancer, Lopez-Berestein и Fidler (ред.), Liss, New York, с 353365 (1989); Lopez-Berestein, там же, с. 317-327; вообще, см. там же). Используемый в описании термин "фармацевтически приемлемые носители или разбавители" хорошо известен специалистам в этой области техники. Носитель или разбавитель может быть твердым носителем или разбавителем для твердых рецептур, жидким носителем или разбавителем для жидких рецептур, или их смесью. Твердые носители/разбавители включают, но не ограничиваются, смолу, крахмал (например, кукурузный крахмал, предварительно желатинизированный крахмал), сахар (например, лактоза, маннит, сахароза, декстроза), материал на основе целлюлозы (например, микрокристаллическая целлюлоза), акрилат (например, полиметилакрилат), карбонат кальция, оксид магния, тальк или их смеси. Для жидких рецептур фармацевтически приемлемые носители могут представлять собой водные или неводные растворы, суспензии, эмульсии или масла. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль и органические эфиры, которые можно использовать в инъекции,такие как этилолеат. Водные растворы включают воду, водно/спиртовые растворы, эмульсии или суспензии, включая физиологический раствор и забуференные среды. Примерами масел являются масла нефтяного, животного, растительного или синтетического происхождения, например арахисовое масло, соевое масло, минеральное масло, оливковое масло, подсолнечное масло и рыбий жир. Парентеральные носители (для подкожной, внутривенной, внутриартериальной или внутримышечной инъекции) включают раствор хлористого натрия, декстрозу Рингера, декстрозу и хлористый натрий,лактатный раствор Рингера и нелетучие масла. Внутривенные носители включают восполнители жидкости и питательных веществ, восполнители электролитов, такие как добавки на основе декстрозы Рингера и т.п. Примерами являются стерильные жидкости, такие как вода и масла, с добавкой поверхностно-активных веществ и других фармацевтически приемлемых вспомогательных средств. Обычно предпочтительными жидкими носителями являются вода, физиологический раствор, водная декстроза и родственные растворы сахаров и гликолей, таких как пропиленгликоль или полиэтиленгликоль, особенно для растворов для инъекций. Примерами масел являются масла нефтяного, животного, растительного или синтетического происхождения, например арахисовое масло, соевое масло, минеральное масло, оливковое масло, подсолнечное масло и рыбий жир. Кроме того, композиции могут дополнительно содержать связующие вещества (например, акация,кукурузный крахмал, желатин, карбомер, этилцеллюлоза, гуаровая смола, гидроксипропилцеллюлоза,гидроксипропилметилцеллюлоза, повидон), диспергирующие вещества (например, кукурузный крахмал,картофельный крахмал, альгиновая кислота, диоксид кремния, кроскармелоза натрия, кросповидон, гуаровая смола, крахмал-гликолят натрия), буферные растворы (например, Трис-гидрохлорид, ацетат, фосфат) с различными значениями рН и ионной силы, добавки, такие как альбумин или желатин, для того чтобы предотвратить абсорбции на поверхности, детергенты (например, Tween 20, Tween 80, Pluronic(например, карбомер, гидроксипропилцеллюлоза, лаурилсульфат натрия), полимерные покрытия (например, полоксамеры или полоксамины), покрытия и пленкообразующие вещества (например, этилцеллюлоза, акрилаты, полиметакрилаты) и/или вспомогательные вещества. В одном варианте осуществления фармацевтические композиции этого изобретения представляют собой композиции контролируемого высвобождения, т.е. композиции, в которых соединение SARM высвобождается в течение некоторого периода после введения. Композиции контролируемого или замедленного высвобождения включают рецептуры в липофильных депо (например, жирные кислоты, воски,масла). В другом варианте осуществления композиция представляет собой композицию немедленного высвобождения, т.е. композицию, в которой все соединение SARM высвобождается сразу после введения. В еще одном варианте осуществления фармацевтическая композиция может доставляться системой с контролируемым высвобождением. Например, вещество может вводиться с использованием внутривенного вливания, вживляемого осмотического насоса, трансдермальных пластырей, липосом, или других способов введения. В одном варианте осуществления может быть использован насос (см. выше:Langer; Sefton, CRC Crit. Ref. Biomed. Eng. 14:201 (1987); Buchwald и др., Surgery 88:507 (1980); Saudek и др., N. Engl. J. Med. 321:574 (1989). В другом варианте осуществления могут быть использованы полимерные материалы. В еще одном варианте осуществления система контролируемого высвобождения может быть размещена вблизи терапевтической мишени, т.е. головного мозга так, что при этом требуется только часть системной дозы (см. выше, например, Goodson, в Medical Applications of ControlledRelase, см. выше, том 2, с. 115-138 (1984). Другие системы регулируемого выделения обсуждаются в обзоре Langer (см. Science, т. 249, с. 1527-1533 (1990). Кроме того, композиции могут содержать включения активного вещества внутри или на поверхности дисперсных препаратов полимерных соединений, таких как полимолочная кислота, полигликолевая кислота, гидрогели и др., или на липосомах, микроэмульсиях, мицеллах, однослойных или многослойных везикулах, гемолизированных эритроцитах или сферопластах. Такие композиции могут влиять на физическое состояние, растворимость, стабильность, скорость высвобождения in vivo и скорость клиренса in vivo. Кроме того, изобретение охватывает дисперсионные композиции, покрытые полимерами (например, полоксамеры или полоксамины), и соединения, конъюгированные с антителами, направленными против тканеспецифичных рецепторов, лигандов или антигенов, или конъюгированные с лигандами тканеспецифичных рецепторов. Кроме того, изобретение охватывает соединения, модифицированные ковалентным связыванием с водорастворимыми полимерами, такими как полиэтиленгликоль, сополимеры полиэтиленгликоля и полипропиленгликоля, карбоксиметилцеллюлоза, декстран, поливиниловый спирт, поливинилпирролидон или полипролин. Известно, что модифицированные соединения обладают существенно большей величиной времени полураспада в крови после внутривенной инъекции, чем соответствующие немодифицированные соединения (Abuchowski и др., 1981; Newmark и др., 1982; и Katre и др., 1987). Кроме того, такие модификации могут повысить растворимость соединения в водном растворе, исключить агрегирование,повысить физическую и химическую стабильность соединения и сильно снизить иммуногенность и реактивность соединения. В результате может быть достигнута желаемая биологическая активность in vivo путем введения таких аддуктов полимера с соединением, при меньшей частоте введения или меньших дозах, чем для немодифицированного соединения. Из уровня техники хорошо известно получение фармацевтических композиций, содержащих активное вещество, например, способом смешивания, гранулирования или формования таблеток. Терапевтически активное вещество часто смешивают с наполнителями, которые являются фармацевтически приемлемыми и совместимыми с активным веществом. Для орального введения соединения SARM или их физиологически допустимые производные, такие как соли, сложные эфиры, N-оксиды и им подобные,смешивают с обычными для этой цели добавками, такими как носители, стабилизаторы или инертные разбавители, и переводят обычными способами в формы, подходящие для введения, такие как таблетки,покрытые оболочкой таблетки, жесткие или мягкие желатиновые капсулы, водные, спиртовые или масляные растворы. Для парентерального введения соединения SARM или их физиологически допустимые производные, такие как соли, сложные эфиры, N-оксиды и им подобные, переводят в формы раствора,суспензии или эмульсии, по желанию в смеси с обычными для этой цели добавками, например солюбилизаторами или др. Активное вещество может быть составлено в композицию в виде нейтрализованных фармацевтиче- 12013399 ски приемлемых солевых форм. Фармацевтически приемлемые соли включают в себя кислотноаддитивные соли (образованные со свободными аминогруппами молекул полипептидов или антител),которые образуются с такими неорганическими кислотами, как, например, хлористо-водородная или фосфорная кислота, или такими органическими кислотами, как уксусная, щавелевая, винная, миндальная и т.п. Кроме того, соли, образовавшиеся со свободными карбоксильными группами, могут быть получены из неорганических оснований, таких как, например, гидроксиды калия, аммония, кальция или железа(III) и таких органических оснований, как изопропиламин, триметиламин, 2-этиламиноэтанол, гистидин,прокаин и т.п. Для медицинского применения соли соединений SARM будут фармацевтически приемлемыми солями. Однако другие соли могут быть использованы при получении соединений согласно изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений этого изобретения включают кислотно-аддитивные соли, которые образуются, например, при смешивании раствора соединения согласно изобретению с раствором фармацевтически приемлемой кислоты, такой как хлористоводородная кислота, серная кислота, метансульфокислота, фумаровая кислота,малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, щавелевая кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Определение термина контактирование в описании означает, что соединение SARM настоящего изобретения вводят в образец, содержащий фермент, в пробирке, колбе, культуре ткани, на чипе, матрице, на планшете, микропланшете, в капилляре или т.п., и инкубируют при температуре и времени, которые достаточны, чтобы обеспечить связывание SARM с ферментом. Способы контактирования образцов с SARM или другими специфическими связывающими компонентами известны специалистам в этой области техники и могут быть выбраны в зависимости от типа протокола анализа, который будет проводиться. Способы инкубации также являются общепринятыми и известны специалистам в этой области техники. В другом варианте осуществления термин контактирование означает, что соединение SARM настоящего изобретения вводят субъекту, подвергающемуся лечению, и обеспечивают контакт соединенияSARM с рецептором андрогенов in vivo. Используемый здесь термин лечение включает превентивное лечение, а также лечение, направленное на ослабление нарушений. Термины ослабление, подавление и ингибирование используются здесь в общеизвестном смысле уменьшения или снижения. Используемый здесь термин развитие означает возрастание по объему или серьезности заболевания, его продвижение, рост или ухудшение. Используемый здесь термин рецидив означает возвращение болезни после стадии ремиссии. Используемый здесь термин введение означает, что субъект подвергается контакту с соединением SARM настоящего изобретения. Применяемое в этом изобретении введение может быть осуществлено in vitro, то есть в пробирке, или in vivo, т.е. в клетках или тканях живого организма, например человека. В одном варианте осуществления настоящее изобретение включает в себя введение субъекту соединений настоящего изобретения. В одном варианте осуществления способ настоящего изобретения включает в себя введение соединения SARM в качестве единственного активного вещества. Однако в объем настоящего изобретения также входят способы лечения ДГП, раскрытые в описании, которые включают в себя введение соединения SARM в сочетании с одним или несколькими терапевтическими средствами. Эти средства включают(но не ограничиваются перечисленными): аналоги LHRH, обратимые антиандрогены, антиэстрогены,противораковые лекарственные препараты, ингибиторы 5-редуктазы, ингибиторы ароматазы, прогестины или средства, действующие через другие ядерные рецепторы гормонов. В одном варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с аналогом LHRH. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с обратимым антиандрогеном. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с антиэстрогеном. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с противораковым лекарственным препаратом. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с ингибитором 5-редуктазы. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с ингибитором ароматазы. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содержащие соединение - селективный модулятор рецептора андрогенов в сочетании с прогестином. В другом варианте осуществления настоящее изобретение обеспечивает композиции и фармацевтические композиции, содер- 13013399 жащие соединение - селективный модулятор рецептора андрогенов в сочетании со средством, действующим через другие ядерные рецепторы гормонов. Следующие ниже примеры представлены для того, чтобы более полно проиллюстрировать предпочтительные варианты осуществления изобретения. Однако никоим образом их не следует рассматривать с целью ограничения широкого замысла этого изобретения. Подробности эксперимента Пример 1. Взаимодействие между соединением VI и 5-редуктазой человека Тестостерон может быть восстановлен ферментом 5-редуктазой в дигидротестостерон (DHT). Полагают, что DHT, который связывается с рецептором андрогенов человека с в 5 раз более высоким сродством, является медиатором андрогенного действия во многих тканях. Поскольку соединение VI имитирует действие тестостерона во многих системах in vitro и in vivo, испытывают соединение VI для того,чтобы определить, взаимодействует ли оно с 5-редуктазой. В этом исследовании (1) определяют, является ли соединение VI субстратом для 5-редуктазы, и (2) определяют, оказывает ли соединение VI какое-либо влияние на превращение тестостерона в DHT под действием 5-редуктазы. Методы. Клетки COS1 (American Type Culture Collection, г. Manassas, шт. Виргиния) высевают в 12 луночные планшеты при плотности посева 60000 клеток на лунку и транзиторно трансфицируют клетки векторами экспрессии для 5-редуктазы человека (получены от Dr. David W. Russell, Southwestern Medical Center, Dallas, шт. Техас). При трансфекции используют реагент LipofectAMINE PLUS (фирма Invitrogen, г. Carlsbad, шт. Калифорния). Для мониторинга эффективности трансфекции клетки одновременно заражают плазмидой pCMV-SPORT-gal (фирма Invitrogen, Carlsbad, CA). Спустя 48 ч после трансфекции, в среду добавляют тестостерон (4 мкМ) и/или соединение VI (2 или 200 мкМ) и инкубируют при 37 С. Аликвоты культуральной среды удаляют через 2 ч, и реакцию останавливают путем добавления ледяного ацетонитрила (1:1, по объему). Концентрации тестостерона и соединения VI в среде инкубации определяют методом жидкостной хроматографии высокого давления (ЖХВД), используя колонку с обращенной фазой (pBondaPak С 18, 3,9300 мм, фирма Waters Corporation, г. Milford, шт. Массачусетс) и подвижную фазу - 38% ацетонитрила в деионизированной воде, при скорости потока 1,5 мл/мин. Анализируемые вещества детектируют по УФ-поглощению при длине волны 254 нм. Для расчета концентраций тестостерона или соединения VI в среде инкубации по окончании реакции строят калибровочные кривые по площади пиков. После реакции клетки подвергают лизису, и клеточный супернатант используют для определения активности -галактозидазы, и чтобы убедиться в равной эффективности трансфекции в различных лунках. Результаты Инкубация соединения VI (2 мкМ) с 5-редуктазой типа 1 или типа 2 показывает, что оно не подвергается метаболизму под действием указанного фермента (фиг. 1). Концентрация соединения VI не изменяется в течение 2-часового периода инкубации, что указывает, что соединение VI не является субстратом для указанных ферментов. При инкубации с 5-редуктазой типа 1 или типа 2 тестостерон (4 мкМ) быстро превращается в DHT, и его концентрация снижается соответственно на 34 и 35% в присутствии этих ферментов. Превращение тестостерона в DHT ингибируется в присутствии соединения VI,причем в присутствии 2 или 200 мкМ соединения VI наблюдается уменьшение концентрации тестостерона менее чем на 10%. Эти данные демонстрируют, что соединение VI является конкурентным ингибитором 5-редуктазы типа 1 и типа 2, таким образом, имеется ингибирующее действие соединения VI на вес простаты и семенных пузырьков, которое заявители наблюдали ранее на интактных животных и животных, у которых удалено одно яичко. Соединение VI не является субстратом, но действует как конкурентный ингибитор 5-редуктазы типа 1 и типа 2. Пример 2. Фармакологическая активность и тканевая селективность соединения VI для крыс с различным гормональным статусом. Селективные модуляторы рецептора андрогенов (SARM) имеют широкий спектр возможных терапевтических областей применения, в том числе гипогонадизм мужчин, остеопороз, мышечное истощение, половое влечение и предупреждение беременности. В предшествующих исследованиях заявителей продемонстрировано, что соединение VI представляет собой сильный и эффективный селективный модулятор рецептора андрогенов (SARM) у кастрированных самцов крыс. Заявители завершили доклинические исследования с целью сопоставления фармакологической активности и тканевой селективности соединения VI и пропионата тестостерона (ТР) у самцов крыс с различным гормональным статусом. В- 14013399 исследование были включены самцы крыс с нормальной тестикулярной функцией (т.е. интактные, без какого-либо хирургического вмешательства), для того чтобы оценить воздействие соединения VI на животных с нормальным уровнем тестостерона в крови. Самцы крыс, которые были подвергнуты односторонней орхиэктомии (т.е. хирургической ампутации одного яичка), были включены, для того чтобы оценить воздействие соединения VI на животных с незначительным андрогенным истощением. Самцы крыс,которые были подвергнуты двухсторонней орхиэктомии (т.е. хирургической ампутации обоих яичек),были включены, для того чтобы оценить воздействие соединения VI на животных с дефицитом андрогенов. Методы Соединение VI было синтезировано и охарактеризовано в лаборатории Dr. Duane Miller (Universityof Tennessee, г. Memphis, шт. Теннеси). Самцы крыс породы Sprague-Dawley были приобретены на фирмеHarlan Biosciences (г. Indianapolis, шт. Индиана). Для животных поддерживали 12-часовой цикл освещения и темноты, причем корм и вода были доступны по желанию. Все исследования на животных были проверены и одобрены Комитетом по уходу и применению животных Университета штата Огайо, и соответствовали Принципам ухода за лабораторными животными. Неполовозрелых самцов крыс Sprague-Dawley весом от 187 до 214 г распределяли случайным образом по 5 животных в 9 групп. За одни сутки до начала лечения лекарственным препаратом, в группах от 4 до 6 и в группах от 7 до 9 проводили соответственно одностороннюю или двустороннюю орхиэктомию, путем срединного скротального надреза. Животные в группах 1-3 не подвергались хирургии. Все лекарственные препараты, даваемые животным, были свежеприготовленными, в виде растворов в полиэтиленгликоле 300 (ПЭГ 300). Животные в группах 4 и 7 получали обработку одним растворителем (т.е., ПЭГ 300). Животные в группах 3, 6, и 9 получали пропионат тестостерона (ТР, 0,5 мг/сут) в результате имплантации подкожных осмотических насосов(модель 2002, фирма Durect Corpration, Palo Alto, CA). Животные в группах 2,5 и 8 получали соединение VI (0,5 мг/сут) путем имплантации подкожных осмотических насосов. После 14-суточной обработки лекарственными препаратами крыс взвешивали, анестезировали и умерщвляли. Пробы крови отбирали путем венепункции абдоминальной аорты. Пробы плазмы анализировали на тестостерон, фолликулостимулирующий гормон (FSH), лютеинизирующий гормон (LH) и остеокальцин. Концентрацию тестостерона измеряли с помощью AniLytics Inc. (Gaithersburg, шт. Мэриленд). Концентрации FSH и LH измеряли по программе National Hormone and Peptide Program (Dr. A. F.Parlow, UCLA, CA). Содержание остеокальцина в плазме определяли, используя ИФА-набор на крысиный остеокальцин, коммерчески доступный от фирмы Biomedical Technologies Inc. (Stoughton, шт. Массачусетс). Вентральные простаты, семенные пузырьки и поднимающие мышцы ануса удаляли и взвешивали. Кроме того, у животных удаляли осмотические насосы с целью проверки правильности их работы. Вес всех органов был нормализован относительно веса тела, и были проанализированы все статистически значимые различия между группами с использованием однофакторного анализа ANOVA, с априорно выбранной величиной альфа при р 0,05. В качестве показателя для оценки андрогенной активности использовали вес простаты и семенных пузырьков, а вес поднимающей мышцы ануса использовали для оценки анаболической активности. Статистический анализ параметров полного анализа крови или химического профиля сыворотки, где это применимо, осуществляли с использованием однофакторного анализа ANOVA, с априорно выбранной величиной альфа при р 0,05. Результаты Независимо от группы обработки содержание плазменного тестостерона было значительно ниже у кастрированных крыс (см. табл. 1, ниже). Односторонняя орхиэктомия приводила к слабому, но статистически незначимому снижению концентраций тестостерона в плазме. Кастрированные крысы-самцы,которые получали экзогенный пропионат тестостерона (0,5 мг/сут), имели более высокое содержание плазменного тестостерона, чем контрольные животные, обработанные растворителем и соединением VI. Однако в любой из групп обработки не наблюдались существенные различия в содержании тестостерона в плазме между животными, которые были подвергнуты односторонней орхиэктомии. Обработка соединением VI не влияет на содержание тестостерона у интактных, или подвергнутых односторонней орхиэктомии, или кастрированных самцов крыс, демонстрируя, что соединение VI слабо влияет или не влияет на продуцирование эндогенного андрогена при фармакологически релевантных дозах. Таблица 1. Содержание тестостерона в плазме (в нг/мл) в группах различной обработки (n=5) р 0,05 по сравнению с группой с односторонней орхиэктомией Концентрации FSH и LH в плазме (табл. 2 и 3 на следующей странице) значительно возрастали у- 15013399 животных, подвергнутых двухсторонней орхиэктомии (т.е. кастрированные контрольные животные). Концентрации FSH и LH в плазме животных, подвергнутых односторонней орхиэктомии, и интактных животных отличаются незначительно, что подтверждает наблюдение, что одностороняя орхиэктомия не оказывает влияния на содержание тестостерона в плазме или на гипофизарные гормоны, которые регулируют его. Обработка пропионатом тестостерона вызывает значительное снижение содержания FSH иLH у кастрированных самцов крыс, демонстрирующее, что ТР подавляет образование гипофизарных гормонов. Однако соединение VI не оказывает влияния на содержание FSH и LH в плазме. Эти данные указывают, что соединение VI не оказывает влияния на выработку гипофизарных гормонов и, следовательно, обладает преимуществом по сравнению с ТР при использовании на интактных животных. Для интактных животных или животных, подвергнутых односторонней орхиэктомии, не наблюдались существенные различия в содержании FSH и LH. Таблица 2. Содержание FSH в плазме (в нг/мл) в группах различной обработки (n=5) р 0,05 по сравнению с группой с односторонней орхиэктомией Таблица 3. Содержание LH в плазме (в нг/мл) в группах различной обработки (n=5) Было исследовано влияние односторонней орхиэктомии, двусторонней орхиэктомии, пропионата тестостерона и соединения VI на содержание остеокальцина в плазме (табл. 4). Остеокальцин представляет собой специфический остеобластный маркер, который может быть использован для оценки эндогенной скорости образования костной ткани. Не наблюдались существенные различия в содержании остеокальцина между интактными животными, животными, подвергнутыми односторонней орхиэктомии, и кастрированными животными в группе контрольных животных, обработанных растворителем. Однако обработка соединением VI приводила к значительному увеличению содержания остеокальцина в плазме у животных, подвергнутых односторонней орхиэктомии, и кастрированных животных. Пропионат тестостерона не оказывал влияния на содержание остеокальцина в плазме. Эти данные демонстрируют, что соединение VI значительно увеличивает скорость образования костной ткани у самцов животных, не оказывая влияния на концентрацию тестостерона, FSH или LH в плазме. Таблица 4. Содержание остеокальцина в плазме (в нг/мл) в группах различной обработки (n=5) При обработке соединением VI у интактных животных уменьшается размер простаты до 79% по сравнению с размером у контрольных животных, при этом отсутствуют статистически значимые изменения размера семенных пузырьков или поднимающей мышцы ануса (фиг. 2 и табл. 5, ниже). Более очевидными были фармакологические эффекты и тканевая селективность соединения VI у животных, под- 16013399 вергнутых односторонней орхиэктомии. Соединение VI уменьшает размер простаты и семенных пузырьков соответственно до 75 и 79% и увеличивает размер поднимающей мышцы ануса до 108% по сравнению с размером у необработанных животных, подвергнутых односторонней орхиэктомии. Эти наблюдения демонстрируют, что соединение VI действует как частичный агонист в простате и семенных пузырьках и как полный агонист в поднимающей мышце ануса. Побочные фармакологические эффекты не наблюдались. Таблица 5. Сопоставление андрогенного и анаболического действия соединения VI и пропионата тестостерона на интактных крыс, крыс, подвергнутых односторонней орхиэктомии, и кастрированных крыс (в% от интактных контрольных крыс, n=5) р 0,05 по сравнению с интактной контрольной группой р 0,05 по сравнению с ТР для крыс того же хирургического статуса (т.е. интактных, подвергнутых односторонней орхиэктомии или кастрированных) р 0,05 по сравнению с контрольной группой крыс того же хирургического статуса Соединение VI демонстрирует сильные и тканеселективные фармакологические эффекты у интактных, подвергнутых односторонней орхиэктомии или кастрированных самцов крыс. Соединение VI приводит к значительному уменьшению веса простаты у интактных животных и подвергнутых односторонней орхиэктомии животных и обладает меньшей эффективностью, чем ТР в отношении увеличения веса простаты у кастрированных животных. Аналогичные фармакологические эффекты были отмечены в семенных пузырьках (другой орган, который обычно рассматривается в качестве маркера андрогенных эффектов), за исключением того, что соединение VI не оказывает влияния на вес семенных пузырьков у интактных животных. Обработка соединением VI приводит к значительному увеличению веса поднимающей мышцы ануса у животных, подвергнутых односторонней орхиэктомии, и кастрированных животных. Эти эффекты были сильнее, чем наблюдаемые в случае пропионата тестостерона. Эти данные демонстрируют тканеселективные фармакологические эффекты соединения VI. Важно отметить, что эти эффекты наблюдались в отсутствие каких-либо значительных изменений концентраций FSH, LH и тестостерона в плазме. Соединение VI увеличивало концентрацию остеокальцина в плазме. В совокупности,эти данные показывают, что соединение VI устанавливает оптимальный фармакологический профиль для самцов животных и, таким образом, является первым представителем нового класса соединенийSARM с тканевой селективностью и биологической доступностью при оральном приеме. Пример 3. Фармакологическая активность и тканевая селективность соединения VII, гидроксифлутамида и финастерида в интактных самцах крыс Соединение VII представляет собой селективный модулятор рецептора андрогенов (SARM) на кастрированных самцах крыс. Это соединение ведет себя как агонист в анаболической ткани, и в то же время как частичный агонист в андрогенной ткани. Когда соединение VII вводится интактным самцам крыс в дозировке 0,5 мг/день, оно значительно снижает вес простаты, до 63 вес.%, наблюдаемого у интактных животных, обработанных только растворителем, не влияя на вес поднимающей мышцы ануса. Эта тканевая селективность соединения VII, наблюдаемая у интактных самцов крыс, может быть объяснена в рамках двух возможных механизмов: 1) в присутствии эндогенного тестостерона соединение VII просто ведет себя как частичный агонист в андрогенной ткани, зависящей от дигидротестостерона; 2) соединение VII представляет собой также ингибитор 5-редуктазы, кроме того, что обладает парциальной агонистической активностью в андрогенных тканях.- 17013399 Методы Самцы крыс породы Sprague-Dawley были приобретены на фирме Harlan Biosciences (г. Indianapolis,шт. Индиана). Для животных поддерживали 12-часовой цикл освещения и темноты, причем корм и вода были доступны по желанию. Самцов крыс Sprague-Dawley весом от 189 до 226 г случайным образом распределяли в группы по 5 животных. Интактных самцов крыс обрабатывали гидроксифлутамидом (0,5,1, 5, 10, или 25 мг/кг), финастеридом (5 мг/кг), соединением VII (0,5, 1, 5, 10, 25 мг/кг) или растворителем в течение 3, 6 или 9 суток. Лекарственные препараты растворяли в смеси диметилсульфоксид(ДМСО): ПЭГ 300 (20:80, по объему) и вводили в виде ежедневной подкожной инъекции, причем дозировку устанавливали в расчете на вес животного, который регистрировали ежедневно. Для контроля на каждый момент времени в исследование была включена группа (n=5) кастрированных крыс. В конце каждого периода обработки животных умерщвляли в течение 8 ч после последней дозы, андрогенные и анаболические ткани (вентральная простата, семенные пузырьки и поднимающая мышца ануса) удаляли и взвешивали. Простату замораживали и сохраняли при температуре -80 С для анализа концентрации дигидротестостерона и тестостерона; и пробы крови собирали и использовали для определения содержания сывороточных маркеров, включая FSH, LH и тестостерон. Вес органов был нормализован относительно веса тела. Изменения в процентах определяли путем сравнения с интактными животными. Статистические анализы всех параметров осуществляли с использованием однофакторного анализа ANOVA, с априорно выбранной величиной альфа при р 0,05. Результаты На фиг. 3-5 показано изменение веса органов во всех группах обработки после различных периодов обработки. Гидроксифлутамид при всех дозировках (0,5, 1, 5, 10, 25 мг/кг) значительно снижал сырой вес простаты, семенных пузырьков и поднимающей мышцы ануса в пределах трех суток обработки. Однако в любом из этих органов не замечена какая-либо типичная взаимосвязь между дозой и откликом. Аналогично, во всех группах дозировки вес простаты, семенных пузырьков и поднимающей мышцы ануса значительно снижался приблизительно до 60, 50 и 85%, соответственно. Между любыми двумя из этих групп дозировки отсутствовали достоверные различия. Для одинаковых моментов времени кастрирование значительно снижало вес простаты, семенных пузырьков и поднимающей мышцы ануса соответственно до 45, 30 и 71%. В группе, обработанной соединением VII, также не наблюдалась типичная взаимосвязь между дозой и откликом, аналогичные результаты получены в большинстве групп дозировки(0,5, 1, 5, 10, 25 мг/кг) после трех дней обработки. В целом, соединение VII снижало вес простаты и семенных пузырьков до 80 и 70%, без влияния на вес поднимающей мышцы ануса. В то же время финастерид (5 мг/кг) значимо снижал вес простаты и семенных пузырьков до 59 и 38%, не оказывая воздействия на вес поднимающей мышцы ануса. Через 6 суток после кастрации вес простаты, семенных пузырьков и поднимающей мышцы ануса дополнительно снижался до 22, 24 и 65% от нормального веса. Однако изменения веса органов у животных, обработанных гидроксифлутамидом, отличались по характеру от изменений после трехдневной обработки. В группах пониженной дозировки (0,5, 1, 5, 10 мг/кг) у животных, обработанных гидроксифлутамидом, не наблюдалось дальнейшее снижение веса любого из этих органов. Напротив, вес органов у животных в этих группах дозировки возвращался к уровню, наблюдаемому у интактных животных. Только при наибольшей дозе (25 мг/кг) вес простаты, семенных пузырьков и поднимающей мышцы ануса значительно снижался, соответственно, до 54, 41 и 65%. Хотя у животных этих групп, обработанных гидроксифлутамидом, не наблюдалось явной взаимосвязи между дозой и откликом, в группе с наибольшей дозировкой начинает проявляться существенное отличие от всех групп с меньшей дозировкой. У животных, обработанных соединением VII, изменения простаты, семенных пузырьков и поднимающей мышцы ануса были аналогичны тем, что наблюдались после трехдневной обработки; не наблюдалось никакой обычной взаимосвязи между дозой и откликом. При более высоких дозах (5, 10, 25 мг/кг) наблюдалось значительное снижение веса простаты и семенных пузырьков в интервале от 70 до 80% для простаты и от 45 до 68% для семенных пузырьков. Важно отметить, что ни одна из этих доз не вызывает каких-либо существенных изменений веса поднимающей мышцы ануса, что указывает на тканеселективную фармакологическую активность соединения VII и его потенциальную ценность при лечении ДГП. Финастерид (5 мг/кг) значимо снижал вес простаты и семенных пузырьков, до 67 и 47%, и при этом не наблюдалось существенных изменений веса поднимающей мышцы ануса. Через 9 суток после кастрации вес простаты, семенных пузырьков и поднимающей мышцы ануса еще более снижался до 15, 14 и 62% соответственно. Изменения веса органов у животных, обработанных гидроксифлутамидом, были подобны изменениям, наблюдаемым после трех или шести дней обработки. Вес простаты и семенных пузырьков снижался до 55 и 29%, а вес поднимающей мышцы ануса изменился незначительно. В группах животных, обработанных соединением VII, наблюдались возрастающие эффекты снижения веса простаты и семенных пузырьков в подгруппах с пониженной дозировкой (0,5, 1 и 5 мг/кг). Однако снижение во всех группах с высокой дозировкой (5, 10, 25 мг/кг) не зависит от дозы; вес простаты и семенных пузырьков значительно снижался до 50 и 45% соответственно. Кроме того, не наблюдались какие-либо существенные изменения веса поднимающей мышцы ануса в большинстве групп дозировки через 9 дней обработки, за исключением того, что наблюдалось существенное увеличение(112%) в группе наибольшей дозировки (25 мг/кг). При обработке гидроксифлутамидом, в конце концов(через 9 суток обработки) обнаруживалась некоторая взаимосвязь между дозой и откликом. В отличие от наблюдаемых эффектов через 6 суток обработки, обнаружено умеренное снижение веса простаты, семенных пузырьков и поднимающей мышцы ануса при пониженных дозах (0,5, 1, 5, 10 мг/кг), причем эти изменения зависели от дозы. Для дозы 25 мг/кг сохранялись эффекты, наблюдаемые для веса всех органов на аналогичном уровне по сравнению с таковым для предыдущих моментов времени. В целом, высокая доза гидроксифлутамида (25 мг/кг) существенно снижала вес органов (простата,семенные пузырьки и поднимающая мышца ануса) после 3, 6 или 9 суток обработки. Однако наблюдались некоторые флуктуации этих изменений в группах с пониженной дозой (0,5, 1, 5, 10 мг/кг), при этом не наблюдалась типичная взаимосвязь между дозой и откликом вплоть до конца 9-дневной обработки. Финастерид при дозе 5 мг/кг значительно снижал вес простаты и семенных пузырьков в сходной степени после 3, 6 или 9 суток обработки, однако он не влиял на вес поднимающей мышцы ануса. СоединениеVII также может снижать вес простаты и семенных пузырьков у интактных животных после 3, 6 или 9 суток обработки, при этом не наблюдалась типичная взаимосвязь между дозой и откликом на момент 3 и 6 суток, хотя некоторые зависящие от дозы изменения были отмечены при пониженных дозах (0,5, 1, 5 мг/кг), через 9 суток обработки. Однако соединение VII не снижало в значимой степени вес поднимающей мышцы ануса при любой дозе после 3, 6 или 9 суток обработки; при обработке дозой 25 мг/кг вес поднимающей мышцы ануса даже увеличился на 12% после 9 суток обработки. Влияние соединения VII на андрогенные ткани было аналогично влиянию гидроксифлутамида, тогда как его влияние на поднимающую мышцу ануса было аналогично влиянию финастерида. Пример 4. Соединение VII снижает вес простаты у интактных крыс Sprague-Dawley Самцов интактных крыс Sprague-Dawley (20 шт.), каждый весом приблизительно 100-175 г, случайным образом распределяли по 5 животных в 4 группы обработки. Животных обрабатывали через оральный зонд растворителем (10% этанола и 90% полиэтиленгликоля) или соединением VII, растворенным в растворителе,в соответствии со следующей методикой обработки: в группе 1 давали только растворитель (0 мг/кг), в группе 2 давали 30 мг/кг соединения VII, в группе 3 - 100 мг/кг соединения VII, в группе 4 - 300 мг/кг соединения VII. Каждое животное получало одну дозу в день в течение семи последовательных дней. На 8-й день животных умерщвляли, и у каждого животного иссекали вентральную простату и взвешивали. Вес простаты (в г) был нормализован относительно веса тела (в г), и эти результаты представлены на фиг. 6. У животных, обработанных 10 мг/кг соединения VII, наблюдалось заметно пониженное соотношение веса простаты к весу тела,0,062% в сравнении с 0,128% в контрольной группе 1 (0 мг/кг). Во всех группах обработки соединение VII сильно снижало вес простаты (нормализован относительно веса тела), больше чем на 48,4% по сравнению с неинтактными контрольными животными (р 0,01). Более того, увеличение дозы 10 мг/кг в 100 раз не приводило к значительному увеличению атрофии простаты (доза 10 мг/кг по сравнению с дозой 1000 мг/кг). Приведенные в описании результаты демонстрируют, что введение соединения VII может быть эффективным для уменьшения размера простаты и, следовательно, для минимизации симптомов, связанных с доброкачественной гиперплазией простаты, при относительно малых фармакологических дозах. Специалистам в этой области техники будет понятно, что настоящее изобретение не ограничивается тем, что конкретно показано и описано выше. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ блокирования способности дигидротестостерона (DHT) индуцировать гиперплазию, который включает стадию контактирования рецептора андрогенов с соединением - селективным модулятором рецептора андрогенов (SARM) формулы IR1 представляет собой СН 3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода;SARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию. 2. Способ ингибирования митогенного действия тестостерона и DHT, который включает стадию контактирования рецептора андрогенов с соединением SARM формулы IR1 представляет собой СН 3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода, тем самым ингибируя митогенную активность тестостерона и DHT. 3. Способ ингибирования рекрутирования коактиваторов или корегуляторов андрогенреспонсивной ДНК, который включает стадию контактирования рецептора андрогенов с соединениемR1 представляет собой CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3, где алкил содержит 1-12 атомов углерода; тем самым ингибируя рекрутирование коактиваторов или корегуляторов андроген-респонсивной ДНК. 4. Способ лечения пациентов-мужчин, страдающих от доброкачественной гиперплазии простаты,который включает стадию введения указанному пациенту соединения - селективного модулятора рецептора андрогенов (SARM) формулы IR1 представляет собой СН 3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3,где алкил содержит 1-12 атомов углерода. 5. Способ по п.1, который предусматривает введение изомера, фармацевтически приемлемой соли,гидрата или N-оксида указанного SARM или любого их сочетания. 6. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой IIR представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН,где алкил содержит 1-12 атомов углерода. 7. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VI 8. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VII 9. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой VIII 10. Способ по п.1, в котором указанное соединение SARM представлено структурной формулой IX 11. Способ по п.1, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5-редуктазы. 12. Способ по п.1, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5-редуктазы. 13. Способ по п.12, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 1. 14. Способ по п.12, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 2. 15. Способ по п.1, в котором фермент 5-редуктаза представляет собой фермент тестостерон-5 редуктазу. 16. Способ по п.4, в котором указанное введение включает внутривенную, внутриартериальную или внутримышечную инъекцию указанному пациенту указанного соединения SARM в жидкой форме; подкожную имплантацию указанному пациенту гранулы, содержащей указанное соединение SARM; оральное введение указанному пациенту указанного соединения SARM в жидкой или твердой форме; или ме- 21013399 стное нанесение на поверхность кожи указанного пациента указанного соединения SARM. 17. Способ предупреждения, подавления, ингибирования или снижения заболеваемости доброкачественной гиперплазией простаты у пациентов-мужчин, который включает стадию введения указанному пациенту соединения SARM формулы ISARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию. 18. Способ по п.17, который включает введение изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного SARM или любого их сочетания. 19. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой IIR представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН,где алкил содержит 1-12 атомов углерода. 20. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой VI 21. Способ по п.17, в котором указанное соединение SARM представлено структурной формулой VII 22. Способ по п.17, в котором соединение SARM представлено структурной формулой VIII 23. Способ по п.17, в котором соединение SARM представлено структурной формулой IX 24. Способ по п.17, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5-редуктазы. 25. Способ по п.17, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5-редуктазы. 26. Способ по п.25, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 1. 27. Способ по п.25, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 2. 28. Способ по п.25, в котором фермент 5-редуктаза представляет собой фермент тестостерон-5 редуктазу. 29. Способ по п.17, в котором указанное введение включает внутривенную, внутриартериальную или внутримышечную инъекцию указанному пациенту указанного соединения SARM в жидкой форме; подкожную имплантацию указанному пациенту гранулы, содержащей указанное соединение SARM; оральное введение указанному пациенту указанного соединения SARM в жидкой или твердой форме; или местное нанесение на поверхность кожи указанного пациента указанного соединения SARM. 30. Способ ингибирования фермента 5-редуктазы, который включает контактирование указанного фермента с эффективным ингибирующим 5-редуктазу количеством соединения SARM формулы IR представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН иR1 представляет собой СН 3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3,где алкил содержит 1-12 атомов углерода; или изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного соединенияSARM, или любого их сочетания; тем самым блокируя способность DHT индуцировать гиперплазию. 31. Способ по п.30, который включает введение изомера, фармацевтически приемлемой соли, гидрата или N-оксида указанного SARM или любого их сочетания. 32. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой IIR представляет собой алкил, галоидалкил, дигалоидалкил, тригалоидалкил, CH2F, CHF2, CF3,CF2CF3, фенил, галоген, алкенил или ОН,где алкил содержит 1-12 атомов углерода. 33. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой VI 34. Способ по п.30, в котором указанное соединение SARM представлено структурной формулой VII 35. Способ по п.30, в котором соединение SARM представлено структурной формулой VIII 36. Способ по п.30, в котором соединение SARM представлено структурной формулой IX 37. Способ по п.30, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью ингибитора фермента 5-редуктазы. 38. Способ по п.30, в котором соединение SARM характеризуется тем, что оно дополнительно обладает активностью конкурентного ингибитора фермента 5-редуктазы. 39. Способ по п.30, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 1. 40. Способ по п.30, в котором фермент 5-редуктаза представляет собой фермент 5-редуктазу типа 2. 41. Способ по п.30, в котором фермент 5-редуктаза представляет собой фермент тестостерон-5 редуктазу.
МПК / Метки
МПК: A61K 31/16, A61P 43/00, A61K 31/32, A61P 13/00, A61K 31/165
Метки: андрогенов, рецептора, лечение, модулятором, простаты, доброкачественной, селективным, гиперплазии
Код ссылки
<a href="https://eas.patents.su/29-13399-lechenie-dobrokachestvennojj-giperplazii-prostaty-selektivnym-modulyatorom-receptora-androgenov-sarm.html" rel="bookmark" title="База патентов Евразийского Союза">Лечение доброкачественной гиперплазии простаты селективным модулятором рецептора андрогенов ( sarm )</a>
Предыдущий патент: Разложение отходов, образующихся при синтезе с использованием катализаторной суспензии
Следующий патент: Способ лечения опухолевых заболеваний
Случайный патент: Устройство и способ сжигания топлива












