Бензоксазиноновые антагонисты рецептора допамина d4.
Номер патента: 1486
Опубликовано: 23.04.2001
Авторы: Вайс Лауренс Дейвид, Беллиотти Томес, Вустров Дейвид Юрген
Формула / Реферат
1. Соединение формулы (I)
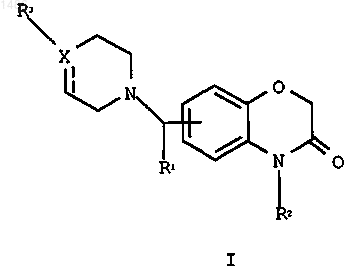
где R1 и R2 означают независимо водород или алкил с числом углеродных атомов от 1 до 6,
X означает С, N или СН, при этом в случае X=С штрихованная линия означает связь, а в других случаях отсутствует;
R3 означает фенил, нафтил, гетероарил, замещенный фенил, замещенный нафтил или замещенный гетероарил, при этом каждый заместитель независимо выбран из группы, включающей галоген, алкоксигруппу с числом углеродных атомов от 1 до 6, алкил с числом углеродных атомов от 1 до 6, цианогруппу, трифторметил или сульфонамидогруппу;
и их фармацевтически приемлемые соли, эфиры, амиды и пролекарства.
2. Соединение по п.1, где группа
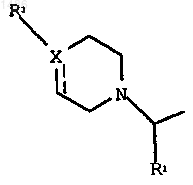
присоединена к бензоксазиноновой группе по 6 или 7 положению.
3. Соединение по п.1, где R1 и R2 означают водород.
4. Соединение по п.1, где R3 означает фенил, метилтолил, толил или сульфонамидогруппу.
5. Соединение по п.1, где X означает N.
6. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил, R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу.
7. Соединение по п.1, где группа
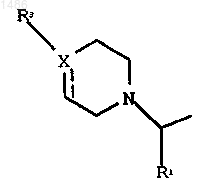
присоединена к бензоксазиноновой группе по 6 или 7 положению, при этом X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил, R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу.
8. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 и R2 означают водород; R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу.
9. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил, R3 означает фенил, метилтолил, толил или сульфонамидогруппу.
10. Соединение по п.1, представляющее собой
4-[4-(3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-пиперазин-1-ил]-бензолсульфонамид;
6-[4-(3,4-диметил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-(4-п-толил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
6-[4-фенил-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-(4-п-толил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
7-(4-фенил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
7-[4-(3,4-диметил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(5-метил-пиридин-2-ил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-(4-п-толил-пиперидин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
6-[4-(3,4-диметил-фенил)-пиперидин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-(4-тиазол-2-ил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
6-(4-бензотиазол-2-ил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
6-[4-(4,5-диметил-тиазол-2-ил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-(4-нафталин-2-ил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
6-[4-(3-хлор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(3,4-дихлор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
2-[4-(3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-пиперазин-1-ил]-бензонитрил;
6-[4-(4-метокси-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он или
6-[4-(2-хлор-4-метил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он.
11. Соединение по п.1, представляющее собой
6-[4-(4-фтор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(3-трифторметил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(3,5-диметил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(2-хлор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(4-трифторметил-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(4-хлор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-[4-(5-метил-пиридин-2-ил)-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
7-[4-(4-метокси-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-[4-(4-хлор-фенил)-пиперазин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-[4-(3,4-диметил-фенил)-пиперидин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
6-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4Н-бензо[1,4]оксазин-3-он;
7-(4-фенил-пиперидин-1-илметил)-4Н-бензо[1,4]оксазин-3-он;
7-(4-нафталин-2-ил-пиперазин-1-илметил)-4Н-бензо[1,4]оксазин-3-он и
7-(4-п-толил-пиперидин-1-илметил)-4Н-бензо[1,4]оксазин-3-он.
12. Способ лечения психоза или шизофрении, включающий назначение пациенту, страдающему психозом или шизофренией, терапевтически эффективного количества соединения по п.1.
13. Фармацевтически приемлемый состав, включающий соединение по п.1.
Текст
1 Область техники Настоящее изобретение относится к соединениям, которые являются антагонистами рецепторов допамина Д 4, к способам лечения психоза и шизофрении с применением соединения, которое является антагонистом рецепторов допамина Д 4, и к фармацевтически приемлемым композициям, которые содержат антагонист рецептора допамина Д 4. Предпосылки создания изобретения Допамин представляет собой нейротрансмиттер, который обнаруживается в мозгах животных, включая человека, и весьма важен для нормальной передачи нервного сигнала. Широко известно, что некоторые соединения блокируют или ингибируют связывание допамина рецепторами допамина. Такие соединения называют антагонистами рецептора допамина. Известно также, что антагонисты рецептора допамина полезны при лечении шизофрении и психоза. Недавно было обнаружено, что существует более чем один тип рецепторов допамина, и что антагонисты рецептора допамина могут предпочтительно ингибировать один тип рецептора допамина, по сравнению с другим. Было выявлено два основных семейства рецепторов допамина, названных Д 1 и Д 2. В семействе Д 2 было выявлено три различных подтипа рецепторов,названных, соответственно, Д 2, Д 3 и Д 4. Распределение и концентрация подтипов рецепторов варьирует в различных областях мозга. Рецепторы подтипа Д 2 локализованы в обоих полушариях мозга, ассоциированных с познавательной и эмоциональной функциями, и в полосатом теле, ассоциированном с двигательными эффектами. Д 4 обнаружен в высоких концентрациях во фронтальной коре и в полушариях, ассоциированных с познавательной и эмоциональной функциями. Антипсихотические препараты, которые являются антагонистами рецепторов подтипа Д 2, используют при лечении психоза и шизофрении, однако, их применению сопутствуют нежелательные внепирамидальные побочные эффекты и возникновение поздней дискинезии. Напротив, антагонисты рецептора Д 4 показали отсутствие побочных внепирамидальных эффектов и поздней дискинезии. Более того, показано, что уровни рецепторов допамина Д 4 у шизофреников повышаются. Таким образом, соединения, являющиеся избирательными антагонистами Д 4, были бы весьма полезными при лечении психоза и шизофрении. Краткое описание изобретения Настоящее изобретение относится к соединениям формулы I где R1 и R2 означают независимо водород или алкил с числом углеродных атомов от 1 до 6,X означает С, N или СН, при этом в случаеX=С штрихованная линия означает связь, а в других случаях отсутствует;R3 означает фенил, нафтил, гетероарил,замещенный фенил, замещенный нафтил или замещенный гетероарил, где каждый заместитель независимо выбран из группы, включающей галоген, алкоксигруппу с числом углеродных атомов от 1 до 6, алкил с числом углеродных атомов от 1 до 6, цианогруппу, трифторметил или сульфонамидогруппу; и их фармацевтически приемлемым солям, эфирам, амидам и пролекарствам. В первую группу предпочтительных соединений формулы (I) входят соединения, где группа присоединена к бензоксазиноновой группе по 6 или 7 положению. Во вторую группу предпочтительных соединений формулы (I) входят соединения, гдеR1 и R2 означают водород. В третью группу предпочтительных соединений формулы (I) входят соединения, гдеR3 означает фенил, метилтолил, толил или сульфонамидогруппу. В четвертую группу предпочтительных соединений формулы (I) входят соединения, где X означает N. В пятую группу предпочтительных соединений формулы (I) входят соединения, где X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил, R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. В шестую группу предпочтительных соединений формулы (I) входят соединения, где группа 3 присоединена к бензоксазиноновой группе по 6 или 7 положению, при этом X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил,R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. В седьмую группу предпочтительных соединений формулы (I) входят соединения, где X означает N или СН; штрихованная линия отсутствует; R1 и R2 означают водород; R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. В воcьмую группу предпочтительных соединений формулы (I) входят соединения, гдe X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил, R3 означает фенил, метилтолил,толил или сульфонамидогруппу. Наиболее предпочтительными соединениями формулы I являются следующиe: 4-[4-(3-оксо-3,4-дигидро-2 Н-бензо[1,4] оксазин-6-илметил)-пиперазин-1-ил]-бензолсульфонамид; 6-[4-(3,4-диметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-п-толил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 6-[4-фенил-пиперазин-1-илметил]-4 Нбензо[1,4]оксазин-3-он; 7-(4-п-толил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-(4-фенил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-[4-(3,4-диметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(5-метил-пиридин-2-ил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-п-толил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 6-[4-(3,4-диметил-фенил)-пиперидин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-тиазол-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он; 6-(4-бензотиазол-2-ил-пиперазин-1-илметил)-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4,5-диметил-тиазол-2-ил)-пиперазин 1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-нафталин-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3,4-дихлор-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 2-[4-(3-оксо-3,4-дигидро-2 Нбензо[1,4]оксазин-6-илметил)-пиперазин-1-ил]бензонитрил; 6-[4-(4-метокси-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 4 6-[4-(2-хлор-4-метил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4-фтор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3-трифторметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3,5-диметил-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(2-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4-трифторметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(5-метил-пиридин-2-ил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(4-метокси-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(4-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(3,4-диметил-фенил)-пиперидин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-(4-фенил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-(4-нафталин-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он; 7-(4-п-толил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; Настоящее изобретение также включает способ лечения психоза, заключающийся в назначении пациенту, страдающему этой болезнью, терапевтически эффективного количества соединения формулы I. Кроме того, настоящее изобретение включает способ лечения шизофрении, заключающийся в назначении пациенту, страдающему этой болезнью, терапевтически эффективного количества соединения формулы I. Кроме того, настоящее изобретение включает фармацевтически приемлемую композицию, которая включает соединение формулы I. Подробное описание изобретения Настоящее изобретение относится к соединениям вышеприведенной формулы (I),где R1 и R2 означают независимо водород или алкил с числом углеродных атомов от 1 до 6,X означает С, N или СН, при этом в случаеX=С штрихованная линия означает связь, а в других случаях отсутствует;R3 означает фенил, нафтил, гетероарил,замещенный фенил, замещенный нафтил или замещенный гетероарил, где каждый заместитель независимо выбран из группы, включающей галоген, алкоксигруппу с числом углеродных атомов от 1 до 6, алкил с числом углеродных атомов от 1 до 6, цианогруппу, трифторметил или сульфонамидогруппу; 5 и к их фармацевтически приемлемым солям,эфирам, амидам и пролекарствам. Термин алкил означает углеводород с линейной или разветвленной цепью. Представительными примерами алкильных групп являются метил, этил, пропил, изопропил, изобутил,бутил, трет-бутил, втор-бутил, пентил и гексил. Термин арил означает циклический ароматический углеводород. Представительные примеры арильных групп включают фенил и нафтил, которые могут быть замещенными или незамещенными. Примеры подходящих заместителей включают галоген, алкил с числом углеродных атомов от 1 до 6, алкоксигруппу с числом углеродных атомов от 1 до 6, -CF3, и сульфонамиды. Термин гетероарил означает циклический углеводород, который содержит один или более гетероатомов. Представительными примерами гетероарильных групп являются тиазол,тиофен и пиридин, пиримидин, хинолин, изохинолин и имидазол. Гетероарильные группы могут быть замещенными или незамещенными. Примеры подходящих заместителей включают алкил с числом углеродных атомов от 1 до 6,алкоксигруппу с числом углеродных атомов от 1 до 6 или галоген. Термин гетероатом означает иной атом,нежели углерод. Примеры гетероатомов включают азот, кислород, серу и фосфор. Термин галоген означает хлор, фтор,бром и йод. Термин сульфонамидная группа означает группу, имеющую структуру -SO2NRaRb, гдеRa и Rb являются сульфонамидными заместителями, хорошо известными специалистам, такими как водород и алкил с числом углеродных атомов от 1 до 6. Символ - означает связь. Атомы в бензоксазиноновой группе могут быть пронумерованы, как показано ниже Термин пациент включает человека. Терапевтически эффективное количество означает количество соединения настоящего изобретения, которое при назначении пациенту снижает интенсивность симптомов психоза или шизофрении. Терапевтически эффективное количество соединения настоящего изобретения может быть легко определено специалистом путем назначения определенного количества соединения пациенту и наблюдения за результатом. Кроме того, специалист в данной области владеет способами определения пациентов с психозом и шизофренией и способен легко идентифицировать пациентов, страдающих от психоза и шизофрении. 6 Термин фармацевтически приемлемые соли, эфиры, амиды и пролекарства в том смысле как он здесь используется, относится к тем карбоксилатным солям, солям присоединения аминокислот, эфирам, амидам и пролекарствам соединений настоящего изобретения, которые являются в пределах разумного с точки зрения медицины, подходящими для использования в контакте с тканями пациента без чрезмерной токсичности, раздражающей способности аллергического ответа и так далее, соразмерными с разумным отношением выгода/риск и эффективными при использовании в упомянутых целях, а также к цвиттерионным формам соединений настоящего изобретения в тех случаях, когда это возможно. Термин соли относится к относительно нетоксичным неорганическим и органическим солям присоединения соединений настоящего изобретения. Такие соли могут быть изготовлены in situ, в ходе окончательного выделения и очистки соединений, или в ходе отдельной реакции очищенного соединения в его свободной основной форме с соответствующей органической или неорганической кислотой, с последующим выделением образовавшейся таким образом соли. Представительные соли включают гидробромиды, гидрохлориды, сульфаты, бисульфаты, нитраты, ацетаты,оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, фосфаты, тозилаты, цитраты, малеаты, фумараты,сукцинаты, тартраты, нафтилаты мезилаты,глюкогептонаты, лактобионаты, лаурилсульфонаты и им подобные. Они могут также включать катионы щелочных и щелочно-земельных металлов, таких как натрий, литий, калий, кальций, магний и им подобные, а также нетоксичный аммоний, четвертичный аммоний и аминокатионы, включая, но не ограничиваясь ими,аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин,триэтиламин, этиламин и им подобные (см.,например, Berge S.М., et al., PharmaceuticalSalts, J. Pharm. Sci., 1977; 66:1-19, включенную в данное описание в виде ссылки). Примеры фармацевтически приемлемых нетоксичных эфиров соединений настоящего изобретения включают эфиры алкилов с числом углеродных атомов от 1 до 6, где алкильная группа представлена линейной или разветвленной цепью. Приемлемые эфиры также включают эфиры циклоалкилов с числом углеродных атомов от 5 до 7, а также эфиры арилалкилов,таких как (но не ограничиваясь им) бензил. Предпочтительны эфиры алкилов с числом углеродных атомов от 1 до 4. Эфиры соединений настоящего изобретения могут быть получены в соответствии с известными способами. Примеры фармацевтически приемлемых нетоксичных амидов соединений настоящего изобретения включают амиды, происходящие из аммиака, первичных алкиламинов с числом уг 7 леродных атомов от 1 до 6 и вторичных диалкиламинов с числом углеродных атомов в каждом алкиле от 1 до 6, где алкильные группы представлены линейными или разветвленными цепями. В случае вторичных аминов амин может быть также в форме 5- или 6-членного гетероцикла, содержащего 1 атом азота. Предпочтительны амиды, происходящие из аммиака, первичные алкиламины с числом углеродных атомов от 1 до 3, вторичные диалкиламины с числом углеродных атомов в каждом алкиле от 1 до 2. Амиды соединений настоящего изобретения получают в соответствии с известными способами. Термин пролекарство относится к соединениям, которые быстро превращаются invivo в соединение одной из приведенных выше формул, например, путем гидролиза в крови. Подробное обсуждение вопроса можно найти в Т. Higuchi and V. Stella, Pro-drugs as Novel Delivery Systems Vol. 14 of the A. C. S. SymposiumDesign, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987,обе публикации включены в данное описание в виде ссылки. Соединения настоящего изобретения назначают пациенту сами по себе или как часть состава, который содержит другие компоненты,такие как наполнители, разбавители и носители,хорошо известные специалистам. Композиции назначают человеку и животному оральным,ректальным, парентеральным (внутривенно,внутримышечно или подкожно), интрацистернальным, интравагинальным, внутрибрюшинным, внутрипузырным, локальным (порошки,мази, капли) путями или в виде аэрозоля для ротовой или носовой полости. Композиции, подходящие для парентеральных инъекций, включают физиологически приемлемые стерильные водные и неводные растворы, дисперсии, суспензии или эмульсии и стерильные порошки, предназначенные для превращения в стерильные инъецируемые растворы или дисперсии. Примеры подходящих водных и неводных носителей, разбавителей,растворителей или наполнителей включают воду, этанол, многоатомные спирты (пропиленгликоль, полиэтиленгликоль, глицерин и им подобные), соответствующие их смеси, растительные масла (как, например, оливковое масло) и допустимые для инъецирования органические эфиры, такие как этилолеат. Соответствующую текучесть устанавливают с помощью покрытий,таких как лецитин, путем отбора частиц определенного размера в случае дисперсий, а также путем использования поверхностно-активных веществ. Эти композиции могут также содержать вспомогательные вещества, такие как консерванты, увлажнители, эмульгаторы и диспергаторы. Для предотвращения деятельности микроорганизмов используют различные антибак 001486 8 териальные и противогрибковые компоненты,например, парабены, хлорбутанол, фенол, сорбиновая кислота и им подобные. При необходимости в композицию включают изотонические компоненты, например, сахара, хлорид натрия и им подобные. Пролонгированное рассасывание инъецированной фармацевтической формы достигают применением компонентов,замедляющих рассасывание, например, моностеарата алюминия и желатина. Твердые формы дозировки для орального назначения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых формах дозировки активный компонент смешивают с как минимум одним обычным инертным наполнителем (или носителем), таким как цитрат натрия или дикальцийфосфат, или (а) сухим разбавителем, таким как крахмалы, лактоза, сахароза, глюкоза, маннитол и кремниевую кислоту; (б) связующим веществом, таким как карбоксиметилцеллюлоза, альгинаты, желатин,поливинилпирролидон, сахароза и арабская камедь; (в) увлажнителями, как, например, глицерин; (г) разрыхляющим компонентом, как, например, агар-агар, карбонат кальция, крахмал из картофеля или тапиоки, альгиновая кислота,некоторые комплексные силикаты и карбонат натрия; (д) замедлителями растворения, как,например, парафин; (е) усилителями всасывания, как, например, соединения четвертичного аммония; (ж) смачивающими веществами, как,например, цетиловый спирт и моностеарат глицерина; (з) адсорбентами, как, например, каолин и бентонит и (и) смазывающими веществами,как, например, тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия или их смеси. В случае капсул,таблеток и пилюль, формы дозировки могут также включать буферные компоненты. Твердые композиции подобного типа используют в качестве содержимого в мягко- и твердозаполненных желатиновых капсулах с использованием таких наполнителей как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и им подобные вещества. Твердые формы дозировки, такие как таблетки, драже, капсулы, пилюли и гранулы могут быть изготовлены с покрытием и скорлупой,например, с покрытием для растворения в кишечнике и другими, хорошо известными специалистам. Они могут содержать омутняющие вещества и могут иметь такой состав, который допускает высвобождение активного соединения или соединений в определенной точке пищеварительного тракта путем задержки растворения. Для этого используют полимерные вещества и воски. Активные соединения также назначают в микроинкапсулированной форме с одним или более упомянутыми наполнителями,если необходимо. 9 Жидкие формы дозировки для орального назначения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным соединениям жидкие формы дозировки содержат инертные разбавители, обычно используемые в фармацевтике, такие как вода или другие растворители,солюбилизирующие вещества,эмульгаторы, как, например, этиловый спирт,изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла, в особенности, хлопковое масло,арахисовое масло, кукурузное масло, оливковое масло, касторовое масло и кунжутное масло,глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и жирно-кислотные эфиры сорбитана или смеси этих веществ и им подобные. Помимо таких инертных разбавителей составы могут также включать вспомогательные вещества, такие как смачивающие компоненты,эмульгаторы и суспензирующие компоненты,подслащивающие вещества, вкусовые добавки,ароматизаторы. Суспензии, вдобавок к активным соединениям могут содержать суспендирующие вещества, как, например, этоксилированный изостеариловый спирт, сорбитоловые или сорбитановые эфиры полиоксиэтилена, микрокристаллическая целлюлоза, метагидроксид алюминия,бентонит, агар-агар и трагакант или смеси этих веществ и им подобные. Составы ректального назначения предпочтительно являются суппозиториями, которые изготавливают смешиванием соединений настоящего изобретения с подходящим не раздражающим наполнителем или носителем, такими как какао-масло, полиэтиленгликоль или суппозиторный воск, которые являются твердыми при обычных температурах, но плавятся в прямой кишке и вагинальной полости, высвобождая активный компонент. Формы дозировки местного назначения соединений настоящего изобретения включают мази, порошки, аэрозоли и ингаляции. Активный компонент смешивают в стерильных условиях с физиологически приемлемым носителем и какими-либо консервантами, буферами или,при необходимости, пропеллантами. Офтальмологические составы, глазные мази, порошки и растворы также рассматриваются как включенные в рамки настоящего изобретения. Соединения настоящего изобретения назначают пациенту с дозировкой в диапазоне от примерно 0.1 до примерно 1000 мг в день. Для нормального взрослого человека с весом тела около 70 кг, дозировка в пределах от примерно 0.01 до примерно 100 мг на килограмм веса тела в день является достаточной. В специальных случаях, однако, дозировку можно варьировать. Например, дозировка может зависеть от множе 001486 10 ства факторов, включая состояние пациента,условия лечения и фармакологическую активность конкретного используемого соединения. Определение оптимальной дозировки для конкретного пациента является рутинной задачей для специалиста. Кроме того, соединения настоящего изобретения могут находиться как в несольватированной, так и в сольватированной фармацевтически приемлемыми растворителями, такими как вода, этанол и им подобные, формах. В общем случае, сольватированные формы рассматриваются как эквивалентные несольватированным формам для целей настоящего изобретения. Соединения настоящего изобретения могут находиться в различных стереоизомерных формах в силу наличия в них асимметричных центров. Подразумевается, что все стереоизомерные формы этих соединений, а также их смеси, включая рацемические, являются частью настоящего изобретения. Следующие ниже примеры иллюстрируют конкретные случаи воплощения настоящего изобретения, но никоим образом не ограничивают их полный перечень, включенный в формулу изобретения. Общие схемы синтеза(5,0 г, 29,9 ммоль), 1,3-пропандиола (3,4 г, 44,9 ммоль) и 0,1 г п-толуолсульфоновой кислоты в 100 мл толуола греют до кипения с обратным холодильником. Образующуюся воду удаляют с помощью ловушки Дина-Старка. Через 2 ч реакционную смесь охлаждают до комнатной температуры и экстрагируют 2100 мл насыщенного бикарбоната натрия, а затем 100 мл солевого раствора. Высушивание над сульфатом натрия и выпаривание растворителя дает 5,6 г(5,6 г, 24,9 ммоль) восстанавливают в присутствии никеля Рэнея в 50 мл тетрагидрофурана(ТГФ) в атмосфере водорода. Когда теоретически необходимое количество водорода израсходовано, катализатор удаляют фильтрацией. К фильтрату при комнатной температуре добавляют хлорацетилхлорид (2,5 г, 22,2 ммоль) и бикарбонат натрия (3,6 г, 42,3 ммоль) и перемешивают в течение 1 ч в атмосфере аргона. Растворитель выпаривают, а твердый остаток растворяют в 50 мл метанола. Раствор подкисляют 1,0 N HCl до рН примерно 1 и перемешивают при комнатной температуре в течение 1 ч. Осадок собирают и сушат под вакуумом с получением 2,5 гN, 6.41. Пример 3. Получение 3-оксо-3,4-дигидро 2 Н-бензо[1,4]оксазин-6-карбальдегида. 3-(хлорацетиламино)-4-гидроксибензальдегид (2,4 г, 13,2 ммоль) и карбонат калия (9,1 г,66,1 ммоль) перемешивают при комнатной температуре в 50 мл ацетонитрила в течение 12 ч. Ацетонитрил выпаривают, а остаток заливают 50 мл воды. После отстаивания при комнатной температуре в течение 10 мин, осадок собирают фильтрацией и перекристаллизовывают из этилацетата с получением 1,4 г (выход 60%) 3-оксо 3,4-дигидро-2 Н-бензо[1,4]оксазин-6-карбальдегида; Тпл=220-222 С. Анализ для С 9H7NO3: С, 61.02; Н, 3.98; N, 7.91. Полученные величины: С, 60.67; Н, 4.03;(0,5 г, 2,8 ммоль) и 4-(пиперазин-1-ил)бензолсульфонамида (0,17 г, 3,1 ммоль) в 20 мл ТГФ. Смесь перемешивали при комнатной температуре в течение ночи. Реакцию гасили добавлением 50 мл воды, после чего ТГФ удаляли под вакуумом. Осадок собирали фильтрацией и перекристаллизовывали из метанола с получением 0,05 г (выход 4%) 4-[4-(3-оксо-3,4 дигидро-2 Н-бензо[1,4]-оксазин-6-илметил)пиперазин-1-ил]-бензолсульфонамида; Тпл= 150-153 С. Анализ для C19H22N4 О 4S: С, 56.70; Н, 5.51; N, 13.92; S, 7,97. Полученные величины: С, 56.57; Н, 5.56;N, 11.92. Пример 6. Получение 4-[4-(метилфенил)пиперазин-1-илметил]-2-нитрофенола. Триацетоксиборгидрид натрия (1,8 г, 8,4 ммоль) добавляют в раствор 4-гидрокси-3 нитробензальдегида (1,3 г, 8,0 ммоль) и 1-(4 метил-фенил)-пиперазина (2,8 г, 16,1 ммоль) в 50 мл ТГФ при комнатной температуре, после чего смесь перемешивают в течение ночи. Реак 13 цию гасят добавлением 400 мл воды, образовавшийся осадок собирают фильтрацией. Выход 1,7 г (33%) маслянистой жидкости 4-4(метилфенил)-пиперазин-1-илметил]-2-нитрофенола. ЯМР-спектроскопия CDCl3:2.2 (s, 3 Н),2.5 (m, 4H), 3.05 (m, 4 Н), 3.4 (s, 2H), 6.8 (d, 2H),7.0 (d, 2H), 7.05 (d, 1H), 7.55 (d, 1H), 8.0 (s, 1H). Пример 7. Получение 6-(4-п-толилпиперазин-1-илметил)-4 Н-бензо[1,4]оксазин-3 она. 4-[4-(метилфенил)-пиперазин-1-илметил]2-нитрофенол (1,7 г, 5,2 ммоль) восстанавливают с никелем Рэнея в 20 мл ТГФ под водородом. Когда теоретически необходимое количество водорода израсходовано, катализатор удаляют фильтрацией. ТГФ выпаривают, а к остатку добавляют 50 мл хлороформа. Затем добавляют хлорацетилхлорид (0,65 г, 5,7 ммоль) и бикарбонат натрия (1,6 г, 19,1 ммоль), смесь перемешивают при комнатной температуре в течение полутора часов, экстрагируют водой (350 мл) и сушат над сульфатом натрия. Растворитель выпаривают, а твердый остаток обрабатывают избытком карбоната калия в 20 мл хлороформа при кипячении с обратным холодильником в течение ночи. Экстракция водой, высушивание над сульфатом натрия и выпаривание растворителя дает твердое вещество желтого цвета. Перекристаллизация из этилацетата приводит к получению 0,27 г (выход 16%) 6-(4 п-толил-пиперазин-1-илметил)-4 Н-бензо(5,1 г, 67,3 ммоль) в соответствии с методикой примера 1 с получением маслянистой жидкости 2-(3-гидрокси-4-нитрофенил)-1,3-диоксана (9,6 г, выход 95%). ЯМР-спектроскопия, CDCl3:1.4 (d, 1H),7.05 (d, 1H), 2.2 (m, 1H), 3.9 (t, 2H), 4.2 (d, 2H),5.4 (s, 1H), 7.2 (s, 1H), 8.0 (d, 1H). Пример 10. Получение 4-(хлорацетиламино)-3-гидроксибензальдегид.(9,3 г, 41,2 ммоль) превращают в 4-(хлорацетиламино)3-гидроксибензальдегид по методике примера 2. Выход 3,7 г (35%), маслянистая жидкость. ЯМР-спектроскопия, ДМСО:4.4 (s, 1H),7.3 (s, 1H), 7.4 (d, 1 Н), 8.2 (d, 1H), 9.7 (s, 1H), 9.8(s, 1H), 10.7 (s, 1H). Пример 11. Получение 3-оксо-дигидро-2 Нбензо[1,4]оксазин-7-карбальдегид. 4-(хлорацетил-амино)-3-гидроксибензальдегид (3,7 г, 17,3 ммоль) превращают в 3-оксо 3,4-дигидро-2 Н-бензо[1,4]оксазин-7-карбальдегид (3,2 г, выход 100%) по методике примера 3; Тпл=178-180 С (разл.). Пример 12. Получение 7-(4-п-толилпиперазин-1-илметил)-4 Н-бензо[1,4]оксазин-3 она. Смесь 3-оксо-дигидро-2 Н-бензо[1,4]оксазин-7-карбальдегида (0,5 г, 2,8 ммоль), 1-(4 метил-фенил)-пиперазина (0,5 г, 2,8 ммоль),уксусной кислоты (0,17 г, 2,8 ммоль) и триацетоксиборгидрида натрия (1,2 г, 5,9 ммоль) в 20 мл 1,2-дихлорэтана перемешивают при комнатной температуре в течение 3 ч. Затем реакцию гасят 50 мл воды и разделяют фазы. Водную фазу экстрагируют этилацетатом (350 мл). Органические фазы объединяют и сушат над сульфатом натрия. Выпаривание растворителя дает твердый остаток, который дважды перекристаллизовывают из ацетонитрила с получением 0,31 г (выход 33%) 7-[4-(4-метил-фенил)пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3 она; Тпл=208-210 С. Анализ для С 20 Н 23N3O2: С, 71.19; Н, 6.87; N, 12.45. Полученные величины: С, 71.10; Н, 6.73;N, 12.32. Пример 13. Получение 7-(4-фенилпиперазин-1-илметил)-4 Н-бензо[1,4]оксазин-3 она. 1-фенил-пиперазин (0.45 г, 2.8 ммоль) превращают в 7-(4-фенил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он по методике примера 12 с выходом 34%; Тпл=191-193 С. Пример 14. Получение 7-[4-(3,4-диметилфенил)-пиперазин-1-илметил]-4 Н-бензо-[1,4] оксазин-3-она. По методике примера 12 1-(3,4-диметилфенил)пиперазин (0,54 г, 2,8 ммоль) превращают в 7-[4-(3,4-диметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он с выходом 28%; Тпл=195-197 С. Соединения, перечисленные ниже, могут быть получены в соответствии с описанными выше способами, используя соответствующие исходные материалы. Примеры 15-26. Пример Название соединения Элементный анализ Биологические способы Клеточные линии, экспрессирующие изоформы рецептора допамина. Клеточную линию, экспрессирующую рецепторы допамина Д 2 (длинная форма) приобретали в Университете Медицинских Наук штата Орегон, Портленд, Орегон. Комплементарную ДНК рецептора Д 2 субклонируют в экспрессионном векторе pRc/CMV. Плазмиды трансфецируют путем электропорации в клетки СНО К 1. Выделяют единственный стабильный трансфектант, устойчивый к антибиотику G418,и используют его в исследованиях на связывание. Для связывания Д 4, получают стабильные трансфектанты клеток СНО К 1, экспрессирующие рецептор допамина подтипа Д 4.2, как описано в Shih, et al., "The expression and functionalin CHO K1 cells", Soc. Neurosci., 1995; 21 (Part 1):621. Культура клеток и получение клеточных мембран. Клетки СНО К 1, экспрессирующие либо Д 2, либо Д 4.2 рецепторы человека, выращивают в культуральных флаконах площадью 162 см 2 на среде F12 (Gibco Laboratories, Грэнд Айленд,Нью-Йорк), дополненной 10% фетальной бычьей сыворотки (FBS, Hyclone, Логан, Юта), в атмосфере 5% СO2/95% воздуха при 37 С. Клетки выращивают до слияния, после чего ростовую среду удаляют и заменяют ее на 0,02% этилендиаминтетраацетат (ЭДТА) в фосфатном солевом буфере (Sigma Chemical Co, Сент Луис,Миссури) и соскребают клетки с флакона. Клетки центрифугируют при примерно 1000g 10 мин при 40 С и затем ресуспендируют в буфере ТЕМ (25 мМ Трис-HCl рН 7,4, 5 мМ ЭДТА, и 6 мМ МgСl2) для Д 2 или в буфере Д 4.2 (50 мМ Трис-HCl рН 7.4, 5 мМ ЭДТА, 1,5 мМ СаСl2, 5 мМ КСl, и 120 мМ NaCl) и гомогенизируют. Мембраны переводят в осадок центрифугированием при 20,000g при 40 С в течение 20 мин. Затем осадки ресуспендируют в соответствующем буфере (1 мл на клетки с одного флакона) и хранят при -70 С до использования в тесте на связывание. Тесты на связывание рецептора; рецепторы допамина Д 2 и Д 4.2. Препарат клеточных мембран (400 мкл) в трех повторностях инкубируют с 50 мкл [3 Н] спиперона (0,2 нМ для Д 2, 0,2 нМ для Д 4.2), 50 мкл буфера, либо конкурентных веществ, в конечном объеме 0,5 мл. Через 60 мин при 25 С инкубацию останавливают быстрым фильтрованием через стекловолоконные фильтры Whatman GF/B (пропитанные в течении часа 0,5% 0,5% полиэтиленимином) на клеточном коллекторе с тремя промывками по 1 мл ледяного буфера. Каждый фильтр, содержащий связанный лиганд, помещают в счетный флакон с 4 мл сцинтилляционной жидкости (Ready Gel, Beckman Instrument Inc., Фуллертон, Калифорния) и считают в жидкостном сцинтилляционном счетчике Beckman LS-6800 с эффективностью 45%. Неспецифическое связывание определяют в присутствии 1 мМ галоперидола. Обсчет данных. Данные по насыщению и конкурентному связыванию анализируют, используя программу итеративной нелинейной аппроксимации по методу наименьших квадратов. В конкурентных экспериментах, видимые величины Ki рассчитывали, исходя из величин IC50 по способуreaction Biochem. Pharmacol., 1973;22:30993108. Экспериментальные соединения готовят в виде исходных растворов в диметилсульфоксиде (ДМСО). Конечная концентрация 0,1% ДМСО в инкубационной смеси не оказывала действия на специфическое связывание. Каждое наблюдение проводят в трех повторностях. Для проведения этих расчетов измеряют величины Кi для взаимодействия различных лигандов с рецептором. Это [3 Н]спиперон, Д 2 человека 0,116+0,01 и Д 4.2 человека 0,093+0,005 нМ(n=3). Результаты тестирования приведены ниже. Данные по связыванию Пример где R1 и R2 означают независимо водород или алкил с числом углеродных атомов от 1 до 6,X означает С, N или СН, при этом в случаеX=С штрихованная линия означает связь, а в других случаях отсутствует;R3 означает фенил, нафтил, гетероарил,замещенный фенил, замещенный нафтил или замещенный гетероарил, при этом каждый заместитель независимо выбран из группы, включающей галоген, алкоксигруппу с числом углеродных атомов от 1 до 6, алкил с числом углеродных атомов от 1 до 6, цианогруппу, трифторметил или сульфонамидогруппу; и их фармацевтически приемлемые соли, эфиры, амиды и пролекарства. 2. Соединение по п.1, где группа присоединена к бензоксазиноновой группе по 6 или 7 положению. 3. Соединение по п.1, где R1 и R2 означают водород. 4. Соединение по п.1, где R3 означает фенил, метилтолил, толил или сульфонамидогруппу. 5. Соединение по п.1, где X означает N. 6. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил,R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. 7. Соединение по п.1, где группа присоединена к бензоксазиноновой группе по 6 или 7 положению, при этом X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил,R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. 8. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 и R2 означают водород; R3 означает фенил или замещенный фенил, где каждый заместитель независимо выбран из группы, включающей алкил с числом углеродных атомов от 1 до 6 или сульфонамидогруппу. 9. Соединение по п.1, где X означает N или СН; штрихованная линия отсутствует; R1 означает водород; R2 означает водород или метил,R3 означает фенил, метилтолил, толил или сульфонамидогруппу. 10. Соединение по п.1, представляющее собой 4-[4-(3-оксо-3,4-дигидро-2 Н-бензо[1,4] оксазин-6-илметил)-пиперазин-1-ил]-бензолсульфонамид; 6-[4-(3,4-диметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-п-толил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 6-[4-фенил-пиперазин-1-илметил]-4 Нбензо[1,4]оксазин-3-он; 7-(4-п-толил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-(4-фенил-пиперазин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-[4-(3,4-диметил-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(5-метил-пиридин-2-ил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-п-толил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 6-[4-(3,4-диметил-фенил)-пиперидин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-тиазол-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он; 6-(4-бензотиазол-2-ил-пиперазин-1-илметил)-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4,5-диметил-тиазол-2-ил)-пиперазин 1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-(4-нафталин-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(3,4-дихлор-фенил)-пиперазин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 24 7-[4-(4-метокси-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(4-хлор-фенил)-пиперазин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(3,4-диметил-фенил)-пиперидин-1 илметил]-4 Н-бензо[1,4]оксазин-3-он; 6-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-[4-(4-метокси-фенил)-пиперидин-1-илметил]-4 Н-бензо[1,4]оксазин-3-он; 7-(4-фенил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он; 7-(4-нафталин-2-ил-пиперазин-1-илметил)4 Н-бензо[1,4]оксазин-3-он и 7-(4-п-толил-пиперидин-1-илметил)-4 Нбензо[1,4]оксазин-3-он. 12. Способ лечения психоза или шизофрении, включающий назначение пациенту, страдающему психозом или шизофренией, терапевтически эффективного количества соединения по п.1. 13. Фармацевтически приемлемый состав,включающий соединение по п.1.
МПК / Метки
МПК: A61K 31/535, C07D 265/36
Метки: допамина, рецептора, антагонисты, бензоксазиноновые
Код ссылки
<a href="https://eas.patents.su/13-1486-benzoksazinonovye-antagonisty-receptora-dopamina-d4.html" rel="bookmark" title="База патентов Евразийского Союза">Бензоксазиноновые антагонисты рецептора допамина d4.</a>












