Замещенные дифенильные производные
Формула / Реферат
1. Дифенильное производное формулы (1)
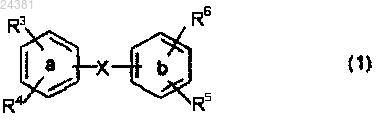
где X представляет собой прямую C-C-связь между кольцами а и b, CH2, CHOH, CO, S, SO, SO2, -N=N- или -CR7=CR8-;
каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, С1-С4-алкокси, С1-С4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группу -OSO2Y;
R7 представляет собой водород, метил, этил или фенил, который замещен R9 и R10 и непосредственно присоединен к R7-несущему атому углерода;
R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH;
каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил, С1-С4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил;
R2 представляет собой метил или этил,
при условии, что на молекулу формулы (1) обязательно приходятся одна или две группы -N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,
или его соли.
2. Дифенильное производное по п.1 формулы (5)

где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, С1-С4-алкокси, С1-С4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группу -OSO2Y;
R7 представляет собой водород, метил, этил или фенил, который замещен R9 и R10 и непосредственно присоединен к R7-несущему атому углерода;
R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH;
каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил, С1-С4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил;
R2 представляет собой метил или этил,
при условии, что на молекулу формулы (5) обязательно приходятся одна или две группы -N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,
или его соли.
3. Дифенильное производное по п.1 формулы (10)
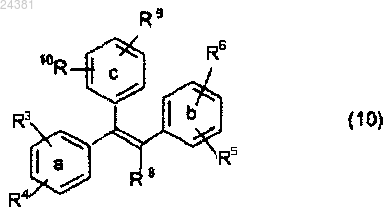
где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, C1-C4-алкокси, C1-C4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группу -OSO2Y;
R8 представляет собой водород, этил, CN, NO2, -CH2-CH2-галоген или CH2CH2OH;
каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, С1-С4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил;
R2 представляет собой метил или этил,
при условии, что на молекулу формулы (10) обязательно приходятся одна или две группы -N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,
или его соли.
4. Дифенильное производное по п.1 формулы (18)
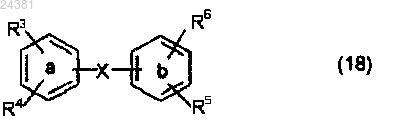
где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2 или -N=N-;
каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил, С1-С1-алкокси, С1-С4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группу -OSO2Y;
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил;
R2 представляет собой метил или этил,
при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы -N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,
или его соли.
5. Дифенильное производное по любому из пп.1 или 4, представляющее собой 4-(3,3-диметилтриазенил-1)-4'-натрий сульфоксибензофенон формулы
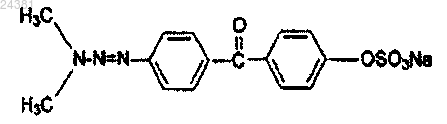
6. Способ получения дифенильного производного по любому из пп.1-5, где аминофенильное производное формулы (2)
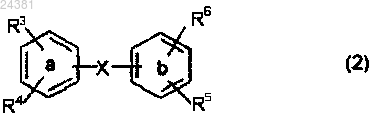
где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2, -N=N- или -CR7=CR8-;
каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил, С1-С4-алкокси, С1-С4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -NH2 или группу -OSO2Y;
R7 представляет собой водород, метил, этил или фенил, который замещен R9 и R10 и непосредственно присоединен к R7-несущему атому углерода;
R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH;
каждый R9, R10 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, C1-C4-алкокси, галоген, нитро, циано, группу -NH2 или группу -OSO2Y;
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил,
при условии, что на молекулу формулы (2) обязательно приходятся одна или две NH2 группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,
диазотируют с помощью диазотирующего агента в присутствии сильной кислоты при низкой температуре в водном растворе с образованием соли диазония формулы (3)
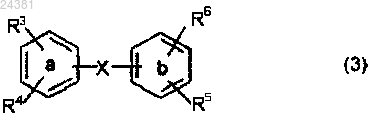
где X представляет собой прямую C-C-связь, CH2, CHOH, CO, S, SO, SO2, -N=N- или -CR7=CR8-;
каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С1-С4-алкил, C1-C4-алкокси, С1-С4-алкил-S-, С1-С4-алкил-SO-, С1-С4-алкил-SO2-, галоген, нитро, циано или группу -OSO2Y;
каждый R4 и R5 независимо друг от друга представляет собой группу -N2+AN- или группу -OSO2Y;
R7 представляет собой водород, метил, этил или фенил, который замещен R9 и R10 и непосредственно присоединен к R7-несущему атому углерода;
R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH;
каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил, С1-С4-алкокси, галоген, нитро, циано, группу -N2+An- или группу -OSO2Y;
An- представляет собой анион галогена или 1/2 сульфат-аниона (SO42-);
Y представляет собой OH или N(R1)2;
R1 представляет собой водород, метил или этил,
при условии, что на молекулу формулы (3) обязательно приходятся одна или две диазоний группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,
и полученные соли диазония формулы (3) затем взаимодействуют с диалкиламинами формулы
HN(R2)2, (4)
где R2 представляет собой метил или этил,
в присутствии связывающих кислоту агентов с получением дифенильного производного формулы (1).
7. Способ по п.6, где дополнительно после реакции солей диазония (3) с диалкиламинами (4) получают соли из полученных соединений.
8. Способ по п.7, где дополнительно после получения солей высвобождают свободные гидроксильные и/или кислотные группы из этих солей.
9. Лекарственное средство для лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов у человека и животных, содержащее по меньшей мере одно дифенильное производное по любому из пп.1-5 или его физиологически приемлемую соль вместе с одним или несколькими фармакологически приемлемыми вспомогательными агентами или основами.
10. Применение по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемой соли для лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов, у человека и животных.
11. Применение по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемых солей для получения противоопухолевого средства для лечения опухолей кожи, а также опухолей мишеневых органов, зависимых от половых гормонов, у человека и животных.
12. Применение по п.11, где опухоль мишеневых органов, зависимых от половых гормонов, представляет собой опухоль молочной железы, опухоль предстательной железы или опухоль яичек.
13. Способ лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов, у человека и животных, включающий введение достаточного количества по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемой соли.
Текст
Изобретение относится к дифенильным производным формулы (1), где заместители определены в формуле изобретения, способу их получения и применению в качестве лекарственного средства для лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов, у человека и животных. Настоящее изобретение относится к замещенным дифенильным производным, содержащим (i) по меньшей мере одну диалкилтриазенильную группу, (ii) по меньшей мере одну сульфоксигруппу и/или по меньшей мере одну сульфамоилоксигруппу на молекулу, и к их солям. Кроме того, изобретение относится к способу получения этих соединений и к их применению в качестве лекарственных средств. Для целей настоящего изобретения дифенильные производные представляют собой фенильные кольца, присоединенные единичной связью или мостиком. Известны триазензамещенные дифенильные производные. Так, в документах DE 1793115 A1,DE 2147781 А 1 и WO 2004/106358 А 1 описаны, кроме прочего, дифенильные производные, которые замещены триазеновыми группами и, например, группами сульфоновой кислоты или оксикарбоновой кислоты. За последние десятилетия триазеновые производные интенсивно исследуются на цитостатическую эффективность. Эти обычные триазеновые цитостатические средства относятся к группе алкилирующих соединений и из-за своих тяжелых побочных эффектов и токсичности никогда не имели широкого клинического применения. Исключение составляет дакарбазин (DTIC), который является пролекарством монометилтриазеноимидазолкарбоксамида (MTIC) и используется, главным образом, при борьбе с лимфомой Ходжкина и саркомой мягких тканей (Cancer Treatment Reports, 60:205-211 (1976. По причине светочувствительности дакарбазина и, в частности, из-за его побочных эффектов, среди которых наиболее важными являются лейкопения и тромбопения, было исследовано большое число арилалкилтриазенов для того, чтобы синтезировать более сильные триазены с лучшей переносимостью (Cancer TreatmentReports, 60:125-134 (1976); J. Med. Chem. 23, 1052-1024 (1980. Несмотря на эти усилия, дакарбазин и темозоломид до настоящего времени являются единственными триазенами, используемыми для клинического применения в лечении глиобластомы, хотя они связаны со значительными побочными эффектами, такими как угнетение костного мозга, нейротоксичность и токсичность для печени, рвота, выпадение волос и экзантема. Первая попытка решить проблему переносимости выбранных триазенов с точки зрения их селективного применения для лечения рака молочной железы описана в документе DE 1793115 А 1 иDE 2147781 А 1. Вторая попытка преодолеть тяжелые побочные эффекты выбранных триазенов была описана в документе WO 2004/106358 А 1. Утверждается, что некоторые тяжелые побочные эффекты известных триазенов снижаются при введении группы оксикарбоновой кислоты. Однако из-за нежелательных побочных эффектов на почки они не подходят для длительного применения. Целью настоящего изобретения является получение соединений, обладающих противоопухолевой активностью, которые подходят для длительной терапии и практически не имеют токсичных побочных эффектов, и при этом обладают улучшенной эффективностью. Авторами изобретения были обнаружены новые дифенильные производные, содержащие (i) по меньшей мере одну диалкилтриазенильную группу и (ii) по меньшей мере одну сульфоксигруппу и/или по меньшей мере одну сульфамоилоксигруппу на молекулу, и их соли, сольваты и сольваты этих солей. Новые дифенильные производные по изобретение имеют неожиданный значительно улучшенный противоопухолевый эффект в отношении опухолей важных мишеневых органов (например, толстая кишка, легкие, печень, поджелудочная железа, почки), в частности, в качестве селективных противоопухолевых средств при опухолях кожи, молочной железы, предстательной железы и яичек, а также мишеневых органов, зависимых от половых гормонов, по сравнению с аналогичными известными активными соединениями (WO 2004/106358 A1, DE 1793115 А 1 и DE 2147781 А 1). По сравнению с аналогичными известными активными соединениями они практически не имеют токсичных побочных эффектов и, поэтому, подходят для длительной терапии. Благодаря своей лучшей переносимости наряду с высокой эффективностью, они могут использоваться в медицинских целях как в виде монотерапии, так и в сочетании с другими канцеростатическими средствами, опухолеспецифическими антителами или антителами, которые присоединены через линкеры к соединениям по изобретению. Внутри клеток они нормализуют пролиферативно-ингибирующий/противоопухолевый эффект, который может остановить неконтролируемый репликативный метаболизм опухолевых клеток и даже привести к регрессии опухоли. Новые дифенильные производные могут использоваться в качестве активных соединений в лекарственных препаратах для человека и животных. Дифенилтриазены, имеющие группу серной кислоты и амидную группу серной кислоты в молекуле, не были описаны и не было информации о какой-либо их эффективности. Для целей настоящего изобретения, предпочтительными являются замещенные дифенильные производные формулы (1) где X представляет собой прямую C-C-связь между кольцами а и b, CH2, CHOH, СО, S, SO, SO2,-N=N- или -CR7=CR8-; каждый R3, R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (1) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их соли. Авторы изобретения также обнаружили способ получения новых дифенильных производных, содержащих (i) по меньшей мере одну диалкилтриазенильную группу и (ii) по меньшей мере одну сульфоксигруппу и/или по меньшей мере одну сульфамоилоксигруппу на молекулу, и их солей, который отличается тем, что аминофенильные производные формулы где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO, -N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -NH2 или группу -OSO2Y;R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9, R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -NH2 или группу -OSO2Y;R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (2) обязательно приходятся одна или две NH2 группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,диазотируют с помощью дизотирующего агента в присутствии сильной кислоты при низкой температуре в водном растворе с образованием соли диазония формулы (3) где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2, -N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-G4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N2+AN- или группу -OSO2Y;R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, галоген, нитро, циано, группу -N2+An- или группу -OSO2Y;An- представляет собой анион галогена или 1/2 сульфат-аниона (SO42-);R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (3) обязательно приходятся одна или две диазоний группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,и полученные соли диазония формулы (3) затем взаимодействуют с диалкиламинами формулы Н N(R2)2 (4),2 где R представляет собой метил или этил,в присутствии связывающих кислоту агентов с получением дифенильного производного формулы(1),после чего, необязательно, получают соли из полученных соединений и, необязательно, высвобождают свободные гидроксильные и/или кислотные группы из этих солей. Растворителями, подходящими для реакции диазотирования, являются все полярные растворители,которые являются инертными в реакционных условиях, например спирты, такие как метанол, этанол, а также диметилформамид и диметилсульфоксид и, в частности, вода, или смеси этих растворителей. В качестве сильной кислоты в реакции диазотирования можно использовать галогенводородные кислоты, предпочтительно хлористо-водородную кислоту, или серную кислоту. В качестве диазотирующих агентов предпочтение отдают нитриту калия и нитриту натрия. В качестве кислотных акцепторов в реакции присоединения можно использовать все обычные агенты, связывающие кислоты. К ним предпочтительно относятся карбонат натрия и карбонат калия. Для целей изобретения солями являются предпочтительно физиологически приемлемые соли. К ним относятся соли обычных оснований, например соли щелочных металлов (например, соли натрия и соли калия), соли щелочно-земельных металлов (например, соли кальция и соли магния) и соли аммония,полученные из аммония или органических С 1-С 16-аминов, таких как этиламин, диэтиламин, триэтиламин,этилдиизопропиламин, моноэтаноламин, диэтаноламин, трисгидроксиэтиламин, дициклогексиламин,диметиламиноэтанол, дибензиламин, N-метилморфолин, дигидроабиетиламин, аргинин, лизин, этилендиамин и метилпиперидин. В качестве альтернативы дифенильные производные по изобретению могут быть получены путем введения сначала триазенильных групп и только после этого путем введения сульфокси и/или сульфамоилоксигрупп. Для этой цели триазенилфенолы формулы где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2, -N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -NH2 или группу -OSO2Y;R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9, R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -NH2 или группу -OSO2Y;R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (2) обязательно приходятся одна или две NH2 группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,могут быть затем сульфатированы или сульфоамидированы. Дифенильные производные по изобретению описаны более подробно ниже, в зависимости от определения X: 1. цис- и транс-Стилбены формулы (5). Если X в формуле (1) представляет собой -CR7=CR8-, то соединения по изобретению имеют формулу где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (5) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их соли. Предпочтение отдают соединениям формулы (5), в которой каждый R3 и R6 представляет собой группу -OSO2Y в 4-м положении и в 4'-м положении; каждый R7 и R8 представляет собой этил иY представляет собой OH или NH2,при условии, что на молекулу формулы (5) обязательно приходятся одна или две группы-N=N-N(CH3)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Кроме того, предпочтение отдают соединениям формулы (5), в которой каждый R4 и R5 независимо друг от друга представляет собой водород, группу (CH3) 2N-N=N- или группу -OSO2Y; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, метил, метокси или группу -OSO2Y; каждый R7 и R8 представляет собой водород иY представляет собой OH или NH2,при условии, что на молекулу формулы (5) обязательно приходятся одна или две -N=N-N(CH3)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Особое предпочтение отдают соединениям формулы (5), в которойR3 представляет собой водород, гидроксил или группу -OSO2Y в 4-м положении;R4 представляет собой группу -OSO2Y во 2-м положении;R5 представляет собой группу (CH3)2N-N=N- в 4'-м положении;R6 представляет собой водород или метил во 2'-м положении; каждый R7 и R8 представляет собой водород иY представляет собой OH или NH2,при условии, что на молекулу формулы (5) обязательно приходятся одна или две группы-N=N-N(CH3)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. В качестве особенно предпочтительных стилбенов формулы (5) для целей изобретения могут быть указаны следующие соединения: или их соли. Соединения формулы (5) могут быть получены способом, аналогичным способу получения соединений формулы (1), из ароматических аминов где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, C1-C4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (6) обязательно приходятся одна или две группы -NH2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец. Если, например, в качестве исходных веществ используются 3,3'-диамино-4,4'-дикалийсульфокси 1,2-диэтилстилбен, нитрит калия и диметиламин, то направление реакции может быть представлено такой схемой: 3,3'-Диамино-4,4'-дикалийсульфокси-1,2-диэтилстилбен, показанный в схеме реакции (7), может быть получен из известного 3,3'-динитриодиэтилстилбестрола (Arch. Pharm. (Weinheim) 311, 184-195(1978 с последующим сульфатированием и восстановлением до диамина. Ароматические амины формулы (6) могут быть получены, по существу, известным способом из соответствующих нитросульфоксиароматических веществ или нитросульфамоилоксиароматических веществ, например путем каталитического восстановления с помощью водорода над палладием/углем в этаноле или над оксидом палладия в метаноле (Chem. Berichte. 72, 839, [(1939)]) или используя никель Ренея в ТГФ (Chem. Berichte. 91, 1905 (1958. Способы синтеза, указанные в настоящем документе, также могут быть использованы для синтеза ароматических аминов, использованных в разделах 2-4. Примеры преобразования ароматических аминов до солей диазония и реакция присоединения их с диалкиламинами с образованием (3,3-диалкилтриазенил-1)арилов подробно описаны в документахDE 1793115 A1, DE 2L47781 A1, GB 1371969 и WO 2004/106358. Получение новых исходных веществ, имеющих сульфокси или сульфамоилоксигруппы, может быть осуществлено с помощью реакции соответствующих ароматических фенолов с бисульфатом щелочного металла (Na, K), как описано в документе ЕР 0722455 A1/US 5703261, необязательно, в качестве альтернативы, с хлорсульфоновой кислотой/пиридином, как описано в документе WO 02/134715 А 1, или с сульфамоилхлоридами в диметилацетамиде, как описано в документах WO 2008/003378 иUS 2003/0225051, с. 44. Варианты синтеза, указанные в настоящем документе, также могут быть использованы в реакциях в соответствии с разделами 2-4 при преобразовании феноловой гидроксильной группы до исходных веществ или конечных продуктов по изобретению, имеющих сульфокси- или сульфамоилоксигруппы. Синтез соединений по изобретению может быть проиллюстрирован схемами реакции 8 и 9: 2. Трифенилэтиленовые производные формулы (10). Если в формуле (1) X представляет собой -CR7=CR8-, a R7 представляет собой фенил, который замещен R9 или R10, и непосредственно присоединен к R7-несущему атому углерода, то эти соединения имеют формулу где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR3 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (1) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или его соли. Предпочтение отдают соединениям формулы (10), в которойR3 представляет собой водород, гидроксил, метокси или группу -OSO2Y;R4 представляет собой группу -N=N-N(CH3)2 в 3-м положении;R5 представляет собой группу -N=N-N(CH3)2 в 3'- или 4'-м положении;R6 представляет собой водород, гидроксил, метокси или группу -OSO2Y в 3'- или 4'-м положении;R8 представляет собой водород, этил, -CH2CH2- или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой гидроксил, метокси или группуY представляет собой OH или NH2,при условии, что на молекулу формулы (1) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Особое предпочтение отдают соединениям формулы (10), в которойR3 представляет собой водород, гидроксил, метокси или группу -OSO2Y в 4-м положении;R4 представляет собой группу -N=N-N(CH3)2 в 3-м положении;R5 представляет собой группу -N=N-N(CH3)2 в 3'- или 4'-м положении;R6 представляет собой водород, гидрокси, метокси или группу -OSO2Y в 4'-м положении;R8 представляет собой водород или этил; каждый R9 и R10 представляет собой, независимо друг от друга гидроксил, метокси или группуY представляет собой OH или NH2,при условии, что на молекулу формулы (10) обязательно приходятся одна или две группы-N=N-N(CH3)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. 3. В качестве особенно предпочтительных трифенилэтиленовых производных формулы (10), можно указать следующие соединения: 1,1-[бис-3,4-(динатрий сульфоксифенил)]-2-этил-2-[4'-(3,3-диметилтриазено-1)фенил]этен или их соли. Соединения формулы (10) могут быть получены способом, аналогичным способу получения соединений формулы (1), из соответствующих ароматических аминов где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, C1-C4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2-CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (10) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b. Если в качестве исходных веществ используются, например, 1-(4-аминофенил)-1-(4-натрий сульфоксифенил)-2-этил-2-фенилэтен, нитрит натрия и диметиламин, то направление реакции может быть представлено следующей схемой: В этом случае соль диазония получают на первой стадии и она незамедлительно может вступать в реакцию с диметиламином на второй стадии с образованием 1-(4-(3,3-диметилтриазено-1-фенил)-1-(4 натрий сульфоксифенил)-2-этил-2-фенилэтена. Ароматические амины формулы (11) могут быть получены из соответствующих нитросульфоксиароматических веществ или нитросульфамоилоксиароматических веществ общеизвестными способами, например, путем каталитического восстановления с помощью водорода над палладием/углем в этаноле или используя Ra-Ni в ТГФ. Трифенилэтиленовые производные формулы (10) могут быть получены путем, показанным на схеме реакции (13). В этом случае синтез проводят известными способами, такими как реакция Виттига,восстановление нитрогруппы с помощью никеля Ренея/гидразина, отщепление эфира, получение триазенилфенола и реакция его с бисульфатом щелочного металла или сульфамоилхлоридом. Вместо бисульфата щелочного металла в ДМФ также можно использовать хлорсульфоновую кислоту в пиридине. 4. Дифенильные производные формулы (18), которые либо не связаны мостиками, либо связаны мостиками с помощью атомов или диатомных групп. В соответствии с изобретением соединение формулы (1) может также быть в форме, показанной формулой где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2 или -N=N-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C1-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR2 представляет собой метил или этил,при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или его соли. Предпочтение отдают соединениям формулы (18), в которойX представляет собой CH2, СО, SO или SO2; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, метил, этил, метокси, CH3S-, CH3SO-, CH3SO2-, галоген (F, Cl, Br, I), нитро, циано или группу -OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(CH3)2 или группуY представляет собой OH или NH2,при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Особое предпочтение отдают соединениям формулы (18), в которойX представляет собой CH2, СО, SO или SO2; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, метил, фтор,хлор, бром или группу -OSO2Y;R5 представляет собой группу (CH3)2N-N=N;Y представляет собой OH или NH2,при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Наибольшее предпочтение отдают соединениям формулы (18), в которойR3 представляет собой гидроксил, метил, хлор или бром во 2-, 3- или 4-м положении;R4 представляет собой группу -OSO2Y во 2-, 3- или 4-м положении;R5 представляет собой группу (CH3)2N-N=N в 4'-м положении;R6 представляет собой водород, метил, фтор, хлор или бром во 2'-, 3'- или 5'-м положении;Y представляет собой OH или NH2,при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или их солям. Наиболее предпочтительные дифенильные производные, связанные мостиком с помощью диатомарной или триатомарной группы, включают следующие соединения: 4-(3,3-диметилтриазенил-1)-4'-гидрокси-2'-натрий сульфоксибензофенон или их соли. Особое предпочтение отдают 4-(3,3-диметилтриазенил-1)-4'-натрий сульфоксибензофенону Исходные вещества для синтеза соединений формулы (18) известны и могут быть получены способом, описанным в документе GB 1373969, и использованы для синтеза соединений формулы (18) путем преобразования гидрокситриазеновых производных формулы (19), описанных в настоящем документе,до конечных продуктов, например соединений формулы (20), как показано в качестве примера на реакционной схеме (21). где значение Y указано в легендах для формулы (18). Настоящее изобретение, кроме того, относится к дифенильным производным, содержащим (i) по меньшей мере одну диалкилтриазенильную группу и (ii) по меньшей мере одну сульфоксигруппу и/или по меньшей мере одну сульфомоилоксигруппу на молекулу, и их солям для применения в качестве лекарственных средств и также к применению этих соединений для получения лекарственных средств предпочтительно для лечения злокачественных новообразований тканей, зависимых от эстрогенов, в частности, опухолей половых органов с эстроген-негативными рецепторами и эстраген-положительными рецепторами, и меланомы. В предпочтительных вариантах осуществления настоящего изобретения замещенные дифенильные производные по изобретению могут использоваться в сочетании с моноклональными антителами. В соответствии с настоящим изобретением предпочтение отдают использованию моноклональных антител, которые имеют высокую селективность в отношении опухолевых клеток (Discovery Medicine,Alain Beck, "The next generation of Antibody-drug Conjugates Comes of Age", October 16, 2010). Замещенные дифенильные производные по изобретению связывают с моноклональным антителом и вводят в опухолевые клетки. В целом, дифенильные производные по изобретению и моноклональные антитела используются в соотношении от 0,5:1 (дифенильное производное к антителу) до 4:1. Моноклональные антитела известны per se. Моноклональные антитела являются иммунологически активными белками, которые продуцируются из клеточной линии, возвращенной до одного В-лимфоцита, и направлены против одного эпитопа (например, опухолевой клетки). Соединения по изобретению могут, например, использоваться для лечения следующих типов опухолей: рака груди (карцинома молочной железы), рака матки (карцинома эндометрия, карцинома corpus),рака шейки матки, рака яичников (карцинома яичников), рака влагалища, рака предстательной железы,рака кожи, меланомы (меланома maligma). Изобретение, кроме того, относится к применению соединений по изобретению в комбинации по меньшей мере с одним дополнительным химиотерапевтическим средством для лечения злокачественного новообразования. Соединения по изобретению также могут использоваться в комбинации с дополнительными химиотерапевтическими средствами, известными для лечения злокачественного новообразования или опухолей, и/или с лекарственными средствами, которые вводят вместе с химиотерапевтическими средствами во время химиотерапии. Примеры таких химиотерапевтических средств, которые могут использоваться в комбинации с другими лекарственными средствами, используемыми в химиотерапии, описаны, например, в документеWO/2007/061978 в разделе "Комбинированная терапия" (с. 23, строка 1 - с. 30, строка 18) или в документе US 2007/135424 А 1 (параграфы 153-171). Для этих способов введения активное соединение может вводиться в подходящей для введения форме. Для перорального введения подходящими являются известные формы введения, которые быстро высвобождают активное соединение и/или высвобождают активное соединение в модифицированной форме, например, таблетки (таблетки без покрытия и с покрытием, например, таблетки с покрытиями,устойчивыми к желудочному соку, или таблетки, покрытые пленкой), капсулы, драже, гранулы, шарики,порошки, эмульсии, суспензии и аэрозоли. Парентеральное введение может осуществляться в обход стадии резорбции (внутривенно, внутриартериально, внутрисердечно, интраспинально или интралюмбально) или с вовлечением резорбции(внутримышечно, подкожно, внутрикожно, чрескожно или внутрибрюшинно). Вводимые формы, подходящие для парентерального введения, представляют собой, в частности, препараты для инъекций и инфузий в форме растворов, суспензий, эмульсий, лиофилизатов и стерильных порошков. Для других методов введения подходящими формами являются, например, лекарственные средства для ингаляции (включая порошки для ингаляторов, небулайзеров), капли/растворы в нос, спреи; таблетки или капсулы для лингвального, сублингвального и защечного введения, суппозитории, препараты для ушей и глаз, пессарии, водные суспензии (лосьоны, растворы, требующие взбалтывания), липофильные суспензии, мази, кремы, молочко, пасты, порошок для присыпания или имплантаты. Активные соединения могут быть преобразованы способом, известным per se, в описанные формы для введения. Это можно осуществить, используя инертные, нетоксические, фармацевтически подходящие вспомогательные агенты. Они включают, среди прочих, агенты основы (например, микрокристаллическая целлюлоза), растворители (например, жидкие полиэтиленгликоли), эмульгаторы (например, натрий додецилсульфат), диспергирующие агенты (например, поливинилпирролидон), синтетические и природные биополимеры (например, альбумин), стабилизирующие агенты (например, антиоксиданты,такие как аскорбиновая кислота), красители (например, неорганические пигменты, такие как оксиды железа) или вкусовые агенты и/или ароматизаторы. В целом, в случае парентерального введения рекомендуется введение в количестве от около 1 до 40 мг/кг, предпочтительно от около 2,5 до 15 мг/кг массы тела для достижения эффективных результатов. В случае перорального введения количество составляет от 1 до 70 мг/кг, предпочтительно от около 1 до 50 мг/кг массы тела. Однако может быть необходимым сделать отклонение от вышеуказанных количеств в зависимости от массы тела, способа введения, ответа у индивидуума на активное соединение, типа препарата и времени или интервала, в который производится введение. Таким образом, в некоторых случаях может быть достаточным использование меньших количеств, чем вышеприведенные минимальные количества, а в других случаях верхний предел вышеуказанных количеств будет превышен. В случае введения относительно больших количеств может быть целесообразно разделить это количество на множество отдельных доз для приема в течение дня. Настоящее изобретение дополнительно относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение по изобретению вместе по меньшей мере с одним фармацевтически приемлемым носителем, вспомогательным веществом или растворителем. Эти носители, вспомогательные вещества или растворители являются обычными фармацевтическими носителями, вспомогательными веществами или растворителями. Фармацевтические композиции по изобретению подходят, например, для ингаляции или внутривенного, внутрибрюшинного, внутримышечного, интравагинального, интрабуккального, чрескожного,подкожного, кожно-слизистого, перорального, ректального, трансдермального, местного, чрезкожного,внутрижелудочного или внутрикожного введения и представлены, например, в форме пилюль, таблеток,таблеток, которые устойчивы к воздействию желудочного сока, таблеток с пленочным покрытием, таблеток с покрытием, составов для замедленного высвобождения для перорального, подкожного или кожного введения (в частности, в качестве лейкопластырей), составов-депо, драже, свечей, гелей, мазей, сиропов, порошков для ингаляций, гранул, суппозиториев, эмульсий, дисперсий, микрокапсул, микросоставов, наносоставов, липосомальных составов, капсул, капсул, устойчивых к воздействию желудочного сока, порошков, горошков для ингаляций, микрокристаллических составов, спреев для ингаляций, пылевидных препаратов, капель, капель в нос, спреев для носа, аэрозолей, ампул, растворов, соков, суспензий,эмульсий, растворов для инфузий или растворов для инъекций и тому подобного. Примеры Проценты в следующих примерах являются, если не указано иного, процентами по массе; части приведены как части по массе. Соотношения растворителей, соотношения разведений и концентрации жидкости/растворов жидкостей в каждом случае приведены по объему. 1. Производные стилбенов формулы (5). Исходные вещества. Пример 1.1. 2-Натрий сульфоксибензальдегид. Следующий способ может служить образцом сульфатирования с помощью бисульфатов щелочного металла: 12,2 г (0,1 моль) 2-гидроксибензальдегида и 33,3 г (0,15 моль) дисульфата натрия смешивали с 100 мл диметилформамида и 130 мл тетрагидрофурана и перемешивали при комнатной температуре в течение 30 ч. Затем к реакционной смеси добавляли 200 мл 1 н. водного раствора карбоната натрия, смесь перемешивали, фильтровали и фильтрат упаривали при пониженном давлении. Остаток растворяли в минимальном количестве воды, фильтровали через активированный уголь и фильтрат упаривали на роторном испарителе. Вещество, указанное в заголовке, может далее взаимодействовать как исходный продукт. Пример 1.2. 4-Натрий сульфоксибензальдегид. Соединение получают способом, аналогичным способу получения 1.1, и далее он взаимодействует как исходный продукт. 3-Натрий сульфоксибензальдегид может быть получен аналогичным образом. Пример 1.3. 2-Сульфамоилоксибензальдегид. Способ ниже может быть образцом сульфамилирования с использованием сульфамоилхлорида. 12,46 г (0,11 моль) сульфамоилхлорида по каплям добавляли в раствор 12,2 г (0,1 моль) 2-гидроксибензальдегида в 200 мл безводного диметилацетамида при 0-5 С. Реакционную смесь перемешивали при комнатной температуре в течение 3 ч и экстрагировали 1000 мл этилацетатом, органическую фазу промывали насыщенным водным раствором гидрокарбоната натрия, сушили над сульфатом натрия, и растворитель удаляли на роторном испарителе. Остаток насыщали раствором этилацетата/петролейным эфиром, кристаллизовали и отфильтровывали отсасыванием. Пример 1.4. 4-Сульфамоилоксибензальдегид. Синтез аналогичен синтезу примера 1.3. 3-Сульфамоилокси производные 3-гидроксибензальдегида могут быть получены аналогичным образом. Пример 1.5. Хлорид (4-нитробензил)трифенилфосфора. Раствор 263 г (1 моль) трифенилфосфина и 172 г (1 моль) хлорида 4-нитробензила в 2 л толуола перемешивали в точке кипения в течение 15 ч. Реакционную смесь охлаждали, кристаллы отфильтрованный отсасыванием и промывали толуолом. Пример 1.6. (Z- и Е)-2-Натрий сульфокси-4'-нитростилбен 0,04 моль метоксида натрия (в растворе метанола) и раствор 17,3 г соли фосфония (из примера 1.5) в 40 мл метанола одновременно небольшими порциями по каплям добавляли в раствор 8,9 г (0,04 моль) натрия бензальдегид-2-сульфата в 50 мл метанола при 0 С при перемешивании. После осветления реакционного раствора растворитель отдистиллировывали на роторном испарителе. Твердый продукт экстрагировали 100 мл этилацетатом при перемешивании для удаления трифенилфосфиноксида, отфильтровавали отсасыванием, сушили на воздухе, затем кипятили с нитрометаном и отделяли от нерастворимого остатка (транс-соединение) путем фильтрации отсасыванием. При охлаждении цис-соединение откристаллизовывали от фильтрата и, необязательно, перекристаллизовали еще раз. Пример 1.7. (Z- и Е)-4-Метокси-2-натрий сульфокси-4'-нитростилбен Синтез аналогичен синтезу примера 1.6. Пример 1.8. (Z- и Е)-4-Нитро-2'-сульфамоилоксистилбен При 0-5 С 13,15 г (0,05 моль) соль фосфония примера 1.5 и 0,05 моль раствор натрия метоксида постепенно одновременно добавляли (после осветления в каждом случае) к раствору, состоящему из 10,4 г(0,05 моль) альдегида примера 1,3 и 75 мл этанола. После осветления реакционного раствора растворитель удаляли на роторном испарителе и остаток перемешивали с 50 мл толуола для удаления трифенилфосфина и отфильтровывали отсасыванием. Остаток, который оставался, нагревали с 75 мл ацетонитрила и отфильтровывали горячий раствор отсасыванием. Оставалось транс-соединение. цис-Соединение откристаллизовывали из ацетонитрила при охлаждении и необязательно перекристаллизовывали из ацетонитрила или изопропанола. Пример 1.9. (Z)-4-Амино-(2-натрий сульфокси)стилбен 3,4 г (0,01 моль) Z-нитросоединения примера 1.8 гидрировали в 300 мл метанола или ТГФ и 20 мл воды, используя 4 г Ra-Ni при комнатной температуре и 2 атм. После того как необходимое количество водорода было поглощено, катализатор отфильтровывали отсасыванием и растворитель отдистиллировывали. Остаток далее взаимодействовал как исходный продукт. Следующие аминосоединения получали аналогичным образом. Пример 1.10. (Е)-4-Амино-2'-натрий сульфоксистилбен (из примера 1.6 Е) Раствор, состоящий из 3,5 г нитрита натрия и 5 мл воды, по каплям добавляли в раствор, состоящий из 15,6 г (0,05 моль) цис-аминостилбена примера 1.9, 100 мл воды и 13 мл конц. хлористо-водородной кислоты, при 0 С, и смесь перемешивали в течение 10 мин. Полученный раствор соли диазония затем быстро по каплям добавляли в раствор, состоящий из 30 г карбоната натрия, 60 мл воды и 7 г водного раствора диметиламина с крепостью 40%. Смесь перемешивали в течение еще 40 мин и реакционный раствор упаривали на роторном испарителе. Остаток растворяли в минимально необходимом количестве воды при 50 С и для выпадения в осадок соединения, указанного в заголовке, использовали насыщенный водный раствор хлорида натрия, его отфильтровывали отсасыванием и сушили. Продукт может быть перекристаллизован из раствора хлорида натрия или из метанола/воды. Следующее соединение получали аналогичным образом. Пример 1.14. (Е)-4-(3,3-Диметилтриазенил-1)-2'-натрий сульфоксистилбен Раствор, состоящий из 3,5 г нитрита натрия и 5 мл зоды, по каплям добавляли к раствору, состоящему из 15,6 г (0,05 моль) Z-аминостилбена примера 1.11, 100 мл воды и 10 мл конц. хлористоводородной кислоты, при 0 С и смесь перемешивали в течение еще 10 мин. Полученный раствор соли диазония затем быстро добавляли по каплям в раствор, состоящий из 30 г карбоната натрия, 60 мл воды и 7 г водного раствора диметиламина с крепостью 40%. Смесь перемешивали в течение еще 40 мин, добавляли 50 мл воды и смесь экстрагировали 300 мл этилацетатом. Органическую фазу отделяли, промывали 300 мл насыщенного водного раствора гидрокарбоната натрия, сушили над сульфатом натрия и упаривали. Продукт очищали с помощью хроматографии и затем необязательно перекристаллизовывали из этанола/циклогексана. Пример 1.16. (Е)-4-(3,3-Диметилтриазенил-1)-2'-сульфамоилоксистилбен (из примера 1.12) 2. Производные трифенилэтилена формулы (12). Исходные вещества. Пример 2.1. [бис-(4-Метоксифенил)]бромметан (CH3O-C6H4-)2CH-Br. Бромоводород пропускали через суспензию 100 г бис-(4-метоксифенил)карбинола и 46 г хлорида кальция в 2 л толуола для насыщения. Выпавшую соль отфильтровывали отсасыванием и фильтрат упаривали. Желтый масляный осадок далее взаимодействовал в исходной форме. Соединение, указанное в заголовке, получали из бромида примера 2.1 способом, аналогичным способу примера 1.5. Пример 2.3. 1,1-[бис-(4-Метоксифенил)]-2-(4-нитрофенил)этен 4,5 г (0,1 моль) гидрида натрия (дисперсия в масле крепостью 53%) вводили в абсолютно сухих условиях в 50 мл DMSO. Смесь нагревали до 70-80 С до прекращения выделения водорода. При охлаждении на льду по каплям добавляли 57 г (0,1 моль) соль фосфония примера 2.2, растворенную в 150 млDMSO, и смесь перемешивали в течение еще 1 ч. Затем по каплям добавляли 15,1 г (0,1 моль) 4-нитробензальдегида, растворенного в 50 мл DMSO, и смесь перемешивали при комнатной температуре в течение еще 15 ч. Затем добавляли 600 мл воды, смесь экстрагировали 500 мл этилацетатом, растворитель удаляли на роторном испарителе и продукт отделяли от трифенилфосфин оксида через колонку с оксидом алюминия. Толуол/этилацетат (9:1) использовали в качестве элюанта. Вторую фракцию освобождали от растворителя на роторном испарителе и далее он взаимодействовал как исходный продукт. Пример 2.4. 1,1-[бис-(4-Метоксифенил)]-2-(4-аминофенил)этен 15,26 г (0,042 моль) нитросоединения примера 2.4 нагревали до кипячения в 500 мл этанола, смешивали с 66 г 80% раствора гидразина гидрата (1,06 моль N2H4) и быстро охлаждали до 50 С и затем смешивали при перемешивании со свежеприготовленным никелем Ренея, суспендированным в нейтральной среде этанола, до тех пор, пока не прекращалось выделение газа при добавлении дополнительной порции катализатора. Смесь затем нагревали при кипячении с обратным холодильником в течение еще 1 ч и горячий реакционный раствор фильтровали. После того как остаток промывали на фильтре 250 мл горячего этанола, объединенные фильтраты упаривали досуха при пониженном давлении и остаток необязательно перекристаллизовывали из этанола. Пример 2.5. 1,1-[бис-(4-Гидроксифенил)]-2-(4-аминофенил)этена По каплям добавляли 84 г конц. хлористо-водородной кислоты к раствору 33 г (0,1 моль) соединения примера 2.4 и 66 мл пиридина. Реакционный раствор затем нагревали при L50C в течение 3 ч и потом упаривали досуха на роторном испарителе, помещали в 200 мл воды и нейтрализовали. Твердый продукт реакции отфильтровывали отсасыванием и сушили. Полученный продукт был далее использован в реакции. 13,55 г (0,05 моль) 1,1-[бис-(4-гидроксифенил)]-2-(4-аминофенил)этена примера 2.5 растворяли в растворе, состоящем из 13 мл концентрированной хлористо-водородной кислоты и 80 мл воды. К нему медленно по каплям добавляли раствор, состоящий из 10 мл воды и 3,5 г нитрита натрия, при 0-5 С при перемешивании. Полученный раствор соли диазония затем быстро по каплям добавляли при 0-5 С к раствору, состоящему из 15 г карбоната натрия, 60 мл воды и 7 г водного раствора диметиламина крепостью 40%. Смесь затем перемешивали в течение еще 30 мин, нейтрализовали, и вещество, указанное в заголовке, отфильтровывали отсасыванием как твердый продукт, необязательно перекристаллизовывали из нитропропана и сушили. Полученный продукт был далее использован в реакции. Конечные продукты. Пример 2.7. 1,1-[бис-4-(Натрий сульфоксифенил)]-2-[4-(3,3-диметилтриазенил-1)фенил]этен 3,60 г (0,01 моль) соединения примера 2.6 и 6,6 г (0,03 моль) бисульфата натрия смешивали с 10 мл диметилформамида и 13 мл тетрагидрофурана и перемешивали при комнатной температуре в течение 30 ч. К реакционной смеси затем добавляли 20 мл 1 н. водного раствора карбоната натрия, смесь перемешивали, твердый продукт отфильтровывали отсасыванием и фильтрат упаривали при пониженном давлении. Остаток растворяли в минимальном необходимом количестве воды, фильтровали через активированный уголь, фильтрат упаривали на роторном испарителе и остаток перекристаллизовывали из метанола/вода. Пример 2.8. 1,1-[бис-4-(Сульфамоилоксифенил)]-2-[4-(3,3-диметилтриазенил-1)фенил]этен 4 г (0,033 моль) сульфамоилхлорида по каплям добавляли к 3,60 г (0,01 моль) соединения примера 2.6 в 20 мл безводного диметилацетамида при 0-5 С. Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Смесь экстрагировали 100 мл этилацетатом, органическую фазу промывали насыщенным водным раствором гидрокарбоната натрия, сушили над сульфатом натрия и растворитель отдистиллировывали на роторном испарителе. Остаток насыщали раствором этилацетата/петролейного эфира, вызывали кристаллизацию и отфильтровывали отсасыванием. 3. Флавоноидные производные формулы (14). Исходные вещества. Пример 3.1. 7,4'-Дигидрокси-3'-нитроизофлавон 20 мл раствора концентрированной серной кислоты и азотной кислоты (3:1) по каплям добавляли к 1 г даидзеина в 200 мл сухого этанола при комнатной температуре при интенсивном перемешивании. Смесь перемешивали в течение еще 2 ч, а затем добавляли еще 400 мл воды. Осадок соединения отфильтровывали отсасыванием и промывали водой до нейтрализации. Продукт желтого цвета перекристаллизовывали из спирта. 2'-Нитризофлавоны получали в соответствии с электронным положением S. Tappmeyer: Синтез сульфатов. Следующие примеры осуществляли способом, аналогичным способу получения 1.1. Соединения,указанные в заголовке, далее взаимодействовали как исходные продукты. Пример 3.2. 7-Натрий сульфокси-4'-метокси-2'-нитроизофлавон Синтез оксисульфаматов. Следующие примеры осуществляли способом, аналогичным способу получения 1.3. Соединения,указанные в заголовке, далее взаимодействовали как исходные продукты. Пример 3.7. 7,4'-Дисульфамоилокси-2'-нитроизофлавон Восстановление нитроизофлавонов до аминоизофлавонов. Восстановление нитросоединений осуществляли путем каталитического восстановления, используя водород/Pd/C в этаноле. Пример 3.9. 7-Натрий сульфокси-2'-амино-4'-метоксиизофлавон Следующее соединения получали аналогичным образом. Пример 3.10. 7,4'-Динатрий сульфокси-2'-аминоизофлавон Раствор, состоящий из 2 г нитрита натрия и 20 мл воды, по каплям добавляли в раствор, состоящий из 4 г (0,02 моль) аминоизофлавона примера 3.14, 30 мл воды и 5 мл конц. хлористо-водородной кислоты при 0 С, смесь перемешивали в течение еще 10 мин и полученный раствор соли диазония быстро по каплям добавляли в раствор, состоящий из 8 г карбоната натрия, 15 мл воды и 2 г водного раствора диметиламина крепостью 40%. Смесь перемешивали в течение еще 60 мин, кристаллический продукт реакции отфильтровывали отсасыванием и перекристаллизовывали из небольшого количества воды. Следующие триазеноизофлавоны по изобретению получали способом, аналогичным способу получения 3.18, из вышеуказанных аминоизофларонов. Пример 3.19. 7,4'-Динатрий сульфокси-2'-(3,3-диметилтриазенил-1)изофлавон 4. Дифенильные производные (18), которые либо не связаны мостиками, либо связаны мостиками с помощью атомов или диатомных групп. Исходные вещества. Пример 4.1. 3-Метил-4-нитро-4'-(3-метил-4-нитробензоилокси)бензофенон Раствор 122 г фенетола (1 моль), 400 г хлорида 3-метил-4-нитробензоила (2 моль) и 1500 мл 1,2-дибромэтана помещали в реакционный сосуд. Частями (экзотермическая реакция) добавляли 400 г хлорида алюминия при 15-20 С при охлаждении. Реакционную смесь затем постадийно перемешивали при 20-30 С, 40 и 80 С в течение 2 ч в каждом случае. Обработка: охлаждали реакционный раствор до 0 С и медленно вводили в 1,6 кг льда. Затем к реакционной смеси добавляли 100 мл конц. хлористо-водородной кислоты, перемешивали и оставляли отстаиваться. Раствор супернатанта сливали и твердый продукт отфильтровывали отсасыванием и промывали водой. Суспендировали отфильтрованный осадок в 400 мл ацетоне, охлаждали до 0 С, отфильтровывали отсасыванием и сушили. Очищение: перекристаллизовывали из нитропропана. Пример 4.2. 4-Гидрсокси-3'-метил-4'-нитробензофенон 322 г (1 моль) 4-нитро-4'-(4-нитробензоилокси)бензофенона (пример 4.1) нагревали в 1,3 л воды,200 мл этанола и 8 5 г гидроксида натрия до растворения твердого продукта. Обработка: реакционную смесь фильтровали через активированный углерод/кизельгур отсасыванием. Onko 0640 осаждался вместе с 4-нитробензойной кислотой из фильтрата путем добавления 120 мл концентрированной хлористо-водородной кислоты. Твердый продукт отфильтровывали отсасыванием и промывали водой. Отфильтрованный осадок перемешивали со 140 г гидрокарбоната натрия и 900 мл воды в течение 1 ч при 70, отфильтровывали горячим путем отсасывания, промывали 4 мл горячей воды и сушили. Пример 4.3. 4-Амино-3-метил-4'-гидроксибензофенон 25,8 г (0,1 моль) 4-гидрокси-3'-метил-4-нитробензофенона (пример 4.2) растворяли в 200 мл этанола. При 80 С раствор 35 г сульфида натрия в 40 мл воды медленно по каплям добавляли при перемешивании. Реакционный раствор затем кипятили с обратным холодильником в течение 2 ч. Обработка: реакционный раствор выливали в 1 л воды, охлаждали до 20 С и осажденный продукт отфильтровывали отсасыванием, сушили и перекристаллизовывали из толуола. 57 г (0,25 моль) 4-амино-3-метил-4'-гидроксибензофенона растворяли в растворе, состоящем из 75 мл концентрированной хлористо-водородной кислоты и 400 мл воды. Раствор, состоящий из 25 мл воды и 17,25 г нитрита натрия, затем медленно по каплям добавляли при 0-5 С при перемешивании. Этот раствор соли диазония затем по каплям добавляли при 0-5 С при перемешивании к раствору, полученному из 75 г карбоната натрия, 150 мл воды и 35 г водного раствора диметиламина крепостью 40%. Смесь перемешивали в течение 1 ч, нейтрализовали и выпавший твердый осадок отфильтровывали отсасыванием, сушили и кристаллизовали из н-гексана/толуола. Конечные продукты. Пример 4.5. 4-(3,3-Диметилтриазенил-1)-4'-натрий сульфокси(дифенилсульфон) 4 г (0,01 моль) 4-гидрокси-4'-(3,3-диметилтриазенил-1)-(дифенилсульфон) и 3,3 г (0,15 моль) бисульфата натрия смешивали с 20 мл диметилформамида и 25 мл тетрагидрофурана и перемешивали при комнатной температуре в течение 30 ч. К реакционной смеси затем добавляли 20 мл 1 н. водного раствора карбоната натрия, смесь перемешивали, твердый продукт отфильтровывали отсасыванием и фильтрат упаривали при пониженном давлении. Остаток растворяли в минимальном необходимом количестве воды, фильтровали через активированный уголь, фильтрат упаривали на роторном испарителе и остаток перекристаллизовывали из метанола/воды или раствора хлорида натрия. Следующие соединения могут быть получены аналогичным путем. Пример 4.6. 4-(3,3-Диметилтриазенил-1)-2'-натрий сульфоксибензофенон 8,6 г (0,075 моль) хлорсульфонамида по каплям добавляли к раствору 13,4 г (0,05 моль) 4-(3,3-диметилтриазенил-1)-4'-гидроксибензофенона (пример 4.6) в 100 мл диметилацетамида при 0 С. Смесь перемешивали при 0 С в течение 1 ч и затем при комнатной температуре в течение еще 12 ч. Затем к ней добавляли насыщенный водный раствор хлорида аммония, смесь экстрагировали этилацета- 20024381 том, сушили над сульфатом натрия, фильтровали и удаляли растворитель. Продукт перекристаллизовывали из циклогексана/этилацетата. Следующие соединения могут быть получены аналогичным путем. Пример 4.14. 4-(3,3-Диметилтриазенил-1)-2'-сульфамоилоксибензофенон ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Дифенильное производное формулы (1) где X представляет собой прямую C-C-связь между кольцами а и b, CH2, CHOH, CO, S, SO, SO2,-N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (1) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или его соли. 2. Дифенильное производное по п.1 формулы (5) где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (5) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматиче- 21024381 ских колец а и b,или его соли. 3. Дифенильное производное по п.1 формулы (10) где каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, C1-C4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR8 представляет собой водород, этил, CN, NO2, -CH2-CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N=N-N(R2)2 или группу -OSO2Y;R2 представляет собой метил или этил,при условии, что на молекулу формулы (10) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или его соли. 4. Дифенильное производное по п.1 формулы (18) где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2 или -N=N-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 1-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N=N-N(R2)2 или группуR2 представляет собой метил или этил,при условии, что на молекулу формулы (18) обязательно приходятся одна или две группы-N=N-N(R2)2 и одна или две группы -OSO2Y, расположенные на любом кольцевом углероде ароматических колец а и b,или его соли. 5. Дифенильное производное по любому из пп.1 или 4, представляющее собой 4-(3,3-диметилтриазенил-1)-4'-натрий сульфоксибензофенон формулы 6. Способ получения дифенильного производного по любому из пп.1-5, где аминофенильное производное формулы (2) где X представляет собой прямую C-C-связь, CH2, CHOH, СО, S, SO, SO2, -N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -NH2 или группу -OSO2Y;R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9, R10 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, галоген, нитро, циано, группу -NH2 или группу -OSO2Y;R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (2) обязательно приходятся одна или две NH2 группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,диазотируют с помощью диазотирующего агента в присутствии сильной кислоты при низкой температуре в водном растворе с образованием соли диазония формулы (3) где X представляет собой прямую C-C-связь, CH2, CHOH, CO, S, SO, SO2, -N=N- или -CR7=CR8-; каждый R3 и R6 независимо друг от друга представляет собой водород, гидроксил, С 1-С 4-алкил,C1-C4-алкокси, С 1-С 4-алкил-S-, С 1-С 4-алкил-SO-, С 1-С 4-алкил-SO2-, галоген, нитро, циано или группу-OSO2Y; каждый R4 и R5 независимо друг от друга представляет собой группу -N2+AN- или группу -OSO2Y;R8 представляет собой водород, этил, CN, NO2, -CH2CH2-галоген или CH2CH2OH; каждый R9 и R10 независимо друг от друга представляет собой водород, гидроксил, C1-C4-алкил,С 1-С 4-алкокси, галоген, нитро, циано, группу -N2+An- или группу -OSO2Y;An- представляет собой анион галогена или 1/2 сульфат-аниона (SO42-);R1 представляет собой водород, метил или этил,при условии, что на молекулу формулы (3) обязательно приходятся одна или две диазоний группы и одна или две -OSO2Y группы, расположенные на любом кольцевом углероде ароматических колец а и b,и полученные соли диазония формулы (3) затем взаимодействуют с диалкиламинами формулыHN(R2)2, (4) 2 где R представляет собой метил или этил,в присутствии связывающих кислоту агентов с получением дифенильного производного формулы (1). 7. Способ по п.6, где дополнительно после реакции солей диазония (3) с диалкиламинами (4) получают соли из полученных соединений. 8. Способ по п.7, где дополнительно после получения солей высвобождают свободные гидроксильные и/или кислотные группы из этих солей. 9. Лекарственное средство для лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов у человека и животных, содержащее по меньшей мере одно дифенильное производное по любому из пп.1-5 или его физиологически приемлемую соль вместе с одним или несколькими фармакологически приемлемыми вспомогательными агентами или основами. 10. Применение по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемой соли для лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов, у человека и животных. 11. Применение по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемых солей для получения противоопухолевого средства для лечения опухолей кожи, а также опухолей мишеневых органов, зависимых от половых гормонов, у человека и животных. 12. Применение по п.11, где опухоль мишеневых органов, зависимых от половых гормонов, представляет собой опухоль молочной железы, опухоль предстательной железы или опухоль яичек. 13. Способ лечения опухолей кожи и мишеневых органов, зависимых от половых гормонов, у человека и животных, включающий введение достаточного количества по меньшей мере одного дифенильного производного по любому из пп.1-5 или его физиологически приемлемой соли.
МПК / Метки
МПК: A61P 35/00, A61K 31/255, C07C 305/24, A61K 31/37, A61K 31/655, C07D 311/12, C07C 307/02
Метки: дифенильные, замещенные, производные
Код ссылки
<a href="https://eas.patents.su/24-24381-zameshhennye-difenilnye-proizvodnye.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные дифенильные производные</a>
Следующий патент: Способ добычи нефти из подземных пластов
Случайный патент: Производные имидазолина, способ их получения и содержащие их фармацевтические композиции