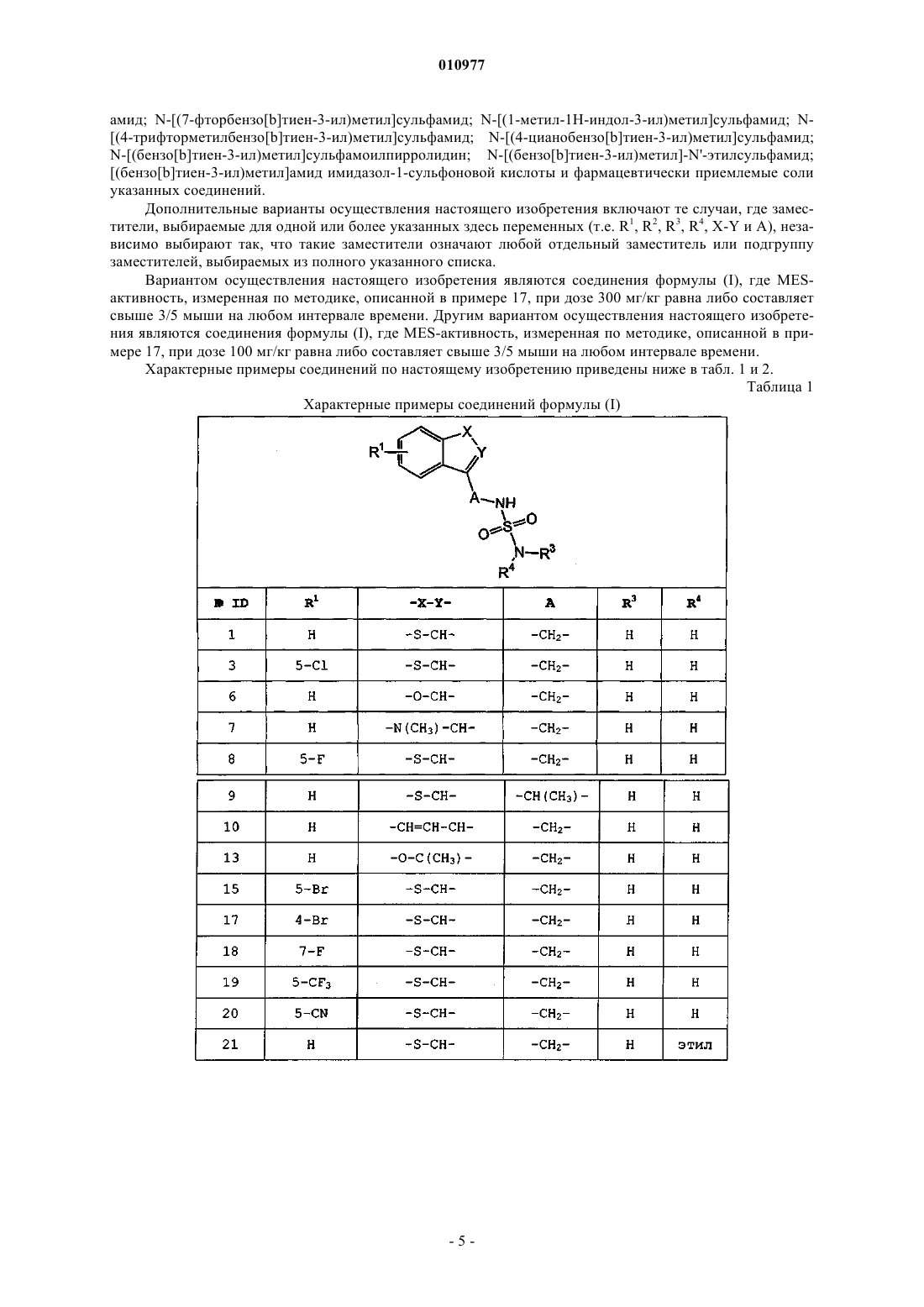
Бензоконденсированные гетероарилсульфамидные производные, полезные в качестве противоконвульсивных средств
Номер патента: 10977
Опубликовано: 30.12.2008
Авторы: Рейтц Аллен Б., Паркер Майкл Х., Марьянофф Брюс Э.
Формула / Реферат
1. Соединение формулы (I)
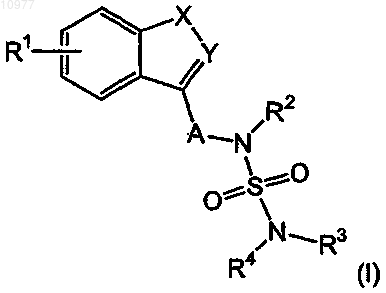
где R1 выбирают из группы, включающей водород, галоген, гидрокси, метокси, трифторметил, нитро и циано;
X-Y выбирают из группы, включающей -S-CH-, -S-C(CH3)-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и
-СН=СН-СН-;
А выбирают из группы, включающей -CH2- и -СН(СН3)-;
R2 выбирают из группы, включающей водород и метил;
каждый из R3 и R4 независимо выбирают из группы, включающей водород и С1-4алкил;
альтернативно, R3 и R4 вместе с атомом азота, с которым связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S;
или фармацевтически приемлемая соль указанного соединения.
2. Соединение по п.1, где
R1 выбирают из группы, включающей водород, галоген, трифторметил, циано и нитро;
X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и -СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(СН3)-;
R2 выбирают из группы, включающей водород и метил;
каждый из R3 и R4 независимо выбирают из группы, включающей водород, метил и этил;
или фармацевтически приемлемая соль указанного соединения.
3. Соединение по п.2, где
R1 выбирают из группы, включающей водород, галоген, трифторметил и циано;
X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и -СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(СН3)-;
R2 означает водород;
каждый из R3 и R4 независимо выбирают из группы, включающей водород и этил;
или фармацевтически приемлемая соль указанного соединения.
4. Соединение по п.3, где
R1 выбирают из группы, включающей водород, 5-хлор, 5-фтор, 5-бром, 4-бром, 7-фтор, 5-трифторметил и 5-циано;
X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и -СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(СН3)-;
R2 означает водород;
каждый из R3 и R4 означает водород; альтернативно, R3 означает водород и R4 означает этил;
или фармацевтически приемлемая соль указанного соединения.
5. Соединение по п.1, где
R1 выбирают из группы, включающей водород, галоген, трифторметил и циано;
X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -O-С(СН3)-, -N(CH3)-CH- и -СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(СН3)-;
R2 выбирают из группы, включающей водород и метил;
R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S;
или фармацевтически приемлемая соль указанного соединения.
6. Соединение по п.5, где
R1 выбирают из группы, включающей водород, галоген, трифторметил и циано;
X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и -СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(CH3)-;
R2 выбирают из группы, включающей водород и метил;
R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-6-членную, насыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S;
или фармацевтически приемлемая соль указанного соединения.
7. Соединение по п.6, где R1 означает водород;
X-Y означает -S-CH-;
А означает -СН2-;
R2 означает водород;
R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-членную кольцевую структуру, выбираемую из группы, включающей пирролидинил и имидазолил;
или фармацевтически приемлемая соль указанного соединения.
8. Соединение по п.2, выбираемое из группы, включающей
N-(бензо[b]тиен-3-илметил)сульфамид;
N-[(5-хлорбензо[b]тиен-3-ил)метил]сульфамид;
N-(3-бензофуранилметил)сульфамид;
N-[(5-фторбензо[b]тиен-3-ил)метил]сульфамид;
N-(1-бензо[b]тиен-3-илэтил)сульфамид;
N-(1-нафталинилметил)сульфамид;
N-[(2-метил-3-бензофуранил)метил]сульфамид;
N-[(5-бромбензо[b]тиен-3-ил)метил]сульфамид;
N-[(4-бромбензо[b]тиен-3-ил)метил]сульфамид;
N-[(7-фторбензо[b]тиен-3-ил)метил]сульфамид;
N-[(1-метил-1Н-индол-3-ил)метил]сульфамид;
N-[(4-трифторметилбензо[b]тиен-3-ил)метил]сульфамид;
N-[(4-цианобензо[b]тиен-3-ил)метил]сульфамид;
N-[(бензо[b]тиен-3-ил)метил]сульфамоилпирролидин;
N-[(бензо[b]тиен-3-ил)метил]-N'-этилсульфамид;
[(бензо[b]тиен-3-ил)метил]амид имидазол-1-сульфоновой кислоты
и фармацевтически приемлемые соли указанных соединений.
9. Соединение по п.8, выбираемое из группы, включающей N-(бензо[b]тиен-3-илметил)сульфамид; N-[(5-фторбензо[b]тиен-3-ил)метил]сульфамид и фармацевтически приемлемые соли указанных соединений.
10. Соединение, выбираемое из группы, включающей N-(бензо[b]тиен-3-илметил)сульфамид и фармацевтически приемлемые соли указанного соединения.
11. Соединение, выбираемое из группы, включающей

и фармацевтически приемлемые соли указанного соединения.
12. Соединение формулы (I)

где R1 выбирают из группы, включающей водород, галоген, гидрокси, метокси, трифторметил, нитро и циано;
X-Y выбирают из группы, включающей -S-CH-, -S-С(CH3)-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и
-СН=СН-СН-;
А выбирают из группы, включающей -СН2- и -СН(CH3)-;
R2 выбирают из группы, включающей водород и метил;
каждый из R3 и R4 независимо выбирают из группы, включающей водород и метил;
альтернативно, R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-3 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S;
или фармацевтически приемлемая соль указанного соединения.
13. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и соединение по п.1.
14. Фармацевтическая композиция, полученная смешением соединения по п.1 и фармацевтически приемлемого носителя.
15. Способ получения фармацевтической композиции, включающий смешение соединения по п.1 и фармацевтически приемлемого носителя.
16. Способ лечения эпилепсии или связанных с эпилепсией нарушений, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения по п.1.
17. Способ лечения эпилепсии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения по п.1.
18. Способ по п.16, где связанное с эпилепсией нарушение означает эссенциальное дрожание или синдром беспокойных конечностей.
19. Применение соединения по п.1 при получении лекарственного средства для лечения эпилепсии или связанных с эпилепсией нарушений у нуждающегося в этом субъекта.
Текст
010977 Перекрестная ссылка на родственные заявки По данной заявке испрашивается приоритет согласно предварительной заявке США 60/604134, поданной 24 августа 2004 г., которая полностью включена посредством ссылки. Область техники, к которой относится изобретение Настоящее изобретение касается новых бензоконденсированных гетероарилсульфамидных производных, фармацевтических композиций, содержащих указанные производные, и применения этих производных для лечения эпилепсии и связанных с эпилепсией нарушений. Предпосылки изобретения Эпилепсия характеризует состояние, при котором субъект испытывает периодически повторяющиеся припадки, вызванные лежащими в основе хроническими процессами. Эпилепсия скорее относится к клиническому феномену, чем к отдельной нозологической форме, поскольку существует множество форм и факторов эпилепсии. Если применять определение эпилепсии по отношению к двум или более неспровоцированным припадкам, распространенность заболеваний эпилепсией в мире среди различных слоев населения по различным оценкам составляет 0,3-0,5%, при этом частота заболеваний эпилепсией оценивается как 5-10 человек на 1000. Существенной стадией в обследовании и лечении страдающего эпилептическим припадком пациента является установление типа испытываемого припадка. Основной характеристикой, позволяющей распознать различные категории эпилептических припадков, является отнесение активности пароксизма к парциальной (являющейся синонимом фокальной) или генерализованной. Парциальными эпилептическими припадками являются те припадки, при которых активность пароксизма ограничивается отдельными участками коры головного мозга. Если сознание полностью сохраняется во время приступа, клинические проявления считаются довольно легкими и приступ носит название простого парциального эпилептического припадка. Если сознание нарушено, эпилептический припадок носит название комплексно-парциального эпилептического припадка. Важная дополнительная подгруппа включает эпилептические припадки, которые начинаются как парциальные припадки, а затем диффузно распространяются по всей коре головного мозга, известные как парциальные припадки с вторичной генерализацией. Генерализованные эпилептические припадки одновременно вовлекают диффузные участки головного мозга в двухсторонне симметричной форме. Малые эпилептические припадки или эпилептические припадки в легкой форме характеризуются внезапными, кратковременными потерями сознания без утраты постурального контроля. Атипичные малые эпилептические припадки обычно включают большую длительность потери сознания, менее внезапное начало и прекращение и более явные моторные симптомы, которые могут включать фокальные или латерализующие характеристики. Генерализованные тоническо-клонические или большие эпилептические припадки, основной тип генерализованных эпилептических припадков, характеризуются бурным началом без предвещающих симптомов. Начальной фазой эпилептического припадка являются обычно тонические сокращения мышц, нарушенное дыхание, заметное усиление симпатического тона, ведущее к повышенной частоте сердечных сокращений, повышенному кровяному давлению и увеличенному размеру зрачка. Через 10-20 с тоническая фаза эпилептического припадка обычно переходит в клоническую фазу, возникающую при наложении периодов мышечной релаксации на тоническое напряжение мышц. Периоды релаксации постепенно нарастают до конца иктальной фазы, обычно длящейся не более 1 мин. Послеприпадочная фаза характеризуется неотвечаемостью, мышечной вялостью и повышенным слюноотделением, что может служить причиной свистящего дыхания и частичной обструкции дыхательных путей. Атонические эпилептические припадки характеризуются внезапной утратой постурального мышечного тонуса, длящейся 1-2 с. Кратковременно нарушается сознание, но обычно не наблюдается послеприпадочной спутанности сознания. Миоклонические эпилептические припадки характеризуются внезапным и кратковременным сокращением мышц, в которое может быть вовлечена одна из частей тела или тело целиком. Ингибиторы угольной ангидразы (CAI) широко используются в медицине, в основном как лекарственные средства против глаукомы и антисекреторные средства или диуретические средства, и являются чрезвычайно полезными соединениями. Однако системные средства против глаукомы (такие как ацетазоламид) потенциально обладают нежелательными побочными действиями, включающими парестезию,нефролитиаз и потерю в весе. Топирамат является хорошо известным противоконвульсивным средством,которое проявляет ингибирование карбоангидразы при концентрации на уровне единиц микромолей и которое, как предполагается, вызывает парестезию, обнаруживаемую у ряда пациентов, принимающих топирамат. Сохраняется потребность в разработке эффективного лечения эпилепсии и связанных с эпилепсией нарушений, и предпочтительно лечения, не сопровождаемого побочными эффектами, связанными с ингибированием угольной ангидразы. Сущность изобретения Настоящее изобретение касается соединения формулы (I)R2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород и С 1-4 алкил; альтернативно, R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-3 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемой соли указанного соединения. Иллюстративным примером изобретения является фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и любое из вышеуказанных соединений. Иллюстрацией изобретения служит фармацевтическая композиция, полученная смешением любого из вышеуказанных соединений и фармацевтически приемлемого носителя. Иллюстрацией изобретения является способ получения фармацевтической композиции, включающий смешение любого из вышеуказанных соединений и фармацевтически приемлемого носителя. Иллюстративным примером изобретения является способ лечения эпилепсии и связанных с эпилепсией нарушений, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества вышеуказанных соединений или фармацевтических композиций. Другим примером изобретения является применение вышеуказанных соединений при получении лекарственного средства для лечения у нуждающегося в этом пациента эпилепсии или связанных с эпилепсией нарушений. Подробное описание изобретения Настоящее изобретение касается соединений формулы (I) где R1, R2, R3, R4, X-Y и А имеют указанные здесь значения. Соединения формулы (I) полезны для лечения эпилепсии и связанных с эпилепсией нарушений. По одному из вариантов осуществления настоящее изобретение касается соединения формулы (I)R2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород и метил; альтернативно, R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержа-2 010977 щую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемой соли указанного соединения. Вариантом осуществления настоящего изобретения являются соединения формулы (I), гдеR2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород и метил; и фармацевтически приемлемые соли указанных соединений. Другим вариантом осуществления настоящего изобретения являются соединения формулы (I), гдеR1 выбирают из группы, включающей водород и галоген; где галоген присоединен в 4, 5 или 7 положении;R2 означает водород; каждый из R3 и R4 означает водород; и фармацевтически приемлемые соли указанных соединений. Другим вариантом осуществления настоящего изобретения являются соединения формулы (I), гдеR2 означает водород; каждый из R3 и R4 означает водород; и фармацевтически приемлемые соли указанных соединений. Другим вариантом осуществления настоящего изобретения являются соединения формулы (I), гдеR1 выбирают из группы, включающей водород, галоген, гидрокси, метокси, трифторметил, нитро и циано; предпочтительно R1 выбирают из группы, включающей водород и галоген; более предпочтительно R1 выбирают из группы, включающей водород и галоген, где галоген присоединен в 4, 5 или 7 положении;R2 выбирают из группы, включающей водород и метил; предпочтительно R2 означает водород; каждый из R3 и R4 независимо выбирают из группы, включающей водород и галоген; предпочтительно каждый из R3 и R4 означает водород; и фармацевтически приемлемые соли указанных соединений. В одном из вариантов осуществления настоящего изобретения R1 выбирают из группы, включающей водород, хлор, фтор и бром. По другому варианту осуществления настоящего изобретения группа R1 отлична от водорода и присоединена в 4, 5 или 7 положение, предпочтительно в 5 положение. По еще одному варианту осуществления настоящего изобретения группа R1 отлична от водорода и присоединена в 5, 6 или 8 положение, предпочтительно в 6 положение. По другому варианту осуществления настоящего изобретения R1 выбирают из группы, включающей водород и галоген. По еще одному варианту осуществления настоящего изобретения R1 выбирают из группы, включающей гидрокси и метокси. По другому варианту осуществления настоящего изобретения R1 выбирают из группы, включающей водород,галоген и трифторметил. По еще одному варианту осуществления настоящего изобретения R1 выбирают из группы, включающей водород, галоген, трифторметил, циано и нитро. По другому варианту осуществления настоящего изобретения R1 выбирают из группы, включающей водород, галоген, трифторметил и циано. По еще одному варианту осуществления настоящего изобретения R1 выбирают из группы, включающей трифторметил и циано. По другому варианту осуществления настоящего изобретения R1 выбирают из группы, включающей водород, 4-бром, 5-хлор, 5-фтор, 5-бром, 5-трифторметил, 5-циано и 7 циано. Согласно варианту осуществления настоящего изобретения R2 означает водород. По другому варианту осуществления настоящего изобретения каждый из R3 и R4 означает водород. По еще одному варианту осуществления настоящего изобретения R2 означает водород, R3 означает водород и R4 означает водород. По одному из вариантов осуществления настоящего изобретения каждый из R3 и R4 независимо выбирают из группы, включающей водород и C1-4 алкил. По другому варианту осуществления настоящего изобретения R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную,частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S.-3 010977 По одному из вариантов осуществления настоящего изобретения каждый из R3 и R4 независимо выбирают из группы, включающей водород, метил и этил. По другому варианту осуществления настоящего изобретения каждый из R3 и R4 независимо выбирают из группы, включающей водород и метил. По еще одному варианту осуществления настоящего изобретения каждый из R3 и R4 независимо выбирают из группы, включающей водород и этил. По еще одному варианту осуществления настоящего изобретенияR3 означает водород и R4 означает этил. По одному из вариантов осуществления настоящего изобретения R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N. По другому варианту осуществления настоящего изобретения R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N. По еще одному варианту осуществления настоящего изобретения R3 иR4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N. Предпочтительно R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-6-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N. Более предпочтительно R3 и R4 вместе с атомом азота, с которым они связаны, образуют 6-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N. Предпочтительно R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7- (более предпочтительно, 5-6-) членную, насыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 (предпочтительно один) дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N (предпочтительно О или N, более предпочтительно N). По другому варианту осуществления настоящего изобретения R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-6-членную, насыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 (предпочтительно один) дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N (предпочтительно О или N, более предпочтительно N). Предпочтительно, 5-7-членная, насыщенная, частично ненасыщенная или ароматическая кольцевая структура содержит 0-1 дополнительных гетероатомов, независимо выбираемых из группы, включающей О, S и N. Предпочтительно гетероатом независимо выбирают из группы, включающей О и N, более предпочтительно гетероатом означает N. Подходящие примеры 5-7-членных, насыщенных, частично ненасыщенных или ароматических кольцевых структур, необязательно содержащих 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N, включают, но не в порядке ограничения, пирролил, пирролидинил, пирролинил, морфолинил, пиперидинил, пиперазинил, имидазолил, пиразолил, пиридил, имидазолил, тиоморфолинил, пиразинил, триазинил, азепинил и тому подобное. Предпочтительные 5-7-членные,насыщенные, частично ненасыщенные или ароматические кольцевые структуры, необязательно содержащие 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, S и N,включают, но не в порядке ограничения, имидазолил, пирролидинил, пиперидинил и морфолинил. По одному из вариантов осуществления настоящего изобретения А означает -CH2-. Согласно варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей-S-CH-, -O-CH-, -О-С(CH3)-, -N(CH3)-CH- и -СН=СН-СН-. По другому варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -S-СН-, -O-CH-, -О-С(CH3)- и -СН=СН-СН-. По еще одному варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -O-С(СН 3)- и -N(CH3)-CH-. По другому варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -S-CH-, -O-CH-, -N(CH3)-CH- и -СН=СН-СН-. По еще одному варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -S-CH-,-О-СН- и -СН=СН-С-. По другому варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -S-CH- и -O-CH-. По еще одному варианту осуществления настоящего изобретенияX-Y выбирают из группы, включающей -S-CH-, -S-C(CH3)-, -O-CH-, -O-С(СН 3)- и -N(CH3)-CH-. Согласно варианту осуществления настоящего изобретения X-Y означает -S-CH-. По другому варианту осуществления настоящего изобретения X-Y означает -СН=СН-СН-. По еще одному варианту осуществления настоящего X-Y означает -N(CH3)-CH-. По другому варианту осуществления настоящего изобретения X-Y выбирают из группы, включающей -О-СН- и -O-С(СН 3)-. Согласно варианту осуществления настоящее изобретение касается соединений, выбираемых из группы, включающей N-(бензо[b]тиен-3-илметил)сульфамид; N-[(5-хлорбензо[b]тиен-3-ил)метил] сульфамид; N-(3-бензофуранилметил)сульфамид; N-[(5-фторбензо[b]тиен-3-ил)метил]сульфамид; N-(1-бензо[(бензо[b]тиен-3-ил)метил]амид имидазол-1-сульфоновой кислоты и фармацевтически приемлемые соли указанных соединений. Дополнительные варианты осуществления настоящего изобретения включают те случаи, где заместители, выбираемые для одной или более указанных здесь переменных (т.е. R1, R2, R3, R4, X-Y и А), независимо выбирают так, что такие заместители означают любой отдельный заместитель или подгруппу заместителей, выбираемых из полного указанного списка. Вариантом осуществления настоящего изобретения являются соединения формулы (I), где MESактивность, измеренная по методике, описанной в примере 17, при дозе 300 мг/кг равна либо составляет свыше 3/5 мыши на любом интервале времени. Другим вариантом осуществления настоящего изобретения являются соединения формулы (I), где MES-активность, измеренная по методике, описанной в примере 17, при дозе 100 мг/кг равна либо составляет свыше 3/5 мыши на любом интервале времени. Характерные примеры соединений по настоящему изобретению приведены ниже в табл. 1 и 2. Таблица 1 Характерные примеры соединений формулы (I) Как использовано здесь, "галоген" означает хлор, бром, фтор и йод. Как принято здесь, термин "алкил", независимо, используется отдельно или как составная часть группы заместителя, включает линейные и разветвленные цепи. Например, радикалы алкила включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и тому подобное. Если не указано иначе, "С 1-4 алкил" означает структуру углеродной цепи из 1-4 атомов углерода. Когда определенная группа является "замещенной" (например, алкил, фенил, арил, гетероалкил, гетероарил), эта группа может иметь один или более заместителей, предпочтительно от одного до пяти заместителей, более предпочтительно от одного до трех заместителей, наиболее предпочтительно одиндва заместителя, независимо выбираемых из перечня заместителей. Применительно к заместителям термин "независимо" означает, что когда возможно присутствие более одного такого заместителя, эти заместители могут быть одинаковыми, либо отличными друг от друга. Для более краткого описания некоторые приведенные здесь количественные выражения не снабжены термином "приблизительно". Понятно, что независимо от того, используется термин "приблизительно" в явной форме или нет, подразумевается, что каждое приведенное здесь количественное выражение означает фактически заданную величину, и очевидно также, что указанный термин означает приближение к такой заданной величине, допустимое с точки зрения специалиста в данной области, включающее приближения, связанные с экспериментальными условиями и/или условиями измерения такой заданной величины. Как использовано здесь, если не оговорено иначе, термин "уходящая группа" означает заряженный или незаряженный атом или группу, которые уходят во время реакции замещения или вытеснения. Подходящие примеры включают, но не в порядке ограничения, Br, Cl, I, мезилат, тозилат и тому подобное. Если не оговорено иначе, положение, по которому связан заместитель R1, определяют, производя отсчет вокруг структуры ядра по часовой стрелке, принимая положения X-Y за 1, 2 и продолжая затем,как указано ниже: Если заместитель X-Y представляет собой -СН=СН-СН-, то группа X-Y считается как 1, 2, 3 и затем счет продолжают по часовой стрелке вокруг структуры ядра, как указано выше. Согласно стандартной номенклатуре, используемой в данном описании, сначала называют концевой участок определяемой боковой цепи, впоследствии переходя к соседней функциональности, двигаясь в сторону точки присоединения. Так, например, заместитель "фенилC1-C6 алкиламинокарбонилC1C6 алкил" означает группу формулыTLC = тонкослойная хроматография (ТСХ) Как использовано здесь, если не оговорено иначе, термины "эпилепсия и связанные с эпилепсией нарушения" или "эпилепсия или связанное с эпилепсией нарушение" означают любое нарушение, при котором субъект (преимущественно человек, взрослый, ребенок или грудной ребенок) испытывает один или более припадков и/или дрожания. Подходящие примеры включают, но не в порядке ограничения,такие состояния, как эпилепсия (включая, но не в порядке ограничения, связанные с локализацией эпилепсии, генерализованные эпилепсии, эпилепсии как с генерализованными, так и локальными припадками и тому подобное), эпилептические припадки как осложнение заболевания или состояния (такие как припадки, вызванные такими заболеваниями или состояниями, как энцефалопатия, фенилкетонурия,ювенильная болезнь Гоше, прогрессирующая миоклоническая эпилепсия Lundborg'a, внезапный приступ,травма головы, стресс, гормональные нарушения, применение или отмена лекарственных средств, применение или отказ от применения алкоголя, депривация сна и тому подобное), эссенциальное дрожание,синдром беспокойных конечностей и тому подобное. Предпочтительно нарушение выбирают из группы,включающей такие нарушения, как эпилепсия (независимо от типа, первопричины или происхождения),эссенциальное дрожание или синдром беспокойных конечностей, более предпочтительно нарушением является эпилепсия (независимо от типа, первопричины или происхождения) или эссенциальное дрожание. Термин "субъект", как использован здесь, означает животное, предпочтительно млекопитающее,наиболее предпочтительно человека, являющееся объектом терапии, наблюдения или эксперимента. Термин "терапевтически эффективное количество", как использован здесь, означает количество активного соединения или фармацевтического агента, вызывающее биологическую реакцию или медикаментозный отклик в системе тканей, организме животного или человека, которых добивается исследователь, ветеринар, врач или другой клиницист, что включает снятие симптомов излечиваемого заболевания или нарушения. Предполагается, что термин "композиция", как использован здесь, охватывает продукт, включающий определенные ингредиенты в определенных количествах, а также любой продукт, образующийся,прямо или косвенно, из комбинаций определенных ингредиентов в определенных количествах. Когда соединения по настоящему изобретению содержат по меньшей мере один хиральный центр,такие соединения могут существовать в виде энантиомеров. Когда соединения содержат два или более хиральных центра, такие соединения могут дополнительно существовать в виде диастереомеров. Само собой разумеется, что все такие изомеры и смеси указанных изомеров входят в объем настоящего изобретения. Кроме того, некоторые кристаллические формы соединений могут существовать в виде полиморфов, и подразумевается, что указанные полиморфы, как таковые, входят в настоящее изобретение. Вдобавок, некоторые соединения могут образовывать сольваты с водой (т.е. гидраты) или общепринятыми органическими растворителями, и подразумевается, что такие сольваты также входят в объем настоящего изобретения. Настоящее изобретение включает в свой объем пролекарства соединений по данному изобретению. Обычно, такие пролекарства являются функциональными производными соединений, легко превращающимися in vivo в требуемое соединение. Таким образом, в способах лечения по настоящему изобретению термин "введение" охватывает лечение различных указанных заболеваний конкретно указанным соединением или соединением, которое конкретно не указано, но превращается в указанное соединение in vivo после ведения пациенту. Общепринятые способы выбора и получения подходящих пролекарственных производных описаны, например, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985. Предназначенные для применения в медицине соли соединений по настоящему изобретению относятся к нетоксическим "фармацевтически приемлемым солям". Однако другие соли могут быть полезны для получения соединений по настоящему изобретению или соответствующих фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений по настоящему изобретению включают кислотно-аддитивные соли, которые могут, например, быть получены смешением раствора соединения с раствором фармацевтически приемлемой кислоты, такой как хлористо-водородная кислота,серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, когда соединения по настоящему изобретению содержат кислотную составляющую, подходящие фармацевтически приемлемые соли таких соединений могут включать соли щелочных металлов, например соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли, полученные с подходящими органическими лигандами, например четвертичные аммониевые соли. Так, характерные фармацевтически приемлемые соли включают следующие:-7 010977 ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, кальцийэдетат,камзилат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат, фумарат, глуцептат, глюконат, глутамат, гликоллиларсанилат, гексилрезорцинат, гидрабамин, гидробромид,гидрохлорид, гидроксинафтоат, йодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, манделат,мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напзилат, нитрат, соль Nметилглюкаминаммония, олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтйодид и валерат. Характерные примеры кислот и оснований, которые могут быть использованы при получении фармацевтически приемлемых солей, включают следующие: кислоты включают такие, как уксусная кислота, 2,2-дихлормолочная кислота, ацилированные аминокислоты, адипиновая кислота, альгиновая кислота, аскорбиновая кислота, L-аспарагиновая кислота,бензолсульфоновая кислота, бензойная кислота, 4-ацетамидобензойная кислота, (+)-камфорная кислота,камфорсульфоновая кислота, (+)-(1S)-камфор-10-сульфоновая кислота, каприновая кислота, капроновая кислота, каприловая кислота, коричная кислота, лимонная кислота, цикламовая кислота, додецилсерная кислота, этан-1,2-дисульфоновая кислота, этансульфоновая кислота, 2-гидроксиэтансульфоновая кислота, муравьиная кислота, фумаровая кислота, галактаровая кислота, гентизиновая кислота, глюкогептоновая кислота, D-глюконовая кислота, D-глюкуроновая кислота, L-глутаминовая кислота, -оксоглутаровая кислота, гликолевая кислота, гиппуровая кислота, бромисто-водородная кислота, хлористо-водородная кислота, (+)-L-молочная кислота, -DL-молочная кислота, лактобионовая кислота, малеиновая кислота,(-)-L-яблочная кислота, малоновая кислота, -DL-миндальная кислота, метансульфоновая кислота, нафталин-2-сульфоновая кислота, нафталин-1,5-дисульфоновая кислота, 1-гидрокси-2-нафтойная кислота,никотиновая кислота, азотная кислота, олеиновая кислота, оротовая кислота, щавелевая кислота, пальмитиновая кислота, памовая кислота, фосфорная кислота, L-пироглутаминовая кислота, салициловая кислота, 4-аминосалициловая кислота, себациновая кислота, стеариновая кислота, янтарная кислота, серная кислота, дубильная кислота, (+)-L-винная кислота, тиоциановая кислота, п-толуолсульфоновая кислота и ундециленовая кислота; и основания включают такие, как аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, деанол, диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, Nметилглюкамин, гидрабамин, 1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин,пиперазин, гидроксид калия, 1-(2-гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Соединения формулы (I), где А означает -СН 2-, могут быть получены способом, представленным схемой 1. Схема 1 Согласно схеме соответственно замещенное соединение формулы (V), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с соответственно замещенным соединением формулы (VI), известным соединением или соединением, полученным известными способами, где соединение формулы (VI) присутствует в количествах, изменяющихся в пределах от приблизительно 2 до приблизительно 5 экв., в органическом растворителе, таком как этанол, метанол, диоксан и тому подобное, предпочтительно в безводном органическом растворителе, преимущественно при повышенной температуре, изменяющейся в пределах от приблизительно 50 до приблизительно 100 С,более предпочтительно приблизительно при температуре кипения, что приводит к образованию соответствующего соединения формулы (Ia). Соединения формулы (I), альтернативно, могут быть получены способом, представленным схемой 2. Согласно схеме соответственно замещенное соединение формулы (VII), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с соответственно замещенным соединением формулы (VI), известным соединением или соединением, полученным известными способами, где соединение формулы (VI) присутствует в количествах, изменяющихся в пределах от приблизительно 2 до приблизительно 5 экв., в органическом растворителе, таком как ТГФ, диоксан и тому подобное, предпочтительно в безводном органическом растворителе, преимущественно при повышенной температуре, изменяющейся в пределах от приблизительно 50 до приблизительно 100 С, более предпочтительно приблизительно при температуре кипения, что приводит к образованию соответствующего соединения формулы (I). Соединения формулы (VII), где А означает -СН 2-, могут, например, быть получены способом, представленным схемой 3. Схема 3 Согласно схеме соответственно замещенное соединение формулы (VIII), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с активирующим агентом,таким как оксалилхлорид, сульфонилхлорид и тому подобное, и затем взаимодействию с источником амина, таким как аммиак, гидроксид аммония и тому подобное, в органическом растворителе, таком как ТГФ, диэтиловый эфир, DCM, DCE и тому подобное, что приводит к образованию соответствующего соединения формулы (IX). Соединение формулы (IX) подвергают взаимодействию с соответственно выбранным восстанавливающим агентом, таким как LAH, боран и тому подобное, в органическом растворителе, таком как ТГФ,диэтиловый эфир и тому подобное, что приводит к образованию соответствующего соединения формулы Согласно схеме соответственно замещенное соединение формулы (X), известное соединение или соединение, полученное известными способами, подвергают взаимодействию со смесью формамида и муравьиной кислоты, где смесь формамида и муравьиной кислоты присутствует в количестве свыше приблизительно 1 экв., предпочтительно в избыточном количестве или свыше приблизительно 5 экв.,при повышенной температуре порядка 150 С, что приводит к образованию соответствующего соединения формулы (XI).-9 010977 Соединение формулы (XI) гидролизуют, осуществляя взаимодействие с концентрированной HCl,концентрированной H2SO4 и тому подобным, при повышенной температуре, предпочтительно при температуре кипения, что приводит к образованию соответствующего соединения формулы (VIIb). Соединения формулы (VII), альтернативно, могут быть получены способом, представленным схемой 5. Схема 5 Согласно схеме соответственно замещенное соединение формулы (XII), где L означает уходящую группу, такую как Br, Cl, I, тозилат, мезилат и тому подобное, известное соединение или соединение,полученное известными способами, подвергают взаимодействию с азидом натрия в органическом растворителе, таком как ДМФА, ДМСО, метанол, этанол и тому подобное, что приводит к образованию соответствующего соединения формулы (XIII). Соединение формулы (XIII) подвергают взаимодействию с соответственно выбранным восстанавливающим агентом, таким как LAH, трифенилфосфин, H2(g) и тому подобное, согласно известным методикам, что приводит к образованию соответствующего соединения формулы (VII). Соединения формулы (VII), где А означает СН 2 и X-Y означает -О-CH2-, могут, например, быть получены способом, представленным схемой 6. Схема 6 Согласно схеме соответственно замещенный фенол, соединение формулы (XIV), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с бромацетоном,известным соединением в присутствии основания, такого как K2CO3, Na2CO3, NaH, триэтиламин, пиридин и тому подобное, в органическом растворителе, таком как ацетонитрил, ДМФА, ТГФ и тому подобное, необязательно, при повышенной температуре, что приводит к образованию соответствующего соединения формулы (XV). Соединение формулы (XV) подвергают взаимодействию с кислотой, такой как полифосфорная кислота, серная кислота, хлористо-водородная кислота и тому подобное, предпочтительно с полифосфорной кислотой, желательно в отсутствие растворителя (для специалиста в данной области очевидно, что полифосфорная кислота выступает в качестве растворителя), что приводит к образованию соответствующего соединения формулы (XVI). Соединение формулы (XVI) подвергают взаимодействию с источником брома, таким как Nбромсукцинимид, в присутствии бензоилпероксида, Br2 и тому подобного, предпочтительно в органическом растворителе, таком как четыреххлористый углерод, хлороформ, DCM и тому подобное, желательно в галогенированном органическом растворителе, что приводит к образованию соответствующего соединения формулы (XVII). Соединение формулы (XVII) подвергают взаимодействию с азидом натрия в органическом растворителе, таком как ДМФА, ДМСО, метанол, этанол и тому подобное, что приводит к образованию соответствующего соединения формулы (XVIII). Соединение формулы (XVIII) подвергают взаимодействию с соответственно выбранным восстанавливающим агентом, таким как LAH, трифенилфосфин, H2(g) и тому подобное, согласно известным методикам, что приводит к образованию соответствующего соединения формулы (VIIc). Соединения формулы (V), где X-Y означает -S-CH-, могут, например, быть получены способом,представленным схемой 7. Согласно схеме соответственно замещенное соединение формулы (XIX), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с диметилацеталем хлорацетальдегида или диметилацеталем бромацетальдегида, известным соединением в присутствии основания, такого как калий-трет-бутилат, натрий-трет-бутилат, карбонат калия, гидроксид калия и тому подобное, в органическом растворителе, таком как ТГФ, ДМФА, ацетонитрил и тому подобное, что приводит к образованию соответствующего соединения формулы (XX). Соединение формулы (XX) подвергают взаимодействию с кислотой, такой как полифосфорная кислота, серная кислота, хлористо-водородная кислота и тому подобное, предпочтительно с полифосфорной кислотой в присутствии хлорбензола,преимущественно в отсутствие растворителя (для специалиста в данной области очевидно, что полифосфорная кислота и/или хлорбензол выступают в качестве растворителя), при повышенной температуре, изменяющейся в пределах от приблизительно 100 до приблизительно 200 С, преимущественно при повышенной температуре, близкой к температуре кипения, что приводит к образованию соответствующего соединения формулы (XXI). Соединение формулы (XXI) подвергают взаимодействию с формилирующим реагентом, таким как дихлорметилметиловый эфир и тому подобное, в присутствии кислотного катализатора Льюиса, такого как тетрахлорид титана, трихлорид алюминия, тетрахлорид олова и тому подобное, в органическом растворителе, таком как DCM, хлороформ и тому подобное, при температуре в пределах от приблизительно 0 С до приблизительно комнатной температуры, что приводит к образованию соответствующего соединения формулы (Va). Соединения формулы (I), где R3 и/или R4 отличны от водорода или R3 и R4 вместе с азотом, к которому они присоединены, образуют кольцевую структуру, могут, альтернативно, быть получены способом, представленным схемой 8. Схема 8 Согласно схеме, соответственно замещенное соединение формулы (Ib) подвергают взаимодействию с соответственно замещенным амином, соединением формулы (XXII), известным соединением или соединением, полученным известными способами, в воде или органическом растворителе, таком как диоксан, этанол, ТГФ, изопропанол и тому подобное, при условии, что соединение формулы (Ib) и соединение формулы (XXII), по меньшей мере, частично растворимы в воде или органическом растворителе, при температуре в пределах от приблизительно комнатной температуры до приблизительно температуры кипения, желательно приблизительно при температуре кипения, что приводит к образованию соответствующего соединения формулы (Ic). Для специалиста в данной области очевидно, что когда реакционная стадия по настоящему изобретению может быть осуществлена в ряде растворителей или систем растворителей, указанная реакционная стадия может также быть выполнена в смеси соответствующих растворителей или систем растворителей. Когда способы получения соединений по настоящему изобретению приводят к образованию смеси стереоизомеров, эти изомеры могут быть разделены общепринятыми способами, такими как препаративная хроматография. Соединения могут быть получены в рацемической форме, либо отдельные энантиомеры могут быть получены как энантиоспецифическим синтезом, так и путем разделения. Соединения могут, например, быть разделены на составляющие энантиомеры общепринятыми способами, такими как получение диастереомерных пар посредством образования солей с оптически активной кислотой, такой как (-)-ди-п-толуоил-D-винная кислота и/или (+)-ди-п-толуоил-L-винная кислота, с последующей фракционированной кристаллизацией и регенерацией свободного основания. Соединения могут также быть- 11010977 разделены путем получения диастереомерных сложных эфиров или амидов, с последующим хроматографическим разделением и удалением хиральных вспомогательных веществ. Альтернативно, соединения могут быть разделены с применением хиральной ВЭЖХ-колонки. В ходе осуществления любого из способов получения соединений по настоящему изобретению может быть необходимо и/или желательно защитить чувствительные или реакционноспособные группы любых рассматриваемых молекул. Это может быть достигнуто с помощью общеизвестных защитных групп, таких как группы, описанные в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, PlenumPress, 1973 и T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons, 1991. Защитные группы могут быть удалены на подходящей последующей стадии с использованием известных из уровня техники способов. Настоящее изобретение также включает фармацевтические композиции, содержащие одно или более соединений формулы (I) с фармацевтически приемлемым носителем. Фармацевтические композиции,содержащие одно или более описанных здесь соединений по изобретению в качестве активного ингредиента, могут быть получены однородным смешением соединения или соединений с фармацевтическим носителем согласно общепринятым методикам составления фармацевтических композиций. Может быть использовано большое разнообразие форм носителя в зависимости от требуемого способа введения (например, орального, парентерального). Так, предназначенные для жидких оральных препаратов, таких как суспензии, эликсиры и растворы, подходящие носители и вспомогательные средства включают такие вещества, как вода, гликоли, масла, спирты, корригенты, консерванты, стабилизаторы, красители и тому подобное; для твердых оральных препаратов, таких как порошки, капсулы и таблетки, подходящие носители и вспомогательные средства включают такие вещества, как крахмалы, сахара, разбавители, гранулирующие средства, лубриканты, связующие вещества, дезинтегрирующие средства и тому подобное. Твердые оральные препараты могут также быть покрыты такими веществами, как сахара, или могут иметь энетросолюбильную оболочку в целях модуляции основного участка абсорбции. Носитель для парентерального введения обычно включает стерильную воду, и могут быть добавлены другие ингредиенты, для повышения растворимости или консервации. Суспензии или растворы для инъекций могут быть также получены с использованием только водных носителей или с соответствующими добавками. Для получения фармацевтических композиций по настоящему изобретению одно или более соединений по настоящему изобретению, в качестве активного ингредиента, однородно смешивают с фармацевтическим носителем согласно технологии составления фармацевтических композиций, может быть использован широкий ряд носителей в зависимости от требуемой для введения формы препарата, например оральной или парентеральной, такой как внутримышечная. При получении композиций в оральной дозированной форме может быть использована любая общепринятая фармацевтическая среда. Так, для жидких оральных препаратов, таких как, например, суспензии, эликсиры и растворы, подходящие носители и вспомогательные средства включают такие вещества, как вода, гликоли, масла, спирты, корригенты, консерванты, красители и тому подобное; для твердых оральных препаратов, таких как, например,порошки, капсулы, каплеты, желатиновые капсулы и таблетки, подходящие носители могут включать крахмалы, сахара, разбавители, гранулирующие средства, лубриканты, связующие вещества, дезинтегрирующие средства и тому подобное. По причине легкости приема таблетки и капсулы представляют собой наиболее удобную оральную единичную дозированную форму, очевидно, что в этом случае используют твердые фармацевтические носители. При необходимости, таблетки можно покрывать сахарной оболочкой или наносить энтеросолюбильное покрытие согласно стандартным способам. Носитель для парентеральных препаратов обычно включает стерильную воду, наряду с другими ингредиентами, которые могут быть включены, например, в таких целях, как повышение растворимости или консервация. Могут быть также получены суспензии для инъекций, в этом случае могут также быть использованы соответствующие жидкие носители, суспендирующие средства и тому подобное. Рассматриваемые здесь фармацевтические композиции содержат, на дозированную единицу, например, таблетку, капсулу, порошок,инъекцию, полную чайную ложку и тому подобное, некоторое количество активного ингредиента, необходимое для доставки вышеуказанной эффективной дозы. Рассматриваемые фармацевтические композиции содержат на единичную дозированную форму, например таблетку, капсулу, порошок, инъекцию,суппозиторий, полную чайную ложку и тому подобное, приблизительно 50-100 мг и могут назначаться при дозировке приблизительно 0,01-20,0 мг/кг/день, предпочтительно приблизительно от 0,1 до 10 мг/кг/день, более предпочтительно приблизительно 0,5-5 мг/кг/день, более предпочтительно приблизительно 1,0-5,0 мг/кг/день. Однако дозировки могут быть изменены в зависимости от потребности пациента, тяжести излечиваемого состояния и используемого соединения. Возможно использование либо ежедневного приема, либо последующего периодического приема. Предпочтительно эти композиции представлены в единичных дозированных формах, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные парентеральные растворы или суспензии,дозированные аэрозоли или жидкие спреи, капли, ампулы, автоинжекторные устройства или суппозитории; для орального, парентерального, интраназального или ректального введения или для введения путем ингаляции или инсуффляции. Альтернативно, композиция может быть представлена в форме, пригодной для приема раз в неделю или раз в месяц; например нерастворимая соль активного соединения,- 12010977 такая как соль в виде деканоата, может быть адаптирована для обеспечения депо препарата, предназначенного для внутримышечного введения. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например общепринятыми ингредиентами для изготовления таблеток, такими как кукурузный крахмал, лактоза, сахароза, сорбит,тальк, стеариновая кислота, стеарат магния, дикальцийфосфат или камеди, и другими фармацевтическими растворителями, например водой, что дает твердую композицию предварительного формулирования,содержащую гомогенную смесь соединения по настоящему изобретению или фармацевтически приемлемой соли указанного соединения. Когда эти композиции предварительного формулирования упоминаются как гомогенные, это означает, что активный ингредиент однородно диспергирован в композиции,так что композиция легко может быть подразделена на равно эффективные дозированные формы, такие как таблетки, пилюли и капсулы. Эту твердую композицию предварительного формулирования затем подразделяют на единичные дозированные формы вышеуказанного типа, содержащие от приблизительно 0,1 до приблизительно 500 мг активного ингредиента по настоящему изобретению. Таблетки или пилюли из новой композиции могут быть покрыты оболочкой или скомпанованы иным образом, что позволяет получить дозированную форму, предоставляющую преимущество пролонгированного действия. Например, таблетка или пилюля может содержать внутренний дозированный компонент и внешний дозированный компонент, последний в форме оболочки вокруг первого. Два компонента могут быть разделены энтеросолюбильным слоем, который предохраняет внутренний компонент от разложения в желудке, пропуская неповрежденным в двенадцатиперстную кишку или обеспечивая отсроченное высвобождение. Для таких энтеросолюбильных слоев или покрытий может быть использован ряд материалов, такие материалы включают некоторые полимерные кислоты с такими веществами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которые новые композиции по настоящему изобретению могут быть включены,для введения орально или путем инъекции, включают водные растворы, соответственно ароматизированные сиропы, водные или масляные суспензии и ароматизированные эмульсии с пищевыми маслами,такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсирами и тому подобными фармацевтическими растворителями. Подходящие диспергирующие или суспендирующие средства для водных суспензий включают такие вещества, как синтетические и натуральные камеди, такие как трагакантовая, акациевая, альгинат, декстран, натрийкарбоксиметилцеллюлоза,метилцеллюлоза, поливинилпирролидон или желатин. Способ лечения эпилепсии и связанных с эпилепсией нарушений, описанных настоящим изобретением, может быть также осуществлен с применением фармацевтической композиции, содержащей любое из вышеуказанных соединений и фармацевтически приемлемый носитель. Фармацевтическая композиция может содержать от приблизительно 0,1 до приблизительно 1000 мг, предпочтительно приблизительно 50-500 мг соединения и может быть сформулирована в любую пригодную для выбранного способа введения форму. Носители включают необходимые и инертные фармацевтические вспомогательные вещества, включающие, но не в порядке ограничения, связующие вещества, суспендирующие средства,лубриканты, ароматизаторы, подсластители, консерванты, красители и покрытия. Композиции, пригодные для орального введения, включают твердые формы, такие как пилюли, таблетки, каплеты, капсулы(каждая из указанных форм включает препараты немедленного высвобождения, высвобождения в определенное время и замедленного высвобождения), гранулы и порошки, и жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, полезные для парентерального введения, включают стерильные растворы, эмульсии и суспензии. Целесообразно соединения по настоящему изобретению вводить в виде разовой суточной дозы, либо суммарную суточную дозу можно вводить ежедневно в подразделенных дозах за два, три или четыре раза. Кроме того, соединения по настоящему изобретению могут быть введены в интраназальной форме посредством местного применения подходящих интраназальных аппаратов или с помощью трансдермальных пластырей для кожи, хорошо известных специалистам в данной области. При введении посредством трансдермальной системы доставки дозированное введение будет, конечно, осуществляться скорее по непрерывной, чем по прерывистой схеме. Например, для орального приема в форме таблетки или капсулы, активный лекарственный компонент может быть объединен с оральным, нетоксическим, фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и тому подобное. Кроме того, если желательно или необходимо,подходящие связующие вещества; лубриканты, дезинтегрирующие средства и красители могут быть также включены в смесь. Подходящие связующие вещества включают, но не в порядке ограничения,крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, сахаристые вещества из кукурузы, природные и синтетические камеди, такие как акациевая и трагакантовая или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и тому подобное. Дезинтегрирующие средства включают, но не в порядке ограничения, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и тому подобное. В жидких формах используют соответственно ароматизированные суспендирующие или диспергирующие средства, такие как синтетические и природные камеди, например трагантовую, акациевую, ме- 13010977 тилцеллюлозу и тому подобное. Для парентерального введения требуются стерильные суспензии и растворы. Изотонические препараты, обычно содержащие подходящие консерванты, используют, когда требуется внутривенное введение. Соединения по настоящему изобретению могут быть введены в любой из вышеуказанных композиций и согласно схемам дозированного приема, известным из уровня техники, будь то лечение эпилепсии или связанных с эпилепсией нарушений. Суточная дозировка продуктов может изменяться в широких пределах, от 0,01 до 1000 мг для взрослого в день. Композиции для орального применения предпочтительно представлять в форме таблеток, содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 и 1000 мг активного ингредиента, что дает возможность симптоматического подбора дозировки для излечиваемого пациента. Эффективное количество лекарственного средства обычно обеспечивается при уровне доз от приблизительно 0,01 до приблизительно 20 мг/кг массы тела в день. Предпочтительно интервал составляет от приблизительно 0,5 до приблизительно 10,0 мг/кг массы тела в день, наиболее предпочтительно от приблизительно 1,0 до приблизительно 5,0 мг/кг массы тела в день. Соединения могут быть введены по схеме приема от 1 до 4 раз в день. Оптимальные для введения дозировки могут быть легко установлены специалистом в данной области, и изменяются в зависимости от конкретного используемого соединения, способа введения, силы препарата и прогрессирования заболевания. Вдобавок, факторы, связанные с конкретным излечиваемым пациентом, включающие возраст пациента, массу, диету и время введения, приводят к необходимости корректировки дозировок. Специалисту в данной области понятно, что испытания in vivo и in vitro с применением подходящих, известных и общепринятых моделей на клетках и/или на животных, позволяют прогнозировать способность испытуемого соединения излечивать или предупреждать данное нарушение. Специалисту в данной области также ясно, что клинические испытания на человеке, включая первичные испытания на человеке, испытания по установлению пределов дозировки и испытания на эффективность, на здоровых пациентах и/или на страдающих указанным нарушением, могут быть выполнены по методикам, хорошо известным в клинической и терапевтической областях. Следующие примеры приведены в целях лучшего понимания изобретения и не предназначены и не могут рассматриваться в качестве ограничивающих изобретение, сформулированноев приложенной формуле изобретения. Пример 1. N-(Бензо[b]тиен-3-илметил)сульфамид (соединение 1). Тианафтен-3-карбоксальдегид (1,62 г, 10,0 ммоль) растворяют в безводном этаноле (50 мл). Добавляют сульфамид (4,0 г, 42 ммоль) и смесь нагревают до температуры кипения с обратным холодильником в течение 16 ч. Смесь охлаждают до комнатной температуры. Добавляют натрийборгидрид (0,416 г,11,0 ммоль) и смесь перемешивают при комнатной температуре в течение 3 ч. Реакционную смесь разбавляют водой (50 мл) и экстрагируют хлороформом (375 мл). Экстракты концентрируют и очищают хроматографией (5% метанол в DCM), получая указанное в заголовке соединение в виде белого твердого вещества. 1(5-Хлор-1-бензотиофен-3-ил)метиламин (0,820 г, 4,15 ммоль) и сульфамид (2,5 г, 26 ммоль) объединяют в безводном диоксане (50 мл) и смесь нагревают до температуры кипения с обратным холодильником в течение 4 ч. Реакционную смесь охлаждают и разбавляют водой (50 мл). Раствор экстрагируют хлороформом (375 мл). Экстракты концентрируют и очищают хроматографией (5% метанол в DCM),получая указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (ДМСО-d6):8,05 (2 Н, м), 7,74 (1 Н, с), 7,40 (1 Н, д, J=6,5 Гц), 7,07 (1 Н, т, J=6,3 Гц), 6,72N-Метилиндол-3-карбоксальдегид (1,66 г, 10,4 ммоль) растворяют в безводном этаноле (50 мл). Добавляют сульфамид (4,5 г, 47 ммоль) и смесь нагревают до температуры кипения с обратным холодильником в течение 16 ч. Добавляют дополнительное количество сульфамида (1,0 г, 10,4 ммоль) и смесь нагревают до температуры кипения с обратным холодильником в течение 24 ч. Смесь охлаждают до комнатной температуры. Добавляют натрийборгидрид (0,722 г, 12,5 ммоль) и смесь перемешивают при комнатной температуре в течение 1 ч. Реакционную смесь разбавляют водой (50 мл) и экстрагируютDCM (375 мл). Экстракты концентрируют и добавляют приблизительно 1 мл метанола для образования суспензии, которую фильтруют, получая указанное в заголовке соединение в виде белого порошка. 1 Бензофуран-3-карбоновую кислоту (1,91 г, 11,8 ммоль) суспендируют в безводном DCM (75 мл). Добавляют оксалилхлорид (2,0 М в DCM, 6,48 мл) и затем одну каплю диметилформамида. Раствор перемешивают при комнатной температуре в течение 2 ч, после чего добавляют гидроксид аммония (концентрированный, 10 мл). Полученную смесь разбавляют водой (100 мл) и экстрагируют DCM (3100 мл). Экстракты концентрируют до серого твердого вещества и растворяют в безводном ТГФ (100 мл). Добавляют литийалюмогидрид (1,0 М в ТГФ, 11,8 мл). Смесь перемешивают при комнатной температуре в течение 16 ч. Добавляют минимальное количество насыщенного водного NaHCO3 и затем MgSO4. Смесь фильтруют и затем экстрагируют 1 н. HCl. Водные экстракты доводят до рН 14 с помощью 3 н. NaOH и экстрагируют с помощью DCM. Органические экстракты сушат сульфатом магния и концентрируют до бесцветного масла. Масло растворяют в диоксане (50 мл) и добавляют сульфамид (3,7 г, 38 ммоль). Смесь нагревают до температуры кипения с обратным холодильником в течение 4 ч, охлаждают до комнатной температуры и концентрируют. Полученный твердый продукт очищают хроматографией (5% метанол в DCM), что дает указанное в заголовке соединение в виде светло-желтого твердого вещества. 1 Н-ЯМР (CD3OD):7,53 (1 Н, д, J=5,7 Гц), 7,44 (1 Н, д, J=6,0 Гц), 7,16-7,26 (2 Н, м), 6,73 (1 Н, с), 4,35 5-Фтор-3-метилбензотиофен (1,14 г, 6,83 ммоль), бензоилпероксид (0,165 г, 0,68 ммоль) и Nбромсукцинимид (1,70 г, 7,52 ммоль) объединяют в четыреххлористом углероде (25 мл) и смесь нагревают до температуры кипения с обратным холодильником в течение 3 ч. Желтый раствор охлаждают,разбавляют водой и экстрагируют DCM (250 мл). Экстракты промывают насыщенным раствором соли(100 мл), сушат сульфатом магния и концентрируют до оранжевого твердого вещества. Твердый продукт растворяют в безводном ДМФА. Добавляют азид натрия (4,0 г, 61 ммоль) и смесь перемешивают в течение 16 ч при комнатной температуре. Реакционную смесь разбавляют водой (100 мл) и экстрагируют диэтиловым эфиром (275 мл). Экстракты промывают насыщенным раствором соли (100 мл), сушат сульфатом магния и концентрируют до желтого масла. Масло растворяют в смеси ТГФ (50 мл) и воды (5- 15010977 мл). Добавляют трифенилфосфин (3,60 г, 13,7 ммоль). Смесь перемешивают при комнатной температуре в течение 16 ч. Реакционную смесь концентрируют и очищают хроматографией (2-5% метанол в DCM). Образовавшийся С-(5-фторбензо[b]тиен-3-ил)метиламин (1,04 г, 5,73 ммоль) растворяют в безводном диоксане (50 мл) и добавляют сульфамид (2,75 г, 28,7 ммоль). Реакционную смесь нагревают до температуры кипения с обратным холодильником в течение 4 ч, охлаждают до комнатной температуры и концентрируют до твердого вещества, которое очищают хроматографией (5% метанол в DCM), получая указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (CD3OD):7,85 (1 Н, дд, J=6,6, 3,6 Гц), 7,66 (1 Н, дд, J=7,4, 1,8 Гц), 7,62 (1 Н, с), 7,13-7,18 3-Ацетилтианафтен (3,00 г, 17,0 ммоль) добавляют к смеси муравьиной кислоты (10 мл) и формамида (10 мл). Раствор нагревают до 150 С в течение 8 ч. Реакционную смесь охлаждают до комнатной температуры, разбавляют водой (50 мл) и экстрагируют диэтиловым эфиром (350 мл). Эфирные экстракты промывают насыщенным водным NaHCO3 и насыщенным раствором соли. Раствор концентрируют и очищают хроматографией (5% метанол в DCM), получая N-(1-бензо[b]тиофен-3 илэтил)формамид (1,76 г) в виде белого твердого вещества, которое суспендируют в концентрированнойHCl (30 мл). Смесь нагревают до температуры кипения с обратным холодильником в течение 1,5 ч, затем разбавляют водой (100 мл). Добавляют 3 н. NaOH до рН 14. Смесь экстрагируют диэтиловым эфиром(3100 мл), затем сушат сульфатом магния и концентрируют до оранжевого масла. Масло растворяют в безводном диоксане (75 мл) и добавляют сульфамид. Смесь нагревают до температуры кипения с обратным холодильником в течение 2 ч, затем разбавляют водой (50 мл). Раствор экстрагируют этилацетатомDCM), получая указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (CD3OD):8,01 (1 Н, дд, J=5,5, 0,7 Гц), 7,85 (1 Н, дт, J=6,0, 0,6 Гц), 7,49 (1 Н, с), 7,31-7,40 1-Нафталинметиламин (2,00 г, 12,7 ммоль) и сульфамид (5,0 г, 52 ммоль) объединяют в безводном диоксане (100 мл) и смесь нагревают до температуры кипения с обратным холодильником в течение 6 ч. Реакционную смесь охлаждают до комнатной температуры и фильтруют. Фильтрат концентрируют до твердого вещества и промывают водой до тех пор, пока ТСХ не укажет на отсутствие остаточных следов сульфамида в твердом продукте. Собранный твердый продукт сушат в вакууме, получая указанное в заголовке соединение в виде белого твердого вещества. 1 2-Метилбензофуран-3-карбальдегид (0,51 г, 3,18 ммоль) растворяют в безводном этаноле (25 мл). Добавляют сульфамид (1,5 г, 16 ммоль) и смесь нагревают до температуры кипения с обратным холодильником в течение 4 дней. Смесь охлаждают до комнатной температуры. Добавляют натрийборгидрид(0,132 г, 3,50 ммоль) и смесь перемешивают при комнатной температуре в течение 24 ч. Реакционную смесь разбавляют водой (100 мл) и экстрагируют DCM (375 мл). Экстракты концентрируют, суспендируют в минимальном количестве DCM и фильтруют, получая указанное в заголовке соединение в виде 5-Бромбензотиофен (1,60 г, 7,51 ммоль) и дихлорметилметиловый эфир (1,29 г, 11,3 ммоль) растворяют в безводном 1,2-дихлорэтане (75 мл). Добавляют тетрахлорид титана (2,14 г, 11,3 ммоль), что приводит к потемнению раствора. После выдерживания в течение 1 ч при комнатной температуре реакционную смесь выливают в смесь насыщенного водного NaHCO3 и льда. Смесь перемешивают приблизительно 30 мин и затем экстрагируют DCM (2100 мл). Экстракты концентрируют и очищают хроматографией (0-5% этилацетат в гексане), получая 5-бромбензо[b]тиофен-3-карбальдегид (1,32 г). 5 бромбензотиофен-3-карбоксальдегид (1,20 г, 4,98 ммоль) и сульфамид (4,0 г, 42 ммоль) объединяют в безводном этаноле (25 мл) и нагревают до температуры кипения с обратным холодильником в течение 3 дней. Реакционную смесь охлаждают до комнатной температуры и добавляют натрийборгидрид (0,207 г,5,47 ммоль). Спустя 5 ч добавляют воду (50 мл) и раствор экстрагируют хлороформом (350 мл). Экстракты концентрируют, суспендируют в минимальном количестве DCM и фильтруют, получая указанное в заголовке соединение в виде желтого твердого вещества. 1 Н-ЯМР (ДМСО-d6):8,12 (1 Н, д, J=1,8 Гц), 7,97 (1 Н, д, J=8,6), 7,71 (1 Н, с), 7,52 (1 Н, дд, J=8,6, 1,9 Гц), 7,12 (1 Н, т, J=6,3 Гц), 6,72 (2 Н, с), 4,28 (2 Н, д, J=6,2 Гц). Пример 10. N-[(4-Бромбензо[b]тиен-3-ил)метил]сульфамид (соединение 17). 4-Бромбензотиофен (1,80 г, 8,45 ммоль) и дихлорметилметиловый эфир (1,46 г, 12,7 ммоль) растворяют в безводном DCM (100 мл). Добавляют тетрахлорид титана (2,40 г, 12,7 ммоль), что приводит к потемнению раствора. После выдерживания в течение 30 мин при комнатной температуре реакционную смесь выливают в смесь насыщенного водного NaHCO3 и льда. Смесь перемешивают приблизительно 30 мин и затем экстрагируют DCM (2150 мл). Экстракты концентрируют и очищают хроматографией (015% этилацетат в гексане), получая 4-бромбензотиофен-3-карбоксальдегид (0,910 г). 4-Бромбензотиофен-3-карбоксальдегид (0,910 г, 3,77 ммоль) и сульфамид (3,0 г, 31 ммоль) объединяют в безводном этаноле (25 мл) и нагревают до температуры кипения с обратным холодильником в течение 3 дней. Реакционную смесь охлаждают до комнатной температуры и добавляют натрийборгидрид (0,157 г, 4,15 ммоль). Спустя 5 ч добавляют воду (50 мл) и раствор экстрагируют хлороформом (350 мл). Экстракты концентрируют, суспендируют в минимальном количестве DCM и фильтруют, получая указанное в заголовке соединение в виде желтого твердого вещества. 1 2-Фтортиофенол (4,14 г, 32,6 ммоль) растворяют в безводном ТГФ (100 мл). Добавляют третбутилат калия (1,0 М в ТГФ, 35,8 мл) и суспензию перемешивают при комнатной температуре в течение 15 мин. Добавляют диметилацеталь 2-хлорацетальдегида и смесь перемешивают в течение 3 дней. До- 17010977 бавляют воду (100 мл) и раствор экстрагируют диэтиловым эфиром (3100 мл). Экстракты концентрируют до желтого масла и очищают хроматографией (5-20% этилацетат в гексане), получая 1-(2,2 диметоксиэтилсульфанил)-2-фторбензол (6,42 г) в виде бесцветного масла. Хлорбензол (25 мл) нагревают до температуры кипения с обратным холодильником и добавляют полифосфорную кислоту (1 мл). Затем добавляют 1-(2,2-диметоксиэтилсульфанил)-2-фторбензол, что приводит к медленному потемнению раствора. После нагревания в течение 3 ч реакционную смесь охлаждают до комнатной температуры и разбавляют водой (50 мл). Раствор экстрагируют бензолом (250 мл). Экстракты концентрируют и очищают хроматографией (0-15% этилацетат в гексане), получая 7-фторбензотиофен (0,77 г). 7 Фторбензотиофен (0,77 г, 5,1 ммоль) и дихлорметилметиловый эфир (0,872 г, 7,6 ммоль) растворяют в безводном DCM (25 мл). Добавляют тетрахлорид титана (1,0 М в DCM, 7,6 мл, 7,6 ммоль), что приводит к потемнению раствора. После выдерживания в течение 30 мин при комнатной температуре реакционную смесь выливают в смесь насыщенного водного NaHCO3 и льда. Смесь перемешивают приблизительно 30 мин и затем экстрагируют DCM (250 мл). Экстракты концентрируют и очищают хроматографией (015% этилацетат в гексане), получая 7-фторбензотиофен-3-карбоксальдегид (0,642 г). 7 Фторбензотиофен-3-карбоксальдегид (0,642 г, 3,77 ммоль) и сульфамид (1,7 г, 18 ммоль) объединяют в безводном этаноле (20 мл) и нагревают до температуры кипения с обратным холодильником в течение 3 дней. Реакционную смесь охлаждают до комнатной температуры и добавляют натрийборгидрид (0,148 г,3,92 ммоль). Спустя 2 ч добавляют воду (25 мл) и раствор экстрагируют хлороформом (325 мл). Экстракты концентрируют, суспендируют в минимальном количестве DCM и фильтруют, получая указанное в заголовке соединение в виде желтого твердого вещества. 1 Н-ЯМР (ДМСО-d6):7,78 (1 Н, д, J=8,0 Гц), 7,43-7,50 (1 Н, м), 7,27 (1 Н, дд, J=10,3, 7,9 Гц), 7,14 (1 Н,т, J=6,4 Гц), 6,74 (2 Н, шир. с), 4,31 (2 Н, д, J=6,4 Гц). Пример 12. N-[(4-Трифторметилбензо[b]тиен-3-ил)метил]сульфамид (соединение 19). 4-Трифторметилбензотиофен (0,27 6 г, 1,37 ммоль) и дихлорметилметиловый эфир (0,236 г, 2,06 ммоль) растворяют в безводном DCM (10 мл). Добавляют тетрахлорид титана (1,0 М в DCM, 2,1 мл, 2,1 ммоль), что приводит к потемнению раствора. После выдерживания в течение 30 мин при комнатной температуре реакционную смесь выливают в смесь насыщенного водного NaHCO3 и льда. Смесь перемешивают приблизительно 30 мин и затем экстрагируют DCM (225 мл). Экстракты концентрируют и очищают хроматографией (0-15% этилацетат в гексане), получая 4-трифторметилбензотиофен-3 карбоксальдегид. 4-Трифторметилбензотиофен-3-карбоксальдег (0,226 г, 0,982 ммоль) и сульфамид (0,471 г, 4,91 ммоль) объединяют в безводном этаноле (5 мл) и нагревают до температуры кипения с обратным холодильником в течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и добавляют натрийборгидрид (0,056 г, 1,47 ммоль). Спустя 5 ч добавляют воду (10 мл) и раствор экстрагируют хлороформом (310 мл). Экстракты концентрируют и очищают хроматографией (5% метанол в DCM), получая указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (ДМСО-d6):8,30 (1 Н, с), 8,25 (1 Н, д, J=8,4 Гц), 7,84 (1 Н, с), 7,68 (1 Н, дд, J=8,5, 1,4 Гц),6,7-6,9 (2 Н, шир. с), 4,4-4,5 (1 Н, шир. с), 4,37 (2 Н, с). Пример 13. N-[(4-Цианобензо[b]тиен-3-ил)метил]сульфамид (соединение 20). 4-Цианобензотиофен (1,15 г, 7,22 ммоль) и дихлорметилметиловый эфир (1,25 г, 10,8 ммоль) растворяют в безводном DCM (100 мл). Добавляют тетрахлорид титана (1,0 М в DCM, 10,8 мл, 10,8 ммоль),что приводит к потемнению раствора. После выдерживания в течение 30 мин при комнатной температуре реакционную смесь выливают в смесь насыщенного водного NaHCO3 и льда. Смесь перемешивают приблизительно 30 мин и затем экстрагируют DCM (250 мл). Экстракты концентрируют и очищают хроматографией (0-15% этилацетат в гексане), получая 4-цианобензотиофен-3-карбоксальдегид. 4-Цианобензотиофен-3-карбоксальдег (0,298 г, 1,59 ммоль) и сульфамид (0,766 г, 7,97 ммоль) объединяют в безводном этаноле (20 мл) и нагревают до температуры кипения с обратным холодильником в- 18010977 течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и добавляют натрийборгидрид(0,091 г, 2,39 ммоль). Спустя 5 ч добавляют воду (20 мл) и раствор экстрагируют хлороформом (320 мл). Экстракты концентрируют и очищают хроматографией (5% метанол в DCM), получая указанное в заголовке соединение в виде белого твердого вещества. 1N-[(Бензо[b]тиен-3-ил)метил]сульфамид (0,250 г, 1,03 ммоль) и пирролидин (0,25 мл) объединяют в безводном диоксане (5 мл) и нагревают до температуры кипения с обратным холодильником в течение 32 ч. Реакционную смесь упаривают и очищают хроматографией, используя 5% метанол в DCM, что дает указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (CDCl3):7,84-7,89 (2 Н, м), 7,38-7,45 (3H, м), 4,49 (3H, шир. с), 3,25 (4 Н, т, J=4,0 Гц), 1,80N-[(Бензо[b]тиен-3-ил)метил]сульфамид (0,250 г, 1,03 ммоль) и этиламин (70% в H2O, 0,10 мл) объединяют в безводном диоксане (5 мл) и нагревают до температуры кипения с обратным холодильником в течение 32 ч. Реакционную смесь упаривают и очищают хроматографией, используя 5% метанол в DCM,что дает указанное в заголовке соединение в виде белого твердого вещества. 1 Н-ЯМР (CDCl3):7,83-7,90 (2 Н, м), 7,36-7,47 (3H, м), 4,51 (2 Н, с), 2,90 (2 Н, кв., J=7 Гц), 1,03 (3H, т,J=7 Гц). Пример 16. [(Бензо[b]тиен-3-ил)метил]амид имидазол-1-сульфоновой кислоты (соединение 102). 3-Бензотиенилметиламин и 3-(имидазол-1-сульфонил)-1-метил-3H-имидазол-1-ийтрифлат объединяют в безводном ацетонитриле. Раствор перемешивают при комнатной температуре в течение ночи,концентрируют и очищают хроматографией (5% метанол в DCM), получая указанное в заголовке соединение в виде желтовато-коричневого твердого вещества. 1H-ЯМР (ДМСО-d6):8,05 (1 Н, дд, J=7,0, 1,6 Гц), 7,99 (1 Н, дд, J=7,1, 1,7 Гц), 7,85 (1 Н, с), 7,66 (1 Н,с), 7,42-7,65 (5 Н, м), 4,34 (2 Н, с). Пример 17. Испытание in vivo: тест максимального электрошока (MES). Противоконвульсивную активность определяют, используя MES тест, осуществляемый согласно методике, описанной подробно ниже. Swinyard E.A., Woodhead J.H., White H.S., Franklin M.R. Experimental selection, quantification, and evaluation of anticonvulsants. В Levy R.H., et al., eds. Antiepileptic Drugs. 3rdCF-1 самцов мышей-альбиносов (25-35 г) выдерживают голодными в течение 16 ч до тестирования. Мышей произвольно делят на контрольную и испытуемую группы, в которых животным дозированно вводят, варьируя концентрации, растворитель или испытуемое соединение соответственно. На день ис- 19010977 пытания за 30 мин до шока мышам орально дозированно вводят растворитель (0,5% метилцеллюлоза) или испытуемое соединение (100-300 мг/кг). Припадки вызывают путем транскорнеального электрошока, используя переменный ток 60 Гц, 50 мА, подаваемый в течение 0,2 с. Мышей в испытуемых группах подвергают воздействию электрического раздражителя при интервалах времени от 15 мин до 4 ч после введения испытуемого соединения. Шок приводит к немедленному тоническому вытяжению всего тела. Испытание завершают после наблюдения полного цикла конвульсии (обычно менее 1 мин после электростимуляции) и после этого сразу же применяют к мышам эйтаназию посредством ингаляционного воздействия углекислого газа. Устранение компонента припадка, выражающегося в тоническом вытяжении всего тела, принимают за конечную точку тестирования. Отсутствие этого компонента свидетельствует о том, что испытуемое соединение обладает способностью предупреждать распространение разряда припадка через нервную ткань. Значение ED50 для испытуемого соединения (рассчитанное, когда целесообразно) соответствует расчетной дозе, требуемой для блокирования тонического экстензорного компонента задней конечности испытуемого грызуна при MES-индуцируемом припадке на 50%. Пробит-анализ используют для расчетаED50 и 95% доверительных пределов (FL). Характерные соединения по настоящему изобретению тестируют по вышеуказанной методике, результаты приведены в табл. 3 ниже. Результаты представлены в виде соотношения (число мышей с полностью предупрежденным тоническим вытяжением всего тела)/(общее число испытуемых мышей) (за заданный период). Таблица 3- 20010977 Пример 18. В качестве конкретного варианта оральной композиции 100 мг соединения 1, полученного по примеру 1, смешивают с достаточно тонкоизмельченной лактозой, обеспечивая суммарное количество от 580 до 590 мг для заполнения твердой желатиновой капсулы размера О. Хотя в приведенном выше описании изложены основные принципы настоящего изобретения, сопровождаемые в целях иллюстрации примерами, ясно, что практическое осуществление изобретения охватывает все возможные изменения, адаптации и/или модификации, входящие в объем приложенной формулы изобретения, а также ее соответствующих эквивалентов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I)R2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород и С 1-4 алкил; альтернативно, R3 и R4 вместе с атомом азота, с которым связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемая соль указанного соединения. 2. Соединение по п.1, гдеR2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород, метил и этил; или фармацевтически приемлемая соль указанного соединения. 3. Соединение по п.2, гдеR2 означает водород; каждый из R3 и R4 независимо выбирают из группы, включающей водород и этил; или фармацевтически приемлемая соль указанного соединения. 4. Соединение по п.3, гдеR2 означает водород; каждый из R3 и R4 означает водород; альтернативно, R3 означает водород и R4 означает этил; или фармацевтически приемлемая соль указанного соединения. 5. Соединение по п.1, гдеR3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемая соль указанного соединения. 6. Соединение по п.5, гдеR3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-6-членную, насыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-2 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемая соль указанного соединения. 7. Соединение по п.6, где R1 означает водород;R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-членную кольцевую структуру,выбираемую из группы, включающей пирролидинил и имидазолил; или фармацевтически приемлемая соль указанного соединения. 8. Соединение по п.2, выбираемое из группы, включающей[(бензо[b]тиен-3-ил)метил]амид имидазол-1-сульфоновой кислоты и фармацевтически приемлемые соли указанных соединений. 9. Соединение по п.8, выбираемое из группы, включающей N-(бензо[b]тиен-3-илметил)сульфамид;N-[(5-фторбензо[b]тиен-3-ил)метил]сульфамид и фармацевтически приемлемые соли указанных соединений. 10. Соединение, выбираемое из группы, включающей N-(бензо[b]тиен-3-илметил)сульфамид и фармацевтически приемлемые соли указанного соединения. 11. Соединение, выбираемое из группы, включающей и фармацевтически приемлемые соли указанного соединения. 12. Соединение формулы (I)R2 выбирают из группы, включающей водород и метил; каждый из R3 и R4 независимо выбирают из группы, включающей водород и метил; альтернативно, R3 и R4 вместе с атомом азота, с которым они связаны, образуют 5-7-членную, насыщенную, частично ненасыщенную или ароматическую кольцевую структуру, необязательно содержащую 1-3 дополнительных гетероатома, независимо выбираемых из группы, включающей О, N и S; или фармацевтически приемлемая соль указанного соединения. 13. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и соединение по п.1. 14. Фармацевтическая композиция, полученная смешением соединения по п.1 и фармацевтически приемлемого носителя. 15. Способ получения фармацевтической композиции, включающий смешение соединения по п.1 и фармацевтически приемлемого носителя. 16. Способ лечения эпилепсии или связанных с эпилепсией нарушений, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения по п.1. 17. Способ лечения эпилепсии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения по п.1. 18. Способ по п.16, где связанное с эпилепсией нарушение означает эссенциальное дрожание или синдром беспокойных конечностей. 19. Применение соединения по п.1 при получении лекарственного средства для лечения эпилепсии или связанных с эпилепсией нарушений у нуждающегося в этом субъекта.
МПК / Метки
МПК: C07D 333/58, A61K 31/343, C07D 307/81, A61K 31/381, A61K 31/404, A61P 25/08, C07D 209/14
Метки: качестве, производные, полезные, бензоконденсированные, противоконвульсивных, средств, гетероарилсульфамидные
Код ссылки
<a href="https://eas.patents.su/24-10977-benzokondensirovannye-geteroarilsulfamidnye-proizvodnye-poleznye-v-kachestve-protivokonvulsivnyh-sredstv.html" rel="bookmark" title="База патентов Евразийского Союза">Бензоконденсированные гетероарилсульфамидные производные, полезные в качестве противоконвульсивных средств</a>
Предыдущий патент: Композиция, содержащая вещества, регулирующие рост и/или развитие растений, и способы ее применения
Следующий патент: Гербицидные смеси с синергическим действием
Случайный патент: Инсектицидные фенил- или пиридилпиперидины