Комбинация инсулина с триазиновыми производными и их применение для лечения диабета
Формула / Реферат
1. Комбинация для применения в качестве лекарственного средства, включающая инсулин и соединение формулы I и/или его физиологически приемлемую соль, где соединение формулы I определено как следующее:
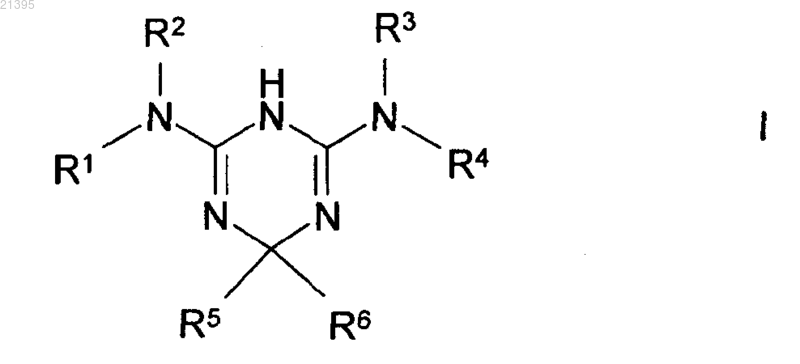
где R1, R2, каждый независимо друг от друга, означают Н или A;
R3, R4, каждый независимо друг от друга, означают Н или A;
R5, R6, каждый независимо друг от друга, означают Н или A;
А означает неразветвленный или разветвленный алкил, имеющий 1-10 атомов C, в котором 1-7 атомов Н могут быть замещены F, или циклический алкил, имеющий 3-7 атомов C.
2. Фармацевтическая комбинация, содержащая в качестве активных компонентов эффективное количество инсулина в комбинации с эффективным количеством по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли, вместе с одним или несколькими фармацевтически приемлемыми адъювантами.
3. Комбинация по п.1 или 2, где соединение формулы I представляет собой 2-амино-3,6-дигидро-4-диметиламино-6-метил-1,3,5-триазин.
4. Комбинация по любому из пп.1-3 для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину.
5. Комбинация по п.4, где заболевание выбрано из группы, включающей диабет, предиабет, низкую толерантность к глюкозе, гипергликемию, метаболический синдром, диабетическую нефропатию, невропатию, ретинопатию, атеросклероз и сердечно-сосудистое заболевание, предпочтительно инсулинзависимый сахарный диабет и неинсулинзависимый сахарный диабет.
6. Комбинация по любому из пп.1-5 для перорального или парентерального введения предпочтительно в виде раствора для инъекций для парентерального введения.
7. Комбинация по любому из пп.1-6, где инсулин находится в фиксированной комбинации с соединением формулы I в одной единице дозирования.
8. Комбинация по любому из пп.1-6, где инсулин и соединение формулы I находятся в отдельных единицах дозирования в одной упаковке.
9. Применение инсулина в комбинации по меньшей мере с одним соединением формулы I, определенным в п.1, и/или его физиологически приемлемой солью для получения лекарственного средства для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину.
10. Применение инсулина в комбинации по меньшей мере с одним соединением формулы I, определенным в п.1, и/или его физиологически приемлемой солью для улучшения гомеостазиса глюкозы.
11. Применение по п.9 или 10, где толерантность к глюкозе и/или секреция инсулина увеличивается в ответ на глюкозу.
12. Применение по любому из пп.9-11, где соединение формулы I вводят в дозировке от 25 до 200 мг/кг массы тела.
13. Применение по любому из пп.9-12, где инсулин и соединение формулы I используются в форме для одновременного или последовательного введения.
14. Способ лечения заболеваний, которые связаны с резистентностью к инсулину, в котором эффективное количество инсулина в комбинации с эффективным количеством по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли вводят млекопитающему, которое нуждается в таком лечении.
15. Фармацевтический набор для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину, включающий в качестве активных компонентов эффективное количество инсулина вместе с одним или несколькими фармацевтически приемлемыми адъювантами в первой единице дозирования и эффективное количество по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли вместе с одним или несколькими фармацевтически приемлемыми адъювантами во второй единице дозирования.
Текст
КОМБИНАЦИЯ ИНСУЛИНА С ТРИАЗИНОВЫМИ ПРОИЗВОДНЫМИ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА Изобретение относится к комбинации для применения в качестве лекарственного средства,включающей инсулин и соединение формулы I где R1, R2, каждый независимо друг от друга, означают H или A; R3, R4, каждый независимо друг от друга, означают H или A; R5, R6, каждый независимо друг от друга, означают H илиA; A означает неразветвлнный или разветвлнный алкил, имеющий 1-10 атомов C, в котором 1-7 атомов Н могут быть замещены F, или циклический алкил, имеющий 3-7 атомов С, и/или его физиологически приемлемую соль. Другой объект изобретения касается фармацевтической комбинации, содержащей в качестве активных компонентов эффективные количества инсулина и по меньшей мере одно соединение формулы (I), вместе с фармацевтически приемлемыми адъювантами, для профилактического или терапевтического лечения и/или мониторинга физиологических и/или патологических состояний, которые связаны с резистентностью к инсулину. Изобретение также относится к фармацевтическому набору, содержащему инсулин в первой единице дозирования и по меньшей мере одно соединение формулы (I) во второй единице дозирования. Изобретение относится к композиции для применения в качестве лекарственного средства, включающего инсулин в комбинации по меньшей мере с одним соединением формулы I где радикалы R1-R6 имеют значения согласно п.1,и/или их физиологически приемлемые соли. Другой объект изобретения касается фармацевтической композиции, содержащей в качестве активных компонентов эффективные количества инсулина и по меньшей мере одного соединение формулы I,вместе с фармацевтически приемлемыми адъювантами, для профилактического или терапевтического лечения и/или мониторинга физиологических и/или патологических состояний, которые связаны с резистентностью к инсулину (ИР). Изобретение также относится к фармацевтическому набору, содержащему инсулин в первой единице дозирования и по меньшей мере одно соединение формулы I во второй единице дозирования. Нарушения обмена веществ, такие как ожирение, ИР и дислипидемия, являются развивающимися как доминантные причины заболеваемости и смертности в мировых масштабах. Особенно в течение последних десятилетий ИР стала очень распространенным состоянием в широких массах людей, с огромными последствиями для системы здравоохранения. ИР определяется как сниженная, несоответствующая реакция тела к нормальному влиянию инсулина. ИР является важным фактором риска для развития сердечно-сосудистой болезни и сахарного диабета II типа (T2DM). Диабет представляет собой хроническую болезнь с множеством патологических проявлений. Он сопровождается нарушениями липидного и сахарного метаболизма так же, как и нарушения кровообращения. К тому же, ИР связана с различными сердечно-сосудистыми факторами риска (например, ожирением, дислипидемией, гипертензией и нарушениями свертываемости крови), которые потом проявляются совместно, упомянутые как метаболический синдром или синдром X. Таким образом, синдром резистентности к инсулину (синдром X) особенно характеризуется уменьшением влияния инсулина (Presse Mdicale (1997), 26(14): 671-677) и включается в множество патологических состояний, как упомянутые выше, в частности диабет, конкретнее неинсулинзависимый диабет, но в дополнение постоянные сердечно-сосудистые осложнения, например атеросклероз, или микрососудистые осложнения, например ретинопатии, нефропатии и невропатии. Сейчас есть большое число данных, что ИР может быть объединяющим причинным фактором, лежащим в основе метаболического синдрома (TurnerHellerstein (2005) Curr Opin Drug DiscoveryDevelop 8(1): 115-126). Современные терапевтические воздействия нацелены на непосредственное увеличение инсулиновой реактивности тканей, применяя триазолидиндионы (TZD). Однако в то время как TZD, как показано,увеличивают инсулиновую чувствительность всего тела, они в последнее время, как стало известно, увеличивают риск сердечной недостаточности. Поэтому для лечения ИР являются необходимыми альтернативы в борьбе против растущей эпидемии болезней нарушения обмена веществ, с одной из их особенностей, являющейся ИР. Также известно, что инсулин применяют как агент для лечения диабета I типа (или инсулинозависимого диабета). Инсулин также применяется как гипогликемический агент в лечении инсулиннезависимого диабета. Предыдущий уровень техники ЕР 0193256 и ЕР 0207581 соответственно изучает производные триазолидин-2,4-диона как антигипергликемические и гиполипидемические, а также соединения,которые были раскрыты как антидиабетические агенты. Эти соединения являются дополнительными активаторами у рецептора, активируемого пролифератором пероксисом (PPAR). Комбинации определенных PPAR производных триазолидин-2,4-диона, таких как росиглитазон, с инсулином также были описаны для лечения диабета SmithKline Beecham в заявке на патент WO 1998/57636. Однако дозы инсулина остаются на высоком уровне и сопровождаются увеличением массы. Поэтом, технической проблемой, формирующей основу настоящего изобретения, является обеспечить фармацевтическую композицию, позволяющую эффективное применение в предупреждении или терапии заболевания, которое вызвано резистентностью к инсулину, особенно такие композиции, которые улучшают терапевтическую эффективность и минимизируют побочные воздействия. Настоящее изобретение решает эту проблему обеспечением композиции для применения как лекарственного средства, содержащего инсулин в комбинации по меньшей мере с одним соединением формулы I и/или его физиологически приемлемыми солями, где соединение формулы I определяется как следующие: в которой R1, R2, каждый независимо друг от друга, означают H или A;R3, R4, каждый независимо друг от друга, означают H, A, алкенил, имеющий 2-6 атомов C, алкинил,имеющий 2-6 атомов C, Ar или Het;R5 и R6 вместе также означают алкилен, имеющий 2, 3, 4 или 5 атомов C;R5, R6, каждый независимо друг от друга, означают H, A, (CH2)nAr, (CH2)mOAr, (CH2)mOA илиR5 и R6 вместе также означают алкилен, имеющий 2, 3, 4 или 5 атомов C, в котором одна группа СН 2 может быть замещена О, NH или NA и/или в которой один атом Н может быть замещен OH;Ar означает фенил, нафтил или бифенил, каждый из которых незамещен или моно-, ди- или тризамещен Hal, A, OA, OH, COOH, COOA, CN, NH2, NHA, NA2, SO2A и/или COA;Het означает моно-, би- или трициклический насыщенный, ненасыщенный или ароматический гетероцикл, имеющий 1-4 атома N, О и/или S, которые могут быть незамещены или моно-, ди- или тризамещены Hal, A, OH, OA, NH2, (CH2)nAr, NHA, NA2, COOH, COOA и/или =O (карбонильный кислород); А означает неразветвленный или разветвленный алкил, имеющий 1-10 атомов C, в котором 1-7 атомов Н могут быть замещены F, или циклический алкил, имеющий 3-7 атомов C;n равно 0, 1 или 2. Неожиданно было продемонстрировано изобретателями, что триазиновые соединения формулы I и их производные могут быть применены как активные ингредиенты в фармацевтической композиции,комбинированной с инсулином, для того, чтобы блокировать медицинские показания, возникающие от ИР, такие как диабет и заболевания, связанные с ним. После подачи заявки на данное изобретение было известно только, что соединения формулы I могут быть приготовлены способами соответственноWO 2001/55122. Соединения формулы I должны быть полезными в лечении заболеваний, вызванных синдромом ИР. Образцы в данный момент находятся под клиническим наблюдением. Однако сейчас комбинация упомянутых производных триазина с инсулином, лежащая в основании изобретения, как было найдено, синергично действует в улучшении регулирования метаболизма глюкозы. Настоящее изобретение показывает сильное улучшение гомеостаза глюкозы. Эти явления стимулируются воздействием композиции инсулина с соединениями формулы I, которая формирует основу изобретенного комбинированного средства для таких упомянутых клинических картин, как инсулинзависимый сахарный диабет(ИЗСД), инсулиннезависимый сахарный диабет (ИНЗСД) и метаболический синдром. Сама по себе композиция изобретения показывает очень важные фармакологические свойства и хорошую переносимость. В сравнении со стандартной инсулиновой терапией дозы инсулина, которые должны быть введены, могут быть значительно уменьшены, если комбинировать с производным триазина формулы I, при этом предупреждено увеличение массы при любой дозе композиции, как проверено в доклинических испытаниях. Следовательно, вышеупомянутые композиции представляют новое комбинированное лекарственное средство, которое является хорошо подходящим для профилактики, лечения и/или мониторинга ИР и/или ИР-обусловленных болезней. Более конкретно, изобретенная композиция дает сильнодействующее антидиабетическое лекарство для большого числа пациентов. Указанные биологически активные вещества композиции изобретения могут быть определены способами, известными специалистам в данной области. Подходящими животными для эксперимента являются, например, мыши, крысы, морские свинки,собаки, коты, приматы или свиньи. Золотым стандартом для in vivo исследований ИР является эугликемический-гиперинсулинемический глюкозный фиксатор. Другими инструментами являются гомеостатическое модельное исследование резистентности к инсулину (HOMA-IR) или зачастую тест на толерантность к глюкозе, отобранный перорально (FSOGTT300-22), в котором 300-22 позиций на протяжении 300 мин с 22 образцами. Способы, которые являются подходящими, чтобы определить изменения в чувствительности к инсулину, должны быть чувствительными, воспроизводимыми, простыми в оперативном отношении и с относительно высокой пропускной способностью. Недавно разработанный, дейтеризованный тест размещения глюкозы (2H-GDT), включающий устойчивую изотоп-массовую спектральную оценку гликолиза целого тела, позволяет оценку ИР путем измерения 2 Н 2 О-продукта на единицу плазмы инсулинглюкоза, который основан на темпе выпуска дейтерия (2 Н) из (пероральной) загрузки животного или человека дейтеризованной [6,6'-2 Н 2]глюкозой и установленными концентрациями инсулина плазмы (TurnerHellerstein (2005), Curr. Opin. Drug.DiscoveryDevelop 8(1): 115-126). К тому же, может быть оценена степень компенсации панкреатической -клетки к ИР путем измерения абсолютного 2H2O продукта, достигнутая после загрузки[6,6'-2 Н 2]глюкозы. Соответствие панкреатической компенсации может быть оценено различением между гликолитическим размещением на единицу окружающего инсулина (отражающий чувствительность инсулина) и абсолютным темпом достигнутого использования глюкозы (отражение панкреатической компенсации ИР). 2H-GDT разработан, чтобы придерживаться следующих принципов:i) окружающие концентрации глюкозы и инсулина должны отразить метаболические условия, физиологически релевантные;ii) тест должен измерить установленное инсулином использование глюкозы тканями и показать ИР в установленных моделях иiii) метод должен отразить сопоставимые метаболические условия, как другие тесты ИР, которые,как доказывают, являются прогнозирующими для сердечно-сосудистых результатов и риска T2DM. Концентрации инсулина сыворотки в "динамическом диапазоне" между основными и максимальными условиями использования глюкозы выполняют эти критерии (Beysen et al. (2007), Diab. Care,30:1143-1149). Кроме того, 2H-GDT, который измеряет гликолиз целого тела у животных или людей количественным образом, сильно коррелирует с эугликемичной-гиперинсулинемичной глюкозной скобкой. Использование сказанного кинетического испытания, следовательно, предпочтено в пределах изобретения, чтобы определить in vivo действие агента на чувствительность инсулина, так же как инсулина компенсационные ответы, в особенности в относительно высокой пропускной способности и во многих обычно используемых преклинических моделях животных. К тому же, 2H-GDT является абсолютно переводным в клиническое урегулирование с подобной степенью простоты и пропускной способности. В значении настоящего изобретения соединение формулы I определяется, чтобы включить фармацевтически приемлемые производные, включающие сольваты, пролекарства, таутомеры, энантиомеры,рацематы и их стереоизомеры, включая их смеси во всех соотношениях. Предпочтение отдается сольватам и/или физиологически приемлемым солям, более предпочтительно физиологически приемлемым солям, наиболее предпочтительно физиологически приемлемым солям присоединения кислоты. Термин "сольваты" производных триазина подразумевает добавки молекул инертного растворителя к соединениям, которые сформированы их взаимной силой притяжения. Сольватами являются, например, моно- или дигидраты или алкоголяты. Термин "пролекарство" подразумевает соединения соответственно изобретению, которые могут быть модифицированы посредством, например, алкильных или ацильных групп, сахаров или олигопептидов и которые быстро расщепляются в организме, чтобы сформировать эффективные соединения соответственно изобретению. Они также включают биоразрушаемые полимерные производные соединений соответственно изобретению, как описано, например, в Int. J. Pharm. 115: 61-67 (1995). Соединение изобретения может быть получено его выделением из его функциональных производных сольволизом, в частности гидролизом, или гидрогенизацией. Подобное возможно для соединений изобретений, находящихся в форме любых необходимых пролекарств, таких как сложные эфиры, карбонаты, карбаматы, мочевины, амиды или фосфаты, в этом случае собственно биологически активная форма освобождается только через метаболизм. Любое соединение, которое может быть превращено in vivo, чтобы обеспечить биоактивный агент (т.е. соединения изобретения), является пролекарством в рамках сущности и объема изобретения. Различные формы пролекарств хорошо известны в области техники и описаны (например,Wermuth et al. (1996), The Practice of Medicinal Chemistry, Chapter, 31: 671-696, Academic Press; Bundgaard,H. (1985), Design of Prodrugs, Elsevier; Bundgaard, H. (1991), A Textbook of Drug Design and Development,Chapter 5: 131-191, Harwood Academic Publishers). Дополнительно известно, что химические вещества превращаются в теле в метаболиты, которые могут, где предназначено, аналогично выделять необходимый биологический эффект - в некоторых обстоятельствах даже в более явной форме. Любое биологически активное соединение, которое превращается метаболизмом in vivo из любого соединения изобретения, является метаболитом в рамках сущности и объема изобретения. Соединения изобретения могут быть представлены в форме их изомеров двойной связи как чистые Е- или Z-изомеры или в форме смесей этих изомеров двойной связи. Где возможно, соединения изобретения могут быть в форме таутомеров, таких как кетоэнольные таутомеры. Формула I также охватывает оптически активные формы (стереоизомеры), такие как энантиомеры. Все стереоизомеры соединений изобретения предусмотрены в смеси, или в чистом состоянии, или в практически чистом виде. Соединения изобретения могут иметь асимметрические центры возле любых атомов углерода. Следовательно, они могут существовать в форме их рацематов, в форме чистых энантиомеров и/или диастеомеров или в форме смесей их энантиомеров и/или диастеомеров. Смеси могут иметь любое необходимое соотношение смеси стереоизомеров. Например, соединения изобретения, которые имеют один или более центров хиральности и которые встречаются в виде рацематов или в виде смесей диастереомеров, которые могут быть разделены по сути известными способами, на их оптически чистые изомеры, т.е. энантиомеры или диастереомеры. Соединения изобретения можно совершить разделением на колонке на хиральные или нехиральные фазы, или перекристаллизацией из оптически активного растворителя по выбору, или применением оптически активной кислоты или основания, или получением производных с оптически активным реагентом, таким как, например, оптически активный спирт, и последующим отщеплением радикала. Изобретение также относится к применению смесей соединений согласно изобретению, например смесей двух диастереомеров, например, в соотношении 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000. Они являются особенно предпочтительно смесями стереоизомерных соединений. Композиция может также содержать смеси соединения и, по меньшей мере, единственного производного или смеси производных соответственно, которые могут содержать сольваты и/или соли для примера. Номенклатура, как использовано здесь для определения соединений, особенно соединений согласно изобретению, в общем основана на правилах IUPAC-организации для химических соединений и особенно органических соединений. Термины, всегда указанные для объяснения вышеупомянутых соединений изобретения, если явно не обозначено иначе в описании или в формуле, имеют следующие значения. Выше и ниже, радикалы R1, R2, R3, R4, R5, R6 имеют значения, указанные для формулы I, если явно не обозначено иначе. А означает алкил, который является неразветвленным (линейный) или разветвленным и имеет 1, 2,3, 4, 5, 6, 7, 8, 9 или 10 атомов C. А предпочтительно означает метил, кроме того, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил, кроме того также пентил, 1-, 2- или 3-метилбутил, 1,1-,1,2- или 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3-или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3 или 3,3-диметилбутил, 1- или 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил, также предпочтительно, например, трифторметил. Кроме того, А предпочтительно означает алкил, имеющий 1, 2, 3, 4, 5 или 6 атомов C, более предпочтительно метил, этил, пропил,изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, трифторметил, пентафторэтил или 1,1,1-трифторэтил. Очень особенно предпочтительно А означает метил. Циклический алкил (циклоалкил) предпочтительно означает циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Алкенил имеет 2, 3, 4, 5 или 6 атомов C и предпочтительно означает винил или пропенил. Алкинил имеет 2, 3, 4, 5 или 6 атомов C и предпочтительно означает ССН или СС-СН 3.Ar означает, например, о-, м- или п-толил, о-, м- или п-этилфенил, о-, м- или п-пропилфенил, о-, мили п-изопропилфенил, о-, м- или п-трет-бутилфенил, о-, м- или п-гидроксифенил, о-, м- или паминофенил, о-, м- или п-(N-метиламино)фенил, о-, м- или п-(N-метиламинокарбонил)фенил, о-, м- или п-метоксифенил, о-, м- или п-этоксифенил, о-, м- или п-этоксикарбонилфенил, о-, м- или п-(N,N-диметиламино)фенил, о-, м- или п-(N-этиламино)фенил, о-, м-или п-(N,N-диэтиламино)фенил, о-,м- или п-фторфенил, о-, м- или п-бромфенил, о-, м- или п-хлорфенил, о-, м- или п-(метилсульфонил)фенил, о-, м- или п-цианофенил, о-, м- или п-карбоксифенил, о-, м- или п-метоксикарбонилфенил, о-, м- или п-ацетилфенил, также предпочтительно 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дифторфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дихлорфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дибромфенил, 2,4- или 2,5-динитрофенил, 2,5- или 3,4-диметоксифенил, 3-амино-4-хлор-, 2-амино-3 хлор-, 2-амино-4-хлор-, 2-амино-5-хлор- или 2-амино-6-хлорфенил, 2,3-диаминофенил, 2,3,4-, 2,3,5-,2,3,6-, 2,4,6- или 3,4,5-трихлорфенил, 2,4,6-триметоксифенил, 2-гидрокси-3,5-дихлорфенил, п-йодфенил,3,6-дихлор-4-аминофенил,4-фтор-3-хлорфенил,2-фтор-4-бромфенил,2,5-дифтор-4-бромфенил,3-бром-6-метоксифенил, 3-хлор-6-метоксифенил, 3-фтор-4-метоксифенил, 3-амино-6-метилфенил или 2,5-диметил-4-хлорфенил. Ar особенно предпочтительно означает фенил, гидроксифенил или метоксифенил. Независимо от дополнительных заместителей, Het означает, например, 2- или 3-фурил, 2- или 3-тиенил, 1-, 2- или 3-пирролил, 1-, 2-, 4- или 5-имидазолил, 1-, 3-, 4- или 5-пиразолил, 2-, 4- или 5-оксазолил, 3-, 4- или 5-изоксазолил, 2-, 4-или 5-тиазолил, 3-, 4- или 5-изотиазолил, 2-, 3- или 4-пиридил, 2-, 4-, 5- или 6-пиримидинил, кроме того, предпочтительно 1,2,3-триазол-1-, -4- или -5-ил,1,2,4-триазол-1-, -3- или -5-ил, 1- или 5-тетразолил, 1,2,3-оксадиазол-4- или -5-ил, 1,2,4-оксадиазол-3- или-5-ил, 1,3,4-тиадиазол-2- или -5-ил, 1,2,4-тиадиазол-3- или -5-ил, 1,2,3-тиадиазол-4- или -5-ил, 3- или 4-пиридазинил, пиразинил, 1-, 2-, 3-, 4-, 5-, 6- или 7-индолил, 4- или 5-изоиндолил, индазолил, 1-, 2-, 4 или 5-бензимидазолил, 1-, 3-, 4-, 5-, 6- или 7-бензопиразолил, 2-, 4-, 5-, 6- или 7-бензоксазолил, 3-, 4-, 5-,6- или 7-бензизоксазолил, 2-, 4-, 5-, 6- или 7-бензотиазолил, 2-, 4-, 5-, 6- или 7-бензизотиазолил, 4-, 5-, 6 или 7-бенз-2,1,3-оксадиазолил, 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолил, 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолил, 3-,4-, 5-, 6-, 7- или 8-циннолинил, 2-, 4-, 5-, 6-, 7- или 8-хиназолинил, 5- или 6-хиноксалинил, 2-, 3-, 5-, 6-, 7 или 8-2 Н-бензо-1,4-оксазинил, также предпочтительно 1,3-бензодиоксол-5-ил, 1,4-бензодиоксан-6-ил,2,1,3-бензотиадиазол-4- или -5-ил, 2,1,3-бензоксадиазол-5-ил или дибензофуранил. Гетероциклические радикалы также могут быть частично или полностью гидрированными. Независимо от дополнительных заместителей, Het может, таким образом, например, также означать 2,3-дигидро-2-, -3-, -4- или -5-фурил, 2,5-дигидро-2-, -3-, -4- или -5-фурил, тетрагидро-2- или -3-фурил,1,3-диоксолан-4-ил, тетрагидро-2- или -3-тиенил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пирролил,2,5-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 1-, 2- или 3-пирролидинил, тетрагидро-1-, -2- илиHet предпочтительно означает пиперидинил, пиперазинил, пирролидинил, морфолинил, фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, триазолил, тетразолил, оксадиазолил, тиадиазолил, пиридазинил, пиразинил, бензимидазолил,бензотриазолил, индолил, бензо-1,3-диоксолил, индазолил или бензо-2,1,3-тиадиазолил, каждый из которых незамещен или моно-, ди- или тризамещен A, СООА, Hal и/или =O (карбонильный кислород).R1 и R2 предпочтительно означают A; R3 и R4 предпочтительно означают Н; R5 предпочтительно означает Н; R6 предпочтительно означает А. Более предпочтительно R1 и R2 означает метил, R3 и R4 означает Н, R5 означает Н и R6 означает метил. В наиболее предпочтительном варианте осуществления настоящего изобретения композиция включает соединение 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазин. В самом предпочтительном варианте осуществления настоящего изобретения композиция включает энантиомер (+)-5,6-дигидро 4-диметиламино-2-имино-6-метил-1,3,5-триазин. Производные триазана соответственно формуле I и исходные материалы для их получения соответственно производятся способами, известными по сути, как описано в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Methods of Organic Chemistry],Georg-Thieme-Verlag, Stuttgart), т.е. при условиях реакции, которые известны и подходят для упомянутых реакций. Применение может также быть осуществлено вариантами, которые известны по сути, но не упомянуты здесь в деталях. Если необходимо, исходные материалы могут также быть сформированы insitu, оставляя их в неизолированном состоянии в сырой смеси, но немедленно преобразовывая их далее в соединение соответственно изобретению. С другой стороны, является возможным осуществить ступенчатую реакцию. Согласно ЕР 1250328 В 1, раскрытие которого включено в описание в полном объеме посредством ссылки, соединения формулы I могут быть получены реакцией соединения формулы IIR7 означает метильную или этильную группу,где реакцию проводят в полярном растворителе (например, этаноле или диметилформамиде) и в присутствии органической (например, камфорсульфокислоты) или неорганической кислоты (например,соляной кислоты). Предпочтительно, тем не менее, что соединения формулы I получают способом, который включает реакцию соединения формулы II в которой R5, R6 имеют значения, указанные выше. Неожиданно, исследования в ходе синтеза производных дигидро-1,3,5-триазинамина показывают,что соединения формулы I могут быть получены, по меньшей мере, со сравнимым или более высоким выходом по сравнению с предыдущим уровнем техники. Значительными преимуществами, которые могут быть упомянуты здесь, являются значительно более короткое время реакции и меньше отходов производства. Это, следовательно, также означает значительно более низкое потребление энергии. Одна молекула воды освобождается в процессе соответственно изобретению на сформированную молекулу соединения формулы I. В процессе предыдущего уровня техники две молекулы спирта освобождались на сформированную молекулу соединения формулы I. Метформин как предпочтительный исходный материал имеет структуру Соединения, имеющие главную формулу II, являются бигуанидами, синтез которых может быть проведен средним специалистом в данной области техники. Некоторые публикации, в которых синтез таких соединений описан, приведены как пример (FR 1537604; FR 2132396; SlottaTschesche (1929),Ber. 62b: 1398; Shapiro et al. (1959), J. Org. Chem. 81: 3725, 3728, 4636). Реакция соединений формул II и III предпочтительно проводится в подходящем полярном растворителе, например спиртах, таких как метанол, этанол, изопропанол, н-пропанол, н-бутанол, изобутанол или трет-бутанол; эфирах, таких как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (THF) или диоксан; гликолевых эфирах, таких как монометиловый или моноэтиловый эфир этиленгликоля, диметиловый эфир этиленгликоля (диглим); кетонах, таких как ацетон или бутанон; амидах, таких как ацетамид, диметилацетамид или диметилформамид (DMF); нитрилах, таких как ацетонитрил; сульфоксидах,таких как диметилсульфоксид (DMSO); сложных эфирах, таких как этилацетат, или смесях указанных растворителей. Особое предпочтение отдают изобутанолу, а также этанолу и изопропанолу. В зависимости от применяемых условий, время реакции находится между несколькими минутами и 14 днями, особенно предпочтительно между 3 и 12 ч. Температура реакции находится между около 50 и 150 С, обычно между 90 и 120 С. Упомянутые соединения соответственно изобретению могут быть применены в их конечной несолевой форме. С другой стороны, настоящее изобретение также включает применение этих соединений в форме их фармацевтически приемлемых солей, которые могут быть получены из различных органических и неорганических кислот и оснований способами, известными в уровне техники. Фармацевтически приемлемые солевые формы соединений соответственно изобретению по большей части приготовлены обычными способами. Реакцию предпочтительно осуществляют в присутствии органической или неорганической кислоты. Таким образом, возможно применение неорганических кислот, например серной кислоты, азотной кислоты, галогеноводородных кислот, таких как соляная кислота или бромисто-водородная кислота,фосфорных кислот, таких как ортофосфорная кислота, сульфаминовая кислота, а также органических кислот, в особенности алифатических, алициклических, аралифатических, ароматических или гетероциклических моно- или полиосновных карбоксильных, сульфоновых или серных кислот, например муравьиной, уксусной, пропионовой, пивалевой, диэтилуксусной, малоновой, янтарной, пимелиновой, фумаровой, малеиновой, молочной, винной, яблочной, лимонной, глюконовой, аскорбиновой, никотиновой,изоникотиновой, метан- или этансульфоновой, этандисульфоновой, 2-гидроксиэтансульфоновой, бензенсульфоновой, п-толуолсульфоновой, нафталинмоно- и дисульфоновых и лаурилсульфоновой кислот. Также подходящими и предпочтительными в значении настоящего изобретения являются кислотные катионные ионообменные смолы, такие как коммерчески доступные смолы Dowex или Amberlyst. Более предпочтительна п-толуолсульфокислота, а также соляная кислота, метансульфоновая кислота,серная кислота или камфорсульфокислота или кислотные катионные ионообменные смолы, напримерDowex 50, Amberlyst 15 или Dowex DR-2030. Наиболее предпочтительно реакцию осуществляют в присутствии п-толуолсульфокислоты или кислотной катионной ионообменной смолы. Основание формулы I может также быть превращено в соль присоединения кислоты, применяя кислоту, например, реакцией эквивалентных количеств основания и кислоты в инертном растворителе, таком как этанол, с последующим испарением. Особенно подходящими кислотами для этой реакции являются те, которые дают физиологически приемлемые соли. Таким образом, можно применять неорганические кислоты, например вышеупомянутые. Соли физиологически неприемлемых кислот, например пи-6 021395 краты, могут быть применены для отделения и/или очистки соединения формулы I. Относительно выше изложенного можно заметить, что выражения "фармацевтически приемлемая соль" и "физиологически приемлемая соль", которые применяются взаимозаменяемыми здесь, в настоящей связи взяты, чтобы означать активный ингредиент, который содержит соединение соответственно изобретению в форме одной из его солей, в особенности если эта солевая форма придает улучшенные фармакокинетические свойства активному ингредиенту по сравнению со свободной формой активного ингредиента или любыми другими солевыми формами активного ингредиента, применяемыми ранее. Фармацевтически приемлемая соль активного ингредиента может также обеспечить этот активный ингредиент первым необходимым фармакокинетическим свойством, которым он не владел ранее и может даже иметь позитивное влияние на фармакодинамику этого активного ингредиента с соответствием его терапевтической эффективности в теле. В очень предпочтительном объекте настоящего изобретения композиция включает 5,6-дигидро-4 диметиламино-2-имино-6-метил-1,3,5-триазин гидрохлорид. В другом самом предпочтительном варианте осуществления настоящего изобретения композиция включает соль энантиомерного соединения(+)-5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазин гидрохлорид. Инсулин, который представляет другой компонент композиции соответственно изобретению, является гипогликемическим гормоном полипептидной природы, который может быть получен соответственно многим известным способам. Эти способы конкретнее могут быть химическими, полусинтетическими, биологическими (особенно простая экстракция инсулина человека или животного) или биогенетическими (экспрессией рекомбинантного инсулина). Для целей изобретения термин "инсулин" включает аналоги инсулина, которые имеют структуру, отличную от инсулина человека, но не значительно модифицированную биологическую активность по сравнению с инсулином человека или животного. Таким образом, аналоги инсулина, которые особенно могут быть упомянуты, включают Insuman (Aventis),Organosuline (Organon), Humalog (Insulin lispro от Lilly), Lantus (Insulin Glargin от Aventis) и Novolog (Insulin Aspart от Novo Nordisk). Как указано выше, изобретение относится к лекарственному средству, содержащему инсулин и по меньшей мере одно триазиновое соединение и/или его производную соответственно изобретению, и обычно эксципиенты и/или адъюванты. В изобретении термин "адъювант" означает любое вещество,которое способствует, усиливает или модифицирует специфическую реакцию против активного ингредиента изобретения, если вводится совместно, одновременно или последовательно. Известными адъювантами для инъекционных растворов являются, например, алюминийсодержащая композиция, такая как гидроксид алюминия или фосфат алюминия, сапонины, такие как QS21, мурамилдипептид или мурамилтрипептид, белки, такие как гамма-интерферон или TNF, M59, сквален или полиолы. В изобретении термин "адъювант" также включает выражения "эксципиент" и "фармацевтически приемлемая среда", которые означают любой растворитель, дисперсную среду, замедлители абсорбции и т.д., которые не вызывают побочного действия, например аллергическую реакцию, у людей или животных. Соответственно,изобретение также относится к фармацевтической композиции, содержащей в качестве активного ингредиента эффективное количество инсулина и эффективное количество по меньшей мере одного соединения формулы I, как определено в ходе настоящей спецификации, и/или его физиологически приемлемые соли вместе с фармацевтически приемлемыми адъювантами."Лекарственное средство", "фармацевтическая композиция" или "фармацевтический препарат" в значении изобретения являются любым агентом в области медицины, который содержит инсулин в комбинации с одним или более триазиновыми соединениями изобретения или его препаратами и может быть применен в профилактике, терапии, последующем или послеоперационном наблюдении пациентов, которые страдают от болезней, которые вызваны ИР, таким образом, чтобы патогенную модификацию их общего состояния или состояние отдельной области организма можно зафиксировать, по меньшей мере,временно. Кроме того, активные ингредиенты могут быть введены сами по себе или в комбинации с еще другими способами лечения. Другие синергетические эффекты могут быть достигнуты применением более чем одного соединения формулы I в фармацевтической композиции. Также возможно, что инсулин и соединение формулы I комбинируются, по меньшей мере, с другим агентом с отличным от активного ингредиента структурным клеточным каркасом. Все активные ингредиенты могут быть применены или совместно, или последовательно. Фармацевтические препараты могут быть приспособлены для введения любым необходимым подходящим способом, например пероральный (включая буккальный или сублингвальный), ректальный,назальный, местный (включая буккальный, сублингвальный или трансдермальный), вагинальный или парентеральный (включая подкожный, внутримышечный, внутривенный или внутрикожный) способы. Такие препараты могут быть приготовлены путем применения всех процессов, известных в фармацевтической области техники, например комбинированием активных компонентов с эксципиентом(ами) или адъювантом(ами). Фармацевтические композиции изобретения могут быть сформированы, чтобы быть введенными пациенту единым путем (например, инъекцией) или разными путями (например, перорально для соединения формулы I, инъекцией для инсулина). Фармацевтическую композицию изобретения получают известным путем, применяя обыкновенные твердые или жидкие носители, разбавители и/или добавки и обычные адъюванты для фармацевтической инженерии и с соответствующей дозировкой. Количество материала эксципиента, который комбинируется с активным ингредиентом(ами), чтобы производить единичную лекарственную форму, меняется в зависимости от лечимого организма и особенности способа введения. Подходящие эксципиенты включают органические и неорганические вещества, которые являются подходящими для разных путей введения, таких как энтеральное (например, пероральное), парентеральное или местное применение, и которые не реагируют с активными ингредиентами изобретения или их солями, примерами подходящих эксципиентов являются вода, растительные масла, бензиловые спирты, алкиленгликоли, полиэтиленгликоли, триацетат глицерина, желатин, углеводы, такие как лактоза или крахмал, стеарат магния, тальк, и вазелиновое масло. Фармацевтический препарат, приспособленный для перорального введения, может быть введен как отдельные единицы, такие как, например, капсулы или таблетки; порошки или гранулы; растворы или суспензии в водной или неводной жидкостях; пищевая пена или вспененные съедобные средства или жидкие эмульсии масло-в-воде или жидкие эмульсии вода-в-масле. Таким образом, например, в случае перорального введения в форме таблетки или капсулы активные ингредиенты могут быть скомбинированы с пероральным, нетоксическим и фармацевтически приемлемым инертным эксципиентом, таким как,например, этанол, глицерин, вода и подобное. Порошки приготовляются измельчением активных ингредиентов, особенно соединений, до подходящего мелкого размера и смешивания их с фармацевтическим эксципиентом измельченным таким же образом, как, например, съедобные углеводы, такие как, например, крахмал или маннитол. Ароматизатор, консервант, диспергатор и краситель могут тоже присутствовать. Капсулы производятся приготовлением порошковой смеси, как описано выше, и наполнением ею сформированных желатиновых оболочек. Глиданты и лубриканты, например высокодисперсная силикатная кислота, тальк, стеарат магния, стеарат кальция или полиэтиленгликоль в твердой форме, могут быть добавлены к порошковой смеси после операции наполнения. Разрыхлитель или солюбилизатор,такой как агар-агар, карбонат кальция или карбонат натрия, могут тоже быть добавлены для того, чтобы улучшить доступность лекарственного средства после того, как капсула была принята. Вдобавок, если желательно или необходимо, подходящие связывающие вещества, лубриканты и разрыхлители, так же как и красители, тоже могут быть включены в смесь. Подходящие связывающие вещества включают крахмал, желатин, природные сахара, такие как, например, глюкоза или беталактоза, подсластители, изготовленные из кукурузы, природная или синтетическая камедь, такая как акациевая, трагакантовая или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и подобное. Лубриканты, применяемые в этих формах дозировки, включают олеат натрия, стеарат натрия,стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и подобное. Разрыхлители включают, не будучи ограниченными вдобавок, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и подобное. Таблетки формируются, например, приготовлением порошковой смеси, гранулированием или сухим прессованием смеси, добавлением лубриканта и разрыхлителя и прессованием всей смеси, чтобы получить таблетки. Порошковая смесь готовится смешиванием активных ингредиентов, особенно соединений, измельченных подходящим способом с разбавителем или основанием, как описано выше, и необязательно со связывающим веществом, таким как, например, карбоксиметилцеллюлоза, альгинат, желатин или поливинилпирролидон, замедлителем растворения, таким как, например, парафин, ускорителем абсорбции, таким как, например, четвертичная соль, и/или абсорбентом, таким как, например, бентонит, каолин или фосфат кальция. Порошковая смесь может быть гранулирована смачиванием ее связывающим веществом, таким как, например, сироп, крахмальная паста, мазь на основе камеди акации, или растворы целлюлозы, или полимерные материалы, и прессованием ее через сито. Как альтернатива гранулированию, порошковая смесь может быть пропущена через таблетирующую машину, дающую комочки неоднородной формы, которые разбиваются, чтобы сформировать гранулы. Гранулы могут быть покрыты добавлением стеариновой кислоты, стеарата, талька или минерального масла для того, чтобы предупредить налипание таблетки к пресс-формам. Активные ингредиенты соответственно изобретению могут также быть скомбинированы с сыпучим инертным эксципиентом и потом немедленно спрессованы, чтобы получить таблетки без выполнения этапов гранулирования или сухого прессования. Прозрачный или непрозрачный защитный слой состоит из уплотняющего слоя шеллака, слоя сахара или полимерного материала и может присутствовать глянцевый слой воска. Красители могут быть добавлены к этим покрытиям для того, чтобы уметь различать разные единицы дозирования. Пероральные жидкости, такие как, например, раствор, сиропы, эликсиры, могут быть приготовлены в форме единиц дозирования таким образом, что принятое количество содержит предварительно нормированное количество активных ингредиентов. Сиропы могут быть приготовлены растворением активных ингредиентов в водном растворе с подходящим ароматизатором, между тем как эликсиры готовятся с применением нетоксической спиртовой среды. Суспензии могут быть сформированы диспергированием активных ингредиентов, особенно соединений, в нетоксической среде. Солюбилизаторы и эмульгаторы,такие как, например, этоксилированные изостеариловые спирты и простые эфиры сорбита и полиэтиле-8 021395 ноксида, консерванты, ароматизирующие добавки, такие как, например, мятное масло или природные подсластители или сахарин, или другие искусственные подсластители, тоже могут быть добавлены. Единица дозирования, сформированная для перорального введения, если желательно, может быть инкапсулирована в микрокапсулы. Препарат может быть также приготовлен таким образом, что выделение продлевается или задерживается, таким как, например, покрытие или вложение измельченного материала в полимеры, воск и подобное. Соединения соответственно изобретению и их соли, сольваты и физиологически функциональные производные могут быть введены в форме липосомных систем доставки, таких как моноламеллярные везикулы, большие моноламеллярные везикулы и мультиламеллярные везикулы. Липосомы могут быть сформированы из различных фосфоролипидов, таких как холестерин, стеариламин или фосфатидилхолины. Соединения согласно изобретению могут быть также сконденсированы или скомплексованы с другой молекулой, которая промотирует направленный транспорт к назначенному месту, включению и/или распределению в пределах целевых клеток. Соединения согласно изобретению и их соли, сольваты и физиологически функциональные производные могут также быть доставлены, используя моноклональные антитела в качестве отдельных носителей, с которыми соединены молекулы соединений. Соединения могут быть также соединены с растворимыми полимерами в виде предназначенных носителей лекарственных средств. Такие полимеры могут охватывать поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидофенол, полигидроксиэтиласпартамидофенол или полилизин полиэтиленоксида, замещенный пальмитоиловыми радикалами. Соединения, кроме того, могут быть соединены с классом разлагаемых микроорганизмами полимеров, которые являются подходящими для того, чтобы достигнуть регулируемое высвобождение лекарственного средства, например полимолочная кислота,поли-эпсилон-капролактон, полигидроксимасляная кислота, полиортоэфиры, полиацетали, полидигидроксипираны, полицианоакрилаты и сшитые или амфипатические блок-сополимеры гидрогелей. Фармацевтические препараты, приспособленные для трансдермального введения, могут быть введены как отдельные пластыри для обширного, закрытого контакта с эпидермисом реципиента. Так, например, активные ингредиенты могут быть выделены из пластыря ионофорезом, как описано в общих терминах в Pharmaceutical Research, 3(6), 318 (1986). Фармацевтические композиции, приспособленные для местного введения, могут быть сформированы в виде мазей, кремов, суспензий, лосьонов, пудр, растворов, паст, гелей, спреев, аэрозолей или масел. Для лечения глаза или другой внешней ткани, например рта и кожи, препараты предпочтительно применяются как мазь для местного применения или крем. В случае препарата, чтобы получить мазь, активные ингредиенты могут быть применены или с парафиновой, или с водорастворимой кремовой основой. Альтернативно, активные ингредиенты могут быть сформированы, чтобы дать крем с кремовой основой масло-в-воде или основой вода-в-масле. Фармацевтические препараты, приспособленные для местного применения на глазе, включают глазные капли, в которых активный ингредиент растворен или суспендирован в подходящем носителе, в особенности водном растворителе. Фармацевтические препараты,приспособленные для местного применения во рту, включают леденцы, пастилки и полоскания. Фармацевтические препараты, приспособленные для ректального введения, могут быть введены в форме суппозиториев или спринцеваний. Для приготовления суппозиториев активные компоненты смешиваются способом, известным по сути с подходящим компонентом основы, таким как полиэтиленгликоль или полусинтетические глицериды. Фармацевтические препараты, приспособленные для назального введения, в которых веществоноситель является твердым, содержит крупный порошок, имеющий размер частиц, например, в области 20-500 мкм, которые вводятся способом вдыхания через нос, т.е. быстрой ингаляцией через носовые проходы из емкости, содержащей порошок, держа ее близко от носа. Подходящие препараты для введения в виде назального спрея или капель для носа с жидкостью в качестве носителя включают растворы активного ингредиента в воде или масле. Фармацевтические препараты, приспособленные для введения ингаляцией, включают мелкочастичные присыпки и мисты, которые могут быть образованы различными типами распылителей под давлением с аэрозолями, нейбулайзерами или инсуффляторами. Инсулин и соединение формулы I могут быть введены ингаляцией. Эффективность ингаляции инсулина особенно обсуждалась Skyler et al. (2001), Lancet 357(9253): 331-335. Например, аэрозоли и способы ингаляции,развитые Inhale Therapeutic Systems, СА и описаны в US 5997848, сделали возможным оптимизировать абсорбцию и воспроизводимость выпускаемой дозы. Фармацевтические препараты, приспособленные для вагинального введения, могут быть введены в виде пессариев, тампонов, кремов, гелей, паст, пен или спреевых препаратов. Фармацевтические препараты, приспособленные для парентерального введения, включают водные и неводные стерильные инъекционные растворы, содержащие антиоксиданты, буферные системы, бактериостатики и жидкие системы, посредством которых препарат оказывается изотоничным крови реципиента, которого будут лечить; и водные и неводные стерильные суспензии, которые могут содержать среду и загустители. Препараты могут быть введены в емкостях одноразового или многоразового дозирования, например запаянные ампулы и виалы, и храниться в замороженном (лиофилизированные) состоя-9 021395 нии, таким образом, является необходимым только добавление стерильного жидкого носителя, например воды для инъекционных целей, непосредственно перед применением. Растворы для инъекции и суспензии, приготовленные в соответствии с рецептурой, могут быть приготовлены из стерильного порошка,гранул и таблеток. Композиция, содержащая инсулин, предпочтительно предназначается для парентерального введения, конкретнее инъекцией. Само собой разумеется, что вдобавок к вышесказанному, в частности упомянутым компонентам,препараты могут также содержать другие агенты, обычные в области техники, учитывая особый тип препарата; таким образом, препараты, которые являются подходящими для перорального введения, могут содержать ароматизаторы. В предпочтительном варианте осуществления настоящего изобретения фармацевтическая композиция вводится перорально или парентерально, более предпочтительно парентерально, наиболее предпочтительно в виде растворов для инъекции для парентерального введения. В особенности активные ингредиенты предусматриваются в водорастворимой форме, такой как фармацевтически приемлемые соли,которые, разумеется, включают как соли присоединения кислоты, так и соли присоединения основания. Кроме того, активные ингредиенты изобретения и их соли могут быть лиофилизированы, и полученные в результате лиофилизаты применяются, например, чтобы произвести составы для инъекции. Указанные составы могут быть стерилизованы и/или могут содержать вспомогательные вещества, такие как протеиновые носители (например, сывороточный альбумин), лубриканты, консерванты, стабилизаторы, наполнители, хелатные агенты, антиоксиданты, растворители, связывающие агенты, суспендирующие агенты,смачивающие агенты, эмульгаторы, соли (для влияния на осмотическое давление), буферные вещества,колоранты, ароматизаторы и одно или более дополнительных активных веществ, например, один или более витаминов. Добавки хорошо известны в области техники и применяются в различных препаратах. Соответствующая доза или диапазон дозирования для введения фармацевтической композиции соответственно изобретению является достаточно высокой для того, чтобы добиться необходимого профилактического или терапевтического эффекта уменьшения симптомов болезней, которые вызваны ИР, как указано ниже. Должно быть понятно, что особенный уровень дозы, частота и период введения любому отдельному человеку будут зависеть от различных факторов, включая активность конкретного применяемого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время и путь введения,скорость выведения, лекарственную комбинацию и тяжесть отдельной болезни, к которой применяется особая терапия. Применяя хорошо известные значения и способы, точная доза может быть определена любым специалистом в данной области техники как задача шаблонного опыта. Термин "эффективное количество", или "эффективная доза", или "доза" применяется здесь взаимозаменяемо и означает количество фармацевтического соединения, имеющего профилактически или терапевтически уместный эффект на болезнь или патологические состояния, т.е. которое вызывает в ткани,системе, животном или человеке биологический или медицинский отклик, который определяется или ожидается, например, исследователем или врачом. "Профилактический эффект" уменьшает вероятность развития болезни или предупреждает о начале болезни. "Терапевтически соответствующий эффект" ослабляет до некоторой степени один или несколько симптомов болезни или возвращает к нормальности либо полностью один, либо более физиологических или биохимических параметров, вызывающих или являющихся причиной болезни или патологических состояний. Вдобавок, выражение "терапевтически эффективное количество" означает количество, которое, по сравнению с соответствующим предметом,который не получал это количество, имеет следующее влияние: улучшенное лечение, выздоровление,предупреждение или исчезновение болезни, синдрома, состояния, недомогания, нарушения или побочного действия или также уменьшение прогресса болезни, недомогания или нарушения. Выражение "терапевтически эффективное количество" также включает количества, которые эффективны для увеличения нормальной физиологической функции. Фармацевтические препараты могут быть введены в форме единиц дозирования, которые содержат наперед определенное количество активного ингредиента на единицу дозирования. Концентрация профилактически или терапевтически активного ингредиента в препарате может варьироваться от около 0,1 до 100 мас.%. Предпочтительно соединение формулы I или его фармацевтически приемлемые соли вводятся в дозах приблизительно 0,5-1,0 мг, более предпочтительно 1-700 мг. Еще наиболее предпочтительно, что единица дозирования соединения формула (I) содержит 12,5-200 мг указанного соединения. Также предпочтительно, что единица дозирования инсулина содержит 10-400 ME (международных единиц) инсулина, более предпочтительно 0,1-1 ME. Хотя терапевтически эффективное количество соединения соответственно изобретению должно быть, прежде всего, определено лечащим врачом или ветеринаром, принимая во внимание множество факторов (например, возраст и вес животного, точное состояние, которое требует лечения, тяжесть состояния, природу препарата и способ введения), эффективное количество соединения соответственно изобретению для лечения ИР и/или патологий, связанных с ИР, синдром, например диабет, находится в диапазоне от 0,02 до 200 мг/кг веса тела реципиента (млекопитающего) на день и, в частности, обычно в диапазоне от 10 до 180 мг/кг веса тела в день, более предпочтительно от 70 до 160 мг/кг, наиболее предпочтительно от 75 до 150 мг/кг. Таким образом, фактическое количество в день для взрослого млекопи- 10021395 тающего весом 70 кг является обычно между 14 и 14000 мг, где это количество может быть введено как единственная доза в день или обычно серией частичных доз (таких как, например, две, три, четыре, пять или шесть) в день, так, что общая дневная доза была такой же. Эффективное количество его соли или сольвата или физиологически функционального производного может быть определено как часть эффективного количества соединения соответственно изобретению по сути. Было предположено, что подобные дозы являются подходящими для лечения других состояний, как упомянуто в этом описании. Композиция содержит терапевтически эффективное количество различных активных компонентов. Соотношение соответствующего количеств инсулина и соединений формулы I в результате варьируется: в особенности дневные диапазоны дозировки инсулина между 0,5 и 1,0 ME на 1 кг веса и дневная дозировка соединения формулы I в диапазоне между 25 и 200 мг, в каждом случае для взрослого. Соответственно, изобретательский способ лечения может быть применен в человеческой и ветеринарной медицине. Соответствующие изобретению соединения формулы I и/или их физиологические соли, пригодные для профилактического или терапевтического лечения и/или контролирования заболевания, которое вызвано ИР, или собственно IRf соответственно. Здесь, соединения могут быть введены до или в течение вспышки болезни один или несколько раз, выступая в роли терапии. Вышеупомянутые лекарственные препараты изобретательского применения, в частности, применяются для терапевтического лечения. Контролирование рассматривается как вид лечения, в котором соединения предпочтительно вводятся в различных интервалах, например, для того, чтобы усилить ответную реакцию и устранить патогены и/или симптомы ИР-зависимого заболевания полностью. Также могут быть применены подобная композиция или разные композиции. Лекарственное средство может быть также применено,чтобы снизить вероятность развития болезни, или еще предупредить начало заболевания, вызванного ИР,заранее, или вылечить возникающие и постоянные симптомы. В значении изобретения профилактическое лечение уместно, если объект обладает любыми предварительными состояниями для вышеупомянутых физиологических или патологических состояний, таких как семейное предрасположение, генетический дефект или перенесенная ранее болезнь. Заболевания относительно изобретения выбраны из группы диабета, предиабета, низкой толерантности к глюкозе, гипергликемии, метаболического синдрома, диабетической нефропатии, невропатии,ретинопатии, атеросклероза и сердечно-сосудистой болезни, кроме того, сосудистого рестеноза, панкреатита и нейродегеративной болезни. В предпочтительном варианте осуществления настоящего изобретения болезнь является метаболическим синдромом. Медицинское показание "метаболический синдром" является комбинацией медицинских расстройств, которые увеличивают риск развития сердечно-сосудистых болезней. Вдобавок к центральному типу ожирения, два дополнительных симптома и черты должны быть осуществлены для классификации как метаболического синдрома: гипергликемия натощак (выраженная T2DM, нарушенный уровень глюкозы натощак, нарушенная толерантность к глюкозе или резистентность к инсулину), высокое кровяное давление и нарушение жирового обмена (например, уменьшенный HDL холестерин и/или увеличенные триглицериды). В другом предпочтительном варианте осуществления изобретения композиция изобретения является подходящей для лечения одного или более патологических состояний, вызванных синдромом ИР, которые выбраны из дислипидемии, ожирения, артериальной гипертензия, макроваскулярных осложнений,в частности атеросклероза, и микрососудистых осложнений, в частности ретинопатии, нефропатии и невропатии. В более предпочтительном варианте осуществления изобретения заболевания являются нефропатией и/или невропатией. Медицинское показание "нефропатии" относится к заболеваниям почки и почечной функции, которые главным образом вызваны не воспалительным процессом. Сложный подтип в контексте изобретения отражается диабетической нефропатией (nephropatia diabetica), которая также известна как синдром Киммелстила-Уилсона и интеркапиллярный гломерулонефрит. Прогрессирующая болезнь почки, вызванная ангиопатией капилляров в почечном клубочке, характеризуется нефротическим синдромом и нодозным гломерулосклерозом. Это происходит из-за длительного сахарного диабета и является основной причиной для диализа во многих западных странах. Кроме того, медицинское показание "невропатии" является обычно коротким для периферической невропатии. Периферическая невропатия определяется как нарушенная функция и структура периферических двигательных, сенсорных и автономных нейронов, включая или целый нейрон или выбранные уровни. Невропатии часто возникают вторично от других болезней, таких как сахарный диабет, или нейротоксических веществ, таких как злоупотребление алкоголем. Еще другой предпочтительный вариант осуществления изобретения, в котором фармацевтическая композиция является особенно подходящей для лечения диабета воспроизведением существенного действия на метаболический синдром от ИР. Таким образом, особое предпочтение изобретательского медицинского показания отдается диабету, более предпочтительно сахарному диабету, наиболее предпочтительно ИЗСД и ИНЗСД. В высшей степени предпочтительно уменьшить гипергликемию ИНЗСД. Композиция также является хорошо подходящей для лечения диабетиков любого типа, включая диабет I типа и диабет II типа, предпочтительно диабет I типа и/или диабет II типа, более предпочтительно T2DM, и на различных стадиях болезни. Соответственно другому объекту изобретения инсулин и по меньшей мере одно соединение формулы I вводятся совместно или последовательно, предпочтительно в форме отдельных фармацевтических композиций, одной - содержащей инсулин в фармацевтически приемлемой среде, другой - содержащей соединение формулы I в фармацевтически приемлемой среде. Не должно быть исключено, однако, что инсулин и по меньшей мере одно соединение формулы I могут быть скомбинированы в такую же фармацевтическую композицию и вводиться. В контексте настоящего изобретения термины "фармацевтическая комбинация" и "комбинированное введение" относятся к одному или другому из этих объектов. Более детально, "комбинированное введение" означает, для цели настоящего изобретения, фиксированные и, в особенности, свободные комбинации, т.е. или инсулин и соединение формулы I присутствуют совместно в одной единице дозирования, или инсулин и указанное соединение, которые присутствуют в отдельных единицах дозирования, вводятся в непосредственной последовательности или при относительно большом интервале времени; относительно большой интервал времени означает время, длящееся в пределах максимум 24 ч. "Единица дозирования" означает в особенности медицинскую форму дозирования, в которой выделение активного ингредиента(ов) обеспечивается с настолько меньшими проблемами, насколько возможно. Это включает в особенности таблетки, таблетки с покрытием или пеллеты, микротаблетки в капсулах и растворы с формой дозировки, преимущественно разработанной так, что два активных компонента (инсулин, с одной стороны, и упомянутое соединение формулы I - с другой стороны) освобождаются или делаются доступными эффективно для тела таким способом, что достигается оптимальный профиль активного ингредиента и, таким образом, профиль действия. Для совместного введения в виде фиксированной композиции, т.е. такой, которая пребывает в единственном фармацевтическом препарате с обоими ингредиентами, она готовится, например, как раствор для инъекции или инфузии или ее лиофилизированная форма, которая наполняется в ампулы. Фиксированная композиция в лиофилизированной форме гарантирует простое и безопасное обращение. Она растворяется в ампуле добавлением обычного фармацевтического инъекционного агента и вводится внутривенно. Растворитель может быть частью комбинированной расфасовки. Для применения в виде отдельных единиц дозирования они предпочтительно готовятся доступными вместе в одной упаковке,или смешиваются перед введением, или вводятся последовательно. Например, две единицы дозирования упаковываются вместе в блистерную упаковку, которая приспосабливается, принимая во внимание относительную последовательность в соответствии друг другу двух единиц дозирования, названием и/или подкрашиванием способом, известным по сути, так, чтобы часы для приема индивидуальных компонентов (режим дозирования) двух единиц дозирования являлись очевидными пациенту. Эта свободная комбинация вводится преимущественно путем индивидуального назначения эффективного количества инсулина и эффективного количества соединения формулы I пациенту. Другой возможностью является обеспечение отдельных препаратов инсулина и указанного соединения, т.е. независимых лекарственных средств. Отдельные препараты преобразуются, чтобы содержать необходимые количества ингредиента для изобретательской комбинации. Соответствующие инструкции даются в листке-вкладыше, описывая комбинированное введение соответствующего лекарственного средства. Дополнительно, изобретение может быть применено на практике как фармацевтический набор, содержащий в виде активных ингредиентов эффективное количество инсулина, совместно с одним или больше фармацевтически приемлемыми адъювантами, в первой единице дозирования, и эффективное количество по меньшей мере одного соединения формулы I, как установлено выше, и/или его физиологически приемлемые соли, совместно с одним или более фармацевтически приемлемых адъювантов, во второй единице дозирования, в частности, для того, чтобы произвести профилактическое или терапевтическое лечение и/или контролирование заболевания, которое вызвано ИР. Набор изобретения может включать информацию, которая содержит написанные инструкции или направляет пользователя к написанным инструкциям для того, как применять на практике способ изобретения. Предыдущее изучение настоящей спецификации в отношении композиции и ее введения рассматривается как действительное и применимое без ограничений к фармацевтическому набору, если целесообразно. Изобретение также относится к применению инсулина в комбинации по меньшей мере с одним соединением формулы I, как установлено соответственно изобретению, и/или его физиологически приемлемыми солями для профилактического или терапевтического лечения и/или контролирования заболевания, которое вызвано ИР. Кроме того, изобретение относится к применению инсулина в комбинации по меньшей мере с одним соединением формулы I, как указано соответственно изобретению, и/или его физиологически приемлемыми солями для производства лекарственного средства для профилактического или терапевтического лечения и/или контролирования заболевания, которое вызвано ИР. Лекарственное средство может быть применено, чтобы предупреждать начало заболевания, вызванного ИР, заранее или лечить возникающие и постоянные симптомы. Заболеваниями относительно изобретения являются предпочтительно диабет и/или вызванные им заболевания, последнее является более предпочтительно выбранным из группы метаболического синдрома, диабетической нефропатии и невропатии. Вдобавок,предыдущее изучение настоящей спецификации в отношении изобретательской композиции является действительным и применимым без ограничений к применению лекарственного средства для профилактики и терапии упомянутых болезней. Объектом настоящего изобретения является также применение инсулина в комбинации по меньшей мере с одним соединением формулы I, как указано здесь, и/или его физиологически приемлемых солей для улучшения гомеостаза глюкозы. Здесь, "улучшение" относится к величинам параметра, которые превосходят начальные показания, в пределах нормальной статистической области, как обусловлено способом измерения и обстоятельством, который включают живые организмы. Толерантность к глюкозе и/или секреция инсулина под влиянием глюкозы исполняют роль предпочтительных параметров для определения гомеостаза глюкозы, где увеличение одного или обоих параметров показывает улучшение гомеостаза глюкозы. Толерантность к глюкозе и/или секреция инсулина, в частности секреция инсулина, предпочтительно увеличивается по меньшей мере на 10%, более предпочтительно по меньшей мере на 20% и наиболее предпочтительно по меньшей мере на 30%. Такое увеличение предпочтительно получается, если соединениеформулы I обеспечивается для введения в диапазоне дозирования от 25 до 200 мг на 1 кг массы тела, более предпочтительно в диапазоне от 75 до 150 мг на 1 кг массы тела. Применение может быть также осуществлено in vitro или in vivo моделями. In vitro применение предпочтительно применяется к образцам людей, страдающих от ИР, более предпочтительно ИЗСД или ИНЗСД. Например, тестирование нескольких соединений формулы I и/или смесей с инсулином делает выделение этой композиции возможным, что лучше удовлетворяет требования для лечения предмета, относящегося к млекопитающим. In vivo мощность дозы выбранного производного предпочтительно приспосабливается к строго ИР соответственным характерным клеткам по отношению к in vitro данным. Поэтому терапевтическая эффективность значительно увеличилась. Кроме того, предыдущее изучение настоящей спецификации в отношении композиции изобретения рассматривается как действительное и применимое без ограничений к применению соединение для уменьшения ИР, если целесообразно. Изобретение конкретнее направлено на применение, как определено выше, в котором инсулин и соединение формулы I находятся в форме, подходящей для совместного введения. Альтернативно, изобретение также направлено на применение, как определено выше, в котором инсулин и соединение формулы I находятся в форме, подходящей для последовательного введения. Другой объект изобретения обеспечивает способ для лечения заболевания, которое вызвано резистентностью к инсулину, в котором эффективное количество инсулина в комбинации с эффективным количеством по меньшей мере одного соединения формулы I, как определено соответственно изобретению, и/или его физиологически приемлемых солей вводится млекопитающим, которым необходимо такое лечение. Млекопитающие, которых лечили, являлись в особенности людьми. Предпочтительное лечение является пероральным или парентеральным введением. Лечение пациентов, страдающих от ИЗСД или ИНЗСД, или людей с риском развития таких заболеваний на основе существующего ИР, посредством комбинированного применения инсулина и триазинового соединения улучшает общую чувствительность к инсулину и улучшает ИР у этих индивидуумов. Так, улучшение предпочтительно достигается,если соединение формулы I вводится в диапазоне дозирования от 25 до 200 мг на 1 кг массы тела, более предпочтительно в диапазоне дозирования от 75 до 150 мг на 1 кг массы тела. В другом предпочтительном объекте триазиновое соединение 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазин применяется в разных дозах, более предпочтительно гидрохлорид 5,6-дигидро-4-диметиламино-2-имино-6 метил-1,3,5-триазина. Инсулин может быть введен через хорошо известное приспособление. Предыдущее изучение изобретения и его вариантов осуществления является действительным и применимым без ограничений к способу лечения, если целесообразно. В объеме настоящего изобретения фармацевтическая композиция, содержащая инсулин и производную триазина формулы I, обеспечивается для первого раза. Изобретение отражает успешное улучшение гомеостаза глюкозы у пациентов с присутствием ИР и/или вызванных болезней, в частности диабетаI типа, по сравнению с лечением самим инсулином. Как результат введения фармацевтической композиции соответственно изобретению, секреция инсулина, по меньшей мере частично или даже полностью,восстанавливается под действием глюкозы. Вдобавок, комбинация инсулина с производными триазина включает сильное потенцирование эффектов инсулина. Следовательно, производные триазина формулыI могут быть предпочтительно соединены с инсулином, чтобы уменьшить терапевтические дозы инсулина, в частности, у пациентов с диабетом I типа, но также у пациентов с диабетом II типа. Постоянное лечение обоих типов пациентов с диабетом такими производными триазина в присутствии пеллет инсулина имеет особую пользу для уменьшения уровня глюкозы натощак и увеличения толерантности к глюкозе соответственно, хотя любой режим дозировки улучшает вышеупомянутые параметры. Другим важным моментом является изменение распределения глюкозы к более низким уровням. Применение композиции является обещанным, новым подходом для широкого спектра терапий, вызывающих полное и непосредственное уменьшение симптомов. Влияние является особой пользой, чтобы эффективно бороться с ИР и/или болезнями, возникающими от ИР. Соединение и его производные характеризируются высокой специфичностью и устойчивостью; низкими затратами на производство и удобной обработкой. Эти особенности формируют основу для воспроизводимого действия, в котором включена перекрестная реактивность и побочные действия, и для надежного и безопасного взаимодействия со структурами их гистосовместимой клетки-мишени. Все ссылки, приведенные здесь, объединены ссылкой в раскрытии изобретения настоящим документом. Должно быть понятно, что это изобретение не ограничено отдельными способами, особыми веществами, применениями и комплектами, описанными здесь, значение которых как таковых может, конечно, измениться. Также должно быть понятно, что терминология применена здесь с целью описания только особых вариантов осуществления и не предназначена, чтобы ограничить область данного изобретения, которая определена только приложенной формулой изобретения. Как применено здесь, включая приложенную формулу изобретения, форма единственного числа слов включает их соответствующие множественные значения, если контекст явно не указывает иначе. Таким образом, например, ссылка на"соль" включает единственную соль или несколько различных солей, и наоборот, и ссылка на "способ" включает ссылку на эквивалентные стадии и способы, известные среднему специалисту в данной области техники, и т.д. Если иначе не определено, все технические и научные термины, использованные здесь,имеют то же самое значение, как обычно понимается средним специалистом в данной области техники,который занимается этим изобретением. Хотя способы и материалы, подобные или эквивалентные описанным здесь, могут применяться в практике или тестировании настоящего изобретения, подходящие примеры описаны ниже. Следующие примеры обеспечены путем иллюстрации, а не путем ограничения. В пределах примеров, применяются стандартные реактивы и буферные системы, которые свободны от загрязняющих действий (всякий раз,когда удобно). Примеры, в частности, должны быть рассмотрены таким образом, что они не ограничены явно продемонстрированными комбинациями признаков, но иллюстрируемые признаки могут неограниченно сочетаться снова, если решена техническая проблема изобретения. На следующих фигурах и в таблицах соединение 5,6-дигидро-4-диметиламино-2-имино-6-метил 1,3,5-триазин сокращено как EMD. Фиг. 1 показывает действие комбинации инсулина и 5,6-дигидро-4-диметиламино-2-имино-6 метил-1,3,5-триазин на глюкозу плазмы в крысиной модели типа 1. Фиг. 2 показывает изменения глюкозы плазмы OGTT (ммоль/л) после 36 дней лечения комбинацией инсулина и 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина. Фиг. 3 показывает изменения инсулина плазмы OGTT (пмоль/л) после загрузки глюкозы и 36-дневного лечения комбинацией инсулина (3 МЕ/день) и 5,6-дигидро-4-диметиламино-2-имино-6 метил-1,3,5-триазина. Фиг. 4 показывает распределение (процент) голодного уровня гипергликемии для каждой группы: контроль, инсулин (3 МЕ/день) + 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина (75 мг/кг два раза в день), так же как и инсулин (3 МЕ/день) + 5,6-дигидро-4-диметиламино-2-имино-6-метил 1,3,5-триазина (150 мг/кг два раза в день). Пример 1. Получение 4-амино-3,6-дигидро-2-диметиламино-6-метил-1,3,5-триазин гидрохлорида. В данном описании все температуры приведены в С. В следующих примерах "общепринятая обработка" означает, если необходимо, добавление воды, рН, если необходимо, приводится к значениям между 2 и 10, в зависимости от состояния конечного продукта, смесь экстрагируется этилацетатом или дихлорметаном, фазы разделяются, органическая фаза высушивается над сульфатом натрия и испаряется,продукт очищается хроматографически на силикагеле и/или перекристаллизацией. Сравнительный эксперимент. Смесь 250,2 г хлоргидрата метформина, 213,6 г диэтилацеталя ацетальдегида и 12,5 г моногидрата толуол-4-сульфокислоты в 500 мл изобутанола нагревали при кипячении с обратным холодильником на протяжении 40 ч. Некоторая часть растворителя была удалена дистилляцией. Смесь охлаждали до 10 С и выделяли белый осадок, получая 224,7 г (77,4%) 4-амино-3,6-дигидро-2-диметиламино-6-метил-1,3,5 триазин гидрохлорида.A) Смесь 1002,6 г хлоргидрата метформина, 359,1 г паральдегида и 51,6 г моногидрата толуол-4 сульфокислоты в 2405,9 г изобутанола нагревали при кипячении с обратным холодильником на протяжении 6 ч. Некоторая часть растворителя была удалена дистилляцией. Смесь охлаждали до 12 С и выделяли белый осадок, получая 953,8 г (81,4%) 4-амино-3,6-дигидро-2-диметиламино-6-метил-1,3,5-триазин гидрохлорида.B) Смесь 100,1 г хлоргидрата метформина, 36,5 г паральдегида и 4 г Dowex DR-2030 в 237,8 мл изобутанола нагревали при кипячении с обратным холодильником на протяжении 6 ч. Последовательно были отфильтрованы катализаторы и некоторая часть растворителя была удалена дистилляцией. Остаток раствора охлаждали до 10-15 С и выделяли белый осадок, получая 93,5 г (80.7%) 4-амино-3,6-дигидро-2 диметиламино-6-метил-1,3,5-триазин гидрохлорида. Пример 2. Эффект короткого постоянного лечения (4 недели) инсулиновыми пеллетами совместно с 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазином на гомеостаз глюкозы. Исследование было осуществлено на гипергликемических и гипоинсулинемических 1 типа крысиных моделях, полученных инъекцией высокой дозы Streptozotocin (STZ). Мужские особи крыс Wistar(Charles River) были обработаны STZ при 62,5 мг/кг ИР. Крысам проверяли начальные уровни глюкозы три дня после STZ инъекций. Животные с уровнями глюкозы ниже 35-40 ммоль/л были исключены из этого исследования. После отбора пеллеты инсулина были подкожно имплантированы (1+1/2 имплантов) на 3 день. Скорость выделения для каждого имплантата была 2 Е на 24 ч. В этих экспериментальных условиях каждой крысе было введено 3 Е на 24 ч инсулина на протяжении 40 дней приблизительно (Limplant LINSHIN CANADA). 5,6-Дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазин был перорально введен в двух дозах, 75 и 150 мг/кг два раза в день, 10 дней после индуцирования диабета. Дополнительные экспериментальные детали известны специалисту в данной области техники, например раскрытиемWO 2003/092726, и могут быть слегка модифицированы в обычном порядке. После имплантации пеллет инсулина уровень инсулина плазмы был стабильным в каждой группе(табл. 2). Вдобавок, пеллеты инсулина существенно понизили глюкозу плазмы до 21,463,1 ммоль/л(табл. 1, фиг. 1) по сравнению с 44,651,54 ммоль/л в контрольной группе без инсулина (данные не показаны) после 36 дней. После введения 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина глюкоза плазмы уменьшилась еще больше. Это действие 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина было зависимым от дозы. При 75 мк/кг два раза в день гипергликемия понизилась в конце лечения от 21,463,1 до 18,862,77 ммоль/л, тогда как гипергликемия понизилась в конце лечения с более высокой дозой 150 мг/кг два раза в день от 21,463,1 до 14,852,03 ммоль/л (табл. 1, фиг. 1). Определение, как быстро введенная глюкоза выводится из крови, было проведено посредством теста на толерантность к глюкозе. Глюкоза была введена перорально, таким образом, общий тест был технически пероральным тестом на толерантность к глюкозе (OGTT), который хорошо известен специалистам в данной области техники. Лабораторное животное было голодным на протяжении 18 ч до того, как ему был введен раствор глюкозы. Кровь была забрана в интервалах (например, табл. 3) для измерения глюкозы (сахара крови) и дополнительно уровни инсулина были измерены, чтобы определить степень ИР или отсутствие соответственно. Для скрининга диабета наиболее важным образцом является 2-часовой образец, в котором значение сахара крови увеличивается у млекопитающих с ослабленной секрецией инсулина или ИР. По сравнению с одним инсулином, комбинация инсулина с 5,6-дигидро-4-диметиламино-2-имино 6-метил-1,3,5-триазином увеличивает толерантность к глюкозе, и этот эффект также был зависимым от дозы (табл. 3, фиг. 2). Чем выше была доза, тем лучше, в среднем, крысы переносили глюкозу. Подробное распределение концентраций глюкозы в плазме OGTT в пределах каждой группы дано ниже (см. фиг. 4). Таблица 1 Уровень глюкозы в плазме натощак (ммоль/л), определенный до и после лечения комбинацией инсулина и 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина Таблица 2 Уровень глюкозы в плазме натощак (пмоль/л), определенный до и после лечения комбинацией инсулина и 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина. СПС обозначает стандартную погрешность среднего значения Таблица 3 Изменения глюкозы в плазме (ммоль/л) после 36 дней лечения комбинацией инсулина и 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина,как определено OGTT По сравнению с одним инсулином, комбинация инсулина с 5,6-дигидро-4-диметиламино-2-имино 6-метил-1,3,5-триазином незначительно увеличила секрецию инсулина в ответ на глюкозу (фиг. 3). Анализ распределения уровней голодной гипергликемии показывает, что комбинация инсулина с 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазином сместила перераспределение концентраций глюкозы в плазме к более низким уровням. Почти 50% крыс, обработанных комбинацией инсулина и 150 гм/кг два раза в день 5,6-дигидро-4-диметиламино-2-имино-6-метил-1,3,5-триазина, демонстрировали уровень гипергликемии, который был ниже чем 10 ммоль/л (фиг. 4). Пример 3. Фармацевтические препараты.A) Инъекционные виалы. Раствор 100 г одного или более активных ингредиентов соответственно изобретению и 5 г гидрофосфата натрия в 3 л бидистиллированной воды был приведен до рН 6,5, применяя 2 н. соляную кислоту, стерильно профильтрован, перенесен в инъекционные виалы, лиофилизирован в стерильных условиях и запечатан в стерильных условиях. Каждая инъекционная виала содержала 5 мг активного ингредиента(ов).B) Суппозитории. Смесь 20 г одного или более активных ингредиентов соответственно изобретению была растоплена с 100 г соевого лецитина и 1400 г масла какао, налита в формы и охлаждена. Каждый суппозиторий содержал 20 мг активного ингредиента(ов).C) Раствор. Раствор был приготовлен из 1 г одного или более активных ингредиентов соответственно изобретению, 9,38 г NaH2PO42H2O, 28,48 г Na2HPO412H2O и 0,1 г хлорида бензалкония в 940 мл бидистиллированной воды. рН было приведено до 6,8 и раствор был доведен до 1 л и стерилизован облучением. Раствор может быть применен в форме капель для глаз.D) Мазь. 500 мг одного или более активных ингредиентов соответственно изобретению было перемешано с 99,5 г вазелина в асептических условиях.E) Таблетки. Смесь 1 кг одного или более активных ингредиентов соответственно изобретению, 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния была спрессована, чтобы получить таблетки обычным способом, таким образом, чтобы каждая таблетка содержала 10 мг активного ингредиента(ов). Другие таблетки с активным ингредиентом 5,6-дигидро-4-диметиламино-2 имино-6-метил-1,3,5-триазином были приготовлены соответственно табл. 4-9. Таблица 4 Таблетка, содержащая 87% производного триазина и адъювантыF) Таблетки с покрытием. Таблетки были спрессованы аналогично предыдущему параграфу Е) и затем покрыты обычным способом покрытием из сахарозы, картофельного крахмала, талька, трагакантовой камеди и красителя.G) Капсулы. 2 кг одного или более активных ингредиентов соответственно изобретению были помещены в жесткие желатиновые капсулы обычным способом таким образом, чтобы каждая капсула содержала 20 мг активного ингредиента(ов). Н) Ампулы. Раствор 1 кг одного или более активных ингредиентов соответственно изобретению в 60 л бидистиллированной воды был стерильно профильтрован, перенесен в ампулы, лиофилизирован в стерильных условиях и запечатан в стерильных условиях. Каждая ампула содержала 10 мг активного ингредиента(ов).I) Спрей для ингаляции. 14 г одного или более активных ингредиентов соответственно изобретению было растворено в 10 л изотонического раствора NaCl и раствор был перенесен в коммерчески доступные емкости для спрея с помповым механизмом. Раствор может быть распылен в рот или нос. Одна ингаляция (около 0,1 мл) соответствует дозе около 0,14 мг. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Комбинация для применения в качестве лекарственного средства, включающая инсулин и соединение формулы I и/или его физиологически приемлемую соль, где соединение формулы I определено как следующее: где R1, R2, каждый независимо друг от друга, означают Н или A;R3, R4, каждый независимо друг от друга, означают Н или A;R5, R6, каждый независимо друг от друга, означают Н или A; А означает неразветвленный или разветвленный алкил, имеющий 1-10 атомов C, в котором 1-7 атомов Н могут быть замещены F, или циклический алкил, имеющий 3-7 атомов C. 2. Фармацевтическая комбинация, содержащая в качестве активных компонентов эффективное количество инсулина в комбинации с эффективным количеством по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли, вместе с одним или несколькими фармацевтически приемлемыми адъювантами. 3. Комбинация по п.1 или 2, где соединение формулы I представляет собой 2-амино-3,6-дигидро-4-диметиламино-6-метил-1,3,5-триазин. 4. Комбинация по любому из пп.1-3 для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину. 5. Комбинация по п.4, где заболевание выбрано из группы, включающей диабет, предиабет, низкую толерантность к глюкозе, гипергликемию, метаболический синдром, диабетическую нефропатию, невропатию, ретинопатию, атеросклероз и сердечно-сосудистое заболевание, предпочтительно инсулинзависимый сахарный диабет и неинсулинзависимый сахарный диабет. 6. Комбинация по любому из пп.1-5 для перорального или парентерального введения предпочтительно в виде раствора для инъекций для парентерального введения. 7. Комбинация по любому из пп.1-6, где инсулин находится в фиксированной комбинации с соединением формулы I в одной единице дозирования. 8. Комбинация по любому из пп.1-6, где инсулин и соединение формулы I находятся в отдельных единицах дозирования в одной упаковке. 9. Применение инсулина в комбинации по меньшей мере с одним соединением формулы I, определенным в п.1, и/или его физиологически приемлемой солью для получения лекарственного средства для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину. 10. Применение инсулина в комбинации по меньшей мере с одним соединением формулы I, определенным в п.1, и/или его физиологически приемлемой солью для улучшения гомеостазиса глюкозы. 11. Применение по п.9 или 10, где толерантность к глюкозе и/или секреция инсулина увеличивается в ответ на глюкозу. 12. Применение по любому из пп.9-11, где соединение формулы I вводят в дозировке от 25 до 200 мг/кг массы тела. 13. Применение по любому из пп.9-12, где инсулин и соединение формулы I используются в форме для одновременного или последовательного введения. 14. Способ лечения заболеваний, которые связаны с резистентностью к инсулину, в котором эффек- 18021395 тивное количество инсулина в комбинации с эффективным количеством по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли вводят млекопитающему, которое нуждается в таком лечении. 15. Фармацевтический набор для профилактического или терапевтического лечения и/или контролирования заболеваний, которые связаны с резистентностью к инсулину, включающий в качестве активных компонентов эффективное количество инсулина вместе с одним или несколькими фармацевтически приемлемыми адъювантами в первой единице дозирования и эффективное количество по меньшей мере одного соединения формулы I, определенного в п.1, и/или его физиологически приемлемой соли вместе с одним или несколькими фармацевтически приемлемыми адъювантами во второй единице дозирования.
МПК / Метки
МПК: A61K 31/53, A61K 38/28, A61P 3/10
Метки: инсулина, производными, диабета, триазиновыми, комбинация, применение, лечения
Код ссылки
<a href="https://eas.patents.su/21-21395-kombinaciya-insulina-s-triazinovymi-proizvodnymi-i-ih-primenenie-dlya-lecheniya-diabeta.html" rel="bookmark" title="База патентов Евразийского Союза">Комбинация инсулина с триазиновыми производными и их применение для лечения диабета</a>
Предыдущий патент: Стекло
Следующий патент: Уплотняющая сборка
Случайный патент: Чип-карта и способ ее применения












