Производные n-(1h-индолил)-1н-индол-2-карбоксамидов, их получение и их применение в терапии
Формула / Реферат
1. Соединение формулы (I)
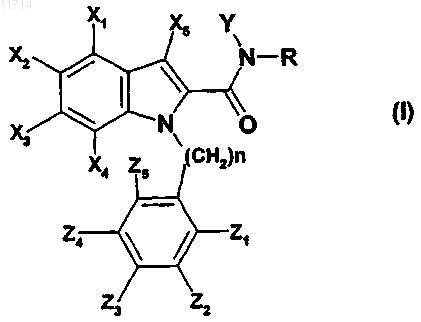
в которой X1, X2, X3, Х4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена или C1-С6-алкильную, С3-С7-циклоалкильную, C1-С6-фторалкильную, C1-С6-алкокси, C1-С6-фторалкокси, циано, C(O)NR1R2, нитро, NR1R2, C1-С6-тиоалкильную, -S(О)-C1-С6-алкильную, -S(О)2-C1-С6-алкильную, SO2NR1R2, NR3COR4, NR3SO2R5 или C6-С10-арильную группу;
X5 обозначает атом водорода или галогена или C1-С6-алкильную, C1-С6-фторалкильную группу;
R обозначает 4-, 5-, 6- или 7-индолильную группу
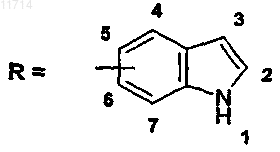
причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С6-алкильной и C1-С6-фторалкильной;
причем R необязательно замещен в положении 4, 5, 6 и/или 7 одной или несколькими группами, выбранными из атомов галогена, C1-С6-алкильной, C1-С6-фторалкильной, C1-С6-алкокси, C1-С6-фторалкоксигрупп;
Y обозначает атом водорода или C1-С6-алкильную группу;
n равно 0, 1, 2 или 3;
R1 и R2 обозначают независимо друг от друга атом водорода или C1-С6-алкильную, С3-С7-циклоалкильную, С3-С7-циклоалкил-С1-С3-алкильную или С6-С10-арильную группу; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, азетидиновую, пирролидиновую, пиперидиновую, азепиновую, морфолиновую, тиоморфолиновую, пиперазиновую, гомопиперазиновую группу, причем указанная группа необязательно замещена C1-С6-алкильной, С3-С7-циклоалкильной, С3-С7-циклоалкил-C1-С3-алкильной или С6-С10-арильной группой;
R3 и R4 обозначают независимо друг от друга атом водорода или C1-С6-алкильную или C6-С10-арильную группу;
R5 обозначает C1-С6-алкильную или С6-С10-арильную группу,
в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
2. Соединение формулы (I) по п.1, отличающееся тем, что
X1, Х2, Х3, Х4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена или C1-С6-алкильную, С3-С7-циклоалкильную, C1-С6-фторалкильную, C1-С6-алкокси, C1-С6-фторалкокси, нитро, NR1R2, C1-С6-тиоалкильную, -S(О)-C1-С6-алкильную, -S(О)2-C1-С6-алкильную или С6-С10-арильную группу;
X5 обозначает атом водорода или C1-С6-алкильную группу;
R обозначает 4-, 5-, 6- или 7-индолильную группу
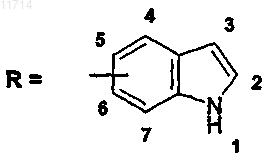
причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими C1-С6-алкильными группами;
Y обозначает атом водорода;
n равно 0, 1, 2 или 3;
R1 и R2 обозначают независимо друг от друга атом водорода,
в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
3. Соединение формулы (I) по п.1 или 2, отличающееся тем, что
R обозначает 5-индолильную группу
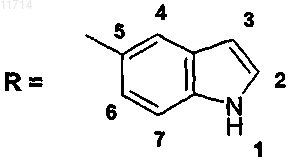
причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С6-алкильной и C1-С6-фторалкильной групп,
причем R необязательно замещен в положении 4, 6 и/или 7 одной или несколькими группами, выбранными из атомов галогена, C1-С6-алкильной, C1-С6-фторалкильной, C1-С6-алкокси, C1-С6-фторалкоксигрупп,
в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
4. Соединение формулы (I) по любому из пп.1-3, отличающееся тем, что X2 и/или X3 не являются атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
5. Соединение формулы (I) по любому из пп.1-4, отличающееся тем, что Х5 является атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
6. Соединение формулы (I) по любому из пп.1-5, отличающееся тем, что Y является атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата.
7. Соединение формулы (I) по п.1, которое представляет собой
N-(1-метил-1Н-индол-5-ил)-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-метокси-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(3-фторбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-трифторметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3,5-диметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-метил-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-фенил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-6-метокси-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-хлор-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-4-метокси-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(3-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(4-трифторметилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(6-хлор-3-трифторметилбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(3-метилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(3-метоксибензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-фтор-1-(3-трифторметоксибензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-трет-бутилбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-хлорбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-фторбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-метилтиофенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-втор-бутилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-5-метокси-1-фенил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-изопропилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-н-пентилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-циклопентилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(бифен-4-ил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-трифторметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-н-пропилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-метилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-изопропилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-трет-бутилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-циклогексилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-этоксифенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-хлорфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3,5-дифторфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(2-фторфенил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-трифторметоксибензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(4-бромбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3,4-диметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(фенетил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-изопропилфенил)-5-трифторметокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-трифторметилбензил)-5-трифторметил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-трифторметилфенил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-трифторбензил)-5-трифторметил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-6-ил)-1-(3,5-диметилфенил)-1Н-индол-2-карбоксамид;
N-(1,2,3-триметил-1Н-индол-5-ил)-1-(3,5диметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-4-ил)-1-(3,5-диметилфенил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-6-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-7-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-[2-(2-фторфенил)этил]-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-[2-(4-фторфенил)этил]-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фенилпропил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-метокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-7-ил)-1-(3,5-диметилфенил)-1Н-индол-2-карбоксамид;
N-(1,2,3-триметил-1Н-индол-5-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-4-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1,2-диметил-1Н-индол-5-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-[2-(4-третбутилфенил)этил]-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-6-метокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-4-метокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-4,6-диметокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-хлор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-метил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-метилсульфонил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-нитро-1Н-индол-2-карбоксамид;
N-(1-изопропил-1Н-индол-5-ил)-1-(3-фторбензил)-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-4-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-изопропил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-бензил-5-трифторметил-1Н-индол-2-карбоксамид;
N-(1Н-индол-5-ил)-5-фтор-(3-фторбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-трифторметокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-4-метил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-трет-бутил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5-амино-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-6-метил-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-6-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-5,6-диметокси-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-(3-фторбензил)-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-бензил-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-[2-(3-трифторметилфенил)этил]-5-фтор-1Н-индол-2-карбоксамид;
N-(1-метил-1Н-индол-5-ил)-1-[2-(3-фторфенил)этил]-5-фтор-1Н-индол-2-карбоксамид.
8. Способ получения соединения формулы (I) по п.1, отличающийся тем, что проводят реакцию соединения общей формулы (IV):
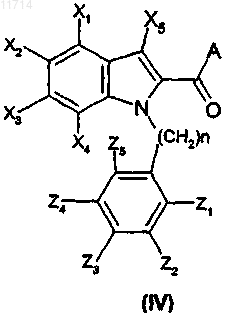
в которой X1, Х2, Х3, Х4, Х5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает C1-С6-алкокси, с амидным соединением общей формулы (V):
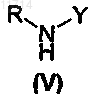
в которой R и Y такие, как определены в общей формуле (I) по п.1,
при температуре кипения растворителя, причем амидное соединение общей формулы (V) получено предварительным взаимодействием триметилалюминия и аминоиндолов общей формулы (V).
9. Способ получения соединения формулы (I) по п.1, отличающийся тем, что превращают соединение общей формулы (IV):
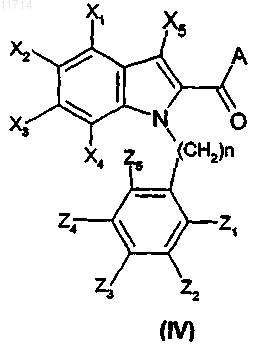
в которой X1, Х2, Х3, Х4, Х5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает гидроксигруппу,
в хлорангидрид кислоты действием тионилхлорида при температуре кипения растворителя,
и тем, что в присутствии основания проводят реакцию соединения общей формулы (IV), в которой X1, Х2, Х3, Х4, Х5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает атом хлора, с аминоиндолом общей формулы (V):
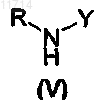
в которой R и Y такие, как определены в общей формуле (I) по п.1,
или тем, что проводят реакцию сочетания между соединением общей формулы (IV), в которой X1, Х2, Х3, Х4, X5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает гидроксигруппу, и аминоиндолом общей формулы (V), в которой R и Y такие, как определены в общей формуле (I) по п.1, в присутствии сочетающего агента и основания в растворителе.
10. Лекарственное средство для профилактики или лечения патологий, в которых участвуют рецепторы типа TRPV1, отличающееся тем, что содержит соединение формулы (I) по любому из пп.1-6 или фармацевтически приемлемую соль, или гидрат, или сольват соединения формулы (I).
11. Лекарственное средство по п.10, которое предназначено для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочно-кишечного тракта, респираторных заболеваний, псориаза, прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии.
12. Фармацевтическая композиция для профилактики или лечения патологий, в которых участвуют рецепторы типа TRPV1, отличающаяся тем, что содержит соединение формулы (I) по любому из пп.1-6 или фармацевтически приемлемую соль или гидрат или сольват этого соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент.
13. Фармацевтическая композиция по п.12, которая предназначена для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочно-кишечного тракта, респираторных заболеваний, псориаза, прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии.
14. Применение соединения формулы (I) по любому из пп.1-7 для получения лекарственного средства, предназначенного для профилактики или лечеэшя патологий, в которых участвуют рецепторы типа TRPV1.
15. Применение соединения формулы (I) по п.14 для получения лекарственного средства, предназначенного для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочно-кишечного тракта, респираторных заболеваний, псориаза, прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии.
16. Применение соединения формулы (I) по п.14, где боль или воспаление выбраны из боли хронической, невропатической (травматической, диабетической, метаболической, вызванной инфекцией, токсической, вызванной противораковым или ятрогенным лечением), (остео-)артритной, ревматической, фибромиалгий, боли в спине, боли, вызванной раковым заболеванием, невралгии лицевого нерва, головных болей, мигрени, зубной боли, ожога, солнечного удара, укуса животного или насекомого, постгерпетической невралгии, мышечной боли, нервного сдавливания (центрального или периферического), травм спинного или головного мозга, ишемии (спинного или головного мозга), нейродегенерации, геморрагических нарушений кровообращения (спинного и/или головного мозга), болей после инсульта.
17. Применение соединения формулы (I) по п.14, где урологические заболевания выбраны из группы, включающей гиперактивность мочевого пузыря, гиперфлексия мочевого пузыря, недержание, императивное мочеиспускание, недержание мочи, цистит, почечные колики, гиперчувствительность в области таза и боли в области таза.
18. Применение соединения формулы (I) по п.14, где гинекологические заболевания выбраны из группы, включающей вульводинию, боли, связанные с сальпингитом, дисменорею.
19. Применение соединения формулы (I) по п.14, где заболевания желудочно-кишечного тракта выбраны из группы, включающей нарушение желудочно-пищеводного рефлекса, язву желудка, язву двенадцатиперстной кишки, функциональную диспепсию, колит, IBS, болезнь Крона, панкреатит, эзофагит, печеночные колики.
20. Применение соединения формулы (I) по п.14, где респираторные заболевания выбраны из группы, включающей астму, кашель, COPD, бронхостеноз, воспалительные заболевания.
Текст
011714 Объектом настоящего изобретения являются производные N-(1 Н-индолил)-1 Н-индол-2 карбоксамидов, которые обладают активностью антагониста in vitro и in vivo в отношении рецепторов типа TRPV1 (или VR1). Уже известны соединения, описанные в документе WO-A-03049702, пригодные для лечения заболеваний, в которых участвуют рецепторы типа VR1. Однако существует потребность в обнаружении и получении продуктов, обладающих высокой активностью in vivo. Для решения этой проблемы изобретением предлагаются новые соединения, которые обладают активностью антагониста in vitro и in vivo в отношении рецепторов типа VR1. Первый объект изобретения относится к соединениям приведенной ниже общей формулы (I). Другим объектом изобретения являются способы получения соединений общей формулы (I). Другим объектом изобретения является применение соединений общей формулы (I), в частности, в лекарственных средствах или фармацевтических композициях. Соединения согласно изобретению соответствуют общей формуле (I) в которой X1, X2, Х 3, Х 4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена или C1-С 6-алкильную, С 3-С 7-циклоалкильную, С 1-С 6-фторалкильную, C1-С 6-алкокси, C1-С 6 фторалкокси, циано, C(O)NR1R2, нитро, NR1R2, C1-С 6-тиоалкильную, -S(О)-С 1-С 6-алкильную, -S(О)2-C1C6-алкильную, SO2NR1R2, NR3COR4, NR3SO2R5 или арильную группу; Х 5 обозначает атом водорода или галогена или C1-С 6-алкильную, C1-С 6-фторалкильную группу;R обозначает 4-, 5-, 6- или 7-индолильную группу, причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С 6-алкильной, C1-С 6-фторалкильной; причем R необязательно замещен в положении 4, 5, 6 и/или 7 одной или несколькими группами,выбранными из атомов галогена, C1-С 6-алкильной, C1-С 6-фторалкильной, C1-С 6-алкокси, C1-С 6 фторалкоксигрупп;Y обозначает атом водорода или C1-С 6-алкильную группу;R1 и R2 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную, C3-С 7 циклоалкильную, С 3-С 7-циклоалкил-С 1-С 3-алкильную или арильную группу; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, азетидиновую, пирролидиновую, пиперидиновую, азепиновую, морфолиновую, тиоморфолиновую, пиперазиновую, гомопиперазиновую группу, причем указанная группа необязательно замещена C1-С 6-алкильной, С 3-С 7-циклоалкильной, С 3-С 7-циклоалкил-С 1-С 3 алкильной или арильной группой;R3 и R4 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную или арильную группу;Ct-Cz, где t и z могут обозначать величины от 1 до 6, означает углеродную цепочку, которая может содержать от t до z атомов углерода, например C1-С 3-углеродную цепочку, которая может содержать от 1 до 3 атомов углерода; алкил означает алифатическую насыщенную линейную или разветвленную группу. В качестве примеров можно назвать метильную, этильную, пропильную, изопропильную, бутильную, изобутильную,трет-бутильную, пентильную группы и т.д.; циклоалкил означает циклическую углеродную группу. В качестве примеров можно назвать циклопропильную, циклобутильную, циклопентильную, циклогексильную группы и т.д.; фторалкил означает алкильную группу, в которой один или несколько атомов водорода замещены атомом фтора; алкокси означает радикал -О-алкил, в котором алкильная группа такая, как определена выше;-1 011714 фторалкокси означает алкоксигруппу, в которой один или несколько атомов водорода замещены атомом фтора; тиоалкил означает радикал -S-алкил, где алкильная группа такая, как определена выше; арил означает циклическую ароматическую группу, содержащую от 6 до 10 атомов углерода. В качестве примера арильных групп можно назвать фенильную или нафтильную группы; атом галогена означает фтор, хлор, бром или йод. Соединения формулы (I) могут быть в форме оснований или солей присоединения кислот. Такие соли присоединения относятся к изобретению. Эти соли преимущественно получают с использованием фармацевтически приемлемых кислот, но соли других кислот, пригодных, например, для очистки или выделения соединений формулы (I), также относятся к изобретению. Соединения формулы (I) могут также быть в форме гидратов или сольватов, а именно в виде ассоциаций или комбинаций с одной или несколькими молекулами воды или растворителя. Такие гидраты или сольваты также относятся к изобретению. Из соединений формулы (I), являющихся объектами изобретения, первая подгруппа соединений состоит из соединений, в которыхX1, X2, X3, X4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена,более конкретно фтор, бром или хлор, или C1-С 6-алкильную, более конкретно метил, пропил, изопропил,втор-бутил, трет-бутил, пентил, С 3-С 7-циклоалкильную, более конкретно циклопентил или циклогексил,C1-С 6-фторалкильную, более конкретно CF3, C1-С 6-алкокси, более конкретно метокси или этокси, C1-С 6 фторалкокси, более конкретно OCF3, нитро, NR1R2, C1-С 6-тиоалкильную, более конкретно тиометил,-S(О)-C1-С 6-алкильную, -S(О)2-С 1-С 6-алкильную, более конкретно S(O)2-CH3, или арильную группу, более конкретно фенил; и/или Х 5 обозначает атом водорода или C1-С 6-алкильную группу, более конкретно метил; и/илиR обозначает 4-, 5-, 6- или 7-индолильную группу, причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими C1-С 6-алкильными группами, более конкретно метильной или изопропильной; и/илиR1 и R2 обозначают независимо друг от друга атом водорода. Вторая подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которыхX1, X2, X3, X4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена,более конкретно фтор, бром или хлор, или C1-С 6-алкильную, более конкретно метил, пропил, изопропил,втор-бутил, трет-бутил, пентил, С 3-С 7-циклоалкильную, более конкретно циклопентил или циклогексил,C1-С 6-фторалкильную, более конкретно CF3, C1-С 6-алкокси, более конкретно метокси или этокси, C1-С 6 фторалкокси, более конкретно OCF3, нитро, C1-С 6-тиоалкильную, более конкретно тиометил, -S(О)-C1 С 6-алкильную, -S(О)2-С 1-С 6-алкильную, более конкретно S(O)2-CH3, или арильную группу, более конкретно фенил; и/или Х 5 обозначает атом водорода или C1-С 6-алкильную группу, более конкретно метил; и/илиR обозначает 4-, 5-, 6- или 7-индолильную группу, причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими C1-С 6-алкильными группами, более конкретно метильной; и/илиn равно 0, 1, 2 или 3. Третья подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которыхX1, X2, X3, Х 4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или C1-С 6 алкильную, С 3-С 7-циклоалкильную, C1-С 6-фторалкильную, C1-С 6-алкокси, C1-С 6-фторалкокси, циано,C(O)NR1R2, нитро, NR1R2, C1-С 6-тиоалкильную, -S(О)-C1-С 6-алкильную, -S(О)2-C1-С 6-алкильную,-SO2NR1R2, NR3COR4, NR3SO2R5 или арильную группу;X5 обозначает атом водорода или галогена или C1-С 6-алкильную, C1-С 6-фторалкильную группу;R обозначает 4-, 5-, 6- или 7-индолильную группу, причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С 6-алкильной, C1-С 6-фторалкильной групп,причем R необязательно замещен в положении 4, 5, 6 и/или 7 одной или несколькими группами,выбранными из атомов галогена, C1-С 6-алкильной, C1-С 6-фторалкильной, C1-С 6-алкокси, C1-С 6 фторалкоксигрупп;Y обозначает атом водорода или C1-С 6-алкильную группу;R1 и R2 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную, С 3-С 7 циклоалкильную, С 3-С 7-циклоалкил-С 1-С 3-алкильную или арильную группу; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, азетидиновую, пирролидиновую, пиперидиновую, азепиновую,морфолиновую, тиоморфолиновую, пиперазиновую, гомопиперазиновую группу, причем указанная группа необязательно замещена C1-С 6-алкильной, С 3-С 7-циклоалкильной, С 3-С 7-циклоалкил-C1-С 3 алкильной или арильной группой;R3 и R4 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную или арильную группу;R5 обозначает C1-С 6-алкильную или арильную группу; при условии, что если Z1, Z2, Z3, Z4 и Z5 одновременно обозначают атомы водорода,то n = 2 или 3. Четвертая подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которыхR обозначает 5-индолильную группу, причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С 6-алкильной и C1-С 6-фторалкильной групп,причем R необязательно замещен в положении 4, 6 и/или 7 одной или несколькими группами, выбранными из атомов галогена, C1-С 6-алкильной, C1-С 6-фторалкильной, C1-С 6-алкокси, C1-С 6-фторалкоксигрупп,при этом X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и Z5, Y, n, R1, R2, R3, R4 и R5 такие, как определены выше в общей формуле (I), или такие, как определены выше в случае первой, второй или третьей подгрупп. Пятая подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которых Х 2 и/или X3 не являются атомом водорода; при этом X1, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4, Z5, R, Y, n, R1, R2, R3, R4 и R5 такие, как определены выше в общей формуле (I), или такие, как определены выше в случае первой, второй, третьей или четвертой подгрупп. Шестая подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которых Х 5 обозначает атом водорода; при этом X1, X2, Х 3, Х 4, Z1, Z2, Z3, Z4, Z5, R, Y, n, R1, R2, R3, R4 и R5 такие, как определены выше в общей формуле (I), или такие, как определены выше в случае первой, второй, третьей, четвертой или пятой подгрупп. Седьмая подгруппа соединений формулы (I), являющихся объектами изобретения, состоит из соединений, в которыхY обозначает атом водорода; при этом X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4, Z5, R, n, R1, R2, R3, R4 и R5 такие, как определены выше в общей формуле (I), или такие, как определены выше в случае первой, второй, третьей, четвертой, пятой или шестой подгрупп. Согласно изобретению соединения общей формулы (I) можно получить способом, который иллюстрирует следующая схема. В соответствии со схемой соединения общей формулы (IV) можно получить путем взаимодействия соединения общей формулы (II), в которой X1, Х 2, X3, Х 4, Х 5 такие, как определены выше в общей формуле (I), и А обозначает C1-С 6-алкокси или гидроксигруппу, и соединения общей формулы (III), в кото-3 011714 рой Z1, Z2, Z3, Z4, Z5 такие, как определены выше в общей формуле (I), и R' обозначает атом брома, йода,тозилатную группу или любую другую эквивалентную группу. Схема Если n=1, 2 или 3, соединение общей формулы (III) может являться алкилгалогенидом, таким как бензилбромид (n=1: Kolasa Т., Bioorg. Med. Chem., 1997, 5(3), 507) или фенетилиодидом (n=2:Abramovitch R., Synth. Commun., 1995, 25(1), 1), и реакцию можно проводить в присутствии основания,такого как гидрид натрия или карбонат калия, в полярном растворителе, таком как диметилформамид,диметилсульфоксид или ацетон. Если n=0, соединением общей формулы (III) является арилйодид или арилбромид и реакцию можно проводить при температуре от 80 до 250 С в присутствии катализатора на основе меди, такого как бромид меди или оксид меди, а также основания, такого как карбонат калия (Murakami Y., Chem. Pharm.Bull., 1995, 43(8), 1281). Можно также применять более мягкие условия, описанные S.L. Buchwald, J. Am.Chem. Soc., 2002, 124, 11684. Альтернативно, соединения общей формулы (IV), в которой n=0, можно получать путем взаимодействия соединения общей формулы (II) и соединения общей формулы (III) типа бороновой кислоты (n=0,R'=B(OH)2) в присутствии основания, такого как триэтиламин или пиридин, а также диацетата меди, по аналогии с методом, описанным у W.W.K.R. Mederski, Tetrahedron, 1999, 55, 12757. Соединения общей формулы (II) являются коммерческими или их можно получить многими способами, описанными в литературе (например, D. Knittel, Synthesis, 1985, 2, 186 и Т. М. Williams, J. Med.Chem., 1993, 36(9), 1291). В случае индолов общей формулы (IV), в которой А обозначает C1-С 6-алкоксигруппу, соединение общей формулы (I) получают взаимодействием соединения общей формулы (IV), такого как полученное выше, и амида соединения общей формулы (V), в которой R и Y являются такими, как определены в общей формуле (I), при температуре кипения растворителя, такого как толуол. Амид соединения общей формулы (V) получают предварительным воздействием триметилалюминия на аминоиндолы общей-4 011714 формулы (V). В случае индолов общей формулы (IV), в которой А обозначает гидроксигруппу, функциональная группа карбоновой кислоты может быть предварительно превращена в галогенангидрид кислоты, такой как хлорангидрид кислоты, под действием тионилхлорида при температуре кипения растворителя, такого как дихлорметан или дихлорэтан. Соединение общей формулы (I) тогда получают путем взаимодействия соединения общей формулы (IV), в которой А обозначает атом хлора, и аминоиндола соединения общей формулы (V), в присутствии основания, такого как триэтиламин. Альтернативно, индол общей формулы (IV), в которой А обозначает гидроксигруппу, можно сочетать с аминоиндолом общей формулы (V) в присутствии агента сочетания, такого как диалкилкарбодиимид, гексафторфосфат бензотриазол-1-ил-окси-триспирролидинфосфония, диэтилцианофосфонат или любого другого сочетающего агента, известного специалисту, в присутствии основания, такого как триэтиламин, в растворителе, таком как диметилформамид. Аминоиндолы общей формулы (V) получают способами, описанными в литературе, такими как описаны у I.T. Forbes, J. Med. Chem., 1993, 36(8), 1104 (Y=H), I.T. Forbes, WO 9205170 (Y=алкил). На схеме соединения формул (II), (III) и (V) и другие реагенты, если способ их получения не описан, являются коммерческими или описаны в литературе, или их можно получить способами, которые там описаны или которые известны специалисту. Соединения общих формул (II), (IV) и (I), в которых X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают циано или арильную группу, можно получить реакцией сочетания, катализуемой металлом, таким как палладий, проводимой с использованием соответствующих соединений общих формул (II), (IV) или (I), в которых X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают атом брома. Соединения общих формул (II), (IV) и (I), в которых X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают группу C(O)NR1R2, можно получить из соответствующих соединений общих формул (II), (IV) или (I), в которых X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают цианогруппу, способами, описанными в литературе или известными специалисту. Соединения общих формул (II), (IV) и (I), в которых X1, X2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают S(О)-алкильную или S(О)2-алкильную группу, можно получить путем окисления соответствующих соединений общих формул (II), (IV) или (I), в которых X1, X2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают C1-С 6-тиоалкильную группу, способами, описанными в литературе или известными специалисту. Соединения общих формул (II), (IV) и (I), в которых Х 1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают группу NR1R2, NR3COR4 или NR3SO2R4, можно получить из соответствующих соединений общих формул (II), (IV) или (I), в которых X1, X2, Х 3, Х 4, X5, Z1, Z2, Z3, Z4 и/или Z5 обозначают нитрогруппу,например, восстановлением с последующим ацилированием или сульфонированием способами, описанными в литературе или известными специалисту. Соединения общих формул (II), (IV) и (I), в которых Х 1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4 и/или Z5 обозначают группу SONR1R2, можно получить способом, аналогичным описанному в Pharmazie, 1990, 45,346, или способами, описанными в литературе или известными специалисту. В нижеследующих примерах описано получение некоторых соединений согласно изобретению. Эти примеры не ограничивают, а только иллюстрируют настоящее изобретение. Номера соединений в примерах соответствуют номерам в табл. 1. Элементный анализ, анализ ЖХ/МС (жидкостная хроматография в сочетании с масс-спектрометрией), инфракрасные спектры и спектры ЯМР подтверждают структуру полученных соединений. Если не указано иное, все химические реагенты, используемые в примерах, приобретены у коммерческих поставщиков. Пример 1 (соединение 1).N-(1-Метил-1 Н-индол-5-ил)-1-(3-трифторметилбензил)-1 Н-индол-2-карбоксамид. 1.1. Этил-1-(3-трифторметилбензил)-1 Н-индол-2-карбоксилат. Перемешивают суспензию 0,492 г (2,6 ммоль) этил-1 Н-индол-2-карбоксилата, 0,683 г (2,86 ммоль) 3-трифторметилбензилбромида и 0,898 г (6,5 ммоль) карбоната калия в 50 мл диметилформамида в течение 24 ч при 60 С. Охлаждают реакционную смесь, выливают ее в смесь ледяной воды и этилацетата. После разделения фаз отделяют органическую фазу, затем промывают ее два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Получают 0,8 г масла, используемое таким,какое оно есть, на следующей стадии. 1.2. N-(1-Метил-1 Н-индол-5-ил)-1-(3-трифторметилбензил)-1 Н-индол-2-карбоксамид (соединение 1). При 0 С вводят по каплям раствор 0,231 г (1,58 ммоль) 1-метил-1 Н-5-аминоиндола (I.T. Forbes, J.Med. Chem., 1993, 36(8), 1104) в 15 мл толуола в раствор 0,93 мл (1,87 ммоль) триметилалюминия (2 М в толуоле) в 6 мл толуола. Перемешивают в течение 15 мин, затем вводят 0,5 г (1,44 моль) этил-1-(3 трифторметилбензил)-1 Н-индол-2-карбоксилата, полученного на стадии 1.1. Смесь нагревают в течение 4 ч при 50 С. Реакционную смесь затем подвергают гидролизу 10 мл воды, затем обрабатывают 100 мл этилацетата. Органическую фазу промывают 1 н. соляной кислотой, два раза 50 мл воды, затем 50 мл-5 011714 насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и дихлорметана, затем перекристаллизовывают в изопропаноле. Получают 0,33 г продукта. Температура плавления: 189-190 С. 1N-(1-Метил-1 Н-индол-5-ил)-5-метокси-1-(3-трифторметилбензил)-1 Н-индол-2-карбоксамид. 2.1. Этил-5-метокси-1 Н-индол-2-карбоксилат. В раствор 1 г (5,23 ммоль) 5-метокси-1 Н-индол-2-карбоновой кислоты в 52 мл этанола вводят по каплям 1,91 мл (26,15 ммоль) тионилхлорида, перемешивая при 0 С. Реакционную смесь нагревают с обратным холодильником в течение 2 ч, потом ее охлаждают и концентрируют при пониженном давлении. Остаток обрабатывают 100 мл этилацетата и промывают этот раствор два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Получают 1,2 г продукта, который используют таким, какой он есть, на следующей стадии. 2.2. Этил-5-метокси-1-(3-трифторметилбензол)-1 Н-индол-2-карбоксилат. В суспензию 0,306 г гидрида натрия в 10 мл диметилформамида вводят по каплям раствор 1,2 г(5,47 ммоль) этил-5-метокси-1 Н-индол-2-карбоксилата, полученного на стадии 2.1 в 50 мл диметилформамида. Перемешивают смесь в течение 1 ч при комнатной температуре, затем вводят 1,01 мл(6,57 ммоль) 3-трифторметилбензилбромида и продолжают перемешивать еще в течение 4 ч. Выливают реакционную смесь в 200 мл ледяной воды и 100 мл этилацетата. После разделения фаз отделяют органическую фазу, затем промывают три раза по 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Получают 2 г продукта, который используют таким, какой он есть, на следующей стадии. 2.3.(соединение 2). При 0 С вводят по каплям раствор 0,278 г (1,91 ммоль) 1-метил-1 Н-5-аминоиндола (I.T. Forbes, J.Med. Chem., 1993, 36(8), 1104) в 15 мл толуола в раствор 1,59 мл (3,18 ммоль) триметилалюминия (2 М в толуоле) в 10 мл толуола. Перемешивают в течение 15 мин, затем вводят 0,6 г (1,59 ммоль) этил-1-(3 трифторметилбензил)-5-метокси-1 Н-индол-2-карбоксилата, полученного на стадии 2.2. Смесь нагревают в течение 4 ч до 50 С. Реакционную смесь затем подвергают гидролизу 10 мл воды, затем обрабатывают 100 мл этилацетата. Органическую фазу промывают 100 мл 1 н. соляной кислоты, два раза 50 мл воды,затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и этилацетата, затем перекристаллизовывают в изопропаноле. Получают 0,55 г продукта. Температура плавления: 176-177 С. 1 Н ЯМР (ДМСО D6):(м.д.) 3,8 (с, 3 Н), 3,89 (с, 3 Н), 5,9 (с, 2 Н), 6,49 (д, 1 Н), 7,2 (м, 8 Н), 7,48 (м,2 Н), 7,9 (м, 2 Н). Пример 3 (соединение 3).(1,2 ммоль) 3-фторбензилхлорида и 0,276 г (2 ммоль) карбоната калия в 10 мл диметилформамида в течение 24 ч при 60 С. Охлаждают реакционную смесь, выливают ее в смесь ледяной воды и этилацетата. После разделения фаз отделяют органическую фазу, затем промывают ее два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Получают 0,195 г масла, которое используют таким, какое он есть, на следующей стадии. 3.2. N-(1-Метил-1 Н-индол-5-ил)-5-фтор-1-(3-фторбензил)-1H-индол-2-карбоксамид (соединение 3). При 0 С вводят по каплям раствор 0,146 г (0,7 ммоль) 1-метил-1 Н-5-аминоиндола (I.T. Forbes, J.Med. Chem., 1993, 36(8), 1104) в 15 мл толуола в раствор 0,7 мл (1,4 ммоль) триметилалюминия (2 М в толуоле) в 3 мл толуола. Перемешивают в течение 15 мин, затем вводят 0,195 г (0,62 моль) этил-5-фтор 1-(3-фторбензил)-1 Н-индол-2-карбоксилата, полученного на стадии 3.1. Смесь нагревают в течение 4 ч при 50 С. Реакционную смесь подвергают гидролизу 10 мл воды, затем обрабатывают 100 мл этилацетата. Органическую фазу промывают 1 н. соляной кислотой, два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем,-6 011714 элюируя смесью циклогексана и дихлорметана. Получают 0,152 г продукта. Температура плавления: 187-189 С. 1N-(1-Метил-1 Н-индол-5-ил)-1-(4-изопропилфенил)-1 Н-индол-2-карбоксамид. 4.1. 1-(4-Изопропилфенил)-1 Н-индол-2-карбоновая кислота. Перемешивают суспензию 128,8 г (0,8 моль) 1 Н-индол-2-карбоновой кислоты, 159,2 г (0,8 моль) 4 бромкумола, 111,6 г (0,808 моль) карбоната калия и 8 г (0,1 моль) оксида меди в 200 мл диметилформамида в течение 24 ч. После охлаждения вводят 6 л воды в полученную суспензию бежевого цвета. Суспензию фильтруют, нерастворимое вещество обрабатывают 1 л раствора 1 н. соляной кислоты. Эту смесь экстрагируют 500 мл дихлорметана. Промывают органическую фазу водой, сушат над сульфатом натрия,затем концентрируют ее при пониженном давлении. Сушат при пониженном давлении и получают 204,4 г твердого вещества белого цвета, которое используют таким, какое он есть, на следующей стадии. Температура плавления: 203-204 С. 4.2. Хлорангидрид 1-(4-изопропилфенил)-1 Н-индол-2-карбоновой кислоты. Перемешивают 111 мг (0,4 ммоль) 1-(4-изопропилфенил)-1H-индол-2-карбоновой кислоты, полученной на стадии 5.1, и 90 мкл (1,2 ммоль) тионилхлорида в 2 мл дихлорэтана в течение 3 ч при нагревании с обратным холодильником. Реакционную среду концентрируют при пониженном давлении. Получают остаток, который используют таким, какой он есть, на следующей стадии. 4.3. N-(1-Метил-1 Н-индол-5-ил)-1-(4-изопропилфенил)-1 Н-индол-2-карбоксамид (соединение 30). Перемешивают суспензию 119 мг (0,4 ммоль) хлорангидрида 1-(4-изопропилфенил)-1 Н-индол-2 карбоновой кислоты, полученной на стадии 5.2, 70 мг (0,48 ммоль) 1-метил-1 Н-5-аминоиндола и 110 мкл(0,8 ммоль) триэтиламина в 2 л тетрагидрофурана в течение 18 ч при комнатной температуре. Реакционную смесь концентрируют при пониженном давлении, обрабатывают 20 мл воды и 50 мл дихлорметана. Органическую фазу отделяют, промывают 50 мл 1 н. соляной кислоты, сушат над сульфатом магния,затем концентрируют ее при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и этилацетата. Получают 0,133 г продукта. Температура плавления: 178-179 С. 1 Н ЯМР (CDCl3):(м.д.) 1,39 (д, 6H), 3,05 (септ., 1 Н), 3,8 (с, 3 Н), 6,4 (д, 1H), 7,29 (м, 11H), 7,78 (м,3 Н). Пример 5 (соединение 4).N-(1-Метил-1 Н-индол-5-ил)-1-(3-трифторметилфенил)-1 Н-индол-2-карбоксамид. 5.1. 1-(3-Трифторметилфенил)-1 Н-индол-2-карбоновая кислота. Соединение можно получить методом, аналогичным описанному на стадии 4.1. примера 4, заменив 4-бромкумол на 3-бром--трифтортолуол. 5.2. N-(1-Метил-1 Н-индол-5-ил)-1-(3-трифторметилфенил)-1 Н-индол-2-карбоксамид. Перемешивают раствор 2 г (6,55 ммоль) 1-(3-трифторметилфенил)-1H-индол-2-карбоновой кислоты(полученной методом, описанным на стадии 4.1 примера 4), 1,14 г (7,86 ммоль) 1-метил-1 Н-5 аминоиндола (I.T. Forbes, J. Med. Chem., 1993, 36(8), 1104), 1,2 мл (7,86 ммоль) диэтилцианофосфоната и 2,03 мл (14,41 ммоль) триэтиламина в 20 мл диметилформамида в течение 18 ч при комнатной температуре. Реакционную смесь концентрируют при пониженном давлении, затем обрабатывают 50 мл воды. Этот раствор экстрагируют два раза 50 мл дихлорметана. Органические фазы объединяют, сушат их над сульфатом натрия, затем концентрируют при пониженном давлении. Полученный остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и этилацетата. Выделяют 1,97 г продукта. Температура плавления: 225-226 С. 1(1,46 ммоль) пиридина в 5 мл дихлорметана в присутствии молекулярных сит 4 в течение 4 дней при комнатной температуре. Смесь выливают в 100 мл воды и 50 мл дихлорметана. Органическую фазу отделяют, промывают ее 1 н. соляной кислотой, сушат над сульфатом магния, затем концентрируют при пониженном давлении. Очищают остаток хроматографией на колонке с силикагелем, элюируя смесью циклогексана и этилацетата. Получают 0,1 г продукта, который используют таким, какой он есть, на следующей стадии. 6.2.-7 011714 При 0 С вводят по каплям раствор 0,0493 г (0,34 ммоль) 1-метил-5-амино-1 Н-индола (I.T. Forbes, J.Med. Chem., 1993, 36(8), 1104) в 5 мл толуола в раствор 0,28 мл (0,56 ммоль) триметилалюминия (2 М в толуоле) в 2 мл толуола. Перемешивают в течение 15 мин, затем вводят 0,1 г (0,28 моль) этил-1-(3 изопропилфенил)-5-трифторметилокси-1 Н-индол-2-карбоксилата, полученного на стадии 6.1. Смесь нагревают в течение 4 ч при 50 С. Реакционную смесь затем подвергают гидролизу 10 мл воды, затем обрабатывают 100 мл этилацетата. Органическую фазу промывают 100 мл 1 н. соляной кислоты, два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния,фильтруют его, затем концентрируют фильтрат при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и этилацетата, затем перекристаллизовывают его в изопропаноле. Получают 0,136 г продукта. Температура плавления: 164-165 С. 1N-(1 Н-индол-5-ил)-5-фтор-1-(3-фторбензил)-1 Н-индол-2-карбоксамид. При 0 С вводят по каплям раствор 0,46 г (3,49 ммоль) 5-амино-Н-индола в 50 мл толуола в раствор 4,76 мл (9,51 ммоль) триметилалюминия (2 М в толуоле) в 10 мл толуола. Перемешивают в течение 15 мин, затем вводят 1 г (3,17 моль) этил-5-фтор-1-(3-фторбензил)-1 Н-индол-2-карбоксилата, полученного на стадии 3.1 примера 3. Смесь нагревают в течение 4 ч при 50 С. Реакционную смесь затем подвергают гидролизу 10 мл воды, затем обрабатывают 100 мл этилацетата. Органическую фазу промывают 100 мл 1 н. соляной кислоты, два раза 50 мл воды, затем 50 мл насыщенного раствора хлорида натрия. Раствор сушат над сульфатом магния, фильтруют его, затем концентрируют фильтрат при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем, элюируя смесью циклогексана и дихлорметана. Получают 0,7 г продукта. Температура плавления: 158-163 С. 1 Н ЯМР (ДМСО D6):(м.д.) 5,87 (с, 2H), 6,38 (м, 1 Н), 6,9 (м, 2 Н), 7,1 (м, 2 Н), 7,31 (м, 5 Н), 7,51 (м,2 Н), 7,92 (с, 1 Н), 10,26 (с, 1 Н), 10,98 (с, 1 Н). Приведенная ниже табл. 1 иллюстрирует химические структуры и физические свойства нескольких соединений общей формулы (I) согласно изобретению. В этой таблице: в колонке "Тпл" указаны температуры плавления в градусах Цельсия (С). Если продукты были выделены в виде твердого аморфного вещества или масла, в этой колонке они охарактеризованы по их массе ([МН]+);- 10011714 Соединения согласно изобретению подвергли фармакологическим испытаниям in vitro и in vivo, которые выявили их применимость в качестве веществ, обладающих терапевтической активностью. Тест на ингибирование индуцированного капсаицином тока в DRG крысы Первичная культура клеток ганглиев спинного корешка (DRG) крысы. Нейроны DRG естественным путем экспрессируют рецептор TRPV1. Первичные культуры DRG новорожденных крыс получали из крысят в возрасте 1 день. После рассечения ганглии обрабатывали трипсином и клетки подвергали механической диссоциации путем осторожного растирания. Клетки повторно суспендировали в обычной среде Игла для культивирования, содержащей 10% эмбриональной бычьей сыворотки, 25 мМ KCl, 2 мМ глютамина, 100 мкг/мл гентамицина и 50 нг/мл NGF, затем накладывали на стеклянные пластинки, покрытые ламинином (0,25106 клеток на пластинку), которые затем помещали в 12-луночные коробки Corning. Клетки инкубировали при 37 С во влажной атмосфере, содержащей 5% СО 2 и 95% воздуха. Цитозин-В-D-арабинозид (1 мкМ) вводили через 48 ч после начала культивирования для предотвращения развития клеток, не являющихся нейронными клетками. Пластинки переносили в экспериментальные камеры для исследования методом фиксации потенциала через 7-10 дней после начала культивирования. Электрофизиология. Измерительные камеры (объемом 800 мкл), содержащие клеточный препарат, помещали на столик инверсионного микроскопа (Olympus IMT2), снабженного оптикой Hoffman (Modulation Contrast, NewYork), и рассматривали с увеличением 400 Х. Камеры непрерывно перфузировали самотеком (2,5 мл/мин) с помощью распределителя растворов с 8 входами и одним выходом, выполненным в виде полиэтиленовой трубки (отверстие 500 мкм) и расположенным на расстоянии по меньшей мере 3 мм от исследуемой клетки. Применяли метод фиксации потенциала с конфигурацией целая клетка. Пипетки из боросиликатного стекла (сопротивление 5-10 МОм) приближали к клетке с помощью пьезоэлектрического микроманипулятора 3D (Burleig, PC1000). Общие токи (установленный мембранный потенциал -60 мВ) регистрировали с помощью усилителя Axopatch 1D (Axon Instruments, Foster city, Californie), соединенного с ПК с программным обеспечением Pclamp8 (Axon Instruments). Следы тока регистрировали на бумаге и одновременно оцифровывали (эталонирование с частотой 15-25 Гц) и записывали на жесткий диск ПК. Нанесение раствора капсаицина 300 нМ вызывает в клетках DRG (зафиксированное напряжение-70 мВ) входящий катионный ток. Для минимизации десенсибилизации рецепторов между двумя нанесениями капсаицина соблюдали интервал, равный минимум одной минуте. После контрольного периода(стабилизация ответа только капсаицина) наносили только тестируемые соединения в концентрации 10 нМ в течение 4-5 мин, в течение которых проводили несколько тестов капсаицин+соединение (получение максимального ингибирования). Результаты выражали в % ингибирования ответа на капсаицин в контроле. Проценты ингибирования ответа на капсаицин (300 нМ) составляли от 20 до 100% для наиболее активных соединений согласно изобретению, которые тестировали в концентрации 10 нМ (см. несколько примеров в табл. 2). Соединения согласно изобретению являются, таким образом, эффективными антагонистами in vitro рецепторов типа TRPV1. Таблица 2 Тест на раздражение роговицы у мышей. Вызывающее раздражение свойство капсаицина можно легко определить по реакции роговицы, поскольку этот орган наиболее иннервирован волокнами С. В этом контексте в предварительных экспериментах нанесение очень малого количества капсаицина (2 мкл при концентрации 160 мкМ) на поверхность роговицы животного вызывает ряд стереотипных поведенческих проявлений, связанных с раздражением, которые легко описать. Из них отметили моргание глаза, потирание инстиллированного глаза передней гомолатеральной лапой, трение мордочки двумя передними лапами, почесывание гомолатеральной мордочки задней лапой. Было отмечено, что продолжительность такого поведения не превышает 2 мин, и животное возвращается к своей обычной активности. К тому же его внешний вид также является обычным. Мышь не забивается в угол со взъерошенной шерстью и никакие внешние проявления боли не наблюдаются. Из этого можно сделать вывод, что продолжительность действия капсаицина в таких дозах меньше двух минут. Краткое описание методологии. Цель серии экспериментов заключалась в определении того, могут ли соединения согласно изобретению влиять на поведенческий ответ, вызванный данным количеством капсаицина. Капсаицин первоначально разводили до 25 мМ в ДМСО и для конечного его применения разводили в Tween 80-10% в физиологическом растворе. Контрольные опыты показали, что в этих условиях раствор не имеет никакого эффекта.- 11011714 На практике тестируемый продукт вводили перорально и с интервалом (время предварительной обработки: t), который зависел от фармакологических данных, животному закапывали в глаз 2 мкл раствора капсаицина в концентрации 160 мМ, полученного, как указано выше. Наблюдение проводили в течение 2 мин после закапывания и в течение этого времени животное потирало несколько раз глаз, в который закапали раствор, передней гомолатеральной лапой. Для данного животного процент защиты вычисляли следующим способом: Р=100-число наблюдаемых потираний/среднее число потираний в группе,обработанной растворителем)100) Среднюю величину процента защиты вычисляли для каждой группы животных (n=число животных,подвергшихся испытанию с применением соединения согласно изобретению). Полученные данные по проценту защиты в этой модели для наиболее активных соединений согласно изобретению, применяемая доза которых составила 60 мг/кг (per os), составляют от 8 до 100% (см. несколько примеров в табл. 3). Таблица 3 Результаты опытных испытаний показывают, что наиболее активные соединения согласно изобретению блокируют действие, вызванное стимуляцией рецепторов TRPV1. Соединения согласно изобретению могут таким образом применяться для получения лекарственных средств, в частности, для получения лекарственного средства, предназначенного для предупреждения или лечения патологий, в которых участвуют рецепторы типа TRPV1. Так, в соответствии с другим аспектом объектом изобретения являются лекарственные средства,содержащие соединение формулы (I) или фармацевтически приемлемую соль или гидрат или сольват этого соединения. Эти лекарственные средства находят применение в терапии, в частности, для предупреждения и/или лечения боли и воспаления, боли хронической, невропатической (травматической, диабетической,метаболической, вызванной инфекцией, токсической, вызванной противораковым или ятрогенным лечением), (остео-)артритной, ревматической, фибромиалгий, боли в спине, боли, вызванной раковым заболеванием, невралгии лицевого нерва, головных болей, мигрени, зубной боли, ожога, солнечного удара,укуса животного или насекомого, постгерпетической невралгии, мышечной боли, нервного сдавливания(центрального или периферического), травм спинного или головного мозга, ишемии (спинного или головного мозга), нейродегенерации, геморрагических нарушений кровообращения (спинного и/или головного мозга), болей после инсульта. Соединения согласно изобретению можно применять для получения лекарственного средства,предназначенного для предупреждения и/или лечения урологических заболеваний, таких как гиперактивность мочевого пузыря, гиперфлексия мочевого пузыря, недержание, императивное мочеиспускание,недержание мочи, цистит, почечные колики, гиперчувствительность в области таза и боли в области таза. Соединения согласно изобретению можно применять для получения лекарственного средства,предназначенного для предупреждения и/или лечения гинекологических заболеваний, таких как вульводиния, боли, связанные с сальпингитом, дисменореей. Эти продукты можно также использовать для получения лекарственного средства, предназначенного для предупреждения и/или лечения заболеваний желудочно-кишечного тракта, таких как нарушение желудочно-пищеводного рефлекса, язва желудка, язва двенадцатиперстной кишки, функциональная диспепсия, колит, IBS, болезнь Крона, панкреатит, эзофагит, печеночные колики. Также продукты согласно настоящему изобретению можно использовать для предупреждения и/или лечения респираторных заболеваний, таких как астма, кашель, COPD, бронхостеноз, воспалительные заболевания. Эти продукты можно также использовать для предупреждения и/или лечения псориаза,пруриго, раздражений кожных, глаз или слизистых, герпеса, опоясывающего лишая. Соединения согласно изобретению можно также использовать для получения лекарственного средства, предназначенного для лечения депрессии. В соответствии с другим своим аспектом настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве активного вещества соединение согласно изобретению. Эти фармацевтические композиции содержат эффективную дозу по меньшей мере одного соединения согласно изобретению или фармацевтически приемлемую соль, гидрат или сольват указанного соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент. Указанные эксципиенты выбирают в соответствии с фармацевтической формой и требуемым способом введения из обычных эксципиентов, известных специалисту в данной области. В фармацевтических композициях по настоящему изобретению для перорального, сублингвального, подкожного, внутримышечного, внутривенного, местного, локального, интратрахеального, интрана- 12011714 зального, чрескожного или ректального введения активное вещество указанной выше формулы (I) или возможно его соль, сольват или гидрат можно вводить в виде единичной дозы в смеси с традиционными фармацевтическими эксципиентами животному или человеку для профилактики или лечения указанных выше нарушений или заболеваний. К приемлемым единичным дозированным формам относятся формы для перорального введения,такие как таблетки, мягкие или твердые желатиновые капсулы, порошки, гранулы и растворы или суспензии для перорального приема, формы для введения: сублингвального, перорального, интратрахеального, глазного, интраназального, путем ингаляции, формы для введения: местного, чрескожного, подкожного, внутримышечного или внутривенного, формы для ректального введения и имплантаты. Для местного применения можно использовать соединения согласно изобретению в составе кремов, гелей,мазей или лосьонов. В качестве примера единичная дозированная форма соединения согласно изобретению в виде таблетки может содержать следующие компоненты: соединение согласно изобретению: 50,0 мг; маннит: 223,75 мг; кроскармеллоза натрия: 6,0 мг; кукурузный крахмал: 15,0 мг; гидроксипропилметилцеллюлоза: 2,25 мг; стеарат магния: 3,0 мг. В указанных единичных дозированных формах суточная доза вводимого активного вещества может составлять от 0,001 до 30 мг активного вещества на 1 кг веса тела в зависимости от галеновой формы. Возможны особые случаи, когда дозировка может быть увеличена или уменьшена; такие дозировки не выходят за рамки изобретения. В соответствии с обычной практикой дозировку, подходящую для каждого пациента, определяет врач в соответствии со способом введения, весом и ответом пациента. В соответствии с другим аспектом настоящее изобретение относится также к способу лечения указанных выше патологий, который включает введение пациенту эффективной дозы соединения согласно изобретению или одной из его фармацевтически приемлемых солей либо гидратов или сольватов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) в которой X1, X2, X3, Х 4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена или C1-С 6-алкильную, С 3-С 7-циклоалкильную, C1-С 6-фторалкильную, C1-С 6-алкокси, C1-С 6 фторалкокси, циано, C(O)NR1R2, нитро, NR1R2, C1-С 6-тиоалкильную, -S(О)-C1-С 6-алкильную, -S(О)2-C1 С 6-алкильную, SO2NR1R2, NR3COR4, NR3SO2R5 или C6-С 10-арильную группу;X5 обозначает атом водорода или галогена или C1-С 6-алкильную, C1-С 6-фторалкильную группу; причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С 6-алкильной и C1-С 6-фторалкильной; причем R необязательно замещен в положении 4, 5, 6 и/или 7 одной или несколькими группами,выбранными из атомов галогена, C1-С 6-алкильной, C1-С 6-фторалкильной, C1-С 6-алкокси, C1-С 6 фторалкоксигрупп;Y обозначает атом водорода или C1-С 6-алкильную группу;R1 и R2 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную, С 3-С 7 циклоалкильную, С 3-С 7-циклоалкил-С 1-С 3-алкильную или С 6-С 10-арильную группу; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, азетидиновую, пирролидиновую, пиперидиновую, азепи- 13011714 новую, морфолиновую, тиоморфолиновую, пиперазиновую, гомопиперазиновую группу, причем указанная группа необязательно замещена C1-С 6-алкильной, С 3-С 7-циклоалкильной, С 3-С 7-циклоалкил-C1-С 3 алкильной или С 6-С 10-арильной группой;R3 и R4 обозначают независимо друг от друга атом водорода или C1-С 6-алкильную или C6-С 10 арильную группу;R5 обозначает C1-С 6-алкильную или С 6-С 10-арильную группу,в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 2. Соединение формулы (I) по п.1, отличающееся тем, чтоX1, Х 2, Х 3, Х 4, Z1, Z2, Z3, Z4 и Z5 обозначают независимо друг от друга атом водорода или галогена или C1-С 6-алкильную, С 3-С 7-циклоалкильную, C1-С 6-фторалкильную, C1-С 6-алкокси, C1-С 6-фторалкокси,нитро, NR1R2, C1-С 6-тиоалкильную, -S(О)-C1-С 6-алкильную, -S(О)2-C1-С 6-алкильную или С 6-С 10 арильную группу;X5 обозначает атом водорода или C1-С 6-алкильную группу; причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими C1-С 6-алкильными группами;R1 и R2 обозначают независимо друг от друга атом водорода,в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 3. Соединение формулы (I) по п.1 или 2, отличающееся тем, что причем R необязательно замещен в положении 1, 2 и/или 3 одной или несколькими группами, выбранными из C1-С 6-алкильной и C1-С 6-фторалкильной групп,причем R необязательно замещен в положении 4, 6 и/или 7 одной или несколькими группами, выбранными из атомов галогена, C1-С 6-алкильной, C1-С 6-фторалкильной, C1-С 6-алкокси, C1-С 6 фторалкоксигрупп,в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 4. Соединение формулы (I) по любому из пп.1-3, отличающееся тем, что X2 и/или X3 не являются атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 5. Соединение формулы (I) по любому из пп.1-4, отличающееся тем, что Х 5 является атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 6. Соединение формулы (I) по любому из пп.1-5, отличающееся тем, что Y является атомом водорода, в форме основания или соли присоединения кислоты, а также в форме гидрата или сольвата. 7. Соединение формулы (I) по п.1, которое представляет собойN-(1-метил-1 Н-индол-5-ил)-1-[2-(3-фторфенил)этил]-5-фтор-1 Н-индол-2-карбоксамид. 8. Способ получения соединения формулы (I) по п.1, отличающийся тем, что проводят реакцию соединения общей формулы (IV): в которой X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает C1-С 6-алкокси, с амидным соединением общей формулы (V): в которой R и Y такие, как определены в общей формуле (I) по п.1,при температуре кипения растворителя, причем амидное соединение общей формулы (V) получено предварительным взаимодействием триметилалюминия и аминоиндолов общей формулы (V). 9. Способ получения соединения формулы (I) по п.1, отличающийся тем, что превращают соединение общей формулы (IV): в которой X1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает гидроксигруппу,в хлорангидрид кислоты действием тионилхлорида при температуре кипения растворителя,и тем, что в присутствии основания проводят реакцию соединения общей формулы (IV), в которойX1, Х 2, Х 3, Х 4, Х 5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает атом хлора, с аминоиндолом общей формулы (V): в которой R и Y такие, как определены в общей формуле (I) по п.1,или тем, что проводят реакцию сочетания между соединением общей формулы (IV), в которой X1,Х 2, Х 3, Х 4, X5, Z1, Z2, Z3, Z4, Z5 и n такие, как определены в общей формуле (I) по п.1, и А обозначает гидроксигруппу, и аминоиндолом общей формулы (V), в которой R и Y такие, как определены в общей формуле (I) по п.1, в присутствии сочетающего агента и основания в растворителе. 10. Лекарственное средство для профилактики или лечения патологий, в которых участвуют рецепторы типа TRPV1, отличающееся тем, что содержит соединение формулы (I) по любому из пп.1-6 или фармацевтически приемлемую соль, или гидрат, или сольват соединения формулы (I). 11. Лекарственное средство по п.10, которое предназначено для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочнокишечного тракта, респираторных заболеваний, псориаза, прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии. 12. Фармацевтическая композиция для профилактики или лечения патологий, в которых участвуют рецепторы типа TRPV1, отличающаяся тем, что содержит соединение формулы (I) по любому из пп.1-6- 16011714 или фармацевтически приемлемую соль или гидрат или сольват этого соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент. 13. Фармацевтическая композиция по п.12, которая предназначена для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочно-кишечного тракта, респираторных заболеваний, псориаза, прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии. 14. Применение соединения формулы (I) по любому из пп.1-7 для получения лекарственного средства, предназначенного для профилактики или лечения патологий, в которых участвуют рецепторы типаTRPV1. 15. Применение соединения формулы (I) по п.14 для получения лекарственного средства, предназначенного для профилактики или лечения боли или воспаления, урологических заболеваний, гинекологических заболеваний, заболеваний желудочно-кишечного тракта, респираторных заболеваний, псориаза,прурита, раздражения кожи, глаз или слизистых, герпеса, опоясывающего лишая или для лечения депрессии. 16. Применение соединения формулы (I) по п.14, где боль или воспаление выбраны из боли хронической, невропатической (травматической, диабетической, метаболической, вызванной инфекцией, токсической, вызванной противораковым или ятрогенным лечением), (остео-)артритной, ревматической,фибромиалгий, боли в спине, боли, вызванной раковым заболеванием, невралгии лицевого нерва, головных болей, мигрени, зубной боли, ожога, солнечного удара, укуса животного или насекомого, постгерпетической невралгии, мышечной боли, нервного сдавливания (центрального или периферического), травм спинного или головного мозга, ишемии (спинного или головного мозга), нейродегенерации, геморрагических нарушений кровообращения (спинного и/или головного мозга), болей после инсульта. 17. Применение соединения формулы (I) по п.14, где урологические заболевания выбраны из группы, включающей гиперактивность мочевого пузыря, гиперфлексия мочевого пузыря, недержание, императивное мочеиспускание, недержание мочи, цистит, почечные колики, гиперчувствительность в области таза и боли в области таза. 18. Применение соединения формулы (I) по п.14, где гинекологические заболевания выбраны из группы, включающей вульводинию, боли, связанные с сальпингитом, дисменорею. 19. Применение соединения формулы (I) по п.14, где заболевания желудочно-кишечного тракта выбраны из группы, включающей нарушение желудочно-пищеводного рефлекса, язву желудка, язву двенадцатиперстной кишки, функциональную диспепсию, колит, IBS, болезнь Крона, панкреатит, эзофагит,печеночные колики. 20. Применение соединения формулы (I) по п.14, где респираторные заболевания выбраны из группы, включающей астму, кашель, COPD, бронхостеноз, воспалительные заболевания.
МПК / Метки
МПК: A61K 31/404, C07D 209/42, A61P 29/00
Метки: производные, терапии, n-(1h-индолил)-1н-индол-2-карбоксамидов, получение, применение
Код ссылки
<a href="https://eas.patents.su/18-11714-proizvodnye-n-1h-indolil-1n-indol-2-karboksamidov-ih-poluchenie-i-ih-primenenie-v-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Производные n-(1h-индолил)-1н-индол-2-карбоксамидов, их получение и их применение в терапии</a>
Предыдущий патент: Получение гидрохлоридов производного тетразола
Следующий патент: Липосомы, включающие радиоактивный изотоп, и цитотоксический агент для комбинированной терапии
Случайный патент: Птицезащитное устройство для линии электропередачи с подвесными изоляторами и линия электропередачи, снабженная такими устройствами












