Бензамиды для лечения нейродегенеративных заболеваний
Номер патента: 2031
Опубликовано: 24.12.2001
Авторы: Пэйлор Ричард Е., Вилкокс Аллан Л., Гэрлэнд Вильям А., Флиттер Вильям Дэвид
Формула / Реферат
1. Ацетамидобензамид формулы
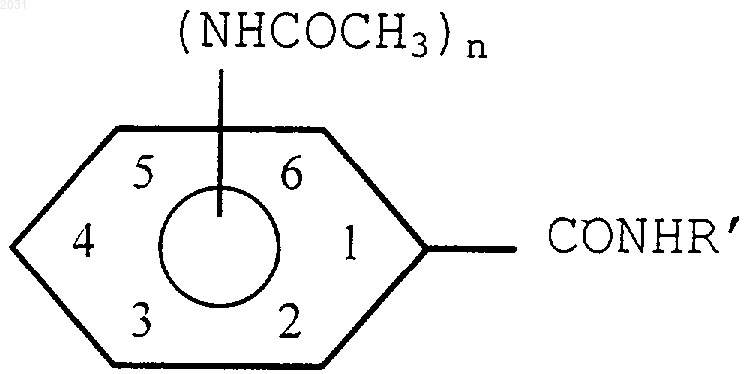
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2, при условии, что когда n=1 и R' представляет собой либо н-бутил, либо н-пропил, ацетамидогруппа не находится в положении 2 кольца; когда n=1, ацетамидогруппа не находится в положении 3 кольца; и когда n=2, ацетамидогруппы не находятся в положениях 3 и 5 кольца.
2. Соединение по п.1, выбираемое из группы, состоящей из N-изопропил-4-ацетамидобензамида, N-трет-амил-4-ацетамидобензамида и N-метилциклопропил-4-ацетамидобензамида.
3. Соединение по п.1, представляющее собой N-трет-бутил-4-ацетамидобензамид.
4. Нитро- или аминобензамид формулы
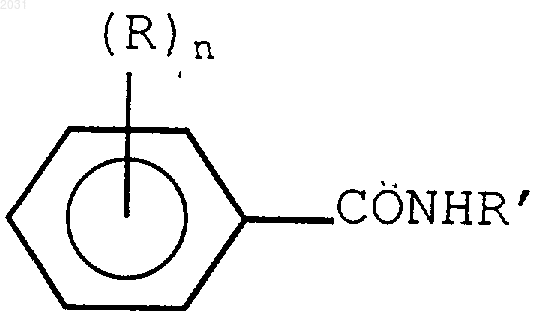
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, каждый R независимо представляет собой -NO2 или -NH2, и n=1 или 2, выбираемое из группы, состоящей из N-трет-амил-4-нитробензамида, N-1,2-диметилпропил-4-нитробензамида, N-н-бутил-3-нитробензамида, N-пeнтил-4-нитpoбeнзaмидa, N-2-метилбутил-4-нитробензамида, N-н-бутил-3,5-динитробензамида, N-метилциклопропил-4-нитробензамида, N-н-бyтил-2-нитpoбeнзaмидa, N-н-пентил-2-нитробензамида и N-метилциклопропил-4-аминобензамида.
5. Способ получения ацетоамидобензамида формулы

где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2, включающий следующие стадии:
а) конденсацию насыщенного алкиламина, содержащего от 3 до 5 атомов углерода, с нитробензоилгалогенидом формулы
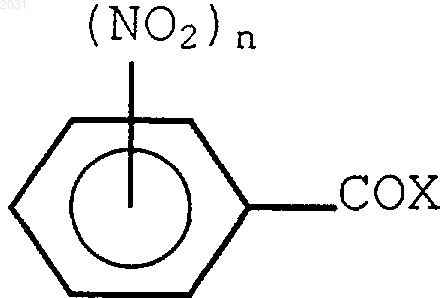
где n=1 или 2 и Х представляет собой галоген, такой как I, Br, F или Сl, с получением соединения III
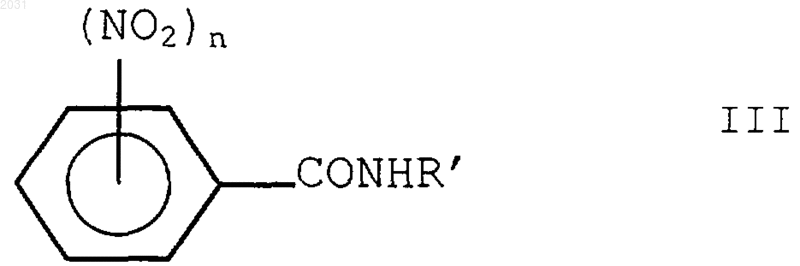
b) восстановление NO2-групп в соединении (III) до NН2-групп; и
с) ацетилирование NН2-групп в NНСОСН3-группы.
6. Способ получения производных бензамида формулы
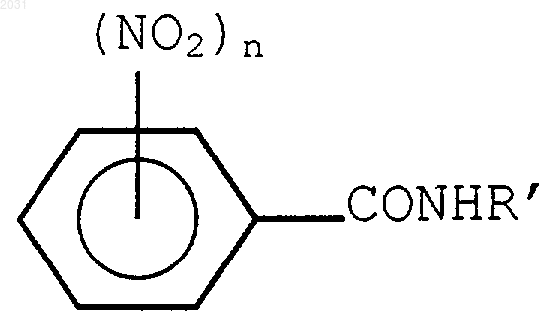
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2 при следующих условиях:
1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является трет-бутилом, изобутилом или пропилом;
2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и
3) когда n=2 и R' представляет собой трет-бутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца, включающий стадию конденсации насыщенного алкиламина, содержащего от 3 до 5 атомов углерода, с нитробензоилгалогенидом формулы
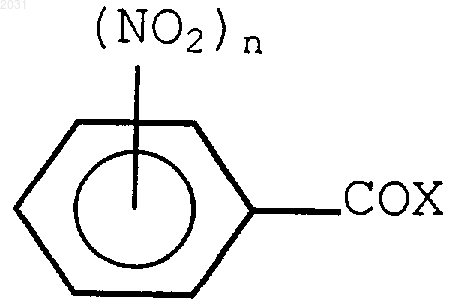
где n=1 или 2 и Х представляет собой галоген, такой как I, Br, F или Сl, с получением соединения формулы
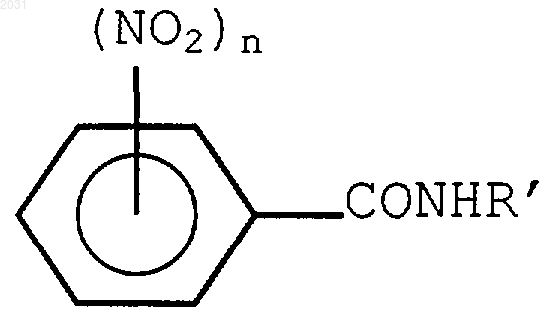
7. Способ получения производных бензамида формулы
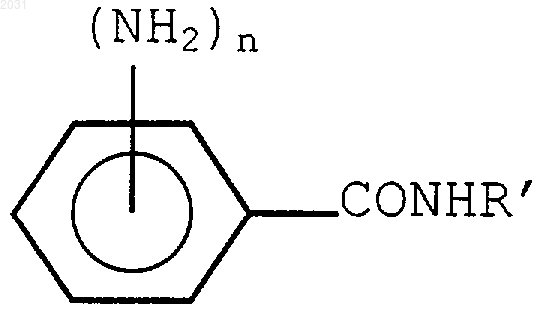
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2, включающий следующие стадии:
а) конденсацию насыщенного алкиламина, содержащего от 3 до 5 атомов углерода, с нитробензоилгалогенидом формулы
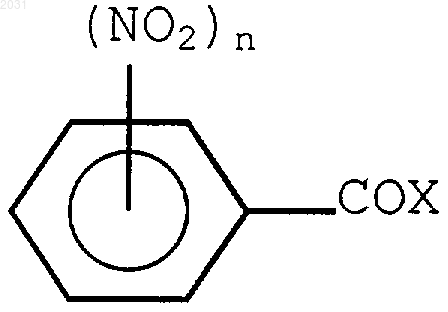
где n=1 или 2, и Х представляет собой галоген, такой как I, Br, F или Сl, с получением соединения формулы
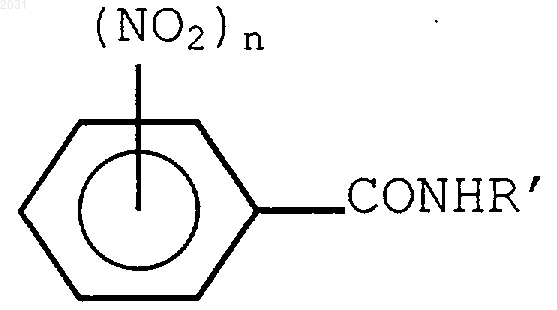
b) восстановление NО2-групп до NH2-групп.
8. Фармацевтическая композиция, включающая производное бензамида формулы I
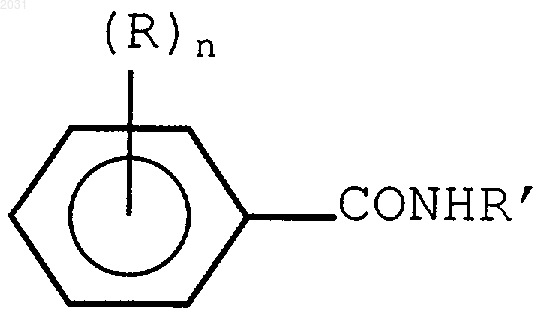
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, каждый R независимо представляет собой -NO2, или -NH2, или -NH-CO-СН3, и n=1 или 2, при следующих условиях:
1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является трет-бутилом, изобутилом или пропилом;
2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и
3) когда n=2 и R' представляет собой трет-бутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца,
в фармацевтически приемлемом носителе.
9. Фармацевтическая композиция по п.8, где производное бензамида представляет собой ацетамидобензамид формулы
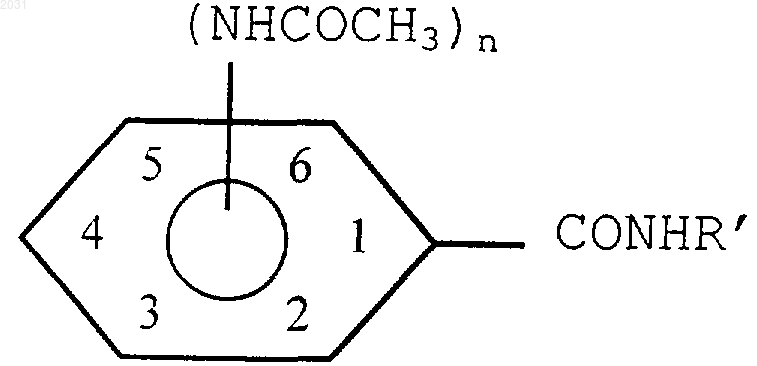
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2.
10. Фармацевтическая композиция по п.9, где n=1 и R' представляет собой трет-бутил или трет-амил.
11. Фармацевтическая композиция по п.10, где производное бензамида представляет собой N-трет-бутил-4-ацетамидобензамид.
12. Фармацевтическая композиция по п.9, где производное бензамида выбирают из группы, состоящей из N-изопропил-4-ацетамидобензамида, N-трет-амил-4-ацетамидобензамид, N-трет-бутил-3-ацетамидобензамида, N-метилциклопропил-4-ацетамидобензамида.
13. Фармацевтическая композиция по п.8, где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, каждый R независимо представляет собой -NO2 или -NH2, и n=1 или 2, при следующих условиях:
1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является трет-бутилом, изобутилом или пропилом;
2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и
3) когда n=2 и R' представляет собой трет-бутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца.
14. Фармацевтическая композиция по п.13, где производное бензамида представляет собой N-трет-бутил-4-аминобензамид.
15. Фармацевтическая композиция по п.13, где производное бензамида выбирают из группы, состоящей из
N-изопропил-4-нитробензамида,
N-трет-бутил-3-нитробензамида,
N-трет-бутил-2-нитробензамида,
N-н-бутил-4-нитробензамида,
N-н-пропил-4-нитробензамида и
N-трет-бутил-3,5-динитробензамида,
N-метилпропил-4-нитробензамида (CPI1084) и
N-трет-бутил-3-аминобензамида.
16. Фармацевтическая композиция по п.8, где носитель является носителем для орального приема или носителем для инъекций.
17. Способ лечения пациента, страдающего от нейродегенеративного состояния, включающий введение пациенту эффективного терапевтического количества фармацевтической композиции по пп.8-16.
18. Способ по п.17, где нейродегенеративное состояние связано с постепенной утратой функций центральной нервной системы.
19. Способ по п.18, где нейродегенеративное состояние представляет собой состояние, связанное с допамином.
20. Способ по п.19, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
21. Способ по п.17, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
22. Способ по п.17, где нейродегенеративное состояние связано с постепенной утратой функций центральной нервной системы, обусловленной митохондриальной дисфункцией.
23. Способ по п.17, где указанное введение является пероральным.
24. Способ по п.17, где указанное введение является парентеральным.
25. Способ по п.17, где указанное введение осуществляют путем внутривенного вливания.
26. Применение производного бензамида формулы I
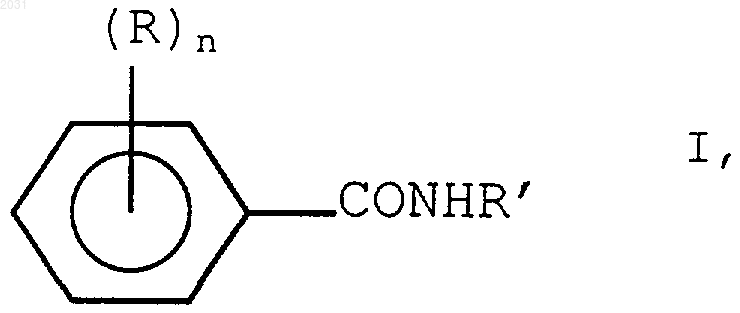
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, каждый R независимо представляет собой -NO2, или -NH2, или -NН-СО-СН3 и n=1 или 2 при следующих условиях:
1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является трет-бутилом, изобутилом или пропилом;
2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и
3) когда n=2 и R' представляет собой трет-бутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца,
для лечения нейродегенеративного состояния.
27. Применение по п.26, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
28. Применение по п.26, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
29. Применение ацетобензамида по п.1 для лечения нейродегенеративного состояния.
30. Применение по п.29, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
31. Применение по п.29, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
32. Применение по п.26, где производное бензамида представляет собой N-трет-бутил-4-аминобензамид.
33. Применение по п.32, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
34. Применение по п.32, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
35. Применение по п.29, где ацетобензамид представляетсобой N-трет-бутил-4-ацетамидобензамид.
36. Применение по п.35, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
37. Применение по п.35, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
38. Применение производного бензамида формулы I
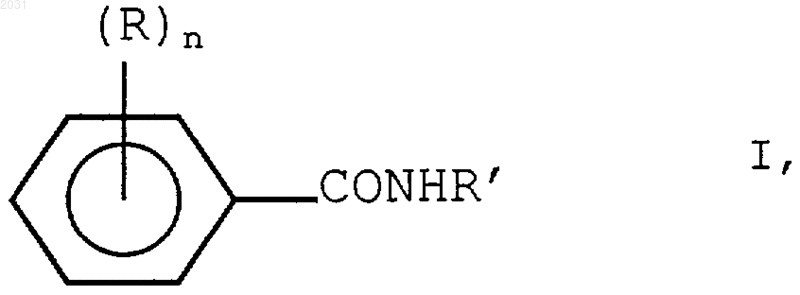
где R', R и n имеют значения, определенные в п.26, в получении композиции для лечения нейродегенеративного состояния.
39. Применение по п.38, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
40. Применение по п.38, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
41. Применение ацетамидобензамида формулы
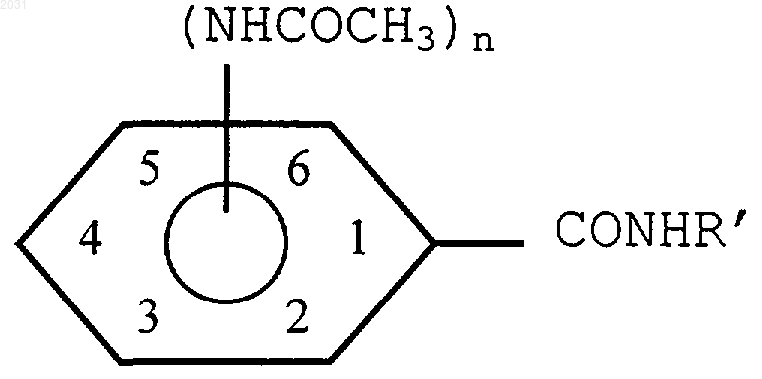
где R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n=1 или 2 для получения композиции для лечения нейродегенеративного состояния.
42. Применение по п.41, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
43. Применение по п.41, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
44. Применение по п.41, где ацетамидобензамид представляет собой соединение по п.1.
45. Применение по п.44, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
46. Применение по п.44, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
47. Применение N-трет-бутил-4-ацетамидобензамида в получении композиции для лечения нейродегенеративного состояния.
48. Применение по п.47, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
49. Применение по п.47, где нейродегенеративное состояние представляет собой болезнь Альцгеймера.
50. Применение по п.38, где производное бензамида представляет собой N-трет-бутил-4-аминобензамид.
51. Применение по п.50, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
Текст
1 Область изобретения Настоящее изобретение относится к производным бензамида, содержащим их фармацевтическим композициям, способам получения этих производных и их применению для лечения и предупреждения нейродегенеративных состояний. Предпосылки создания изобретения Нейродегенеративные состояния охватывают целый ряд серьезных нарушений, включающих болезнь Паркинсона, амиотрофический боковой склероз (ALS, болезнь Лу Гехрига)(LouGehrig), рассеянный склероз, болезнь Хантингтона, болезнь Альцгеймера, диабетическую ретинопатию, мультиинфарктную деменцию, дегенерацию желтого пятна сетчатки и другие. Эти нарушения характеризуются постепенным,но неослабным ухудшением состояния здоровья пациента в течение определенного периода времени. Механизмы и причины этих заболеваний постепенно изучались и на этой основе предлагались различные методы лечения. Одно из таких нейродегенеративных нарушений, болезнь Паркинсона, связано с аномальным истощением допамина в избранных участках головного мозга. Недавние обзоры литературы в области изучения болезни Паркинсона сделаны Марсденом (Marsden C.D.) в статье "Болезнь Паркинсона (Parkinson's Disease), опубликованной в Lancet (April 21, 1990), 948-952, и Кальне (Calne(Treatment of Parkinson's Disease), опубликованной в NEJM (Sept. 30, 1993), 329, 1021-1027. Показано, что дефицит допамина идентифицирован как ключевая характеристика болезни Паркинсона, а деструкция допаминэргического нигростриального метаболического пути идет параллельно с истощением допамина у пациентов с болезнью Паркинсона. Быстрое развитие симптомов, подобных болезни Паркинсона, у небольшой группы больных - потребителей незаконных лекарственных препаратов в г. Сан-Хосе, шт. Калифорния, связано со следами токсичных примесей,присутствующих в лекарствах, полученных в домашних условиях. Последующие исследования, проводимые Лэнгстоном на моделях животных, включающих обезьян, показали, что причиной заболевания с симптомами, подобными болезни Паркинсона, которые развивались у потребителей незаконных лекарств, является 1 метил-4-фенил-1,2,5,6-тетрагидропиридинSynthesis", Science, February 25, 1983, 219, 979980). Эти ранние открытия и стимулированные ими многочисленные исследования привели к созданию надежных моделей болезни Паркинсона (Heikkila R.E. et al., "Dopaminergic Neurotoxicity of 1-Methyl-4-Phenyl-1,2,5,6-Tetrahydropyridine in Mice", Science, June 29, 1984, 224, 002031Parkinson's Disease", European Journal of Pharmacology, 1991, 208, 273-286). Эти и другие работы описывают результаты исследований для того,чтобы помочь в объяснении механизма нарушения двигательной активности при болезни Паркинсона, вызванного введением МФТГП. Они ясно указывают на тот факт, что МФТГП является причиной появления паркинсоно-подобных симптомов у людей, принимающих загрязненные примесями незаконные лекарственные препараты, и что подобные двигательные нарушения были установлены у других приматов и подопытных животных, которым непосредственно вводили МФТГП. Результаты работ дополнительно указывают, что введение МФТГП вызывает заметное уменьшение у них концентрации допамина. Сделанные открытия привели к разработке биологического испытания для агентов, эффективных при лечении нейродегенеративных нарушений, связанных с допамином, таких как болезнь Паркинсона. В этом испытании подопытным животным дают некоторое количество МФТГП, адекватное тому количеству, которое вызывает сильное снижение уровня допамина. Далее вводят исследуемые соединения для того,чтобы определить, способны ли они предупредить потери допамина у подопытных животных. В той степени, в какой сохраняется концентрация допамина, исследуемое соединение можно рассматривать в качестве эффективного агента для замедления или остановки развития нейродегенеративного заболевания, например болезни Паркинсона. Была также разработана и другая методика биологического испытания для агентов, эффективных при лечении нейродегенеративных нарушений, связанных с допамином. В этом испытании в "полосатое тело" подопытных животных вводят нейротоксикант,6 гидроксидопамин. Это соединение оказывает действие, направленное на снижение концентрации допамина, и широко применяется для моделирования такого состояния. Исследуемые соединения вводят для того, чтобы определить,способны ли они предупредить или снизить потери допамина у подопытных животных. Как и в предыдущем случае, в той степени, в какой сохраняется концентрация допамина, исследуемое соединение можно расматривать в качестве эффективного терапевтического агента. Митохондриальная функция связана со многими нейродегенеративными нарушениями,такими как амиотрофический боковой склерозAustin, TX, 1995, например на страницах 53-61 и 73-99). Митохондриальное нарушение представляет собой механизм, по которому МФТГП истощает содержание допамина в неостриатумеDisease", CNS Drugs, 1994, 1, 45-46). Таким образом агент, который защищает от митохондриальной дисфункции, вызванной МФТГП, может быть полезным при лечении заболеваний центральной нервной системы, когда причина, лежащая в основе заболевания, представляет собой митохондриальную дисфункцию. Кроме того, имеются модели для определения эффективности лекарственных средств при лечении других нейродегенеративных состояний. Например, эффективность против болезни Альцгеймера можно определить в испытаниях на клеточных культурах. В двух таких испытаниях соединения оценивают на их способность осуществлять защиту против амилоида 6 ета(25-35) или утраты нервных клеток, вызываемых глутаматом, в культурах астроцитов или гиппокампа эмбриона крысы. В другом испытании соединения оценивают на их способность вмешиваться в образование амилоидного бета(1-40) бета-складчатого листа. Соединения,которые оказывают этот эффект, можно рассматривать как возможные агенты для лечения болезни Альцгеймера. Хотя бензамидные производные известны,их назначение было в основном связано с применением в качестве промежуточных соединений для химического синтеза или в области, не связанной с настоящим изобретением. Незначительные структурные изменения приводят к большим различиям в их эффективности и токсичности. Скрининг значительного большинства производных бензамида показал незначительную активность или ее полное отсутствие у этих соединений. Однако в литературе имеются сообщения относительно биологической активности других, отличающихся по структуре бензамидов. К этим сообщениям относятся следующие работы:arousal" Science (1994) 263:689-690. Другие бензамидосодержащие фармацевтические композиции и их применение для лечения или предупреждения нейродегенеративных состояний раскрыты в совместном патенте США 5 472 983. Изложение сущности изобретения Раскрываются фармацевтические композиции на основе бензамида, обладающие активностью против нейродегенеративных заболеваний. Эти композиции включают одно и более соединений из числа производных ацетамидобензамида, аминобензамида или нитробензамида формулы I в качестве активного агента в фармацевтически приемлемом носителе.R1 в формуле I представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, каждый R независимо представляет собой -NH-CO-СН 3, -NO2 или -NH2, и n = 1 или 2, при следующих условиях: 1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является третбутилом, изобутилом или пропилом; 2) когдаn=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 и R' представляет собой трет-бутил и оба R представляют собой -NO2,эти группы R не находятся в положениях 3 и 5 кольца. Носитель предпочтительно является веществом для приема внутрь, однако может также представлять собой и носитель, применяемый для инъекций. Эти фармацевтические композиции могут быть в нерасфасованном виде "ангро" или представлены в виде единичной дозы. В предпочтительном варианте фармацевтические композиции включают одно и более производных ацетамидобензамида формулы II в качестве активного агента. Эти композиции проявляют активность против болезни Паркинсона, измеряемую их способностью предупреждать снижение уровня допамина, вызываемое МФГТП и 6-гидроксидопамином.R' в формуле II представляет собой прямой, разветвленный или циклический насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n = 1 или 2. Некоторые из бензамидных производных,применяемых в этих композициях, являются известными соединениями, в то время как другие являются новыми. Эти новые соединения, а также некоторые другие новые нитробензамиды и аминобензамиды, которые могут использоваться в качестве промежуточных химических соединений для получения активных веществ,составляют дополнительные аспекты настоящего изобретения. Таким образом, предмет изобретения составляют ацетамидо-бензамиды формулы II, гдеR' представляет собой прямой, разветвленный или циклический насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n = 1 или 2,при условии, что когда n=1 и R' представляет собой либо н-бутил либо н-пропил, ацетамидогруппа не находится в положении 2 кольца; когда n=1, ацетамидогруппа не находится в положении 3 кольца; и когда n=2, ацетамидогруппы не находятся в положениях 3 и 5 кольца. Следующие нитро- и аминобензамиды составляют еще один аспект изобретения: N-третамил-4-нитробензамид (CPI1033), N-1,2-диметил-пропил-4-нитробензамид (CPI1085), N-нбутил-3-нитробензамид (CPI1135), N-н-пентил 4-нитробензамид (CPI1140), N-2-метилбутил-4 нитробензамид (CPI1146), N-н-бyтил-3,5-динитpoбeнзaмид (CPI1147), N-метилциклопропил-4 нитробензамид (CPI1164), N-н-бутил-2-нитробензамид(CPI1173),N-н-пентил-2-нитробензамид (CPI1174), и N-метилциклопропил-4 аминобензамид (CPI1240). Цифровые обозначения CPI, которые указаны для каждого из этих соединений и используются по всему описанию,являются их внутренними идентификационными номерами и применяются для того, чтобы упростить представление данных в примерах. Другим аспектом настоящего изобретения является способ лечения пациента, страдающего от нейродегенеративного заболевания и, в частности, от заболевания, связанного с допамином. Способ включает введение соответствующего эффективного терапевтического количества одной и более вышеописанных фармацевтических композиций. Еще одним аспектом настоящего изобретения является способ лечения пациента, страдающего от нарушения, которое характеризуется постепенной утратой функций центральной нервной системы (ЦНС). Способ включает введение такому пациенту эффективного количества одной и более вышеописанных фармацевтических композиций. 6 Наиболее важным аспектом настоящего изобретения является способ лечения пациента,страдающего постепенной потерей функции ЦНС, связанной с болезнью Паркинсона. Способ включает введение такому пациенту (предпочтительно внутрь) эффективного количества одной и более вышеописанных фармацевтических композиций. Другим аспектом настоящего изобретения является способ лечения пациента, страдающего постепенной потерей функции ЦНС, которая обусловлена митохондриальной дисфункцией. Способ включает введение такому пациенту эффективного количества одной и более вышеописанных фармацевтических композиций. Дополнительным аспектом настоящего изобретения являются способы получения соединений формул I и II. Эти способы включают конденсацию алкиламина, содержащего от 3 до 5 атомов углерода, с моно- или динитробензоилгалогенидом, имеющим нитроконфигурацию,соответствующую желаемому нитро-, аминоили ацетамидозамещению в целевом соединении, необязательное восстановление нитрогрупп, и необязательное превращение аминобензамидов в ацетамидобензамиды путем взаимодействия с ацетилгалогенидом. Подробное описание изобретения Бензамиды Настоящее изобретение предусматривает применение некоторых ацетамидобензамидов,аминобензамидов и нитробензамидов в качестве активных фармацевтических агентов. Ацетамидобензамиды описываются формулой I, когда R представляет собой ацетамидогруппу, и формулой II. В этих формулах R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n = 1 или 2. Ацетамидогруппа (или группы) могут присутствовать в любом месте кольца. Предпочтительные примеры включают случай, когда n=1 и ацетамидогруппа находится в положении 2, 3 или 4 кольца, и когда n=2 и ацетамидогруппы находятся в положениях 2 и 3, 2 и 4, 2 и 5, 2 и 6,3 и 4 или 3 и 5 кольца. Что касается алкилзаместителей R', то предпочтительными являются соединения, гдеR' представляет собой алкил, который не включает водород у альфа-углеродного атома, то есть атома углерода, который связан с атомом азота кольца. Примерами предпочтительных R'-групп являются трет-бутил и трет-амил. Особый интерес представляют следующие ацетамидобензамиды формулы I: 7 Наиболее предпочтительным производным бензамида является N-трет-бутил-4-ацетамидобензамид (CPI1189). В семействе ацетамидобензамидов имеются многочисленные новые соединения. В частности, это ацетамидобензамиды формулы I, когда R представляет собой ацетамидогруппу, и формулы II, где n = 1 или 2 и R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, при условии, что когда n=1 иR' представляет собой либо н-бутил либо нпропил, ацетамидогруппа не находится в положении 2 кольца; когда n=1, ацетамидогруппа не находится в положении 3 кольца; и когда n=2,ацетамидогруппы не находятся в положениях 3 и 5 кольца. Пять вышеуказанных ацетамидобензамидов, используемых в качестве предпочтительных активных агентов, представляют собой предпочтительные новые соединения, причем наиболее предпочтительным является соединение CPI1189. Аминобензамиды и нитробензамиды, применяемые в качестве активных агентов, описываются формулой I, где R - амино- или нитрогруппа. В этих формулах R' представляет собой насыщенный алкил, содержащий от 3 до 5 атомов углерода, и n = 1 или 2, с теми же предпочтительными значениями заместителей и их положениями, указанными для ацетамидобензамидов, и кроме того, при условии, что 1) когдаn=1 и R представляет собой -NO2 в положении 4 кольца, R' не является трет-бутилом, изобутилом или пропилом; 2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 иR' представляет собой трет-бутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца. Особый интерес представляют следующие аминобензамиды и нитробензамиды формулы I:N-трет-бутил-3-аминобензамид (CPI1248). В семействе аминобензамидов и нитробензамидов имеются многочисленные новые соединения; кроме того, имеются и дополнительные новые соединения, которые служат промежуточными продуктами в синтезе указанных соединений и описанных выше производных ацетамидобензамидов. В частности, эти новые амино- и нитробензамиды включают следующие соединения:(CPI1240). Когда производное бензамида содержит аминогруппу, как в случае соединения CPI1240,данный аминный заместитель может присутствовать как сам по себе, так и в виде соли. В солевой форме аминогруппа протонируется в катионную форму в сочетании с фармацевтически приемлемым анионом, таким как хлорид, бромид, иодид, гидроксил, нитрат, сульфонат, метансульфонат, ацетат, тартрат, оксалат, сукцинат или пальмоат. Когда в описании делают ссылку на аминобензамиды, следует понимать,что сюда включены также и упомянутые соли. Совместный патент США 5 472 983, на который выше была сделана ссылка, раскрывает несколько бензамидов, полезных при лечении нейродегенеративных заболеваний, основанном на их защитном действии (изучение на модели болезни Паркинсона, инициируемой МФТГП,на мышах). N-трет-бутил-4-ацетамидобензамид(CPI1189) представляет собой продукт биопревращения in vivo одного из этих бензамидов (Nтрет-бутил-4-нитробензамида (CPI1020, найденный в крови крыс и мышей, которым соединение CPI1020 вводилось внутрь. Это вещество,по-видимому, образуется в организме благодаря восстановлению кольцевой нитрогруппы соединения CPI1020 в аминогруппу (CPI1160) с последующим ацетилированием аминофункциональности. Соединения, заявленные в настоящем изобретении, экспериментально иллюстрированные продуктом CPI1189, обладают гораздо большей активностью, чем CPI1020 (примерно в 10 раз) для защиты мышей от снижения концентрации допамина в полосатом теле, вызванного подкожным введением МФТГП. На основании структуро-подобных молекул, таких как ацетаминофен, которые содержат ацетамидогруппу,эти соединения должны быть более безопасны,чем CPI1020, поскольку они не должны трансформироваться в ходе обмена веществ в организме, приводя к образованию метаболитов,содержащих гидроксиламины (положительный результат теста Эймса) и, вероятно, не приводить к появлению амино-метаболитов, которые способны оказывать сердечно-сосудистый и/или анорексический эффект. Фармацевтические композиции На основе производных бензамидов формулы I и II можно приготовить фармацевтические композиции, пригодные как для внутрен 9 него приема, так и для введения другими путями, в частности, парентерального путем инъекций или внутривенным вливанием. Фармацевтические композиции, использующиеN-трет-бутил-3-аминобензамид (CPI1248),являются предпочтительными, причем композиции на основе N-трет-бутил-4-ацетамидобензамида (CPI1189) в настоящее время являются наиболее предпочтительными. Композиции для внутреннего введения могут присутствовать в нерасфасованных жидких растворах, суспензиях или порошках. Однако более распространены композиции в виде дозируемых единиц, что облегчает достижение точности введения. Типичные дозируемые единичные формы включают предварительно заполненные и градуированные ампулы и шприцы для жидких композиций и таблетки, лепешки,капсулы и др. в случае твердых композиций. В таких композициях бензамидное производное составляет небольшую часть от общего веса (от 0,1 до 50 вес.%, предпочтительно, от 1 до 40 вес.%), причем оставшаяся часть приходится на различные носители и вспомогательные добавки, полезные для приготовления дозированной формы. Жидкие композиции включают подходящие водные и неводные растворители совместно с буферирующими, суспендирующими и диспергирующими агентами, красителями, отдушками и другими добавками. Твердые формы включают, например, любой из следующих ингредиентов или соединений аналогичной природы: связующее, такое как микрокристаллическая целлюлоза, трагакант или желатин; нейтральную добавку, такую как крахмал или лактозу, дезинтегрирующий агент, такой как альгининовая кислота, примогель (Primogel) или кукурузный крахмал; смазку, такую как стеарат магния; добавку для придания скользящих свойств (глайдент), такую как коллоидальная двуокись кремния; подслащивающую добавку, такую как сахароза или сахарин; или вкусовую добавку, такую как мята перечная, метилсалицилат или вещество с апельсиновым привкусом. Инъекции основаны как правило на стерильных физиологических или фосфатнобуферных растворах и других известных носителях. И здесь бензамидное производное составляет небольшую часть от общего веса, часто от 0,05 до 10 вес.%, причем оставшаяся часть приходится на инъекционный носитель и другие 10 вспомогательные добавки. Жидкие формы могут представлять собой растворы или суспензии. Указанные компоненты для композиций внутреннего введения или для инъекций являются исключительно иллюстративными. Другие материалы, а также методики приготовления препаративных форм описаны в сб. Remington'sPharmaceutical Sciences. 17th edition, part 8, 1985,Mack Publishing Company, Easton, Pennsylvania,который приводится в настоящем описании в виде ссылки. Соединения, заявленные в настоящем изобретении, назначают также в виде форм с пролонгированным высвобождением или доставляют из систем доставки с пролонгированным высвобождением. Описание типичных представителей таких систем можно найти в Remington's Pharmaceutical Sciences. Состояния, подвергаемые лечению, и описание курса лечения Состояния, подвергаемые лечению бензамидсодержащими фармацевтическими композициями, можно классифицировать как нейродегенеративные нарушения. К ним относятся нарушения, характеризующиеся длительной низкой нагрузкой на центральную нервную систему (ЦНС) и постепенным снижением функции ЦНС. Такие нарушения включают болезнь Паркинсона, амиотрофический боковой склероз(ALS, болезнь Лу Гехрига)(Lou Gehrig), рассеянный склероз, болезнь Хантингтона, болезнь Альцгеймера,диабетическая ретинопатия,мультиинфарктная деменция, дегенерация желтого пятна сетчатки и другие. Каждое из этих состояний отличается постепенным снижением функции ЦНС. Фармацевтические композиции,содержащие производные бензамидов, при их введении внутрь или в виде инъекций внутривенно, могут замедлить и возможно даже в некоторой степени восстановить утраченную функцию. Величина вводимых доз для лечения этих состояний колеблется от 0,1, по крайней мере,до 10 мг/кг/ч, все дозы вводят примерно за период от 1 до 120 ч, и в особенности от 24 до 96 ч. Можно назначить предварительный болюс примерно от 0,1 до 10 мг/кг для достижения адекватной установившейся концентрации лекарства в организме. Предполагается, что максимальная общая доза увеличивается примерно до 2 г/сут на 40-80 кг веса тела пациента. Для указанных нейродегенеративных нарушений курс лечения обычно растягивается на много месяцев или лет, поэтому прием внутрь предпочтителен для пациента с точки зрения удобства и выносливости к принимаемому лекарству. При введении внутрь характерный курс рассчитан на 1-5, часто 2-4 и как правило 3 дозы в сутки. Используя такую схему, каждая доза обеспечивает примерно от 1 до 20 мг/кг бензамида, причем предпочтительной является доза 11 примерно от 1 до 10 мг/кг и наиболее предпочтительной от 1 до 5 мг/кг веса тела. Конечно, бензамидное производное можно вводить в виде только одного активного агента либо в сочетании с другими агентами, включая и другие активные производные бензамидов. Способы получения соединений Производные бензамидов, заявленные в настоящем изобретении, получают из обычных исходных соединений и легко достигаемых реакций. Одной из представительных реакционных схем, которая протекает с участием третбутиламина, но которую можно осуществить с любым алкиламином, включает следующие реакции. На стадии (А) образуются N-третбутилнитробензамиды (III). Эту реакцию осуществляют при температуре ниже 10 С. Стадия (А) в качестве бензамидов формулы (III) дает соединения, где R представляет собой -NO2. На стадии (В) нитрогруппы в моно- и динитробензамиде III подвергают восстановлению. Его обычно проводят в присутствии восстановителя, такого как гидразин, и подходящего катализатора, такого как гетерогенная платина, гидроокись железа (III), палладиевый или никелевый катализатор (как правило на носителе) или в присутствии газообразного водорода и катализатора. Стадия (В) в качестве бензамидов формулы (IV) дает соединения, где R представляет собой -NH2. На стадии (С) аминобензамиды формулы(IV) превращают в ацетамидобензамиды формулы (V) путем взаимодействия с ацетилгалогенидом, таким как ацетилхлорид. Реакцию осуществляют в присутствии мягкого основания и в интервале температур от низких до температуры окружающей среды, например, в интервале от -20 С до +20 С. Реакция приводит к получению соединений, заявленных в настоящем изобретении, где R представляет собой ацетамидо. 12 Для получения заявленных соединений можно использовать и альтернативные схемы синтеза. Ниже примеры таких схем даны для соединения CPI1189, используемого в качестве иллюстративного. Используя альтернативные схемы синтеза, можно получить другие соединения путем введения в реакцию соответствующих исходных продуктов, таких как 2- или 3-амино- или нитробензонитрил, или 2,3-, 2,4-,2,5-, 2,6-, 3,4- или 3,5-диамино- или динитробензонитрил и соответствующий спирт (альтернативный путь 1), или аналогично замещенные производные толуола и соответствующий алкиламин (альтернативный путь 3). Альтернативный путь 1. Этот маршрут начинают с ацетилирования,например, 4-аминобензонитрила (А), переводя его в соединение (В) стандартными методами. Кислый гидролиз трет-бутанола в присутствии 4-ацетамидобензонитрила (В) обеспечивает на практике синтез, приводящий к получению соединения CPI1189. Альтернативный путь 2. Ацетилирование по стандартной методике недорогого исходного продукта в виде парааминобензойной кислоты (ПАБК) (С) обеспечивает дешевый способ получения 4-ацетамидобензойной кислоты (D). Превращение (D) в хлорангидрид (Е) по стандартной методике (например, с использованием SOCl2) с последующим амидированием также стандартными методами,уже описанным выше, обеспечивает получение соединения CPI1189 из недорогого сырья. Альтернативный путь 3. Другой способ получения заявленных соединений начинают с ацетилирования, проводимого по стандартной методике, например,паратолуидина (F) в 4-ацетамидотолуол (G). Синтетическое промежуточное соединение (G) можно превратить в 4-ацетамидобензойную кислоту (D) с помощью известных окислителей(например, КМnО 4) и затем перевести его в соединение CPUI1189, как описано в альтернативной реакции 2. Примеры Изобретение дополнительно описано в следующих Примерах, которые иллюстрируют несколько предпочтительных вариантов осуществления изобретения, не ограничивая при этом его объем, определяемый формулой изобрете 13 ния. Примеры 1-19 иллюстрируют получение ацетамидобензамидов, а также нитро- и аминобензамидов. Они являются представителями бензамидных производных, используемых в композициях и способах настоящего изобретения. Примеры 20-24 иллюстрируют получение фармацевтических композиций, основанных на этих соединениях. В конце приведены результаты биологических испытаний, подтверждающих активность заявленных композиций. Обозначения сигналов в спектрах ЯМР: d - дуплет; s синглет; bs -широкий синглет; Hz - частота (Гц). Пример 1. Получение N-трет-бутил-4 аминобензамида (CPI1160). Трет-бутиламин (14,6 г, 0,200 моль) перемешивают в этилацетате (150 мл, очищен промыванием с помощью 5% раствора карбоната натрия, насыщенным раствором хлорида натрия, высушен над сульфатом магния и отфильтрован через рифленый бумажный фильтр) и охлаждают до 5 С на ледяной бане. К смеси по каплям прибавляют 4-нитробензоилхлорид(18,6 г, 0,100 моль) в очищеном этилацетате (75 мл) с такой скоростью, чтобы поддерживать температуру ниже 10 С. По окончании прикапывания раствора бензоилхлорида ледяную баню удаляют и реакционную смесь перемешивают в течение 4 ч, а затем фильтруют через воронку Бюхнера. Фильтрат трижды промывают 5% НСl, один раз раствором хлорида натрия,сушат над сульфатом магния и фильтруют через рифленый бумажный фильтр. Растворитель отпаривают, получая в остатке кристаллический продукт белого цвета, который сушат в печи под вакуумом при 24 мм и температуре 45 С в течение 14 часов. По описанной методике получают 17,13 г кристаллов N-трет-бутил-4 нитробензамида (CPI1020) с выходом 77% и т.пл. 162-163 С. Спектр протонного магнитного резонанса (ПМР) (89,55 МГц в CDCl3) показал поглощение при 8,257 м.д. (d, 8.8 Hz, 2H; 3,5aryl H); 7.878 м.д.(d, 8.8 Hz, 2H; 2.6-aryl H); 6.097 м.д. (bs, 1H; N-H); 1.500 м.д. (s, 9 Н: tretbutyl H). К соединению CPI1020 (5 г, 22,5 ммоль)в 95% этаноле при 55 С прибавляют катализатор(Pd/C)(5%, 75 мг). По каплям в течение 30 мин добавляют раствор гидразина (1,2 мл) в 95% этанопе (10 мл) дополнительное количество(0,5 г) в 95% этаноле (5 мл) и кипятят с обратным холодильником еще в течение часа. Полученную реакционную смесь фильтруют через воронку Бюхнера, уменьшают объем растворителя путем испарения под вакуумом и экстрагируют дихлорметаном. Объединенный экстракт сушат над сульфатом магния, растворитель отпаривают, получая в остатке 3,90 г N-третбутил-4-аминобензамида (CPI1160) с выходом 90% и т.пл. 125-127 С. Спектр (ПМР) (90 МГц в СDСl3) показал поглощения при 7,290 м.д. (2 Н, 002031H). Пример 2. Получение N-трет-бутил-4 ацетамидобензамида (CPI1189). К соединению CPI1160 (1,0 г, 5,2 ммоль) и триэтиламину (0,58 г, 5,7 ммоль) в этилацетате прибавляют по каплям ацетилхлорид (0,45 г,5,7 ммоль) в этилацетате (25 мл) при температуре 3 С с такой скоростью, чтобы поддерживать температуру в смеси ниже 10 С. Смеси дают нагреться до комнатной температуры, перемешивают в течение часа и промывают 5% раствором НСl. Перекристаллизация из ацетона дает 1,08 г N-трет-бутил-4-ацетамидобензамида(CPI1189) с выходом 89% и т.пл. 119-121 С. Спектр (ПМР) (90 МГц в ДМСО-d6) показал поглощения при 9,726 м.д. (1H, bs, N-H); 7.715 м.д. (4 Н, dd, 4.4 Hz; aryl H); 7.295 м.д. (1H, bs;NH); 2.844 м.д. (3 Н, s; CH3CO); 1.448 м.д. (9 Н,s; t-butyl H). Пример 3. Получение N-трет-бутил-Знитробензамида (CPI1034), N-трет-бутил-Заминобензамида (CPI1248) и N-трет-бутип-3 ацетамидобензамида (CPI1234). Следуют методикам амидирования примера 1, используя 3-нитробензоилхлорид вместо 4 нитробензоилхлорида. Методика дает N-третбутил-3-нитробензамид (CPI1034) с выходом 92% и т.пл. 123-125 С. Спектр (ПМР) (в CDCl3) показал поглощения при 8,517 м.д. (2-aryl H, s,1H): 8.337 м.д.(4-аrуl H, d, 8.8 Hz. 1H); 8.121 м.д.(6-аrуl Н, d, 6.4 Hz, 1H); 7.618 м.д.(5-аrуl Н,m, 1H); 6.032 м.д. (N-H, bs, 1H); 1.484 м.д.(tbutyl H, s, 9H). Восстановление гидразином, катализируемое гидроокисью железа (III) дает N-трет-бутилЗ-аминобензамид (CPI1248) с выходом 53% и т.пл. 118-120 С. Спектр (ПМР) (в СDСl3) показал поглощения при 7,088 м.д. (4-6 -aryl H, m,3 Н); 6.794 м.д.(2-аrуl Н, s, 1H); 5.902 м.д. (N-Н,bs, 1H): 3.145 м.д. (aryl N-H, bs, 2H); 1.458 м.д.(t-butyl H, s, 9 Н). Ацетилирование СРI1248, описанное в примере 2, дает N-трет-бутил-3-ацетамидобензамид (CPI1234) с выходом 75% и т.пл. 194195 С. Спектр (ПМР) (в СDСl3) показал поглощения при 7,778 м.д. (4-6-aryl Н, m, 3 Н); 7.392 м.д. (2-аryl Н, s, 1H); 6.08 м.д. (N-H, bs, 1H); 2.174 м.д.(асеtуl СН 3, s, 9 Н); 1.500 м.д. (t-butylH, s, 9 Н). Пример 4. Получение N-трет-бутил-2 нитробензамида (CPI1035) и N-тpeт-бyтил-2aцeтaмидoбeнзaмидa. Повторяют методику примера 3, используя на стадии амидирования 2-нитробензоилхлорид. Реакция дает N-трет-бутил-2-нитробензамид(CPI1035). Восстановление нитробензамида гидразином дает N-трет-бутил-2-аминобензамид. 15 Ацетилирование аминобензамида дает Nтрет-бутил-2-ацетамидобензамид. Пример 5. Получение N-изопропип-4 нитробензамида (CPI1026) и N-изопропил-4 ацетамидобензамида (CPI1232). Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и изопропиламин. Реакция дает N-изопропил-4 нитробензамид (CPI1026). Восстановление нитробензамида гидразином дает N-изопропил-4-аминобензамид. Ацетилирование аминобензамида дает Nизопропил-4-ацетамидобензамид (CPI1232). Пример 6. Получение N-трет-амил-4 нитробензамида (CPI1033) и N-трет-амил-4 ацетамидобензамида (CPI1233). Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и трет-амиламин. Реакция дает N-трет-амил-4 нитробензамид (CPI1033). Восстановление нитробензамида гидразином дает N-трет-амил-4-аминобензамид. Ацетилирование аминобензамида дает Nтрет-амил-4-ацетамидобензамид (CPI1233). Пример 7. Получение N-изобутил-4 ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и изобутиламин. Реакция дает N-изобутил-4 нитробензамид (CPI1044). Восстановление нитробензамида гидразином дает N-изобутил-4-аминобензамид. Ацетилирование аминобензамида дает Nизобутил-4-ацетамидобензамид. Пример 8. Получение N-н-бутил-4 нитробензамида (CPI1045) и N-н-бутил-4 ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и н-бутиламин. Реакция дает N-н-бутил-4 нитробензамид (CPI1045). Восстановление нитробензамида гидразином дает N-н-бутил-4-аминобензамид. Ацетилирование аминобензамида дает Nн-бутил-4-ацетамидо-бензамид. Пример 9. Получение N-н-пропил-4 нитробензамида (CPI1047) и N-н-пропил-4 ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и н-пропиламин. Реакция дает N-н-пропил-4 нитробензамид (CPI1047). Восстановление нитробензамида гидразином дает N-н-пропип-4-аминобензамид. Ацетилирование аминобензамида дает Nн-пропил-4-ацетамидобензамид. Пример 10. Получение N-1,2-диметилпропил-4-нитробензамида (CPI1085) и N-1,2 диметилпропил-4-ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид 16 и 1,2-диметилпропиламин. Реакция дает N-1,2 диметилпропил-4-нитробензамид (CPI1085). Восстановление нитробензамида гидразином дает N-1,2-диметилпропил-4-аминобензамид. Ацетилирование аминобензамида дает N1,2-диметилпропип-4-ацетамидобензамид. Пример 11. Получение N-н-пентил-4 нитробензамида (CPI1140) и N-н-пeнтил-4aцeтaмидoбeнзaмидa. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и н-пентиламин. Реакция дает N-н-пентил-4 нитробензамид (CPI1140). Восстановление нитробензамида гидразином дает N-н-пентил-4-аминобензамид. Ацетилирование аминобензамида дает Nн-пентил-4-ацетамидобензамид. Пример 12. Получение N-2-метилбутил-4 нитробензамида (CPI1146) и N-2-метилбутил-4 ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 4-нитробензоилхлорид и 2-метилбутиламин. Реакция дает N-2 метилбутил-4-нитробензамид (CPI1146). Восстановление нитробензамида гидразином дает N-2-метилбутил-4-аминобензамид. Ацетилирование аминобензамида дает N2-метилбутил-4-ацетамидобензамид. Пример 13. Получение N-н-пентил-2 нитробензамида (CPI1174) и N-н-пентил-2 ацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 2-нитробензоилхлорид и н-пентиламин. Реакция дает N-н-пентил-2 нитробензамид (CPI1174). Восстановление нитробензамида гидразином дает N-н-пентил-2-аминобензамид. Ацетилирование аминобензамида дает Nн-пентил-2-ацетамидобензамид. Пример 14. Получение N-трет-бутил-2,3 диацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 2,3-динитробензоилхлорид. Реакция дает N-трет-бутил-2,3-динитробензамид. Восстановление нитробензамида гидразином дает N-трет-бутил-2,3-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-бутил-2,3-диацетамидобензамид. Пример 15. Получение N-трет-амил-2,4 диацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 2,4-динитробензоилхлорид и трет-амиламин. Реакция дает N-третамил-2,4-динитробензамид. Восстановление нитробензамида гидразином дает N-трет-амил-2,4-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-амил-2,4-диацетамидобензамид. Пример 16. Получение N-трет-бутил-2,5 диацетамидобензамида. 17 Повторяют методику примера 3, используя на стадии амидирования 2,5-динитробензоилхлорид. Реакция дает N-трет-бутил-2,5-динитробензамид. Восстановление нитробензамида гидразином дает N-трет-бутил-2,5-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-бутил-2,5-диацетамидобензамид. Пример 17. Получение N-трет-бутил-2,6 диацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 2,6-динитробензоилхлорид. Реакция даетN-трет-бутил-2,6 динитробензамид. Восстановление нитробензамида гидразином дает N-трет-бутил-2,6-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-бутил-2,6-ди-ацетамидобензамид. Пример 18. Получение N-трет-бутил-3,4 диацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 3,4-динитробензоилхлорид. Реакция дает N-трет-бутил-3,4-динитробензамид. Восстановление нитробензамида гидразином дает N-трет-бутил-3,4-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-бутил-3,4-диацетамидобензамид. Пример 19. Получение N-трет-бутил-3,5 диацетамидобензамида. Повторяют методику примера 3, используя на стадии амидирования 3,5-динитробензоилхлорид. Реакция дает N-трет-бутил-3,5 динитробензамид. Восстановление нитробензамида гидразином дает N-трет-бутил-3,5-диаминобензамид. Ацетилирование аминобензамида дает Nтрет-бутил-3,5-диацетамидобензамид. Получение фармацевтических композиций. Пример 20. Соединение примера 1 смешивают в виде сухого порошка с сухим желатиновым связующим приблизительно в весовом соотношении 1:2. В качестве смазки добавляют незначительное количество стеарата магния. Смесь прессуют в таблетки весом 240-270 мг(80-90 мг активного бензамида) на специальном прессе. Если эти таблетки назначают больному,страдающему от дегенеративного нарушения,связанного с допамином, один, два или три раза в сутки, то такой курс лечения замедляет течение заболевания. Пример 21. Соединение примера 2 смешивают в виде сухого порошка с крахмалом, применяемым в качестве разбавителя, приблизительно в весовом соотношении 1:1. Полученной смесью заполняют капсулы вместимостью 250 мг (125 мг активного бензамида). Если эти капсулы назначают больному, страдающему от дегенеративного нарушения, связанного с допамином, один, два или три раза в сутки, то такой курс лечения замедляет течение заболевания. 18 Пример 22. Соединение примера 3 суспендируют в подслащенной водной среде до концентрации около 50 мг/мл. Если 5 мл этого жидкого продукта назначают больному, страдающему от дегенеративного нарушения, связанного с допамином, один, два или три раза в сутки, то такой курс лечения замедляет течение заболевания. Пример 23. Соединение примера 4 смешивают в виде сухого порошка с сухим желатиновым связующим приблизительно в весовом соотношении 1:2. В качестве смазки добавляют незначительное количество стеарата магния. Смесь прессуют в таблетки весом 450-900 мг (150-300 мг активного бензамида) на специальном прессе. Если эти таблетки назначают больному, страдающему от дегенеративного нарушения, связанного с допамином, один, два или три раза в сутки,то такой курс лечения замедляет течение заболевания. Пример 24. Соединение примера 14 растворяют в стерильном буферном солевом растворе для инъекций до концентрации около 5 мг/мл. Если 5 мл этого жидкого продукта назначают больному, страдающему от дегенеративного нарушения, связанного с допамином, такого как болезнь Паркинсона, один, два или три раза в сутки, то такой курс лечения замедляет течение заболевания. Следует ожидать, что любое из соединений формулы I можно использовать в любой из описанных лекарственных форм, и что любую из этих композиций можно вводить любым способом таким образом, чтобы можно было лечить любое из указанных в описании дегенеративных состояний. Методики скрининга при заболевании Паркинсона Изучение снижения содержания допамина(МФТГП-модель) Мышей C57BL/6J предварительно обрабатывают либо носителем (1% метилцеллюлоза) либо лекарством (перорально) за 30 мин до введения МФТГП. МФТГП растворяют в изотоническом растворе (0,9%) и вводят подкожно единичную дозу из расчета 15 мг свободного основания на кг веса тела для того, чтобы достигнуть снижения уровня допамина до 0,5 наномолей на мг белка. Группы мышей (в количестве 8-10 в группе) получают либо носитель и изотонический раствор, либо носитель и МФТГП, либо лекарство и МФТГП. Через 72 ч после введения МФТГП мышей умерщвляют путем смещения шейного отдела позвоночника и вырезают неостриатум. Ткань гомогенизируют в 0,4 н. растворе хлорной кислоты, центрифугируют, верхний слой анализируют методом высокоэффективной жидкостной хроматографии с электрохимическим детектором (ВЭЖХ-ЭХД) на содержание допамина. В промежутке между сбо 19 ром и анализом верхние слои после центрифугирования хранят в морозильнике при -90 С. Лекарства соединяют с метилцеллюлозой и гомогенизируют в воде для введения в соответствующих дозах, равных 10-50 мг/кг для соединений CPI1160, CPI1189 и CPI1234, и 50-100 мг/кг для соединения CPI1020. Результаты представительных экспериментов приведены в таблицах 1 и 2. Результаты таблицы 1 показывают, что композиции, заявленные в настоящем изобретении и включающие соединения CPI1160, CPI1189 и CPI1234,эффективны для предупреждения снижения содержания допамина, вызываемого МФТГП. Таблица 1. Эффективность соединений Для сравнения те же опыты проводят на композициях, содержащих соединение CPI1020- родственное производное бензамида, продуктом биопревращения которого являетсяCPI1189. Результаты приведены в таблице 2. При дозе 50 мг/кг CPI1189 осуществляет полную защиту от нейротоксичного влияния МФТГП (105%), тогда как CPI1020 не является столь эффективным (56%). Таблица 2. Сравнение эффективности соединений CPI1189 и Методику повторяют на ряде других соединений, заявленных в настоящем изобретении. Результаты, приведенные в таблице 3, показывают, что и другие бензамиды обнаруживают защитные свойства. Таблица 3. Защитные свойства бензамидов в испытании на истощение допамина в присутствии МФТГП Испытуемое соединение Степень защиты, % 1160 94 1232 70 1233 40 1234 77 1241 40 Испытание на долговременный защитный эффект Дополнительные исследования проводят для того, чтобы определить долговременный 20 защитный эффект со стороны заявленных соединений на процесс истощения допамина. Используя вышеописанную общую методику испытаний, мышей C57BL/6J предварительно обрабатывают либо носителем, либо соединением и МФТГП, а затем умерщвляют через 3 и через 14 суток после введения дозы. Результаты приведены в таблице 4. Таблица 4. Эффективность соединения CPI1189 в испытании на модели в присутствии МФТГП Влияние времени пост-дозирования на стриарные концентрации допамина Процентное соотношение метилЛечение целлюлоза/ изотонический контрольный раствор Метилцеллюлоза/МФТГП 67,5 Результаты эксперимента показывают, что соединение CPI1189 способно осуществлять защиту от снижения уровня допамина, индуцированного МФТГП, у животных, умерщвленных как через 3 суток, так и через 14 суток после введения МФТГП. Это говорит о том, что эффект соединения CPI1189 обусловлен нейрозащитой, а не преходящим действием на метаболизм допамина. Изучение снижения содержания допамина(6-гидроксидопаминовая модель) Испытания проводят для того, чтобы оценить способность CPI1189 осуществлять защиту от повреждений, вызванных 6-гидроксидопамином. Это общепринятая модель для изучения болезни Паркинсона, в которой, как полагают, 6-гидроксидопамин продуцирует токсические эффекты путем вызова оксидативного стресса. Такое соединение, как 6-гидроксидопамин широко используют с 60-х годов в качестве нейротоксиканта. Поскольку он главным образом действует на катехоламинэргические нейроны, его используют в основном для экспериментального изучения болезни Паркинсона. Соединение получило всемирное применение как средство для создания одностороннего (локального) поражения в ниграстриарной системе. Животные, обработанные этим токсином, обнаруживают биохимические и поведенческие изменения, которые можно измерить и фармакологически испытать для того, чтобы оценить силу поражения и определить эффект от возможного терапевтического вмешательства. Определяют защитный отклик от введения дозы соединения CPI1189 на поражение ниграстриарной системы, вызванное 6-гидроксидопамином. Степень поражения измеряют, исходя из стриарных концентраций допамина. Для испытаний используют акклиматизированных 21 самцов крыс Sprague Dawley, возрастом 55-120 дней. 6-Гидроксидопамин фирмы Рисерч Биокемикалз Инк. (Research Biochemicals Incorporated) готовят в 0,9% растворе NaCl, содержащем 0,1 мг/мл аскорбиновой кислоты утром перед опытом. Измельченное соединение CPI1189 (размером частиц меньшим или равным 106 мкм) готовят в 1%-ой суспензии метилцеллюлозы также утром перед опытом и вводят внутрь дозированный объем 0,0005 мл/г, используя калибровочную интубационную иглу размером 3" х 18. Животных анестезируют и хирургически делают интрастриарную (только правостороннюю) инъекцию 6-гидроксидопамина или солевого раствора. Животных умерщвляют через неделю после введения 6-гидроксидопамина. Немедленно после этого препарированную стриарную ткань собирают и анализируют методом ВЭЖХ-ЭХД на содержание белка, используя анализ с бицинхониновой кислотой. Результаты приведены в таблице 5. Таблица 5. Тестируемая (правая) сторона (полушария головного мозга) в процентном выражении от контрольной(левой) стороны, при условии, что инъекцию 6 гидроксидопамина делают только в правый неостриатум Доля от контрольЛечение ной стороны, % Метилцеллюлоза/6-гидроксидопамин 69,677,65 100 мг/кг СРI1189/6-гидроксидопамин 77,6113,5 50 мг/кг CPI1189/6-гидроксидопамин 72,828,32 Результаты экспериментов показывают,что соединение CPI1189 способно осуществлять защиту против снижения уровня допамина, вызванного 6-гидроксидопамином. Испытание на активность против болезни Альцгеймера Действие бензамидов на образование бетаскладчатых листов А-бета(1-40). Определение агрегации амилоидов в растворе методом спектров флуоресценции Тиофлавина Т. Было разработано несколько методик для оценки активности заявленных соединений в качестве средств для лечения болезни Альцгеймера. Одна из таких методик построена на наблюдении, что у таких больных обнаружен необычный уровень агрегации амилоидов. Тиофлавин Т (ThT) связан с бетаскладчатыми листами, в частности с агрегированными фибрилами синтетического А-бета(140), вызывая новый пик возбуждения при 440 нм и усиленную эмиссию при 490 нм. Согласно этому принципу, агенты, которые способны задерживать или обратимо влиять на образование такой ассоциации, могут оказать благоприятное терапевтическое воздействие. Эксперименты проводят на 96 пластинах с лунками и флуоресцентные изменения оценивают с помощью флуоресцентного планшетридера Цитофлуор II (CytoFluor II). В каждую лунку вносят аликвоту в 95 мкл Тиофлавина Т(рН 6,0), 2 мкл NRT (10 мкМ), приготовленного в фосфатном буфере (рН 6,0) в присутствии 0,05% метилцеллюлозы и 3 мкл А-бета(1-40) (3 мкг) в dH2O. Измерение флуоресценции начинают после добавления А-бета(1-40) и продолжают в течение 4 часов, за которые образование бета-складчатых листов достигает своего плато. Степень защиты этого образования в % рассчитывают из разницы, выраженной в единицах относительной флуоресценции, между агрегацией в присутствии и в отсутствие испытуемых соединений. Результаты приведены в таблице 6. Таблица 6. Активность бензамидов в скрининге против заболевания Альцгеймера Соединение Степень защиты, % Защитное действие бензамидов против Амилоида бета-(25-35) или истощения нервных клеток, вызываемых глутаматом в культурах астроцитов или нейронов гиппокампа эмбриона крысы. Проводят еще один тест на активность против болезни Альцгеймера. Иссекают гиппокамп 18-дневного эмбриона крысы SpragueDawley, а затем разлагают его путем истирания с получением первичных нейронных/астроцитарных культур. Клетки (3 х 105) наносят на пластинки размером 35 мм, покрытые поли-Dлизином, содержащие минимальное количество основной питательной среды Игла (Eagle) с добавлением 10% фетальной коровьей сыворотки. Через 3-5 часов первоначальную среду удаляют и заменяют 1 мл свежей питательной среды. Культуры сохраняют при температуре 37 С в увлажненном инкубаторе, содержащем 5% СО 2 и 95% воздуха. Эксперимент на нейронную токсичность,вызванную А-бета(25-35): 30 мкМ А-бета(2535), растворенного в dH2O, добавляют к клеткам(7DIV) в присутствии или в отсутствие 100 мкМ бензамида, приготовленного в 1% метилцеллюлозе, в течение 96 ч. Эксперимент на нейронную токсичность,вызванную глутаматом: 30 мкМ глутамата добавляют к клеткам (9DIV) в присутствии или в отсутствие бензамида в течение 48 ч. Жизнеспособность нейронов выражают в виде процентного соотношения между числом морфологически жизнеспособных нейронов после 48 или 96 ч лечения и числом нейронов до лечения в одних и тех же предварительно маркированных зонах культуры(три зоны/культуру, n=6). Результаты приведены в таблице 7, которая содержит данные, выраженные в виде среднего значения со стандартным отклонением (СКО), в сравнении с результатами контрольного опыта. Таблица 7. Активность бензамида в скрининге против истощения нервных клеток Соединение Степень защиты, % Степень защиты, % А-бета(25-35) Глутамат 1233 23 1234 9 1241 10 1135 16 1140 8 17 1146 50 1173 36 1240 23 1026 8 где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2, при условии, что когда n=1 и R' представляет собой либо н-бутил, либо н-пропил, ацетамидогруппа не находится в положении 2 кольца; когда n=1, ацетамидогруппа не находится в положении 3 кольца; и когда n=2, ацетамидогруппы не находятся в положениях 3 и 5 кольца. 2. Соединение по п.1, выбираемое из группы, состоящей из N-изопропил-4-ацетамидобензамида, N-трет-амил-4-ацетамидобензамида и N-метилциклопропил-4-ацетамидобензамида. 3. Соединение по п.1, представляющее собой N-трет-бутил-4-ацетамидобензамид. 4. Нитро- или аминобензамид формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, каждыйR независимо представляет собой -NO2 или-NH2, и n=1 или 2, выбираемое из группы, состоящей из N-трет-амил-4-нитробензамида, N1,2-диметилпропил-4-нитробензамида, N-н-бутил-3-нитробензамида, N-пeнтил-4-нитpoбeнзaмидa, N-2-метилбутил-4-нитробензамида, N-нбутил-3,5-динитробензамида,N-метилциклопропил-4-нитробензамида, N-н-бyтил-2-нитpoбeнзaмидa, N-н-пентил-2-нитробензамида и Nметилциклопропил-4-аминобензамида. 5. Способ получения ацетоамидобензамида формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2, включающий следующие стадии:(III) до NН 2-групп; и с) ацетилирование NН 2-групп в NНСОСН 3 группы. 6. Способ получения производных бензамида формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2 при следующих условиях: 1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является третбутилом, изобутилом или пропилом; 2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 и R' представляет собой третбутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца, включающий стадию конденсации насыщенного алкиламина, содержащего от 3 до 5 атомов углерода, с нитробензоилгалогенидом формулы 7. Способ получения производных бензамида формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2, включающий следующие стадии: а) конденсацию насыщенного алкиламина,содержащего от 3 до 5 атомов углерода, с нитробензоилгалогенидом формулыb) восстановление NО 2-групп до NH2 групп. 8. Фармацевтическая композиция, включающая производное бензамида формулы I где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, каждыйR независимо представляет собой -NO2, или-NH2, или -NH-CO-СН 3, и n=1 или 2, при следующих условиях: 1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является третбутилом, изобутилом или пропилом; 2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 и R' представляет собой третбутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца,в фармацевтически приемлемом носителе. 9. Фармацевтическая композиция по п.8,где производное бензамида представляет собой ацетамидобензамид формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2. 10. Фармацевтическая композиция по п.9,где n=1 и R' представляет собой трет-бутил или трет-амил. 11. Фармацевтическая композиция по п.10,где производное бензамида представляет собойN-трет-бутил-4-ацетамидобензамид. 12. Фармацевтическая композиция по п.9,где производное бензамида выбирают из группы, состоящей из N-изопропил-4-ацетамидобензамида, N-трет-амил-4-ацетамидобензамид, Nтрет-бутил-3-ацетамидобензамида, N-метилциклопропил-4-ацетамидобензамида. 13. Фармацевтическая композиция по п.8,где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, каждыйR независимо представляет собой -NO2 или 26 1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является третбутилом, изобутилом или пропилом; 2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 и R' представляет собой третбутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца. 14. Фармацевтическая композиция по п.13,где производное бензамида представляет собойN-трет-бутил-4-аминобензамид. 15. Фармацевтическая композиция по п.13,где производное бензамида выбирают из группы, состоящей изN-трет-бутил-3-аминобензамида. 16. Фармацевтическая композиция по п.8,где носитель является носителем для орального приема или носителем для инъекций. 17. Способ лечения пациента, страдающего от нейродегенеративного состояния, включающий введение пациенту эффективного терапевтического количества фармацевтической композиции по пп.8-16. 18. Способ по п.17, где нейродегенеративное состояние связано с постепенной утратой функций центральной нервной системы. 19. Способ по п.18, где нейродегенеративное состояние представляет собой состояние,связанное с допамином. 20. Способ по п.19, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 21. Способ по п.17, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 22. Способ по п.17, где нейродегенеративное состояние связано с постепенной утратой функций центральной нервной системы, обусловленной митохондриальной дисфункцией. 23. Способ по п.17, где указанное введение является пероральным. 24. Способ по п.17, где указанное введение является парентеральным. 25. Способ по п.17, где указанное введение осуществляют путем внутривенного вливания. 26. Применение производного бензамида формулы I где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, каждыйR независимо представляет собой -NO2, или-NH2, или -NН-СО-СН 3 и n=1 или 2 при следующих условиях: 1) когда n=1 и R представляет собой -NO2 в положении 4 кольца, R' не является третбутилом, изобутилом или пропилом; 2) когда n=1 и R представляет собой -NO2 в положении 2 кольца, R' не является изобутилом или пропилом; и 3) когда n=2 и R' представляет собой третбутил и оба R представляют собой -NO2, эти группы R не находятся в положениях 3 и 5 кольца,для лечения нейродегенеративного состояния. 27. Применение по п.26, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 28. Применение по п.26, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 29. Применение ацетобензамида по п.1 для лечения нейродегенеративного состояния. 30. Применение по п.29, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 31. Применение по п.29, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 32. Применение по п.26, где производное бензамида представляет собой N-трет-бутил-4 аминобензамид. 33. Применение по п.32, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 34. Применение по п.32, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 35. Применение по п.29, где ацетобензамид представляет собой N-трет-бутил-4-ацетамидобензамид. 36. Применение по п.35, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 37. Применение по п.35, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 38. Применение производного бензамида формулы I где R', R и n имеют значения, определенные в п.26, в получении композиции для лечения нейродегенеративного состояния. 39. Применение по п.38, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 40. Применение по п.38, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 41. Применение ацетамидобензамида формулы где R' представляет собой насыщенный алкил,содержащий от 3 до 5 атомов углерода, и n=1 или 2 для получения композиции для лечения нейродегенеративного состояния. 42. Применение по п.41, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 43. Применение по п.41, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 44. Применение по п.41, где ацетамидобензамид представляет собой соединение по п.1. 45. Применение по п.44, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 46. Применение по п.44, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 47. Применение N-трет-бутил-4-ацетамидобензамида в получении композиции для лечения нейродегенеративного состояния. 48. Применение по п.47, где нейродегенеративное состояние представляет собой болезнь Паркинсона. 49. Применение по п.47, где нейродегенеративное состояние представляет собой болезнь Альцгеймера. 50. Применение по п.38, где производное бензамида представляет собой N-трет-бутил-4 аминобензамид. 51. Применение по п.50, где нейродегенеративное состояние представляет собой болезнь Паркинсона.
МПК / Метки
МПК: A61P 25/28, A61K 31/166, C07C 237/30
Метки: лечения, бензамиды, нейродегенеративных, заболеваний
Код ссылки
<a href="https://eas.patents.su/15-2031-benzamidy-dlya-lecheniya-nejjrodegenerativnyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Бензамиды для лечения нейродегенеративных заболеваний</a>
Предыдущий патент: Полимерные производные камптотецинов
Следующий патент: Инсектицидные композиции и способы борьбы с вредителями
Случайный патент: Зубчатое нагреваемое устройство для укладки волос и способ его изготовления



















