Дифосфатная соль n-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4′-(трифторметокси)[1,1'-дифенил]-3-карбоксамида и фармацевтическая композиция
Номер патента: 20048
Опубликовано: 29.08.2014
Авторы: Де Ла Крус Марилин, Додд Стефани Кей, Уэйкоул Лиладхар Мурлидхар, Баджва Джоуджиндер Сингх, Ву Раинн
Формула / Реферат
1. Дифосфатная соль N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида.
2. Фармацевтическая композиция, модулирующая активность хэджхог сигнального пути, включающая:
(а) терапевтически эффективное количество соли по п.1 и
(б) по меньшей мере один фармацевтически приемлемый носитель, разбавитель, растворитель или эксципиент.
Текст
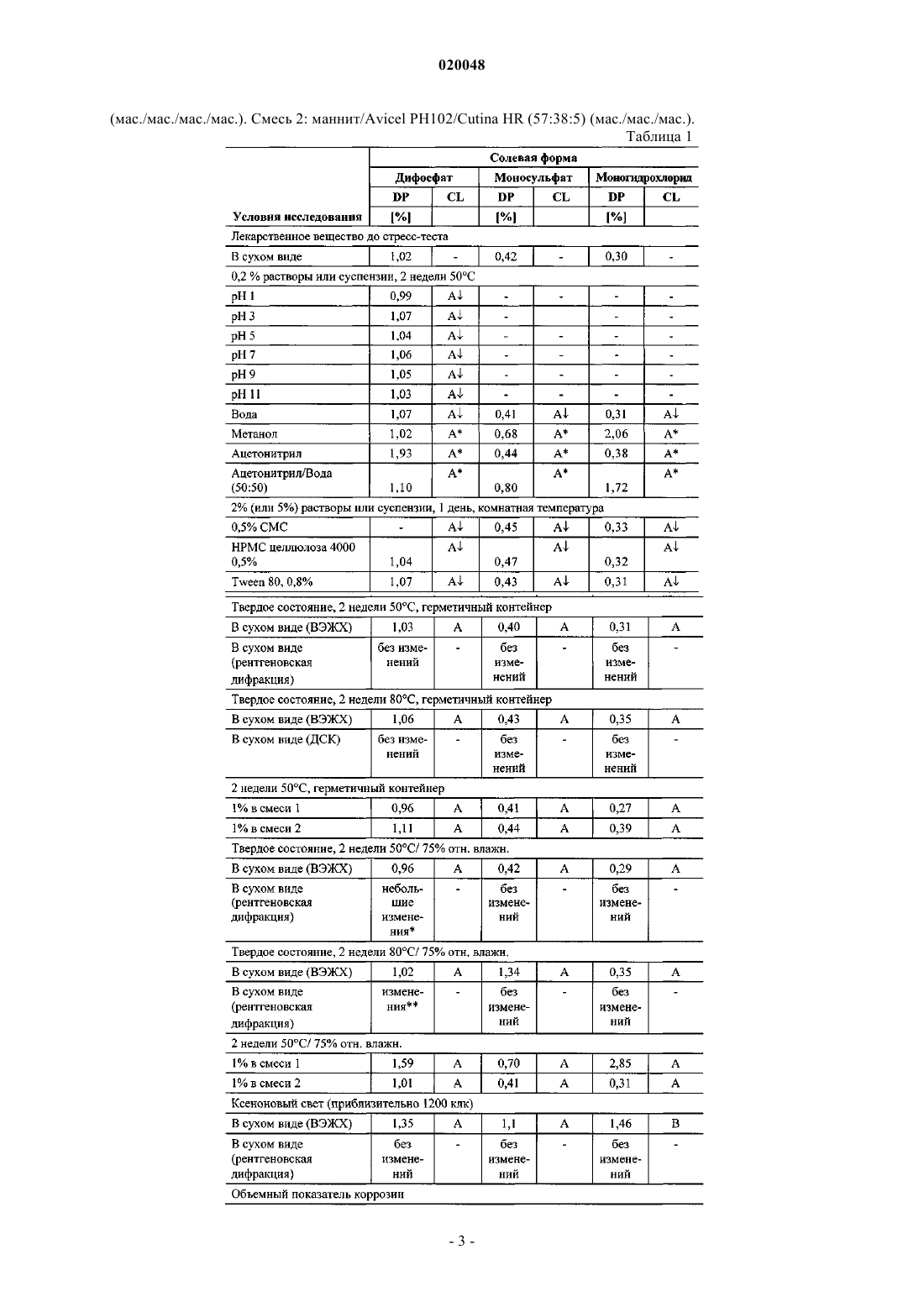
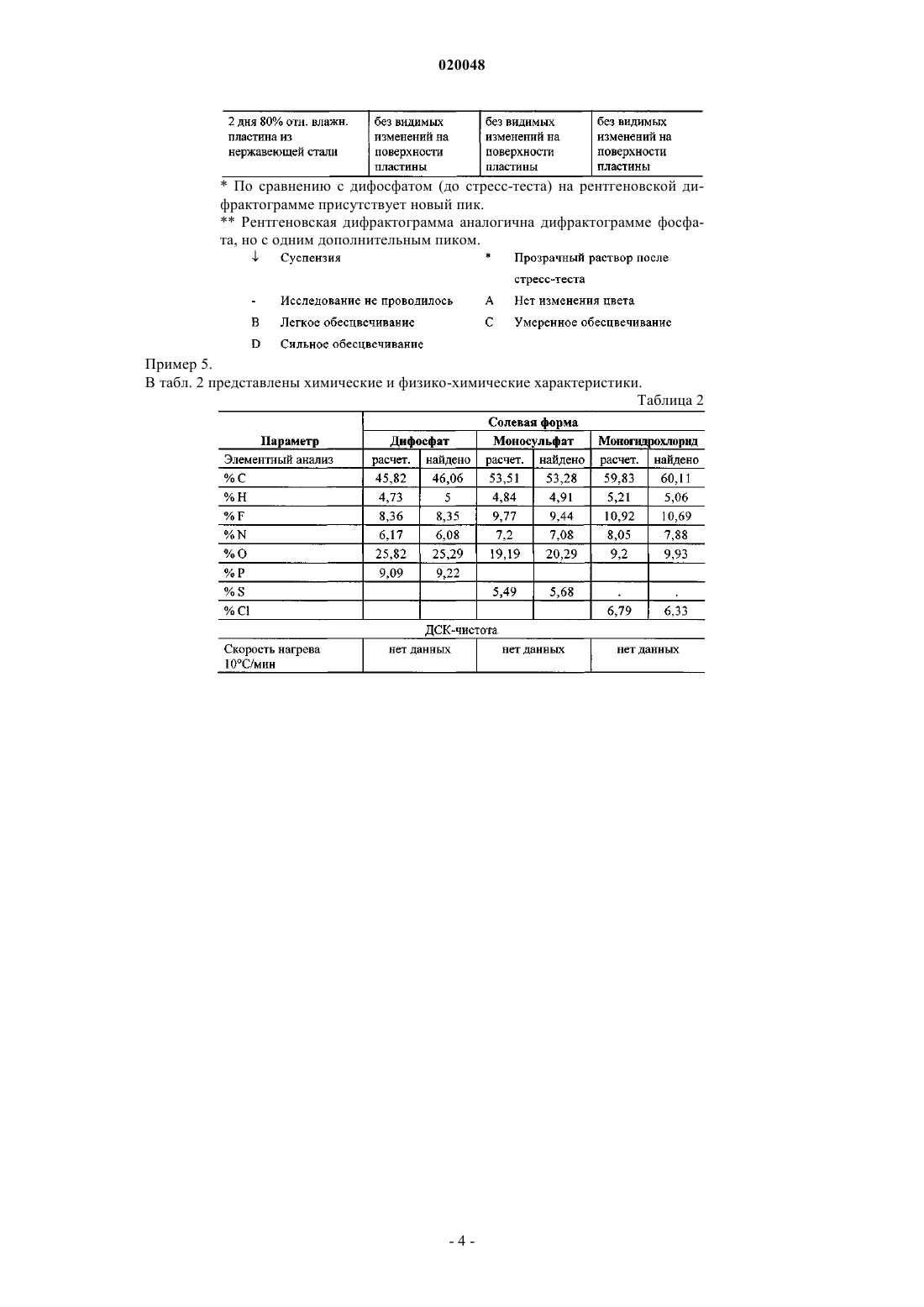
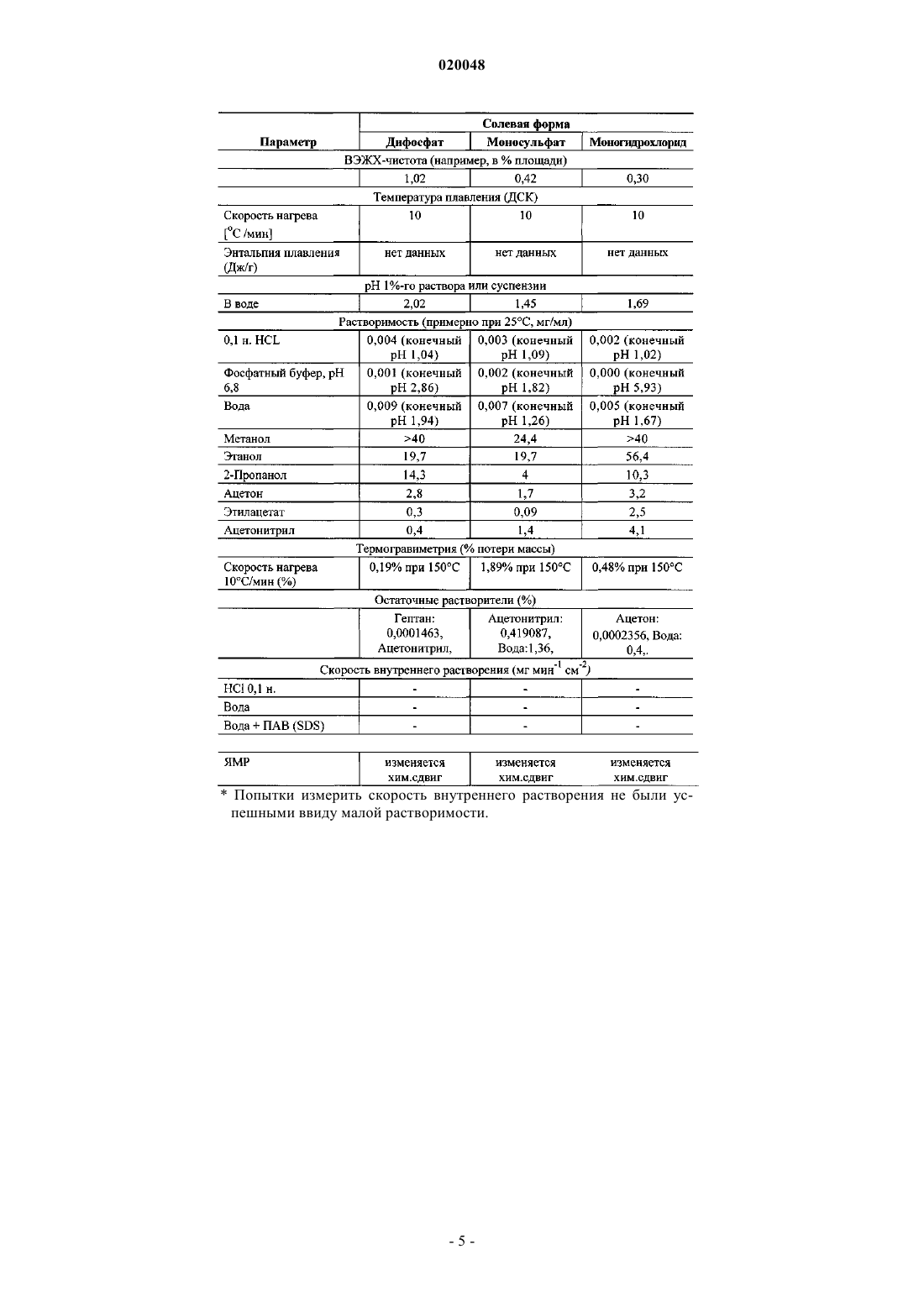
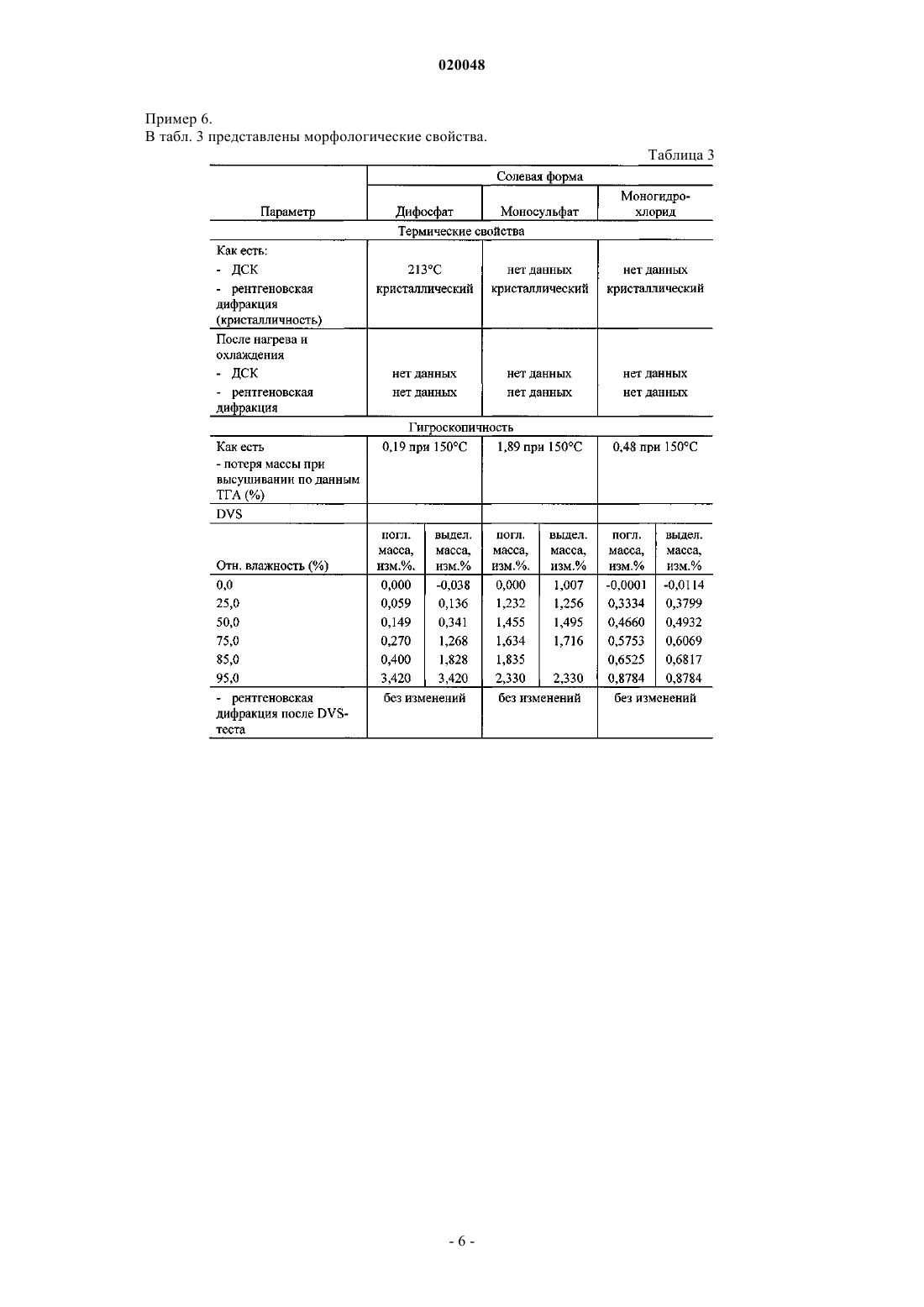
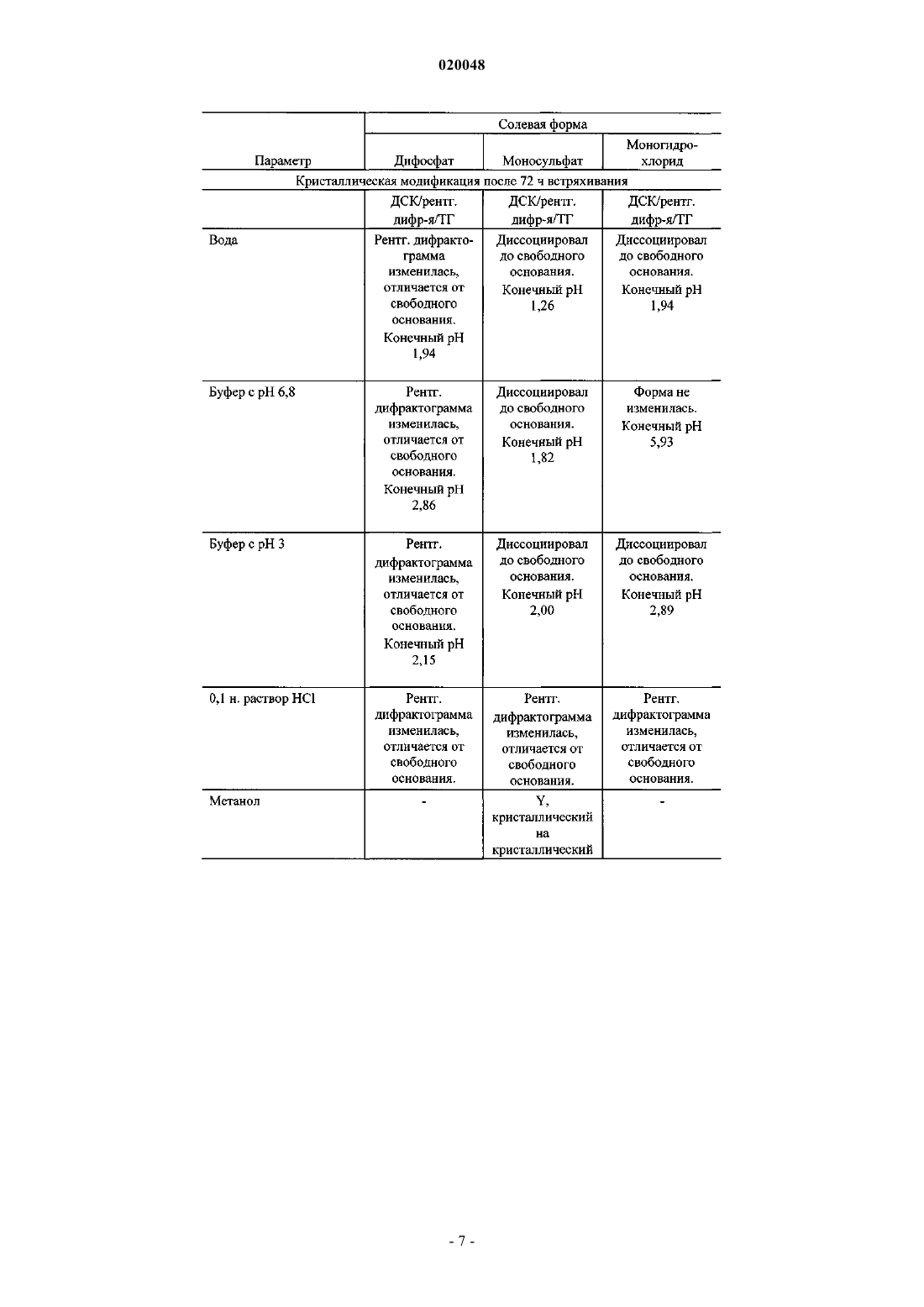
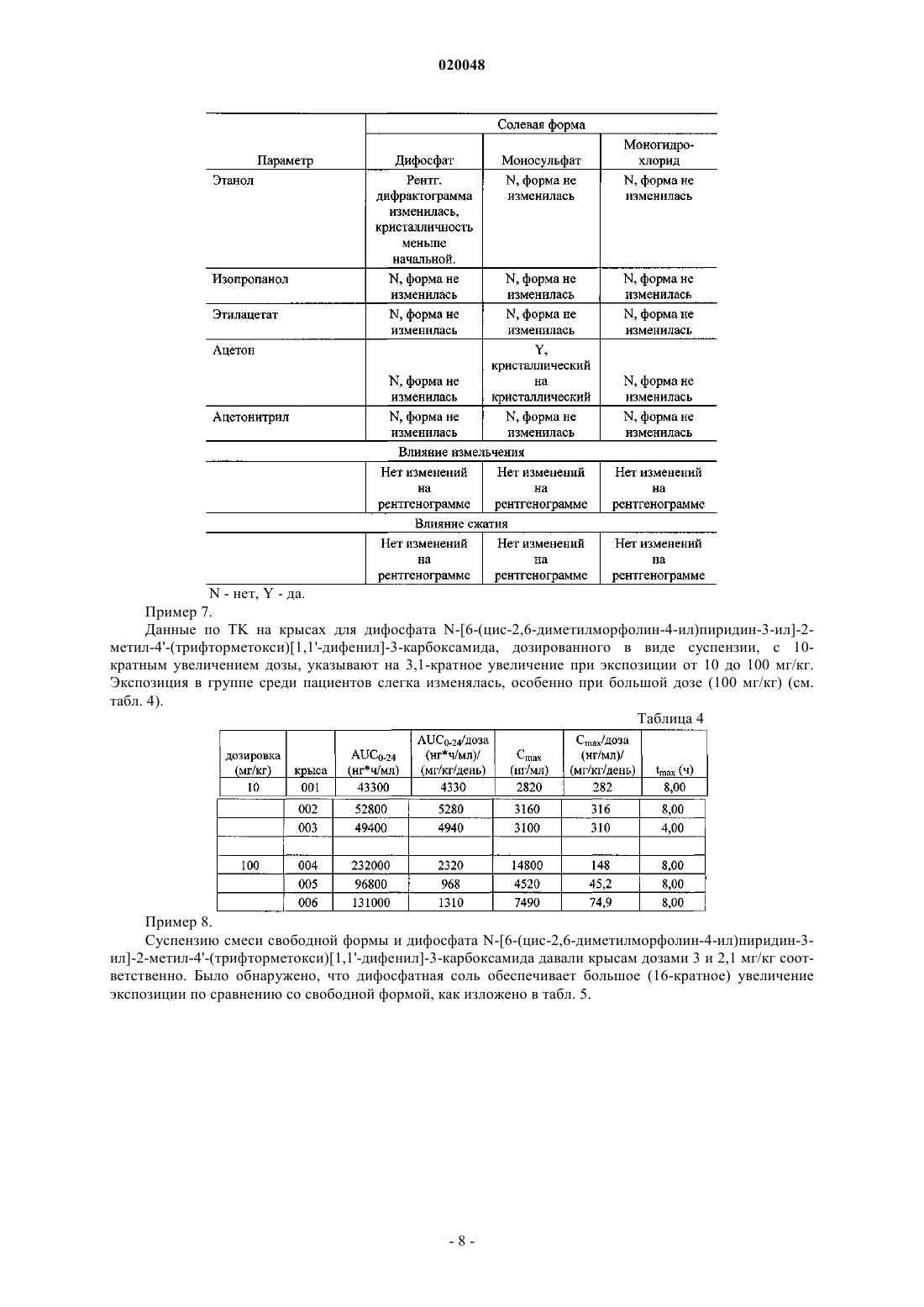
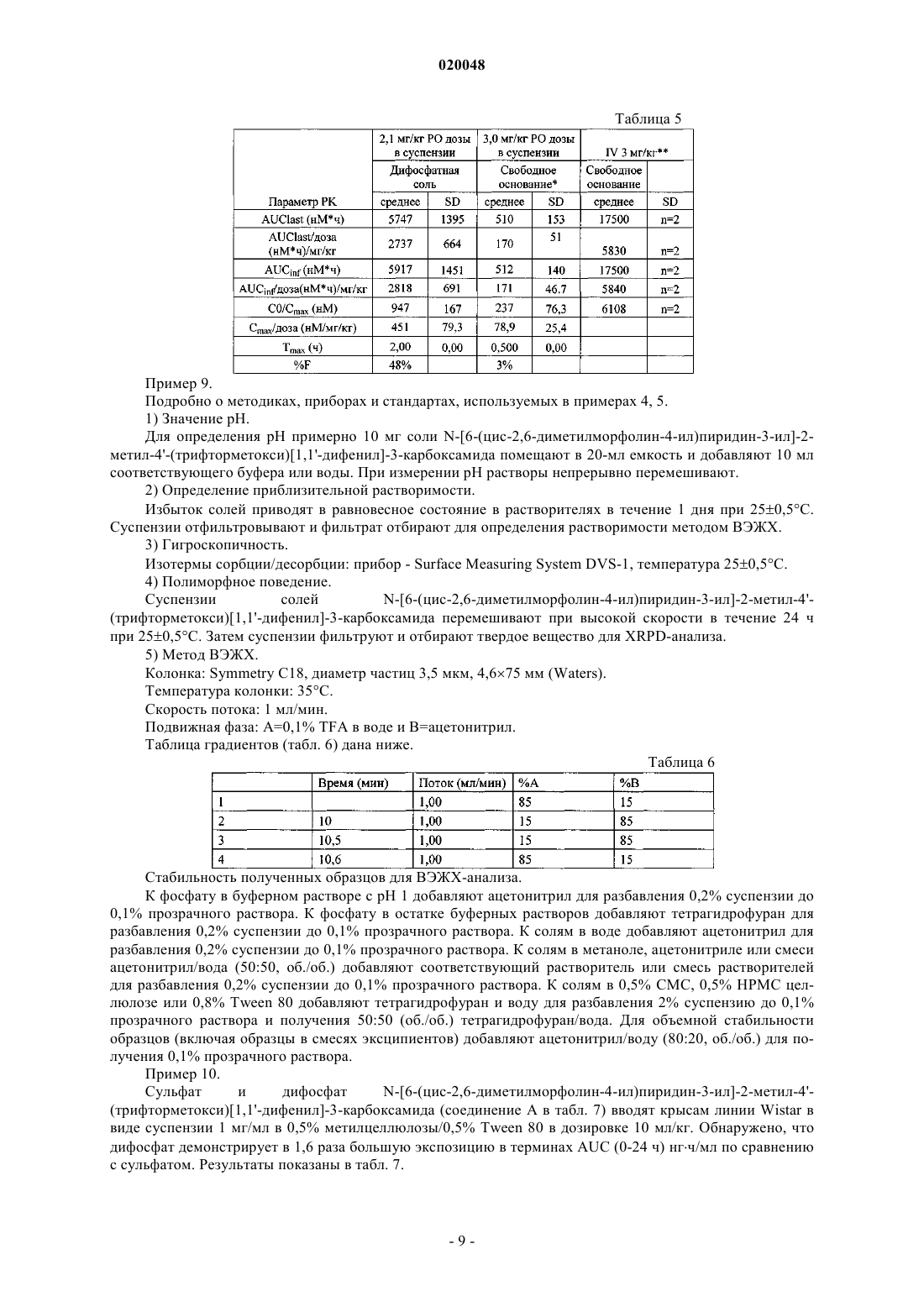
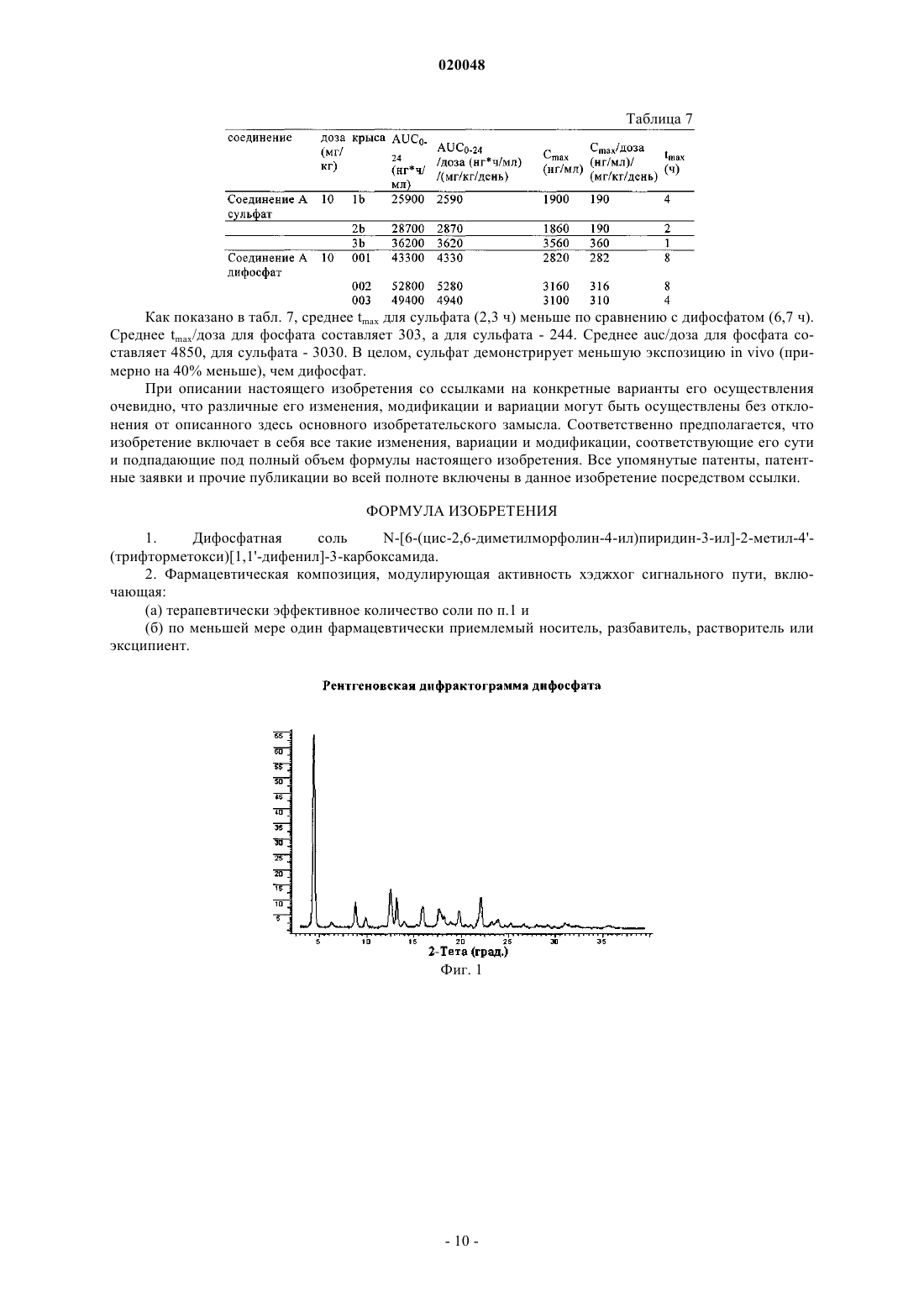
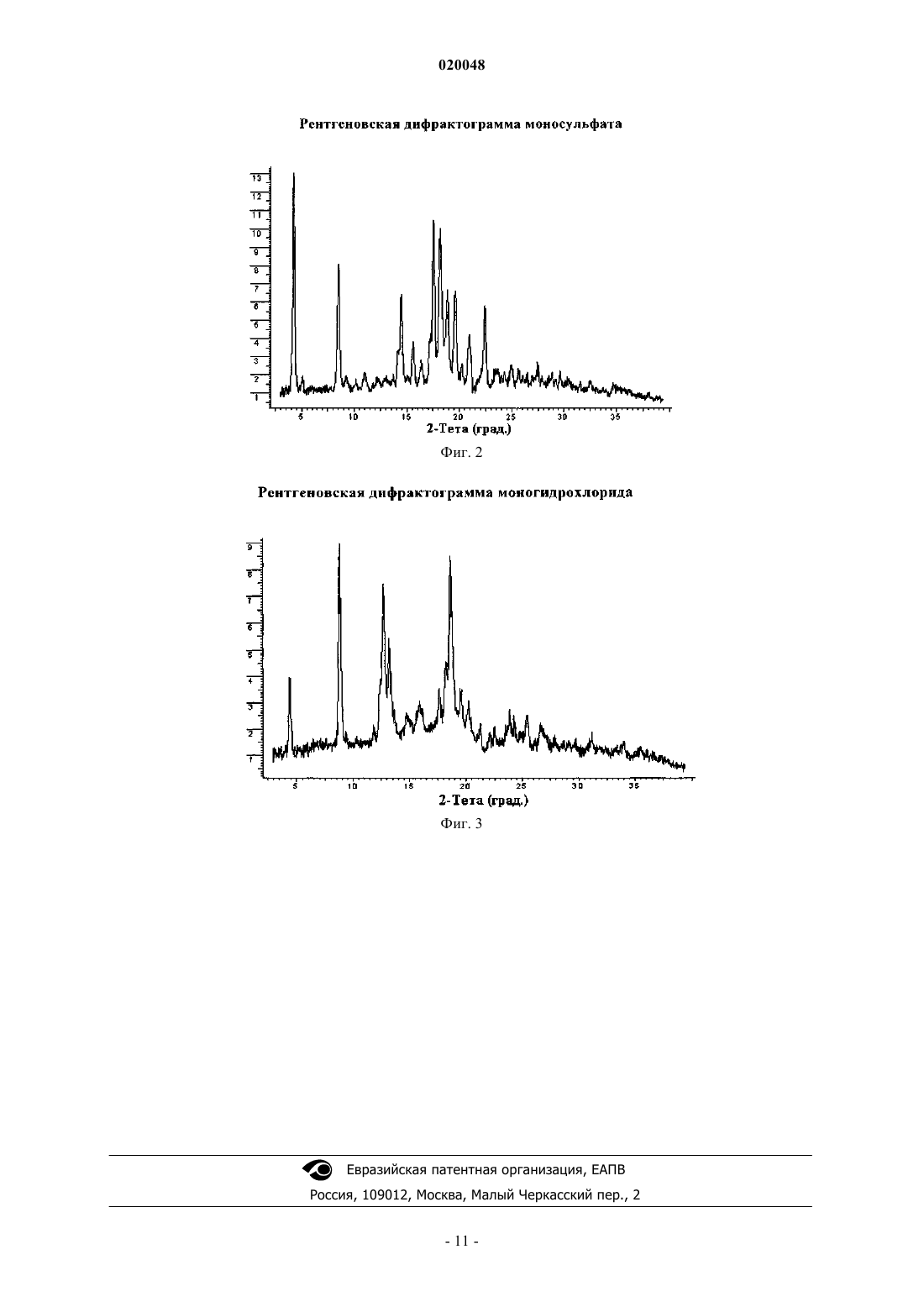
В изобретении описано получение и приведены характеристики дифосфатной соли Баджва Джоуджиндер Сингх, Де Ла Крус Марилин, Додд Стефани Кей,Уэйкоул Лиладхар Мурлидхар, Ву Раинн (US) и фармацевтической композиции,модулирующей активность хэджхог сигнального пути,включающей терапевтически эффективное количество дифосфата[1,1'-дифенил]-3-карбоксамида и по меньшей мере один фармацевтически приемлемый носитель,разбавитель, растворитель или эксципиент. Предпосылки создания изобретения Область изобретения Настоящее изобретение относится к солям, в частности к дифосфатной соли N-[6-(цис-2,6 диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида,а также к фармацевтическим композициям, модулирующим активность хэджхог сигнального пути и содержащим эту соль. Уровень техники Как следует из WO 2007/131201, N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'(трифторметокси)[1,1'-дифенил]-3-карбоксамид имеет формулу (I) Данное соединение обладает ценными фармакологическими свойствами, и поэтому оно может быть использовано, например, в качестве модулятора активности хэджхог сигнального пути, подходящего для терапии заболеваний, обусловленных модулированием активности хэджхог сигнального пути. WO 2007/131201 не раскрывает каких-либо конкретных солей, гидратов солей или сольватов N-[6-(цис-2,6 диметилморфолин-4-ил)-пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. Было обнаружено, что соли настоящего изобретения демонстрируют, в дополнение к хорошим физико-химическим свойствам, высокую проницаемость и высокую биодоступность. Краткое изложение изобретения Настоящее изобретение относится к дифосфату N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3 ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. Кроме того, настоящее изобретение относится к фармацевтическим композициям, содержащим:(а) терапевтически эффективное количество заявленной соли N-[6-(цис-2,6-диметилморфолин-4 ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида и(б) по меньшей мере один фармацевтически приемлемый носитель, разбавитель, растворитель или эксципиент. Настоящее изобретение может быть использовано в способе лечения заболевания, обусловленного модулированием активности хэджхог сигнального пути, включающем стадию введения субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества заявленной соли - дифосфата N[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3 карбоксамида. Краткое описание фигур На фиг. 1 представлена рентгеновская дифрактограмма дифосфата N-[6-(цис-2,6-диметилморфолин 4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. На фиг. 2 представлена рентгеновская дифрактограмма моносульфата N-[6-(цис-2,6 диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. На фиг. 3 представлена рентгеновская дифрактограмма моногидрохлорида N-[6-(цис-2,6 диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. Подробное описание изобретения Как используется в данном патенте, термин "соль" относится к соединению, полученному посредством взаимодействия лекарственного средства на основе органической кислоты или основания с фармацевтически приемлемой органической или неорганической кислотой или основанием; как используется в данном изобретении, термин "соль" включает гидраты и сольваты солей, полученных в соответствии с изобретением. Примеры фармацевтически приемлемых неорганических или органических кислот или оснований перечислены, например, в табл. 1-8 Handbook of Pharmaceutical Salts, Ed. Р.Н. Stahl и C.G.Wermuth, VHCA, Zurich 2002, р. 334-345. В частности, соли включают гидрохлоридные, фосфатные,сульфатные, мезилатные, эзилатные и безилатные формы, но не ограничиваются ими. Как используется в данном изобретении, термин "полиморф" относится к отдельной "кристаллической модификации", или"полиморфной форме", или "кристаллической форме", которые отличаются друг от друга по характеру рентгеновских дифрактограмм, физико-химическим и/или фармакокинетическим свойствам, и термоди-1 020048 намической устойчивости. Один из вариантов осуществления настоящего изобретения относится к дифосфату N-[6-(цис-2,6 диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. Настоящее изобретение может быть использовано для лечения карциномы, включая карциному мочевого пузыря (включая прогрессирующий и метастатический рак мочевого пузыря), груди, толстой кишки (включая колоректальный рак), почек, печени, легких (включая мелкоклеточный и немелкоклеточный рак легких и аденокарциному легких), яичников, простаты, яичек, мочеполового тракта, лимфатической системы, прямой кишки, гортани, поджелудочной железы (включая экзокринную и эндокринную карциному поджелудочной железы), пищевода, желудка, желчного пузыря, шеи, щитовидной железы и кожи (включая плоскоклеточную карциному), опухолей центральной и периферической нервных систем, включая астроцитому, нейробластому, глиому, бластому костного мозга и невриному; опухолей мезенхимального происхождения, включая фибросаркому, рабдомиосаркому и остеосаркому, и других опухолей, включая меланому, карциному из клеток Меркеля, пигментную ксеродерму, кератоакантому,семиному, фолликулярный рак щитовидной железы и тератокарциному. Настоящее изобретение может также быть использовано для лечения мастоцитоза, опухолей эмбриональных клеток, детских сарком и прочих видов рака. Настоящее изобретение также пригодно для ингибирования роста и пролиферации гематобластозов лимфоидного происхождения, таких как лейкемия, включая острый лимфоцитарный лейкоз (ALL), острый лимфобластный лейкоз, В-клеточную лимфому, Т-клеточную лимфому, лимфому Ходжкина, неходжкинскую лимфому, волосато-клеточную лимфому, гистиоцитную лимфому и лимфому Беркитта; и гематобластозов миелоидного происхождения, включая острый и хронический миелолейкоз (CML), миелодиспластический синдром, миелоидную лейкемию и промиелоцитарный лейкоз. Пример 1. Получение дифосфатной соли. В 250-мл трехгорлую колбу в атмосфере азота помещают 7,0 г (0,0144 моль) свободного основания[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 2-метил-4'-трифторметоксидифенил-3 карбоновой кислоты и 178,5 мл ацетонитрила хроматографической чистоты. Суспензию нагревают до 58 С в атмосфере азота в течение 20 мин с получением прозрачного раствора. Затем к реакционному раствору в течение 18 мин добавляют 3,405 г 85% фосфорной кислоты в воде (2 экв.). В течение 5 мин при добавлении фосфорной кислоты осаждается дифосфат N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3 ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида. Белую суспензию перемешивают и охлаждают до комнатной температуры в течение 100 мин. После этого суспензию охлаждают до 05 С в течение 5 мин и перемешивают 1 ч. Затем смесь фильтруют на воронке Бюхнера и полученное твердое вещество промывают ацетонитрилом (39,4 мл). Лекарственное вещество сушат в вакууме при 50 С в течение 16 ч с получением 9,63 г фосфатной соли (выход: 98%). Пример 2. Получение моносульфатной соли. В 100-мл трехгорлую колбу в атмосфере азота помещают 3,0 г (6,18 ммоль) свободного основанияN-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3 карбоксамида и 35 мл ацетонитрила хроматографической чистоты. Суспензию нагревают до 50 С в атмосфере азота в течение 30 мин с получением прозрачного раствора. Затем к смеси в течение 10 мин добавляют 1,5 мл 6 М серной кислоты (1,5 экв). После этого смесь перемешивают при 50 С в течение 3 ч и охлаждают до 25 С в течение 25 мин. В течение 5 мин осаждается твердое вещество. Суспензию перемешивают 16 ч при 25 С. После этого смесь фильтруют на воронке Бюхнера и твердый осадок промывают 10 мл ацетонитрила. Лекарственное вещество сушат в вакууме при 55 С в течение 16 ч с получением 3,0 г сульфатной соли (выход: 83%). Пример 3. Получение моногидрохлоридной соли. В 100-мл трехгорлую колбу в атмосфере азота помещают 3,0 г (6,18 ммоль) свободного основанияN-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3 карбоксамида и 25 мл ацетона хроматографической чистоты. Суспензию перемешивают 25 мин при 25 С в атмосфере азота с получением прозрачного раствора. Затем к смеси в течение 10 мин добавляют 1,5 мл 6 M соляной кислоты (1,5 экв). В течение 5 мин осаждается твердое вещество. Суспензию перемешивают 16 ч при 25 С. После этого смесь фильтруют на воронке Бюхнера и твердое вещество промывают 10 мл ацетона. Лекарственное вещество сушат в вакууме при 55 С в течение 16 ч с получением 3,0 г гидрохлоридной соли (выход: 93%). Пример 4. В табл. 1 приведены показатели стабильности, измеренные по распаду продуктов (или анализу) и появлению цвета. Распад продуктов (DP) анализировали методом ВЭЖХ (см. табл. 3). Он рассчитывался как площадь-% продуктов. Композиции смесей (в мас.%) следующие. Смесь 1: лактоза 200 меш/модифицированный кукурузный крахмал 1500 LM/аэросил 200/стеарат магния 78,5:20:0,5:1 По сравнению с дифосфатом (до стресс-теста) на рентгеновской дифрактограмме присутствует новый пик.Рентгеновская дифрактограмма аналогична дифрактограмме фосфата, но с одним дополнительным пиком. Попытки измерить скорость внутреннего растворения не были успешными ввиду малой растворимости.N - нет, Y - да. Пример 7. Данные по TK на крысах для дифосфата N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2 метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида, дозированного в виде суспензии, с 10 кратным увеличением дозы, указывают на 3,1-кратное увеличение при экспозиции от 10 до 100 мг/кг. Экспозиция в группе среди пациентов слегка изменялась, особенно при большой дозе (100 мг/кг) (см. табл. 4). Таблица 4 Пример 8. Суспензию смеси свободной формы и дифосфата N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3 ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида давали крысам дозами 3 и 2,1 мг/кг соответственно. Было обнаружено, что дифосфатная соль обеспечивает большое (16-кратное) увеличение экспозиции по сравнению со свободной формой, как изложено в табл. 5. Пример 9. Подробно о методиках, приборах и стандартах, используемых в примерах 4, 5. 1) Значение рН. Для определения рН примерно 10 мг соли N-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2 метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида помещают в 20-мл емкость и добавляют 10 мл соответствующего буфера или воды. При измерении рН растворы непрерывно перемешивают. 2) Определение приблизительной растворимости. Избыток солей приводят в равновесное состояние в растворителях в течение 1 дня при 250,5 С. Суспензии отфильтровывают и фильтрат отбирают для определения растворимости методом ВЭЖХ. 3) Гигроскопичность. Изотермы сорбции/десорбции: прибор - Surface Measuring System DVS-1, температура 250,5C. 4) Полиморфное поведение. Суспензии солейN-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'(трифторметокси)[1,1'-дифенил]-3-карбоксамида перемешивают при высокой скорости в течение 24 ч при 250,5 С. Затем суспензии фильтруют и отбирают твердое вещество для XRPD-анализа. 5) Метод ВЭЖХ. Колонка: Symmetry C18, диаметр частиц 3,5 мкм, 4,675 мм (Waters). Температура колонки: 35 С. Скорость потока: 1 мл/мин. Подвижная фаза: А=0,1% TFA в воде и В=ацетонитрил. Таблица градиентов (табл. 6) дана ниже. Таблица 6 Стабильность полученных образцов для ВЭЖХ-анализа. К фосфату в буферном растворе с рН 1 добавляют ацетонитрил для разбавления 0,2% суспензии до 0,1% прозрачного раствора. К фосфату в остатке буферных растворов добавляют тетрагидрофуран для разбавления 0,2% суспензии до 0,1% прозрачного раствора. К солям в воде добавляют ацетонитрил для разбавления 0,2% суспензии до 0,1% прозрачного раствора. К солям в метаноле, ацетонитриле или смеси ацетонитрил/вода (50:50, об./об.) добавляют соответствующий растворитель или смесь растворителей для разбавления 0,2% суспензии до 0,1% прозрачного раствора. К солям в 0,5% CMC, 0,5% НРМС целлюлозе или 0,8% Tween 80 добавляют тетрагидрофуран и воду для разбавления 2% суспензию до 0,1% прозрачного раствора и получения 50:50 (об./об.) тетрагидрофуран/вода. Для объемной стабильности образцов (включая образцы в смесях эксципиентов) добавляют ацетонитрил/воду (80:20, об./об.) для получения 0,1% прозрачного раствора. Пример 10. Сульфат и дифосфатN-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'(трифторметокси)[1,1'-дифенил]-3-карбоксамида (соединение А в табл. 7) вводят крысам линии Wistar в виде суспензии 1 мг/мл в 0,5% метилцеллюлозы/0,5% Tween 80 в дозировке 10 мл/кг. Обнаружено, что дифосфат демонстрирует в 1,6 раза большую экспозицию в терминах AUC (0-24 ч) нгч/мл по сравнению с сульфатом. Результаты показаны в табл. 7. Как показано в табл. 7, среднее tmax для сульфата (2,3 ч) меньше по сравнению с дифосфатом (6,7 ч). Среднее tmax/доза для фосфата составляет 303, а для сульфата - 244. Среднее auc/доза для фосфата составляет 4850, для сульфата - 3030. В целом, сульфат демонстрирует меньшую экспозицию in vivo (примерно на 40% меньше), чем дифосфат. При описании настоящего изобретения со ссылками на конкретные варианты его осуществления очевидно, что различные его изменения, модификации и вариации могут быть осуществлены без отклонения от описанного здесь основного изобретательского замысла. Соответственно предполагается, что изобретение включает в себя все такие изменения, вариации и модификации, соответствующие его сути и подпадающие под полный объем формулы настоящего изобретения. Все упомянутые патенты, патентные заявки и прочие публикации во всей полноте включены в данное изобретение посредством ссылки. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Дифосфатная сольN-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'(трифторметокси)[1,1'-дифенил]-3-карбоксамида. 2. Фармацевтическая композиция, модулирующая активность хэджхог сигнального пути, включающая:(а) терапевтически эффективное количество соли по п.1 и(б) по меньшей мере один фармацевтически приемлемый носитель, разбавитель, растворитель или эксципиент.
МПК / Метки
МПК: A61K 31/5377, A61K 35/00, C07D 413/04
Метки: дифосфатная, композиция, n-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4'-(трифторметокси)[1,1'-дифенил]-3-карбоксамида, фармацевтическая, соль
Код ссылки
<a href="https://eas.patents.su/12-20048-difosfatnaya-sol-n-6-cis-26-dimetilmorfolin-4-ilpiridin-3-il-2-metil-4-triftormetoksi11-difenil-3-karboksamida-i-farmacevticheskaya-kompoziciya.html" rel="bookmark" title="База патентов Евразийского Союза">Дифосфатная соль n-[6-(цис-2,6-диметилморфолин-4-ил)пиридин-3-ил]-2-метил-4′-(трифторметокси)[1,1'-дифенил]-3-карбоксамида и фармацевтическая композиция</a>
Предыдущий патент: Ветроэнергетическая установка
Следующий патент: Датчик давления
Случайный патент: Комбинированная терапия для лечения рака