Производные 1-[алкил], 1-[(гетероарил)алкил] и 1-[(арил)алкил]-7-пиридинил-имидазо[1, 2-a]пиримидин-5(1н)она
Номер патента: 4933
Опубликовано: 28.10.2004
Авторы: Маргери Северен, Саади Мурад, Йеш Филипп, Локхид Алистер
Формула / Реферат
1. Производное имидазо[1,2-a]пиримидона, представленное формулой (I), или его соль, или их сольват, либо их гидрат
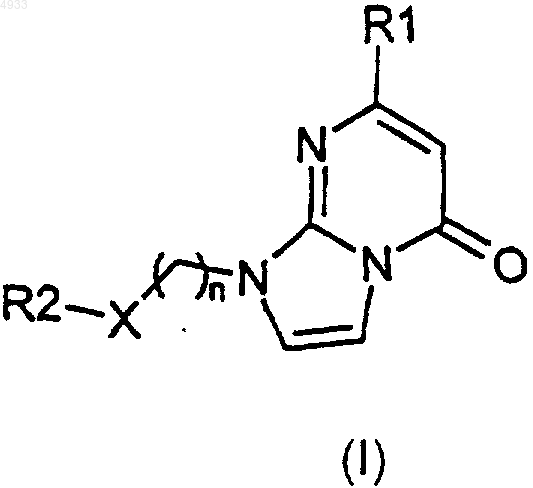
где X представляет собой связь, этениленовую группу, этиниленовую группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6алкильной группы, гидроксигруппы и C1-4алкоксигруппы; карбонильную группу, атом кислорода, атом серы, сульфонильную группу, сульфинильную группу или атом азота, возможно замещенный C1-6алкильной группой;
R1 является 2-, 3- или 4-пиридильной группой, возможно замещенной C1-4алкильной группой, C1-4алкоксигруппой или атомом галогена;
R2 представляет собой C1-6алкильную группу, C1-2пергалогенированную алкильную группу, C1-3галогенированную алкильную группу, бензильную группу, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо, пиридильное кольцо, индольное кольцо, пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо, причем данная бензильная группа и данные кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из C1-6алкильной группы, фенильного кольца, атома галогена, C1-2пергалогенированной алкильной группы, C1-3галогенированной алкильной группы, гидроксильной группы, C1-4алкоксигруппы, нитро, циано, амино, C1-6моноалкиламиногруппы или C2-10диалкиламиногруппы; и
n равняется числу от 0 до 3.
2. Производное имидазо[1,2-a]пиримидона, или его соль, или их сольват, либо их гидрат по п.1, где R1 представляет собой незамещенную 4-пиридильную группу или 3-пиридильную группу.
3. Производное имидазо[1,2-a]пиримидона, или его соль, или их сольват, либо их гидрат по п.1 или 2, где R2 представляет собой трифторметильную группу, 2,2,2-трифторэтил, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо или индольное кольцо, причем данные кольца возможно замещены.
4. Производное имидазо[1,2-a]пиримидона, которое выбрано из группы, состоящей из
1) 1-[2-(фенил)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
2) 1-[2-(1H-индол-3-ил)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
3) 1-[3-(фенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
4) 1-[3-(1H-индол-3-ил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
5) 1-[3-(4-метоксифенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
6) 1-[2-(фенокси)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
7) 1-[3-(2-метоксифенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
8) 1-[3-(2-хлорфенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
9) 1-[3-(2-метилфенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
10) 1-[2-(фенилтио)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
11) 1-[3-(2,5-диметоксифенил)пропил]-7-пиридин-4-илимидазо[1,2-a]-пиримидин-5(1H)-она,
12) 1-[3-(4-метилфенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
13) 1-[3-(4-трифторметилфенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
14) 1-[4-(фенил)бутил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
15) 1-[3-(фенил)пропил]-7-пиридин-3-илимидазо[1,2-a]пиримидин-5(1H)-она,
16) 1-(2-фенил-2-оксоэтил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
17) (S)-1-(4,4,4-трифтор-3-гидроксибутил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
18) 1-(4,4,4-трифторбут-2-енил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
19) (R)-1-(4,4,4-трифтор-3-гидроксибутил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
20) 1-(4,4,4-трифторбут-1-енил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
21) 1-[2-(2,5-диметоксифенил)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
22) 1-[3-(2-фторфенил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
23) 1-(3-фенил-3-оксопропил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
24) 1-[3-(пиридин-3-ил)пропил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
25) (S)-1-(4,4,4-трифторбутил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
26) 1-[2-(2-метоксифенил)этил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
27) 1-[2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафт-2-ил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
28) 1-[2-(4-фенилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
29) 1-[2-(3-метоксифенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
30) 1-[2-(2-нафтил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
31) 1-[2-(4-метилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
32) 1-[2-(4-фторфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
33) 1-[2-(4-хлорфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она.
34) 1-(2-(4-фторфенил)-2-гидроксиэтил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
35) 1-(2-нафтил-2-гидроксиэтил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она;
36) 1-(2-(1,1,4,4-тетраметил-1,2,3,4-тетрагидронафт-6-ил)-2-гидроксиэтил)-7-пиридин-4-илимидазо[1,2-a]пиримидин-5(1H)-она,
или его соль, или их сольват, либо их гидрат.
5. Лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного имидазо[1,2-a]пиримидона, представленного формулой (I), или его солей, или их сольвата, либо их гидрата по п.1.
6. Ингибитор GSK3b, выбранный из группы производного имидазо[1,2-a]пиримидона, представленного формулой (I), или его солей, или их сольвата, либо их гидрата по п.1.
7. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения заболевания, вызываемого анормальной активностью GSK3b.
8. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративного заболевания.
9. Применение соединения по п.8, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, тауопатий, сосудистой деменции, острого инсульта, травматических повреждений, инсультов, травмы головного мозга, травмы спинного мозга, периферических невропатий, ретинопатий или глаукомы.
10. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения инсулиннезависимого сахарного диабета; ожирения; маниакально-депрессивного расстройства; шизофрении; алопеции или рака.
11. Применение по п.10, где рак представляет собой рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, T- или B-клеточный лейкоз либо индуцированные вирусом опухоли.
Текст
1 Область техники Настоящее изобретение относится к соединениям, которые полезны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызываемых анормальной активностью GSK3. Предшествующий уровень техникиGSK3 (киназа-3 гликогенсинтазы) является пролин-направленной серин-треонинкиназой, которая играет важную роль в контроле метаболизма, дифференцировки и выживания. Первоначально была идентифицирована как фермент, способный фосфорилировать и поэтому ингибировать гликогенсинтазу. Позже было установлено, что GSK3 идентична таупротеинкиназе 1 (ТРК 1), ферменту, который фосфорилирует тау-белок в эпитопах, для которых также обнаружено, что они гиперфосфорилированы при болезни Альцгеймера и при некоторых тауопатиях. Интересно, что фосфорилирование GSK3 под действием протеинкиназы В (АКТ) вызывает потерю ею киназной активности, и была высказана гипотеза, что это ингибирование может опосредовать некоторые из эффектов нейротрофических факторов. Более того, фосфорилирование под действием GSK3 -катенина, белка,вовлеченного в клеточное выживание, приводит к его деградации по убиквитинзависимому протеасомному пути. Таким образом понятно, что ингибирование активности GSK3 может приводить к нейротрофической активности. В самом деле, существует доказательство того, что литий, неконкурентный ингибитор GSK3, усиливает невритогенез в некоторых моделях и, кроме того, увеличивает нейронную выживаемость через индукцию факторов выживаемости, таких какBcl-2, и ингибирование экспрессии проапоптотических факторов, таких как Р 53 и Вах. Недавними исследованиями продемонстрировано, что -амилоид увеличивает активность GSK3 и фосфорилирование тау-белка. Более того, это гиперфосфорилирование, равно как и нейротоксические эффекты -амилоида,блокируются хлоридом лития и GSK3 антисмысловой мРНК. Эти результаты научных наблюдений строго доказывают, что GSK3 может быть связующим звеном между двумя главными патологическими процессами при болезни Альцгеймера: анормальным процессингом АРР(белка-предшественника амилоида) и гиперфосфорилированием тау-белка. Несмотря на то, что тау-гиперфосфорилирование приводит к дестабилизации нейронного цитоскелета, патологические последствия анормальной активности GSK3 вероятнее всего проявляются не только вследствие патологического фосфорилирования тау-белка, поскольку,как упомянуто выше, чрезмерная активность 2 этой киназы может оказывать влияние на выживаемость посредством регуляции экспрессии апоптотических и антиапоптотических факторов. Более того, было показано, что индуцированное -амилоидом увеличение активностиGSK3 приводит к фосфорилированию и поэтому ингибированию пируват-дегидрогеназы,главнейшего фермента в продукции энергии и в синтезе ацетилхолина. Совокупность этих экспериментальных данных указывает на то, что GSK3 может найти применение при лечении невропатологических последствий и нарушений познавательной способности и дефицита внимания, связанных с болезнью Альцгеймера, равно как и других острых и хронических нейродегенеративных заболеваний. Таковые включают в себя болезнь Паркинсона, тауопатии (например, лобно-височно-теменную деменцию, кортикобазальную дегенерацию, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции,включая сосудистую деменцию; острый инсульт и другие травматические повреждения; инсульты (например, возрастную дегенерацию желтого пятна); травму головного и спинного мозга; периферические невропатии; ретинопатии и глаукому, но не ограничиваются ими. В дополнение к этому, GSK3 может найти применение при лечении других заболеваний, таких как инсулиннезависимый сахарный диабет (как, например, диабет II типа) и ожирение; маниакально-депрессивное расстройство; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточный рак легкого,рак щитовидной железы, Т- или В-клеточный лейкоз и некоторые индуцированные вирусом опухоли. Описание изобретения Задачей настоящего изобретения является получение соединений, полезных в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения заболевания, вызываемого анормальной активностью GSK3, в особенности нейродегенеративных заболеваний. Более конкретно задачей является получение новых соединений, полезных в качестве активного ингредиента лекарства,которое делает возможным профилактику и/или лечение нейродегенеративных заболеваний,таких как болезнь Альцгеймера. Таким образом,авторами настоящего изобретения предложены соединения, обладающие ингибиторной активностью против GSK3. В результате, авторами обнаружено, что соединения, представленные следующей далее формулой (I), обладают желаемой активностью и полезны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения вышеупомянутых заболеваний. Таким образом, согласно настоящему изобретению предложены производные имида 3 зо[1,2-а]пиримидона, представленные формулой(I), или их соли, их сольваты либо их гидраты. где Х представляет собой связь, этениленовую группу, этиниленовую группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, гидроксигруппы и С 1-4 алкоксигруппы; карбонильную группу, атом кислорода, атом серы, сульфонильную группу, сульфинильную группу или атом азота, возможно замещенныйR1 является 2-, 3- или 4-пиридильной группой, возможно замещенной С 1-4 алкильной группой, С 1-4 алкоксигруппой или атомом галогена;R2 представляет собой C1-6 алкильную группу, С 1-2 пергалогенированную алкильную группу, C1-3 галогенированную алкильную группу,бензильную группу, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо, пиридильное кольцо, индольное кольцо,пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо, причем данная бензильная группа и данные кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из С 1-6 алкильной группы,фенильного кольца, атома галогена, С 1-2 пергалогенированной алкильной группы, С 1-3 галогенированной алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, нитро, циано, амино, С 1-6 моноалкиламиногруппы или С 2-10 диалкиламиногруппы; иn равняется числу от 0 до 3. Согласно другому аспекту настоящего изобретения предложено лекарство, содержащее в качестве активного ингредиента вещество,выбранное из группы, состоящей из производных пиримидона, представленных формулой (I),и их физиологически приемлемых солей, и их сольватов, и их гидратов. В качестве предпочтительных воплощений данного лекарства предложено вышеупомянутое лекарство, которое используют для профилактического и/или терапевтического лечения заболеваний, вызываемых анормальной активностью GSK3, и вышеупомянутое лекарство, которое используют для профилактического и/или терапевтического лечения нейродегенеративных заболеваний и, в дополнение к этому, других заболеваний, таких как инсулиннезависимый сахарный диабет (например, диабет II типа) и ожирение; маниакально-депрессивное расстройство; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Т- или В-клеточный лей 004933 4 коз и некоторые индуцированные вирусом опухоли. Согласно следующим предпочтительным воплощениям настоящего изобретения предложено вышеупомянутое лекарство, где заболеваниями являются нейродегенеративные заболевания, и они выбраны из группы, состоящей из болезни Альцгеймера, болезни Паркинсона,тауопатий (например, лобно-височно-теменной деменции, кортикобазальной дегенерации, болезни Пика, прогрессирующего супрануклеарного паралича) и других деменций, включая сосудистую деменцию; острого инсульта и других травматических повреждений; инсультов(например, возрастной дегенерации желтого пятна); травмы головного и спинного мозга; периферических невропатий; ретинопатий и глаукомы; и вышеупомянутое лекарство в форме фармацевтической композиции, содержащей упомянутое выше вещество в качестве активного ингредиента вместе с одной или более чем одной фармацевтической добавкой. Кроме того, согласно настоящему изобретению предложен ингибитор активности GSK3,содержащий в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных имидазо[1,2-а]пиримидона формулы (I), и их солей, и их сольватов, и их гидратов. Согласно еще одному аспекту настоящего изобретения предложены способ профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызываемых анормальной активностью GSK3, который включает в себя стадию, на которой пациенту вводят профилактически и/или терапевтически эффективное количество вещества, выбранного из группы, состоящей из производных имидазо[1,2-а]пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов; и применение вещества, выбранного из группы, состоящей из производных имидазо[1,2-а]пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов, для изготовления вышеупомянутого лекарства. Как использовано здесь, С 1-6 алкильная группа представляет собой прямую или разветвленную алкильную группу, имеющую от 1 до 6 углеродных атомов, например метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, неопентильную группу, 1,1-диметилпропильную группу, нгексильную группу, изогексильную группу и им подобные; С 1-4 алкоксигруппа представляет собой алкоксигруппу, имеющую от 1 до 4 углеродных атомов, например метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, буток 5 сигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу и им подобные; атом галогена представляет собой атом фтора, хлора, брома или иода;C1-2 пергалогенированная алкильная группа представляет собой алкильную группу, где все атомы водорода замещены атомами галогена,например СF3 или C2F5; С 1-3 галогенированная алкильная группа представляет собой алкильную группу, где по меньшей мере один атом водорода не замещен атомом галогена; С 1-5 моноалкиламиногруппа представляет собой аминогруппу, замещенную одной С 1-5 алкильной группой, например метиламиногруппу,этиламиногруппу, пропиламиногруппу, изопропиламиногруппу, бутиламиногруппу, изобутиламиногруппу, тpeт-бутиламиногруппу, пентиламиногруппу и изопентиламиногруппу; С 2-10 диалкиламиногруппа представляет собой аминогруппу, замещенную двумя С 1-5 алкильными группами, например диметиламиногруппу, этилметиламиногруппу, диэтиламиногруппу, метилпропиламиногруппу и диизопропиламиногруппу; этениленовая и этиниленовая группы представляют собой соответственно следующие группы: Уходящая группа представляет собой группу, которая может быть легко отщеплена и заменена, такой группой может быть, например,тозил, мезил, бромид и им подобные. Соединения, представленные вышеупомянутой формулой (I), могут образовывать соли. Примеры солей включают в себя, если присутствует кислотная группа, соли щелочных металлов и щелочно-земельных металлов, таких как литий, натрий, калий, магний и кальций; соли аммония и аминов, таких как метиламин, диметиламин, триметиламин, дициклогексиламин,трис(гидроксиметил)аминометан, N,N-бис(гидроксиэтил)пиперазин, 2-амино-2-метил-1-пропанол, этаноламин, N-метилглюкамин и L-глюкамин; или соли с основными аминокислотами,такими как лизин, -гидроксилизин и аргинин. Соли кислотных соединений, полученные присоединением основания, получают с использованием стандартных методик, хорошо известных в данной области техники. Если присутствует основная группа, то примеры включают в себя соли с минеральными кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота; соли с органическими кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, уксусная кислота, пропионовая кислота, винная кислота, фумаровая кислота, малеиновая кислота, яблочная кислота,щавелевая кислота, янтарная кислота, лимонная 6 кислота, бензойная кислота, миндальная кислота, коричная кислота, молочная кислота, гликолевая кислота, глюкуроновая кислота, аскорбиновая кислота, никотиновая кислота и салициловая кислота; или соли с кислыми аминокислотами, такими как аспарагиновая кислота и глутаминовая кислота. Соли основных соединений,полученные присоединением кислот, получают с использованием стандартных методик, хорошо известных в данной области техники, при которых осуществляют растворение свободного основания в водно-спиртовом растворе, содержащем соответствующую кислоту, и выделяют соль путем упаривания раствора или посредством взаимодействия свободного основания и кислоты в органическом растворителе, в этом случае соль выделяется непосредственно, или ее осаждают с помощью второго органического растворителя, или она может быть получена в результате концентрирования раствора, но не ограничиваются указанными методиками. Кислоты, которые могут быть использованы для получения солей присоединения кислот, предпочтительно включают в себя те кислоты, которые при соединении со свободным основанием дают фармацевтически приемлемые соли, то есть соли, анионы которых относительно безвредны для организма животного в фармацевтических дозах солей, так что целебные свойства, присущие свободному основанию, не отягощаются побочными эффектами, приписываемыми анионам. Несмотря на то, что предпочтительны терапевтически приемлемые соли основных соединений, все соли, полученные присоединением кислот, находятся в пределах объема настоящего изобретения. В дополнение к этому, производные имидазо[1,2-а]пиримидона, представленные вышеупомянутой формулой (I), и их соли, их сольваты и гидраты также попадают в пределы объема настоящего изобретения. Производные имидазо[1,2-а]пиримидона, представленные вышеупомянутой формулой (I), могут иметь один или более чем один асимметричный углеродный атом. Что касается стереохимии таких асимметричных углеродных атомов, то они могут независимо существовать как в (R), так и в (S) конфигурации, и производное имидазо[1,2-а]пиримидона может существовать в виде стереоизомеров, таких как оптические изомеры или диастереоизомеры. Любые стереоизомеры в чистом виде, любые смеси стереоизомеров, рацематы и им подобные попадают в пределы объема настоящего изобретения. Примеры предпочтительных соединений по настоящему изобретению показаны здесь далее в таблице. Однако объем настоящего изобретения не ограничивается этими соединениями. Кроме того, предпочтительные соединения по настоящему изобретению, представленные формулой (I), включают в себя(1) соединения, где R1 представляет собой 3- или 4-пиридильную группу и более предпочтительно 4-пиридильную группу, которая может быть замещена С 1-2 алкильной группой, С 1-2 алкоксигруппой или атомом галогена; и/или(2) Х представляет собой связь, этениленовую группу, возможно замещенную метиленовую группу, карбонильную группу, атом серы, атом кислорода или возможно замещенный атом азота. Кроме того, более предпочтительные соединения по настоящему изобретению, представленные формулой (I), включают в себя(1) соединения, где R1 представляет собой незамещенную 4-пиридильную группу;(2) соединения, где R2 представляет собой трифторметильную группу, 2,2,2-трифторэтильную группу, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо или индольное кольцо, причем данные кольца возможно замещены; и/или(3) соединения, где Х представляет собой этениленовую группу, возможно замещенную метиленовую группу, карбонильную группу,атом серы или атом кислорода. Особенно предпочтительные соединения по настоящему изобретению, представленные формулой (I), включают в себя 1) 1-[2-(фенил)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,2) 1-[2-(1H-индол-3-ил)этил]-7-пиридин-4 илимидазо[1,2-а]пиримидин-5(1 Н)-он,3) 1-[3-(фенил)пропил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,4) 1-[3-(1H-индол-3-ил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,5) 1-[3-(4-метоксифенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,6) 1-[2-(фенокси)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,7) 1-[3-(2-метоксифенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,8) 1-[3-(2-хлорфенил)пропил]-7-пиридин-4 илимидазо[1,2-а]пиримидин-5(1 Н)-он,9) 1-[3-(2-метилфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,10) 1-[2-(фенилтио)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,11) 1-[3-(2,5-диметоксифенил)пропил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,12) 1-[3-(4-метилфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,13) 1-[3-(4-трифторметилфенил)пропил]-7 пиридин-4-илимидазо[1,2-а]-пиримидин-5(1 Н)-он,14) 1-[4-(фенил)бутил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он,15) 1-[3-(фенил)пропил]-7-пиридин-3-илимидазо[1,2-а]пиримидин-5(1H)-он,16) 1-(2-фенил-2-оксоэтил)-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,17) (S)-1-(4,4,4-трифтор-3-гидроксибутил)-7 пиридин-4-илимидазо[1,2-а]-пиримидин-5(1H)-он, 004933 8 18) 1-(4,4,4-трифторбут-2-енил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,19) (R)-1-(4,4,4-трифтор-3-гидроксибутил)-7 пиридин-4-илимидазо[1,2-а]-пиримидин-5(1H)-он,20) 1-(4,4,4-трифторбут-1-енил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,21) 1-[2-(2,5-диметоксифенил)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он,22) 1-[3-(2-фторфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,23) 1-(3-фенил-3-оксопропил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,24) 1-[3-(пиридин-3-ил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,25) (S)-1-(4,4,4-трифторбутил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-он,26) 1-[2-(2-метоксифенил)этил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,27) 1-[2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафт-2-ил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,28) 1-[2-(4-фенилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,29) 1-[2-(3-метоксифенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]-пиримидин-5(1 Н)-он,30) 1-[2-(2-нафтил)-2-оксоэтил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он,31) 1-[2-(4-метилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он,32) 1-[2-(4-фторфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он,33) 1-[2-(4-хлорфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он,34) 1-(2-(4-фторфенил)-2-гидроксиэтил)-7 пиридин-4-илимидазо[1,2-а]-пиримидин-5(1H)-он,35) 1-(2-нафтил-2-гидроксиэтил)-7-пиридин 4-илимидазо[1,2-а]-пиримидин-5(1H)-он и 36) 1-(2-(1,1,4,4-тетраметил-1,2,3,4-тетрагидронафт-6-ил)-2-гидроксиэтил)-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он. Еще в одном своем аспекте настоящее изобретение касается способов получения имидазо[1,2-а]пиримидоновых соединений, представленных вышеупомянутой формулой (I). Эти соединения могут быть получены, например, согласно способам, раскрытым ниже. Способ получения Имидазо[1,2-а]пиримидоновые соединения,представленные вышеупомянутой формулой (I),могут быть получены согласно схеме 1. Схема 1(На приведенной выше схеме определенияR1, R2, Х и n являются такими же, как они уже описаны для соединения формулы (I. Производному 7-пиридин-4-илимидазо[1,2-а] пиримидин-5(1H)-она, представленному вышеуказанной формулой (III), где R1 такой, как он 9 определен для соединения формулы (I), дают возможность взаимодействовать с основанием,таким как гидрид натрия, карбонат натрия или карбонат калия, в растворителе, таком как N,Nдиметилформамид, N-метилпирролидин, N,Nдиметилацетамид или хлороформ, при подходящей температуре в интервале от 0 до 130 С в атмосфере обычного воздуха, а затем с соединением формулы (II), где R2, Х и n такие, как они определены для соединения формулы (I), иL представляет собой уходящую группу, предпочтительно бромидную или мезильную группу, которое добавляют для получения соединения вышеупомянутой формулы (I). Соединение формулы (II) имеется в продаже или может быть синтезировано в соответствии с хорошо известными специалистам в данной области техники способами. Соединение формулы (III) может быть получено согласно способу, раскрытому на схеме 2. Схема 2(На приведенной выше схеме определениеR1 является тем же, как оно уже описано). В соответствии с этим способом 3-кетоэфиру формулы (V) дают возможность взаимодействовать с 2-аминоимидазолом формулы(IV). Взаимодействие может быть осуществлено в присутствии соли аммония, такой как ацетат аммония, в спиртовом растворителе, таком как метанол, этанол и им подобные, или без него,при подходящей температуре в интервале 25140 С в атмосфере обычного воздуха. Соединения формулы (V) или (IV) имеются в продаже или могут быть синтезированы в соответствии с хорошо известными специалистам в данной области техники способами. Например, соединения формулы (V), гдеR1 представляет собой пиридильную группу,возможно замещенную С 1-4 алкильной группой,С 1-4 алкоксигруппой или атомом галогена, могут быть получены в результате взаимодействия никотиновой кислоты, возможно замещенной С 1-4 алкильной группой, С 1-4 алкоксигруппой или галогеном, с моноэфиром малоновой кислоты. Взаимодействие может быть осуществлено с использованием способов, хорошо известных специалисту в данной области техники, например в присутствии агента сочетания, такого как 1,1'-карбонил-бис-1H-имидазол, в растворителе,таком как тетрагидрофуран, при температуре в интервале от 20 до 70 С. В указанных выше реакциях иногда могут быть необходимы введение или снятие защиты с функциональной группы. Подходящая защит 004933 10 ная группа Рg может быть выбрана в зависимости от типа функциональной группы, и может быть применен метод, описанный в литературе. Примеры защитных групп, методов введения и снятия защиты даются, например, в Protective(John WileySons, Inc., New York). Соединения по настоящему изобретению обладают ингибиторной активностью противGSK3. В соответствии с этим соединения по настоящему изобретению полезны в качестве активного ингредиента для изготовления лекарства, которое дает возможность осуществления профилактического и/или терапевтического лечения заболевания, вызываемого анормальной активностью GSK3, и в особенности нейродегенеративных заболеваний, таких как болезнь Альцгеймера. В дополнение к этому, соединения по настоящему изобретению также полезны в качестве активного ингредиента для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, тауопатии (например, лобно-височно-теменная деменция, кортикобазальная дегенерация, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; острый инсульт и другие травматические повреждения; инсульты (например, возрастная дегенерация желтого пятна); травма головного и спинного мозга; периферические невропатии; ретинопатии и глаукома; и другие заболевания, такие как инсулиннезависимый сахарный диабет (как, например, диабет II типа) и ожирение; маниакально-депрессивное расстройство; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточный рак легких, рак щитовидной железы, Т- или В-клеточный лейкоз и некоторые индуцированные вирусом опухоли. Кроме того, настоящее изобретение относится к способу лечения нейродегенеративных заболеваний, вызываемых анормальной активностью GSK3, и других вышеупомянутых заболеваний, при котором в организм млекопитающего при необходимости вводят эффективное количество соединения формулы (I). В качестве активного ингредиента лекарства по настоящему изобретению может быть использовано вещество, которое выбрано из группы, состоящей из соединения, представленного вышеупомянутой формулой (I), и его фармакологически приемлемых солей, и их сольватов, и их гидратов. Данное вещество, per se, может быть введено в виде лекарства по настоящему изобретению, однако, желательно вводить лекарство в форме фармацевтической композиции, которая содержит вышеупомянутое вещество в виде активного ингредиента и одну или более чем одну фармацевтическую добавку. В качестве активного ингредиента лекарства по настоящему изобретению могут быть использо 11 ваны два или более чем два вышеупомянутых вещества в комбинации. Указанная выше фармацевтическая композиция может быть дополнена активным ингредиентом другого лекарства для лечения упомянутых выше заболеваний. Тип фармацевтической композиции особо не ограничен, и данная композиция может быть предложена в виде любого препарата для перорального или парентерального введения. Например, фармацевтическая композиция может быть приготовлена в форме фармацевтических композиций для перорального введения, таких как гранулы, мелкозернистые гранулы, порошки, твердые капсулы, мягкие капсулы, сиропы,эмульсии, суспензии, растворы и им подобные,или в форме фармацевтических композиций для парентерального введения, таких как инъекции для внутривенного, внутримышечного или подкожного введения, капельные инфузии, трансдермальные препараты, препараты для введения через слизистую оболочку, назальные капли,ингаляции, суппозитории и им подобные. Инъекции или капельные инфузии могут быть приготовлены в виде порошкообразных препаратов,например в форме лиофилизованных препаратов, и могут быть использованы путем растворения непосредственно перед применением в соответствующей водной среде, такой как физиологический раствор. Препараты продолженного высвобождения, такие как препараты с полимерным покрытием, можно вводить непосредственно интрацеребрально. Типы фармацевтических добавок, используемых для изготовления фармацевтической композиции, пропорции содержания фармацевтических добавок относительно активного ингредиента и способы изготовления фармацевтической композиции могут быть соответствующим образом выбраны специалистами в данной области техники. В качестве фармацевтических добавок могут быть использованы неорганические или органические вещества либо твердые или жидкие вещества. Как правило, фармацевтические добавки могут быть внесены в отношении, изменяющемся в интервале от 1 до 90 мас.% в расчете на массу активного ингредиента. Примеры эксципиентов, используемых для приготовления твердых фармацевтических композиций, включают в себя, например, лактозу,сахарозу, крахмал, тальк, целлюлозу, декстрин,каолин, карбонат кальция и им подобные. Для приготовления жидких композиций для перорального введения может быть использован традиционный инертный разбавитель, такой как вода или растительное масло. Жидкая композиция может содержать, в дополнение к инертному разбавителю, вспомогательные вещества, такие как увлажняющие агенты, суспензионные вспомогательные средства, подсластители, ароматические соединения, красители и консерванты. Жидкая композиция может быть внесена в капсулы, изготовленные из абсорбируемого материала, такого 12 как желатин. Примеры растворителей или суспензионных сред, используемых для приготовления композиций для парентерального введения,например инъекций, суппозиториев, включают в себя воду, пропиленгликоль, полиэтиленгликоль, бензиловый спирт, этилолеат, лецитин и им подобные. Примеры материалов для основ,используемых для суппозиториев, включают в себя, например, масло какао, эмульгированное масло какао, лауриновый липид, витепсол. Доза и частота введения лекарства по настоящему изобретению особенно не ограничены, и они могут быть соответственно выбраны в зависимости от условий, таких как цель профилактического и/или терапевтического лечения,тип заболевания, масса тела или возраст пациента, сложность заболевания и им подобные. Как правило, суточная доза для перорального введения взрослому может составлять от 0,01 до 1000 мг (масса активного ингредиента), и доза может быть введена 1 раз в день или несколько раз в день в виде разделенных порций либо 1 раз в несколько дней. Если лекарство используется в виде инъекции, то введение взрослому предпочтительно может быть осуществлено непрерывно или периодически в суточной дозе от 0,001 до 100 мг (масса активного ингредиента). Химические примеры Настоящее изобретение будет раскрыто более подробно со ссылкой на следующие далее общие примеры, однако, объем настоящего изобретения не ограничивается этими примерами. Пример 1 (cоединение 1 из нижеследующей таблицы). 1-[2-(Фенил)этил]-7-пиридин-4-илимидазо(Z)-бут-2-ендиоат (1:1). 1.1. 7-Пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он. Смесь, содержащую 7,31 г (38 ммоль) этил 3-(4-пиридил)-3-оксопропионата, 5 г (38 ммоль) 2 аминоимидазола полусульфата и 5,86 г (76 ммоль) ацетата аммония, нагревают при 140 С в продолжение 18 ч. Охлажденную смесь обрабатывают 30 мл ацетонитрила и фильтруют, осадок добавляют к воде и нагревают с обратным холодильником при температуре флегмы в течение 30 мин. Получающийся раствор охлаждают и осадок выделяют фильтрованием. Полученный таким образом неочищенный продукт перекристаллизовывают из этанола, что дает 3,0 г чистого продукта в виде твердого вещества серой окраски. Т.пл. 368-370 С. 1.2. 1-[2-(Фенил)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он(Z)-бут-2-ендиоат (1:1). Суспензию 0,1 г (0,47 ммоль) 7-пиридин-4 илимидазо[1,2-а]пиримидин-5(1 Н)-она в 4 мл безводного N,N-диметилформамида обрабатывают 72 мг (0,52 ммоль) карбоната калия и получающуюся смесь нагревают при 70 С в течение 30 мин. Добавляют 96 мг (0,52 ммоль) 2 13(фенил)этилбромида и реакционную смесь нагревают при 130 С в продолжение 1 ч. Охлажденный раствор обрабатывают водой и экстрагируют этилацетатом. Органическую фазу высушивают и упаривают, что дает неочищенный продукт, который очищают хроматографией на силикагеле с элюированием смесью дихлорметан/метанол в соотношениях от 100/0 до 95/5. 0,338 г чистого продукта, полученного в форме свободного основания, растворяют в горячем этаноле и обрабатывают 1 эквивалентом (Z)-бут-2-ендикислоты, охлажденный раствор фильтруют, что позволяет получить 0,12 г твердого вещества. Т.пл. 190-192 С. Пример 2 (cоединение 4 из нижеследующей таблицы). 1-[3-(1 Н-Индол-3-ил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-он. 2.1. 3-(1 Н-Индол-3-ил)пропанол (J. Med.Chem. (1995), 38(11), 1998). К суспензии 4,8 г (126,8 ммоль) алюмогидрида лития в 240 мл диэтилового эфира при 0 С по каплям добавляют 10 г (52,8 ммоль) 3(1H-индол-3-ил)пропановой кислоты, растворенной в 430 мл диэтилового эфира, и получающуюся смесь перемешивают при комнатной температуре в течение 1 ч. Реакционную смесь разбавляют 100 мл диэтилового эфира при 0 С и обрабатывают избытком насыщенного водного раствора сульфата натрия. Добавляют дополнительное количество твердого сульфата натрия и органическую фазу фильтруют для удаления солей. Растворитель выпаривают досуха, что дает 9 г (98%) продукта в виде масла. 2.2. 3-(1H-Индол-3-ил)пропилбромид (Chem.Pharm. Bull. (1988), 36(8), 2853). К раствору 2 г (11,41 ммоль) 3-(1H-индол 3-ил)пропанола в 40 мл диоксана добавляют при комнатной температуре 5,3 г (12,55 ммоль) дибромтрифенилфосфорана и получающийся раствор перемешивают в продолжение 18 ч. Добавляют избыток циклогексана и получающийся осадок отфильтровывают и отбрасывают. Растворитель выпаривают досуха, что дает 2,7 г(99%) продукта в виде масла, которое используют на последующей стадии без дальнейшей очистки. 2.3. 1-[3-(1 Н-Индол-3-ил)пропил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он. К суспензии 0,10 г (0,47 ммоль) 7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она в 3 мл безводного N,N-диметилформамида добавляют 0,072 г (0,52 ммоль) карбоната калия и получающуюся смесь нагревают при 130 С в течение 10 мин. Добавляют 0,116 г (0,52 ммоль) 3-(1 Н-индол-3-ил)пропилбромида и нагревание продолжают в течение 16 ч. Охлажденную суспензию обрабатывают водой, экстрагируют этилацетатом и органические экстракты высушивают над сульфатом натрия. Неочищенный продукт очищают хроматографией 14 на силикагеле с элюированием смесью дихлорметан/метанол/аммиак в соотношении 90/10/1, что позволяет получить 0,11 г чистого продукта. Т.пл. 201-203 С. Пример 3 (cоединение 10 из нижеследующей таблицы). 1-[2-(Фенилтио)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-он гидрохлорид (1:1). К суспензии 0,2 г (0,94 ммоль) 7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она в 4,5 мл безводного N,N-диметилформамида добавляют 0,169 г (1,23 ммоль) карбоната калия и получающуюся смесь нагревают при 70 С в продолжение 20 мин. Добавляют 0,267 г (1,23 ммоль) 2-бромэтилфенилсульфида и нагревание продолжают при 130 С в течение 1,5 ч. К охлажденной смеси добавляют воду и получающийся раствор экстрагируют этилацетатом. Объединенные экстракты промывают водой и упаривают. Неочищенный продукт очищают хроматографией на силикагеле с элюированием смесью дихлорметан/метанол в соотношениях от 100/0 до 96/4, получая чистое соединение в форме свободного основания. Данное соединение переводят в соль гидрохлорид путем добавления соляной кислоты к этанольному раствору свободного основания. Получают 0,133 г продукта в виде твердого вещества белого цвета. Т.пл. 219-221 С. Пример 4 (cоединение 6 из нижеследующей таблицы). 1-[2-(Фенокси)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-он(Z)-бут-2-ендиоат (1:1). К суспензии 0,4 г (1,88 ммоль) 7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она в 6 мл безводного N,N-диметилформамида добавляют 0,312 г (2,25 ммоль) карбоната калия и получающуюся смесь нагревают при 70 С в продолжение 30 мин. Добавляют 0,378 г (1,88 ммоль) 2-феноксиэтилбромида и нагревание продолжают при 130 С в течение 2 ч. К охлажденной смеси добавляют воду и получающийся раствор экстрагируют этилацетатом. Объединенные экстракты промывают водой и упаривают. Неочищенный продукт очищают хроматографией на силикагеле с элюированием смесью дихлорметан/метанол в соотношениях от 100/0 до 96/4, получая чистое соединение в форме свободного основания. Продукт, полученный в форме свободного основания, переводят в соль путем обработки 1 эквивалентом (Z)-бут-2-ендикислоты. Таким образом получают 0,217 г конечного продукта. Т.пл. 158-160 С. Список химических структур и физических данных для соединений вышеупомянутой формулы (I), иллюстрирующих настоящее изобретение, дается в таблице. Соединения получают в соответствии со способами примера. В таблице: R1 является незамещенной 4 пиридильной группой (4-ру) или 3-пиридильной группой (3-ру), Ph представляет собой фенильную группу, (S) указывает стереохимию углеродного атома и в структуре R2 представляет собой связь, соединенную с X. Пример анализа. Ингибиторная активность лекарства по настоящему изобретению противGSK3. Могут быть использованы два различных протокола. По первому протоколу: 7,5 мкМ предварительно фосфорилированного GS1-пептида и 10 мкМ АТФ (содержащего 300000 имп/мин 33 РАТФ) инкубируют в 25 мМ Трис-НСl буфере,рН 7,5, содержащем 0,6 мМ DTT (дитиотреитол),6 мМ MgCl2, 0,6 мМ EGTA (этиленгликольтетрауксусная кислота), 0,05 мг/мл БСА (бычий сывороточный альбумин), в течение 1 ч при комнатной температуре в присутствии GSK3 17 По второму протоколу: 4,1 мкМ предварительно фосфорилированного GS1-пептида и 42 мкМ АТФ (содержащего 260000 имп/мин 33 РАТФ) инкубируют в 80 мМ Mes-NaOH буфере,рН 6,5, содержащем 1 мМ ацетата Мg, 0,5 мМEGTA, 5 мМ 2-меркаптоэтанола, 0,02% Твина 20, 10% глицерина, в течение 2 ч при комнатной температуре в присутствии GSK3. Ингибиторы растворяют в ДМСО (конечная концентрация растворителя в реакционной среде 1%). Реакцию останавливают 100 мкл раствора,приготовленного из расчета 25 г полифосфорной кислоты (85% Р 2O5), 126 мл 85%-ной Н 3 РO4,Н 2O до 500 мл и затем разбавленного 1:100 перед использованием. Аликвоту реакционной смеси затем переносят на катионообменные фильтры Whatman Р 81 и промывают раствором,описанным выше. Радиоактивность включенного 33P определяют с помощью жидкостной сцинтилляционной спектрометрии. Фосфорилированный пептид GS-1 имеет следующую последовательность:GSK3-ингибиторную активность соединений по настоящему изобретению выражают вIС 50, и, в качестве иллюстрации, интервал значений IС 50 для соединений в таблице лежит между 10 наномолярной и 1 микромолярной концентрациями. Пример приготовления препаратов(1) Таблетки. Представленные ниже ингредиенты смешивают обычным способом и прессуют посредством использования традиционной аппаратуры. Соединение из примера 1 30 мг Целлюлоза кристаллическая 60 мг Крахмал кукурузный 100 мг Лактоза 200 мг Магния стеарат 4 мг(2) Мягкие капсулы. Представленные ниже ингредиенты смешивают обычным способом и смесью заполняют мягкие капсулы. Соединение из примера 1 30 мг Масло оливковое 300 мг Лецитин 20 мг(3) Парентеральные препараты. Представленные ниже ингредиенты смешивают обычным способом для приготовления инъекций из расчета на 1 мл ампулу. Соединение из примера 1 3 мг Натрия хлорид 4 мг Вода дистиллированная для инъекций 1 мл Промышленная применимость Соединения по настоящему изобретению обладают GSK3-ингибиторной активностью и полезны в качестве активного ингредиента лекарства для профилактического и/или терапев 004933 18 тического лечения заболеваний, вызываемых анормальной активностью GSK3, и в особенности нейродегенеративных заболеваний. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производное имидазо[1,2-а]пиримидона,представленное формулой (I), или его соль, или их сольват, либо их гидрат где Х представляет собой связь, этениленовую группу, этиниленовую группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, гидроксигруппы и С 1-4 алкоксигруппы; карбонильную группу, атом кислорода, атом серы, сульфонильную группу, сульфинильную группу или атом азота, возможно замещенныйR1 является 2-, 3- или 4-пиридильной группой, возможно замещенной С 1-4 алкильной группой, С 1-4 алкоксигруппой или атомом галогена;R2 представляет собой C1-6 алкильную группу, С 1-2 пергалогенированную алкильную группу, C1-3 галогенированную алкильную группу, бензильную группу, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо, пиридильное кольцо, индольное кольцо,пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо, причем данная бензильная группа и данные кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из C1-6 алкильной группы,фенильного кольца, атома галогена, С 1-2 пергалогенированной алкильной группы, C1-3 галогенированной алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, нитро, циано, амино, C1-6 моноалкиламиногруппы или С 2-10 диалкиламиногруппы; иn равняется числу от 0 до 3. 2. Производное имидазо[1,2-а]пиримидона,или его соль, или их сольват, либо их гидрат по п.1, где R1 представляет собой незамещенную 4-пиридильную группу или 3-пиридильную группу. 3. Производное имидазо[1,2-а]пиримидона,или его соль, или их сольват, либо их гидрат по п.1 или 2, где R2 представляет собой трифторметильную группу, 2,2,2-трифторэтил, фенильное кольцо, нафтильное кольцо, 5,6,7,8-тетрагидронафтильное кольцо или индольное кольцо,причем данные кольца возможно замещены. 4. Производное имидазо[1,2-а]пиримидона,которое выбрано из группы, состоящей из 1) 1-[2-(фенил)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она, 19 2) 1-[2-(1H-индол-3-ил)этил]-7-пиридин-4 илимидазо[1,2-а]пиримидин-5(1H)-она,3) 1-[3-(фенил)пропил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,4) 1-[3-(1H-индол-3-ил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,5) 1-[3-(4-метоксифенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,6) 1-[2-(фенокси)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,7) 1-[3-(2-метоксифенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,8) 1-[3-(2-хлорфенил)пропил]-7-пиридин-4 илимидазо[1,2-а]пиримидин-5(1 Н)-она,9) 1-[3-(2-метилфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-она,10) 1-[2-(фенилтио)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,11) 1-[3-(2,5-диметоксифенил)пропил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,12) 1-[3-(4-метилфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-она,13) 1-[3-(4-трифторметилфенил)пропил]-7 пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)она,14) 1-[4-(фенил)бутил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,15) 1-[3-(фенил)пропил]-7-пиридин-3-илимидазо[1,2-а]пиримидин-5(1H)-она,16) 1-(2-фенил-2-оксоэтил)-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,17) (S)-1-(4,4,4-трифтор-3-гидроксибутил)-7 пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,18) 1-(4,4,4-трифторбут-2-енил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-она,19) (R)-1-(4,4,4-трифтор-3-гидроксибутил)-7 пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,20) 1-(4,4,4-трифторбут-1-енил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-она,21) 1-[2-(2,5-диметоксифенил)этил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,22) 1-[3-(2-фторфенил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1H)-она,23) 1-(3-фенил-3-оксопропил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,24) 1-[3-(пиридин-3-ил)пропил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,25) (S)-1-(4,4,4-трифторбутил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,26) 1-[2-(2-метоксифенил)этил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,27) 1-[2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафт-2-ил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,28) 1-[2-(4-фенилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она, 20 29) 1-[2-(3-метоксифенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,30) 1-[2-(2-нафтил)-2-оксоэтил]-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она,31) 1-[2-(4-метилфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,32) 1-[2-(4-фторфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,33) 1-[2-(4-хлорфенил)-2-оксоэтил]-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она. 34) 1-(2-(4-фторфенил)-2-гидроксиэтил)-7 пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)она,35) 1-(2-нафтил-2-гидроксиэтил)-7-пиридин 4-илимидазо[1,2-а]пиримидин-5(1 Н)-она; 36) 1-(2-(1,1,4,4-тетраметил-1,2,3,4-тетрагидронафт-6-ил)-2-гидроксиэтил)-7-пиридин-4-илимидазо[1,2-а]пиримидин-5(1H)-она,или его соль, или их сольват, либо их гидрат. 5. Лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного имидазо(I), или его солей, или их сольвата, либо их гидрата по п.1. 6. Ингибитор GSK3, выбранный из группы производного имидазо[1,2-а]пиримидона,представленного формулой (I), или его солей,или их сольвата, либо их гидрата по п.1. 7. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения заболевания,вызываемого анормальной активностью GSK3. 8. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративного заболевания. 9. Применение соединения по п.8, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера,болезни Паркинсона, тауопатий, сосудистой деменции; острого инсульта, травматических повреждений; инсультов, травмы головного мозга, травмы спинного мозга; периферических невропатий; ретинопатий или глаукомы. 10. Применение соединения по пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения инсулиннезависимого сахарного диабета; ожирения; маниакально-депрессивного расстройства; шизофрении; алопеции или рака. 11. Применение по п.10, где рак представляет собой рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Тили В-клеточный лейкоз либо индуцированные вирусом опухоли.
МПК / Метки
МПК: A61P 25/00, A61K 31/519, C07D 487/04
Метки: 1-[(арил)алкил]-7-пиридинил-имидазо[1, 1-[(гетероарил)алкил, 1-[алкил, производные, 2-a]пиримидин-5(1н)она
Код ссылки
<a href="https://eas.patents.su/11-4933-proizvodnye-1-alkil-1-geteroarilalkil-i-1-arilalkil-7-piridinil-imidazo1-2-apirimidin-51nona.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 1-[алкил], 1-[(гетероарил)алкил] и 1-[(арил)алкил]-7-пиридинил-имидазо[1, 2-a]пиримидин-5(1н)она</a>
Предыдущий патент: Имидазоимидазолы и имидазотриазолы в качестве противовоспалительных агентов
Следующий патент: Асимметрический синтез прегабалина
Случайный патент: Трехслойная огнеупорная панель и ее применение












