Стереоспецифический синтез хиральных 1-арил- и 1-гетероарил-2-замещенных этил-2-аминов
Номер патента: 1364
Опубликовано: 26.02.2001
Авторы: Пауэрс Мэттью Р., Леон Патрик, Казимир Жан-Поль, Робин Даниэль, Грондар Люк, О'брайен Майкл К
Формула / Реферат
1. Способ стереоспецифического синтеза [(1-необязательно замещенный арил)- или (1-необязательно замещенный гетероарил)]-2-замещенного этил-2-амина, имеющего хиральный атом в положении 2, включающий взаимодействие 2-амино-2-замещенного этилового спирта, имеющего хиральный атом в положении 2, с [(необязательно замещенный арил)- или (тригалогенметил)сульфонил]-галогенидом или ангидридом в присутствии основания с образованием [(N-арилсульфонил)- или (N-тригалогенметилсульфонил)]-2-замещенного азиридина, имеющего хиральный центр в положении 2.
2. Способ по п.1, дополнительно включающий реакцию указанного азиридина с [(необязательно замещенный арил)- или (необязательно замещенный гетероарил)] литиевым соединением с образованием литиевой соли [(N-необязательно замещенный арил)-или (N-тригалогенметил)сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2-амина, имеющего хиральный центр в положении 2.
3. Способ по п.2, дополнительно включающий обработку указанной литиевой соли одной или более сильными кислотами в присутствии электрофильного акцептора.
4. Способ по п. 1 получения соединения формулы
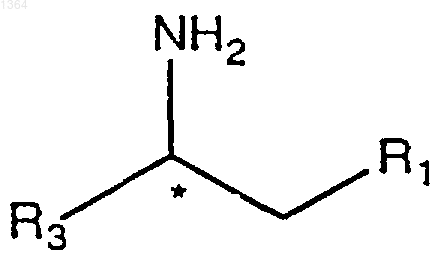
где * означает хиральный атом углерода;
R1 представляет необязательно замещенный арил или необязательно замещенный гетероарил; и
R3 представляет необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил;
включающий взаимодействие соединения формулы
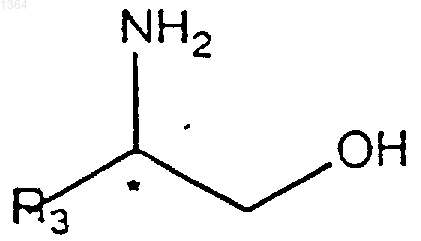
с соединением формулы
R2-SO2-R',
где R' представляет галоген или OSO2R2; и
R2 представляет необязательно замещенный арил или тригалогенметил;
в присутствии основания с образованием соединения азиридина формулы
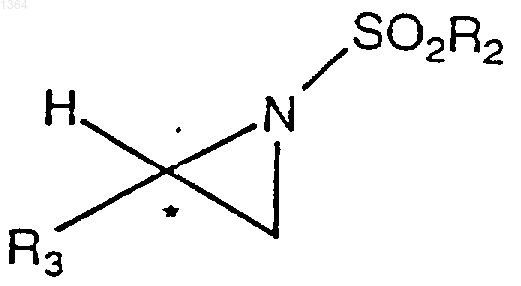
5. Способ по п.4, дополнительно включающий реакцию указанного соединения азиридина с соединением формулы Li-R1 с образованием соединения лития формулы
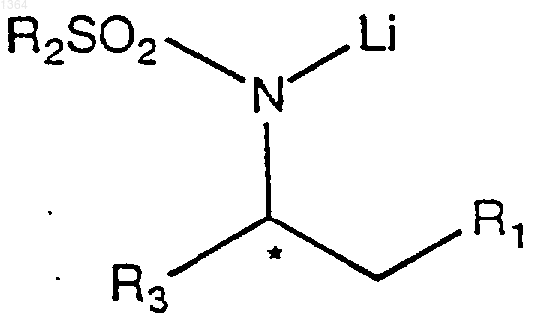
или его агрегата, где
R1 представляет необязательно замещенный арил или необязательно замещенный гетероарил;
R2 представляет необязательно замещенный арил или тригалогенметил; и
R3 представляет необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил.
6. Способ по п.5, дополнительно включающий обработку указанного соединения лития сильной кислотой или смесью сильных кислот в присутствии электрофильного акцептора.
7. Способ по п.4, где указанную реакцию проводят в апротонном органическом растворителе.
8. Способ по п.7, где указанным апротонным органическим растворителем является трет-бутилметиловый эфир.
9. Способ по п.4, где R2-SO2-R' представляет собой п-толуолсульфонилхлорид.
10. Способ по п.4, где указанную реакцию проводят при температуре от около 25шС до около 90шС.
11. Способ по п.4, где указанную реакцию проводят при температуре от около 25шС до около 40шС.
12. Способ по п.4, где указанное основание выбирают из группы, состоящей из водного раствора гидроксида щелочного металла, водного раствора карбоната щелочного металла и апротонного органического амина.
13. Способ по п.4, где указанным основанием является водный гидроксид натрия.
14. Способ по п.4, где R1 представляет необязательно замещенный гетероарил.
15. Способ по п.14, где R1 представляет 3-хлортиен-2-ил.
16. Способ по п.4, где R3 представляет алкил.
17. Способ по п.16, где R3 представляет этил.
18. Способ по п.5, где реакцию указанного соединения азиридина проводят в растворителе, выбранном из группы, включающей апротонный органический эфир, алифатический углеводород и ароматический углеводород.
19. Cпособ по п.18, где указанную реакцию указанного соединения азиридина проводят в трет-бутилметиловом эфире.
20. Способ по п.5, дополнительно включающий выделение указанного соединения лития в виде твердого вещества.
21. Способ по п.5, где указанную реакцию проводят при температуре от около -80шС до около 50шС.
22. Способ по п.21, где указанную реакцию проводят при температуре от около -40шС до около 50шС.
23. Способ по п.6, где указанная смесь сильных кислот содержит метансульфоновую кислоту и трифторуксусную кислоту.
24. Способ по п.6, где указанным электрофильным акцептором является тиоанизол.
25. Способ по п.6, где указанную обработку проводят при температуре от около 45шС и до, приблизительно, температуры кипения.
26. [(N-арилсульфонил)-или (N-тригалогенметилсульфонил)]-2-замещенный азиридин, имеющий хиральный центр в положении 2.
27. Соединение азиридина по п.26 формулы
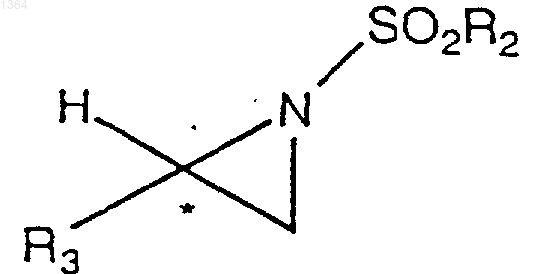
где R2 представляет необязательно замещенный арил или тригалогенметил; и
R3 представляет необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил.
28. Соединение азиридина по п.27, представляющее собой 1-п-толуолсульфонил-2-(R)-этилазиридин.
29. Литиевая соль [(N-необязательно замещенный арил)- или (N-тригалогенметил)сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2-амина, имеющего хиральный центр в положении 2.
30. Литиевая соль по п.29 формулы
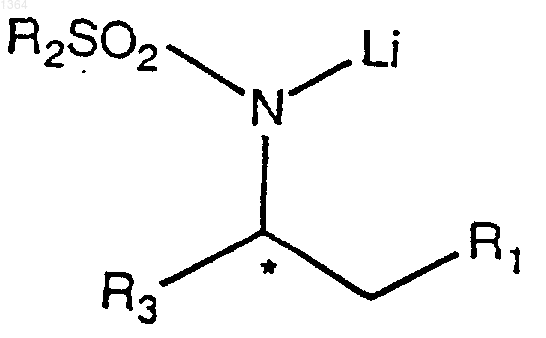
или ее агрегат, где
R1 представляет необязательно замещенный арил или необязательно замещенный гетероарил;
R2 представляет необязательно замещенный арил или тригалогенметил; и
R3 представляет необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил.
31. Соединение лития по п.30, представляющее собой литиевую соль (R)-1-(3-хлортиен-2-ил)-2-бутилтолуолсульфонамида.
Текст
1 Область изобретения Настоящее изобретение относится к способам стереоспецифического синтеза [(1 необязательно замещенный арил-) или (1 необязательно замещенный гетероарил)]-2 замещенных этил-2-аминов, имеющих хиральный атом (центр) в положении 2. Изобретение относится также к промежуточным продуктам для получения замещенных этил-2-аминов. Замещенные этил-2-амины и промежуточные продукты для их получения полезны в качестве промежуточных соединений в синтезе сердечно-сосудистых средств, включая антигипертензивные средства, антиишемические средства, кардиопротекторные средства, которые улучшают состояние пациента при ишемических повреждениях или инфаркте миокарда вследствие ишемии миокарда, антилиполитических средств, снижающих уровень липидов в плазме крови, уровень триглицеридов в сыворотке и уровень холестерина в плазме. Например, в патенте US 5364862 описаны замещенные этил-2-амины, используемые как полупродукты в синтезе антигипертензивных и антиишемических гетероциклических производных аденозина и их аналогов. Они также используются в синтезе N9-циклопентилзамещенных производных аденина, которые описаны как лиганды аденозиновых рецепторов и полезны для лечения сердечно-сосудистых заболеваний, таких как артериальная гипертония,тромбоз и атеросклероз, а также заболеваний центральной нервной системы, включая психотические состояния, такие как шизофрения, и судорожных нарушений, таких как эпилепсия(см. патент US 4954504). Они также полезны в синтезе N-6 и 5'-N замещенных производных карбоксамидоаденозина, благотворно влияющих на сердечно-сосудистую систему и обладающих антигипертензивным действием, что описано в патенте US 5 310 731. Уровень техники В патенте US 5364862 Spada и др. описан стереоспецифический синтез хиральных необязательно замещенных гетероарил-2-замещенных этил-2-аминов реакцией гетероарильных анионов с 2-замещенными этиленоксидами с последующим стереоспецифическим превращением полученного хирального этилового спирта в амин. Имеются сообщения об ускорении реакций ацидолитического (кислотного) расщепления,например, удаление различных защитных групп, в присутствии электрофильных акцепторов. В Yajima и др. описано снятие защиты уPharm. Bull. 26, (12), 3752-3757, (1978). В Kiso и др. описано также удаление защитной группы уO-бензил серина, треонина и тирозина, а также снятие защиты у Ne-бензилоксикарбониллизина,Chem. Pharm. Bull. 28, (2), 673-676 (1980). Ме 001364 2 тодики удаления защитных п-толуолсульфонильных и п-метоксибензолсульфонильных групп у Nim-функциональной группы гистидина описаны в Kitagawa и др., Chem. Pharm. Bull. 28,(3), 926-931 (1980). Сущность изобретения Настоящее изобретение относится к способам стереоспецифического синтеза [(1 необязательно замещенный арил-) или (1 необязательно замещенный гетероарил)-]-2 замещенных этил-2-аминов, имеющих хиральный атом в положении 2, включающим реакцию 2-амино-2-замещенного этилового спирта,имеющего хиральный атом в положении 2, с[(N-арилсульфонил)- или (N-тригалоидметилсульфонил)]-2-замещенного азиридина, имеющего хиральный центр в положении 2. Детальное описание изобретения Используемые в описании настоящего изобретения термины имеют следующие значения, если не указано иное."Арил" означает фенил или нафтил."Необязательно замещенный арил" означает арильную группу, которая замещена одним или более заместителями арильной группы. Примеры заместителей арильной группы включают алкил, алкокси, амино, арил, гетероарил,тригалогенметил,нитро,карбокси,карбоалкокси, карбоксиалкил, циано, алкиламино,галоид, гидрокси, гидроксиалкил, меркаптил,алкилмеркаптил или карбамоил. Преимущественно заместители арильной группы включают галоген, гидрокси, алкил, арил, алкокси, тригалогенметил, циано, нитро и алкилмеркапто."Гетероарил" означает 4-10-членную ароматическую циклическую структуру, в которой один или более атомов в кольце представляет собой иной, нежели углерод элемент, напримерN, О или S. Примеры гетероарильных групп включают пиридил, пиридазинил, пиримидинил, изохинолинил, хинолинил, хиназолинил,имидазолил, пирролил, фуранил, тиенил, тиазолил и бензотиазолил. Преимущественно гетероарильной группой является тиенил."Необязательно замещенный гетероарил" означает, что гетероарильная группа может быть замещена одним или более заместителем арильной группы. Примеры заместителей арильной группы включают алкокси, алкиламино, арил, карбалкокси, карбамоил, циано, галоген, гетероарил, тригалоидметил, гидрокси,меркаптил, алкилмеркаптил или нитро. Предпочтительно заместители гетероарильной группы включают галоген, гидрокси, алкил, арил,алкокси, тригалогенметил, циано, нитро и алкилмеркаптил."Алкил" означает насыщенную алифатическую углеводородную группу, которая может быть прямой или разветвленной и иметь от 1 до 20 углеродных атомов в цепи. Преимущественно алкильная группа может быть прямой или разветвленной и иметь от 1 до 10 атомов углерода в цепи. Низший алкил означает алкильную группу, которая может быть прямой или разветвленной и иметь от 1 до 6 атомов углерода,такую как метил, этил, пропил или трет-бутил."Разветвленный" означает, что низшая алкильная группа присоединена к линейной алкильной цепи."Необязательно замещенный аралкил" означает, что арильная группа аралкильной группы может быть замещена одним или более заместителями арильной группы."Необязательно замещенный гетероаралкил" означает, что гетероарильная группа или гетероаралкильная группа может быть замещена одним или более заместителями арильной группы."Электрофильный акцептор" означает агент, который может обладать промотирующим действием на реакции ацидолитического расщепления, например, как описано у Yajima и др., Chem. Pharm. Bull. 26, (12), 3752-3757,(1978), Kiso и др., Chem. Pharm. Bull. 28, (2),673-676 (1980), Kitagawa и др., Chem. Pharm.Bull. 28, (3), 926-931 (1980). Настоящее изобретение относится к реакции 2-амино-2-замещенного этилового спирта с сульфонилгалогенидом или ангидридом, предпочтительно в присутствии апротонного органического растворителя. Подходящие для реакции апротонные органические растворители включают апротонные органические эфиры,ароматические углеводороды, гетероароматические углеводороды, алифатические углеводороды и апротонные органические амиды. Наиболее предпочтительными примерами апротонных органических растворителей являются диэтиловый эфир, трет-бутилметиловый эфир, изопропилметиловый эфир, диизопропиловый эфир,тетрагидрофуран, тетрагидропиран и диоксан. В частных случаях воплощения изобретения наиболее предпочтительным апротонным органическим растворителем является третбутилметиловый эфир. Предпочтительно реакцию сульфонилгалогенида или ангидрида проводят при температуре около от 25 до 90 С; наиболее предпочтительно в интервале от 25 до около 40 С. Пригодные сульфонилгалогениды и ангидриды включают фенил-, тол-4-ил-, 2,4,6 триметилфенил-,2,4-диметилфенил,4-метоксифенил-, 4-нитрофенил-, 4-бромфенил-нафт-1-ил-,нафт-2-ил- и трифторметилсульфонилхлорид и 4 ангидрид. В частных случаях воплощения изобретения наиболее предпочтительным сульфонилхлоридом является п-толуолсульфонилхлорид (т.е.тол-4-ил-сульфонилхло-рид). В соответствии с настоящим изобретением реакцию 2-амино-2-замещенного этилового спирта с сульфонилгалогенидом или ангидридом проводят в присутствии основания. Приемлемые для реакции основания включают водные растворы гидроксидов щелочных металлов,водные растворы карбонатов щелочных металлов и апротонные органические амины. Предпочтительные примеры подходящих гидроксидов щелочных металлов включают гидроксид натрия, гидроксид калия и гидроксид лития; примеры подходящих карбонатов щелочных металлов включают карбонат калия, карбонат натрия и карбонат цезия; и примеры подходящих апротонных органических аминов включают триэтиламин, диизопропилэтиламин, Nметилморфолин и пиридин. В частных случаях воплощения изобретения наиболее предпочтительным основанием является водный раствор гидроксида натрия. Далее настоящее изобретение относится также к реакции [(N-арилсульфонил)- или (Nтригалоидметилсульфонил)]-2-замещенного азиридина, имеющего хиральный атом в положении 2 и полученного взаимодействием 2 амино-2-замещенного этилового спирта с сульфонилгалогенидом или ангидридом, с [(необязательно замещенный арил)- или (необязательно замещенный гетероарил)] литиевым соединением с образованием литиевой соли [(Nнеобязательно замещенный арил)- или (Nтригалоидметил)сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2 амина, имеющего хиральный центр в положении 2. В частном случае реализации изобретения образующуюся в реакции литиевую соль выделяют в виде твердого вещества. Литийорганические соединения могут существовать в виде тетрамеров, гексамеров и в более высокой степени агрегации в углеводородных или эфирных растворителях, как описано, например, Carey(1980). Образование таких агрегатов литиевых солей способом настоящего изобретения также включено в объем настоящего изобретения. Предпочтительно реакцию образования литиевой соли проводят в апротонном органическом растворителе. Апротонные органические растворители, которые пригодны для указанной реакции, включают апротонные органические эфиры, алифатические углеводороды и ароматические углеводороды. В частном случае реализации изобретения предпочтительным апротонным органическим растворителем является апротонный органический эфир и особенно 5 предпочтительным является трет-бутилметиловый эфир. Образование литиевой соли предпочтительно происходит при температуре от около-80 С до около 50 С, более предпочтительно от около -40 С до около 50 С. Еще одним объектом изобретения является обработка литиевой соли [(N-необязательно замещенный арил)- или (N-тригалоидметил) сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2-амина, имеющего хиральный центр в положении 2, одной или более сильными кислотами в присутствии электрофильных акцепторов. Указанную обработку осуществляют преимущественно при температуре от около 45 С до температуры кипения реакционной смеси. Пригодные для обработки сильные кислоты включают метансульфоновую кислоту,трифторуксусную кислоту, трифторметансульфоновую кислоту, трихлорметансульфоновую кислоту, трихлоруксусную кислоту, серную кислоту, хлористоводородную кислоту, бромистоводородную кислоту и фосфорную кислоту. В частном случае реализации изобретения обработку проводят преимущественно смесью сильных кислот; наиболее предпочтительна смесь метансульфоновой и трифторуксусной кислот. Пригодные для обработки электрофильные акцепторы включают анизол, тиоанизол, дифенилдисульфид, фенилбензилсульфид, триметоксибензол, м-крезол и 1,2-этандиол. В частном случае реализации изобретения предпочтительным электрофильным акцептором является тиоанизол. Преимущественно настоящее изобретение относится к способу получения соединения формулы I гдеозначает хиральный атом углерода;R1 представляет необязательно замещенный арил или необязательно замещенный гетероарил; иR3 представляет необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил, включающий взаимодействие соединения формулы II с соединением формулы III где R' представляет галоген или OSO2R2; иR2 представляет необязательно замещенный арил или тригалоидметил, в присутствии осно 001364 6 вания с образованием соединения азиридина формулы IV Еще одним объектом настоящего изобретения является способ получения соединения формулы I, где R1 представляет необязательно замещенный гетероарил; более предпочтительно R1 представляет 3-хлортиен-2-ил. Другим предпочтительным воплощением изобретения является способ получения соединения формулы I, где R3 - алкил; более предпочтительно R3 представляет этил. Еще одним предпочтительным воплощением изобретения является способ получения соединения формулы I, включающий действие азиридина формулы IV с соединением формулыLi-R с образованием соединения формулы V и его агрегатов. Другим воплощением настоящего изобретения является способ получения соединения формулы I, включающий обработку литиевого соединения формулы V сильной кислотой или смесью сильных кислот в присутствии электрофильного акцептора. На схеме 1 представлены преимущественные способы проведения процесса настоящего изобретения. Схема 1 В случае необходимости или по желанию для предотвращения взаимодействия между химически активными заместителями (например, любыми заместителями арильной или гетероарильной группы) при проведении реакций или обработок согласно изобретению, заместители могут быть защищены стандартными защитными группами, которые впоследствии могут быть удалены известными методами или в случае необходимости оставлены с целью получения желаемого продукта (см., например,Green, Protective groups in Organic Synthesis,Wiley, New York (1982. Селективная защита или снятие защиты также может быть необходима или желательна при превращении или удалении существующих заместителей или при 7 проведении последующей реакции, приводящей к конечному целевому продукту. Настоящее изобретение относится также к промежуточным продуктам для получения [(1 необязательно замещенный арил-) или (1 необязательно замещенный гетероарил)]-2 замещенных этил-2-аминов. Соединение, также являющееся объектом изобретения,представляет собой[(Nарилсульфонил)- или (N-тригалоидметилсульфонил)]-2-замещенный азиридин, имеющий хиральный атом в положении 2, полученный реакцией 2-амино-2-замещенного этилового спирта с сульфонилгалогенидом или ангидридом в соответствии со способом настоящего изобретения. Предпочтительно указанный азиридин представляет собой соединение формулыIV. В частном воплощении изобретения указанный азиридин включает 1-п-толуолсульфонил 2(R)-этилазиридин. Другим соединением настоящего изобретения является литиевая соль [(N-необязательно замещенный арил)- или (N-тригалоидметил)сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2-амина, имеющего хиральный центр в положении 2, и полученная реакцией азиридина с [(необязательно замещенный арил)- или (необязательно замещенный гетероарил)] литиевым соединением в соответствии со способом настоящего изобретения. Предпочтительным литиевым соединением является соединение формулы V. В преимущественном воплощении изобретения литиевая соль включает литиевую соль (R)-1-(3-хлортиен-2 ил)-2-бутилтолуолсульфонамида. Настоящее изобретение иллюстрируется,но не ограничивается следующими примерами. Пример 1. Получение 1-п-толуолсульфонил-2(R)-этилазиридина.R-(-)-2-амино-1-бутанол (99,96 г, 105 мл) и трет-бутилметиловый эфир (ТБМЭ) (277 г, 366 мл) объединяют в атмосфере азота. Смесь перемешивают несколько минут и в течение 10 мин добавляют 10N водный раствор гидроксида натрия (449 мл). Реакционную смесь охлаждают до приблизительно 10 С и в течение приблизительно 50 мин добавляют раствор п-толуолсульфонилхлорида (ТсХ) (464 г) в (ТБМЭ) (711 г), выдерживают при температуре реакционной смеси около 32 С. После завершения добавления смесь перемешивают около 30 мин при 40 С, добавляют воду (900 мл) при охлаждении смеси до 25 С. Разделяют слои и органический слой промывают последовательно водой (150 г) и 25%-ным водным раствором хлорида натрия(300 г). К органическому слою добавляют толуол (450 г) и смесь перегоняют при пониженном давлении, поддерживая температуру смеси около 45 С до тех пор, пока содержание воды в смеси не достигнет около 0,1%. Полученный 8 раствор без дальнейшей обработки используют в примере 2. Пример 2. Получение литиевой соли (R)-1(3-хлортиен-2-ил)-2-бутилтолуолсульфонамида. Раствор 3-хлортиофена (48,75 г) в ТБМЭ(291 г) охлаждают до -10 С в атмосфере азота и добавляют 2,5 М н-бутиллитий в гексане (151,3 мл) с такой скоростью, чтобы температура реакции сохранялась между 0 С и 5 С. После окончания добавления смесь охлаждают до -5 С и добавляют раствор 1-п-толуолсульфонил-2(R)-этилазиридина (74,1 г, в виде 56,9 вес.% раствора в ТБМЭ) с такой скоростью, чтобы сохранить температуру реакционной смеси ниже 9 С (в течение этого времени образуется твердый осадок). Через 5 мин смесь охлаждают до 0 С и собирают осадок вакуумной фильтрацией, промывают осадок при 0 С ТБМЭ (60 мл) и сушат в вакууме при 40 С, получая литиевую сольMS (FAB), m/z 350 (100%), 1 Н ЯМР (200 МГц,ДМСО) 0.8 (т, 3 Н); 2.25 (с, 3 Н); 6.85 (д, 1 Н); 7.05 (д, 2 Н); 7.35 (д, 2 Н). Пример 3. Получение (R)-1-(3-хлортиен-2 ил)-2-аминобутана В колбу, снабженную обратным холодильником и механической мешалкой, загружают трифторуксусную кислоту (470 г) и добавляют к ней литиевую соль (R)-1-(3-хлортиен-2-ил)-2 бутилтолуолсульфонамида (120 г). Температура смеси повышается от 25 С до приблизительно 60 С. После остывания раствора добавляют тиоанизол (85,2 г) с последующим добавлением метансульфоновой кислоты (65,9 г). Реакционную смесь нагревают при 80 С около 6 ч. Смесь охлаждают до 18 С и добавляют толуол (600 мл). Затем при перемешивании добавляют по каплям 6 М водный раствор гидроксида натрия(800 мл), поддерживая температуру реакционной смеси ниже 60 С. Разделяют образовавшиеся слои и органическую фазу промывают водой до тех пор, пока рН промывных вод достигнет 9 и затем промывают солевым раствором. Органический раствор охлаждают до 18 С, добавляют толуол (200 мл) и затем концентрированную соляную кислоту (42 мл). Полученную суспензию перегоняют при 47 С и давлении 180 мм Нg с целью азеотропного удаления воды. После удаления около 200 мл азеотропа толуол/вода смесь охлаждают до 40 С, позволяют дойти до атмосферного давления и затем охлаждают за 1 ч до 15 С. Выпавшее в осадок твердое вещество собирают вакуумной фильтрацией, промывают 60 мл толуола и сушат в вакууме, получая (R)-1(3-хлортиен-2-ил)-2-аминобутан в виде хлористоводородной соли с Т.пл. 137, 6 С. MS (EI)[(1-необязательно замещенный арил)- или (1 необязательно замещенный гетероарил)]-2 замещенного этил-2-амина, имеющего хиральный атом в положении 2, включающий взаимодействие 2-амино-2-замещенного этилового спирта, имеющего хиральный атом в положении 2, с [(необязательно замещенный арил)- или(тригалогенметил)сульфонил]-галогенидом или ангидридом в присутствии основания с образованием [(N-арилсульфонил)- или (N-тригалогенметилсульфонил)]-2-замещенного азиридина, имеющего хиральный центр в положении 2. 2. Способ по п.1, дополнительно включающий реакцию указанного азиридина с [(необязательно замещенный арил)- или (необязательно замещенный гетероарил)] литиевым соединением с образованием литиевой соли [(Nнеобязательно замещенный арил)-или (Nтригалогенметил)сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2 амина, имеющего хиральный центр в положении 2. 3. Способ по п.2, дополнительно включающий обработку указанной литиевой соли одной или более сильными кислотами в присутствии электрофильного акцептора. 4. Способ по п.1 получения соединения формулы гдеозначает хиральный атом углерода;R1 представляет необязательно замещенный арил или необязательно замещенный гетероарил; иR3 представляет необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил; включающий взаимодействие соединения формулыR2-SO2-R',где R' представляет галоген или OSO2R2; иR2 представляет необязательно замещенный арил или тригалогенметил; в присутствии основания с образованием соединения азиридина формулы 10 5. Способ по п.4, дополнительно включающий реакцию указанного соединения азиридина с соединением формулы Li-R1 с образованием соединения лития формулыR1 представляет необязательно замещенный арил или необязательно замещенный гетероарил;R2 представляет необязательно замещенный арил или тригалогенметил; иR3 представляет необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил. 6. Способ по п.5, дополнительно включающий обработку указанного соединения лития сильной кислотой или смесью сильных кислот в присутствии электрофильного акцептора. 7. Способ по п.4, где указанную реакцию проводят в апротонном органическом растворителе. 8. Способ по п.7, где указанным апротонным органическим растворителем является трет-бутилметиловый эфир. 9. Способ по п.4, где R2-SO2-R' представляет собой п-толуолсульфонилхлорид. 10. Способ по п.4, где указанную реакцию проводят при температуре от около 25 С до около 90 С. 11. Способ по п.4, где указанную реакцию проводят при температуре от около 25 С до около 40 С. 12. Способ по п.4, где указанное основание выбирают из группы, состоящей из водного раствора гидроксида щелочного металла, водного раствора карбоната щелочного металла и апротонного органического амина. 13. Способ по п.4, где указанным основанием является водный гидроксид натрия. 14. Способ по п.4, где R1 представляет необязательно замещенный гетероарил. 15. Способ по п.14, где R1 представляет 3 хлортиен-2-ил. 16. Способ по п.4, где R3 представляет алкил. 17. Способ по п.16, где R3 представляет этил. 18. Способ по п.5, где реакцию указанного соединения азиридина проводят в растворителе,выбранном из группы, включающей апротонный органический эфир, алифатический углеводород и ароматический углеводород. 19. Cпособ по п.18, где указанную реакцию указанного соединения азиридина проводят в трет-бутилметиловом эфире. 20. Способ по п.5, дополнительно включающий выделение указанного соединения лития в виде твердого вещества. 21. Способ по п.5, где указанную реакцию проводят при температуре от около -80 С до около 50 С. 22. Способ по п.21, где указанную реакцию проводят при температуре от около -40 С до около 50 С. 23. Способ по п.6, где указанная смесь сильных кислот содержит метансульфоновую кислоту и трифторуксусную кислоту. 24. Способ по п.6, где указанным электрофильным акцептором является тиоанизол. 25. Способ по п.6, где указанную обработку проводят при температуре от около 45 С и до, приблизительно, температуры кипения. 26.(Nтригалогенметилсульфонил)]-2-замещенный азиридин, имеющий хиральный центр в положении 2. 27. Соединение азиридина по п.26 формулы где R2 представляет необязательно замещенный арил или тригалогенметил; иR3 представляет необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необяза 12 тельно замещенный гетероарил или необязательно замещенный гетероаралкил. 28. Соединение азиридина по п.27, представляющее собой 1-п-толуолсульфонил-2-(R)этилазиридин. 29. Литиевая соль [(N-необязательно замещенный арил)- или (N-тригалогенметил) сульфонил]-1-[(необязательно замещенный арил)- или (необязательно замещенный гетероарил)]-2-замещенного алкил-2-амина, имеющего хиральный центр в положении 2. 30. Литиевая соль по п.29 формулыR1 представляет необязательно замещенный арил или необязательно замещенный гетероарил;R2 представляет необязательно замещенный арил или тригалогенметил; иR3 представляет необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необязательно замещенный гетероарил или необязательно замещенный гетероаралкил. 31. Соединение лития по п.30, представляющее собой литиевую соль (R)-1-(3-хлортиен 2-ил)-2-бутилтолуолсульфонамида.
МПК / Метки
МПК: A61P 9/12, C07C 303/38, C07D 203/24
Метки: 1-арил, 1-гетероарил-2-замещенных, стереоспецифический, синтез, этил-2-аминов, хиральных
Код ссылки
<a href="https://eas.patents.su/7-1364-stereospecificheskijj-sintez-hiralnyh-1-aril-i-1-geteroaril-2-zameshhennyh-etil-2-aminov.html" rel="bookmark" title="База патентов Евразийского Союза">Стереоспецифический синтез хиральных 1-арил- и 1-гетероарил-2-замещенных этил-2-аминов</a>
Предыдущий патент: Кристаллический фармацевтический продукт
Следующий патент: Сокращение времени цикла замедленного коксования
Случайный патент: Способ и система возврата утерянных вещей с использованием мобильной связи











