Жидкие составы фактор некроза опухоли – связывающих белков
Номер патента: 9079
Опубликовано: 26.10.2007
Авторы: Самаритани Фабрицио, Агостинетто Рита, Дель Рио Алессандра
Формула / Реферат
1. Стабильный фармацевтически приемлемый водный состав ФНО-связывающего белка, содержащий ФНО-связывающий белок, буфер и изотонический агент, где буфером является фосфатный буфер, и он сохраняет значение рН между 6 и 7.
2. Состав по п.1, где изотоническим агентом является хлорид натрия.
3. Состав по п.1 или 2, где изотоничность обеспечивается маннитом.
4. Состав по одному из предшествующих пунктов, где ФНО-связывающим белком является ТВР-1.
5. Состав по одному из предшествующих пунктов, где ФНО-связывающим белком является ТВР-2.
6. Состав по одному из предшествующих пунктов, где концентрация ФНО-связывающего белка составляет от 5 до 170 мг/мл.
7. Состав по одному из предшествующих пунктов, где концентрация буфера составляет от 5 до 150 мМ.
8. Состав по одному из предшествующих пунктов, где концентрация изотонического агента составляет от 5 до 50 мМ.
9. Состав по одному из предшествующих пунктов, включающий ТВР-1, 0,1М буфер на основе фосфата натрия с рН 6,5 и 0,025М хлорид натрия.
10. Способ приготовления жидкого фармацевтического состава по любому из пп.1-9, включающий разведение ФНО-связывающего белка раствором эксципиентов.
11. Форма выпуска жидкого фармацевтического состава по любому из пп.1-9, герметически закупоренная в стерильных условиях в емкости, пригодной для хранения до использования.
Текст
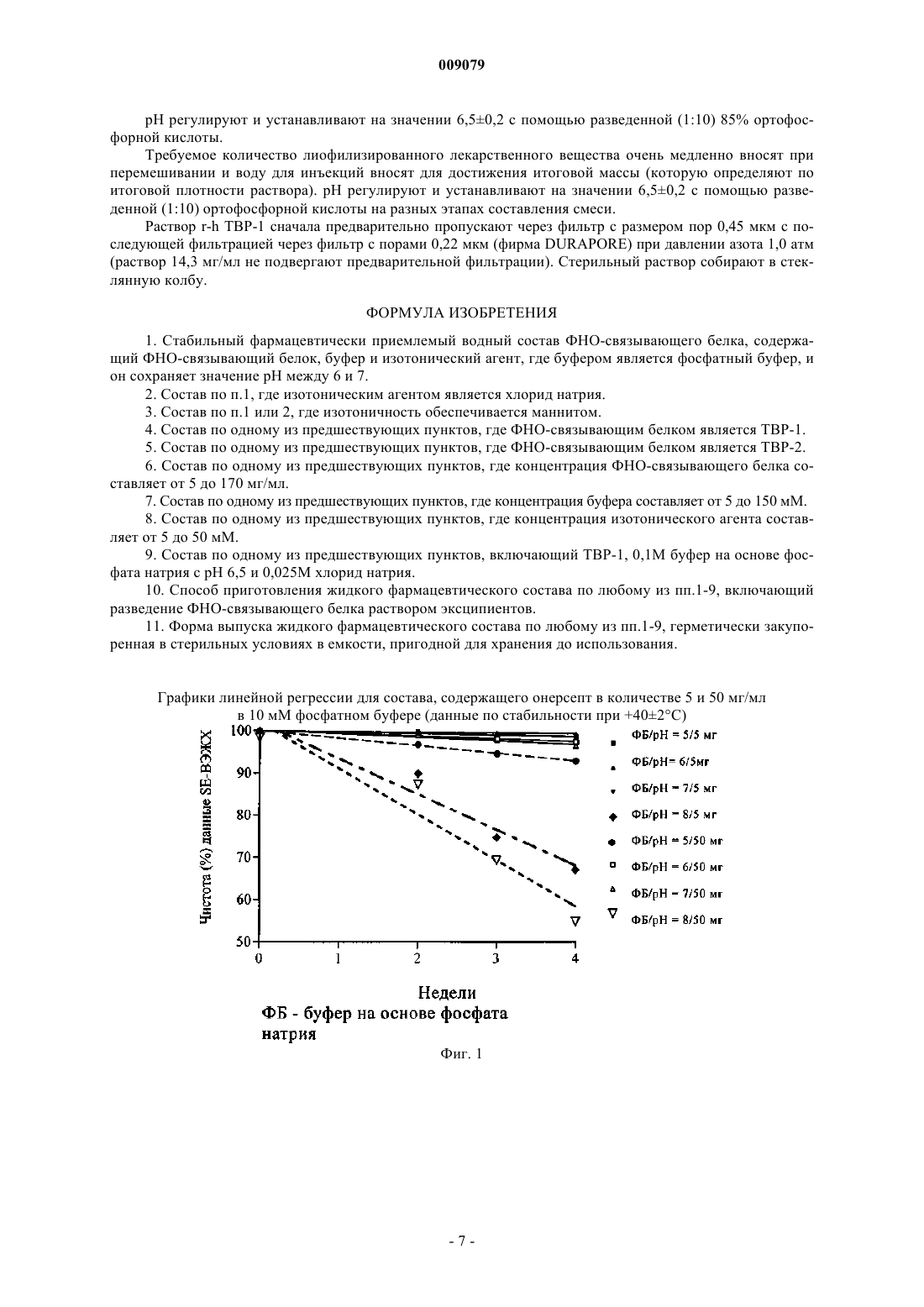
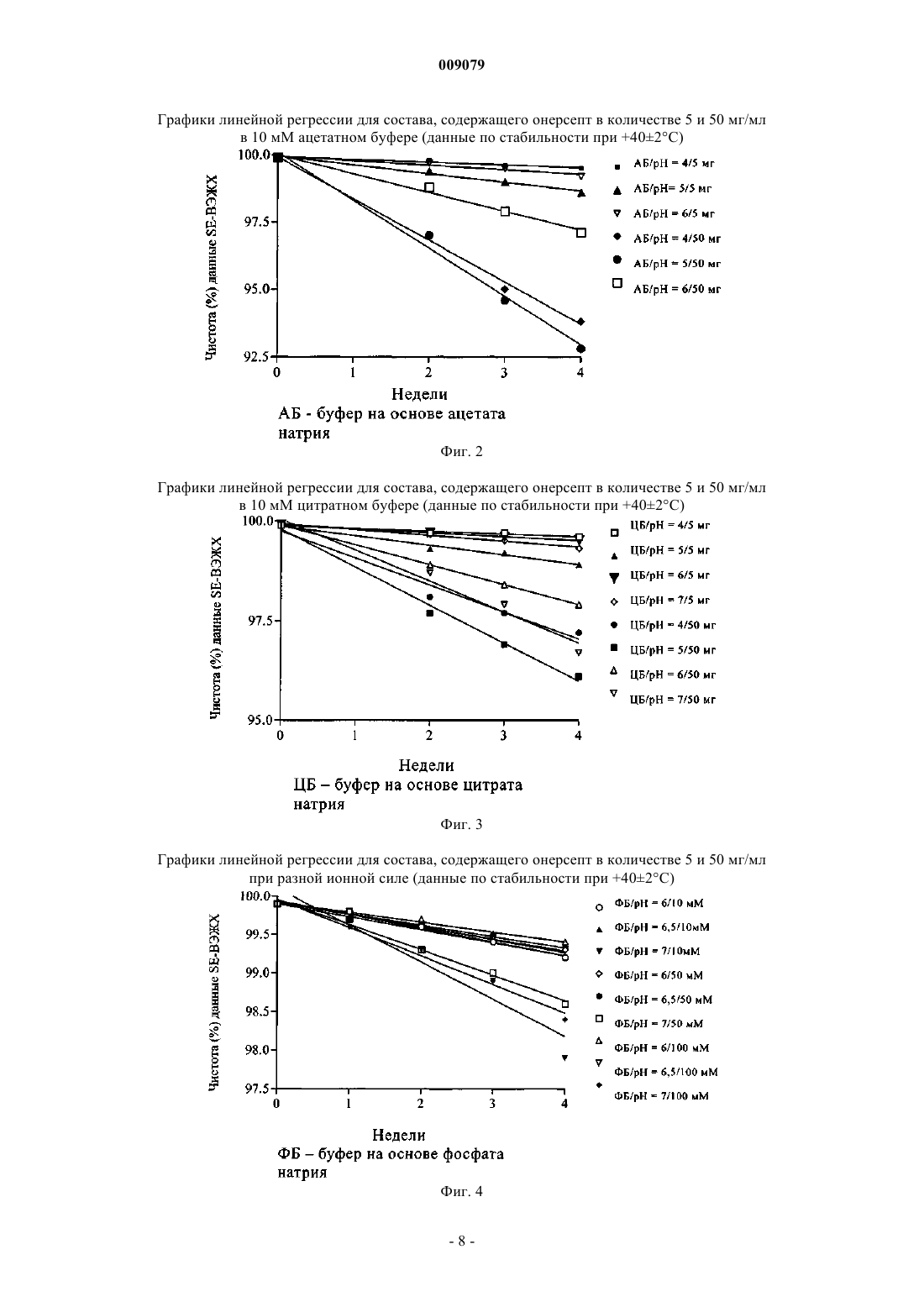
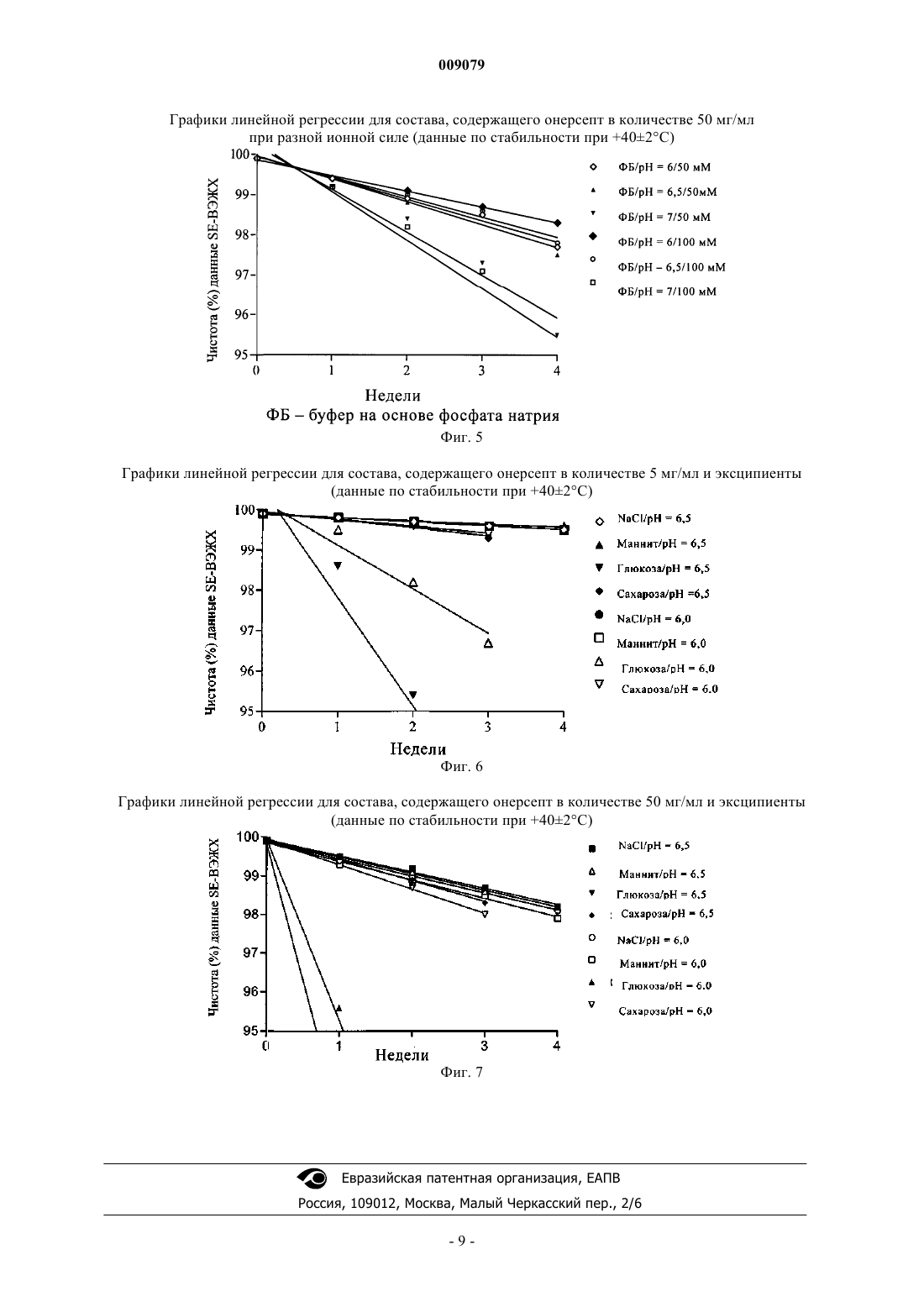
009079 Область техники, к которой относится изобретение Настоящее изобретение относится к жидким стабильным составам ФНО-связывающих белков. Предпосылки создания изобретения Фактор некроза опухолей-альфа (ФНО-) - мощный цитокин, который вызывает широкий спектр биологических реакций, опосредованных связыванием с рецептором на поверхности клетки. Stauber и др.(J. Biol. Chem. 263, 1988, cc. 19098-19104) выделили рецептор ФНО-альфа из линии клеток ретикулоклеточной саркомы человека. Hohmann и др. (J. Biol. Chem. 264, 1989, cc. 14927-14934) пришли к заключению, что имеется два разных белка, которые выступают в качестве основных рецепторов для ФНОальфа: один из них ассоциирован с миелоидными клетками, а другой - с эпителиальными клетками. Используя моноклональные антитела, Brockhaus и др. (Proc. Nat. Acad. Sci. 87, 1990, cc. 3127-3131) получили доказательство для 2 разных ФНО-связывающих белков, каждый из которых специфически и с высокой степенью афинности связывается с ФНО-альфа и ФНО-бета. Gray и др. (Proc. Nat. Acad. Sci. 87,1990, cc. 7380-7384) выделили кДНК одного из рецепторов. Они обнаружили, что она кодирует белок из 455 аминокислот, который подразделяется на внеклеточный домен из 171 остатка аминокислот и на цитоплазматический домен из 221 остатка аминокислот. Aggarwal и др. (Nature 318, 1985, cc. 665-667) показали, что факторы некроза опухолей альфа и бета инициируют свое воздействие на функции клетки путем связывания с общими рецепторами на поверхности клетки. Рецепторы ФНО-альфа и ФНО-бета имеют разные размеры и по-разному экспрессируются в разных клеточных линиях (см. Hohmann и др. 1989;Engelmann и др. в J. Biol. Chem. 265, 1990, cc. 1531-1536). ФНОР, иногда называемый также ФНОР 55, является меньшим из двух рецепторов. Последовательности нуклеиновых кислот кДНК обоих рецепторов были клонированы и определены (см. Loetscher и др., Cell 61, 1990, cc. 351-359; Nophar и др., EMBO J. 9, 1990, cc. 3269-3278; Schall и др., Cell 61, 1990,cc. 361-370; Smith и др., Science 248, 1990, cc. 1019-1023). Известно, что белки подвергаются деградации по нескольким метаболическим путям, особенно через дезамидирование, агрегацию, клипирование пептидного скелета и окисление. Многие из этих реакций могут быть существенно ослаблены в результате обезвоживания белка. Однако создание водного состава для лекарственных белков имеет преимущества, заключающиеся в элиминации ошибок при восстановлении, за счет чего повышается точность дозирования и упрощается клиническое использование продукта, что приводит к повышению контактности больного. Таким образом, целью настоящего изобретения было разработать водный состав ФНО-связывающих белков, который должным образом контролирует продукты деградации, остается стабильным при энергичном перемешивании (которое индуцирует агрегирование) и устойчив к микробной контаминации (что делает возможным комплексное использование или многодозовую упаковку). Описание изобретения Основным объектом настоящего изобретения, таким образом, является стабильный фармацевтически приемлемый водный состав ФНО-связывающего белка, включающий ФНО-связывающий белок человека, буфер и изотонический агент. Предпочтительно поддерживать величину рН раствора от 6 до 7 с помощью буфера. Буфер может быть любым фармацевтически приемлемым буфером, способным поддерживать такое значение рН. Предпочтительным является фосфатный буфер. Изотоническим агентом может быть любой фармацетически приемлемый агент, включая любую нейтральную соль или сахар. Например, это может быть хлористый натрий или маннит. Консервант может быть включен в состав для замедления микробного роста, что позволяет осуществлять комплексное использование или многодозовую упаковку ФНО-связывающего белка. К консервантам относятся фенол, бензиловый спирт, мета-крезол, метилпарабен, пропилпарабен, бензалкониум хлорид и бензетониум хлорид. Предпочтительными консервантами являются мета-крезол и бензиловый спирт. В случае необходимости жидкие составы могут быть также сублимационно или лиофильно высушены. Согласно настоящему изобретению понятие ФНО-связывающий белок означает любой белок,имеющий сродство с ФНО-альфа, или ФНО-бета и/или белок, включающий целиком или частично внеклеточный растворимый фрагмент белка, относящегося к семейству рецепторов ФНО. Ниже приводятся некоторые представители семейства рецепторов ФНО. Рецептор 1 фактора некроза опухоли (ФНО-Р 1), также называемый представителем 1 А суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 1 А), или рецептором фактора некроза опухоли альфа (ФНОАР), или ФНО-Р 55-кДа, или ФНОР 60-кДа (см. описание в разделе On line Mendelian Inheritancein men OMIM191190 на сайте http://www.ncbi.nlm.nih.gov/entrez/query.fcgidb=OMIM). Рецептор 2 фактора некроза опухоли (ФНО-Р 2), также называемый представителем 1 В суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 1 В), или рецептором фактора некроза опухоли бета(ФНОВР), или ФНО-Р 75-кДа, или ФНОР 80-кДа (см. описание в разделе OМIМ 191191). ОХ 40 антиген (ОХ 40), также называемый представителем 4 суперсемейства рецепторов фактора(TXGP1L), или активируемым в лимфоцитах антигеном АСТ 35 (АСТ 35), или CD134 (см. описание в разделе ОМIM600315). Рецептор CD40L (CD40), также называемый представителем 5 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 5), или поверхностным антигеном CD40 В-клеток, или CDw40, или Вр 50 (см. описание в базе данных по белкам Swiss-Prot,P25942). Рецептор FASL (FAS), также называемый представителем 6 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 6), или апоптоз-опосредованным поверхностным антигеном FAS, или Аро-1 антигеном, или CD95 (см. описание в базе данных по белкам Swiss-Prot,P25445). Ловушка-рецептор 3 (ЛР 3), также называемый представителем 6 В суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 6 В), или ловушкой-рецептором для лиганда FAS, или М 68 (см. описание в базе данных по белкам Swiss-Prot,P25445). Антиген CD27 (CD27), также называемый представителем 7 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 7), или активируемым в Т-клетках антигеном S152 (S152) (см. описание в разделе ОМIМ 602250). Активируемый в лимфоцитах антиген CD30 (CD 30), также называемый представителем 8 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 8) (см. описание в разделе OMIM153243). Индуцируемый активацией лимфоцитов (ILA), также называемый представителем 9 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 9) или CD137 (см. описание в разделе ОМIM602250). Рецептор клеточной гибели 4 (DR4), также называемый представителем 10 А суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 10 А), или рецептором 1 ФНО-связанного апоптоз-индуцирующего лиганда (TRAILR1), или АРО 2 (см. описание в разделе ОМIМ 6603611). Рецептор клеточной гибели 5 (DR5), также называемый представителем 10 В суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 10 В), или рецептором 2 ФНО-связанного апоптоз-индуцирующего лиганда (TRAILR2), или TRICK2 (см. описание в разделе ОМIМ 603612). Ловушка-рецептор 1 (ЛР 1), также называемый представителем 10 С суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 10 С), рецептором 3 ФНО-связанного апоптоз-индуцирующего лиганда (TRAILR3) или рецептором TRAIL без внутриклеточного домена (TRID) (см. описание в разделе ОМIМ 603613). Ловушка-рецептор 2 (ЛР 2), также называемый представителем 10D суперсемейства рецепторов фактора некроза опухоли (ФНО-PCC10D), рецептором 4 ФНО-связанного апоптоз-индуцирующего лиганда (TRAILR4) или рецептором TRAIL с процессированным доменом клеточной гибели (TRUNDD)(см. описание в разделе ОМIМ 603014). Рецепторный активатор NF-KAPPA-B (RANK), также называемый представителем 11 А суперсемейства рецепторов фактора некроза опухоли (ФНО-РСC11 А), или рецептором фактора дифференциации остеокластоцитов (ODFR), или PDB2, или TRANCER (см. описание в разделе ОМIM603499). Остеопрогерин (ОПГ), также называемый представителем 11 В суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 11 В) или фактором ингибирования остеокластоцитогенеза (см. описание в разделе ОМIМ 602643). Рецептор клеточной гибели 3 (DR3), также называемый представителем 12 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 12), или АРО 3, или лимфоцит-ассоциированным рецептором клеточной гибели (LARD) (см. описание в разделе ОМIМ 603366). Трансмембранный активатор и Caml посредник (TACI), также называемый представителем 13 В суперсемейства рецепторов фактора некроза опухоли (ФНО-РССПВ (см. описание в разделе ОМIМ 604907). Рецептор BAFF (BAFFR), также называемый представителем 13 С суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 13 С), или АРО 3, или рецептором фактора активирования В-клеток (см. описание в разделе ОМIМ 606269). Медиатор проникновения вируса герпеса в клетку (HVEM), также называемый представителем 14 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 14), или медиатором А проникновения вируса герпеса в клетку (HVEA), или TR2 (см. описание в разделе ОМIМ 602746). Рецептор фактора роста нервов (NGFR), также называемый представителем 16 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 16) или p75(NTR) (см. описание в разделе OMIM162010). Фактор созревания В-клеток (ВСМА), также называемый представителем 17 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 17) или ВСМ (см. описание в разделе OMIM 109545). Глюкокортикоид-индуцируемый ФНОР-связанный ген (GITR), также называемый представителем 18 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 18) или представителем семейства индуцируемой активации ФНОР (AITR) (см. описание в разделе ОМIМ 603905).TRADE, также называемый представителем 19 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 19), или индуктором токсичности и JNK, или TROY, или TAJ (см. описание в базе данных по белкам Swiss-Prot,Q9NS68).-2 009079 Рецептор Х-связанного эктодиплазина-А 2 (XEDAR), также называемый рецептором EDA-A2 (см. описание в базе данных по белкам Swiss-Prot,Q9HAV5). Рецептор клеточной гибели 6 (DR6), также называемый представителем 21 суперсемейства рецепторов фактора некроза опухоли (ФНО-РСС 21) (см. описание в разделе ОМIМ 605732). Согласно предпочтительному варианту осуществления настоящего изобретения ФНО-связывающий белок выбирается либо из рекомбинантного белка человека h-TBP-1 (рекомбинантного внеклеточного растворимого фрагмента ФНО-рецептора 1 человека, содержащего аминокислотную последовательность, соответствующую фрагменту из 20-180 аминокислот, описанную Nophar и др.), международное непатентованное название которого (МНН) онерсепт, либо из рекомбинантного белка человека hTBP-2 (рекомбинантного внеклеточного растворимого фрагмента ФНО-рецептора 2 человека, содержащего аминокислотную последовательность, соответствующую фрагменту из 23-257 аминокислот, описанную Smith и др.). Наиболее предпочтительным является рекомбинантный белок человека hTBP-1 (r-hTBP-1). Для всех других белков растворимый внеклеточный домен представлен в соответствующем списке Swiss-Prot. Для того, чтобы создать стабильный жидкий состав, оценивали влияние рН/буфера, ионной силы и эксципиентов. В приведенном ниже описании представлены эксперименты, выполненные с ТВР-1 (онерсептом). Примеры Материалы Лекарственное вещество онерсепт (поставляется фирмой Istituto di Ricerca Cesare Serono, Ardea,Италия). Ацетонитрил (фирма Merck). Ледяная уксусная кислота (фирма Merck). Сульфат аммония (фирма Merck). Лимонная кислота (фирма Merck).D(+)-маннит (фирма Merck). Оpтoфосфорная кислота (фирма Merck). Сахароза (фирма Merck). Азид натрия (фирма Merck). Хлорид натрия (фирма Merck). Гидроксид натрия (фирма Merck). Сульфат натрия безводный (фирма Merck). Натрий фосфорнокислый однозамещенный моногидрат (фирма Merck). Натрий фосфорнокислый двузамещенный дигидрат (фирма Merck). Трифторуксусная кислота (фирма Baker). Оборудование Системы ВЭЖХ (фирма Waters). Мерные пипетки (фирма Gilson). Штативы из нержавеющей стали (фирма Sartorius). рН-Метры (модель 713, фирма Metrohm). Осмометр (модель Osmomat 030-D, фирма Gonotec). Мембранные фильтры с диаметром пор 0,45 и 0,22 мкм (коды HVLP04700 и GWVP04700, фирмаMillipore). Колонка TSK gel G2000 SWXL (код 08540, фирма TosoHaas). Колонка TSK gel Phenyl-5PW стеклянная, внутренний диаметр 0,8 см, длина 7,5 см (код 08804,фирма TosoHaas). Материал внутренней упаковки Флаконы из боросиликатного стекла I типа (DIN 2R, фирма Nuova Ompi). Крышки из резины Flurotec (S2F452, D777-1, В 2-40, фирма Daikyo Seiko). Шприцы из боросиликатного стекла I типа (корпусы шприцов HYPAK SCF с фиксированными иглами и SCF защитными колпачками для игл, объемом 1,0 мл W 7974 серые, фирма Becton Dickinson). Крышки из резины Flurotec, 1 мл-1 BG B2-40c FLT 4023/50 г (фирма Daykio). Бромбутиловые крышки (HYPAK SCF фиксирующие крышки - BSCF объемом 1,0 мл 4023/50 серые(фирма Becton Dickinson). Аналитические исследования и методы Применяют следующие аналитические исследования и методы. Определение рН (потенциометрический). Визуальная оценка изменений (цвет, прозрачность/опалесценция, наличие частиц). Определение чистоты, оценка с помощью SE-ВЭЖХ (рабочая инструкция TF 08/01). Определение чистоты, оценка с помощью HI-ВЭЖХ (рабочая инструкция TF 09/01). Определение осмотического давления (криоскопическое измерение), только в нулевой точке.-3 009079 Биоисследование. В первую очередь, оценивают воздействие рН/буфера, ионной силы и эксципиентов. Также оценивают совместимость с крышками (с покрытием и без него). После выбора наилучших условий последующие три силы исследуют в предварительно наполненных шприцах: 10 мг/мл 50 мг/мл 60 мг/мл Исследование стабильности проводят после хранения на протяжении 3 месяцев при температуре+53 С; +252 С и +402 С, для чего проводят следующие исследования. Определение рН. Визуальная оценка изменений (цвет, прозрачность/опалесценция, наличие частиц). Исследование (SE-ВЭЖХ). Определение чистоты (SE-ВЭЖХ). Определение чистоты (НI-ВЭЖХ). Определение осмотического давления (в нулевой точке). Биоисследование. Влияние рН. Для оценки влияния рН/буфера растворы онерсепта в концентрации 5 и 50 мг/мл приготавливают разведением лекарственного вещества в буферных растворах при разных значениях рН: ацетате натрия при рН 4, 5 и 6; цитрате натрия при рН 4, 5, 6 и 7; фосфате натрия при рН 5, 6, 7 и 8. Растворами (примерно 20 мл/партию) наполняют стеклянные флаконы объемом 3 мл (по 1 мл), накрывают крышками, закупоривают, хранят при +53 С, +252 С и +402 С и анализируют раз в неделю на протяжении месяца. Результаты представлены в виде графиков на фиг. 1, 2, 3 и в табл. 1. Таблица 1 Онерсепт представлен в составе в количестве 5 и 50 мг/мл в 10 мМ буферах (снижение чистоты определяют с помощью SE-ВЭЖХ при +402 С). ФБ = буфер на основе фосфата натрия, ЦБ = буфер на основе цитрата натрия, АБ = буфер на основе ацетата натрия. Из приведенной выше таблицы и из графиков следует, что зависимость рН наблюдается при 5 и 50 мг/мл: незначительная потеря чистоты (в процентах) наблюдается при рН 6,0 и 7,0 для обеих концентраций. Цитратный и ацетатный буферы при pН 4,0 также оказывают положительное воздействие на общее содержание, хотя при рН 8,0 в фосфатном буфере наблюдают быстрое разрушение. После месяца хранения при +402 С не наблюдают окисления при анализе с помощью HI-ВЭЖХ или изменения рН. Действие ионной силы. С целью проверить действие разных ионных сил растворы онерсепта, содержащие 5 и 50 мг/мл,приготавливают в фосфатном буфере с тремя различными молярными концентрациями (10, 50 и 100 мМ) при рН 6,0, 6,5 и 7,0 каждый. Растворами (примерно 20 мл/партию) наполняют стеклянные флаконы объемом 3 мл (по 1 мл), накрывают крышками, закупоривают, хранят при +53 С, +252 С и +402 С и анализируют раз в неделю на протяжении месяца. Результаты показаны в виде графиков на фиг. 4, 5 и представлены в табл. 2.-4 009079 Таблица 2 Онерсепт представлен в составе в количестве 5 и 50 мг/мл при разной ионной силе (снижение чистоты определяют с помощью SE-ВЭЖХ при +402 С). Из графиков и приведенной выше таблицы следует, что степень агрегации не зависит от концентрации буфера: рН 7,0 имеет отрицательное воздействие на чистоту (%) при каждой концентрации буфера,хотя небольшая потеря наблюдается как при рН 6,0, так и при рН 6,5. После месяца хранения при+402 С не наблюдают окисления при анализе с помощью HI-ВЭЖХ или изменения рН. Действие других эксципиентов (стабилизаторов). С целью проверить действие разных эксципиентов растворы онерсепта, содержащие 5 и 50 мг/мл,приготавливают в 40 мМ фосфатном буфере при рН 6,0 и 6,5 и доводят до изотоничности с помощью хлорида натрия, маннита, глюкозы и сахарозы. Растворами (примерно 20 мл/партию) наполняют стеклянные флаконы объемом 3 мл (по 1 мл), накрывают крышками, закупоривают, хранят при +53 С,+252 С и +402 С и анализируют раз в неделю на протяжении месяца. Результаты показаны в виде графиков на фиг. 6, 7 и в табл. 3. Таблица 3 Онерсепт представлен в составе в количестве 5 и 50 мг/мл с эксципиентами (снижение чистоты определяют с помощью SE-ВЭЖХ при +402 С). Как показано на графиках и в таблице выше, хлорид натрия и маннит действуют одинаково, выступая в качестве изотонических агентов. Поэтому выбирают хлорид натрия, который и так уже присутствует в растворе лекарственного вещества. Кроме того, отсутствует сдвиг значения рН после 1 месяца хранения при +402 С, несмотря на то, что наблюдают модифицированный образец на хроматографическом профиле при проведении HI-ВЭЖХ для составов онерсепта, содержащих глюкозу и сахарозу в качестве-5 009079 стабилизаторов. Из всех этих результатов следует неожиданное заключение о том, что наиболее стабильными жидкими составами являются те эксципиенты, которые обычно используются в качестве стабилизаторов. Таким образом, наиболее стабильными составами являются те, которые содержат только подходящий буфер для разведения действующего вещества и изотонический агент. В этих условиях диапазон значений рН, пригодный для хорошей стабилизации, составляет от 6,0 до 7, предпочтительно от 6 до 6,5. Изотоничность может быть получена внесением требуемых количеств хлорида натрия или маннита, предпочтительно хлорида натрия. Кроме того, аналогичные эксперименты показывают практически такие же результаты по стабильности ТВР-1 до 170 мг/м, а также ТВР-2. Примеры фармацевтического изготовления Материалы Лекарственное вещество r-h ТВР-1; хлорид натрия (фирма Merck); натрий фосфорнокислый двузамещенный дигидрат (Фирма Merck); натрий фосфорнокислый однозамещенный моногидрат (фирмаMerck); opтo-фосфорная кислота 85% (фирма Merck); вода для инъекций. Контейнер/упаковка Первичный контейнер является стеклянным шприцом с иглой из нержавеющей стали и резиновым поршнем. Он состоит из следующего. Шприц. Описание:SCF объем 1,0 мл W7974 серый (фирма Becton Dickinson). Материалы, композиция: шприц: боросиликатное стекло типа I; игла: сталь; смазывающее вещество: DC360, силиконовое масло-диметикон; колпачок для иглы: эластомер. Фиксирующая пробка. Описание:HYPAK SCF фиксирующая пробка; BSCF объем 1,0 mL 4023/50 серый (фирма Becton Dickinson). Материалы, композиция: эластомер: бромбутил, инертный минерал, нетрадиционная отверждающаяся система; смазывающее вещество: DC360, силиконовое масло-диметикон. Пример приготовления растворов r-h ТВР-1 в 0,1 М буфере на основе фосфата натрия, рН 6,5; хлорид натрия 0,025 М.A) Раствор r-h ТВР-1 в концентрации 14,3 мг/мл. Для приготовления 1 л партии конечного продукта используют следующие количества.r-h ТВР-1 14,3 г Хлорид натрия 1,46 г Натрий фосфорнокислый двузамещенный дигидрат 10,5 г Натрий фосфорнокислый однозамещенный моногидрат 5,68 г Б) Раствор r-h ТВР-1 в концентрации 71,4 мг/мл. Для приготовления 1 л партии конечного продукта используют следующие количества.r-h ТВР-1 71,4 г Хлорид натрия 1,46 г Натрий фосфорнокислый двузамещенный дигидрат 10,5 г Натрий фосфорнокислый однозамещенный моногидрат 5,68 гB) Раствор r-h ТВР-1 в концентрации 142,9 мг/мл. Для приготовления 1 л партии конечного продукта используют следующие количества.r-h ТВР-1 142,9 г Хлорид натрия 1,46 г Натрий фосфорнокислый двузамещенный дигидрат 10,5 г Натрий фосфорнокислый однозамещенный моногидрат 5,68 г Способ приготовления. Жидкое лекарственное вещество, содержащее r-h ТВР-1, лиофилизируют и полученный порошок собирают для титрования. Необходимые количества хлорида натрия, фосфорнокислого натрия двузамещенного дигидрата и фосфорнокислого натрия однозамещенного моногидрата растворяют примерно в 800 г воды для инъекций. Их количества определяют исходя из количества солей, поступающих от лиофилизированного лекарственного вещества.-6 009079 рН регулируют и устанавливают на значении 6,50,2 с помощью разведенной (1:10) 85% ортофосфорной кислоты. Требуемое количество лиофилизированного лекарственного вещества очень медленно вносят при перемешивании и воду для инъекций вносят для достижения итоговой массы (которую определяют по итоговой плотности раствора). рН регулируют и устанавливают на значении 6,50,2 с помощью разведенной (1:10) ортофосфорной кислоты на разных этапах составления смеси. Раствор r-h TBP-1 сначала предварительно пропускают через фильтр с размером пор 0,45 мкм с последующей фильтрацией через фильтр с порами 0,22 мкм (фирма DURAPORE) при давлении азота 1,0 атм(раствор 14,3 мг/мл не подвергают предварительной фильтрации). Стерильный раствор собирают в стеклянную колбу. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Стабильный фармацевтически приемлемый водный состав ФНО-связывающего белка, содержащий ФНО-связывающий белок, буфер и изотонический агент, где буфером является фосфатный буфер, и он сохраняет значение рН между 6 и 7. 2. Состав по п.1, где изотоническим агентом является хлорид натрия. 3. Состав по п.1 или 2, где изотоничность обеспечивается маннитом. 4. Состав по одному из предшествующих пунктов, где ФНО-связывающим белком является ТВР-1. 5. Состав по одному из предшествующих пунктов, где ФНО-связывающим белком является ТВР-2. 6. Состав по одному из предшествующих пунктов, где концентрация ФНО-связывающего белка составляет от 5 до 170 мг/мл. 7. Состав по одному из предшествующих пунктов, где концентрация буфера составляет от 5 до 150 мМ. 8. Состав по одному из предшествующих пунктов, где концентрация изотонического агента составляет от 5 до 50 мМ. 9. Состав по одному из предшествующих пунктов, включающий ТВР-1, 0,1 М буфер на основе фосфата натрия с рН 6,5 и 0,025 М хлорид натрия. 10. Способ приготовления жидкого фармацевтического состава по любому из пп.1-9, включающий разведение ФНО-связывающего белка раствором эксципиентов. 11. Форма выпуска жидкого фармацевтического состава по любому из пп.1-9, герметически закупоренная в стерильных условиях в емкости, пригодной для хранения до использования. Графики линейной регрессии для состава, содержащего онерсепт в количестве 5 и 50 мг/мл в 10 мМ фосфатном буфере (данные по стабильности при +402 С)-7 009079 Графики линейной регрессии для состава, содержащего онерсепт в количестве 5 и 50 мг/мл в 10 мМ ацетатном буфере (данные по стабильности при +402 С) Фиг. 2 Графики линейной регрессии для состава, содержащего онерсепт в количестве 5 и 50 мг/мл в 10 мМ цитратном буфере (данные по стабильности при +402 С) Фиг. 3 Графики линейной регрессии для состава, содержащего онерсепт в количестве 5 и 50 мг/мл при разной ионной силе (данные по стабильности при +402 С)-8 009079 Графики линейной регрессии для состава, содержащего онерсепт в количестве 50 мг/мл при разной ионной силе (данные по стабильности при +402 С) Фиг. 5 Графики линейной регрессии для состава, содержащего онерсепт в количестве 5 мг/мл и эксципиенты(данные по стабильности при +402 С) Фиг. 6 Графики линейной регрессии для состава, содержащего онерсепт в количестве 50 мг/мл и эксципиенты(данные по стабильности при +402 С)
МПК / Метки
МПК: A61K 47/02, A61K 38/16
Метки: некроза, связывающих, фактор, жидкие, составы, белков, опухоли
Код ссылки
<a href="https://eas.patents.su/10-9079-zhidkie-sostavy-faktor-nekroza-opuholi-svyazyvayushhih-belkov.html" rel="bookmark" title="База патентов Евразийского Союза">Жидкие составы фактор некроза опухоли – связывающих белков</a>
Предыдущий патент: Замещенные производные 1-пиперидин-4-ил-4-пирролидин-3-илпиперазина и их применение в качестве антагонистов нейрокининов
Следующий патент: Композиции с микрочастицами бупренорфина для инъекций и их применение
Случайный патент: Водный состав с противокомкующими и водоотталкивающими свойствами