Фармацевтическая композиция для лечения диабетической невропатии
Формула / Реферат
1. Применение цитидин-5'-дифосфохолина или его фармацевтически приемлемой соли для получения фармацевтического средства для профилактики или лечения диабетической невропатии.
2. Применение по п.1, где диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов.
3. Применение по п.1, где диабетическая невропатия выбрана из периферической невропатии и семейной вегетативной дисфункции.
4. Применение по любому из пп.1-3, где фармацевтическое средство для профилактики или лечения получено в виде дозированной формы для перорального введения.
Текст
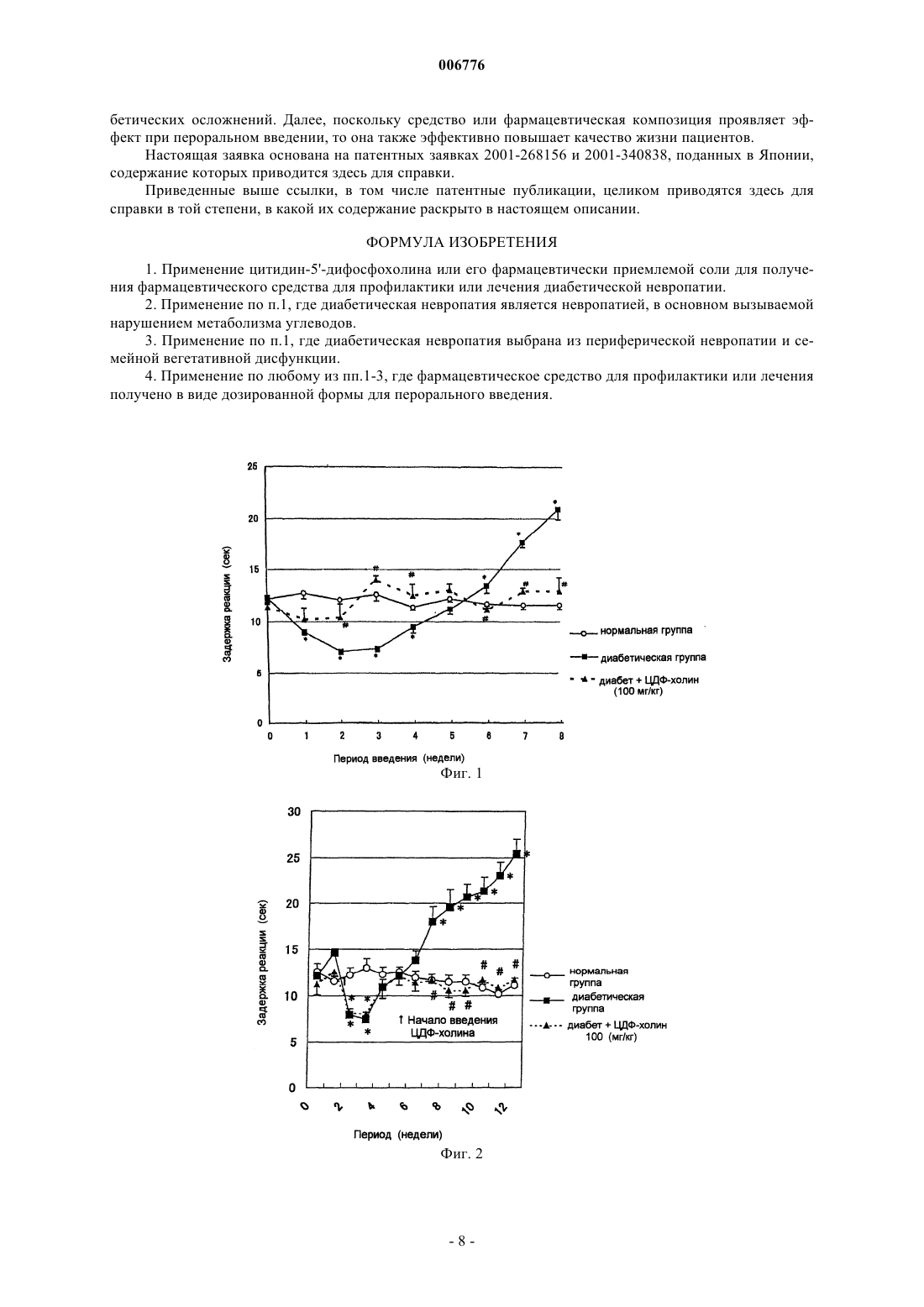
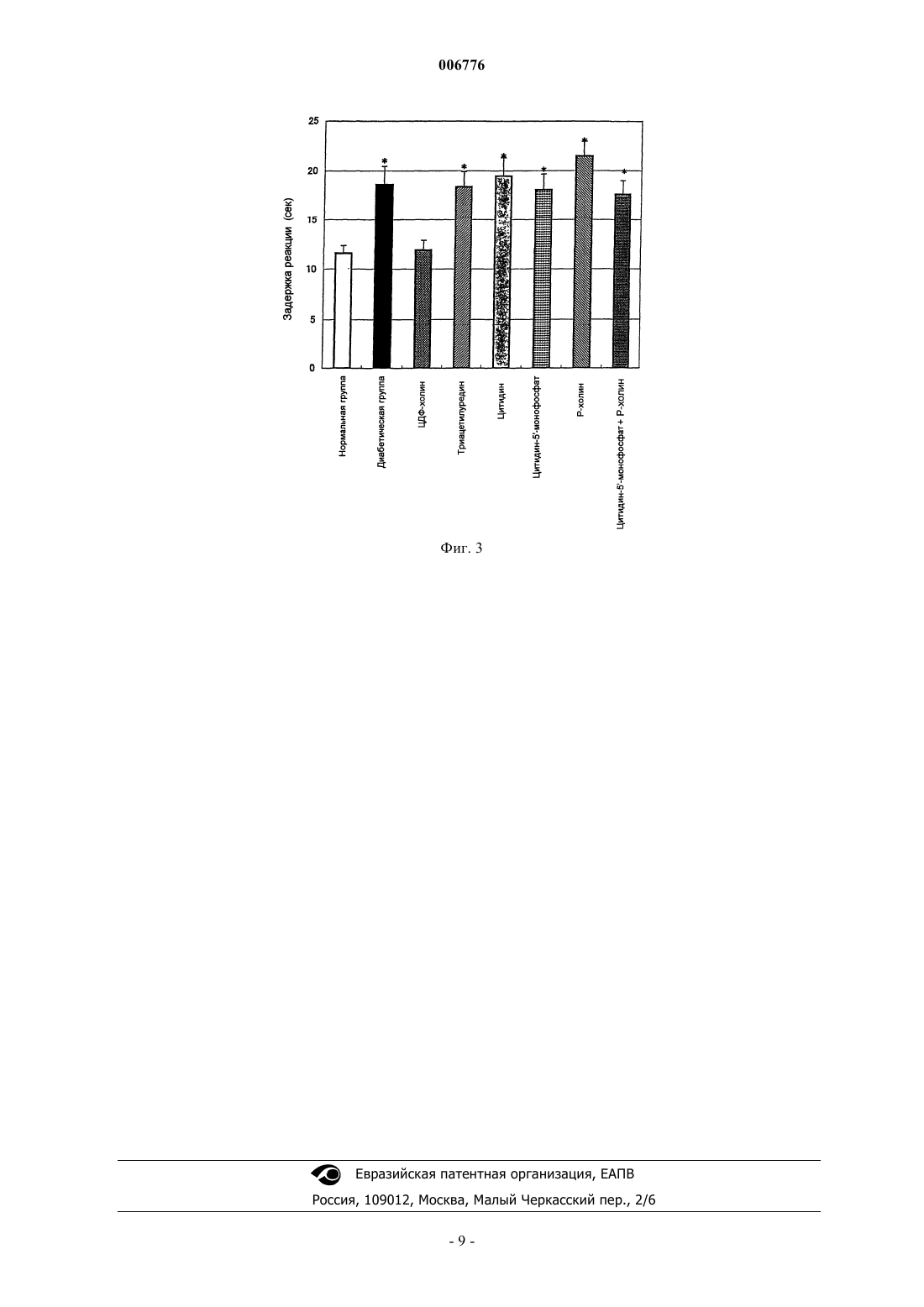
006776 техники, к которой относится изобретение Настоящее изобретение относится к средству для профилактики или лечения диабетической невропатии, которое содержит цитидин-5'-дифосфохолин (ЦДФ-холин, CDP-cholin) в виде активного ингредиента, к способу профилактики или лечения указанного заболевания, который заключается во введении эффективного количества ЦДФ-холина, к использованию ЦДФ-холина для приготовления фармацевтического средства для профилактики или лечения указанного заболевания и к фармацевтической композиции для профилактики или лечения указанного заболевания, которая содержит эффективное количество ЦДФ-холина и фармацевтически приемлемый носитель. Предпосылки изобретения В настоящее время лечение диабета является симптоматическим и основано на введении инсулина или гипогликемических средств. Однако долговременное регулирование содержания сахара в крови является сложным, не говоря уже о полном излечении диабета, и в случае продолжения болезни в течение длительного периода времени она индуцирует разнообразные осложнения. Из этих осложнений общее болезненное состояние диабетической периферической невропатии представляет собой полиневропатию,билатерально симметричную и доминантную от сенсорного нерва. В случае проявления острых симптомов наблюдается возбуждение нервов, такое как сенсорная аномалия, аллодиния (ощущение боли при легком прикосновении к поверхности тела) и т.п., а при хронических симптомах наблюдается пониженное восприятие (онемение конечностей, ощущение холода и т.п.), боль и т.п. Кроме того, у больных диабетом, страдающих полиневропатией, в основном развивается диабетическая семейная вегетативная дисфункция, и, таким образом, каждый орган, контролируемый пучком вегетативных нервных волокон,оказывается под угрозой аномалии, и наблюдаются аномальные движения кишечника, такие как запор и понос, импотенция, ортостатическая гипотензия, дисгидроз, замедленное опорожнение желудка и т.п. В применении к диабетической невропатии, проявляющей подобные разносторонние симптомы,был разрешен препарат эпалрестат (производится компанией Ono Pharmaceutical Co., Ltd.), который является ингибитором альдозоредуктазы и используется только в Японии. Однако были отмечены многочисленные проблемы, связанные с эффективностью и побочными действиями этого лекарственного средства [The Informed Prescriber, vol. 11, pages 122 and 125, December (1996)]. Кроме того, гидрохлорид мексилетина (производится компанией Nippon Boehringer Ingelheim Co., Ltd), который использовался в качестве терапевтического лекарства в случае тахиаритмии (желудочковой), был дополнительно разрешен и применялся благодаря своей эффективности и улучшению субъективных симптомов (спонтанная боль, онемение) диабетической невропатии. Однако его спонтанная скорость снижения боли не превышает 50%, как было установлено для фазы III - при проведении контролируемого клинического испытания, - и лекарственное средство нельзя считать вполне удовлетворительным в качестве терапевтического агента при диабетической невропатии. Главная задача современной терапии диабета заключается в предотвращении возникновения и развития диабетических осложнений, поэтому требуется разработка лекарственного средства для лечения диабетических осложнений, которое обладало бы высоким терапевтическим действием и высокой безопасностью. При данных обстоятельствах, в плане взаимосвязи между соединениями, относящимися к нуклеиновым кислотам, и невропатией, было отмечено, что триацетилуридин эффективен для периферической невропатии (пониженной чувствительности), индуцированной таксолом, который является антираковым средством [WO 00/11952]. Однако периферическая невропатия, индуцированная таксолом, являющимся противораковым средством, и диабетическая невропатия представляют собой совершенно разные заболевания с точки зрения вызывающих их причин. Кроме того, в указанной выше международной публикации не рассматривается и даже не предлагается к рассмотрению вопрос об эффективности триацетилуридина по отношению к невропатии, вызванной нарушением обмена углеводов, в частности, диабетической невропатии. Более того, в указанной выше международной публикации в качестве примера активного ингредиента приводится ЦДФ-холин, а не триацетилуридин. Однако ЦДФ-холин приведен в указанной выше международной публикации просто в качестве примера, без указания каких-либо конкретных данных, и практически отсутствует описание или информация, относящаяся к действию ЦДФ-холина на диабетическую невропатию. Описание изобретения Учитывая вышесказанное, авторы настоящего изобретения провели интенсивное изучение эффективности соединений, относящихся к нуклеиновым кислотам, в отношении диабетической невропатии и установили, что, в то время как ЦДФ-холин повсеместно разрешен для использования только для внутривенного введения и для применения при заболеваниях центральной нервной системы, таких как расстройство сознания, вызванное ранением или проведением операции на мозге, он при пероральном введении неожиданно оказывает значительное улучшающее воздействие на симптомы, наблюдаемые при диабетической периферической невропатии, такие как сенсорная аномалия и т.п., и на симптомы, являющиеся следствием диабетической вегетативной дисфункции, такие как пониженная проходимость желудочно-кишечного тракта и т.д., что и составляет предмет настоящего изобретения.-1 006776 Таким образом, в настоящем изобретении заявляется следующее:(1) Средство для профилактики или лечения диабетической невропатии, которое содержит в качестве активного ингредиента ЦДФ-холин или его фармацевтически приемлемую соль.(2) Средство для профилактики или лечения диабетической невропатии, как указано выше в (1), при этом диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов.(3) Средство для профилактики или лечения диабетической невропатии, как указано выше в (1), при этом диабетическая невропатия является периферической невропатией.(4) Средство для профилактики или лечения диабетической невропатии, как указано выше в (1), при этом диабетическая невропатия является семейной вегетативной дисфункцией.(5) Средство для профилактики или лечения диабетической невропатии, как указано выше в (1)-(4),которое приготовлено в виде дозированной формы для перорального введения.(6) Способ профилактики или лечения диабетической невропатии, который заключается во введении эффективного количества ЦДФ-холина или его фармацевтически приемлемой соли.(7) Способ, как указано выше в (6), при этом диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов.(8) Способ, как указано выше в (6), при этом диабетическая невропатия является периферической невропатией.(9) Способ по вышеуказанному (6), при этом диабетическая невропатия является семейной вегетативной дисфункцией.(10) Способ, как указано выше в (6)-(9), который представляет собой пероральное введение.(11) Применение ЦДФ-холина или его фармацевтически приемлемой соли для получения фармацевтического средства для профилактики или лечения диабетической невропатии.(12) Применение, как указано выше в (11), при этом диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов.(13) Применение, как указано выше в (11), при этом диабетическая невропатия является периферической невропатией.(14) Применение, как указано выше в (11), при этом диабетическая невропатия является семейной вегетативной дисфункцией.(15) Применение, как указано выше в (11)-(14), в котором фармацевтическое средство для профилактики или лечения приготовлено в виде дозированной формы для перорального введения.(16) Фармацевтическая композиция для профилактики или лечения диабетической невропатии, которая содержит эффективное количество ЦДФ-холина или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.(17) Фармацевтическая композиция, как указано выше в (16), при этом диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов.(18) Фармацевтическая композиция, как указано выше в (16), при этом диабетическая невропатия является периферической невропатией.(19) Фармацевтическая композиция, как указано выше в (16), при этом диабетическая невропатия является семейной вегетативной дисфункцией.(20) Фармацевтическая композиция, как указано выше в (16)-(19), которая приготовлена в виде дозированной формы для перорального введения.(21) Коммерческий набор, включающий в себя фармацевтическую композицию, как указано выше в(16)-(20), вместе с прилагающимся письменным руководством, при этом в письменном руководстве указывается, что фармацевтическая композиция может и должна использоваться для профилактики или лечения диабетической невропатии. Краткое описание чертежей На фиг. 1 показаны результаты действия ЦДФ-холина, касающиеся исследования (определение порога) термической болевой реакции, где по вертикальной оси указана величина задержки реакции (в сек),а по горизонтальной оси приведен период введения (в неделях) ЦДФ-холина. На фиг. 2 показаны результаты действия ЦДФ-холина, касающиеся исследования (определение порога) термической болевой реакции, где по вертикальной оси указана величина задержки реакции (в сек),а по горизонтальной оси указан период после индукции диабета. На фиг. 3 показаны результаты действия ЦДФ-холина и родственных соединений, касающиеся исследования (определение порога) термической болевой реакции, где по вертикальной оси указана величина задержки реакции (в сек). Наилучший вариант осуществления изобретения В настоящем изобретении заявлено средство для профилактики или лечения диабетической невропатии, которое содержит в качестве активного ингредиента ЦДФ-холин или его фармацевтически приемлемую соль.-2 006776 В настоящем изобретении заявлен также способ профилактики или лечения диабетической невропатии, который заключается во введении эффективного количества ЦДФ-холина или его фармацевтически приемлемой соли. Далее в настоящем изобретении заявлено применение ЦДФ-холина или его фармацевтически приемлемой соли для получения фармацевтического средства для профилактики или лечения диабетической невропатии. Наконец, в настоящем изобретении заявлена фармацевтическая композиция для профилактики или лечения диабетической невропатии, которая содержит эффективное количество ЦДФ-холина или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель, а также коммерческий набор, включающий в себя указанную фармацевтическую композицию и письменное руководство, которое касается фармацевтической композиции. ЦДФ-холин и его фармацевтически приемлемая соль эффективны для профилактики или лечения диабетической невропатии, в частности, невропатии, которая вызывается в основном нарушением метаболизма углеводов. Такая невропатия включает в себя периферическую невропатию и семейную вегетативную дисфункцию, при этом общее болезненное состояние периферической невропатии представляет собой билатерально симметричную и доминантную по сенсорному нерву полиневропатию. Классификация, название и т.п. для невропатии в настоящем описании даются в соответствии с The Merck Manual 17th Edition. В соответствии с настоящим изобретением можно, например, ингибировать возникновение как симптомов острого состояния (сенсорная аномалия, аллодиния и т.п.), так и симптомов хронического состояния (онемение конечностей, ощущение холода, боли и т.п.) или смягчить указанные симптомы после их возникновения путем введения больному диабетом ЦДФ-холина или его фармацевтически приемлемой соли до того, как разовьются симптомы, характерные для периферической невропатии, или после их возникновения. Более того, можно ингибировать возникновение симптомов, характерных для семейной вегетативной дисфункции, таких как аномальное движение кишечника, замедленное опорожнение желудка и т.п., вызванных ухудшением проходимости желудочно-кишечного тракта, или смягчить указанные симптомы после их возникновения, путем введения больному диабетом ЦДФ-холина до того,как разовьются симптомы, характерные для семейной вегетативной дисфункции, или после их возникновения. В качестве активного ингредиента фармацевтической композиции для профилактики или лечения диабетической невропатии в соответствии с настоящим изобретением ЦДФ-холин может быть в свободной форме или солевой форме. Примеры солевой формы включают в себя, не ограничиваясь ими, соли щелочных металлов, такие как соль лития, соль натрия, соль калия и т.п.; соли щелочноземельных металлов, такие как соль магния и т.п.; и т.д. Из них наиболее предпочтительна фармацевтически приемлемая соль. ЦДФ-холин и его фармацевтически приемлемая соль может находиться в виде гидрата или сольвата. В случае гидрата примером может быть гидрат или гидрат соли, в котором одна молекула ЦДФхолина или его соли удерживает 1-20 молекул воды, или с нею связано 1-20 молекул воды. Кроме того, в соответствии с настоящим изобретением, может быть использован ЦДФ-холин и его соль, его гидрат или гидрат его соли (далее для простоты обозначают как ЦДФ-холин) в форме кристаллов или в некристаллической форме. Подобный ЦДФ-холин является известным соединением и доступен в виде коммерческого продукта или же может быть получен известными методами (см. японскую заявку JP-A-6-31306, европейскую заявку ЕР 329627 или патент США 6057301 и т.п.). ЦДФ-холин эффективен для профилактики и лечения вышеуказанной диабетической невропатии путем любого из перорального введения, парентерального введения, интраректального введения и местного нанесения. Средство или фармацевтическая композиция для профилактики или лечения диабетической невропатии согласно изобретению могут быть получены путем смешения вышеуказанного ЦДФ-холина с обычным носителем для получения препаратов и путем превращения смеси в препарат. Содержание ЦДФ-холина в препарате или композиции можно приблизительно определить как составляющее не менее 0,01% (мас./мас.), преимущественно в интервале 1-80% (мас./мас.). В качестве носителя для приготовления препаратов используют вещества, которые обычно применяются в данной области техники и которые не взаимодействуют с ЦДФ-холином. Конкретные примеры включают в себя лактозу, глюкозу, маннит, декстрин, крахмал, сахарозу, алюмосиликат магния, синтетический алюмосиликат, кристаллическую целлюлозу, натриевую соль карбоксиметилцеллюлозы, гидроксипропилкрахмал, кальциевую соль карбоксиметилцеллюлозы, ионообменную смолу, метилцеллюлозу,желатин, гуммиарабик, гидроксипропилцеллюлозу, гидроксипропилцеллюлозу с малым количеством заместителей, гидроксипропилметилцеллюлозу, поливинилпирролидон, поливиниловый спирт, легкий диоксид кремния, стеарат магния, тальк, карбоксивиниловый полимер, оксид титана, сложный эфир жирной кислоты и сорбитана, лаурилсульфат натрия, глицерин, сложный эфир жирной кислоты и глицерина, очищенный ланолин, глицерированный желатин, полисорбат, макроголь, растительное масло, воск,-3 006776 жидкий парафин, белый вазелин, неионогенное поверхностно-активное вещество, пропиленгликоль, воду и т.п. Примером дозированной формы является таблетка, капсула, гранула, порошок, сироп, суспензия,мазь, гель, пластырь, инъекция, глазные капли и т.п. Указанные препараты могут быть получены в соответствии с известными методами с использованием вышеуказанного носителя для получения препаратов. В случае жидких препаратов они могут быть получены в форме, предусматривающей перед использованием растворение или суспендирование в воде или другой подходящей среде. Можно также известным образом нанести покрытие на таблетку или гранулу. Путь введения средства или фармацевтической композиции для профилактики или лечения диабетической невропатии в соответствии с настоящим изобретением может быть любым, и его выбирают, в зависимости от дозированной формы средства или фармацевтической композиции, из перорального введения, парентерального введения, интраректального введения и местного нанесения. Несмотря на то, что доза ЦДФ-холина, являющегося активным ингредиентом средства или фармацевтической композиции для профилактики или лечения диабетической невропатии, варьирует в зависимости от способа введения, симптомов и возраста пациента и т.п., она обычно составляет около 0,11000 мг/кг/день, предпочтительно около 0,5-500 мг/кг/день, и может вводиться в виде однократной дозы или в виде разделенной (на курс лечения) общей дозы. Средство или фармацевтическая композиция для профилактики или лечения диабетической невропатии в соответствии с настоящим изобретением может содержать другие ингредиенты, эффективные для лечения диабета, такие как пероральное гипогликемическое средство и т.п. Средство или фармацевтическая композиция для профилактики или лечения диабетической невропатии в соответствии с настоящим изобретением может вводиться в комбинации с гипогликемическим средством (например, инсулином, гликлазидом, глибенкламидом, толбутамидом, ацетогексамидом и т.д.). Примеры Настоящее изобретение подробно поясняется примерами и примерами составов, которые не следует рассматривать как ограничивающие настоящее изобретения. Пример 1. Действие, оказываемое ЦДФ-холином на диабетическую периферическую невропатию (1) Тестируемое соединение: мононатриевая соль цитидин-5'-дифосфохолина (ЦДФ-холин Na: выпускается компанией Yamasa Corporation). Тест: исследование (определение порога) термической болевой ответной реакции у больных диабетом мышей (in vivo). Этот тест проводят в соответствии с методикой, приведенной у Osawa and Kamei [Eur. J. Pharmacol.,372, 221-228 (1999)].(2) Введение ЦДФ-холина ЦДФ-холин Na растворяют в дистиллированной воде и вводят перорально в дозе 100 мг/кг один раз в день сразу же после индуцирования диабета.(3) Исследование (определение порога) термической болевой ответной реакции Исследование проводят с помощью теста на отдергивание хвоста мыши, а именно проводят фототермическую стимуляцию хвоста мыши и определяют задержку реакции, т.е. интервал времени, пока мышь не шевельнет хвостом, почувствовав тепло. Данные о том, как задержка реакции изменяется в диабетической группе по сравнению с нормальной группой, а также результаты при введении 100 мг/кг ЦДФ-холина в диабетической группе, приведены на фиг. 1. Как видно на этой фигуре, задержка реакции значительно сокращается на ранних стадиях болезни(от 1 до 4 недель) в диабетической группе по сравнению с нормальной группой, т.е. проявляется симптом(гипералгезия), сходный с аллодинией, наблюдаемой у больных диабетом людей. Значительное увеличение задержки реакции наблюдается, начиная с 6 недель, и также наблюдается снижение чувствительности сенсорного нерва, как и у больных диабетом людей. Когда 100 мг/кг ЦДФ-холина вводят диабетической группе, в которой с течением времени наблюдается противоречивая двухстадийная невропатия, то вышеуказанная невропатия практически полностью ингибируется, и задержка реакции сдвигается на тот же уровень, что и в нормальной группе. На фигуре результаты показывают величину среднего значениястандартная ошибка задержки реакции у 10 мышей, гдеуказывает на достоверное отличие (Р 0,05) от нормальной группы, ауказывает на достоверное отличие (Р 0,05) от диабетической группы. Результаты показывают, что пероральное введение ЦДФ-холина до возникновения симптомов, характерных для диабетической периферической невропатии, проявляющей многообразие симптомов, позволяет ингибировать возникновение этих симптомов.-4 006776 Когда доза ЦДФ-холина была установлена в размере 300 мг/кг, то был обнаружен аналогичный эффект. Ранее уже было подтверждено, что введение от 100 до 300 мг/кг ЦДФ-холина нормальной группе не оказывает эффекта на задержку реакции. Пример 2: Действие, оказываемое ЦДФ-холином на диабетическую периферическую невропатию(2) Тестируемое соединение: ЦДФ-холин Na. Тест: исследование (определение порога) термической болевой ответной реакции у больных диабетом мышей (in vivo) (см. метод Osawa and Kamei [Eur. J. Pharmacol., 372, 221-228 (1999)]).(2) Введение ЦДФ-холина ЦДФ-холин Na растворяют в дистиллированной воде и вводят перорально в дозе 100 мг/кг один раз в день, начиная с того дня, как пройдет 5 недель от введения стрептозотоцина.(3) Исследование (определение порога) термической болевой ответной реакции Исследование проводят с помощью теста на отдергивание хвоста мыши. Результаты приведены на фиг. 2. Как показано на этой фигуре, в том случае, когда введение ЦДФ-холина (100 мг/кг) диабетической группе было начато через 5 недель после введения стрептозотоцина, увеличение задержки реакции, а именно - понижение чувствительности сенсорных нервов, было практически полностью ингибировано, и задержка реакции сдвинулась на тот же уровень, что и у нормальной группы. На фигуре результаты показывают величину среднего значениястандартная ошибка задержки реакции у 12-13 мышей, гдеуказывает на достоверность отличия (Р 0,05) от нормальной группы, ауказывает на достоверность отличия (Р 0,05) от диабетической группы. Результаты показывают, что пероральное введение ЦДФ-холина даже после возникновения симптомов, характерных для диабетической невропатии, проявляющей многообразие симптомов, позволяет ингибировать эти симптомы. Хотя на сей раз данные не приводятся, аналогичный эффект наблюдается, когда доза ЦДФ-холина составляет 30 мг/кг. Пример 3. Действие, оказываемое ЦДФ-холином на диабетическую периферическую невропатию (3) Тестируемое соединение: ЦДФ-холин Na. Тест: исследование (определение порога) термической болевой ответной реакции у больных диабетом мышей (in vivo) (см. метод Osawa and Kamei [Eur. J. Pharmacol., 372, 221-228 (1999)]).(2) Введение ЦДФ-холина ЦДФ-холин Na растворяют в дистиллированной воде и вводят перорально в дозе 100 мг/кг один раз в день, начиная с того дня, когда прошло 8 недель от введения стрептозотоцина.(3) Исследование (определение порога) термической болевой ответной реакции Исследование проводят, используя тест на отдергивание хвоста. В результате по прошествии 8 недель после введения стрептозотоцина в диабетической группе задержка реакции со временем увеличивается, однако увеличение задержки реакции, или дальнейшее снижение чувствительности сенсорных нервов, не наблюдается в группе, которой вводят 100 мг/кг ЦДФ-холина, и значительное ингибирование эффекта увеличения задержки реакции наблюдается по прошествии 11 недель после введения стрептозотоцина. Пример 4. Действие, оказываемое ЦДФ-холином на диабетическую семейную вегетативную дисфункцию Тестируемое соединение: ЦДФ-холин Na. Тест: тест на транспортабельность порошка активированного угля в желудочно-кишечном тракте у больных диабетом мышей (in vivo).(1) Подготовка больных диабетом мышей Стрептозотоцин (200 мг/кг), растворенный в цитратном буфере (рН 4,5), вводят внутрибрюшинно мышам-самцам линии ICR (7-11 на группу, масса тела - приблизительно 20 г), чтобы индуцировать диабет.(2) Введение ЦДФ-холина ЦДФ-холин Na растворяют в дистиллированной воде и вводят перорально в дозе 100 мг/кг один раз в день сразу же после индуцирования диабета.(3) Тест на транспортабельность порошка активированного угля в желудочно-кишечном тракте-5 006776 Для проведения испытаний используют мышей, которым за 8 недель до проведения теста ввели стрептозотоцин. Готовят 5%-ную суспензию порошка активированного угля, используя 0,5%-ный водный раствор карбоксиметилцеллюлозы, и вводят перорально в количестве 0,1 мл/мышь животным, которым за день до проведения эксперимента перестают давать пищу. Через 30 мин вылущивают желудочнокишечный тракт от пилорического отдела желудка до прямой кишки и измеряют общую длину. Далее фиксируют положение порошка активированного угля после продвижения и измеряют расстояние продвижения от пилорического отдела желудка. Это значение пересчитывают в численное отношение, приняв общую длину от пилорического отдела желудка до прямой кишки за 100%, и полученные данные анализируют и используют для определения проходимости порошка активированного угля в желудочнокишечном тракте. Информация о том, как менялась проходимость желудочно-кишечного тракта для порошка активированного угля в диабетической группе по сравнению с нормальной группой, и результаты при введении 100 мг/кг ЦДФ-холина диабетической группе, представлена в табл. 1. В табл. 1 нормальная группа, диабетическая группа и диабетическая группа, которой вводили ЦДФ-холин, разделены на три категории менее чем 40%; не менее чем 40%, но не более 60%; и не менее 60% проходимости желудочнокишечного тракта для порошка активированного угля, и для каждой категории указано в процентах количество попаданий. Как следует из этой таблицы, ни у одной мыши в нормальной группе не выявлена менее чем 40%ная проходимость желудочно-кишечного тракта для порошка активированного угля, частота случаев,когда проходимость желудочно-кишечного тракта мышей для порошка активированного угля составляет не менее 40%, но менее 60%, превышает 90%. Напротив, у мышей в диабетической группе выявлен высокий процент (54,5%) мышей, у которых проходимость желудочно-кишечного тракта для порошка активированного угля составляет менее 40%, что указывает на явно выраженную деградацию проходимости желудочно-кишечного тракта для порошка активированного угля, по сравнению с нормальной группой. Функциональная деградация проходимости желудочно-кишечного тракта для порошка активированного угля, которая очень часто обнаруживается в диабетической группе, вызывается семейной вегетативной дисфункцией. В группе, которой для лечения этого заболевания давали 100 мг/кг ЦДФ-холина,ни у одной из мышей проходимость желудочно-кишечного тракта для порошка активированного угля не составляла менее 40%, что свидетельствует о полном ингибировании деградации проходимости желудочно-кишечного тракта для порошка активированного угля, очень часто наблюдаемой в диабетической группе. Из полученных результатов видно, что пероральное введение ЦДФ-холина позволяет ингибировать возникновение или уменьшить интенсивность симптомов, характерных для диабетической семейной вегетативной дисфункции, таких как деградация проходимости желудочно-кишечного тракта для порошка активированного угля, и т.п. Таблица 1 Пример 5. Действие, оказываемое родственными соединениями на диабетическую периферическую невропатию Тестируемое соединение 1: ЦДФ-холин Na Доза 100 мг/кг (1,959 х 10-4 моль/кг) Тестируемое соединение 2: триацетилуридин Доза 100 мг/кг (2,7 х 10-4 моль/кг) Тестируемое соединение 3: цитидин Доза 100 мг/кг (4,111 х 10-4 моль/кг) Тестируемое соединение 4: динатриевая соль цитидин-5'-монофосфата (5'-СМР 2Na) Доза 100 мг/кг (2,723 х 10-4 моль/кг) Тестируемое соединение 5: кальциевая соль хлорида фосфорилхолина (Р-холин) Доза 100 мг/кг (3,88 х 10-4 моль/кг) Тестируемое соединение 6: динатриевая соль цитидин-5'-монофосфата (5'-СМР 2Na) + кальциевая соль хлорида фосфорилхолина (Р-холин)-6 006776 Доза: 72 мг/кг (1,959 х 10-4 моль/кг) в виде 5'-СМР 2Na и 50,5 мг/кг (1,959 х 10-4 моль/кг) в виде Рхолина Тест: исследование (определение порога) термической болевой ответной реакции у больных диабетом мышей (in vivo) (см. метод Osawa and Kamei [Eur. J. Pharmacol., 372, 221-228 (1999)]).(2) Введение тестируемого соединения Тестируемое соединение растворяют или суспендируют в 0,5%-ном водном растворе карбоксиметилцеллюлозы и вводят перорально один раз в день, начиная с того дня, когда прошло 5 недель после введения стрептозотоцина.(3) Исследование (определение порога) термической болевой ответной реакции Исследование проводят с помощью теста на отдергивание хвоста мыши. В результате, в диабетической группе задержка реакции значительно возросла по прошествии 6 недель после введения стрептозотоцина и после проявления пониженной чувствительности сенсорного нерва, аналогичной той, которая наблюдается и у больных диабетом людей. В том случае, когда введение ЦДФ-холина (100 мг/кг) диабетической группе начинают по прошествии 5 недель после введения стрептозотоцина, увеличение задержки реакции, а именно понижение чувствительности сенсорных нервов, практически полностью ингибируется, и задержка реакции соответствует ее уровню в нормальной группе. Тем не менее, для группы других вводимых испытуемых соединений (включая триацетилуридин) наблюдается значительное увеличение задержки реакции, как и в диабетической группе, и ингибирующий эффект на пониженную чувствительность сенсорных нервов, который обеспечивается ЦДФ-холином, не обнаруживается. В связи с этим в качестве типичных данных на фиг. 3 приводятся значения, полученные по прошествии 7 недель после введения стрептозотоцина. На фигуре результаты показывают величину среднего значениястандартная ошибка задержки реакции у 12-13 мышей, гдеуказывает на достоверное отличие (Р 0,01) от нормальной группы. Было также подтверждено, что результаты, показывающие ту же тенденцию, что и для 7 недельного интервала, получают по прошествии 6 или 8 недель после введения стрептозотоцина. Сообщалось, что пероральное введение ЦДФ-холина приводит практически к тому же уровню биодоступности, что и при внутривенном введении [Methods Find. Exp. Clin. Pharmacol. 17, Suppl. В, 1-15(1995)], и в сочетании с приведенными выше результатами, показывающими отсутствие эффективности у родственных соединений, можно сделать вывод, что ЦДФ-холин сам является действующим началом. Пример препарата 1: таблетка ЦДФ-холин 30,0 мг Мелкокристаллическая целлюлоза 25,0 мг Лактоза 39,5 мг Крахмал 40,0 мг Тальк 5,0 мг Стеарат магния 0,5 мг Таблетки готовят обычным способом из приведенной выше композиции. Пример препарата 2: капсула ЦДФ-холин 30,0 мг Лактоза 40,0 мг Крахмал 15,0 мг Тальк 5,0 мг Капсулы готовят обычным способом из приведенной выше композиции. Пример препарата 3: инъекция ЦДФ-холин 30,0 мг Глюкоза 100,0 мг Для приготовления инъекции приведенную выше композицию растворяют в очищенной воде для инъекций. Промышленная применимость Средство или фармацевтическая композиция для профилактики или лечения диабетической невропатии согласно изобретению, содержащая ЦДФ-холин в качестве активного ингредиента, ингибирует возникновение симптомов, характерных для диабетической невропатии, таких как диабетическая периферическая невропатия и диабетическая семейная вегетативная дисфункция, и, кроме того, показывает потенциальное улучшающее воздействие даже после возникновения указанных симптомов и обладает повышенной безопасностью. Таким образом, средство или фармацевтическая композиция может использоваться для профилактики или лечения невропатии в качестве терапевтического лекарства против диа-7 006776 бетических осложнений. Далее, поскольку средство или фармацевтическая композиция проявляет эффект при пероральном введении, то она также эффективно повышает качество жизни пациентов. Настоящая заявка основана на патентных заявках 2001-268156 и 2001-340838, поданных в Японии,содержание которых приводится здесь для справки. Приведенные выше ссылки, в том числе патентные публикации, целиком приводятся здесь для справки в той степени, в какой их содержание раскрыто в настоящем описании. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение цитидин-5'-дифосфохолина или его фармацевтически приемлемой соли для получения фармацевтического средства для профилактики или лечения диабетической невропатии. 2. Применение по п.1, где диабетическая невропатия является невропатией, в основном вызываемой нарушением метаболизма углеводов. 3. Применение по п.1, где диабетическая невропатия выбрана из периферической невропатии и семейной вегетативной дисфункции. 4. Применение по любому из пп.1-3, где фармацевтическое средство для профилактики или лечения получено в виде дозированной формы для перорального введения.
МПК / Метки
МПК: C07H 19/10, A61P 25/00, A61K 31/7068
Метки: диабетической, невропатии, композиция, лечения, фармацевтическая
Код ссылки
<a href="https://eas.patents.su/10-6776-farmacevticheskaya-kompoziciya-dlya-lecheniya-diabeticheskojj-nevropatii.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция для лечения диабетической невропатии</a>
Предыдущий патент: Новые соединения 3-арил-2,5-дигидрокси-1,4-бензохинона, способ их получения и фармацевтические композиции, содержащие их
Следующий патент: Фармацевтические композиции адсорбатов аморфного лекарственного средства
Случайный патент: Композиции эндорибонуклеаз и способы их использования