Новые соединения карбамат и тиокарбамат подофиллотоксина, способ их получения и содержащие их фармацевтические композиции
Номер патента: 5200
Опубликовано: 30.12.2004
Авторы: Пьер Алан, Пфеффер Брюно, Моннере Клод, Бертунеск Эмманюэль, Хикман Джон, Атасси Ганем, Мересс Филипп, Ренар Пьер
Формула / Реферат
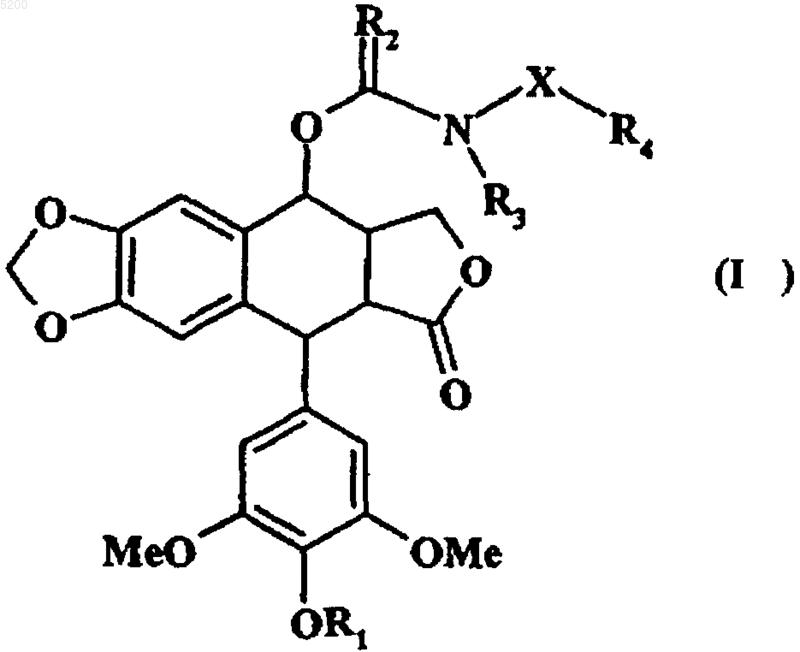
1. Соединения формулы (I)

в которой R1 представляет собой атом водорода,
R2 представляет собой атом кислорода,
R3 представляет собой атом водорода или линейную или разветвленную (C1-C6)алкильную группу,
X представляет собой линейную или разветвленную (C1-C6)алкиленовую группу,
R4 представляет собой группу, выбираемую из
амино, необязательно замещенного одной или двумя одинаковыми или различными группами, выбираемыми из линейного или разветвленного (C1-C6)алкила,
группы формулы -N(R3)-X1-OR5, в которой R3 имеет вышеуказанные значения, X1 представляет собой линейную или разветвленную (C1-C6)алкиленовую группу и R5 представляет собой атом водорода,
группы формулы -O-X1-OR5, в которой R5 и X1 имеют вышеуказанные значения,
их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием, причем изомеры следует понимать как обозначающие энантиомеры и диастереоизомеры.
2. Соединения формулы (I) по п.1, отличающиеся тем, что X представляет собой линейную (C2-C4)алкиленовую группу, их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием.
3. Соединения формулы (I) по п.1, отличающиеся тем, что R4 представляет собой группу -N(R3)-X1-OR5 или -O-X1-OR5, в которых R3 представляет собой атом водорода, X1 представляет собой линейную (C2-C4)алкиленовую цепочку, а R5 представляет собой атом водорода, их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием.
4. Соединения формулы (I) по п.1, которые представляют собой
(5S,5aS,8aS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этил(метил)карбамат,
(5S,5aS,8aR,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этил(метил)карбамат,
(5S,5aS,8aS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 3-(диметиламино)пропилкарбамат,
(5S,5aS,8aS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(2-гидроксиэтокси)этилкарбамат,
(5S,5aS,8aS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-[(2-гидроксиэтил)амино]этилкарбамат,
(5S,5aS,8aS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5a,6,8,8a,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этилкарбамат,
и их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием.
5. Способ получения соединений формулы (I), отличающийся тем, что в качестве исходного продукта применяют соединение формулы (II)
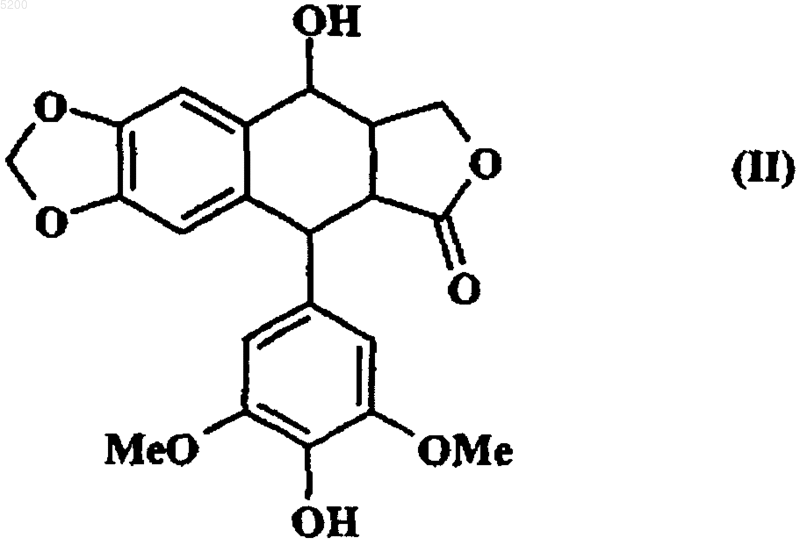
которое подвергают при основных условиях воздействию соединения формулы (V)
G-L (V),
в которой
G представляет собой традиционную защитную группу для гидроксифункций, а
L представляет собой традиционную в органической химии уходящую группу,
с получением соединений формулы (IV/B)
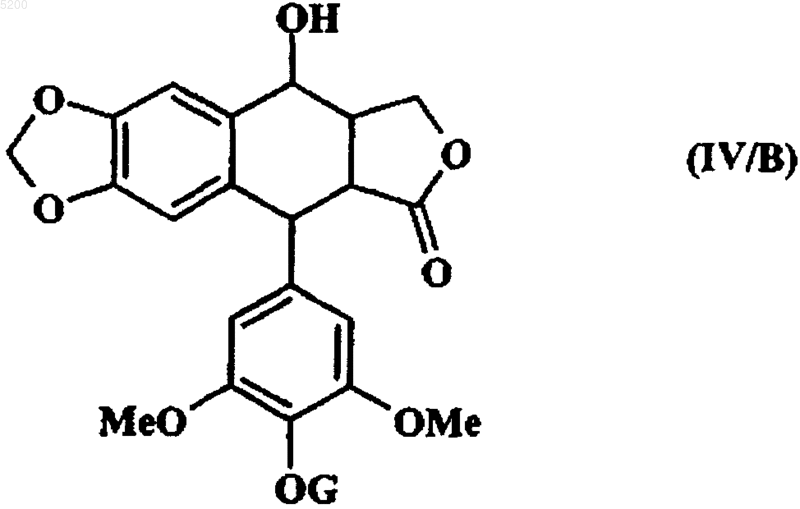
в которой G имеет вышеуказанные значения,
полученное соединение формулы (IV) обрабатывают в основной среде соединением формулы (VI)
Ph-O-C(R2)Cl (VI),
в которой Ph представляет собой необязательно замещенную фенильную группу, а
R2 представляет собой атом кислорода,
с получением соединений формулы (VII)
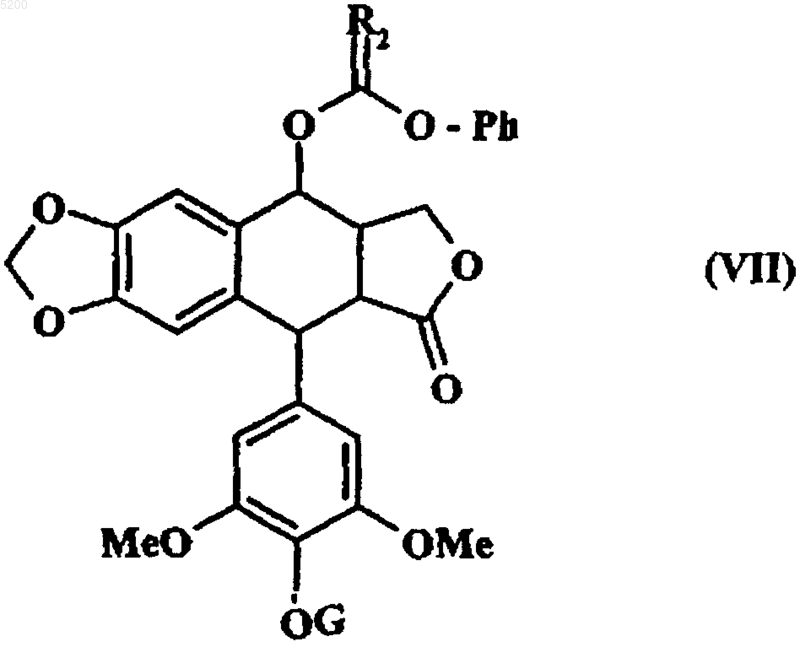
в которой G, Ph и R2 имеют вышеуказанные значения,
полученное соединение формулы (VII) подвергают взаимодействию в основной среде с соединением формулы (VIII)
R4-X-NH-R3 (VIII),
в котором R4, R3 и X имеют значения, указанные для формулы (I),
с получением соединения формулы (IX)
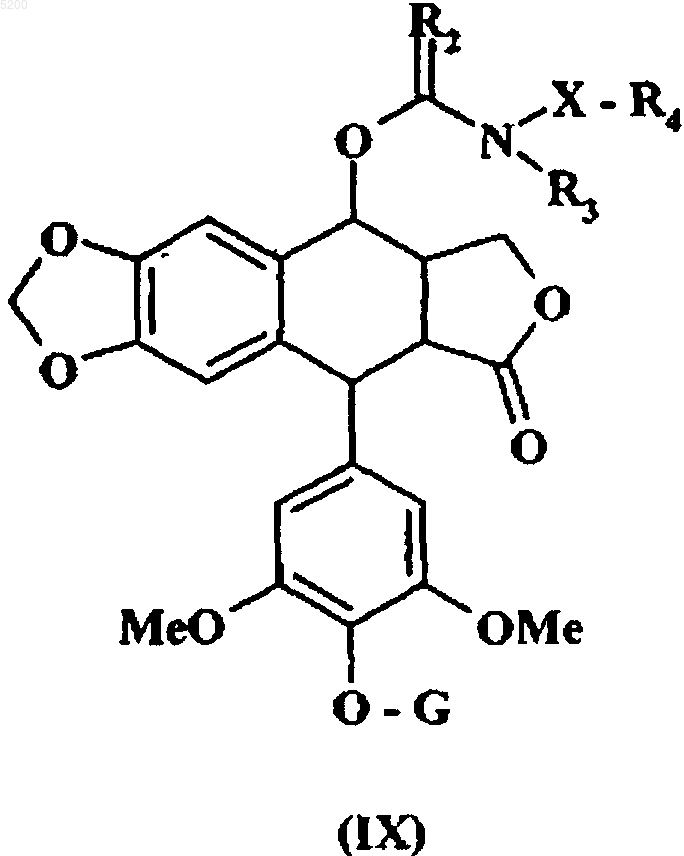
в которой G, R2, R3, R4 и X имеют вышеуказанные значения,
гидроксифункцию полученного соединения формулы (IX) депротектируют любым традиционным в органической химии способом с получением соединений формулы (I)
в которой R1, R2, R3, R4 и X имеют значения, указанные для формулы (I),
полученные соединения очищают в случае необходимости согласно традиционной методике очистки, при желании их можно разделять согласно традиционной методике разделения, и при желании переводят в их аддитивные соли с фармацевтически приемлемой кислотой или основанием.
6. Фармацевтические композиции, включающие в качестве активного ингредиента по меньшей мере одно соединение по любому из пп.1-4, отдельно или в сочетании с одним или более фармацевтически приемлемыми, инертными, нетоксичными эксципиентами или носителями.
7. Фармацевтические композиции по п.6, содержащие по меньшей мере один активный ингредиент по любому из пп.1-4, предназначенные для лечения рака.
Текст
1 Настоящее изобретение относится к новым соединениям карбамату и тиокарбамату подофиллотоксина, к способу их получения и к содержащим их фармацевтическим композициям. Соединения по изобретению представляют собой производные подофиллотоксина, природного лигнана, известного благодаря его применению при лечении рака. Другие синтетические производные, такие как этопозид и тенипозид, в настоящее время применяются в качестве химиотерапевтических агентов при лечении, в особенности, мелкоклеточного рака легких. Эти различные соединения действуют, ингибируя каталитическую активность топоизомеразы II. Были осуществлены различные модификации этих соединений, такие как модификации,описанные в патентных заявках JP 948782, WO 97/13776 и US 3,634,459. Однако требования,предъявляемые к противораковым терапевтическим средствам, вызывают необходимость постоянного развития новых противоопухолевых и цитотоксических агентов с целью получения лекарственных препаратов, которые одновременно являются более активными, более растворимыми и лучше переносятся. Дополнительно к тому факту, что эти соединения новы, они имеют неожиданную активность in vitro и invivo, которая превосходит наблюдавшуюся до этого. Соединения, открытые заявителем, соответственно, имеют свойства, которые делают их особенно полезными при лечении рака. Более конкретно, настоящее изобретение относится к соединениям формулы (I)R1 представляет собой атом водорода,R2 представляет собой атом кислорода,R3 представляет собой атом водорода или линейную или разветвленную (C1-С 6)алкильную группу,Х представляет собой линейную или разветвленную (С 1-С 6)алкиленовую группу,R4 представляет собой группу, выбираемую из амино, необязательно замещенного одной или двумя одинаковыми или различными группами, выбираемыми из линейного или разветвленного (С 1-С 6)алкила,группу формулы -N(R3)-X1-OR5, в которойR3 имеет вышеуказанные значения, X1 представляет собой линейную или разветвленную(С 1-С 6)алкиленовую группу и R5 представляет собой атом водорода, 005200 2 группу формулы -O-X1-OR5, в которой R5 и X1 имеют вышеуказанные значения,их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием,причем изомеры следует понимать как обозначающие энантиомеры и диастереоизомеры. Дополнительно были изучены соединения формулы (I)R1 представляет собой группу, выбираемую из водорода, линейного или разветвленного (С 1-С 6)алкила, арила, арил-(С 1-С 6)алкила, в котором алкильный остаток может быть линейным или разветвленным, гетероарила, гетероарил-(С 1-С 6)алкила, в котором алкильный остаток может быть линейным или разветвленным,линейного или разветвленного (С 1-С 6)алкоксикарбонила, арилоксикарбонила, арил-(С 1-С 6)алкоксикарбонила, в котором остаток алкокси может быть линейным или разветвленным, гетероциклоалкоксикарбонила, линейного или разветвленного (С 1-С 6)алкилсульфонила, арилсульфонила, арил-(С 1-С 6)алкилсульфонила, в котором алкильный остаток может быть линейным или разветвленным, и фосфоно,R2 представляет собой атом кислорода или серы,R3 представляет собой атом водорода, линейную или разветвленную (С 1-С 6)алкильную группу, циклоалкильную группу или арил-(С 1-С 6) алкильную группу, в которой алкильный остаток может быть линейным или разветвленным,Х представляет собой линейную или разветвленную (С 1-С 6)алкиленовую группу,R4 представляет собой группу, выбираемую из амино, необязательно замещенного одной или двумя одинаковыми или различными группами, выбираемыми из линейного или разветвленного (С 1-С 6)алкила, арила и арил-(С 1 С 6)алкила, в котором алкильный остаток может быть линейным или разветвленным,группу формулы -N(R3)-X1-OR5, в которойR3 имеет значения, указанные здесь ранее, X1 представляет собой линейную или разветвленную (С 1-С 6)алкиленовую группу и R5 представляет собой группу, выбираемую из водорода,линейного или разветвленного (С 1-С 6)алкила,арила и арил-(С 1-С 6 алкила, в котором алкильный остаток может быть линейным или разветвленным,группу формулы -N(R3)-Х 1-NR6R7, в которой R3 и X1 имеют значения, указанные здесь 3 ранее, и R6 и R7, которые могут быть одинаковыми или различными, каждый представляет собой группу, выбираемую из водорода, линейного или разветвленного (С 1-С 6)алкила, арила и арил-(С 1-С 6)алкила, в котором алкильный остаток может быть линейным или разветвленным,гидрокси,линейного или разветвленного (С 1-С 6)алкокси, арилокси,группу формулы -O-X1-OR5, в которой R5 и X1 имеют значения, указанные здесь ранее,и группу формулы -O-X1-NR6R7, в которойR6, R7 и X1 имеют значения, указанные здесь ранее,их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием,причем арил обозначает группу, выбираемую из фенила, бифенила, нафтила, дигидронафтила,тетрагидронафтила, инденила, инданила и бензолциклобутила, каждая их этих групп необязательно имеет один или более одинаковых или различных заместителей, выбираемых из галогена, гидрокси, линейного или разветвленного(С 1-С 6)алкокси, циано, нитро, амино, линейного или разветвленного (С 1-С 6)алкиламино, ди-(С 1 С 6)алкиламино, в которых каждый алкильный остаток может быть линейным или разветвленным, карбокси, линейным или разветвленным(С 1-С 6)алкоксикарбонилом, линейным или разветвленным (С 1-С 6)тригалоалкилом, линейным или разветвленным (С 1-С 6)алкилкарбонилокси,линейным или разветвленным (С 1-С 6)алкилкарбонилом, и аминокарбонилом, в котором аминоостаток необязательно замещен одной или двумя одинаковыми или различными линейной или разветвленной (С 1-С 6)алкильными группами,гетероарил обозначает ароматическую моноциклическую группу, ароматическую бициклическую группу или бициклическую группу, в которой одно или более колец является ароматическим, а другое кольцо частично гидрогенизовано, каждая из этих групп имеет от 5 до 12 членов кольца и содержит в системе колец 1, 2 или 3 гетероатома, выбираемых из кислорода,азота и серы, возможно, чтобы упомянутый гетероарил был необязательно замещен заместителями, описанными для арильной группы,циклоалкил обозначает моноциклическую или бициклическую группу, которая является насыщенной или ненасыщенной, но не имеет ароматического характера, которая содержит от 3 до 10 атомов углерода и необязательно замещена одной или более одинаковыми или различными группами, выбираемыми из галогена,линейного или разветвленного (С 1-С 6)алкила,линейного или разветвленного (С 1-С 6)тригалоалкила, гидрокси, амино, линейного или разветвленного (С 1-С 6)алкиламино и ди-(С 1-С 6)алкиламино, в котором алкильный остаток может быть линейным или разветвленным, 005200 4 гетероциклооалкил обозначает группу, как указано выше, содержащую в системе колец 1 или 2 гетероатома, выбираемых из кислорода,азота и серы, упомянутый гетероциклоалкил необязательно замещен одним или более заместителями, такими, как описанные для циклоалкильной группы. Изомеры следует понимать как обозначающие энантиомеры и диастереоизомеры. Среди фармацевтически приемлемых солей можно упомянуть, без привнесения какихлибо ограничений, соляную кислоту, бромоводородную кислоту, серную кислоту, фосфорную кислоту, уксусную кислоту, трифтороуксусную кислоту, молочную кислоту, пирувовую кислоту, малоновую кислоту, сукциновую кислоту,глутаровую кислоту, фумаровую кислоту, винно-каменную кислоту, малеиновую кислоту,лимонную кислоту, аскорбиновую кислоту, оксалиловую кислоту, метансульфоновую кислоту, камфорную кислоту, пр. Среди фармацевтически приемлемых оснований можно упомянуть, без привнесения каких-либо ограничений, гидроксид натрия, гидроксид калия, триэтиламин, трет-бутиламин, пр. Заместитель R1 по изобретению имеет предпочтительное значение - атом водорода. Заместитель R2 по изобретению имеет предпочтительное значение - атом кислорода. В особенно преимущественном осуществлении предпочтительными соединениями по изобретению являются соединения формулы (I),в которой Х представляет собой линейную (С 1 С 6)алкиленовую группу. Заместители R3 изобретению имеют предпочтительное значение - атом водорода и линейная или разветвленная (С 1-С 6)алкильная группа. По преимущественному осуществлению изобретения, предпочтительными соединениями по изобретению являются соединения формулы(I), в которой R4 представляет собой группу,выбираемую из амино, замещенной одной или двумя одинаковыми или различными линейными или разветвленными (С 1-С 6)алкильными группами,группы формулы -N(R3)-X1-OR5, в которойR3 представляет собой атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу и X1 и R2 имеют значения, указанные для формулы (I),и группы формулы -O-X1-OR5, в которой X1 и R5 имеют значения, указанные для формулы (I). В особенно преимущественном осуществлении предпочтительные соединения по изобретению представляют собой соединения формулы (I), в которой R4 представляет собой группу-N(R3)-X1-OR5 или -O-X1-OR5, в которых R3 представляет собой атом водорода, X1 представляет собой линейную (С 2-С 4)алкиленовую цепочку, a R5 представляет собой атом водорода. Предпочтительными соединениями по изобретению являются(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этил(метил)карбамат,(5S,5 аS,8 аR,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этил(метил)карбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 3-(диметиламино)пропилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(2-гидроксиэтокси)этилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-[(2-гидроксиэтил)амино]этилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этилкарбамат. Изомеры и аддитивные соли с фармацевтически приемлемой кислотой или основанием предпочтительных соединений образуют неотъемлемую часть изобретения. Соединения формулы (I) получают способом, согласно которому в качестве исходного материала применяется соединение формулы (II) которое подвергают при основных условиях либо воздействию соединения формулы (III)R'1 представляет собой группу, выбираемую из линейного или разветвленного (С 1 С 6)алкила, арила, арил-(С 1-С 6)алкила, в котором алкильный остаток может быть линейным или разветвленным, гетероарила, гетероарил-(С 1-С 6) алкила, в котором алкильный остаток может быть линейным или разветвленным, линейного или разветвленного (С 1-С 6)алкилкарбонила,арилкарбонила, арил-(С 1-С 6)алкилкарбонила, в котором алкильный остаток может быть линейным или разветвленным, гетероциклоалкилкарбонила, линейного или разветвленного (С 1-С 6) алкилсульфонила, арилсульфонила и арил-(С 1 С 6)алкилсульфонила, в котором алкильный остаток может быть линейным или разветвленным, и Х представляет собой атом водорода или атом галогена,с получением соединений формулы (IV/A) в которой R'1 имеет значения, указанные здесь ранее,либо воздействию соединения формулы (V)G представляет собой необязательную защитную группу для гидрокси-функций, aL представляет собой уходящую группу,традиционную в органической химии,с получением соединений формулы (IV/B)(IV/B) составляет соединения формулы (IV) в которой Т представляет собой группу R'1 или G, как указано здесь ранее,это соединение формулы (IV) обрабатывают в основной среде соединением формулы (VI)Ph представляет собой необязательно замещенную фенильную группу, aR2 представляет собой атом кислорода или атом серы,с получением соединений формулы (VII) в которой Т, Ph и R2 имеют значения, указанные здесь ранее, 7 это соединение формулы (VII) подвергают реакции в основной среде с соединением формулы (VIII)(VIII),в котором R4, R3 и Х имеют значения, указанные для формулы (I),с получением, соответственно, соединений формулы (I/a), частного случая соединений формулы (I), или соединений формулы (IX), по которой Т представляет собой группу R'1 или группу G, в которых R'1, G, R2, R3, R4 и Х имеют значения, указанные здесь ранее,гидрокси-функцию этих соединений формулы (IX) депротектируют по традиционным способам органической химии с получением соединений формулы (I/b), частного случая соединений формулы (I) в которой R2, R3, R4 и X имеют значения,указанные для формулы (I),соединения (I/a) и (I/b) составляют совокупность соединений по изобретению, эти соединения очищают, при необходимости, согласно традиционной методике очистки, их можно разделять согласно традиционной методике разделения и их переводят, при желании, в их аддитивные соли с фармацевтически приемлемой кислотой или основанием. При этом предметом настоящего изобретения является способ получения соединений формулы (I), который отличается тем, что в качестве исходного продукта применяют соединение формулы (II) которое подвергают при основных условиях воздействию соединения формулы (V)G представляет собой традиционную защитную группу для гидрокси-функций, aL представляет собой традиционную в органической химии уходящую группу,с получением соединений формулы (IV/B) в которой G имеет вышеуказанные значения,полученное соединение формулы (IV) обрабатывают в основной среде соединением формулы (VI)Ph представляет собой необязательно замещенную фенильную группу, aR2 представляет собой атом кислорода,с получением соединений формулы (VII)(VIII),в котором R4, R3 и Х имеют значения, указанные для формулы (I),с получением соединения формулы (IX) в которой G, R2, R3, R4 и Х имеют вышеуказанные значения,гидрокси-функцию полученного соединения формулы (IX) депротектируют любым традиционным в органической химии способом с получением соединений формулы (I) в которой R1, R2, R3, R4 и Х имеют значения, указанные для формулы (I),полученные соединения очищают в случае необходимости согласно традиционной методике очистки, при желании, их можно разделять согласно традиционной методике разделения, и,при желании, переводят в их аддитивные соли с фармацевтически приемлемой кислотой или основанием. Соединения формул (II), (V), (VI) и (VIII) либо являются коммерчески доступными, либо их получают по традиционным способам органического синтеза. Соединения формулы (I) проявляют особенно ценные противоопухолевые свойства. Они имеют отличную цитотоксичность invitro на линиях клеток из крысиных или человеческих опухолей и активны in vivo. Характерные свойства этих соединений позволяют применять их терапевтически в качестве противоопухолевых агентов. Настоящее изобретение также относится к фармацевтическим композициям, включающим в качестве активного ингредиента по меньшей мере одно активное соединение формулы (I),его оптический изомер или аддитивную соль с фармацевтически приемлемой кислотой или основанием, отдельно или в комбинации с одним или более фармацевтически приемлемыми,инертными, нетоксичными эксципиентами или носителями. Среди композиций по изобретению можно упомянуть более конкретно те, которые пригодны для орального, парентерального(внутривенного, внутримышечного или под 005200 10 кожного) на- или чреcкожного, назального, ректального наязычного, глазного или респираторного применения, в особенности таблетки, драже, подъязычные таблетки, мягкие желатиновые капсулы, твердые желатиновые капсулы, суппозитории, кремы, мази, кожные гели, инъекционные или питьевые препараты, аэрозоли, глазные или назальные капли, пр. Применяемая дозировка варьируется согласно возрасту и весу пациента, пути приема, природе и сложности нарушения и назначению возможных одновременных лечений и колеблется от 0,5 до 500 мг в день за один или более приемов. Следующие примеры иллюстрируют изобретение, но ни коим образом его не ограничивают. Применяемые исходные материалы либо являются известными продуктами, либо их получают известными способами. Получение 1. Карбонат (5S,5 аS,8 аS,9R)-9(4-[(бензоилокси)карбонил]окси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил 4-нитрофенила. Стадия 1. Карбонат 4-[(5R,5aS,8aS,9S)-9 гидрокси-6-оксo-5,5a,6,8,8a,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил]-2,6-диметоксифенил бензоила. 0,55 ммоль триэтиламина и 0,37 ммоль бензоилхлороформата последовательно добавляют к раствору 0,25 ммоль (5S,5 аS,8 аS,9S)-9-гидрокси-5-(4-гидрокси-3,5-диметоксифенил)-5,8,8 а,9 тетрагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-6(5 аН)-она в 10 мл безводного дихлорометана при 0 С и в атмосфере аргона. После перемешивания на протяжении 1 ч реакционную смесь промывают водой. Органическую фазу затем сушат, фильтруют и затем концентрируют при сниженном давлении. Хроматография на силикагеле (циклогексан/этилацетат: 60/40) дает возможность выделить ожидаемый продукт. Стадия 2. Карбонат (5S,5 аS,8 аS,9R)-9-(4[(бензоилокси)карбонил]окси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 4-нитрофенила. 0,155 мл безводного пиридина добавляют к раствору 1,71 ммоль п-нитрофенилхлороформата в 5 мл безводного дихлорометана. В реакционной смеси образуется белый осадок. Затем по каплям в атмосфере аргона добавляют раствор 0,502 ммоль соединения, полученного на cтадии 1, в 5 мл дихлорометана. Перемешивают на протяжении 45 мин при комнатной температуре,затем на реакционную смесь выливают 15 мл воды. Органическую фазу промывают водой,сушат над MgSO4, фильтруют и концентрируют при сниженном давлении. Хроматография на силикагеле (циклогексан/этилацетат: 4/1) дает возможность выделить ожидаемый продукт. Точка плавления=125-130 С Пример 1. (5S,5 аS,8 аS',9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гекса 11 гидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-(диметиламино)этил(метил)карбамат. Стадия 1. Карбонат 4-[(5R,5aS,8aS,9S)-9(2-(диметиламино)этил](метил)амино]карбонилокси)-6-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил]-2,6-диметоксифенилбензоил. 0,228 ммоль N,N,N'-триметилэтилендиамина и 0,228 ммоль триэтиламина последовательно добавляют к раствору 0,171 ммоль соединения по получению 1 в 5 мл безводного дихлорометана при комнатной температуре и в атмосфере аргона. После перемешивания на протяжении 1 ч реакционную смесь гидролизируют. Органическую фазу затем промывают водой,затем сушат над MgSО 4, фильтруют и концентрируют при сниженном давлении. Хроматография на силикагеле (дихлорометан/метанол: 97/3) дает возможность выделить ожидаемый продукт. Точка плавления=102-103 С Стадия 2. (5S,5aS,8aS,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-(диметиламино)этил(метил)карбамат. 5% палладий-на-углероде (90,8 мг) добавляют к раствору 0,138 ммоль соединения, полученного на cтадии 1, в 8 мл этилацетата. Реакционную смесь перемешивают в атмосфере водорода (атмосферное давление) на протяжении 1 ч 45 мин, затем фильтруют через Celite для удаления катализатора. Фильтрат концентрируют при сниженном давлении. Неочищенный продукт хроматографируют на силикагеле (дихлорометан/метанол: 96/4), выделяя ожидаемый продукт. Точка плавления=184-186 С Масс-спектр (ES/MS): m/z=529 [М+H]+,551 [М+Na]+ Пример 2. (5S,5 аS,8 аS,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-(диметиламино)этил(метил)карбамат. Стадия 1. Карбонат 4-[(5R,5aR,8aS,9S)-9(2-(диметиламинo)этил](метил)амино]карбонилокси)-6-оксо-5,5a,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5-ил]-2,6-диметоксифенилбензоил. 0,184 ммоль N,N,N'-триметилэтилендиамина и 0,184 ммоль триэтиламина последовательно добавляют к раствору 0,141 ммоль соединения по получению 1 в 4 мл безводного дихлорометана. После перемешивания на протяжении 2 ч 30 мин при комнатной температуре в атмосфере аргона в реакционную смесь добавляют 3 мл тетрагидрофуранa и 1 М раствор фторида тетрабутиламмония (0,285 ммоль) в тетрагидрофуране. После реакции на протяжении 2 ч добавляют 0,3 ммоль фторида тетрабутиламмония. Перемешивают на протяжении 3 ч 30 мин и реакционную смесь выливают на воду (15 мл) и разводят дихлорометаном (10 мл). Водную фазу 12 экстрагируют дихлорометаном и объединенные органические фазы промывают водой и концентрированным водным раствором NaCl, и затем сушат над MgSО 4, фильтруют и концентрируют при сниженном давлении. Хроматография на силикагеле (дихлорометан/метанол: 97/3) дает возможность выделить ожидаемый продукт. Масс-спектр (DIC/NH3): m/z=663 [M+H]+ Стадия 2. (5S,5aS,8aR,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нaфто[2,3-d][1,3]диоксол-5 ил 2-(диметиламино)этил(метил)карбамат. Продукт получают согласно способу на стадии 2 примера 1, используя в качестве субстрата соединение, полученное на стадии 1. Масс-спектр (DIC/NН 3): m/z=529 [M+H]+ Пример 3. (5S,5 аS,8 аS,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 3-(диметиламино)пропилкарбамат. Продукт получают согласно способу в примере 1, стадии 1 и 2, используя диметиламинопропиламин вместо N,N,N'-триметилэтилендиамина в качестве реагента на cтадии 1.[a]D(CHCl3)=-23 Масс-спектр (DIC/NH3): m/z=529 [M+H]+ Пример 4. (5S,5aS,8 аR,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-(2-гидроксиэтокси)этилкарбамат. Продукт получают согласно способу в примере 1, стадии 1 и 2, используя 2-аминоэтоксиэтанол вместо N,N,N'-триметилэтилендиамина в качестве реагента на cтадии 1. Масс-спектр (DIC/NH3): m/z=683 [M+NH4]+ Пример 5. (5S,5aS,8 аR,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3S4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-[(2-гидроксиэтил)амино]этилкарбамат. Продукт получают согласно способу в примере 1, стадии 1 и 2, используя 2-аминоэтиламиноэтанол вместо N,N,N'-триметилэтилендиамина в качестве реагента на cтадии 1. Пример 6. (5S,5 аS,8aR,9R)-9-(4-Гидрокси 3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4':6,7]нафто[2,3-d][1,3]диоксол-5 ил 2-(диметиламино)этилкарбамат. Продукт получают согласно способу в примере 1, стадии 1 и 2, используя диметиламиноэтиламинo вместо N,N,N'-триметилэтилендиамина в качестве реагента на cтадии 1. Фармакологическое изучение соединений по изобретению Пример 7. Активность in vitro. Соединения по изобретению тестировали на различных линиях клеток человека и крыс: крысиная лейкемия L1210,эпидермоидная карцинома А-431,немелкоклеточная карцинома легких А 549,мелкоклеточная карцинома легких Н 69,карцинома толстой кишки НТ 29,эпидермальная буккальная карцинома KВ-3-1.Hepes, pH 7,4. Клетки распределяли на микропластинках и подвергали действию цитотоксических соединений на протяжении четырех периодов деления, что составляет от 48 до 96 ч. Количество жизнеспособных клеток определяют затем при помощи колориметрического анализа, Тетразольного Анализа Микрокультур (J.Carmichael и др., Cancer Res.: 47, 936-942,(1987. Результаты выражают в виде IC50, цитотоксической концентрации, которая ингибирует пролиферацию обрабатываемых клеток на 50%. В этих тестаx соединение по примеру 6 имеет такие значения IC50: Пример 8. Действие на клеточный цикл. Клетки L1210 инкубируют на протяжении 21 ч при 37 С в присутствии различных концентраций тестируемых соединений. Клетки затем фиксируют, используя 70% этанол (об.об.),дважды промывают в PBS и инкубируют 30 мин при 20 С в PBS, содержащем 100 мкг/мл РНКазы и 50 мкг/мл йодида пропидия. Результаты выражают в виде процентного соотношения клеток, которые накопили фазу G2+M через 21 ч, по сравнению с контролем (контроль: 20%). При концентрации 100 нМ соединение по примеру 6 индуцирует 86% накопление клеток в фазе G2+M через 21 ч. Пример 9. Активность in vivo. Противоопухолевая активность соединений при лейкемии Р 388. Линия Р 388 (крысиная лейкемия) поставлялась Национальным Институтом Рака (National Cancer Institute) (Федерик, США). Опухолевые клетки (10 клеток) вводили на 0 день в перитониальную полость мышей BDF1 женского пола (Iffa-Credo, Франция) весом от 18 до 20 г (группы по 6 животных). Продукты вводили внутривенно на 1 день. Противоопухолевую активность выражают в % Т/С: Соединение по примеру 6 является активным против лейкемии Р 388 и индуцирует Т/С в 203% при 6,25 мг/кг. Противоопухолевая активность соединений при карциноме легких Льюиса (Lewis). Карцинома Льюиса (LLC) представляет собой плотную опухоль, которая появлялась спонтанно в легких мыши С 57 В 1/6 и поддерживается последовательными трансплантациями фрагментов подкожным путем. LLC получали от Отдела лечения рака Банка опухолей Национального Института Рака (Division of CancerInstitute), Федерик, MD, США. При получении от Iffa-Credo (Лион, Франция) мыши были возрастом от 4 до 6 недель и весили от 20 до 22 г в начале эксперимента. На первый день эксперимента (D0) опухоли удаляли и разрезали на фрагменты по 30 мг приблизительно, которые сразу же вводили подкожным путем мышам B6D2F1. Мышей,которым были имплантированы фрагменты,затем случайным образом разделяли на обрабатываемые группы и контрольную группу (по 7 животных в группе). Параметр, применяемый для оценки противоопухолевой активности,представляет собой повышение времени выживания. Дополнительно, в конце эксперимента,на 90 день, подсчитывали количество выживших животных в каждой группе. Продукты вводили согласно схеме, показанной ниже. Результаты выражали в % Т/С,подсчитанных, как в предыдущем тесте. Доза,Путь ВыживСхема Т/С% мг/кг введения шие D90 Пример 1 25 Внутривенно D 4, 8, 12 165 111 Пример 6 3,12 Внутривенно D 4, 8, 12 168 111 Продукт Пример 10. Фармацевтическая композиция: раствор для инъекций. Соединение по примеру 10 мг Дистиллированная вода для препаратов для инъекций 25 мл ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения формулы (I) в которой R1 представляет собой атом водорода,R2 представляет собой атом кислорода,R3 представляет собой атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу,Х представляет собой линейную или разветвленную (С 1-С 6)алкиленовую группу,R4 представляет собой группу, выбираемую из амино, необязательно замещенного одной или двумя одинаковыми или различными группами, выбираемыми из линейного или разветвленного (С 1-С 6)алкила,группы формулы -N(R3)-X1-OR5, в которойR3 имеет вышеуказанные значения, X1 представляет собой линейную или разветвленную(С 1-С 6)алкиленовую группу и R5 представляет собой атом водорода, 15 группы формулы -O-X1-OR5, в которой R5 и X1 имеют вышеуказанные значения,их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием, причем изомеры следует понимать как обозначающие энантиомеры и диастереоизомеры. 2. Соединения формулы (I) по п.1, отличающиеся тем, что Х представляет собой линейную (С 2-С 4)алкиленовую группу, их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием. 3. Соединения формулы (I) по п.1, отличающиеся тем, что R4 представляет собой группу -N(R3)-X1-OR5 или -O-X1-OR5, в которых R3 представляет собой атом водорода, X1 представляет собой линейную (С 2-С 4)алкиленовую цепочку, a R5 представляет собой атом водорода, их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием. 4. Соединения формулы (I) по п.1, которые представляют собой(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил-2-(диметиламино)этил(метил)карбамат,(5S,5 аS,8 аR,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этил(метил)карбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 3-(диметиламино)пропилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(2-гидроксиэтокси)этилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-[(2-гидроксиэтил)амино]этилкарбамат,(5S,5 аS,8 аS,9R)-9-(4-гидрокси-3,5-диметоксифенил)-8-оксо-5,5 а,6,8,8 а,9-гексагидрофуро[3',4': 6,7]нафто[2,3-d][1,3]диоксол-5-ил 2-(диметиламино)этилкарбамат,и их изомеры, а также их аддитивные соли с фармацевтически приемлемой кислотой или основанием. 5. Способ получения соединений формулы(I), отличающийся тем, что в качестве исходного продукта применяют соединение формулы (II) которое подвергают при основных условиях 16 воздействию соединения формулы (V)(V),в которой G представляет собой традиционную защитную группу для гидроксифункций, aL представляет собой традиционную в органической химии уходящую группу,с получением соединений формулы (IV/B) в которой G имеет вышеуказанные значения,полученное соединение формулы (IV) обрабатывают в основной среде соединением формулы (VI)(VI),в которой Ph представляет собой необязательно замещенную фенильную группу, аR2 представляет собой атом кислорода,с получением соединений формулы (VII)(VIII),в котором R4, R3 и Х имеют значения, указанные для формулы (I),с получением соединения формулы (IX) в которой G, R2, R3, R4 и Х имеют вышеуказанные значения,гидроксифункцию полученного соединения формулы (IX) депротектируют любым традиционным в органической химии способом с получением соединений формулы (I) в которой R1, R2, R3, R4 и Х имеют значения,указанные для формулы (I),полученные соединения очищают в случае необходимости согласно традиционной методике очистки, при желании, их можно разделять согласно традиционной методике разделения, и, 18 при желании, переводят в их аддитивные соли с фармацевтически приемлемой кислотой или основанием. 6. Фармацевтические композиции, включающие в качестве активного ингредиента по меньшей мере одно соединение по любому из пп.1-4, отдельно или в сочетании с одним или более фармацевтически приемлемыми, инертными, нетоксичными эксципиентами или носителями. 7. Фармацевтические композиции по п.6,содержащие по меньшей мере один активный ингредиент по любому из пп.1-4, предназначенные для лечения рака.
МПК / Метки
МПК: A61P 35/00, A61K 31/365, C07D 493/04
Метки: соединения, новые, карбамат, композиции, подофиллотоксина, способ, получения, фармацевтические, тиокарбамат, содержащие
Код ссылки
<a href="https://eas.patents.su/10-5200-novye-soedineniya-karbamat-i-tiokarbamat-podofillotoksina-sposob-ih-polucheniya-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Новые соединения карбамат и тиокарбамат подофиллотоксина, способ их получения и содержащие их фармацевтические композиции</a>
Предыдущий патент: Производные стрептограминов, способ их получения и композиции на их основе
Следующий патент: Содержащая циклезонид водная фармацевтическая композиция
Случайный патент: Совокупность дозированных лекарственных форм, содержащих опиоид












