Новые производные инденоиндолона, способ их получения и содержащие их фармацевтические композиции
Номер патента: 4711
Опубликовано: 24.06.2004
Авторы: Бутэн Жан Альбер, Делагранж Филипп, Буссар Мари-Франсуа, Руссо Анн, Вержбиский Мишель
Формула / Реферат
1. Соединение формулы (I)

где R означает атом водорода или линейный или разветвленный (C1-C6)алкенил, или линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb, которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (C1-C6)алкильную группу, или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл,
каждый из R1, R2, R3, R4, R5, R6, R7 и R8, которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкенильную группу, гидроксильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, линейную или разветвленную (C1-C6)алкенилоксигруппу, арил(C1-C6)алкильную группу, в которой алкильный остаток является линейным или разветвленным, арил(C1-C6)алкоксигруппу, в которой алкоксильный остаток является линейным или разветвленным, карбоксильную группу, линейную или разветвленную (C1-C6)ацилоксигруппу или арилкарбонилоксигруппу,
или одна из групп R1-R8 образует вместе с расположенной рядом одной из групп R1-R8(C1-C2)алкилендиоксигруппу,
его оптические изомеры, если они существуют, и его аддитивные соли с фармацевтически приемлемыми кислотой или основанием, при условии, что
когда R не означает атом водорода, тогда как минимум одна из групп R1-R8 означает гидроксильную группу или линейную или разветвленную (C1-C6)ацилоксигруппу, и
соединения формулы (I) являются иными, кроме индено[1,2-b]индол-10(5H)-она,
понятно, что под термином "арил" имеются в виду "фенил", "бифенилил", "нафтил" или "тетрагидронафтил", каждая из этих групп необязательно замещена одним или несколькими одинаковыми или различными атомами или группами, выбранными из атомов галоида и линейных или разветвленных (C1-C6)алкильных групп, гидроксильных групп, линейных или разветвленных (C1-C6)алкоксигрупп, линейных или разветвленных (C1-C6)полигалоидалкильных групп, аминогрупп (необязательно замещенных одной или несколькими линейными или разветвленными (C1-C6)алкильными группами), нитрогрупп, линейных или разветвленных (C1-C6)ацильных групп и (C1-C2)алкилендиоксигрупп.
2. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-8-гидрокси-5-метилиндено[1,2-b]индол-10(5H)-он.
3. Соединение формулы (I) по п.1, которое означает 2,4-диметокси-8-гидроксииндено[1,2-b]индол-10(5H)-он.
4. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-5-(2-диметиламиноэтил)-8-гидроксииндено[1,2-b]индол-10(5H)-он.
5. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-8-гидрокси-5-[2-(4-морфолинил)этил]индено[1,2-b]индол-10(5H)-он.
6. Способ получения соединений формулы (I) по п.1, отличающийся тем, что соединение формулы (II)
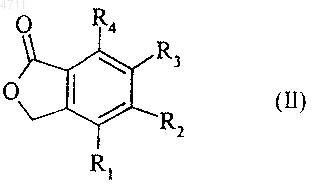
где R1, R2, R3 и R4 являются такими, как указано для формулы (I),
подвергается реакции с N-бромсукцинимидом с образованием соединения формулы (III)
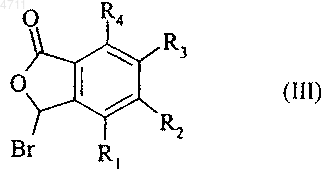
где R1, R2, R3 и R4 являются такими, как указано выше,
которое реагирует с трифенилфосфином с образованием соединения формулы (IV)
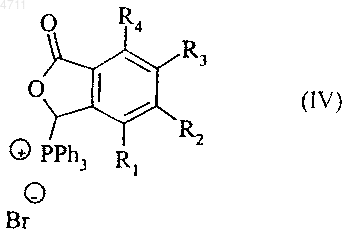
где R1, R2, R3 и R4 являются такими, как указано выше,
последнее соединение взаимодействует с соединением формулы (V)
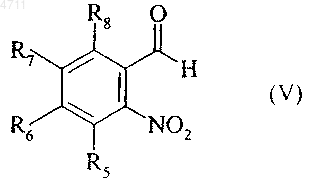
где R5, R6, R7 и R8 являются такими, как указано для формулы (I),
с образованием соединения формулы (VI)
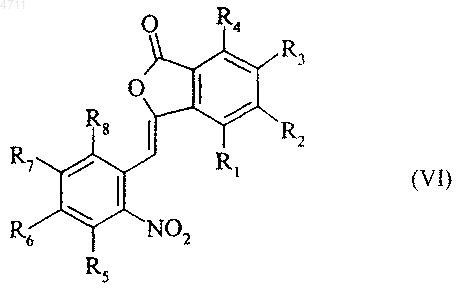
где R1, R2, R3, R4, R5, R6, R7 и R8 являются такими, как указано выше,
соединение формулы (VI) обрабатывают основанием и получают соединение формулы (VII)
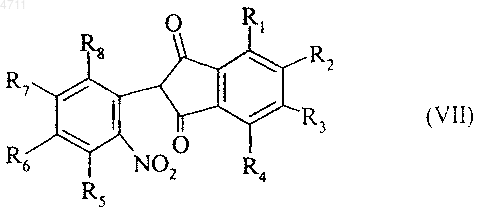
где R1, R2, R3, R4, R5, R6, R7 и R8 являются такими, как указано выше,
которое затем подвергают действию восстанавливающего агента для получения после разделения изомеров, где необходимо, соединения формулы (Ia), являющегося частным случаем соединений формулы (I)
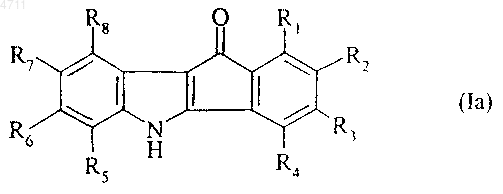
где R1, R2, R3, R4, R5, R6, R7 и R8 являются такими, как указано выше,
полученное соединение, если желательно, подвергают реакции с соединением формулы (VIII)
R'- Z (VIII),
где R' означает линейный или разветвленный (C1-C6)алкенил или линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb, которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (C1-C6)алкильную группу, или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл, и
Z означает уходящую группу, как, например, атом галоида или мезил, тозил или трифторметансульфонил,
для получения соединения формулы (Ib), представляющего частный случай соединений формулы (I)
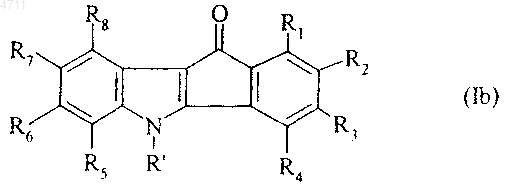
где R1, R2, R3, R4, R5, R6, R7, R8 и R' являются такими, как указано выше,
такие соединения формул (Ia) и (Ib) составляют совокупность соединений формулы (I), которые, если необходимо, очищают в соответствии с обычными методиками очистки, разделяют, если целесообразно, на их изомеры в соответствии с обычной методикой разделения и превращают, если желательно, в их аддитивные соли с фармацевтически приемлемыми кислотой или основанием.
7. Фармацевтическая композиция, включающая в качестве активного ингредиента соединение формулы (I) по любому из пп.1-5 в комбинации с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми носителями.
8. Фармацевтическая композиция по п.7 для применения при получении лекарственных средств для лечения нарушений мелатонинергической системы.
Текст
1 Настоящее изобретение относится к новым производным инденоиндолона, к способу их получения и к содержащим их фармацевтическим композициям, а также к их применению при лечении нарушений мелатонинергической системы. Ряд производных инденоиндолона описан в литературе, например, в J. Chem. Soc. PerkinTrans. I 1974, 13, 1523-1525, без указания какойлибо фармакологической активности этих соединений. Соединения по настоящему изобретению являются новыми и обладают очень ценными фармакологическими характеристиками в отношении мелатонинергических рецепторов. Многочисленные исследования последних десяти лет продемонстрировали ключевую роль мелатонина (N-ацетил-5-метокситриптамина) во многих физиопатологических явлениях и в регуляции циркадного ритма. Полупериод его существования довольно короткий, благодаря тому факту, что он быстро метаболизируется. Большой интерес поэтому представляет возможность предоставить клиницистам аналоги мелатонина, которые метаболически более устойчивы, имеют агонистический или антагонистический характер и от которых можно ожидать терапевтический эффект, превышающий эффект самого гормона. В добавление к их полезному действию в отношении нарушений циркадного ритма (J.Neurosurg. 1985, 63, pp. 321-341) и нарушений сна (Psychopharmacology, 1990, 100, pp. 222226), лиганды мелатонинергической системы обладают ценными фармакологическими свойствами по отношению к центральной нервной системе, в частности, анксиолитическими и антипсихотическими свойствами (Neuropharmacology of Pineal Secretions, 1990, 8 (3-4), pp. 264272) и болеутоляющими свойствами (Pharmacopsychiat., 1987, 20, pp. 222-223) и также свойствами для лечения болезни Паркинсона (J. Neurosurg. 1985, 63, pp. 321-341) и болезни Альцгеймера (Brain Research, 1990, 528, pp. 170-174). Соединения также продемонстрировали активность в отношении некоторых видов рака(Melatonin - Clinical Perspectives, Oxford University Press, 1988, pp. 164-165), овуляции (Science 1987, 227, pp. 714-720), диабета (Clinical Endocrinology, 1986, 24, pp. 359-364) и при лечении ожирения (International Journal of Eating Disorders, 1996, 20, pp. 443-446). Эти различные эффекты усиливаются при посредничестве специфических мелатониновых рецепторов. Молекулярно-биологические исследования продемонстрировали существование ряда подтипов рецепторов, способных к связыванию этого гормона (Trends Pharmacol. Sci., 1995, 16,p. 50; международная заявка на патент WO 97/04094). Для различных видов, включая млекопитающих, стали возможными обнаружение 2 местонахождения и характеристика некоторых из таких рецепторов. Для того чтобы можно было лучше понять физиологические функции этих рецепторов, большим преимуществом является возможность иметь в распоряжении специфические лиганды. Более того, такие соединения, благодаря селективному взаимодействию с тем или иным из этих рецепторов, могут быть отличными лекарственными средствами для клинициста при лечении патологий, связанных с мелатонинергической системой, о некоторых из которых упоминалось выше. Соединения по настоящему изобретению в дополнение к тому, что являются новыми, проявляют сильное сродство к мелатониновым рецепторам и значительную селективность к сайтам типа МТ 3. Настоящее изобретение, главным образом,относится к соединениям формулы (I) где R означает атом водорода или линейный или разветвленный (C1-С 6)алкенил, или линейную или разветвленную (С 1-С 6)алкильную группу,необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb, которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1 С 6)алкильную группу, или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл,каждый из R1, R2, R3, R4, R5, R6, R7 и R8,которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу,линейную или разветвленную (C1-С 6)алкенильную группу, гидроксильную группу, линейную или разветвленную (С 1-С 6)алкоксигруппу, линейную или разветвленную (C1-С 6)алкенилоксигруппу, арил(С 1-С 6)алкильную группу, в которой алкильный остаток является линейным или разветвленным, арил(С 1-С 6)алкоксигруппу, в которой алкоксильный остаток является линейным или разветвленным, карбоксильную группу, линейную или разветвленную (С 1 С 6)ацилоксигруппу или арилкарбонилоксигруппу,или одна из групп R1-R8 образует вместе с расположенной рядом одной из групп R1-R8 (С 1 С 2)алкилендиоксигруппу,к их оптическим изомерам, если они существуют, и к их аддитивным солям с фармацевтически приемлемыми кислотой или основанием,при условии, что когда R не означает атом водорода, тогда,как минимум, одна из групп R1-R8 означает гид 3 роксильную группу или линейную или разветвленную (С 1-С 6)ацилоксигруппу,и соединения формулы (I) являются иными, кроме индено[1,2-b]индол-10(5H)-она. Под термином "арил" имеют в виду "фенил", "бифенилил", "нафтил" или "тетрагидронафтил", каждая из этих групп необязательно замещена одним или несколькими одинаковыми или различными атомами или группами, выбранными из атомов галоида и линейных или разветвленных (C1-С 6)алкильных групп, гидроксильных групп, линейных или разветвленных(С 1-С 6)алкоксигрупп, линейных или разветвленных (С 1-С 6)полигалоидалкильных групп, аминогрупп (необязательно замещенных одной или несколькими линейными или разветвленными(С 1-С 6)алкильными группами), нитрогрупп, линейных или разветвленных (С 1-С 6)ацильных групп и (С 1-С 2)алкилендиоксигрупп. Под термином "азотсодержащий гетероцикл" подразумевают насыщенную 5-7-членную моноциклическую группу, содержащую один,два или три гетероатома, один из этих гетероатомов является атомом азота, а остальные, необязательно присутствующие гетероатомы выбираются из атомов кислорода, азота и серы. Предпочтительными азотсодержащими гетероциклами являются пирролидинильные, пиперидильные, морфолинильные и пиперазинильные остатки. Среди фармацевтически приемлемых кислот могут быть упомянуты, не предполагая каких-либо ограничений этими примерами, соляная кислота, бромисто-водородная кислота,серная кислота, фосфорная кислота, уксусная кислота, трифторуксусная кислота, молочная кислота, пировиноградная кислота, малоновая кислота, янтарная кислота, глутаровая кислота,фумаровая кислота, винная кислота, малеиновая кислота, лимонная кислота, аскорбиновая кислота, метансульфокислота, камфорная кислота,щавелевая кислота и т.д. Среди фармацевтически приемлемых оснований могут быть упомянуты, не предполагая каких-либо ограничений этими примерами, гидроокись натрия, гидроокись калия, триэтиламин, трет-бутиламин и т.д. Изобретение также относится к способу получения соединений формулы (I), отличающемуся тем, что соединение формулы (II) где R1, R2, R3 и R4 являются такими, как указано для формулы (I),подвергается реакции с N-бромсукцинимидом с образованием соединения формулы где R1, R2, R3 и R4 являются такими, как указано выше,которое реагирует с трифенилфосфином с образованием соединения формулы (IV) где R5, R6, R7 и R8 являются такими, как указано для формулы (I),с образованием соединения формулы (VI) где R1, R2, R3, R4, R5, R6, R7 и R8 являются такими, как указано выше,которое затем подвергают действию восстанавливающего агента для получения после разделения изомеров, если необходимо, соединения формулы (Iа), являющегося частным случаем соединений формулы (I)(VIII),где R' означает линейный или разветвленный(С 1-С 6)алкенил или линейную или разветвленную (С 1-С 6)алкильную группу, необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb,которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу,или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл, иZ означает уходящую группу, как, например, атом галоида или мезил, тозил или трифторметансульфонил,для получения соединения формулы (Ib),представляющего частный случай соединений формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8 и R' являются такими, как указано выше,эти соединения формул (Iа) и (Ib) составляют совокупность соединений формулы (I),которые, если необходимо, очищают согласно обычным методикам очистки, разделяют, если целесообразно, на их изомеры в соответствии с обычной методикой разделения и превращают,если желательно, в их аддитивные соли с фармацевтически приемлемыми кислотой или основанием. Соединения формулы (I), где одна из группR1-R8 является гидроксильной группой, могут быть также получены при каталитическом гидрировании соответствующих простых бензиловых эфиров или путем деметилирования соответствующих простых метиловых эфиров. Доказано, что соединения по изобретению и содержащие их фармацевтические композиции являются полезными для лечения нарушений мелатонинергической системы. Фармакологическое изучение соединений по изобретению на самом деле продемонстрировало, что они не являются токсичными, имеют высокое селективное сродство к мелатониновым рецепторам и обладают существенной активностью в отношении центральной нервной системы и, в частности, были обнаружены лечебные свойства в отношении нарушений сна,анксиолитические, антипсихотические и обезболивающие свойства, как и свойства, относящиеся к капиллярному кровообращению, что позволило установить, что соединения по изобретению полезны при лечении стресса, нарушений сна, тревоги, аффективных сезонных расстройств, сердечно-сосудистых патологий,патологий пищеварительной системы, бессонницы и усталости из-за нарушения суточного ритма организма, шизофрении, приступов пани 004711 6 ки, меланхолии, нарушений аппетита, ожирения, бессонницы, психических нарушений, эпилепсии, диабета, болезни Паркинсона, старческого слабоумия, различных нарушений, связанных с нормальным или патологическим старением, мигрени, потери памяти, болезни Альцгеймера и нарушений мозгового кровообращения. Что касается других сфер активности, то оказалось, что соединения по изобретению могут быть использованы для лечения нарушений половых функций, что они обладают ингибирующими овуляцию свойствами и иммуномодулирующими свойствами и что их возможно использовать при лечении злокачественных заболеваний. Соединения предпочтительно используют при лечении сезонных аффективных расстройств, нарушений сна, сердечно-сосудистых патологий, бессонницы и усталости вследствие нарушения суточного ритма организма, нарушений аппетита и ожирения. Например, соединения используются для лечения аффективных сезонных расстройств и нарушений сна. Представленное изобретение относится также к фармацевтическим композициям, включающим соединение формулы (I) в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями. Среди фармацевтических композиций согласно изобретению могут быть упомянуты,главным образом, такие, которые пригодны для перорального, парентерального, назального,перкутанного или чрескожного, прямокишечного, перлингвального, глазного введения или введения через дыхательные пути, в частности,таблетки или драже, подъязычные таблетки,саше, дозы лекарства в виде порошка, завернутого аптечным способом в бумагу, желатиновые капсулы, покрытые глазурованной оболочкой таблетки, лепшки, суппозитории, кремы, мази,гели для кожи и ампулы с содержимым для приема внутрь или для инъекций. Доза варьируется в соответствии с полом,возрастом и весом больного, со способом введения, с природой терапевтического показания или с возможными сопутствующими лечениями и лежит в диапазоне от 0,01 мг до 1 г за 24 ч в виде одного или нескольких введений. Следующие примеры иллюстрируют изобретение, но никак не ограничивают его. Использованные исходные соединения являются известными продуктами или их получают в соответствии с известными методиками. Строение соединений, описанных в примерах, определяли согласно обычным спектрометрическим методикам (инфракрасная спектрометрия, ЯМР, масс-спектрометрия).N-бромсукцинимида и затем реакционную смесь, облучаемую галогеновой лампой, кипятят с обратным холодильником в течение 5 ч. Смесь затем охлаждают до комнатной температуры и фильтруют, фильтрат затем упаривают,прибавляют толуол, полученную суспензию фильтруют и фильтрат упаривают. Полученный остаток фильтруют через двуокись кремния и получают ожидаемый продукт. Стадия Б.(5,6-Диметоксифталидил) трифенилфосфонийбромид. Прибавляют 10 ммоль трифенилфосфина к 10 ммоль полученного на предыдущей стадии соединения в растворе толуола и затем реакционную смесь кипятят с обратным холодильником в течение 3 ч. После охлаждения до комнатной температуры смесь фильтруют и полученный слой осадка затем промывают и сушат,получают ожидаемый продукт. Температура плавления: 260 С. Стадия В. 3-(5-Бензилокси-2-нитробензилиден)-5,6-диметоксифталид. К 10 ммоль 5-бензилокси-2-нитробензальдегида, растворенного в диметилформамиде,прибавляют 10 ммоль триэтиламина и затем порциями 10 ммоль соединения, полученного на предыдущей стадии. Реакционную смесь затем нагревают при 50 С в течение 1 ч 30 мин и затем охлаждают до комнатной температуры и упаривают. Затем прибавляют диэтиловый эфир и смесь перемешивают в течение ночи, а затем фильтруют. Полученный слой осадка затем промывают и получают ожидаемый продукт. Температура плавления: 170 С. Стадия Г. 2-(5-Бензилокси-2-нитрофенил)3-гидрокси-5,6-диметокси-1 Н-инден-1-он. Прибавляют 10 мл 4 н. раствора гидроокиси натрия к 10 ммоль полученного на предыдущей стадии соединения, растворенного в метаноле. Смесь затем нагревают при 40 С в течение часа и затем охлаждают до 0 С и устанавливают рН=1 с помощью 4 н. раствора соляной кислоты(12 мл). После перемешивания в течение ночи при комнатной температуре образовавшийся осадок белого цвета отфильтровывают, промывают и затем сушат и очищают путем хроматографии на колонке с двуокисью кремния (элюент: дихлорметан/метанол 99/1), получают ожидаемый продукт. Температура плавления: 120 С. Стадия Д. 8-Бензилокси-2,3-диметоксииндено[1,2-b]индол-10(5H)-он. 8 Раствор полученного на предыдущей стадии соединения (10 ммоль) в диметилформамиде обрабатывают в атмосфере водорода в присутствии никелевого катализатора Ренея. После удаления катализатора при фильтрации растворитель удаляют путем выпаривания и остаток сушат, получают ожидаемый продукт. Температура плавления: 235 С. Пример 2. 2,3-Диметокси-8-гидроксииндено[1,2-b]индол-10(5H)-он. К раствору описанного в примере 1 соединения (10 ммоль) в смеси метанол/ диметилформамид 70/30 прибавляют 20 ммоль 1 н. раствора гидроокиси натрия и затем 1 г 10% палладия на угле. Смесь помещают в атмосферу водорода под давлением 80 мбар на 2 ч при комнатной температуре и затем катализатор отфильтровывают, к фильтрату прибавляют раствор 1 н. соляной кислоты (20 мл) и растворители удаляют путем выпаривания. Полученный в результате осадок обрабатывают изопропиловым спиртом и полученную в результате суспензию фильтруют, фильтрат упаривают и полученный осадок промывают, получают ожидаемый продукт. Температура плавления: 260 С. Пример 3. 2,3-Диметокси-8-гидрокси-5 метилиндено[1,2-b]индол-10(5H)-он. К раствору 10 ммолей описанного в примере 2 соединения в диметилформамиде прибавляют 11 ммоль карбоната калия и затем реакционную смесь нагревают до 90 С и прибавляют 11 ммоль йодистого метила. Реакционную смесь затем выдерживают в течение ночи при 60 С и растворитель затем удаляют при выпаривании, прибавляют воду и полученную суспензию фильтруют. Отфильтрованный осадок перекристаллизовывают из этанола, получают ожидаемый продукт. Температура плавления: 241 С. Элементный микроанализ: вычислено найдено Пример 4. 7-Бензилокси-8-метоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии с методикой, описанной в примере 1,исходя из фталида и 4-бензилокси-5-метокси-2 нитробензальдегида. Пример 5. 7-Гидрокси-8-метоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии с методикой, описанной в примере 2,исходя из соединения, описанного в примере 4. Температура плавления: 260 С. Элементный микроанализ: вычислено найдено 9 Пример 6. 8-Бензилокси-1,4-диметоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии с методикой, описанной в примере 1,исходя из 4,7-диметоксифталида и 5-бензилокси-2-нитробензальдегида. Пример 7. 1,4-Диметокси-8-гидроксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 2,исходя из соединения, описанного в примере 6. Температура плавления: 260 С. Пример 8. 1,4-Диметокси-8-гидрокси-5 метилиндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 7. Пример 9. 8-Бензилокси-1-гидрокси-4 метоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают путем селективного деметилирования соединения, описанного в примере 6, согласно способу, описанному в Tet. 1996, 52(43), 13623-640. Пример 10. 1,8-Дигидрокси-4-метоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 2,исходя из соединения, описанного в примере 9. Пример 11. 2,3-Диметоксииндено[1,2-b] индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 1,исходя из 5,6-диметоксифталида и 2-нитробензальдегида. Температура плавления: 260 С. Пример 12. 2,3-Диметокси-7,8-метилендиоксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 1,исходя из 5,6-диметоксифталида и 4,5-метилендиокси-2-нитробензальдегида. Пример 13. 7,8-Метилендиоксииндено[1,2b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 1,исходя из фталида и 4,5-метилендиокси-2 нитробензальдегида. Пример 14. 8-Бензилокси-1,3-диметоксииндено[1,2-b]индол-10(5H)-он. При использовании методики в соответствии со способом, описанным в примере 1, исходя из 4,6-диметоксифталида и 5-бензилокси-2 нитробензальдегида получают требующийся продукт в смеси с 8-бензилокси-2,4-диметоксииндено[1,2-b]индол-10(5H)-оном. Требующийся продукт получают при разделении смеси при хроматографии на колонке с двуокисью кремния (элюент: дихлорметан/ метанол 98/2) и выпаривании второй элюированной фракции. Пример 15. 1,3-Диметокси-8-гидроксииндено[1,2-b]индол-10(5H)-он. 10 Требующийся продукт получают в соответствии со способом, описанным в примере 2,исходя из соединения, описанного в примере 14. Пример 16. 8-Бензилокси-2,4-диметоксииндено[1,2-b]индол-10(5H)-он. При использовании методики в соответствии со способом, описанным в примере 1, исходя из 4,6-диметоксифталида и 5-бензилокси-2 нитробензальдегида получают требующийся продукт в смеси с 8-бензилокси-1,3-диметоксииндено[1,2-b]индол-10(5H)-оном. Требующийся продукт получают при разделении смеси при хроматографии на колонке с двуокисью кремния (элюент: дихлорметан/ метанол 98/2) и выпаривании первой элюированной фракции. Пример 17. 2,4-Диметокси-8-гидроксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 2,исходя из соединения, описанного в примере 16. Пример 18. 5-Алил-2,3-диметокси-8 гидроксииндено[1,2-b]индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 2,заменяя йодистый метил бромистым аллилом. Пример 19. 1,3-Диметокси-5-(2-диметиламиноэтил)-8-гидроксииндено[1,2-b]индол 10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 15,заменяя йодистый метил 2-хлор-N,Nдиметилэтиламином. Пример 20. 1,4-Диметокси-5-(2-диметиламиноэтил)-8-гидроксииндено[1,2-b]индол 10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 7,заменяя йодистый метил 2-хлор-N,Nдиметилэтиламином. Пример 21. 2,3-Диметокси-5-(2-диметиламиноэтил)-8-гидроксииндено[1,2-b]индол 10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 2,заменяя йодистый метил 2-хлор-N,Nдиметилэтиламином. Температура плавления: 216 С. Элементный микроанализ: вычислено найдено Пример 22. 2,3-Диметокси-8-гидрокси-5[2-(4-морфолинил)этил]индено[1,2-b]индол 10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 3, 11 Пример 23. 2,3,8-Триметоксииндено[1,2-b] индол-10(5H)-он. Требующийся продукт получают в соответствии со способом, описанным в примере 1,заменяя 5-бензилокси-2-нитробензальдегид 5 метокси-2-нитробензальдегидом. Пример 24. Натриевая соль (8-гидрокси 2,3-диметокси-10-оксоиндено[1,2-b]индол 5(10H)-ил)уксусной кислоты. Стадия А. Метиловый эфир (8-гидрокси 2,3-диметокси-10-оксоиндено[1,2-b]индол 5(10H)-ил)уксусной кислоты. Требующийся продукт получают в соответствии со способом, описанным в примере 3,исходя из соединения, описанного в примере 2,заменяя йодистый метил метиловым эфиром хлоруксусной кислоты. Стадия Б. Натриевая соль (8-гидрокси-2,3 диметокси-10-оксоиндено[1,2-b]индол-5(10H)ил)уксусной кислоты. Требующийся продукт получают при гидролизе гидроокисью натрия сложного эфира,полученного на предыдущей стадии А. Температура плавления: 260 С. Элементный микроанализ: вычислено найдено Фармакологическое исследование соединений по изобретению Пример 25. Изучение связывания со связывающими сайтами МТ 3 мелатонина. Связывание с сайтами МТ 3 отличается в высшей степени быстрой кинетикой ассоциации и диссоциации и локализацией в ткани (мозг). Эксперименты по связыванию с сайтами МТ 3 проводят на мембранах мозга хомячков с применением 2-[125I]иодмелатонина в качестве радиоактивного лиганда в соответствии с протоколом, описанным P. Paul et al. (J. Pharmacol.Exp. Ther. 1999, 290, 334). Мембраны инкубируют 30 мин с 2-[125I]иодмелатонином при температуре 4 С и при различных концентрациях исследуемых соединений. После инкубирования мембраны быстро фильтруют и затем промывают холодным буфером, используя систему для фильтрования. Фиксированную радиоактивность измеряют с помощью сцинтилляционного счетчика. Значения концентраций, вызывающих 50%-ное ингибирование, IC50, найденные для соединений по изобретению, свидетельствуют о 12 сильном сродстве к сайтам типа МТ 3, эти значения составляют от 0,2 до 100 нМ. Для сравнения, мелатонин в данном тесте имеет IC50 в 45 нМ. Пример 26. Фармацевтическая композиция. Состав для получения 1000 таблеток, каждая из которых содержит 10 мг активного ингредиента: Соединение из примера 1 10 г Гидроксипропилцеллюлоза 2 г Пшеничный крахмал 10 г Лактоза 100 г Стеарат магния 3 г Тальк 3 г ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) где R означает атом водорода или линейный или разветвленный (С 1-С 6)алкенил, или линейную или разветвленную (С 1-С 6)алкильную группу,необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb, которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1 С 6)алкильную группу, или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл,каждый из R1, R2, R3, R4, R5, R6, R7 и R8,которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу,линейную или разветвленную (С 1-С 6)алкенильную группу, гидроксильную группу, линейную или разветвленную (С 1-С 6)алкоксигруппу, линейную или разветвленную (C1-С 6)алкенилоксигруппу, арил(С 1-С 6)алкильную группу, в которой алкильный остаток является линейным или разветвленным, арил(С 1-С 6)алкоксигруппу, в которой алкоксильный остаток является линейным или разветвленным, карбоксильную группу, линейную или разветвленную (С 1-С 6) ацилоксигруппу или арилкарбонилоксигруппу,или одна из групп R1-R8 образует вместе с расположенной рядом одной из групп R1-R8(С 1 С 2)алкилендиоксигруппу,его оптические изомеры, если они существуют, и его аддитивные соли с фармацевтически приемлемыми кислотой или основанием,при условии, что когда R не означает атом водорода, тогда как минимум одна из групп R1-R8 означает гидроксильную группу или линейную или разветвленную (С 1-С 6)ацилоксигруппу, и 13 соединения формулы (I) являются иными,кроме индено[1,2-b]индол-10(5H)-она,понятно, что под термином "арил" имеются в виду "фенил", "бифенилил", "нафтил" или"тетрагидронафтил", каждая из этих групп необязательно замещена одним или несколькими одинаковыми или различными атомами или группами, выбранными из атомов галоида и линейных или разветвленных (С 1-С 6)алкильных групп, гидроксильных групп, линейных или разветвленных (С 1-С 6)алкоксигрупп, линейных или разветвленных (С 1-С 6)полигалоидалкильных групп, аминогрупп (необязательно замещенных одной или несколькими линейными или разветвленными (С 1-С 6)алкильными группами),нитрогрупп, линейных или разветвленных (С 1 С 6)ацильных групп и (С 1-С 2)алкилендиоксигрупп. 2. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-8-гидрокси-5-метилиндено[1,2-b]индол-10(5H)-он. 3. Соединение формулы (I) по п.1, которое означает 2,4-диметокси-8-гидроксииндено[1,2b]ндол-10(5H)-он. 4. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-5-(2-диметиламиноэтил)-8-гидроксииндено[1,2-b]индол-10(5H)-он. 5. Соединение формулы (I) по п.1, которое означает 2,3-диметокси-8-гидрокси-5-[2-(4-морфолинил)этил]индено[1,2-b]индол-10(5H)-он. 6. Способ получения соединений формулы(I) по п.1, отличающийся тем, что соединение формулы (II) где R1, R2, R3 и R4 являются такими, как указано для формулы (I),подвергается реакции с N-бромсукцинимидом с образованием соединения формулы где R1, R2, R3 и R4 являются такими, как указано выше,которое реагирует с трифенилфосфином с образованием соединения формулы (IV) где R5, R6, R7 и R8 являются такими, как указано для формулы (I),с образованием соединения формулы (VI) где R1, R2, R3, R4, R5, R6, R7 и R8 являются такими, как указано выше,которое затем подвергают действию восстанавливающего агента для получения после разделения изомеров, где необходимо, соединения формулы (Iа), являющегося частным случаем соединений формулы (I)(VIII),где R' означает линейный или разветвленный(С 1-С 6)алкенил или линейную или разветвленную (С 1-С 6)алкильную группу, необязательно замещенную карбоксильной группой или группой формулы -NRaRb, где каждый из Ra и Rb,которые могут быть одинаковыми или различными, означает атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу,или вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероцикл, иZ означает уходящую группу, как, например, атом галоида или мезил, тозил или трифторметансульфонил,для получения соединения формулы (Ib),представляющего частный случай соединений формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8 и R' являются такими, как указано выше,такие соединения формул (Iа) и (Ib) составляют совокупность соединений формулы(I), которые, если необходимо, очищают в соответствии с обычными методиками очистки, разделяют, если целесообразно, на их изомеры в соответствии с обычной методикой разделения и превращают, если желательно, в их аддитив 16 ные соли с фармацевтически приемлемыми кислотой или основанием. 7. Фармацевтическая композиция, включающая в качестве активного ингредиента соединение формулы (I) по любому из пп.1-5 в комбинации с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми носителями. 8. Фармацевтическая композиция по п.7 для применения при получении лекарственных средств для лечения нарушений мелатонинергической системы.
МПК / Метки
МПК: A61P 25/00, C07D 209/94, A61K 31/403
Метки: инденоиндолона, новые, композиции, фармацевтические, содержащие, получения, способ, производные
Код ссылки
<a href="https://eas.patents.su/9-4711-novye-proizvodnye-indenoindolona-sposob-ih-polucheniya-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Новые производные инденоиндолона, способ их получения и содержащие их фармацевтические композиции</a>
Предыдущий патент: Протеинкиназа candida albicans, обладающая активностью фосфорилирования циклинзависимых протеинкиназ, и способы ее применения
Следующий патент: Способ индукции антивирусной резистентности растений
Случайный патент: Передатчик для системы связи













