Новые соли с полезными органолептическими свойствами
Формула / Реферат
1. Соединение общей формулы (I)
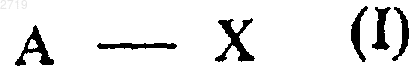
где А представляет собой положительно заряженный ион (катион) лекарственного вещества,
Х представляет собой отрицательно заряженный ион (анион) подслащивающего вещества,
и его сольваты, имеющие полезные органолептические свойства.
2. Соединение общей формулы (I) и его сольваты по п.1, отличающееся тем, что
А принимает значения, определенные в п.1,
Х означает отрицательно заряженный ион формул

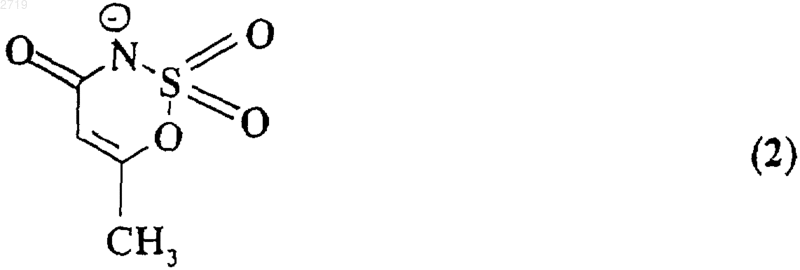
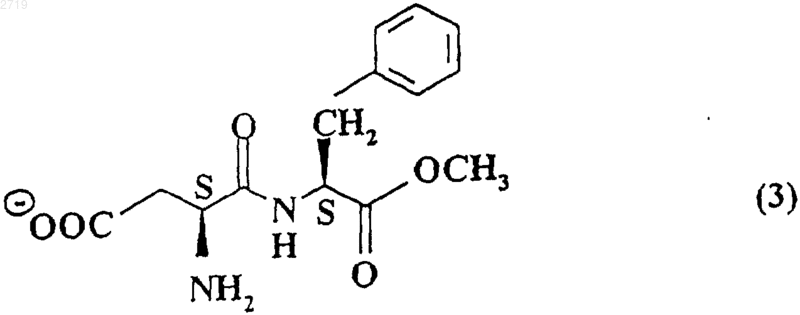
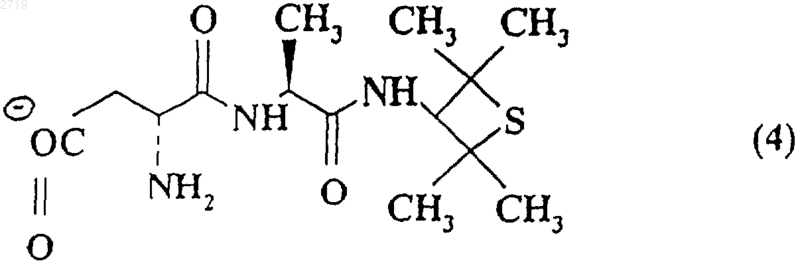
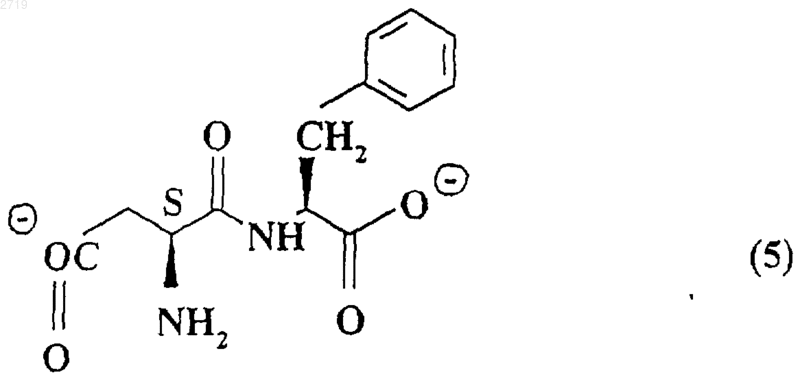
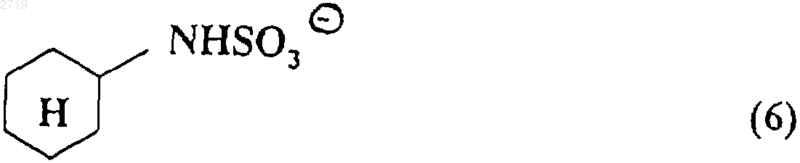
и его сольваты.
3. Соединение общей формулы (I) и его сольваты по п.1, отличающееся тем, что А представляет собой положительно заряженный ион дротаверина, преноксдиазина, селегилина, азитромицина, циметидина, ципрофлоксацина, клопидогрела, ирбесартина, эритромицина, флуоксетина, ранитидина, кларитромицина, эналаприла.
4. Соль дротаверина, образованная анионом формулы (1), и ее сольваты.
5. Соль дротаверина, образованная анионом формулы (2), и ее сольваты.
6. Соль дротаверина, образованная анионом формулы (3), и ее сольваты.
7. Соль дротаверина, образованная анионом формулы (4), и ее сольваты.
8. Соль дротаверина, образованная анионом формулы (5), и ее сольваты.
9. Соль дротаверина, образованная анионом формулы (6), и ее сольваты.
10. Соль преноксдиазина, образованная анионом формулы (1), и ее сольваты.
11. Соль преноксдиазина, образованная анионом формулы (2), и ее сольваты.
12. Соль преноксдиазина, образованная анионом формулы (3), и ее сольваты.
13. Соль преноксдиазина, образованная анионом формулы (4), и ее сольваты.
14. Соль преноксдиазина, образованная анионом формулы (5), и ее сольваты.
15. Соль преноксдиазина, образованная анионом формулы (6), и ее сольваты.
16. Фармацевтический препарат, отличающийся тем, что он содержит, по меньшей мере, одно соединение общей формулы (I), где А и Х имеют значения, определенные в п.1, и/или его/их сольваты.
17. Фармацевтический препарат по п.16, отличающийся тем, что он находится в твердой форме.
18. Фармацевтический препарат по п.16, отличающийся тем, что он находится в жидкой форме.
19. Способ получения соединений общей формулы (I), отличающийся тем, что катионная форма (положительно заряженный ион) лекарственного вещества реагирует с анионной формой (отрицательно заряженным ионом) подслащивающего вещества.
20. Способ по п.19, отличающийся тем, что реакцию проводят в жидкой среде.
21. Ингибитор ФДЭ-IV, содержащий, по меньшей мере, одно из соединений и/или их сольватов по пп.4-9 в качестве терапевтически активного компонента.
22. Применение, по меньшей мере, одного из соединений и/или их сольватов по пп.4-9 для получения фармацевтических композиций для ингибирования фермента ФДЭ-IV.
23. Спазмолитический агент, содержащий, по меньшей мере, одно из соединений и/или их сольватов по пп.4-9 в качестве терапевтически активного компонента.
24. Применение, по меньшей мере, одного из соединений и/или их сольватов по пп.4-9 для получения спазмолитических фармацевтических композиций.
Текст
1 Объектом настоящего изобретения являются соединения общей формулы (I) где А представляет собой положительно заряженный ион (катион) лекарственного вещества,Х представляет собой отрицательно заряженный ион (анион) подслащивающего вещества формул и их сольваты, которые обладают полезными органолептическими свойствами, фармацевтические препараты, содержащие названные выше соединения и/или их сольваты, а также получение соединений общей формулы (I). Неприятный горький вкус, возникающий в процессе или сразу после приема, является обычным для широкого круга лекарственных веществ. К таким веществам относятся различные активные ингредиенты, такие как дротаверин, преноксдиазин, азитромицин, циметидин,ципрофлоксацин, эритромицин, флуоксетин,кларитромицин и ранитидин. Горький вкус лекарственного вещества,которое изготовлено в виде жидкой суспензии,может ощущаться при питье суспензии или сразу после ее проглатывания. Вместе с тем горький вкус препарата, который содержит горький активный ингредиент, может ощущаться при приеме только из-за того, если этот горький агент остается во рту слишком долго, при случайном разжевывании или высвобождении лю 002719 2 бым другим путем, т.е. если он входит в контакт с вкусовыми сосочками языка. Обычно среди способов введения некоторых лекарственных веществ пероральная лекарственная форма является предпочтительной, так как она обеспечивает простую и дешевую дозировку. Однако часто необходимо учитывать взаимодействие с пациентом, когда он должен принимать таблетку, капсулу или суспензию. Пациенты имеют ряд причин, по которым они не хотят или не способны глотать препараты,предназначенные для перорального приема,включая, например, плохой внешний вид лекарственной формы, ее слишком большой размер,неприятный вкус или просто страх, что не разжеванное лекарство может застрять в гортани. Пациент, у которого имеются проблемы при приеме пероральных лекарственных форм, часто имеет позывы к рвоте, что реально препятствует пероральному приему лекарства. Эта проблема весьма обычна среди детей, но также возникает и у взрослых. В связи с этим желательно готовить фармацевтические препараты таким способом, при котором появление указанных выше проблем может быть исключено. Обычно для маскировки горькости лекарственных веществ полезными являются покрытие и маскировка. Таким образом, например, созданы разжевываемые таблетки, и они в значительной степени более приемлемы для пациентов, как детей, так и взрослых, имеющих затруднения с глотанием таблеток или капсул целиком. Однако часто случается, что лекарственное вещество имеет горький вкус, что он фактически непереносим при жевании, и неприятный вкус или последующие вкусовые ощущения, вызываемые этим горьким ингредиентом, мешают пациенту согласиться на пероральный прием лекарства. Таким образом целью исследований было найти производные лекарственных соединений,которые не имели бы неприятного вкуса или не вызывали бы неприятных последующих вкусовых ощущений, но терапевтически были бы равны известным формам фармацевтически активных ингредиентов, главным образом гидрохлоридам. Неожиданно было обнаружено, что эту задачу можно решить не с помощью покрытия или маскировки, а путем приготовления солей или солей-сольватов лекарственных веществ с подслащивающими веществами и затем при использовании их в качестве активных ингредиентов или в качестве части активных ингредиентов в фармацевтических препаратах. В данном контексте используется понятие лекарственное вещество для активных ингредиентов любого лекарственного средства для человека или животного, органолептические свойства которого, особенно вкус и последующие вкусовые ощущения, неприятны для пациентов или некоторых групп пациентов или для животных. 3 Подслащивающие вещества в данном случае определяются как любое природное или синтетическое подслащивающее вещество, которое используется для подслащивания пищевых продуктов для человека или животного и известно из литературы на момент подачи данной заявки. Полезными подслащивающими веществами являются, например, сахарин, ацесульфам, аспартам, алитам, циклогексиламиносульфоновая кислота, глициризиновая кислота и подобные соединения. Хотя здесь используется понятие лекарственное вещество главным образом для перечисленных выше соединений, но не исключаются и любые другие соединения, которые имеют неприятные органолептические свойства. Лекарственные вещества, из которых могут быть получены новые производные общей формулы (I), включают, но не ограничиваются только ими, дротаверин, преноксдиазин, селегилин, лекарственные вещества с фентиазиновой структурой, ципрофлоксацин, флуоксетин, эналаприл, клопидогрел, ирбесартан, азитромицин,эритромицин, кларитромицин, циметидин и ранитидин. Новые соединения общей формулы (I) имеют такой же качественный терапевтический профиль, что и известные исходные фармацевтически активные ингредиенты и их известные соли. Например, как известно, спазмолитический агент дротаверин и его гидрохлорид являются ингибиторами изофермента фосфодиэстеразы IV (ФДЭ-IV) (ЕР-0664127 А 2). Новые соли дротаверина и их сольваты общей формулы (I) также являются селективными ингибиторами ФДЭ-IV: Ингибирование фермента ФДЭ-IV человеСоединение ческих клеток U937(линия клеток), IC50 Дротаверин гид 4,7.10-6 моля рохлорид Дротаверин цик 1.10-6 моля ламат (пример 2) Дротаверин саха 3,8.10-6 моля римид (пример 1) Метод оценки. Активность циклического нуклеотида фосфордиэстеразы измеряют с помощью двухступенчатой методики. Стандартная смесь для проведения оценки содержит: 30 мкл фермента ФДЭ IV, 20 мкл испытуемого соединения или его сольвата, 20 мкл субстрата [3H]цАМФ(220000 радиологических распадов/мин), 30 мкл 40 мМ буфера Tris (pH = 7,6), содержащего 2,5 мМ MgSO4. Реакцию инициируют путем добавления субстрата. Образцы выдерживают при 30 С в течение 30 мин и реакцию останавливают кипячением пробирок для испытания в течение 2 мин. 4 После охлаждения пробирок добавляют 50 мкл Clotalux atrox (0,5 мг/мл диcт. воды) и образцы выдерживают и встряхивают в течение 30 мин при 37 С. Не прореагировавший цАМФ удаляют с помощью хроматографии на смоле Dowex 1 х 8(Хлороформ): 1 мл Dowex добавляют к образцу и после хорошего перемешивания смолу оставляют для осаждения в течение 60 мин при комнатной температуре. Смесь 500 мкл надосадочной жидкости и 5 мл жидкой сцинцилляционной смеси используют для определения количества образовавшегося 3H-аденозина. Результаты расчетов где I - ферментативная активность в присутствии ингибитора,С - контроль (0 время),Т - суммарная ферментативная активность. Величину IС 50 рассчитывают с использованием Medusa Version 1.4. Кроме того, на фиг. 1-7 показано, что фармакологические профили являются одинаковыми в случае солей дротаверина общей формулы(I) и известного гидрохлорида дротаверина. Фиг. 1. Изучен расслабляющий эффект на спонтанный трахеальный тонус двух солей дротаверина. Обе соли с концентрационной зависимостью уменьшают напряжение трахеального тонуса. Как можно увидеть на фиг. 1, с точки зрения эффективности между двумя солями нет существенного различия. Фиг. 2. Изучен расслабляющий эффект на трахеальный тонус, предварительно сокращенный гистамином, двух солей дротаверина. Обе соли с концентрационной зависимостью уменьшают напряжение трахеального тонуса. Как можно увидеть на фиг. 2, с точки зрения эффективности между двумя солями нет существенного различия. Фиг. 3. Изучен ингибирующий эффект двух солей дротаверина на индуцированное аллергеном (овальбумином) трахеальное сокращение на изолированном трахеальном препарате, полученном из морских свинок, предварительно сенсибилизированных овальбумином. Рассчитывают площадь под кривой индуцированного овальбумином сокращения (ППС, AUC) и ее уменьшение в процентах используется для характеристики лекарственного действия. Обе соли с концентрационной зависимостью уменьшают аллергическую реакцию. В этом отношении между двумя солями нет существенного различия. Фиг. 4. Бронхолитический эффект in vivo двух солей дротаверина изучен на индуцированном аллергеном (овальбумином) бронхостенозе у предсенсибилизированных аллергеном(овальбумином) морских свинок после интрадуоденального введения. Обе соли дротаверина 5 проявляют концентрационнозависимый бронхолитический эффект. В этом отношении между двумя солями нет существенного различия. Фиг. 5. Продолжительность бронхолитического действия эквимолярной дозы ( доза ЕД 50) двух солей дротаверина изучена в опыте с индуцированным аллергеном (овальбумином) бронхостенозе. Обе соли проявляют длительный бронхолитический эффект. Различие между двумя временными кривыми не имеет существенного значения, так что фармакологическое действие двух солей практически идентично. Фиг. 6. Бронхолитический эффект in vivo двух солей дротаверина изучен в опыте с индуцированным гистамином бронхостенозе у морских свинок после интрадуоденального введения. Обе соли дротаверина проявляют бронхолитический эффект, зависящий от дозы. Между двумя солями нет существенного различия в бронхолитическом действии. Фиг. 7. Животные с предварительно повышенной чувствительностью к аллергену(овальбумину) подвергаются лечению с помощью эквимолярных доз солей дротаверина в течение семи дней (одна п/о доза/день). На 8-ой день половина животных из группы, обработанной каждой солью, обработана растворителем, и через 30 мин был вызван бронхостеноз путем в/в инъекции аллергена (овальбумина). Обе соли имеют бронхолитическое действие даже через 24 ч после последней обработки. Значительного отличия между двумя солями не выявлено."р" (фигуры (4)-(7 означает доверительный интервал и "п" означает количество животных используемых в эксперименте. Другую половину групп животных, обработанных каждой солью, снова обрабатывают соответствующей солью и через 30 мин вызывают бронхостеноз с помощью в/в инъекции аллергена. Острое бронхолитическое действие после подострого лечения для обеих солей выше, чем ожидалось, исходя из опытов по оценке острого эффекта (фиг. 4). С точки зрения эффективности между двумя солями нет существенного различия. Таким образом, названные выше новые соли дротаверина и их сольваты, имеющие приятный сладкий вкус, могут быть использованы в фармацевтике в качестве спазмолитических агентов, антидепрессантов, транквилизаторов,агентов против слабоумия, противовоспалительных агентов, антиаллергенов, противоастматических агентов, агентов для защиты печени, диуретических агентов и т.д., а также в лекарственных средствах для профилактики и лечения различных заболеваний, в том числе расстройств центральной нервной системы, таких как депрессия и слабоумие, а также других заболеваний, таких как воспаление, аллергические заболевания, астма, заболевания печени и болезни почек. 6 Соединения общей формулы (I) могут быть получены реакцией положительно заряженной формы (катиона) лекарственного вещества с отрицательно заряженной формой (анионом) подслащивающего вещества с использованием способов, которые сами по себе известны. Названная выше реакция преимущественно проводится в растворителе и соединения общей формулы (I) получают и очищают с помощью обычных методик. Используемые лекарственные вещества и подслащивающие вещества представляют собой коммерческие продукты. Фармацевтические препараты могут быть приготовлены из соединений общей формулы(I) с помощью обычных методик получения препаратов и с использованием приемлемых наполнителей, разбавителей, смазывающих веществ, связующих веществ, пигментов и стабилизирующих агентов. Следует отметить, что соединения общей формулы (I) могут проявлять неочевидные преимущества с точки зрения биодоступности и/или технологии получения препарата. Далее изобретение описано подробнее с помощью следующих примеров, но без ограничения формулы изобретения этими примерами. Пример 1. Раствор 20 г основания дротаверина в 20 см 3 абсолютного этанола (40 С) добавляют к раствору 9,02 г сахаримида в 60 см 3 горячего абсолютного (безводного) этанола. Раствор, подвергающийся кристаллизации, медленно охлаждают; при достижении 10 С его осветляют и покрывают спиртом. Полученный сырой этаналат дротаверин сахаримида (28,2 г) перекристаллизовывают из трехкратного объема 96%-ного спирта с выходом 95%. Получают кристаллы светло-желтого цвета, т.пл. 95-97 С. Данные элементного анализа и спектров(ИК, ЯМР) доказывают, что полученное вещество представляет собой сольват (содержащий один моль этанола) соли, образующейся при взаимодействии дротаверина и сахаримида. Элементный анализ рассчитан для эмпирической формулы C31H42N2O8S.C2H5OH. Вычислено, %: С 63,24, Н 6,75, N 4,47, S 5,12; Найдено, %: С 63,59, Н 6,68, N 4,37, S 5,25. Отнесение сигналов: ИК-спектр (Bruker IFS28, таблетки KBr): 3498 OH этанола; 3085, 3064 CH (ароматика); 2978, 2933,2882 CH (алифатические связи); 2788-2338(м, 2 Н, сахарин, 5,6-Н); 7,28 (с, 1 Н, 8-Н); 6,95 (д,1 Н, 2'-Н, J2'.6 = 1,9); 6,82 (дд, 1 Н, 6'-Н, J5'.6 = 8,2); 6,75 (д, 6'-Н); 6,73 (с, 1H, 5-H); 4,49 (с, 2 Н, СН 2); 4,17 (кв, 2 Н, 6-ОСН 2, JOCH2CH3 = 7,0); 4,09 (м, 2 Н, 7 3-Н 2); 4,00 (кв, 6H, 7-OCH2, 3'-ОСН 2, 4'-ОСН 2); 3,72 (кв, 2 Н, этанол, ОСН 2); 3,00 (м, 2 Н, 4-Н 2); 1,48 (т, 3 Н); 1,40 (т, 3 Н); 1,38 (т, 3 Н); 1,33 (т, 3 Н,СН 3); 1,22 (т, 3 Н, этанол, СН 3). Пример 2. Растворяют 21,6 г гидрохлорида дротаверина в 40 см 3 96%-ного горячего спирта и затем добавляют раствор 10,2 г цикламата натрия в 25 см 3 дистиллированной воды. При охлаждении раствора цикламат дротаверина кристаллизуется при 32 С; после дополнительного охлаждения его выдерживают при 5 С в течение 2 ч для кристаллизации, затем осветляют, покрывают и сушат 50%-ным спиртом. Вес: 14,4 г (цвет: почти белый). Сырой продукт перекристаллизовывают из трехкратного объема 96%-ного спирта с выходом 80%; получают почти белый продукт. Т.пл.: плавление начинается при 158 С и является длительным процессом. Данные элементного анализа и спектров(ИК, ЯМР) доказывают, что полученное вещество представляет собой соль, образующуюся при взаимодействии дротаверина и циклогексиламиносульфоновой кислоты. Отнесение сигналов: ИК-спектр (Bruker IFS28, таблетки KВr): 3285 NH; 3093, 3056 CH (ароматика); 2975,2923, 2854 CH (алифатические связи); 1661(т, 3 Н, СН 3); 2,11 (м, 2H); 1,68 (м, 2H); 1,55 (м,1 Н); 1,4-1,05 (м, 5 Н, цикламат, 2,3,4,5,6-Н 2). Если продукт перекристаллизовывают из водно-органического растворителя, то продукт,содержащий 1 моль воды в виде гидрата, может быть отделен. В случае этого моногидрата цикламата дротаверина спектр 1H ЯМР аналогичен спектру соли, не содержащей воды, но ИКспектр имеет следующий вид: ИК-спектр (Bruker IFS28, таблетки KBr): 3285 NH; 3093, 3056 CH (ароматика); 2975,2923, 2854 CH (алифатические связи); 1646CN; 1603, 1562, 1518 (колебания ароматической структуры); 1278, 1035 C-O-C; OH (H2O) 3477, 3441. Пример 3. В 75 см 3 кипящего безводного этанола растворяют 10,9 г преноксдиазина в виде основания и 5,55 г (0,03 моля каждого) сахаримида. Прозрачный раствор кристаллизуют при охлаждении и перемешивании. Полученные кристаллы отделяют и покрывают не 002719 8 большим количеством этилового спирта. Сырой продукт подвергают вакуумной сушке. Выход 16,03 г (97,4%). Т.пл. 131-132 С. Полученный сахаримид преноксдиазина перекристаллизовывают с использованием безводного спирта в 5,2-кратном объеме, выход 96%. Т.пл. 131-132 С. Элементный анализ для С 30 Н 32N4O4S. Вычислено, %: С 66,16, Н 5,92, N 10,29, S 5,89%. Найдено, %: С 66,45, Н 6,06, N 10,48, S 5,92%. Данные элементного анализа и спектральные данные (ИК, ЯМР) доказывают, что полученное вещество является солью, образующейся в результате реакции преноксдиазина с сахаримидом. Отнесение сигналов: ИК-спектр (Bruker IFS28, таблетки KBr): 3064, 3035, 3013; CH (ароматика); 2962, 2940,2919, 2868 CH (алифатические связи); 27662120 NH+; 1644 C=O (сахарин); 1583, 1525,1495 (колебания ароматической структуры); 751, 716 (монозамещ. ароматика). Спектр 1H ЯМР (Bruker DRX-400, 400 МГц, CDCl3): 7,79 (м, 2 Н, сахарин, 4,7-Н); 7,62Nipagin 5,0 г Сахароза 10,0 г Маннит 5,0 г Отдушка Сколько нужно Смесь смешивают с питьевой водой до объема 100 мл, получают жидкий сироп общим объемом 100 мл. Проверка органолептических свойств приведенной выше композиции показала, что характерный горький вкус дротаверина не проявляется. Пример 5. Готовая к применению суспензия. Смешивают те же компоненты, что и в примере 4, но к твердой смеси добавляют дистиллированную воду и смесь разливают по бутылкам. Проверка органолептических свойств приведенной выше композиции показала, что характерный горький вкус дротаверина не проявляется. Пример 6 .Таблетки. Ингредиенты: 150 г сахаримида дротаверина (пример 1), 5 г стеарата 9 магния, 8 г талька, 50 г предварительно желатинизированного крахмала, 10 г поливинилпирролидона, 100 г лактозы, 90 г микрокристаллической целлюлозы. Ингредиенты смешивают, гранулируют и прессуют в таблетки общим весом 413 мг, содержащие 150 мг активного вещества. Проверка органолептических свойств приведенной выше композиции показала, что характерный горький вкус дротаверина не проявляется. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I) где А представляет собой положительно заряженный ион (катион) лекарственного вещества,Х представляет собой отрицательно заряженный ион (анион) подслащивающего вещества,и его сольваты, имеющие полезные органолептические свойства. 2. Соединение общей формулы (I) и его сольваты по п.1, отличающееся тем, что А принимает значения, определенные в п.1,Х означает отрицательно заряженный ион формул и его сольваты. 3. Соединение общей формулы (I) и его сольваты по п.1, отличающееся тем, что А представляет собой положительно заряженный ион дротаверина, преноксдиазина, селегилина, азитромицина, циметидина, ципрофлоксацина, кло 002719 10 пидогрела, ирбесартина, эритромицина, флуоксетина, ранитидина, кларитромицина, эналаприла. 4. Соль дротаверина, образованная анионом формулы (1), и ее сольваты. 5. Соль дротаверина, образованная анионом формулы (2), и ее сольваты. 6. Соль дротаверина, образованная анионом формулы (3), и ее сольваты. 7. Соль дротаверина, образованная анионом формулы (4), и ее сольваты. 8. Соль дротаверина, образованная анионом формулы (5), и ее сольваты. 9. Соль дротаверина, образованная анионом формулы (6), и ее сольваты. 10. Соль преноксдиазина, образованная анионом формулы (1), и ее сольваты. 11. Соль преноксдиазина, образованная анионом формулы (2), и ее сольваты. 12. Соль преноксдиазина, образованная анионом формулы (3), и ее сольваты. 13. Соль преноксдиазина, образованная анионом формулы (4), и ее сольваты. 14. Соль преноксдиазина, образованная анионом формулы (5), и ее сольваты. 15. Соль преноксдиазина, образованная анионом формулы (6), и ее сольваты. 16. Фармацевтический препарат, отличающийся тем, что он содержит, по меньшей мере, одно соединение общей формулы (I), где А и Х имеют значения, определенные в п.1,и/или его/их сольваты. 17. Фармацевтический препарат по п.16,отличающийся тем, что он находится в твердой форме. 18. Фармацевтический препарат по п.16,отличающийся тем, что он находится в жидкой форме. 19. Способ получения соединений общей формулы (I), отличающийся тем, что катионная форма (положительно заряженный ион) лекарственного вещества реагирует с анионной формой (отрицательно заряженным ионом) подслащивающего вещества. 20. Способ по п.19, отличающийся тем, что реакцию проводят в жидкой среде. 21. Ингибитор ФДЭ-IV, содержащий, по меньшей мере, одно из соединений и/или их сольватов по пп.4-9 в качестве терапевтически активного компонента. 22. Применение, по меньшей мере, одного из соединений и/или их сольватов по пп.4-9 для получения фармацевтических композиций для ингибирования фермента ФДЭ-IV. 23. Спазмолитический агент, содержащий,по меньшей мере, одно из соединений и/или их сольватов по пп.4-9 в качестве терапевтически активного компонента. 24. Применение, по меньшей мере, одного из соединений и/или их сольватов по пп.4-9 для получения спазмолитических фармацевтических композиций.
МПК / Метки
МПК: A61P 13/06, A61K 47/48
Метки: новые, соли, полезными, органолептическими, свойствами
Код ссылки
<a href="https://eas.patents.su/8-2719-novye-soli-s-poleznymi-organolepticheskimi-svojjstvami.html" rel="bookmark" title="База патентов Евразийского Союза">Новые соли с полезными органолептическими свойствами</a>
Предыдущий патент: Приспособление для вытаскиваемых пробок и аналогичных бутылочных затычек
Следующий патент: Терапевтическая композиция для введения толтеродина с контролируемым высвобождением и способ лечения мочевого пузыря с её использованием
Случайный патент: Способ очистки углеводородов от меркаптанов












